4′-азидо, 3′-фторзаміщені похідні нуклеозидів як інгібітори реплікації рнк вірусу гепатиту c
Номер патенту: 110428
Опубліковано: 25.12.2015
Автори: Чжан Чжумін, Чжан Цзін, Сміт Марк, Таламас Франсіско Ксав'єр
Формула / Реферат
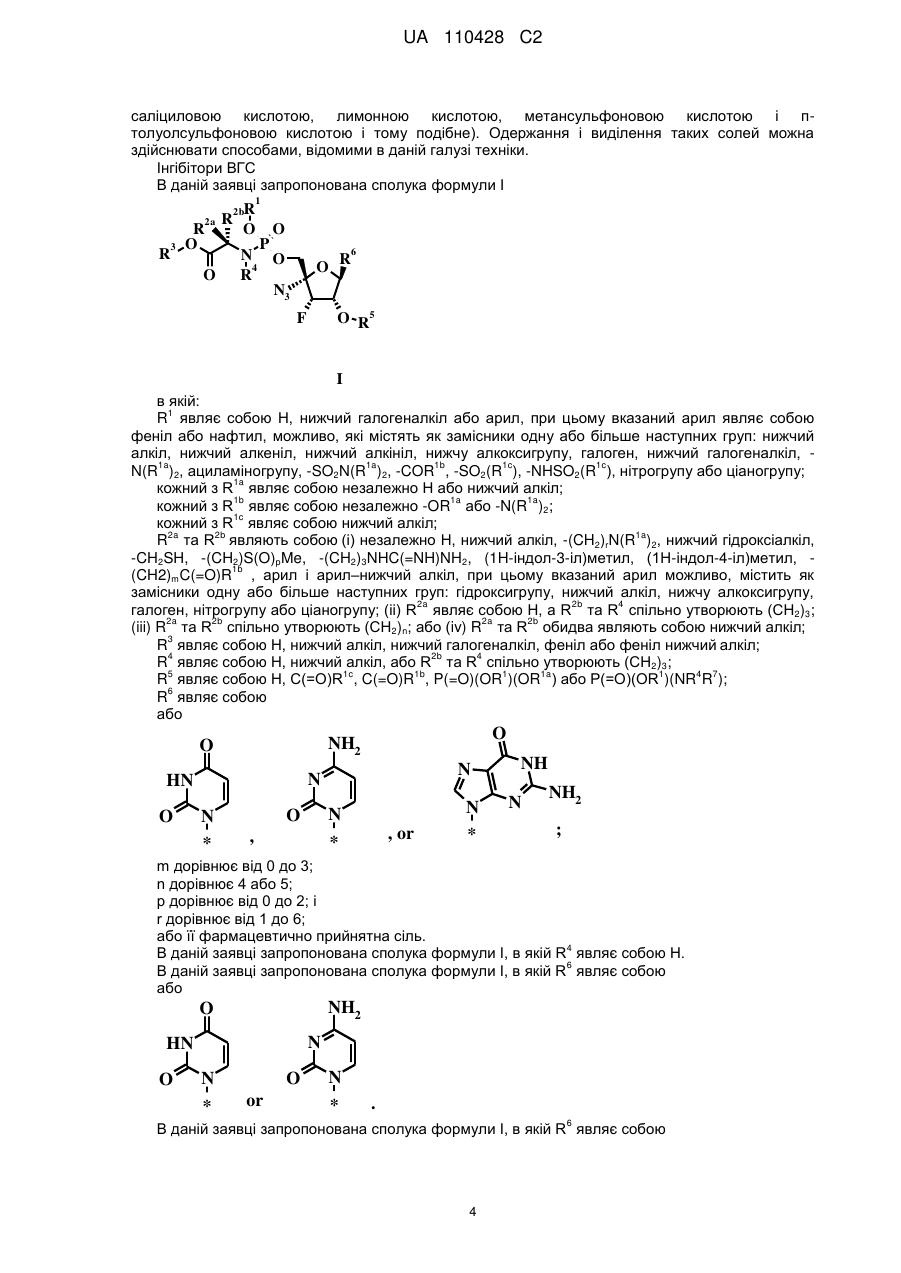
1. Сполука формули І
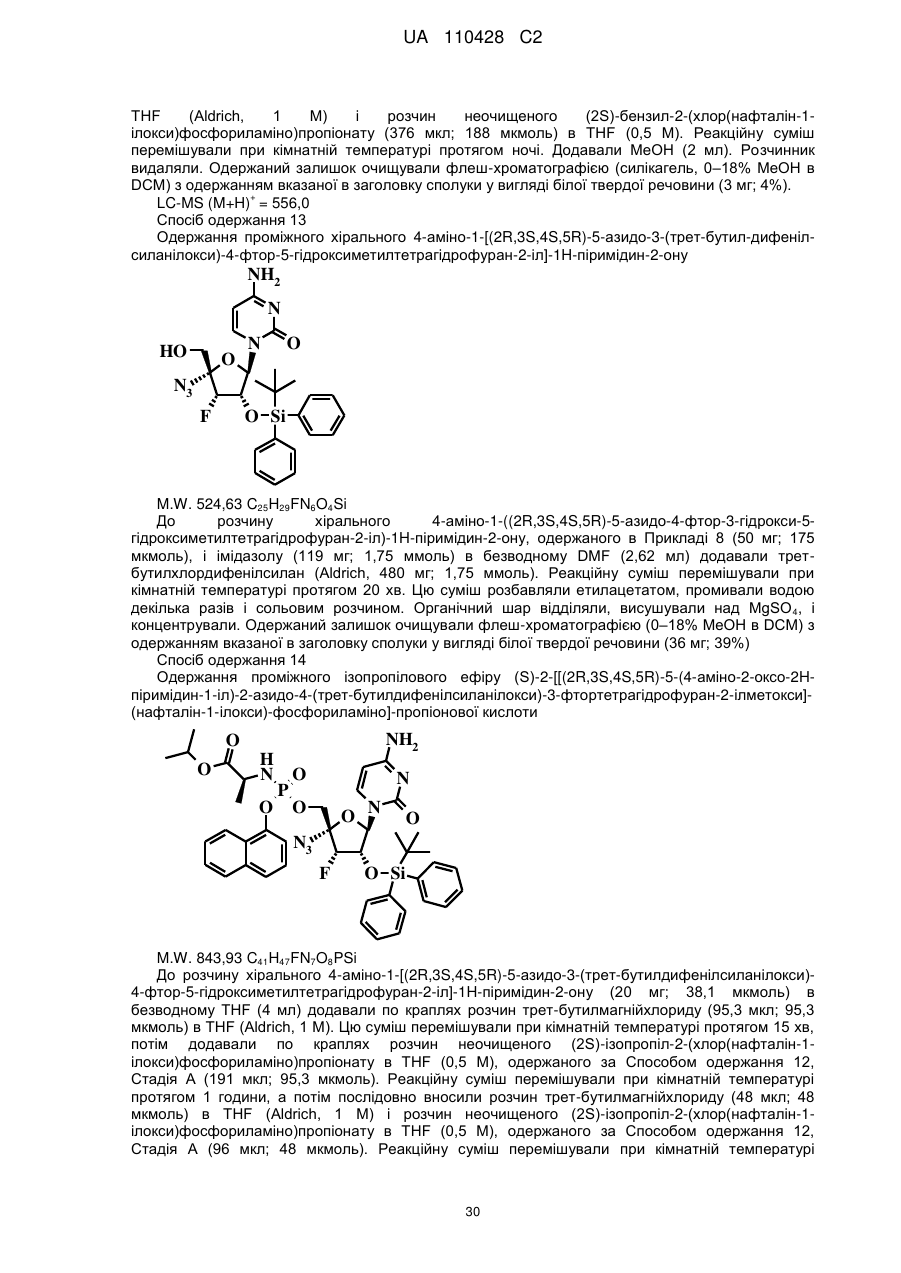
 , І
, І
в якій:
R1 являє собою Н, С1-С12-галогеналкіл або арил, при цьому вказаний арил являє собою феніл або нафтил, які можливо містять як замісники одну або декілька наступних груп: С1-С12-алкіл, С2-С7-алкеніл, С2-С7-алкініл, С1-С12-алкоксигрупу, галоген, С1-С12-галогеналкіл, -N(R1a)2, ациламіногрупу, -SO2N(R1a)2, -COR1b, -SO2(R1c), -NHSO2(R1c), нітрогрупу або ціаногрупу;
кожний з R1a являє собою незалежно Н або С1-С12-алкіл;
кожний з R1b являє собою незалежно -OR1a або -N(R1a)2;
кожний з R1c являє собою С1-С12-алкіл;
R2a являє собою Н;
R2b являє собою метил;
R3 являє собою ізопропіл, етил або бензил;
R4 являє собою Н, С1-С12-алкіл, або R2b та R4 спільно утворюють (СН2)3;
R5 являє собою Н, C(=O)R1c, C(=O)R1b, P(=O)(OR1)(OR1a) або P(=O)(OR1)(NR4R7);
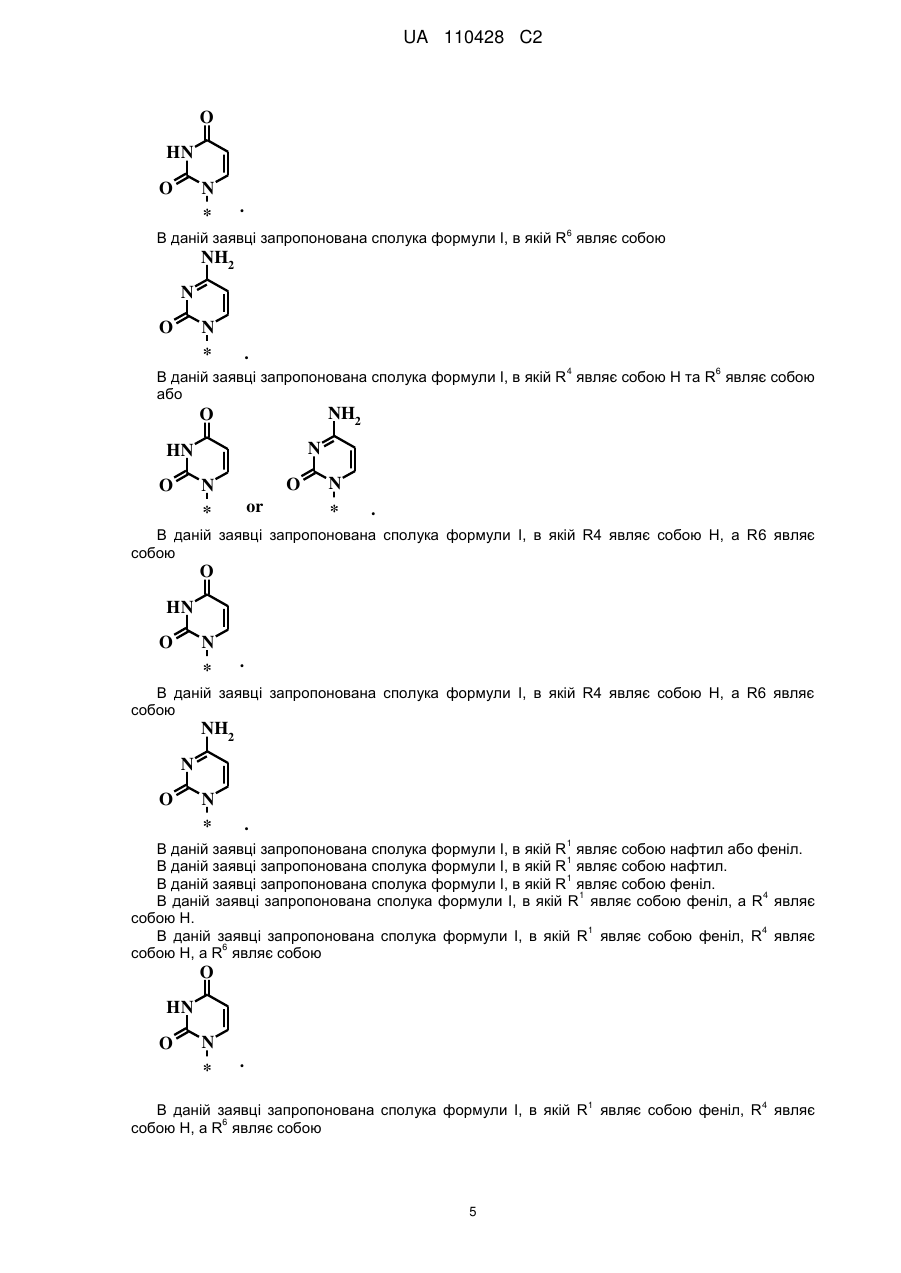
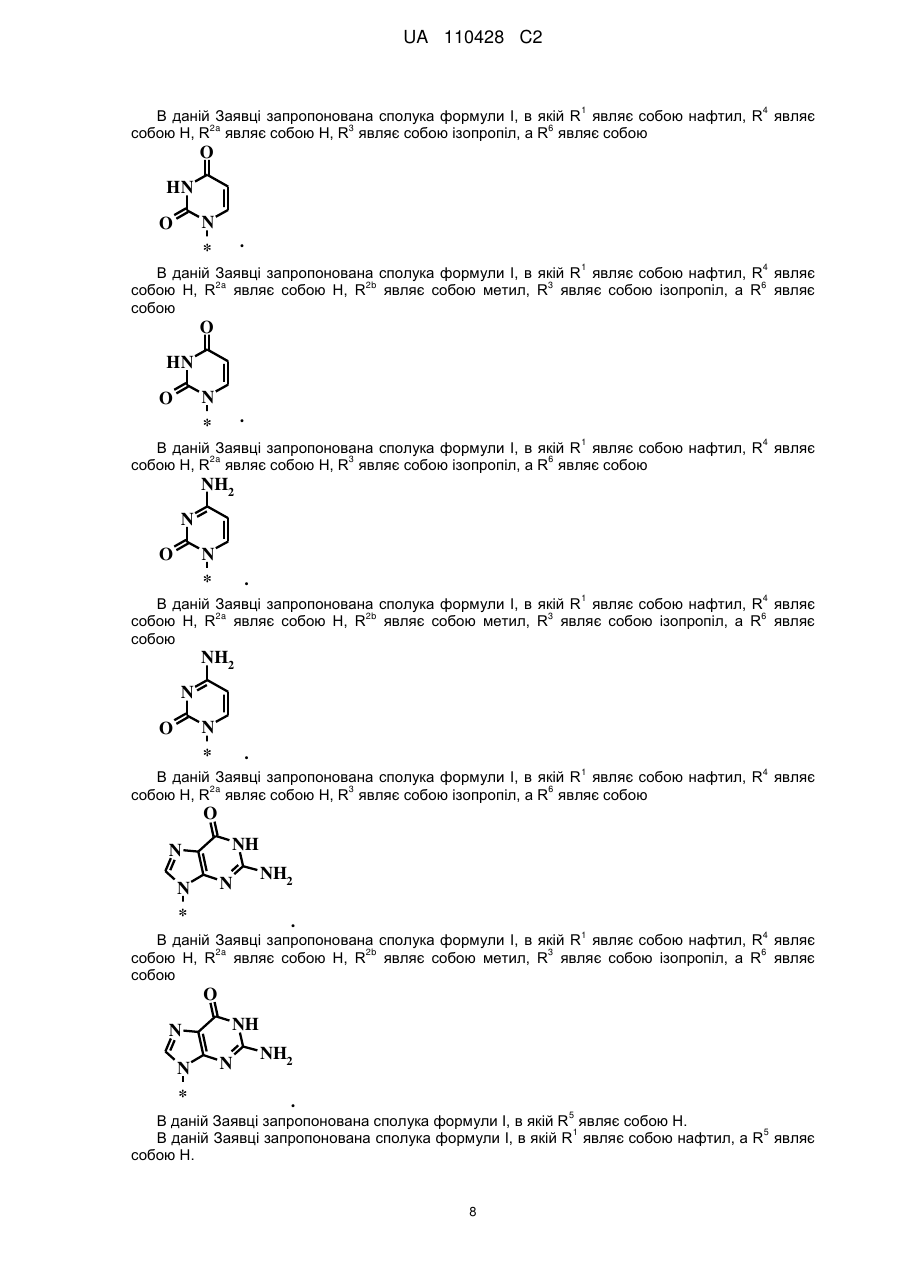
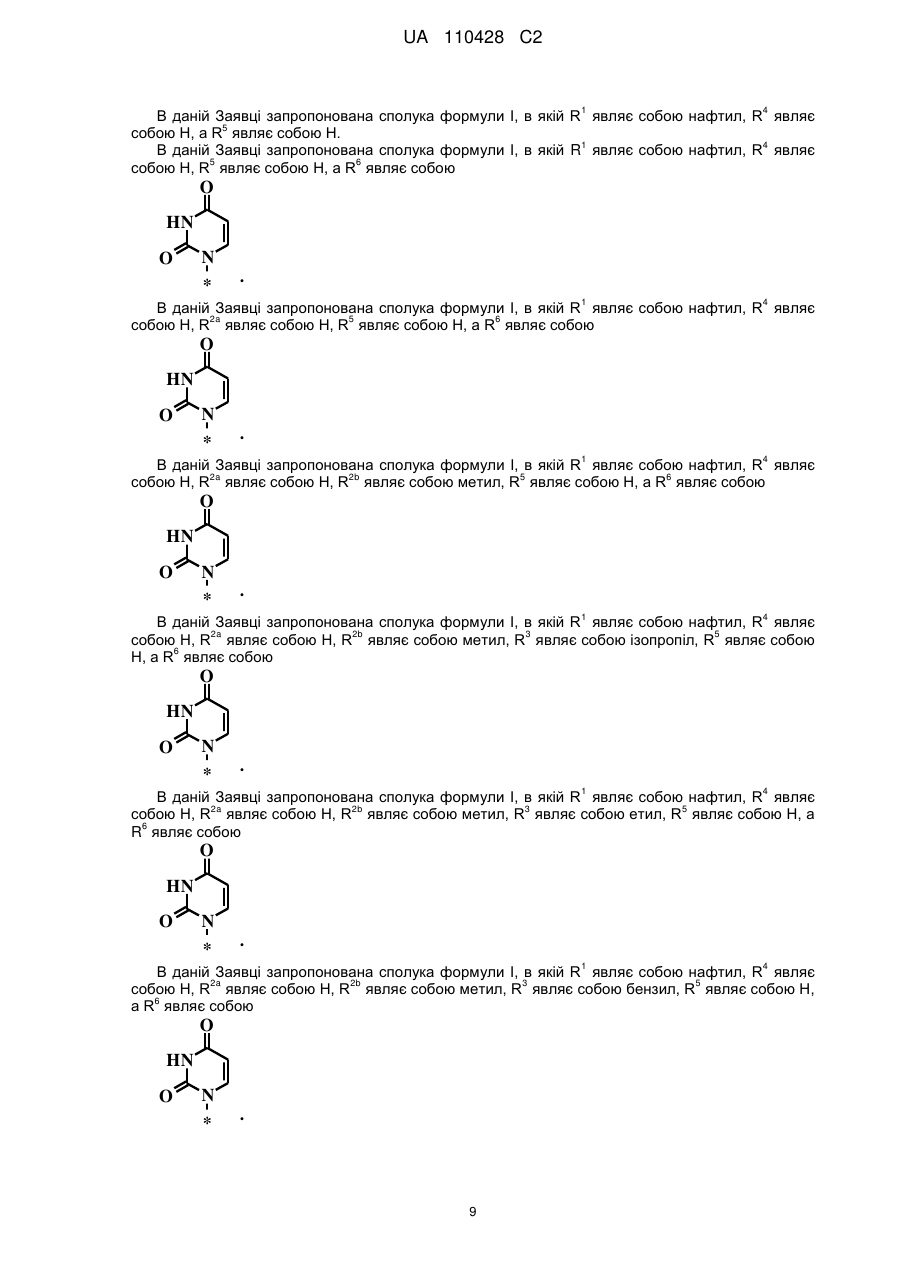
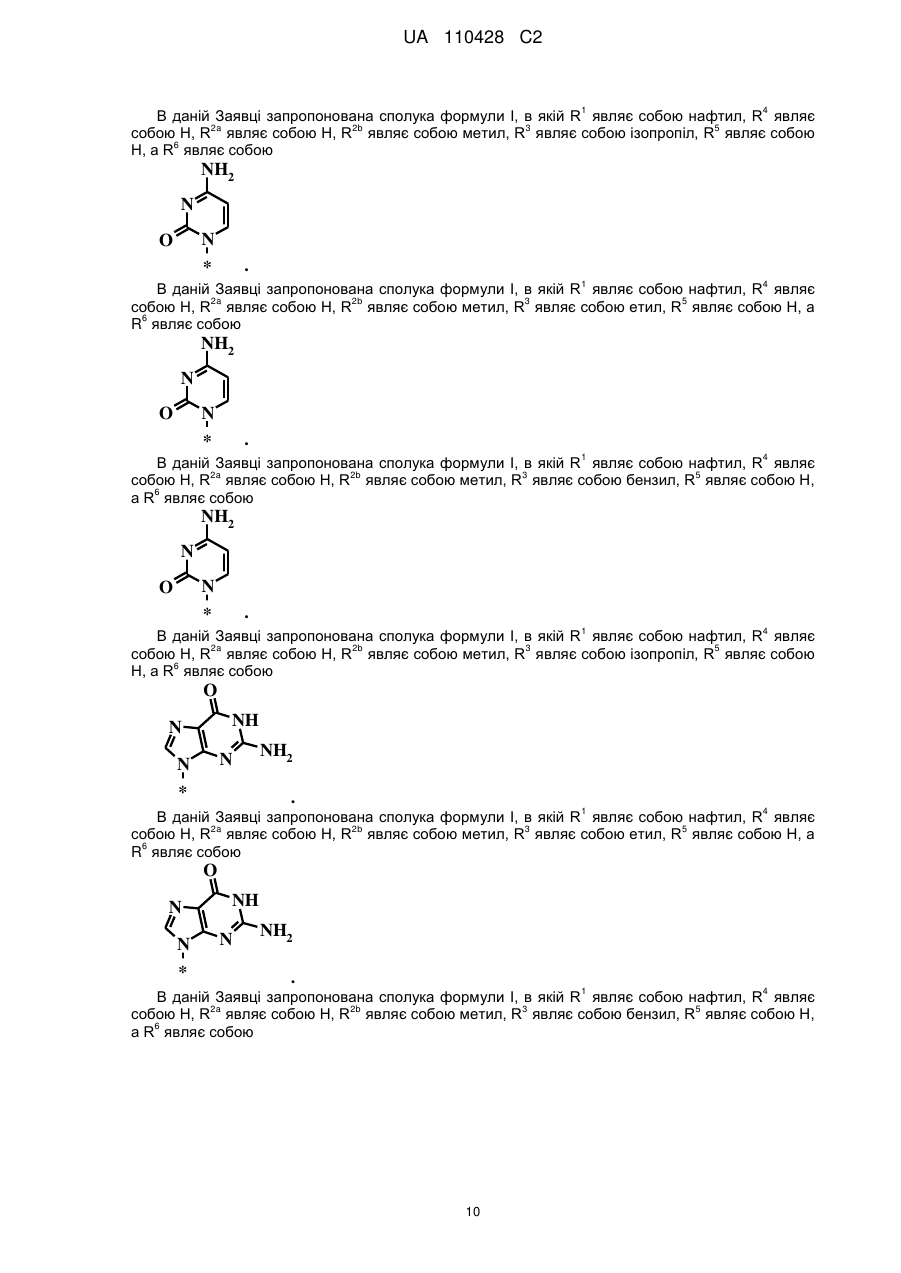
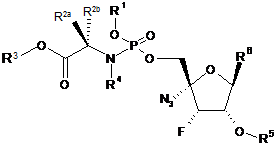
R6 являє собою
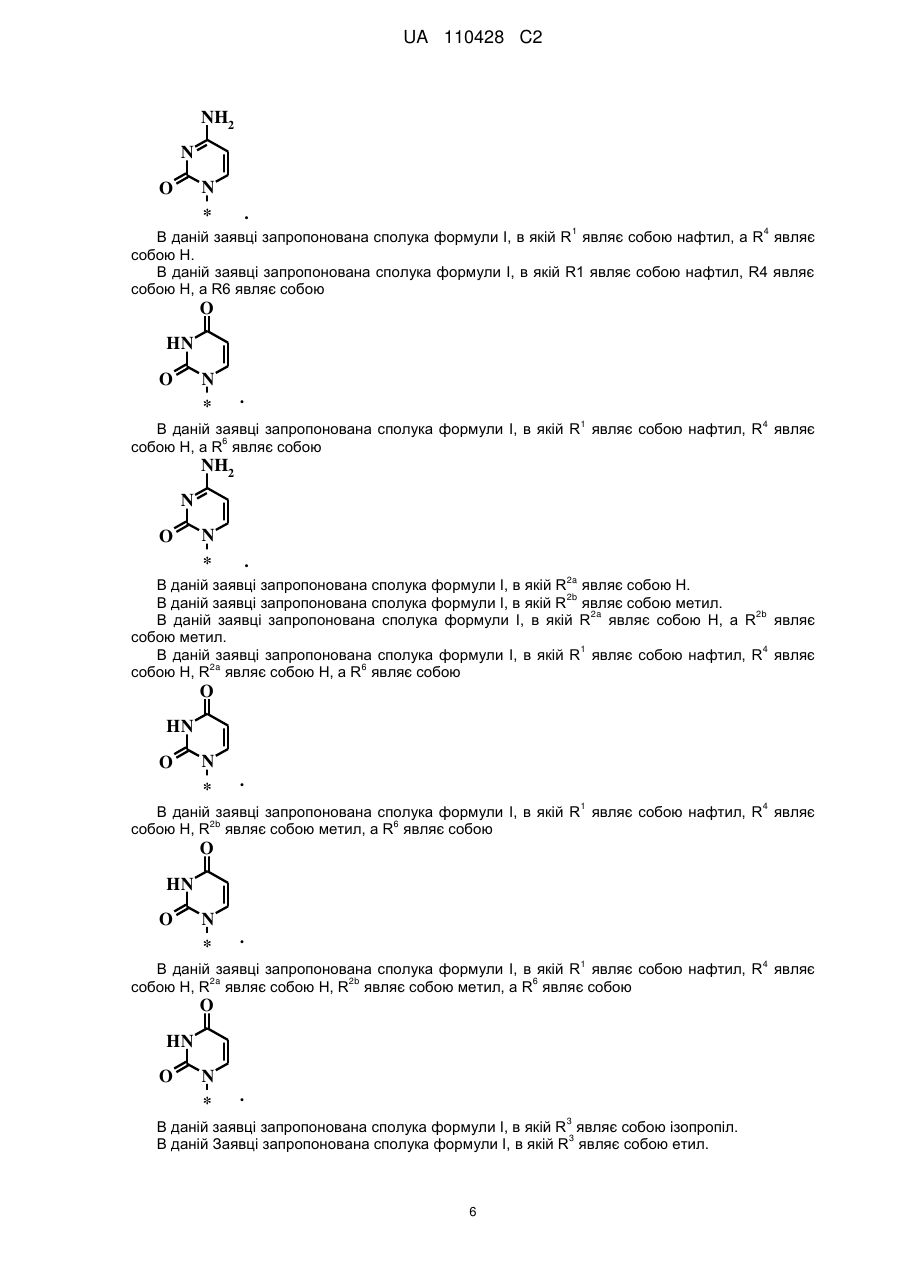
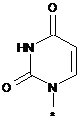 або
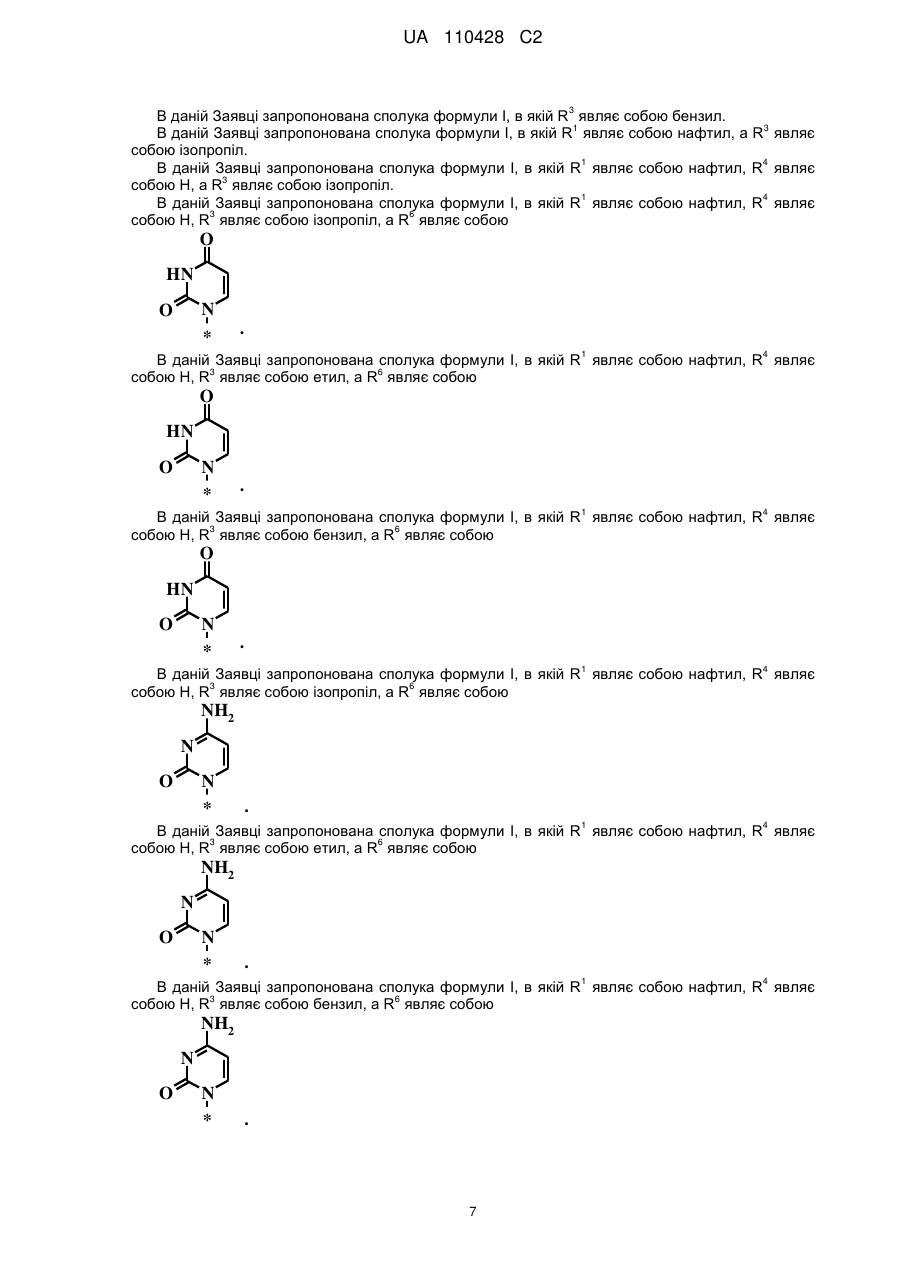
або 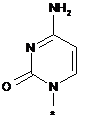 ;
;
m дорівнює від 0 до 3;
n дорівнює 4 або 5;
р дорівнює від 0 до 2; і
r дорівнює від 1 до 6;
або її фармацевтично прийнятна сіль.
2. Сполука за п. 1, в якій R4 являє собою Н.
3. Сполука за п. 2, в якій R1 являє собою нафтил або феніл.
4. Сполука за п. 3, в якій R5 являє собою Н.
5. Сполука за п. 3, в якій R5 являє собою C(=O)R1c.
6. Сполука за п. 5, в якій R1c являє собою етил.
7. Сполука за п. 4, в якій R6 являє собою
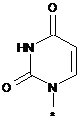 .
.
8. Сполука за п. 4, в якій R6 являє собою
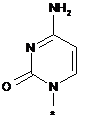 .
.
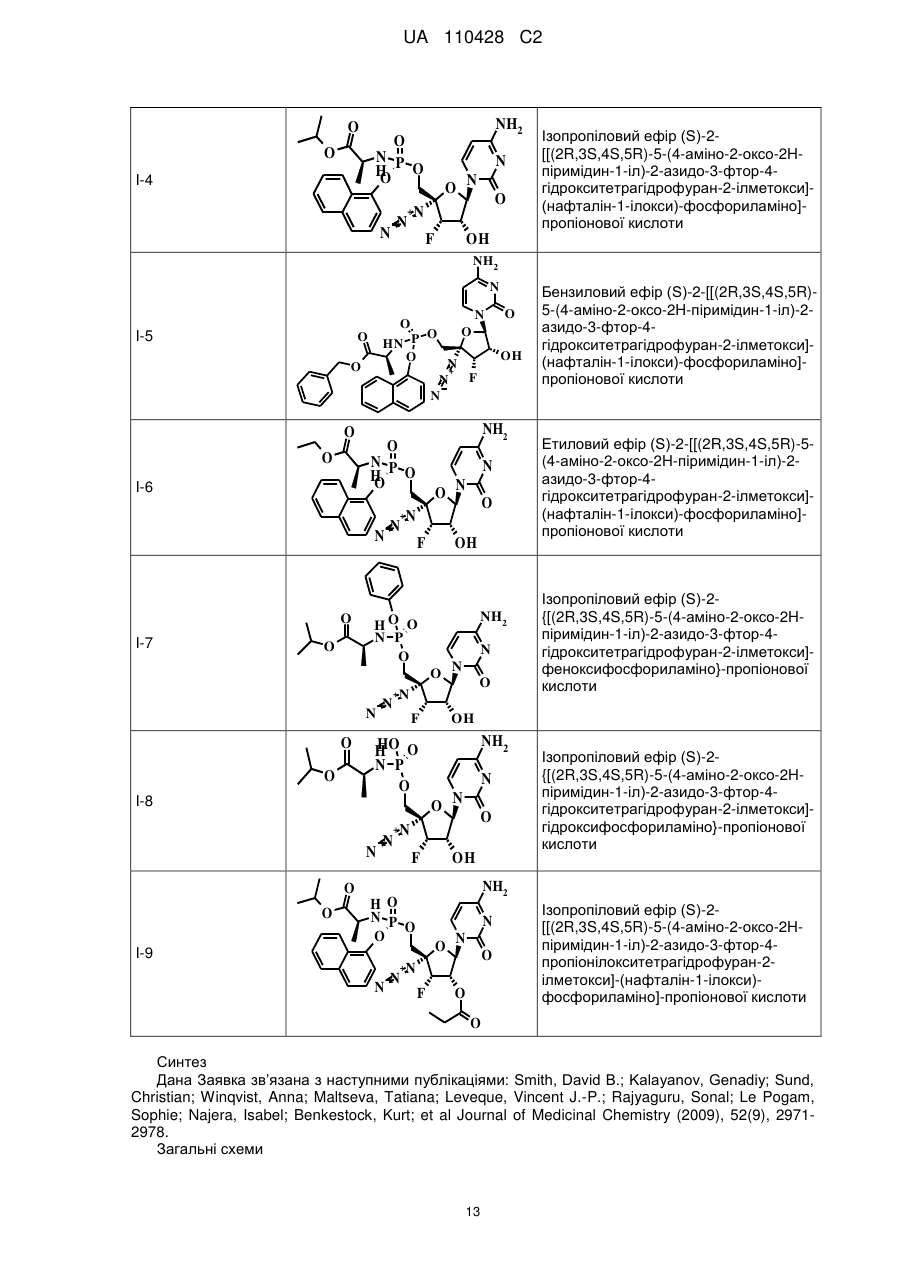
9. Сполука загальної формули І, вибрана з групи, яка складається з наступних сполук:
ізопропіловий ефір (S)-2-{[(2R,3S,4S,5R)-2-азидо-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-феноксифосфориламіно}-пропіонової кислоти;
етиловий ефір (S)-2-{[(2R,3S,4S,5R)-2-азидо-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-феноксифосфориламіно}-пропіонової кислоти;
етиловий ефір (S)-2-[[(2R,3S,4S,5R)-2-азидо-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)-фосфориламіно]-пропіонової кислоти;
ізопропіловий ефір (S)-2-[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2-азидо-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)-фосфориламіно]-пропіонової кислоти;
бензиловий ефір (S)-2-[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2-азидо-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)-фосфориламіно]-пропіонової кислоти;
етиловий ефір (S)-2-[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2-азидо-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)-фосфориламіно]-пропіонової кислоти;
ізопропіловий ефір (S)-2-{[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2-азидо-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-феноксифосфориламіно}-пропіонової кислоти;
ізопропіловий ефір (S)-2-{[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2-азидо-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-гідроксифосфориламіно}-пропіонової кислоти і
ізопропіловий ефір (S)-2-[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2-азидо-3-фтор-4-пропіонілокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)-фосфориламіно]-пропіонової кислоти.
10. Застосування сполуки за будь-яким з пп. 1-9 для лікування або профілактики інфекції вірусу гепатиту С (ВГС).
11. Застосування сполуки за будь-яким з пп. 1-9 для виготовлення лікарського засобу для лікування або профілактики інфекції вірусу гепатиту С (ВГС).
12. Сполука за будь-яким з пп. 1-9 для лікування або профілактики інфекції вірусу гепатиту С (ВГС).
13. Спосіб лікування інфекції вірусу гепатиту С (ВГС), який включає введення пацієнту, який цього потребує, терапевтично ефективної кількості сполуки за будь-яким з пп. 1-9.
14. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-9 і терапевтично інертні носії.
Текст
Реферат: Даний винахід стосується застосування нуклеозидних похідних формули І R 3 O 2b R R2a R O N O R 1 P O O O 4 R 6 N3 F O 5 R ,І де символи мають значення, визначені в описі, і їх фармацевтично прийнятних солей, а також фармацевтичних композицій, які містять такі сполуки. UA 110428 C2 (12) UA 110428 C2 UA 110428 C2 Даний винахід відноситься до нуклеозидних похідних як інгібіторів реплікації РНК реплікона ВГС. Зокрема, даний винахід стосується застосування пуринових і пиримідинових нуклеозидних похідних як інгібіторів реплікації субгеномної РНК вірусу гепатиту C (ВГС) і фармацевтичних композицій, що містять такі сполуки. Вірус гепатиту C є головною причиною хронічних захворювань печінки у світі. Пацієнти, інфіковані ВГС, мають ризик розвитку цирозу печінки і подальшого печінковоклітинного раку, і, отже, ВГС є головним показником до пересадки печінки. У наш час доступні тільки два схвалені терапевтичні способи для лікування ВГС-інфекції (R. G. Gish, Sem. Liver. Dis., 1999, 19, 35). Це монотерапія за допомогою інтерферону-α і, з недавнього часу, комбінована терапія за допомогою нуклеозидного аналога, рибавірину (Virazole), та інтерферону-α. Багато лікарських речовин, схвалених для лікування вірусних інфекцій, являють собою нуклеозиди або аналоги нуклеозидів, і більшість таких лікарських речовин - нуклеозидних аналогів інгібують реплікацію вірусу після їх перетворення на відповідні трифосфати, шляхом інгібування ферментів вірусної полімерази. Це перетворення на трифосфат звичайно опосередковане клітинними кіназами, і тому пряму оцінку нуклеозидів як інгібіторів реплікації ВГС зручно здійснювати тільки за допомогою клітинного аналізу. Для ВГС відсутній істинний клітинний аналіз реплікації вірусу або тваринна модель інфікування. Вірус гепатиту C належить до сімейства Flaviridae. Він являє собою РНК-вірус, при цьому РНК кодує великий поліпротеїн, який після процесування генерує необхідний механізм реплікації, щоб забезпечити синтез дочірньої РНК. Вважають, що більшість не-структурних білків, що кодуються геномом РНК ВГС, залучена в реплікацію РНК. Lohmann та співавт. [V. Lohmann et al., Science, 1999, 285, 110-113] описали конструкцію клітинної лінії людської гепатоми (Huh7), в яку вводили молекули субгеномної РНК ВГС, і було показано, що вони реплікуються з високою ефективністю. Вважають, що механізм реплікації РНК в цих лініях клітин ідентичний реплікації повнорозмірного генома РНК ВГС в інфікованих гепатоцитах. Клони субгеномної кДНК ВГС, які були використані для виділення цих клітинних ліній, слугували основою для розробки клітинного аналізу для ідентифікації інгібіторів реплікації ВГС на основі нуклеозидних аналогів. СУТЬ ВИНАХОДУ Сполуки формули I корисні для лікування захворювань, опосередкованих вірусом гепатиту C (ВГС) і для виготовлення фармацевтичних композицій, які включають такі сполуки. У даній заявці запропонована сполука формули I 1 2bR 2a R 3 R O O R O O P 6 N O 4 R N3 O R F O R5 I в якій: 1 R являє собою H, нижчий галогеналкіл або арил, причому вказаний арил являє собою феніл або нафтил, можливо, які містять як замісники одну або більше наступних груп: нижчий алкіл, нижчий алкеніл, нижчий алкініл, нижчу алкоксигрупу, галоген, нижчий галогеналкіл, 1a 1a 1b 1c 1c N(R )2, ациламіногрупу, -SO2N(R )2, -COR , -SO2(R ), -NHSO2(R ), нітрогрупу або ціаногрупу; 1a кожен з R являє собою незалежно H або нижчий алкіл; 1b 1a 1a кожен з R являє собою незалежно -OR або - N(R )2; 1c кожен з R являє собою нижчий алкіл; 2a 2b 1a R та R являють собою (i) незалежно H, нижчий алкіл, - -(CH2)rN(R )2, нижчий гідроксіалкіл, -CH2SH, -(CH2)S(O)pMe, -(CH2)3NHC(=NH)NH2, (1H-індол-3-іл)метил, (1Н-індол-41b іл)метил, -(CH2)mC(=O)R , арил і арил-нижчий алкіл, при цьому вказаний арил, можливо, містить як замісники одну або більше наступних груп: гідроксигрупу, нижчий алкіл, нижчу 2a 2b 4 алкоксигрупу, галоген, нітрогрупу або ціаногрупу; (ii) R являє собою H, а R та R спільно 2a 2b 2a 2b утворюють (CH2)3; (iii) R та R спільно утворюють CH2)n n; або (iv) R та R обидва являють собою нижчий алкіл; 3 R являє собою H, нижчий алкіл, нижчий галогеналкіл, феніл або феніл нижчий алкіл; 4 2b 4 R являє собою H, нижчий алкіл, або R та R спільно утворюють (CH2)3; 1 UA 110428 C2 5 1c 1b 1 1a 1 4 7 R являє собою H, C(=O)R , C(=O)R , P(=O)(OR )(OR ) або P(=O)(OR )(NR R ); 6 R являє собою або N N HN O O NH2 O O N * , N N * , or * NH N NH2 ; m дорівнює від 0 до 3; n дорівнює 4 або 5; p дорівнює від 0 до 2; і r дорівнює від 1 до 6; або її фармацевтично прийнятна сіль. У даній заявці запропонований спосіб лікування інфекції вірусом гепатиту C (ВГС), який включає введення пацієнту, який цього потребує, терапевтично ефективної кількості сполуки формули I. У даній заявці запропонована композиція, яка включає сполуку формули I і фармацевтично прийнятний ексципієнт. Докладний опис винаходу Показали, що сполуки формули I являють собою інгібітори субгеномної реплікації вірусу гепатиту C в лінії клітин гепатоми. Ці сполуки потенційно ефективні як противірусні лікарські засоби для лікування ВГС-інфекцій у людини. Термін "алкіл", який використовується в даному описі, означає вуглеводневий залишок з лінійним або розгалуженим ланцюгом, що містить від 1 до 12 атомів вуглецю. Переважно, термін "алкіл" означає вуглеводневий залишок з лінійним або розгалуженим ланцюгом, що містить від 1 до 7 атомів вуглецю. Найбільш прийнятні метил, етил, пропіл, ізопропіл, н-бутил, ізобутил, терт-бутил або пентил. Алкіл може бути незаміщеним або заміщеним. Замісники вибирають з однієї або декількох наступних груп: циклоалкіл, нітрогрупа, аміногрупа, алкіламіногрупа, діалкіламіногрупа, алкілкарбоніл та циклоалкілкарбоніл. Термін "циклоалкіл", який використовується в даному описі, означає можливо заміщену циклоалкільну групу, що містить від 3 до 7 атомів вуглецю, наприклад, циклопропіл, циклобутил, циклопентил, циклогексил або циклогептил. Термін "алкокси", який використовується в даному описі, означає можливо заміщену алкілокси-групу з лінійним або розгалуженим ланцюгом, в якому алкільний фрагмент розкритий вище, таку як метокси-, етокси-, н-пропілокси-, ізопропілокси-, н-бутилокси-, ізобутилокси-, третбутилокси-, пентилокси-, гексилокси-, гептилоксигрупа, включаючи їх ізомери. Термін "алкоксіалкіл", який використовується в даному описі, означає алкоксигрупу, розкриту вище, яка приєднана до алкільної групи, розкритої вище. Прикладами є метоксиметил, метоксіетил, метоксипропіл, етоксиметил, етоксіетил, етоксипропіл, пропілоксипропіл, метоксибутил, етоксибутил, пропілоксибутил, бутилоксибутил, трет-бутилоксибутил, метоксипентил, етоксипентил, пропілоксипентил, включаючи їх ізомери. Термін "алкеніл", який використовується в даному описі, означає радикал з незаміщеним або заміщеним вуглеводневим ланцюгом, що включає від 2 до 7 атомів вуглецю, переважно, від 2 до 4 атомів вуглецю, і містить один або два олефінові подвійні зв'язки, переважно, один олефіновий подвійний зв'язок. Прикладами є вініл, 1-пропеніл, 2-пропеніл (аліл) або 2-бутеніл (кротил). Термін "алкініл", який використовується в даному описі, означає радикал з незаміщеним або заміщеним вуглеводневим ланцюгом, що містить від 2 до 7 атомів вуглецю, переважно, від 2 до 4 атомів вуглецю, і включає один або, якщо можливо, два потрійні зв'язки, переважно, один потрійний зв'язок. Прикладами є етиніл, 1-пропініл, 2-пропініл, 1-бутиніл, 2-бутиніл або 3бутиніл. Термін "гідроксіалкіл", який використовується в даному описі, означає алкільну групу з лінійним або розгалуженим ланцюгом, розкриту вище, в якій 1, 2, 3 або більше атомів водню заміщені гідроксигрупою. Прикладами є гідроксиметил, 1-гідроксіетил, 2-гідроксіетил, 1гідроксипропіл, 2-гідроксипропіл, 3-гідроксипропіл, гідроксіізопропіл, гідроксибутил і тому подібне. Термін "галогеналкіл", який використовується в даному описі, означає алкільну групу з лінійним або розгалуженим ланцюгом, розкриту вище, в якій 1, 2, 3 або більше атомів водню 2 UA 110428 C2 заміщені атомами галогену. Прикладами є 1-фторметил, 1-хлорметил, 1-бромметил, 1іодметил, трифторметил, трихлорметил, трибромметил, трийодметил, 1-фторетил, 1-хлоретил, 1-брометил, 1-іодетил, 2-фторетил, 2-хлоретил, 2-брометил, 2-іодетил, 2,2-дихлоретил, 3бромпропіл або 2,2,2-трифторетил і тому подібне. Термін "алкілтіо", який використовується в даному описі, означає (алкіл)S- групу з лінійним або розгалуженим ланцюгом, в якій алкільний фрагмент розкритий вище. Прикладами є метилтіо-, етилтіо-, н-пропілтіо-, ізо-пропілтіо-, н-бутилтіо-, ізобутилтіо- або трет-бутилтіогрупа. Термін “арил”, який використовується в даному описі, означає можливо заміщений феніл і нафтил (наприклад, 1-нафтил, 2-нафтил або 3-нафтил). Підходящі замісники для арилу можна вибирати з тих, які вказані для алкілу, і до цього переліку для вибору додатково можна додати наступні замісники: галоген, гідроксигрупа і можливо заміщений алкіл, галогеналкіл, алкеніл, алкініл та арилоксигрупа. Термін “гетероцикліл”, який використовується в даному описі, означає можливо заміщені насичені, частково ненасичені або ароматичні моноциклічні, біциклічні або трициклічні гетероциклічні системи, які містять один або більше гетероатомів, вибраних з азоту, кисню і сірки, які можуть бути також конденсовані з можливо заміщеним насиченим, частково ненасиченим або ароматичним моноциклічним карбоциклом або гетероциклом. Прикладами підходящих гетероциклів є оксазоліл, ізоксазоліл, фурил, тетрагідрофурил, 1,3діоксоланіл, дигідропіраніл, 2-тієніл, 3-тієніл, піразиніл, ізотіазоліл, дигідрооксазоліл, піримідиніл, тетразоліл, 1-піролідиніл, 2-піролідиніл, 3-піролідиніл, піролідиноніл, (N-оксид)піридиніл, 1-піроліл, 2-піроліл, триазоліл, наприклад, 1,2,3-триазоліл або 1,2,4-триазоліл, 1піразоліл, 2-піразоліл, 4-піразоліл, піперидиніл, морфолініл (наприклад, 4-морфолініл), тіоморфолініл (наприклад, 4-тіоморфолініл), тіазоліл, піридиніл, дигідротіазоліл, імідазолідиніл, піразолініл, піперазиніл, 1-імідазоліл, 2-імідазоліл, 4-імідазоліл, тіадіазоліл, наприклад, 1,2,3тіадіазоліл, 4-метилпіперазиніл, 4-гідроксипіперидин-1-іл. Підходящі замісники для гетероциклілу можна вибирати з тих, які були вказані для алкілу, і до цього переліку для вибору додатково можна додати наступні замісники: можливо заміщений алкіл, алкеніл, алкініл, оксогрупа (=O) або аміносульфоніл. Термін “ацил” ("алкілкарбоніл"), який використовується в даному описі, означає групу формули C(=O)R, в якій R являє собою водень, незаміщений або заміщений вуглеводневий залишок з лінійним або розгалуженим ланцюгом, що містить від 1 до 7 атомів вуглецю, або фенільну групу. Найбільш переважно, ацильні групи являють собою ті, в яких R являє собою водень, незаміщений вуглеводневий залишок з лінійним або розгалуженим ланцюгом, що містить від 1 до 4 атомів вуглецю, або фенільну групу. Термін галоген означає фтор, хлор, бром або йод, переважно фтор, хлор, бром. В графічному представленні сполук, наведених в даній заявці, потовщена загострена лінія ( ) означає замісник, який знаходиться вище площини кільця, до якого належить асиметричний атом вуглецю, а точкова лінія ( ) означає замісник, який розташований нижче площини кільця, до якого належить асиметричний атом вуглецю. Сполуки формули I виявляють стереоізомерію. Ці сполуки можуть являти собою будь-який ізомер сполуки формули I або суміші таких ізомерів. Сполуки і проміжні продукти за даним винаходом, які містять один або більше асиметричних атомів вуглецю, можуть бути одержані у вигляді рацемічних сумішей стереоізомерів, які можна розділяти. Сполуки формули I виявляють таутомерію, і це означає, що сполуки за даним винаходом можуть існувати у вигляді двох або більше хімічних сполук, які здатні легко перетворюватися одна на одну. У багатьох випадках це просто означає обмін атомом водню між двома іншими атомами, з кожним з яких він утворює ковалентний зв’язок. Таутомірні сполуки існують у рухливій рівновазі одна з одною, і спроби одержати окремі сполуки звичайно призводять до утворення суміші з усіма хімічними та фізичними властивостями, які очікувалися, виходячи зі структури її компонентів. Найбільш поширений тип таутомерії включає карбонільні, або кето-сполуки, і ненасичені гідрокси-сполуки, або еноли. Структурна зміна полягає в переміщенні атома водню між атомами вуглецю і кисню з перегрупуванням зв’язків. Наприклад, у багатьох аліфатичних альдегідах і кетонах, таких як ацетальдегід, переважає кето-форма; в фенолах основним компонентом є енольна форма. Сполуки формули I, які є основними, можуть утворювати фармацевтично прийнятні солі з неорганічними кислотами, такими як галогеноводневі кислоти (наприклад, хлороводнева кислота і бромоводнева кислота), сірчана кислота, азотна кислота і фосфорна кислота і тому подібне, а також з органічними кислотами (наприклад, з оцтовою кислотою, винною кислотою, бурштиновою кислотою, фумаровою кислотою, малеїновою кислотою, яблучною кислотою, 3 UA 110428 C2 саліциловою кислотою, лимонною кислотою, метансульфоновою кислотою і птолуолсульфоновою кислотою і тому подібне). Одержання і виділення таких солей можна здійснювати способами, відомими в даній галузі техніки. Інгібітори ВГС В даній заявці запропонована сполука формули I 1 2bR 2a R 3 R O O R O O P 6 N O 4 R N3 O R O R5 F I в якій: 1 R являє собою H, нижчий галогеналкіл або арил, при цьому вказаний арил являє собою феніл або нафтил, можливо, які містять як замісники одну або більше наступних груп: нижчий алкіл, нижчий алкеніл, нижчий алкініл, нижчу алкоксигрупу, галоген, нижчий галогеналкіл, 1a 1a 1b 1c 1c N(R )2, ациламіногрупу, -SO2N(R )2, -COR , -SO2(R ), -NHSO2(R ), нітрогрупу або ціаногрупу; 1a кожний з R являє собою незалежно H або нижчий алкіл; 1b 1a 1a кожний з R являє собою незалежно -OR або -N(R )2; 1c кожний з R являє собою нижчий алкіл; 2a 2b 1a R та R являють собою (i) незалежно H, нижчий алкіл, -(CH2)rN(R )2, нижчий гідроксіалкіл, -CH2SH, -(CH2)S(O)pMe, -(CH2)3NHC(=NH)NH2, (1H-індол-3-іл)метил, (1H-індол-4-іл)метил, 1b (CH2)mC(=O)R , арил і арил–нижчий алкіл, при цьому вказаний арил можливо, містить як замісники одну або більше наступних груп: гідроксигрупу, нижчий алкіл, нижчу алкоксигрупу, 2a 2b 4 галоген, нітрогрупу або ціаногрупу; (ii) R являє собою H, а R та R спільно утворюють (CH2)3; 2a 2b 2a 2b (iii) R та R спільно утворюють (CH2)n; або (iv) R та R обидва являють собою нижчий алкіл; 3 R являє собою H, нижчий алкіл, нижчий галогеналкіл, феніл або феніл нижчий алкіл; 4 2b 4 R являє собою H, нижчий алкіл, або R та R спільно утворюють (CH2)3; 5 1c 1b 1 1a 1 4 7 R являє собою H, C(=O)R , C(=O)R , P(=O)(OR )(OR ) або P(=O)(OR )(NR R ); 6 R являє собою або N N HN O O NH2 O * N N O N , , or * * NH N NH2 ; m дорівнює від 0 до 3; n дорівнює 4 або 5; p дорівнює від 0 до 2; і r дорівнює від 1 до 6; або її фармацевтично прийнятна сіль. 4 В даній заявці запропонована сполука формули I, в якій R являє собою H. 6 В даній заявці запропонована сполука формули I, в якій R являє собою або NH2 O N HN O O N * or N * . 6 В даній заявці запропонована сполука формули I, в якій R являє собою 4 UA 110428 C2 O HN N O * . 6 В даній заявці запропонована сполука формули I, в якій R являє собою NH2 N N O . * 4 6 В даній заявці запропонована сполука формули I, в якій R являє собою H та R являє собою або NH2 O N HN O N O or * N * . В даній заявці запропонована сполука формули I, в якій R4 являє собою H, а R6 являє собою O HN N O * . В даній заявці запропонована сполука формули I, в якій R4 являє собою H, а R6 являє собою NH2 N O N . * 1 В даній заявці запропонована сполука формули I, в якій R являє собою нафтил або феніл. 1 В даній заявці запропонована сполука формули I, в якій R являє собою нафтил. 1 В даній заявці запропонована сполука формули I, в якій R являє собою феніл. 1 4 В даній заявці запропонована сполука формули I, в якій R являє собою феніл, а R являє собою H. 1 4 В даній заявці запропонована сполука формули I, в якій R являє собою феніл, R являє 6 собою H, а R являє собою O HN O N * . 1 4 В даній заявці запропонована сполука формули I, в якій R являє собою феніл, R являє 6 собою H, а R являє собою 5 UA 110428 C2 NH2 N N O . * 1 4 В даній заявці запропонована сполука формули I, в якій R являє собою нафтил, а R являє собою H. В даній заявці запропонована сполука формули I, в якій R1 являє собою нафтил, R4 являє собою H, а R6 являє собою O HN N O * . 1 4 В даній заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 6 собою H, а R являє собою NH2 N O N . * 2a В даній заявці запропонована сполука формули I, в якій R являє собою H. 2b В даній заявці запропонована сполука формули I, в якій R являє собою метил. 2a 2b В даній заявці запропонована сполука формули I, в якій R являє собою H, а R являє собою метил. 1 4 В даній заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 6 собою H, R являє собою H, а R являє собою O HN O N * . 1 4 1 4 В даній заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2b 6 собою H, R являє собою метил, а R являє собою O HN O N * . В даній заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 6 собою H, R являє собою H, R являє собою метил, а R являє собою O HN O N * . 3 В даній заявці запропонована сполука формули I, в якій R являє собою ізопропіл. 3 В даній Заявці запропонована сполука формули I, в якій R являє собою етил. 6 UA 110428 C2 3 В даній Заявці запропонована сполука формули I, в якій R являє собою бензил. 1 3 В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, а R являє собою ізопропіл. 1 4 В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 3 собою H, а R являє собою ізопропіл. 1 4 В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 3 6 собою H, R являє собою ізопропіл, а R являє собою O HN N O * . 1 4 1 4 1 4 1 4 1 4 В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 3 6 собою H, R являє собою етил, а R являє собою O HN N O * . В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 3 6 собою H, R являє собою бензил, а R являє собою O HN N O * . В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 3 6 собою H, R являє собою ізопропіл, а R являє собою NH2 N N O * . В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 3 6 собою H, R являє собою етил, а R являє собою NH2 N N O * . В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 3 6 собою H, R являє собою бензил, а R являє собою NH2 N O N * . 7 UA 110428 C2 1 4 1 4 1 4 1 4 1 4 1 4 В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 3 6 собою H, R являє собою H, R являє собою ізопропіл, а R являє собою O HN N O . * В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 6 собою H, R являє собою H, R являє собою метил, R являє собою ізопропіл, а R являє собою O HN N O . * В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 3 6 собою H, R являє собою H, R являє собою ізопропіл, а R являє собою NH2 N N O . * В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 6 собою H, R являє собою H, R являє собою метил, R являє собою ізопропіл, а R являє собою NH2 N N O . * В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 3 6 собою H, R являє собою H, R являє собою ізопропіл, а R являє собою O NH N N N * NH2 . В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 6 собою H, R являє собою H, R являє собою метил, R являє собою ізопропіл, а R являє собою O N N * NH N NH2 . 5 В даній Заявці запропонована сполука формули I, в якій R являє собою H. 1 5 В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, а R являє собою H. 8 UA 110428 C2 1 4 1 4 1 4 1 4 1 4 1 4 В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 5 собою H, а R являє собою H. 1 4 В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 5 6 собою H, R являє собою H, а R являє собою O HN O N * . В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 5 6 собою H, R являє собою H, R являє собою H, а R являє собою O HN O N * . В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 5 6 собою H, R являє собою H, R являє собою метил, R являє собою H, а R являє собою O HN O N * . В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 5 собою H, R являє собою H, R являє собою метил, R являє собою ізопропіл, R являє собою 6 H, а R являє собою O HN O N * . В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 5 собою H, R являє собою H, R являє собою метил, R являє собою етил, R являє собою H, а 6 R являє собою O HN O N * . В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 5 собою H, R являє собою H, R являє собою метил, R являє собою бензил, R являє собою H, 6 а R являє собою O HN O N * . 9 UA 110428 C2 1 4 1 4 1 4 1 4 1 4 1 4 В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 5 собою H, R являє собою H, R являє собою метил, R являє собою ізопропіл, R являє собою 6 H, а R являє собою NH2 N N O . * В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 5 собою H, R являє собою H, R являє собою метил, R являє собою етил, R являє собою H, а 6 R являє собою NH2 N N O . * В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 5 собою H, R являє собою H, R являє собою метил, R являє собою бензил, R являє собою H, 6 а R являє собою NH2 N N O . * В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 5 собою H, R являє собою H, R являє собою метил, R являє собою ізопропіл, R являє собою 6 H, а R являє собою O NH N N N * NH2 . В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 5 собою H, R являє собою H, R являє собою метил, R являє собою етил, R являє собою H, а 6 R являє собою O N N * NH N NH2 . В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 5 собою H, R являє собою H, R являє собою метил, R являє собою бензил, R являє собою H, 6 а R являє собою 10 UA 110428 C2 O NH N NH2 N N * . 5 1c В даній Заявці запропонована сполука формули I, в якій R являє собою C(=O)R . 1 4 В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 5 собою H, R являє собою H, R являє собою метил, R являє собою ізопропіл, R являє собою 1c 6 C(=O)R , а R являє собою NH2 N N O * . 1c В даній Заявці запропонована сполука формули I, в якій R являє собою етил. 1 4 В даній Заявці запропонована сполука формули I, в якій R являє собою нафтил, R являє 2a 2b 3 5 собою H, R являє собою H, R являє собою метил, R являє собою ізопропіл, R являє собою 6 C(=O)CH2CH3, а R являє собою NH2 N O N * . В даній Заявці запропонована сполука, вибрана з групи, яка складається з наступних сполук: ізопропіловий ефір (S)-2-{[(2R,3S,4S,5R)-2-азидо-5-(2,4-діоксо-3,4-дигідро-2H-піримідин1-іл)-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-фенокси-фосфориламіно}-пропіонової кислоти; етиловий ефір (S)-2-{[(2R,3S,4S,5R)-2-азидо-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1іл)-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-фенокси-фосфориламіно}-пропіонової кислоти; етиловий ефір (S)-2-[[(2R,3S,4S,5R)-2-азидо-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1іл)-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)-фосфориламіно]пропіонової кислоти; ізопропіловий ефір (S)-2-[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2-азидо-3фтор-4-гідрокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)-фосфориламіно]пропіонової кислоти; бензиловий ефір (S)-2-[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2-азидо-3фтор-4-гідрокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)-фосфориламіно]пропіонової кислоти; етиловий ефір (S)-2-[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2-азидо-3фтор-4-гідрокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)-фосфориламіно]пропіонової кислоти; ізопропіловий ефір (S)-2-{[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2-азидо-3фтор-4-гідрокситетрагідрофуран-2-ілметокси]-феноксифосфориламіно}-пропіонової кислоти; ізопропіловий ефір (S)-2-{[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2-азидо-3фтор-4-гідрокситетрагідрофуран-2-ілметокси]-гідроксифосфориламіно}-пропіонової кислоти; і ізопропіловий ефір (S)-2-[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2-азидо-3фтор-4-пропіонілокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)-фосфориламіно]пропіонової кислоти. 11 UA 110428 C2 В даній Заявці запропонований спосіб лікування інфекції вірусом гепатиту C (ВГС), який включає введення пацієнту, який цього потребує, терапевтично ефективної кількості сполуки формули I. В даній Заявці запропонований вказаний вище спосіб, який додатково включає введення модулятора імунної системи або противірусного агента, який інгібує реплікацію ВГС, або їх комбінацію. В даній Заявці запропонований вказаний вище спосіб, в якому модулятор імунної системи являє собою інтерферон або хімічно дериватизований інтерферон. В даній Заявці запропоновані вказані вище способи, в яких противірусний агент вибирають з групи, яка складається з інгібітору протеази ВГС, інгібітору полімерази ВГС, інгібітору гелікази ВГС, інгібітору праймази ВГС, інгібітору злиття ВГС та їх комбінації. В даній Заявці запропонований спосіб інгібування реплікації ВГС в клітині, який включає введення сполуки формули I. В даній Заявці запропонована композиція, яка включає сполука формули I і фармацевтично прийнятний ексципієнт. В даній Заявці запропоноване застосування сполуки формули I у виготовленні лікарського засобу для лікування ВГС-інфекції. В даній Заявці запропоновані сполука, композиція або спосіб, розкриті в даному описі. Сполуки Вибіркові приклади сполук, що охоплюються даним винаходом і входять в обсяг даного винаходу, представлені в нижче наведеній Таблиці. Ці приклади і способи одержання, які йдуть далі, наведені для того щоб допомогти фахівцю в даній галузі техніки більш чіткого зрозуміти та здійснити на практиці даний винахід. Їх слід розглядати не як обмеження обсягу даного винаходу, а лише як його ілюстрацію і наглядний приклад. В загальному випадку номенклатура, яка використана в даній Заявці, основана на TM AUTONOM v.4.0, комп’ютеризованій системі Інституту Бельштейна для генерації систематичної номенклатури IUPAC. При невідповідності між зображеною структурою та її назвою перевагу має зображена структура. Крім того, якщо стереохімія структури або її частини не відображена, наприклад, за допомогою жирної або пунктирної ліній, слід розуміти, що така структура або її частина охоплює всі її стереоізомери. В Таблиці I зображені приклади сполук загальної формули I. № сполуки Структура Назва O O O N P H O O O I-1 NH O N O +N N N O O I-2 F OH O O N P H O O NH O N O +N N O O I-3 N F NH O N O +N N N F Етиловий ефір (S)-2-{[(2R,3S,4S,5R)-2азидо-5-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-3-фтор-4гідрокситетрагідрофуран-2-ілметокси]феноксифосфориламіно}-пропіонової кислоти OH O O N P H O O Ізопропіловий ефір (S)-2{[(2R,3S,4S,5R)-2-азидо-5-(2,4-діоксо3,4-дигідро-2H-піримідин-1-іл)-3-фтор4-гідрокситетрагідрофуран-2ілметокси]-феноксифосфориламіно}пропіонової кислоти OH 12 Етиловий ефір (S)-2-[[(2R,3S,4S,5R)-2азидо-5-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-3-фтор-4гідрокситетрагідрофуран-2-ілметокси](нафталін-1-ілокси)-фосфориламіно]пропіонової кислоти UA 110428 C2 O NH2 O N P O H O O I-4 N O N O +N N N F Ізопропіловий ефір (S)-2[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2Hпіримідин-1-іл)-2-азидо-3-фтор-4гідрокситетрагідрофуран-2-ілметокси](нафталін-1-ілокси)-фосфориламіно]пропіонової кислоти OH NH2 N I-5 O O HN P O O O I-6 OH NH2 O N P H O O N O N O +N N O I-7 O N F HO O N P O OH NH2 N O N O +N N O O I-8 F O Етиловий ефір (S)-2-[[(2R,3S,4S,5R)-5(4-аміно-2-оксо-2H-піримідин-1-іл)-2азидо-3-фтор-4гідрокситетрагідрофуран-2-ілметокси](нафталін-1-ілокси)-фосфориламіно]пропіонової кислоти Ізопропіловий ефір (S)-2{[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2Hпіримідин-1-іл)-2-азидо-3-фтор-4гідрокситетрагідрофуран-2-ілметокси]феноксифосфориламіно}-пропіонової кислоти OH NH2 N O N O +N O Бензиловий ефір (S)-2-[[(2R,3S,4S,5R)5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2азидо-3-фтор-4гідрокситетрагідрофуран-2-ілметокси](нафталін-1-ілокси)-фосфориламіно]пропіонової кислоти N H HO O N P O N O O N + N F N O O N N F OH NH2 HO N P O O N O N I-9 O +N N Ізопропіловий ефір (S)-2{[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2Hпіримідин-1-іл)-2-азидо-3-фтор-4гідрокситетрагідрофуран-2-ілметокси]гідроксифосфориламіно}-пропіонової кислоти N F O Ізопропіловий ефір (S)-2[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2Hпіримідин-1-іл)-2-азидо-3-фтор-4пропіонілокситетрагідрофуран-2ілметокси]-(нафталін-1-ілокси)фосфориламіно]-пропіонової кислоти O Синтез Дана Заявка зв’язана з наступними публікаціями: Smith, David B.; Kalayanov, Genadiy; Sund, Christian; Winqvist, Anna; Maltseva, Tatiana; Leveque, Vincent J.-P.; Rajyaguru, Sonal; Le Pogam, Sophie; Najera, Isabel; Benkestock, Kurt; et al Journal of Medicinal Chemistry (2009), 52(9), 29712978. Загальні схеми 13 UA 110428 C2 Способи, що обговорювалися вище, описані нижче більш детально. Наявний у продажу нуклеозид 3’-фтор-3’-дезоксиуридин (1) можна одержати також способами, описаними в літературі: Gosselin, G. et al, Collect. Czech. Chem. Commun. (2006), Vol. 71, No. 7, 991–1010. Йодування з наступним відщепленням йоду в основних умовах може призводити до проміжного продукту 3. Введення азидогрупи по положенню 4’ в проміжному продукті 3, з наступним окисним заміщенням 5’-йодиду за допомогою м-хлорпербензойної кислоти в проміжному продукті 4 з одержанням сполуки 5 можна здійснити способами, описаними в літературі: Smith, D. B. et al, J. Med. Chem. (2009), 52(9), 2971-2978. Зняття захисної 5’-м-хлорбензойної групи в проміжному продукті 5 дає проміжний уридин 6 (Схема 1). Одержання проміжного цитидину 10 було розкрите в літературі: Smith, D. B. et al, J. Med. Chem. (2009), 52(9), 2971-2978. Як варіант, сполуку 10 можна ефективно одержати синтетичним шляхом, який показаний на Схемі 2. 5 Проміжний гуанозин 12 можна одержати реакцією трансамінування з проміжного продукту 8 із захищеним гуаніном, з наступним зняттям захисту (Схема 3). 14 UA 110428 C2 Фосфорамідати за даним винаходом можна одержати шляхом конденсації нуклеозида 6, 10 або 12 з підходящим чином заміщеним фосфохлоридатом 11 в присутності сильної основи (Схема 4). Конденсацію можна здійснювати по незаміщеному нуклеозиду 6, 10 або 12. Конденсований продукт 16 в формулі I спочатку одержують у вигляді суміші двох діастереомерів при реакції конденсації, і їх можна розділити на відповідні оптичні ізомери на хіральній колонці, шляхом хіральної ВЕРХ або хіральної надкритичної флюїдної хроматографії. 5 Реакцію конденсації можна також здійснювати по захищеному нуклеозиду 6, 10 або 12. Наприклад, нуклеозид 6 можна захищати по положенню 2’ з утворенням проміжного продукту 17. Реакція конденсації зі сполукою 17 може призводити до сполуки 18 в формулі I з 5 покращеним виходом. У випадку, якщо R являє собою триетилсилільну групу, в сполуці 18 можна селективно знімати захист з видаленням 2’-триетилсилільної групи, шляхом обробки оцтовою кислотою або мурашиною кислотою при кімнатній температурі з одержанням сполуки 6 16, в якій R являє собою цитидин (Схема 5). Дозування ТА введення Як показано в наведеній нижче Таблиці II, сполуки формули I потенційно ефективні як противірусні лікарські засоби для лікування ВГС-інфекцій у людини або метаболізують до сполуки, яка має таку активність. В іншому втіленні даного винаходу, діючу речовину, або її похідне, або її сіль можна вводити в комбінації з іншим противірусним агентом, таким як агент проти гепатиту, включаючи сполуки формули I. Якщо діючу речовину, або її похідне, або її сіль вводять в комбінації з іншим противірусним агентом, її активність може зростати, у порівнянні з вихідною сполукою. Це можна легко оцінити шляхом одержання похідного і тестування його активності проти ВГС способом, розкритим в даному описі. 15 UA 110428 C2 Спосіб введення діючої речовини може варіюватися від безперервного (внутрішньовенне вливання) до декількох пероральних введень на добу (наприклад, чотири рази на добу) і може включати пероральне, місцеве, парентеральне, внитрішньом’язове, внутрішньовенне, підшкірне, трансдермальне (можливо, з агентом, що посилює проникність), трансбуккальне введення і введення за допомогою супозиторієв та інші шляхи введення. 4'-Заміщені нуклеозидні похідні, а також їх фармацевтично застосовні солі можна застосовувати як лікарські засоби в формі будь-якої фармацевтичної композиції. Фармацевтичну композицію можна вводити ентерально, як перорально, наприклад, в формі таблеток, таблеток, покритих оболонкою, драже, твердих і м’яких желатинових капсул, розчинів, емульсій, сиропів або суспензій, так і ректально, наприклад, в формі супозиторієв. Їх можна також вводити парентерально (внутрішньом’язово, внутрішньовенно; підшкірно; або шляхом внутрішньогрудинної ін’єкції або за допомогою інфузії), наприклад, в формі розчинів для ін’єкції; інтраназально, наприклад, в формі назальних спреїв або спреїв для інгаляції; місцево і тому подібне. Для виготовлення фармацевтичних препаратів 4'-заміщені нуклеозидні похідні, а також їх фармацевтично застосовні солі можна включати в лікарську форму спільно з терапевтично інертним неорганічним або органічним ексципієнтом для виготовлення таблеток, таблеток, покритих оболонкою, драже, твердих і м’яких желатинових капсул, розчинів, емульсій або суспензій. Сполуки формули I можна включати в лікарську форму в суміші з фармацевтично прийнятним носієм. Наприклад, сполуки за даним винаходом можна вводити перорально у вигляді фармацевтично прийнятних солей. Оскільки сполуки за даним винаходом здебільшого розчинні у воді, їх можна вводити внутрішньовенно у фізіологічному сольовому розчині (наприклад, забуференому приблизно до pH 7,2–7,5). В цих цілях можна застосовувати стандартні буфери, наприклад, фосфати, бікарбонати або цитрати. Зрозуміло, середній фахівець в даній галузі техніки може модифікувати композиції, не виходячи за межі ідеї даного опису, з одержанням чисельних композицій для конкретних способів введення, не роблячи композиції за даним винаходом нестабільними і не обмежуючи їх терапевтичну активність. Зокрема, модифікацію запропонованих сполук з метою покращення їх розчинності у воді або іншому розчиннику можна легко здійснити, наприклад, за рахунок невеликих модифікацій (композиція у вигляді солі, етерифікація, і тому подібне), що відповідає рівню навиків середнього фахівця в даній галузі техніки. Крім того, середній фахівець в даній галузі техніки зможе модифікувати спосіб введення і схему дозування конкретної сполуки, з тем щоб привести фармакокінетичні властивості запропонованих сполук до максимального сприятливо ефекту у пацієнтів. Для парентеральних композицій носій звичайно включає стирильну воду або водний розчин хлориду натрію, хоча можуть бути включені і інші інгредієнти, в тому числі сприяючі диспергуванню. Зрозуміло, у випадку, якщо необхідно використовувати стерильну воду і підтримувати стерильність, такі композиції і носії також треба стерилізувати. Можна виготовляти також суспензії, що ін’єктуються, при цьому можна використовувати підходящі рідкі носії, суспендуючі агенти і тому подібне. Підходящими ексципієнтами для таблеток, таблеток, покритих оболонкою, драже і твердих желатинових капсул є, наприклад, лактоза, кукурудзяний крохмаль та його похідні, тальк і стеаринова кислота або її солі. За бажанням таблетки або капсули можуть бути покриті кишково-розчинною оболонкою або виготовлені для пролонгованого вивільнення стандартними способами. Підходящими ексципієнтами для м’яких желатинових капсул є, наприклад, рослинні олії, воски, жири, напівтверді та рідкі поліоли. Підходящими ексципієнтами для розчинів для ін’єкцій є, наприклад, вода, сольовий розчин, спирти, поліоли, гліцерин або рослинні олії. Підходящими ексципієнтами для супозиторієв є, наприклад, природні і затверділі масла, воски, жири, напіврідкі та рідкі поліоли. Підходящими ексципієнтами для розчинів і сиропів для ентерального застосування є, наприклад, вода, поліоли, цукроза, інвертований цукор і глюкоза. Фармацевтичні препарати за даним винаходом можуть бути також представлені у вигляді композицій з пролонгованим вивільненням або інших підходящих композицій. Фармацевтичні препарати можуть також містити консерванти, солюбілізатори, стабілізатори, зволожувальні агенти, емульгатори, підсолоджувачі, барвники, ароматизатори, солі для регуляції осмотичного тиску, буфери, маскуючі агенти або антиоксиданти. 16 UA 110428 C2 Фармацевтичні препарати можуть також містити інші терапевтично активні агенти, відомі в даній галузі техніки. Дозування може варіюватися у широких межах і його, зрозуміло, слід підбирати відповідно до індивідуальних вимог у кожному конкретному випадку. У випадку перорального введення підходить добова доза приблизно в інтервалі від 0,01 до 100 мг/кг маси тіла на добу в монотерапії і/або в комбінованій терапії. Переважне добове дозування знаходиться в інтервалі приблизно від 0,1 і 500 мг/кг маси тіла, більш переважно, від 0,1 до 100 мг/кг маси тіла і, найбільш переважно, від 1,0 до 100 мг/кг маси тіла на добу. Стандартний препарат містить приблизно від 5% до 95% діючої речовини (вага/вага). Добову дозу можна вводити у вигляді єдиної дози або розділеними дозами, як правило, від 1 до 5 доз на добу. В деяких лікарських формах переважна про-лікарська форма сполуки, зокрема, включаючи ацильовані (ацетильовані та інші) похідні, піридинові ефіри і різні сольові форми запропонованих сполук. Середньому фахівцю в даній галузі техніки відомо, яким чином можна легко модифікувати запропоновані сполуки до їх пролікарської форми, щоб сприяти доставці діючої речовини до цільового сайту в організмі хазяїна або пацієнта. Середній фахівець в даній галузі техніки зможе також використовувати переваги підходящих фармакокінетичних параметрів пролікарських форм, де це застосовно, в доставці запропонованих сполук до цільового сайту в організмі хазяїна або пацієнта, щоб зробити максимальним передбачуваний ефект сполуки. Показання до застосування і спосіб лікування Сполуки за даним винаходом, їх ізомерні форми та їх фармацевтично прийнятні солі корисні для лікування і профілактики ВГС-інфекції. В даній Заявці запропонований спосіб лікування інфекції вірусом гепатиту C (ВГС), що включає введення пацієнту, який цього потребує, терапевтично ефективної кількості сполуки будь-якої формули I. В даній Заявці запропонований спосіб інгібування реплікації ВГС в клітині, який включає введення сполуки будь-якої формули I. Комбінована терапія Сполуки за даним винаходом, їх ізомерні форми та їх фармацевтично прийнятні солі корисні для лікування і профілактики ВГС-інфекції окремо або при використанні в комбінації з іншими сполуками, направлені до вірусних або клітинних елементів або функцій, залучених у життєвий цикл ВГС. Класи сполук, корисних в даному винаході, включають, без обмеження, всі класи противірусних засобів проти ВГС. Для комбінованої терапії механістичні класи агентів, які можуть бути корисні при їх комбінації із сполуками за даним винаходом, включають, наприклад, нуклеозидні і ненуклеозидні інгібітори полімерази ВГС, інгібітори протеази, інгібітори гелікази, інгібітори NS4B і медичні агенти, які функціонально інгібують внутрішній сайт зв’язування рибосоми (IRES), а також інші лікарські засоби, які інгібують приєднання ВГС до клітини або входження вірусу, трансляцію РНК ВГС, транскрипцію РНК ВГС, реплікацію або дозрівання ВГС, збирання або вивільнення вірусу. Конкретні сполуки цих класів, корисні в цілях даного винаходу, включають, без обмеження, макроциклічні, гетероциклічні та лінійні інгібітори протеази ВГС, такі як телапревір (VX-950), боцепревір (SCH-503034), нарлапревір (SCH-9005 18), ITMN-191 (R-227), TMC-435350 (відомий також як TMC-435), MK-7009, BI-201335, BI-2061 (цилупревір), BMS650032, ACH-1625, ACH-1095 (інгібітор кофактора протеази ВГС NS4A), VX-500, VX-8 13, PHX1766, PHX2054, IDX-136, IDX-3 16, ABT-450 EP-0 13420 (і споріднені сполуки) і VBY-376; нуклеозидні інгібітори полімерази ВГС (реплікази), корисні в цілях даного винаходу, включають, без обмеження, R7128, PSI-785 1, IDX-184, IDX-102, R1479, UNX-08 189, PSI-6130, PSI-938 та PSI-879, а також різні інші нуклеозидні і нуклеотидні аналоги та інгібітори ВГС, включаючи (без обмеження) ті, які одержують як 2'-C-метил-модифіковані нуклеоз(т)иди, 4'-аза-модифіковані нуклеоз(т)иди, і 7'-деаза-модифіковані нуклеоз(т)иди. Не-нуклеозидні інгібітори полімерази ВГС (реплікази), корисні в цілях даного винаходу, включають, без обмеження, HCV-796, HCV-371, VCH-759, VCH-916, VCH- 222, ANA-598, MK-3281, ABT-333, ABT-072, PF-00868554, BI-207127, GS-9190, A- 837093, JKT-109, GL-59728 і GL-60667. Крім того, сполуки за даним винаходом можна застосовувати в комбінації з антагоністами циклофіліну та імунофіліну (наприклад, без обмеження, сполуки DEBIO, NM-811, а також циклоспорин і його похідні), інгібітори кіназ, інгібітори білків теплового шоку (наприклад, HSP90 та HSP70), інші імуномодулючі агенти, які можуть включати, без обмеження, інтерферони (альфа, -бета, -омега, -гамма, -лямбда або синтетичні), такі як Intron A, Roferon-A, CanferonA300, Advaferon, Infergen, Humoferon, Sumiferon MP, Alfaferone, IFN-β, Feron і тому подібне; поліетиленгліколь-дериватизовані (пегільовані) сполуки інтерферону, такі як ПЭГ-інтерферон-α 17 UA 110428 C2 2a (Pegasys), ПЕГ-інтерферон-α-2b (PEGIntron), пегільований IFN-α-con1 і тому подібне; композиції тривалої дії і похідні сполуки інтерферону, такі як злитий з альбуміном інтерферон, Albuferon, Locteron, і тому подібне; інтерферони з системами контрольованої доставки різних типів (наприклад, ITCA-638, омега-інтерферон, що доставляється підшкірною системою доставки DUROS); сполуки, які стимулюють синтез інтерферону в клітинах, такі як резиквімод і тому подібне; інтерлейкіни; сполуки, які збільшують розвиток T-клітинної відповіді T-хелперів 1 типу, такі як SCV-07 і тому подібне; агоністи TOLL-подібного рецептора, такі як CpG-10101 (актилон), ізоторабін, ANA773 і тому подібне; тимозин α-1; ANA-245 та ANA-246; гістамін дигідрохлорид; пропагерманій; тетрахлордекаоксид; ампліген; IMP-321; KRN-7000; антитіла, такі як цивацир, XTL-6865 і тому подібне і профілактичні і терапевтичні вакцини, такі як InnoVac C, HCV E1E2/MF59 і тому подібне. Крім того, будь-який з вище описаних способів, який включає введення інгібітору NS5A, агоніста рецептора інтерферону I типу (наприклад, IFN-α) і агоніста рецептора інтерферону II типу (наприклад, IFN-γ), можна посилити введенням ефективної кількості антагоніста TNF-α. Не обмежуючі приклади антагоністів TNF-α, які підходять для застосування в такій комбінованій терапії, включають ENBREL, REMICADE та HUMIRA. Крім того, сполуки за даним винаходом можна застосовувати в комбінації з засобами проти найпростіших та іншими противірусними засобами, які вважаються ефективними в лікуванні ВГС-інфекції, такими як, без обмеження, проліки нітазоксанід. Нітазоксанід можна застосовувати як агент в комбінації із сполуками, розкритими в даному винаході, а також в комбінації з іншими агентами, корисними в лікуванні ВГС-інфекції такими як пегільований інтерферон α-2a і рибавірин. Сполуки за даним винаходом можна також застосовувати з іншими формами інтерферонів і пегільованих інтерферонів, рибавірину або його аналогів (наприклад, тарабаварин, левовірон), сполуками мікроРНК, малої інтерферуючої РНК (наприклад, SIRPLEX-140-N і тому подібне), аналогами нуклеотидів або нуклеозидів, імуноглобулінами, гепатопротекторами, протизапальними агентами та іншими інгібіторами NS5A. Інгібітори інших мішеней життєвого циклу ВГС включають інгібітори NS3 гелікази; інгібітори кофактора NS4A; інгібітори антисмислового олігонуклеотиду, такі як ISIS-14803, AVI-4065 і тому подібне; кодована вектором коротка шпилькова РНК (кшРНК); ВГС-специфічні рибозими, такі як гептазим, RPI, 13919 і тому подібне; інгібітори входження, такі як HepeX-C, HuMax-HepC і тому подібне; інгібітори альфаглюкозидази, такі як целгозивір, UT-231B і тому подібне; KPE-02003002 та BIVN 401 і інгібітори IMPDH. Інші наглядні приклади сполук–інгібіторів ВГС включають ті, які розкриті в наступних публікаціях: патенти США №№ 5 807 876; 6 498 178; 6 344 465; і 6 054 472; опубліковані патентні заявки PCT №№ WO97/40028; WO98/4038 1; WO00/56331, WO02/04425; WO03/007945; WO03/010141; WO03/000254; WO01/32153; WO00/06529; WO00/18231; WO00/10573; WO00/13708; WO01/85172; WO03/037893; WO03/037894; WO03/037895; WO02/100851; WO02/100846; WO99/01582; WO00/09543; WO02/18369; WO98/17679, WO00/056331; WO98/22496; WO99/07734; WO05/073216, WO05/073195 і WO08/021927. Крім того, комбінації, наприклад, рибавірину та інтерферону, можна вводити в рамках множинної комбінованої терапії щонайменше з однією сполукою за даним винаходом. Даний винахід не обмежений згаданими вище класами сполук і має на увазі відомі і нові сполуки, а також комбінації біологічно активних агентів. Слід розуміти, що комбінована терапія за даним винаходом включає будь-яку хімічно сумісну комбінацію сполук цієї вибіркової групи з іншими сполуками вибіркової групи або іншими сполуками поза вибіркової групи, и, крім того, така комбінація не виключає противірусну активність сполук даної вибіркової групи або противірусну активність фармацевтичної композиції як таку. Комбінована терапія може бути послідовною, що являє собою терапію спочатку першим агентом, а потім другим агентом (наприклад, кожна терапія включає різну сполуку за даним винаходом, або одна терапія включає сполуку за даним винаходом, а інша терапія включає один або більше біологічно активних агентів), або являє собою терапію двома агентами одночасно (паралельно). Послідовна терапія може включати достатній період часу після завершення першої терапії до начала другої терапії. Лікування двома агентами одночасно може бути в одній і тій самій добовій дозі або в окремих дозах. Комбінована терапія не обов’язково обмежена двома агентами і може включати три або більше агентів. Дозування як для паралельної, так і для послідовної комбінованої терапії залежать від абсорбції, розподілення, метаболізму і швидкості екскреції компонентів комбінованої терапії, а також від інших чинників, відомих фахівцю в даній галузі техніки. Величина дози також буде варіюватися залежно від тяжкості стану, який необхідно покращати. Крім того, слід розуміти, що для кожного конкретного суб’єкта можна підбирати особливі режими дозування і схеми у часі, відповідно до 18 UA 110428 C2 індивідуальних потреб і думки фахівця в даній галузі техніки, який здійснює введення лікарських засобів і спостереження за ходом комбінованої терапії. В даній Заявці запропонований спосіб лікування інфекції вірусом гепатиту C (ВГС), який включає введення пацієнту, який цього потребує, терапевтично ефективної кількості сполуки будь-якої формули I. В даній Заявці запропонований вказаний вище спосіб, який додатково включає введення модулятора імунної системи або противірусного агента, який інгібує реплікацію ВГС, або їх комбінацію. В даній Заявці запропонований вказаний вище спосіб, в якому модулятор імунної системи являє собою інтерферон або хімічно дериватизований інтерферон. В даній заявці запропоновані вказані вище способи, які відрізняються тим, що противірусний агент вибирають з групи, яка складається з інгібітору протеази ВГС, інгібітору полімерази ВГС, інгібітору гелікази ВГС, інгібітору праймази ВГС, інгібітору злиття ВГС та їх комбінації. Приклади Загальні умови Сполуки за даним винаходом можна одержати різними способами, представленими в наглядних реакціях синтезу, описаних нижче в розділі Прикладів. Вихідні речовини і реагенти, які використовують при одержанні цих сполук, як правило, або можна придбати у фірм-постачальників, таких як Aldrich Chemical Co., або можна одержати способами, відомими фахівцю в даній галузі техніки, керуючись процедурами, представленими в літературі, наприклад: Fieser and Fieser's Reagents for Organic Synthesis; Wiley & Sons: New York, 1991, томи 1–15; Rodd's Chemistry of Carbon Compounds, Elsevier Science Publishers, 1989, томи 1–5 з Додатками; Organic Reactions, Wiley & Sons: New York, 1991, томи 1–40. Слід розуміти, що схеми реакцій синтезу, наведені в розділі Прикладів, є лише ілюстрацією способів, якими сполуки за даним винаходом можна синтезувати, при цьому можливі різні модифікації цих схем реакцій синтезу, які можна порадити здійснити фахівцю в даній галузі техніки, що звернувся до змісту даної Заявки. Вихідні речовини і проміжні продукти у схемах реакцій синтезу можна за бажанням виділяти та очищати звичайними способами, включаючи без обмеження, фільтрацію, перегонку, кристалізацію, хроматографію і тому подібне. Можна одержати характеристики цих речовин звичайними засобами, включаючи фізичні константи і дані спектрів. Якщо не вказане інше, описані тут реакції звичайно здійснюють в інертній атмосфері при атмосферному тиску, в діапазоні температур реакції приблизно від -78 °C до 150 °C, часто приблизно від 0 °C до 125 °C, і найбільш часто і в цілях зручності приблизно при кімнатній температурі, наприклад, близько 20 °C. Різні замісники в сполуках за даним винаходом можуть бути присутніми у вихідних сполуках, бути введені в будь-який з проміжних продуктів або бути введені після утворень кінцевих продуктів відомими способами, за допомогою реакцій заміщення або перегрупування. Якщо замісники самі по собі реакційно-здатні, то замісники можна самі по собі захищати способами, відомими в даній галузі техніки. В даній галузі техніки відома велика кількість захисних груп, які можна застосовувати. Приклади багатьох з можливих груп можна знайти в наступному виданні: “Protective Groups in Organic Synthesis”, Green et al., John Wiley and Sons, 1999. Наприклад, нітрогрупи можна вводити нітруванням, і нітрогрупу можна перетворювати в інші групи, такі як аміногрупа (шляхом відновлення) і галоген (шляхом діазотування аміногрупи і заміною діазогрупи на галоген). Ацильні групи можна вводити ацилюванням за Фриделем-Крафтсом. Ацильні групи можна потім перетворювати у відповідні алкільні групи різними способами, включаючи відновлення за Кіжнером-Вольфом і відновлення за Клеменсоном. Аміногрупи можна алкілувати з утворенням моно- та діалкіламіногруп; меркапто- та гідроксигрупи можна алкілувати з утворенням відповідних ефірів. Первинні спирти можна окиснювати за допомогою окиснювачів, відомих в даній галузі техніки, з утворенням карбонових кислот або альдегідів, а вторинні спирти можна окиснювати з утворенням кетонів. Таким чином, можна використовувати реакції заміщення або перегрупування з одержанням різних замісників у молекулах вихідної речовини, проміжних продуктів або кінцевого продукту, включаючи виділення продуктів. Абревіатура Абревіатура, що використовується в даній заявці, включає наступне: ацетил (Ac), оцтова кислота (HOAc), азо-біс-ізобутирилнітрил (AIBN), 1-N-гідроксибензотриазол (HOBt), атмосфери (Атм), високоефективна рідинна хроматографія (ВЕРХ), 9-борабіцикло[3.3.1]нонан (9-BBN або BBN), метил (Me), трет-бутоксикарбоніл (Boc), ацетонітрил (MeCN), ди-трет-бутил пірокарбонат або boc-ангібрид (BOC2O), 1-(3-диметиламінопропіл)-3-етилкарбодіімід гідрохлорид (EDCI), бензоїл (Bz), бензил (Bn), м-хлорпербензойна кислота (MCPBA), м-хлорбензойна кислота 19 UA 110428 C2 (MCBA), бутил (Bu), метанол (MeOH), бензилоксикарбоніл (cbz або Z), точка плавлення (mp), карбоніл діімідазол (CDI), MeSO2- (мезил або Ms), 1,4-діазабіцикло[2.2.2]октан (DABCO), масспектр (ms), трифторид діетиламіносірки (DAST), метил-трет-бутиловий ефір (MTBE), дибензиліденацетон (Dba), N-карбоксіангідрид (NCA), 1,5-діазабіцикло[4.3.0]нон-5-ен (DBN), Nбромсукцинімід (NBS), 1,8-діазабіцикло[5.4.0]ундец-7-ен (DBU),N-метилморфолін (NMM), N-метилпіролідон (NMP), 1,2-дихлоретан (DCE), піридиній хлорхромат (PCC), N,N'дициклогексилкарбодіімід (DCC), піридиній дихромат (PDC), дихлорметан (DCM), пропіл (Pr), діетил азодикарбоксилат (DEAD), феніл (Ph), ди-ізо-пропілазодикарбоксилат, DIАD, фунти на дюйм квадратний (psi), ди-ізо-пропілетиламін (DIPEA), піридин (pyr), ди-ізо-бутилалюмінійгідрид, DIBAL-H, кімнатна температура, кт або КТ, N,N-диметилацетамід (DMA), третбутилдиметилсиліл або t-BuMe2Si, (TBDMS), 4-N,N-диметиламінопіридин (DMAP), триетиламін (Et3N або TEA), N,N-диметилформамід (DMF), трифлат або CF3SO2- (Tf), диметил сульфоксид (DMSO), трифтороцтова кислота (TFA), 1,1'-біс-(дифенілфосфіно)етан (dppe), 2,2,6,6тетраметилгептан-2,6-діон (TMHD), 1,1'-біс-(дифенілфосфіно)ферроцен (dppf), тонкошарова хроматографія (ТШХ), етилацетат (EtOAc), тетрагідрофуран (THF), діетиловий ефір (Et 2O), триметилсиліл або Me3Si (TMS), етил (Et), п-толуолсульфонова кислота моногідрат (TsOH або pTsOH), літій гексаметилдисилазан (LiHMDS), 4-Me-C6H4SO2- або тозил (Ts), ізопропіл (i-Pr), N-уретан-N-карбоксіангідрид (UNCA), етанол (EtOH). Загальноприйнята номенклатура, включаючи префікси нормальний (н-), ізо-, вторинний (втор-), третинний (трет-) і неовживаються в своєму звичайному значенні, якщо вони використовуються з алкільною групою (J. Rigaudy and D. P. Klesney, Nomenclature in Organic Chemistry, IUPAC 1979 Pergamon Press, Oxford.). Приклади одержання Спосіб одержання 1 Одержання проміжного хірального 1-((2R,3S,4S,5S)-4-фтор-3-гідрокси-5йодметилтетрагідрофуран-2-іл)-1H-піримідин-2,4-діону O NH I O F N O OH M.W. 356,09 C9H10FIN2O4 Хіральний 3’-дезокси-3’-α-фторуридин (Green ChemPharma) (5,2 г; 21 ммоль) та PPh3 (7,7 г; 29 ммоль) розчиняли в суміші CH3CN/піридин (95:5, 250 мл). Додавали йод (7,0 г; 27,5 ммоль) і реакційну суміш перемішували при кімнатній температурі в атмосфері азоту протягом 12 год. Додавали воду (80 мл) і розчинник випарювали досуху при зниженому тиску. Здійснювали азеотропну перегонку з CH3CN і потім з CHCl3 для видалення залишкової води. Одержаний залишок очищували хроматографією на колонці із силікагелем (2–4% EtOH в CH2Cl2) з одержанням вказаного в заголовку продукту (5 г). 1 H ЯМР (300 М Гц, DMSO-d6):δ 11,45 (s, 1H), 7,72-7,69 (d, J=8,1Hz, 1H), 5,87-5,84 (d, J=8,1 Гц, 1H), 5,74-5,71 (m, 2H), 5,00-4,80 (dd, J = 54,3 Гц, 4,2 Гц, 1H), 4,53-4,41 (m, 1H), 4,32-4,19 (m, 1H), 3,56-3,40 (m, 2H). Спосіб одержання 2 Одержання проміжного хірального 1-((2R,3S,4S)-4-фтор-3-гідрокси-5метилентетрагідрофуран-2-іл)-1H-піримідин-2,4-діону O NH O F N O OH M.W. 228,18 C9H9FN2O4 20 UA 110428 C2 До хірального 1-((2R,3S,4S,5S)-4-фтор-3-гідрокси-5-йодметил-тетрагідрофуран-2-іл)-1Hпіримідин-2,4-діону (10,7 г) в метанолі (650 мл) додавали NaOMe (16,2 г; 30 ммоль). Реакційну суміш нагрівали при температурі флегми протягом 2 годин. Цю суміш охолоджували до кімнатної температури, додавали порціями катіонообмінну смолу (H+, промиту водою) при 0 °C до досягнення pH 6~7. Смолу видаляли фільтрацією і промивали метанолом, і фільтрат випарювали досуху при зниженому тиску. Одержаний залишок очищували хроматографією на колонці із силікагелем (використовували етилацетату як елюант) з одержанням вказаної в заголовку сполуки у вигляді жовтої твердої речовини (2,3 г) 1 H ЯМР (300 М Гц, DMSO-d6):δ 11,53 (s, 1H), 7,79-7,76 (d, J=8,1 Гц, 1H), 6,14-6,12 (d, J=6,3 Гц, 1H), 6,08-6,06 (d, J=7,5 Гц, 1H), 5,74-5,71 (d, J=8,1 Гц, 1H), 5,40-5,19 (dd, J = 55,8 Гц, 4,5 Гц, + 1H), 4,71-4,54 (m, 3H).MS [M+H] = 229,2 Спосіб одержання 3 Одержання проміжного хірального 1-((2R,3S,4S,5S)-5-азидо-4-фтор-3-гідрокси-5йодметилтетрагідрофуран-2-іл)-1H-піримідин-2,4-діону O NH I O O N N3 F OH M.W. 397,11 C9H9FIN5O4 [Bn(Et)3N]Cl (17 г; 75 ммоль) та NaN3 (4,5 г; 69 ммоль) суспендували у безводному CH3CN (200 мл) і перемішували при кімнатній температурі протягом ночі. Одержану тонку суспензію фільтрували в розчин хірального 1-((2R,3S,4S)-4-фтор-3-гідрокси-5-метилентетрагідрофуран-2іл)-1H-піримідин-2,4-діону (2 г; 8,8 ммоль) в сухому THF (30 мл). Додавали 4-метилморфолін (0,3 мл, 2,6 ммоль), одержаний розчин охолоджували на водно-льодяній бані і додавали по краплях розчин йоду (8 г; 31 ммоль) в безводному THF (30 мл) протягом 60 хв. Реакційну суміш перемішували при 0–9 °C протягом 16 годин. Додавали N-ацетил-L-цистеїн, і цей розчин перемішували до зменшення утворення пухирців. Розчинник концентрували при зниженому тиску до половини об’єму, потім додавали 0,1 M розчин Na2S2O3 і насичений водний розчин NaHCO3. Цю суміш екстрагували за допомогою 10% EtOH в CH 2Cl2 і промивали сольовим розчином. Органічні шари висушували над Na2SO4, фільтрували і випарювали досуху при зниженому тиску. Суміш очищували хроматографією на колонці із силікагелем [етилацетат : CH2Cl2 : EtOH; 200:100:3] з одержанням неочищеного бажаного продукту. Неочищений продукт очищували хроматографією на силікагелі (0~3% EtOH в CH2Cl2) двічі з одержанням вказаної в заголовку сполуки у вигляді білої твердої речовини (0,73 г; 21%) 1 H ЯМР (300 М Гц, CDCl3):δ 9,09 (s, 1H), 7,38-7,35 (d, J=8,1 Гц, 1H), 5,83-5,80 (d, J=8,1 Гц, 1H), 5,76-5,75 (d, J=4,2 Гц, 1H), 5,45-5,26 (dd, J = 52,2 Гц, 5,7 Гц, 1H), 4,84-4,77 (m, 1H) , 3,60-3,48 (m, 1H). Спосіб одержання 4 Одержання проміжного хірального (2R,3S,4S,5R)-2-азидо-5-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-3-фтор-4-гідрокситетрагідрофуран-2-ілметилового ефіру 3-хлорбензойної кислоти O Cl NH O N O O O N3 F OH M.W. 425,76 C16H13ClFN5O6 Розчин хірального 1-((2R,3S,4S,5S)-5-азидо-4-фтор-3-гідрокси-5-йодметилтетрагідрофуран2-іл)-1H-піримідин-2,4-діону (0,76 г; 1,9 ммоль) в CH2Cl2 (120 мл) об’єднували з сумішшю (Bu)4NHSO4 (796 мг; 2,35 ммоль) і м-хлорбензойною кислотою (500 мг; 3,2 ммоль) в K2HPO4 21 UA 110428 C2 (1,75 M, 40 мл). Одержану двофазну систему інтенсивно перемішували при кімнатній температурі і додавали одну порцію м-хлорпербензойної кислоти (3,6 г) [55% у рівновазі з 3хлорбензойною кислотою (10%) і водою (35%)]. Через 1 годину вносили 3 рази по 1,2 г цієї суміші реагентів з інтервалом 1 година. Після останнього внесення одержану суміш інтенсивно перемішували при кімнатній температурі протягом 18 годин. Додавали розчин Na 2S2O3 (0,1 M) і насичений водний розчин NaHCO3 (pH 7~8). Цю суміш інтенсивно перемішували при кімнатній температурі протягом 15 хв. Органічний шар відділяли, і водний шар екстрагували за допомогою CH2Cl2. Об’єднаний органічний екстракт промивали насиченим водним розчином NaHCO3. Органічний шар відділяли і концентрували при зниженому тиску. Одержаний залишок очищували хроматографією на колонці із силікагелем (0~3% EtOH в CH 2Cl2) з одержанням вказаної в заголовку сполуки у вигляді білої твердої речовини (0,35 г; 43%) 1 H ЯМР (300 М Гц, CDCl3):δ 9,00 (s, 1H), 8,09-7,91 (m, 2H), 7,59-7,56 (m, 1H), 7,44-7,39 (m, 1H), 7,32-7,29 (d, J=8,1 Гц, 1H), 5,79-5,73 (m, 2H), 5,61-5,42 (dd, J = 51,9 Гц, 5,7 Гц, 1H), 4,81-4,78 (m, 1H). Спосіб одержання 5 Одержання проміжного хірального 1-((2R,3S,4S,5R)-5-азидо-4-фтор-3-гідрокси-5гідроксиметилтетрагідрофуран-2-іл)-1H-піримідин-2,4-діону O NH HO O N O N3 F OH M.W. 287,21 C9H10FN5O5 Розчин NH3 в MeOH (7 н; 10 мл) додавали до хірального (2R,3S,4S,5R)-2-азидо-5-(2,4діоксо-3,4-дигідро-2H-піримідин-1-іл)-3-фтор-4-гідрокситетрагідрофуран-2-ілметилового ефіру 3хлорбензойної кислоти (100 мг; 0,24 ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 2 годин. Розчинник випарювали і одержаний залишок очищували за допомогою препаративної ВЕРХ з одержанням вказаної в заголовку сполуки у вигляді білої твердої речовини (34,5 мг; 51%) + 1 MS [M+H] = 288,0; H ЯМР (300 М Гц, DMSO-d6):δ 11,52 (s, 1H), 7,84-7,82 (d, J=8,1 Гц, 1H), 6,18-6,15 (m, 2H), 5,88-5,77 (m, 2H), 5,23-5,03 (dd, J = 53,7 Гц, 4,5 Гц, 1H), 4,60-4,40 (m, 1H), 3,543,53 (d, J = 5,1 Гц,2H). Спосіб одержання 6 Одержання проміжного хірального (2R,3S,4S,5S)-5-азидо-2-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-4-фтор-5-йодметилтетрагідрофуран-3-іл-ефір-2,4-діону бензойної кислоти O NH I O N N3 O O F O M.W. 501,22 C16H13FIN5O5 До розчину хірального 1-((2R,3S,4S,5S)-5-азидо-4-фтор-3-гідрокси-5йодметилтетрагідрофуран-2-іл)-1H-піримідин-2,4-діону, одержаного за Способом одержання 3 (1,5 г; 3,78 ммоль), і DMAP (0,87 г; 7,56 ммоль) в сухому THF (20 мл) в атмосфері азоту при 0 °C додавали по краплях BzCl (0,67 мл, 5,67 ммоль). Реакційну суміш перемішували при 0 °C протягом 5 хв. Цю суміш потім розбавляли за допомогою EA, промивали сольовим розчином і водним розчином HCl (0,1 M). Органічний шар відділяли, висушували над Na 2SO4 і концентрували. Одержаний залишок очищували хроматографією на колонці із силікагелем (PE : 22 UA 110428 C2 EA = від 5 : 1 до 2 : 1) з одержанням вказаної в заголовку сполуки у вигляді білої твердої речовини (1,78 г; 94 %). + MS [M+H] = 502 Спосіб одержання 7 Одержання проміжного хірального (2R,3S,4S,5S)-5-азидо-2-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-4-фтор-5-бензоїлметилтетрагідрофуран-3-іл-ефір-2,4-діону бензойної кислоти O NH O N O O O N3 O F O M.W. 495,43 C23H18FN5O7 До суміші хірального (2R,3S,4S,5S)-5-азидо-2-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-4фтор-5-йодметилтетрагідрофуран-3-іл-ефір-2,4-діону бензойної кислоти (1,78 г; 3,55 ммоль) в DMSO додавали бензоат натрію (2,56 г; 17,76 ммоль) і 18-Краун-6 (0,187 г; 0,71 ммоль). Реакційну суміш нагрівали в атмосфері азоту при 100 °C протягом 18 годин. Цю суміш охолоджували до кімнатної температури, розбавляли етилацетатом, потім промивали сольовим розчином і водою. Органічний шар відділяли і концентрували при зниженому тиску. Одержаний залишок очищували хроматографією на колонці із силікагелем (PE : EA = 5 : 1) з одержанням вказаної в заголовку сполуки у вигляді білої твердої речовини (1,30 г; 74 %). + MS [M+H] = 496 Спосіб одержання 8 Одержання проміжного хірального 4-аміно-1-((2R,3S,4S,5R)-5-азидо-4-фтор-3-гідрокси-5гідроксиметилтетрагідрофуран-2-іл)-1H-піримідин-2-ону NH2 N HO O N O N3 F OH M.W. 286,22 C9H11FN6O4 До розчину хірального (2R,3S,4S,5S)-5-азидо-2-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-4фтор-5-бензоїлметилтетрагідрофуран-3-іл-ефір-2,4-діону бензойної кислоти (0,2 г; 2,6 ммоль) і 1H-тетразолу (0,283 г; 26 ммоль) в сухому піридині (5 мл) в атмосфері азоту при 0 °C додавали 4-хлорфенілфосфорoдихлоридат (0,297 г; 7,9 ммоль). Реакційну суміш перемішували при 0– 5 °C протягом 5 хв, потім доводили до кімнатної температури і перемішували протягом 5 годин. Цю суміш концентрували при зниженому тиску. Одержаний залишок ділили між DCM і насиченим розчином NaHCO3. Органічний шар відділяли, промивали сольовим розчином, висушували над Na2SO4 і концентрували з одержанням неочищеного 1H-тетразолового проміжного продукту 9 на Схемі 2 і використовували безпосередньо без додаткового очищення на наступній стадії. 1H-тетразоловий продукт 9 (0,2 г) розчиняли в діоксані (70 мл) при кімнатній температурі, додавали NH3·H2O (10 мл). Реакційну суміш перемішували при кімнатній температурі протягом 0,5 години. Аналіз за допомогою ТШХ показав, що вихідна речовина було повністю витрачена. Розчинник видаляли при зниженому тиску, і одержаний залишок розчиняли в метанольному розчині NH3 (7 н, 10 мл). Реакційну суміш перемішували при кімнатній температурі протягом 16 годин. Цю суміш концентрували і одержаний залишок очищували за допомогою препаративної ВЕРХ з одержанням вказаної в заголовку сполуки у вигляді білої твердої речовини (50 мг; 50 %). 23 UA 110428 C2 + 1 MS [M+H] = 287,2; H ЯМР (300 М Гц, DMSO-d6):δ 7,752-7,727 (d, 1 H, J = 7,5), 7,352 (br, 2 H), 6,220-6,195 (d, 1 H, J = 7,5), 6,018-5,997 (d, 1 H, J = 6,3), 5,816-5,791 (d, 1 H, J = 7,5), 5,758-5,719 (t, 1 H), 5,195-5,001 (dd, 1 H, J = 4,5, J = 53,4), 4,548-4,436 (m, 1 H), 3,539-3,462 (m, 2 H) Спосіб одержання 9 Одержання проміжного хірального (2R,3S,4S,5R)-2-(2-ацетиламіно-6-оксо-1,6-дигідропурин9-іл)-5-азидо-4-фтор-5-бензоїлметилтетрагідрофуран-3-ілового ефіру бензойної кислоти O O N O NH O N O N N3 N H O F O M.W. 576,51 C26H21FN8O7 До суміші N-(6-оксо-6,9-дигідро-1H-пурин-2-іл)-ацетаміду (154 мг; 0,8 ммоль) в MeCN (20 мл) додавали бичачий сироватковий альбумін (BSA) (325 мг; 0,8 ммоль). Цю суміш нагрівали при 60 °C доти, доки вона не перетворювалася в прозорий розчин. Додавали розчин хірального (2R,3S,4S,5S)-5-азидо-2-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-4-фтор-5бензоїлметилтетрагідрофуран-3-іл-ефір-2,4-діону бензойної кислоти, одержаного за Способом одержання 7 (200 мг; 0,4 ммоль) в MeCN, з наступним внесенням TMSOTf (357 мг; 1,6 ммоль). Одержану реакційну суміш нагрівали при мікрохвильовому опроміненні при 100 °C протягом 1 години. Цю суміш охолоджували до кімнатної температури, потім гасили насиченим розчином NaHCO3 (10 мл). Суміш екстрагували за допомогою EA (10 мл × 3). Органічний шар відділяли, промивали сольовим розчином (10 мл), висушували над Na2SO4, і концентрували. Одержаний залишок очищували хроматографією на колонці (DCM : MeOH = 50 : 1) з одержанням неочищеної вказаної в заголовку сполуки (120 мг; 51%) + + LC-MS (M+H) = 577,2; LC-MS (M+Na) = 599,1 Спосіб одержання 10 Одержання проміжного хірального 2-аміно-9-((2R,3S,4S,5R)-5-азидо-4-фтор-3-гідрокси-5гідроксиметилтетрагідрофуран-2-іл)-1,9-дигідропурин-6-ону O N O N HO NH N NH2 N3 F OH M.W. 326,25 C10H11FN8O4 До розчину неочищеного хірального (2R,3S,4S,5R)-2-(2-ацетиламіно-6-оксо-1,6дигідропурин-9-іл)-5-азидо-4-фтор-5-бензоїлметилтетрагідрофуран-3-ілового ефіру бензойної кислоти (120 мг; 0,26 ммоль) в MeOH (2 мл) додавали метанольний розчин аміаку (2 мл, 7 н). Реакційну суміш перемішували при 25 °C протягом 18 годин. Аналіз за допомогою ТШХ показав, що реакція була завершена. Цю суміш концентрували у вакуумі, очищували за допомогою препаративної ВЕРХ з одержанням вказаної в заголовку сполуки у вигляді білої твердої речовини (15 мг; 22%). + LC-MS (M+H) = 327,0 Приклад 1 Одержання ізопропілового ефіру (S)-2-{[(2R,3S,4S,5R)-2-азидо-5-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-феноксифосфориламіно}пропіонової кислоти 24 UA 110428 C2 O O H N O O NH P O O O N O N3 F OH I-1 M.W. 556,45 C21H26FN6O9P Стадія A. (S)-ізопропіл-2-амінопропіонат гідрохлорид (Oakwood, 300 мг; 1,95 ммоль) і фенілфосфорoдихлоридат (Aldrich, 397 мг; 280 мкл; 1,79 ммоль) суспендували в безводному DCM (10 мл). Реакційну суміш охолоджували до -78 °C. Додавали по краплях триетиламін (362 мг; 498 мкл; 3,58 ммоль). Реакційну суміш перемішували при -78 °C протягом 1 години, потім нагрівали до кімнатної температури і перемішували протягом 5 годин. Розчинник видаляли, одержаний залишок промивали сухим ефіром. Фільтрат концентрували з одержанням неочищеного (2S)-ізопропіл-2-(хлор(фенокси)фосфориламіно)пропіонату у вигляді світложовтого масла (0,5 г; 91%), який використовували без додаткового очищення. Стадія B. До розчину хірального 1-((2R,3S,4S,5R)-5-азидо-4-фтор-3-гідрокси-5гідроксиметилтетрагідрофуран-2-іл)-1H-піримідин-2,4-діону, одержаного за Способом одержання 5 (54 мг; 188 мкмоль), в безводному THF (3,75 мл) додавали по краплях розчин третбутилмагнійхлориду (470 мкл; 470 мкмоль) в THF (Aldrich, 1 M). Цю суміш перемішували при кімнатній температурі протягом 15 хв, потім додавали по краплях розчин (0,5 M) неочищеного (2S)-ізопропіл-2-(хлор(фенокси)фосфориламіно)пропіонату (940 мкл; 470 мкмоль) в THF. Реакційну суміш перемішували при кімнатній температурі протягом 3 годин. Потім додавали MeOH (2 мл). Розчинник видаляли. Одержаний залишок очищували флеш-хроматографією (силікагель, 40 г; 0–15% MeOH в DCM) з одержанням вказаної в заголовку сполуки у вигляді брудно-білої твердої речовини (22 мг; 21%) + LC-MS (M+H) = 557,0 Приклад 2 Одержання етилового ефіру (S)-2-{[(2R,3S,4S,5R)-2-азидо-5-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-феноксифосфориламіно}пропіонової кислоти O O O H N O NH P O O O N O N3 F OH I-2 M.W. 542,42 C20H24FN6O9P Стадія A. (S)-етил-2-амінопропіонат гідрохлорид (Aldrich, 300 мг; 1,95 ммоль) і фенілфосфорoдихлоридат (Aldrich, 434 мг; 306 мкл; 1,95 ммоль) суспендували в безводному DCM (20 мл). Реакційну суміш охолоджували до -78 °C. Додавали по краплях триетиламін (395 мг; 544 мкл; 3,91 ммоль). Реакційну суміш перемішували при -78 °C протягом 1 години, потім нагрівали до кімнатної температури і перемішували протягом 5 годин. Розчинник видаляли, одержаний залишок промивали сухим ефіром. Фільтрат концентрували з одержанням неочищеного (2S)-етил-2-(хлор(фенокси)фосфориламіно)пропіонату у вигляді світло-жовтого масла (0,5 г; 88%) і використовували без додаткового очищення. Стадія B. До розчину хірального 1-((2R,3S,4S,5R)-5-азидо-4-фтор-3-гідрокси-5гідроксиметилтетрагідрофуран-2-іл)-1H-піримідин-2,4-діону, одержаного за Способом одержання 5 (50 мг; 174 мкмоль), в безводному THF (5 мл) додавали по краплях розчин трет 25 UA 110428 C2 бутилмагнійхлориду (435 мкл; 435 мкмоль) в THF (Aldrich, 1 M). Цю суміш перемішували при кімнатній температурі протягом 15 хв, потім додавали по краплях розчин неочищеного (2S)етил-2-(хлор(фенокси)фосфориламіно)пропіонату (870 мкл; 435 мкмоль) в THF (0,5 M). Реакційну суміш перемішували при кімнатній температурі протягом ночі. Потім додавали MeOH (2 мл). Розчинник видаляли. Одержаний залишок очищували флеш-хроматографією (силікагель, 40 г; 0–15% MeOH в DCM) з одержанням вказаної в заголовку сполуки у вигляді брудно-білої твердої речовини (7 мг; 7,4%). + LC-MS (M+H) = 543,0 Приклад 3 Одержання етилового ефіру (S)-2-[[(2R,3S,4S,5R)-2-азидо-5-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)фосфориламіно]-пропіонової кислоти O O O H N O NH P O O O N O N3 F OH I-3 M.W. 592,48 C24H25FN6O9P Стадія A. Нафталін-1-ол (Aldrich, 0,72 г; 4,99 ммоль) та оксихлорид фосфору (V) (Aldrich, 767 мг; 466 мкл; 5,00 ммоль) суспендували в безводному ефірі (20 мл) і температуру знижували до -78 °C. Додавали по краплях триетиламін (505 мг; 695 мкл; 4,99 ммоль) і реакційну суміш перемішували при -78 °C протягом 0,5 години. Реакційну суміш нагрівали до кімнатної температури і перемішували протягом ночі. Цю суміш фільтрували, і фільтрат концентрували з одержанням неочищеного нафталін-1-іл-фосфорoдихлоридату у вигляді світло-жовтого масла (1,3 г; 100%), який використовували в наступній стадії без додаткового очищення. Стадія B. (S)-етил-2-амінопропіонат гідрохлорид (Aldrich, 300 мг; 1,95 ммоль) і нафталін-1-іл фосфорoдихлоридат (510 мг; 1,95 ммоль) суспендували в безводному DCM (30 мл). Реакційну суміш охолоджували до -78 °C. Додавали по краплях триетиламін (395 мг; 544 мкл; 3,91 ммоль). Реакційну суміш перемішували при -78 °C протягом 1 години, потім нагрівали до кімнатної температури і перемішували протягом 5 годин. Розчинник видаляли і одержаний залишок промивали сухим ефіром. Фільтрат концентрували з одержанням неочищеного (2S)-етил-2(хлор(нафталін-1-ілокси)фосфориламіно)пропіонату у вигляді світло-жовтого масла (0,6 г; 90%), яке використовували без додаткового очищення. Стадія C. До розчину хірального 1-((2R,3S,4S,5R)-5-азидо-4-фтор-3-гідрокси-5гідроксиметилтетрагідрофуран-2-іл)-1H-піримідин-2,4-діону, одержаного за Способом одержання 5 (90 мг; 313 мкмоль), в безводному THF (6,25 мл) додавали по краплях розчин третбутилмагнійхлориду (783 мкл; 783 мкмоль) в THF (Aldrich, 1 M). Цю суміш перемішували при кімнатній температурі протягом 15 хв, потім додавали по краплях розчин в THF (0,5 M) неочищеного (2S)-етил-2-(хлор(нафталін-1-ілокси)фосфориламіно)пропіонату (1,57 мл, 783 мкмоль). Реакційну суміш перемішували при кімнатній температурі протягом 3 годин. Потім додавали MeOH (2 мл). Розчинник видаляли. Одержаний залишок очищували флешхроматографією (силікагель, 40 г; 0–15% MeOH в DCM) з одержанням вказаної в заголовку сполуки у вигляді світло-коричневої твердої речовини (70 мг; 38%). + LC-MS (M+H) = 593,0 Спосіб одержання 11 Одержання проміжного хірального 4-аміно-1-((2R,3S,4S,5R)-5-азидо-4-фтор-5гідроксиметил-3-триетилсиланілокситетрагідрофуран-2-іл)-1H-піримідин-2-ону 26 UA 110428 C2 NH2 N O N HO O N3 F O Si M.W. 400,49 C15H25FN6O4Si До розчину хірального 4-аміно-1-((2R,3S,4S,5R)-5-азидо-4-фтор-3-гідрокси-5гідроксиметилтетрагідрофуран-2-іл)-1H-піримідин-2-ону, одержаного за Способом одержання 8 (300 мг; 1,05 ммоль), в піридині (24,5 мл) при -5 °C додавали по краплях хлортриетилсилан (Fluka, 440 мг; 2,92 ммоль) протягом 15 хв. Реакційну суміш перемішували при 0 °C протягом 2 годин, потім гасили додаванням метанолу (5 мл). Цю суміш очищували безпосередньо флешхроматографією (5–15% MeOH в DCM) з одержанням вказаної в заголовку сполуки у вигляді білої твердої речовини (0,29 г; 69%) Спосіб одержання 12 Одержання проміжного ізопропілового ефіру (S)-2-[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2Hпіримідин-1-іл)-2-азидо-3-фтор-4-триетилсиланілокситетрагідрофуран-2-ілметокси]-(нафталін-1ілокси)-фосфориламіно]-пропіонової кислоти NH2 O O H N O N P O O O N O N3 F O Si M.W. 719,79 C31H43FN7O8PSi Стадія A. (S)-ізопропіл-2-амінопропіонат гідрохлорид (Oakwood, 0,706 г; 4,21 ммоль) і нафталін-1-іл фосфорoдихлоридат, одержаний в Прикладі 3, Стадія A (1,1 г; 4,21 ммоль), суспендували в безводному DCM (25 мл). Реакційну суміш охолоджували до -78 °C. Додавали по краплях триетиламін (852 мг; 1,17 мл, 8,42 ммоль). Реакційну суміш перемішували при -78 °C протягом 1 години, потім нагрівали до кімнатної температури і перемішували протягом 5 годин. Розчинник видаляли, і одержаний залишок промивали із сухим етиловим ефіром і фільтрували. Фільтрат концентрували з одержанням неочищеного (2S)-ізопропіл-2-(хлор(нафталін-1ілокси)фосфориламіно)пропіонату у вигляді світло-жовтого масла (1,3 г; 87%), яке використовували без додаткового очищення. Стадія B. До розчину хірального 4-аміно-1-((2R,3S,4S,5R)-5-азидо-4-фтор-5-гідроксиметил-3триетилсиланілокситетрагідрофуран-2-іл)-1H-піримідин-2-ону, одержаного за Способом одержання 11 (0,29 г; 724 мкмоль), в безводному THF (42 мл) додавали по краплях розчин третбутилмагнійхлориду (1,81 мл, 1,81 ммоль) в THF (Aldrich, 1 M). Цю суміш перемішували при кімнатній температурі протягом 15 хв, потім додавали по краплях розчин в THF (0,5 M) неочищеного (2S)-ізопропіл-2-(хлор(нафталін-1-ілокси)фосфориламіно)пропіонату (3,62 мл, 1,81 ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 1 години, а потім послідовно вносили розчин трет-бутилмагнійхлориду (0,9 мл, 0,9 ммоль) в THF (Aldrich, 1 M) і розчин неочищеного (2S)-ізопропіл-2-(хлор(нафталін-1-ілокси)фосфориламіно)пропіонату (1,81 мл, 0,9 ммоль) в THF (0,5 M). Реакційну суміш перемішували при кімнатній температурі ще протягом 2 годин. Додавали MeOH (5 мл). Розчинник видаляли. Одержаний залишок очищували 27 UA 110428 C2 флеш-хроматографією (силікагель, 40 г; 2–18% MeOH в DCM) з одержанням вказаної в заголовку сполуки у вигляді брудно-білої твердої речовини (430 мг; 83%). + LC-MS (M+H) = 720,3 Приклад 4 Одержання ізопропілового ефіру (S)-2-[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)2-азидо-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)-фосфориламіно]пропіонової кислоти NH2 O H N O O N P O O O N O N3 F OH I-4 M.W. 605,52 C25H29FN7O8P Ізопропіловий ефір (S)-2-[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2-азидо-3фтор-4-триетилсиланілокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)-фосфориламіно]пропіонової кислоти, одержаний за Способом одержання 12 (0,43 г; 597 мкмоль), розчиняли в оцтовій кислоті (80%, 28 мл). Реакційну суміш перемішували при кімнатній температурі протягом 5 годин. Розчинник випарювали при зниженому тиску і залишки оцтової кислоти видаляли азеотропним концентруванням з MeOH три рази. Одержаний залишок очищували флеш-хроматографією (силікагель, 2–18% MeOH в DCM) з одержанням вказаної в заголовку сполуки у вигляді білої твердої речовини (0,2 г; 55%). + LC-MS (M+H) = 606,1 Приклад 5 Одержання бензилового ефіру (S)-2-[[(2R,3S,4S,5R)-5-(4-аміно-2-оксо-2H-піримідин-1-іл)-2азидо-3-фтор-4-гідрокситетрагідрофуран-2-ілметокси]-(нафталін-1-ілокси)-фосфориламіно]пропіонової кислоти NH2 O O H N O N P O O O N O N3 F OH I-5 M.W. 653,57 C29H29FN7O8P Стадія A. (S)-Бензил 2-амінопропіонат гідрохлорид (Chem Impex, 0,66 г; 3,06 ммоль) і нафталін-1-іл фосфорoдихлоридат, одержаний в Прикладі 3, Стадія A (0,8 г; 3,06 ммоль), суспендували в безводному DCM (15 мл). Реакційну суміш охолоджували до -78 °C. Додавали по краплях триетиламін (619 мг; 852 мкл; 6,12 ммоль). Реакційну суміш перемішували при -78 °C протягом 1 години, потім нагрівали до кімнатної температури і перемішували протягом 5 годин. Розчинник видаляли, і одержаний залишок промивали із сухим етиловим ефіром і фільтрували. Фільтрат концентрували з одержанням неочищеного (2S)-бензил-2-(хлор(нафталін-1ілокси)фосфориламіно)пропіонату у вигляді світло-жовтого масла (1 г; 81%), який використовували без додаткового очищення. Стадія B. До розчину хірального 4-аміно-1-((2R,3S,4S,5R)-5-азидо-4-фтор-3-гідрокси-5гідроксиметилтетрагідрофуран-2-іл)-1H-піримідин-2-ону, одержаного за Способом одержання 8 (85 мг; 292 мкмоль), в безводному THF (8,5 мл) додавали по краплях розчин третбутилмагнійхлориду (742 мкл; 742 мкмоль) в THF (Aldrich, 1 M). Цю суміш перемішували при кімнатній температурі протягом 1 години, потім додавали по краплях розчин неочищеного (2S)бензил-2-(хлор(нафталін-1-ілокси)фосфориламіно)пропіонату (1,48 мл, 742 мкмоль) в THF (0,5 M). Реакційну суміш перемішували при кімнатній температурі протягом 1 години, а потім 28
ДивитисяДодаткова інформація
Назва патенту англійською4'-azido, 3'-fluoro substituted nucleoside derivatives as inhibitors of hcv rna replication
Автори англійськоюSmith, Mark, Talamas, Francisco Xavier, Zhang, Jing, Zhang, Zhuming
Автори російськоюСмит Марк, Таламас Франсиско Ксавьер, Чжан Цзин, Чжан Чжумин
МПК / Мітки
МПК: A61K 31/7072, A61P 31/14, C07H 19/16, A61K 31/708, C07H 19/06
Мітки: нуклеозидів, вірусу, інгібітори, 4'-азидо, похідні, 3'-фторзаміщені, реплікації, рнк, гепатиту
Код посилання
<a href="https://ua.patents.su/37-110428-4-azido-3-ftorzamishheni-pokhidni-nukleozidiv-yak-ingibitori-replikaci-rnk-virusu-gepatitu-c.html" target="_blank" rel="follow" title="База патентів України">4′-азидо, 3′-фторзаміщені похідні нуклеозидів як інгібітори реплікації рнк вірусу гепатиту c</a>
Попередній патент: Спосіб одержання водовугільної суспензії
Наступний патент: Штам дріжджів saccharomyces cerevisiae imb y-5055, що використовується для зброджування квасного сусла при виробництві квасу
Випадковий патент: Ваговимірювальна система