Похідні бензімідазолу та їх застосування
Номер патенту: 108390
Опубліковано: 27.04.2015
Автори: Маєда Дзунко, Сіваку Масахіко (померлий), Такахасі Фуміє, Фукахорі Хідехіко, Като Кодзі, Імада Сунао, Асано Тору, Козукі Йосіхіро
Формула / Реферат
1. Сполука формули (І) або її сіль:
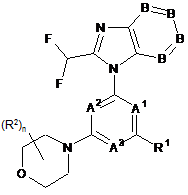 , (І)
, (І)
де
А1, А2 і А3 є однаковими або відрізняються один від одного і являють собою СН або N, за умови, що щонайменше два з А1-А3 являють собою N,
В є однаковими або відрізняються один від одного і являють собою CR3 або N, за умови, що щонайменше три з чотирьох В являють собою CR3,
R1 являє собою -NH-нижчий алкілен-С(О)-ОН або -L1-L2-Y,
R2 є однаковими або відрізняються один від одного і являють собою атоми галогену, -ОН, -О-нижчий алкіл, -CN або нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з галогену, -ОН, -О-нижчого алкілу і -CN,
n дорівнює цілому числу від 0 до 8,
R3 є однаковими або відрізняються один від одного і являють собою Н, -О-нижчий алкіл, ціано, -N(R4)2, -C(O)-OH, -С(О)-О-нижчий алкіл, -C(O)-N(R4)2 або нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -ОН, -О-нижчого алкілу, -N(R4)2, -C(O)-OH, -С(О)-О-нижчого алкілу, -C(O)-N(R4)2 і галогену,
R4 є однаковими або відрізняються один від одного і являють собою Н або нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -ОН, -О-нижчого алкілу, -CN, галогену, циклоалкілу і фенілу,
L1 являє собою -нижчий алкінілен-, -NR5-, -NR5-S(O)2, -NR5-C(O)-, -О-, -S- або -S(O)m-,
m є однаковими або відрізняються один від одного і дорівнюють 1 або 2,
L2 являє собою зв'язок, -ALK-X2-, -ALK-NR6-C(O)-, -ALK-NR6-C(O)-O-ALK-, -ALK-S(O)m-X1- або -ALK-C(O)-X2-,
ALK є однаковими або відрізняються один від одного і являють собою нижчий алкілен, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -ОН, -О-нижчого алкілу, -CN, галогену, циклоалкілу і фенілу,
X1 являє собою зв'язок, -NR6- або -NR6-ALK-,
X2 є однаковими або відрізняються один від одного і являють собою зв'язок, -NR6-, -NR6-ALK-, -О-, -S-, -NR6-ALK-O-, -NR6-ALK-C(O)-NR6- або -NR6-ALK-C(O)-,
R5 є однаковими або відрізняються один від одного і являють собою -R4, нижчий алкеніл або циклоалкіл,
R6 є однаковими або відрізняються один від одного і являють собою Н, циклоалкіл, феніл, неароматичний гетероцикл, що може бути заміщений нижчим алкілом або нижчим алкілом, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -ОН, -О-нижчого алкілу, -CN, галогену, -N(R4)2, циклоалкілу, фенілу і неароматичного гетероциклу,
Y являє собою нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -ОН, -О-нижчого алкілу, -N(нижчий алкіл)2 і -С(О)-N(нижчий алкіл)2, циклоалкілу, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, арилу, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, ароматичного гетероциклу, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, або неароматичного гетероциклу, що може бути заміщений одним або декількома замісниками, вибраними з групи D1,
група D1 складається з:
(1) галогену,
(2) -O-R8,
(3) -S-R8,
(4) -CN,
(5) -NO2,
(6) -NR4R7, де R7 являє собою -R8, -C(O)-R8, -C(O)-C(O)-N(R8)2, -C(O)-O-R8 і -S(O)2-R8,
(7) -C(O)-R8,
(8) -S(O)2-R8 і -S(O)2-N(R8)2,
(9) -C(O)-O-R8,
(10) -C(O)-N(R8)2,
(11) -C(O)-C(O)-N(R8)2,
(12) -O-C(O)-R8, -O-C(O)-NH-C(=NH)-NH2 і -O-C(O)-N(R8)2,
(13) -L3-циклоалкілу, -L3-арилу, -L3-ароматичного гетероциклу і -L3-неароматичного гетероциклу, де кожен циклоалкіл, арил, ароматичний гетероцикл і неароматичний гетероцикл може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -O-R6, -CN, галогену, -N(R6)2, -C(O)-R6, -C(O)-O-R6, -C(O)-N(R6)2, -N(R6)-C(O)-O-R6, -S(О)2-нижчого алкілу, циклоалкілу, фенілу і неароматичного гетероциклу; оксо; циклоалкілу, арилу, ароматичного гетероциклу і неароматичного гетероциклу, кожний з яких може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -ОН, -О-нижчого алкілу, -CN і галогену; і замісників (1)-(12),
(14) оксо, і
(15) нижчого алкілу, -О-нижчого алкілу і нижчого алкенілу, кожний з яких може бути заміщений одним або декількома замісниками, вибраними з замісників, описаних у (1)-(14),
L3 є однаковими або відрізняються один від одного і являють собою зв'язок, -О-, -S-, -NR5-, -NR5-S(O)2, -NR5-C(O)-, -C(O)-NR5-, -S(O)m-, -ALK-, -O-ALK-, -ALK-O-, -O-ALK-O-, -S-ALK-, -ALK-S-, -ALK-S(O)m-, -S(O)m-ALK-, -NR5-ALK-, -ALK-NR5-, -C(O)-NR5-ALK-, -C(O)-NR5-ALK-C(O)-, -C(O)-NR5-ALK-O-ALK-, -NR5-C(O)-ALK-, -NR5-C(O)-ALK-C(O)-, -NR5-C(O)-ALK-O-ALK-, -ALK-C(O)-NR5-, -ALK-NR5-C(O)-, -C(O)-O-, -ALK-C(O)-O-, -C(O)-O-ALK-, -C(O)-ALK-, -ALK-C(O)-, -NR5-C(O)-ALK-NR5- або -C(O)-,
R8 є однаковими або відрізняються один від одного і являють собою Н; циклоалкіл, феніл, піридил або неароматичний гетероцикл, кожний з яких може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -ОН, -О-нижчого алкілу, -CN і галогену; -R9 або -ALK-L-R9,
де R9 являє собою нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -O-R6, -S-R6, -CN, -N(R6)2, -C(O)-R6, -C(O)-O-R6, -C(O)-N(R6)2, -N(R6)-C(O)-O-R6, -циклоалкілу, фенілу і неароматичного гетероциклу, і
L4 являє собою -С(О)-, -C(O)-NR5-, -NR5-, -NR5-S(O)2-, -NR5-C(O)-, -NR5-C(O)-O-, -O-, -S- або -S(O)m-,
за умови, що, у випадку, коли R1 характеризується наступною формулою (II), усі В являють собою СН, W являє собою NH або О, В1 являє собою зв'язок або нижчий алкілен, і В2 являє собою зв'язок або нижчий алкілен,
 , (II)
, (II)
R10 являє собою -С(О)-(нижчий алкілен, заміщений -NН-С(О)-О-нижчим алкілом)-S-нижчий алкіл, -С(О)-неароматичний гетероцикл, -С(О)-нижчий алкілен-NН-нижчий алкілен-(циклоалкіл, що може бути заміщений -ОН), -С(О)-нижчий алкілен-NН-(циклоалкіл, що може бути заміщений групою, вибраною з групи, що складається з нижчого алкілу і -ОН), -С(О)-нижчий алкілен-NH-неароматичний гетероцикл, -С(О)-нижчий алкілен-NН-(нижчий алкіл, заміщений -ОН) або -С(О)-(циклоалкіл, заміщений одним або декількома замісниками, вибраними з групи, що складається з -NH2, -N(нижчий алкіл)2 і -NH-C(O)-O-нижчого алкілу), або
R4 і R10 утворюють разом з атомом N, з яким вони зв'язані, 4-8-членну моноциклічну гетероциклічну групу, що містить від 1 до 4 гетероатомів, вибраних з О, S і N, і, крім того, заміщену щонайменше одним замісником, вибраним із групи D2,
де група D2 складається з:
(а) -О-(нижчий алкіл, заміщений одним або декількома замісниками, вибраними з групи, що складається з -O-R6, -S-R6, -CN, -N(R6)2, -C(O)-R6, -С(О)-O-R6, -C(O)-N(R6)2, -N(R6)-C(O)-O-R6, циклоалкілу і неароматичного гетероциклу), -О-(циклоалкіл, феніл, піридил або неароматичний гетероцикл, кожний з яких може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -ОН, -О-нижчого алкілу, -CN і галогену) і -O-ALK-L4-R9,
(b) -SR8,
(c) -NO2,
(d) -NR11R7, де R7 являє собою -R8, -C(O)-R8, -C(O)-C(O)-N(R8)2, -C(O)-O-R8 і -S(O)2-R8, і R11 являє собою нижчий алкіл, заміщений одним або декількома замісниками, вибраними з групи, що складається з -ОН, -О-нижчого алкілу, -CN, галогену, циклоалкілу і фенілу,
(e) -C(O)-R8,
(f) -S(O)2-R8 і -S(O)2-N(R8)2,
(g) -С(О)-О-(нижчий алкіл, заміщений одним або декількома замісниками, вибраними з групи, що складається з -O-R6, -S-R6, -CN, -N(R6)2, -C(O)-R6, -C(O)-O-R6, -C(O)-N(R6)2, -N(R6)-C(O)-O-R6, циклоалкілу, фенілу, піридилу і неароматичного гетероциклу), -С(О)-О-(циклоалкіл, феніл або неароматичний гетероцикл, кожний з яких може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -ОН, -О-нижчого алкілу, -CN і галогену) і -C(O)O-ALK-L4-R9,
(h) -C(O)-N(R8)2,
(і) -C(O)-C(O)-N(R8)2,
(j) -О-С(О)-(нижчий алкіл, заміщений одним або декількома замісниками, вибраними з групи, що складається з -O-R6, -S-R6, -CN, -N(R6)2, -C(O)-R6, -C(O)-O-R6, -C(O)-N(R6)2, -N(R6)-C(O)-O-R6, циклоалкілу, фенілу, піридилу і неароматичного гетероциклу), -О-С(О)-(циклоалкіл, феніл або неароматичний гетероцикл, кожний з яких може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -ОН, -O-нижчого алкілу, -CN і галогену), -O-C(O)-ALK-L4-R9, -O-C(O)-NH-C(=NH)-NH2 і -O-C(O)-N(R8)2,
(k) нижчого алкілу, заміщеного одним або декількома замісниками, вибраними з групи, що складається з -CN, -N(R6)2, -C(O)-R6, -C(O)-O-R6, -C(O)-N(R6)2, -N(R6)-C(O)-O-R6, -S(О)2-нижчого алкілу, циклоалкілу і фенілу,
(l) циклоалкілу, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -ОН, -O-нижчого алкілу, -CN і галогену,
(m) арилу, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -ОН, -О-нижчого алкілу, -CN і галогену,
(n) ароматичного гетероциклу, заміщеного одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -ОН, -О-нижчого алкілу, -CN і галогену, і
(о) неароматичного гетероциклу, заміщеного одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -ОН, -О-нижчого алкілу, -CN і галогену.
2. Сполука або її сіль за п. 1, де R1 являє собою -NH-нижчий алкілен-С(О)-ОН або -L1-L2-Y, L1 являє собою -нижчий алкінілен-, -NR5-, -NR5-S(O)2-, -NR5-С(О)-, -О-, -S- або -S(O)m-, m дорівнює 1 або 2, L2 являє собою зв'язок, -ALK-X2-, -ALK-NR6-C(O)-, -ALK-NR6-C(O)-O-ALK-, -ALK-S(O)m-X1- або -ALK-C(O)-X2-, ALK є однаковими або відрізняються один від одного і являють собою нижчий алкілен, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -ОН, -О-нижчого алкілу, -CN, галогену і циклоалкілу, X1 являє собою зв'язок, -NR6- або -NR6-ALK-, X2 є однаковими або відрізняються один від одного і являють собою зв'язок, -NR6-, -NR6-ALK-, -О-, -S-, -NR6-ALK-О-, -NR6-ALK-C(O)-NR6- або -NR6-ALK-C(O)-, R4 є однаковими або відрізняються один від одного і являють собою Н, або нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -ОН, -О-нижчого алкілу, -CN, галогену і циклоалкілу, R5 є однаковими або відрізняються один від одного і являють собою -R4, нижчий алкеніл або циклоалкіл, R6 є однаковими або відрізняються один від одного і являють собою Н, циклоалкіл, неароматичний гетероцикл, який може бути заміщений нижчим алкілом, або нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -ОН, -О-нижчого алкілу, -CN, галогену, -N(R4)2, циклоалкілу і неароматичного гетероциклу, Y являє собою нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -ОН, -О-нижчого алкілу, -N(нижчий алкіл)2 і -С(О)-N(нижчий алкіл)2, циклоалкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, або неароматичний гетероцикл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, за умови, що L2 являє собою -ALK-X2a-, -ALK-NR6-C(O)-, -ALK-NR6-C(O)-O-ALK-, -ALK-S(O)m-X1- або -ALK-C(O)-X2-, причому, увипадку, коли Х2а являє собою -NR6-, -NR6-ALK-, -О-, -S-, -NR6-ALK-О-, -NR6-ALK-C(O)-NR6- або -NR6-ALK-C(O)-, додатково Y являє собою арил, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, або ароматичний гетероцикл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1.
3. Сполука або її сіль за п. 2, де R1 являє собою -L1-L2-Y, L1 являє собою -NR5-, -NR5-S(O)2-, -NR5-C(O)- або -О-, де R5 являє собою Н або нижчий алкіл, L2 являє собою зв'язок, -ALK-, -ALK-S-, -ALK-S(O)m-X1- або -ALK-C(O)-X2-, де X1 являє собою зв'язок або -NR6-, X2 являє собою зв'язок, -NR6-, -NR6-ALK- або -О-, ALK являє собою нижчий алкілен, R6 являє собою Н або нижчий алкіл, і Y являє собою циклоалкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, або неароматичний гетероцикл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1.
4. Сполука або її сіль за п. 3, де -L1-L2 являє собою -NH- або -О-.
5. Сполука або її сіль за п. 4, де всі В являють собою СН, і n дорівнює 0.
6. Сполука або її сіль за п. 5, де А1 і А3 являють собою N, і А2 являє собою СН.
7. Сполука або її сіль за п. 5, де А2 і А3 являють собою N, і А1 являє собою СН.
8. Сполука або її сіль за п. 1, де сполука являє собою
метил-{(3S)-1-[транс-4-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}окси)циклогексил]-2-оксопіролідин-3-іл}карбамат,
метил-{(3R)-l-[транс-4-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}окси)циклогексил]-2-оксопіролідин-3-іл}карбамат,
етил-{(3R)-1-[транс-4-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}окси)циклогексил]-2-оксопіролідин-3-іл}карбамат,
[(3S)-3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-iл)пipимiдин-4-iл}aмiнo)пipoлiдин-l-iл][(2R)-тeтpaгiдpoфypaн-2-iл]мeтaнoн,
[(3S)-3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)піролідин-1-іл](тетрагідро-2Н-піран-4-іл)метанон,
метил-{(3S)-1-[транс-4-({4-[2-(дифторметил)-1Н-бензімідазол-1-іл]-6-(морфолін-4-іл)піримідин-2-іл}аміно)циклогексил]-2-оксопіролідин-3-іл}карбамат,
метил-{(3R)-l-[транс-4-({4-[2-(дифторметил)-1Н-бензімідазол-1-іл]-6-(морфолін-4-іл)піримідин-2-іл}аміно)циклогексил]-2-оксопіролідин-3-іл}карбамат,
метил-{(3R)-1-[транс-4-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)циклогексил]-2-оксопіролідин-3-іл}карбамат,
1-[(3S)-3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)піролідин-1-іл]-2-(тетрагідрофуран-2-іл)етанон,
1-[(3S)-3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)піролідин-1-іл]-2-(тетрагідро-2Н-піран-4-іл)етанон,
1-[3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}оксі)азетидин-1-іл]-2-(тетрагідрофуран-2-іл)етанон,
метил-4-{[(3S)-3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)піролідин-1-іл]карбоніл}піперидин-1-карбоксилат,
[(3S)-3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}окси)піролідин-1-іл](тетрагідрофуран-3-іл)метанон,
4-{[(3S)-3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}окси)піролідин-1-іл]карбоніл}-1-метилпіролідин-2-он,
2-(1-ацетилпіперидин-4-іл)-1-[(3S)-3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)піролідин-1-іл]етанон,
[(3S)-3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)піролідин-1-іл](тетрагідрофуран-3-іл)метанон,
4-{[(3S)-3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)піролідин-1-іл]карбоніл}-1-метилпіролідин-2-он,
1-[(3S)-3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)піролідин-1-іл]-2-(піперидин-1-іл)етанон,
(5S)-5-{[3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}оксі)азетидин-1-іл]карбоніл}піролідин-2-он,
(5S)-5-{[3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)азетидин-1-іл]карбоніл}піролідин-2-он,
2-(1-ацетилпіперидин-4-іл)-1-[3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)азетидин-1-іл]етанон,
[3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)азетидин-1-іл](тетрагідрофуран-3-іл)метанон,
4-{[3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)азетидин-1-іл]карбоніл}-1-метилпіролідин-2-он,
[(3S)-3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)піролідин-1-іл][цис-4-(гідроксиметил)циклогексил]метанон або
[(3S)-3-({6-[2-(дифторметил)-1Н-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}аміно)піролідин-1-іл][транс-4-(гідроксиметил)циклогексил]метанон.
9. Фармацевтична композиція, яка містить сполуку або її сіль за п. 1 і фармацевтично прийнятний наповнювач.
10. Фармацевтична композиція для профілактики або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань або гематологічної пухлини, яка містить сполуку або її сіль за п. 1 і фармацевтично прийнятний наповнювач.
11. Застосування сполуки або її солі за п. 1 для одержання фармацевтичної композиції для профілактики або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань або гематологічної пухлини.
12. Застосування сполуки або її солі за п. 1 для профілактики і/або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань і гематологічної пухлини.
13. Сполука або її сіль за п. 1 для профілактики або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань або гематологічної пухлини.
14. Спосіб профілактики або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань або гематологічної пухлини, який включає введення суб'єкту ефективної кількості сполуки або її солі за п. 1.
Текст
Реферат: Винахід стосується сполуки, що застосовна як засіб для профілактики і/або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань і гематологічної пухлини, основана на селективній інгібуючій дії відносно РІ3Kδ і/або інгібуючій продукцію IL-2 дії, і/або інгібуючій проліферацію В-клітин дії (включаючи інгібуючу активацію дію). Автори даного винаходу проводили пошук сполуки, що має селективну інгібуючу дію відносно РІ3Kδ і/або інгібуючу продукцію IL-2 дію, і/або інгібуючу проліферацію В-клітин дію (включаючи інгібуючу активацію дію) і знайшли, що гетероциклічна сполука згідно з даним винаходом має селективну інгібуючу дію відносно РІ3Kδ і/або інгібуючу продукцію IL-2 дію, і/або інгібуючу проліферацію В-клітин дію (включаючи інгібуючу активацію дію), здійснивши тим самим даний винахід. UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 60 ГАЛУЗЬ ТЕХНІКИ, ДО ЯКОЇ НАЛЕЖИТЬ ВИНАХІД Даний винахід стосується гетероциклічної сполуки, яка застосовна як активний інгредієнт фармацевтичної композиції, наприклад фармацевтичної композиції для профілактики і/або лікування захворювань, пов'язаних з фосфатидилінозитол-3-кіназою δ (PI3Kδ). РІВЕНЬ ТЕХНІКИ Фосфатидилінозитол-3-кіназа (PI3K) являє собою ліпід-опосередковану сигнальну кіназу, яка повсюдно є присутньою у всіх видів, від рослин або дріжджів до ссавців, включаючи людей. PI3K являє собою фермент для фосфорилування гідроксильної групи в 3-положенні фосфатидилінозитолу, фосфатидилінозитол-4-фосфату і фосфатидилінозитол-4,5-дифосфату, які являють собою фосфоліпіди клітинної мембрани, і з кожного з зазначених субстратів продукуються фосфатидилінозитол-3-фосфат, фосфатидилінозитол-3,4-дифосфат і фосфатидилінозитол-3,4,5-трифосфат (PIP3). Продуковані таким чином фосфориловані фосфатидилінозитоли діють як внутрішньоклітинний вторинний месенджер. Зокрема, PIP3 викликає міграцію різних молекул, що містять плекстрин-гомологічні (РН) домени, у прилегле до клітинної мембрани положення з індукцією активації молекул, а тому, як передбачається, є найбільш важливим фосфорилованим фосфатидилінозитолом ("The Journal of Biological Chemistry", 1999, Vol. 274, p. 8347-8350). PI3K підрозділяється на три класи, I, II і III, відповідно до різних характеристик, і виходячи з точки зору, що єдиним ферментом, продукуючим PIP3 in vivo, є PI3K I класу, I клас PI3K вважається найбільш важливим класом ("Biochimica et Biophysica Acta", 2008, Vol. 1784, p. 159185). I клас PI3K підрозділяється на IA і IB. PI3K IA класу складається з гетеродимерів, включаючи сполучення каталітичної субодиниці масою 110 кДа (p110α, β або δ) і регуляторної субодиниці масою 50-85 кДа (p85α, p85β, p55α, p55γ або p50α), а PI3K IB класу являє собою гетеродимер з каталітичної субодиниці масою 110 кДа (p110γ) і регуляторної субодиниці масою 101 кДа (p101) ("Nature Immunology", 2003, № 4, p. 313-319). Тут і далі в даному документі відповідні PI3K називають PI3Kα, β, δ і γ, відповідно до каталітичних субодиниць, що входять у їх склад. PI3Kα і β широко представлені в біологічному організмі, і повідомлялося, що дефіцит PI3Kα і β у мишей летальний для плоду в обох випадках ("The Journal of Biological Chemistry", 1999, Vol. 274, p. 10963-10968; і "Mammalian Genome", 2002, Vol. 13, p. 169-172). У результаті досліджень з використанням селективних відносно підтипу сполук повідомлялося, що PI3Kα відіграє важливу роль у сигнальному шляху інсуліну, і інгібітор PI3Kα обумовлює резистентність до інсуліну ("Cell", 2006, Vol. 125, p. 733-747). Крім того, повідомлялося, що PI3Kβ бере участь в агрегації тромбоцитів, і інгібітор PI3Kβ має антитромботичний ефект ("Nature Medicine", 2005, Vol. 11, p. 507-514). З іншого боку, усі дефіцитні по PI3Kδ або γ миші народжуються нормальними, і не було виявлено ніяких проблем стосовно росту, тривалості життя, розмноження і т. п. ("Science", 2000, Vol. 287, p. 1040-1046; і "Molecular and Cellular Biology", 2002, Vol. 22, p. 8580-8591). Зокрема, експресія PI3Kδ помітно знижена в клітинах крові і лімфоїдних тканинах, і було виявлено, що у дефіцитних по PI3Kδ мишей наявні суттєві порушення активації лімфоцитів. Широко відомий тісний взаємозв'язок між активацією лімфоцитів і імунітетом/запаленням, і сполуки, селективно інгібуючі PI3Kδ, є потенційними інгібіторами імунітету/запалення, маючи і потужну інгібуючу активацію лімфоцитів дію, і безпеку. Інтерлейкін-2 (IL-2) являє собою тип цитокіну, який продукується, головним чином, активованими Т-клітинами. IL-2 індукує проліферацію й активацію лімфоцитів через IL-2рецептор, що являє собою рецептор для IL-2. IL-2 є дуже важливою молекулою в сигнальному шляху активації імунної системи, і інгібітори його продукції (наприклад, такролімус і циклоспорин А) використовують у клініці як імуносупресуючі засоби. Крім того, моноклональні антитіла проти рецептора IL-2, такі як базиліксимаб і даклізумаб, використовують у клініці як імуносупресуючі засоби. Поряд з Т-клітинами В-клітини являють собою одну з основних субпопуляцій лімфоцитів і є основними клітинами гуморального імунітету. Відомо, що гуморальний імунітет грає винятково важливу роль у профілактиці інфекції, що викликається патогенами, і т. п., але при аутоімунних захворюваннях, таких як ревматоїдний артрит і т. п., відбувається аномальна активація гуморального імунітету, що глибоко залучена в патогенез. Відомо що, анти-CD20 антитіло, ритуксимаб, використовують у клініці як ліки для лікування ревматоїдного артриту. Як про сполуку, що має інгібуючу дію відносно PI3K, повідомлялося, наприклад, про описані нижче сполуки формули (A-1) (патентний документ 1), формули (A-2) (патентний документ 2), формули (A-3) (патентний документ 3), формули (B-1) (патентний документ 4), формули (B-2) (патентний документ 5), формули (B-3) (патентний документ 6), формули (C) (патентний документ 7), формули (D-1) (патентний документ 8), формули (D-2) (патентний документ 9), 1 UA 108390 C2 5 10 формули (E-1) (патентний документ 10), формули (E-2) (патентний документ 11), формули (E-3) (патентний документ 12), формули (F) (патентний документ 13), формули (G) (патентний документ 14), формули (H) (патентний документ 15 і непатентний документ 1), формули (J) (патентний документ 16) і формули (K) (патентний документ 17). Однак описана нижче сполука формули (I) відповідно до даної заявки відрізняється від сполук формул (A-1)-(E-3), (H) і (K) за 1 структурою групи R формули (I). Вона відрізняється за структурою від сполук формул (F) і (G) 2 тим, що містить бензімідазоліл-1-ільну групу. Як група R формули (J) була розкрита гетероарильна група, але не було конкретного розкриття бензімідазоліл-1-ільної групи, і не було розкриття сполуки формули (I) згідно з даним винаходом в патентному документі 16. Крім того, у яких-небудь документах відсутній опис селективної інгібуючої дії відносно PI3Kδ. 2 UA 108390 C2 2 5 10 15 20 1 2 де R у формулах (A-1)-(E-3) являє собою дифторметильну групу або т. п. R і R у формулі (F) об'єднані один з одним і з атомом N, з яким вони зв'язані, з утворенням незаміщеної або 3 заміщений морфоліногрупи, X являє собою зв'язок або т. п., і R являє собою незаміщену або 2 заміщену індолільну групу. R у формулі (G) являє собою заміщену індол-4-ільну групу в 5- або 3 6 6-положенні. R у формулі (H) являє собою дифторметильну групу або т. п., і R являє собою 1 2 морфоліногрупу, що може бути заміщена, або т. п. У формулі (J) Y і Y являють собою N, CH 4 6 7 1 2 або т. п., X являє собою NR CR R або т. п., R являє собою гетероциклічну групу або т. п., і R являє собою гетероарильну групу або т. п. У формулі (K) X, Y і Z являють собою N або CH, за 1 2 умови, що щонайменше два з X, Y і Z являють собою N, R являє собою гетероарил або т. п., R являє собою гетероцикл або т. п., Q являє собою зв'язок, азетидинілен-4-аміно або т. п., T 5 7 являє собою -C(O)-, -C(=S)- або -S(O)2-, і R являє собою галоген або -O-S(O)2-R . Стосовно інших символів може бути зроблене посилання на публікацію. Повідомлялося, що описані нижче сполуки формули (L-1) (патентний документ 18), формули (L-2) (патентний документ 19), формули (L-3) (патентний документ 20), формули (L-4) (патентний документ 21) і формули (L-5) (патентний документ 22) мають протипухлинну активність. Крім того, у непатентному документі 2 було зроблене припущення, що вторинний амін формули (M) має інгібуючу Lck активність і інгібуючу продукцію IL-2 дію і застосовується при аутоімунних захворюваннях і реакції відторгнення при трансплантації органів. Однак сполука формули (I) згідно з даним винаходом неодмінно містить дифторметильну групу, що відрізняє її за структурою від сполук формул (L-1), (L-2) і (M). Вона також відрізняється від 1 сполук формул (L-3) і (L-5) за структурою групи R формули (I). Крім того, вона відрізняється від сполук формул (L-4) за структурою замісника на бензімідазольному кільці. Крім того, у якихнебудь документах відсутній опис селективної інгібуючої дії відносно PI3Kδ. 25 30 35 у формулі (L-1) і X, і Y являють собою N, або один з X і Y являє собою N, а інший являє 7 6 собою CR , і R являє собою H або C1-6алкіл; у формулі (L-2) і X, і Y являють собою N, або один 3 1 з X і Y являє собою N, а інший являє собою CR , і R являє собою морфоліногрупу або т. п.; у 1 2 формулі (L-3) X являє собою N або CH, R являє собою CHnF3-n (n дорівнює 1 або 2), і R являє собою морфоліно, що може бути заміщений, або т. п.; у формулі (L-4) X являє собою N або CH, і 1 1 R являє собою галоген або гідроксильну групу; у формулі (L-5) X являє собою N або CH, R являє собою морфоліногрупу, що може бути заміщена 1-4 C1-6алкільними групами, і Y являє 1 собою C1-6алкіл; і у формулі (M) R являє собою морфоліногрупу або т. п. Стосовно інших символів може бути зроблене посилання на публікацію. Крім того, повідомлялося про похідне хіназолін-4-ону як селективний інгібітор PI3Kδ (патентні документи 23-25), і була зазначена його застосовність при запаленні, імунних 3 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 захворюваннях або гематологічних пухлинах (лейкоз і т. п.). Повідомлялося про похідне тіазолілсечовини як інші селективні інгібітори PI3Kδ (патентний документ 26), поряд з його застосовністю при запаленні, імунних захворюваннях або т. п. Крім того, пізніше дати пріоритету даної заявки був розкритий винахід, що стосується триазинового або піримідинового похідного, що має селективну інгібуючу дію відносно PI3Kδ, що є винаходом з відомого рівня техніки, зробленим авторами даного винаходу (патентний документ 27). Сполука згідно з даним винаходом відрізняється від сполуки, розкритої в 1 попередній заявці, за структурою групи R у формулі (I). МАТЕРІАЛИ, ВИКОРИСТАНІ ПРИ ЕКСПЕРТИЗІ ЗАЯВКИ Патентні документи [Патентний документ 1] Брошура міжнародної публікації WO 2008/032027. [Патентний документ 2] Брошура міжнародної публікації WO 2008/032077. [Патентний документ 3] Брошура міжнародної публікації WO 2008/032086. [Патентний документ 4] Брошура міжнародної публікації WO 2008/032028. [Патентний документ 5] Брошура міжнародної публікації WO 2008/032036 [Патентний документ 6] Брошура міжнародної публікації WO 2008/032041. [Патентний документ 7] Брошура міжнародної публікації WO 2008/032033. [Патентний документ 8] Брошура міжнародної публікації WO 2008/032060. [Патентний документ 9] Брошура міжнародної публікації WO 2008/032064. [Патентний документ 10] Брошура міжнародної публікації WO 2008/032072. [Патентний документ 11] Брошура міжнародної публікації WO 2008/032089. [Патентний документ 12] Брошура міжнародної публікації WO 2008/032091. [Патентний документ 13] Брошура міжнародної публікації WO 2007/042810. [Патентний документ 14] Брошура міжнародної публікації WO 2008/125839. [Патентний документ 15] Опис опублікованої заявки на європейський патент № 1864665. [Патентний документ 16] Брошура міжнародної публікації WO 2009/007751. [Патентний документ 17] Брошура міжнародної публікації WO 2009/120094. [Патентний документ 18] Опис опублікованої заявки на європейський патент № 1020462. [Патентний документ 19] Міжнародна публікація WO 00/43385. [Патентний документ 20] Брошура опублікованої заявки на європейський патент № 1389617. [Патентний документ 21] Брошура опублікованої заявки на європейський патент № 1557415. [Патентний документ 22] Брошура опублікованої заявки на європейський патент № 1741714. [Патентний документ 23] Брошура міжнародної публікації WO 01/81346. [Патентний документ 24] Брошура міжнародної публікації WO 03/035075. [Патентний документ 25] Брошура міжнародної публікації WO 2005/113556. [Патентний документ 26] Брошура міжнародної публікації WO 2008/000421. [Патентний документ 27] Брошура міжнародної публікації WO 2010/092962. Непатентні документи [Непатентний документ 1] Journal of the National Cancer Institute, 2006, Vol. 98, p. 545-556. [Непатентний документ 2] Bioorganic & Medicinal Chemistry Letters, 2006, Vol. 16, p. 59735977. РОЗКРИТТЯ ВИНАХОДУ Задачі, які мають бути вирішені даним винаходом Надана фармацевтична композиція, наприклад фармацевтична композиція, що має інгібуючу дію відносно PI3Kδ, зокрема фармацевтична композиція для профілактики і/або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань і гематологічних пухлин, і гетероциклічна сполука, що застосовна як активний інгредієнт фармацевтичної композиції. Засоби вирішення задач Автори даного винаходу широко вивчали селективну інгібуючу дію відносно PI3Kδ і/або інгібуючу продукцію IL-2 дію, і/або інгібуючу проліферацію В-клітин дію (включаючи інгібуючу активацію дію), і в результаті вони знайшли, що нове триазинове або піримідинове похідне має чудову селективну інгібуючу дію відносно PI3Kδ і/або інгібуючу продукцію IL-2 дію, і/або інгібуючу проліферацію В-клітин дію (включаючи інгібуючу активацію дію) і може являти собою засіб для профілактики і/або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань і гематологічних пухлин, оформивши тим самим даний винахід. Тобто даний винахід стосується сполуки формули (I) або її солі і фармацевтичної композиції, що містить сполуку або її сіль і наповнювач. 60 4 UA 108390 C2 , 5 10 15 20 25 30 35 40 45 50 де 1 2 3 A , A і A є однаковими або відрізняються один від одного і являють собою CH або N, за 1 3 умови, що щонайменше два з A -A являють собою N, 3 B є однаковими або відрізняються один від одного і являють собою CR або N, за умови, що 3 щонайменше три з чотирьох B являють собою CR , 1 1 2 R являє собою -NH-нижчий алкілен-C(O)-OH або -L -L -Y, 2 R є однаковими або відрізняються один від одного і являють собою атоми галогену, -OH, O-нижчий алкіл, -CN або нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з галогену, -OH, -O-нижчого алкілу і -CN, n дорівнює цілому числу від 0 до 8, 3 R є однаковими або відрізняються один від одного і являють собою H, -O-нижчий алкіл, 4 4 ціано, -N(R )2, -C(O)-OH, -C(O)-O-нижчий алкіл, -C(O)-N(R )2 або нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -OH, -O4 4 нижчого алкілу, -N(R )2, -C(O)-OH, -C(O)-O-нижчого алкілу, -C(O)-N(R )2 і галогену, 4 R є однаковими або відрізняються один від одного і являють собою H або нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -OH, -O-нижчого алкілу, -CN, галогену, циклоалкілу і фенілу, 1 5 5 5 L являє собою -нижчий алкінілен-, -NR -, -NR -S(O)2-, -NR -C(O)-, -O-, -S- або -S(O)m-, m є однаковими або відрізняються один від одного і дорівнюють 1 або 2, 2 2 6 6 1 L являє собою зв'язок, -ALK-X -, -ALK-NR -C(O)-, -ALK-NR -C(O)-O-ALK-, -ALK-S(O)m-X - або 2 -ALK-C(O)-X -, ALK є однаковими або відрізняються один від одного і являють собою нижчий алкілен, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -OH, -O-нижчого алкілу, -CN, галогену, циклоалкілу і фенілу, 1 6 6 X являє собою зв'язок, -NR - або -NR -ALK-, 2 6 6 X є однаковими або відрізняються один від одного і являють собою зв'язок, -NR -, -NR 6 6 6 6 ALK-, -O-, -S-, -NR -ALK-O-, -NR -ALK-C(O)-NR - або -NR -ALK-C(O)-, 5 4 R є однаковими або відрізняються один від одного і являють собою -R , нижчий алкеніл або циклоалкіл, 6 R є однаковими або відрізняються один від одного і являють собою H, циклоалкіл, феніл, неароматичний гетероцикл, що може бути заміщений нижчим алкілом або нижчим алкілом, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з 4 -OH, -O-нижчого алкілу, -CN, галогену, -N(R )2, циклоалкілу, фенілу і неароматичного гетероциклу, Y являє собою нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -OH, -O-нижчого алкілу, -N(нижчий алкіл)2 і -C(O)-N(нижчий алкіл)2, циклоалкілу, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, арилу, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, ароматичного гетероциклу, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, або неароматичного гетероциклу, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, група D1 складається з: (1) галогену, 8 (2) -O-R , 8 (3) -S-R , (4) -CN, (5) -NO2, 4 7 7 8 8 8 8 8 (6) -NR R , де R являє собою -R , -C(O)-R , -C(O)-C(O)-N(R )2, -C(O)-O-R і -S(O)2-R , 8 (7) -C(O)-R , 5 UA 108390 C2 8 5 10 15 20 25 30 35 8 (8) -S(O)2-R і -S(O)2-N(R )2, 8 (9) -C(O)-O-R , 8 (10) -C(O)-N(R )2, 8 (11) -C(O)-C(O)-N(R )2, 8 8 (12) -O-C(O)-R , -O-C(O)-NH-C(=NH)-NH2 і -O-C(O)-N(R )2, 3 3 3 3 (13) -L -циклоалкілу, -L -арилу, -L -ароматичного гетероциклу і -L -неароматичного гетероциклу, де кожен циклоалкіл, арил, ароматичний гетероцикл і неароматичний гетероцикл може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, що може бути заміщений одним або декількома замісниками, вибраними з 6 6 6 6 6 6 групи, що складається з -O-R , -CN, галогену, -N(R )2, -C(O)-R , -C(O)-O-R , -C(O)-N(R )2, -N(R )6 C(O)-O-R , -S(O)2-нижчого алкілу, циклоалкілу, фенілу і неароматичного гетероциклу; оксо; циклоалкілу, арилу, ароматичного гетероциклу і неароматичного гетероциклу, кожний з яких може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -OH, -O-нижчого алкілу, -CN і галогену; і замісників (1)-(12), (14) оксо, і (15) нижчого алкілу, -O-нижчого алкілу і нижчого алкенілу, кожний з яких може бути заміщений одним або декількома замісниками, вибраними з замісників, описаних у (1)-(14), 3 5 L є однаковими або відрізняються один від одного і являють собою -зв'язок, -O-, -S-, -NR -, 5 5 5 NR -S(O)2-, -NR -C(O)-, -C(O)-NR -, -S(O)m-, -ALK-, -O-ALK-, -ALK-O-, -O-ALK-O-, -S-ALK-, -ALK-S5 5 5 5 , -ALK-S(O)m-, -S(O)m-ALK-, -NR -ALK-, -ALK-NR -, -C(O)-NR -ALK-, -C(O)-NR -ALK-C(O)-, -C(O)5 5 5 5 5 NR -ALK-O-ALK-, -NR -C(O)-ALK-, -NR -C(O)-ALK-C(O)-, -NR -C(O)-ALK-O-ALK-, -ALK-C(O)-NR -, 5 5 -ALK-NR -C(O)-, -C(O)-O-, -ALK-C(O)-O-, -C(O)-O-ALK-, -C(O)-ALK-, -ALK-C(O)-, -NR -C(O)-ALK5 NR - або -C(O)-, 8 R є однаковими або відрізняються один від одного і являють собою H; циклоалкіл, феніл, піридил або неароматичний гетероцикл, кожний з яких може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -OH, -O-нижчого 9 4 9 9 алкілу, -CN і галогену; -R або -ALK-L -R , де R являє собою нижчий алкіл, що може бути 6 заміщений одним або декількома замісниками, вибраними з групи, що складається з -O-R , -S6 6 6 6 6 6 6 R , -CN, -N(R )2, -C(O)-R , -C(O)-O-R , -C(O)-N(R )2, -N(R )-C(O)-O-R , -циклоалкілу, фенілу і неароматичного гетероциклу, і 4 5 5 5 5 5 L являє собою -C(O)-, -C(O)-NR -, -NR -, -NR -S(O)2-, -NR -C(O)-, -NR -C(O)-O-, -O-, -S- або S(O)m-, 1 за умови, що, у випадку, коли R характеризується наступною формулою (II), усі B являють 1 2 собою CH, W являє собою NH або O, B являє собою зв'язок або нижчий алкілен, і B являє собою зв'язок або нижчий алкілен, , 10 40 45 50 55 R являє собою -C(O)-(нижчий алкілен, заміщений -NH-C(O)-O-нижчим алкілом)-S-нижчий алкіл, -C(O)-неароматичний гетероцикл, -C(O)-нижчий алкілен-NH-нижчий алкілен-(циклоалкіл, що може бути заміщений -OH), -C(O)-нижчий алкілен-NH-(циклоалкіл, що може бути заміщений групою, вибраною з групи, що складається з нижчого алкілу і -OH), -C(O)-нижчий алкілен-NHнеароматичний гетероцикл, -C(O)-нижчий алкілен-NH-(нижчий алкіл, заміщений -OH) або -C(O)(циклоалкіл, заміщений одним або декількома замісниками, вибраними з групи, що складається з -NH2, -N(нижчий алкіл)2 і -NH-C(O)-O-нижчого алкілу), або 4 10 R і R утворюють разом з атомом N, з яким вони зв'язані, 4-8-членну моноциклічну гетероциклічну групу, що містить від 1 до 4 гетероатомів, вибраних з O, S і N, і, крім того, заміщену щонайменше одним замісником, вибраним із групи D2, де група D2 складається з: (a) -O-(нижчий алкіл, заміщений одним або декількома замісниками, вибраними з групи, що 6 6 6 6 6 6 6 6 складається з -O-R , -S-R , -CN, -N(R )2, -C(O)-R , -C(O)-O-R , -C(O)-N(R )2, -N(R )-C(O)-O-R , циклоалкілу і неароматичного гетероциклу), -O-(циклоалкіл, феніл, піридил або неароматичний гетероцикл, кожний з яких може бути заміщений одним або декількома замісниками, вибраними 4 9 з групи, що складається з нижчого алкілу, -OH, -O-нижчого алкілу, -CN і галогену) і -O-ALK-L -R , 8 (b) -SR , (c) -NO2, 6 UA 108390 C2 11 5 10 15 20 25 30 35 40 45 50 55 60 7 7 8 8 8 8 8 11 (d) -NR R , де R являє собою -R , -C(O)-R , -C(O)-C(O)-N(R )2, -C(O)-O-R і -S(O)2-R , і R являє собою нижчий алкіл, заміщений одним або декількома замісниками, вибраними з групи, що складається з -OH, -O-нижчого алкілу, -CN, галогену, циклоалкілу і фенілу, 8 (e) -C(O)-R , 8 8 (f) -S(O)2-R і -S(O)2-N(R )2, (g) -C(O)-O-(нижчий алкіл, заміщений одним або декількома замісниками, вибраними з 6 6 6 6 6 6 6 групи, що складається з -O-R , -S-R , -CN, -N(R )2, -C(O)-R , -C(O)-O-R , -C(O)-N(R )2, -N(R )6 C(O)-O-R , циклоалкілу, фенілу і неароматичного гетероциклу), -C(O)-O-(циклоалкіл, феніл, піридил або неароматичний гетероцикл, кожний з яких може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -OH, -O-нижчого 4 9 алкілу, -CN і галогену) і -C(O)O-ALK-L -R , 8 (h) -C(O)-N(R )2, 8 (i) -C(O)-C(O)-N(R )2, (j) -O-C(O)-(нижчий алкіл, заміщений одним або декількома замісниками, вибраними з групи, 6 6 6 6 6 6 6 6 що складається з -O-R , -S-R , -CN, -N(R )2, -C(O)-R , -C(O)-O-R , -C(O)-N(R )2, -N(R )-C(O)-O-R , циклоалкілу, фенілу і неароматичного гетероциклу), -O-C(O)-(циклоалкіл, феніл, піридил або неароматичний гетероцикл, кожний з яких може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -OH, -O-нижчого алкілу, -CN і 4 9 8 галогену), -O-C(O)-ALK-L -R , -O-C(O)-NH-C(=NH)-NH2 і -O-C(O)-N(R )2, (k) нижчого алкілу, заміщеного одним або декількома замісниками, вибраними з групи, що 6 6 6 6 6 6 складається з -CN, -N(R )2, -C(O)-R , -C(O)-O-R , -C(O)-N(R )2, -N(R )-C(O)-O-R , -S(O)2-нижчого алкілу, циклоалкілу і фенілу, (l) циклоалкілу, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -OH, -O-нижчого алкілу, -CN і галогену, (m) арилу, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -OH, -O-нижчого алкілу, -CN і галогену, (n) ароматичного гетероциклу, заміщеного одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -OH, -O-нижчого алкілу, -CN і галогену, і (o) неароматичного гетероциклу, заміщеного одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -OH, -O-нижчого алкілу, -CN і галогену. Якщо не зазначене інше, то, у випадку, коли позначення хімічних формул згідно з цим описом також використовуються в інших хімічних формулах, ті самі позначення мають ті самі значення. Крім того, даний винахід стосується фармацевтичної композиції для профілактики і/або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань і гематологічної пухлини, яка містить як активний інгредієнт сполуку формули (I) або її сіль. Крім того, фармацевтична композиція включає засіб для профілактики і/або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань і гематологічної пухлини, який містить сполуку формули (I) або її сіль. Відповідно до конкретного варіанта здійснення, даний винахід стосується засобу для профілактики і/або лікування реакцій відторгнення при трансплантації нирок, печінки і серця, відповідно до іншого варіанта здійснення - засобу для профілактики і/або лікування хронічного відторгнення і гострого відторгнення, і згідно з ще одним варіантом здійснення - засобу для профілактики і/або лікування відторгнення, пов'язаного з антитілами. Крім того, даний винахід стосується використання сполуки формули (I) або її солі при виробництві фармацевтичної композиції для профілактики і/або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань і гематологічної пухлини, і використання сполуки формули (I) або її солі для профілактики і/або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань і гематологічної пухлини, сполуки формули (I) або її солі для профілактики і/або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань і гематологічної пухлини, і способу профілактики або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань і гематологічної пухлини, який включає введення суб'єкту ефективної кількості сполуки формули (I) або її солі. У даному документі термін "суб'єкт" являє собою людину або будь-яку з інших тварин, що потребує відповідної профілактики або лікування, і відповідно до конкретного варіанта здійснення, людину, що потребує відповідної профілактиці або лікування. Крім того, даний винахід стосується селективного інгібітору PI3Kδ і/або інгібітору продукції IL-2, і/або інгібітору проліферації В-клітин, кожний з який містить сполуку формули (I) або її сіль. 7 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 Ефекти даного винаходу Сполука формули (I) має селективну інгібуючу дію відносно PI3Kδ і/або інгібуючу продукцію IL-2 дію, і/або інгібуючу проліферацію В-клітин дію (включаючи інгібуючу активацію дію), а тому може бути використана як засіб для профілактики або лікування реакцій відторгнення при трансплантації різних органів, алергічних захворювань, аутоімунних захворювань і гематологічної пухлини. ВАРІАНТИ ЗДІЙСНЕННЯ ДАНОГО ВИНАХОДУ Нижче даний винахід буде описано більш докладно. "Нижчий алкіл" являє собою нерозгалужений або розгалужений алкіл, що містить від 1 до 6 атомів вуглецю (тут і далі називаний просто C 1-6), і його приклади включають метил, етил, нпропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, н-пентил, н-гексил і т. п. Відповідно до іншого варіанта здійснення, нижчий алкіл являє собою C1-4алкіл, відповідно до іншого варіанта здійснення - метил, етил або трет-бутил, і відповідно до іншого варіанта здійснення метил. "Нижчий алкеніл" являє собою нерозгалужений або розгалужений C 2-6алкеніл і його приклади включають вініл, пропеніл, бутеніл, пентеніл, 1-метилвініл, 1-метил-2-пропеніл, 1,3бутадієніл, 1,3-пентадієніл і т. п. Відповідно до іншого варіанта здійснення, нижчий алкеніл являє собою C2-4алкеніл, і відповідно до іншого варіанта здійснення - пропеніл. "Нижчий алкілен" являє собою двовалентну групу, утворену шляхом видалення будь-якого атома водню "нижчого алкілу". Відповідно, "C1-6алкілен" являє собою нерозгалужений або розгалужений алкілен, що містить 1-6 атомів вуглецю, і його приклади включають метилен, етилен, триметилен, тетраметилен, пентаметилен, гексаметилен, метилметилен, диметилметилен, етилметилен, метилетилен, диметилетилен, етилетилен і т. п. Відповідно до іншого варіанта здійснення, нижчий алкілен являє собою метилен, етилен, і відповідно до іншого варіанта здійснення - метилен. "Нижчий алкенілен" являє собою нерозгалужений або розгалужений C 2-6алкенілен і його приклади включають вінілен, етиліден, пропенілен, бутенілен, пентенілен, гексенілен, 1,3бутадієнілен, 1,3-пентадієнілен і т. п. Відповідно до іншого варіанта здійснення, нижчий алкенілен являє собою C2-4алкенілен, і відповідно до іншого варіанта здійснення - пропенілен. "Нижчий алкінілен" являє собою нерозгалужений або розгалужений C 2-6алкінілен і його приклади включають етинілен, пропінілен, бутинілен, пентинілен, гексинілен, 1,3-бутадіїнілен, 1,3-пентадіїнілен і т. п. Відповідно до іншого варіанта здійснення, нижчий алкінілен являє собою C2-4алкінілен, і відповідно до іншого варіанта здійснення - пропінілен. "Галоген" являє собою F, Cl, Br або I, відповідно до іншого варіанта здійснення - F, і відповідно до іншого варіанта здійснення - Cl. "Циклоалкіл" являє собою насичену C3-10вуглеводневу кільцеву групу, що може містити місток і може бути об'єднана з неароматичною гетероциклічною групою з утворенням спірокільця. Його конкретні приклади включають циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил, циклогексеніл, циклооктил, біцикло[3.3.0]октан, гексагідро-1'H-спіро1,3-діоксан-2,2'-пентален, 1,4-діоксаспіро[4.5]декан, біцикло[2.2.2]октил, адамантил, азаспіро[5.5]ундеканіл, октагідроциклопента[c]пірол, інданіл і т. п. Відповідно до іншого варіанта здійснення, циклоалкіл являє собою циклопропіл, циклобутил, циклопентил, циклогексил, октагідропентален, дицикло[2.2.2]октил або адамантил, відповідно до іншого варіанта здійснення - C3-8циклоалкіл, відповідно до іншого варіанта здійснення - C3-6циклоалкіл, відповідно до іншого варіанта здійснення - циклогексил, відповідно до іншого варіанта здійснення - октагідропентален, і відповідно до іншого варіанта здійснення - адамантил. "Арил" являє собою ароматичну C 6-14вуглеводневу кільцеву групу, що містить від одного до трьох кілець, і його приклади включають феніл, нафтил і т. п. Відповідно до іншого варіанта здійснення, арил являє собою феніл. "Ароматичний гетероцикл" являє собою ароматичний гетероцикл, який містить 5-6-кільцевих атомів, які містять як атом, що складає кільце, щонайменше один гетероатом, вибраний з O, N і S, і він може бути конденсований з бензольним кільцем або ароматичним гетероциклом. Його приклади включать піридил, піроліл, піразиніл, піримідиніл, піридазиніл, імідазоліл, триазоліл, триазиніл, тетразоліл, тіазоліл, піразоліл, ізотіазоліл, оксазоліл, ізооксазоліл, тіадіазоліл, оксадіазоліл, тієніл, фурил, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, ізохіноліл, хіназолініл, хіноксалініл, фталазиніл, бензтіазоліл, бензізотіазоліл, бензтіадіазоліл, бензоксазоліл, бензізоксазоліл, бензофураніл, бензотієніл, карбазоліл, дибензо[b,d]фураніл, дибензо[b,d]тієніл, тієнопіридил, тієнопіримідиніл, тієнопіразил, 1,4-бензодіоксин-2-іл, [1,2,4]триазоло[4,3-a]піридил, імідазо[1,2-a]піридил і т. п. Відповідно до іншого варіанта 8 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 60 здійснення, ароматичний гетероцикл являє собою імідазоліл, піридил, піразиніл, індоліл, індазоліл, бензімідазоліл або бензтіазоліл. "Неароматичний гетероцикл" являє собою неароматичний гетероцикл, який містить 4-8 кільцевих членів, які містять як атом, що складає кільце, щонайменше один гетероатом, вибраний з O, N і S, що може містити ненасичені зв'язки в частині кільця і може бути з'єднаний місточковим зв’язком. Неароматичний гетероцикл може бути конденсований з бензольним кільцем або ароматичним гетероциклом. Крім того, атом сірки, який являє собою атом, що складає кільце, може бути окислений. Приклади неароматичного гетероциклу включають азетидиніл, піролідиніл, піперидиніл, піперазиніл, азепаніл, діазепаніл, морфолініл, тіоморфолініл, хінуклідиніл, 1,1-діоксидтіоморфолініл, тетрагідропіридиніл, оксетаніл, тетрагідрофураніл, тетрагідропіраніл, тетрагідротієніл, 4,5-дигідротіазоліл, діоксоланіл, діоксаніл, тетрагідротіопіраніл, тетрагідроізохіноліл, оксазолідиніл, тропан, 3,9діазаспіро[5.5]ундеканіл, 2,8-діазаспіро[4.5]деканіл, октагідропіроло[1,2-a]піразил, 5,6,7,8тетрагідро-1,7-нафталідил, 3,4-дигідро-2H-1,4-бензоксазиніл, 1,3-бензодіоксоліл, хроменіл, 1,4бензтіазиніл, 4,5-дигідро-1,3-тіазоліл і т. п. Відповідно до іншого варіанта здійснення, неароматичний гетероцикл являє собою азетидиніл, піролідиніл, піперидиніл, піперазиніл, морфолініл, тетрагідрофураніл, тетрагідропіраніл або азепаніл, відповідно до іншого варіанта здійснення - піролідиніл, піперидиніл, тетрагідропіраніл або азепаніл, відповідно до іншого варіанта здійснення - піперидиніл, і відповідно до іншого варіанта здійснення - піролідиніл. "Циклічний аміно" являє собою неароматичну гетероциклічну групу, що містить азотовмісну групу, має положення для зв'язування на атомі азоту серед вищевказаних "неароматичних гетероциклічних сполук" і може утворювати спірокільце, і його конкретні приклади включають піролідин-1-іл, піперидин-1-іл, азепан-1-іл, піперазин-1-іл, 1,3-оксазолідин-2-он, морфолін-4-іл, тіоморфолін-4-іл, 1,1-діоксидтіоморфолін-4-іл, 2-окса-6-азаспіро[3.3]гепт-6-ил, 1-окса-3азаспіро[4.5]декан-2-он, 2,5-діазабіцикло[2.2.1]гептан, 2-окса-5-азаспіро[3.4]октан, 2-окса-5азабіцикло[2.2.1]гептан і т. п. Відповідно до іншого варіанта здійснення, циклічний амін являє собою піролідин-1-іл. 10 4 Більше того, моноциклічна гетероциклічна група у виразі "R і R утворюють разом з атомом N, з яким вони зв'язані, 4-8-членну моноциклічну гетероциклічну групу, що містить 1-4 гетероатоми, вибрані з O, S і N", являє собою 4-8-членну моноциклічну групу, що містить 1-4 гетероатоми, вибрані з O, S і N, у вищеописаних "ароматичному гетероциклі" і "циклічному аміно". Згідно з цим описом, вираз "який може бути заміщений" означає відсутність заміщення або заміщення 1-5 замісниками. Відповідно до визначених варіантів здійснення, це являє собою відсутність заміщення або заміщення 1-3 замісниками, відповідно до іншого варіанта здійснення - відсутність заміщення або заміщення 1 замісником, і відповідно до іншого варіанта здійснення - відсутність заміщення. Крім того, у випадку множини замісників замісники можуть бути однаковими або відрізнятися один від одного. Відповідно до визначених варіантів здійснення, група D1 складається з: (1) галогену, (2) -OH, (3) -O-нижчого алкілу, (4) -CN, (5) -NO2, 4a 7 4a 7 (6) -NR R , де R являє собою H або нижчий алкіл, R являє собою нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з галогену, -OH, -O-нижчого алкілу й арилу, -C(O)-нижчого алкілу, -C(O)-нижчий алкілен-N(нижчий алкіл)2, нижчого алкенілу, -C(O)-нижчий алкілен-NH-(нижчий алкіл, заміщений циклоалкілом), C(O)-нижчий алкілен-NH-(циклоалкіл, що може бути заміщений нижчим алкілом), -C(O)Oнижчого алкілу або H, (7) -C(O)-нижчого алкілу, 4 (8) -C(O)-нижчий алкілен-N(R )2, (9) -C(O)O-нижчого алкілу, (10) -C(O)OH, 4 (11) -C(O)-N(R )2, (12) -O-C(O)-NH-C(=NH)-NH2, 5 5 5 5 (13) -L -циклоалкілу, -L -арилу, -L -ароматичного гетероциклу і -L -неароматичного гетероциклу, де кожен циклоалкіл, арил, ароматичний гетероцикл і неароматичний гетероцикл може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, що може бути заміщений одним або декількома замісниками, вибраними з 9 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 групи, що складається з -OH, галогену, -O-нижчого алкілу і неароматичного гетероциклу, -OH, O-нижчого алкілу, -NH2, галогену, -C(O)O-нижчого алкілу, -C(O)-нижчого алкілу, оксо, -NH-S(O)24 нижчого алкілу, -NH-S(O)2-циклоалкілу, -NH-C(O)-нижчого алкілу, -NR -C(O)-O-(нижчий алкіл, що може бути заміщений -OH), -S(O)2-нижчого алкілу, -NH-(нижчий алкіл, що може бути заміщений 5 OH), циклоалкілу, що може бути заміщений -OH, і неароматичного гетероциклу, де L є однаковими або відрізняються один від одного і являють собою зв'язок, -O-, -нижчий алкілен, O-нижчий алкілен-O-, -C(O)-NH-, -NH-C(O)-, -C(O)-нижчий алкілен- або -C(O)-; відповідно до іншого варіанта здійснення, циклоалкіл може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з галогену, OH і -O-нижчого алкілу, галогену, -OH, -O-нижчого алкілу, -NH-нижчий алкілен-OH, -NH2, -NHC(O)-O-нижчого алкілу, -NH-нижчого алкілу і -C(O)-O-нижчого алкілу; арил може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, галогену, -O-нижчого алкілу і -C(O)-O-нижчого алкілу; ароматичний гетероцикл може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу і -NH2; і неароматичний гетероцикл може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -OH, галогену, -Oнижчого алкілу і неароматичного гетероциклу, -NH2, галогену, -C(O)-O-нижчого алкілу, -C(O)нижчого алкілу, оксо, -NH-S(O)2-нижчого алкілу, -NH-S(O)2-циклоалкілу, -NH-C(O)-нижчого 4 алкілу, -NR -C(O)-O-(нижчий алкіл, що може бути заміщений -OH), -S(O)2-нижчого алкілу, -NH(нижчий алкіл, заміщений -OH), циклоалкілу, що може бути заміщений -OH, і неароматичного гетероциклу, (14) оксо, і (15) нижчого алкілу, -O-нижчого алкілу і нижчого алкенілу, кожний з яких може бути заміщений одним або декількома замісниками, вибраними з замісників, описаних у (1)-(14) вище. Відповідно до іншого варіанта здійснення, група D1 складається з: (1) галогену, (2) -OH, (3) -O-нижчого алкілу, 4a 7 4a 7 (4) -NR R , де R являє собою H або нижчий алкіл, R являє собою нижчий алкіл, що може бути заміщений -OH, -C(O)-нижчий алкілен-N(нижчий алкіл)2, -C(O)-нижчий алкілен-NH-(нижчий алкіл, заміщений циклоалкілом), -C(O)-(циклоалкіл, заміщений -NH2), -C(O)-нижчий алкілен-NHтетрагідропіран, -C(O)-нижчий алкілен-N(нижчий алкіл)-(циклоалкіл, що може бути заміщений нижчим алкілом) або -C(O)-нижчий алкілен-NH-(циклоалкіл, що може бути заміщений нижчим алкілом), 4 (5) -C(O)-нижчий алкілен-N(R )2, (6) -C(O)O-нижчого алкілу, 5 (7) -L -(арил, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, галогену і -O-нижчого алкілу), 5 (8) -L -(неароматичний гетероцикл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -NH-C(O)-O-нижчого алкілу, NH-C(O)-нижчого алкілу, -C(O)-O-нижчого алкілу, -C(O)-нижчого алкілу, -S(O)2-нижчого алкілу, оксо і -NH-нижчого алкілу), 5 (9) -L -(циклоалкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, що може бути заміщений однією або декількома групами, вибраними з групи, що складається з галогену і -OH, галогену, -OH, -O-нижчого алкілу і -C(O)O-нижчого алкілу), і (10) нижчого алкілу, що може бути заміщений одним або декількома замісниками, вибраними з замісників, описаних вище в пунктах (1)-(9). Відповідно до іншого варіанта здійснення, група D1 складається з: (1) -OH, (2) -O-нижчого алкілу, 4a 7 4a 7 (3) -NR R , де R являє собою H або нижчий алкіл, R являє собою нижчий алкіл, що може бути заміщений -OH, -C(O)-(циклоалкіл, заміщений -NH2), -C(O)-нижчий алкілен-NHтетрагідропіран, -C(O)-нижчий алкілен-N(нижчий алкіл)-(циклоалкіл, що може бути заміщений нижчим алкілом) або -C(O)-нижчий алкілен-NH-(циклоалкіл, що може бути заміщений нижчим алкілом), 10 UA 108390 C2 5a 5 10 15 20 25 30 35 40 45 50 55 (4) -L -(неароматичний гетероцикл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -NH-C(O)-O-нижчого алкілу, 5a NH-C(O)-нижчого алкілу, -C(O)-O-нижчого алкілу, -C(O)-нижчого алкілу й оксо), де L являє собою зв'язок, -C(O)-нижчий алкілен- або -C(O)-, і 5b (5) -L -(циклоалкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, що може бути заміщений -OH, галогеном, -OH і -O5b нижчим алкілом), де L являє собою зв'язок або -C(O)-. Крім того, відповідно до іншого варіанта здійснення, група D1 складається з: 5a (1) -L -(неароматичний гетероцикл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, -NH-C(O)-O-нижчого алкілу, 5a C(O)O-нижчого алкілу, -C(O)-нижчого алкілу й оксо), де L являє собою зв'язок, -C(O)-нижчий алкілен- або -C(O)-, і (2) -C(O)-(циклоалкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з нижчого алкілу, що може бути заміщений -OH, -OH і -Oнижчим алкілом). Визначені варіанти здійснення сполуки формули (I) згідно з даним винаходом представлені нижче. 1 2 3 1 2 3 (1) Відповідно до визначеного варіанта здійснення A , A і A , будь-який з A , A і A являє 1 3 2 собою CH, відповідно до іншого варіанта здійснення, A і A являють собою N, і A являє собою 2 3 1 CH, і відповідно до іншого варіанта здійснення, A і A являють собою N, і A являє собою CH. 3 3 (2) Відповідно до визначеного варіанта здійснення B, усі B являють собою CR , де R являє собою H, нижчий алкіл, що може бути заміщений галогеном або -O-нижчим алкілом, відповідно 3 до іншого варіанта здійснення, R являє собою H або нижчий алкіл, відповідно до іншого 3 варіанта здійснення, R являє собою нижчий алкіл, крім того, відповідно до іншого варіанта 3 здійснення, R являє собою H, крім того, згідно з іншим варіантом здійснення, один з B являє собою N, а інші являють собою CH, і згідно ще з одним іншим варіантом здійснення, усі B являють собою CH. 1 1 1 2 (3) Відповідно до визначеного варіанта здійснення R , R являє собою -L -L -Y. 1 1 5 5 (4) Відповідно до визначеного варіанта здійснення L , L являє собою -NR -, -NR -S(O)2-, 5 1 NR -C(O)- або -O-, відповідно до іншого варіанта здійснення, L являє собою -NH-, -N(нижчий алкіл)- або -O-, відповідно до іншого варіанта здійснення - -NH- або -O-, згідно ще з одним іншим варіантом здійснення - -NH-, і, крім того, відповідно до іншого варіанта здійснення - -O-. 2 (5) Відповідно до визначеного варіанта здійснення, L являє собою зв'язок, -ALK-, -ALK-S-, 1 2 1 6 2 ALK-S(O)m-X - або -ALK-C(O)-X -, де X являє собою зв'язок або -NR -, X являє собою зв'язок, 6 6 6 NR -, -NR -ALK- або -O-, ALK являє собою нижчий алкілен, і R являє собою H або нижчий алкіл; 2 відповідно до іншого варіанта здійснення, L являє собою зв'язок, нижчий алкілен або -нижчий алкілен-C(O)NH-; відповідно до іншого варіанта здійснення - зв'язок або нижчий алкілен; згідно ще з одним іншим варіантом здійснення - зв'язок; згідно ще з одним іншим варіантом здійснення - нижчий алкілен; і згідно ще з одним іншим варіантом здійснення - метилен. (6) Відповідно до визначених варіантів здійснення, Y являє собою циклоалкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, арил, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, ароматичний гетероцикл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, або неароматичний гетероцикл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1; відповідно до іншого варіанта здійснення - циклоалкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, або неароматичний гетероцикл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1; відповідно до іншого варіанта здійснення - циклоалкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1; згідно ще з одним іншим варіантом здійснення неароматичний гетероцикл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1; згідно ще з одним іншим варіантом здійснення - циклогексил або циклічний аміно; згідно ще з одним іншим варіантом здійснення - циклогексил; згідно ще з одним іншим варіантом здійснення - циклічний аміно; згідно ще з одним іншим варіантом здійснення - піперидиніл, піролідиніл або азетидиніл; і згідно ще з одним іншим варіантом здійснення - піролідиніл або азетидиніл. (7) Відповідно до визначених варіантів здійснення, n дорівнює цілому числу з 0, 1 або 2, і відповідно до іншого варіанта здійснення - 0. 2 (8) Відповідно до визначених варіантів здійснення, R є однаковими або відрізняються один від одного і являють собою нижчий алкіл, що може бути заміщений галогеном. 11 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 (9) Сполука або її сіль, що являє собою сполучення будь-яких двох або декількох з описаних вище варіантів здійснення (1)-(8). Сполука або її сіль, що являють собою сполучення будь-яких двох або декількох з описаних вище варіантів здійснення (1)-(8), також включені в даний винахід, як описано вище в пункті (9), і їх конкретні приклади також включають наступні варіанти здійснення. 1 1 2 1 (10) Сполука або її сіль, де R являє собою -NH-нижчий алкілен-C(O)-OH або -L -L -Y, L 5 5 5 являє собою -нижчий алкінілен-, -NR -, -NR -S(O)2-, -NR -C(O)-, -O-, -S- або -S(O)m-, m дорівнює 2 2 6 6 1 або 2, L являє собою зв'язок, -ALK-X -, -ALK-NR -C(O)-, -ALK-NR -C(O)-O-ALK-, -ALK-S(O)m1 2 X - або -ALK-C(O)-X -, ALK є однаковими або відрізняються один від одного і являють собою нижчий алкілен, що може бути заміщений одним або декількома замісниками, вибраними з 1 групи, що складається з -OH, -O-нижчого алкілу, -CN, галогену і циклоалкілу, X являє собою 6 6 2 зв'язок, -NR - або -NR -ALK-, X є однаковими або відрізняються один від одного і являють 6 6 6 6 6 6 собою зв'язок, -NR -, -NR -ALK-, -O-, -S-, -NR -ALK-O-, -NR -ALK-C(O)-NR - або -NR -ALK-C(O)-, 4 R є однаковими або відрізняються один від одного і являють собою H, або нижчий алкіл, який може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з 5 -OH, -O-нижчого алкілу, -CN, галогену і циклоалкілу, R є однаковими або відрізняються один від 4 6 одного і являють собою -R , нижчий алкеніл або циклоалкіл, R є однаковими або відрізняються один від одного і являють собою H, циклоалкіл, неароматичний гетероцикл, який може бути заміщений нижчим алкілом, або нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -OH, -O-нижчого алкілу, -CN, галогену, 4 N(R )2, циклоалкілу і неароматичного гетероциклу, Y являє собою нижчий алкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи, що складається з -OH, -Oнижчого алкілу, -N(нижчий алкіл)2 і -C(O)-N(нижчий алкіл)2, циклоалкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, або неароматичний гетероцикл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, за умови, що 2 2a 6 6 1 L являє собою -ALK-X -, -ALK-NR -C(O)-, -ALK-NR -C(O)-O-ALK-, -ALK-S(O)m-X - або -ALK2 2a 6 6 6 6 C(O)-X -, причому, у випадку, коли X являє собою -NR -, -NR -ALK-, -O-, -S-, -NR -ALK-O-, -NR 6 6 ALK-C(O)-NR - або -NR -ALK-C(O)-, Y являє собою арил, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, або ароматичний гетероцикл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1. 1 1 2 1 (11) Сполука або її сіль, як описано в пункті (10), де R являє собою -L -L -Y, L являє собою 5 5 5 5 2 -NR -, -NR -S(O)2-, -NR -C(O)- або -O-, де R являє собою H або нижчий алкіл, L являє собою 1 2 1 6 2 зв'язок, -ALK-, -ALK-S-, -ALK-S(O)m-X - або -ALK-C(O)-X -, де X являє собою зв'язок або -NR -, X 6 6 6 являє собою зв'язок, -NR -, -NR -ALK- або -O-, ALK являє собою нижчий алкілен, R являє собою H або нижчий алкіл, і Y являє собою циклоалкіл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1, або неароматичний гетероцикл, що може бути заміщений одним або декількома замісниками, вибраними з групи D1. 1 2 (12) Сполука або її сіль, як описано в пункті (11), де -L -L - являє собою -NH- або -O-. (13) Сполука або її сіль, як описано в пункті (12), де всі B являють собою CH, і n дорівнює 0. 1 3 2 (14) Сполука або її сіль, як описано в пункті (13), де A і A являють собою N, і A являє собою CH. 2 3 1 (15) Сполука або її сіль, як описано в пункті (13), де A і A являють собою N, і A являє собою CH. Приклади конкретних сполук, що включені в сполуку формули (I) або її сіль, включають наступні сполуки: метил-{(3S)-1-[транс-4-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4іл)піримідин-4-іл}окси)циклогексил]-2-оксопіролідин-3-іл}карбамат, метил-{(3R)-1-[транс-4-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4іл)піримідин-4-іл}окси)циклогексил]-2-оксопіролідин-3-іл}карбамат, етил-{(3R)-1-[транс-4-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин4-іл}окси)циклогексил]-2-оксопіролідин-3-іл}карбамат, [(3S)-3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}аміно)піролідин-1-іл][(2R)-тетрагідрофуран-2-іл]метанон, [(3S)-3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}аміно)піролідин-1-іл](тетрагідро-2H-піран-4-іл)метанон, метил-{(3S)-1-[транс-4-({4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6-(морфолін-4іл)піримідин-2-іл}аміно)циклогексил]-2-оксопіролідин-3-іл}карбамат, метил-{(3R)-1-[транс-4-({4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6-(морфолін-4іл)піримідин-2-іл}аміно)циклогексил]-2-оксопіролідин-3-іл}карбамат, 12 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 60 метил-{(3R)-1-[транс-4-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4іл)піримідин-4-іл}аміно)циклогексил]-2-оксопіролідин-3-іл}карбамат, 1-[(3S)-3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}аміно)піролідин-1-іл]-2-(тетрагідрофуран-2-іл)етанон, 1-[(3S)-3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}аміно)піролідин-1-іл]-2-(тетрагідро-2H-піран-4-іл)етанон, 1-[3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}оксі)азетидин-1-іл]-2-(тетрагідрофуран-2-іл)етанон, метил-4-{[(3S)-3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}аміно)піролідин-1-іл]карбоніл}піперидин-1-карбоксилат, [(3S)-3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}окси)піролідин-1-іл](тетрагідрофуран-3-іл)метанон, 4-{[(3S)-3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}окси)піролідин-1-іл]карбоніл}-1-метилпіролідин-2-он, 2-(1-ацетилпіперидин-4-іл)-1-[(3S)-3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін4-іл)піримідин-4-іл}аміно)піролідин-1-іл]етанон, [(3S)-3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}аміно)піролідин-1-іл](тетрагідрофуран-3-іл)метанон, 4-{[(3S)-3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}аміно)піролідин-1-іл]карбоніл}-1-метилпіролідин-2-он, 1-[(3S)-3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}аміно)піролідин-1-іл]-2-(піперидин-1-іл)етанон, (5S)-5-{[3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}оксі)азетидин-1-іл]карбоніл}піролідин-2-он, (5S)-5-{[3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}аміно)азетидин-1-іл]карбоніл}піролідин-2-он, 2-(1-ацетилпіперидин-4-іл)-1-[3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4іл)піримідин-4-іл}аміно)азетидин-1-іл]етанон, [3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}аміно)азетидин-1-іл](тетрагідрофуран-3-іл)метанон, 4-{[3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}аміно)азетидин-1-іл]карбоніл}-1-метилпіролідин-2-он, [(3S)-3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}аміно)піролідин-1-іл][цис-4-(гідроксиметил)циклогексил]метанон і [(3S)-3-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}аміно)піролідин-1-іл][транс-4-(гідроксиметил)циклогексил]метанон, і їх солі. Залежно від виду замісників сполука формули (I) може існувати у формі таутомерів або геометричних ізомерів. Згідно з цим описом, сполука формули (I) буде описана тільки в одній формі ізомеру, хоча даний винахід включає інші ізомери, виділені форми ізомерів або їх суміші. Крім того, у деяких випадках сполука формули (I) може містити асиметричні атоми вуглецю або осьову асиметрію, і, відповідно, вона може існувати у формі основаних на цьому оптичних ізомерів. Даний винахід включає як виділену форму оптичних ізомерів сполуки формули (I), так і їх суміші. Більше того, даний винахід також включає фармацевтично прийнятні проліки сполуки, представленої формулою (I). Фармацевтично прийнятні проліки являють собою сполуку, яка містить групу, що може бути перетворена в аміногрупу, гідроксильну групу, карбоксильну групу або т. п. за допомогою сольволізу або у фізіологічних умовах. Приклади групи, що утворює проліки, включають групи, описані в Prog. Med., 5, 2157-2161 (1985); і "Pharmaceutical Research and Development" (Hirokawa Publishing Company, 1990), Vol. 7, Molecular Design, 163-198. Більше того, залежно від виду замісників сіль сполуки формули (I) може утворювати кислотно-адитивну сіль або сіль з основою, і такі солі включені в даний винахід, оскільки вони являють собою фармацевтично прийнятні солі. Їх конкретні приклади включають кислотноадитивні солі з неорганічними кислотами, такими як соляна кислота, бромистоводнева кислота, йодистоводнева кислота, сірчана кислота, азотна кислота і фосфорна кислота, і з органічними кислотами, такими як мурашина кислота, оцтова кислота, пропіонова кислота, щавлева кислота, малонова кислота, бурштинова кислота, фумарова кислота, малеїнова кислота, молочна кислота, яблучна кислота, мигдальна кислота, винна кислота, дибензилвинна кислота, дитолуолвинна кислота, лимонна кислота, метансульфонова кислота, етансульфонова кислота, бензолсульфонова кислота, пара-толуолсульфонова кислота, аспарагінова кислота і глутамінова кислота, і солі з неорганічними основами, такими як натрій, калій, магній, кальцій і 13 UA 108390 C2 5 10 15 20 25 30 алюміній, або з органічними основами, такими як метиламін, етиламін, етаноламін, лізин і орнітин, солі з різними амінокислотами, такими як ацетиллейцин, і похідними амінокислот, а також солі амонію. Крім того, даний винахід також включає різні гідрати або сольвати і поліморфні кристалічні речовини сполуки формули (I) і її фармацевтично прийнятних солей. Крім того, даний винахід також включає сполуки, мічені різними радіоактивними або нерадіоактивними ізотопами. "Селективний інгібітор PI3Kδ" означає інгібітор, що виявляє потужну активність, причому інгібуюча активність відносно PI3Kδ у 10 разів або більше, відповідно до іншого варіанта здійснення - у 30 разів або більше, і відповідно до іншого варіанта здійснення - у 100 разів або більше перевищує інгібуючу активність відносно PI3Kα в одиницях значень IC50. Способи одержання Сполука формули (I) і її фармацевтично прийнятні солі можуть бути одержані з використанням різних відомих способів синтезу на основі характеристик, що виникають зі структури кістяка їх молекул або типу їх замісників. У деяких випадках, у процесі одержання, заміна релевантної функціональної групи придатною захисною групою (група, що може бути легко перетворена в релевантну функціональну групу) на стадії одержання проміжної речовини з вихідної речовини може бути ефективною, залежно від типу функціональної групи в технології виробництва. Приклади такої функціональної групи включають аміногрупу, гідроксильну групу і карбоксильну групу, і така захисна група для такої функціональної групи може включати, rd наприклад, захисні групи, описані в Greene and Wuts, "Protective Groups in Organic Synthesis (3 edition, 1999)", які за необхідності можуть бути вибрані і використовуватися залежно від умов реакції. У такому способі, після введення захисної групи і наступної реакції, захисна група може бути видалена за необхідності одержання цільової сполуки. Крім того, проліки сполуки формули (I) можуть бути одержані шляхом введення конкретної групи на стадії одержання проміжної речовини з вихідної речовини або шляхом проведення реакції з застосуванням одержаної сполуки формули (I), як у випадку вищезгаданої захисної групи. Реакцію можна проводити з застосуванням відомих фахівцям у даній галузі техніки способів, таких як звичайна етерифікація, амідування, дегідратація і т. п. Нижче будуть описані типові способи одержання сполуки формули (I). Кожний зі способів одержання також може проводитися відповідно до посилань, прикладених до даного опису. Крім того, способи одержання згідно з даним винаходом не обмежені представленими нижче прикладами. Спосіб одержання 1 , 35 21 1 40 45 50 2 де X являє собою відхідну групу, R являє собою -NH-нижчий алкілен-C(O)-OH або -L -L -Y, 5 5 5 і L являє собою -NR -, -NR -S(O)2-, -NR -C(O)-, -O-, -S- або -S(O)m-. Те ж варто застосовувати і далі в даному документі. Сполука (I-1) згідно з даним винаходом може бути одержана за допомогою реакції іпсо1 2 заміщення сполуки (1), наприклад -L -L -Y. Приклади відхідної групи X включають галоген, метилсульфінільні, метилсульфонільні групи і т. п. 1 Зазначену взаємодію проводять шляхом використання сполуки (1) і, наприклад, сполуки -L 2 L -Y в еквівалентних кількостях або кожної в надлишку, перемішування їх суміші в розчиннику, що є інертним відносно реакційної суміші, або за відсутності розчинника, у діапазоні температур від температури охолодження до нагрівання і перегонки зі зворотним холодильником, переважно при 0-100 °C, звичайно протягом 0,1 години - 5 діб. Приклади використовуваного в цій реакції розчинника конкретно не обмежені, але включають такі ароматичні вуглеводні, як бензол, толуол, ксилол і т. п., ефіри, такі як діетиловий ефір, тетрагідрофуран, діоксан, 1 14 UA 108390 C2 5 10 диметоксіетан і т. п., галогеновані вуглеводні, такі як дихлорметан, 1,2-дихлоретан, хлороформ і т. п., N,N-диметилформамід, N,N-диметилацетамід, диметилсульфоксид, етилацетат, ацетонітрил і їх суміші. У деяких випадках для полегшення процесу протікання реакції є переважним використання органічних основ, таких як триетиламін, N,N-діізопропілетиламін, Nметилморфолін і т. п., або неорганічних основ, таких як карбонат калію, карбонат натрію, карбонат цезію, гідроксид калію і т. п. У деяких випадках для полегшення процесу протікання реакції може бути корисним проведення реакції шляхом нагрівання реакційної суміші мікрохвильовим опроміненням. Документи nd Sandler S. R. and Karo W. "Organic Functional Group Preparations", 2 edition, Vol. 1, Academic Press Inc., 1991. th "Jikken Kagaku Koza (Courses in Experimental Chemistry) (5 Edition) (Vol. 14)", edited by The Chemical Society of Japan, Maruzen, 2005. Спосіб одержання 2 15 20 Сполука формули (I-2) може бути одержана шляхом здійснення взаємодії сполуки (2) і сполуки (3). Умови реакції були тими ж, що й у способі одержання 1. Спосіб одержання 3 , 12 25 30 35 де L являє собою -нижчий алкінілен. Сполука (I-3) згідно з даним винаходом може бути одержана в реакції сполучення по Соногашира сполуки (4) і похідного, що містить кінцевий алкін. Приклади відхідної групи X включають галоген і т. п. Зазначену взаємодію проводять шляхом використання сполуки (4) і похідного, що містить кінцевий алкін, в еквівалентних кількостях або кожного в надлишку, і перемішування їх суміші в розчиннику, що є інертним відносно реакційної суміші, у температурних умовах, що варіюють від кімнатної температури до температури нагрівання і перегонки зі зворотним холодильником, звичайно протягом 0,1 години - 5 діб, у присутності основи і паладієвого каталізатора. Зазначену взаємодію переважно проводять в атмосфері інертного газу. Приклади використовуваного в цій реакції розчинника конкретно не обмежені, але включають такі ароматичні вуглеводні, як бензол, толуол, ксилол і т. п., ефіри, такі як діетиловий ефір, тетрагідрофуран, діоксан, диметоксіетан і т. п., галогеновані вуглеводні, такі як дихлорметан, 1,2-дихлоретан, хлороформ і т. п., спирти, такі як метанол, етанол, 2-пропанол, бутанол і т. п., 15 UA 108390 C2 5 10 15 20 N,N-диметилформамід, диметилсульфоксид і їх змішаний розчинник. Як основа переважними є неорганічні основи, такі як карбонат калію, карбонат натрію, карбонат цезію, гідроксид калію і т. п. Як паладієвий каталізатор переважними є тетракис(трифенілфосфін)паладій, дихлорбіс(трифенілфосфін)паладій, паладій-1,1'-біс(дифенілфосфіно)фероценхлорид і т. п. Крім того, у деяких випадках для полегшення процесу протікання реакції може бути корисним проведення реакції шляхом нагрівання реакційної суміші мікрохвильовим опроміненням. Документи "Metal-Catalyzed Cross-Coupling Reactions", edited by A. d. Meijere and F. Diederich, Vol. 1, VCH Publishers Inc., 1997. th "Jikken Kagaku Koza (Courses in Experimental Chemistry) (5 Edition)", edited by The Chemical Society of Japan, Vol. 13 (2005) (Maruzen). 1 Різні замісники на R у сполуці формули (I) можуть бути легко перетворені в інші функціональні групи шляхом використання сполуки формули (I) як вихідної речовини і за допомогою взаємодій, описаних у представлених далі прикладах, причому взаємодії очевидні фахівцям у даній галузі техніки, або їх модифікованих способів. Наприклад, стадії, що можуть звичайно використовуватися фахівцями в даній галузі техніки, такі як O-алкілування, Nалкілування, окислювання, відновлення, відновне алкілування, утворення кільця, гідроліз, амідування, ацилювання, зняття захисних груп, епоксилювання і т. п., можуть бути довільно об'єднані і здійснені. Одержання вихідної сполуки Відповідно до вищевказаного способу одержання, вихідна сполука може бути одержана з використанням, наприклад, будь-якого їх зазначених нижче способів, способів, описаних у представлених далі прикладах одержання, відомих способів або їх модифікованих способів. Синтез вихідних речовин 1 25 30 35 40 Цей спосіб одержання являє собою спосіб одержання сполуки (9), де X являє собою -S(O)mметил у сполуці (1), що являє собою вихідну сполуку в способі одержання 1. Сполука (7) може бути одержана шляхом здійснення взаємодії сполуки (5) зі сполукою (6). Умови реакції є такими ж, як і в способі одержання 1. Сполука (8) може бути одержана шляхом здійснення взаємодії сполуки (7) зі сполукою (3). Умови реакції є такими ж, як і в способі одержання 1. Сполука (9) може бути одержана в реакції окислювання сполуки (8). Зазначену взаємодію проводили з використанням сполуки (9) в еквівалентній кількості або в надлишку, у температурному діапазоні від охолодження до нагрівання. Як розчинник можуть бути використані такі розчинники, як ароматичні вуглеводні і галогеновані вуглеводні, окремо або у вигляді суміші двох або декількох видів розчинників. Приклади окислювача включають мета-хлорпероксибензойну кислоту, пероксіоцтову кислоту і розчин пероксиду водню. 16 UA 108390 C2 Синтез вихідних речовин 2 5 10 15 20 25 30 35 40 Цей спосіб одержання являє собою спосіб одержання сполуки (13), де X являє собою 1 21 S(O)m-метил, і R являє собою R у сполуці (2), що являє собою вихідну сполуку в способі одержання 2. Сполука (11) може бути одержана шляхом здійснення взаємодії сполуки (10) зі сполукою (6). Умови реакції є такими ж, як і в способі одержання 1. Сполука (12) може бути одержана шляхом здійснення реакції іпсо-заміщення сполуки (11), 1 2 наприклад -L -L -Y. Умови реакції є такими ж, як і в способі одержання 1. Сполука (13) може бути одержана в реакції окислювання сполуки (12). Умови реакції є такими ж, як і в реакції окислювання, описаній в синтезі вихідної речовини 1. Інші вихідні сполуки (1), (2) і (4) можуть бути одержані, наприклад, способами, описаними в наступних документах: WO 2002/088112, EP 1389617, WO 2008/032033, WO 2008/032036, WO 2008/032041 або WO 2008/032060. Сполуки формули (I) можуть бути виділені й очищені у вигляді їх вільних сполук, фармацевтично прийнятних солей, гідратів, сольватів або їх поліморфних кристалічних речовин. Фармацевтично прийнятні солі сполуки формули (I) можуть бути одержані шляхом здійснення обробки в традиційній реакції утворення солі. Виділення й очищення проводили шляхом використання звичайних хімічних операцій, таких як екстракція, фракційна кристалізація, різні типи фракційної хроматографії і т. п. Різні ізомери можуть бути одержані шляхом вибору відповідної вихідної сполуки або розділені з використанням відмінності у фізико-хімічних властивостях між ізомерами. Наприклад, оптичні ізомери можуть бути одержані за допомогою загального способу проведення оптичного розщеплення рацематів (наприклад, фракційна кристалізація для індукції діастереоізомерних солей з оптично активними основами або кислотами, хроматографія з застосуванням хіральної колонки і т. п., і інші), і, крім того, ізомери також можуть бути одержані з відповідної оптично активної вихідної сполуки. Фармакологічна активність сполуки формули (I) була підтверджена в тестах, представлених нижче. 1. Інгібуюча активність відносно ферменту PI3Kδ У цьому експерименті використовували набір для аналізу PI3-кінази методом HTRF (Millipore Corporation, за каталогом № 33-016) і фермент PI3Kδ людини (Millipore Corporation, за каталогом № 14-604). Спосіб вимірювань відповідав прикладеним інструкціям. Його короткий опис полягає в наступному. У 384-ямковому планшеті змішували PI3Kδ (10 нг/ямку), фосфатидилінозитол-4,5-бісфосфат (10 мкМ), ATP (30 мкМ) і тестовану сполуку (всього 20 мкл), і інкубували при кімнатній температурі протягом 30 хвилин. Для зупинення реакції в суміш додавали ЕДТО і біотинільований фосфатидилінозитол-3,4,5-трифосфат. Після цього в суміш додавали мічене європієм анти-GST антитіло, зв'язаний з GST домен GRP1 PH і стрептавідин-APC, а потім інкубували протягом ночі. Співвідношення HTRF вимірювали з використанням планшетного 17 UA 108390 C2 5 10 HTRF-рідера. Значення IC50 сполуки обчислювали логістичним методом, приймаючи швидкість інгібування без додавання ферменту за 100 % і швидкість інгібування без додавання тестованої сполуки, але з додаванням ферменту, за 0 %. 2. Інгібуюча активність відносно ферменту PI3Kα У 384-ямковому планшеті в реакційному буфері (50 мМ Hepes, 10 мМ NaCl, 10 мМ MgCl 2, 2 мМ EGTA, 2 мМ DTT, pН 7,3) змішували PI3Kα людини (12 нг/ямку, Millipore Corporation, за каталогом № 14-602), фосфатидилінозитол (0,2 мкг/ямку) і тестовану сполуку (всього 10 мкл), і інкубували при температурі 37 °C протягом 3 годин. Після реакції в суміш додавали 10 мкл реагенту Kinase-Glo Plus (Promega, за каталогом № V3772), і вимірювали люмінесценцію на люмінометрі. Значення IC50 сполуки обчислювали логістичним методом, приймаючи швидкість інгібування без додавання ферменту за 100 % і швидкість інгібування без додавання тестованої сполуки за 0 %. Значення IC50 (нМ) для деяких типових сполук представлені в таблиці 1. У цій таблиці "Приклад" являє собою № прикладу, описаного нижче для тестованих сполук. 15 Таблиця 1 Приклад 1 4 10 13 16 18 20 25 28 29 30 33 34 35 36 37 38 39 40 43-1 43-2 44 45 67 69 75 77 78 85 87 99 100 120 121 123 132 133 PI3Kδ 29 60 5,8 36 69 50 19 69 35 45 12 11 14 18 17 20 23 27 20 8 8,6 14 56 47 22 25 18 8,5 21 4,9 16 5,7 27 13 4,5 12 5,2 PI3Kα 2800 >3000 >3000 980 >10000 7700 1800 6200 >3000 >3000 >3000 >3000 >3000 4200 6700 1900 2200 3900 >10000 13000 8000 5000 6800 990 10000 5400 5400 2900 5500 >10000 >10000 >3000 6400 4900 >3000 >10000 5900 Приклад 134 135 136 137 158 193 194 195 196 215 216 224 248 371 389 423 441 A4 A290 A293 A298 A299 A300 A449 A451 A463 A464 A466 A475 A561 A564 A567 18 PI3Kδ 4,7 3,0 4,0 5,2 11 4,9 5,8 4,1 4,8 13 13 3,3 34 35 11 24 48 31 7,4 19 28 26 26 20 35 27 10 15 25 14 19 11 PI3Kα 6600 8000 >10000 >10000 6700 8200 3300 >10000 >10000 >10000 >10000 7300 720 5000 >10000 >10000 1400 730 3800 3200 3500 4900 6500 1400 2200 3100 2200 2000 1400 2900 3000 1600 UA 108390 C2 5 10 15 20 25 30 3. Тест на інгібування продукції IL-2 у щурів in vivo В експерименті використовували самців щурів LEW/CrlCrlj (Charles River Laboratories, Japan, Inc.) (у віці 6 тижнів, маса тіла від 130 до 180 г). Тестовану сполуку суспендували в 0,5 % розчині метилцелюлози і вводили перорально в кількості 5 мл/кг. Продукцію IL-2 індукували шляхом ін'єкції конканаваліну А (Funakoshi Corporation, за каталогом № L-1000) у хвостову вену в дозі 15 мг/кг. Тест проводили відповідно до протоколу, представленого нижче. За 2 години або за 16 годин до введення конканаваліну А щурам перорально вводили тестовану сполуку. Через 3 години після введення конканаваліну А збирали кров. Концентрацію IL-2 у крові визначали кількісно з використанням набору ELISA (R&D Systems, Inc., за каталогом № DY502E). Ступінь інгібування обчислювали, як відношення кількості IL-2, продукованого в групі, що одержувала тестовану сполуку, до кількості IL-2, продукованого в контрольній групі з введенням розчинника. У результаті було підтверджено, що при введенні тестованої сполуки (10 мг/кг), наприклад, за 2 години до введення конканаваліну А, деякі типові сполуки прикладів 10, 29, 33, 34, 37, 43-1 і A4 демонстрували значення інгібуючої активності, що дорівнюють 77, 51, 75, 72, 81, 73 і 58 %, відповідно, і мали чудову інгібуючу продукцію IL-2 активність. 4. Тест на інгібування проліферації В-клітин у щурів У 96-ямковому планшеті в культуральному середовищі RPMI-1640 з додаванням 10 % FCS 5 змішували клітини селезінки (1,0×10 клітин/ямку), одержані від самців щурів LEW/CrlCrlj (Charles River Laboratories, Japan, Inc.), мишачий F(ab') 2-фрагмент антищурячого IgM (3 мкг/ямку, SouthernBiotech Associates, Inc., за каталогом № 3082-14) і розчинену в ДМСО тестовану сполуку (кінцева концентрація ДМСО 0,1 %) (всього 200 мкл). Клітини культивували в CO2-інкубаторі протягом 48 годин, і за 4 години до завершення культивування в суміш додавали 3 [ H]тимідин (925 ГБк/ммоль, Moravek Biochemicals, Inc., за каталогом № MT6038) у кількості 0,037 МБк/ямку. Клітини збирали на GF/C скляний фільтр із використанням харвестера клітин, і вимірювали радіоактивність фільтра з використанням рідинного сцинтиляційного лічильника. Логістичним методом обчислювали значення IC50 для сполуки, приймаючи dpm (число розпадів на хвилину) без додавання IgM за швидкість інгібування в 100 % і dpm без додавання тестованої сполуки за швидкість інгібування в 0 %. Результати для деяких типових сполук представлені в таблиці 2. Таблиця 2 Приклад Приклад IC50 (нМ) Приклад IC50 (нМ) Приклад IC50 (нМ) 10 2,9 121 2,0 215 6,7 A299 2,5 36 6,8 132 1,5 216 5,7 A300 2,6 37 1,52 134 3,4 224 1,5 A449 0,4 38 2,9 135 2,5 248 1,4 A451 1,2 40 9,0 136 1,7 389 4,4 A463 1,4 43-1 2,1 137 4,6 423 3,1 A466 1,8 43-2 3,1 158 10 441 1,8 A475 1,1 85 2,6 193 4,1 A290 2,2 A561 3,9 87 3,5 195 3,0 A293 2,6 A564 2,2 99 35 IC50 (нМ) 2,5 196 3,6 A298 1,2 A567 1,8 У представлених вище тестах було підтверджено, що деякі типові сполуки мають чудову селективну інгібуючу дію відносно PI3Kδ і/або інгібуючу продукцію IL-2 дію, і/або інгібуючу проліферацію В-клітин дію (включаючи інгібуючу активацію дію). Відповідно, сполука формули (I) може бути використана як засіб для профілактики або лікування реакцій відторгнення при 19 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 60 трансплантації різних органів, алергічних захворювань, аутоімунних захворювань і/або гематологічних пухлин. Крім того, оскільки сполука формули (I) являє собою інгібітор PI3Kδ, що має суттєво більш потужну інгібуючу дію відносно PI3Kδ, ніж інгібуюча дія відносно PI3Kα, вона може бути чудовим імуносупресуючим засобом, що не викликає резистентності до інсуліну, основаної на інгібуючій дії відносно PI3Kα. Різні типи органів включають нирки, печінку і серце. Реакція відторгнення при трансплантації органів включає хронічне відторгнення і гостре відторгнення, і її механізм в основному класифікують на відторгнення, пов'язане з антитілами, і відторгнення, пов'язане з Т-клітинами. Сполука формули (I) або її сіль застосовні, зокрема, як засіб для профілактики і/або лікування відторгнення, пов'язаного з антитілами. Фармацевтична композиція, що містить як активний інгредієнт один або два, або декілька видів сполуки формули (I) або її сіль, може бути приготовлена з використанням наповнювачів, які звичайно використовують у даній галузі техніки, тобто наповнювачів для фармацевтичних препаратів, носіїв для фармацевтичних препаратів і т. п., відповідно до звичайно застосовуваних способів. Введення може виконуватися або шляхом перорального введення за допомогою таблеток, пігулок, капсул, гранул, порошків, розчинів і т. п., або шляхом парентерального введення, такого як застосування ін'єкцій, таких як внутрішньосуглобова, внутрішньовенна і внутрішньом’язова ін'єкції, супозиторіїв, очних крапель, очних мазей, черезшкірних рідких препаратів, мазей, черезшкірних пластирів, черезслизових рідких препаратів, черезслизових пластирів, засобів для інгаляцій і т. п. Тверду композицію для застосування при пероральному введенні використовують у формі таблеток, порошків, гранул і т. п. У такій твердій композиції один або декілька активних інгредієнтів змішують щонайменше з одним неактивним наповнювачем, таким як лактоза, маніт, глюкоза, гідроксипропілцелюлоза, мікрокристалічна целюлоза, крохмаль, полівінілпіролідон і/або алюмометасилікат магнію. У стандартному способі, композиція може містити неактивні добавки, такі як мастило, таке як стеарат магнію, розпушувач, такий як карбоксиметилкрохмаль натрію, стабілізатор або засіб, що сприяє розчинності. За необхідності, таблетки або пігулки можуть бути покриті цукром або плівкою зі шлунковорозчинної або кишковорозчинної речовини. Рідка композиція для перорального введення включає фармацевтично прийнятні емульсії, розчини, суспензії, сиропи, еліксири і т. п. і також містить звичайно використовувані інертні розріджувачі, наприклад очищену воду і етанол. На доповнення до інертного розріджувача рідка композиція також може містити допоміжні засоби, такі як засіб, що сприяє розчинності, зволожувач і засіб, що сприяє суспендуванню, підсолоджувачі, смакоароматизатори, віддушки або антисептики. Ін'єкції для парентерального введення включають стерильні водні або неводні розчини, суспензії й емульсії. Водний розчинник включає, наприклад, дистильовану воду для ін'єкцій і фізіологічний сольовий розчин. Приклади неводного розчинника включають пропіленгліколь, поліетиленгліколь, рослинні олії, такі як маслинова олія, спирти, такі як етанол, полісорбат 80 (Японська Фармакопея), і т. п. Така композиція може додатково містити засіб, що регулює тонічність, антисептик, зволожувач, емульгатор, засіб, що сприяє диспергуванню, стабілізатор або засіб, що сприяє розчинності. Композиції стерилізують, наприклад, шляхом фільтрування через затримуючий бактерії фільтр, змішування з бактерицидом або опромінення. Крім того, композиції також можуть бути використані шляхом приготування стерильної твердої композиції і її розчинення або суспендування в стерильній воді або стерильному розчиннику для ін'єкцій перед її застосуванням. Засіб для зовнішнього застосування включає мазі, пластири, креми, желе, припарки, спреї, лосьйони, очні краплі й очні мазі. Засоби містять звичайно використовувані основи для мазей, основи для лосьйонів, водні і неводні рідкі препарати, суспензії й емульсії. Приклади основ для мазей або основ для лосьйонів включають поліетиленгліколь, пропіленгліколь, білий вазелін, знебарвлений бджолиний віск, поліоксіетиленгідрогенізовану касторову олію, гліцерилмоностеарат, стеариловий спирт, цетиловий спирт, лауромакрогол і сорбітансесквіолеат. Як черезслизові засоби, такі як засіб для інгаляцій і трансназальний засіб, використовують засоби у твердому, рідкому або напівтвердому стани, що можуть бути приготовлені відповідно до загальноприйнятого відомого способу. Наприклад, відповідним чином може бути доданий відомий наповнювач, а також засіб для регулювання рівня pН, антисептик, поверхнево-активна речовина, мастило, стабілізатор, загусник і т. п. Для введення може бути використаний придатний пристрій для інгаляції або нагнітання повітря. Наприклад, сполука може бути 20 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 введена окремо або в порошковій складеній суміші, або у вигляді розчину або суспензії в сполученні з фармацевтично прийнятним носієм, з використанням відомого пристрою або розпилювача, такого як пристрій для інгаляції з дозованим введенням. Для однократного або багаторазового введення може застосовуватися порошковий інгалятор і т. п., і може бути використаний сухий порошок або капсула, що містить порошок. Як альтернатива, засіб може бути у формі, такій як аерозольний спрей під тиском, у якому використовують придатний пропелент, наприклад придатний газ, такий як хлорфторалкан, гідрофторалкан і вуглекислий газ. Як правило, при пероральному введенні добова доза складає відповідно приблизно від 0,001 до 100 мг/кг, переважно від 0,1 до 30 мг/кг і більш переважно від 0,1 до 10 мг/кг маси тіла, введених однією порцією або 2-4 окремими порціями. У випадку внутрішньовенного введення, відповідним чином вводять добову дозу приблизно від 0,0001 до 10 мг/кг маси тіла, один раз на добу або двічі або декілька разів на добу. Крім того, черезслизовий засіб вводять у дозі приблизно від 0,001 до 100 мг/кг маси тіла, один раз на добу або двічі або декілька разів на добу. Доза відповідним чином визначається на основі конкретного випадку, беручи до уваги симптоми, вік і стать, іт. п. Незважаючи на варіації, що залежать від шляхів введення, лікарських форм, ділянок введення або типів наповнювачів і добавок, фармацевтична композиція згідно з даним винаходом містить від 0,01 до 100 % по вазі, а в деяких варіантах здійснення від 0,01 до 50 % по вазі, одного або декількох видів сполуки формули (I) або її солі, що являє собою активний інгредієнт. Сполука формули (I) може бути використана в сполученні з різними засобами для лікування або профілактики захворювань, при яких сполука формули (I) вважається ефективною. При такому сумісному застосуванні, ліки можуть бути введені одночасно або окремо, послідовно або через бажані часові інтервали. Сполуки для одночасного введення можуть бути або змішаними, або мати роздільні форми. Приклади Тут і далі в тексті способи одержання сполуки формули (I) і її вихідних сполук будуть описані більш детально з посиланням на приклади, але даний винахід не обмежується сполуками, описаними нижче в прикладах. Крім того, у прикладах одержання будуть описані способи одержання кожної з вихідних сполук. Крім того, способи одержання сполуки формули (I) не обмежуються способами одержання в представлених нижче конкретних прикладах, але сполука формули (I) може бути одержана шляхом сполучення способів одержання або шляхом застосування деякого способу, що очевидний фахівцю в даній галузі техніки. Крім того, у деяких випадках у представлених нижче прикладах одержання, прикладах і таблицях можуть використовуватися наступні скорочення. PEx: № прикладу одержання; Ex: № прикладу; Syn: № прикладу, одержаного тим же способом; PSyn: № прикладу одержання, одержаного тим же способом; Str: структурна формула; DAT: фізико-хімічні дані; ESI+: значення m/z при мас-спектрометрії (іонізація ESI, дані + представлені у вигляді (M+H) , якщо не зазначене інше); ESI-: значення m/z (іонізація ESI, дані 1 представлені у вигляді (M+H) , якщо не зазначене інше); ЯМР1: δ (м.ч.) при H-ЯМР у ДМСО-d6; 1 ЯМР2: δ (м.ч.) при H-ЯМР у CDCl3; с: синглет (спектр); д: дублет (спектр); т: триплет (спектр); кв.: квартет (спектр); ушир.: уширений (спектр) (наприклад: ушир.с); RT: час утримування (хв.) при ВЕРХ; [М] у прикладах одержання і прикладах: [моль/л]; препаративна SFC: препаративна надкритична рідинна хроматографія, DEA: діетиламін. Крім того, наприклад, опис "26+44" у колонці Syn таблиць із прикладами вказує на те, що дане одержання проводять тим же способом, що й описаний у прикладі 26, а потім одержують продукт тим же способом, що й описаний у прикладі 44, як вихідну речовину. Крім того, у таблицях прикладів одержання, наприклад, у колонці PSyn прикладу одержання 148 присутнє позначення Syn. 87, що означає, що сполуку прикладу одержання 148 одержують тим же способом, що й описаний у прикладі 87. У таблицях прикладів, наприклад, у колонці Syn прикладу 295 присутнє позначення PSyn. 8, що означає, що сполуку прикладу 295 одержують тим же способом, що й описаний у прикладі одержання 8. У структурній формулі HCl означає гідрохлорид, і цифра перед HCl означає молярне відношення. Наприклад, 2HCl означає дигідрохлорид. Крім того, у структурній формулі Me означає метильну групу, Et означає етильну групу, Ph означає фенільну групу, iBu означає ізобутильну групу, tBu означає трет-бутильну групу, і Boc означає трет-бутоксикарбонільну групу. Позначення "*" у структурі сполуки вказує на те, що сполука є оптично активною речовиною. 21 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад одержання 1 До розчину 4,6-дихлор-2-(метилсульфаніл)піримідину (5 г) у N,N-диметилформаміді (50 мл) додавали карбонат калію (5,3 г) і 2-(дифторметил)-1H-бензімідазол (3,9 г), і перемішували суміш при кімнатній температурі протягом 5 годин. До реакційної суміші додавали воду, а потім екстрагували етилацетатом. Органічний шар промивали насиченим сольовим розчином і сушили над безводним сульфатом магнію. Розчинник випарювали в умовах зниженого тиску, а потім очищали залишок методом колонкової хроматографії на силікагелі (гексан/етилацетат) з одержанням 1-[6-хлор-2-(метилсульфаніл)піримідин-4-іл]-2-(дифторметил)-1H-бензімідазолу (5,49 г) у вигляді білого порошку. Приклад одержання 2 До розчину 1-[6-хлор-2-(метилсульфаніл)піримідин-4-іл]-2-(дифторметил)-1H-бензімідазолу (2,2 г) у N,N-диметилформаміді (11 мл) додавали карбонат калію (1,4 г) і морфолін (0,88 мл), і перемішували суміш при кімнатній температурі протягом 1 години. До реакційного розчину додавали воду, а потім екстрагували етилацетатом. Органічний шар промивали насиченим сольовим розчином і сушили над безводним сульфатом магнію. Розчинник випарювали в умовах зниженого тиску, а потім очищали залишок методом колонкової хроматографії на силікагелі (гексан/етилацетат) з одержанням 2-(дифторметил)-1-[2-(метилсульфаніл)-6морфолін-4-ілпіримідин-4-іл]-1H-бензімідазолу (2,1 г) у вигляді білого порошку. Приклад одержання 3 До розчину 2-(дифторметил)-1-[2-(метилсульфаніл)-6-морфолін-4-ілпіримідин-4-іл]-1Hбензімідазолу (3 г) у дихлорметані (60 мл) при охолодженні на льоду додавали метахлорпероксибензойну кислоту (75 % вологість, 1,9 г), і перемішували суміш при 0 °C протягом 15 хвилин. До реакційної суміші додавали насичений водний розчин бікарбонату натрію, а потім екстрагували дихлорметаном. Органічний шар промивали водою і насиченим сольовим розчином, і сушили над безводним сульфатом магнію. Розчинник випарювали в умовах зниженого тиску, а потім очищали залишок методом колонкової хроматографії на силікагелі (хлороформ/метанол) з одержанням 2-(дифторметил)-1-[2-(метилсульфініл)-6-морфолін-4ілпіримідин-4-іл]-1H-бензімідазолу (2,8 г) у вигляді блідо-жовтої аморфної речовини. Приклад одержання 4 До розчину 2-(дифторметил)-1-[2-(метилсульфаніл)-6-морфолін-4-ілпіримідин-4-іл]-1Hбензімідазолу (2,1 г) у дихлорметані (21 мл) при охолодженні на льоду додавали метахлорпероксибензойну кислоту (75 % вологість, 2,7 г), і перемішували суміш при 0 °C протягом 15 хвилин. До реакційної суміші додавали насичений водний розчин бікарбонату натрію, а потім екстрагували дихлорметаном. Органічний шар промивали водою і насиченим сольовим розчином, і сушили над безводним сульфатом магнію. Розчинник випарювали в умовах зниженого тиску, а потім очищали залишок методом колонкової хроматографії на силікагелі (хлороформ/метанол) з одержанням 2-(дифторметил)-1-[2-(метилсульфоніл)-6-морфолін-4ілпіримідин-4-іл]-1H-бензімідазолу (2,27 г) у вигляді блідо-жовтої аморфної речовини. Приклад одержання 5 До суміші 1-[6-хлор-2-(метилсульфаніл)піримідин-4-іл]-2-(дифторметил)-1H-бензімідазолу (1 г) і N,N-диметилацетаміду (10 мл) додавали трет-бутил-4-(гідроксиметил)піперидин-1-карбамат (1 г) і карбонат цезію (3 г), і перемішували суміш при 120 °C протягом 3 годин. Реакційну суміш вливали у воду, а потім екстрагували гексаном/етилацетатом (1/1). Органічний шар промивали водою і насиченим сольовим розчином, і сушили над безводним сульфатом магнію. Розчинник випарювали в умовах зниженого тиску, а потім очищали залишок методом колонкової хроматографії на силікагелі (гексан/етилацетат) з одержанням трет-бутил-4-[({6-[2(дифторметил)-1H-бензімідазол-1-іл]-2-(метилсульфаніл)піримідин-4-іл}окси)метил]піперидин-1карбамату (680 мг) у вигляді білої аморфної речовини. Приклад одержання 6 N-(2-{[6-хлор-2-(метилсульфаніл)піримідин-4-іл]аміно}-5-метилфеніл)ацетамід (270 мг) розчиняли в суміші етанолу (2,8 мл) і 1,4-діоксану (2,8 мл), додавали 6M соляну кислоту (9,6 мл), а потім нагрівали зі зворотним холодильником протягом 3 годин. Після охолодження на повітрі до кімнатної температури, значення pН коректували до 6-7 з використанням насиченого водного бікарбонату натрію, а потім екстрагували етилацетатом. Органічний шар сушили над безводним сульфатом магнію, і випарювали розчинник в умовах зниженого тиску з одержанням 1 N -[6-хлор-2-(метилсульфаніл)піримідин-4-іл]-4-метилбензол-1,2-діаміну (230 мг). Приклад одержання 7 Суміш 2-(метилсульфаніл)-6-(морфолін-4-іл)піримідин-4-аміну (500 мг), 2-бром-1-метил-3нітробензолу (1 г), трис(дибензиліденацетон)дипаладію(0) (202 мг), (9,9-диметил-9H-ксантен4,5-діїл)біс(дифенілфосфіну) (192 мг) і карбонату цезію (1,0 г) у толуолі перемішували в 22 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 мікрохвильовому реакторі при 140 °C протягом 1 години. Реакційну суміш фільтрували через целіт і концентрували в умовах зниженого тиску. Залишок очищали методом колонкової хроматографії на силікагелі (гексан/етилацетат) з одержанням N-(2-метил-6-нітрофеніл)-2(метилсульфаніл)-6-(морфолін-4-іл)піримідин-4-аміну (756 мг) у вигляді жовтого порошку. Приклад одержання 8 N-(2-метил-6-нітрофеніл)-2-(метилсульфаніл)-6-(морфолін-4-іл)піримідин-4-амін (750 мг) розчиняли в етанолі (22,5 мл), додавали гексагідрат хлориду заліза(III) (56 мг) і активоване вугілля (75 мг), а потім перемішували при 80 °C. По краплях додавали моногідрат гідразину, а потім нагрівали зі зворотним холодильником протягом ночі. Реакційну суміш охолоджували до кімнатної температури і фільтрували через целіт. Маточний розчин концентрували, і очищали залишок методом колонкової хроматографії на силікагелі (гексан/етилацетат) з одержанням 32 метил-N -[2-(метилсульфаніл)-6-(морфолін-4-іл)піримідин-4-іл]бензол-1,2-діаміну (544 мг) у вигляді блідо-жовтого порошку. Приклад одержання 9 До трет-бутил-[(2S)-1-{[транс-4-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4іл)піримідин-4-іл}окси)циклогексил]аміно}-4-(метилсульфаніл)-1-оксобутан-2-іл]карбамату (760 мг) додавали метилйодид (3,5 мл), а потім перемішували при кімнатній температурі протягом ночі. Метилйодид випарювали в умовах зниженого тиску з одержанням цільової сполуки, йодиду [(3S)-3-[(трет-бутоксикарбоніл)аміно]-4-{[транс-4-({6-[2-(дифторметил)-1H-бензімідазол1-іл]-2-(морфолін-4-іл)піримідин-4-іл}окси)циклогексил]аміно}-4-оксобутил](диметил)сульфонію (919 мг). Приклад одержання 10 4,6-Дихлор-2-(метилсульфаніл)піримідин (50 мг) і трет-бутил-(2-аміно-4метилфеніл)карбамат (57 мг) розчиняли в диметилацетаміді (250 мкл), додавали N,Nдіізопропілетиламін (69 мкл), а потім перемішували при 100 °C протягом 7 годин. Після завершення реакції суміш охолоджували до кімнатної температури, додавали воду, а потім екстрагували етилацетатом. Екстракти промивали насиченим сольовим розчином, органічний шар сушили над безводним сульфатом магнію, і випарювали розчинник в умовах зниженого тиску. Залишок очищали методом колонкової хроматографії на силікагелі (етилацетат/гексан) з одержанням цільової сполуки, трет-бутил-(2-{[6-хлор-2-(метилсульфаніл)-піримідин-4-іл]аміно}4-метилфеніл)карбамату (50 мг), у вигляді білого порошку. Приклад одержання 11 Трет-бутил-(2-{[6-хлор-2-(метилсульфаніл)піримідин-4-іл]аміно}-4-метилфеніл)карбамат (8,5 г) розчиняли в 1,4-діоксані (85 мл), додавали 4M розчин (56 мл) хлороводню в 1,4-діоксані, а потім перемішували при кімнатній температурі протягом 8 годин. Після завершення реакції додавали насичений водний розчин бікарбонату натрію і 4M водний розчин гідроксиду натрію. Суміш гасили, витримували й екстрагували етилацетатом. Органічний шар сушили над безводним сульфатом магнію, і випарювали розчинник в умовах зниженого тиску з одержанням 2 N -[6-хлор-2-(метилсульфаніл)піримідин-4-іл]-4-метилбензол-1,2-діаміну (6 г) у вигляді жовтого порошку. Приклад одержання 12 2 N -[6-хлор-2-(метилсульфаніл)піримідин-4-іл]-4-метилбензол-1,2-діамін (6 г) і дифтороцтовий ангідрид (7,4 г) розчиняли в ацетонітрилі (60 мл), а потім перемішували при кімнатній температурі протягом 1 години. Після підтвердження зникнення вихідної речовини, додавали 4M розчин (53 мл) хлороводню в 1,4-діоксані, а потім перемішували при 100 °C протягом 10 годин. Після завершення реакції суміш охолоджували до кімнатної температури, додавали воду, а потім екстрагували етилацетатом. Органічний шар промивали насиченим сольовим розчином. Об'єднаний органічний шар сушили над безводним сульфатом магнію, і випарювали розчинник в умовах зниженого тиску. Залишок очищали методом колонкової хроматографії на силікагелі (етилацетат/гексан) з одержанням 1-[6-хлор-2(метилсульфаніл)піримідин-4-іл]-2-(дифторметил)-6-метил-1H-бензімідазолу (2,9 г) у вигляді білого порошку. Приклад одержання 13 (3a'R,5's,6a'S)-5,5-диметилгексагідро-1'H-спіро[1,3-діоксан-2,2'-пентален]-5'-ол (1,0 г), 1Hізоіндол-1,3(2H)-діон (780 мг) і трифенілфосфін (1,39 г) розчиняли в тетрагідрофурані (17 мл), при 0 °C по краплях додавали 2,2M розчин (2,41 мл) етилазодикарбонату в тетрагідрофурані, а потім перемішували при 0 °C протягом 1 години і при кімнатній температурі протягом 4 годин. До реакційного розчину додавали силікагель, а потім концентрували й очищали методом колонкової хроматографії на силікагелі (гексан/етилацетат) з одержанням 2-[(3a'R,5'r,6a'S)-5,5 23 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 диметилгексагідро-1'H-спіро[1,3-діоксан-2,2'-пентален]-5'-іл]-1H-ізоіндол-1,3(2H)-діон (1,1 г) у вигляді білого порошку. Приклад одержання 14 До суміші етил-4-(4-ціанфеніл)-1-піперазинкарбоксилату (10 г), боргідриду натрію (3,4 г) і тетрагідрофурану (50 мл) при охолодженні на льоду під потоком азоту додавали суміш йоду (9,8 г) і тетрагідрофурану (50 мл), а потім перемішували при тій же температурі протягом 1 години, а потім нагрівали зі зворотним холодильником протягом 3 годин. Реакційний розчин охолоджували на льоду, і додавали 6M розчин соляної кислоти для коректування значення pН до 1. Реакційний розчин перемішували при 70 °C протягом 30 хвилин. Залишали охолоджуватися, додавали гідроксид натрію для коректування значення pН до 10, а потім екстрагували етилацетатом. Екстракти промивали насиченим сольовим розчином, органічний шар сушили над безводним сульфатом натрію, і випарювали розчинник в умовах зниженого тиску. Залишок подрібнювали в порошок з використанням тетрагідрофурану, етилацетату і діізопропілового ефіру з одержанням етил-4-[4-(амінометил)феніл]-1-піперазинкарбоксилату (5,2 г). Приклад одержання 15 2-(Дифторметил)-1-[2-(метилсульфаніл)-6-морфолін-4-ілпіримідин-4-іл]-1H-бензімідазол (2,1 г) розчиняли в хлористому метилені (21 мл), при охолодженні на льоду додавали метахлорпероксибензойну кислоту (75 % вологість, 2,7 г), а потім перемішували при 0 °C протягом 15 хвилин. Додавали насичений водний бікарбонат натрію, а потім екстрагували хлористим метиленом. Екстракти промивали водою і насиченим сольовим розчином, органічний шар сушили над безводним сульфатом магнію, і випарювали розчинник в умовах зниженого тиску. Залишок очищали методом колонкової хроматографії на силікагелі (хлороформ/метанол) з одержанням 2-(дифторметил)-1-[2-(метилсульфоніл)-6-морфолін-4-ілпіримідин-4-іл]-1Hбензімідазолу (2,27 г) у вигляді блідо-жовтої аморфної речовини. Приклад одержання 16 До суміші 2-[(3a'R,5'r,6a'S)-5,5-диметилгексагідро-1'H-спіро[1,3-діоксан-2,2'-пентален]-5'-іл]1H-ізоіндол-1,3(2H)-діону (1,1 г), тетрагідрофурану (22 мл) і етанолу (22 мл) додавали моногідрат гідразину (0,75 мл), а потім нагрівали зі зворотним холодильником протягом 2 годин. Нерозчинні речовини видаляли шляхом фільтрування через целіт, і концентрували в умовах зниженого тиску. До залишку додавали хлороформ, потім сушили над сульфатом натрію, а потім випарювали розчинник в умовах зниженого тиску з одержанням (3a'R,5's,6a'S)-5,5диметилгексагідро-1'H-спіро[1,3-діоксан-2,2'-пентален]-5'-аміну (0,74 г) у вигляді білого порошку. Приклад одержання 17 Бензил-9-оксо-3-азаспіро[5.5]ундекан-3-карбоксилат (230 мг) розчиняли в метанолі (4,5 мл), і додавали хлористий метилен (1,5 мл) і ацетат амонію (1,47 г), а потім перемішували при кімнатній температурі протягом 10 хвилин. Потім додавали триацетоксиборгідрид натрію (323 мг), а потім перемішували при кімнатній температурі протягом ночі. До реакційного розчину додавали насичений водний бікарбонат натрію, а потім екстрагували хлороформом. Органічний шар промивали насиченим сольовим розчином і сушили над безводним сульфатом натрію. Розчинник випарювали в умовах зниженого тиску з одержанням бензил-9-аміно-3азаспіро[5.5]ундекан-3-карбоксилату (255 мг). Приклад одержання 80 Транс-4-(дибензиламіно)циклогексанол (200 мг), 2-(3-бромпропокси)тетрагідро-2H-піран (604 мг), подрібнений гідроксид калію (179 мг) і бромід тетрабутиламонію (44 мг) суспендували в ксилолі (2 мл), а потім перемішували при кімнатній температурі протягом 2 годин. До реакційної суміші додавали етилацетат і воду, органічний шар екстрагували і промивали насиченим сольовим розчином і сушили над безводним сульфатом магнію. Розчинник випарювали в умовах зниженого тиску. Залишок очищали методом колонкової хроматографії на аміносилікагелі (гексан/етилацетат=100/0-80/20) з одержанням транс-N,N-дибензил-4-[3(тетрагідро-2H-піран-2-ілокси)пропокси]-циклогексанаміну (174 мг). Приклад одержання 81 Транс-N,N-дибензил-4-[3-(тетрагідро-2H-піран-2-ілокси)пропокси]-циклогексанамін (170 мл) розчиняли в метанолі (1 мл), додавали 4M розчин (972 мкл) хлороводню в 1,4-діоксані, а потім перемішували при кімнатній температурі протягом 2 годин. Реакційний розчин нейтралізували додаванням насиченого водного розчину бікарбонату натрію й екстрагували етилацетатом. Органічний шар промивали насиченим сольовим розчином, а потім сушили над безводним сульфатом магнію, і випарювали розчинник в умовах зниженого тиску з одержанням 3-{[транс-4(дибензиламіно)циклогексил]окси}пропан-1-олу (110 мг). 60 24 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад одержання 82 До 3-{[транс-4-(дибензиламіно)циклогексил]окси}пропан-1-олу (110 мг) при охолодженні на льоду додавали тозилхлорид (60 мг) і піридин (51 мкл), а потім перемішували при кімнатній температурі протягом 1 години. До реакційної суміші додавали N,N-диметилформамід (1,1 мл), карбонат калію (43 мг) і піролідин (26 мкл), а потім перемішували при кімнатній температурі протягом ночі. До реакційної суміші додавали етилацетат і воду, органічний шар екстрагували, промивали насиченим сольовим розчином, а потім сушили над безводним сульфатом магнію. Потім розчинник випарювали в умовах зниженого тиску. Залишок очищали методом колонкової хроматографії на аміносилікагелі (гексан/етилацетат=90/10-70/30) з одержанням транс-N,Nдибензил-4-[3-(піролідин-1-іл)пропокси]циклогексанаміну (70 мг). Приклад одержання 83 Транс-N,N-дибензил-4-[3-(піролідин-1-іл)пропокси]циклогексанамін (115 мг) розчиняли в етанолі (2,3 мл), додавали 20 % гідроксид паладію на вугіллі (50 % вологість), а потім проводили каталітичне відновлення при кімнатній температурі протягом 4 годин в атмосфері азоту при тиску 3 атм. Після заміщення азоту, каталізатор видаляли шляхом фільтрування, а потім концентрували в умовах зниженого тиску з одержанням транс-4-[3-(піролідин-1іл)пропокси]-циклогексанаміну (48 мг). Приклад одержання 84 Триетилфосфоноацетат (107 мг) розчиняли в тетрагідрофурані (1 мл), додавали 60 % гідрид натрію (19 мг), а потім перемішували при кімнатній температурі протягом 30 хвилин. По краплях додавали розчин трет-бутил-(транс-4-формілциклогексил)карбамату (90 мг) у тетрагідрофурані (1 мл), а потім перемішували при кімнатній температурі протягом 2 годин. Додавали етилацетат і воду, а потім екстрагували етилацетатом. Екстракти промивали насиченим сольовим розчином, а потім сушили над безводним сульфатом магнію, і випарювали розчинник в умовах зниженого тиску. Залишок очищали методом колонкової хроматографії на силікагелі (гексан/етилацетат=95/5-50/50) з одержанням етил-(2E)-3-{транс-4-[(третбутоксикарбоніл)аміно]циклогексил}-акрилату (100 мг). Приклад одержання 85 Гідрид натрію (60 %, 394 мг) суспендували в 1,2-диметоксіетані (20 мл), додавали третбутил-4-гідроксибензилкарбамат (1 г) і 15-краун-5-ефір (1,09 г), а потім перемішували при кімнатній температурі протягом 30 хвилин. Додавали 4,6-дихлор-2-(метилсульфоніл)піримідин, а потім перемішували при 80 °C протягом ночі. Реакційний розчин охолоджували до кімнатної температури, потім додавали водний розчин хлориду амонію (50 мл), а потім екстрагували етилацетатом. Екстракти промивали водою і насиченим сольовим розчином, і сушили органічний шар над безводним сульфатом магнію. Осушник видаляли шляхом фільтрування, і випарювали розчинник в умовах зниженого тиску. Залишок очищали методом колонкової хроматографії на силікагелі (гексан/етилацетат=95/5-85/15) з одержанням трет-бутил-{4-[(4,6дихлорпіримідин-2-іл)окси]бензил}карбамату (762 мг). Приклад одержання 86 Суміш 4,6-дихлор-2-(метилсульфаніл)піримідину (700 мг), 2-(дифторметил)-4-етокси-1Hбензімідазолу (761 мг), карбонату калію (744 мг) і N,N-диметилформаміду (7 мл) перемішували при кімнатній температурі протягом ночі. До суміші додавали воду, а потім екстрагували етилацетатом. Органічний шар промивали насиченим сольовим розчином і сушили над безводним сульфатом натрію. Осушник видаляли шляхом фільтрування, а потім випарювали розчинник в умовах зниженого тиску. Залишок очищали методом колонкової хроматографії на силікагелі (хлороформ/метанол=100/0-80/20) з одержанням 1-[6-хлор-2(метилсульфаніл)піримідин-4-іл]-2-(дифторметил)-4-етокси-1H-бензімідазолу (464 мг) (приклад одержання 86-1) і 1,1'-[2-(метилсульфаніл)піримідин-4,6-діїл]біс[2-(дифторметил)-4-етокси-1Hбензімідазолу]. 1,1'-[2-(Метилсульфаніл)піримідин-4,6-діїл]біс[2-(дифторметил)-4-етокси-1Hбензімідазол] суспендували в етилацетаті і нагрівали. Залишали охолоджуватися, нерозчинні речовини збирали шляхом фільтрування з одержанням 1,1'-[2-(метилсульфаніл)піримідин-4,6діїл]біс[2-(дифторметил)-4-етокси-1H-бензімідазолу] (275 мг) (приклад одержання 86-2). Приклад одержання 87 До суміші транс-4-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4іл}окси)циклогексанаміну (700 мг) і N,N-диметилформаміду (7,0 мл) додавали N-(третбутоксикарбоніл)-N-метил-L-метіонін (622 мг), 1H-бензотриазол-1-ол (319 мг) і N-[3(диметиламіно)пропіл]-N'-етилкарбодііміду гідрохлорид (452 мг), а потім перемішували при кімнатній температурі протягом ночі. Після завершення реакції додавали воду, а потім екстрагували етилацетатом. Органічний шар промивали насиченим сольовим розчином, а потім сушили над безводним сульфатом магнію. Осушник видаляли шляхом фільтрування, а потім 25 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 60 випарювали розчинник в умовах зниженого тиску. Залишок очищали методом хроматографії на силікагелі (гексан/етилацетат=90/10-40/60) з одержанням трет-бутил-[(2S)-1-{[транс-4-({6-[2(дифторметил)-1H-бензімідазол-1-іл]-2-(морфолін-4-іл)піримідин-4-іл}окси)циклогексил]аміно}-4(метилсульфаніл)-1-оксобутан-2-іл]метилкарбамату (859 мг). Приклад одержання 88 До суміші метил-[(2S)-1-({транс-4-[(трет-бутоксикарбоніл)аміно]-циклогексил}аміно)-4(метилсульфаніл)-1-оксобутан-2-іл]карбамату (1,5 г), хлористого метилену (15 мл) і метанолу (15 мл) додавали метилйодид (11,6 мл), а потім перемішували при кімнатній температурі протягом ночі. Розчинник випарювали в умовах зниженого тиску, і до суміші залишку і диметилформаміду (7,5 мл) додавали карбонат цезію (3,6 г), а потім перемішували протягом ночі. До реакційного розчину додавали воду, а потім екстрагували етилацетатом. Органічний шар промивали насиченим сольовим розчином. Органічний шар сушили над безводним сульфатом натрію, осушник видаляли шляхом фільтрування, а потім випарювали розчинник в умовах зниженого тиску. До залишку додавали етанол, одержану тверду речовину збирали шляхом фільтрування і сушили в умовах зниженого тиску з одержанням метил-[(3S)-1-{транс-4[(трет-бутоксикарбоніл)аміно]циклогексил}-2-оксопіролідин-3-іл]карбамату (0,88 г). Приклад одержання 89 До розчину 1,1'-[2-(метилсульфаніл)піримідин-4,6-діїл]біс[2-(дифторметил)-1Hбензімідазолу] (2 г) у N,N-диметилацетаміді (10 мл) додавали трет-бутил-(3S)-3(гідроксиметил)піролідин-1-карбоксилат (965 мг) і карбонат цезію (2,1 г), а потім перемішували при 60 °C протягом 5 годин. Після завершення реакції до реакційної суміші додавали воду з льодом, і збирали одержану тверду речовину шляхом фільтрування. Після сушіння одержану речовину розчиняли в дихлорметані й очищали методом колонкової хроматографії (гексан/етилацетат=90/10-65/35) з одержанням трет-бутил-(3S)-3-[({6-[2-(дифторметил)-1Hбензімідазол-1-іл]-2-(метилсульфаніл)піримідин-4-іл}окси)метил]піролідин-1-карбоксилату (2,01 г). Приклад одержання 90 Суміш 1-[6-хлор-2-(метилсульфаніл)піримідин-4-іл]-2-(дифторметил)-1H-бензімідазолу (350 мг), метил-[(3R)-1-(транс-4-аміноциклогексил)-2-оксопіролідин-3-іл]карбамату гідрохлориду (344 мг), карбонату калію (178 мг), N-етил-N-ізопропілпропан-2-аміну (1,1 мл) і N,Nдиметилацетаміду (1,75 мл) перемішували при 60 °C протягом ночі. До реакційного розчину додавали воду і етилацетат. Нерозчинну речовину збирали шляхом фільтрування, а потім екстрагували етилацетатом. Розчинник випарювали в умовах зниженого тиску, а потім об’єднували залишок і нерозчинні речовини. Додавали етилацетат, суміш суспендували, перемішували, а потім збирали шляхом фільтрування. Одержану речовину промивали водою і сушили з одержанням метил-{(3R)-1-[транс-4-({6-[2-(дифторметил)-1H-бензімідазол-1-іл]-2(метилсульфаніл)піримідин-4-іл}аміно)циклогексил]-2-оксопіролідин-3-іл}карбамату (446 мг). Приклад 1 Суміш 2-дифторметил-1-[2-(метилсульфоніл)-6-морфолін-4-ілпіримідин-4-іл]-1Hбензімідазолу (770 мг), трет-бутил-(3S)-3-амінопіролідин-1-карбоксилату (525 мг), карбонату калію (390 мг) і N,N-диметилацетаміду (19 мл) перемішували в мікрохвильовому реакторі при 100 °C протягом 1 години. Реакційну суміш охолоджували до кімнатної температури, потім вливали у воду, а потім екстрагували етилацетатом. Органічний шар промивали насиченим сольовим розчином і сушили над безводним сульфатом магнію. Розчинник випарювали в умовах зниженого тиску, а потім очищали залишок методом колонкової хроматографії на аміносилікагелі (гексан/етилацетат=80/20-50/50) з одержанням трет-бутил-(3S)-3-({4-[2(дифторметил)-1H-бензімідазол-1-іл]-6-морфолін-4-ілпіримідин-2-іл}аміно)піролідин-1карбоксилату (310 мг) у вигляді блідо-жовтої аморфної речовини. Приклад 22 Суміш 2-(дифторметил)-1-[2-(метилсульфоніл)-6-морфолін-4-ілпіримідин-4-іл]-1Hбензімідазолу (100 мг), 1-бензил-3-(метиламіно)піролідину (93 мг), карбонату калію (50 мг) і N,Nдиметилацетаміду (2,5 мл) перемішували в мікрохвильовому реакторі при 100 °C протягом 1 години. Реакційну суміш охолоджували до кімнатної температури, потім вливали воду, а потім екстрагували етилацетатом. Органічний шар промивали насиченим сольовим розчином і сушили над безводним сульфатом магнію. Розчинник випарювали в умовах зниженого тиску, а потім очищали залишок методом колонкової хроматографії на аміносилікагелі (гексан/етилацетат=80/20-50/50). Цільові фракції об’єднували і концентрували в умовах зниженого тиску. Залишок розчиняли в 1,4-діоксані, і додавали 4M розчин (61 мкл) хлороводню в 1,4-діоксані. Потім, додавали діізопропіловий ефір (10 мл). Одержаний порошок збирали шляхом фільтрування, промивали діізопропіловим ефіром, і сушили в умовах зниженого тиску з 26 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 60 одержанням гідрохлориду N-(1-бензилпіролідин-3-іл)-4-[2-(дифторметил)-1H-бензімідазол-1-іл]N-метил-6-морфолін-4-ілпіримідин-2-аміну (28 мг) у вигляді блідо-жовтого порошку. Приклад 26 До суміші дигідрохлориду 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6-морфолін-4-іл-N-[(3S)піролідин-3-іл]піримідин-2-аміну (58 мг) і N,N-диметилформаміду (1,2 мл) додавали фенілацетальдегід (21 мг), триацетоксиборгідрид натрію (75 мг) і оцтову кислоту (0,29 мл), і перемішували суміш при кімнатній температурі протягом ночі. До реакційної суміші додавали насичений водний розчин бікарбонату натрію, а потім екстрагували етилацетатом. Органічний шар промивали насиченим сольовим розчином і сушили над безводним сульфатом магнію. Розчинник випарювали в умовах зниженого тиску, а потім очищали залишок методом колонкової хроматографії на аміносилікагелі (гексан/етилацетат=80/20-50/50, а потім хлороформ/метанол=100/0-80/20) з одержанням 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6морфолін-4-іл-N-[(3S)-1-(2-фенілетил)піролідин-3-іл]піримідин-2-аміну (30 мг) у вигляді білого порошку. Приклад 43 До розчину 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6-морфолін-4-іл-N-(піперидин-4ілметил)піримідин-2-аміну (400 мг) у 1,2-дихлоретані (8 мл) додавали 4-фторциклогексанон (210 мг), і перемішували суміш при кімнатній температурі протягом 10 хвилин. Потім додавали триацетоксиборгідрид натрію (382 мг), а потім перемішували при кімнатній температурі протягом ночі. До реакційної суміші додавали насичений водний розчин бікарбонату натрію, а потім екстрагували хлороформом. Органічний шар промивали насиченим сольовим розчином і сушили над безводним сульфатом натрію. Розчинник випарювали в умовах зниженого тиску, а потім очищали залишок методом колонкової хроматографії на аміносилікагелі (гексан/етилацетат=70/30-40/60) з одержанням двох типів представлених нижче сполук, кожної у вигляді білого порошку. 4-[2-(Дифторметил)-1H-бензімідазол-1-іл]-N-{[1-(транс-4-фторциклогексил)піперидин-4іл]метил}-6-(морфолін-4-іл)піримідин-2-амін (109 мг). Значення Rf при проведенні ТШХ на аміносилікагелі (гексан/етилацетат=50/50) для цієї сполуки складало 0,35. 4-[2-(Дифторметил)-1H-бензімідазол-1-іл]-N-{[1-(цис-4-фторциклогексил)піперидин-4іл]метил}-6-(морфолін-4-іл)піримідин-2-амін (87 мг). Значення Rf при проведенні ТШХ на аміносилікагелі (гексан/етилацетат=50/50) для цієї сполуки складало 0,28. Одержаний вище 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-N-{[1-(транс-4фторциклогексил)піперидин-4-іл]метил}-6-(морфолін-4-іл)піримідин-2-амін (80 мг) розчиняли в суміші хлороформу (1,5 мл) і метанолу (0,3 мл), і додавали 4M розчин (0,37 мл) хлороводню в 1,4-діоксані. Суміш перемішували при кімнатній температурі протягом 10 хвилин. Реакційну суміш концентрували з одержанням дигідрохлориду 4-[2-(дифторметил)-1H-бензімідазол-1-іл]N-{[1-(транс-4-фторциклогексил)піперидин-4-іл]метил}-6-(морфолін-4-іл)піримідин-2-аміну (сполука прикладу 43-1, 87 мг) у вигляді білого порошку. Аналогічним чином, з одержаного вище 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-N-{[1-(цис4-фторциклогексил)піперидин-4-іл]метил}-6-(морфолін-4-іл)піримідин-2-аміну (62 мг) одержували дигідрохлорид 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-N-{[1-(цис-4фторциклогексил)піперидин-4-іл]метил}-6-(морфолін-4-іл)піримідин-2-аміну (сполука прикладу 43-2, 70 мг) у вигляді білого порошку. Приклад 44 До суміші 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6-(морфолін-4-іл)-N-[(1-фенілпіперидин4-іл)метил]піримідин-2-аміну (38 мг), хлороформу (0,75 мл) і метанолу (0,35 мл) додавали 4M розчин (0,2 мл) хлороводню в 1,4-діоксані, і перемішували суміш при кімнатній температурі протягом 10 хвилин. Реакційну суміш концентрували в умовах зниженого тиску з одержанням дигідрохлориду 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6-(морфолін-4-іл)-N-[(1фенілпіперидин-4-іл)метил]піримідин-2-аміну (43 мг) у вигляді білого порошку. Приклад 45 До суміші дигідрохлориду 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6-морфолін-4-іл-N-[(3S)піролідин-3-іл]піримідин-2-аміну (75 мг) і N,N-диметилформаміду (1,5 мл) додавали 2(диметиламіно)етилбромід (26 мг) і карбонат калію (85 мг), і перемішували суміш при кімнатній температурі протягом ночі. До реакційної суміші додавали воду, а потім екстрагували етилацетатом. Органічний шар промивали насиченим сольовим розчином і сушили над безводним сульфатом магнію. Розчинник випарювали в умовах зниженого тиску, а потім очищали залишок методом колонкової хроматографії на аміносилікагелі 27 UA 108390 C2 5 10 15 20 25 30 35 40 45 50 55 60 (гексан/етилацетат=50/50-0/100, а потім хлороформ/метанол=100/0-80/20). Цільові фракції об’єднували і концентрували в умовах зниженого тиску. Залишок розчиняли в 1,4-діоксані (0,5 мл), і додавали 4M розчин (80 мкл) хлороводню в 1,4-діоксані. Потім додавали діізопропіловий ефір (10 мл). Одержаний порошок збирали шляхом фільтрування, промивали діізопропіловим ефіром, і сушили в умовах зниженого тиску з одержанням дигідрохлориду 4-[2-(дифторметил)1H-бензімідазол-1-іл]-N-{(3S)-1-[2-(диметиламіно)етил]піролідин-3-іл}-6-морфолін-4-ілпіримідин2-аміну (10 мг) у вигляді білого порошку. Приклад 52 До суміші 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6-морфолін-4-іл-N-(піперидин-4ілметил)піримідин-2-аміну (100 мг) і етанолу (2 мл) додавали 2-(фторметил)оксиран (19 мкл) і N,N-діізопропілетиламін (79 мкл), і перемішували суміш у мікрохвильовому реакторі при 120 °C протягом 1 години. До реакційної суміші додавали воду, а потім екстрагували етилацетатом. Органічний шар промивали насиченим сольовим розчином і сушили над безводним сульфатом магнію. Розчинник випарювали в умовах зниженого тиску, а потім очищали залишок методом колонкової хроматографії на аміносилікагелі (етилацетат/гексан) з одержанням 1-{4-[({4-[2(дифторметил)-1H-бензімідазол-1-іл]-6-(морфолін-4-іл)піримідин-2-іл}аміно)метил]піперидин-1іл}-3-фторпропан-2-олу (81 мг) у вигляді білого порошку. Приклад 53 До суміші трет-бутил-(3S)-3-({4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6-морфолін-4ілпіримідин-2-іл}аміно)піролідин-1-карбоксилату (300 мг) і 1,4-діоксану (3 мл) додавали 4M розчин (1,5 мл) хлороводню в 1,4-діоксані, і перемішували суміш при кімнатній температурі протягом 2 годин. До реакційної суміші додавали діізопропіловий ефір (10 мл). Одержаний порошок збирали шляхом фільтрування, промивали діізопропіловим ефіром, і сушили в умовах зниженого тиску з одержанням дигідрохлориду 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6морфолін-4-іл-N-[(3S)-піролідин-3-іл]піримідин-2-аміну (354 мг) у вигляді блідо-жовтого порошку. Приклад 54 До суміші трет-бутил-4-({4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6-морфолін-4ілпіримідин-2-іл}аміно)піперидин-1-карбоксилату (42 мг) і метанолу (0,84 мл) додавали 4M розчин хлороводню в 1,4-діоксані, і перемішували суміш при кімнатній температурі протягом 4 годин. Реакційну суміш нейтралізували додаванням насиченого водного розчину бікарбонату натрію, і екстрагували хлороформом. Органічний шар сушили над безводним сульфатом магнію, і випарювали розчинник в умовах зниженого тиску. Залишок очищали методом колонкової хроматографії на аміносилікагелі (гексан/етилацетат=50/50) з одержанням 4-[2(дифторметил)-1H-бензімідазол-1-іл]-6-морфолін-4-іл-N-піперидин-4-ілпіримідин-2-аміну (27 мг) у вигляді блідо-жовтого порошку. Приклад 66 До суміші 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6-морфолін-4-іл-N-піперидин-4ілпіримідин-2-аміну (18 мг) і N,N-диметилформаміду (0,36 мл) додавали N,N-диметилгліцин (4,8 мг), 1-гідроксибензотриазол (6,2 мг) і N-[3-(диметиламіно)пропіл]-N'-етилкарбодііміду гідрохлорид (8,8 мг), і перемішували суміш при кімнатній температурі протягом 6 годин. До реакційної суміші додавали воду, а потім екстрагували хлороформом. Органічний шар сушили над безводним сульфатом магнію. Розчинник випарювали в умовах зниженого тиску, а потім очищали залишок методом колонкової хроматографії на аміносилікагелі (етилацетат, а потім хлороформ/метанол=96/4). Цільові фракції об’єднували і концентрували в умовах зниженого тиску. Залишок отверджували шляхом додавання невеликої кількості діізопропілового ефіру з одержанням 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-N-{1-[(диметиламіно)ацетил]піперидин-4іл}-6-морфолін-4-ілпіримідин-2-аміну (9 мг) у вигляді білого порошку. Приклад 71 До суміші 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6-морфолін-4-іл-N-(піперидин-4ілметил)-1,3,5-триазин-2-аміну (50 мг) і піридину (2 мл) додавали оцтовий ангідрид (14 мкл), і перемішували суміш при кімнатній температурі протягом ночі. До реакційної суміші додавали толуол, а потім концентрували в умовах зниженого тиску. Залишок розчиняли в дихлорметані, додавали силікагель, а потім концентрували в умовах зниженого тиску. Залишок очищали методом колонкової хроматографії на силікагелі (гексан/етилацетат, а потім хлороформ/метанол) з одержанням N-[(1-ацетилпіперидин-4-іл)метил]-4-[2-(дифторметил)-1Hбензімідазол-1-іл]-6-морфолін-4-іл-1,3,5-триазин-2-аміну (44 мг) у вигляді білого порошку. Приклад 74 До суміші 4-[2-(дифторметил)-1H-бензімідазол-1-іл]-6-морфолін-4-іл-N-(піперидин-4ілметил)піримідин-2-аміну (50 мг) і 1,2-диметоксіетану (1 мл) додавали бромбензол (24 мкл), трис(дибензиліденацетон)дипаладій(0) (6,5 мг), дициклогексил(2',4',6'-триізопропілбіфеніл-2 28
ДивитисяДодаткова інформація
Назва патенту англійськоюHetero ring compound
Автори англійськоюShiwaku, Yasumasa, Takahashi, Fumie, Imada, Sunao, Asano, Toru, Kozuki, Yoshihiro, Maeda, Junko, Kato, Koji, Fukahori, Hidehiko
Автори російськоюСиваку Масахико (умерший), Такахаси Фумие, Имада Сунао, Асано Тору, Козуки Йосихиро, Маеда Дзунко, Като Кодзи, Фукахори Хидехико
МПК / Мітки
МПК: C07D 405/14, A61K 31/541, A61P 43/00, C07D 409/14, C07D 403/04, C07D 471/04, A61P 1/04, C07D 417/14, A61K 31/55, A61P 29/00, C07D 413/14, A61P 17/06, A61P 37/06, A61P 37/02, A61P 37/08, C07D 401/14, C07D 471/10, A61P 35/02, C07D 403/14, A61P 11/06, A61P 19/02, A61K 31/5377
Мітки: бензимідазолу, застосування, похідні
Код посилання
<a href="https://ua.patents.su/374-108390-pokhidni-benzimidazolu-ta-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Похідні бензімідазолу та їх застосування</a>
Попередній патент: Спосіб отримання метанвмісного газу з синтез-газу та установка для його здійснення
Наступний патент: Пристрій і спосіб очищення технологічного розчину гравітаційним осадженням
Випадковий патент: Метод проведення дискретного плазмаферезу з використанням полівінілхлоридних контейнерів












