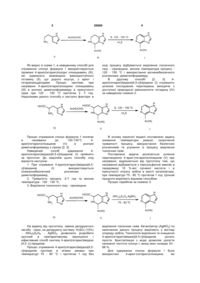
Спосіб одержання 4-арил(гетарил)імідазо[4,5-с]піридинів
Номер патенту: 55660
Опубліковано: 27.12.2010
Автори: Бородкін Ярослав Сергійович, Матвєєва Дар'я Ігорівна, Абрамянц Маргарита Григорівна, Смоляр Микола Миколайович
Формула / Реферат
Спосіб одержання 4-арил(гетарил)імідазо[4,5-с]піридинів формули І
 , I
, I
де Аr = С6Н5 (а), 4-СН3ОС6Н4 (б), 4-ВrС6Н4 (в), 4-С6Н5СН2ОС6Н4 (г), 3,4,5-(СН3О)3С6Н2 (д);
Ht = піридин-3-іл (є), піридин-4-іл (ж), тієн-2-іл (з), хінолін-8-іл (і), 1,3-диметил-2-оксобензімідазол-5-іл (к), 1-феніл-3-метилпіразол-4-іл (л), 1,3-дифенілпіразол-4-іл (м), N-бензиліндол-3-іл (н), 1-феніл-2-хлор-4-метилпірол-3-іл (о),
шляхом перетворення 4-арил(гетарил)спінацинів при нагріванні, який відрізняється тим, що 4-арил(гетарил)спінацини піддають взаємодії з персульфатом амонію в середовищі 10 %-вої сірчаної кислоти при температурі 75-80 °С в присутності нітрату срібла впродовж 1 год., цільові продукти виділяють відомим способом.
Текст
Спосіб одержання 4-арил(гетарил)імідазо[4,5с]піридинів формули І H N N де Аr = С6Н5 (а), 4-СН3ОС6Н4 (б), 4-ВrС6Н4 (в), 4С6Н5СН2ОС6Н4 (г), 3,4,5-(СН3О)3С6Н2 (д); Ht = піридин-3-іл (є), піридин-4-іл (ж), тієн-2-іл (з), хінолін-8-іл (і), 1,3-диметил-2-оксобензімідазол-5іл (к), 1-феніл-3-метилпіразол-4-іл (л), 1,3дифенілпіразол-4-іл (м), N-бензиліндол-3-іл (н), 1феніл-2-хлор-4-метилпірол-3-іл (о), шляхом перетворення 4-арил(гетарил)спінацинів при нагріванні, який відрізняється тим, що 4арил(гетарил)спінацини піддають взаємодії з персульфатом амонію в середовищі 10 %-вої сірчаної кислоти при температурі 75-80 °С в присутності нітрату срібла впродовж 1 год., цільові продукти виділяють відомим способом. N Ar(Ht) (І) Ar(Ht) де Аr = С6Н5 (а), 4-СН3ОС6Н4 (б), 4-ВrС6Н4 (в), 4-С6Н5СН2ОС6H4 (г), 3,4,5-(СН3О)3С6Н2 (д); Ht = піридин-3-іл (e), піридин-4-іл (ж), тієн-2-іл (з), хінолін-8-іл (і), 1,3-диметил-2 (11) N UA N оксобензімідазол-5-іл (к), 1-феніл-3-метилпіразол4-іл (л), 1,3-дифенілпіразол-4-іл (м), Nбензиліндол-3-іл (н), 1-феніл-2-хлор-4-метилпірол3-іл (о). 4-Арил(гетарил)імідазо[4,5-с]піридини (І) можуть використовуватись в якості синтонів для отримання біологічно активних сполук з метою приготування лікарських форм або композицій [1]. Відомий спосіб одержання 4арил(гетарил)імідазо[4,5-е]піридинів [2, 3] полягає в отриманні сполук формули І шляхом послідовних перетворень виходячи з гістаміну (II) і арил(гетарил)альдегідів за наступною схемою 1: (19) Корисна модель відноситься до галузі органічної хімії, до способу одержання 4арил(гетарил)імідазо[4,5-с]піридинів формули І H N 55660 (13) U ,I 3 55660 H N NH2 H N HN -H2S H N S, 120 - 150 0C N Ar(Ht)CHO N 4 N Ar(Ht) Ar(Ht) II III I Як видно зі схеми 1, в наведеному способі для отримання сполук формули І використовуються проміжні 4-арил(гетарил)похідні спінацеаміну (III), які одержують взаємодією важкодоступного гістаміну (II), що дорого коштує, з арил- і гетарилальдегідами. Процес протікає при нагріванні 4-арил(гетарил)похідних спінацеаміну (III) в розчині диметилформаміду в присутності сірки при 120 - 150 °С протягом 2 -7 год. Недоліками даного способу є наступні фактори: в H N HOOC NH2 N ході процесу відбувається виділення токсичного газу - сірководню, висока температура процесу 120 - 150 °С і використання вогненебезпечного розчинника -диметилформаміду. В другому способі [2, 3] 4арил(гетарил)імідазо[4,5-с]піридини (І) отримують шляхом послідовних перетворень виходячи з доступної природньої амінокислоти гістидину (IV) за наведеною схемою 2: H N HN N -H2S H N S, 120 - 150 0C N HOOC Ar(Ht)CHO N Ar(Ht) Ar(Ht) IV V Процес отримання сполук формули 1 полягає в нагріванні до 120-130°С 4арил(гетарил)спінацинів (V) в розчині диметилформаміду з сіркою [2, 3]. Наведений спосіб одержання 4арил(гетарил)імідазо[4,5-с]піридинів (І) прийнято за прототип. До недоліків цього способу слід віднести наступне: 1. При отриманні 4-арил(гетарил)імідазо[4,5с]піридинів (І) використовується пожежонебезпечний розчинник диметилформамід. 2. Тривалість процесу -2-7 год та висока температура - 120 - 130 °С. 3. Виділення токсичного газу - сірководню. H N HOOC NH2 N I В основу корисної моделі поставлено задачу зниження температури реакції, скорочення тривалості процесу, використання безпечних розчинників та усунення із процесу виділення токсичних газів. Поставлена задача досягається шляхом перетворення 4-арил-(гетарил)спінацинів (V) при нагріванні, відрізняється від прототипу тим, що нагрівання відбувається з персульфатом амонію в середовищі 10 %-вої сірчаної кислоти і в присутності нітрату срібла в якості каталізатора, при температурі 75 - 80 °С протягом 1 год. Цільові продукти виділяють відомим способом. Процес перебігає за схемою 3: H N HOOC Ar(Ht)CHO HN N Ar(Ht) IV На відміну від прототипу, заміна дегідруючого засобу - сірки, на дегідруючу систему: H2SO4 (10%) - (NH4)2S2О8 - AgNO3, дозволило розробити зручний в препаративному відношенні і ефективний спосіб синтезу 4-арил(гетарил)імідазо [4,5 -с] піридинів. Процес отримання 4-арил(гетарил)імідазо[4,5с]піридинів протікає в м'яких умовах при температурі 75 - 80 °С і протягом 1 год без N V H N (NH4)2S2O8,AgNO3 75 - 80 0C N N Ar(Ht) I виділення токсичних газів. Каталізатор (AgNO3) по закінченню даного процесу виділяють у вигляді хлориду срібла. Технологія виділення та очищення 4-арил(гетарил)імідазо[4,5-с]піридинів досить проста. Кристалізація з води дозволяє досягти належної чистоти сполук І, вихід яких складає 53 88 %. Для одержання сполук формули І були використані 4-арил-(гетарил)спінацини, які 5 55660 6 отримані за відомими методиками [2, 3] з 9.94 с (1H, Н2'). Знайдено, %: С 67.26; Н 4.12; N доступних гістидину (IV) та арил і 28.43. C11H8N4. Вирахувано, %: С 67.33; Н 4.11; N гетарилальдегідів (фірми виробники хімічних 28.56. реактивів «Merck», «Fluka», «Aldrich», 4-(Піридин-4-іл)імідазо[4,5-с]піридин (І ж). «Lancaster», та ін.). Вихід 65 %, т.топл. 273 -275 °С. Спектр ЯМР 1Н Приклад 1. Спосіб отримання 4(ДМСО-d6), , м.д.: 7.60 д (1Н, Н7, J=5.3 Гц), 8.43 д фенілімідазо[4,5-с]піридину (І а). (1H, H6, J=5.3 Гц), 8.47 с (1Н, H2), 8.61 д (2Н, Н2'6', До розчину 5 ммоль 4-фенілспінацину (V а) в J=4.5 Гц), 8.65 д (2Н, Н3'5', J=4.5 Гц). Знайдено, %: 10мл 10 %-вої сірчаної кислоти, який містить 0.01 г С 67.29; Н 4.15; N28.49. C11H8N4. Вирахувано, %: С азотнокислого срібла, при інтенсивному 67.33; Н 4.11; N 28.56. перемішуванні та температурі 75 - 80 °С додають 4-(Тієн-2-іл)імідазо[4,5-с]піридин (І з). Вихід 10 ммоль персульфата амонія в 5 мл води 88%, т.топл. 198 -199 °С. Спектр ЯМР 1Н (ДМСОвпродовж 0.5 год і витримують реакційну суміш в d6), , м.д.: 7.36 т (1Н, H4'), 7.86 д (1H, Н7, J=5.5 Гц), даних умовах 0.5 год. Суміш охолоджують і 8.03 д (1Н, H3', J=4.6 Гц), 8.30 д (1Н, H6, J=5.5 Гц), додають розчин 0.1 г хлорида натрія в 1 мл води. 8.41 д (1Н, Н5', J=4.6 Гц), 8.67 с (1Н, Н2). Знайдено, Відфільтровують хлорид срібла, що випадає в %: С 59.63; Н 3.52; N20.79; S 15.78. C10H7N3S. осад, доводять pH фільтрату до ~ 9 карбонатом Вирахувано, %: С 59.68; Н 3.51; N 20.88; S 15.93. натрію. Продукт реакції, що випадає в осад, 4-(Хінолін-8-іл)імідазо[4,5-с]піридин (І i). Вихід відфільтровують і перекристалізовують з води. 69 %, т.топл.>300 °С. Спектр ЯМР 1Н (ДМСО-d6), , 1 Вихід 71 %, т.топл. 82 - 83 °С. Спектр ЯМР Н м.д.: 7.71 - 7.84 м (1Н, H6'), 7.97 д (1Н, Н7', J=7.5 (ДМСО-d6), , м.д.: 7.58 - 7.68 м (3Н, С6Н5), 7.74 д Гц), 8.20 - 8.27 м (2Н, H4'5'), 8.55 д (1Н, Н7, J=7.6 (1Н, Н7, J=5.7 Гц), 8.15 - 8.21 м (2Н, С6Н5), 8.47 д Гц), 8.76 с (1H, Н2), 8.75 - 9.15 м (2Н, Н2'3'), 9.86 д (1Н, Н6, J=5.7 Гц), 8.50 с (1H, H2). Знайдено, %: С (1H, Н6, J=7.6 Гц). Знайдено, %: С 73.02; Н 4.15; N 73.75; Н 4.73; N 21.45. C12H9N3. Вирахувано, %: С 22.67. C15H10N4. Вирахувано, %: С 73.15; Н 4.09; N 73.83; Н 4.65; N 21.52. 22.75. Аналогічним шляхом отримують сполуки (І б-o) 4-(1,3-Диметил-2-оксобензімідазол-5виходячи з 5 ммоль 4-арил(гетарил)спінацинів (V іл)імідазо[4,5-с]піридин (І к). Вихід 63 %, т.топл. б-o), 10 %-вої сірчаної кислоти, 0.01 г 227 - 228 °С. Спектр ЯМР 1Н (ДМСО-d6) , м.д.: азотнокислого срібла, 10 ммоль персульфата 3.33 с (6Н, 2СН3), 7.30 д (1H, Н7, J=8.0 Гц), 7.84 д амонія. Процес отримання сполук формули І (1Н, Н6, J=8.0 Гц), 8.35 - 8.39 м (3Н, С6Н3), 8.78 с протікає при температурі 75 - 80 °С протягом 1 год. (1Н, Н2). Знайдено, %: С 64.43; Н 4.72; N24.97. 4-(n-Метоксифеніл)імідазо[4,5-с]піридин (І б). C15H13N5O. Вирахувано, %: С 64.50; Н 4.69; N 1 Вихід 69 %, т.топл. 186 - 187 °С. Спектр ЯМР Н 25.08. (ДМСО-d6), , м.д.: 3.85 с (3Н, ОСН3), 7.07 д (2Н, 4-(1-Феніл-3-метилпіразол-4-іл)імідазо[4,5H3'5', С6Н4, .J=6.2 Гц), 7.35 д (1Н, Н7, J=6.0 Гц), 8.12 с]піридин (І л). Вихід 57 %, т.топл. 102-103 °С. с (1Н, Н2), 8.31 д (2Н, H2'6', J=6.2 Гц), 8.45 д (1Н, H6, Спектр ЯМР 1Н (ДМСО-d6), , м.д.: 2.68 с (3Н, J=6.0 Гц). Знайдено, %: С 69.20; Н 4.98; N 18.55. СН3), 7.20 - 7.80 м (6Н, С6Н5, Н2), 8.20 - 8.42 м (2Н, C13H11N3O. Вирахувано, %: С 69.32; Н 4.92; N Н7, Н5'), 9.33 д (1Н, Н6, J=8.0 Гц). Знайдено, %: С 18.66. 69.68; Н 4.79; N25.37. C16H13N5. Вирахувано, %: С 4-(n-Бромфеніл)імідазо[4,5-с]піридин (І в). 69.80; Н 4.76; N25.44. 1 Вихід 70 %, т.топл. 216 -218 °С. Спектр ЯМР Н 4-(1,3-Дифенілпіразол-4-іл)імідазо[4,5(ДМСО-d6), , м.д.: 7.55 д (1Н, Н7, J=4.8 Гц), 7.72 д с]піридин (І м). Вихід 53 %, т.топл. 175 - 177 °С. 3'5' 2 (2Н, H , С6Н4, J=8.4 Гц), 8.30 с (1Н, Н ), 8.39 д Спектр ЯМР 1Н (ДМСО-d6), , м.д.: 7.30 - 7.75 м (2Н, Н2'6', С6Н4, J=8.4 Гц), 8.53 д (1Н, Н6, J=4.8 Гц). (10Н, 2С6Н5), 7.82 - 8.00 м (2Н, Н2, Н5'), 8.35 д (1Н, Знайдено, %: С 52.51; Н 3.08; N 15.25. C12H8BrN3. Н7, J=7.5 Гц), 9.17 д (1Н, Н6, J=7.5 Гц). Знайдено, Вирахувано, %: С 52.58; Н 2.94; N 15.33. %: С 74.69; Н 4.55; N20.65. C21H15N5. Вирахувано, 4-(n-Бензилоксифеніл)імідазо[4,5-с]піридин (І %: С 74.75; Н 4.48; N20.76. 1 г). Вихід 68 %, т.топл. 231 - 233 °С. Спектр ЯМР Н 4-(N-Бензиліндол-3-іл)імідазо[4,5-с]піридин (І (ДМСО-d6), , м.д.: 5.25 м (2Н, СН2), 7.32 д (2Н, н). Вихід 77 %, т.топл. 250 - 252 °С. Спектр ЯМР 1Н H3'5', С6Н4, J=8.5 Гц), 7.37 - 7.47 м (5Н, С6Н5), 8.05 д (ДМСО-d6), , м.д.: 5.16 с (2Н, СН2), 7.00 т (1H, Н5'), (1Н, Н7, J=6.6 Гц), 8.37 д (2Н, Н2'6', С6Н4, J=8.5 Гц), 7.19 т (1H, H6'), 7.31 - 7.40 м (9Н, С6Н5, 7-Н, 6-Н, 8.53 д (1Н, H6, J=6.6 Гц), 8.75 с (1Н, Н2). Знайдено, H4'), 7.83 с (1Н, 2-Н); 7.95 д (1Н, Н7', J=8.0 Гц), 8.46 %: С 75.67; Н 5.13; N 13.88. C19H15N3O. с (1Н, 2-Н). Знайдено, %: С 77.59; Н 5.06; N 17.16. Вирахувано, %: С 75.73; Н 5.03; N13.94. C21H16N4. Вирахувано, %: С 77.75; Н 4.97; N 17.27. 4-(3,4,5-Триметоксифеніл)імідазо[4,5-с]піридин 4-(1-Феніл-2-хлор-4-метилпірол-3(І д). Вихід 70 %, т.топл. 148 - 150 °С. Спектр ЯМР іл)імідазо[4,5-с]піридин (І о). Вихід 67 %, т.топл. 1 Н (ДМСО-d6), , м.д.: 3.90 с (9Н, 3ОСН3), 7.35 д 150-152 °С. Спектр ЯМР 1Н (CD3OD), , м.д.: 2.15 с (1Н, Н7, J=6.0 Гц), 7.79 с (2Н, С6Н2), 8.20 с (1Н, Н2), (3Н, СН3), 7.21 с (1Н, H5'), 7.25 - 7.50 м (5Н, С6Н5), 8.43 д (1Н, Н6, J=6.0 Гц). Знайдено, %: С 63.12; Н 7.57 д (1Н, Н7, J=8.0 Гц), 7.83 д (1Н, Н6, J=8.0 Гц), 5.35; N14.60. C15H15N3O3. Вирахувано, %: С 63.15; 7.93 с (1H, Н2). Знайдено, %: С 66.08; Н 4.30; N Н 5.30; N 14.73. 18.09. С17Н13N4С1. Вирахувано, %: С 66.13; Н 4.24; 4-(Піридин-3-іл)імідазо[4,5-с]піридин (І є). N 18.15. Вихід 67 %, т.топл. 253 -255 °С. Спектр ЯМР 1H Як видно з наведених прикладів, 5' 7 (ДМСО-d6), , м.д.: 7.63 т (1Н, Н ), 7.69 д (1Н, Н , запропонований спосіб одержання 4J=5.6 Гц), 8.54 д (1H, В6, J=5.6 Гц), 8.55 с (1Н, Н2), 4' 6' 8.72 д (1Н, H , J=7.2 Гц), 9.07 д (1Н, Н , J=7.2 Гц), 7 55660 8 арил(гетарил)імідазо[4,5-с]піридинів (І а-о) має Katritzky. - New-York. "Acad. Press", 2005. - Vol. 89. перевагу по відношенню до прототипу: -P. 161-278. 1. Скорочення тривалості процесу до 1 год, 2. Смоляр Н.Н., Абрамянц М.Г., Ютилов Ю.М. температури реакції до 75 - 80 °С. Дегидрирование 4-фенил-замещенных 2. Виключення із процесу пожежонебезпечних спинацеамина и спинацина // Журн. орган, химии. розчинників та викидів в атмосферу токсичних 2006. -Т. 42, вып. 4.-С. 560-563. продуктів. 3. Смоляр Н.Н., Абрамянц М.Г., Завязкина Джерела інформації Т.И., Матвеева Д.И., Бородкин Я.С., Волоский И.А. 1. Yutilov Yu.M. Imidazopyridines: 1- and 3Синтез и дегидрирование 4-гетарил-производных Deazapurines // Adv. Heterocycl. Chem. / Ed. A.R. спинацеамина и спинацина // Журн. орган, химии. 2009. -Т. 45, вып. 8. - С. 1228-1231. Комп’ютерна верстка В. Мацело Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 4-aryl(hetaryl)imidazo[4,5-c]pyridines
Автори англійськоюSmoliar Mykola Mykolaiovych, Abramiants Marharyta Hryhorivna, Borodkin Yaroslav Serhiiovych, Matvieeva Daria Ihorivna
Назва патенту російськоюСпособ получения 4-арил(гетарил)имидазо[4,5-с]пиридинов
Автори російськоюСмоляр Николай Николаевич, Абрамянц Маргарита Григорьевна, Бородкин Ярослав Сергеевич, Матвеева Дарья Игоревна
МПК / Мітки
МПК: C07D 471/02, C07D 249/18
Мітки: одержання, 4-арил(гетарил)імідазо[4,5-с]піридинів, спосіб
Код посилання
<a href="https://ua.patents.su/4-55660-sposib-oderzhannya-4-arilgetarilimidazo45-spiridiniv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 4-арил(гетарил)імідазо[4,5-с]піридинів</a>
Попередній патент: Пилоприбиральний насадок
Наступний патент: Захоплювач для випробувань пластинчастих зразків композитних матеріалів
Випадковий патент: Спосіб визначення тактики оперативного втручання при дифузному токсичному зобі