Спосіб одержання кветіапіну (варіанти) і проміжні сполуки
Номер патенту: 73547
Опубліковано: 15.08.2005
Автори: Ракоці Дьйордьне, Кованьіне Лакс Дьйордьі, Верецкейне Донат Дйордьі, Кражнаі Дьйордь, ШІМІГ Дьюла, Тьомпе Петер, Божінг Даніель, Надь Кальман
Формула / Реферат
1. Спосіб одержання 11-[4-/2-(2-гідроксіетоксі)етил/-1-піперазиніл]дибензо[b,f]-1,4-тіазепіну формули (I) 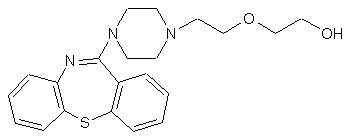 (I)
(I)
або його фармацевтично прийнятної кислотно-адитивної солі, який включає реакцію похідної галогенетилпіперазинілтіазепіну формули (VIII)
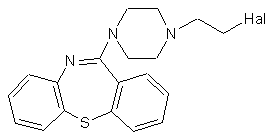 , (VIII)
, (VIII)
де Hal означає атом галогену, з етиленгліколем;
і, при необхідності, перетворення одержаного продукту в кислотно-адитивну сіль з використанням фармацевтично прийнятної неорганічної або органічної кислоти.
2. Спосіб згідно з пунктом 1, в якому реакцію проводять в присутності неорганічної основи.
3. Спосіб одержання 11-[4-/2-(2-гідроксіетоксі)етил/-1-піперазиніл]дибензо[b,f]-1,4-тіазепіну формули (І) або його фармацевтично прийнятної кислотно-адитивної солі, який включає циклізацію похідної галогенетилпіперазину формули (VII)
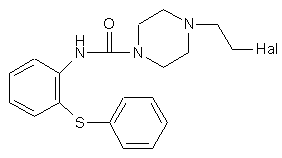 , (VII)
, (VII)
де Hal означає атом галогену, у присутності дегідратуючого агента, і
реакцію одержаної похідної галогенетилпіперазинілтіазепіну формули (VIII), де Hal визначений вище, з етиленгліколем;
і, при необхідності, перетворення одержаного продукту в кислотно-адитивну сіль з використанням фармацевтично прийнятної неорганічної або органічної кислоти.
4. Спосіб згідно з пунктом 3, в якому вихідною сполукою є галогеналкілпіперазин формули (VII), де Hal означає атом хлору, а дегідратуючим агентом є пентаоксид фосфору.
5. Спосіб згідно з пунктом 3, в якому реакцію сполуки формули (VIII), де Hal означає атом хлору, з етиленгліколем проводять в присутності неорганічної основи.
6. Спосіб одержання 11-[4-/2-(2-гідроксіетоксі)етил/-1-піперазиніл]дибензо[b,f]-1,4-тіазепіну формули (І) або його фармацевтично прийнятної кислотно-адитивної солі, який включає реакцію похідної гідроксіетилпіперазину формули (VI)
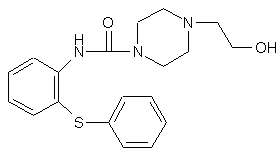 , (VI)
, (VI)
з галогенуючим агентом, циклізацію одержаної похідної галогенетилпіперазину формули (VII), де Hal означає атом галогену, у присутності дегідратуючого агента, і реакцію одержаної похідної галогенетилпіперазинілтіазепіну формули (VIII), де Hal визначений вище, з етиленгліколем;
і, при необхідності, перетворення одержаного продукту в кислотно-адитивну сіль з використанням фармацевтично прийнятної неорганічної або органічної кислоти.
7. Спосіб згідно з пунктом 6, в якому галогенуючим агентом є оксихлорид фосфору.
8. Спосіб згідно з пунктом 6, в якому реакцію сполуки формули (VIII), де Hal означає атом хлору, з етиленгліколем проводять в присутності неорганічної основи.
9. Спосіб одержання 11-[4-/2-(2-гідроксіетоксі)етил/-1-піперазиніл]дибензо[b,f]-1,4-тіазепіну формули (І) або його фармацевтично прийнятної кислотно-адитивної солі, який включає реакцію похідної гідроксіетилпіперазину формули (VI) одночасно з галогенуючим агентом і дегідратуючим агентом, і реакцію одержаної похідної галогенетилпіперазинілтіазепіну формули (VIII), де Hal означає атом галогену, з етиленгліколем;
і, при необхідності, перетворення одержаного продукту в кислотно-адитивну сіль з використанням фармацевтично прийнятної неорганічної або органічної кислоти.
10. Спосіб згідно з пунктом 9, в якому реакцію сполуки формули (VIII), де Hal означає атом хлору, з етиленгліколем проводять в присутності неорганічної основи.
11. Спосіб одержання 11-[4-/2-(2-гідроксіетокси)етил/-1-піперазиніл]дибензо[b,f]-1,4-тіазепіну формули (І) або його фармацевтично прийнятної кислотно-адитивної солі, який включає реакцію похідної уретану формули (IV)
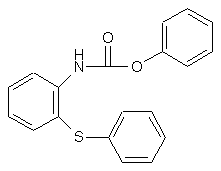 (IV)
(IV)
з 1-(2-гідроксіетил)піперазином формули (V)
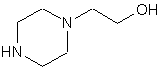 , (V)
, (V)
наступну реакцію одержаної похідної гідроксіетилпіперазину формули (VI) одночасно з галогенуючим агентом і дегідратуючим агентом, і реакцію одержаної похідної галогенетилпіперазинілтіазепіну формули (VIII), де Hal означає атом галогену, з етиленгліколем;
і, при необхідності, перетворення одержаного продукту в кислотно-адитивну сіль з використанням фармацевтично прийнятної неорганічної або органічної кислоти.
12. Спосіб згідно з пунктом 11, в якому реакцію сполуки формули (VIII), де Hal означає атом хлору, з етиленгліколем проводять в присутності неорганічної основи.
13. Похідна піперазину формули (IX)
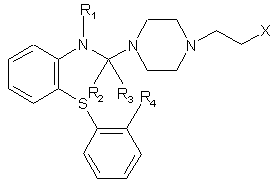 , (IX)
, (IX)
в якій або
R1 означає атом водню,
R2 разом з R3 представляють атом кисню, і
R4 означає атом водню;
або
R1 утворює разом з R2 валентний зв'язок між сусідніми атомами азоту і вуглецю,
R3 утворює разом з R4 валентний зв'язок між сусідніми атомами вуглецю, і
Х означає гідроксильну групу або атом галогену,
і її кислотно-адитивні солі з неорганічними або органічними кислотами.
14. Похідна піперазину за пунктом 13, яка являє собою гідроксіетилпіперазин формули (VI)
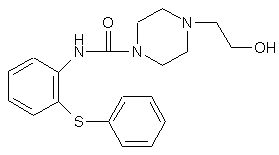 , (VI)
, (VI)
і її кислотно-адитивні солі.
15. Похідна піперазину за пунктом 13, яка являє собою галогенетилпіперазин формули (VII)
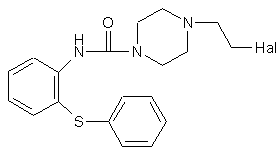 , (VII)
, (VII)
де Hal означає атом галогену, і її кислотно-адитивні солі.
16. Похідна піперазину за пунктом 15, яка являє собою N-[4-(2-хлоретил)піперазин-1-карбоніл]-2-амінодифенілсульфід і його кислотно-адитивні солі.
17. Похідна піперазину за пунктом 13, яка являє собою галогенетилпіперазинілтіазепін формули (VIII)
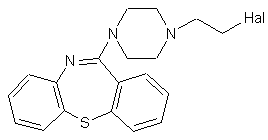 , (VIII)
, (VIII)
де Hal означає атом галогену, і її кислотно-адитивні солі.
18. Похідна піперазину за пунктом 17, яка являє собою 11-[4-(2-хлоретил)піперазин-1-іл]дибензо[b,f]-1,4-тіазепін і його кислотно-адитивні солі.
Текст
Винахід стосується нового способу піп'еразиніл]дибензо[b,f]-1,4-тіазепіну формули одержання 11-[4-/2-(2-гідроксиетокси)етил/-1 відомого під міжнародною непатентованою назвою кветіапін. Сполука має антидофамінергічну активність і/або активність антагоніста серотонінових рецепторів і використовується в клінічній практиці в якості антипсихотичного або нейролептичного засобу. Крім того, винахід стосується нових проміжних сполук, використовуваних у новому способі винаходу. Згідно із способом, відомим з ЕР 240228, сполуку формули І одержують шляхом реакції імінохлориду формули з 1-(2-гідроетокси)етилпіперазином. Одержаний неочищений маслянистий продукт піддають очищенню за допомогою хроматографії з використанням колонки із силікагелем, одержуючи вихід 77,7% у розрахунку на приблизно 0,5моль. Імінохлорид формули XI, використовуваний в якості вихідної сполуки, одержують шляхом циклізації похідної уретану формули і галогенування одержаного дибензо[b,f]-1,4-тіазепін-11(10Н)-ону формули оксихлоридом фосфору згідно з ЕР 282236. Вихід реакції циклізації складає 87%, а реакції галогенування - 92,6%. Таким чином, у випадку описаного вище відомого способу загальний вихід, розрахований для похідної уретану формули IV, складає 62,6%. Той факт, що кристалічний продукт прийнятної чистоти можна одержати тільки після очищення за допомогою колонкової хроматографії, робить виробництво в промислових масштабах з використанням відомого способу важким і надзвичайно неекономічним. Імінохлорид формули XI є досить нестабільною сполукою і гідролізується атмосферною вологою. При роботі з великими кількостями сполуки ця побічна реакція зменшує ви хід, а продукт гідролізу забруднює кінцевий продукт. Ще один недолік полягає в тому, що одержання 1-(2-гідроетокси)етилпіперазину може здійснюватися в кілька стадій, що робить відомий спосіб ще менш економічним. Згідно з іншим способом, відомим з ЕР 282236, похідну піперазину формули піддають реакції з 2-галогенетоксиетанолом, одержуючи продукт формули І з ви ходом 78%. Похідну піперазину формули XII одержують шляхом реакції імінохлориду формули XI з піперазином з виходом 88%; таким чином, загальний вихід реакції синтезу, розрахований для похідної уретану формули IV, складає лише 55,3%. Метою даного винаходу є створення економічного способу одержання кветіапіну. Було виявлено, що описана вище ціль досягається завдяки способу одержання 11-[4-/2-(2гідроксиетокси)етил/-1-піперазиніл]дибензо[b,f]-1,4-тіазепіну формули І або його фармацевтично прийнятної кислотно-адитивної солі за допомогою а1) реакції похідної галогенетилпіперазинілтіазепіну формули де Hal означає атом галогену, з етиленгліколем; або а2) циклізації похідної галогенетилпіперазину формули де Hal означає атом галогену, у присутності дегідратуючого агента і реакції одержаної похідної галогенетилпіперазинілтіазепіну формули VIII, де Hal визначений вище, з етиленгліколем; або а3) реакції похідної гідроксиетилпіперазину формули з галогенуючим агентом, циклізації одержаної похідної галогенетилпіперазину формули VII, де Hal означає атом галогену, у присутності дегідратуючого агента, і реакції одержаної похідної галогенетилпіперазинілтіазепіну формули VIII, де Hal визначений вище, з етиленгліколем; або а4) реакції похідної гідроксиетилпіперазину формули VI одночасно з галогенуючим агентом і дегідратуючим агентом, і реакції одержаної похідної галогенетилпіперазинілтіазепіну формули VIII, де Hal означає атом галогену, з етиленгліколем; або а5) реакції похідної уретану формули IV з 1-(2-гідроксиетил)піперазином формули і подальшої реакції одержаної похідної гідроксиетилпіперазину формули VI одночасно з галогенуючим агентом і дегідратуючим агентом, і реакції одержаної похідної галогенетилпіперазинілтіазепіну формули VIII, де Hal означає атом галогену, з етиленгліколем; і, при необхідності, перетворення одержаного продукту в кислотно-адитивну сіль з використанням фармацевтично прийнятної неорганічної або органічної кислоти. Крім того, винахід включає нові похідні піперазину формули де або R1 означає атом водню, R2 разом з R3 означають атом кисню, і R4 означає атом водню; або R1 утворює разом з R2 валентний зв'язок між сусідніми атомами азоту і вуглецю, R3 утворює разом з R4 валентний зв'язок між сусідніми атомами вуглецю, і X означає гідроксильну гр упу або атом галогену, і їх кислотно-адитивні солі з неорганічними або органічними кислотами. Нові похідні піперазину є проміжними сполуками в новому способі винаходу. У способі а1) винаходу додержуються звичайних умов реакції Віл'ямсона. По-перше, етиленгліколь перетворюють в алкоголят, використовуючи металевий натрій або будь-які інші придатні неорганічні основи. Звичайно і натрій, і етиленгліколь використовують у надлишку; у перерахуванні на 1моль похідної галогенетилпіперазинілтіазепіну формули VIII, беруть переважно 1,5-1,7моль натрію і 20-30моль, переважніше 25-27моль етиленгліколю. Температура реакції складає звичайно 50-150°С, переважно приблизно 100°С. Як правило, реакція триває 5-15 годин, звичайно приблизно 9 годин. У способі а 2) винаходу кращою вихідною сполукою є похідна галогенетилпіперазину формули VII, де Hal означає атом хлору, а придатним дегідратуючим агентом є пентаоксид фосфору. У реакційну суміш переважно додають також оксихлорид фосфору, а замикання кільця здійснюють переважно при кипінні реакційної суміші. Одержану похідну галогенетилпіперазинілтіазепіну формули VIII перетворюють у продукт формули І згідно з методом, описаним в способі а 1). У способі а3) винаходу в якості галогенуючого агента переважно використовують тіонілхлорид або оксихлорид фосфору, переважніше останній. Реакцію галогенування проводять у нейтральному органічному розчиннику, або як розчинник можуть використовувати також надлишок галогенуючого агента. Звичайне галогенування здійснюють при кипінні реакційної суміші. Одержану похідну галогенетилпіперазину формули VII перетворюють у продукт формули І згідно з методом, описаним у способі а2). У способі а4) винаходу галогенування похідної гідроксиетилпіперазину формули VI і подальше замикання кільця здійснюють в одну стадію без виділення похідної галогенетилпіперазину формули VII, яка утворюється під час галогенування. Придатним галогенуючим агентом є оксихлорид фосфору, кращим дегідратуючим агентом - пентаоксид фосфору. У реакційну суміш можна додавати нейтральний органічний розчинник, або як розчинник використовують надлишок галогенуючого агента. Температура реакції переважно дорівнює температурі кипіння реакційної суміші. У більшості випадків час реакції складає 6-10 годин, переважно - 7-8 годин. Після закінчення реакції реакційну суміш вливають у воду, підлуговують і екстрагують органічним розчинником, який не змішується з водою, наприклад, дихлорметаном. Потім виконують процедуру, описану в способі а1) винаходу для одержання продукту формули І. У способі а 5) винаходу реакцію похідної уретану формули IV з 1-(2-гідроксиетил)піперазином здійснюють у нейтральному органічному розчиннику, звичайно в неполярному органічному розчиннику, переважно толуолі. Як правило, температура реакції вище кімнатної температури, переважно реакцію здійснюють при температурі кипіння розчинника. Час реакції відносно невеликий, звичайно реакція протікає за 2 години. Спочатку реакційну суміш промивають водним лугом, потім водою для того, щоб видалити фенол, що утворюється, органічну фазу висушують і упарюють. Осад кристалізують з органічного розчинника. Одержану похідну гідроксиетилпіперазину формули VI перетворюють у продукт формули І способом, описаним у способі а4) винаходу. Продукт формули І може бути перетворений у фармацевтично прийнятну кислотно-адитивну сіль способом, відомим per se. Переважно одержують геміфумарат. При необхідності, основу формули І можна виділити з його кислотно-адитивної солі способом, відомим per se. Похідну уретану формули IV можна одержати відомим з літератури способом шляхом реакції 2амінодифенілсульфіду формули з фенілхлорформіатом формули Сполуку формули І одержують способом винаходу із загальним виходом 66-67%, розрахованим для похідної уретану формули IV. Стадії способу винаходу можуть бути легко здійснені, вихідні сполуки і реагенти легко доступні. Спосіб винаходу не включає ні однієї процедури, яка могла б викликати труднощі або понизити вихід. Одержаний кветіапін формули І має високу чистоту. Похідні гідроксиетилпіперазину формули VI, похідні галогенетилпіперазину формули VII і похідні галогенетилпіперазинілтіазепіну формули VIII, усі з яких є проміжними сполуками в способі винаходу і представляють собою нові сполуки. Нові перераховані вище проміжні сполуки мають формулу IX. Таким чином, кращими новими похідними піперазину формули IX є такі сполуки: - похідна гідроксиетилпіперазину формули VI і її кислотно-адитивні солі; - похідна галогенетилпіперазину формули VII, де Hal визначений вище, і її кислотно-адитивні солі; і - похідна галогенетилпіперазинілтіазепіну формули VIII, де Hal визначений вище, і її кислотно-адитивні солі. Особливо кращою похідною галогенетилпіперазину формули VII є N-[4-(2-хлоретил)піперазин-1карбоніл]-2-амінодифенілсульфід і її кислотно-адитивні солі. Особливо кращою похідною галогенетилпіперазинілтіазепіну формули VIII є 11-[4-(2хлоретил)піперазин-1-іл]дибензо[b,f]-1,4-тіазепін і її кислотно-адитивні солі. Нові проміжні сполуки можуть бути одержані способами, описаними вище. Далі винахід пояснюється наступними Прикладами. Одержання вихідної сполуки формули IV Феніл-2-фенілтіофенілкарбамат 20,13г (0,1моль) 2-амінодифенілсульфіду розчиняють у 250мл дихлорметану й одержаний розчин охолоджують до 5°С. Половину розчину 18,79г (15,1мл, 0,2моль) фенілхлорформіату в 26мл дихлорметану повільно додають до розчину, що перемішується, 2-амінодифенілсульфіду, потім додають іншу половину розчину фенілхлорформіату, а також розчин 3,0г (0,075моль) гідроксиду натрію і 9,2г (0,0875моль) карбонату натрію в 50мл води, одночасно стежачи за тим, щоб внутрішня температура реакційної суміші не перевищувала 10°С. Після припинення додавання реакційну суміш перемішують при кімнатній температурі протягом 3 годин, органічну фазу відокремлюють, промивають 3 рази розведеною соляною кислотою, використовуючи загальний об'єм 250мл, висушують над безводним сульфатом магнію й упарюють. Осад кристалізують з н-гексану. У такий спосіб одержують 29г (90,2%) названої сполуки. Т. пл. 90-91°С. Аналіз: для C19H15NO 2S (321.401) визначено: С 71,01%; Η 4,70%; Ν 4,36%; S 9,98%; знайдено: С 71,19%; Η 4,69%; Ν 4,33%; S 9,84%. Приклад 1 N-[4-(2-гідроксиетил)піперазин-1-карбоніл]-2-амінодифенілсульфід - сполука формули VI 32,1г (0,1моль) феніл-2-фенілтіофенілкарбамату розчиняють у 600мл толуолу і до розчину, що перемішується, додають 13,0г (0,1моль) 1-(2-гідроксиетил)піперазину. Реакційну суміш перемішують при температурі кипіння протягом 2 годин, потім охолоджують до кімнатної температури і промивають 600мл 1н. розчину гідроксиду натрію, потім двічі по 200мл води. Органічну фазу висушують над безводним сульфатом магнію й упарюють. Осад кристалізують із суміші н-гексану і етилацетату (10:1), фільтрують, промивають н-гексаном і висушують. У такий спосіб одержують 33,9г (94,8 %) названої сполуки у вигляді білих кристалів. Т. пл. 96-98°С. Аналіз: для C19H23N3 O2S (357.478) визначено: С 63,84%; Η 6,49%; Ν 11,75%; S 8,97%; знайдено: С 63,57%; Η 6,52%; Ν 11,71%; S 9,02%. Приклад 2 N-[4-(2-хлоретил)піперазин-1-карбоніл]-2-амінодифенілсульфід - сполука формули VII 18,8г (0,05моль) N-[4-(2-гідроксиетил)піперазин-1-карбоніл]-2-амінодифенілсульфіду кип'ятять у 65мл тіонілхлориду протягом 15 хвилин, потім упарюють і залишок кристалізують з н-гексану. Одержують 18,5г (89,7%) продукту, який є гідрохлоридом названої сполуки. Т. пл. 180-183°С. Одержання основи: До суспензії 10,31г (0,025моль) гідрохлориду в 250мл ізопропанолу додають 2,78г (0,0275моль) триетиламіну, реакційну суміш перемішують при кімнатній температурі протягом 1 години, додають воду, екстрагують дихлорметаном, висушують над безводним сульфатом магнію й упарюють. У такий спосіб одержують 8,0г (85,1%) названої сполуки. Одержання солі з бензолсульфокислотою: До розчину 7,5г (0,02моль) названої основи в 15мл етанолу додають розчин 3,48г (0,022моль) бензолсульфокислоти у 10мл етанолу. Розчин перемішують при кімнатній температурі протягом 1 години, потім охолоджують крижаною водою, фільтрують і висушують. У такий спосіб одержують 6,6г (60,8%) продукту, який є означає бензолсульфонатом названої сполуки. Т. пл. 110-112°С. Аналіз: для C25H28CIN3 O4S 2 (534.101) визначено: С 56,22%; Η 5,28%; Ν 7,87%; СІ 6,64% S 12,01%; знайдено: С 55,96%; Η 5,35%; Ν 7,73%; СІ 6,50% S 12,05%. Приклад 3 11-[4-(2-хлоретил)-1-піперазиніл]дибензо[b,f]-1,4-тіазепін - сполука формули VIII Метод А) Суміш 8,2г (0,02моль) гідрохлориду N-[4-(2-хлоретил)піперазин-1-карбоніл]-2-амінодифенілсульфіду, 84мл оксихлориду фосфор у і 8,5г (0,06моль) пентаоксиду фосфор у витримують при температурі кипіння протягом 15 годин. Розчин охолоджують, потім ретельно упарюють, залишок вливають у крижану воду, розчин підлуговують додаванням водного розчину аміаку й екстрагують дихлорметаном. Органічну фазу упарюють, залишок кристалізують з діізопропілового ефіру, фільтрують і висушують. У такий спосіб одержують 5,4г (75,4%) названої сполуки. Т. пл.113-115°С. Метод В) Суміш 35,7г (0,1моль) N-[4-(2-гідроксиетил)піперазин-1-карбоніл]-2-амінодифенілсульфіду, 200мл оксихлориду фосфор у і 31,2г (0,22моль) пентаоксиду фосфору кип'ятять протягом 7 годин. Розчин охолоджують, упарюють, залишок обробляють крижаною водою, підлуговують водним розчином аміаку, екстрагують дихлорметаном, висушують над безводним сульфатом магнію і знову упарюють. Залишок кристалізують з діізопропілового ефіру, кристали відфільтровують і висушують. У такий спосіб одержують 28,6г (80%) названої сполуки Т. пл.114-116°С. Аналіз: для C19H20CIN3S (357.908) визначено: С 63,76%; Η 5,63%; Ν 11,74%; СІ 9,91% S 8,96%; знайдено: С 63,70%; Η 5,57%; Ν 11,68%; СІ 9,89% S 9,07%. Приклад 4 Геміфумарат 11-[4-/2-(2-гідроксиетокси)етил/-1-піперазиніл]дибензо[b,f]-1,4-тіазепіну - сполука формули І 1,17г металевого натрію розчиняють у 50мл етиленгліколю і до одержаного розчину додають розчин 10,7г (0,03моль) 11-[4-(2-хлоретил)-1-піперазиніл]дибензо[b,f]-1,4-тіазепіну у 60мл толуолу. Реакційну суміш перемішують при 100°С протягом 9 годин, потім після охолодження додають 210мл води. Після розділення толуольну фазу екстрагують розведеною соляною кислотою, розчин підлуговують додаванням водного розчину аміаку, екстрагують дихлорметаном, органічний розчин висушують над безводним сульфатом магнію й упарюють при зниженому тиску. У такий спосіб одержують 11,27г (98%) названої основи. Одержання солі: 10г (0,026моль) одержаної основи розчиняють у 130мл етанолу і додають до розчину 3,13г (0,027) фумарової кислоти. Суміш перемішують при температурі кипіння протягом 25 хвилин, потім охолоджують до кімнатної температури. Суміш витримують у холодильнику протягом ночі, потім кристали відфільтровують, промивають холодним етанолом і висушують. У такий спосіб одержують 9,8г (85,4%) названої сполуки Т. пл.172-174°С. Аналіз: для C46H54N5 O8S 2 (883.107) визначено: С 62,56%; Η 6,16%; Ν 9,52%; S 7,26%; знайдено: С 62,19%; Η 6,19%; Ν 9,57%; S 7,24%.
ДивитисяДодаткова інформація
Назва патенту англійськоюA method for the preparation of quetiapine (variants) and intermediary compounds
Автори англійськоюNagy Kalman
Назва патенту російськоюСпособ получения кветиапина (варианты) и промежуточные соединения
Автори російськоюНадь Кальман
МПК / Мітки
МПК: C07D 295/215, C07D 281/00
Мітки: спосіб, варіанти, кветіапіну, сполуки, проміжні, одержання
Код посилання
<a href="https://ua.patents.su/4-73547-sposib-oderzhannya-kvetiapinu-varianti-i-promizhni-spoluki.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання кветіапіну (варіанти) і проміжні сполуки</a>
Попередній патент: Уловлювач стрічки похилого конвеєра
Наступний патент: Електрична машина харченка з безвитковою обмоткою якоря
Випадковий патент: Спосіб вирощування післяукісного соняшника на зрошуваних землях








