Спосіб одержання заміщених 4,4а,5,7,7а,8-гексагідрофуро[2,3-f]ізобензофуран-4-карбонових кислот
Номер патенту: 78469
Опубліковано: 25.03.2013
Автори: Горак Юрій Ігорович, Обушак Микола Дмитрович, Матійчук Василь Степанович, Литвин Роман Зіновійович, Гомза Юрій Володимирович
Формула / Реферат
Спосіб одержання заміщених 4,4а,5,7,7а,8-гексагідрофуро[2,3-f]ізобензофуран-4-карбонових кислот, що включає взаємодію заміщених алілових спиртів з ангідридом ненасиченої карбонової кислоти у середовищі бензолу, який відрізняється тим, що як спирти використовують 2-фурилаліловий або 5-арил-2-фурилалілові спирти, як ангідрид - малеїновий ангідрид і одержують сполуки загальної формули
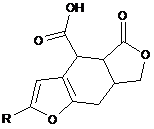 ,
,
де R=H, арил.
Текст
Реферат: Спосіб одержання заміщених 4,4а,5,7,7а,8-гексагідрофуро[2,3-f]ізобензофуран-4-карбонових кислот включає взаємодію заміщених алілових спиртів з ангідридом ненасиченої карбонової кислоти у середовищі бензолу. Як спирти використовують 2-фурилаліловий або 5-арил-2фурилалілові спирти, як ангідрид - малеїновий ангідрид і одержують сполуки загальної формули OH O O O R O . UA 78469 U (12) UA 78469 U UA 78469 U 5 10 15 20 25 Корисна модель стосується органічної хімії, а саме способів одержання корисних органічних сполук, які можуть бути використані у фармакології як лікарські препарати, зокрема аналоги лігнанів і гетеролігнанів, що виявляють протиракову, антиревматичну та антиастматичну активність. Відомий спосіб отримання ізобензофуранів [Элдерфилд P. Гетероциклические соединения / Р. Элдерфилд. - М.: Из-во иностранной литературы, 1954., II т. - 437 с.], за яким при взаємодії арилфталідів з ароматичними магнійорганічними сполуками в інертній атмосфері утворюються 1,3-діарилізобензофурани. Недоліками способу є невисокі виходи кінцевих продуктів, трудомісткість процесу, а також важкодоступність вихідних речовин. Найближчим за технічною суттю - прототипом є спосіб одержання ізобензотіофенів [Klemm L.Н. Intramolecular Diels-Alder cyclization into the thiophene ring / L.H. Klemm, K.W. Gopinath // Journal of Heterocyclic Chemistry.-1965. - Vol. 2, № 3. - P. 225-227], який полягає у реакції [4+2]циклоприєднання, де тієнілалілові спирти реагують з хлорангідридом фенілпропіолової кислоти у бензолі так, що відбувається О-ацилювання з наступною внутрішньомолекулярною реакцією циклоприєднання, в результаті чого формується біциклічна конденсована гетеросистема. Недоліком способу є відсутність замісників у положенні 2 тіофенового циклу та обмеженість способу, який полягає у використанні виключно похідних тіофену. В основу корисної моделі поставлено задачу удосконалити спосіб одержання заміщених 4,4а,5,7,7а, 8-гексагідрофуро[2,3-f]ізобензофуран-4-карбонових кислот шляхом уведення арильних фрагментів у положення 2 фуранового циклу та використання в реакції [4+2]циклоприєднання з малеїновим ангідридом доступних сполук фуранового ряду, а саме 2фурилалілових або 5-арил-2-фурилалілових спиртів, що дасть змогу одержувати цільові продукти, які містять фурановий та арилфурановий цикл та значно розширити межі цієї реакції. Поставлена задача вирішується тим, що у способі одержання заміщених 4,4а,5,7,7а,8гексагідро[2,3-f]ізобензофуран-4-карбонових кислот, що включає взаємодію заміщених алілових спиртів з ангідридом ненасиченої карбонової кислоти у середовищі бензолу, при цьому як спирти використовують 2-фурилаліловий або 5-арил-2-фурилалілові спирти, як ангідрид малеїновий ангідрид і одержують сполуки загальної формули 30 OH O O O R 35 O , де R=Н, арил. Автори вперше запропонували використати 3-(2-фурил)акролеїн та 3-(5-арил-2фурил)акролеїни як вихідні сполуки. Вони реагують з борогідридом натрію у середовищі тетрагідрофурану, утворюючи відповідно 2-фурилаліловий та 5-арил-2-фурилалілові спирти, які вступають у реакцію [4+2]-циклоприєднання з малеїновим ангідридом так, що фурановий цикл зберігається, а в реакцію вступає екзоциклічний подвійний зв'язок. При цьому формується ізобензофуранова система з карбоксильною групою у шестичленному карбоциклі: 40 NaBH4 O R O HO H O O R O O R THF O O HO OH H O H + O R O 1 H O O O Benzene, t , UA 78469 U 5 10 15 20 де R=H, арил. 1 Будову синтезованих сполук підтвердили даними спектроскопії ЯМР Н, склад - елементним аналізом. Приклад 1. До розчину 0,003 моль (0,8 г) 5-(2,4-дихлорфеніл)-2-фурил-2-пропен-1-олу у 10 мл бензолу додають 0,003 (0,3 г) моль розтертого у порошок малеїнового ангідриду. Суміш кип'ятять зі зворотним холодильником до моменту виділення осаду (6-7 год.) і 3-4 год. після цього, після чого цю суміш охолоджують, відфільтровують осад, який промивають бензолом та спиртом і перекристалізовують із суміші спирт-ДМФА. Вихід 5-оксо-2-(2,4-дихлорфеніл)4,4а,5,7,7,7а, 8-гексагідрофуро[2,3-f]ізобензофуран-4-карбонової кислоти 0,59 г (54 %). Т. пл. 1 233-234 °C. Спектр ЯМР Н, , м.ч.: 2,31 (1H, т, J=1,6 Гц); 2,65 (1Н, т, J=1,6 Гц); 3,03 (1Н, д.д, J=17,6 і 9,3 Гц); 3,09-3,14 (1Н, м); 3,93-3,96 (1Н, м); 4,18 (1H, д.д, J=7,8 і 2,3 Гц); 4,45 (1Н, д.д, J=8,2 і 5,1 Гц); 7,28 (1Н, с, фуран); 7,48 (1Н, д.д, J=8,6 і 2,0 Гц, С 6Н3); 7,69 (1Н, д, J=2,0 Гц, С6Н3); 7,77 (1Н, д, J=8,6 Гц, С6Н3). Знайдено, %: С 55, 29; Н 3,03. С17Н12Сl2O5. Вираховано, %: С 55,61; Н 3,29. Приклад 2. 5-Оксо-2-(2-трифторметилфеніл)-4,4а, 5,7,7,7а, 8-гексагідрофуро[2,3f]ізобензофуран-4-карбонову кислоту одержують аналогічно. Вихід 0,47 г (43 %). Т. пл. 1781 179 °C. Спектр ЯМР Н, , м.ч.: 2,33 (1Н, с); 2,67 (1Н, ш.с); 3,05 (1Н, д, J=8,9 Гц); 3,10-3,15 (1Н, м); 4,03-4,19 (2Н, м); 4,77 (1Н, д, J=6,8 Гц); 6,93 (1Н, с, фуран); 7,53 (1H, т, J=7,8 Гц, С 6Н4); 7,717,83 (3Н, м). Знайдено, %: С 58, 83; Н 3,15. С18Н13 F3O5. Вираховано, %: С 59,05; Н 3,58. Запропонований спосіб дає змогу одержувати цільові продукти - заміщені 4,4а,5,7,7а,8гексагідро[2,3f]ізобензофуран-4-карбонові кислоти, використовуючи дешеві та легкодоступні вихідні реагенти, які містять фурановий або арилфурановий цикл і значно розширити межі цієї реакції, що підтверджує одержання передбачуваного технічного результату. 25 ФОРМУЛА КОРИСНОЇ МОДЕЛІ 30 Спосіб одержання заміщених 4,4а,5,7,7а,8-гексагідрофуро[2,3-f]ізобензофуран-4-карбонових кислот, що включає взаємодію заміщених алілових спиртів з ангідридом ненасиченої карбонової кислоти у середовищі бензолу, який відрізняється тим, що як спирти використовують 2-фурилаліловий або 5-арил-2-фурилалілові спирти, як ангідрид - малеїновий ангідрид і одержують сполуки загальної формули OH O O O R O , де R=H, арил. 35 Комп’ютерна верстка Л. Ціхановська Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 2
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of substituted 4,4a,5,7,7a,8-hexahydrofuro[2,3-f]isobenzofuran-4-carboxylic acids
Автори англійськоюHorakYurii Ihorovych, Obushak Mykola Dmytrovych, Lytvyn Roman Zinoviiovych, Homza Yurii Volodymyrovych, Matiichuk Vasyl Stepanovych
Назва патенту російськоюСпособ получения замещенных 4,4а,5,7,7а,8-гексагидрофуро[2,3-f]изобензофуран-4-карбоновых кислот
Автори російськоюГорак Юрий Игоревич, Обушак Николай Дмитриевич, Литвин Роман Зиновьевич, Гомза Юрий Владимирович, Матийчук Василий Степанович
МПК / Мітки
МПК: C07D 307/00, C07D 307/87, C07D 307/78
Мітки: заміщених, кислот, спосіб, 4,4а,5,7,7а,8-гексагідрофуро[2,3-f]ізобензофуран-4-карбонових, одержання
Код посилання
<a href="https://ua.patents.su/4-78469-sposib-oderzhannya-zamishhenikh-44a577a8-geksagidrofuro23-fizobenzofuran-4-karbonovikh-kislot.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання заміщених 4,4а,5,7,7а,8-гексагідрофуро[2,3-f]ізобензофуран-4-карбонових кислот</a>
Попередній патент: Спосіб одержання 2-арил-3-оксо-5-(5-r-2-фурил)-2,3,3а,4,5,7а-гексагідро-1н-4-ізоіндол-4-карбонових кислот
Наступний патент: Спосіб одержання заміщених 4а,5,6,7,7а,8-гексагідро-4н-фуро[2,3f]ізоіндол-5-онів
Випадковий патент: Тверда лікарська форма, що містить інгібітор віл протеази








