(6r,12ar)-6-(1,3-бензодіоксол-5-іл)-2-метил-2,3,6,7,12,12a-гексагідропіразино[1′,2′:1,6]піридо[3,4-b]індол-1,4-діон та його фармацевтично прийнятні солі
Формула / Реферат
(6R,12aR)-6-(1,3-бензодіоксол-5-ил)-2-метил-2,3,6,7,12,12а-гексагідропіразино-[1',2':1,6]піридо[3,4-b]індол-1,4-діон структурної формули (І)
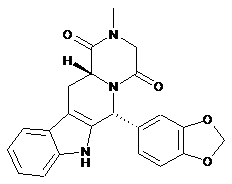 (І)
(І)
та його фармацевтично прийнятні солі.
Текст
Реферат: (6R,12aR)-6-(1,3-бензодіоксол-5-іл)-2-метил-2,3,6,7,12,12а-гексагідропіразино[1',2':1,6]піридо[3,4-b]індол-1,4-діон структурної формули (І) N O H N O O N H O (І) та його фармацевтично прийнятні солі. UA 84818 U (54) (6R,12aR)-6-(1,3-БЕНЗОДІОКСОЛ-5-ІЛ)-2-МЕТИЛ-2,3,6,7,12,12aГЕКСАГІДРОПІРАЗИНО[1',2':1,6]ПІРИДО[3,4-b]ІНДОЛ-1,4-ДІОН ТА ЙОГО ФАРМАЦЕВТИЧНО ПРИЙНЯТНІ СОЛІ UA 84818 U UA 84818 U 5 Корисна модель належить до хімічних сполук, які є похідними тетрациклічних сполук. У патенті США US 3917599 описуються деякі похідні піразино[2',1',:6,1]піридо[3,4-b]індолу, які є інгібіторами циклічної гуанозін-3'-5'-монофосфатфосфодіестерази (скорочено - цГМФ ФДЕ) та мають гіпотензивний вплив, і можуть бути використані при серцевій недостатності або кардіальній недостатності. Вказані сполуки на практиці не проявили себе сильнодіючими інгібіторами ФДЭ. Сполука (6R,12аR)-6-(1,3-бензодіоксол-5-ил)-2-метил-2,3,6,7,12,12агексагідропіразино[1',2':1,6]піридо[3,4-b]індол-1,4-діон структурної формули (І) N O H N O O N H 10 15 20 25 30 35 40 45 50 O , яке надалі скорочено називатиметься сполука формули (І), також проявляє селективність відносно інгібування цГМФ ФДЕ, і як наслідок цього селективного інгібування ФДЕ підвищується вміст цГМФ, що покращує антиагрегаційні умови для кров'яних пластинок, призводить до антисудиноспазматичної і судинорозширювальної дії. Сполука формули (І) і її солі можуть бути використані при лікуванні ряду таких захворювань, як: гіпертонія, гіперемічна серцева недостатність, знижена пропускна спроможність кровоносних судин, наприклад постпідшкірна транслумінальна коронарна ангіопластика, захворювання периферійних судин, глаукома, а також є корисними при лікуванні дисфункції ерекції. Фармацевтично прийнятні солі сполуки формули (І) можуть бути кислими аддуктами, які отримані відомими в органічній хімії способами з використанням фармацевтично прийнятних кислот. Приклади таких аддуктів охоплюють гідрохлоридні, гідробромідні, сульфатні, фосфатні, ацетатні, цитратні та інші солі сполуки формули (І). До фармацевтично прийнятних солей сполуки формули (І) також належать солі металів, які здатні утворюватися при взаємодії сполуки формули (І) з лугами. До їх прикладів належать натрієві і калієві солі. Біологічну активність сполуки формули (І) визначають згідно з наведеними далі методами випробувань. Фосфодіестеразна активність Спорідненість з'єднання з цГМФ і цАМФ ФДЕ оцінюють шляхом визначення величини ІС 50 (концентрація інгібіторів, яку потрібно для 50 %-го інгібування ензимної дії), ФДЕ-ензими виділяють з кров'яних пластинок кролика по методу У. Дж. Томпсона та ін. (Biochem, 1971, 10, 311). Незалежний від кальцію/кольмодулину [Са/САМ] цГМФ ФДЕ-ензим з GMP PDE і цГМФінгібований цАМФ ФДЕ-ензим отримують з кров'яних пластинок кролика, тоді як з чотирьох основних ФДЕ-ензимів виділяють Са/САМ-залежну цГМФ ФДЕ (фракція І). Випробування проводять відповідно до модифікованого "періодичного" методу У. Дж. Томпсона і М.М. Епплмана (Віоchеm, 1979, 18, 5228). Дія, що перешкоджає агрегації кров'яних пластинок Цю дію оцінюють шляхом визначення здатності з'єднання інгібувати агрегацію кров'яних пластинок в лабораторних умовах, яке ініційоване чинником (АПФ), що активує кров'яні пластинки, і потенціювати антиагрегативну дію на кров'яні тільця в лабораторних умовах активаторів гуанілатциклази, зокрема нітропрусиду і РФВЭ. Промиті кров'яні пластини готують по методу Дж. Ф. Мустарда та ін. (Methoas in Enzymol. 1989, 169, 3), а агрегацію визначають відповідно до стандартної турбідиметричної технології, яка описана Г. В. Р. Борном в J. Рhysiol (Лондон), 1962, 162, 67 Р. Антигіпертонічна дія Цю дію оцінюють після внутрішньовенного або перорального введення з'єднання в організм щурів, що страждають спонтанною гіпертонією. За допомогою канюлі, імплантованої в сонну артерію, тварин, що знаходяться у свідомості, або анестизованих тварин. Інгібувальна активність сполуки формули (І) відносно cGMP PDE і сАМР PDE "ін вітро" визначалася як описано вище і порівнювалася з показниками активності деяких з'єднань, описаних в заявці ЕР 0201188 А. Фермент-інгібувальна активність виражається або у вигляді 1 UA 84818 U -4 5 10 15 20 25 30 величин ІС50 (інгібувальна концентрація) в наномолях, або у вигляді активностей при 10 молярній концентрації. -4 Отримані значення величини ІС50 (у нМ або активности при 10 М) склали: для cGMP PDE, залежний від Са/САМ, величина складала 2,4; для сСАМР PDE, інгібованим cGMP, величина складала 45,000. Ступінь селективності склав приблизно 18,7. Результати випробувань показують, що сполука формули (І) є більше сильнодіючим і селективним інгібітором обох цГМФ ФДЕ. Сполука формули (І) може бути отримана за двостадійним способом. На першій стадії до перемішуваного розчину сполуки (R,3R)-метил-1,2,3,4-тетрагідро-1-(3,4метилендіоксифеніл)-9Н-піридо[3,4-b]індол-3-карбоксилат (0,5 г) і NaHCO3 (0,14 г) у безводному СНСl3 (20 мл) при 0 °C по краплях додавали хлор-ацетилхлорид (0,27 мл). Отриману суміш перемішували при тій же температурі впродовж 1 год. і розбавляли СНСl 3 (20 мл). Після цього до вмісту суміші при перемішуванні по краплях додавали воду (10 мл) і потім насичений розчин NaHCO3. Органічний шар промивали водою до нейтрального значення рН і висушували над Na2SO4. Після упарювання розчинника при зниженому тиску отримували (6R,12aR)-метил-1,2,3,4тетрагідро-2-хлорацетил-1-(3,4-метилендіоксифеніл)-9Н-піридо[3,4-b]індол-1,4-діол-3карбоксилат у вигляді олії, який кристалізували з ефіру до твердого стану (0,38 г, т.п. 233 °C) та використали без подальшого очищення на наступній стадії. На другій стадії до перемішуваної суспензії проміжної сполуки (0,38 г) у матенолі (20 мл) при кімнатній температурі додавали розчин метиламіну (0,4 мл) і отриману суміш нагрівали при 50 °C в атмосфері азоту впродовж 16 ч. Розчинник видаляли при зниженому тиску і залишок розчиняли в СН2Сl2 (50 мл). Після промивання водою (3 рази по 20 мл), висушування над Na2SO4 і упарювання насухо залишок очищували хроматографіюванням з елююванням системою розчинників СН2Сl2/метанол (у співвідношенні 99/1) та перекристалізовували з 2-пропанола, отримуючи сполуку (І) у вигляді кристалів білого кольору (0,22 г), температура плавлення 302-303 °C. У продукті знайдено, %: С 67,82; Н 4,94; N 10,75. Для сполуки брутто-формулою C22H19N3O4 розраховано, %: С 67,77, Н 4,92, N 10,74. Сполуку формули (І) випробовували при терапевтичних дозах до 5 мг/кг внутрішньовенно і орально на щурах і собаках, та на чоловіках-добровольцях при дозах у межах 1-500 мг. При цьому не виявлено ніяких надмірних ознак токсичності. Наявні відомості дозволяють зробити висновок, що ця сполука може бути віднесена до сполук з низькою токсичністю. 35 ФОРМУЛА КОРИСНОЇ МОДЕЛІ (6R,12aR)-6-(1,3-бензодіоксол-5-іл)-2-метил-2,3,6,7,12,12а-гексагідропіразино[1',2':1,6]піридо[3,4-b]індол-1,4-діон структурної формули (І) N O H N O O N H 40 O (І) та його фармацевтично прийнятні солі. Комп’ютерна верстка Д. Шеверун Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 2
ДивитисяДодаткова інформація
МПК / Мітки
МПК: C07D 471/00
Мітки: прийнятні, 6r,12ar)-6-(1,3-бензодіоксол-5-іл)-2-метил-2,3,6,7,12,12a-гексагідропіразино[1',2':1,6]піридо[3,4-b]індол-1,4-діон, солі, фармацевтично
Код посилання
<a href="https://ua.patents.su/4-84818-6r12ar-6-13-benzodioksol-5-il-2-metil-23671212a-geksagidropirazino1216pirido34-bindol-14-dion-ta-jjogo-farmacevtichno-prijjnyatni-soli.html" target="_blank" rel="follow" title="База патентів України">(6r,12ar)-6-(1,3-бензодіоксол-5-іл)-2-метил-2,3,6,7,12,12a-гексагідропіразино[1′,2′:1,6]піридо[3,4-b]індол-1,4-діон та його фармацевтично прийнятні солі</a>
Попередній патент: Проїзний квиток громадського транспорту
Наступний патент: Спосіб роботи роторного двигуна внутрішнього згоряння
Випадковий патент: Спосіб формування панкреатоєюноанастомозу








