Спосіб боротьби з небажаною рослинністю
Формула / Реферат
Способ борьбы с нежелательной растительностью путем обработки растений и почвы, на которой будут произрастать растения производным пиридина, отличающийся тем, что в качестве производного пиридина используют соединение общей формулы
где R1 - метил;
R2 - этил, изопропил;
А-СОOR3, CONHOH, 1,3-оксазолинил-2;
R3-водород, С1-С3-алкил, цианометил, 2-хлораллил, 2-пропинил, 1,1-диметил-2-пропинил, 2,2,2-трихлорэтил, фурфурил, катион, выбранный из группы натрий, кальций, изопропиламмоний, диизопропиламмоний, таллоаммоний;
В - водород, COR4, где R4 - метил, n-хлорфенил, n-нитрофенил, n-метоксифенил, при условии, что, когда В - COR4, A-COOR3, где R3 отличен от водорода или солеобразующего катиона, W-кислород, Ζ не является изопропиламиногруппой;
W - кислород или сера;
Υ - водород, С1-С3-алкил, С1-С3-алкокси, диметиламино, диэтиламино, фенил, циано;
Ζ - водород, С1-С3-алкил, этокси, метилтио, трифторметил, изопропиламино, диметиламино, фенил;
Υ и Ζ совместно образуют группу -C(L)=С(M)-C(Q)=C(R), где L - водород, бром, метил; Μ - водород, хлор, бром, фтор, Q - водород, этокси; R - водород, хлор, метокси, при условии, что только один из радикалов L, М, Q или R может представляв собой заместитель, отличный от водорода, галогена или алкокси, и когда W - кислород и A-COOR3, при условии, что R3 не может быть ненасыщенным алкилом, Υ не может быть диметиламино, диэтиламино, Ζ не может быть метилтио, диметиламино, изопропиламино, в количестве 0,032-1,000 кг/га.
Текст
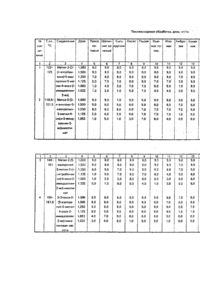
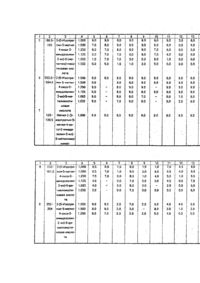
Изобретение относится к химическим способам защиты растений, а именно к способу борьбы с нежелательной растительностью на основе производных пиридина. Известен способ борьбы с нежелательной растительностью на основе 2,6-диметокси-4метилникотиннитрила. Однако он неэффективен. Известен способ борьбы с нежелательной растительностью, использующий в качестве действующего начала 4-амино-3,5,6-трихлорпиколиновую кислоту (тордон). Однако он неэффективен по отношению к просу петушьему, сыти круглой, овсюгу. Целью изобретения является усиление гербицидного действия. Указанная цель достигается путем обработки растений и почвы, на которой произрастают растения производным пиридина общей формулы где R1 - метил; R2 - этил, изопропил; А - COOR3, CONHOH, 1,3-оксазолинил-2; R3 - водород; С1-С3 - алкил, цианометил, 2-хлораллил, 2-пропинил, 1,1-диметил, 2-пропинил, 2,2,2трихлорэтил, фур фурил, катион, выбранный из группы натрий, кальций, изопропиламмоний, диизопропиламмоний, изопропиламмоний, диизопропил-аммонйй, таллоаммоний; В - водород, COR4, где R4 - метил, n-хлорфенил, n-нитрофенил, n-метоксифенил при условии, что когда B-COR4A представляет собой COOR3, в котором R3 отличен от водорода или солеобразующего катона; W кислород; Ζ не является изопропиламино-группой; W - кислород или сера; Υ - водород, С1-С3 -алкил, С1-С3-алкокси, диметиламино, диэтиламино, фенил, циано; Ζ - водород, С1-С3-алкил, этокси, метилтио, трифторметил, изопропиламино, диметиламино, фенил; Υ и Ζ совместно образуют гр уппу C(L)=C(M)-C(Q)=C(R), где L - водород, бром, метил; Μ - водород, хлор, бром, фтор; Q - водород, этокси; R - водород, хлор, метокси, при условии, что только один из радикалов L, М, Q или R может представлять собой заместитель, отличный от водорода, галогена или алкокси, и когда W - кислород и А -COOR3 при условии, что R3 не может быть ненасыщенным алкилом, Υ не может быть диметиламино, диэтиламино, Ζ не может быть метилтио, диметиламино, изопропиламино, в количестве 0,032-1.000 кг/га. Сложные эфиры 2-(2-имидазолин-2-ил)пиридина формулы (1), в которой А -COOR3, a R3 - заместитель, отличный от водорода или солеобразующего катона, и R1, R2 , Υ и Ζ-описаны выше могут быть получены по реакции имидазопирролопиридиндиона с подходящим спиртом и соответствующим алкилатом щелочного металла при 20-50°С. В эти х реакциях спирт может выполнять роль реагента и растворителя. В этой ситуации вторичный растворитель не требуется. Однако при использовании для реакции дорогостоящего растворителя, в реакционную смесь может быть добавлен менее дорогой вторичный растворитель, например диоксан, тетрагидрофуран или иной апротонный растворитель. Количество апротонного растворителя, добавляемого в реакционную смесь, может колебаться в широких пределах. Сложные эфиры 2-(2-имидазолин-2-ил)пиридина могут быть преимущественно получены также из ацетамида диоксопирролопиридина его циклизацией сильным основанием, таким как 1,5-диазабицикло(5,5,0)ундец-5-ен (ДБУ), в присутствии инертного органического растворителя, например ксилола или толуола, с получением сырого имидазопирролопиридина формулы (III). Реакционную смесь нагревают до 100-150°С и воду удаляют из реакционной смеси в ходе реакции с применением любых подходящих средств, например водоотделителя Дина-Старка. Затем к реакционной смеси добавляют минимум один эквивалент спирта, представленного формулой R3OH, где R3 - член указанной группы, отличный от водорода или солеобразующего катиона, и полученную таким путем реакционную смесь нагревают до кипения с обратным холодильником при при 100-150°С с получением сложного эфира 2-(2-имидазолин-2-ил)пиридина формулы. Еще один вариант, относящийся к получению сложных эфиров 2-(2-имидазолин-2-ил)пиридина формулы [1] основан на циклизации сложного эфира карбамоил-никотиновой кислоты с пятихлористым фосфором при повышенной температуре, как правило при 60-100°С. Реакцию предпочтительно проводят в присутствии инертного органического растворителя, например, толуола или бензола. Достигается хороший выход хлористоводородной соли целевого сложного эфира формулы [1]. Хлористоводородную соль затем легко преобразуют в сложный эфир формулы [1] растворением соли присоединения кислоты в воде и нейтрализацией полученного таким путем раствора основанием, например карбонатом натрия или калия. В еще одном варианте получения сложных эфиров 2-(2-имидазолин-2-ил)пиридинов формулы [1] согласно изобретению проводят циклизацию сложного эфира карбамоилникотиновой кислоты с использованием смеси пятихлористого фосфора и оксихлорида фосфора. Реакционную смесь перемешивают при комнатной температуре на протяжении 4-8 ч, после чего РОCl3 удаляют в вакууме. Оставшийся остаток диспергируют в органическом растворителе, например толуоле. Растворитель отгоняют и остаток диспергируют в воде и нагревают до 80-100°С. После охлаждения рН водной смеси доводят до 5-6 бикарбонатом натрия и продукт экстрагируют в метиленхлориде получением целевого сложного эфира 2-(2имидазолин-2-ил)пиридина формулы [1]. Сложный эфир 2-(2-имидазолин-2-ил)пиридина формулы [1], в которой А-COOR3 , R3 - алкил С1-С3, алкенил С 3-С12, 2-хлораллил, 2-пропинил, 1,1-диметил-2-пропинил, a Y, Z, R1 и R2 описаны выше, может быть преобразован в соответствующую гидроксаминовую кислоту по реакции с гидроксиламином при повышенном давлении и температуре от 25 до 125°С. Эта реакция может быть проведена в протонном растворителе, например, низшем алканоле, или в апротонном растворителе, таком как тетрагидрофуран, диоксан и т.п. Производные N-замещенного имидазолинона формулы [1], где В - COR4, W-O; R1, R2, R3 , Υ и Ζ - описаны выше, исключая случай, когда Υ и Ζ являются алкиламино, гидрокси или гидрокси - низшеалкилом, могут быть получены по реакции соответственно замещенного 2-(2-имидазолин-2-ил)пиридина избытком ацилгалогенида, ацилангидрида или сульфонилгалогенида как тактовым или в растворителе, например пиридине или толуоле при повышенной температуре от 50 до 125°С. Сложные эфиры формулы [1], в которой В - водород, W - кислород, A-COOR3, где R3 - алкил С1-С3, R1, R2, Υ и Ζ определены выше, могут быть получены по реакции соответствующей кислоты, т.е. когда А-СООН, с подходящим спиртом в присутствии каталитического количества сильной минеральной кислоты, такой как хлористоводородная кислота, серная кислота и т.п., при температуре от 50 до 100°С. Кислота формулы [1], описанная выше, в которой А - СООН, В - водород, W - кислород, a R1, R2, Υ и Z определены выше, также легко преобразуется в соответствующий метиловый эфир по реакции с диазометаном при температуре от 0 до 25°С, Полученный таким путем метиловый эфир может быть затем введен в реакцию с алкилатом щелочного металла, например алкилатом натрия или калия, для удобства показанным как R3ONa, и подходящим спиртом, представленным структурой R3OH, где R3-алкил С 1-С3, в случае необходимости замещенный фурилом, 2-хлораллидом. В еще одном варианте осуществления изобретения, соединения формулы [1], в которой А - COOR3 и R3 водород, a R1, R2, Υ и Ζ - определены выше, могут быть получены гидрогенолизом бензильного эфира имидазолинилпиридина, представленного формулой [ΧΥ], где R1, R 2, Υ и Ζ определены выше, с использованием палладиевого или платинового катализатора. В этой реакции бензиловый эфир формулы (XV) растворяют или диспергируют в органическом растворителе, например низшем спирте, простом эфире, таком как диоксан, тетрагидрофуран и т.п., толуоле или ксилоле. Катализатор, предпочтительно палладий на угле, добавляют к смеси и смесь нагревают до 20-25°С. Нагретую смесь затем обрабатывают газообразным водородом с получением целевой кислоты. В альтернативе, кислоты формулы [1], в которой А - СООН, могут быть получены обработкой водного раствора сложного эфира формулы [1] сильным основанием. На практике сложный эфир формулы [1] обычно обрабатывают одним эквивалентом основания в водном растворе и смесь нагревают до 20-50°С. Смесь затем охлаждают и доводят до рН 6,5-7,5, предпочтительно рН 7, добавлением сильной минеральной кислоты. Подобная обработка дает целевую кислоту. Кислоты формулы [1], в которой А -СООН, В - водород, W - кислород, a Y, Z, R1 и R2 указаны выше, могут быть получены по реакции соответственно замещенного имидазолинона с алкиллитием предпочтительно в присутствии инертного растворителя, такого как тетрагидрофуран, в атмосфере азота при температуре от -70 до -80°С. Полученную таким путем смесь затем обрабатывают гексатимелфосфорамидом и двуокисью углерода, предпочтительно, в инертном растворителе, например тетрагидрофуране, с получением целевого продукта. Соединения формулы [1], в которых А-COOR3 и R3 представляет собой солеобразующий катион, такой как щелочной металл, щелочноземельный металл, аммоний или алифатический аммоний, a R1, R2, Υ и Ζ описаны выше, могут быть получены растворением 2-(2-имидазолин-2-ил)пиридиновой кислоты формулы [1] в продходящем растворителе с последующей обработкой раствора кислоты одним эквивалентом солеобразующего катиона. Для получения соединений, в которых солеобразующим катионом является неорганическая соль, например, натрий, кальций, кислота формулы [1] может быть растворена или диспергирована в воде или низшем спирте или их смесях. Один эквивалент солеобразующего катиона обычно в виде гидроокиси, карбоната, бикарбоната и т.п., но предпочтительно в виде гидроокиси, смешивают с раствором кислоты формулы [1]. По прошествии нескольких минут, соединение формулы [1], в которой R 3 неорганический солеобразующий катион, как правило выпадает в осадок и может быть выделено из смеси либо фильтрацией, либо азеотропной дистилляцией с использованием органического растворителя, например диоксана. Для получения соединения формулы [1], в которой A-COOR3 и R3 - аммоний или органический аммоний, кислоту формулы [1] растворяют или диспергируют в органическом растворителе, например диоксан, тетрагидрофуран и т.п., и смесь обрабатывают одним эквивалентом аммиака, или амина или гидроокиси тетраалкиламмония. На практике спустя несколько минут соль аммония или органического аммония выпадает в осадок и может быть выделена любым известным методом, например фильтрованием или центрифугированием. Кроме того, реакционная смесь может быть концентрирована, остающийся растворитель удален гексаном, а остаток затем высушен для выделения аммониевой или органическоаммониевой соли формулы [1]. Многие из производных 2-(2-имидазолин-2-ил)-хинолина согласно изобретению могут быть получены по методикам, описанным выше для 2-(2-имидазолин-2-ил)-пиридиновых соединений формулы [1]. Например, сложные эфиры 2-{2-имидазолин-2-ил) хинолинкарбоновой кислоты формулы, где R3 - заместитель, отличный от водорода или солеобразующего катиона, а R1, R2, L, Μ, Q и R описаны выше, могут быть получены обработкой диона подходящим спиртом и алкилатом щелочного металла при температуре от 20 до 50°С. В этих реакциях, как и в аналогичных реакциях получения пиридинов формулы [1], спирт выполняет функцию как реагента, так и растворителя. Как таковой вторичный растворитель не требуется, но в случае необходимости он может использоваться. При использовании вторичного растворителя предпочтительно употребление апротонного растворителя, такого как тетрагидрофуран или диоксан. Сложные эфиры 2-{2-имидазолин-2-ил)-хинолин-карбоновой кислоты также могут быть получены из ацетамида диоксипирролохинолина, где R1, R2, L, Μ, Q и R описаны выше, их циклизацией сильным основанием, например 1,5-диазабицикло (5, 4,0) ундец-5-еном (ДБУ) в присутствии инертного органического растворителя, например ксилол или толуол, с получением сырого имидазопирролохинолиндиона; Реакционную смесь нагревают до 100-150°С и воду отделяют от реакционной смеси с применением водоотделителя Дина-Старка. Затем к реакционной смеси добавляют минимум один эквивалент спирта R3OH, где R 3 - выше описанный заместитель, но с исключением водорода и солеобразующи х катионов, и таким путем полученную смесь нагревают до кипения с обратным холодильником при 100-150°С с получением сложного эфира. Сложные эфиры 2-(2-имидазолин-2-ил)хинолинкарбоновой кислоты могут быть также получены циклизацией сложного эфира карбамоилхинолинкарбоновой кислоты с помощью пятихлористого фосфора при повышенной температуре от 60 до 100°С. Реакцию обычно проводят в присутствии инертного, органического растворителя, например толуола или бензола, с получением хлористоводородной соли сложного эфира 2-(2-имидазолин-2-ил)хинолинкарбоновой кислоты. Обработка полученной таким образом галоидоводородной соли основанием, например карбонатом натрия или калия, дает тогда сложный эфир 2{2-имидазолин-2-ил)хинолинкарбоновой кислоты. Сложные эфиры 2-(2-имидазолин-2-ил)хинолинкарбоновой кислоты образуются также циклизацией сложных эфиров карбамоилхинолинкарбоновой кислоты. Циклизация сложного эфира карбамоилхинолинкарбоновой кислоты обеспечивается его реагированием со смесью пятихлористого фосфора и оксихлорида фосфора. Реакционную смесь перемешивают несколько часов при температуре от 15 до 35°С и РОСІ3 затем отгоняют в вакууме. Остаток от этой обработки диспергируют в органическом растворителе, например толуоле. Затем растворитель отделяют от результирующей смеси и остаток диспергируют в воде, нагреваемой до 80-100°С. После охлаждения рΗ водной смеси доводят до 5-6 добавлением бикарбоната натрия или калия и продукт экстрагируют в метиленхлорид с получением сложного эфира 2-(2-имидазолин-2-ил)хинолинкарбоновой кислоты. Хинолиновый эфир, в котором R3 соответствует приведенным определениям, но с исключением водорода или солеобразующих катионов, a R1, R2. L, Μ, Q и R описаны выше, легко преобразуют в соответствующую соль присоединения кислоты по реакции указанного сложного эфира с минимум одним эквивалентом сильной кислоты. Используя сильные минеральные кислоты, такие как хлористоводородная кислота, серная кислота и бромистоводородная кислота, хотя могут применяться также и органические кислоты. На практике оказалось, что реакция протекает наиболее удовлетворительно в присутствии инертного органического растворителя, например эфира, хлороформа, метиленхлорида или их смесей, сернокислотные соли получают как правило по данной методике, но с заменой упомянутых растворителей низшим алифатическим спиртом. Получение производных 2-(2-имидазолин-2-ил)хинолина, в которой А - СООН, В - водород, W - кислород, a R1, R2, L, Μ, Q и R имеют приведенные выше определения при условии, что L, М, Q и R не являются галогеном, может быть осуществлено гидрогенолизом бензилового эфира 2-(2-имидазолин-2ил)хинолинкарбоновой кислоты. Реакция предполагает диспергирование бензилового эфира в органическом растворителе и обработку полученной таким путем реакционной смеси газообразным водородом в присутствии катализатора, такого как палладий или платина на угле-носителе. Гидрогенолиз обычно проводят при температуре от 20 до 50°С. Получение производных 2-(2-имидазолин-2-ил)хинолина формулы, в которых А-COOR3 , R3 солеобразующий катион, В - водоррд, W - кислород, a R1, R2, L, Μ, Q и R определены выше, может быть осуществлено растворением кислоты в подходящем растворителе и обработкой полученной таким путем смеси минимум одним эквивалентом солеобразующего катиона. Реакция по существу идентична описанной для получения пиридинов формулы [1], в которой А -COOR 3, a R 3 - солеобразующий катион. Следует иметь также в виду, что имидазолинилхинолинкарбоновые кислоты и их сложные эфиры, представленные формулой [II], в которой В - Н, могут быть таутомерными. Следует также иметь в виду, что когда R 1 и R2 представляют собой разные заместители на производных 2-{2-имидазолин-2-ил)хинолина и имидазопирролохинолиндионахуглерод, к которому присоединены R1 и R2, является асимметрическим центром и продукты (а также их промежуточные продукты) существуют в d- и Iформах, а также dl-фррмах. Пример 1. Получение метил-2-(5-изопропил-5-метил-4-оксо-2-имидазолин-2-ил)-никотината (соединение№27). К 20 мл сухого метанола, в котором реагирует 10 г гидрида натрия добавляют 2 г смеси имидазопирролопиридинов. После перемешивания, продолжающегося в течение 16 ч, добавляют 0,03 г ледяной уксусной кислоты (для нейтрализации основания), раствор концентрируют под вакуумом и остаток хроматографируют из раствора в эфире на силикагеле. Соединение, выходящее с более высокой скоростью (целевой эфир), получают в нескольких фракциях, объединяют, концентрируют и кристаллизуют из ацетонитрила, получая при этом имидазолинилникотинат, имеющий т.пп. 121-123°С. Аналитически чистый образец, полученный перекристаллизацией смеси из хлористого метилена с гексаном, имеет т.пл. 121-122°с. Пример 2. Получение метил-2-{5-изопропил-5-метил-4-оксо-2-имидазолин-ил)-никотинат. Смесь 25 г амида и 1 мл 1,5-диазабицикло-(5,4,0)ундец-5-ена (ДБУ) в 500 мл ксилола кипятят с обратным холодильником в течение 1 ч с ловушкой воды Дина-Старка. Смесь несколько охлаждают; ловушк у воды удаляют, добавляют 100 мл безводного метанола и смесь кипятят с обратным холодильником в течение 1 ч. Затем под вакуумом удаляют растворители, продукт выделяют хроматографически так, как описано выше, и получают 13,65 г продукта, имеющего т.пл. 120-122°С и идентичного продукту, полученному в примере 1. Пример 3. Получение метил-2-(5-изопропил-5-метил-4-оксо-2-имидазолин-2-ил) никотината. Методика А. Смесь 13,65 г никотината и 9,69 г пяти-хлористого фосфора в 110 мл сухого толуола нагревают при перемешивании при 80°С. Через 1,5 ч вязкую смесь охлаждают, фильтруют, твердое соединение промывают эфиром и суша т. Это хлористоводородная соль целевого продукта. Эту соль растворяют в 60 мл воды; раствор нейтрализуют бикарбонатом натрия, результирующий осадок удаляют фильтрованием, промывают водой, сушат на воздухе и получают продукт, идентичный продукту, полученному по примеру 1. Методика В. Смесь 5 г никотината и 7,1 г пятихлористого фосфора в 40 мл оксихлорида фосфора перемешивают при комнатной температуре в течение ночи. Оксихлорид фосфора удаляют под вакуумом, остаток суспендируют в 40 мл толуола и снова концентрируют. Э ту операцию повторяют. К остатку добавляют 40 мл воды, смесь нагревают и кипятят с обратным холодильником в течение 1 ч. После охлаждения смесь экстрагируют хлористым метиленом, экстракт сушат, концентрируют и получают 1,05 г целевого продукта. рН водной фазы, оставшейся после экстракции хлористым метиленом, доводят до 5-6 раствором бикарбоната натрия и смесь снова экстрагируют хлористым метиленом. Сухой экстракт концентрируют, остаток кристаллизуют и получают дополнительно 2,65 г целевого продукта, идентичного продукту, описанному в примере 1. По одной или больше из вышеописанных методик получают используемые эфиры никотиновой кислоты. Пример 4. Получение этил-2-(5-изопропил-5-метил-4-оксо-2-имидазолин-2-ил)-3-хинолинкарбоновой кислоты (соединение №44). Методика А. К 2-изопропил-2-метил-5-Н-имида-зо(1’,2':1,2)пиразоло(3,4-хинолин-3Н/2Н),5-диону (2 г, 0,0068 моль) в абсолютированном этаноле (40 мл) в атмосфере азота прибавляют 50%-й гидрид натрия (0,34 г, 0,00716 моль) при охлаждении льдом. Наблюдается выделение газа. Через 10 мин реакционную смесь нейтрализуют водным раствором хлорида аммония, отгоняют и распределяют в делительной воронке между водой и этилацетатом. Органический слой отделяют, суша т безводным сульфатом магния, фильтруют, отгоняют, остаток перекристаллизовывают из смеси этилацетатгексан и получают 1,38 г (60%) белого твердого соединения с т.пл. 146-147,5°С. Таким же образом (по методике А) можно получить эфиры. Пример 5. Получение натриевой соли 2-(5-изопропил-5-метил-4-оксо-2-имидазолин-2-ил)-3хинолинкарбоновой кислоты (соединение № 42). Раствор 2-(5-изопропил-5-метил-4-оксо-2-имидазолин-2-ил)-3-хинолинкарбоновой кислоты (2,33 г, 0,0075 моль) в воде (22 мл), содержащей гидроокись натрия (0,3 г, 0,0075 моль), перемешивают при комнатной температуре в течение ночи, промывают хлористым метиленом, водный слой отделяют, выпаривают до оранжевого твердого соединения, которое промывают эфиром и сушат на воздухе. Получают дигидрат продукта в виде твердого соединения кремового цвета, т.пл. 235-250°С (с разложением). Данные анализа рассчитано для C17H16N3O 3Na+2H2O: С 55,27; Η 5,45; N 11,37; Na 6,22. Найдено: С 55,56; Η 5,31; N 11,35. Na 6,30. Пример 6. Оценка послевсходового гербицидного эффекта испытуемых соединений. Послевсходовую гербицидную активность соединений по настоящему изобретению демонстрируют с помощью нижеследующи х испытаний, в которых множество однодольных и двудольных растений обрабатывают испытуемыми соединениями, диспергированными в водно-ацетоновых смесях. В испытаниях проростки растений выращивают во временных плоских ящиках на протяжении двух недель. Испытуемые соединения диспергируют в смесях 50/50 ацетон/вода, содержащих 0,5% "Твина 20" (полиоксиэтиленсорбитанмонолауратного поверхностно-активного вещества), в количестве, достаточном для обеспечения эквивалента приблизительно от 0,032 до 1 кг/га активного соединения при нанесении на растения через распылительное сопло, работающее под давлением 40 фунт/кв.дюйм (2,81 кгс/см 2) на протяжении предопределенного времени. После распыления, растения помещают на полки теплицы и выдерживают там обычным способом, принятым для содержания растений в теплицах. Спустя 4-5 недель после обработки проростки растений осматривают и проставляют оценки в соответствии с приведенной ниже системой. Полученные данные представлены в табл. 1. 4 -аномальный рост, т.е. выраженное физиологическое нарушение роста или деформации, но при общем эффекте меньшей силы для отнесения к группе 5 по шкале оценивания., В большинстве случаев данные представлены для одиночного испытания, для некоторых случаев они представляют собой усредненные значения, полученные более, чем в одном испытании. Пример 7. Оценка довсходового гербицидного эффекта испытуемых соединений. Довсходовая гербицидная активность соединений проиллюстрирована следующими испытаниями, в которых семена различных однодольных и двудольных растений отдельно смешивают с горшочной почвой и высаживают приблизительно на 1 дюйм от поверхности почвы в отдельных емкостях на 1 винт. После высаживания емкости опыляют выбранными водными растворами ацетона, содержащими испытуемые соединения в количестве, достаточном для обеспечения эквивалента, примерно 0,032-1 кг/га. Обработанные емкости затем помещают на стеллажи в теплице, поливают водой и ухаживают в соответствии с общепринятой процедурой для теплиц. После 4-5 недель после обработки испытания заканчивают и каждую емкость осматривают и оценивают в соответствии с системой оценки, упомянутой выше. Результаты испытаний приведены в табл. 2. Пример 8. Оценка действия испытуемых соединений в качестве водных гербицидов с использованием водяного пациента Elchhomia cressipes в качестве вида растений. В этих испытаниях заливные участки, имеющие сформировавшиеся популяции водяного гиацинта с высаживанием 5 деток за одиннадцать месяцев до оценки действия соединений, опрыскивали испытуемым раствором с расходом 333 л/га, содержащим 0,5 мас.% ПАВ и достаточное количество испытуемого соединения для обеспечения 0,125-1,0 кг/га указанного соединения. Спустя 44 дня после послевсходовой обработки подопытные заливные участки обследовали. Данные спектроскопии для соединений. Фур фурил-5-этил-2-(5-изопропил-5-метил-4-оксо-2-имидазолин-2-ил)никотинат (соединение 40), Метил-5-изопропил-2-{5-изопропил-5-метил-4-оксо-2-имидазолин-2-ил)никотинат: (соединение 32). Метил-2-(5-изопропил-5'-метил-4-оксо -2-имидазолин-2-ил)-5-пропил-никотинат (соединение 29). 5-Изопропил-5-метил-2[3-(2-оксазолин-2-ил)-2-пиридил]-2-имидазолин-4-он: (соединение 12). 78). Метил-2-{1-ацетил-4-изопропил-4-метил-5-оксо-2-имидазолин-2-ил)-3-хинолинкарбоксилат (соединение
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod to control undesirable vegetation
Автори англійськоюMARINUS LOS
Назва патенту російськоюСпособ борьбы с нежелательной растительностью
Автори російськоюМаринус Лос
МПК / Мітки
МПК: A01P 13/00, A01N 43/50, A01N 43/40, A01N 43/42
Мітки: боротьби, спосіб, рослинністю, небажаною
Код посилання
<a href="https://ua.patents.su/43-19159-sposib-borotbi-z-nebazhanoyu-roslinnistyu.html" target="_blank" rel="follow" title="База патентів України">Спосіб боротьби з небажаною рослинністю</a>
Попередній патент: Машина для розподілу та ущільнення щебеневої баластної призми залізничної колії, яка безперервно переміщується
Наступний патент: Машина для подовжнього контактного роликового зварювання корпусів банок
Випадковий патент: Механізм подання гірничої машини