N-метиламінометилізоіндольні сполуки, композиції, що їх включають, і способи їх застосування
Формула / Реферат
1. Сполука формули (І):
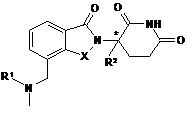 (I)
(I)
або її фармацевтично прийнятна сіль, сольват або стереоізомер, де:
* означає хіральний центр;
X являє собою СН2 або С=О;
R1 являє собою Н, (С1-С8)алкіл, (С3-С7)циклоалкіл, (С2-С8)алкеніл, (С2-С8)алкініл, бензил, арил, (С0-С4)алкіл-(С1-С6)гетероциклоалкіл, (С0-С4)алкіл-(С2-С9)гетероарил, C(O)R3, C(S)R3, C(O)OR4, (С1-С8)алкіл-N(R6)2, (C1-C8)aлкiл-OR5, (С1-С8)алкіл-С(О)OR5, C(O)NHR3, C(S)NHR3, C(O)NR3R3', C(S)NR3R3' або (С1-С8)алкіл-O-(CO)R5;
R2 являє собою Н, СН3 або (С2-С8)алкіл;
R3 і R3' представляють незалежно
(С1-С8)алкіл;
(С3-С7)циклоалкіл;
(С2-С8)алкеніл;
(С2-С8)алкініл;
бензил;
(С0-С4)алкіл-(С5-С10)арил, необов'язково заміщений одним або декількома з:
(С1-С6)алкілу, зазначеного алкілу, необов'язково заміщеного одним або декількома галогенами,
(С1-С6)алкокси, зазначеного алкокси, необов'язково заміщеного одним або декількома галогенами,
SCY3, де Y являє собою водень або галоген,
NZ2, де Z являє собою водень або (С1-С6)алкіл,
(С1-С6)алкілендіокси або
галоген;
(С0-С4)алкіл-(С1-С6)гетероциклоалкіл;
(С0-С4)алкіл-(С2-С9)гетероарил;
(C0-C8)алкіл-N(R6)2;
(С1-С8)алкіл-ОR5;
(С1-С8)алкіл-С(О)OR5;
(С1-С8)алкіл-О(СО)R5 або
C(O)OR5;
R4 являє собою (С1-С8)алкіл, (С2-С8)алкеніл, (С2-С8)алкініл, (С1-С4)алкіл-ОR5, бензил, арил, (С0-С4)алкіл-(С1-С8)гетероциклоалкіл або (С0-С4)алкіл-(С2-С9)гетероарил;
R5 являє собою (С1-С8)алкіл, (С2-С8)алкеніл, (С2-С8)алкініл, бензил, (С5-С10)арил або (С2-С9)гетероарил;
у кожному випадку R6 являє собою незалежно Н, (С1-С8)алкіл, (С2-С8)алкеніл, (С2-С8)алкініл, бензил, (С5-С10)арил, (С2-С9)гетероарил або (С0-С8)алкіл-С(О)О-R5, або
дві R6 групи можуть з'єднуватися для утворення гетероциклоалкільної групи.
2. Сполука за п. 1, яка має структуру формули (II):
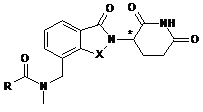 , (II)
, (II)
або її фармацевтично прийнятна сіль, сольват або стереоізомер, де:
* означає хіральний центр;
X являє собою СН2 або С=О;
R являє собою (С1-С6)алкіл; (С1-С6)алкокси; аміно; (С1-С6)алкіламіно; діалкіламіно, де кожна з алкільних груп являє собою незалежно (С1-С6)алкіл; (С0-С4)алкіл-(С6-С10)арил, необов'язково заміщений одним або більше (С1-С6)алкілом, (С1-С6)алкокси або галогеном; 5-10-членний гетероарил, необов'язково заміщений одним або більше (С1-С6)алкілом; -NHR' або (C0-C8)алкіл-N(R")2;
R' являє собою: (С1-С6)алкіл;
(С0-С4)алкіл-(С6-С10)арил, необов'язково заміщений одним або більше:
(С1-С6)алкілом, зазначеним алкілом, необов'язково заміщеним одним або більше галогеном,
(С1-С6)алкокси, зазначеним алкокси, необов'язково заміщеним одним або більше галогеном,
(С1-С6)алкілендіокси або
галоген; або
5-10-членний гетероарил, необов'язково заміщений одним або більше (С1-С6)алкілом; і в кожному випадку R" являє собою незалежно Н, (С1-С8)алкіл, (С2-С8)алкеніл, (С2-С8)алкініл, бензил, (С6-С10)арил, 5-10-членний гетероарил або (С0-С8)алкіл-С(О)О-(С1-С8)алкіл.
3. Сполука за п. 2, де X являє собою С=O.
4. Сполука за п. 2, де R являє собою метил або етил.
5. Сполука за п. 2, де R являє собою NHR', і де R' являє собою (С6-С10)арил, необов'язково заміщений одним або більше (С1-С6)алкілом або (С1-С6)алкокси.
6. Сполука за п. 5, де зазначений алкіл або алкокси заміщений одним або більше галогеном.
7. Сполука за п. 2, де R являє собою 5-10-членний гетероарил.
8. Сполука за п. 2, де X являє собою СН2.
9. Сполука за п. 8, де R являє собою метил або етил.
10. Сполука за п. 2 або 7, де R являє собою NHR', і де R' являє собою (С6-С10)арил, необов'язково заміщений одним або більше (С1-С6)алкілом, (С1-С6)алкокси або галогеном.
11. Сполука за п. 10, де R' являє собою феніл, необов'язково заміщений одним або більше метилом, метокси, трифторметилом або хлоридом.
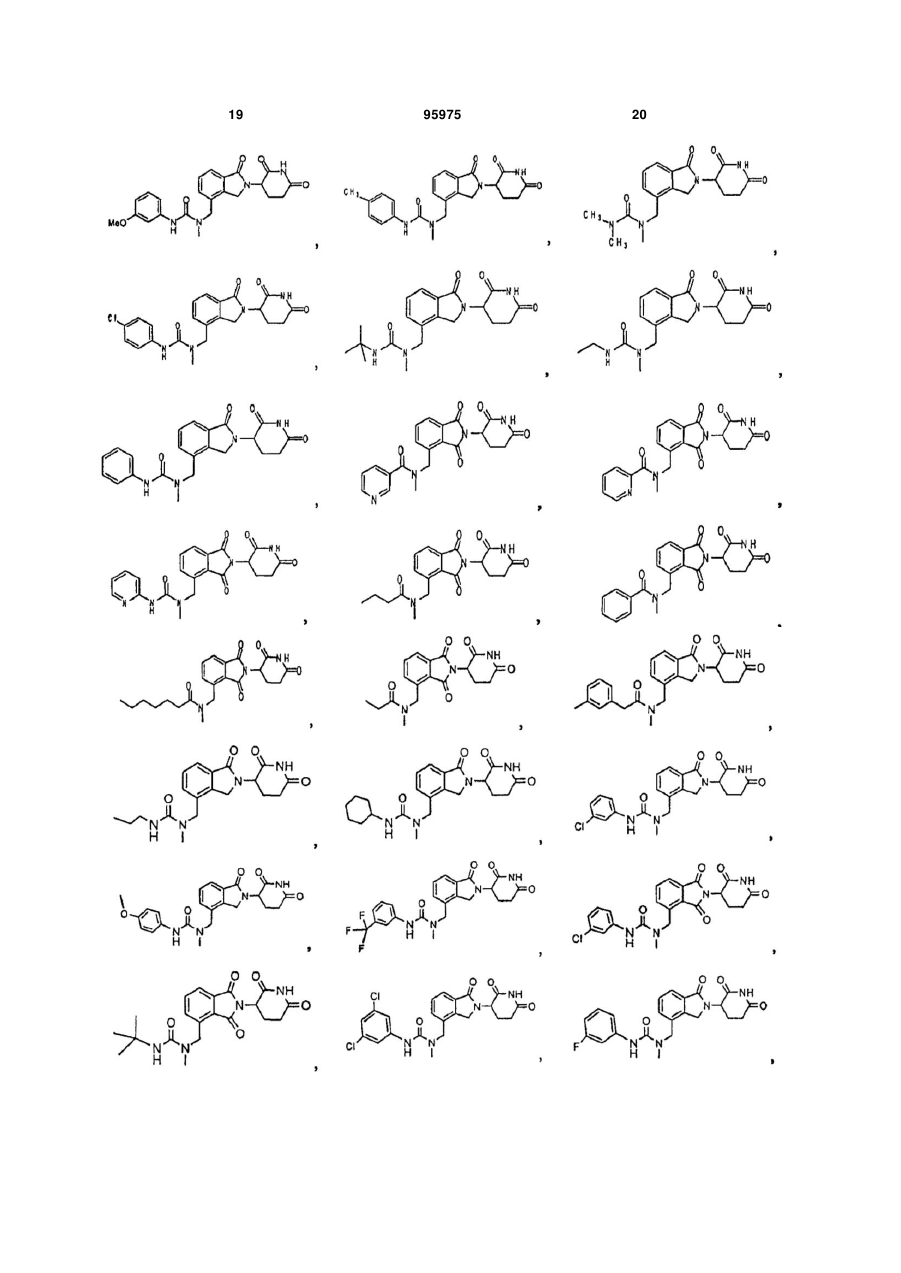
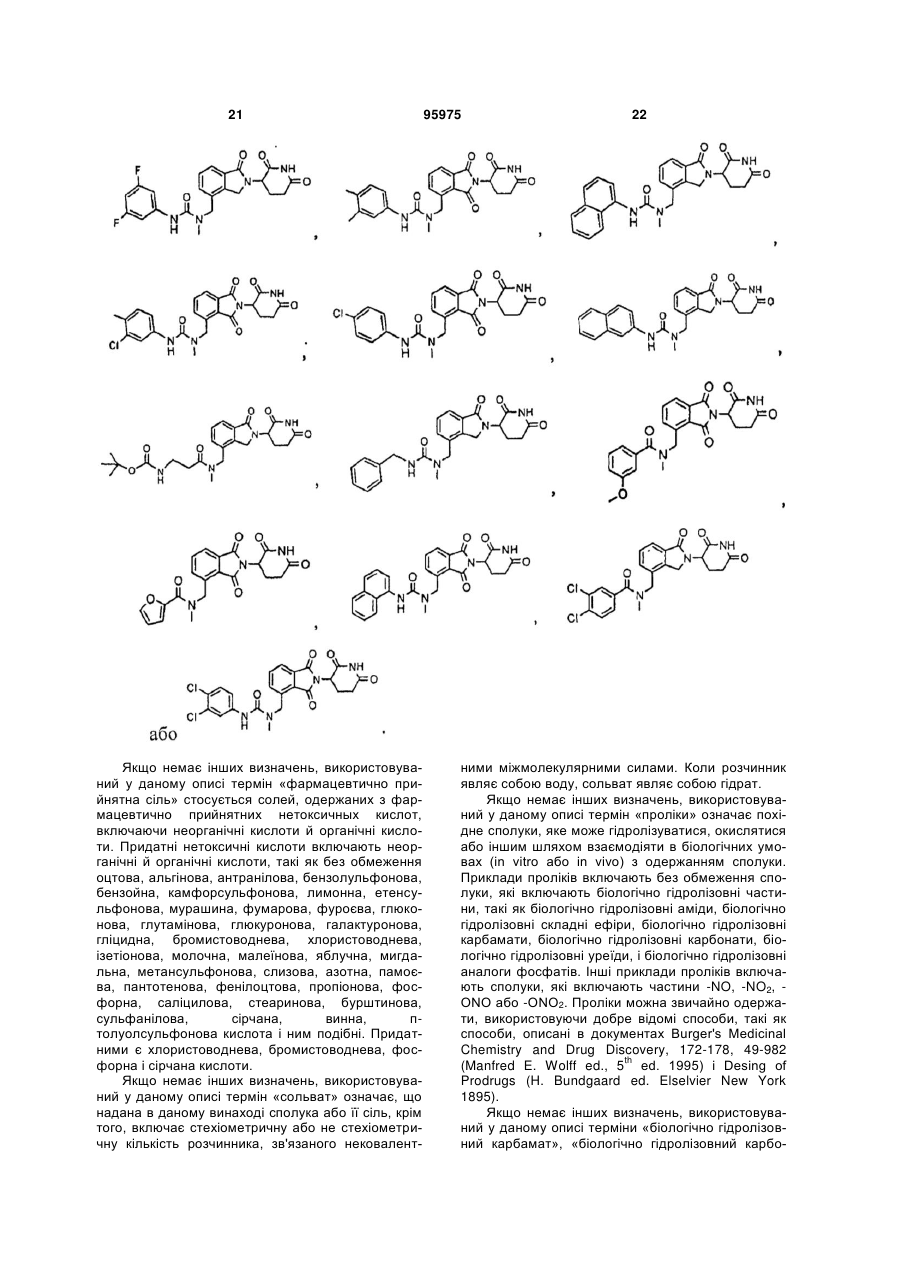
12. Сполука за п. 2 або її фармацевтично прийнятна сіль, сольват або стереоізомер, де сполука являє собою:
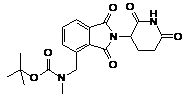 ,
,
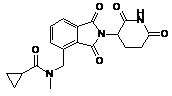 ,
,
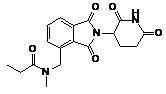 ,
,
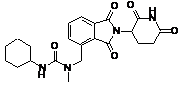 ,
,
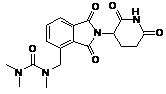 ,
,
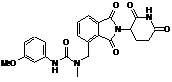 ,
,
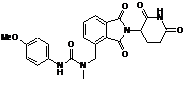 ,
,
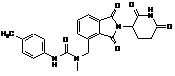 ,
,
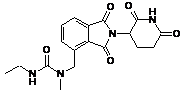 ,
,
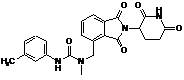 ,
,
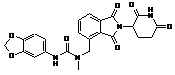 ,
,
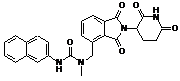 ,
,
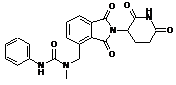 ,
,
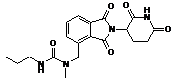 ,
,
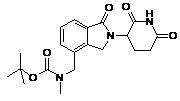 ,
,
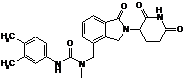 ,
,
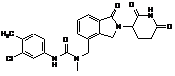 ,
,
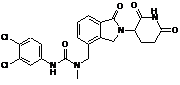 ,
,
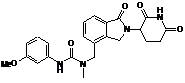 ,
,
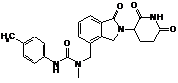 ,
,
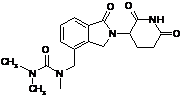 ,
,
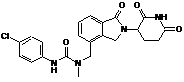 ,
,
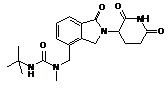 ,
,
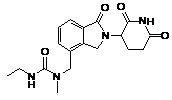 ,
,
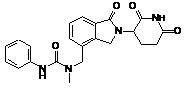 ,
,
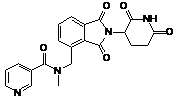 ,
,
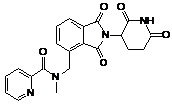 ,
,
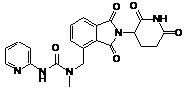 ,
,
,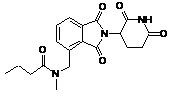 ,
,
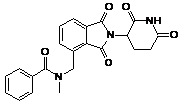 ,
,
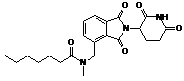 ,
,
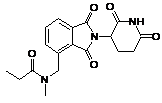 ,
,
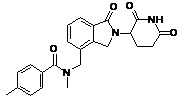 ,
,
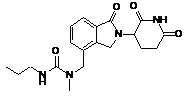 ,
,
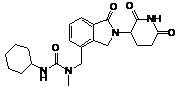 ,
,
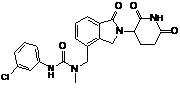 ,
,
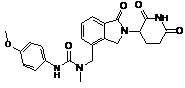 ,
,
 ,
,
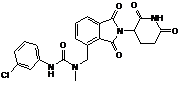 ,
,
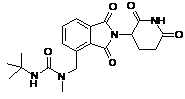 ,
,
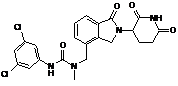 ,
,
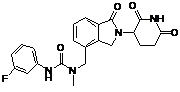 ,
,
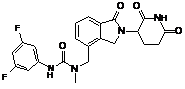 ,
,
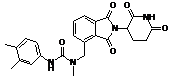 ,
,
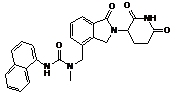 ,
,
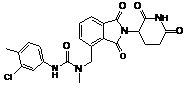 ,
,
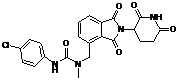 ,
,
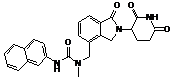 ,
,
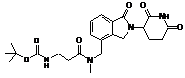 ,
,
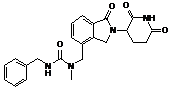 ,
,
 ,
,
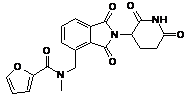 ,
,
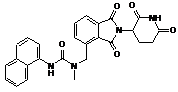 ,
,
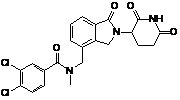
або 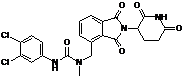 .
.
13. Фармацевтична композиція, яка включає сполуку за п. 1.
14. Спосіб лікування, ведення пацієнта або профілактики захворювання або розладу, який включає введення пацієнту, що потребує такого лікування, ведення або профілактики, терапевтично або профілактично ефективної кількості сполуки за п. 1, де захворювання або розлад являє собою рак, розлад, пов'язаний з ангіогенезом, біль, дегенерацію жовтої плями або пов'язаний з нею синдром, захворювання шкіри, легеневий розлад, розлад, пов'язаний із впливом азбесту, паразитарне захворювання, імунодефіцитний розлад, розлад ЦНС, травму ЦНС, атеросклероз або пов'язаний з ним розлад; функціональне порушення сну або пов'язаний з ним розлад, гемоглобінопатію або пов'язаний з нею розлад або розлад, пов'язаний з TNF-a.
15. Спосіб за п. 14, де захворювання являє собою рак.
16. Спосіб за п. 15, де рак являє собою гематологічний або солідний рак.
17. Спосіб за п. 14, який, крім того, включає введення одного або декількох додаткових активних засобів.
18. Спосіб за п. 14, де сполука або її фармацевтично прийнятна сіль, сольват або стереоізомер вводяться перорально або парентерально.
19. Стандартна лікарська форма, яка включає сполуку за п. 1.
20. Стандартна лікарська форма за п. 19, яка придатна для перорального або парентерального введення.
21. Стандартна лікарська форма за п. 20, яка придатна для перорального введення.
22. Стандартна лікарська форма за п. 21, яка являє собою таблетку або капсулу.
Текст
УКРАЇНА (19) UA (11) 95975 (13) C2 (51) МПК (2011.01) A61K 31/4035 (2006.01) C07D 401/04 (2006.01) C07D 401/14 (2006.01) C07D 405/14 (2006.01) A61P 35/00 A61K 31/4439 (2006.01) ДЕРЖАВНА СЛУЖБА ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ УКРАЇНИ ОПИС ДО ПАТЕНТУ НА ВИНАХІД (54) N-МЕТИЛАМІНОМЕТИЛІЗОІНДОЛЬНІ СПОЛУКИ, КОМПОЗИЦІЇ, ЩО ЇХ ВКЛЮЧАЮТЬ, І СПОСОБИ ЇХ ЗАСТОСУВАННЯ 2 N * NH X O R2 R1 N (I) або її фармацевтично прийнятна сіль, сольват або стереоізомер, де: * означає хіральний центр; X являє собою СН2 або С=О; 1 R являє собою Н, (С1-С8)алкіл, (С3-С7)циклоалкіл, (С2-С8)алкеніл, (С2-С8)алкініл, бензил, арил, (С0С4)алкіл-(С1-С6)гетероциклоалкіл, (С0-С4)алкіл-(С23 3 4 С9)гетероарил, C(O)R , C(S)R , C(O)OR , (С16 5 С8)алкіл-N(R )2, (C1-C8)aлкiл-OR , (С1-С8)алкіл 3' C2 3 (13) 3 95975 O 3 (11) O 5 С(О)OR , C(O)NHR , C(S)NHR , C(O)NR R , 3 3' 5 C(S)NR R або (С1-С8)алкіл-O-(CO)R ; 2 R являє собою Н, СН3 або (С2-С8)алкіл; 3 3' R і R представляють незалежно (С1-С8)алкіл; (С3-С7)циклоалкіл; (С2-С8)алкеніл; (С2-С8)алкініл; бензил; (С0-С4)алкіл-(С5-С10)арил, необов'язково заміщений одним або декількома з: (С1-С6)алкілу, зазначеного алкілу, необов'язково заміщеного одним або декількома галогенами, (С1-С6)алкокси, зазначеного алкокси, необов'язково заміщеного одним або декількома галогенами, SCY3, де Y являє собою водень або галоген, NZ2, де Z являє собою водень або (С1-С6)алкіл, (С1-С6)алкілендіокси або галоген; (С0-С4)алкіл-(С1-С6)гетероциклоалкіл; (С0-С4)алкіл-(С2-С9)гетероарил; 6 (C0-C8)алкіл-N(R )2; 5 (С1-С8)алкіл-ОR ; 5 (С1-С8)алкіл-С(О)OR ; 5 (С1-С8)алкіл-О(СО)R або 5 C(O)OR ; 4 R являє собою (С1-С8)алкіл, (С2-С8)алкеніл, (С25 С8)алкініл, (С1-С4)алкіл-ОR , бензил, арил, (С0С4)алкіл-(С1-С8)гетероциклоалкіл або (С0-С4)алкіл(С2-С9)гетероарил; 5 R являє собою (С1-С8)алкіл, (С2-С8)алкеніл, (С2С8)алкініл, бензил, (С5-С10)арил або (С2С9)гетероарил; 6 у кожному випадку R являє собою незалежно Н, (С1-С8)алкіл, (С2-С8)алкеніл, (С2-С8)алкініл, бензил, (С5-С10)арил, (С2-С9)гетероарил або (С0-С8)алкіл5 С(О)О-R , або 6 дві R групи можуть з'єднуватися для утворення гетероциклоалкільної групи. 2. Сполука за п. 1, яка має структуру формули (II): UA (21) a200903664 (22) 14.09.2007 (24) 26.09.2011 (86) PCT/US2007/020201, 14.09.2007 (31) 60/845,227 (32) 15.09.2006 (33) US (46) 26.09.2011, Бюл.№ 18, 2011 р. (72) МЮЛЛЕР ДЖОРДЖ В., US, ЧЕН РОДЖЕР С.К., US (73) СЕЛДЖИН КОРПОРЕЙШН, US (56) WO02059106 A 01.08.2002 US2005143344 A1 30.06.2005 BOGER D L ET AL: "TWO COMPARISONS OF THE PERFORMANCE OF POSITIONAL SCANNING AND DELETION SYNTHESIS FOR THE IDENTIFICATION OF ACTIVE CONSTITUENTS INMIXTURE COMBINATORIAL LIBRARIES" JOURNAL OF ORGANIC CHEMISTRY, AMERICAN CHEMICAL SOCIETY. EASTON, US, vol. 65, no. 5, 2000, pages 1467-1474, XP000915282 ISSN: 0022-3263 (57) 1. Сполука формули (І): (19) 1 3 95975 5-10-членний гетероарил, необов'язково заміщений одним або більше (С1-С6)алкілом; і в кожному випадку R" являє собою незалежно Н, (С1С8)алкіл, (С2-С8)алкеніл, (С2-С8)алкініл, бензил, (С6-С10)арил, 5-10-членний гетероарил або (С0С8)алкіл-С(О)О-(С1-С8)алкіл. 3. Сполука за п. 2, де X являє собою С=O. 4. Сполука за п. 2, де R являє собою метил або етил. 5. Сполука за п. 2, де R являє собою NHR', і де R' являє собою (С6-С10)арил, необов'язково заміщений одним або більше (С1-С6)алкілом або (С1С6)алкокси. 6. Сполука за п. 5, де зазначений алкіл або алкокси заміщений одним або більше галогеном. 7. Сполука за п. 2, де R являє собою 5-10-членний гетероарил. 8. Сполука за п. 2, де X являє собою СН2. 9. Сполука за п. 8, де R являє собою метил або етил. 10. Сполука за п. 2 або 7, де R являє собою NHR', і де R' являє собою (С6-С10)арил, необов'язково заміщений одним або більше (С1-С6)алкілом, (С1С6)алкокси або галогеном. 11. Сполука за п. 10, де R' являє собою феніл, необов'язково заміщений одним або більше метилом, метокси, трифторметилом або хлоридом. 12. Сполука за п. 2 або її фармацевтично прийнятна сіль, сольват або стереоізомер, де сполука являє собою: O O NH * N O X O R N , (II) або її фармацевтично прийнятна сіль, сольват або стереоізомер, де: * означає хіральний центр; X являє собою СН2 або С=О; R являє собою (С1-С6)алкіл; (С1-С6)алкокси; аміно; (С1-С6)алкіламіно; діалкіламіно, де кожна з алкільних груп являє собою незалежно (С1-С6)алкіл; (С0С4)алкіл-(С6-С10)арил, необов'язково заміщений одним або більше (С1-С6)алкілом, (С1-С6)алкокси або галогеном; 5-10-членний гетероарил, необов'язково заміщений одним або більше (С1С6)алкілом; -NHR' або (C0-C8)алкіл-N(R")2; R' являє собою: (С1-С6)алкіл; (С0-С4)алкіл-(С6-С10)арил, необов'язково заміщений одним або більше: (С1-С6)алкілом, зазначеним алкілом, необов'язково заміщеним одним або більше галогеном, (С1-С6)алкокси, зазначеним алкокси, необов'язково заміщеним одним або більше галогеном, (С1-С6)алкілендіокси або галоген; або O O H N O N O O O H N N O O N , , O O O , H N O N O O O N O N Me O , N H , N , O O O O H N N Me O O O N H , N O O N N H N O , O H N N O , N H H N O O O O N O O O O H3 C O N H , O O O O N H N O H N N O O N O H N O O N H O N H3 C O H N N O O O O N O N H O H N N O O N O H N O O N O N O O O 4 N , N H N , 5 95975 6 O O O O N O H N O O O O O N H O N N H , O O H3 C N , , O O O O O N H N N H3 C O N H O N H N N O N H , Cl N O O N H , N , O N NH O N N H3 C O N H NH O O H N O N H , O O O N O O O Cl H N N Cl O Me O H N N N O H3 C O O H NCH3 N N N CH3 , , O O O O O O NH NH NH N Cl N O O N H N N H N , N , , O O NH NH NH N N O N O O O O N N N N N , O O O N H O O O O O O O O N H N , , O O O O O O NH NH NH N N O O N N N , , , , O O O N NH O NH O O O O N N N , , O O NH , O O NH O N O N H N O O O N O O NH O N O O O O O N H O O O N N NH O N O N N H , O O O N , Cl N H N , 7 95975 O O 8 N O O N O N O N N H F , N F N H Cl , N , O O O O O NH N Cl NH N O N O O N , Cl N H N , N H F N , O O O NH O O NH N N NH O N O O O N N H N H , N O O NH O NH N O O N O Cl O N H , O O NH N N , O O Cl O O O N H F O O O F O NH O O O O O F N H NH NH O N H O O O O NH O O O N N H , N N H , N , O O NH O O N NH N O O N O O O O O O O NH O O N N H N H N N O , , O O O NH N , O O NH NH O N O N O O O N H N O O O O O Cl N , , N Cl або O O NH N Cl O O O Cl N H N . 13. Фармацевтична композиція, яка включає сполуку за п. 1. 14. Спосіб лікування, ведення пацієнта або профілактики захворювання або розладу, який включає введення пацієнту, що потребує такого лікування, ведення або профілактики, терапевтично або профілактично ефективної кількості сполуки за п. 1, де захворювання або розлад являє собою рак, розлад, пов'язаний з ангіогенезом, біль, дегенерацію жовтої плями або пов'язаний з нею синдром, захворювання шкіри, легеневий розлад, розлад, пов'язаний із впливом азбесту, паразитарне за хворювання, імунодефіцитний розлад, розлад ЦНС, травму ЦНС, атеросклероз або пов'язаний з ним розлад; функціональне порушення сну або пов'язаний з ним розлад, гемоглобінопатію або пов'язаний з нею розлад або розлад, пов'язаний з TNF-. 15. Спосіб за п. 14, де захворювання являє собою рак. 16. Спосіб за п. 15, де рак являє собою гематологічний або солідний рак. 9 95975 10 17. Спосіб за п. 14, який, крім того, включає введення одного або декількох додаткових активних засобів. 18. Спосіб за п. 14, де сполука або її фармацевтично прийнятна сіль, сольват або стереоізомер вводяться перорально або парентерально. 19. Стандартна лікарська форма, яка включає сполуку за п. 1. 20. Стандартна лікарська форма за п. 19, яка придатна для перорального або парентерального введення. 21. Стандартна лікарська форма за п. 20, яка придатна для перорального введення. 22. Стандартна лікарська форма за п. 21, яка являє собою таблетку або капсулу. Дана заявка вимагає пріоритет тимчасової заявки на патент US 60/845227, поданої 15 вересня 2006 p., повністю включеної в даний опис як посилання. 1. Галузь, до якої належить винахід Даний винахід стосується Nметиламінометилізоіндольних сполук. Описані також фармацевтичні композиції, які включають ці сполуки, і способи лікування, профілактики і ведення пацієнтів з різними розладами. 2. Попередній рівень техніки 2.1 Патологія раку й інших захворювань Рак характеризується в першу чергу збільшенням кількості патологічних клітин, які походять з нормальної тканини, проникненням цих патологічних клітин у прилеглі тканини або лімфатичним або гематогенним поширенням злоякісних клітин у регіональні лімфовузли й у віддалені ділянки (метастази). Клінічні дані і молекулярно-біологічні дослідження вказують на те, що рак являє собою багатостадійний процес, який починається з невеликих пренеопластичних змін, які у визначених умовах можуть прогресувати в неоплазію. Неопластичне ураження може виникнути клонально і розвити зрослу здатність до проникнення, росту, метастазування і гетерогенності, особливо в умовах, у яких неопластичні клітини уникають імунного контролю хазяїна (Roitt, I., Brostoff, J. and Kale, D., rd Immunology, 17.1-17.12 (3 ed, Mosby, St. Louis, Mo., 1993). Існує величезна множина форм раку, які детально описані в медичній літературі. Приклади включають рак легень, ободової кишки, передміхурової залози, молочної залози, мозку і кишечнику. Частота раку продовжує зростати в міру старіння загальної популяції, оскільки розвиваються нові випадки раку і збільшується сприйнятливість до раку популяції (наприклад, люди, інфіковані СНІДом або піддані надлишковому впливу сонячного випромінювання). Однак можливості лікування раку обмежені. Наприклад, у випадку злоякісних уражень крові (наприклад, множинної мієломи), є небагато варіантів лікування, особливо коли звичайна хіміотерапія виявляється неефективною і трансплантація кісткового мозку не є варіантом лікування. Тому існує величезна потреба в нових способах і композиціях, які можна застосовувати для лікування пацієнтів, що страждають на рак. Багато типів раку пов'язані з утворенням нових кровоносних судин, процесом, відомим як ангіогенез. Було виявлено декілька механізмів, які беруть участь у викликаному пухлинами ангіогенезі. Найпрямішим з цих механізмів є секреція пухлинними клітинами цитокінів з ангіогенними властивостями. Приклади цих цитокінів включають кислотний і основний фактор росту фібробластів (a,b-FGF), ангіогенін, фактор росту судинного ендотелію (VEGF) і TNF-α (фактор пухлинного некрозу). Альтернативно, пухлинні клітини можуть вивільняти ангіогенні пептиди за допомогою продукції протеаз і наступного руйнування позаклітинної матриці, де накопичуються деякі цитокіни (наприклад, b-FGF). Ангіогенез може також бути викликаний побічно за допомогою залучення запальних клітин (особливо макрофагів) і наступного вивільнення ними ангіогенних цитокінів (наприклад, TNF-α, b-FGF). Різноманітні інші захворювання і розлади також пов'язані з небажаним ангіогенезом або характеризуються ним. Наприклад, посилений або нерегульований ангіогенез був залучений при ряді захворювань і медичних станів, включаючи без обмеження очні неоваскулярні захворювання, неоваскулярні захворювання судинної оболонки ока, неоваскулярні захворювання сітківки, рубеоз (неоваскуляризація кута), вірусні захворювання, генетичні захворювання, запальні захворювання, алергійні захворювання й аутоімунні захворювання. Приклади таких захворювань і станів включають без обмеження: діабетичну ретинопатію; ретинопатію недоношеності; відторгнення рогівкового трансплантата; неоваскулярну глаукому; ретролентальну фіброплазію; артрит і проліферативну вітреоретинопатію. Відповідно, сполуки, які можуть регулювати ангіогенез або інгібувати продукцію визначених цитокінів, включаючи TNF-α, можна застосовувати при лікуванні і профілактиці різних захворювань і станів. 2.2. Спосіб лікування раку Сучасне лікування раку може включати хірургічне лікування, хіміотерапію, гормональну терапію і/або променеву терапію для знищення неопластичних клітин у пацієнта (див., наприклад, Stockdate, 1998, Medicine, vol. 3, Rubenstein and Federman, eds., Chapter 12, Section IV). З недавнього часу, лікування раку може також включати біологічну терапію або імунотерапію. Усі ці підходи мають суттєві недоліки в плані впливу на пацієнта. Операція, наприклад, може бути протипоказана через стан здоров'я пацієнта або може бути неприйнятною для пацієнта. Крім того, при операції неопластична тканина може бути не повністю видалена. Променева терапія ефективна тільки тоді, 11 коли неопластична тканина виявляє більш високу чутливість до опромінення, ніж здорова тканина. Променева терапія може також часто викликати важкі побічні ефекти. Хоча гормональна терапія може бути ефективною, вона часто застосовується для запобігання або затримання рецидиву раку після того, як за допомогою інших видів лікування видалили більшість ракових клітин. Способи біологічної терапії і імунотерапії обмежені по кількості і можуть викликати побічні ефекти, такі як висипки або набряки, подібні до грипу симптоми, включаючи лихоманку, озноб і утому, проблеми з боку шлунково-кишкового тракту або алергійні реакції. Що стосується хіміотерапії, то існують різноманітні хіміотерапевтичні засоби, доступні для лікування раку. Більшість хіміотерапевтичних засобів для лікування раку діє шляхом прямого або непрямого інгібування синтезу ДНК, шляхом інгібування біосинтезу попередників деоксирибонуклеотиду трифосфату для запобігання реплікації ДНК і супутнього клітинного розподілу. Gilman et ai, Goodman and Gilman's: The Pharmacological Basis of Therapeutics, Tenth Ed. (McGraw Hill, New York). Незважаючи на наявність різноманітних хіміотерапевтичних засобів, хіміотерапія має багато недоліків (Stockdale, Medicine, vol. З, Rubenstein and Federman, eds., ch. 12, sect. 10, 1998). Майже всі хіміотерапевтичні засоби є токсичними, і хіміотерапія викликає значні і часто небезпечні побічні ефекти, включаючи важку нудоту, пригнічення кісткового мозку і пригнічення імунітету. Крім того, навіть при введенні комбінації хіміотерапевтичних засобів, багато пухлинних клітин є стійкими або у них розвивається стійкість до хіміотерапевтичних засобів. Дійсно, ті клітини, які стійкі до визначених хіміотерапевтичних засобів, застосовуваних у протоколах лікування, часто виявляються стійкими до інших препаратів, навіть якщо ці засоби діють механізмом, що відрізняється від механізмів дії препаратів, застосовуваних при специфічному лікуванні. Цей феномен іменується плейотропною лікарською стійкістю або стійкістю до багатьох лікарських засобів. Через лікарську стійкість, багато форм раку виявляються або стають рефракторними до стандартних протоколів хіміотерапевтичного лікування. Інші захворювання або стани, які пов'язані з небажаним ангіогенезом або характеризуються ним, також важко лікувати. Однак передбачалося, що деякі сполуки, такі як протамін, гепарин і стероїди, можна застосовувати при лікуванні конкретних захворювань Taylor et al., Nature 297:307 (1982); Folkman et al., Science 221:719 (1983); and US Pat. Nos. 5001116 and 4994443. Усе ще існує значна потреба в безпечних і ефективних способах лікування, профілактики і ведення пацієнтів, які страждають на рак і інші захворювання і стани, зокрема захворювання, що стійкі до стандартних способів лікування, таких як хірургічне лікування, променева терапія, хіміотерапія і гормональна терапія, при одночасному зниженні або виключенні токсичних впливів і/або побічних ефектів, пов'язаних зі звичайними способами лікування. 95975 12 3. Короткий опис суті винаходу Даний винахід частково спрямований на Nметиламінометилізоіндольні сполуки і їх фармацевтично прийнятні солі, сольвати (наприклад, гідрати), проліки або стереоізомери. Даний винахід також охоплює способи лікування або ведення пацієнтів з різними захворюваннями або розладами. Способи включають введення пацієнту, який потребує такого лікування або введення, терапевтично ефективної кількості сполуки за даним винаходом або її фармацевтично прийнятної солі, сольвату, стереоізомера або проліків. Даний винахід також охоплює способи профілактики різних захворювань і розладів, які включають введення пацієнту, що потребує такої профілактики, профілактично ефективної кількості сполуки за даним винаходом або її фармацевтично прийнятної солі, сольвату, гідрату, стереоізомера або проліків. Даний винахід також охоплює фармацевтичні композиції, стандартні лікарські форми, схеми введення і набори, які включають сполуку за даним винаходом або її фармацевтично прийнятну сіль, сольват, гідрат, стереоізомер, клатрат або проліки. 4. Детальний опис винаходу В одному варіанті здійснення, даний винахід охоплює N-метиламінометилізоіндольні сполуки і їх фармацевтично прийнятні солі, сольвати, стереоізомери і проліки. В іншому варіанті здійснення, даний винахід охоплює способи лікування, ведення пацієнтів і профілактики різних захворювань і розладів, які включають введення пацієнту, що потребує такого лікування або профілактики, терапевтично або профілактично ефективної кількості сполуки за даним винаходом або її фармацевтично прийнятної солі, сольвату або стереоізомера проліків. Приклади захворювань і розладів описані в даній заявці. У визначених варіантах здійснення, сполука за даним винаходом або її фармацевтично прийнятна сіль, сольват стереоізомер або проліки вводяться в комбінації з іншим лікарським засобом (другим активним засобом) або способом лікування. Другі активні засоби включають дрібні молекули і великі молекули (наприклад, білки й антитіла), приклади яких представлені в даному описі, а також стовбурові клітини. Способи або види лікування, які можна застосовувати в комбінації з введенням сполук за даним винаходом, включають без обмеження хірургічне лікування, переливання крові, біологічну терапію, променеву терапію або інші види лікування, не основані на медикаментозній терапії, використовувані в даний час для лікування, профілактики або ведення пацієнтів з різними розладами, описаними в даній заявці. Даний винахід також охоплює фармацевтичні композиції (наприклад, стандартні лікарські форми), які можна застосовувати в способах, описаних у даній заявці. Визначені фармацевтичні композиції включають сполуку за даним винаходом або її фармацевтично прийнятну сіль, сольват стереоі 13 95975 зомер або проліки і, необов'язково, другий активний засіб. 4.1. Сполуки В одному варіанті здійснення, даний винахід охоплює сполуки формули (І): (I) і їх фармацевтично прийнятні солі, сольвати, стереоізомери і проліки, де: * означає хіральний центр; X являє собою СН2 або С=О; 1 R являє собою Н, (С1-С8)алкіл, (С3С7)циклоалкіл, (С2-С8)алкеніл, (С2-С8)алкініл, бензил, арил, (С0-С4)алкіл-(С1-С6)гетероциклоалкіл, 3 3 ((С0-С4)алкіл-(С2-С9)гетероарил, C(O)R , C(S)R , 4 6 5 C(O)OR , (С1-С8)алкіл-N(R )2, (C1-C8)aлкiл-OR , 5 3 3 (С1-С8)aлкiл-C(O)OR , C(O)NHR , C(S)NHR , 3 3' 3 3' 5 C(O)NR R , C(S)NR R або (С1-С8)алкіл-O-(CO)R ; 2 R являє собою Η, СН3 або (С2-С8)алкіл; 3 3 R і R представляють незалежно (С1-С8)алкіл; (С3-С7)циклоалкіл; (С2-С8)алкеніл; (С2-С8)алкініл; бензил; (С0-С4)алкіл-(С5-С10)арил, необов'язково заміщений одним або декількома з: (С1-С6)алкілу, самого зазначеного алкілу, необов'язково заміщеного одним або декількома галогенами, (С1-С6)алкокси, самого зазначеного алкокси, необов'язково заміщеного одним або декількома галогенами, SCY3, де Υ являє собою водень або галоген, ΝΖ2, де Ζ являє собою водень або (С1С6)алкіл, (С1-С6)алкілендіокси, або галоген; (С0-С4)алкіл-(С1-С6)гетероциклоалкіл; (С0-С4)алкіл-(С2-С9)гетероарил; 6 (C0-C8)алкіл-N(R )2; 5 (С1-С8)алкіл-OR ; 5 (С1-С8)алкіл-С(О)OR ; 5 (С1-С8)алкіл-О(СО)R або 5 C(O)OR ; 4 R являє собою (С1-С8)алкіл, (С2-С8)алкеніл, 5 (С2-С8)алкініл, (С1-С4)алкіл-ОR , бензил, арил, (С0С4)алкіл-(С1-С8)гетероциклоалкіл або (С0-С4)алкіл(С2-С9)гетероарил; 5 R являє собою (С1-С8)алкіл, (С2-С8)алкеніл, (С2-С8)алкініл, бензил, (С5-С10)арил або (С2С9)гетероарил; 6 у кожнім випадку R являє собою незалежно Н, (С1-С8)алкіл, (С2-С8)алкеніл, (С2-С8)алкініл, бензил, (С5-С!0)арил, (С2-С9)гетероарил або (С05 С8)алкіл-С(О)-R , або 6 дві R групи можуть з'єднуватися для утворення гетероциклоалкільної групи. 14 В одному варіанті здійснення, X являє собою С=О. В іншому варіанті здійснення, X являє собою СН2. 1 В одному варіанті здійснення, R являє собою 1 Н. В іншому варіанті здійснення, R являє собою СН3. В іншому варіанті здійснення, R являє собою 1 (С2-С8)алкіл. В іншому варіанті здійснення, R являє собою (С3-С7)циклоалкіл. В іншому варіанті 1 здійснення, R являє собою (С2-С8)алкеніл. В ін1 шому варіанті здійснення, R являє собою (С21 С8)алкініл. В іншому варіанті здійснення, R являє 1 собою бензил. В іншому варіанті здійснення, R являє собою арил. В іншому варіанті здійснення, 1 R являє собою (С0-С4)алкіл-(С1С6)гетероциклоалкіл. В іншому варіанті здійснен1 ня, R являє собою (С0-С4)алкіл-(С2-С9)гетероарил. 1 В іншому варіанті здійснення, R являє собою 3 1 C(O)R . В іншому варіанті здійснення, R являє 3 1 собою C(S)R . В іншому варіанті здійснення, R 4 являє собою C(O)OR . В іншому варіанті здійснен1 6 ня, R являє собою (С1-C8)алкіл-N(R )2. В іншому 1 варіанті здійснення, R являє собою (С1-С8)алкіл5 1 OR . В іншому варіанті здійснення, R являє собою 5 (С1-С8)алкіл-С(О)OR . В іншому варіанті здійснен1 3 ня, R являє собою C(O)NHR . В одному варіанті 1 здійснення, R являє собою C(O)NH-(C0-C4)алкіл(C5-С10)арил, де арил необов'язково заміщений, як 1 описано нижче. В іншому варіанті здійснення, R 3 являє собою C(S)NHR . В іншому варіанті здійс1 3 3 нення, R являє собою C(O)NR R . В іншому варі1 3 3 анті здійснення, R являє собою C(S)NR R . В ін1 шому варіанті здійснення, R являє собою (С15 С8)алкіл-О(СО)R . 2 В одному варіанті здійснення, R являє собою 2 Н. В іншому варіанті здійсненняД являє собою (С1-С8)алкіл. 3 В одному варіанті здійснення, R являє собою 3 (С1-C8)алкіл. В іншому варіанті здійснення, R являє собою (С3-С7)циклоалкіл. В іншому варіанті 3 здійснення, R являє собою (С2-С8)алкеніл. В ін3 шому варіанті здійснення, R являє собою (С2С8)алкініл. В іншому варіанті здійснення, R являє 3 собою бензил. В іншому варіанті здійснення, R являє собою (С0-С4)алкіл-(С5-С10)арил, необов'язково заміщений одним або більше з: (С1-С6)алкілу, причому сам зазначений алкіл необов'язково заміщений одним або декількома галогенами; (С1С6)алкокси, причому сам зазначений алкокси необов'язково заміщений одним або декількома галогенам; SCY3, де Υ являє собою водень або галоген; ΝΖ2, де Ζ являє собою водень або (С1С6)алкіл; (С1-С6)алкілендіокси або галоген. В ін3 шому варіанті здійснення, R являє собою (С0С4)алкіл-(С1-С6)гетероциклоалкіл. В іншому варіа3 нті здійснення, R являє собою (С0-С4)алкіл-(С23 С9)гетероарил. В іншому варіанті здійснення, R 6 являє собою (C0-C8)алкіл-N(R )2. В іншому варіанті 3 5 здійснення, R являє собою (С1-С8)алкіл-OR . В 3 іншому варіанті здійснення, R являє собою (С15 С8)алкіл-С(О)OR . В іншому варіанті здійснення, 3 5 R являє собою (С1-С8)алкіл-О(СО)OR . В іншому 3 5 варіанті здійснення, R являє собою C(O)OR . 3' В одному варіанті здійснення, R являє собою 3' (С1-С8)алкіл. В іншому варіанті здійснення, R являє собою (С3-С7)циклоалкіл. В іншому варіанті 15 95975 3' здійснення, R являє собою (С2-С8)алкеніл. В ін3' шому варіанті здійснення, R являє собою (С23' С8)алкініл. В іншому варіанті здійснення, R являє 3' собою бензил. В іншому варіанті здійснення, R являє собою арил. В іншому варіанті здійснення, 3' R являє собою (С0-С4)алкіл-(С1С6)гетероциклоалкіл. В іншому варіанті здійснен3' ня, R являє собою (С0-С4)алкіл-(С23' С9)гетероарил. В іншому варіанті здійснення, R 6 являє собою (C0-C8)алкіл-N(R )2. В іншому варіанті 3' 5 здійснення, R являє собою (C1-C8)aлкiл-OR . В 3' іншому варіанті здійснення, R являє собою (C15 С8)алкіл-С(О)OR . В іншому варіанті здійснення, 3' 5 R являє собою (С1-С8)алкіл-O(CO)OR . В іншому 3' 5 варіанті здійснення, R являє собою C(O)OR . 4 В одному варіанті здійснення, R являє собою 4 (С1-С8)алкіл. В іншому варіанті здійснення, R являє собою (С2-С8)алкеніл. В іншому варіанті здійс4 нення, R являє собою (С2-С8)алкініл. В іншому 4 варіанті здійснення, R являє собою (С1-С4)алкіл5 4 OR . В іншому варіанті здійснення, R являє собою 4 бензил. В іншому варіанті здійснення, R являє 4 собою арил. В іншому варіанті здійснення, R являє собою (С0-С4)алкіл-(С1-С6)гетероциклоалкіл. В 4 іншому варіанті здійснення, R являє собою (С0С4)алкіл-(С2-С9)гетероарил. 5 В одному варіанті здійснення, R являє собою 5 (С1-С8)алкіл. В іншому варіанті здійснення, R являє собою (С2-С8)алкеніл. В іншому варіанті здійс5 нення, R являє собою (С2-С8)алкініл. В іншому 5 варіанті здійснення, R являє собою бензил. В ін5 шому варіанті здійснення, R являє собою (С55 С10)арил. В іншому варіанті здійснення, R являє собою (С2-С9)гетероарил. 6 В одному варіанті здійснення, R являє собою 6 Н. В іншому варіанті здійснення, R являє собою 6 (С1-С8)алкіл. В іншому варіанті здійснення, R являє собою (С2-С8)алкеніл. В іншому варіанті здійс6 нення, R являє собою (С2-С8)алкініл. В іншому 6 варіанті здійснення, R являє собою бензил. В ін6 шому варіанті здійснення, R являє собою (С56 С10)арил. В іншому варіанті здійснення, R являє собою (С2-С9)гетероарил. В іншому варіанті здійс6 5 нення, R являє собою (С0-С8)алкіл-С(О)О-R . В 6 іншому варіанті здійснення, дві R групи з'єднуються для утворення гетероциклоалкільної групи. В іншому варіанті здійснення, даний винахід 1 2 3 3' 4 охоплює будь-яку комбінацію X, R , R , R , R , R , 5 6 R і/або R , як описано вище. В одному варіанті здійснення, даний винахід охоплює сполуки формули (II): (II) і їх фармацевтично прийнятні солі, сольвати, стереоізомери і проліки, де: * означає хіральний центр; X являє собою СН2 або С=О; R являє собою (С1-С6)алкіл; (С1-С6)алкокси; аміно; (С1-С6)алкіламіно; діалкіламіно, де кожна з алкільних груп являє собою незалежно (С1 16 С6)алкіл; (С0-С4)алкіл-(С6-С10)арил, необов'язково заміщений одним або більше (С1-С6)алкілом, (С1С6)алкокси або галогеном; 5-10-членний гетероарил, необов'язково заміщений одним або більше (С1-С6)алкілом; -NHR або (С0-С8)алкіл-N(R")2; R' являє собою: (С1-С6)алкіл; (С0-С4)алкіл-(С6-С10)арил, необов'язково заміщений одним або більше: (С1-С6)алкілом, зазначеного алкілу, необов'язково заміщеного одним або більше галогеном, (С1-С6)алкокси, зазначеного алкокси, необов'язково заміщеного одним або більше галогеном, (С1-С6)алкілендіокси або галоген; або 5-10-членний гетероарил, необов'язково заміщений одним або більше (С1-С6)алкілом; і в кожнім випадку R" являє собою незалежно Н, (С1С8)алкіл, (С2-С8)алкеніл, (С2-С8)алкініл, бензил, (С6-С10)арил, 5-10-членний гетероарил або (С0С8)алкіл-С(О)О-(С1-С8)алкіл. В одному варіанті здійснення, X являє собою С=О. В одному варіанті здійснення, X являє собою СН2. В одному варіанті здійснення, R являє собою (С1-С6)алкіл. У визначених конкретних варіантах здійснення, R являє собою метил, етил, пропіл, циклопропіл або гексил. В іншому варіанті здійснення, R являє собою (С1-С6)алкокси. У визначених конкретних варіантах здійснення R являє собою трет-бутокси. В іншому варіанті здійснення, R являє собою аміно. В іншому варіанті здійснення, R являє собою (С1-С6)алкіламіно. В іншому варіанті здійснення, R являє собою діалкіламіно, де кожна з алкільних груп являє собою незалежно (С1-С6)алкіл. У визначених конкретних варіантах здійснення R являє собою диметиламіно. В іншому варіанті здійснення, R являє собою (С0-С4)алкіл-(С6-С10)арил, необов'язково заміщений одним або більше (С1-С6)алкілом, (С1С6)алкокси або галогеном. У визначених конкретних варіантах здійснення, R являє собою феніл або -СН2-феніл, необов'язково заміщений одним або більше метилом і/або галогеном. В іншому варіанті здійснення, R являє собою 5-10-членний гетероарил, необов'язково заміщений одним або більше (С1-С6)алкілом. У визначених конкретних варіантах здійснення, R являє собою піридил або фураніл. В іншому варіанті здійснення, R являє собою NHR'. В одному варіанті здійснення, R' являє собою (С1-С6)алкіл, необов'язково заміщений одним або більше галогеном. У визначених конкретних варіантах здійснення, R' являє собою метил, етил, пропіл, трет-бутил, циклогексил або трифторметил. В одному варіанті здійснення, R' являє собою (С0-С4)алкіл-(С6-С10)арил, необов'язково заміщений одним або більше (С1-С6)алкілом, (С1С6)алкокси, (С1-С6)алкілендіокси або галогеном. У визначених конкретних варіантах здійснення, R' являє собою феніл, необов'язково заміщений одним або більше метилом, метокси і/або хлоридом. В іншому варіанті здійснення, R' являє собою нафтил. В іншому варіанті здійснення, R' являє собою 17 феніл, заміщений (С1-С6)алкілендіокси, зокрема метилендіокси. В іншому варіанті здійснення, R' являє собою толуїл. В іншому варіанті здійснення, R' являє собою 5-10-членний гетероарил, необов'язково заміщений одним або більше (С1-С6)алкілом. У визначених конкретних варіантах здійснення, R' являє собою піридил або нафтил. В одному варіанті здійснення, R являє собою (C0-C8)алкіл-N(R")2. В іншому варіанті здійснення, R" являє собою Н. В іншому варіанті здійснення, R" являє собою (С1-С6)алкіл. В іншому варіанті здійснення, R" являє собою (С2-С6)алкеніл. В іншому варіанті здійснення, R" являє собою (С2-С6)алкініл. В іншому 95975 18 варіанті здійснення, R" являє собою бензил. В іншому варіанті здійснення, R" являє собою (С6С10)арил. В іншому варіанті здійснення, R" являє собою 5-10-членний гетероарил. В іншому варіанті здійснення, R" являє собою (С0-С8)алкіл-С(О)О(С1-С8)алкіл. У визначених конкретних варіантах здійснення, один з R" являє собою Н, а інший з R" являє собою (С0-С8)алкіл-С(O)O-(С1-С8)алкіл, зокрема -СОО-ізобутил. В іншому варіанті здійснення, винахід охоплює будь-яку комбінацію X, R і/або R', як описано вище. Приклади включають без обмеження сполуки, що наведені нижче, або їх фармацевтично прийнятну сіль, сольват (наприклад, гідрат) або стереоізомер: 19 95975 20 21 Якщо немає інших визначень, використовуваний у даному описі термін «фармацевтично прийнятна сіль» стосується солей, одержаних з фармацевтично прийнятних нетоксичных кислот, включаючи неорганічні кислоти й органічні кислоти. Придатні нетоксичні кислоти включають неорганічні й органічні кислоти, такі як без обмеження оцтова, альгінова, антранілова, бензолульфонова, бензойна, камфорсульфонова, лимонна, етенсульфонова, мурашина, фумарова, фуроєва, глюконова, глутамінова, глюкуронова, галактуронова, гліцидна, бромистоводнева, хлористоводнева, ізетіонова, молочна, малеїнова, яблучна, мигдальна, метансульфонова, слизова, азотна, памоєва, пантотенова, фенілоцтова, пропіонова, фосфорна, саліцилова, стеаринова, бурштинова, сульфанілова, сірчана, винна, птолуолсульфонова кислота і ним подібні. Придатними є хлористоводнева, бромистоводнева, фосфорна і сірчана кислоти. Якщо немає інших визначень, використовуваний у даному описі термін «сольват» означає, що надана в даному винаході сполука або її сіль, крім того, включає стехіометричну або не стехіометричну кількість розчинника, зв'язаного нековалент 95975 22 ними міжмолекулярними силами. Коли розчинник являє собою воду, сольват являє собою гідрат. Якщо немає інших визначень, використовуваний у даному описі термін «проліки» означає похідне сполуки, яке може гідролізуватися, окислятися або іншим шляхом взаємодіяти в біологічних умовах (in vitro або in vivo) з одержанням сполуки. Приклади проліків включають без обмеження сполуки, які включають біологічно гідролізовні частини, такі як біологічно гідролізовні аміди, біологічно гідролізовні складні ефіри, біологічно гідролізовні карбамати, біологічно гідролізовні карбонати, біологічно гідролізовні уреїди, і біологічно гідролізовні аналоги фосфатів. Інші приклади проліків включають сполуки, які включають частини -NO, -NO2, ΟΝΟ або -ΟΝΟ2. Проліки можна звичайно одержати, використовуючи добре відомі способи, такі як способи, описані в документах Burger's Medicinal Chemistry and Drug Discovery, 172-178, 49-982 th (Manfred E. Wolff ed., 5 ed. 1995) і Desing of Prodrugs (H. Bundgaard ed. Elselvier New York 1895). Якщо немає інших визначень, використовуваний у даному описі терміни «біологічно гідролізовний карбамат», «біологічно гідролізовний карбо 23 нат», «біологічно гідролізовний уреїд» і «біологічно гідролізовний фосфат» означають відповідно карбамат, карбонат, уреїд і фосфат сполуки, яка або: 1) не перешкоджає біологічній активності сполуки, але може надати цій сполуці переважні властивості in vivo, такі як захоплення, тривалість дії або початок дії; або 2) є біологічно неактивною, але перетворюється in vivo у біологічно активну речовину. Приклади біологічно гідролізовних карбаматів включають без обмеження нижчі алкіламіни, заміщені етилендіаміни, амінокислоти, гідроксіалкіламіни, гетероциклічні і гетероароматичні аміни і поліефіраміни. Якщо немає інших визначень, використовуваний у даному описі термін «стереоізомер» охоплює всі енантіомерно/стереомерно чисті і енантіомерно/стереомерно збагачені сполуки, надані в даному описі. Якщо немає інших визначень, використовуваний у даному описі термін «стереомерно чистий» означає склад, який включає один стереоізомер сполуки і, власне кажучи, вільний від інших стереоізомерів цієї сполуки. Наприклад, стереомерна сполука, яка має один хіральний центр, буде, власне кажучи, вільною від протилежного енантіомера сполуки. Стереомерно чистий склад для сполуки, яка має два хіральних центри, буде, власне кажучи, вільний від інших діастереомерів сполуки. Типова стереомерно чиста сполука включає більше ніж приблизно 80% мас. одного стереоізомера сполуки і менше ніж приблизно 20% мас. інших стереоізомерів сполуки, переважніше більше ніж приблизно 90% мас. одного стереоізомера сполуки і менше ніж приблизно 10% мас. інших стереоізомерів сполуки, ще переважніше більше ніж приблизно 95% мас. одного стереоізомера сполуки і менше ніж приблизно 5% мас. інших стереоізомерів сполуки, а найбільш переважно більше ніж приблизно 97% мас. одного стереоізомера сполуки і менше ніж приблизно 3% мас. інших стереоізомерів сполуки. Поки немає інших визначень, використовуваний у даному описі термін «стереомерно збагачений» означає склад, який включає більше ніж приблизно 55% мас. одного стереоізомера сполуки, більше ніж приблизно 60% мас. одного стереоізомера сполуки, переважно більше ніж приблизно 70% мас, переважніше більше ніж приблизно 80% мас. одного стереоізомера сполуки. Якщо немає інших визначень, використовуваний у даному описі термін «енантіомерно чиста» означає стереомерно чисту сполуку, яка має один хіральний центр (наприклад, >97% еее). Аналогічним чином, термін «енантіомерно збагачена» означає стереомерно збагачену композицію сполуки, яка має один хіральний центр. Якщо немає інших визначень, використовуваний у даному описі термін «алкіл» стосується насиченого прямоланцюгового або розгалуженого вуглеводню, що має ряд атомів вуглецю, як визначено в даному описі. Репрезентативні насичені прямоланцюгові алкіли включають -метил, -етил, н-пропіл-, -н-бутил-, -н-пентил- і -н-гексил; тоді як насичені розгалужені алкіли включають -ізопропіл, -втор-бутил-, -ізобутил-, -трет-бутил-, -ізопентил-, 95975 24 2-метилбутил, 3-метилбутил, 2-метилпентил, 3метилпентил, 4-метилпентил, 2- метилгексил, 3метилгексил, 4-метилгексил, 5-метилгексил, 2,3диметилбутил і ним подібні. Термін «алкіл» також охоплює циклоалкіл. Як використовується в даному описі, термін «циклоалкіл» означає вид алкілу, що містить від 3 до 15 атомів вуглецю, без чергування або резонування подвійних зв'язків між атомами вуглецю. Він може містити від 1 до 4 кілець. Приклади ненасичених циклоалкілів включають без обмеження циклопропіл, циклобутил, циклопентил, циклогексил і адамантил. Циклоалкіл може бути заміщений одним або декількома замісниками, як визначено нижче. Якщо немає інших визначень, використовуваний у даному описі термін «алкеніл» означає прямоланцюговий або розгалужений вуглеводень, що має від 2 до 20 атомів вуглецю, зокрема від 2 до 10 атомів вуглецю, конкретніше від 2 до 6 атомів вуглецю, і включає щонайменше один подвійний міжвуглецевий зв'язок. Репрезентативні прямоланцюгові і розгалужені (С2-С10)алкеніли включають вініл, аліл, 1-бутеніл, 2-бутеніл, ізобутиленіл, 1пентеніл, 2-пентеніл, 3-метил-1-бутеніл, 2-метил2-бутеніл, 2,3-диметил-2-бутеніл, 1-гексеніл, 2гексеніл, 3-гексеніл, 1-гептеніл, 2-гептеніл, 3гептеніл, 1-октеніл, 2-октеніл, 3-октеніл, 1-ноненіл, 2-ноненіл, 3-ноненіл, 1-деценіл, 2-деценіл і 3деценіл. Подвійний зв'язок алкенільної групи може бути неспряжено зв'язаний або спряжено зв'язаний з іншою ненасиченою групою. Алкенільна група може бути незаміщеною або заміщеною. Якщо немає інших визначень, використовуваний у даному описі термін «алкініл» означає прямоланцюговий або розгалужений нециклічний вуглеводень, який має від 2 до 20 атомів вуглецю, зокрема від 2 до 10 атомів вуглецю, конкретніше 26 атомів вуглецю, і включає щонайменше один міжвуглецевий потрійний зв'язок. Репрезентативні прямоланцюгові і розгалужені (С2-С10)алкініли включають ацетиленіл, пролініл, 1-бутиніл, 2бутиніл, 1-пентиніл, 2-пентиніл, 3-метил-1-бутиніл, 4-пентиніл, 1-гексиніл, 2-гексиніл, 5-гексиніл, 1гептиніл, 2-гептиніл, 6-гептиніл, 1-октиніл, 2октиніл, 7-октиніл, 1-нонініл, 2-нонініл, 8-нонініл, 1дециніл, 2-дециніл, 9-дециніл і ним подібні. Потрійний зв'язок алкінільної групи може бути неспряжено зв'язаний або спряжено зв'язаний з іншою ненасиченою групою. Алкінільна група може бути незаміщеною або заміщеною. Якщо немає інших визначень, використовуваний у даному описі термін «алкокси» стосується О-(алкілу), де алкіл визначений у даному описі. Приклади алкокси включають без обмеження ОСН3, -ОСН2ОСН3, -О(СН2)2ОСН3, -О(СН2)3ОСН3, О(СН2)4ОСН3, -О(СН2)5ОСН3, -О-циклопропіл, -Оізобутил і ним подібні. Використовуваний у даному описі термін «арил» означає карбоциклічне ароматичне кільце, яке містить від 5 до 14 кільцевих атомів. Усі кільцеві атоми карбоциклічної арильної групи являють собою атоми вуглецю. Структури арильного кільця включають сполуки, які мають одну або декілька кільцевих структур, таких як моно-, бі- або трицик 25 лічні сполуки, а також бензоконденсовані карбоциклічні частини, такі як 5,6,7,8-тетрагідронафтил і ним подібні. Зокрема, арильна група являє собою моноциклічне кільце або біциклічне кільце. Репрезентативні арильні групи включають феніл, антраценіл, фтореніл, інденіл, азуленіл, фенантреніл і нафтил. Якщо немає інших визначень, використовуваний у даному описі термін «гетероарил» означає ароматичне кільце, яке містить від 5 до 14 кільцевих атомів, з яких щонайменше одне (наприклад, одне, два або три) являє собою гетероатом (наприклад, азот, кисень або сірку). Структури гетероарильного кільця включають сполуки, які мають одну або декілька кільцевих структур, таких як моно-, бі- або трициклічні сполуки, а також конденсовані гетероциклічні частини. Приклади гетероарилів включають без обмеження триазоліл, тетразоліл, оксадіазоліл, піридил, фурил, бензофураніл, тіофеніл, тіазоліл, бензотіофеніл, бензоізоксазоліл, бензоізотіазоліл, хінолініл, ізохінолініл, піроліл, індоліл, оксазоліл, бензоксазоліл, імідазоліл, бензімідазоліл, тіазоліл, бензотіазоліл, ізоксазоліл, піразоліл, ізотіазоліл, пуридиніл, піридазиніл, піримідиніл, піразиніл, триазиніл, цинолініл, фталазиніл, хіназолініл, бензохіназолініл, хіноксалініл, акридиніл, піримідил, оксазоліл, бензо[1,3]діоксол і 2,3-дигідробензо[1,4]діоксин. Якщо немає інших визначень, використовуваний у даному описі термін «гетероциклоалкіл» стосується циклоалкільної групи, у якій щонайменше один з атомів вуглецю в кільці заміщений гетероатомом (наприклад, О, S або N), такої як, але не обмежуючись цим, морфоліно або піперидиніл. Слід зазначити, що якщо є розбіжність між зображеною структурою і назвою, що надана цій структурі, перевага повинна бути віддана зображеній структурі. Крім того, якщо стереохімія структури або частини структури не зазначена, наприклад, жирними або пунктирними лініями, то структуру або частину структури варто трактувати як таку, що охоплює всі її стереоізомери. 4.2. Способи лікування, профілактики і ведення пацієнтів Винахід охоплює способи лікування, профілактики і/або ведення пацієнтів, які страждають на різні захворювання або розлади, з використанням сполуки за даним винаходом або її фармацевтично прийнятної солі, сольвату, стереоізомера або проліків. Без обмеження якою-небудь визначеною теорією, сполуки за винаходом можуть контролювати ангіогенез або інгібувати продукцію визначених цитокінів, включаючи без обмеження TNF-α, IL (інтерлейкін)-1β, IL-12, IL-18, GM-CSF (колонієстимулюючий фактор гранулоцитів-макрофагів) і/або IL-6. Без обмеження якою-небудь визначеною теорією, сполуки за винаходом можуть стимулювати продукцію визначених інших цитокінів, включаючи IL-10, а також діяти як спільно стимулюючий сигнал для активації Т-клітин, приводячи до збільшеної продукції цитокінів, таких як без обмеження IL12 і/або IFN-. Крім того, сполуки за винаходом можуть підсилити ефекти клітин NK (натуральних кілeрів) і антитілообумовленої клітинної цитотоксичності (ADCC). Крім того, сполуки за винаходом 95975 26 можуть бути імуномодуляторними і/або цитотоксичними і, таким чином, можуть використовуватися як хіміотерапевтичні засоби. Отже, без обмеження якою-небудь визначеною теорією, деякі або усі з таких характеристик, властивих сполукам за винаходом, можуть зробити їх придатними для лікування, ведення і/або профілактики різних захворювань або розладів. Приклади захворювань або розладів включають без обмеження рак, розлади, пов'язані з ангіогенезом, болем, включаючи складний регіональний больовий синдром ("CRPS"), дегенерацію жовтої плями ("MD") і пов'язані з нею синдроми, шкірні захворювання, легеневі розлади, розлади, пов'язані з азбестом, паразитарні захворювання, імунодефіцитні розлади, розлади ЦНС, травми ЦНС, атеросклероз і пов'язані з ним розлади, дисфункціональні розлади сну і пов'язані з ними розлади, гемоглобінопатію і пов'язані з нею розлади (наприклад, анемію), розлади, пов'язані з TNF-α і іншими цитокінами, і інші різні захворювання і розлади. Якщо немає інших визначень, використовувані у даному описі терміни «лікувати» і «лікування» стосуються усунення або полегшення захворювання або розладу або одного або декількох симптомів, пов'язаних з захворюванням або розладом. У визначених варіантах здійснення, ці терміни стосуються мінімізації поширення або погіршення захворювання або розладу в результаті введення одного або декількох профілактичних або терапевтичних засобів суб'єкту з таким захворюванням або розладом. Якщо немає інших визначень, використовувані у даному описі терміни «запобігати», «запобігання» і «профілактика» стосуються запобігання початку, рецидиву або поширення захворювання або розладу, або одного або декількох його симптомів. Якщо немає інших визначень, використовувані у даному описі терміни «вести пацієнта» або «ведення пацієнта» стосуються запобігання або уповільнення прогресування, поширення або погіршення захворювання або розладу, або одного або декількох його симптомів у пацієнта. Часто, сприятливі ефекти, здійснювані на суб'єкта в результаті застосування профілактичного або терапевтичного засобу, не приводять до виліковування захворювання або розладу. Якщо немає інших визначень, використовуваний у даному описі термін «терапевтично ефективна кількість» сполуки являє собою кількість, достатню для забезпечення терапевтичного ефекту при лікуванні або веденні пацієнта, що має захворювання або розлад, або для затримання виникнення або мінімізації одного або декількох симптомів, пов'язаних з захворюванням або розладом. Терапевтично ефективна кількість сполуки означає кількість терапевтичного засобу, окремо або в комбінації з іншими способами лікування, яка забезпечує терапевтичний ефект при лікуванні або веденні пацієнта, що має захворювання або розлад. Термін «терапевтично ефективна кількість» може охоплювати кількість, яка поліпшує загальне лікування, знижує або дозволяє уникнути розвитку симптомів або причин захворювання або розладу 27 або підсилює терапевтичну ефективність іншого терапевтичного засобу. Якщо немає інших визначень, використовуваний у даному описі термін «профілактично ефективна кількість» сполуки являє собою кількість, достатню для запобігання захворюванню або розладу або запобігання його рецидиву. Профілактично ефективна кількість сполуки означає кількість терапевтичного засобу, окремо або в комбінації з іншими засобами, яка забезпечує профілактичний ефект при запобіганні захворюванню. Термін «профілактично ефективна кількість» може охоплювати кількість, яка поліпшують загальну профілактику або підвищує профілактичну ефективність іншого профілактичного засобу. Приклади раку і передракових станів включають без обмеження ті, котрі описані в патентах US 6281230 і 5635517, виданих Muller et al., у різних патентних публікаціях Zeldis, включаючи публікацію №№ 2004/0220144А1, опубліковану 4 листопада 2004 р. (Лікування мієлодиспластичного синдрому); 2004/0029832А14А1, опубліковану 12 лютого 2004 р. (Лікування різних типів раку); і 2004/0087546, опубліковану 6 травня 2004 р. (Лікування мієлопроліферативних захворювань). Приклади також включають ті, котрі описані в PCT/US04/14004, поданій 5 травня 2004 р. Усі ці посилання повністю включені в даний опис як посилання. Визначені приклади раку включають без обмеження види раку шкіри, такі як меланома; рак лімфовузлів; молочної залози; шийки матки; тіла матки; шлунково-кишкового тракту; легені; яєчника; передміхурової залози; ободової кишки; прямої кишки; ротової порожнини; мозку; голови і шиї; горла; сім'яників; нирки; підшлункової залози; кісти; селезінки; печінки; сечового міхура; гортані; носових ходів; і форми раку, пов'язані зі СНІДом. Ці сполуки особливо корисні для лікування злоякісних захворювань крові і кісткового мозку, таких як множинна мієлома і гострі і хронічні лейкози, наприклад, лімфобластичного, мієлогенного, лімфоцитарного і мієлоцитарного лейкозів. Сполуки за винаходом можна застосовувати для лікування, запобігання або ведення пацієнтів з первинними або метастатичними пухлинами. Інші визначені форми раку включають без обмеження задавнені злоякісні ураження, амілоїдоз, нейробластому, менінгіому, гемангіоперицитому, множинні метастази в мозок, багатоформну гліобластому, гліобластому, гліому стовбура головного мозку, злоякісну пухлину мозку з несприятливим прогнозом, злоякісну гліому, рецидивуючу злоякісну гліому, анапластичну астроцитому, анапластичну олігодендрогліому, нейроендокринну пухлину, прямокишкову аденокарциному, рак ободової і прямої кишки Dukes C&D, неоперабельну карциному ободової і прямої кишки, метастатичну печінковоклітинну карциному, саркому Капоші, каротипічний гострий мієлобластичний лейкоз, хронічний лімфолейкоз (CLL), лімфому Ходжкіна, неходжкінську лімфому, шкірну Т-клітинну лімфому, шкірну В-клітинну лімфому, дифузійну велико-В-клітинну лімфому, низькодиференційовану фолікулярну лімфому, метастатичну меланому (локалізовану 95975 28 меланому, що включає без обмеження очну меланому), злоякісну мезотеліому, синдром злоякісної мезотеліоми з плевральним випотом, очеревинну карциному, папілярну серозну карциному, гінекологічну саркому, саркому м'яких тканин, склеродермію, шкірний васкуліт, гістицитоз клітин Лангерганса, лейоміосаркому, прогресуючу осифікувальну фібродисплазію, рак передміхурової залози, стійкий до гормональної терапії, резектовану саркому м'яких тканин з високим ризиком, неоперабельну печінковоклітинну карциному, макроглобулінемію Вальденстрема, млявоплинну мієлому, безболісну мієлому, рак фаллопієвих труб, андрогеннезалежний рак передміхурової залози, андрогенобумовлений неметастатичний рак передміхурової залози IV стадії, рак передміхурової залози, нечутливий до гормональної терапії, рак передміхурової залози, нечутливий до хіміотерапії, папілярну карциному щитовидної залози, фолікулярну карциному щитовидної залози, медулярну карциному щитовидної залози і лейоміому. В іншому варіанті здійснення, рак є рефракторним або стійким до хіміотерапії або опромінення. В одному визначеному варіанті здійснення, даний винахід охоплює способи лікування, профілактики або ведення пацієнтів з різними формами лейкозів, таких як хронічний лімфолейкоз, хронічний мієлолейкоз, гострий лімфобластичний лейкоз, гострий мієлолейкоз і гострий мієлобластичний лейкоз, включаючи лейкози, що є рецидивуючими, рефракторними або стійкими, як описано в патентній публікації US 2006/0030594, опублікованій 9 лютого 2006 p., що повністю включена в даний опис як посилання. Термін «лейкоз» стосується злоякісних новоутворень тканин, що утворюють кров. Лейкоз включає без обмеження хронічний лімфолейкоз, хронічний мієлолейкоз, гострий лімфобластичний лейкоз, гострий мієлолейкоз і гострий мієлобластичний лейкоз. Лейкоз може бути рецидивуючим, рефракторним або стійким до звичайного лікування. Термін «рецидивуючий» стосується ситуації, при якій у пацієнтів, що мали ремісію лейкозу після лікування, наявне повернення лейкозних клітин у кістковому мозку і зменшення нормальних клітин крові. Термін «рефракторний або стійкий» стосується ситуації, коли у пацієнтів, навіть після інтенсивного лікування, у кістковому мозку наявні залишкові лейкозні клітини. В іншому визначеному варіанті здійснення, даний винахід охоплює способи лікування, профілактики або ведення пацієнтів з різними типами лейкозів, включаючи неходжкінську лімфому (NHL). Термін «лімфома» стосується гетерогенної групи новоутворень, які виникають у ретикулоендотеліальній і лімфатичній системах. «NHL» стосується злоякісної моноклональної проліферації лімофоїдних клітин в ділянках імунної системи, що включають лімфовузли, кістковий мозок, селезінку, печінку і шлунково-кишковий тракт. Приклади NHL включають без обмеження лімфому з клітин мантії (MCL), лімфоцитарну лімфому проміжного диференціювання, проміжну лімфоцитарну лімфому (ILL), дифузійну низькодиференційовану лімфоцитарну лімфому (PDL), центроцитарну лімфому, 29 дифузійну лімфому з дрібно сегментованих клітин (DSCCL), фолікулярну лімфому і будь-який тип лімфом із клітин мантії, що видні під мікроскопом (вузлова, дифузійна, бластна і мантієклітинна лімфома). Приклади захворювань і розладів, пов'язаних або характеризованих небажаним ангіогенезом, включають без обмеження запальні захворювання, аутоімунні захворювання, вірусні захворювання, генетичні захворювання, алергійні захворювання, бактеріальні захворювання, очні неоваскулярні захворювання, неоваскулярні захворювання судинної оболонки ока, неоваскулярні захворювання сітківки і рубеоз (неоваскуляризацію кута). Визначені приклади захворювань і розладів, пов'язаних або характеризованих небажаним ангіогенезом, включають без обмеження ендомеріоз, хворобу Крона, серцеву недостатність, задавнену серцеву недостатність, ураження нирок, ендотоксемію, синдром токсичного шоку, остеоартрит, реплікацію ретровірусу, виснаження, менінгіт, фіброз, викликаний діоксидом кремнію, фіброз, викликаний азбестом, ветеринарний розлад, гіперкальцемію, пов'язану зі злоякісними захворюваннями, інсульт, циркуляторний шок, періодонтит, гінгівіт, макроцитарну анемію, рефракторну анемію і синдром 5q-делеції. Приклади болю включають без обмеження ті, котрі описані в патентній публікації US 2005/0203142, опублікованій 15 вересня 2005 p., що повністю включена в даний опис як посилання. Визначені типи болю включають без обмеження ноцицептивний біль, нейропатичний біль, змішаний біль з ноцицептивного і нейропатичного болю, вісцеральний біль, мігрень, головний біль і післяопераційний біль. Приклади ноцицептивного болю включають без обмеження біль, пов'язаний з хімічними або термічними опіками, порізами шкіри, контузіями шкіри, остеоартритом, ревматоїдним артритом, тендонітом, і міофасціальний біль. Приклади нейропатичного болю включають без обмеження CRPS (синдром комплексного регіонального болю) типу І, CRPS типу II, рефлекторну симпатичну дистрофію (RSD), рефлекторну нейросудинну дистрофію, рефлекторну дистрофію, симпатично підтримуваний больовий синдром, каузалгію, атрофію кісти Sudeck, алгонейродистрофію, плечовий синдром, посттравматичну дистрофію, трійчасту невралгію, постгерпетичну невралгію, біль, викликаний раком, фантомний біль у кінцівках, фіброміалгію, синдром хронічної втоми, біль при ушкодженні спинного мозку, центральний біль після інсульту, радикулопатію, діабетичну нейропатію, біль після інсульту, люетичну нейропатію, і інші хворобливі нейропатичні стани, такі як стани, викликані лікарськими засобами, такими як вінкристин і велкаде. Використовувані в даному описі терміни «синдром комплексного регіонального болю», «CRPS» і «CRPS і пов'язані з ними синдроми» означають розлад у вигляді хронічного болю, що характеризується одним або більше з наступних: болю, спонтанного або викликаного, включаючи алодинію (хворобливу реакцію на подразник, що звичайно 95975 30 не є хворобливим) і гіпералгезію (посилену реакцію на подразник, що звичайно лише незначно хворобливий), біль, що диспропорційний явищу, що його викликає (наприклад, роки сильного болю після розтягання зв'язок гомілковостопного суглоба); регіональний біль, що не обмежується областю розподілу іннервації одного периферичного нерва; і порушення автономної регуляції (наприклад, набряк, зміна кровотоку і гіпергідроз), пов'язане з трофічними змінами шкіри (порушення росту волосся і нігтів і виразка шкіри). Приклади MD і пов'язаних з нею синдромів включають без обмеження ті, котрі описані в патентній публікації US 2004/0091455, опублікованій 13 травня 2004 p., що повністю включена в даний опис як посилання. Конкретні приклади включають без обмеження атрофічну (суху) MD, ексудативну (вологу) MD, вікову макулопатію (ARM), неоваскеуляризацію судинної оболонки ока (CNVM), відшарування пігментного епітелію сітківки (PED) і атрофію пігментного епітелію сітківки (RPE). Приклади захворювань шкіри включають без обмеження ті, котрі описані в патентній публікації US 2005/0214328А1, опублікованій 28 вересня 2005 p., що повністю включена в даний опис як посилання. Конкретні приклади включають без обмеження кератози і пов'язані з ними симптоми, шкірні захворювання або розлади, що характеризуються розростаннями епітелію, вуграми і зморшками. Використовуваний у даному описі термін «кератоз» стосується будь-якого ураження на епідермісі, що відмічається по наявності обмежених розростань рогового шару, включаючи без обмеження актиновий кератоз, себорейний кератоз, кератоакантому, фолікулярний кератоз (хвороба Дар'є), інвертований фолікулярний кератоз, долоннопідошовну кератодермію (РРК, кератоз долонь або підошов), волосяний кератоз і сухий кератоз. Термін «актиновий кератоз» також стосується старечого кератозу (keratosis senilis), старечих бородавок, старечого плоского кератозу, сонячного кератозу, кератодермії або кератоми. Термін «себорейний кератоз» також стосується себорейної бородавки, сенільної бородавки або базальноклітинної папіломи. Кератоз характеризується одним або декількома з наступних симптомів: шорсткуватий зовнішній вигляд, лущення, еритематозні папули, бляшки, спікули або вузлики на відкритих поверхнях шкіри (наприклад, обличчі, кистях рук, вухах, ногах і грудній клітці), розростання кератину, іменовані шкірними рогами, гіперкератоз, телангіектазії, еластоз, пігментований лентигіноз, акантоз, паракератоз, дискератози, папіломатоз, гіперпігментацію базальних клітин, клітинну атипію, мітотичні фігури, аномальну міжклітинну адгезію, щільні запальні інфільтрати і невелику поширеність плоскоклітинних карцином. Приклади шкірних захворювань або розладів, що характеризуються розростаннями епідермісу, включають без обмеження будь-які стани, захворювання або розлади, відзначені присутністю розростань епідермісу, включаючи без обмеження інфекції, пов'язані з вірусом папіломи, миш'якові кератози, ознаку Leser-Trelat, бородавчасту диске 31 ратому (WD), остистий трихостаз (TS), варіабельну еритрокератодермію (EKV), іхтіоз плода («арлекінів» іхтіоз), вроджену вузлуватість пальців кистей, шкірну меланоакантому, порокератоз, псоріаз, плоскоклітинну карциному, зливний і сітчастий папіломатоз (CRP), акрохордони, шкірний ріг, хворобу Cowden (синдром множинної гамартоми), чорний папульозний дерматоз (DPN), синдром епідермального невусу (ENS), простий іхтіоз, заразний молюск, вузлуватий свербець і акантоз, що чорнить (AN). Приклади легеневих захворювань включають без обмеження ті, котрі описані в патентній публікації US 2005/0239842A1, опублікованій 27 жовтня 2005 p., що повністю включена в даний опис як посилання. Конкретні приклади включають без обмеження первинну легеневу гіпертензію (РРН); вторинну легеневу гіпертензію (SPH); сімейну РРН; спорадичну РРН; прекапілярну легеневу гіпертензію; легеневу артеріальну гіпертензію (РАН); гіпертензію легеневої артерії; ідіопатичну легеневу гіпертензію, тромботичну легеневу артеріопатію (ТРА); плексогенну легеневу артеріопатію; функціональну легеневу гіпертензію I-IV класів і легеневу гіпертензію, пов'язану з дисфункцією лівого шлуночка, захворюванням мітрального клапана, стискаючим перикардитом, аортальним стенозом, кардіоміопатією, фіброзом средостіння, аномальним легеневим венозним дренажем, легеневим венооклюзійним захворюванням, колагеновим судинним захворюванням, уродженим серцевим захворюванням, інфекцією вірусу ВІЛ, лікарськими препаратами і токсинами, такими як фенфлураміни, вродженим серцевим захворюванням, легеневою венозною гіпертензією, хронічним обструктивним легеневим захворюванням, інтер етиці альним легеневим захворюванням, порушеним сном диханням, розладом у вигляді альвеолярної гіповентиляції, хронічним впливом великої висоти, легеневим захворюванням немовлят, альвеолярно-капілярною дисплазією, серпоподібноклітинним захворюванням, іншим розладом згортання, хронічними тромбоемболіями, захворюванням сполучної тканини, вовчаком, включаючи системний і шкірний вовчак, шистосомоз, саркоїдоз, або легеневим капілярним гемангіоматозом. Приклади пов'язаних з азбестом розладів включають без обмеження ті, котрі описані в патентній публікації US 2005/0100529, опублікованій 12 травня 2005 p., що повністю включена в даний опис як посилання. Конкретні приклади включають без обмеження мезотеліому, азбестоз, злоякісний плевральний випіт, доброякісний ексудативний випіт, плевральні бляшки, плевральне зневапняковування, дифузійне плевральне стовщення, округлений ателектаз, фіброзні об'ємні утворення і рак легень. Приклади паразитарних захворювань включають без обмеження ті, котрі описані в заявці на патент US № 11/271,963, поданій 14 листопада 2005 p., що повністю включена в даний опис як посилання. Паразитарні захворювання включають захворювання і розлади, викликані людськими внутрішньоклітинними паразитами, такими як без 95975 32 обмеження P. falcifarium, P. ovale, P. vivax, P. malariae, L. donovari, L. infantum, L. aethiopica, L major, L. tropica, L. mexicana, L. braziliensis, T. Gondii, B. microti, B. divergens, B. coli, C. parvum, С cayetanensis, E. histolytica, I. belli, S. mansonii, S. haematobium, Trypanosoma ssp., Toxoplasma ssp. і О. volvulus. Включені також інші захворювання і розлади, викликані нелюдськими внутрішньоклітинними паразитами, такими як без обмеження Babesia bovis, Babesia canis, Banesia Gibsoni, Besnoitia darlingi, Cytauxzoonfelis, Eimeria ssp., Hammondia ssp. і Theileria ssp. Конкретні приклади включають без обмеження малярію, бабезіоз, трипаносомоз, лейшманіоз, токсоплазмоз, менінгоенцефаліт, кератит, амебіаз, лямбліоз, криптоспородіоз, ізоспороз, циклоспороз, мікроспоридоз, аскаридоз, трихуріоз, анкілостомоз, стронгілоїдоз, токсокаріоз, трихіноз, лімфатичний філаріоз, онхоцеркоз, філаріоз, шистосомоз і дерматит, викликаний шистосомами тварин. Приклади імунодефіцитних розладів включають без обмеження ті, котрі описані в заявці на патент US 11/289,723, поданій 30 листопада 2005 р. Конкретні приклади включають без обмеження недостатність аденозиндеамінази, недостатність антитіл при нормальному або підвищеному рівні імуноглобулінів, атаксію-телеангіектазію, синдром «голих» лімфоцитів, звичайний варіабельний імунодефіцит, недостатність Ig з гіпер-IgM, делеції важкого ланцюга Ig, недостатність IgA, імунодефіцит з тимомою, сітчастий дисгенез, синдром Nezelof, селективну недостатність підкласу IgG, минущу гіпогаммаглобулінемію немовлячого віку, синдром Віскотта-Олдрича, Х-зчеплену агаммаглобулінемію, X-зчеплений важкий комбінований імунодефіцит. Приклади розладів ЦНС включають без обмеження ті, котрі описані в патентній публікації US 2005/0143344A1, опублікованій 30 червня 2005 p., що повністю включена в даний опис як посилання. Визначені приклади включають без обмеження бічний аміотрофічний склероз, хворобу Альцгеймера, хворобу Паркінсона, хворобу Хантінгтона, розсіяний склероз і інші нейроімунологічні розлади, такі як синдром Туретта, делірій або порушення свідомості, які виникають протягом короткого періоду часу, й амнестичний розлад або невеликі порушення пам'яті, які виникають під час відсутності інших порушень центральної нервової системи. Приклади ушкоджень ЦНС і пов'язаних з ними синдромів включають без обмежень ті, котрі описані в заявці на патент US № 11/284,403, поданій 18 листопада 2005 p., що повістю включена в даний опис як посилання. Визначені приклади включають без обмеження травму/ушкодження ЦНС і пов'язані з ними синдроми включають без обмежень первинне ушкодження мозку, вторинне ушкодження мозку, травматичне ушкодження мозку, вогнищеве ушкодження мозку, дифузійне ушкодження аксонів, травму голови, струс мозку, синдром порушень після струсу мозку, контузію і поранення мозку, субдуральну гематому, посттравматичну епілепсію, хронічний вегетативний стан, повне SCI (ушкодження спинного мозку), неповне SCI, гостре SCI, підгостре SCI, синдром гострого 33 ушкодження шийного відділу спинного мозку, синдром Брауна-Секара, синдром ушкодження переднього відділу спинного мозку, синдром конуса довгастого мозку, синдром кінського хвоста, нейрогенний шок, спінальний шок, змінений рівень свідомості, головний біль, нудоту, блювання, втрату пам'яті, запаморочення, диплопію, затуманене зір, емоційну лабільність, розлади сну, дратівливість, нездатність сконцентруватися, нервозність, поведінкове порушення, недостатність пізнавальної функції і судоми. Інші захворювання або розлади включають без обмеження вірусні, генетичні, алергійні й аутоімунні захворювання. Визначені приклади включають без обмеження ВІЛ, гепатит, респіраторний дистрес-синдром дорослих, захворювання, пов'язані з резорбцією кісткової тканини, хронічні легеневі запальні захворювання, дерматит, склеродермію, септичний шок, сепсис, ендотоксичний шок, гемодинамічний шок, синдром сепсису, постішемічне реперфузійне ушкодження, менінгіт, псоріаз, фібротичне захворювання, кахексію, хвороби трансплантат проти хазяїна, відторгнення трансплантата, аутоімунне захворювання, ревматоїдний спондиліт, хворобу Крона, виразковий коліт, запальне кишкове захворювання, розсіяний склероз, 95975 34 системний червоний вовчак, ENL (вузлову еритему) при лепрі, радіаційне ушкодження, рак, астму або гіпероксичне альвеолярне ушкодження. Приклади атеросклерозу і пов'язаних з ним станів включають без обмежень ті, котрі описані в патентній публікації US 2002/0054899, опублікованій 9 травня 2002 p., що повністю включена в даний опис як посилання. Визначені приклади включають без обмеження усі форми станів, пов'язаних з атеросклерозом, включаючи рестеноз після судинного втручання, такого як ангіопластика, стентування, атеректомія і шунтування. Усі форми судинних втручань передбачені винаходом, включаючи захворювання серцево-судинної і ниркової систем, такі як без обмеження ниркова ангіопластика, черезшкірне втручання на коронарних артеріях (РСІ), черезшкірна траслюмінальна ангіопластика (РОТА), коронарне шунтування, ангіопластика з імплантацією стента, периферичне черезшкірне транслюмінальне втручання на клубових, стегнових або підколінних артеріях і хірургічне втручання з використанням імпрегнованих штучних трансплантатів. У таблиці нижче представлений перелік основних системних артерій, які можуть потребувати лікування, і вони усі передбачені даним винаходом. 35 Приклади функціональних розладів сну і пов'язаних з ними синдромів включають без обмеження ті, котрі описані в патентній публікації US 2005/0222209А1, опублікованій 6 жовтня 2005 p., що повністю включена в даний опис як посилання. Визначені приклади включають без обмеження храп, апное уві сні, безсоння, нарколепсію, синдром утоми ніг, страхи під час сну, лунатизм, їду під час сну і функціональний розлад сну з хронічними неврологічними або запальними станами. Хронічні неврологічні або запальні стани включають без обмеження синдром комплексного регіонального болю, хронічний біль у поперековій області, біль у кістяковій мускулатурі, артрит, радикулопатію, біль, пов'язаний з онкологічними захворюваннями, фіброміалгію, синдром хронічної втоми, вісцеральний біль, біль у сечовому міхурі, хронічний панкреатит, нейропатії (діабетичну, постгерпетичну, травматичну або запальну) і нейродегенеративні розлади, такі як хвороба Паркінсона, хвороба Альцгеймера, бічний аміотрофічний склероз, розсіяний склероз, хвороба Хантінгтона, брадикінезію; м'язову регідність; паркінсонівський тремор; паркінсонівську ходу; загальмованість рухів; депресію; порушення довгострокової пам'яті, синдром Рубінштейна-Тейбі (RTS); деменцію; нестійкість положення; гіпокінетичні розлади; синуклеїнові розлади; множинні системні атрофії; дегенерацію смугастого і чорного тіл; оливо-мосто-мозочкову атрофію; синдром Шая-Драгера; ураження рухових нейронів з паркінсонівськими ознаками; деменцію, пов'язану з тілом Леві; патологічні розлади Тау; прогресуючий супрануклеарний параліч; кортикобазальну дегенерацію; лобноскроневу деменцію; амілоїдні патологічні розлади; невелике когнітивне порушення; хворобу Альцгеймера з паркінсонізмом; хворобу Вільсона; хворобу Галлервордена-Спатца; хворобу Чедіака-Хагаши; спинномозочкову атаксію SCA-3; Х-зчеплений дистонічний паркінсонізм; пріонове захворювання; гімперкінетичні розлади; хорею; розмашистий гіперкінез кінцівок; дистонічні тремори; бічний аміотрофічний склероз (ALS); травму ЦНС і міоклонус. Приклади гемоглобінопатії і пов'язаних з нею розладів включають без обмеження ті, котрі описані в патентній публікації US 2005/143420A1, опублікованій 30 червня 2005 p., що повністю включена в даний опис як посилання. Визначені приклади включають без обмеження гемоглобінопатію, серпоподібноклітинну анемію і будь-які інші розлади, + пов'язані з диференціацією клітин CD34 . Приклади розладів, пов'язаних з TNF-α і іншими цитокінами, включають без обмеження ті, котрі описані в документах WO 98/03502 і WO 98/54170, що повністю обидва включені в даний опис як посилання. Визначені приклади включають без обмеження: ендотоксемію або синдром токсичного шоку; кахексію; респіраторний дистрес-синдром дорослих; захворювання, пов'язані з резорбцією кісткової тканини, такі як артрит; гіперкальцемію; реакцію трансплантата проти хазяїна; церебральну малярію; запалення; пухлинний ріст; хронічні легеневі запальні захворювання; реперфузійне ушкодження; інфаркт міокарда; інсульт; циркуляторний шок; ревматоїдний артрит; хворобу Крона; 95975 36 ВІЛ-інфекцію і СНІД; інші розлади, такі як ревматоїдний артрит, ревматоїдний спондиліт, остеоартрит і інші артритні стани, септичний шок, сепсис, ендотоксичний шок, хворобу трансплантат проти хазяїна, виснаження, хворобу Крона, виразковий коліт, розсіяний склероз, системний червоний вовчак, ENL при лепрі, ВІЛ, СНІД і опортуністичні інфекції при СНІДі; розлади, пов'язані з цАМФ, такі як септичний шок, сепсис, ендотоксичний шок, гемодинамічний шок і синдром сепсису, постішемічне реперфузійне ушкодження, малярію, мікобактеріальну інфекцію, менінгіт, псоріаз, застійну серцеву недостатність, фібротичні захворювання, кахексію, відторгнення трансплантата, онкогенні або ракові стани, астму, аутоімунні захворювання, радіаційні ушкодження і гіпероксичне альвеолярне ушкодження; вірусні інфекції, такі як інфекції, викликані вірусами герпесу; вірусний кон'юнктивіт; або атопічний дерматит. В інших варіантах здійснення, даний винахід також включає застосування сполук за даним винаходом при різних імунологічних видах застосування, зокрема, як ад'ювантів вакцин, зокрема ад'ювантів протиракової вакцини, як описано в тимчасовій заявці на патент US 60/712,823, поданій 1 вересня 2005 p., що повністю включена в даний опис як посилання. Цей аспект винаходу також стосується застосування сполук за даним винаходом в комбінації з вакцинами для лікування або запобігання раку або інфекційним захворюванням, і інших різних видів застосування імуномодулюючих сполук, таких, котрі забезпечують зниження або десенсибілізацію алергійних реакцій. Дози сполуки за даним винаходом або її фармацевтично прийнятної солі, сольвату, стереоізомера або проліків варіюються, залежно від таких факторів як: конкретне показання, що підлягає лікуванню, профілактиці або веденню пацієнта; вік і стан пацієнта; і кількість другого використовуваного активного засобу, якщо він застосовується. У цілому, сполука за даним винаходом або її фармацевтично прийнятна сіль, сольват, стереоізомер або проліки можна застосовувати в кількості приблизно від 0,1 мг до приблизно 500 мг на день, і дозу можна підібрати звичайним чином (наприклад, однакова кількість, що вводиться щодня в період лікування, профілактики або ведення пацієнта), циклами (наприклад, введення протягом одного тижня з перервою протягом наступного тижня) або в кількості, яка збільшується або зменшується протягом курсу лікування, профілактики або ведення пацієнта. В інших варіантах здійснення, доза може складати приблизно від 1 мг до приблизно 300 мг, приблизно від 0,1 мг до приблизно 150 мг, приблизно від 1 мг до приблизно 200 мг, приблизно від 10 мг до приблизно 100 мг, приблизно від 0,1 мг до приблизно 50 мг, приблизно від 1 мг до приблизно 50 мг, приблизно від 10 мг до приблизно 50 мг, приблизно від 20 мг до приблизно 30 мг, приблизно від 10 мг до приблизно 25 мг, приблизно від 1 мг до приблизно 20 мг. 4.3. Другий активний засіб Сполуку за даним винаходом або її фармацевтично прийнятна сіль, сольват, стереоізомер або 37 проліки можна комбінувати з іншими фармакологічно активними сполуками (другими активними засобами) у способах і композиціях за винаходом. Вважається, що визначені комбінації можуть працювати синергічно при лікуванні визначених типів захворювань або розладів, і станів і симптомів, пов'язаних з такими захворюваннями або розладами. Сполука за даним винаходом або її фармацевтично прийнятна сіль, сольват, стереоізомер або проліки можуть також працювати для полегшення побічних ефектів, пов'язаних з визначеними другими активними засобами, і навпаки. Один або декілька других активних інгредієнтів або засобів можуть застосовуватися в способах і композиціях за винаходом. Другі активні засоби можуть являти собою великі молекули (наприклад, білки) або дрібні молекули (наприклад, синтетичні, неорганічні, металоорганічні або органічні молекули). Приклади крупномолекулярних активних засобів включають без обмеження гематопоетичні ростові фактори, цитокіни і моноклональні і поліклональні антитіла. Визначені приклади активних засобів являють собою анти-СD40 моноклональні антитіла (такі як, наприклад, SGN-40, герцептин, ритуксимаб); інгібітори гістондеацетилази (такі як, наприклад, SAHA і LAQ 824); інгібітори білка-90 теплового шоку (такі як, наприклад, 17-AAG); інгібітори кінази рецептора інсуліноподібного ростового фактора-1; інгібітори кінази рецептора судинного ендотеліального фактора росту (такі як, наприклад, РТК787); інгібітори рецептора інсулінового ростового фактора; інгібітори ацилтрансферази лізофосфатидинової кислоти; інгібітори кінази ІкВ; інгібітори р38МАРK; інгібітори EGFR (епідермального фактора росту) (такі як, наприклад, гефітиніб і ерлотиніб НСI); HER-2 антитіла (такі як, напри® клад, трастузумаб (Herceptin ) і пертузумаб (Omnitarg™)); анти-VEGFR антитіла (проти судинного ендотеліального фактора росту) (такі як, наприклад, бевацизумаб (Avastin™)); інгібітори VEGFR (такі як, наприклад, flk-1 специфічні інгібітори кінази, SU5416 і ptk787/zk222584); інгібітори Р13К (такі як, наприклад, вортманін); інгібітори CMet (такі як, наприклад, РНА-665752); моноклональні антитіла (такі як, наприклад, ритуксимаб ® ® (Rituxan ), тоситумомаб (Веххаr ), едреколомаб ® (Раnоrех ) і G250); і анти-TNF-α антитіла. Приклади дрібномолекулярних активних засобів включають без обмеження дрібномолекулярні протиракові засоби й антибіотики (наприклад, кларитроміцин). Визначені другі активні сполуки, який можна комбінувати зі сполуками за даним винаходом, варіюються, залежно від визначеного показання, що підлягає лікуванню, профілактиці або веденню пацієнта. Наприклад, для лікування, профілактики раку або ведення пацієнта, що страждає ним, другі активні засоби включають без обмеження: семаксаніб; циклоспорин; етанерцепт; доксициклін; бортезоміб; ацивіцин; акларубіцин; акодазол гідрохлорид; акронін; адозелезин; алдеслейкін; алтретамін; амбоміцин; аметантрон ацетат; амсакрин; анастрозол; антраміцин; аспарагіназу; аспе 95975 38 рлін; азацитидин; азетепу; азотоміцин; батимустат; бензодепу; бікалутамід; бісантрен гідрохлорид; біснафід димесилат; бізелесин; блеоміцин сульфат; брехінар натрію; бропіримін; бусульфан; кактиноміцин; калустерон; карацемід; карбетимер; карбоплатин; кармустин; карубіцин гідрохлорид; карзелесин; цедефінгол; целекоксиб; хлорамбуцил; циролеміцин; цисплатин; кладрибін; криснатол месилат; циклофосфамід; цитарабін; дакарбазин; дактиноміцин; даунорубіцин гідрохлорид; децитабін; дексомаплатин; дезагуанін; дезагуанін месилат; діазикуон; доцетаксел; доксорубіцин; доксорубіцин гідрохлорид; дролоксифен; дролоксифен цитрат; дромостанолон пропіонат; дуазоміцин; едатрексат; ефломітин гідрохлорид; елсамітруцин; ендоплатин; енпромат; епіпропідин; епірубіцин гідрохлорид; ербулозол; есорубіцин гідрохлорид; естрамустин; естрамустин фосфат натрію; етанідазол; етопозид; етопозид фосфат; етоприн; фадрозол гідрохлорид; фазарабін; фенритинід; флоксуридин; флударабін фосфат; фторурацил; фторцитабін; фосхідон; фострієцин натрію; гемцитабін; гемцитабін гідрохлорид; гідроксисечовину; ідарубіцин гідрохлорид; іфосфамід; ілмофосин; іпроплатин; іринотекан; іринотекан гідрохлорид; ланреотид ацетат; летрозол; лейпролід ацетат; ліарозол гідрохлорид; лометрексол натрію; ломустин; лосоксантрон гідрохлорид; масопрокол; мехлоретамін гідрохлорид; мегестрол ацетат; меленгестрол ацетат; мелфалан; меногарил; меркаптопурин; метотрексат; метотрексат натрію; метоприн; метуредепу; мітиндомід; мітокарцин; мітокромін; мітогілін; мітомалцин; мітоміцин; мітоспер; мітотан; мітоксантрон гідрохлорид; мікофенольну кислоту; нокодазол; ногаламіцин; ормаплатин; оксисуран; паклітаксел; пегаспаргазу; пеліоміцин; пентамусин; пепломіцин сульфат; перфосфамід; піпоброман; піпосульфан; піроксантрон гідрохлорид; плікаміцин; пломестан; порфімер натрію; порфіроміцин; преднімустин; прокарбазин гідрохлорид; пуроміцин; пуроміцин гідрохлорид; піразофурин; рибоприн; сафінгол; сафінгол гідрохлорид; семустин; симтразен; спарфосат натрію; спарсоміцин; спірогерманій гідрохлорид; спіромустин; спіроплатин; стрептонігрин; стрептозоцин; сулофенур; талісоміцин; текогалан натрію; таксотере; тегафур; телоксантрон гідрохлорид; темопорфін; теніпозид; тероксирон; тестолактон; теаміприн; тіогуанін; тіотепу; тіазофурин; тирапамазин; тереміфен цитрат; трестолон ацетат; трицирбін фосфат; триметрексат; триметресат глюкуронат; трипторелін; тубулозол гідрохлорид; урацил іприт; уредепу; вапреотид; вертепорфін, вінбластин сульфат; вінкристин сульфат; віндезин; віндезин сульфат; вінепідин сульфат; вінгліцинат сульфат; вінлейрозин сульфат; вінорелбін тартрат; вінросидин сульфат; вінзолідин сульфат; ворозол; зеніплатин; зиностатин і зорубіцин гідрохлорид. Інші другі засоби включають без обмеження: 20-епі-1,25-дигідроксивітамін D3; 5-етинілурацил; абіратерон; акларубіцин; ацилфулвен; алеципінол; адозелесин; алдеслейкін; антагоністи ALL-TK; алтретамін; амбамустин; амідокс; аміфостин; амінолевулінову кислоту; амрубіцин; амсакрин; анагре 39 лід; анастрозол; андрографолід; інгібітори ангіогенезу; антагоніст D; антагоніст G; антарелікс; антидорсалізуючий морфогений білок-1; антиандроген із приводу карциноми передміхурової залози; антинеопластон; антисмислові олігонуклеотиди; афідиколін гліцинат; модулятори гена апоптозу; регулятори апоптозу; апуринову кислоту; ара-CDP-DLPTBA (кон'югат тіоефіру-ліпіду 1-β-Dарабінофуранозилцитозину; аргініндеаміназу; асулакрин; атаместан; аксинастатин 1; аксинастатин 2; аксинастатин 3; азасетрон; азатоксин; азатирозин; похідні бакатину III; баланол; батимастат; антагоністи BCR/ABL; бензохлорини; бензоїлстауроспорин; похідні бета лактаму; бетакламіцин В; бетулінову кислоту; інгібітор bFGF (фактора росту фібробластів b); бікалутамід; бісантрен; бісазиридинілспермін; біснафід; бістратен А; бізелесин; брефлат; бропіримін; будотитан; бутионін сульфоксимін; кальципотріол; калфостин С; похідні камптотецину; капеситабін; карбоксамідамінотриазол; карбоксіамідотриазол; CaRest М3; CARN 700; інгібітор, одержаний із хрящової тканини; карзелесин; інгібітори казеїнкінази (ICOS); кастаноспермін; цекропін В; цетрорелікс; хлорини; хлорохіноксалін сульфонамід; цикапрост; циспорфірин; кладрибін; аналоги кломіфену; клодержазол; колісміцин А; колісміцин В; комбретастатин А4; аналог комбретастатину; конагенін; крамбесцидин 816; криснатол; криптофіцин 8; похідні криптофіцину А; курацин А; циклопентантрахінони; циклоплатам; ципеміцин; цитарабін окфостат; цитолітичний фактор; цитостатин; дакліксимаб; децитабін; дегідродидемнін В; деслорелін; дексаметазон; дексіфосфамід; дексразоксан; дексверапаміл; діазихон; дидемнін В; дідокс; діетилнорспермін; дигідро-5азацитидин; дигідротаксол 9-; діоксаміцин; дифенілспіромустин; доцетаксел; докосанол; доласетрон; доксифлуридин; доксорубіцин; дролоксифен; дронабінол; дуокарміцин SA; ебселен; екомустин; еделфозин; едреколомаб; ефломітин; елемен; емітефур; епірубіцин; епристерид; аналог естрамустину; агоністи естрогену; антагоністи естрогену; етанідазол; етопозид фосфат; ексеместан; фадрозол; фазарабін; фенретинід; філграстим; фінастерид; флавопіридол; флезеластин; флуастерон; флударабін; фтордауноруніцин гідрохлорид; форфенімекс; форместан; фострієцин; фотемустин; гадоліній тексафірин; нітрат галію; галоцитабін; ганірелікс; інгібітори гелатинази; гемцитабін; інгібітори глутатіону; гепсульфам; герегулін; гексаметилен бісакетамід; гіперцин; ібандронову кислоту; ідарубіцин; ідоксифен; ідрамантон; ® ілмофозин; іломастат; іматиніб (Gleevec ), іміхімод; імуностимулюючі пептиди; інгібітор рецептора інстуліноподібного фактора росту-1; агоністи інтерферону; інтерферони; інтерлейкіни; йобенгуан; йододоксорубіцин; 4-іпомеанол; іроплакт; ірсогладин; ізобенгазол; ізохомогалікондрин В; ітасетрон; ясплакінолід; кагалалід F; триацетат ламеларину-N; ланреотид; лейнаміцин; ленограстим; лентинансульфат; лептолстатин; летрозол; фактор, інгібуючий лейкоз; лейкоцитарний альфаінтерферон; лейпролід+естроген+прогестерон; лейпрорелін; левамісол; ліарозол; лінійний аналог поліаміну; ліпофільний дисахаридний пептид; лі 95975 40 пофільні сполуки платини; лісоклінамід 7; лобаплатин; ломбрицин; лометрексол; лонідамін; лосоксантрон; локсорибін; луртотекан; лютецію тексафірин; лізофілін; літичні пептиди; мейтансин; маностатин А; маримастат; масопрокол; маспін; інгібітори матрилізину; інгібітори матричної металопротеїнази; меногарил; мербарон; метерелін; метіоніназу; метоклопрамід; інгібітор MIF (міграції макрофагів); міфепристон; мілтефозин; міримостим; мітолактол; аналоги мітоміцину; мітонафід; мітотоксин фактор росту фібробластів-сапорин; мітоксантрон; мофаротен; молграмостим; ербітукс, людський хоріонічний гонадотропін; монофосфорил ліпід А+стрептокіназа клітинної стінки мікобактрії; мопідамол; іпритний протираковий засіб; мікапероксид В; екстракт мікобактеріальної клітинної стінки; міриапорон; N-ацетилдиналін; N-заміщені бензаміди; нафарелін; гарестип; налоксон+пентазоцин; напавін; нафтерпін; нартограстим; недаплатин; неморубіцин; неридронову кислоту; нілутамід; нізаміцин; модулятори оксиду азоту; нітроксидний антиоксидант; нітрулін; облі® мерсен (Genasense ); 06-бензилгуанін; октреотид; окіценон; олігонуклеотиди; онапристон; ондансетрон; орацин; пероральний індуктор цитокіну; ормаплатин; осатерон; оксаліплатин; оксауноміцин; паклітаксел; аналоги паклітакселу; похідні паклітакселу; плауамін; пальмітоїлризоксин; памідронову кислоту; панакситріол; паноміфен; парабактин; пазеліптин; пегаспаргазу; пелдесин; пентосан полісульфат натрію; пентостатин; пентрозол; перфлуброн; перфосфамід; периліловий спирт; феназиноміцин; фенілацетат; інгібітори фосфатази; піцибаніл; пілокарпін гідрохлорид; пірарубіцин; піритрексим; плацетин А; плацетин В; інгібітор активатора плазміногена; комплекс платини; сполуки платини; комплекс платини-триаміну; порфімер натрію; порфіроміцин; преднізон; пропіл бісакридон; простагландин J2; імуномодлуятори на основі білка А; інгібітори протеїнкінази С; мікроалгал; інгібітори протеїнтирозинфосфатази; інгібітори пурин нуклеозидфосфорилази; пурпурини; піразолакридин; кон'югат піридоксилованого гемоглобіну-поліоксіетилену; антагоністи raf (білкарегулятора експресії α-фетопротеїну); інгібітори ras фарнесил протеїнтрансферази, інгібітори ras; інгібітор ras-GAP (активатора гуанозин-5трифосфатази); деметилований ретеліптин; етидронат ренію Re 186; ризоксин; біозими; RII ретинамід; рогітукін; ромуртид; рехінімекс; рубігінон В1; рубоксил; сафінгол; саінтопін; SarCNU Sаr(хлорнітрозосечовину); сакрофітол А; сарграмостин; міметики Sdi; семустин; інгібітор 1, одержуваний при старінні; смислові олігонуклеотиди; інгібітори передачі сигналів; сизофіран; собузоксан; боркаптат натрію; фенілацетат натрію; солверол; білок, що зв'язує соматомедин; сонермін; спарфозову кислоту; спікаміцин D; спіромустин; спленопентин; спонгістатин 1; скваламін; стипіамід; інгібітори стромелізину; сульфінозин; надактивний антагоніст вазоактивного кишкового пептиду; сурадисту; сурамін; свінсонін; талімустин; тамоксифен метйодид; тауромустин; тазаротен; текогалан натрію; тегафур; телурапірилій; інгібітори теломерази; темопорфін; теніпозид; тетрахло 41 рдекаоксид; тетразомін; талібластин; тіокоралін; тромбопоетин; міметик тромбопоетину; тималфазин; агоніст рецептора тимопоетину; тимотринан; тиреостимулюючий гормон; етилетіопурпурин олова; тирапазамін; титаноцен біхлорид; топсентин; тореміфен; інгібітори трансляції; третиноїн; триацетилуридин; трицирибін; триметрексат; трипторелін; тропізетрон; туростерид; інгібітори тирозинкінази; інгібітори UBC; убенімекс; інгібуючий ріст фактор, одержаний з урогенітального синуса; антагоністи рецептора урокінази; .вапреотид; варіолін В; веларесол; верамін; вердини; вертепорфін; вінорелбін; вінксалтин; вітаксин; ворозол; занотерон; зеніплатин; зиласкорб і циностатин стималамер. Визначені другі активні засоби включають без обмеження 2-метоксіестрадіол, теломестатин, індуктори апоптозу в клітинах множинної мієломи (такі як, наприклад, TRAIL), статини, семаксаніб, циклоспорин, етанерцепт, доксициклін, бортезо® міб, облімерсен (Genasense ), ремікад, доцетаксел, целекоксиб, мелфалан, дексаметазон ® (Decadron ), стероїди, гемцитабін, цисплатин, темозоломід, етопозид, циклофосфамід, темодар, карбоплатин, прокарбазин, гліадел, тамоксифен, ® топотекан, метотрексат, Arisa , такол, таксотере, фторурацил, лейковорин, іринотекан, кселоду, СРТ-11, інтерферон альфа, пегильований інтерферон альфа (наприклад, PEG INTRON-A), капецитабін, цисплатин, тіотепу, флударабін, карбоплатин, ліпосомальний даунорубіцин, цитарабін, доксетаксол, паклітаксел, вінбластин, IL-2, GMCSF, дакарбазин, вінорелбін, золедронову кислоту, палмітронат, біаксин, бусульфан, преднізон, бісфосфанат, триоксид миш'яку, вінкристин, док® сорубіцин (Doxil ), паклітаксел, генцикловір, адрі® аміцин, естрамустин натрійфосфат (Emcyt ), суліндак і етопозид. Аналогічним чином, приклади визначених других засобів відповідно до показань, що підлягають лікуванню, профілактиці або веденню пацієнтів, можна знайти в наступних посиланнях, усі з який повністю включені в даний опис як посилання: патенти US 6281230 і 5635517; заявки на патент US 10/411649, 10/483213, 10/411656, 10/693794, 10/699154 і 10/981189; і попередні заявки на патенти US 60/554923, 60/565172, 60/626975, 60/630599, 60/631870 і 60/533862. Приклади другого активного засобу, який можна застосовувати для лікування, профілактики і/або ведення пацієнтів при болю, включають без обмеження звичайні терапевтичні засоби, застосовувані для лікування або профілактики болю, такі як антидепресанти, протисудомні засоби, гіпотензивні засоби, анксиолітики, блокатори кальцієвих каналів, м'язові релаксанти, ненаркотичні анальгетики, опіоїдні анальгетики, протизапальні засоби, інгібітори СОХ-2, імуномодулюючі засоби, агоністи або антагоністи альфа-адренергічних рецепторів, імуносупресорні засоби, кортикостероїди, гіпербаричний кисень, кетамін, інші анальгетичні засоби, антагоністи NMDA (N-метил-dаспартату) і інші терапевтичні засоби, що розкриті, наприклад, у довіднику Physician's Desl Reference 2003. Визначені приклади включають без обме 95975 42 ® ження ацетат саліцилової кислоти (аспірин ), це® ® лекоксиб (Celebrex ), Enbrel , кетамін, габапентин ® ® (Neurontin ), фенітоїн (Dilantin ), карбамазепін ® ® (Tegretol ), окскарбазепін (Trileptal ), вальпроєву ® кислоту (Depakene ), морфін сульфат, гідроморфон, преднізон, гризеофульвін, пентоній, алендронат, дифенгідрамід, гуанетидин, кеторолак ® (Acular ), тирокальцитонін, диметилсульфоксид ® (DMSO), клонідин (Catapress ), бретилій, кетансерин, резерпін, дроперидол, атропін, фентоламін, бупівакаїн, лідокаїн, ацетамінофен, нортриптилін ® ® (Pamelor ), амітриптилін (Elavil ), іміпрамін ® ® (Tofranil ), доксепін (Sinequan ), кломіпрамін ® ® (Anafranil ), флюоксетин (Prozac ), сертралін ® ® (Zoloft ), нефазодон (Serzone ), венлафаксин ® ® (Effexor ), тразадон (Desyrel ), бупропіон ® (Wellbutrin ), мексилетин, ніфедипін, пропранолол, трамадол, ламотригін, зиконотид, кетамін, декстрометорфан, бензодіазепін, баклофен, тізанідин і феноксибензамін. Приклади другого активного засобу, який можна застосовувати для лікування, профілактики і/або ведення пацієнтів з MD і пов'язаними з нею синдромами, включають без обмеження стеорїд, світловий сенсибілізатор, інтегрин, антиоксидант, інтерферон, похідне ксантину, гормон росту, нейротрофічний фактор, регулятор неоваскуляризації, анти-VEGF антитіло, простагландин, антибіотик, фітоестроген, антизапальну сполуку або сполуку проти ангіогенезу, або їхню комбінацію. Визначені приклади включають без обмеження вертепорфін, пурлітин, ангіостатичний стероїд, rhuFab (рекомбінантний людський фрагмент антитіла Fab), інтерферон-2α, пентоксифілін, етіопурпурин олова, мотексафін лютецію, 9-фтор-11,21-дигідрокси-16,171-метилетилідинбіс(окси)прегна-1,4-дієн-3,20-діон, латанопрост (див. патент US 6225348), тетрациклін і його похідні, рифаміцин і його похідні, макроліди, метронідазол (патенти US 6218369 і 6015803), геністеїн, геністин, 6'-О-Маl геністин, 6'О-Ас геністин, даідзеїн, даідзин, 6'-O-Mal даідзин, 6'-О-Ас даідзин, гліцитеїн, гліцитин, 6'-O-Mal гліцитин, біочанін А, формононетин (патент US 6001368), триамсинолонацетомід, дексаметазон (патент US 5770589), талідомід, глутатіон (патент US 5632984), основний фактор росту фібробластів (bFGF), що трансформує фактор росту b (TGF-b), одержаний з мозку нейротрофічний фактор (BDNF), фактор-0 активатор плазміногена 2 типи (РАІ-2), ΕΥΕ101 (Eyetech Pharmaceuticals), LY333531 (Eli Lilly), Miravant і імплантат RETISERT (Bausch & Lomb). Усі наведені вище посилання повністю включені в даний опис як посилання. Приклади другого активного засобу, який можна застосовувати для лікування, профілактики і/або ведення пацієнтів зі шкірними захворюваннями, включають без обмеження кератолітики, ретиноїди, α-гідроксикислоти, антибіотики, колаген, ботуліновий токсин, інтерферон і імуномодуляторні засоби. Визначені приклади включають без обмеження 5-фторурацил, масопрокол, трихлороцтову кислоту, саліцилову кислоту, молочну кислоту, лактат амонію, сечовину, третиноїн, ізотретиноїн, антибіотики, колаген, ботуліновий токсин, інтерферон, кортикостероїд, трансретиноєву 43 кислоту і колагени, такі як людський плацентарний колаген, плацнетарний колаген тварин, дермалоген, алодерм, фасцію, циметру, аутологен, зидерм, зипласт, расопласт і ізолаген. Приклади другого активного засобу, який можна застосовувати для лікування, профілактики і/або ведення пацієнтів з легеневою гіпертензією і пов'язаними з нею розладами, включають без обмеження антикоагулянти, діуретики, серцеві глікозиди, блокатори кальцієвих каналів, судинорозширювальні засоби, аналоги простацикліну, антагоністи ендотеліну, інгібітори фосфодіестерази (наприклад, інгібітори PDE V), інгібітори ендопептидази, засоби, які знижують рівень ліпідів, інгібітори тромбоксану і інші терапевтичні засоби, які, як відомо, знижують тиск у легеневій артерії. Визначені приклади включають без обмеження ® варфарин (Coumadin ), діуретик, серцевий глікозид, дигоксин-кисень, дилтіазем, ніфедипін, судинорозширювальний засіб, такий як простациклін (наприклад, простагландин 12 (PG12), епопросте® ® нол (ЕРО, Floran ), трепростиніл (Remodulin ), ® оксид азоту (N0), босентан (Tracleer ), аміодипін, ® ® епопростанол (Floran ), трепростиніл (Remodulin ), ® простациклін тадалафіл (Cialis ), симвастатин ® ® (Zocor ), омапатрилат (Vanlev ), ірбесатран ® ® (Avapro ), правастатин (Pravachol ), дигоксин, L® аргінін, ілопрост, бетапрост і силденафіл (Viagra ). Приклади другого активного засобу, який можна застосовувати для лікування, профілактики і/або ведення пацієнтів з розладами, пов'язаними з впливом азбесту, включають без обмеження антрациклін, платину, алкілуючий агент, облімерсен ® (Genasense ), цисплатин, циклофосфамід, темодар, карбоплатин, прокарбазин, гліадел, тамоксифен, топотекан, метотрексат, таксотере, іринотекан, капецитабін, цисплатин, тіотепу, флударабін, карбоплатин, ліпосомний даунорубіцин, цитарабін, доксетаксол, паклітаксел, вінбластин, IL-2, GMCSF, дакарбазин, вінорелбін, золедронову кислоту, палмітронат, біаксин, бусульфан, преднізон, бісфосфонат, миш'яковий триоксид, вінкристин, ® доксорубіцин (Doxil ), ганцикловір, адріаміцин, блеоміцин, гіалуронідазу, мітоміцин С, мепакрин, тетрациклін і гемцитабін. Приклади другого активного засобу, який можна застосовувати для лікування, профілактики і/або ведення пацієнтів з паразитарними захворюваннями, включають без обмеження хлорохін, хінін, хінідин, піриметамін, сульфадіазин, доксициклін, кліндаміцин, мефлохін, галофантрин, примахін, гідроксихлорохін, прогуаніл, атоваквон, азитроміцин, сурамін, пентамідин, метарсопрол, ніфуртимокс, бензнідазол, амфотерицин В, сполуки пентавалентної сурми (наприклад, стибоглюкуронат натрію), інтерферон гамма, ітраконазол, комбінацію мертвих промастигот і БЦЖ, лейковорин, кортикостероїди, сульфонамід, спіраміцин, IgG (серологію), триметоприм і сульфаметоксазол. Приклади другого активного засобу, який можна застосовувати для лікування, профілактики і/або ведення пацієнтів з імунодефіцитними розладами, включають без обмеження: антибіотики (лікувальні або профілактичні), такі як, але не обмежуючись цим, ампіцилін, кларитроміцин, тетра 95975 44 циклін, пеніцилін, цефалоспорини, стрептоміцин, канаміцин і еритроміцин; противірусні засоби, такі як без обмеження амантадин, римантадин, ацикловір і рибаварин; імуноглобулін; плазму; препарати, що підсилюють імунітет, такі як без обмеження левамісол і ізоприносин; біологічні агенти, такі як без обмеження гамма-глобулін, фактор перенесення, інтерлейкіни й інтерферони; гормони, такі як без обмеження тимусні гормони; і інші імунологічні агенти, такі як без обмеження стимулятори В-клітин (наприклад, BAFF/BlyS), цитокіни (наприклад, IL-2, IL-4 і IL-5), фактори росту (наприклад, TGF-α), антитіла (наприклад, анти-СD40 і IgM), олігонуклеотиди, що містять неметиловані мотиви CpG, і вакцини (наприклад, вірусні і пухлинні пептидні вакцини). Приклади другого активного засобу, який можна застосовувати для лікування, профілактики і/або ведення пацієнтів з розладами ЦНС, включають без обмеження: агоніст або антагоніст допаміну, такий як без обмеження леводопа, LDOPA, кокаїн, α-метилтирозин, резерпін, тетрабеназин, бензотропін, паргілін, фенодолпам месилат, каберголін, праміпексол дигідрохлорид, ропінорол, амантадин гідрохлорид, селегілін гідрохлорид, карбідопа, перголід месилат, синемет CR, і симетрел; інгібітор МАО (моноаміноксидази), такий як без обмеження іпроніазид, клоргілін, фенелзин і ізокарбоксазид; інгібітор СОМТ (катехоло-метилтрансферази), такий як без обмеження толкапон і ентакапон; інгібітор холінестерази, такий як без обмеження фізостигмін саліцилат, фізостигмін сульфат, фізостигмін бромід, неостигмін бромід, неостигмін метилсульфат, амбеноній хлорид, едрофоній хлорид, такрин, пралідоксим хлорид, обідоксим хлорид, тримедоксим бромід, діацетил моноксим, ендрофоній, піридостигмін і демекарій; протизапальний засіб, такий як без обмеження напроксен натрію, диклофенак натрію, дифлокенак калію, целекоксиб, суліндак, оксапрозин, дифлунісал, етодолак, мелоксикам, ібупрофен, кетопрофен, набуметон, рефекоксиб, метотрексат, лефлуномід, сульфасалазин, солі золота, імуноглобулін RHo-D, мікофенілат мофетил, циклоспорин, азатіоприн, такролімус, басиліксимаб, даклізумаб, саліцилову кислоту, ацетилсаліцилову кислоту, метилсаліцилат, дифлунісал, салсалат, олсалазин, сульфасалазин, ацетамінофен, індометацин, суліндак, мефенамову кислоту, меклофенамат натрію, толметин, кеторолак, дихлофенак, флурбінпрофен, оксапрозин, піроксикам, мелоксикам, ампіроксикам, дроксикам, півоксикам, теноксикам, фенілбутазон, оксифенбутазон, антипірин, амінопірин, апазон, зилейтон, ауротіоглюкозу, тіомалат золота натрію, ауранофін, метотрексат, колхіцин, алопуринол, пробенецид, сульфінпіразон і бензбромарон або бетаметазон і інші глюкокортикоїди; і протиблювотний засіб, такий як без обмеження метоклопромід, домперидон, прохлорперазин, прометазин, хлорпромазин, триметобензамід, ондансетрон, гранісетрон, гідроксизин, ацетиллейцин моноетаноламін, алізаприд, азасетрон, бензхінамід, біетанаутин, бромоприд, буклізин, клебоприд, циклізин, дименгідринат, дифенідол, доласетрон, меклізин, металлатал, ме 45 топімазин, набілон, оксипернідил, піпамазин, скополамін, сулпірид, тетрагідроканабінол, тіетилперазин, тіопроперазин, тропісетрон і їх суміш. Приклади другого активного засобу, який можна застосовувати для лікування, профілактики і/або ведення пацієнтів з ушкодженнями ЦНС і пов'язаними з ними синдромами, включають без обмеження імуномодуляторні агенти, імуносупресивні агенти, гіпотензивні засоби, протисудомні засоби, фібринолітичні засоби, протитромбоцитарні засоби, антипсихотичні засоби, антидепресанти, бензодіазепіни, буспірон, амантадин і інші відомі або звичайні засоби, застосовувані у пацієнтів із травмою/ушкодженням ЦНС і пов'язаними з ними синдромами. Визначені приклади включають без обмеження: стероїди (наприклад, глюкокортикоїди, такі як без обмеження метилпреднізолон, дексметазон і бетаметазон); протизапальний засіб, включаючи без обмеження напроксен натрію, диклофенак натрію, диклофенак калію, целекоксиб, суліндак, оксапрозин, дифлунісал, етодолак, мелоксикам, ібупрофен, кетопрофен, набуметон, рефекоксиб, метотрексат, лефлуномід, сульфасалазин, солі золота, імуноглобулін RHo-D, мікофенілат мофетил, циклоспорин, азатіоприн, такролімус, басиліксимаб, даклізумаб, саліцилову кислоту, ацетилсаліцилову кислоту, метилсаліцилат, дифлунісал, салсалат, олсалазин, сульфасалазин, ацетамінофен, індометацин, суліндак, мефенамову кислоту, меклофенамат натрію, толметин, кеторолак, дихлофенак, флурбінпрофен, оксапрозин, піроксикам, мелоксикам, ампіроксикам, дроксикам, півоксикам, теноксикам, фенілбутазон, оксифенбутазон, антипірин, амінопірин, апазон, зилейтон, ауротіоглюкозу, тіомалат золота натрію, ауранофін, метотрексат, колхіцин, алопуринол, пробенецид, сульфінпіразон і бензбромарон; аналог цАМФ, включаючи без обмеження dbцАМФ; агент, який включає препарат метилфенідату, що включає 1-треометилфенідат, dтреометилфенідат, dl-треометилфенідат, 1еритрометилфенідат, d-еритрометилфенідат, dlеритрометилфенідат, і їх суміш; і діуретичний засіб, такий як без обмеження маніт, фуросемід, гліцерин і сечовина. Приклади другого активного засобу, який можна застосовувати для лікування, профілактики і/або ведення пацієнтів з функціональними розладами сну і пов'язаними з ними синдромами, включають без обмеження трициклічний антидепресивний засіб, селективний інгібітор зворотного захоплення серотоніну, антиепілептичний засіб (габапентин, прегабалін, карбамазепін, окскарбазепін, левітирацетам, топірамат), антиаритмічний засіб, засіб, що блокує кальцієві канали, селективний інгібітор медіаторів запалення, опіоїдний засіб, другу протизапальну сполуку, комбінована засіб і інші відомі або звичайні засоби, застосовувані при лікуванні порушень сну. Визначені приклади включають без обмеження нейронтин, оксиконтин, морфін, топірамат, амітриптилін, нортриптилін, карбамазепін, леводопу, L-DOPA, кокаїн, αметилтирозин, резерпін, тетрабеназин, бензотропін, паргілін, фенодолпам месилат, каберголін, праміпексол дигідрохлорид, ропінорол, амантадин 95975 46 гідрохлорид, селегілін гідрохлорид, карбідопу, перголід месилат, синемет CR, симетрел, іпроніазид, клоргілін, фенелзин, ізокарбоксазид, толкапон, ентакапон, фізостигмін саліцилат, фізостигмін сульфат, фізостигмін бромід, неостигмін бромід, неостигмін метилсульфат, амбеноній хлорид, едрофоній хлорид, такрин, пралідоксим хлорид, обідоксим хлорид, тримедоксим бромід, діацетил моноксим, ендрофоній, піридостигмін, демекарій, напроксен натрію, диклофенак натрію, диклофенак калію, целекоксиб, суліндак, оксапрозин, дифлунісал, етодолак, мелоксикам, ібупрофен, кетопрофен, набуметон, рефекоксиб, метотрексат, лефлуномід, сульфасалазин, солі золота, імуноглобулін RHo-D, мікофенілат мофетил, циклоспорин, азатіоприн, такролімус, басиліксимаб, даклізумаб, саліцилову кислоту, ацетилсаліцилову кислоту, метилсаліцилат, дифлунісал, салсалат, олсалазин, сульфасалазин, ацетамінофен, індометацин, суліндак, мефенамову кислоту, меклофенамат натрію, толметин, кеторолак, дихлофенак, флурбінпрофен, оксапрозин, піроксикам, мелоксикам, ампіроксикам, дроксикам, півоксикам, теноксикам, фенілбутазон, оксифенбутазон, антипірин, амінопірин, апазон, зилейтон, ауротіоглюкозу, тіомалат золота натрію, ауранофін, метотрексат, колхіцин, алопуринол, пробенецид, сульфінпіразон, бензбромарон, бетаметазон і інші глюкокортикоїди, метоклопромід, домперидон, прохлорперазин, прометазин, хлорпромазин, триметобензамід, ондансетрон, гранісетрон, гідроксизин, ацетиллейцин моноетаноламін, алізаприд, азасетрон, бензхінамід, біетанаутин, бромоприд, буклізин, клебоприд, циклізин, дименгідринат, дифенідол, доласетрон, меклізин, металлатал, метопімазин, набілон, оксипернідил, піпамазин, скополамін, сулпірид, тетрагідроканабінол, тіетилперазин, тіопроперазин, тропісетрон і їх суміш. Приклади другого активного засобу, який можна застосовувати для лікування, профілактики і/або ведення пацієнтів з гемоглобінопатією і пов'язаними з нею розладами, включають без обмеження: інтерлейкіни, такі як IL-2 (включаючи рекомбінантний IL-II ("rIL2") і канарипокс IL-2), IL-10, IL12 і IL-18; інтерферони, такі як інтерферон альфа2а, інтерферон альфа-2b, інтерферон альфа-n1, інтерферон альфа-n3, інтерферон бета-іа, і інтерферон гамма-Ib, і G-CSF (гранулоцитарний колонієстимулюючий фактор); гідроксисечовину; бутирати або похідні бутиратів; оксид азоту; HTMOXIN™ (NIPRJSAN™; див. патент US 5800819); антагоністи каналів Gardos, такі як клодержазол і похідні триарилметану; дефероксамін; білок С; і переливання крові, або замінників крові, таких як Hemospan™ або Hemospan™ PS (сангарт). Введення сполуки за даним винаходом або її фармацевтично прийнятної солі, сольвату, стереоізомера або проліків і других активних засобів пацієнту може відбуватися одночасно або послідовно однаковими або різними шляхами введення. Придатність визначеного шляху введення, використовуваного для визначеного активного засобу, буде залежати від самого активного засобу (наприклад, чи можна його вводити перорально без 47 руйнування перед надходженням у потік крові) і захворювання, що піддається лікуванню. Переважним шляхом введення для сполук за даним винаходом є пероральний. Переважні шляхи введення для других активних засобів або інгредієнтів за винаходом відомі середнім фахівцям у даній галузі. Див., наприклад, довідник Physicians' Desc th Reference, 1755-1760 (56 ed., 2002). В одному варіанті здійснення винаходу, другий активний засіб вводиться внутрівенно або підшкірно й один або два рази на день у кількості приблизно від 1 до приблизно 1000 мг, приблизно від 5 до приблизно 00 мг, приблизно від 10 до приблизно 350 мг або приблизно від 50 до приблизно 200 мг. Визначена кількість другого активного засобу буде залежати від визначеного застосовуваного засобу, типу захворювання, що піддається лікуванню або веденню, тяжкості і стадії захворювання і кількості (кількостей) сполук за винаходом і будь-яких необов'язкових додаткових активних засобів, що одночасно вводяться пацієнту. Як обговорюється в інших розділах даного опису, винахід включає спосіб зменшення, лікування і/або запобігання побічним або небажаним ефектам, пов'язаним зі звичайним лікуванням, включаючи без обмеження хірургічне лікування, хіміотерапію, променеву терапію, гормональну терапію, біологічну терапію і імунотерапію. Сполуки за винаходом й інші активні інгредієнти можна вводити пацієнту перед, під час або після виникнення побічного ефекту, пов'язаного зі звичайним лікуванням. 4.4 Циклічне лікування У визначених варіантах здійснення, профілактичні або терапевтичні засоби за винаходом циклічно вводяться пацієнту. Циклічне лікування включає введення активного засобу протягом деякого періоду часу, і повторення цього послідовного введення. Циклічне лікування може знизити розвиток стійкості до одного або декількох з цих видів лікування, допомогти уникнути або знизити побічні ефекти одного з видів лікування і/або підвищити ефективність лікування. Отже, в одному визначеному варіанті здійснення, сполука за винаходом вводиться щодня однією або дробовими дозами циклом від чотирьох до шести тижнів з періодом відпочинку приблизно в один тиждень або два тижні. Винахід, крім того, допускає збільшення частоти, кількості і тривалості циклів введення. Таким чином, інший визначений варіант здійснення винаходу включає введення сполуки за винаходом протягом більшої кількості циклів, ніж звичайно, коли вона вводиться окремо. У ще одному визначеному варіанті здійснення, сполука за винаходом вводиться протягом більшої кількості циклів, що звичайно викликало б токсичність, що обмежує дозу, у пацієнта, якому також не вводиться другий активний інгредієнт. В одному варіанті здійснення, сполука за винаходом вводиться щодня і безупинно протягом трьох або чотирьох тижнів у дозі приблизно від 0,1 мг до приблизно 500 мг на день, з наступною перервою на один або два тижні. В іншому варіанті здійснення, доза може складати приблизно від 1 мг до приблизно 300 мг, приблизно від 0,1 мг до 95975 48 приблизно 150 мг, приблизно від 1 мг до приблизно 200 мг, приблизно від 10 мг до приблизно 100 мг, приблизно від 0,1 мг до приблизно 50 мг, приблизно від 1 мг до приблизно 50 мг, приблизно від 10 мг до приблизно 50 мг, приблизно від 20 мг до приблизно 30 мг або приблизно від 1 мг до приблизно 20 мг, з наступною перервою. В одному варіанті здійснення винаходу, сполука за винаходом і другий активний інгредієнт вводяться перорально, при введенні сполуки за винаходом, яке відбувається за 30-60 хвилин до другого активного інгредієнта, протягом циклу від чотирьох до шести тижнів. В іншому варіанті здійснення винаходу, комбінація сполуки за винаходом і другого активного інгредієнта вводиться внутрішньовенним вливанням протягом приблизно 90 хвилин за кожен цикл. Звичайно, кількість циклів, протягом яких проводиться комбіноване лікування пацієнта, буде складати приблизно від одного до приблизно 24 циклів, типовіше приблизно від двох до приблизно 16 циклів, а ще типовіше приблизно від чотирьох до приблизно трьох циклів. 4.5 Фармацевтичні композиції і лікарські форми Фармацевтичні композиції можна використовувати при одержанні окремих, одиночних стандартних лікарських форм. Фармацевтичні композиції і лікарські форми за винаходом включають сполуку за винаходом або її фармацевтично прийнятну сіль, сольват, стереоізомер або проліки. Фармацевтичні композиції і лікарські форми за винаходом можуть, крім того, включати один або декілька ексципієнтів. Фармацевтичні композиції і лікарські форми за винаходом можуть також включати один або декілька додаткових активних інгредієнтів. Приклади необов'язкових других або додаткових активних інгредієнтів описані вище в розділі 4.3. Одиничні дозовані стандартні лікарські форми за винаходом придатні для перорального, через слизові оболонки (наприклад, назального, під'язичного, піхвового, защічного або прямокишкового), парентерального (наприклад, підшкірного, внутрішньовенного, болюсного ін'єкційного, внутрішньом'язового або внутрішньоартеріального), місцевого (наприклад, у вигляді очних крапель або інших офтальмологіческих препаратів), трансдермального або черезшкірного введення пацієнту. Приклади дозованих форм включають без обмеження: звичайні таблетки; овальні, покриті таблетки; капсули, такі як м'які еластичні желатинові капсули; саше; пастилки; коржі; дисперсії; супозиторії; порошки; аерозолі (наприклад, інтраназальні спреї або інгалятори); гелі; рідкі дозовані форми, що придатні для перорального введення і введення через слизові оболонки пацієнту, включаючи суспензії (наприклад, водні або неводні рідкі суспензії, емульсії масло-у-воді або рідкі емульсії вода-в-маслі), розчини й еліксири; рідкі дозовані форми, що придатні для парентерального введення пацієнту; очні краплі або інші офтальмологічні препарати, що придатні для місцевого введення; і стерильні тверді препарати (наприклад, кристалічні або аморфні тверді препарати), що можуть розчинятися для 49 забезпечення рідких лікарських форм, які придатні для парентерального введення пацієнту. Склад, форма і тип дозованих форм за винаходом буде звичайно змінюватися від їхнього застосування. Наприклад, дозована форма, застосовувана при гострому лікуванні захворювання, може містити більші кількості одного або декількох активних інгредієнтів, які вона включає, ніж дозована форма, застосовувана при хронічному лікуванні того ж захворювання. Аналогічним чином, парентеральна дозована форма може містити менші кількості одного або декількох активних інгредієнтів, які вона включає, ніж дозована форма, застосовувана при хронічному лікуванні того ж захворювання. Ці й інші аспекти, по яких визначені дозовані форми, охоплювані даним винаходом, будуть варіюватися одна від одної, будуть цілком очевидні для фахівців у даній галузі. Див., наприклад, документ Remington's Pharmaceutical th Sciences, 18 ed., Mack Publishing, Easton PA (1990). Типові фармацевтичні композиції і дозовані форми включають один або декілька ексципієнтів. Придатні ексципієнти добре відомі фахівцям в галузі фармакології, і необмежуючі приклади придатних ексципієнтів представлені в даному описі. Те, чи придатний конкретний ексципієнт для включення у фармацевтичну композицію і дозовану форму, залежить від різноманітних факторів, добре відомих у даній галузі, включаючи без обмеження шлях, яким дозована форма буде введена пацієнту. Наприклад, пероральні дозовані форми, такі як таблетки, можуть містити ексципієнти, що не придатні для застосування в парентеральних лікарських формах. Придатність конкретного ексципієнта може також залежати від визначених активних інгредієнтів у дозованій формі. Наприклад, руйнування деяких активних інгредієнтів можна прискорити деякими ексципієнтами, такими як лактоза, або при контакті з водою. Активні інгредієнти, що включають первинні або вторинні аміни, особливо сприйнятливі до такого прискореного руйнування. Отже, даний винахід включає фармацевтичні композиції і дозовані форми, які необов'язково містять небагато лактози, інших моно- або дисахаридів. Використовуваний у даному описі термін «позбавлена лактози» означає, що кількість присутньої лактози, якщо вона є, власне кажучи, недостатня для збільшення швидкості руйнування активного інгредієнта. Позбавлені лактози композиції за винаходом можуть включати ексципієнти, що добре відомі в даній галузі і перераховані, наприклад, у Фармакопеї США (U.S. Pharmacopeia (USP) 25-NF20 (2002). У цілому, позбавлені лактози композиції включають активні інгредієнти, зв'язуючу речовину/наповнювач і мастильну речовина у фармацевтично сумісних і фармацевтично прийнятних кількостях. Переважні позбавлені лактози дозовані форми включають активні інгредієнти, мікрокристалічну целюлозу, попередньо желатинізований крохмаль і стеарат магнію. Даний винахід, крім того, включає безводні фармацевтичні композиції і дозовані форми, які включають активні інгредієнти, оскільки вода може 95975 50 сприяти руйнуванню деяких сполук. Наприклад, додавання води (наприклад, 5%) широко прийняте у фармацевтичних сферах як засіб імітації тривалого збереження для визначення характеристик, таких як тривалість збереження або стійкість сполук протягом часу. Див., наприклад, документ Jens T. Carstensen, Drug Stability: Principles & Practice, nd 2 Ed., Marcel Dekker, NY, NY, 1995, pp. 379-80. При дії, вода і тепло прискорюють руйнування деяких сполук. Таким чином, вплив води на сполуку може мати велике значення, оскільки волога і/або вологість звичайно зустрічаються під час одержання, маніпулювання, упаковування, збереження, транспортування і застосування сполук. Безводні фармацевтичні композиції і дозовані форми за винаходом можна одержати, використовуючи безводні інгредієнти або інгредієнти, що містять низьку кількість вологи, й інгредієнти з низьким вмістом вологи або низкою вологістю. Фармацевтичні композиції і дозовані форми, які включають лактозу і щонайменше один активний інгредієнт, що включає первинний або вторинний амін, є переважно безводними, якщо очікується суттєвий контакт із вологою і/або вологістю під час виготовлення, упаковування і/або збереження. Безводну фармацевтичну композицію варто одержувати і зберігати так, щоб підтримувати її безводну природу. Відповідно, безводні композиції переважно упаковуються з використанням матеріалів, які, як відомо, запобігають впливу води, так, щоб їх можна було включити в придатні складені набори. Приклади придатної упаковки включають без обмеження герметично запаяна фольга, пластики, контейнери стандартних доз (наприклад, флакончики), блістерні упаковки і стрічкові упаковки. Винахід, крім того, включає фармацевтичні композиції і дозовані форми, які включають одну або декілька сполук, що знижують швидкість, з якою буде руйнуватися активний інгредієнт. Такі сполуки, які у даному описі іменуються «стабілізаторами», включають без обмеження актиоксиданти, такі як аскорбінова кислота, буфери рН або сольові буфери. Подібно кількостям і типам ексципієнтів, кількості і визначені типи активних інгредієнтів у дозованій формі можуть відрізнятися, залежно від таких факторів як, без обмеження, шлях, яким вона повинна вводитися пацієнтам. Однак типові дозовані форми за винаходом включають сполуку за винаходом в кількості приблизно від 0,10 до приблизно 500 мг. Типові дозовані форми включають сполуку за винаходом в кількості приблизно 0,1, 1, 2, 5, 7,5, 10, 12,5, 15, 17,5, 20, 25, 50, 100, 150, 200, 250, 300, 350, 400, 450 або 500 мг. Типові дозовані форми включають другий активний інгредієнт у кількості приблизно від 1 до приблизно 1000 мг, приблизно від 5 до приблизно 500 мг, приблизно від 10 до приблизно 350 мг або приблизно від 50 до приблизно 200 мг. Звичайно, визначена кількість другого активного засобу буде залежати від визначеного застосовуваного засобу, типу раку, що піддається лікуванню або веденню, і кількості (кількостей) сполуки за винаходом і будь 51 яких необов'язкових додаткових активних засобів, що одночасно вводяться пацієнту. 4.5.1 Пероральні дозовані форми Фармацевтичні композиції за винаходом, що придатні для перорального введення, можуть бути представлені у вигляді дозованих форм, таких як без обмеження звичайні таблетки (наприклад, жувальні таблетки), овальні покриті таблетки, капсули і рідини (наприклад, ароматизовані сиропи). Такі дозовані форми містять задані кількості активних інгредієнтів і можуть бути одержані способами фармакології, добре відомими фахівцям у даній галузі. Див., загалом, документ Remington's th Pharmaceutical Sciences, 18 ed., Mack Publishing, Easton PA (1990). Типові пероральні дозовані форми за винаходом одержують об'єднанням активних інгредієнтів у суміші щонайменше з одним ексципієнтом відповідно до звичайних методик фармацевтичного змішання. Ексципієнти можуть приймати широку розмаїтість форм, залежно від форми препарату, бажаного для введення. Наприклад, ексципієнти, що придатні для застосування в дозованих формах у вигляді пероральної рідини або аерозольних дозованих форм, включають без обмеження воду, гліколі, масла, спирти, ароматизуючі агенти, консерванти і барвні агенти. Приклади ексципієнтів, що придатні для використання у твердих пероральних дозованих формах (наприклад, порошках, звичайних таблетках, капсулах і овальних покритих таблетках) включають без обмеження крохмалі, цукри, мікрокристалічну целюлозу, розріджувачі, гранулюючі агенти, лубриканти, зв'язуючі агенти і розпушувальні агенти. Через легкість їх введення, таблетки і капсули представляють найпереважніші пероральні стандартні дозовані форми, і в цьому випадку використовуються тверді ексципієнти. При бажанні, таблетки можуть бути покриті стандартними водними або неводними методиками. Такі дозовані форми можуть бути одержані кожним зі способів фармакології. У цілому, фармацевтичні композиції і дозовані форми одержують рівномірним і ретельним змішуванням активних інгредієнтів з рідкими носіями, дрібно здрібненими твердими носіями, або обома способами, і потім, при необхідності, профілюванням продукту в бажаний вигляд. Наприклад, таблетку можна одержати пресуванням або формуванням. Пресовані таблетки можуть бути одержані пресуванням у придатній машині активних інгредієнтів у вільнотекучій формі, такій як порошок або гранули, необов'язково змішані з ексципієнтом. Формовані таблетки можуть виготовлятися формуванням у придатній машині суміші порошкоподібної сполуки, зволоженої інертним рідким розріджувачем. Приклади ексципієнтів, що можуть використовуватися в пероралних дозованих формах за винаходом, включають без обмеження зв'язуючі агенти, наповнювачі, розпушувачі і лубриканти. Зв'язуючі агенти, що придатні для використання у фармацевтичних композиціях і дозованих формах, включають без обмеження кукурудзяний крохмаль, картопляний крохмаль або інші крохмалі, желатин, натуральні і синтетичні смоли, такі як акація, аль 95975 52 гінат натрію, альгінова кислота, інші альгінати, порошкоподібний трагакант, кізельгур, целюлоза і її похідні (наприклад, етилцелюлоза, ацетат целюлози, кальційкарбоксиметилцелюлоза, натрійкарбоксиметилцелюлоза), полівінілпіролідон, метилцелюлозу, попередньо желатинізований крохмаль, гідроксипропілметилцелюлозу, (наприклад, №№ 2208, 2906, 2910), мікрокристалічну целюлозу і їх суміші. Придатні форми мікрокристалічної целюлози включають без обмеження матеріали, продавані у вигляді AVICEL-PH-101, AVICEL-PH-103, AVICEL RC-581, AVICEL-PH-105 ( що постачаються FMC Corporation, American Viscose Division, Avicel Sales, Marcus Hook, PA), і їх суміші. Визначеним зв'язуючим агентом є суміш мікрокристалічної целюлози і натрійкарбоксиметилцелюлози, продавана у вигляді AVICEL RC-581. Придатні безводні ексципієнти або ексципієнти, що мають низьку вологість, або добавки включають AVICEL-PH-103™ ікрохмаль Starch 1500 LM. Приклади наповнювачів, що придатні для використання в описаних у даній заявці фармацевтичних композиціях і дозованих формах, включають без обмеження тальк, карбонат кальцію (наприклад, гранули або порошок), мікрокристалічну целюлозу, порошкоподібну целюлозу, декстрати, каолін, маніт, кремінну кислоту, сорбіт, крохмаль, попередньо желатинізований крохмаль і їх суміші. Зв'язуючий агент або наповнювач у фармацевтичних композиціях за винаходом звичайно присутній в кількості приблизно від 50 до приблизно 99% мас. фармацевтичної композиції або дозованої форми. Розпушувачі використовуються в композиціях за винаходом для надання таблеток, які руйнуються при впливі водного середовища. Таблетки, що містять занадто багато розпушувача, можуть зруйнуватися при збереженні, тоді як ті, котрі містять занадто мало розпушувача, можуть не зруйнуватися з бажаною швидкістю або в бажаних умовах. Таким чином, для формування твердих пероральних дозованих форм за винаходом, варто використовувати достатню кількість розпушувача, яка є ні занадто великою, ні занадто малою, що може викликати несприятливі зміни вивільнення активних інгредієнтів. Кількість використовуваного розпушувача варіюється на основі типу сполуки і легко визначається середніми фахівцями в даній галузі. Типові фармацевтичні композиції включають приблизно від 0,4 до приблизно 15% мас. розпушувача, переважно приблизно від 1 до приблизно 5% мас. розпушувача. Розпушувачі, що можуть використовуватися у фармацевтичних композиціях і дозованих формах за винаходом, включають без обмеження агарагар, альгінову кислоту, карбонат кальцію, мікрокристалічну целюлозу, натрійкроскармелозу, кросповідон, полакрилін калію, гліколяткрохмаль натрію, крохмаль картоплі або тапіоки, інші крохмалі, попередньо желатинізований крохмаль, глини, інші альгіни, іншу целюлозу, смоли і їх суміші. Лубриканти, що можуть використовуватися у фармацевтичних композиціях і дозованих формах за винаходом, включають без обмеження стеарат 53 кальцію, стеарат магнію, мінеральне масло, легке мінеральне масло, гліцерин, сорбіт, маніт, поліетилегліколь, інші гліколі, стеаринову кислоту, лаурилсульфат натрію, тальк, гідровану рослинну олію (наприклад, арахісову олію, олію бавовняного насіння, олію соняшника, кунжутну олію, маслинову олію, кукурудзяну олію і олію соєвих бобів), стеарат цинку, етил олеат, етиллауреат, агар і їх суміші. Додаткові лубриканти включають, наприклад, силоїдний силікагель (AEROSIL200, що виготовляється компанією W.R. Grace Co. Of Baltimore), кремнезем діоксиду кремнію (що випускається Degussa Co. Of Piano, TX), CAB-O-SIL (пірогенний діоксид кремнію, продаваний Cabot Co. Of Boston, MA), і їх суміші. Лубриканти, якщо вони взагалі використовуються, звичайно використовуються в кількості менше ніж приблизно 1% мас. фармацевтичної композиції або дозованої форми, у яку вони включені. Тверда пероральна дозована форма за винаходом включає сполуку за винаходом, безводну лактозу, мікрокристалічну целюлозу, полівінілпіролідон, стеаринову кислоту, колоїдний безводних діоксид кремнію і желатин. 4.5.2 Лікарські форми з контрольованим вивільненням Активні інгредієнти за винаходом можна вводити засобом контрольованого вивільнення або пристроями доставки, що добре відомі середнім фахівцям у даній галузі. Приклади включають без обмеження ті, котрі описані в патентах US 3845770, 3916899, 3536809, 3598123, і 4008719, 5674533, 5059595, 5591767, 5120548, 5073543, 5639476, 5354556, і 5733566, кожний з який включений у даний опис як посилання. Такі дозовані форми можна застосовувати для забезпечення повільного або контрольованого вивільнення одного або декількох активних інгредієнтів з використанням, наприклад, гідроксипропілметилцелюлози, інших полімерних матриць, гелів, проникних мембран, осмотичних систем, багатошарових покриттів, мікрочастинок, ліпосом, мікросфер або їх комбінації для забезпечення бажаного профілю вивільнення, у пропорціях, що варіюються. Придатні склади контрольованого вивільнення, відомі середнім фахівцям у даній галузі, включаючи ті, котрі описані в даній заявці, можна легко вибрати для застосування з активними інгредієнтами за винаходом. Таким чином, винахід включає одиничні дозовані стандартні лікарські форми, що придатні для перорального введення, такі як без обмеження таблетки, капсули, гелеві капсули й овальні покриті таблетки, що пристосовані для контрольованого вивільнення. Усі фармацевтичні продукти контрольованого вивільнення мають загальну мету поліпшення медикаментозної терапії, у порівнянні з терапією, що досягається їх аналогами неконтрольованого вивільнення. В ідеалі, застосування оптимально сконструйованого препарату контрольованого вивільнення при медикаментозному лікуванні характеризується мінімумом використовуваної лікарської речовини для лікування або боротьби зі станом за мінімальну кількість часу. Переваги складів контрольованого вивільнення включають 95975 54 тривалу активність препарату, знижену частоту введення і збільшення дотримання пацієнтом запропонованого лікування. Крім того, склади контрольованого вивільнення можна застосовувати для впливу на час початку дії або інші характеристики, такі як рівні препарату в крові, і, таким чином, вони можуть впливати на виникнення побічних (наприклад, несприятливих) ефектів. Більшість складів контрольованого вивільнення призначені для первісного вивільнення деякої кількості лікарського засобу (активного інгредієнта), що швидко створює бажаний терапевтичний ефект, і поступового і безупинного вивільнення іншої кількості лікарського засобу для підтримання цього рівня терапевтичного або профілактичного ефекту протягом тривалого періоду часу. Для підтримання цього постійного рівня лікарського засобу в організмі, лікарський засіб повинен вивільнятися з лікарської форми зі швидкістю, яка буде заміщати кількість лікарського засобу, що метаболізується і виділяється з організму. Контрольоване вивільнення активного інгредієнта може стимулюватися різними умовами, включаючи без обмеження рН, температуру, ферменти, воду або інші фізіологічні умови або сполуки. 4.5.3 Парентеральні дозовані форми Парентеральні дозовані форми можна вводити пацієнтам різними шляхами, включаючи без обмеження підшкірний, внутрішньовенний (включаючи болюсну ін'єкцію), внутрішньом'язовий і внутрішньоартеріальний. Через те, що їх введення звичайне обходить природні захисні механізми пацієнтів проти забруднюючих агентів, парентеральні дозовані форми переважно стерильні або можуть стерилізуватися перед введенням пацієнту. Приклади парентеральних дозованих форм включають без обмеження розчини, готові для ін'єкції, сухі продукти, готові для розчинення або суспендування у фармацевтично прийнятному носії для ін'єкції, суспензії, готові для ін'єкції, і емульсії. Придатні носії, які можна використовувати з одержанням парентеральних лікарських форм за винаходом, добре відомі фахівцям у даній галузі. Приклади включають без обмеження: воду для ін'єкцій по Фармакопеї США; водні носії, такі як без обмеження хлорид натрію для ін'єкцій, розчин Рінгера для ін'єкцій, декстрозу для ін'єкцій, декстрозу і хлорид натрію для ін'єкцій, і розчин лактату Рінгера для ін'єкцій; змішувані з водою носії, такі як без обмеження етиловий спирт, поліетиленгліколь і поліпропіленгліколь; і неводні носії, такі як без обмеження кукурудзяна олія, олія бавовняного насіння, арахісова олія, кунжутна олія, етилолеат, ізопропілміристат і бензилбензоат. Сполуки, що збільшують розчинність одного або декількох активних інгредієнтів, описаних у даній заявці, також можуть бути включені в парентеральні дозовані форми за винаходом. Наприклад, цикл о декстрин і його похідні можна використовувати для збільшення розчинності імуномодуляторної сполуки за винаходом і її похідних. Див., наприклад, патент US 5134127, що повністю включений у даний опис як посилання. 55 4.5.4 Дозовані форми для місцевого застосування і введення через слизові оболонки Дозовані форми для місцевого застосування і введення через слизові оболонки за винаходом включають без обмеження спреї, аерозолі, розчини, емульсії, суспензії, очні краплі або інші офтальмологічні препарати або інші форми, відомі фахівцю в даній галузі. Див., наприклад, документи th th Remington's Pharmaceutical Sciences, 16 and 18 eds., Mack Publishing, Easton PA (1980 & 1990); і th Introduction to Pharmaceutical Dosage Forms, 4 ed., Lea & Febiger, Philadelphia (1985). Дозовані форми, що придатні для лікування слизових тканин всередині ротової порожнини, можуть складатися у вигляді розчинів для полоскання ротової порожнини або у вигляді гелів для порожнини рота. Придатні ексципієнти (наприклад, носії і розріджувачі) і інші матеріали, які можна використовувати з одержанням дозованих форм для місцевого застосування і введення через слизові оболонки, охоплювані даним винаходом, добре відомі фахівцям у фармацевтичних сферах і залежать від визначеної тканини, на яку буде наноситися дана фармацевтична композиція. Враховуючи цей факт, типові ексципієнти включають без обмеження воду, ацетон, етанол, етиленгліколь, пропіленгліколь, бутан-1,3-діол, ізопропілміристат, ізопропілпальмітат, мінеральну олію і їх суміші для утворення розчинів, емульсій або гелів, які є нетоксичними і фармацевтично прийнятними. При бажанні, до фармацевтичних композицій і дозованих форм можуть також додаватися змочувальні речовини або зволожувачі. Приклади таких додаткових інгредієнтів добре відомі в даній галузі. Див., наприклад, документи Remington's Pharmaceutical th th Sciences, 16 and 18 eds., Mack Publishing, Easton PA (1980 & 1990). pH фармацевтичної композиції або дозованої форми можна також регулювати для поліпшення доставки одного або декількох активних інгредієнтів. Аналогічним чином, для поліпшення доставки можна регулювати полярність розчинника-носія, його іонну силу або тонічність. Такі сполуки як стеарати також можуть додаватися до фармацевтичних композицій або дозованих форм для переважної зміни гідрофільності або ліпофільності одного або декількох активних інгредієнтів для того, щоб поліпшити доставку. У цьому відношенні, стеарати можуть служити як ліпідний носій для сполуки, як емульгуючий агент або поверхнево-активна речовина, і як посилюючий доставку або посилюючий проникнення агент. Різні солі, гідрати або сольвати активних інгредієнтів можна використовувати для додаткового регулювання властивостей одержаної композиції. 4.6 Набори В одному варіанті здійснення, активні інгредієнти за винаходом переважно не вводяться пацієнту одночасно або однаковим шляхом введення. Тому даний винахід включає набори, які, при використанні медичним працівником, можуть спростити введення відповідних кількостей активних інгредієнтів пацієнту. 95975 56 Набір за винаходом включає дозовану форму сполуки за винаходом. Набори, охоплювані даним винаходом, можуть, крім того, включати додаткові активні інгредієнти, такі як облімерсен ® (Genasense ), мелфалан, G-CSF, GM-CSF, ЕРО, топотекан, дакарбазин, іринотекан, таксотере, IFN, інгібітор СОХ-2, пентоксифілін, ципрофлоксацин, дексаметазон, IL2, IL8, IL18, Ara-С, вінорелбін, ізотретиноїн, 13 цисретиноєву кислоту або її фармакологічно активний мутант або похідне, або їх комбінацію. Приклади додаткових активних інгредієнтів включають без обмеження ті, котрі описані в даному описі (див., наприклад, розділ 4.3). Набори за винаходом можуть, крім того, включати пристрої, які використовуються для введення активних інгредієнтів. Приклади таких пристроїв включають без обмеження шприци, мішечки з крапельницею, трансдермальні системи й інгалятори. Набори за винаходом можуть, крім того, включати клітини або кров для переливання, а також фармацевтично прийнятні носії, які можна використовувати для введення одного або декількох активних інгредієнтів. Наприклад, якщо активний інгредієнт наданий у твердій формі, яка може бути розчинена для парентерального введення, то набір може включати запаяний контейнер придатного носія, у якому активний інгредієнт може бути розчинений, для утворення позбавленого матеріалу у вигляді частинок стерильного розчину, який придатний для парентерального введення. Приклади фармацевтично прийнятних носіїв включають без обмеження: воду для ін'єкцій по Фармакопеї США; водні носії, такі як без обмеження хлорид натрію для ін'єкцій, розчин Рінгера для ін'єкцій, декстрозу для ін'єкцій, декстрозу і хлорид натрію для ін'єкцій, і розчин лактату Рінгера для ін'єкцій; змішувані з водою носії, такі як без обмеження етиловий спирт, поліетиленгліколь і поліпропіленгліколь; і неводні носІЇ, такі як без обмеження кукурудзяна олія, олія бавовняного насіння, арахісова олія, кунжутна олія, етилолеат, ізопропілміристат і бензилбензоат. 5. Приклади Визначені варіанти здійснення винаходи ілюструються наступними необмежувальними прикладами. 5.1. Складний трет-бутиловий ефір [2-(2,6діоксопіперидин-3-іл)-1,3-діоксо-2,3-дигідро-1Нізоіндол-4-ілметил]метилкарбамінової кислоти 5.1.1 Складний диметиловий ефір 3метилфталевої кислоти Перемішану суміш 3метилфталевого ангідриду (10,0 г, 61,7 ммоль) у метанолі (90 мл) кип'ятили в посудині зі зворотним холодильником протягом 1 години. Суміші дали можливість остудитися до кімнатної температури і концентрували з одержанням 13 г половини складного ефіру. До перемішаної суспензії половини складного ефіру (13 г) додавали метилйодид (18,7 57 г, 131,5 ммоль) і бікарбонат натрію (13,0 г, 154,2 ммоль) у ДМФА (диметилформаміді) (75 мл). Одержану суміш перемішували при 75°С в масляній бані протягом 1,5 години. Суміш охолоджували до кімнатної температури і виливали у льодяну воду (250 мл). Суміш екстрагували EtOAc (4×80 мл), і об'єднані екстракти ЕtOАс промивали водою (3×50 мл), розсолом (50 мл) і сушили (MgSO4). Розчинник видаляли у вакуумі з одержанням 12,4 г неочищеного продукту. Неочищений продукт очищали флеш-хроматографією (SiO2, гексан:ЕtOАс 7:3) з одержанням 12,1 г складного диметилового ефі1 ру 3-метилфталевої кислоти у вигляді масла: Н ЯМР (CDCI3) δ 7,84-7,81 (дд, J=1,3 і 7,1 Гц, 1H), 7,42-7,32 (м, 2Н), 3,94 (с, 3Н), 3,88 (с, 3Н), 2,35 (с, 3Н). 5.1.2 Складний диметиловий ефір 3метилфталевої кислоти Перемішану суміш складного диметилового ефіру 3-метилфталевої кислоти (12,1 г, 57,9 ммоль) і N-бромсукциніміду (12,4 г, 69,5 ммоль) в ацетонітрилі (150 мл) нагрівають при 70°С (масляна баня), у той час, як світлова лампа потужністю 200 Вт, розташована на відстані 2 см, світила на реакційну суміш протягом ночі. Одержану суміш охолоджували і концентрували. Залишок розчиняли в етилацетаті (150 мл), промивали водою (3×50 мл), розсолом (50 мл) і сушили (MgSO4). Розчинник видаляли у вакуумі, і залишок очищали флешхроматографією (SiO2, гексан:ЕtOАс 8:2) з одержанням складного диметилового ефіру 3бромметилфталевої кислоти (13,9 г, 83%) у вигля1 ді твердої речовини: Н ЯМР (CDCI3) δ 7,94-7,90 (дд, J=1,1 і 7,9 Гц, 1H), 7,65-7,62 (дд, J=1,0 і 6,9 Гц, 1Н), 7,47 (т, J=7,8H, 1H), 4,54 (с, 2Н), 3,97 (с, 3Н), 3,90 (с, 3Н). 5.1.3 Складний трет-бутиловий ефір метилкарбамінової кислоти Перемішаний розчин 2М метиламіну/ТГФ (тетрагідрофурану) (30 мл, 60 ммоль) і триетиламіну (6,1 г, 66 ммоль) у метиленхлориді (50 мл) охолоджували до -20°С. Повільно додавали розчин дитрет-бутилдикарбамату (14,4 г, 66 ммоль) у метиленхлориді (50 мл) при температурі від -10°С до 20°С. Після додавання, суміш перемішували при 20°С протягом 30 хвилин, потім зігрівали до кімнатної температури протягом ночі. Суміш промивали водою (2×40 мл) і розсолом (40 мл) і сушили (MgSO4). Розчинник видаляли і залишок перемішували з гексаном (15 мл). Суміш фільтрували і фільтрат концентрували. Залишок очищали флешхроматографією (SiO2, гексан:ЕtOАс 8:2) з одержанням складного трет-бутилового ефіру метилкарбамінової кислоти (6,6 г, 84%) у вигляді масла: 1 Н ЯМР (CDCI3) δ 4,57 (ушир. 1H), 2,74 (д, J=4,9 Гц, 3Н), 1,44 (с, 9Н). 95975 58 5.1.4 Складний диметиловий ефір 3-[(третбутоксикарбонілметиламіно)-метил]фталевої кислоти Розчин складного трет-бутилового ефіру метилкарбамінової кислоти (5,0 г, 38,0 ммоль) у ДМФА (50 мл) охолоджували в льодяній бані і порціями додавали NaH (60%, 1,7 г, 41,8 ммоль) при 10°С. Суміш перемішували ще протягом 30 хвилин. Повільно додавали розчин складного диметилового ефіру 3-бромметилфталевої кислоти (10,9 г, 38,0 ммоль) у ДМФА (20 мл), підтримуючи температуру на рівні 10-15°С. Одержану суміш перемішували при кімнатній температурі протягом ночі. Суміш виливають у льодяну воду (400 мл) і екстрагували ЕtOАс (4×70 мл). Об'єднані екстракти ЕtOАс промивали водою (3×50 мл), розсолом (50 мл) і сушили (MgSO4). Розчинник видаляли у вакуумі і залишок очищали флеш-хроматографією (SiO2, гексан:ЕtOАс 8:2) з одержанням складного диметилового ефіру 3-[(третбутоксикарбонілметиламіно)метил]фталевої кис1 лоти (7,7 г, 60%) у вигляді масла: H ЯМР (CDCI3) δ 7,93-7,89 (м, 1Н), 7,49-7,46 (м, 2Н), 4,46 (с, 2Н), 3,94 (с, 3Н), 3,89 (с, 3Н), 2,87-2,76 (ушир., 3Н), 1,49-1,42 (ушир., 9Н). 5.1.5 Складний трет-бутиловий ефір [2-(2,6діоксопіперидин-3-іл)-1,3-діоксо-2,3-дигідро-1Hізоіндол-4-ілметил]метилкарбамінової кислоти Стадія 1: Гідроксид натрію (0,6 г, 15,4 ммоль) додавали до перемішаного розчину складного диметилового ефіру 3-[(третбутоксикарбонілметиламіно)метил]фталевої кислоти (2,6 г, 7,7 ммоль) у етанолі (30 мл) і води (6 мл). Суміш кип'ятили в посудині зі зворотним холодильником протягом 1 години. Суміш охолоджували і концентрували у вакуумі. До залишку додавали воду (30 мл), і одержану суміш промивали простим ефіром (30 мл). Водний шар охолоджували і підкисляли 6н. НСI до рН 2. Одержану суміш екстрагували СН2Сl2 (3×30 мл) і сушили над MgSO4. Розчинник видаляли у вакуумі з одержанням суміші складного монометилового ефіру 3[(трет-бутоксикарбонілметиламіно)метил]фталевої кислоти і його ізомерного складного монометилового ефіру, яку використовують на наступній стадії без подальшого очищення. Стадія 2: Перемішану суміш 3-[(третбутоксикарбонілметиламіно)-метил] фталевої кислоти (2,3 г, 7,1 ммоль) з попередньої стадії і ааміноглутарімідгідрохлориду (1,3 г, 7,8 ммоль) у піридині (40 мл) кип'ятили в посудині зі зворотним холодильником протягом 5 годин. Суміш охоло 59 джували і концентрували у вакуумі. Залишок розчиняли в EtOAc (100 мл) і воді (50 мл). Розчин ЕtOАс відокремлювали і промивали водою (40 мл), 1н. лимонною кислотою (2×40 мл), водою (2×40 мл) і розсолом (40 мл) і потім сушили (MgSO4). Розчинник видаляли у вакуумі і залишок очищали флеш-хроматографією (SiO2, CH2Cl2:EtOAc 8:2) з одержанням складного трет-бутилового ефіру [2(2,6-діоксопіперидин-3-іл)-1,3-діоксо-2,3-дигідро1Н-ізоіндол-4-ілметил]метилкарбамінової кислоти 1 (1,7 г, 60%): точка плавлення 138-140°С; НЯМР (ДМСО-d6) δ 11,14 (с, 1Н), 7,91-7,81 (м, 2Н), 7,57 (ушир., 1Н), 5,19-5,12 (дд, J=5,3 і 12,6 Гц, 1H), 4,85 (с, 2Н), 2,97-2,83 (м, 1H), 2,89 (с, 3Н), 2,63-2,50 (м, 13 2Н), 2,07-2,03 (м, 1Н), 1,44-1,29 (д, 9Н); С ЯМР (ДМСО-d6) δ 172,70, 169,74, 167,48, 166,87, 154,75, 138,31, 134,99, 132,31, 131,74, 127,42, 121,98, 79,13, 48,86, 47,32, 34,84, 30,90, 27,93, 21,94; Аналітично розраховано для C20H23N3O6: С, 59,84; Η, 5,78; Ν, 10,47. Знайдено: С, 59,51; Η, 5,68; Ν, 10,31. 5.2 Гідрохлорид 2-(2,6-діоксопіперидин-3-іл)-4метиламінометилізоіндол-1,3-діону До перемішаного розчину складного третбутилового ефіру [2-(2,6-діоксопіперидин-3-іл)-1,3діоксо-2,3-дигідро-1H-ізоіндол-4ілметил]метилкарбамінової кислоти (8,1 г, 20,2 ммоль) у метиленхлориді (80 мл) додавали 2н. НСІ/простий ефір (25 мл). Суміш перемішували при кімнатній температурі протягом ночі. Суміш фільтрували, промивали СН2Сl2 (20 мл) і сушили з одержанням гідрохлориду 2-(2,6-діоксопіперидин3-іл)-4-метиламінометилізоіндол-1,3-діону (5,3 г, 77%) у вигляді твердої речовини не зовсім білого 1 кольору: Н ЯМР (ДМСО-d6) δ 11,17 (с, 1H), 9,64 (с, 2Н), 8,11-7,91 (м, 3Н), 5,22-5,15 (дд, J=4,9 і 12,5 Гц, 1H), 4,55 (с, 2Н), 2,98-2,84 (м, 1H), 2,64-2,50 (м, 13 2Н), 2,60 (с, 3Н), 2,08-2,03 (м, 1H); С ЯМР (ДМСО-d6) δ 172,69, 169,60, 167,22, 166,51, 136,40, 134,86, 131,45, 130,65, 129,20, 123,88, 48,89, 45,66, 32,39, 30,84, 21,96. 5.3 [2-(2,6-Діоксопіперидин-3-іл)-1,3-діоксо-2,3дигідро-1Н-ізоіндол-4-ілметил]метиламід циклопропанкарбонової кислоти Триетиламін (0,50 г, 4,8 ммоль) додавали до перемішаної суспензії гідрохлориду 2-(2,6діоксопіперидин-3-іл)-4-метиламінометилізоіндол1,3-діону (0,7 г, 1,9 ммоль) і циклопропанкарбонілхлориду (0,2 г, 2,1 ммоль) у ТГФ (20 мл) при 5°С. Після додавання, суміш перемішували при кімнатній температурі протягом 2 годин. Суміш концент 95975 60 рували у вакуумі, і твердий залишок перемішували з 1н. НСI (25 мл). Неочищений продукт перемішували з гарячим ЕtOАс (15 мл) з одержанням 0,5 г (74%) продукту у вигляді твердої речовини білого 1 кольору: точка плавлення 243-245°С; Н ЯМР (ДМСО-d6) δ 11,13 (с, 1H), 7,91-7,82 (м, 2Н), 7,577,45 (м, 1H), 5,19-5,14 (дд, J=4,2 і 12,2 Гц, 1H), 4,97 (с, 2Н), 3,21 (с, 3Н), 2,92-2,85 (м, 1H), 2,64-2,51 (м, 13 2Н), 2,08-1,84 (м, 2Н), 0,81-0,63 (м, 4Н); С ЯМР (ДМСО-d6) δ 173,16, 172,71, 169,77, 167,55, 166,89, 138,05, 135,25, 134,93, 132,54, 131,74, 127,58, 121,90, 48,87, 46,35, 35,63, 30,91, 21,96, 10,62, 7,28; Аналітично розраховано для C19H19N3O5: С, 61,78; Η, 5,18; Ν, 11,38. Знайдено: С, 61,58; Η, 4,90; Ν, 11,21. 5.4 N-[2-(2,6-діоксопіперидин-3-іл)-1,3-діоксо2,3-дигідро-1Н-ізоіндол-4-ілметил]-Nметилпропіонамід Триетиламін (0,50 г, 4,8 ммоль) додавали до перемішаної суспензії гідрохлориду 2-(2,6діоксопіперидин-3-іл)-4-метиламінометилізоіндол1,3-діону (0,7 г, 1,9 ммоль) і пропіонілхлориду (0,3 г, 2,7 ммоль) у ТГФ (30 мл). Суміш перемішували при кімнатній температурі протягом ночі. Реакційну суміш гасили метанолом (1 мл) і концентрували. Залишок розчиняли в метиленхлориді (70 мл) і промивали 1н. НСI (30 мл), водою (30 мл) і розсолом (30 мл), і потім сушили (MgSO4). Розчинник видаляли, і залишок очищали хроматографією (SiO2, CH2Cl2:EtOAc 8:2) з одержанням 0,3 г (36%) продукту у вигляді твердої речовини білого кольо1 ру: точка плавлення 206-208°С; Н ЯМР (ДМСО-d6) δ 11,14 (с, 1Н), 7,89-7,81 (м, 2Н), 7,53 (м, 1Н), 5,195,12 (дд, J=4,9 і 12,4 Гц, 1H), 4,95 (5,03) (с, 2Н), 3,03 (2,87) (с, 3Н), 2,87 (м, 1H), 2,63-2,29 (м, 4Н), 13 2,08-1,99 (м, 1H), 1,09-0,97 (м, 3Н); С ЯМР (ДМСО-d6) δ 173,44, 172,66, 169,72, 167,50, 166,84, 138,08, 134,80, 132,52, 131,67, 127,49, 121,79, 48,79, 46,13, 35,38, 30,84, 25,52, 21,88, 9,06; Аналітично розраховано для C18H19N3O5: С, 60,50; Η, 5,36; Ν, 11,76. Знайдено: С, 60,37; Η, 5,52; Ν, 11,41. 5.5 3-Циклогексил-1-[2-(2,6-діоксопіперидин-3іл)-1,3-діоксо-2,3-дигідро-1Н-ізоіндол-4-ілметил]-1метилсечовина Триетиламін (0,30 г, 2,9 ммоль) додавали до перемішаної суспензії гідрохлориду 2-(2,6дioксопіперидин-3-іл)-4-метиламінометилізоіндол1,3-діону (0,7 г, 1,9 ммоль) і циклогексилізоціанату (0,30 г, 2,5 ммоль) у ТГФ (20 мл). Суміш перемішували при кімнатній температурі протягом 3 годин.
ДивитисяДодаткова інформація
Назва патенту англійськоюN-methylaminomethyl isoindole compounds, compositions comprising thereof and methods of using the same
Автори англійськоюMuller George W., Chen, Roger, S.C.
Назва патенту російськоюN-метиламинометилизоиндольные соединения, композиции, содержащие их, и способы их применения
Автори російськоюМюллер Джордж В., Чен Роджер С.К.
МПК / Мітки
МПК: C07D 401/14, A61K 31/4439, A61K 31/4035, C07D 405/14, A61P 35/00, C07D 401/04
Мітки: сполуки, включають, n-метиламінометилізоіндольні, застосування, способи, композиції
Код посилання
<a href="https://ua.patents.su/46-95975-n-metilaminometilizoindolni-spoluki-kompozici-shho-kh-vklyuchayut-i-sposobi-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">N-метиламінометилізоіндольні сполуки, композиції, що їх включають, і способи їх застосування</a>
Попередній патент: Спосіб одержання кремнію (варіанти)
Наступний патент: Похідні 2-арил-6-фенілімідазо[1,2-a]піридинів, їх одержання і застосування в терапії
Випадковий патент: Спосіб лікування хворих з больовим синдромом, обумовленим остеохондрозом хребта