1,2,4-оксадіазольні сполуки для лікування аутоімунних захворювань
Номер патенту: 101348
Опубліковано: 25.03.2013
Автори: Джонсон Крістофер Норберт, Хір Джаг Пол, Херст Девід Найджел, Хейгтмен Томас Деніел, Скідмор Джон, Уолл Йан Девід
Формула / Реферат
1. Сполука формули (І) або її фармацевтично прийнятна сіль:
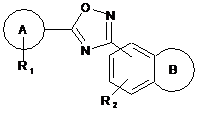 , (I)
, (I)
де:
А являє собою фенільне або 5- або 6-членне гетероарильне кільце;
R1 являє собою до двох замісників, незалежно вибраних з галогену, С(1-3)алкокси, С(1-3)фторалкілу, ціано, необов'язково заміщеного фенілу, С(1-3)фторалкокси, С(1-6)алкілу і С(3-6)циклоалкілу;
R2 являє собою водень, галоген або С(1-4)алкіл;
В являє собою 7-членне насичене кільце, вибране з наступних:
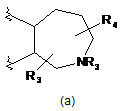 ,
, 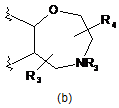 ,
, 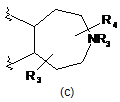 ,
,
R3 являє собою водень або С(1-3)алкіл, необов'язково заміщений киснем;
R4 являє собою (CH2)1-3CONH2, (СН2)1-3ОН, СО2Н або (СН2)1-3СО2Н.
2. Сполука формули (І) або її фармацевтично прийнятна сіль, де:
А являє собою феніл або піридил;
R1 являє собою до двох замісників, незалежно вибраних з хлору, ціано й ізопропокси;
R2 являє собою водень;
В являє собою (а) або (b);
R3 являє собою водень;
R4 являє собою (CH2)2CONH2, (СН2)1-3OН, СО2Н або (СН2)1-3СО2Н.
3. Сполука, вибрана з групи:
3-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1Н-2-бензазепін-1-іл]пропанаміду,
3-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1Н-2-бензазепін-1-іл]пропанової кислоти,
3-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1Н-2-бензазепін-1-іл]-1-пропанолу,
[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4-бензоксазепін-3-іл]метанолу,
[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4-бензоксазепін-3-іл]карбонової кислоти,
3-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4-бензоксазепін-3-іл]пропанової кислоти,
[9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4-бензоксазепін-5-іл]оцтової кислоти,
[9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4-бензоксазепін-5-іл]оцтової кислоти,
[9-(5-{5-хлор-6-[(1-метилетил)окси]3-піридиніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4-бензоксазепін-5-іл]оцтової кислоти,
4-[9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4-бензоксазепін-5-іл]бутанової кислоти,
4-[9-(5-{5-хлор-6-[(1-метилетил)окси]3-піридиніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4-бензоксазепін-5-іл]бутанової кислоти,
4-[9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4-бензоксазепін-5-іл]бутанової кислоти
та їх фармацевтично прийнятних солей.
4. Застосування сполуки за будь-яким з пп. 1-3 для лікування станів або розладів, опосередкованих S1P1-рецепторами.
5. Застосування за п. 4, при якому станом або розладом є розсіяний склероз, аутоімунні захворювання, хронічні запальні розлади, астма, запальні нейропатії, артрит, трансплантація, хвороба Крона, виразковий коліт, червоний вовчак, псоріаз, ішемія-реперфузійне пошкодження, тверді пухлини й метастази пухлини, хвороби, пов'язані з ангіогенезом, судинні захворювання, больові стани, гострі вірусні хвороби, запальні стани кишечнику, інсулінозалежні і інсулінонезалежні діабети.
6. Застосування за п. 4, при якому станом є червоний вовчак.
7. Застосування сполуки за будь-яким з пп. 1-3 для одержання лікарського засобу для лікування станів або розладів, опосередкованих S1P1-рецепторами.
8. Застосування за п. 7, при якому станом або розладом є розсіяний склероз, аутоімунні захворювання, хронічні запальні розлади, астма, запальні нейропатії, артрит, трансплантація, хвороба Крона, виразковий коліт, червоний вовчак, псоріаз, ішемія-реперфузійне пошкодження, тверді пухлини й метастази пухлини, хвороби, пов'язані з ангіогенезом, судинні захворювання, больові стани, гострі вірусні хвороби, запальні стани кишечнику, інсулінозалежні і інсулінонезалежні діабети.
9. Застосування за п. 7, при якому станом є червоний вовчак.
10. Фармацевтична композиція, що містить сполуку згідно з будь-яким з пп. 1-3 як активне начало.
11. Спосіб лікування станів або розладів у ссавців, включаючи людей, які можуть опосередкуватися через S1P1-рецептори, який включає введення пацієнтові терапевтично безпечної і ефективної кількості сполуки формули (І) або її фармацевтично прийнятної солі.
12. Спосіб лікування за п. 11, в якому станом є червоний вовчак.
Текст
Реферат: Даний винахід стосується нових похідних оксадіазолу формули (І) O N A N R1 B R2 (I) або їх фармацевтично прийнятних солей. Сполуки формули (І) і їх фармацевтично прийнятні солі корисні при лікуванні станів або розладів, які опосередкуються через S1P1-рецептор. Зокрема, сполуки формули (І) та їх фармацевтично прийнятні солі корисні при лікуванні розсіяного склерозу, аутоімунних захворювань, хронічних запальних розладів, астми, запальних нейропатії, артриту, трансплантації, хвороби Крона, виразкового коліту, червоного вовчака, псоріазу, реперфузійного для ішемій пошкодження, твердих пухлин і метастазів пухлини, UA 101348 C2 (12) UA 101348 C2 розладів, пов'язаних з ангіогенезом, судинних захворювань, больових станів, гострих вірусних захворювань, станів запального кишечнику, інсулінозалежних і інсулінонезалежних діабетів. UA 101348 C2 5 10 15 20 25 30 35 40 45 50 55 Даний винахід стосується нових похідних оксадіазолу, що мають фармакологічну активність, способів їх одержання, фармацевтичних композицій, що їх містять їх, та їх застосування при лікуванні різних розладів. 1-фосфат сфінгозину (S1P) є біоактивним ліпідним медіатором, що утворюється шляхом фосфорилування сфінгозину сфінгозинкіназами і виявляється при високих рівнях у крові. Він продукується й секретується рядом типів клітин, включаючи клітини гематопоетичного походження, такі як тромбоцити й лаброцити (Okamoto et al. 1998 J. Biol. Chem. 273(42):27104; Sanchez and Hla 2004, J.Cell Biochem. 92:913). Він надає широкий ряд біологічної дії, включаючи регуляцію клітинної проліферації, диференціації, рухливості, васкуляризації й активації запальних клітин і тромбоцитів (Pyne and Pyne 2000, Biochem. J. 349: 385). Описано п'ять підтипів S1P відповідних рецепторів, S1P1 (Edg-1), S1P2 (Edg-5), S1P3 (Edg-3), S1P4 (Edg-6), і S1P5 (Edg-8), створюючих частину сімейства рецепторів гена G-білок сполучної ендотеліальної диференціації (Chun et al. 2002 Pharmacological Reviews 54:265, Sanchez and Hla 2004 J. Cellular Biochemistry, 92:913). Вказані 5 рецепторів показують диференціальну мРНК експресію, причому S1P1-3 широко експресується, S1P4 експресується в лімфоїдних і гематопоетичних тканинах, а S1P5 перш за все в головному мозку і у меншій мірі в селезінці. Вони сигналізують через різні підгрупи G білків, промотуючи безліч біологічних відповідних реакцій (Kluk and Hla 2002 Biochem et Biophysica Acta 1582:72, Sanchez and Hla 2004, J Cellular Biochem 92:913). Пропоновані ролі S1P1 рецептора включають транспортування лімфоцитів, індукцію/супресію цитокінів і дії ендотеліальних клітин (Rosen and Goetzl 2005 Nat Rev immunol. 5:560). Агоністи S1P1 рецептора використовуються в ряді аутоімунних і трансплантаційних тваринних моделей, включаючи моделі експериментального аутоімунного енцефаліту (ЕАЄ) MS, для зниження тяжкості індукованого захворювання (Brinkman et al. 2003 JBC 277:21453; Fujino et al. 2003 J. Pharmacol. Exp. Ther. 305:70; Webb et al. 2004 J. Neuroimmunol. 153:108; Rausch et al. 2004 J. Magn. Reson. Imaging 20:16). Повідомляється, що дана активність опосередкується дією агоністів S1P1 на циркуляцію лімфоцитів через лімфатичну систему. Лікування S1P1 агоністами приводить в результаті до секвестування лімфоцитів у вторинних лімфоїдних органах, таких як лімфові вузли, включаючи оборотну периферичну лімфопенію на моделях тварин (Chiba et al. 1998, J. Immunology 160:5037, Forrest et al. 2004 J. Pharmacol. Exp. Ther. 309:758; Sanna et al. 2004 JBC 279:13839). Опубліковані дані по агоністах говорять про те, що лікування сполукою індукує втрату S1P1 рецептора з клітинної поверхні через інтерналізацію (Graler and Goetzl 2004 FASEB J. 18:551; Matloubian et al. 2004 Nature 427:355; Jo et al. 2005 Chem. Biol. 12:703), і це є даним зменшенням S1P1 рецептора в імунних клітинах, що сприяє зниженню руху Т клітин з лімфатичних вузлів назад в потік крові. Делеція S1P1 гена викликає смертність ембріонів. Експерименти з перевірки ролі S1P1 рецептора в міграції й транспортуванні лімфоцитів включають сприйнятливе перенесення мічених S1P1 дефіцитних клітин Т в опромінюваних мишей дикого типу. Дані клітини показали зменшений вихід з вторинних лімфоїдних органів (Matloubian et al. 2004 Nature 427:355). S1P1 приписується також роль у модуляції сполук ендотеліальних клітин (Allende et al. 2003 102:3665, Blood Singelton et al. 2005 FASEB J 19:1646). Відносно даної ендотеліальної дії повідомляється, що S1P1 агоністи надають дію на ізольовані лімфатичні вузли, що можливо сприяє ролі в модуляції імунних розладів. S1P1 агоністи викликали закриття ендотеліальних стромальних "хвірток" лімфатичних синусів, які осушують лімфатичні вузли й запобігають виходу лімфоцитів (Wei et al. 2005, Nat. Immunology 6:1228). Показано, що сполука FTY720 (JP11080026-A) знижує циркуляцію лімфоцитів у тварин і людини, модулюючи хворобливу активність на тваринних моделях імунних розладів і знижуючи швидкості ремісії при тимчасовій ремісії розсіяного склерозу, що повторюється (Brinkman et al. 2002 JBC 277:21453, Mandala et al. 2002 Science 296:346, Fujino et al. 2003 J. Pharmacology and Experimental Therapeutics 305:45658, Brinkman et al. 2004 American J. Transplantation 4:1019, Webb et al. 2004 J. Neuroimmunology 153:108, Morris et al. 2005 Eur. J. Immunol. 35:3570, Chiba 2005 Pharmacology and Therapeutics 108:308, Kahan et al. 2003, Transplantation 76:1079, Kappos et al. 2006 New Eng. J. Medicine 335:1124). Дана сполука є проліками, які фосфорилюють in vivo сфінгозинкіназами, даючи молекулу, яка має агоністичну активність при S1P1, S1P3, S1P4 і S1P5 рецепторах. Клінічні дослідження продемонстрували, що лікування сполукою FTY720 приводить у результаті до брадикардії в перші 24 години лікування (Kappos et al. 2006 New Eng J. Medicine 335:1124). Вважають, що брадикардія є наслідком агонізму в S1P3 рецептора на основі ряду експериментів, заснованих на клітинах і тваринах. Вони включають використання S1P3 нокаутованих тварин, які, на відміну від мишей дикого типу, не демонструють брадикардію унаслідок введення FTY720 і використання S1P1 селективних сполук (Hale et al. 2004 Bioorganic 1 UA 101348 C2 5 10 15 20 25 30 35 40 45 & Midicinal Chemistry Letters 14:3501, Sanna et al. 2004 JBC 279:13839, Koyrakh et al. 2005 American J. Transplantation 5:529). Тому існує потреба в сполуках агоністах S1P1 з селективністю відносно S1P3, які, можна було б чекати, проявляють знижену тенденцію викликати брадикардію. Наступні патентні заявки описують похідні оксадіазолу як S1P1 агоністів: WO03/105771, WO05/058848, WО06/047195, WO06/100633, WO06/115188, WO06/131336, WO07/024922 і WO07/116866. Наступні патентні заявки описують похідні тетрагідроізохінолініл-оксадіазолу як агоністів S1P рецептора: WO06/064757, WO06/001463, WO04/113330. WO08/064377 описує бензоциклогептильні аналоги, що володіють активністю S1P1 рецептора. В даний час виявлений структурно новий клас сполук, які надають S1P1 рецептор. Даний винахід надає сполуки формули (I) або їх фармацевтично прийнятні солі: А являє собою фенільне або 5- або 6-членне гетероарильне кільце; R1 являє собою до двох замісників, незалежно вибраних з галогену, С(1-3)алкокси, С(1-3) фторалкілу, ціано, необов'язково заміщеного фенілу, С(1-3)фторалкокси, С(1-6)алкілу і С(36)циклоалкілу; R2 являє собою водень, галоген або С(1-4)алкіл; В являє собою 7-членне насичене кільце, вибране з наступних: R3 являє собою водень або С(1-3)алкіл, необов'язково заміщений киснем; R4 являє собою (СН2)1-3СОNH2, (СН2)1-3ОH, СО2H або (СН2)1-3СО2Н. У одному з втілень винаходу А являє собою феніл; та/або R1 являє собою до двох замісників, незалежно вибраних з хлору й ізопропокси; та/або R2 являє собою водень; та/або В являє собою (а) або (b); та/або R3 являє собою водень; та/або R4 являє собою (СН2)2СОNH2, (СН2)1-3ОH, СО2H або (СН2)2СО2Н. У одному з втілень винаходу А являє собою феніл або піридил; R1 являє собою до двох замісників, незалежно вибраних з хлору, ціано й ізопропокси; R2 являє собою водень; В являє собою (а) або (b); R3 являє собою водень; R4 являє собою (СН2)2СОNH2, (СН2)1-3ОH, СО2H або (СН2)2СО2Н. У одному втіленні А являє собою феніл або піридил. У ще одному втіленні А являє собою феніл. У ще одному втіленні А являє собою 3,4дизаміщений феніл. У одному втіленні R1 являє собою два замісники, одним з яких є С (1-3)алкокси, інший вибраний з галогену або ціано. У ще одному втіленні R1 являє собою два замісники, одним з яких є ізопропокси, а інший вибраний з хлору або ціано. В ще одному втіленні R 1 означає два замісники, вибрані з хлору, ізопропокси й ціано. У ще одному втіленні R 1 являє собою хлор та ізопропокси. У ще одному втіленні R1 являє собою хлор в 3-положенні й ізопропокси в 4 2 UA 101348 C2 5 10 15 20 25 30 35 40 45 50 55 60 положенні, коли А являє собою феніл, або R1 являє собою хлор у 5-положенні й ізопропокси в 6-положенні, коли А являє собою піридиніл. У ще одному втіленні R 1 являє собою ізопропокси й ціано. У ще одному втіленні R1 являє собою ціано в 3-положенні і ізопропокси в 4-положенні, коли А являє собою феніл, або R1 являє собою хлор в 5-положенні і ізопропокси в 6-положенні, коли А являє собою піридиніл. У ще одному втіленні В являє собою (а) або (b). У ще одному втіленні В являє собою (b). У одному втіленні R2 являє собою водень. У одному втіленні R3 являє собою водень. У одному втіленні R4 являє собою (СН2)2СОNH2, (СН2)1-3ОH, СО2H або (СН2)1-3СО2Н. У ще одному втіленні - (СН2)1-3СО2H. Термін "алкіл" як група або частина групи, наприклад, алкокси або гідроксіалкіл, відноситься до прямої або розгалуженої алкільної групи в усіх ізомерних формах. Термін "С (1-6)алкіл" відноситься до алкільної групи, описаній вище, що містить, принаймні 1 і саме більше 6 вуглецевих атомів. Приклади таких алкільних груп включають метил, етил, пропіл, ізопропіл, нбутил, ізобутил, втор-бутил або трет-бутил. Приклади таких алкоксигруп включають метокси, етокси, пропокси, ізопропокси, бутокси, ізобутокси, втор-бутокси і трет-бутокси. Відповідні С(3-6)циклоалкільні групи включають циклопропіл, циклобутил, циклопентил і циклогексил. Використовуваний в описі термін "галоген" відноситься до фтору (F), хлору (Cl), брому (Br) або йоду (I), і термін "галоїд" відноситься до галогенів: фтору (-F), хлору (-Cl), брому (-Br) і йоду (-I). Термін "гетероарил" означає ненасичене кільце, яке включає один або більш гетероатомів, вибраних з O, N або S. Приклади 5- або 6-членних гетероарильних кілець включають піроліл, триазоліл, тіадіазоліл, тетразоліл, імідазоліл, піразоліл, ізотіазоліл, тіазоліл, ізоксазоліл, оксазоліл, оксадіазоліл, фуразаніл, фураніл, тієніл, піридил, піримідиніл, піразиніл, піридазиніл і триазиніл. У деяких зі сполук формули (I), залежно від характеру замісника, є хіральні атоми вуглецю, й, отже, сполуки формули (I) можуть існувати як стереоізомери. Винахід поширюється на всі оптичні ізомери, такі як стереоізомерні форми сполук формули (I), включаючи енантіомери, діастереоізомери та їхні суміші, такі як рацемати. Різні стереоізомерні форми можуть виділятися або розділятися один від одного за допомогою загальноприйнятих способів, або будь-який заданий ізомер може виходити за допомогою звичайного стереоселективного або асиметричного синтезу. Деякі зі сполук, пропонованих у даній заявці, можуть існувати у всіляких таутомерних формах, і слід розуміти, що винахід охоплює всі такі таутомерні форми. Зрозуміло, що деякі сполуки винаходу містять і кислотну й основну групи й можуть тому існувати у вигляді цвітеріонів при деяких значеннях рН. Придатними сполуками винаходу є 3-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1H-2бензазепін-1-іл]пропанамід 3-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1H-2бензазепін-1-іл]пропанова кислота 3-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1H-2бензазепін-1-іл]-1-пропанол [7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4бензоксазепін-3-іл]метанол [7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4бензоксазепін-3-іл]карбонова кислота [9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4бензоксазепін-5-іл]оцтова кислота [9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4бензоксазепін-5-іл]оцтова кислота [9-(5-{5-хлор-6-[(1-метилетил)окси]-3-піридиніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4бензоксазепін-5-іл]оцтова кислота 4-[9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4бензоксазепін-5-іл]бутанова кислота 4-[9-(5-{5-хлор-6-[(1-метилетил)окси]3-піридиніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро1,4-бензоксазепін-5-іл]бутанова кислота 4-[9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4бензоксазепін-5-іл]бутанова кислота 3 UA 101348 C2 5 10 15 20 25 30 35 40 45 50 55 3-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4бензоксазепін-3-іл]пропанова кислота або їх фармацевтично прийнятні солі. Фармацевтично прийнятні похідні сполук формули (I) включають будь-яку фармацевтично прийнятну сіль, складний ефір або сіль такого ефіру сполуки формули (I), які після введення реципієнтові здатні давати (безпосередньо або побічно) сполуку формули (I) або її активний метаболіт або залишок. Сполуки формули (I) можуть утворювати солі. Очевидно зрозуміло, що для використання в медицині солі сполук формули (I) мають бути фармацевтично прийнятними. Відповідні фармацевтично прийнятні солі, очевидно, зрозумілі фахівцям в даній галузі й включають солі, що описуються в J. Pharm. Sci., 1977, 66, 1-19, такі як кислотно-адитивні солі, що утворюються з неорганічними кислотами, наприклад, соляною, бромистоводневою, сірчаною, азотною або фосфорною кислотою; й органічними кислотами, наприклад бурштиновою, малеїновою, оцтовою, фумаровою, лимонною, винною, бензойною, п-толуолсульфоновою, метансульфоновою або нафталінсульфоновою кислотою. Деякі зі сполук формули (I) можуть утворювати кислотно-адитивні солі з одним або більше еквівалентами кислоти. Даний винахід охоплює в своєму об'ємі всі можливі стехіометричні і не стехіометричні форми. Солі можуть також виходити з фармацевтично прийнятних основ, включаючи неорганічні й органічні основи. Солі, вироблювані з неорганічних основ, включають солі алюмінію, амонію, кальцію, міді, тривалентного заліза, двовалентного заліза, літію, магнію, солі тривалентного марганцю, двовалентного марганцю, калію, натрію, цинку й аналогічні. Солі, вироблювані з фармацевтично прийнятних основ, включають солі первинних, вторинних і третинних амінів; заміщені аміни, включаючи заміщені аміни, що зустрічаються в природі; і циклічні аміни. Конкретні фармацевтично прийнятні органічні основи включають аргінін, бетаїн, кафеїн, холін, N, N’-дибензилетилендіамін, діетиламін, 2-діетиламіноетанол, 2-диметиламіноетанол, етаноламін, етилендіамін, N-етилморфолін, N-етилпіперидин, глюкамін, глюкозамін, гістидин, гідрабамін, ізопропіламін, лізин, метилглюкамін, морфолін, піперазин, піперидин, прокаїн, пурини, теобромін, триетиламін, триметиламін, трипропіламін, трис(гідроксиметил) амінометан (TRIS, трометанол) і аналогічні. Солі можуть також утворюватися з основних іонообмінних смол, наприклад поліамінових смол. Коли сполука даного винаходу є основною, солі можуть виходити з фармацевтично прийнятних кислот, включаючи неорганічні й органічні кислоти. Такі кислоти включають оцтову, бензолсульфонову, бензойну, камфорсульфонову, лимонну, етансульфонову, етандисульфонову, фумарову, глюконову, глутамінову, бромистоводневу, соляну, ізетіонову, молочну, малеїнову, яблучну, мигдальну, метансульфонову, слизову, памову, пантотенову, фосфорну, пропіонову, бурштинову, сірчану, винну, п-толуолсульфонову кислоту й аналогічні. Фармацевтично прийнятні солі можуть виходити загальноприйнятим способом за допомогою реакції з відповідною кислотою або похідним кислоти. Фармацевтично прийнятні солі з основами можуть виходити загальноприйнятим способом за реакцією з відповідною неорганічною або органічною основою. Сполуки формули (I) можуть виходити в кристалічній або некристалічній формі, і, якщо вони кристалічні, можуть необов'язково гідратуватися або сольватуватися. Даний винахід включає в своєму об'ємі стехіометричні гідрати або сольвати, а також сполуки, що містять змінні кількості води та/або розчинника. Об'ємом винаходу охоплюються всі солі, сольвати, гідрати, комплекси, поліморфи, проліки, радіомічені похідні, стереоізомери й оптичні ізомери сполук формули (I). У додатковому аспекті даний винахід надає способи одержання сполуки формули (I). Сила й ефективність сполук даного винаходу відносно S1P1 рецептора може бути визначена за допомогою GTPγS аналізу на клонованому рецепторі людини, як описано в даному описі. Сполуки формули (I) продемонстрували агоністичну активність в S1P1 рецептора з використанням функціональних аналізів, описаних у даній заявці. Сполуки формули (I) і їх фармацевтично прийнятні солі тому є корисними в лікуванні станів або розладів, які опосередкуються через S1P1 рецептор. Зокрема, сполуки формули (I) та їх фармацевтично прийнятні солі корисні в лікуванні розсіяного склерозу, аутоімунних розладів, хронічних запальних розладів, астми, запальних нейропатій, артриту, трансплантації, хвороби Крону, виразкового коліту, червоного вовчаку, псоріазу, реперфузійного для ішемій пошкодження, твердих пухлин і метастазів пухлини, хвороб, пов'язаних з ангіогенезом, судинних захворювань, больових станів, гострих вірусних хвороб, запальних станів кишечнику, інсулін- і не інсулінозалежних діабетів (далі в описі званих "Розлади згідно з винаходом"). 4 UA 101348 C2 5 10 15 20 25 30 35 40 45 50 55 60 Сполуки формули (I) і їх фармацевтично прийнятні солі корисні, отже, в лікуванні червоного вовчаку. Сполуки формули (I) та їх фармацевтично прийнятні солі корисні, отже, в лікуванні псоріазу. Сполуки формули (I) та їх фармацевтично прийнятні солі корисні, отже, в лікуванні розсіяного склерозу. Слід розуміти, що термін "лікування", використовуваний в описі, включає профілактику, а також пом'якшення встановлених симптомів. Таким чином, винахід надає також сполуки формули (I) або їх фармацевтично прийнятні солі для використання як терапевтичних засобів, зокрема, в лікуванні станів або розладів, опосередкованих через S1P1 рецептор. Зокрема, винахід надає сполуку формули (I) або її фармацевтично прийнятну сіль як терапевтичну речовину в лікуванні розсіяного склерозу, аутоімунних захворювань, хронічних запальних розладів, астми, запальних нейропатій, артриту, трансплантації, хвороби Крону, виразкового коліту, червоного вовчаку, псоріазу, реперфузійного для ішемій пошкодження, твердих пухлин і метастазів пухлини, хвороб, пов'язаних з ангіогенезом, судинних захворювань, больових станів, гострих вірусних хвороб, запальних станів кишечнику, інсулін- і не інсулінозалежних діабетів. Сполуки формули (I) і їх фармацевтично прийнятні солі корисні як терапевтичні речовини в лікуванні червоного вовчаку. Сполуки формули (I) і їх фармацевтично прийнятні солі корисні як терапевтичні речовини в лікуванні псоріазу. Сполуки формули (I) і їх фармацевтично прийнятні солі корисні як терапевтичні речовини в лікуванні розсіяного склерозу. Далі винахід відноситься до способу лікування станів або розладів у ссавців, включаючи людей, які опосередкують через S1P1 рецептор, який включає введення страждаючому на захворювання пацієнтові терапевтично безпечної й ефективної кількості сполуки формули (I) або її фармацевтично прийнятній солі. Зокрема, винахід надає спосіб лікування розсіяного склерозу, аутоімунних захворювань, хронічних запальних розладів, астми, запальних нейропатій, артриту, трансплантації, хвороби Крону, виразкового коліту, червоного вовчаку, псоріазу, реперфузійного для ішемій пошкодження, твердих пухлин і метастазів пухлини, хвороб, пов'язаних з ангіогенезом, судинних захворювань, больових станів, гострих вірусних хвороб, запальних станів кишечнику, інсулін- і не інсулінозалежних діабетів, який включає введення страждаючому на захворювання пацієнтові терапевтично безпечної й ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. Винахід відноситься до способу лікування червоного вовчаку, який включає введення страждаючому на захворювання пацієнтові терапевтично безпечної й ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. Винахід відноситься до способу лікування псоріазу, який включає введення страждаючому на захворювання пацієнтові терапевтично безпечної й ефективної кількості сполуки формули (I) або її фармацевтично прийнятній солі. Винахід відноситься до способу лікування розсіяного склерозу, який включає введення страждаючому на захворювання пацієнтові терапевтично безпечної й ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. У ще одному аспекті винахід відноситься до сполуки формули (I) або її фармацевтично прийнятної солі для використання у виробництві лікарського засобу для вживання в лікуванні станів або розладів, опосередкованих через S1P1 рецептор. Зокрема, винахід відноситься до сполуки формули (I) або її фармацевтично прийнятній солі для використання у виробництві лікарського засобу для вживання в лікуванні розсіяного склерозу, аутоімунних захворювань, хронічних запальних розладів, астми, запальних нейропатій, артриту, трансплантації, хвороби Крону, виразкового коліту, червоного вовчаку, псоріазу, реперфузійного для ішемій пошкодження, твердих пухлин і метастазів пухлини, хвороб, пов'язаних з ангіогенезом, судинних захворювань, больових станів, гострих вірусних хвороб, запальних станів кишечнику, інсулін- і неінсулінозалежних діабетів. Сполуки формули (I) і їх фармацевтично прийнятні солі корисні у виробництві лікарського засобу для використання в лікуванні червоного вовчаку. Сполуки формули (I) і їх фармацевтично прийнятні солі корисні у виробництві лікарських засобів для використання в лікуванні псоріазу. Сполуки формули (I) і їх фармацевтично прийнятні солі корисні у виробництві лікарських засобів для використання в лікуванні розсіяного склерозу. Щоб використовувати сполуки формули (I) і їх фармацевтично прийнятні солі в терапії, їх зазвичай формують у вигляді фармацевтичної композиції відповідно до стандартної 5 UA 101348 C2 5 10 15 20 25 30 35 40 45 50 55 фармацевтичної практики. Даний винахід надає також фармацевтичну композицію, яка включає сполуку формули (I) або її фармацевтично прийнятну сіль і фармацевтично прийнятний носій або наповнювач (або ексципієнт). У подальшому аспекті даний винахід відноситься до способу одержання фармацевтичної композиції, що включає змішування сполуки формули (I) або її фармацевтично прийнятної солі й фармацевтично прийнятного носія або ексципієнта. Фармацевтичну композицію згідно з винаходом, яка може виходити змішуванням відповідним чином при температурі довкілля й атмосферному тиску, зазвичай пристосовують для орального, парентерального або ректального введення, і як такі можуть бути у формі пігулок, капсул, оральних рідких препаратів, порошків, гранул, пастил, реконстуйованих порошків, ін'єктованих або вливаних розчинів, або суспензій, або медичних свічок. Зазвичай віддається перевага композиціям, що вводяться орально. Пігулки й капсули для орального введення можуть бути у формі дозованих одиниць і можуть містити звичайні ексципієнти, такі як сполучні агенти (наприклад, заздалегідь желатинований кукурудзяний крохмаль, полівінілпіролідон або гідроксипропілметилцелюлозу); наповнювачі (наприклад, лактозу, мікрокристалічну целюлозу або дигідрофосфат кальцію); таблетуючі змащувальні агенти (наприклад, стеарат магнію, тальк або діоксид кремнію); дезинтегратори (наприклад, картопляний крохмаль або натрій-крохмальгліколят); і прийнятні змочуючі агенти (наприклад, лаурилсульфат натрію). На пігулки можуть наноситися покриття відповідно до способів, добре відомих в звичайній фармацевтичній практиці. Оральні рідкі препарати можуть бути у формі, наприклад, водних або масляних суспензій, розчинів, емульсій, сиропів або еліксирів, або можуть бути у формі сухого продукту для реконстуювання перед використанням з водою або іншим відповідним носієм. Такі рідкі препарати можуть містити загальноприйняті добавки, такі як суспендуючі агенти (наприклад, сироп сорбіту, похідні целюлози або гідрогеновані їстівні жири), емульгуючі агенти (наприклад, лецитин або аравійську камедь), неводні носії (які можуть включати харчові масла, наприклад, мигдалеве масло, масляні складні ефіри, етиловий спирт або фракціоновані рослинні олії), консерватори (наприклад, метил або пропіл-п-гідроксибензоати або сорбінову кислоту), і, на бажання, звичайні смакові або ароматизуючі агенти або забарвлюючі агенти, буферні солі й підсолоджуючі агенти, як це відповідає. Препарати для орального введення можуть формуватися відповідним чином для забезпечення контрольованого вивільнення активної сполуки. Для парентерального введення рідкі форми дозованих одиниць готують з використанням сполуки винаходу або її фармацевтично прийнятних солей і стерильного носія. Рецепторні форми для ін'єкції можуть бути представлені у формі дозованих одиниць, наприклад, в ампулах або у вигляді множинних доз з використанням сполуки винаходу або її фармацевтично прийнятних похідних і стерильного носія, необов'язково з додаванням консерванту. Композиції можуть бути представлені в таких формах, як суспензії, розчини або емульсії в масляних або водних носіях, і можуть містити рецептуруючі агенти, такі як суспендуючі, стабілізуючі та/або диспергуючі агенти. Альтернативно, активний інгредієнт може бути у вигляді порошку для рецептурного складання форми з відповідним носієм, наприклад, стерильною вільною від пірогенів водою, перед використанням. Сполука, залежно від використовуваних носіїв і концентрації, може або суспендуватися, або розчинятися в носієві. При приготуванні розчинів сполука може розчинятися для ін'єкцій і стерилізуватися на фільтрі перед заповненням відповідної судини або ампули й запечатуванням. У носієві переважно розчиняються ад'юванти, такі як місцеві анестезуючі агенти, консерванти й буферні агенти. Для посилення стабільності композиції можуть виморожуватися після заповнення судини, й воду видаляють у вакуумі. Парентеральні суспензії готують по суті так само, за винятком того, що сполука суспендується в носієві замість того, щоб розчинятися, й стерилізація не може досягатися за допомогою фільтрування. Сполуку можна стерилізувати шляхом піддавання її дії етиленоксиду перед суспендуванням у стерильному носієві. Для полегшення рівномірного розподілу сполуки в композицію можна переважно включати поверхнево-активний або змочуючий агент. Лосьйони можуть складатися у вигляді рецептурних форм з водною або масляною основою і зазвичай містять також один або більш емульгуючих агентів, стабілізуючих агентів, диспергуючих, суспендуючих агентів, загусників або забарвлюючих агентів. Краплі можуть формуватися з водною або неводною основою, включаючи також один або більш диспергуючих, стабілізуючих або суспендуючих агентів. Вони можуть також містити консервант. Сполуки формули (I) або їх фармацевтично прийнятні солі можуть також формуватися в рецепторні препарати у вигляді ректальних композицій, таких як супозиторії або затримуючі 6 UA 101348 C2 5 10 15 20 25 30 35 40 45 50 55 клізми, наприклад, що містять загальноприйняті супозиторні основи, такі як масло какао або інші гліцериди. Сполуки формули (I) або їх фармацевтично прийнятні солі можуть також формуватися у вигляді запасних препаратів. Такі довго діючі рецептурні форми можуть вводитися за допомогою імплантації (наприклад, підшкірно або внутрішньом'язово) або шляхом внутрішньом'язової ін'єкції. Так, наприклад, сполуки згідно з винаходом можуть формуватися в рецептурні форми з відповідними полімерними або гідрофобними матеріалами (наприклад, у вигляді емульсії у відповідному маслі) або іонообмінними смолами, або у вигляді помірно розчинних похідних, наприклад, у вигляді помірно розчинної солі. Для внутрішньоносового введення сполуки формули (I) або її фармацевтично прийнятні солі можуть формуватися у вигляді розчинів для введення за допомогою відповідного вимірювального або дозуючого приладу або, альтернативно, у вигляді порошкової суміші з відповідним носієм для введення з використанням відповідного доставляючого пристрою. Такі сполуки формули (I) або їх фармацевтично прийнятні солі можуть формуватися для орального, букального, парентерального, топічного (включаючи офтальмічне й носове), запасного або ректального введення або у вигляді форми, відповідної для введення за допомогою інгаляції або інсуфляції (вдування) (через рот або через ніс). Сполуки формули (I) або їх фармацевтично прийнятні солі можуть формуватися в рецептурні препарати для топічного введення у формі мазей, кремів, гелів, лосьйонів, песаріїв або вагінальних супозиторіїв, аерозолів або крапель (наприклад, очних, вушних або носових крапель). Мазі й креми можуть, наприклад, формуватися з водною або масляною основою з додаванням відповідних згущуючих та/або гелетвірних агентів. Мазі для введення стосовно очей можуть вироблятися стерильним способом з використанням стерилізованих компонентів. Композиція може містити від 0,1 % до 99 % по вазі, переважно від 10 до 60 % по вазі активного матеріалу залежно від способу введення. Доза сполуки, використовуваної при лікуванні згаданих вище розладів, варіюється зазвичай з урахуванням серйозності розладів, ваги пацієнта й інших аналогічних чинників. Проте, як загальне керівництво відповідними одиничними дозами можуть бути 0,05-1000 мг, 1,0-500 мг або 1,0-200 мг, і такі одиничні дози можуть вводитися більше одного разу на день, наприклад, два або три рази на день. Сполуки формули (I) або їх фармацевтично прийнятні солі можуть використовуватися у вигляді комбінаційних препаратів, у поєднанні з іншими активними інгредієнтами. Наприклад, сполуки винаходу можуть використовуватися у поєднанні з циклоспорином А, метотрексатом, стероїдами, рапаміцином, інгібіторами прозапального цитокіну, імуномодуляторами, що включають біологічні агенти або інші терапевтично активні сполуки. Винахід, про який йдеться, включає мічені ізотопом сполуки, які ідентичні сполукам, що характеризуються формулами I та іншими, але в яких один або більше атомів замінені атомом, що показує атомну масу або масове число, відмінні від атомної маси або масового числа, зазвичай виявлюваних у природі. Приклади ізотопів, які можуть включатися в сполуки винаходу, 3 11 включають ізотопи водню, вуглецю, азоту, кисню, фосфору, фтору, йоду і хлору, такі як Н, С, 14 18 123 125 С, F, I і I. Сполуки даного винаходу і фармацевтично прийнятні солі вказаних сполук, які містять згадані вище ізотопи та/або інші ізотопи інших атомів, охоплюються обсягом даного винаходу. Ізотопно мічені сполуки даного винаходу, наприклад сполуки, в які включені радіоактивні 3 14 ізотопи, такі як Н, С, корисні в аналізах розподілу ліків та/або субстрату в тканині. Мічені 3 14 тритієм, тобто Н, і вуглець-14, тобто С ізотопи є особливо переважними зважаючи на легкість 11 8 приготування і здатності до детектування. C і F ізотопи особливо корисні в РЕТ (томографія з 125 емісією позитрона), а I ізотопи особливо корисні в SPECТ (комп'ютерна томографія з емісією одного фотона), і все це корисно при візуалізації головного мозку. Далі, заміщення важчими 2 ізотопами, такими як дейтерій, тобто Н, можуть давати деякі терапевтичні переваги, що є результатом вищої метаболічної стабільності, наприклад, вимог збільшеного in vivo терміну напівжиття або знижених доз, і тому можуть бути переважними при деяких обставинах. Мічені ізотопом сполуки формули (I) та інші згідно з винаходом можуть зазвичай виходити шляхом здійснення процедур, описаних на схемах та/або в прикладах, наведених нижче, шляхом заміщення не ізотопно міченого реагенту вільно доступним ізотопно міченим реагентом. У додатковому аспекті даний винахід надає способи одержання сполуки формули (I). Один спосіб, який може використовуватися для одержання сполук формули (I), коли В являє собою 7 UA 101348 C2 5 10 15 20 ілюструється на схемі 1, де R 1, R2 і А мають значення, визначені для формули (1), наведені вище, і бічний ланцюг R4 розташований в 1-положенні, коли n являє собою 1-3, R2 являє собою водень або С(1-4)алкіл, R3 являє собою водень, R являє собою алкіл (наприклад, етил), hal являє собою хлор, бром або йод, і Р і Р1 є захисними групами. Сполуки формули (i), які є комерційно доступними (наприклад, Fluorochem), можуть перетворюватися на сполуки формули (ii), де, наприклад, Р1 являє собою захисну групу, таку як бензил, за допомогою обробки алкілуючим агентом, таким як бензилбромід, у присутності основи, такої як карбонат калію, у відповідному розчиннику, такому як ДМФ. Сполуки формули (ii) можуть перетворюватися на сполуки формули (iii) за допомогою гідролізу з використанням відповідної основи, такої як водний розчин гідроксиду натрію, у відповідному розчиннику, такому як етанол, при підвищеній температурі, як-от 80ºС. Сполуки формули (iii) можуть перетворюватися на сполуки формули (iv) за допомогою загальноприйнятих прийомів, таких як обробка відповідним амід-сполучним агентом, таким як етилхлорформіат, з подальшою реакцією з аміаком при зниженій температурі, як-от -10ºС, і у відповідному розчиннику, такому як ТГФ. Сполуки формули (iv) можуть перетворюватися на сполуки формули (v) шляхом обробки відповідним відновним агентом, таким як літійалюмінійгідрид, при низькій температурі, такий як нижче 15ºС, у розчиннику, такому як ТГФ, потім підвищення температури, наприклад, 8 UA 101348 C2 45 до 80ºС. Сполуки формули (v) можуть перетворюватися на сполуки формули (vii) за допомогою обробки відповідним ацилгалогенідом (vi) у присутності основи, такої як триетиламін, в розчиннику, такому як дихлорметан. Ацилуючі агенти (vi) зазвичай комерційно доступні або можуть бути отримані з використанням стандартних способів. Сполуки формули (vii) можуть перетворюватися на сполуки формули (viii), наприклад, за допомогою обробки оксихлоридом фосфору в розчиннику, такому як ацетонітрил, при підвищеній температурі, такій як температура дефлегмації, з подальшим відновленням з використанням відповідного відновного агента, такого як борогидрид натрію, у відповідному розчиннику, такому як метанол, що додається при низькій температурі, як-от 0ºС, і підігрівання до кімнатної температури. Сполуки формули (viii) можуть перетворюватися на захищену похідну (ix), в якій Р являє собою відповідну захисну групу, таку як трет-бутилоксикарбоніл (ВОС), наприклад, за допомогою обробки біс(1,1-диметилетил) дикарбонатом у присутності основи, такої як триетиламін у відповідному розчиннику, такому як дихлорметан (DCM). Сполуки формули (ix), в якій Р 1 являє собою захисну групу, таку як бензил, можуть піддаватися зняттю захисту, даючи сполуки формули (x), наприклад, за допомогою гідролізу з використанням відповідного каталізатора, такого як паладій. Сполуки формули (x) можуть перетворюватися на сполуки формули (xi) за допомогою обробки відповідним реагентом, таким як трифторметансульфоновий ангідрид, з використанням відповідної основи, такої як піридин. Сполуки формули (xi) можуть перетворюватися на сполуки формули (xii) за допомогою обробки відповідним джерелом ціаніду, таким як ціанід цинку, у присутності каталізатора, такого як тетракистрифенілфосфінпаладій(0), у відповідному розчиннику, такому як диметилформамід (ДМФ), при підвищеній температурі, як-от 80ºС. Сполуки формули (xii) можуть перетворюватися на сполуки формули (xiii) за допомогою обробки гідрохлоридом гідроксиламіну й відповідною основою, такою як бікарбонат натрію, в розчиннику, такому як метанол або етанол, при підвищеній температурі, як-от 60ºС. Сполуки формули (xiii) можуть перетворюватися на сполуки формули (xvi) за допомогою обробки хлорангідридом карбонової кислоти формули (xv) у присутності основи, такої як триетиламін, у відповідному розчиннику, такому як ДМФ. Такі реакції в типовому випадку проводяться при перемішуванні протягом якогось періоду часу при кімнатній температурі, потім при підвищених температурах, як-от 120ºС. Хлорангідриди кислоти формули (xv) є або комерційно доступними, або можуть виходити з відповідної кислоти (xiv) за допомогою звичайних засобів. Альтернативно, сполуки формули (xiii) можуть перетворюватися на сполуки формули (xvi) за допомогою обробки карбоновою кислотою формули (xiv) у присутності відповідного амідного агента сполучення, такого як гідрохлорид 1-(3диметиламінопропіл)-3-етилкарбодиіміду (EDAC), 1-гідроксибензотриазолу (HOBt), у відповідному розчиннику, такому як ДМФ. Такі реакції зазвичай здійснюються при підвищеній температурі, як-от 50-80ºС. Зазвичай кислота (xiv), EDAC і HOBt перемішуються протягом якогось періоду часу при кімнатній температурі перед додаванням сполуки формули (xiii). Сполуки формули (xvi) можуть перетворюватися на сполуки формули (xvii) за допомогою обробки основою, такою як водний гідроксид натрію, в спиртовому розчиннику, такому як етанол або метанол. Сполуки формули (xvii), в якій Р являє собою відповідну захисну групу, таку як трет-бутилоксикарбоніл (ВОС), можуть перетворюватися на певні сполуки формули (I) за допомогою обробки відповідною кислотою, зазвичай трифтороцтовою кислотою або соляною кислотою. Один із способів, який може використовуватися для одержання сполук формули (I), в якій В являє собою 50 ілюструється на схемі 2, на якій R1, R2 і А мають значення, визначені для формули (I), і бічний ланцюг R4 розташований у 5-положенні бензоксазепінового кільця, R3 являє собою водень, R4 являє собою (СН2)2СО2Н, R являє собою алкіл (наприклад, метил) і Р є захисною групою. 5 10 15 20 25 30 35 40 9 UA 101348 C2 5 10 15 20 25 30 Сполуки формули (xviii), які є комерційно доступними (наприклад, Aldrich), можуть перетворюватися на сполуки формули (xx), наприклад, за допомогою обробки реагентом Віттіга (xix), таким як (карбетоксиметилен) трифенілфосфоран, у відповідному розчиннику, такому як дихлорметан. Сполуки формули (xx) можуть перетворюватися на сполуки формули (xxii) за допомогою обробки відповідним N-захищеним (таким як Boc) етаноламіном (xxi) в умовах Міцунобу з використанням, наприклад, діізопропілазодикарбоксилату (DIAD) і трифенілфосфіну у відповідному розчиннику, такому як ТГФ. Сполуки формули (xxii), в якій Р являє собою відповідну захисну групу, таку як трет-бутилоксикарбоніл (ВОС), можуть перетворюватися на сполуки формули (xxiii) за допомогою обробки кислотою, зазвичай трифтороцтовою або соляною кислотою. Сполуки формули (xxiii) можуть перетворюватися на сполуки формули (xxiv) за допомогою обробки відповідним реагентом, таким як 1,8-діазабіцикло[5.4.0]ундец-7-ен (DBU), у відповідному розчиннику, такому як ТГФ. Сполуки формули (xxiv) можуть перетворюватися на відповідну N-захищену похідну (xxv), де Р являє собою відповідну захисну групу, таку як третбутилоксикарбоніл (ВОС), наприклад, за допомогою обробки біс(1,1-диметилетил) дикарбонатом у присутності основи, такої як триетиламін, у відповідному розчиннику, такому як дихлорметан (DCM). Сполуки формули (xxv) можуть перетворюватися на сполуки формули (xxvi) за допомогою обробки відповідним джерелом ціаніду, таким як ціанід цинку, у присутності каталізатора, такого як тетракистрифенілфосфінпаладій(0), у відповідному розчиннику, такому як диметилформамід (ДМФ), при підвищеній температурі, як-от 80ºС. Сполуки формули (xxvi) можуть перетворюватися на сполуки формули (xxvii) за допомогою обробки гідрохлоридом гідроксиламіну, як в разі перетворення (xii) в (xiii) на схемі 1. Сполуки формули (xxvii) можуть перетворюватися на сполуки формули (xxviii) за допомогою обробки хлорангідридом карбонової кислоти формули (xv), як описано для перетворення (xiii) в (xvi) на схемі 1. Сполуки формули (xxviii) можуть перетворюватися на сполуки формули (xxiх) за допомогою обробки основою, такою як водний гідроксид натрію, в спиртовому розчиннику, такому як етанол або метанол. Сполуки формули (xxix), в яких Р являє собою (ВОС), можуть перетворюватися на деякі сполуки формули (I) за допомогою обробки кислотою, зазвичай трифторооцтовою або соляною кислотою, як описано на схемі 1. Один із способів, який може використовуватися для повчання сполук формули (I), в якій В являє собою 10 UA 101348 C2 5 ілюструється на схемі 3, на якій R1, R2 і А мають значення, визначені для формули (I), і бічний ланцюг R4 розташований в 5-положенні бензоксазепінового кільця, R3 являє собою водень і R4 являє собою (СН2)3СО2Н, R являє собою алкіл (наприклад, метил) і Р є захисною групою. 20 Сполуки формули (ххх), в якій R2 являє собою водень, а R являє собою алкіл (наприклад, етил), і Р являє собою захисну групу (наприклад, ВОС), можуть перетворюватися на сполуки формули (xxxi) з використанням відповідного відновного агента, такого як борогідрид літію, у відповідному розчиннику, такому як метанол. Сполуки формули (xxxi) можуть перетворюватися на сполуки формули (xxxii) за допомогою окиснення з використанням відповідних методів, таких як окиснення Swern. Сполуки формули (xxxii) можуть перетворюватися на сполуки формули (xxxiii), наприклад, за допомогою обробки реагентом Віттіга (xix), таким як (карбетоксиметилен)трифенілфосфоран, у відповідному розчиннику, такому як дихлорметан. Сполуки формули (xxxiii) можуть перетворюватися на сполуки формули (xxxiv) за допомогою гідрування з використанням відповідного каталізатора, такого як паладій. Сполуки формули (xxxiv) можуть перетворюватися на сполуки формули (xxxv) з використанням методів, описаних для перетворення сполук формули (xxvi) на деякі сполуки формули (I) на схемі 2. Один із способів, який може використовуватися для одержання сполук формули (I), в якій В являє собою 25 ілюструється на схемі 4, на якій R 1, R2 і А мають значення, визначені для формули (I), і бічний ланцюг R4 розташований у 5-положенні бензоксазепінового кільця і являє собою (СН2)2СО2Н, R3 являє собою водень, R являє собою алкіл (наприклад, метил) і Р є захисною групою. 10 15 11 UA 101348 C2 5 10 15 Сполуки формули (xxxii) можуть перетворюватися на сполуки формули (xxxvi), наприклад, за допомогою обробки відповідним реагентом, таким як оксид метоксиметилдифенілфосфіну (xxxv), у присутності відповідної основи, такої як діізопропіламід літію (LDA), у відповідному розчиннику, такому як ТГФ, з подальшим, необов'язково, додаванням основи, такої як гідрид натрію. Сполуки формули (xxxvi) можуть перетворюватися на сполуки формули (xxxvii) за допомогою окислення з використанням відповідних методів, таких як з використанням хлорформіату піридинію (PCC), у відповідному розчиннику, такому як дихлорметан. Сполуки формули (xxxvii) можуть перетворюватися на сполуки формули (I) з використанням методів, описаних для перетворення сполук формули (xxvi) на деякі сполуки формули (I) на схемі 2. Один із способів, який може використовуватися для одержання сполук формули (I), в якій В являє собою ілюструється на схемі 5, на якій R1, R2 і А мають значення, визначені для формули (I), і бічний ланцюг R4 розташований у 3-положенні бензоксазепінового кільця і являє собою (СН2)2СО2Н, R3 являє собою водень, R являє собою алкіл (наприклад, метил) і Р є захисною групою. 12 UA 101348 C2 5 10 15 20 25 30 35 40 45 Комерційно доступні сполуки (наприклад, Aldrich, де R=Me) формули (xxxviii) можуть перетворюватися на сполуки формули (ХL) за допомогою обробки сполуками формули (xxxix), в якій Р являє собою відповідну захисну групу, таку як трет-бутилоксикарбоніл (ВОС) [які можуть бути одержані з використанням, наприклад, методу, описаного в Journal of Organic Chemistry (1987), 52(12), 2361-4], з використанням умов Міцунобу, наприклад, діізопропілазодикарбоксилату (DIAD) і трифенілфосфіну у відповідному розчиннику, такому як толуол. Сполуки формули (XL), в якій Р являє собою відповідну захисну групу, таку як третбутилоксикарбоніл (ВОС), можуть перетворюватися на сполуки формули (xLi) за допомогою обробки кислотою, зазвичай 4-толуолсульфоновою кислотою, у відповідному розчиннику, такому як метанол. Сполуки формули (xLi) можуть перетворюватися на сполуки формули (xLii), наприклад, за допомогою обробки відповідною кислотою, такою як трифтороцтова кислота, при кімнатній температурі, потім нагрівання при температурі дефлегмації у присутності відповідної основи, такої як триетиламін, і у відповідному розчиннику, такому як толуол. Сполуки формули (xLii) можуть перетворюватися на сполуки формули (xLiii) за допомогою обробки відповідним відновним агентом, таким як боран-ТГФ комплекс, у відповідному розчиннику, такому як ТГФ, при відповідній температурі, як-от температура дефлегмації. Сполуки формули (xLiii) можуть перетворюватися на захищену похідну (xLiv), де Р являє собою відповідну захисну групу, таку як трет-бутилоксикарбоніл (ВОС), наприклад, за допомогою обробки біс(1,1-диметилетил) дикарбонатом у присутності основи, такої як триетиламін, у відповідному розчиннику, такому як дихлорметан (DCM). Сполуки формули (xLiv) можуть перетворюватися на сполуки формули (xLv) за допомогою обробки відповідним джерелом ціаніду, таким як ціанід цинку, у присутності каталізатора, такого як тетракистрифенілфосфінпаладій(0), у відповідному розчиннику, такому як диметилформамід (ДМФ), при підвищеній температурі, як-от 80ºС. Сполуки формули (xLv) можуть перетворюватися на сполуки формули (xLvi) за допомогою обробки гідрохлоридом гідроксиламіну й відповідною основою, такою як бікарбонат натрію, в розчиннику, такому як метанол або етанол, при підвищеній температурі, як-от 60ºС. Сполуки формули (xLvi) можуть перетворюватися на сполуки формули (xLvii) за допомогою обробки хлорангідридом карбонової кислоти формули (xv), як описано на схемі 1 для перетворення сполук (xiii) на сполуки формули (xvi). Сполуки формули (xLvii) можуть перетворюватися на сполуки формули (xLviii) за допомогою окислення відповідним агентом окислення, таким як перйодинон Dess Martin, у відповідному розчиннику, такому як дихлорметан. Сполуки формули (xLviii) можуть перетворюватися на сполуки формули (xLix), наприклад, за допомогою обробки реагентом Віттіга (xix), таким як (карбетоксиметилен)трифенілфосфоран, у відповідному розчиннику, такому як дихлорметан. Сполуки формули (xLix) можуть перетворюватися на сполуки формули (L) за допомогою гідрування з використанням відповідного каталізатора, такого як паладій, у відповідному розчиннику, такому як етанол. Сполуки формули (L) можуть перетворюватися на сполуки формули (Li) за допомогою обробки основою, такою як водний гідроксид натрію, в спиртовому розчиннику, такому як етанол або метанол. Сполука формули (Li), в якій, наприклад, Р представляє ВОС, можуть перетворюватися на деякі сполуки формули (I) за допомогою обробки кислотою, зазвичай трифторооцтовою кислотою або соляною кислотою, як описано на схемі 1. Один із способів, який може використовуватися для одержання сполук формули (I), в якій В являє собою ілюструється на схемі 6, на якій R1, R2 і А мають значення, визначені для формули (I) вище, і бічний ланцюг R4 розташований у 3-положенні бензоксазепінового кільця і представлений формулою СО2Н, R3 являє собою водень, і Р є захисною групою. 13 UA 101348 C2 5 10 15 20 25 30 35 40 45 Сполуки формули (xLvii) можуть перетворюватися на сполуки формули (Lii) за допомогою окиснення відповідним окисним агентом, таким як триоксид хрому, в сірчаній кислоті у відповідному розчиннику, такому як ацетон. Сполуки формули (Lii), в якій, наприклад, Р являє собою ВОС, можуть перетворюватися на деякі сполуки формули (I) за допомогою обробки кислотою, зазвичай трифтороцтовою кислотою або соляною кислотою. Всі публікації, що включають, але не обмежені ними, патенти і патентні заявки, цитовані в даному описі, включені в опис шляхом посилання на них, неначебто було вказано, що кожна окрема публікація була конкретно й окремо включена в опис повністю. Наступне Одержання й Приклади ілюструють одержання сполук згідно з винаходом. g – грами міліграм – міліграми мл – мілілітри мкл - мікролітри MеCN – ацетонітрил MеOH – метанол EtOH – етанол Et2O – діетиловий ефір EtOAc – етилацетат DCM – дихлорметан DIAD – діізопропилазодикарбоксилат DME – 1,2-біс(метилокси)етан ДМФ – N, N-диметилформамід ДМСО – диметилсульфоксид EDAC – гідрохлорид N-(3-диметиламінопропіл)-N’-етилкарбодиіміду EDC – гідрохлорид N-(3-диметиламінопропіл)-N’-етилкарбодиіміду EDCl – гідрохлорид N-(3-диметиламінопропіл)-N’-етилкарбодиіміду HOBT/HOBt – гідроксибензотриазол IPA – ізопропіловий спирт NCS – N-хлоросукцинімід PyBOP – гексафторфосфат бензотриазол-1-ілокситрипіролідинофосфонію ТГФ – тетрагідрофуран dba – дибензилиденацетон КТ – кімнатна температура ºС – градуси Цельсія М – молярний Н – протон s – синглет d – дублет t – триплет q – квартет МГц – мегагерц MeOD – дейтерований метанол LCMS – рідинна хроматографія мас спектрометрія LC/MS – рідинна хроматографія/Мас Спектрометрія MS – мас спектрометрія ES – електророзпилення + + MH – мас іон + Н 14 UA 101348 C2 5 10 15 20 25 30 35 40 MDAP – мас направлена автоматизована препаративна рідинна хроматографія насич. – насичений Основний хімічний розділ Способи, описані нижче, даються в цілях ілюстрації, проміжні сполуки в прикладах одержання можуть необов'язково бути отримані з описаних конкретних комплектів. Одержання 1 Фенілметил 3-{3-[(фенілметил)окси]феніл}пропаноату Суміш 3-(3-гідроксифеніл)пропанової кислоти (Flurochem, 12,46 г, 75 ммоль), карбонату калію (31,1 г, 225 ммоль), і бензилброміду (18,7 мл, 158 ммоль) в DMF (120 мл) перемішували при 65ºС протягом 16 годин. Суміш охолоджували до кімнатної температури, розбавляли простим ефіром (200мл) і водою (400 мл) і водну фазу реекстрагували простим ефіром (100 мл). Об'єднані органічні екстракти промивали водою (3×100 мл), сушили (сульфатом магнію) й випарювали, одержуючи майже безбарвне масло (26,5 г), яке використовували без подальшого очищення. 1 H ЯМР (CDCl3) δ 2,68 (2H, т), 2,94 (2H, т), 5,01 (2H, с), 5,11 (2H, с), 6,78-6,82 (3H, м), 7,177,43 (11H, м). Одержання 2 3-{3-[(Фенілметил)окси]феніл}пропанова кислота Суміш фенілметилу 3-{3-[(фенілметил)окси]фенілу}пропаноату (26,5 г, 76 ммоль) і 2М водного розчину гідроксиду натрію (115 мл, 229 ммоль) в етанолі (250 мл) перемішували при 60ºС протягом 30 хвилин, потім етанол випарювали. Залишок розбавляли водою (200 мл) і екстрагували простим ефіром (2×150 мл). Водну фазу підкисляли 2М водним розчином HCl і екстрагували простим ефіром (250 мл і 100 мл), потім об'єднані ефірні екстракти сушили (сульфатом магнію) і випарювали, одержуючи білу тверду речовину (19,6 г). m/z (ES-) 255[M-H] . Одержання 3 3-{3-[(Фенілметил)окси]феніл}пропанаміду Етилхлорформіат (8,08 мл, 84 ммоль) по краплях додавали до розчину 3-{3[(фенілметил)окси]феніл}пропанової кислоти (19,6 г, 76 ммоль) і триетиламіну (11,7 мл, 84 ммоль) в THF (ТГФ) (250 мл) при -10ºС, одержуючи білу суспензію. Суміш перемішували при 10ºС протягом 15 хвилин, потім однією порцією додавали аміак (120 мл, 1830 ммоль), даючи можливість нагрітися до кімнатної температури протягом 2 годин. THF випарювали й водну суспензію екстрагували DCM (200 мл і 2×50 мл). Об'єднані органічні речовини сушили (сульфатом магнію), випарювали, суспендували в простому ефірі й фільтрували, одержуючи + білу тверду речовину (16,2 г). m/z (ES+) 256[M+H] . Одержання 4 3-{3-[(Фенілметил)окси]феніл}пропіламіну Розчин 3-{3-[(фенілметил)окси]феніл}пропанамиду (16,13 г, 63,2 ммоль) в THF (350 мл) протягом 15 хвилин додавали до перемішуваного розчину LiAlH4 (1М розчин в THF, 126 мл, 126 ммоль) в атмосфері аргону при охолоджуванні в крижаній бані. Суміш потім перемішували при 65ºС протягом 2 годин, перш ніж її охолоджували до 0ºС і гасили шляхом обережного 15 UA 101348 C2 5 10 15 20 25 30 35 додавання води (4,8 мл), 15 % водного розчину гідроксиду натрію (4,8 мл) і води (14,4 мл) все при охолоджуванні льодом. Суміш фільтрували, випарювали, повторно розчиняли в DCM (200 мл), потім промивали водою (100 мл), сушили (сульфатом магнію) і випарювали, одержуючи воскоподібну тверду речовину. Її розподіляли між етилацетатом (200 мл) і 2М водним розчином гідроксиду натрію (150 мл), потім фільтрували й відокремлювали. Органічну фазу сушили + (сульфатом магнію) і випарювали, одержуючи безбарвне масло (14,1 г). m/z (ES+) 242[M+H] . Одержання 5 Метил 4-оксо-4-[(3-{3-[(фенілметил)окси]феніл}пропіл)аміно]бутаноату Метил 4-хлор-4-оксобутаноат (1,58 г, 10,5 ммоль) по краплях додавали до перемішуваного розчину (3-{3-[(фенілметил)окси]феніл}пропіл)аміну (2,41 г, 9,99 ммоль) і триетиламіну (1,53 мл, 11,0ммоль) у DCM (30 мл) при охолоджуванні крижаною банею. Суміш перемішували протягом 30 хвилин, потім промивали 2М водним розчином соляної кислоти (30 мл), сушили (сульфатом магнію), випарювали й очищали за допомогою флеш-хроматографії (етилацетат/ізогексан, 1:1), + одержуючи смолу, яка кристалізувалася при пошкрябуванні. (1,91 г). m/z (ES+) 356 [M+H] . Одержання 6 Метил 3-{7-[(фенілметил)окси]-2,3,4,5-тетрагідро-1Н-2-бензазепін-1-іл}пропаноату Розчин метил 4-оксо-4-[(3-{3-[(фенілметил)окси]феніл}пропіл)аміно]бутаноату (10,4г, 29,3ммоль) і оксихлориду фосфору (8,95 мл, 96 ммоль) в MеCN (250 мл) перемішували при температурі кипіння із зворотним холодильником в атмосфері аргону протягом 2,5 годин, потім охолоджували й випарювали. Залишок розчиняли в метанолі (150 мл), охолоджували до 0ºС, потім впродовж 25 хвилин, порціями додавали борогидрид натрію (7,65 г, 202 ммоль), і суміш залишали стояти протягом 16 годин. Додавали воду (600 мл), потім суміш екстрагували DCM (200 мл і 2×75 мл). Об'єднані органічні речовини сушили (сульфатом магнію), випарювали й очищали за допомогою флеш-хроматографії (3 % метанол у DCM, потім 10 % метанол у DCM), одержуючи в'язку світло-коричневу смолу (4,2 г, LCMS: 62 % чистоти). Її використовували в + Одержанні 7 без подальшого очищення. m/z (ES+) 340[M+H] . Одержання 7 1,1-Диметилетил 1-[3-(метилокси)-3-оксопропіл]-7-[(фенілметил)окси]-1,3,4,5-тетрагідро-2Н2-бензазепін-2-карбоксилату ВОС-ангідрид (3,16 мл, 13,6 ммоль) додавали до розчину метил 3-{7-[(фенілметил)окси]2,3,4,5-тетрагідро-1Н-2-бензазепін-1-іл}пропаноату (4,2 г, 12,4 ммоль) і триетиламіну (2,07 мл, 14,9 ммоль) у DCM (50 мл) і перемішували при кімнатній температурі протягом 1 години. Реакційну суміш промивали водою (50 мл), сушили (сульфатом магнію), випарювали й очищали за допомогою флеш-хроматографії двічі (етилацетат/ізогексан, 1:4), одержуючи безбарвну смолу (1,81 г). LCMS: 4 % домішок залишалося. Її використовували в Одержанні 8 без + подальшого очищення. m/z (ES+) 440[M+H] . 16 UA 101348 C2 Одержання 8 1,1-Диметилетил бензазепін-2-карбоксилату 5 10 15 20 25 30 7-гідрокси-1-[3-(метилокси)-3-оксопропіл]-1,3,4,5-тетрагідро-2Н-2 Розчин 1,1-диметилетил 1-[3-метилокси)-3-оксопропіл]-7-[(фенілметил)окси]-1,3,4,5тетрагідро-2Н-2-бензазепін-2-карбоксилату (0,088 г, 0,200 ммоль) у метанолі (4 мл) гідрували при безперервному режимі потоку при 50ºС. Випарювання давало безбарвну смолу (55 мг). m/z + (ES+) 350[M+H] . Одержання 9 1,1-Диметилетил 1-[3-метилокси)-3-оксопропіл]-7-{[(трифторметил)сульфоніл]окси}-1,3,4,5тетрагідро-2Н-2-бензазепін-2-карбоксилату Трифторметансульфоновий ангідрид (0,041 мл, 0,240 ммоль) додавали до розчину 1,1диметилетил 7-гідрокси-1-[3-(метилокси)-3-оксопропіл]-1,3,4,5-тетрагідро-2Н-2-бензазепін-2карбоксилату (0,070 г, 0,200 ммоль) у піридині (2 мл) і перемішували при кімнатній температурі протягом 30 хвилин. Додавали простий ефір (40 мл), потім суміш промивали 2М водним розчином HCl (20 мл), водою (20 мл), сушили (сульфатом магнію) й випарювали, одержуючи + блідо-жовту смолу (95мг). m/z (ES+) 482[M+H] . Одержання 10 1,1-Диметилетил 7-ціано-1-[3-(метилокси)-3-оксопропіл]-1,3,4,5-тетрагідро-2Н-2-бензазепін2-карбоксилату Суміш 1,1-диметилетил 1-[3-(метилокси)-3-оксопропіл]-7-{[(трифторметил)сульфоніл]окси}1,3,4,5-тетрагідро-2Н-2-бензазепін-2-карбоксилату (1,8 г, 3,74 ммоль) ціаніду цинку (0,878 г, 7,48 ммоль) і тетракис(трифенілфосфін)паладію (0,864 г, 0,748 ммоль) у DMF (15 мл) перемішували при 90ºС у атмосфері аргону протягом 18 годин, потім охолоджували до кімнатної температури й розбавляли водою/етилацетатом (по 60 мл кожного). Органічний шар промивали водою (3×20 мл), сушили (сульфатом магнію) й очищали за допомогою флеш-хроматографії + (етилацетат/ізогексан, 1:3), одержуючи безбарвну смолу (608 мг). m/z (ES+) 359[M+H] . Одержання 11 1,1-Диметилетил 7-[(гідроксіаміно)(іміно)метил]-1-[3-(метилокси)-3-оксопропіл]-1,3,4,5тетрагідро-2Н-2-бензазепін-2-карбоксилату 17 UA 101348 C2 5 10 15 20 25 30 Суміш 1,1-диметилетил 7-ціано-1-[3-(метилокси)-3-оксопропіл]-1,3,4,5-тетрагідро-2Н-2бензазепін-2-карбоксилату (0,072 г, 0,201 ммоль), гідрохлориду гідроксиламіну (0,028 г, 0,402 ммоль) і бікарбонату натрію (0,067 г, 0,804 ммоль) в етанолі (4 мл) перемішували при 60ºС протягом 3 годин, потім залишали при кімнатній температурі протягом 64 годин. Додавали етилацетат (40 мл), і суміш промивали водою (50 мл), сушили (сульфатом магнію), і + випарювали, одержуючи безбарвну смолу (80мг, LCMS: 81 % чистоти). m/z (ES+) 392[M+H] . Одержання 12 1,1-Диметилетил 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1-[3(метилокси)-3-оксопропіл]-1,3,4,5-тетрагідро-2Н-2-бензазепін-2-карбоксилату Суміш 1,1-диметилетил 7-[(гідроксіаміно)(іміно)метил]-1-[3-(метилокси)-3-оксопропіл]-1,3,4,5тетрагідро-2Н-2-бензазепін-2-карбоксилату (0,57 г, 1,46 ммоль) 3-хлор-4-[(1метилетил)окси]бензойної кислоти (Paragos Product, 0,344 г, 1,60 ммоль), EDC (0,307 г, 1,60 ммоль) і HOBt (0,245 г, 1,60 ммоль) у DMF (8 мл) перемішували при кімнатній температурі протягом 20 хвилин, потім нагрівали при 120ºС протягом 3 годин. Реакційну суміш охолоджували до кімнатної температури й розбавляли етилацетатом/водою (по 80 мл кожного). Органічну фазу промивали насиченим водним розчином бікарбонату натрію й водою (3×20 мл), потім сушили (сульфатом магнію), випарювали й очищали за допомогою флеш-хроматографії + (етилацетат/ізогексан, 1:3), одержуючи білу піну (515 мг). m/z (ES+) 570[M+H] . Одержання 13 3-(7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2-{[(1,1диметилетил)окси]карбоніл}-2,3,4,5-тетрагідро-1Н-2-бензазепін-1-іл)пропанова кислота 2М Водний розчин гідроксиду натрію (0,5 мл, 1,0 ммоль) додавали до розчину 1,1диметилетилу 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1-[3-(метилокси)3-оксопропіл]-1,3,4,5-тетрагідро-2Н-2-бензазепін-2-карбоксилату (0,090 г, 0,16 ммоль) у етанолі (4 мл) і перемішували при кімнатній температурі протягом 17 годин. Суміш випарювали й залишок розподіляли між водою і простим ефіром, потім підкисляли 2М водним розчином HCl. Органічну фазу сушили (сульфатом магнію) й випарювали, одержуючи білу піну (86 мг). m/z + (ES+) 556[M+H] . Одержання 14 Метил-3-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро1Н-2-бензазепін-1-іл)пропаноату 18 UA 101348 C2 5 10 15 20 25 30 35 Трифтороцтову кислоту (1 мл, 12,98 ммоль) додавали до розчину 1,1-диметилетил 7-(5-{3хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1-[3-(метилокси)-3-оксопропіл]-1,3,4,5тетрагідро-2Н-2-бензазепін-2-карбоксилату (0,10 г, 0,175 ммоль) у DCM (1 мл) і перемішували при кімнатній температурі протягом 30 хвилин. Розчин випарювали, знову розчиняли в простому ефірі (30 мл), промивали 1М водним розчином карбонату калію, сушили (сульфатом + магнію) й випарювали, одержуючи безбарвну смолу (71 мг). m/z (ES+) 470[M+H] . Одержання 15 1,1-Диметилетил 4-[({4-бром-2-[(метилокси)карбоніл]феніл}окси)метил]-2,2-диметил-1,3оксазолідин-3-карбоксилату DIAD (6,40 мл, 32,9 ммоль) додавали до розчину 1,1-диметилетил 4-(гідроксиметил)-2,2диметил-1,3-оксазолідин-3-карбоксилату (6,92 г, 29,9 ммоль), метил 5-бром-2-гідроксибензоату (6,91 г, 29,9 ммоль) і трифенілфосфіну (8,63 г, 32,9 ммоль) у толуолі (70 мл), потім суміш перемішували при 80ºС протягом 18 годин. Розчин охолоджували, випарювали й очищали за допомогою флеш-хроматографії (етилацетат/ізогексан, 1:9), одержуючи безбарвне масло (7,56 + г). m/z (ES+) 344 і 346 (1:1 [M+H-100] ). Одержання 16 Метил 5-бром-2-{[2-({[(1,1-диметилетил)окси]карбоніл}аміно)-3-гідроксипропіл]окси}бензоату До розчину 1,1-диметилетил 4-[({4-бром-2-[(метилокси)карбоніл]феніл}окси)метил]-2,2диметил-1,3-оксазолідин-3-карбоксилату (7,54 г, 17,0 ммоль) у метанолі (100 мл) додавали пара-толуолсульфонову кислоту (0,10 г, 0,53 ммоль), і суміш перемішували при кімнатній температурі протягом 16 годин. Розчин випарювали насухо й очищали за допомогою флешхроматографії (етилацетат/ізогексан, 2:3), одержуючи безбарвне в'язке масло (5,55 г). m/z (ES+) + 404 і 406 (1:1 [M+H] ). Одержання 17 7-Бром-3-(гідроксиметил)-3,4-дигідро-1,4-бензоксазепін-5(2Н)-он Метил 5-бром-2-{[2-({[(1,1-диметилетил)окси]карбоніл}аміно)-3-гідроксипропіл]окси}бензоат (5,52г, 13,7 ммоль) розчиняли в DCM (15 мл) і TFA (15 мл, 195 ммоль) і перемішували при кімнатній температурі протягом 1 години. Розчин випарювали, потім залишок знову розчиняли в толуолі (60 мл) і триетиламіні (8 мл, 57,4 ммоль) перед тим, як його нагрівали в умовах дефлегмації протягом 2 годин. Суміш випарювали насухо, знову розчиняли в етилацетаті (100 мл), промивали водою (20 мл), сушили (сульфатом магнію) й випарювали. Залишок розчиняли в 19 UA 101348 C2 5 10 15 20 25 30 35 40 2М аміаку в метанолі (50 мл) і перемішували при кімнатній температурі протягом 5 днів. Випарювання й очищення за допомогою флеш-хроматографії (3,5 % метанол у DCM) давали + білу тверду речовину (2,71г). m/z (ES+)272 і 274 (1:1 [M+H] ). Одержання 18 (7-Бром-2,3,4,5-тетрагідро-1,4-бензоксазепін-3-іл)метанол 1М Борановий-THF комплекс у THF (26,0 мл, 26,0 ммоль) додавали до суспензії 7-бром-3(гідроксиметил)-3,4-дигідро-1,4-бензоксазепін-5(2Н)-ону (2,36 г, 8,67 ммоль) у THF (5 мл), і суміш нагрівали в умовах дефлегмації протягом 5 годин, потім охолоджували до кімнатної температури. Додавали 5М водний розчин HCl (50 мл), і суміш нагрівали в умовах дефлегмації протягом 1 години, потім охолоджували до кімнатної температури. Випарювання й азеотропна дистиляція залишкового розчинника етанолом (100 мл) залишали залишок, який знову розчиняли в етанолі (100 мл) і триетиламіні (20 мл), потім знову концентрували. Очищення за допомогою флеш-хроматографії (5 % метанол у DCM) давало сирий продукт, який розподіляли між етилацетатом (300 мл) і водою (100 мл). Дану суміш перетворювали на основу 2М водним розчином гідроксиду натрію, потім органічні речовини сушили (сульфатом магнію) й + випарювали, одержуючи білу тверду речовину (1,93 г). m/z(ES+) 258 і 260(1:1 [M+H] ). Одержання 19 1,1-Диметилетил 7-бром-3-(гідроксиметил)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату Суміш (7-бром-2,3,4,5-тетрагідро-1,4-бензоксазепін-3-іл)метанолу (1,93 г, 7,48 ммоль) і ВОСангідриду (2,08 мл, 8,97 ммоль) у THF (30 мл) і насиченого водного розчину бікарбонату натрію (30 мл) перемішували при кімнатній температурі протягом 2 годин. Суміш розбавляли етилацетатом (100 мл), промивали водою (50 мл), сушили (сульфатом магнію), випарювали й очищали за допомогою флеш-хроматографії (етилацетат/ізогексан, 2:3), одержуючи білу тверду + речовину (2,36 г). m/z (ES+) 258 і 260 (1:1 [M+H-100] ). Одержання 20 1,1-Диметилетил 7-ціано-3-(гідроксиметил)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату Суміш 1,1-диметилетил 7-бром-3-(гідроксиметил)-2,3-дигідро-1,4-бензоксазепін-4(5Н)карбоксилату (2,05 г, 5,72 ммоль), ціаніду цинку (1,34 г, 11,5 ммоль) і тетракис(трифенілфосфін) паладію (0,992 г, 0,858 ммоль) у DMF (20 мл) перемішували при 80ºC у атмосфері аргону протягом 3 годин. Суміш охолоджували, розбавляли етилацетатом/водою (по 150 мл кожного) й шари розділяли. Органічну фазу промивали водою (3×30 мл), сушили (сульфатом магнію), випарювали й очищали за допомогою флеш-хроматографії (етилацетат/ізогексан, 1:1), + одержуючи білу тверду речовину (1,43 г). m/z (ES+) 205 [M+H-100] . Одержання 21 1,1-Диметилетил 7-[(гідроксіаміно)(іміно)метил]-3-(гідроксиметил)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату 20 UA 101348 C2 5 10 15 20 25 30 35 Суміш 1,1-диметилетил 7-ціано-3-(гідроксиметил)-2,3-дигідро-1,4-бензоксазепін-4(5Н)карбоксилату (1,43 г, 4,70 ммоль), гідрохлориду гідроксиламіну (0,653 г, 9,40 ммоль) і бікарбонату натрію (1,974 г, 23,5 ммоль) в етанолі (20 мл) перемішували при 50ºС протягом 15 годин, потім охолоджували й розбавляли сумішшю етилацетат/вода (по 100 мл кожного). Водну фазу повторно екстрагували етилацетатом (50 мл), потім об'єднані органічні речовини сушили + (сульфатом магнію) й випарювали, одержуючи білу піну (1,60 г). m/z (ES+) 338 [M+H] . Одержання 22 1,1-Диметилетил 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-3-(гідроксиметил)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату Суміш 1,1-диметилетил 7-[(гідроксіаміно)(іміно)метил]-3-(гідроксиметил)-2,3-дигідро-1,4бензоксазепін-4(5Н)-карбоксилату (1,59 г, 4,71 ммоль), 3-хлор-4-[(1-метилетил)окси]бензойної кислоти (Paragos Product, 1,012 г, 4,71 ммоль), HOBt (0,794 г, 5,18 ммоль) і EDC (0,994 г, 5,18 ммоль) у ДМФ (20мл) перемішували при кімнатній температурі протягом 30 хвилин, потім нагрівали при 100ºС протягом 5 годин. Суміш охолоджували, розбавляли етилацетатом (150 мл), потім промивали водою (100 мл), насиченим водним розчином бікарбонату натрію й водою (3×50 мл). Випарювання, а потім очищення за допомогою флеш-хроматографії + (етилацетат/ізогексан, 45:55) давали білу тверду речовину (673 мг). m/z (ES+) 516 [M+H] . Одержання 23 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-4-{[(1,1диметилетил)окси]карбоніл}-2,3,4,5-тетрагідро-1,4-бензоксазепін-3-карбонова кислота Реагент Джонса [одержаний з триоксиду хрому (0,213 г, 2,13 ммоль) і сірчаної кислоти (184 мкл, 3,45 ммоль), доведений до 0,8 мл водою] додавали до охолодженого льодом розчину 1,1диметилетил 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-3-(гідроксиметил)2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату (0,103 г, 0,2 ммоль) в ацетоні (4 мл), і одержану суміш перемішували на льоду протягом 2 годин. Додавали IPA (0,5 мл) з подальшим додаванням води (20 мл) і етилацетату (40 мл). Органічну фазу сушили (сульфатом магнію), випарювали й очищали за допомогою флеш-хроматографії (етилацетат/ізогексан 1:1, потім 1 % оцтова кислота в суміші етилацетат/ізогексан, 1:1), одержуючи білу тверду речовину (72 мг). m/z + (ES+) 530 [M+H] . Одержання 24 1,1-Диметилетил 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-3-форміл2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату Перйодинан Десс-Мартина (0,127 г, 0,300 ммоль) додавали до розчину 1,1-диметилетил 7(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-3-(гідроксиметил)-2,3-дигідро-1,4 21 UA 101348 C2 5 10 15 20 25 30 35 бензоксазепін-4(5Н)-карбоксилату (0,155 г, 0,30 ммоль) у DCM (5 мл) в атмосфері аргону, і одержану суміш перемішували при кімнатній температурі протягом 1 години. Додавали DCM (30 мл), потім суміш промивали розчином тіосульфату натрію (3 г) в насиченому водному бікарбонаті натрію (20 мл). Органічну фазу сушили (сульфатом магнію), випарювали й очищали за допомогою флеш-хроматографії (етилацетат/ізогексан, 2:3), одержуючи камедь, яку + розтирали з ефіром, одержуючи білу тверду речовину (136 мг). m/z (ES+) 513 [M ]. Одержання 25 1,1-Диметилетил 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-3-[(1E)-3(етилокси)-3-оксо-1-пропен-1-іл]-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату Суміш 1,1-диметилетил 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-3форміл-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату (0,136 г, 0,265 ммоль) і 5 етил(трифеніл- -фосфаніліден) ацетату (0,101 г, 0,291 ммоль) в ТГФ (4 мл) перемішували при 40ºС у атмосфері аргону протягом 1 години. Випарювання й очищення за допомогою флешхроматографії (етилацетат/ізогексан, 1:4), давали безбарвну камедь (109 мг). m/z (ES+) 584 + [M+H] . Одержання 26 1,1-Диметилетил 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-3-[3етилокси)-3-оксопропіл]-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату Розчин 1,1-диметилетил 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-3[(1E)-3-(етилокси)-3-оксо-1-пропен-1-іл]-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату (0,109г, 0,187ммоль) в етанолі (20 мл) гідрували 10 % Pd/C (0,030 г, 0,282 ммоль, 50 % вода) протягом 45 хвилин, потім фільтрували, випарювали й очищали за допомогою флешхроматографії (етилацетат/ізогексан, 1:4), одержуючи безбарвну камедь (59 мг). m/z (ES+) 586 + [M+H] . Одержання 27 3-(7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-4-{[(1,1диметилетил)окси]карбоніл}-2,3,4,5-тетрагідро-1,4-бензоксазепін-3-іл)пропанова кислота 2М Водний розчин гідроксиду натрію (1,0 мл, 2,0 ммоль) додавали до розчину 1,1диметилетил 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-3-[3-(етилокси)-3оксопропіл]-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату (0,059 г, 0,101 ммоль) в етанолі (4 мл) і перемішували при кімнатній температурі протягом 2 годин. Суміш випарювали, потім розподіляли між водою й етилацетатом (25 мл кожен) і підкисляли 2М водним HCl. Органічну фазу сушили (сульфатом магнію) і випарювали, одержуючи безбарвну камедь (55 мг). m/z (ES-) 556 [M-H] . Одержання 28 Етил (2Е)-3-(3-бром-2-гідроксифеніл)-2-пропеноату 22 UA 101348 C2 5 10 15 20 25 30 35 До розчину 3-бром-2-гідроксибензальдегіду (WO/9606822; 1,005 г, 5,0 ммоль) у дихлорметані (20 мл) при кімнатній температурі додавали (карбоксиметилен)трифенілфосфоран (Aldrich; 2,09 г, 6,0ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 3 годин, потім розчинник випарювали. Очищення залишку за допомогою хроматографії з елююванням 20 % етилацетатом у циклогексані давало вказану в заголовку сполуку у вигляді білої твердої речовини (1,2 г). МС + (ES) C11H11BrO3 обчислено 270, 272; знайдено 271, 273 [M+H] . Одержання 29 Етил (2Е)-3-(3-бром-2-{[2-({[(1,1-диметилетил)окси]карбоніл}аміно)етил]окси}феніл)-2пропеноату До розчину етил (2Е)-3-(3-бром-2-гідроксифеніл)-2-пропеноату (Одержання 28) (870 мг, 3,21ммоль), 1,1-диметилетил (2-гідроксиетил) карбамату (Aldrich; 517 мг, 3,21 ммоль) і трифенілфосфіну (926 мг, 3,53 ммоль) у тетрагідрофурані (20 мл) при 0ºС додавали діізопропілазодикарбоксилат (714 мг, 3,53 ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 2 годин. Розчинник випарювали, а залишок розчиняли в етилацетаті, потім промивали двічі сольовим розчином. Органічну фазу сушили й випарювали. Очищення за допомогою хроматографії з елююванням 20 % етилацетатом у циклогексані давало продукт у вигляді безбарвного масла (1,23 г). МС (ES) C 18H24BrNO5 обчислено 413, 415; знайдено 414, 416 + [M+H] . Одержання 30 Етил (2Е)-3-{2-[(2-аміноетил)окси]-3-бромфеніл}-2-пропеноату сіль трифторооцтової кислоти До розчину етил (2Е)-3-(3-бром-2-{[2-({[(1,1-диметилетил)окси]карбоніл}аміно)етил]окси}феніл)-2-пропеноату (Одержання 29) (0,207 г, 0,5 ммоль) у дихлорметані (4 мл) на крижаній бані повільно додавали трифторооцтову кислоту (1 мл). Через 1 годину реакційну суміш концентрували насухо й залишок переганяли азеотропно з діетиловим ефіром. Залишок сушили у вакуумі, одержуючи сирий або неочищений продукт у вигляді масла (0,214 г). МС (ES) + C13H16BrNO3 обчислено 313, 315; знайдено 314, 316 [M+H] . Одержання 31 Етил (9-бром-2,3,4,5-тетрагідро-1,4-бензоксазепін-5-іл)ацетату До розчину етил (2Е)-3-{2-[(2-аміноетил)окси]-3-бромфеніл}-2-пропеноату (Одержання 30) (1,4 г, 4,46 ммоль) у тетрагідрофурані (40 мл) при кімнатній температурі в атмосфері азоту 23 UA 101348 C2 5 10 15 20 25 30 додавали 1,8-діазабіцикло[5.4.0]ундец-7-ен (0,678 г, 4,46 ммоль), і реакційну суміш перемішували при кімнатній температурі протягом ночі. Розчинник випарювали, а залишок очищали за допомогою хроматографії при елююванні 0-2 % метанолом у дихлорметані, одержуючи вказану в заголовку сполуку у вигляді безбарвного масла (1,31 г). МС (ES) + C13H16BrNO3 обчислено 313, 315; знайдено 314, 316 [M+H] . Одержання 32 1,1-Диметилетил (9-бром-5-[2-(етилокси)-2-оксоетил]-2,3-дигідро-1,4-бензоксазепін-4(5Н)карбоксилату До розчину етил (9-бром-2,3,4,5-тетрагідро-1,4-бензоксазепін-5-іл)ацетату (Одержання 31) (12,3г, 39,2 ммоль) у тетрагідрофурані (200 мл) при 0ºС додавали триетиламін (4,77 г, 47,1 ммоль), потім ди-трет-бутилдикарбонат (9,42 г, 43,2 ммоль). Через 2 хвилини крижану баню видаляли й реакційну суміш залишали стояти при кімнатній температурі впродовж кінця тижня (вихідних). Розчинник випарювали й залишок очищали за допомогою хроматографії при елююванні 3-15 % етилацетатом у циклогексані, одержуючи продукт у вигляді безбарвного + масла (15,7 г). МС (ES) C18H24BrNO5 обчислено 413, 415; знайдено 414, 416 [M+H] . Одержання 33 1,1-Диметилетил 9-ціано-5-[2-(етилокси)-2-оксоетил]-2,3-дигідро-1,4-бензоксазепін-4(5Н)карбоксилату Розчин 1,1-диметилетил 9-бром-5-[2-(етилокси)-2-оксоетил]-2,3-дигідро-1,4-бензоксазепін4(5Н)-карбоксилату (Одержання 32) (1,02 г, 2,47 ммоль) у N, N-диметилформаміді (ДМФ) (7 мл) дегазували у вакуумі протягом 15 хвилин, потім додавали ціанід цинку (348 мг, 2,98 ммоль) і тетракис(трифенілфосфін)паладій(0) (285 мг, 0,247 ммоль), і одержану жовту суміш перемішували в атмосфері азоту при 100ºС протягом 5 годин. Охолоджену суміш фільтрували і промивали ДМФ. Фільтрат випарювали й залишок розподіляли між етилацетатом і сольовим розчином. Об'єднані органічні екстракти промивали сольовим розчином, і органічну фазу сушили і випарювали. Очищення за допомогою флеш-хроматографії при елююванні 20 % етилацетатом в циклогексані давало вказану в заголовку сполуку у вигляді безбарвної твердої + речовини (760 мг). МС (ES) C19H24N2O5 обчислено 360; знайдено 361 [M+H] . Одержання 34 1,1-Диметилетил 5-[2-(етилокси)-2-оксоетил]-9-[(гідроксіаміно)(іміно)метил]-2,3-дигідро-1,4бензоксазепін-4(5Н)-карбоксилату 24 UA 101348 C2 5 10 15 20 25 Суміш 1,1-диметилетил 9-ціано-5-[2-(етилокси)-2-оксоетил]-2,3-дигідро-1,4-бензоксазепін4(5Н)-карбоксилату (Одержання 33) (1,08 г, 3,0 ммоль), гідрохлориду гідроксиламіну (521 мг, 7,5 ммоль) і бікарбонату натрію (630 міліграм, 7,5 ммоль) в етанолі (15 мл) нагрівали із зворотним холодильником протягом 5 годин. Реакційну суміш охолоджували до кімнатної температури, фільтрували через целіт і розчинник випарювали. Залишок очищали за допомогою хроматографії при елююванні 0-5 % метанолом в дихлорметані, одержуючи вказану в заголовку сполуку у вигляді безбарвної піни (0,968 г). МС (ES) C19H27N3O6 обчислено 393; знайдено 394 + [M+H] . Одержання 35 1,1-Диметилетил 9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-5-[2(етилокси)-2-оксоетил]-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату До розчину 1,1-диметилетил 5-[2-(етилокси)-2-оксоетил]-9-[(гідроксіаміно)(іміно)метил]-2,3дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату (Одержання 34) (826 мг, 2,09 ммоль) і триетиламіну (255мг, 2,52 ммоль) у N, N-диметилформаміді (21 мл) додавали 3-хлор-4-[(1метилетил)окси]бензоїлхлорид (Одержання 41) (401 мг, 2,09 ммоль) в атмосфері азоту. Суміш перемішували при кімнатній температурі протягом 10 хвилин, потім при 120ºС протягом 20 хвилин. Через 20 хвилин додавали ще триетиламін (51 мг, 0,504 ммоль) і 3-хлор-4-[(1метилетил)окси]бензоїлхлорид (80,2 мг, 0,418 ммоль), і суміш перемішували при 120ºС протягом 6 годин. Суміш охолоджували до кімнатної температури й розчинник випарювали. Залишок розчиняли в етилацетаті й розчин промивали 2 нормальним гідроксидом натрію, потім сольовим розчином, сушили (сульфатом натрію) й випарювали. Очищення залишку за допомогою хроматографії при елююванні 20 % етилацетатом у циклогексані давало вказану в 35 заголовку сполуку у вигляді піни (740 мг). МС (ES) C 29H34 ClN3O7 обчислено 571; знайдено 572 + [M+H] . Одержання 36 Натрієва сіль (9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-4-{[(1,1диметилетил)окси]карбоніл}-2,3,4,5-тетрагідро-1,4-бензоксазепін-5-іл) оцтової кислоти 25 UA 101348 C2 5 10 15 20 25 Суміш 1,1-диметилетил 9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-5-[2(етилокси)-2-оксоетил]-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату (Одержання 35) (120 мг, 0,21ммоль), етанолу (1 мл) і 2М гідроксиду натрію (2 мл) перемішували при 60ºС протягом 1 години. Реакційну суміш охолоджували й розчинник випарювали. Залишок суспендували у воді (2 мл) і екстрагували етилацетатом (2×2 мл). Об'єднані екстракти сушили (сульфатом натрію) і випарювали. Розтирання залишку з діетиловим ефіром давало вказану в заголовку сполуку у вигляді безбарвної твердої речовини (90 мг). МС (ES) C27H30ClN3O7 обчислено 543; знайдено + 544 [M+H] . Одержання 37 1,1-Диметилетил 9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-5-[2(етилокси)-2-оксоетил]-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату i) Оксалілхлорид (152 мг, 105 мкл, 1,2 ммоль) додавали до перемішуваного розчину 3-ціано4-[(1-метилетил)окси]бензойної кислоти (WO2001002355; 205 мг, 1 ммоль) в сухому дихлорметані (5 мл) з подальшим додаванням N, N-диметилформаміду (1 крапля, каталізатор) і реакційну суміш перемішували при кімнатній температурі протягом 1 години. Розчинник потім випарювали, а залишок сушили у вакуумі протягом 30 хвилин. ii) Розчин неочищеного хлорангідриду кислоти (стадія i) (1 ммоль) в ацетонітрилі (5 мл) додавали по краплях до перемішуваного розчину 1,1-диметилетил 5-[2-(етилокси)-2-оксоетил]9-[(гідроксіаміно)(іміно)метил]-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату (Одержання 34) (393 мг, 1ммоль) і триетиламіну (121 мг, 167 мкл, 1,2 ммоль) в ацетонітрилі (5 мл) і суміш перемішували при кімнатній температурі протягом 1 години, потім нагрівали при температурі кипіння із зворотним холодильником протягом 72 годин. Реакційну суміш охолоджували, й розчинник випарювали. Залишок очищали за допомогою хроматографії при елююванні 15-25 % етилацетатом у циклогексані, одержуючи вказану в заголовку сполуку у вигляді безбарвного + масла (180 мг). МС (ES) C30H34N4O7 обчислено 562; знайдено 563 [M+H] . 26 UA 101348 C2 Одержання 38 (9-(5-{3-Ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-4-{[(1,1диметилетил)окси]карбоніл}-2,3,4,5-тетрагідро-1,4-бензоксазепін-5-іл)оцтової кислоти 5 10 15 20 25 30 Суміш 1,1-диметилетил 9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-5-[2(етилокси)-2-оксоетил]-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату (Одержання 37) (170 мг, 0,30ммоль), 2М гідроксиду натрію (2 мл) і етанолу (4 мл) перемішували при 60ºС протягом 1 години. Реакційну суміш охолоджували до кімнатної температури й етанол випарювали. Залишок розбавляли водою (5 мл) і підкисляли крижаною оцтовою кислотою. Суміш екстрагували етилацетатом (3×5 мл). Об'єднані екстракти сушили (сульфатом натрію) й випарювали. Залишок сушили в умовах високого вакууму, одержуючи вказану в заголовку сполуку у вигляді безбарвної піни (150 мг). МС (ES) C 28H30N4O7 обчислено 534; знайдено 535 + [M+H] . Одержання 39 1,1-Диметилетил 9-(5-{5-хлор-6-[(1-метилетил)окси]-3-піридиніл}-1,2,4-оксадіазол-3-іл)-5-[2(етилокси)-2-оксоетил]-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату i) Оксалілхлорид (152 мг, 105 мкл, 1,2 ммоль) додавали до перемішуваного розчину 5-хлор6-[(1-метилетил)окси]-3-піридинкарбонової кислоти (WO9702244; 215 мг, 1 ммоль) у сухому дихлорметані (5 мл) з подальшим додаванням ДМФ (1 крапля, каталізатор) і реакційну суміш перемішували при кімнатній температурі протягом 1 години. Розчинник потім випарювали, а залишок сушили у вакуумі протягом 30 хвилин. ii) Розчин неочищеного хлорангідриду кислоти (стадія i) (1 ммоль) в ацетонітрилі (5 мл) додавали по краплях до перемішуваного розчину 1,1-диметилетил 5-[2-(етилокси)-2-оксоетил]9-[(гідроксіаміно)(іміно)метил]-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату (Одержання 34) (393 мг, 1ммоль) і триетиламіну (121 мг, 167 мкл, 1,2 ммоль) в ацетонітрилі (5 мл) і суміш перемішували при кімнатній температурі протягом 1 години, потім нагрівали при температурі кипіння із зворотним холодильником протягом 72 годин. Реакційну суміш охолоджували і розчинник випарювали, а залишок очищали за допомогою хроматографії. Елюювання 15-25 % етилацетатом в циклогексані давало вказану в заголовку сполуку у вигляді блідо-жовтого масла 35 + (180 мг). МС (ES) C28H33 ClN4O7 обчислено 572; знайдено 573 [M+H] . Одержання 40 (9-(5-{5-хлор-6-[(1-метилетил)окси]-3-піридиніл}-1,2,4-оксадіазол-3-іл)-4-{[(1,1диметилетил)окси]карбоніл}-2,3,4,5-тетрагідро-1,4-бензоксазепін-5-іл)оцтової кислоти 27 UA 101348 C2 5 10 15 20 25 30 35 Суміш 1,1-диметилетил 9-(5-{5-хлор-6-[(1-метилетил)окси]-3-піридиніл}-1,2,4-оксадіазол-3іл)-5-[2-(етилокси)-2-оксоетил]-2,3-дигідро-1,4-бензоксазепін-4(5Н)-карбоксилату (Одержання 39) (170 мг, 0,30 ммоль), 2М гідроксиду натрію (5 мл) і етанолу (8 мл) перемішували при 60ºС протягом 1 години. Реакційну суміш охолоджували до кімнатної температури й етанол випарювали. Залишок розбавляли водою (10 мл) і підкисляли крижаною оцтовою кислотою. Суміш екстрагували етилацетатом (3×5 мл). Об'єднані екстракти сушили (сульфатом натрію) й випарювали. Залишок сушили в умовах високого вакууму, одержуючи вказану в заголовку 35 сполуку у вигляді безбарвної піни (150 мг). МС (ES) C 26H29 ClN4O7 обчислено 544; знайдено 545 + [M+H] . Одержання 41 3-Хлор-4-[(1-метилетил)окси]бензоїлхлориду Круглодонну колбу завантажували 3-хлор-4-[(1-метилетил)окси]бензойною кислотою (Paragos Product List, 10,2 г, 47,5 ммоль), дихлорметаном (158 мл) і оксалілхлоридом (8,29 мл, 95 ммоль). Реакційну суміш охолоджували до 0ºС на бані лід/вода перед додаванням N, Nдиметилформаміду (0,158 мл). Розчину давали можливість підігрітися до температури довкілля протягом ночі. Розчинник випарювали, одержуючи вказану в заголовку сполуку у вигляді кремової твердої речовини (11,4 г). δH (CDCl3, 400 МГц): 1,44 (6H, д), 4,73 (1H, септет), 6,98 (1H, д), 8,0 (1H, дд), 7,98 (1H, д). Одержання 42 1,2-Диметилетил 9-ціано-5-(2-гідроксиетил)-2,3-дигідро-1,4-бензоксазепін-4(5Н)карбоксилату До розчину 1,1-диметилетил 9-ціано-5-[2-(етилокси)-2-оксоетил]-2,3-дигідро-1,4бензоксазепін-4(5Н)-карбоксилату (Одержання 33) (282 мг, 0,78 ммоль) в етанолі (5 мл) додавали борогідрид літію, 2,0М розчин у ТГФ (0,587 мл, 1,17 ммоль). Після перемішування при кімнатній температурі протягом 1 години додавали діетиловий ефір (5 мл). Через 30 хвилин додавали борогідрид літію, 2,0М розчин у ТГФ (0,500 мл, 1,0 ммоль) і реакційну суміш перемішували при кімнатній температурі протягом 3 днів. Суспензію розчиняли в метанолі (40 мл) і гасили при 0ºС 2М соляною кислотою. Більшість розчинника випарювали. Залишок розбавляли етилацетатом і промивали сольовим розчином. Органічну фазу сушили і випарювали, одержуючи вказану в заголовку сполуку (224 мг). МС (ES) C 17H22N2O4 обчислено + 318, знайдено 319 [M+H] . Одержання 43 1,1-Диметилетил 9-ціано-5-[(2E)-4-(етилокси)-4-оксо-2-бутен-1-іл]-2,3—дигідро-1,4бензоксазепін-4(5H)-карбоксилату 28
ДивитисяДодаткова інформація
Назва патенту англійськоюNormal;heading 1;heading 2;heading 3;1,2,4 -oxadiazole compounds for the treatment of autoimmune diseases
Автори англійськоюHeer, Jag, Paul, Heightman, Thomas, Daniel, Hurst, David, Nigel, Johnson Christopher Norbert, Skidmore, John, Wall, Ian, David
Назва патенту російською1,2,4-оксадиазольные соединения для лечения аутоиммунных заболеваний
Автори російськоюХир Джаг Пол, Хейгтмен Томас Дениэл, Херст Девид Найджел, Джонсон Кристофер Норберт, Скидмор Джон, Уолл Йан Девид
МПК / Мітки
МПК: C07D 413/14, A61P 37/00, A61K 31/553, C07D 413/04
Мітки: 1,2,4-оксадіазольні, захворювань, аутоімунних, лікування, сполуки
Код посилання
<a href="https://ua.patents.su/47-101348-124-oksadiazolni-spoluki-dlya-likuvannya-autoimunnikh-zakhvoryuvan.html" target="_blank" rel="follow" title="База патентів України">1,2,4-оксадіазольні сполуки для лікування аутоімунних захворювань</a>
Попередній патент: Пристрій для приготування напою із знімною інжекційною деталлю, знімна інжекційна деталь, система (варіанти), що включає пристрій для приготування напою
Наступний патент: Похідні оксадіазолу, активні у відношенні сфінгозин-1-фосфату (s1p)
Випадковий патент: Кришка для контейнера, зокрема для пляшки