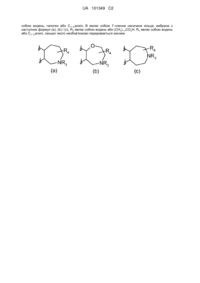
Похідні оксадіазолу, активні у відношенні сфінгозин-1-фосфату (s1p)
Номер патенту: 101349
Опубліковано: 25.03.2013
Автори: Херст Девід Найджел, Демон Емманюель Юбер, Джонсон Крістофер Норберт, Скідмор Джон, Хір Джаг Пол, Уітерінгтон Джейсон, Хейгтмен Томас Деніел, Уолл Йан Девід
Формула / Реферат
1. Сполука формули (І) або її фармацевтично прийнятна сіль:
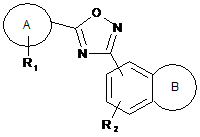 , (I)
, (I)
А являє собою феніл або 5- або 6-членне кільце гетероарилу;
R1 являє собою до двох замісників, незалежно вибраних з галогену, С(1-3)алкокси, С(1-3)фторалкілу, ціано, необов'язково заміщеного фенілу, С(1-3)фторалкокси, С(1-6)алкілу і С(3-6)циклоалкілу;
R2 являє собою водень, галоген або С(1-4)алкіл;
В являє собою 7-членне насичене кільце, вибране з наступних кілець:
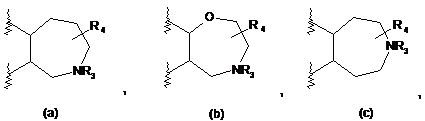
R3 являє собою водень або (CH2)1-4CO2H;
R4 являє собою водень або С(1-3)алкіл, ланцюг якого необов'язково переривається киснем.
2. Сполука формули (І) або її фармацевтично прийнятна сіль за п. 1, у якій:
А являє собою феніл;
R1 являє собою до двох замісників, незалежно вибраних із хлору, ізопропокси і ціано;
R2 являє собою водень;
В являє собою кільце (а);
R3 являє собою водень або (CH2)1-3CO2H;
R4 являє собою водень.
3. Сполука формули (І) або її фармацевтично прийнятна сіль за п. 1, у якій:
А являє собою феніл або піридиніл; і/або
R1 являє собою до двох замісників, незалежно вибраних із хлору, ізопропокси і ціано; і/або
R2 являє собою водень; і/або
В являє собою кільце (b); і/або
R3 являє собою водень або (CH2)1-4CO2H; і/або
R4 являє собою водень.
4. Сполука формули (І) або її фармацевтично прийнятна сіль за п. 1, у якій:
А являє собою феніл або піридиніл;
R1 являє собою до двох замісників, незалежно вибраних із хлору, метокси, ізопропокси, трифторметилу, фенілу і ціано;
R2 являє собою водень;
В являє собою кільце (с);
R3 являє собою водень або (CH2)1-3CO2H;
R4 являє собою водень.
5. Сполука за п. 1, вибрана з групи:
7-(5-{3-хлор-4-[(1-метилетилокси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1Н-2-бензазепіну,
[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5-тетрагідро-2Н-2-бензазепін-2-іл]оцтової кислоти,
2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1Н-2-бензазепін-7-іл)-1,2,4-оксадіазол-5-іл]бензонітрилу,
[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5-тетрагідро-2Н-2-бензазепін-2-іл]оцтової кислоти,
4-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5-тетрагідро-2Н-2-бензазепін-2-іл]бутанової кислоти,
3-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5-тетрагідро-2Н-2-бензазепін-2-іл]пропанової кислоти,
2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1Н-3-бензазепін-6-іл)-1,2,4-оксадіазол-5-іл]бензонітрилу,
6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1Н-3-бензазепіну,
3-[6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3Н-3-бензазепін-3-іл]пропанової кислоти,
[6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3Н-3-бензазепін-3-іл]оцтової кислоти,
6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1Н-2-бензазепіну,
[6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5-тетрагідро-2Н-2-бензазепін-2-іл]оцтової кислоти,
8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4-бензоксазепіну,
3-[8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]пропанової кислоти,
4-[8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]бутанової кислоти,
[8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]оцтової кислоти,
7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1Н-3-бензазепіну,
2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1Н-3-бензазепін-7-іл)-1,2,4-оксадіазол-5-іл]бензонітрилу,
7-{5-[4-[(1-метилетил)окси]-3-(трифторметил)феніл]-1,2,4-оксадіазол-3-іл}-2,3,4,5-тетрагідро-1Н-3-бензазепіну,
7-{5-[2-(трифторметил)-4-біфеніліл]-1,2,4-оксадіазол-3-іл}-2,3,4,5-тетрагідро-1Н-3-бензазепіну,
3-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3Н-3-бензазепін-3-іл]пропанової кислоти,
[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3Н-3-бензазепін-3-іл]оцтової кислоти,
[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3Н-3-бензазепін-3-іл]оцтової кислоти,
(7-{5-[4-[(1-метилетил)окси]-3-(трифторметил)феніл]-1,2,4-оксадіазол-3-іл}-1,2,4,5-тетрагідро-3Н-3-бензазепін-3-іл)оцтової кислоти,
(7-{5-[2-(трифторметил)-4-біфеніліл]-1,2,4-оксадіазол-3-іл}-1,2,4,5-тетрагідро-3Н-3-бензазепін-3-іл)оцтової кислоти,
4-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3Н-3-бензазепін-3-іл]бутанової кислоти,
4-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3Н-3-бензазепін-3-іл]бутанової кислоти,
4-(7-{5-[4-[(1-метилетил)окси]-3-(трифторметил)феніл]-1,2,4-оксадіазол-3-іл}-1,2,4,5-тетрагідро-3Н-3-бензазепін-3-іл)бутанової кислоти,
4-(7-{5-[2-(трифторметил)-4-біфеніліл]-1,2,4-оксадіазол-3-іл}-1,2,4,5-тетрагідро-3Н-3-бензазепін-3-іл)бутанової кислоти,
2-(метилокси)-5-[3-(2,3,4,5-тетрагідро-1Н-3-бензазепін-7-іл)-1,2,4-оксадіазол-5-іл]бензонітрилу,
9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4-бензоксазепіну,
2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1,4-бензоксазепін-9-іл)-1,2,4-оксадіазол-5-іл]бензонітрилу,
4-[9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]бутанової кислоти,
4-[9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]бутанової кислоти,
2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1,4-бензоксазепін-7-іл)-1,2,4-оксадіазол-5-іл]бензонітрилу,
гідрохлориду 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4-бензоксазепіну,
3-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]пропанової кислоти,
3-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]пропанової кислоти,
4-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]бутанової кислоти,
4-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]бутанової кислоти,
2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1,4-бензоксазепін-8-іл)-1,2,4-оксадіазол-5-іл]бензонітрилу,
4-[8-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]бутанової кислоти,
5-[9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]пентанової кислоти,
[9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]оцтової кислоти,
3-[9-(5-{5-хлор-6-[(1-метилетил)окси]-3-піридиніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]пропанової кислоти,
3-[9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]пропанової кислоти,
3-[9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]пропанової кислоти,
форміату 2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1Н-3-бензазепін-7-іл)-1,2,4-оксадіазол-5-іл]-3-піридинкарбонітрилу,
гідрохлориду 7-(5-{5-хлор-6-[(1-метилетил)окси]-3-піридиніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1Н-3-бензазепіну,
4-[7-(5-{5-хлор-6-[(1-метилетил)окси]-3-піридиніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3Н-3-бензазепін-3-іл]бутанової кислоти
і їх фармацевтично прийнятних солей.
6. Сполука за п. 1, що являє собою гідрохлорид 4-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3Н-3-бензазепін-3-іл]бутанової кислоти або її фармацевтично прийнятну сіль.
7. Сполука за п. 1, що являє собою 4-[9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4-бензоксазепін-4(5Н)-іл]бутанову кислоту або її фармацевтично прийнятну сіль.
8. Застосування сполуки за будь-яким з пп. 1-7 для лікування станів або порушень, опосередковуваних рецепторами S1P1.
9. Застосування за п. 8, у якому станом або порушенням є розсіяний склероз, аутоімунні захворювання, хронічні запальні порушення, астма, запальні невропатії, артрит, трансплантація, хвороба Крона, неспецифічний виразковий коліт, червоний вовчак, псоріаз, реперфузійне ушкодження при ішемії, солідні пухлини і метастази пухлин, захворювання, пов'язані з розвитком кровоносних судин, васкулярні захворювання, хворобливі (болючі) стани, гострі вірусні захворювання, запальні захворювання кишечнику, інсулінозалежний та інсулінонезалежний діабет.
10. Застосування за п. 9, де станом є червоний вовчак.
11. Застосування сполуки за будь-яким з пп. 1-7 для виготовлення лікарського засобу для застосування при лікуванні станів або порушень, опосередковуваних рецепторами S1P1.
12. Застосування за п. 11, де станом або порушенням є розсіяний склероз, аутоімунні захворювання, хронічні запальні порушення, астма, запальні невропатії, артрит, трансплантація, хвороба Крона, неспецифічний виразковий коліт, червоний вовчак, псоріаз, реперфузійне ушкодження при ішемії, солідні пухлини і метастази пухлин, захворювання, пов'язані з розвитком кровоносних судин, васкулярні захворювання, хворобливі (болючі) стани, гострі вірусні захворювання, запальні захворювання кишечнику, інсулінозалежний та інсулінонезалежний діабет.
13. Застосування за п. 12, де станом є червоний вовчак.
14. Фармацевтична композиція, що містить як активне начало сполуку за будь-яким з пп. 1-7.
15. Спосіб лікування станів або порушень у ссавців, у тому числі у людей, що можуть бути опосередковані за допомогою рецепторів S1P1, який включає введення пацієнтові, що страждає на захворювання, терапевтично безпечної й ефективної кількості сполуки формули (І) або її фармацевтично прийнятної солі.
16. Спосіб лікування за п. 15, де станом є червоний вовчак.
Текст
Реферат: Дана заявка стосується похідних оксадіазолу формули (І), активних у відношенні сфінгозин-1фосфату (SIP) і особливо застосовних для лікування червоного вовчака. У формулі А являє собою феніл або 5- або 6-членне кільце гетероарилу; R1 являє собою до двох замісників, незалежно вибраних з галогену, С(1-3)алкокси, С(1-3)фторалкілу, ціано, необов'язково заміщеного фенілу, С(1-3)фторалкокси, С(1-6)алкілу і С(3-6)циклоалкілу; R2 являє UA 101349 C2 (12) UA 101349 C2 собою водень, галоген або С(1-4)алкіл; В являє собою 7-членне насичене кільце, вибране з наступних формул (а), (b) і (с), R3 являє собою водень або (СН2)1-4СО2Н; R4 являє собою водень або С(1-3)алкіл, ланцюг якого необов'язково переривається киснем. UA 101349 C2 5 10 15 20 25 30 35 40 45 50 55 60 Дійсний винахід стосується нових похідних оксадіазолу, що володіють фармакологічною активністю, способів їх одержання, фармацевтичних композицій, що містять їх, і їх застосування при лікуванні різних порушень. Сфінгозин-1-фосфат (S1P) є біологічно активним ліпідним медіатором, утвореним фосфорилюванням сфінгозину сфінгозинкіназами, і виявлені в крові при високих рівнях. Він продукується і секретується цілим рядом типів клітин, що включають в себе клітини гемопоетичного походження, такі як тромбоцити і опасисті клітини (Okamoto et al 1998 J Biol Chem 273(42): 27104; Sanchez and Hla 2004, J Cell Biochem 92:913). Він володіє широким спектром біологічних дій, що включають у себе регуляцію проліферації, диференціації, рухливості клітин, васкуляризації й активації запальних клітин і тромбоцитів (Pyne and Pyne 2000, Biochem J. 349: 385). Описано п'ять підтипів S1P-сприйнятливих рецепторів, S1P1 (Edg-1), S1P2 (Edg-5), S1P3 (Edg-3), S1P4 (Edg-6) і S1P5 (Edg-8), що утворюють частину зв'язаних з Gбілком сімейства рецепторів гену ендотеліальної диференціації (Chun et al 2002 Pharmacological Reviews 54:265, Sanchez and Hla 2004 J Cellular Biochemistry, 92:913). Ці 5 рецепторів виявляють диференціальну експресію мРНК, причому S1P1-3 експресується широко, S1P4 експресується на лімфоїдних і гемопоетичних тканинах і S1P5 в основному експресується в головному мозку й у меншому ступені в селезінці. Вони передають сигнал через різні субпопуляції G-білка для стимуляції безлічі біологічних реакцій (Kluk and Hla 2002 Biochem et Biophysica Acta 1582:72, Sanchez and Hla 2004, J Cellular Biochem 92:913). Можливі ролі рецептора S1P1 містять у собі спрямовану міграцію лімфоцитів, індукцію/придушення цитокинів і впливи на ендотеліальні клітини (Rosen and Goetzl 2005 Nat Rev Immunol. 5:560). Агоністи рецептора S1P1 застосовували в ряді тваринних моделей аутоімунних реакцій і трансплантацій, що включають у себе моделі експериментального аутоімунного енцефаломієліта (ЕАЕ), для зменшення важкості індукованого захворювання (Brinkman et al 2003 JBC 277:21453; Fujino et al 2003 J Pharmacol Exp Ther 305:70; Webb et al 2004 J Neuroimmunol 153:108; Rausch et al 2004 J Magn Reson Imaging 20:16). Описано, що ця активність опосередковується дією агоністів S1P1 на циркуляцію лімфоцитів через лімфатичну систему. Обробка агоністами S1P1 приводить до секвестрації лімфоцитів у вторинних лімфатичних органах, таких як лімфатичні вузли, що індукують оборотну периферичну лімфопенію у тваринних моделей (Chiba et al 1998, J Immunology 160:5037, Forrest et al 2004 J Pharmacol Exp Ther 309:758; Sanna et al 2004 JBC 279:13839). Опубліковані дані по агоністам дозволяють припустити, що обробка сполукою індукує втрату рецептора S1P1 з поверхні клітин за допомогою інтерналізації (Graler and Goetzl 2004 FASEB J 18:551; Matloubian et al 2004 Nature 427:355; Jo et al 2005 Chem Biol 12:703) і саме це зменшення рецептора S1P1 на імунних клітинах сприяє зменшенню руху Т-клітин від лімфатичних вузлів назад у кровотік. Делеція гену S1P1 викликає ембріональну летальність. Експерименти по вивченню ролі рецептора S1P1 у міграції і спрямованій міграції лімфоцитів містили в собі адоптивне перенесення Т-клітин з дефіцитом міченого S1P1 в організм опромінених мишей дикого типу. Ці клітини показували зменшений вихід із вторинних лімфатичних органів (Matloubian et al 2004 Nature 427:355). S1P1 приписувалася також роль у модуляції сполуки ендотеліальних клітин (Allende et al 2003 102:3665, Blood Singelton et al 2005 FASEB J 19:1646). Що стосується цієї ендотеліальної дії, було описано, що агоністи S1P1 мають дію на виділені лімфатичні вузли, що може сприяти ролі в модуляції імунних порушень. Агоністи S1P1 викликали закриття ендотеліальних, що відносяться до строми "воріт" лімфатичних синусів, які дренують лімфатичні вузли і запобігають виходу лімфоцитів (Wei wt al 2005, Nat. Immunology 6:1228). Було показано, що імуносупресивна сполука FTY720 (JP11080026-А) знижує циркуляцію лімфоцитів у тварин і людини, володіє модулюючою захворювання активністю на тваринних моделях імунних порушень і знижує швидкості ремісії при зменшенні рецидивів розсіяного склерозу (Brinkman et al 2002 JBC 277:21453, Mandala et al 2002 Science 296:346, Fujino et al 2003 J Pharmacology and Experimental Therapeutics 305:45658, Brinkman et al 2004 American J Transplantation 4:1019, Webb et al 2004 J Neuroimmunology 153:108, Morris et al 2005 Eur J Immunol 35:3570, Chiba 2005 Pharmacology and Therapeutics 108:308, Kahan et al 2003, Transplantation 76:1079, Kappos et al 2006 New Eng J Medicine 335:1124). Ця сполука є проліками, що фосфорилюються in vivo сфінгозинкіназами з утворенням молекули, що має активність агоніста у відношенні рецепторів S1P1, S1P3, S1P4 і S1P5. Клінічні дослідження показали, що лікування FTY720 приводить до брадикардії в перші 24 години лікування (Kappos et al 2006 New Eng J Medicine 335:1124). На підставі ряду експериментів, проведених на клітинах і тваринах, вважається, що брадикардія є результатом агонізму у відношенні рецептора S1P3. Вони включають застосування тварин з дефіцитом S1P3, що на відміну від 1 UA 101349 C2 5 10 15 20 25 30 35 40 45 мишей дикого типу, не виявляють брадикардію після введення FTY720 і застосування S1P1селективних сполук (Hale et al 2004 Bioorganic & Medicinal Chemistry Letters 14:3501, Sanna et al 2004 JBC 279:13839, Koyrakh et al 2005 American J Transplantation 5:529). Тому існує потреба в сполуках-агоністах у відношенні S1P1 із селективністю в порівнянні з S1P3, які, як можна припускати, виявляють зменшену тенденцію індукувати брадикардію. У наступних заявках на патенти описані похідні оксадіазолу в якості агоністів S1P1: WO03/105771, WO05/058848, WO06/047195, WO06/100633, WO06/115188, WO06/131336, WO07/024922 і WO07/116866. У наступних заявках на патенти описані похідні тетрагідроізохінолінілоксадіазолу в якості агоністів S1P1: WO06/064757, WO06/001463, WO04/113330. У WO08/064377 описані бензоциклогептилсполуки, що володіють активністю у відношенні рецептора S1P1. Тепер виявлений структурно новий клас сполук, що є агоністами рецептора S1P1. Дійсний винахід відноситься до сполук формули (I) або їх фармацевтчно прийнятних солей: А являє собою феніл або 5- або 6-членне кільце гетероарилу; R1 являє собою до двох замісників, незалежно обраних з галогену, С (1-3)алкокси, С(13)фторалкілу, ціано, необов'язково заміщеного фенілу, С (1-3)фторалкокси, С(1-6)алкілу і С(36)циклоалкілу; R2 являє собою водень, галоген або С(1-4)алкіл; В являє собою 7-членне насичене кільце, обране з наступних кілець: R3 являє собою водень або (СН2)1-4СО2Н; R4 являє собою водень або С(1-3)алкіл, ланцюг якого необов'язково переривається киснем; В одному варіанті здійснення винаходу А являє собою феніл; R1 являє собою до двох замісників, незалежно обраних із хлору, ізопропокси і ціано; R2 являє собою водень; В являє собою кільце (а); R3 являє собою водень або (СН2)1-3СО2Н; R4 являє собою водень. В одному варіанті здійснення винаходу А являє собою феніл або піридиніл; R1 являє собою до двох замісників, незалежно обраних із хлору, ізопропокси і ціано; R2 являє собою водень; В являє собою кільце (b); R3 являє собою водень або (СН2)1-4СО2Н; R4 являє собою водень. В одному варіанті здійснення винаходу А являє собою феніл або піридиніл; R1 являє собою до двох замісників, незалежно обраних із хлору, метокси, ізопропокси, трифторметилу, фенілу і ціано; R2 являє собою водень; В являє собою кільце (с); R3 являє собою водень або (СН2)1-3СО2Н; R4 являє собою водень. В одному варіанті здійснення А являє собою феніл. В іншому варіанті здійснення А являє собою 3,4-дизаміщений феніл. В одному варіанті здійснення R1 являє собою два замісники, 2 UA 101349 C2 5 10 15 20 25 30 35 40 45 один із яких являє собою С(1-3)алкокси, інший обраний з галогену або ціано. В іншому варіанті здійснення R1 являє собою два замісники, один із яких являє собою ізопропокси, а другий обраний із хлору або ціано. В іншому варіанті здійснення R 1 являє собою два замісники, обрані з хлору, ізопропокси і ціано. В іншому варіанті здійснення R1 являє собою хлор та ізопропокси. У наступному варіанті здійснення R1 являє собою хлор у 3-положенні і ізопропокси в 4-положенні, коли А являє собою феніл, або R1 являє собою хлор у 5-положенні і ізопропокси в 6-положенні, коли А являє собою піридиніл. В іншому варіанті здійснення R 1 являє собою ізопропокси і ціано. У наступному варіанті здійснення R1 являє собою ціано в 3-положенні і ізопропокси в 4положенні, коли А являє собою феніл, або R 1 являє собою хлор у 5-положенні і ізопропокси в 6положенні, коли А являє собою піридиніл. В одному варіанті здійснення R2 являє собою водень. В одному варіанті здійснення В являє собою кільце (b). В іншому варіанті здійснення В являє собою кільце (с). В одному варіанті здійснення R3 являє собою (СН2)1-3СО2Н, в іншому одному варіанті здійснення R3 являє собою (СН2)3СО2Н. В одному варіанті здійснення R4 являє собою водень. Дійсний винахід відноситься також до сполук формули (ІА) або їх фармацевтично прийнятних солей: А являє собою феніл або 5- або 6-членне кільце гетероарилу; R1 являє собою до двох замісників, незалежно обраних з галогену, С (1-3)алкокси, С(13)фторалкілу, ціано, необов'язково заміщеного фенілу, С (1-3)фторалкокси, С(1-6)алкілу і С(36)циклоалкілу; R2 являє собою водень, галоген або С(1-4)алкіл; В являє собою 7-членне насичене кільце, обране з наступних кілець: R3 являє собою водень або (СН2)1-3СО2Н; R4 являє собою водень або С(1-3)алкіл, ланцюг якого необов'язково переривається киснем. В одному варіанті здійснення винаходу А являє собою феніл і/або R1 являє собою до двох замісників, незалежно обраних із хлору, ізопропокси і ціано; і/або R2 являє собою водень; і/або В являє собою кільце (а); і/або R3 являє собою водень або (СН2)1-3СО2Н; і/або R4 являє собою водень. В одному варіанті здійснення винаходу А являє собою феніл і/або R1 являє собою до двох замісників, незалежно обраних із хлору, ізопропокси і ціано; і/або R2 являє собою водень; і/або В являє собою кільце (b); і/або R3 являє собою водень або (СН2)1-3СО2Н; і/або R4 являє собою водень. В одному варіанті здійснення винаходу А являє собою феніл і/або R1 являє собою до двох замісників, незалежно обраних із хлору, метокси, ізопропокси, трифторметилу, фенілу і ціано; і/або R2 являє собою водень; і/або 3 UA 101349 C2 5 10 15 20 25 30 35 40 45 50 55 60 В являє собою кільце (с); і/або R3 являє собою водень або (СН2)1-3СО2Н; і/або R4 являє собою водень. Термін "алкіл" як групу або частину групи, наприклад, алкокси або гідроксіалкілу, відноситься до нерозгалуженої або розгалуженої алкільної групи у всіх її ізомерних формах. Термін "С(1-6)алкіл" відноситься до алкільної групи, що має значення, зазначені вище, що містить щонайменше 1 і щонайбільше 6 атомів вуглецю. Приклади таких алкільних груп містять у собі метил, етил, пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил або трет-бутил. Приклади таких алкоксигруп містять у собі метокси, етокси, пропокси, ізопропокси, бутокси, ізобутокси, вторбутокси і трет-бутокси. Підходящі С(3-6)циклоалкільні групи містять у собі циклопропіл, циклобутил, циклопентил і циклогексил. Застосовуваний у контексті термін "галоген" відноситься до фтору (F), хлору (Cl), брому (Br) або йоду (I) і термін "гало" відноситься до атома галогену: фтору (-F), хлору (-Cl), брому (-Br) і йоду (-I). Термін "гетероарил" являє собою ненасичене кільце, що містить один або декілька гетероатомів, обраних з O, N або S. Приклади 5- або 6-членних гетероарильних кілець містять в собі піроліл, триазоліл, тіадіазоліл, тетразоліл, імідазоліл, піразоліл, ізотіазоліл, тіазоліл, ізоксазоліл, оксазоліл, оксадіазоліл, фуразаніл, фураніл, тієніл, піридил, піримідиніл, піразиніл, піридазиніл і триазиніл. У деяких сполуках формули (I), в залежності від природи замісника, є хіральні атоми вуглецю і тому сполуки формули (I) можуть існувати у вигляді стереоізомерів. Винахід поширюється на всі оптичні ізомери, такі як стереоізомерні форми сполук формули (I), що включають у себе енантіомери, діастереоізомери і їх суміші, такі як рацемати. Різні стереоізомерні форми можна розділити або відщепити одного від одного загальноприйнятими способами або будь-який даний ізомер можна одержати загальноприйнятим стереоселективним або асиметричним синтезом. Деякі сполуки контексту можуть існувати в різних таутомерних формах, і повинно бути зрозуміло, що винахід включає у себе всі такі таутомерні форми. Вважається, що деякі сполуки винаходу містять як кислотні, так і основні групи і тому можуть існувати у вигляді цвіттеріонів при деяких величинах рН. Підходящими сполуками є: 7-(5-{3-хлор-4-[(1-метилетилокси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1H-2бензазепін [7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5-тетрагідро-2H-2бензазепін-2-іл]оцтова кислота 2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1H-2-бензазепін-7-іл)-1,2,4-оксадіазол-5іл]бензонітрил [7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5-тетрагідро-2H-2бензазепін-2-іл]оцтова кислота 4-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5-тетрагідро-2H-2бензазепін-2-іл]бутанова кислота 3-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5-тетрагідро-2H-2бензазепін-2-іл]пропанова кислота 2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1H-3-бензазепін-6-іл)-1,2,4-оксадіазол-5іл]бензонітрил 6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1H-3бензазепін 3-[6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3H-3бензазепін-3-іл]пропанова кислота [6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3H-3бензазепін-3-іл]оцтова кислота 6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1H-2бензазепін [6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5-тетрагідро-2H-2бензазепін-2-іл]оцтова кислота 8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4бензоксазепін 3-[8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]пропанова кислота 4 UA 101349 C2 5 10 15 20 25 30 35 40 45 50 55 60 4-[8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]бутанова кислота [8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]оцтова кислота 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1H-3бензазепін 2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1H-3-бензазепін-7-іл)-1,2,4-оксадіазол-5іл]бензонітрил 7-{5-[4-[(1-метилетил)окси]-3-(трифторметил)феніл]-1,2,4-оксадіазол-3-іл}-2,3,4,5-тетрагідро1H-3-бензазепін 7-{5-[2-(трифторметил)-4-біфеніліл]-1,2,4-оксадіазол-3-іл}-2,3,4,5-тетрагідро-1H-3-бензазепін 3-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3H-3бензазепін-3-іл]пропанова кислота [7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3H-3бензазепін-3-іл]оцтова кислота [7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3H-3бензазепін-3-іл]оцтова кислота (7-{5-[4-[(1-метилетил)окси]-3-(трифторметил)феніл]-1,2,4-оксадіазол-3-іл}-1,2,4,5тетрагідро-3H-3-бензазепін-3-іл)оцтова кислота (7-{5-[2-(трифторметил)-4-біфеніліл]-1,2,4-оксадіазол-3-іл}-1,2,4,5-тетрагідро-3H-3бензазепін-3-іл)оцтова кислота 4-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3H-3бензазепін-3-іл]бутанова кислота 4-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3H-3бензазепін-3-іл]бутанова кислота 4-(7-{5-[4-[(1-метилетил)окси]-3-(трифторметил)феніл]-1,2,4-оксадіазол-3-іл}-1,2,4,5тетрагідро-3H-3-бензазепін-3-іл)бутанова кислота 4-(7-{5-[2-(трифторметил)-4-біфеніліл]-1,2,4-оксадіазол-3-іл}-1,2,4,5-тетрагідро-3H-3бензазепін-3-іл)бутанова кислота 2-(метилокси)-5-[3-(2,3,4,5-тетрагідро-1H-3-бензазепін-7-іл)-1,2,4-оксадіазол-5-іл]бензонітрил 9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4бензоксазепін 2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1,4-бензоксазепін-9-іл)-1,2,4-оксадіазол-5іл]бензонітрил 4-[9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]бутанова кислота 4-[9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]бутанова кислота 2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1,4-бензоксазепін-7-іл)-1,2,4-оксадіазол-5іл]бензонітрил гідрохлорид 7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5тетрагідро-1,4-бензоксазепіну 3-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]пропанова кислота 3-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]пропанова кислота 4-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]бутанова кислота 4-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]бутанова кислота 2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1,4-бензоксазепін-8-іл)-1,2,4-оксадіазол-5іл]бензонітрил 4-[8-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]бутанова кислота 5-[9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]пентанова кислота [9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]оцтова кислота 3-[9-(5-{5-хлор-6-[(1-метилетил)окси]-3-піридиніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]пропанова кислота 5 UA 101349 C2 5 10 15 20 25 30 35 40 45 50 55 60 3-[9-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]пропанова кислота 3-[9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]пропанова кислота форміат 2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1H-3-бензазепін-7-іл)-1,2,4оксадіазол-5-іл]-3-піридинкарбонітрилу гідрохлорид 7-(5-{5-хлор-6-[(1-метилетил)окси]-3-піридиніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5тетрагідро-1H-3-бензазепіну 4-[7-(5-{5-хлор-6-[(1-метилетил)окси]-3-піридиніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро3H-3-бензазепін-3-іл]бутанова кислота, або їх фармацевтчно прийнятні солі. В одному варіанті здійснення винаходу сполукою формули (I) є: 4-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3H-3бензазепін-3-іл]бутанова кислота або її фармацевтично прийнятна сіль. В іншому варіанті здійснення винаходу сполукою формули (I) є: 4-[9-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]бутанова кислота або її фармацевтично прийнятна сіль. Фармацевтично прийнятні похідні сполук формули (I) включають у себе будь-яку фармацевтично прийнятну сіль, складний ефір або сіль такого складного ефіру сполуки формули (I), що при введенні реципієнтові здатні утворювати (безпосередньо або опосередковано) сполуку формули (I) або її активний метаболіт або залишок. Сполуки формули (I) можуть утворювати солі. Повинно бути зрозуміло, що для застосування в терапії солі сполук формули (I) повинні бути фармацевтично прийнятними. Підходящі фармацевтично прийнятні солі повинні бути відомі фахівцеві в даній галузі і включають у себе солі, описані в J. Pharm. Sci, 1977, 66, 1-19, такі як кислотно-адитивні солі, утворені з неорганічними кислотами, наприклад, хлористоводневою, бромистоводневою, сірчаною, азотною або фосфорною кислотою; і органічними кислотами, такими як бурштинова, малеїнова, оцтова, фумарова, лимонна, винна, бензойна, п-толуолсульфонова, метансульфонова або нафталінсульфонова кислота. Деякі зі сполук формули (I) можуть утворювати кислотноадитивні солі з одним або декількома еквівалентами кислоти. Дійсний винахід включає в себе усі можливі стехіометричні та нестехіометричні форми. Солі можна також одержати з фармацевтично прийнятних основ, що включають у себе неорганічні основи й органічні основи. Солі, отримані з неорганічних основ, включають у себе солі алюмінію, амонію, кальцію, міді, заліза (III), заліза (II), літію, магнію, марганцю (III), марганцю (II), калію, натрію, цинку тощо. Солі, утворені з фармацевтично прийнятних органічних основ, включають у себе солі первинних, вторинних і третинних амінів; заміщених амінів, що включають у себе заміщені аміни, що зустрічаються в природі; і циклічні аміни. Конкретні фармацевтично прийнятні органічні основи включають у себе аргінін, бетаїн, кофеїн, холін, N, N'-дибензилетилендіамін, діетиламін, 2діетиламіноетанол, 2-диметиламіноетанол, етаноламін, етилендіамін, N-етилморфолін, Nетилпіперидин, глюкамін, глюкозамін, гістидин, гідрабамін, ізопропіламін, лізин, метилглюкамін, морфолін, піперазин, піперидин, прокаїн, пурини, теобромін, триетиламін, триметиламін, трипропіламін, тріс(гідроксиметил)амінометан (TRIS, трометамол) тощо. Солі можна також одержати з основних іонообмінних смол, наприклад, поліамінних смол. Коли сполука дійсного винаходу є основною, солі можна одержати з фармацевтично прийнятних кислот, що включають у себе неорганічні й органічні кислоти. Такі кислоти включають у себе оцтову, бензолсульфонову, бензойну, камфорасульфонову, лимонну, етансульфонову, етандисульфонову, фумарову, глюконову, глутамінову, бромистоводневу, хлористоводневу, ізетіонову, молочну, малеїнову, яблучну, мигдальну, метансульфонову, слизову, памову, пантотенову, фосфорну, пропіонову, бурштинову, сірчану, винну, п-толуолсульфонову кислоту тощо. Фармацевтично прийнятні кислотно-адитивні солі можна одержати загальноприйнятим способом реакцією з підходящою кислотою або похідним кислоти. Фармацевтично прийнятні солі з основами можна одержати загальноприйнятим способом реакцією з підходящою неорганічною або органічною основою. Сполуки формули (I) можна одержати в кристалічній або некристалічній формі і, якщо в кристалічній формі, може бути необов'язково в гідратованій або сольватованій формі. Даний винахід включає в свій обсяг стехіометричні гідрати або сольвати, а також сполуки, що містять варіабельні кількості води і/або розчинника. В обсяг винаходу включені всі солі, сольвати, гідрати, комплекси, поліморфи, проліки, радіомічені похідні, стереоізомери й оптичні ізомери сполук формули (I). Активності й ефективності сполук даного винаходу у відношенні рецептора S1P1 можна 6 UA 101349 C2 5 10 15 20 25 30 35 40 45 50 55 60 визначити аналізом GTPS, проведеному на клонованому рецепторі людини, як описано в контексті. Сполуки формули (I) демонстрували активність агоніста у відношенні рецептора S1P1 із застосуванням описаних у контексті функціональних аналізів. Сполуки формули (I) і їх фармацевтично прийнятні солі тому є застосовними при лікуванні станів або порушень, що опосередковуються за допомогою рецептора S1P1. Зокрема, сполуки формули (I) і їх фармацевтично прийнятні солі є застосовними при лікуванні розсіяного склерозу, аутоімунних захворювань, хронічних запальних порушень, астми, запальних невропатій, артриту, при трансплантації, при лікуванні хвороби Крона, неспецифічного виразкового коліту, червоного вовчаку, псоріазу, реперфузійного ушкодження при ішемії, солідних пухлин і метастаз пухлин, захворювань, пов'язаних з розвитком кровоносних судин, васкулярних захворювань, хворобливих станів, гострих вірусних захворювань, запальних захворювань кишечнику, інсулінзалежного та інсуліннезалежного діабету (нижче в контексті названі "порушеннями винаходу"). Сполуки формули (I) і їх фармацевтично прийнятні солі, отже, є застосовними при лікуванні червоного вовчаку. Сполуки формули (I) і їх фармацевтично прийнятні солі, отже, є застосовними при лікуванні псоріазу. Сполуки формули (I) і їх фармацевтично прийнятні солі, отже, є застосовними при лікуванні розсіяного склерозу. Повинно бути зрозуміло, що термін "лікування", застосовуваний у контексті, включає у себе профілактику, а також ослаблення встановлених симптомів. Таким чином, винахід пропонує також сполуки формули (I) або їх фармацевтично прийнятні солі для застосування як терапевтичних речовин, зокрема при лікуванні станів або порушень, опосередковуваних за допомогою рецептора S1P1. Зокрема, винахід пропонує сполуку формули (I) або її фармацевтично прийнятну сіль для застосування як терапевтичної речовини при лікуванні розсіяного склерозу, аутоімунних захворювань, хронічних запальних порушень, астми, запальних невропатій, артриту, при трансплантації, при лікуванні хвороби Крона, неспецифічного виразкового коліту, червоного вовчаку, псоріазу, реперфузійного ушкодження при ішемії, солідних пухлин і метастаз пухлин, захворювань, пов'язаних з розвитком кровоносних судин, васкулярних захворювань, хворобливих станів, гострих вірусних захворювань, запальних захворювань кишечнику, інсулінзалежного і інсуліннезалежного діабету. Сполуки формули (I) і їх фармацевтично прийнятні солі є застосовними як терапевтичні речовини при лікуванні червоного вовчаку. Сполуки формули (I) і їх фармацевтично прийнятні солі є застосовними як терапевтичні речовини при лікуванні псоріазу. Сполуки формули (I) і їх фармацевтично прийнятні солі є застосовними як терапевтичні речовини при лікуванні розсіяного склерозу. Винахід далі відноситься до способу лікування станів або порушень у ссавців, у тому числі в людей, що можуть бути опосередковані за допомогою рецептора S1P1, що містить введення пацієнтові, що страждає на захворювання, терапевтично безпечної й ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. Зокрема, винахід пропонує спосіб лікування розсіяного склерозу, аутоімунних захворювань, хронічних запальних порушень, астми, запальних невропатій, артриту, спосіб застосування при трансплантації, при лікуванні хвороби Крона, неспецифічного виразкового коліту, червоного вовчаку, псоріазу, реперфузійного ушкодження при ішемії, солідних пухлин і метастаз пухлин, захворювань, пов'язаних з розвитком кровоносних судин, васкулярних захворювань, хворобливих станів, гострих вірусних захворювань, запальних захворювань кишечнику, інсулінзалежного та інсуліннезалежного діабету, що містить введення пацієнтові, що страждає на захворювання, терапевтично безпечної й ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. Винахід відноситься до способу лікування червоного вовчаку, що містить введення пацієнтові, що страждає на таке захворювання, терапевтично безпечної й ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. Винахід відноситься до способу лікування псоріазу, що містить введення пацієнтові, що страждає на таке захворювання, терапевтично безпечної й ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. Винахід відноситься до способу лікування розсіяного склерозу, що містить введення пацієнтові, що страждає на таке захворювання, терапевтично безпечної й ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. 7 UA 101349 C2 5 10 15 20 25 30 35 40 45 50 55 60 В іншому аспекті винахід відноситься до застосування сполуки формули (I) або її фармацевтично прийнятної солі при виготовленні лікарського засобу для застосування при лікуванні станів або порушень, опосередковуваних за допомогою рецептора S1P1. Зокрема, винахід відноситься до сполуки формули (I) або її фармацевтично прийнятної солі для застосування при виготовленні лікарського засобу для застосування при лікуванні розсіяного склерозу, аутоімунних захворювань, хронічних запальних порушень, астми, запальних невропатій, артриту, при трансплантації, при лікуванні хвороби Крона, неспецифічного виразкового коліту, червоного вовчаку, псоріазу, реперфузійного ушкодження при ішемії, солідних пухлин і метастаз пухлин, захворювань, пов'язаних з розвитком кровоносних судин, васкулярних захворювань, хворобливих станів, гострих вірусних захворювань, запальних захворювань кишечнику, інсулінзалежного та інсуліннезалежного діабету. Сполуки формули (I) і їх фармацевтично прийнятні солі є застосовними при виготовленні лікарського засобу для застосування при лікуванні червоного вовчаку. Сполуки формули (I) і їх фармацевтично прийнятні солі є застосовними при виготовленні лікарського засобу для застосування при лікуванні псоріазу. Сполуки формули (I) і їх фармацевтично прийнятні солі є застосовними при виготовленні лікарського засобу для застосування при лікуванні розсіяного склерозу. Для застосування сполук формули (I) і їх фармацевтично прийнятних солей у терапії їх звичайно виготовляють у складі фармацевтичної композиції відповідно до стандартної фармацевтичної практики. Дійсний винахід пропонує також фармацевтичну композицію, що містить сполуку формули (I) або її фармацевтично прийнятну сіль і фармацевтично прийнятний носій або ексципіент. У наступному аспекті дійсний винахід відноситься до способу одержання фармацевтичної композиції, причому спосіб містить змішування сполуки формули (I) або її фармацевтично прийнятної солі і фармацевтично прийнятного носія або ексципієнта. Фармацевтичну композицію винаходу, яку можна одержати змішуванням підходящим чином при температурі навколишнього середовища й атмосферному тиску, звичайно адаптують для перорального, парентерального або ректального введення, і, як така, вона може бути у формі таблеток, капсул, пероральних рідких препаратів, порошків, гранул, коржів, перестворюваних порошків, розчинів, що вводяться ін'єкцією або інфузією, або суспензій або супозиторіїв. Композиції, що вводяться перорально, звичайно є кращими. Таблетки і капсули для перорального введення можуть бути в дозованій лікарській формі і можуть містити загальноприйняті ексципієнти, такі як зв'язувальні агенти (наприклад, кукурудзяний крохмаль, що набухає в холодній воді, полівінілпіролідон або гідроксипропілметилцелюлозу); наповнювачі (наприклад, лактозу, мікрокристалічну целюлозу або гідрофосфат кальцію); таблетувальні змащувальні речовини (наприклад, стеарат магнію, тальк або діоксид кремнію); дезінтегрувальні агенти (наприклад, картопляний крохмаль або натрієву сіль гліколяту крохмалю) і прийнятні змочувальні агенти (наприклад, лаурилсульфат натрію). Таблетки можна покрити оболонкою відповідно до способів, добре відомих у звичайній фармацевтичній практиці. Пероральні рідкі препарати можуть бути у формі, наприклад, водної або масляної суспензії, розчинів, емульсій, сиропів або еліксирів або можуть бути у формі сухого продукту для перетворення з водою або іншим підходящим наповнювачем перед застосуванням. Такі рідкі препарати можуть містити загальноприйняті добавки, такі як суспендуючі агенти (наприклад, сироп сорбіту, похідні целюлози або гідрогенізовані харчові жири), емульгуючі агенти (наприклад, лецитин або аравійську камедь), неводні наповнювачі (які можуть містити в собі харчові олії, наприклад, мигдальну олію, маслянисті складні ефіри, етиловий спирт або фракціоновані рослинні олії), консерванти (наприклад, метил- або пропіл-п-гідроксибензоати або сорбінову кислоту) і, якщо необхідно, загальноприйняті коригенти або фарбувальні речовини, буферні солі й підсолоджувальні агенти, якщо потрібні. Препарати для перорального введення можна підходящим чином виготовити так, щоб відбувалося регульоване вивільнення активної сполуки. Для парентерального введення рідкі дозовані лікарські форми одержують із застосуванням сполуки винаходу або її фармацевтично прийнятних солей і стерильного наповнювача. Препарати для ін'єкції можна представити у вигляді дозованої лікарської форми, наприклад, в ампулах, або у вигляді багатьох доз із застосуванням сполуки винаходу або її фармацевтично прийнятних похідних і стерильного наповнювача, необов'язково з доданим консервантом. Композиції можуть мати такі форми, як суспензії, розчини або емульсії в масляних або водних наповнювачах, і можуть містити агенти, що утворюють форму препарату, такі як 8 UA 101349 C2 5 10 15 20 25 30 35 40 45 50 55 60 суспендувальні, стабілізувальні і/або диспергувальні агенти. Альтернативно, активний інгредієнт може бути у формі порошку для перетворення з підходящим наповнювачем, наприклад, стерильною, такою, що не містить пірогенів, водою, перед застосуванням. Сполуку, в залежності від наповнювача і застосовуваної концентрації, можна або суспендувати, або розчинити в наповнювачі. При одержанні розчинів сполуку можна розчинити для ін'єкції і стерилізувати пропущенням через фільтр перед заповненням розчином підходящого пухирця або ампули і герметизувати. Переважно ад'юванти, такі як місцеві анестетики, консерванти і буферні агенти, розчиняють у наповнювачі. Для підвищення стабільності композицію можна заморозити після заповнення в ампулу і воду видалити у вакуумі. Парентеральні суспензії одержують власне кажучи таким же способом, за винятком того, що сполуку замість розчинення суспендують у наповнювачі, і стерилізацію не можна виконувати фільтруванням. Сполуку можна стерилізувати впливом етиленоксиду перед суспендуванням у стерильному наповнювачі. У композицію переважно включають поверхнево-активну речовину або змочувальний агент для полегшення рівномірного розподілу сполуки. Лосьйони можна виготовити з водною або масляною основою, вони звичайно містять також один або декілька емульгуючих агентів, що стабілізуючих агентів, диспергуючих агентів, суспендуючих агентів, загусних агентів або фарбувальних агентів. Краплі можна виготовити з водною або неводною основою, що містить також один або декілька диспергуючих агентів, стабілізуючих агентів, солюбілізуючих агентів або суспендуючих агентів. Вони можуть містити також консервант. Сполуки формули (I) або їх фармацевтично прийнятні солі можна також виготовити в складі ректальних композицій, таких як супозіторії або утримуючі клізми, наприклад, суппозіторії, що містять загальноприйнятні основи, такі як какао-олія або інші гліцериди. Сполуки формули (I) або їх фармацевтично прийнятні солі можна виготовити також у складі препаратів-депо. Такі препарати тривалої дії можна вводити імплантацією (наприклад, підшкірно або внутрішньом'язово) або внутрішньом'язовою ін'єкцією. Так, наприклад, сполуку винаходу можна виготовити з підходящими полімерними або гідрофобними речовинами (наприклад, у вигляді емульсії в підходящій олії) або іонообмінними смолами, або у вигляді слабкорозчинних похідних, наприклад, у вигляді слабкорозчинної солі. Для інтраназального введення сполуки формули (I) або їх фармацевтично прийнятні солі можна виготовити у вигляді розчинів для введення за допомогою пристрою для подачі підходящим чином обмірюваної кількості або уніфікованої дози або в альтернативному випадку у вигляді порошкоподібної суміші з підходящим носієм для введення із застосуванням підходящого пристрою для доставки. Таким чином, сполуки формули (I) або їх фармацевтично прийнятні солі можна виготовити для перорального, букального, парентерального, місцевого (у тому числі офтальмічного і назального) введення, введення типу депо або ректального введення, або у формі, що підходить для введення інгаляцією або інсуфляцією (або через рот, або через ніс). Сполуки формули (I) або їх фармацевтично прийнятні солі можна виготовити для місцевого введення у формі мазей, кремів, гелів, лосьйонів, песарій, аерозолів або крапель (наприклад, крапель для очей, вух або носа). Мазі та креми можна виготовляти, наприклад, з водною або масляною основою з додаванням підходящих загусних і/або гелеутворюючих агентів. Мазі для введення в очі можна виготовити стерильним способом із застосуванням стерилізованих компонентів. Композиція може містити від 0,1 % до 99 мас. %, переважно від 10 до 60 мас. % активної речовини, у залежності від способу введення. Доза сполуки, застосовуваної при лікуванні вищевказаних порушень, звичайно варіює звичайним чином залежно від важкості порушень, маси тіла пацієнта, що страждає на захворювання, й інших аналогічних факторів. Однак, у якості загальних орієнтованих підходящих уніфікованих доз можуть бути кількості 0,05-1000 мг, 1,0-500 мг або 1,0-200 мг, і такі уніфіковані дози можна вводити більш ніж один раз на день, наприклад, два або три рази на день. Сполуки формули (I) або їх фармацевтично прийнятні солі можна застосовувати в комбінованих препаратах, у комбінації з іншими активними інгредієнтами. Наприклад, сполуки винаходу можна застосовувати в комбінації з циклоспорином А, метотрексатом, стероїдами, рапаміцином, інгібіторами прозапальних цитокінів, імуномодуляторами, що включають у себе біологічні або інші терапевтично активні сполуки. Предмет винаходу включає у себе також мічені ізотопом сполуки, що є ідентичними сполукам, описаним у формулах (I) і наступних, за винятком того факту, що один або кілька атомів замінені атомом, що має атомну масу або масове число, відмінне від атомної маси або масового числа атома, що звичайно знаходиться в природі. Приклади ізотопів, які можна 9 UA 101349 C2 5 10 15 20 25 30 35 включити в сполуки винаходу, включають у себе ізотопи водню, вуглецю, азоту, кисню, 3 11 14 18 123 125 фосфору, фтору, йоду і хлору, такі як H, C, C, F, I і I. Сполуки дійсного винаходу і фармацевтично прийнятні солі зазначених сполук, що містять вищевказані ізотопи і/або інші ізотопи інших атомів, знаходяться в обсязі дійсного винаходу. Мічені ізотопом сполуки дійсного винаходу, наприклад, сполуки, у які включені радіоактивні 3 14 ізотопи, такі як Н, С, застосовуються в аналізах розподілу в лікарському засобі і/або тканині3 14 субстраті. Особливо кращими є ізотопи тритій, тобто Н, і вуглець-14, тобто С, унаслідок 11 8 легкості їх одержання і детекторності. Ізотопи С і F є особливо застосовними в РЕТ 125 (позитронній емісійній томографії) і ізотопи I є особливо застосовними в SPECT (однофотонній емісійній комп'ютерній томографії, ОЕКТ), причому усі вони застосовуються при одержанні зображення головного мозку. Крім того, заміна більш важкими ізотопами, такими як 2 дейтерій, тобто Н, може забезпечувати деякі терапевтичні переваги, що є результатом більш високої метаболічної стабільності, наприклад, збільшеного напівперіоду існування in vivo або знижених дозових потреб, і тому вони можуть бути в деяких випадках кращими. Мічені ізотопами сполуки формули (I) і наступних формул даного винаходу звичайно одержують проведенням методик, описаних нижче в схемах і/або в прикладах, заміною не міченого ізотопом реагенту на легко доступний мічений ізотопом реагент. У наступному аспекті даний винахід відноситься до способів одержання сполуки формули (I). Один шлях, який можна застосовувати для одержання сполук формули (I), коли В являє собою: ілюструється на схемі 1, у якій R1, R2, R4 і А мають значення, зазначені у формулі (I), за винятком того, що R2 не є хлором, бромом або йодом, R являє собою алкіл (наприклад, етил, трет-бутил) і hal являє собою хлор, бром або йод. Схема 1 Сполуки формули (i), що є комерційно доступними або які можна одержати декількома шляхами (наприклад, як описано в Johnson, Paul D.; et al; Bioorganic & Medicinal Chemistry Letters (2003), 13(23), 4197-4200), можна перетворити в сполуки формули (ii) обробкою йодоформом у присутності підходящого нітриту, такого як трет-бутилнітрит, у підходящому розчиннику, такому як тетрагідрофуран (ТГФ). Сполуки формули (ii) можна перетворити в сполуки формули (iii) обробкою підходящим відновлювальним агентом, таким як диборан або літійалюмінійгідрид, у розчиннику, такому як ТГФ, при підвищеній температурі, такій як 80 °C. Сполуки формули (iii) можна перетворити в захищене похідне (iv), де Р являє собою підходящу захисну групу, таку як трет-бутилоксикарбоніл (ВОС), наприклад, обробкою біс-(1,1диметилетил)дикарбонатом у присутності основи, такої як триетиламін, у підходящому 10 UA 101349 C2 5 10 15 20 25 30 35 40 розчиннику, такому як дихлорметан (DCM). Сполуки формули (iv) можна перетворити в сполуки формули (v) обробкою підходящим джерелом ціаніду, таким як ціанід цинку, у присутності каталізатора, такого як тетракистрифенілфосфінпаладій(0), у підходящому розчиннику, такому як диметилформамід (ДМФА), при підвищеній температурі, такій як 80 °C. Сполуки формули (v) можна перетворити в сполуки формули (vi) обробкою гідрохлоридом гідроксиламіну і підходящою основою, такою як бікарбонат натрію, у розчиннику, такому як метанол або етанол, при підвищеній температурі, такій як 60 °C. Сполуки формули (vi) можна перетворити в сполуки формули (ix) обробкою хлорангідридом карбонової кислоти формули (viii) у присутності основи, такої як триетиламін, у підходящому розчиннику, такому як ДМФА. Такі реакційні суміші звичайно перемішують протягом деякого періоду часу при кімнатній температурі, потім при підвищених температурах, таких як 120 °C. Хлорангідриди кислот формули (viii) є або комерційно доступними, або їх можна одержати з відповідної кислоти (vii) загальноприйнятими способами. Альтернативно сполуки формули (vi) можна перетворити в сполуки формули (ix) обробкою карбоновою кислотою формули (vii) у присутності підходящого амідного агента сполучення, такого як гідрохлорид 1-(3-диметиламінопропіл)-N’-етилкарбодііміду (ЕDAC), і 1гідроксибензотриазол (НОВТ), у підходящому розчиннику, такому як ДМФА. Такі реакції звичайно проводять при підвищеній температурі, такій як 50-80 °C. Звичайно кислоту (vii), EDAC і HOBt перемішують протягом деякого періоду часу при кімнатній температурі перед додаванням сполуки формули (vi). Сполуки формули (ix), у якій Р=ВОС, можна перетворити в сполуки формули (х) обробкою підходящою кислотою, звичайно трифтороцтовою кислотою або хлористоводневою кислотою, у підходящому розчиннику, такому як 1,4-діоксан. Сполуки формули (х) можна перетворити в сполуки формули (xii) обробкою алкілувальним агентом (xi) у присутності основи, такої як карбонат кальцію, у розчиннику, такому як ДМФА або ацетонітрил. Такі реакції можна проводити при підвищеній температурі, такій як 70 °C. Алкілувальні агенти (xi) звичайно є комерційно доступними або їх можна одержати із застосуванням стандартних способів. Сполуки формули (xii) можна перетворити в деякі сполуки формули (I), у яких В являє собою: і R3 являє собою (СН2)1-4СО2Н, обробкою основою, такою як водний гідроксид натрію, у спиртовому розчиннику, такому як етанол або метанол. Для допомоги розчиненню можна додати співрозчинник, такий як ТГФ. Реакцію гідролізу можна проводити при кімнатній температурі або при підвищеній температурі, такій як 50-80 °C. Альтернативно, це перетворення можна проводити із застосуванням твердого гідроксиду натрію в етанолі в мікрохвильовому реакторі при такій температурі, як 100 °C, або коли R = трет-бутил, із застосуванням трифтороцтової кислоти (TFA) або HCl. Сполуки формули (I), у яких R2 і R4, обоє, являють собою водень, В являє собою: R3 являє собою (СН2)1-4СО2Н, R1 і А мають значення, зазначені у формулі (I), і залишок оксадіазолу приєднаний до залишку бензазепіну в положенні 6, можна альтернативно одержати шляхом, ілюстрованим на схемі 2. Схема 2 11 UA 101349 C2 20 Комерційно доступну сполуку формули (xiii) можна перетворити в сполуку формули (xiv) обробкою гідрохлоридом гідроксиламіну, як описано на схемі 1 для перетворення (v) в (vi). Сполуки формули (xiv) можна перетворити в сполуки формули (xv) обробкою хлорангідридом карбонової кислоти формули (viii) у присутності основи, такої як триетиламін, як описано на схемі 1 для перетворення (vi) у (ix). Сполуки формули (xv) можна перетворити в сполуки формули (xvi) обробкою підходящою основою, такою як н-бутиллітій, з наступною обробкою алілбромідом у розчиннику, такому як ТГФ, при знижених температурах, таких як -78 °C. Сполуки формули (xvi) можна перетворити в сполуки формули (xvii) обробкою озоном у підходящому розчиннику, такому як DCM, при зниженій температурі, такій як -78 °C, з наступним відновленням із застосуванням підходящого відновлювального агента, такого як комплекс боран-диметилсульфід, у підходящому розчиннику, такому як ТГФ. Сполуки формули (xvii) можна перетворити в сполуки формули (ix), звичайно циклізацією в умовах Міцунобу, наприклад, із застосуванням діізопропілазодикарбоксилату (DIAD) і трифенілфосфіну в підходящому розчиннику, такому як DCM, з наступним введенням підходящої захисної групи для атома азоту бензазепіну, такої як ВОС, як описано на схемі 1, для перетворення (iii) у (iv). Сполуки формули (ixa) можна перетворити в сполуки формули (I), як описано на схемі 1 для перетворення (ix) в деякі сполуки формули (I). Один шлях, який можна застосовувати для одержання сполук формули (I), у якій В являє собою: 25 ілюструється на схемі 3, у якій R3 являє собою (СН2)1-4СО2Н, R1, R2, R4 і А мають значення, зазначені у формулі (I), за винятком того, що R 2 не є хлором, бромом або йодом, R являє собою алкіл (наприклад, метил, трет-бутил) і Hal являє собою хлор, бром або йод. Схема 3 5 10 15 Сполуки формули (xviii), що є або комерційно доступними (наприклад, від Aldrich), або їх 12 UA 101349 C2 5 10 15 20 25 30 35 40 45 одержують із застосуванням стандартних способів, можна перетворити в сполуки формули (хх) звичайно реакцією із захищеним етаноламіном (xix), де Р 1 являє собою підходящу захисну групу, таку як ВОС, в умовах Міцунобу із застосуванням, наприклад, DIAD і трифенілфосфіну в підходящому розчиннику, такому як ТГФ. Сполуки формули (хх) можна перетворити в сполуки формули (ххi) і/або (xii) обробкою кислотою, звичайно трифтороцтовою кислотою або хлористоводневою кислотою. Сполуки формули (xxi) можна також перетворити в сполуки формули (xxii) нагріванням у підходящому розчиннику, такому як толуол, при підвищених температурах, таких як 80 °C. Сполуки формули (xii) можна перетворити в сполуки формули (xxiii) обробкою підходящим відновлювальним агентом, таким як літійалюмінійгідрид, при низькій температурі, такій як нижче 15 °C, у розчиннику, такому як ТГФ, потім підвищенням температури, наприклад, до 80 °C. Сполуки формули (xxiii) можна перетворити в сполуки формули (xxiv) обробкою кислотою Льюіса, такою як трибромід бору, або сильною кислотою, такою як HBr. Сполуки формули (xxiv) можна перетворити в захищене похідне (xxv), у якого Р2 являє собою підходящу захисну групу, таку як трет-бутилоксикарбоніл (ВОС), як описано на схемі 1 для перетворення (iii) у (iv). Сполуки формули (xxv) можна перетворити в сполуки формули (xxvi) обробкою трифторметансульфоновим ангідридом у підходящому розчиннику, такому як піридин. Сполуку формули (xxvi) можна перетворити в сполуку формули (xxvii) обробкою підходящим ціанідом, таким як ціанід цинку, у присутності каталізатора, такого як тетракистрифенілфосфінпаладій(0), у підходящому розчиннику, такому як ДМФА. Сполуки формули (xxvii) можна перетворити в сполуки формули (I) із застосуванням способів, аналогічних до способів, описаних для перетворення сполук формули (v) в деякі сполуки формули (I) (схема 1). Альтернативний шлях для одержання проміжного продукту (xxvii), у якого ціаногрупа знаходиться в 9-положенні і Р2 являє собою підходящу захисну групу, таку як ВОС, і R 2 і R4 являють собою водень (представлений формулою (xxviia)), ілюструється на схемі 4. Схема 4 Сполуку формули (xxxii) можна перетворити в сполуку формули (xxxiii) обробкою параформальдегідом і сухим хлоридом магнію в підходящому розчиннику, такому як ТГФ, з нагріванням при кип'ятінні зі зворотним холодильником. Сполуки формули (xxxiii) можна перетворити в сполуки формули (xxxiv) обробкою етаноламіном у присутності відновлювального агента, такого як натрійтриацетоксиборогідрид. Сполуки формули (xxxiv) можна перетворити в захищене похідне (xxxv), у якого Р 2 являє собою підходящу захисну групу, таку як ВОС, як описано на схемі 1 для перетворення (iii) у (iv). Сполуки формули (xxxv) можна перетворити в сполуки формули (xxxvi), звичайно циклізацією в умовах Міцунобу із застосуванням, наприклад, діізопропілазодикарбоксилату (DIAD) і трифенілфосфіну в підходящому розчиннику, такому як ТГФ. Сполуки формули (xxxvi) можна перетворити в сполуки формули (xxviia) обробкою підходящим ціанідним джерелом, таким як ціанід цинку, як описано на схемі 1 для перетворення (iv) у (v). Один шлях, який можна застосовувати для одержання сполук формули (I), у якій R1, R2, R4 і А мають значення, описані у формулі (I), R3 являє собою (СН2)1-4СО2Н і В являє собою: ілюструється на схемі 5. R являє собою алкіл (наприклад, етил, трет-бутил) і Hal являє собою хлор, бром або йод. Схема 5 13 UA 101349 C2 5 10 Сполуку формули (xxxvii), у якій, наприклад, ціаногрупа знаходиться в 7-положенні (отримана, наприклад, із застосуванням способу, описаного в Micheli, F. et al. Journal of Medicinal Chemistry (2007), 50(21), 5076-5089), можна перетворити в сполуки формули (I) із застосуванням способів, аналогічних до способів, описаних для перетворень сполук формули (v) у деякі сполуки формули (I) (схема 1). Усі публікації, що включають у себе, але не обмежувані ними, патенти і заявки на патенти, цитовані в даному описі винаходу, включені в контекст як посилання, так якби кожна окрема публікація була спеціально й окремо зазначена як включена в контекст як посилання, начебто цілком викладена. Нижченаведені описи і приклади ілюструють одержання сполук винаходу. Абревіатури: г мг мл мкл ВОС2О МеСN МеОН EtOH Et2O EtOAc DCM DIAD DIPEA DME ДМФА ДМСО d6-ДМСО EDAC EDC EDCl HOBT/HOBt IPA MeOD NCS PPh3 PyBOP ТГФ TFA dba к.т. °C М Н с - Грами - Міліграми - Міллілітри - Мікролітри - біс-(1,1-диметилетил)дикарбонат - Ацетонітрил - Метанол - Етанол - діетиловий ефір - Етилацетат - Дихлорметан - Діізопропілазодикарбоксилат - Діізопропілетиламін - 1,2-біс(метилокси)етан - N, N-диметилформамід - Диметилсульфоксид - Дейтерований диметилсульфоксид - гідрохлорид N-(3-диметиламінопропіл)-N’-етилкарбодііміду - гідрохлорид N-(3-диметиламінопропіл)-N’-етилкарбодііміду - гідрохлорид N-(3-диметиламінопропіл)-N’-етилкарбодііміду - Гідроксибензотриазол - ізопропіловий спирт - дейтерований метанол - N-хлорсукцинімід - Трифенілфосфін - гексафторфосфат бензотриазол-1-ілокситрипіролідинфосфонію - Тетрагідрофуран - трифтороцтова кислота - Дибензиліденацетон - кімнатна температура - градуси Цельсія - Молярний - Протон - Синглет 15 14 UA 101349 C2 д т кв. МГц MeOD РХ/МС МС ES MH+ DMAP насич. SCХ 5 10 15 20 25 30 35 - Дублет - Триплет - Квартет - Мегагерц - дейтерований метанол - рідинна хроматографія/мас-спектрометрія - мас-спектрометрія - Електророзпилення - маса іона + Н+ - мас-направлена автоматизована препаративна рідинна хроматографія - Насичений - твердофазна катіонообмінна хроматографія Розділ загальної хімії Способи, описані нижче, приводяться для ілюстративних цілей, проміжні продукти в одержаннях або прикладах не обов'язково були отримані з конкретно описаних кількостей. Одержання 1 7-Йод-2,3,4,5-тетрагідро-1Н-2-бензазепін-1-он 7-Аміно-2,3,4,5-тетрагідро-1Н-2-бензазепін-1-он (можна одержати, як описано в публікації: Preparation of benzazepinylpyrrolidonylsulfonamides as Factor Xa inhibitors; WO2007059952) (500 мг, 2,84 ммоль) і трийодметан (2234 мг, 5,67 ммоль) розчиняли в ТГФ (100 мл). Потім по краплях протягом 20 хвилин додавали 1,1-диметилетилнітрит (0,675 мл, 5,67 ммоль), розчинений у ТГФ (20 мл), і розчин, що утворився, перемішували протягом 1 години. Суміш нагрівали при 50 °C протягом 30 хвилин. Велику частину розчинника видаляли випарюванням і сирий продукт піддавали хроматографії Biotage (EtOAc/гексан, 3:1), одержуючи при цьому зазначену в заголовку сполуку (550 мг) у вигляді блідо-жовтої твердої речовини. МС (ЕS): для + C10H10INO потрібно 287; знайдено 287,8 (М+Н) . Одержання 2 7-Йод-2,3,4,5-тетрагідро-1Н-2-бензазепін 7-Йод-2,3,4,5-тетрагідро-1H-2-бензазепін-1-он (одержання 1) (550 мг, 1,916 ммоль) розчиняли в сухому ТГФ (70 мл) і обробляли комплексом боран-ТГФ (1 М) (11,49 мл, 11,49 ммоль) і нагрівали при кип'ятінні зі зворотним холодильником протягом 4 годин. Потім реакційну суміш витримували протягом ночі. Додавали додатковий комплекс боран-ТГФ (1 М, 2 мл) і реакційну суміш нагрівали при температурі флегми протягом додаткових 2 годин і 30 хвилин. Для охолодження реакційної суміші обережно додавали метанол. Реакційну суміш перемішували до припинення виділення пухирців газу. Потім обережно порціями додавали 2 н HCl (водний) (20 мл) і після зменшення виділення пухирців газу розчин нагрівали при 75 °C протягом 30 хвилин. Аналіз РХ/МС показав один основний продукт. Реакційну суміш охолоджували і додавали воду (20 мл). Суміш промивали EtOAc (40 мл), підлужнювали 2 н NaOH (водним) і екстрагували EtOAc (50 мл). Шар EtOAc сушили над безводним MgSO 4 і упарювали, одержуючи при цьому зазначену в заголовку сполуку (400 мг) у вигляді білої твердої + речовини. МС (ЕS): для C10H12IN потрібно 273; знайдено 274 (М+Н) . Одержання 3 1,1-Диметилетил 7-йод-1,3,4,5-тетрагідро-2H-2-бензазепін-2-карбоксилат 7-Йод-2,3,4,5-тетрагідро-1H-2-бензазепін (одержання 2) (450 мг, 1,648 ммоль) розчиняли в DCM (30 мл) і обробляли ВОС2О (0,459 мл, 1,977 ммоль) з наступною обробкою триетиламіном 15 UA 101349 C2 5 10 15 20 25 30 35 40 45 (0,459 мл, 3,30 ммоль). Реакційну суміш перемішували при к.т. протягом 30 хвилин. Аналіз РХ/МС показав один основний продукт. Реакційну суміш промивали 0,5 М HCl (20 мл), насич. NaHCO3 (20 мл), сушили над безводним MgSO 4 і упарювали, одержуючи при цьому зазначену в заголовку сполуку (650 мг) у вигляді безбарвного масла. МС (ЕS): для C15H20INО2 потрібно 373; + знайдено 318 (М+Н-56) . Одержання 4 1,1-Диметилетил-7-ціано-1,3,4,5-тетрагідро-2Н-2-бензазепін-2-карбоксилат 1,1-Диметилетил-7-йод-1,3,4,5-тетрагідро-2H-2-бензазепін-2-карбоксилат (одержання 3) (650 мг, 1,742 ммоль), ціанід цинку(II) (123 мг, 1,045 ммоль) і тетракис(трифенілфосфін)паладій(0) (201 мг, 0,174 ммоль) перемішували в сухому ДМФА при 80 °C протягом 45 хвилин. До охолодженого розчину додавали EtOAc (100 мл) перед промиванням водою (2 70 мл) і насиченим розчином солі (100 мл). Шар EtOAc сушили над безводним MgSO 4 і упарювали. ТШХ (EtOAc/гексан, 1:3) показала 2 плями, одну з дуже високим RF. Сирий продукт піддавали хроматографії Biotage (EtOAc/гексан, 1:3) і нижню пляму RF виділяли. При розпарюванні одержували зазначену в заголовку сполуку (350 мг) у вигляді безбарвного масла. МС (ЕS): для + C16H20N2О2 потрібно 272; знайдено 217 (М+Н-56) . Одержання 5 1,1-Диметилетил-7-[(гідроксіаміно)(іміно)метил]-1,3,4,5-тетрагідро-2H-2-бензазепін-2карбоксилат 1,1-Диметилетил-7-ціано-1,3,4,5-тетрагідро-2H-2-бензазепін-2-карбоксилат (одержання 4) (350 мг, 1,285 ммоль), гідрохлорид гідроксиламіну (223 мг, 3,21 ммоль) і бікарбонат натрію (540 мг, 6,43 ммоль) суспендували в етанолі (15 мл) і суспензію перемішували при 55 °C протягом 5 годин. Реакційну суміш витримували протягом ночі. Аналіз РХ/МС показав один основний продукт. Неорганічні речовини видаляли фільтруванням, промиваючи 10 % розчином МеОН/DCM для розчинення будь-якого осадового продукту. Випарювання розчинника давало білу тверду речовину. Розтирання з простим ефіром давало зазначену в заголовку сполуку (320 + мг). МС (ЕS): для C16H23N3О3 потрібно 305; знайдено 306,2 (М+Н) . Одержання 6 3-Хлор-4-[(1-метилетил)окси]бензойна кислота Пропан-2-ол (2,45 мл) і РРh3 (1,18 г) розчиняли в ТГФ (30 мл), охолоджували до 0 °C, обробляли метил-3-хлор-4-гідроксибензоатом (6,00 г) з наступним додаванням по краплях DIAD (9,44 мл) і суміш перемішували при к.т. протягом ночі. Реакційну суміш упарювали й очищали на картриджах діоксиду кремнію (4 100 г), елюючи 0-40 % розчином EtOAc у пентані, одержуючи при цьому сирий продукт (7,00 г) у вигляді безбарвного масла. Його розчиняли в МеОН (30 мл) і 2 М водному NaOH (30 мл) і розчин перемішували при к.т. протягом часу із суботи до понеділка. Реакційну суміш потім упарювали і знову розчиняли в Н2О. Цей розчин промивали Et2O, підкисляли до рН=1 і екстрагували Et2O. Ці останні екстракти сушили над безводним MgSO 4, фільтрували й упарвали, одержуючи при цьому зазначену в заголовку сполуку (4,16 г) у виглядіді білої твердої речовини. Н (МеОD, 400 МГц): 1,37 (6H, д), 4,77 (1H, септет), 7,12 (1H, 35 + д), 7,90 (1H, д), 7,98 (1H, с). МС (ЕS): для C10H11 ClО3 потрібно 214; знайдено 215 (М+Н) . Одержання 7 1,1-Диметилетил-7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5тетрагідро-2H-2-бензазепін-2-карбоксилат 16 UA 101349 C2 5 10 15 3-Хлор-4-[(1-метилетил)окси]бензойна кислота (одержання 6) (105 мг, 0,491 ммоль), EDC (113 мг, 0,589 ммоль) і HOBT (90 мг, 0,589 ммоль) розчиняли в сухому ДМФА (5 мл) і розчин перемішували протягом 5 хвилин. Додавали 1,1-диметилетил-7-[гідроксіаміно(аміно)метил]1,3,4,5-тетрагідро-2Н-2-бензазепін-2-карбоксилат (одержання 5) (150 мг, 0,491 ммоль) і суміш перемішували протягом 1 години, нагрівали при 90 °C протягом 2 годин і потім витримували протягом ночі. Реакційну суміш нагрівали при 90 °C протягом додаткових 3 годин. Додавали EtOAc (50 мл) і реакційну суміш промивали насич. NaHCO 3 (водний) (50 мл) і водою (2 50 мл) перед сушінням над безводним MgSO4 і випарюванням розчинника. Отримане сире масло піддавали хроматографії Biotage (EtOAc/гексан, 1:4), одержуючи при цьому 100 мг безбарвного масла. Масло повільно починало затвердівати протягом ночі з утворенням білої восковидної твердої речовини. Розтирання із сумішшю простий ефір/гексан давало зазначену в заголовку сполуку (38 мг) у вигляді білої твердої речовини після фільтрування. З розчину повільно осаджувалася додаткова порція речовини (30 мг). Н (400 МГц, d6-ДМСО): 1,31 (9H, с), 1,36 (6H, д), 1,69 (2H, м), 3,06 (2H, м), 3,65 (2H, м), 4,44 (2H, с), 4,84-4,94 (1H, м), 7,38-7,46 (2H, м), 7,847,91 (2H, м), 8,11 (1H, дд), 8,18 (1H, д). Одержання 8 1,1-Диметилетил-[7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5тетрагідро-2H-2-бензазепін-2-іл]ацетат 20 25 30 35 40 45 7-(5-{3-Хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1H-2бензазепін (приклад 1) (60 мг, 0,143 ммоль) і карбонат цезію (140 мг, 0,428 ммоль) перемішували в сухому ДМФА (5 мл) і обробляли трет-бутилбромацетатом (0,032 мл, 0,214 ммоль). Суміш перемішували при к.т. протягом 1,5 години. Додавали EtOAc (50 мл) і простий ефір (20 мл) і суміш промивали водою (3 × 60 мл) і насиченим розчином солі (40 мл). Сушіння над безводним MgSO4 і випарювання розчинника давало прозоре, безбарвне масло (80 мг). Масло піддавали хроматографії Biotage (EtOAс/гексан, 3:1), одержуючи при цьому зазначену в 35 заголовку сполуку (65 мг) у вигляді прозорого, безбарвного масла. МС (ЕS): для C27H32 ClN3О4 + потрібно 497; знайдено 498 (М+Н) . Одержання 9 1,1-Диметилетил-7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5тетрагідро-2H-2-бензазепін-2-карбоксилат 3-Ціано-4-[(1-метилетил)окси]бензойну кислоту (можна одержати, як описано в WO2005/58848) (302 мг, 1,474 ммоль), EDC (339 мг, 1,768 ммоль) і HOBT (271 мг, 1,768 ммоль) перемішували в ДМФА (3 мл) протягом 5 хвилин. Додавали 1,1-диметилетил-7[(гідроксіаміно)(іміно)метил]-1,3,4,5-тетрагідро-2H-2-бензазепін-2-карбоксилат (одержання 5) (450 мг, 1,474 ммоль) і реакційну суміш перемішували при к.т. протягом 1 години. Після цього усе ще була присутня деяка кількість 3-ціано-4-[(1-метилетил)окси]бензойної кислоти. Додавали додаткові кількості EDC (100 мг) і 1,1-диметилетил-7-[(гідроксіаміно)(іміно)метил]-1,3,4,5тетрагідро-2H-2-бензазепін-2-карбоксилату (100 мг) і реакційну суміш перемішували протягом 1 години. Потім реакційну суміш нагрівали при 80 °C протягом 3 годин і витримували протягом ночі. Реакційну суміш потім нагрівали при 90 °C протягом 1 години. Додавали EtOAc (70 мл) і реакційну суміш промивали насич. NaHCO3 (50 мл) і водою (2 70 мл), сушили над безводним MgSO4 і упарювали. Отриману сиру речовину піддавали хроматографії Biotage (EtOAc/гексан 1:2), одержуючи при цьому після випарювання білу тверду речовину. Розтирання з простим ефіром давало зазначену в заголовку сполуку (320 мг) у вигляді білої твердої речовини. ЯМР 17 UA 101349 C2 5 10 15 20 25 30 35 40 45 (400 МГц, d6-ДМСО): 1,31 (9H, с), 1,38 (6H, д), 1,69 (2H, шир. с), 3,06 (2H, шир. с), 3,65 (2H, шир. с), 4,44 (2H, с), 4,94-5,03 (1Н, м), 7,38-7,43 (1Н, м), 7,56 (1Н, д), 7,84-7,91 (2H, м), 8,40 (1Н, дд), 8,50 (1Н, д). Одержання 10 1,1-Диметилетил-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5тетрагідро-2H-2-бензазепін-2-іл]ацетат Гідрохлорид 2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1Н-2-бензазепін-7-іл)-1,2,4оксадіазол-5-іл]бензонітрилу (приклад 3) (70 мг, 0,170 ммоль) і карбонат цезію (167 мг, 0,511 ммоль) у сухому ДМФА (5 мл) обробляли трет-бутилацетатом (0,038 мл, 0,256 ммоль) і перемішували при к.т. протягом 3 годин, одержуючи при цьому один продукт. Додавали EtOAc (40 мл) і суміш промивали водою (2 50 мл), сушили над безводним MgSO4 і упарювали, одержуючи при цьому зазначену в заголовку сполуку (85 мг) у вигляді прозорого, безбарвного + масла. МС (ЕS): для C28H32N4О4 потрібно 488; знайдено 489 (М+Н) . Одержання 11 Етил-4-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5-тетрагідро2H-2-бензазепін-2-іл]бутаноат Гідрохлорид 2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1Н-2-бензазепін-7-іл)-1,2,4оксадіазол-5-іл]бензонітрилу (приклад 3) (70 мг, 0,170 ммоль) і карбонат цезію (167 мг, 0,511 ммоль) у сухому ДМФА (5 мл) обробляли етил-4-бромбутиратом (0,037 мл, 0,256 ммоль) і перемішували при 60 °C протягом 2 годин. Додавали додаткову кількість етил-4-бромбутирату (37 мкл) і реакційну суміш нагрівали при 60 °C протягом 3 годин. Реакційну суміш витримували протягом ночі. Додавали EtOAc (50 мл) і суміш промивали водою (2 60 мл), сушили над безводним MgSO4 і упарювали, одержуючи при цьому зазначену в заголовку сполуку (90 мг) у вигляді прозорого, безбарвного масла. МС (ЕS): для C28H32N4О4 потрібно 488; знайдено 489,0 + (М+Н) . Одержання 12 1,1-Диметилетил-3-[7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5тетрагідро-2H-2-бензазепін-2-іл]пропаноат Гідрохлорид 2-[(1-метилетил)окси]-5-[3-(2,3,4,5-тетрагідро-1Н-2-бензазепін-7-іл)-1,2,4оксадіазол-5-іл]бензонітрилу (приклад 3) (70 мг, 0,170 ммоль) і карбонат цезію (167 мг, 0,511 ммоль) перемішували в сухому ДМФА (5 мл) і обробляли 1,1-диметилетил-3-бромпропаноатом (0,043 мл, 0,256 ммоль), потім перемішували при 60 °C протягом 2 годин. Додавали додаткові кількості 1,1-диметилетил-3-бромпропаноату (44 мкл) і реакційну суміш перемішували при 60 °C протягом 3 годин. Реакційну суміш витримували протягом ночі. Додавали 1,1-диметилетил-3бромпропаноат (43 мкл) і реакційну суміш перемішували при 60 °C протягом 7 годин, потім витримували протягом ночі. Додавали EtOAc (50 мл) і реакційну суміш промивали водою (2 50 мл), сушили над безводним MgSO4 і упарювали, одержуючи при цьому прозоре, безбарвне масло (100 мг). Масло повільно затвердівало. Розтирання із сумішшю простий ефір/гексан давало зазначену в заголовку сполуку (70 мг) у вигляді білої твердої речовини. МС (ЕS): для C29H34N4О4 потрібно 502; знайдено 503,0 (М+Н). Одержання 13 1,1-Диметилетил-6-{[(трифторметил)сульфоніл]окси}-1,2,4,5-тетрагідро-3H-3-бензазепін-3карбоксилат 18 UA 101349 C2 5 10 15 20 25 30 35 До перемішуваного розчину 1,1-диметилетил-6-гідрокси-1,2,4,5-тетрагідро-3H-3-бензазепін3-карбоксилату (можна одержати, як описано в WO2006/002928) (6,545 г) у сухому DCM (100 мл) в атмосфері аргону при –10 °C додавали триетиламін (4 мл). Через 10 хвилин по краплях протягом 10 хвилин додавали трифторметансульфоновий ангідрид (4,7 мл). Безбарвний розчин перетворювався в бурштиновий, потім у червоний. Реакційній суміші давали можливість досягти к.т. протягом 30 хвилин, потім перемішували при к.т. протягом 18 годин. Потім реакційну суміш виливали на насичений розчин карбонату натрію (100 мл) і шар DCM збирали, сушили й упарювали. Зазначену в заголовку сполуку (5 г) одержували хроматографією (елюювання DCM). Н (400 МГц, CDCl3): 7,22-7,12 (3H, м), 3,59-3,57 (4H, м), 3,01-2,99 (4H, м), 1,48 (9H, с); МС + (ES): для C16H20F3NО5S потрібно 395; знайдено 340 [М+Н-56] . Одержання 14 1,1-Диметилетил-6-ціано-1,2,4,5-тетрагідро-3H-3-бензазепін-3-карбоксилат 1,1-Диметилетил-6-{[(трифторметил)сульфоніл]окси}-1,2,4,5-тетрагідро-3H-3-бензазепін-3карбоксилат (одержання 13) (5 г), ціанід цинку(II) (1,5 г) і тетракис(трифенілфосфін)паладій(0) (1,5 г) нагрівали в сухому ДМФА при 150 °C протягом 18 годин. Охолоджену реакційну суміш розбавляли EtOAc (200 мл) і фільтрували. Фільтрат промивали насиченим бікарбонатом натрію (200 мл), водою (200 мл) і насиченим розчином солі (200 мл). Сиру реакційну суміш сушили звичайним способом і упарювали. Очищення хроматографією (елюювання DCM) давало зазначену в заголовку сполуку (3,4 г). Н (400 МГц, CDCl3): 7,50 (1Н, д), 7,35 (1Н, д), 7,27-7,21 (1Н, м), 3,62-3,56 (4H, м), 3,22-3,20 (2H, м), 2,97-2,94 (2H, м), 1,47 (9H, с); МС (ES): для + + C16H20N2О2 потрібно 272; знайдено 217 [М+Н-56] , 273 [M+H] . Одержання 15 1,1-Диметилетил-6-[(гідроксіаміно)(іміно)метил]-1,2,4,5-тетрагідро-3H-3-бензазепін-3карбоксилат 1,1-Диметилетил-6-ціано-1,2,4,5-тетрагідро-3H-3-бензазепін-3-карбоксилат (одержання 14) (1,15 г), гідрохлорид гідроксиламіну (1,18 г) і бікарбонат натрію (1,76 г) нагрівали при 60 °C у етанолі (100 мл) протягом 18 годин в атмосфері аргону. Охолоджену реакційну суміш упарювали досуха, розподіляли між DCM (100 мл) і водою (100 мл). Шар DCM збирали і водний шар промивали DCM (50 мл). Об'єднані шари DCM сушили й упарювали. Зазначену в заголовку сполуку (506 мг) виділяли хроматографією, елююючи 5 % метанолом у DCM. Н (400 МГц, CDCl3): 7,27 (1Н, с) 7,16-7,13 (2H, м), 5,38 (1Н, шир. с), 3,58-3,55 (4H, м), 3,05 (2H, шир. с), 2,89 (2H, шир. с), 1,46 (2H шир., с), 1,12 (9H, шир. с); МС (ЕS): для C16H23N3О3 потрібно 305; знайдено + 306 [М+Н] . Одержання 16 1,1-Диметилетил-6-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5тетрагідро-3H-3-бензазепін-3-карбоксилат 40 1,1-Диметилетил-6-[(гідроксіаміно)(іміно)метил]-1,2,4,5-тетрагідро-3H-3-бензазепін-3карбоксилат (одержання 15) (360 мг, 1,179 ммоль) розчиняли в ТГФ (50 мл) і розчин 19 UA 101349 C2 5 10 15 20 25 30 35 40 45 перемішували з гідридом натрію (60 % дисперсія в мінеральному маслі, 51,9 мг, 1,297 ммоль) в атмосфері аргону при кімнатній температурі протягом 30 хвилин. Потім додавали метил-3ціано-4-[(1-метилетил)окси]бензоат (можна одержати, як описано в WO2005058848) (388 мг, 1768 ммоль) у вигляді розчину в ТГФ (5 мл) і реакційну суміш нагрівали при температурі флегми протягом 1,5 години. Охолоджений розчин упарювали і розподіляли між DCM (100 мл) і водою (100 мл). Шар води промивали DCM (50 мл) і об'єднані шари DCM сушили (гідрофобною фритою) і упарювали. Продукт виділяли хроматографією на діоксиді кремнію (елюювання DCM), одержуючи при цьому 1,1-диметилетил-6-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4оксадіазол-3-іл)-1,2,4,5-тетрагідро-3H-3-бензазепін-3-карбоксилат (505 мг, 1,011 ммоль, вихід 86 %) у вигляді білої піни. Н (400 МГц, CDCl3): 8,41 (1Н, с), 8,33 (1Н, дд), 7,7 (1Н, дд), 7,31-7,25 (2H, м), 7,13 (1Н, д), 4,80 (1Н, септ.), 3,63-3,62 (4H, м), 3,3-3,2 (2H, м), 2,95-3,05 (2H, м), 1,47 (6H, + д), 1,43 (9H, шир. с); МС (ЕS) для C27H30N4О4 потрібно 474; знайдено 475 [М+Н] . Одержання 17 1,1-Диметилетил-6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5тетрагідро-3H-3-бензазепін-3-карбоксилат 1,1-Диметилетил-6-[(гідроксіаміно)(іміно)метил]-1,2,4,5-тетрагідро-3H-3-бензазепін-3карбоксилат (одержання 15) (170 мг, 0,557 ммоль) розчиняли в ТГФ (30 мл) і розчин перемішували з гідридом натрію (24,49 мг, 0,612 ммоль) в атмосфері аргону при кімнатній температурі протягом 30 хвилин. Потім додавали метил-3-хлор-4-[(1-метилетил)окси]бензоат (можна одержати, як описано в WO2005058848) (191 мг, 0,835 ммоль) і реакційну суміш нагрівали при температурі флегми протягом 1,5 години. Охолоджену реакційну суміш упарювали і розподіляли між DCM (100 мл) і водою (100 мл). Шар води промивали DCM (50 мл) і об'єднані шари DCM сушили (гідрофобною фритою) і упарювали. Зазначену в заголовку сполуку виділяли хроматографією на діоксиді кремнію (елюювання DCM). 1,1-Диметилетил-6-(5{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5-тетрагідро-3H-3-бензазепін-3карбоксилат (260 мг, 0,537 ммоль, вихід 96 %) виділяли у вигляді не зовсім білої піни. Н (400 МГц, CDCl3): 8,22 (1Н, с), 8,05 (1Н, д), 7,68 (1Н, д), 7,30-7,24 (2H, м), 7,06 (1Н, д), 4,72 (1Н, септ.), 3,65-3,55 (4H, м), 3,35-3,25 (2H, м), 2,95-3,05 (2H, м), 1,45 (6H, д), 1,43 (9H, с); МС (ЕS): для 35 + C26H30 ClN3О4 потрібно 483; знайдено 484 [М+Н] . Одержання 18 1,1-Диметилетил-3-[6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5тетрагідро-3H-3-бензазепін-3-іл]пропаноат У 5 мл мікрохвильову реакційну посудину додавали 6-(5-{3-хлор-4-[(1метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1Н-3-бензазепін (вільна основа прикладу 8, отримана стандартними способами, наприклад, розподілом між органічним й основним водним розчинниками, і збором органічного розчинника) (70 мг) у ДМФА (3 мл) з одержанням коричневого розчину. Потім додавали карбонат калію (101 мг) з наступним додаванням 1,1-диметилетил-3-бромпропаноату (38,1 мг, 0,182 ммоль). Реакційну суміш нагрівали при 100 °C протягом 10 хвилин. Охолоджену реакційну суміш розбавляли DCM (5 мл) і очищали SCX (промивання метанолом і елюювання сирого складного аміноефіру розчином аміаку в метанолі). Очищення за допомогою MDAP давало складний аміноефір, 1,1диметилетил-3-[6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5тетрагідро-3H-3-бензазепін-3-іл]пропаноат (25 мг, 0,046 ммоль, вихід 25,4 %), виділений у 35 + вигляді блідо-жовтого масла. МС (ЕС): для C28H34 ClN3О4 потрібно 511; знайдено 512 [М+Н] . Одержання 19 1,1-Диметилетил-[6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5тетрагідро-3H-3-бензазепін-3-іл]ацетат 20 UA 101349 C2 5 10 15 20 25 30 35 40 45 У 5 мл микрохвильову реакційну посудину додавали гідрохлорид 6-(5-{3-хлор-4-[(1метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1Н-3-бензазепіну (приклад 8) (110 мг, 0,262 ммоль). Потім додавали карбонат калію (101 мг) з наступним додаванням 1,1диметилетилбромацетату (51,0 мг, 0,262 ммоль). Реакційну суміш нагрівали при 100 °C протягом 10 хвилин. Охолоджену реакційну суміш розбавляли DCM (5 мл) і очищали SCX (промивання метанолом і елюювання сирого складного аміноефіру розчином аміаку в метанолі). 1,1-Диметилетил-[6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)1,2,4,5-тетрагідро-3H-3-бензазепін-3-іл]ацетат (120 мг, 0,241 ммоль, вихід 92 %) виділяли у 35 + вигляді блідо-жовтого масла. МС (ЕS): для C27H32 ClN3О4 потрібно 497; знайдено 498 [М+Н] . Одержання 20 3-Ціано-N-гідрокси-2-метилбензолкарбоксімідамід Суспензію 2,6-диціанотолуолу (25,0 г, 176 ммоль), гідрохлориду гідроксиламіну (73,0 г, 1,06 моль) і триетиламіну (142 г, 1,41 моль) у хлороформі (500 мл) перемішували при 50 °C протягом 7 годин, потім витримували при кімнатній температурі протягом ночі. Реакційну суміш охолоджували на льоду, обробляли 5 М HCl до рН 1 і екстрагували три рази хлороформом. Водний шар екстрагували ТГФ (х7), охолоджували на льоду, рН підвищували до 4 40 % NaOH і екстрагували ТГФ (х3). Останні екстракти ТГФ поєднували й упарювали досуха, одержуючи при цьому тьмяно-жовту тверду речовину, що складається з продукту і приблизно третини 1 еквівалента триетиламіну (11,0 г). Н ЯМР (400 МГц, d4-МеОН) (серед іншого) 7,70-7,76 (1Н, м), 7,57-7,63 (1Н, м), 7,35-7,62 (1Н, м), 2,58 (3H, с); МС (ЕС): для C9H9N3О потрібно 175; + знайдено 176 [М+Н] . Перші сім екстрактів ТГФ поєднували, упарювали досуха і розчиняли у воді. Водний розчин екстрагували двічі хлороформом, рН регулювали до рН 4 і екстрагували ТГФ (х3). Розпарювання комбінованих екстрактів ТГФ давало додаткові 4,5 г продукту. Одержання 21 3-(5-{3-Хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2-метилбензонітрил До розчину 3-ціано-N-гідрокси-2-метилбензолкарбоксімідаміду (одержання 20) (1,70 г, 9,70 ммоль) у ТГФ (100 мл) додавали гідрид натрію (0,427 г, 10,67 ммоль) в атмосфері аргону при к.т. і суспензію перемішували протягом 30 хв. Потім додавали метил-3-хлор-4-[(1метилетил)окси]бензоат (можна одержати, як описано в WO2005058848) (3,33 г, 14,56 ммоль) і реакційну суміш нагрівали при кип'ятінні зі зворотним холодильником протягом 45 хвилин, потім охолоджували до к.т. і перемішували протягом 3 днів. Окремо до суспензії 3-ціано-N-гідрокси-2-метилбензолкарбоксімідаміду (одержання 20) (10,48 г, 59,8 ммоль) у ТГФ (250 мл) в атмосфері аргону при к.т. порціями додавали гідрид натрію (2,87 г, 71,8 ммоль) і суспензію, що утворилася, перемішували при к.т. протягом 30 хвилин. Додавали метил-3-хлор-4[(1-метилетил)окси]бензоат (19,9 г, 87 ммоль) і реакційну суміш нагрівали при кип'ятінні зі зворотним холодильником протягом 4 годин, потім перемішували при к.т. протягом 16 годин. Дві реакційні суміші поєднували. Додавали воду (200 мл), потім суміш екстрагували DCM (2 × 250 мл). Органічні шари поєднували, промивали насиченим розчином солі (100 мл) і концентрували у вакуумі, одержуючи при цьому сиру білу тверду речовину (28,1 г). Тверду речовину знову розчиняли в DCM (200 мл), ТГФ (150 мл) і EtOH (50 мл) і пропускали через невисокий шар діоксиду кремнію (висота 1 см). Елюювання DCM з наступним концентруванням у вакуумі давало блідо-жовту тверду речовину, 3-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4оксадіазол-3-іл)-2-метилбензонітрил (18,10 г, 51,2 ммоль, вихід 80 %). Елюювання діоксиду кремнію сумішшю DCM-EtOH (2:1) з наступним концентруванням давало блідо-жовту тверду речовину, 3-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2-метилбензонітрил 21 UA 101349 C2 1 5 10 15 20 25 30 35 40 45 50 (2,81 г, 6,35 ммоль, вихід 10 %). Обидві порції були аналітично ідентичними. Н ЯМР (400 МГц, CDCl3) 8,27 (1Н, д), 8,22 (1Н, д), 8,05 (1Н, дд), 7,77 (1Н, д), 7,45 (1Н, т), 7,07 (1Н, д), 4,73 (1Н, 35 + септ.), 2,90 (3H, с), 1,47 (6H, д); MC (ЕS) для C19H16 ClN3О2 потрібно 353; знайдено 354 [М+Н] . Одержання 22 2-(3-Бутен-1-іл)-3-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)бензонітрил До розчину діізопропіламіну (15,15 мл, 106 ммоль) у сухому ТГФ (650 мл) при –78 °C в n атмосфері Ar по стінці колби додавали BuLi (44,3 мл, 70,9 ммоль) і розчин, що утворився, -1 перемішували протягом 1 години. В атмосфері Ar при швидкості 10 мл/хв по краплях додавали розчин 3-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2метилбензонітрилу (одержання 21) (12,54 г, 35,4 ммоль) у сухому ТГФ (100 мл) в атмосфері Ar і темно-синій розчин, що утворився, перемішували при –78 °C протягом 45 хв. При швидкості 3 -1 мл/хв по краплях додавали алілбромід (6,13 мл, 70,9 ммоль) і темно-червоний розчин, що утворився, перемішували протягом 30 хв при –78 °C. Додавали 1 М HCl (водний) (375 мл), суміші давали можливість нагрітися до к.т., потім шари розділяли. Водний шар екстрагували EtOAc (2 125 мл), потім об'єднані органічні шари промивали насиченим розчином солі (250 мл), сушили (MgSO4), фільтрували і концентрували у вакуумі, одержуючи при цьому сире червоне масло (12,8 г). Масло знову розчиняли в DCM (20 мл) і додавали в попередньо змочену (ізогексаном) колонку діоксиду кремнію (5 см 5 см). Елюювання сумішшю EtOAc-ізогексан (1:3) і концентрування необхідних фракцій давало блідо-жовтогарячу тверду речовину, 2-(3-бутен-1іл)-3-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)бензонітрил (9,50 г, 20,98 1 ммоль, вихід 59,2 %). Н ЯМР (400 МГц, CDCl3) 8,26 (1Н, д), 8,24 (1Н, д), 8,05 (1Н, дд), 7,79 (1Н, д), 7,46 (1Н, т), 7,07 (1Н, д), 5,94 (1Н, ддт), 5,07 (1Н, дкв.), 5,01 (1Н, дд), 4,73 (1Н, септ.), 35 3,40 (2H, т), 2,47 (2H, кв.д), 1,45 (6H, д); MC (ЕS): для C22H20 ClN3О2 потрібно 393; знайдено 394 + [М+Н] . Одержання 23 3-[2-(Амінометил)-6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)феніл]-1пропанол Через розчин 2-(3-бутен-1-іл)-3-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3іл)бензонітрил (одержання 22) (8,26 г, 20,97 ммоль) у DCM (125 мл) в атмосфері Ar при –78 °C -1 барботували Ar, потім О2 (4 хв. кожного). Озонізатор (модель 502; 75 л/год. ; 0,3 А) включали і жовтогарячий розчин озонували доти, поки він не зафарбовувався в темний зелено-сірий колір (3 години). Озонізатор виключали і через розчин барботували О 2, потім Ar (10 хв. кожний). Розчину давали можливість нагрітися до к.т. в атмосфері Ar, потім його концентрували у вакуумі, одержуючи при цьому непрозоре жовте масло. Його знову розчиняли в сухому ТГФ (200 мл), додавали ВН3.DMS (9,96 мл, 105 ммоль) (увага: відбувається виділення газу) і розчин перемішували при к.т. протягом 18 годин і потім при 40 °C протягом 3 годин. Реакційну суміш охолоджували до 0 °C, потім обережно додавали 0,1 М водний HCl (150 мл) (увага: відбувається виділення газу), потім залишали для перемішування при к.т. протягом 18 годин. Розчин пропускали безпосередньо через колонку SCX-2 (50 г), промиваючи МеОН. Продукт елюювали 0,5 М NH3 у МеОН; концентрування у вакуумі давало жовтогарячу піну, 3-[2(амінометил)-6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)феніл]-1-пропанол 1 (2,73 г, 3,95 ммоль, вихід 18,9 %). Н ЯМР (400 МГц, CDCl3) (серед іншого) 8,23 (1Н, д), 8,05 (1Н, дд), 7,86 (1Н, д), 7,46 (1Н, д), 7,34 (1Н, т), 7,06 (1Н, д), 4,72 (1Н, септ.), 4,03 (2H, с), 3,47 (2H, 35 т), 3,27 (2H, т), 1,78 (2H, квін.), 1,45 (6H, д); MC (ЕS): для C21H24 ClN3О3 потрібно 401; знайдено + 402 [М+Н] . Одержання 24 1,1-Диметилетил-[6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5тетрагідро-2H-2-бензазепін-2-іл]ацетат 22 UA 101349 C2 5 10 15 20 25 30 35 40 45 50 До розчину 3-[2-(амінометил)-6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3іл)феніл]-1-пропанолу (одержання 23) (424 мг, 1,055 ммоль) і трифенілфосфіну (1384 мг, 5,28 ммоль) у сухому DCM (150 мл) при к.т. в атмосфері Ar протягом 2 хв по краплями додавали DIAD (0,974 мл, 5,01 ммоль) і блідо-жовтий розчин, що утворився, перемішували при к.т. протягом 2 годин. Розчин концентрували до 10 мл, потім пропускали через картридж SCX-2 (10 г), промивали МеОН. Продукт елюювали 0,5 М розчином NH 3 у МеОН; концентрування у вакуумі давало блідо-жовтогаряче масло (>900 мг). Очищення SCX-2 повторювали для видалення оксиду трифенілфосфіну, що залишився, одержуючи при цьому блідо-жовте масло (314 мг). Масло знову розчиняли в DCM (40 мл), послідовно додавали ВОС2О (0,367 мл, 1,583 ммоль) і DMAP (6,44 мг, 0,053 ммоль) і суміш перемішували в атмосфері Ar протягом 2 годин. Додавали насичений водний NH4Cl (20 мл), потім водний шар екстрагували DCM (25 мл). Органічні шари поєднували, пропускали через гідрофобну фриту і концентрували у вакуумі, одержуючи при цьому сире блідо-коричневе масло (496 мг). Флеш-хроматографія (діоксид кремнію; Flash 25 М; лінійний градієнт (0,1-1 %) МеОН у DCM) давала жовте масло, 1,1-диметилетил-6-(5-{3-хлор-4[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,3,4,5-тетрагідро-2H-2-бензазепін-2карбоксилат (130 мг). Цю речовину знову розчиняли в 4 М HCl у діоксані (5 мл, 20,00 ммоль) і перемішували при к.т. протягом 3 годин. Розчин додавали в колонку SCX-3 (10 г) і колонку промивали МеОН. Продукт елюювали 0,5 М NH3 у МеОН; концентрування у вакуумі давало тьмяно-білу тверду речовину (102 мг). Продукт знову розчиняли в сухому ДМФА (3 мл); додавали карбонат калію (74,1 мг, 0,536 ммоль) і трет-бутилбромацетат (0,042 мл, 0,281 ммоль), потім суспензію опромінювали до 100 °C протягом 10 хв. у мікрохвильовій печі. Суміш розбавляли DCM (7 мл), потім додавали в картридж SCX-3 (10 г) і промивали МеОН. Продукт елюювали 0,5 М NH3 у МеОН; концентрування у вакуумі давало жовтогаряче масло (57 мг). Мас-направлене автоочищення зі зверненою фазою (MDAP) давало продукт у розчині водаMeCN. Необхідні фракції додавали в картридж SCX-3 (1 г) і промивали МеОН. Продукт елюювали 0,5 М NH3 у МеОН; концентрування у вакуумі давало прозору плівку (21,4 мг) суміші з відношенням 5:2 1,1-диметилетил-[6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3іл)-1,3,4,5-тетрагідро-2H-2-бензазепін-2-іл]ацетату і [6-(5-{3-хлор-4-[(1-метилетил)окси]феніл}1,2,4-оксадіазол-3-іл)-1,3,4,5-тетрагідро-2H-2-бензазепін-2-іл]оцтової кислоти. Основний 1 компонент: Н ЯМР (400 МГц, CDCl3) 8,22 (1Н, д), 8,05 (1Н, дд), 7,68 (1Н, д), 7,26 (1Н, д), 7,25 (1Н, т), 7,06 (1Н, д), 4,72 (1Н, септ.), 4,14 (2H, с), 3,28 (2H, шир. с), 3,23 (2H, т), 3,16 (2H, с), 1,77 35 (2H, м), 1,47 (9H, с), 1,43 (6H, д); MС (ЕS): для C27H32 ClN3О4 потрібно 497; знайдено 498 + [М+Н] . Одержання 25 8-(Метилокси)-3,4-дигідро-1,4-бензоксазепін-5(2H)-он DIAD (32,1 мл, 165 ммоль) додавали по краплях протягом 15 хв до перемішуваного, охолоджуваного льодом розчину метил-2-гідрокси-4-(метилокси)бензоату (24,18 г, 150 ммоль), 1,1-диметилетил-(2-гідроксіетил)карбамату (27,3 г, 150 ммоль) і трифенілфосфіну (43,3 г, 165 ммоль) у ТГФ (450 мл), потім суміш перемішували і давали їй можливість нагрітися до кімнатної температури протягом 2 годин. Реакційну суміш упарювали, одержуючи при цьому 129,9 г в'язкого жовтого масла. Додавали трифтороцтову кислоту (60 мл, 779 ммоль) у дихлорметані (DCM) (350 мл) і реакційну суміш витримували при кімнатній температурі протягом 65 годин, потім упарювали досуха. Утворений залишок розчиняли в 500 мл простого ефіру і розчин екстрагували 2 М HCl (200 мл і 2 75 мл). Об'єднані кислотні екстракти промивали 200 мл простого ефіру, потім додавали 500 мг льоду разом з 250 мл EtOAc і суміш підлужували 50 % гідроксидом натрію при енергійному перемішуванні. Органічний шар відокремлювали і водний шар додатково екстрагували 4 × 75 мл EtOAc і об'єднані органічні шари сушили (сульфатом магнію) і упарювали, одержуючи при цьому 21,1 г жовтого масла. Олію розчиняли в толуолі (350 мл) і розчин перемішували і кип'ятили зі зворотним холодильником протягом 24 годин, потім 23 UA 101349 C2 5 10 15 20 25 30 35 40 упарювали й очищали флеш-хроматографією з елююванням EtOAc, одержуючи при цьому зазначену в заголовку сполуку (8,61 г) у вигляді білої твердої речовини. MС (ЕS): для C10H11NО3 + потрібно 193; знайдено 194 [М+Н] . Одержання 26 8-Гідрокси-3,4-дигідро-1,4-бензоксазепін-5(2H)-он Суміш 8-(метилокси)-3,4-дигідро-1,4-бензоксазепін-5(2H)-ону (одержання 25) (7,98 г, 41,3 ммоль) і бромистоводневої кислоти (100 мл, 1842 ммоль) перемішували і нагрівали при 110 °C протягом 7 годин. Потім реакційну суміш упарювали і двічі піддавали азеотропній перегонці з 150 мл етанолу, одержуючи при цьому зазначену в заголовку сполуку (8,66 г) у вигляді яснокоричневої твердої речовини, яку застосовували без очищення. MС (ЕS): для C 9H9NО3 потрібно + 179; знайдено 180 [М+Н] . Одержання 27 8-[(Фенілметил)окси]-3,4-дигідро-1,4-бензоксазепін-5(2H)-он Суміш 8-гідрокси-3,4-дигідро-1,4-бензоксазепін-5(2H)-ону (одержання 26) (8,66 г, 48,3 ммоль), бензилброміду (6,32 мл, 53,2 ммоль) і карбонату калію (20,04 г, 145 ммоль) у ДМФА (80 мл) перемішували і нагрівали при 60 °C протягом 2 годин. Охолоджену реакційну суміш розбавляли сумішшю EtOAc/вода (300 мл кожного) і водний шар екстрагували EtOAc (2 75 мл). Об'єднані органічні шари промивали 3 × 100 мл води, сушили (сульфатом магнію), упарювали, розтирали з простим ефіром і фільтрували, одержуючи при цьому зазначену в заголовку сполуку (8,39 г) у вигляді білої твердої речовини. MС (ЕS): для C 16H15NО3 потрібно + 269; знайдено 270 [М+Н] . Одержання 28 8-[(Фенілметил)окси]-2,3,4,5-тетрагідро-1,4-бензоксазепін 1 M Літійалюмінійгідрид (62,4 мл, 62,4 ммоль) у ТГФ додавали в атмосфері аргону до перемішуваного розчину 8-(фенілметил)окси]-3,4-дигідро-1,4-бензоксазепін-5(2H)-ону (одержання 27) (8,39 г, 31,2 ммоль) у ТГФ (150 мл) при охолодженні крижаною банею протягом 5 хвилин. Утворений розчин нагрівали з перемішуванням при 60 °C протягом 3 годин. Реакційну суміш охолоджували й обережно гасили повільним додаванням при охолодженні льодом 150 мл 2 М гідроксиду натрію з наступним додаванням 150 мл EtOAc. Органічний шар відокремлювали, і водний шар екстрагували 100 мл EtOAc. Об'єднані органічні екстракти сушили (сульфат магнію) і упарювали, одержуючи при цьому зазначену в заголовку сполуку (7,53 г) у вигляді + легкого безбарвного масла. MС (ЕS): для C16H17NО2 потрібно 255; знайдено 256 [М+Н] . Одержання 29 1,1-Диметилетил-8-[(фенілметил)окси]-2,3-дигідро-1,4-бензоксазепін-4(5H)-карбоксилат BOC2О (7,52 мл, 32,4 ммоль) додавали до розчину 8-[(фенілметил)окси]-2,3,4,5-тетрагідро1,4-бензоксазепіну (одержання 28) (7,52 г, 29,5 ммоль) у DCM (100 мл) і суміш витримували при кімнатній температурі протягом 30 хвилин. Потім реакційну суміш упарювали досуха й очищали флеш-хроматографією з елююванням 5 % EtOAc у ізогексані і заміною на 15 % EtOAc у ізогексані для елюювання продукту. Розтирання з ізогексаном і фільтрування давало 7,37 г білої + твердої речовини. MС (ЕS): для C21H25NО4 потрібно 355; знайдено 300 [М+Н-56] . 24 UA 101349 C2 Одержання 30 1,1-Диметилетил-8-гідрокси-2,3-дигідро-1,4-бензоксазепін-4(5H)-карбоксилат 5 10 15 20 25 30 35 1,1-Диметилетил-8-[(фенілметил)окси]-2,3-дигідро-1,4-бензоксазепін-4(5H)-карбоксилат (одержання 29) (7,35 г, 20,68 ммоль) у суміші ТГФ (40 мл) і EtOH (40 мл) гідрували з 10 % паладієм на вугіллі (0,735 г, 6,91 ммоль) протягом 18 годин, потім фільтрували й упарювали, одержуючи при цьому зазначену в заголовку сполуку (5,49 г) у вигляді білої твердої речовини. + MС (ЕS): для C14H19NО4 потрібно 265; знайдено 166 [М+Н-100] . Одержання 31 1,1-Диметилетил-8-{[(трифторметил)сульфоніл]окси}-2,3-дигідро-1,4-бензоксазепін-4(5H)карбоксилат Трифторметансульфоновий ангідрид (0,253 мл, 1,498 ммоль) додавали до охолодженого льодом розчину 1,1-диметилетил-8-гідрокси-2,3-дигідро-1,4-бензоксазепін-4(5H)-карбоксилату (одержання 30) (0,265 г, 0,999 ммоль) у піридині (4 мл) і суміш перемішували протягом однієї години. Реакційну суміш упарювали, розчиняли в 40 мл EtOAc і промивали 20 мл 2 М HCl і 20 мл насиченого бікарбонату натрію, потім сушили (сульфатом магнію) і упарювали, одержуючи при цьому зазначену в заголовку сполуку (399 мг) у вигляді жовтої смоли. MС (ЕS): для + C15H18F3NО6S потрібно 397; знайдено 298 [М+Н-100] . Одержання 32 1,1-Диметилетил-8-ціано-2,3-дигідро-1,4-бензоксазепін-4(5H)-карбоксилат Суміш 1,1-диметилетил-8-{[(трифторметил)сульфоніл]окси}-2,3-дигідро-1,4-бензоксазепін4(5H)-карбоксилату (одержання 31) (0,397 г, 0,999 ммоль), ціаніду цинку (0,176 г, 1,499 ммоль) і тетракис(трифенілфосфін)паладію(0) (0,115 г, 0,100 ммоль) у ДМФА (4 мл) перемішували і нагрівали при 80 °C протягом 2 годин, потім охолоджували і розбавляли сумішшю EtOAc/вода (40 мл кожного) і органічний шар промивали 3 × 20 мл води, сушили (сульфатом магнію), упарювали й очищали флеш-хроматографією з елююванням сумішшю 1:4 EtOAc/ізогексан, одержуючи при цьому зазначену в заголовку сполуку (198 мг) у вигляді смоли, що повільно + кристалізувалася. MС (ЕS): для C15H18F3N2О3 потрібно 274; знайдено 175 [М+Н-100] . Одержання 33 1,1-Диметилетил-8-[(гідроксіаміно)(іміно)метил]-2,3-дигідро-1,4-бензоксазепін-4(5H)карбоксилат Суміш 1,1-диметилетил-8-ціано-2,3-дигідро-1,4-бензоксазепін-4(5H)-карбоксилату (одержання 32) (0,195 г, 0,711 ммоль), гідрохлориду гідроксиламіну (0,099 г, 1,422 ммоль) і бікарбонату натрію (0,299 г, 3,55 ммоль) у етанолі (5 мл) перемішували і нагрівали при 60 °C протягом 3 годин. Реакційну суміш охолоджували, упарювали і розчиняли в суміші EtOAc/вода (40 мл кожного, необхідно деяке нагрівання) і органічний шар сушили (сульфатом магнію) і 25 UA 101349 C2 5 10 15 20 25 30 35 40 45 упарювали, одержуючи при цьому зазначену в заголовку сполуку (210 мг) у вигляді білої твердої + речовини. MС (ЕS): для C15H21N3О4 потрібно 307; знайдено 308 [М+Н] . Одержання 34 1,1-Диметилетил-8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро1,4-бензоксазепін-4(5H)-карбоксилат Суміш 1,1-диметилетил-8-[(гідроксіаміно)(іміно)метил]-2,3-дигідро-1,4-бензоксазепін-4(5H)карбоксилату (одержання 33) (0,195 г, 0,634 ммоль), 3-хлор-4-[(1-метилетил)окси]бензойної кислоти (одержання 6) (0,136 г, 0,634 ммоль), EDC (0,146 г, 0,761 ммоль) і HOBT (0,107 г, 0,698 ммоль) і ДМФА (4 мл) перемішували при кімнатній температурі протягом 20 хвилин, потім нагрівали при 100 °C протягом 17 годин. Охолоджену реакційну суміш розбавляли сумішшю EtOAc/вода (4 мл кожного) і органічний шар збирали, сушили (сульфатом магнію), упарювали й очищали хроматографією Biotage у суміші 1:4 EtOAc/ізогексан, одержуючи при цьому зазначену 35 в заголовку сполуку (172 мг) у вигляді білої твердої речовини. MС (ЕS): для C25H28 ClN3О5 + 37 + потрібно 485; знайдено 486 [М+Н] ; для C25H28 СlN3О5 потрібно 487; знайдено 488 [М+Н] . Одержання 35 Етил-3-[8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]пропаноат Суміш 8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4бензоксазепіну (приклад 13) (0,036 г, 0,199 ммоль), етил-3-бромпропаноату (0,084 г, 0,199 ммоль) і DIPEA (0,097 мл, 0,557 ммоль) перемішували і нагрівали при 80 °C протягом 4 годин, коли додавали додаткову порцію етил-3-бромпропаноату (0,084 г, 0,199 ммоль) і DIPEA (0,097 мл, 0,557 ммоль), і суміш нагрівали протягом ночі, коли додавали додаткову порцію етил-3бромпропаноату (0,084 г, 0,199 ммоль) і DIPEA (0,097 мл, 0,557 ммоль), і суміш нагрівали протягом ще 3 годин, коли прореагували усі вихідні сполуки. Охолоджену реакційну суміш розбавляли сумішшю EtOAc/вода (30 мл кожного) і органічний шар сушили (сульфатом магнію), упарювали й очищали флеш-хроматографією з елююванням сумішшю 1:1 EtOAc/ізогексан, одержуючи при цьому зазначену в заголовку сполуку у вигляді безбарвної смоли. MС (ЕS): для 35 + C25H28 ClN3О5 потрібно 485; знайдено 486 [М+Н] . Одержання 36 Етил-4-[8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3-дигідро-1,4бензоксазепін-4(5H)-іл]бутаноат Суміш 8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4бензоксазепіну (приклад 13) (0,127 г, 0,3 ммоль), DIPEA (0,052 мл, 0,300 ммоль) і етил-4бромбутаноату (0,059 г, 0,300 ммоль) в ацетонітрилі (5 мл) перемішували і нагрівали при 70 °C протягом 15 годин. Охолоджену реакційну суміш розбавляли і розчиняли в суміші EtOAc/вода (30 мл кожного) і органічний шар сушили (сульфатом магнію), упарювали й очищали флешхроматографією з елююванням сумішшю 1:1 EtOAc/ізогексан, одержуючи при цьому зазначену 35 в заголовку сполуку (106 мг) у вигляді безбарвної смоли. MС (ЕS): для C26H30 ClN3О5 потрібно + 499; знайдено 500 [М+Н] . Одержання 37 1,1-Диметилетил-[8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3дигідро-1,4-бензоксазепін-4(5H)-іл]ацетат 26 UA 101349 C2 5 10 15 20 25 30 35 40 Суміш 8-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-2,3,4,5-тетрагідро-1,4бензоксазепіну (приклад 13) (0,127 г, 0,301 ммоль), 1,1-диметилетилбромацетату (0,117 г, 0,601 ммоль) і DIPEA (0,210 мл, 1,203 ммоль) в ацетонітрилі (5 мл) перемішували і нагрівали при 70 °C протягом однієї години. Охолоджену реакційну суміш розбавляли сумішшю EtOAc/вода (30 мл кожного) і органічний шар сушили (сульфатом магнію), упарювали й очищали флешхроматографією з елююванням сумішшю 1:2 EtOAc/ізогексан, одержуючи при цьому зазначену 35 в заголовку сполуку (130 мг) у вигляді безбарвної смоли. MС (ЕS): для C26H30 ClN3О5 потрібно + 499; знайдено 500 [М+Н] . Одержання 38 1-Метилетил-4-[(1-метилетил)окси]-3-(трифторметил)бензоат Суміш 4-гідрокси-3-(трифторметил)бензойної кислоти (2,5 г, 12,1 ммоль), 2-йодпропану (2,42 мл, 24,3 ммоль) і карбонату калію (3,35 г, 24,3 ммоль) у N, N'-диметилформаміді (200 мл) нагрівали при 70 °C протягом 4 годин. Реакційну суміш частково концентрували у вакуумі і залишок розподіляли між EtOAc (150 мл) і водою (150 мл), що містить деяку кількість водного гідроксиду натрію. Водну фазу екстрагували додатковим EtOAc (2 100 мл) і об'єднані органічні фракції сушили (гідрофобна фрита як розподільник фаз) і концентрували у вакуумі, одержуючи при цьому сиру зазначену в заголовку сполуку у вигляді жовтого масла (3,6 г, 12,1 ммоль). Н (d6-ДМСО, 400 МГц): 8,16 (1Н, дд), 8,08 (1Н, д), 7,43 (1Н, д), 5,13 (1Н, септет), 4,91 (1Н, септет), 1,32 (12H, д). Одержання 39 4-[(1-Метилетил)окси]-3-(трифторметил)бензойна кислота До суміші 1-метилетил-4-[(1-метилетил)окси]-3-(трифторметил)бензоату (одержання 38) (3,63 г, 12,5 ммоль) у етанолі (100 мл) додавали водний гідроксид натрію (12,5 М, 10,0 мл, 125 ммоль) і реакційну суміш нагрівали для кип'ятіння зі зворотним холодильником протягом 3 годин. Суміш концентрували у вакуумі і залишок розподіляли між EtOAc (100 мл) і водою (100 мл) і підкисляли водною хлористоводневою кислотою. Водний шар екстрагували додатково EtOAc (100 мл) і об'єднані органічні шари сушили і концентрували у вакуумі, одержуючи при цьому зазначену в заголовку сполуку у вигляді жовтої твердої речовини (2,68 г, 10,8 ммоль). MС + (ЕS-): для C11H11F3О3 потрібно 248; знайдено 247 [М-Н] . Одержання 40 2-(Трифторметил)-4-біфенілкарбонова кислота Реакційну суміш ділили на 4 частини із застосуванням чверті зазначеної кількості кожного із зазначених реагентів: 4-бром-3-(трифторметил)бензонітрилу (4 г, 16,00 ммоль), фенілборонової кислоти (3,90 г, 32,0 ммоль) і карбонату калію (6,63 г, 48,0 ммоль) у ДМФА (64 мл) і до кожної суміші додавали тетракистрифенілфосфінпаладій(0) (1,849 г, 1,600 ммоль). Кожну реакційну суміш нагрівали в мікрохвильовій печі при 150 °C протягом 30 хвилин. Об'єднані реакційні суміші фільтрували через целіт, промивали EtOAc і розчинник видаляли у вакуумі. Залишок розподіляли між EtOAc (100 мл) і водою (100 мл) і органічну фазу промивали розчином бікарбонату натрію (100 мл). Органічну фазу сушили (MgSO4), фільтрували і розчинник видаляли у вакуумі. Коричневе масло розтирали з DCM і фільтрували, одержуючи при цьому 27 UA 101349 C2 5 10 15 20 25 30 35 40 45 блідо-жовту тверду речовину, 2-(трифторметил)-4-біфенілкарбоксамід (2,47 г), яку застосовували без додаткового очищення. До 2-(трифторметил)-4-біфенілкарбоксаміду (2 г, 7,54 ммоль) у етанолі (80 мл) додавали гідроксид калію (4,23 г, 75 ммоль) і воду і суміш нагрівали до 90 °C протягом 18 годин. Реакційну суміш концентрували у вакуумі і залишок розподіляли між DCM (100 мл) і 2 М HCl (100 мл). Органічну фазу відокремлювали і сушили (гідрофобна фрита як розподільник фаз) і розчинник видаляли у вакуумі, одержуючи при цьому сирий продукт. Хроматографічне очищення із застосуванням Biotage Horizon, картриджа зі зверненою фазою, і елююванням 5-100 % MeCN у воді давало зазначену в заголовку сполуку у вигляді не зовсім білої твердої речовини (960 мг). РХМС (ES-): для C14H9F3О2 потрібно 266; + знайдено 265 [М-Н ]. Одержання 41 1,1-Диметилетил-7-[(гідроксіаміно)(іміно)метил]-1,2,4,5-тетрагідро-3H-3-бензазепін-3карбоксилат Суспензію 1,1-диметилетил-7-ціано-1,2,4,5-тетрагідро-3H-3-бензазепін-3-карбоксилату (можна одержати, як описано в WO2002040471) (5 г, 18,36 ммоль), гідрохлориду гідроксиламіну (2,55 г, 36,7 ммоль) і бікарбонату натрію (7,71 г, 92 ммоль) у етанолі (250 мл) нагрівали при 50 °C протягом ночі. До реакційної суміші додавали додатковий гідрохлорид гідроксиламіну (0,638 г, 9,18 ммоль) і нагрівання при 50 °C продовжували протягом 5 годин. Реакційній суміші дозволяли остудитися і тверду речовину відокремлювали фільтруванням, розчин концентрували у вакуумі, одержуючи при цьому зазначену в заголовку сполуку у вигляді білої твердої речовини (5,77 г, 17,01 ммоль, вихід 93 %). Н (d6-ДМСО, 400 МГц): 9,56 (1Н, с), 7,527,37 (2H, м), 7,14 (1Н, д), 5,77 (2H, шир. с), 3,50-3,32 (4H, м), 2,91-2,80 (4H, м), 1,41 (9H, с). MС + (ЕS): для C16H23N3О3 потрібно 305; знайдено 306 [М+Н] . Одержання 42 1,1-Диметилетил-7-(5-{3-хлор-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5тетрагідро-3H-3-бензазепін-3-карбоксилат До розчину 3-хлор-4-[(1-метилетил)окси]бензойної кислоти (одержання 6) (1,406 г, 6,55 ммоль) у ДМФА додавали HOBT (1,103 г, 7,20 ммоль) і EDC (1,381 г, 7,20 ммоль), утворений розчин перемішували в атмосфері аргону протягом 10 хв при кімнатній температурі. Потім до реакційної суміші додавали 1,1-диметилетил-7-[(гідроксіаміно)(іміно)метил]-1,2,4,5-тетрагідро3H-3-бензазепін-3-карбоксилат (одержання 41) (2 г, 6,55 ммоль) і розчин нагрівали при 80 °C протягом ночі. Розчинник видаляли у вакуумі, і залишок розчиняли в метанолі й очищали Biotage Horizon, картриджем зі зверненою фазою при елююванні 5-100 % ацетонітрилу у воді. Фракції, що містять продукт (останні 5) концентрували у вакуумі, одержуючи при цьому зазначену в заголовку сполуку у вигляді жовтого масла (950 мг, 1,87 ммоль, вихід 29 %). Н (d6ДМСО, 400 МГц): 8,19 (1Н, д), 8,11 (1Н, дд), 7,83-7,89 (2H, м), 7,45 (1Н, д), 7,37 (1Н, д), 4,89 (1Н, 35 септ.), 3,50 (4H, шир. с), 2,96 (4H, шир. с), 1,41 (9H, с), 1,36 (6H, д). MС (ЕS): для C26H30 ClN3О4 + потрібно 483; знайдено 384 [М+Н-100] . Одержання 43 1,1-Диметилетил-7-(5-{3-ціано-4-[(1-метилетил)окси]феніл}-1,2,4-оксадіазол-3-іл)-1,2,4,5тетрагідро-3H-3-бензазепін-3-карбоксилат 3-Ціано-4-[(1-метилетил)окси]бензойну кислоту (можна одержати, як описано в WO2005/58848) (687 мг, 3,63 ммоль), HOBT (539 мг, 3,99 ммоль) і EDC (762 мг, 3,99 ммоль) перемішували в ДМФА (30 мл) в атмосфері аргону протягом 20 хвилин. Додавали 1,1диметилетил-7-[(гідроксіаміно)(іміно)метил]-1,2,4,5-тетрагідро-3H-3-бензазепін-3-карбоксилат 28
ДивитисяДодаткова інформація
Назва патенту англійськоюNormal;heading 1;heading 2;heading 3;oxadiazole derivatives active on sphingosine-1-phosphate (s1p)
Автори англійськоюDemont, Emmanuel, Hubert, Heer, Jag, Paul, Heightman, Thomas, Daniel, Hurst, David, Nigel, Johnson Christopher Norbert, Skidmore, John, Wall, Ian, David, Witherington, Jason
Назва патенту російськоюПроизводные оксадиазола, активные в отношении сфингозин-1-фосфата (s1p)
Автори російськоюДемон Эмманюэль Юбер, Хир Джаг Пол, Хейгтмен Томас Дениэл, Херст Девид Найджел, Джонсон Кристофер Норберт, Скидмор Джон, Уолл Йан Девид, Уитерингтон Джейсон
МПК / Мітки
МПК: C07D 271/06, C07D 413/04, A61K 31/55, C07D 267/00, C07D 223/00, A61P 17/00, C07D 413/14, A61P 37/00
Мітки: похідні, оксадіазолу, відношенні, сфінгозин-1-фосфату, s1p, активні
Код посилання
<a href="https://ua.patents.su/72-101349-pokhidni-oksadiazolu-aktivni-u-vidnoshenni-sfingozin-1-fosfatu-s1p.html" target="_blank" rel="follow" title="База патентів України">Похідні оксадіазолу, активні у відношенні сфінгозин-1-фосфату (s1p)</a>
Попередній патент: 1,2,4-оксадіазольні сполуки для лікування аутоімунних захворювань
Наступний патент: Похідні 1-бензил-3-гідроксиметиліндазолу та їх застосування у лікуванні хвороб, основаних на експресії мср-1 та сх3cr1
Випадковий патент: Спосіб діагностики скоротливої активності матки в ранньому післяпологовому періоді у жінок із звичним невиношуванням вагітності в анамнезі