Спосіб одержання 6-заміщених 7-оксо-4a,5,6,7,7a,8-гексагідро-4н-тієно[2,3-f]ізоіндол-8-карбонових кислот
Номер патенту: 115687
Опубліковано: 25.04.2017
Автори: Обушак Микола Дмитрович, Матійчук Василь Степанович, Кінжибало Василь Володимирович, Литвин Роман Зіновійович, Гомза Юрій Володимирович, Горак Юрій Ігорович
Формула / Реферат
Спосіб одержання 6-заміщених 7-оксо-4а,5,6,7,7а,8-гексагідро-4H-тієно[2,3-f]ізоіндол-8-карбонових кислот, що містить взаємодію амінів з малеїновим ангідридом, який відрізняється тим, що як аміни використовують N-арил-3-(3-тієніл)аліламіни, реакцію проводять у середовищі бензолу і одержують сполуки загальної формули
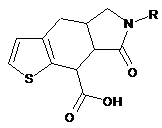 ,
,
де R = арил, алкіл, циклоалкіл.
Текст
Реферат: Спосіб одержання 6-заміщених 7-оксо-4а,5,6,7,7а,8-гексагідро-4H-тієно[2,3-f]ізоіндол-8карбонових кислот, що містить взаємодію амінів з малеїновим ангідридом, причому як аміни використовують N-арил-3-(3-тієніл)аліламіни, реакцію проводять у середовищі бензолу. UA 115687 U (12) UA 115687 U UA 115687 U 5 10 15 20 25 Корисна модель стосується органічної хімії, а саме способів одержання корисних органічних сполук, які можуть бути використані у фармакології як лікарські препарати та біомаркери, які дозволяють діагностувати низку захворювань, таких як хвороба Альцгеймера або ревматоїдний артрит, що починаються з безсимптомної фази хвороби. Відомий спосіб отримання ізоіндолів за дії сильних основ на четвертинні солі ізоіндолінію спосіб Віттіґа, за яким при взаємодії еквівалентних кількостей ефірного розчину феніллітію і броміду Ν,Ν-диметилізоіндолінію в інертній атмосфері одержують N-метилізоіндол з виходом 74 % [Бабичев Φ.С, Ковтуненко В.А. Химия изоиндола /Ф.С. Бабичев В.А. Ковтуненко. - К., Наук, думка, 1983. – 280 с.]. Недоліками способу є низька відтворюваність результатів - виходи ізоіндолів коливаються в широких межах, а також важкодоступність вихідних речовин. Найближчим за технічною сутністю - прототипом є спосіб одержання ізоіндолокарбонових кислот [Zubkov F.I. Thermal and catalytic intramolecular [4+2]-cycloaddition in 2-alkenylfurans /F.I. Zubkov, E.V. Nikitina, A.V. Varlamov //Russian Chemical Reviews. - 2005. - Vol. 74, № 7. - P. 639669], який полягає у реакції [4+2]-циклоприєднання, де фурфуриламіни реагують з малеїновим ангідридом так, що відбувається N-ацилювання з наступною внутрішньомолекулярною реакцією циклоприєднання, в результаті чого формується біциклічна конденсована гетеросистема. Недоліком способу є трансформація фуранового циклу і застосування виключно похідних фурану. В основу корисної моделі поставлено задачу розробити спосіб одержання 6-заміщених 7оксо-4а, 5,6,7,7а, 8-гексагідро-4H-тієно[2,3-f|ізоіндол-8-карбонових кислот шляхом застосування функціоналізованих похідних тіофену та використання в реакції [4+2]-циклоприєднання з малеїновим ангідридом доступних амінів, що дасть змогу одержувати цільові продукти із збереженням тіофенового циклу і розширити межі цієї реакції. Поставлена задача досягається тим, що у способі одержання 6-заміщених 7-оксо-4а, 5,6,7,7а, 8-гексагідро-4H-тієно[2,3-f]ізоіндол-8-карбонових кислот, що містить взаємодію амінів з малеїновим ангідридом, який відрізняється тим, що як аміни використовують N-арил-3-(3тієніл)аліламіни, реакцію проводять у середовищі бензолу і одержують сполуки загальної формули N R O S OH 30 35 40 O , де R = арил, алкіл, циклоалкіл. Автори вперше запропонували використати 3-(3-тієніл)акролеїн як вихідну сполуку. Вона реагує з ароматичними амінами, утворюючи основи Шиффа, а відновленням останніх борогідридом натрію у середовищі абсолютного етанолу отримують відповідно М-арил(алкіл, циклоалкіл)-3-(3-тієніл)аліламіни, які взаємодіють з малеїновим ангідридом у реакції [4+2]циклоприєднання так, що тіофеновий цикл зберігається, а в реакцію вступає екзоциклічний подвійний зв'язок. При цьому формується тієноізоіндольна система з карбоксильною групою у шестичленному карбоциклі. Спосіб можна проілюструвати прикладами, результати яких зведено у таблиці, де виходи 1 13 наведені після перекристалізації. Підтверджено будову цих сполук спектроскопією ЯМР H і С, рентгеноструктурним аналізом та елементним аналізом. Таблиця 6-Заміщені 7-оксо-4а, 5,6,7,7а, 8-гексагідро-4H-тієно[2,3-f]ізоіндол-8-карбонові кислоти № сполуки 1 2 3 4 5 Вихід, % 87 90 78 82 86 R Cyclohexyl 4-СН3С6Н4 4-ОСН3С6Н4 4-COOEtC6H4 С6Н5 1 Т.пл, °C 261-262 245-246 224-225 270-271 262-263 UA 115687 U Одержання сполук 1-5 здійснюють за реакціями: O NH 2 AcONa, спирт N N R R S R N R NaBH4, EtOH S O S O O O S HO O H N R Бензол, t H S O OH O 5 10 15 20 25 , де R = арил, алкіл. Приклад 1. До розчину 0,003 моль (0,66 г) циклогексил-3-(3-тієніл)аліламіну у 10 мл бензолу додають 0,003 моль (0,3 г) розтертого у порошок малеїнового ангідриду, суміш кип'ятять зі зворотним холодильником до моменту виділення осаду {Ъ-4 год.) і 1 год. після цього. Суміш охолоджують, осад відфільтровують, промивають послідовно бензолом і спиртом та перекристалізовують із суміші спирт-ДМФА-вода. Вихід сполуки 1 0,83 г (87 %). Т.пл. 261-262 °C. 1 Спектр ЯМР H, δ, м.ч.: (400 MHz, DMSO-d6) δ = 1.05-1.15 (m, 1H, C6H11), 1.23-1.39 (m, 3Н, C6H11), 1.43-1.48(m, 1Н, C6H11), 1.53 (d, J=11.8 Hz, 1Н, C6H11), 1.60 (d, J=11.5 Hz, 2H, C6H11), 1.75 (dd, J=6.0 Hz, J=2.8 Hz, 2H, C6H11), 2.45 (dd, J=15.2 Hz, J=11.4 Hz, 1H, H-4A), 2.52 (dd, J=12.6 Hz, J=5.6 Hz, 1H, H-4B), 2.81-2.93 (m, 1H, H-4a), 2.87 (dd, J=16.4 Hz, J=4.7 Hz, 1H, H-7a), 3.02 (t, J=9.4 Hz, 1H, H-5A), 3.53 (dd, J=8.8 Hz, J=6.8 Hz, 1H, H-5B), 3.73 (tt, J=11.7 Hz, J=3.7 Hz, 1H, NСН-C6H11), 3.97(d, J=4.7 Hz, 1H, H-8), 6.84 (d, J=5.2 Hz, 1H, thiophen), 7.39 (d, J=5.2 Hz, 1H, thiophen), 12.52 (s, 1H, COOH). Приклад 2. Сполуку "2" одержують аналогічно. Вихід 0,88 г (90 %). Т. пл. 245-246 °C. Спектр 1 ЯМР H, δ, м.ч.: (400 MHz, DMSO-d6): δ = 2.28 (s, 3H, CH3), 2.57 (dd, J=14.2 Hz, J=11.5 Hz, 1H, H4A), 2.87 (dd, J=13.1 Hz, J=5.5 Hz, 1H, H-4B), 2.96 (dd, J=15.5 Hz, J=4.7 Hz, 1H, H-7a), 3.02-3.10 (m, 1H, H-4a), 3.66 (t, J=9.7 Hz, 1H, H-5A), 3.97 (dd, J=8.9 Hz, J=12 Hz, 1H, H-5B), 4.08 (d, J=4.9 Hz, 1H, H-8), 6.89 (d, J=5.2 Hz, 1H, thiophen), 7.18 (d, Jortho, meta=8.2 Hz, 2H, meta C6H5), 7.43 (d, J=5.2 Hz, 1H, thiophen), 7.54 (d, Jortho, meta=8.5 Hz, 2H, ortho C6H5), 12.74 (s, 1H, COOH). Запропонований спосіб дає змогу одержувати цільові продукти 6-заміщені 7-оксо-4а, 5,6,7,7а, 8-гексагідро-4H-тієно[2,3-f]ізоіндол-8-карбонові кислоти, використовуючи дешеві та легкодоступні вихідні реагенти, із збереженням тіофенового циклу та розширити межі реакції, що підтверджує одержання передбачуваного технічного результату. ФОРМУЛА КОРИСНОЇ МОДЕЛІ 30 Спосіб одержання 6-заміщених 7-оксо-4а,5,6,7,7а,8-гексагідро-4H-тієно[2,3-f]ізоіндол-8карбонових кислот, що містить взаємодію амінів з малеїновим ангідридом, який відрізняється тим, що як аміни використовують N-арил-3-(3-тієніл)аліламіни, реакцію проводять у середовищі бензолу і одержують сполуки загальної формули N R O S OH 35 O , де R=арил, алкіл, циклоалкіл. 2 UA 115687 U Комп’ютерна верстка В. Мацело Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 3
ДивитисяДодаткова інформація
МПК / Мітки
МПК: C07D 209/02, C07D 209/00, C07D 209/44
Мітки: одержання, кислот, 7-оксо-4a,5,6,7,7a,8-гексагідро-4н-тієно[2,3-f]ізоіндол-8-карбонових, 6-заміщених, спосіб
Код посилання
<a href="https://ua.patents.su/5-115687-sposib-oderzhannya-6-zamishhenikh-7-okso-4a5677a8-geksagidro-4n-tiehno23-fizoindol-8-karbonovikh-kislot.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 6-заміщених 7-оксо-4a,5,6,7,7a,8-гексагідро-4н-тієно[2,3-f]ізоіндол-8-карбонових кислот</a>
Попередній патент: Спосіб хірургічного лікування дифузного токсичного зоба
Наступний патент: Спосіб одержання 5-(5-арил-2-фурил)-5,8,9,10-тетрагідропіримідо[4,5-b]хінолін-2,4,6-тріонів
Випадковий патент: Композитний матеріал для запобігання утворенню висолів на поверхні будівельних виробів із цементного бетону









