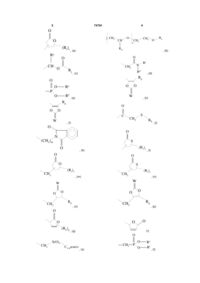
Похідні 6-азаурацилу, що пригнічують інтерлейкін-5, спосіб їх одержання, композиція на їх основі та спосіб її одержання
Номер патенту: 74791
Опубліковано: 15.02.2006
Автори: Лакрампе Жан Фернан Арман, Фрейне Едді Жан Едгар, Коісманс Ірвін, Фортін Джером Мішель Клод, Дерозі Фредерік Дірк
Формула / Реферат
1. Сполука формули:
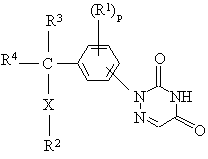 , (I)
, (I)
її N-оксиди, фармацевтично прийнятні адитивні солі та стереоізомеричні форми, де:
р являє собою ціле число 0, 1 або 2;
Х є прямим зв’язком;
Y є О, S, NR5 або S(O)2;
кожний R1 незалежно представляє атом хлору або трифторометил;
R2 являє собою Гет1;
R3 представляє водень, С1-6алкіл або С3-7циклоалкіл;
R4 представляє водень, С1-6алкіл або С3-7циклоалкіл;
кожний R5 незалежно представляє аміносульфоніл, моно- або ді(С1-4алкіл)аміносульфоніл або Гет6сульфоніл;
кожний R11 незалежно вибирають з фенілу, -С(=О)-О-R14, -С(=О)-S-R14 або -С(=О)-NH-R14;
кожний R14 незалежно представляє водень; С1-20ацил або С1-20алкілС1-20ацил (з прямим або розгалуженим, насиченим або ненасиченим вуглеводневим ланцюгом, який має у складі від 1 до 20 атомів вуглецю), необов‘язково заміщений одним або більшою кількістю замісників, вибраних з гідроксигрупи, меркаптогрупи, гідроксіС1-4алкілу, меркаптоС1-4алкілу, NR17R18, арилу, моно- або ді-(С1-4алкіл)аміногрупи, ціаногрупи та Гет5; С1-20алкіл, необов‘язково заміщений одним або більшою кількістю замісників, вибраних з гідроксигрупи, меркаптогрупи, гідроксіС1-4алкілу, меркаптоС1-4алкілу, NR17R18, арилу, моно- або ді-(С1-4алкіл)аміногрупи, ціаногрупи та Гет5; С1-4алкілоксикарбоніл, арилС1-4арилоксикарбоніл, арилС1-4алкілоксигруп, арилС1-4алкілтіокарбоніл, арилС1-4алкілтіогруп, Гет5С1-4алкілоксигрупу, арилС1-4алкілтіогрупу, С3-7циклоалкіл та Гет5С1-4алкілтіогрупу; С3-20алкеніл, необов‘язково заміщений фенілом; С3-20алкініл; С3-7циклоалкілу, необов‘язково заміщеного одним або більшою кількістю замісників, вибраних з гідроксигрупи, меркаптогрупи, атома галогену, меркаптоС1-4алкілу та гідроксіС1-4алкілу; Гет5 або феніл, або R14 представляє радикал однієї з наступних формул:
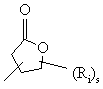 , (a)
, (a)
 , (b)
, (b)
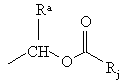 , (c)
, (c)
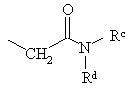 , (d)
, (d)
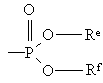 , (e)
, (e)
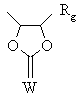 , (h)
, (h)
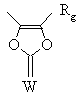 , (i)
, (i)
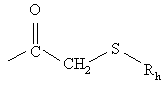 , (j)
, (j)
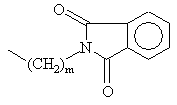 , (k)
, (k)
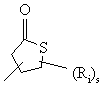 , (l)
, (l)
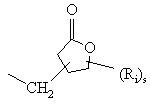 , (m)
, (m)
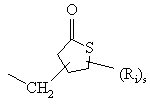 , (n)
, (n)
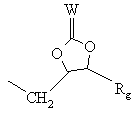 , (o)
, (o)
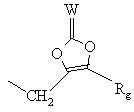 , (p)
, (p)
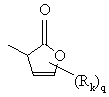 , (q)
, (q)
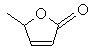 (r)
(r)
![]() , (s)
, (s)
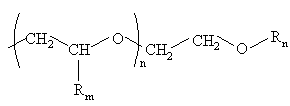
 , (t)
, (t)
де m є від 1 до 4, n є від 0 до 5, q є від 0 до 2, r є від 0 до 2 та s є від 0 до 4;
Rb вибирають з водню, С1-6алкілу, фенілу, С3-7циклоалкілу, С1-4алкілоксіС1-6алкілу та С1-4 алкіл-Y-С1-4алкілу;
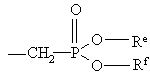
кожний з Ra, Rc, Rd, Re та Rf незалежно вибирають з водню, С1-6алкілу, фенілу та С3-7циклоалкілу, або Re та Rf, узяті разом, можуть утворювати –СН2-СН2-, –СН2–СН2–СН2- або –СН2–СН2–СН2–СН2–;
кожний з Rg, Rh та Rk незалежно є воднем або С1-4алкілом;
Ri вибирають з гідроксигрупи, С3-7циклоалкілу та С1-4алкілу, або два Ri, узяті разом, можуть утворювати –СН2-СН2-, –СН2–СН2–СН2- або –СН2–СН2–СН2–СН2– (утворюючи таким чином спірорадикал);
Rj вибирають з –О-Rb; С1-6алкілу, необов‘язково заміщеного фенілом або С3-7циклоалкілом; фенілу; С3-7циклоалкілу, необов‘язково заміщеного С1-4алкілоксигрупою та моно- або ді(С1-4алкіл)аміногрупою;
Rm є воднем або С1-4алкілоксигрупою;
Rn є воднем, С1-4алкілом, С3-7циклоалкілом, фенілом або фенілС1-4алкілом; та
W є О або S;
кожний Z незалежно є О або S;
кожен з R17 та R18 незалежно вибирають з водню, С1-6алкілу необов‘язково заміщеного одним або більшою кількістю замісників, незалежно вибраними з гідроксигрупи, меркаптогрупи, арилу, моно- або ді(С1-4алкіл)аміногрупи, С1-4алкілоксигрупи та піридинілу; С1-4алкілоксикарбонілу; арилу; С1-4алкілкарбонілу; С1-4алкілтіокарбонілу; арилкарбонілу; арилтіокарбонілу; ариламінокарбонілу; ариламінотіокарбоніл; С3-7циклоалкілу; С1-4алкандіїл-С(=О)-Z-C1-6алкілу; -С(=О)-Z-C1-6алкілу; -Y-C1-4алкандіїл-С(=О)-Z-C1-6алкілу та R6;
арил є фенілом;
Гет1 є тіазолілом, піридинілом або оксадіазолілом, де вказані гетероцикли кожний незалежно є дизаміщені фенілом та або і) R11 або іі) С1-4алкілом, заміщеним R11, де R11 є групою –С(=О)-О-R14;
Гет5 є гетероциклом, вибраним з піролілу, піролінілу, імідазолілу, імідазолінілу, піразолілу, піразолінілу, триазолілу, тетразолілу, фуранілу, тетрагідрофуранілу, тієнілу, тіоланілу, діоксоланілу, оксазолілу, оксазолінілу, ізоксазолілу, тіазолілу, тіазолінілу, ізотіазолілу, тіадіазолілу, оксадіазолілу, піридинілу, піримідинілу, піразинілу, піранілу, піридазинілу, піролідинілу, піперидинілу, піперазинілу, морфолінілу, тіоморфолінілу, тетрагідропіранілу, діоксанілу, дитіанілу, тритіанілу, триазинілу, бензотієнілу, ізобензотієнілу, бензофуранілу, ізобензофуранілу, бензотіазолілу, бензоксазолілу, бензодіоксанілу, індолілу, ізоіндолілу, індолінілу, пуринілу, 1Н-піразоло[3,4-d]піримідинілу, бензімідазолілу, хінолілу, ізохінолілу, цинолінілу, фталазинілу, хіназолінілу, хіноксалінілу, тіазолопіридинілу, оксазолопіридинілу та імідазо[2,1-b]тіазолілу; де вказані гетероцикли кожний незалежно може бути заміщений, якщо припустимо, одним, двома, трьома або чотирма замісниками, кожен незалежно вибраний з карбонілу, С1-4алкілу, C(=O)-Z-C1-6алкілу та R6;
Гет6 є піролідинілом,
за умови, що
R14 є відмінним за гідроген, С1-4алкіл, С3-7циклоалкіл, амінокарбонілметилен, моно- або ді(С1-4алкіл)амінокарбонілметилен у випадку, коли R11 є С(=О)-О-R14.
2. Сполука за п.1, яка відрізняється тим, що
R3 є воднем, метилом, етилом, пропілом або циклогексилом;
R4 є воднем або метилом;
кожний R14 незалежно є дигідрофуранілом, С5-20алкілом, С3-20алкенілом, полігалогенС1-6алкілом, Гет6, радикалом формули (а) або С1-20алкілом, заміщеним одним або більшою кількістю замісників, вибраних з фенілу, С1-4алкіламіногрупи, ціаногрупи, Гет5, гідроксигрупи та С3-7циклоалкілу;
кожний R17 та R18 незалежно є воднем або фенілом; та
Гет5 є піперидинілом або піперазинілом, необов‘язково заміщеним С1-4алкілом, сульфонамідогрупою або R6.
3. Сполука за п.1, яка відрізняється тим, що складова 6–азаурацилу є у парапозиції відносно атома вуглецю, до якого приєднано -Х-R2, замісники R3 та R4.
4. Сполука за п.1, яка відрізняється тим, що Гет1 є тіазолілом.
5. Сполука за п.1, яка відрізняється тим, що R3 та R4 обидва є метилом.
6. Сполука за п.1, яка відрізняється тим, що р дорівнює 1 або 2, а кожний R1 є атомом хлору.
7. Сполука за п.1, яка відрізняється тим, що R3 та R4 обидва є метилом, -Х-R2 є необов‘язково заміщеним 2-тіазолілом або 3-оксадіазолілом, складова 6–азаурацилу є у парапозиції відносно атома вуглецю, до якого приєднано -Х-R2, замісники R3 та R4, та р дорівнює 2, причому обидва замісники R1 представлені хлорними радикалами, знаходяться в ортопозиції відносно атома вуглецю, до якого приєднані –Х-R2, замісники R3 та R4.
8. Сполука за п. 7, яка відрізняється тим, що радикал –Х-R2 є двозаміщеним фенілом та або (і) R11, де R11 є групою формули –С(=О)-Z-R14, у якій Z є О, та R14 є С1-20алкілом, заміщеним гідроксигрупою або Гет5, де Гет5 є піперазинілом заміщеним Гет6сульфонілом, або R14 є радикалом формули (а), в якій Ri є С1-6алкілом та s дорівнює 2, або (іі) С1-6алкілом, заміщеним R11, де R11 є групою формули –С(=О)-Z-R14, у якій Z є О та R14 є радикалом формули (а), де Rі є С1-6алкілом та s дорівнює 2.
9. Сполука за п.1, вибрана зі сполук формул (А), (В), (С), (D):
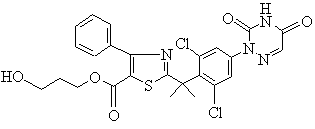 , (A)
, (A)
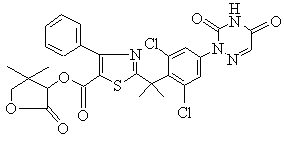 , (B)
, (B)
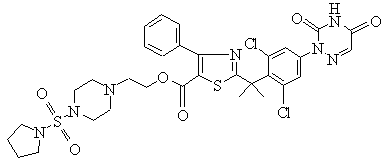 , (C)
, (C)
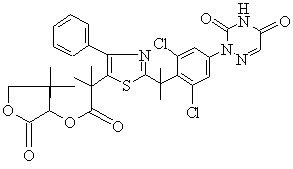 . (D)
. (D)
10. Композиція, яка містить фармацевтично прийнятний носій та, як активний інгредієнт, терапевтично ефективну кількість сполуки за п.1.
11. Спосіб одержання композиції за п.10, який відрізняється тим, що фармацевтично прийнятний носій ретельно змішують з терапевтично ефективною кількістю сполуки за п.1.
12. Застосування сполуки за п.1 для виробництва медикаментів для лікування еозинофілзалежних запальних захворювань.
13. Спосіб одержання сполуки за п.1, який включає етапи:
реакція проміжної сполуки формули (ІІ), де W1 є придатною для заміщення групою, з відповідним реагентом формули (ІІІ), необов‘язково у інертному розчиннику та необов‘язково у присутності основи при температурі від –70![]() C до температури кипіння зі зворотним холодильником;
C до температури кипіння зі зворотним холодильником;
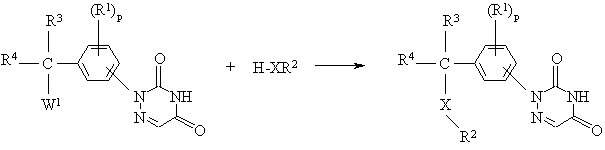 ,
,
(II)
(III)
(I)
+W1H
де R1, R2, R3, R4, р та Х визначені у п.1; та, якщо бажано, перетворення сполук формули (І) за допомогою відомих з рівня техніки перетворень, та далі, якщо бажано, перетворення сполуки формули (І) у терапевтично активну нетоксичну кислу адитивну сіль шляхом обробки кислотою або у терапевтично активну нетоксичну основну адитивну сіль шляхом обробки основою або, навпаки, перетворення кислої адитивної солі у вільну основу шляхом обробки лугом, або перетворення основної адитивної солі у вільну кислоту шляхом обробки кислотою; а також, якщо бажано, одержання їх стереохімічно ізомерних форм або форм N-оксиду.
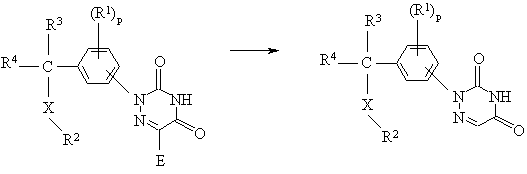
14. Спосіб одержання сполуки за п.1, який включає етапи:
видалення групи Е триазиндіону формули (V)
 ,
,
(V)
(I)
де Е є відповідною групою – акцептором електронів, та R1, R2, R3, R4, Х та число р визначені у п.1; та, якщо бажано, перетворення сполук формули (І) за допомогою відомих з рівня техніки перетворень, та далі, якщо бажано, перетворення сполуки формули (І) у терапевтично активну нетоксичну кислу адитивну сіль шляхом обробки кислотою або у терапевтично активну нетоксичну основну адитивну сіль шляхом обробки основою або, навпаки, перетворення кислої адитивної солі у вільну основу шляхом обробки лугом, або перетворення основної адитивної солі у вільну кислоту шляхом обробки кислотою; а також, якщо бажано, одержання їх стереохімічно ізомерних форм або форм N-оксиду.
15. Спосіб мічення рецептора, який містить етапи:
а) мічення сполуки за п.1 радіоактивними ізотопами;
б) введення зазначеної радіоктивноміченої сполуки до біологічного матеріалу;
в) визначення випромінювання від радіоктивноміченої сполуки.
16. Спосіб візуалізації органа, який відрізняється тим, що вводять достатню кількість радіоактивноміченої сполуки формули (І) у складі відповідної композиції та визначають випромінювання від радіоактивної сполуки.
Текст
1. Сполука формули: 2 (19) 1 3 74791 4 O CH2 O O CH O Ra Rm , (a) , (b) O O O Rj Rc N CH2 Rd , (c) , (d) Rg O O O O Re O Rf , (e) P W Rg , (h) O O O S C W CH2 Rh , (i) , (j) O O N (CH2)m S O (Ri)s , (k) O , (l) O O S (Ri)s CH2 , (m) (Ri)s CH2 , (n) W W O O O O Rg CH2 Rg CH2 , (o) , (p) O O O O (Rk)q (r) , (q) O CH2 Rn n (Ri)s CH CH2 CH2 S(O)r C1-6алкіл CH2 , (s) P O O Re Rf , (t) 5 74791 6 де m є від 1 до 4, n є від 0 до 5, q є від 0 до 2, r є де вказані гетероцикли кожний незалежно може від 0 до 2 та s є від 0 до 4; бути заміщений, якщо припустимо, одним, двома, Rb вибирають з водню, С1-6алкілу, фенілу, С3-7 циктрьома або чотирма замісниками, кожен незалежлоалкілу, С1-4алкілоксіС1-6алкілу та С1-4 алкіл-Y-С1-4 но вибраний з карбонілу, С1-4алкілу, C(=O)-Z-C1-6 алкілу; алкілу та R6; a c d e f 6 кожний з R , R , R , R та R незалежно вибирають Гет є піролідинілом, з водню, С1-6алкілу, фенілу та С3-7циклоалкілу, або за умови, що Re та Rf, узяті разом, можуть утворювати –СН2R14 є відмінним за гідроген, С1-4алкіл, С3-7 циклоалСН2-, –СН2–СН2–СН2- або –СН2–СН2–СН2–СН2–; кіл, амінокарбонілметилен, моно- або ді(С1-4 алкожний з Rg, Rh та Rk незалежно є воднем або С1-4 кіл)амінокарбонілметилен у випадку, коли R11 є алкілом; С(=О)-О-R14. Ri вибирають з гідроксигрупи, С3-7циклоалкілу та 2. Сполука за п.1, яка відрізняється тим, що С1-4алкілу, або два Ri, узяті разом, можуть утворюR3 є воднем, метилом, етилом, пропілом або циквати –СН2-СН2-, –СН2–СН2–СН2- або –СН2–СН2– логексилом; СН2–СН2– (утворюючи таким чином спірорадикал); R4 є воднем або метилом; Rj вибирають з –О-Rb; С1-6алкілу, необов„язково кожний R14 незалежно є дигідрофуранілом, С5-20 заміщеного фенілом або С3-7циклоалкілом; фенілу; алкілом, С3-20алкенілом, полігалогенС1-6алкілом, С3-7циклоалкілу, необов„язково заміщеного С1-4 Гет6, радикалом формули (а) або С1-20алкілом, алкілоксигрупою та моно- або ді(С1-4 алзаміщеним одним або більшою кількістю замісникіл)аміногрупою; ків, вибраних з фенілу, С1-4алкіламіногрупи, ціаноRm є воднем або С1-4алкілоксигрупою; групи, Гет5, гідроксигрупи та С3-7циклоалкілу; Rn є воднем, С1-4алкілом, С3-7циклоалкілом, фенікожний R17 та R18 незалежно є воднем або фенілом або фенілС1-4алкілом; та лом; та W є О або S; Гет5 є піперидинілом або піперазинілом, неокожний Z незалежно є О або S; бов„язково заміщеним С1-4алкілом, сульфонамідокожен з R17 та R18 незалежно вибирають з водню, групою або R6. С1-6алкілу необов„язково заміщеного одним або 3. Сполука за п.1, яка відрізняється тим, що склабільшою кількістю замісників, незалежно вибранидова 6–азаурацилу є у парапозиції відносно атома ми з гідроксигрупи, меркаптогрупи, арилу, моновуглецю, до якого приєднано -Х-R2, замісники R3 або ді(С1-4алкіл)аміногрупи, С1-4алкілоксигрупи та та R4. піридинілу; С1-4алкілоксикарбонілу; арилу; С1-4 ал4. Сполука за п.1, яка відрізняється тим, що Гет1 є кілкарбонілу; С1-4алкілтіокарбонілу; арилкарбонілу; тіазолілом. 3 арилтіокарбонілу; ариламінокарбонілу; ариламіно5. Сполука за п.1, яка відрізняється тим, що R та 4 тіокарбоніл; С3-7циклоалкілу; С1-4алкандіїл-С(=О)R обидва є метилом. Z-C1-6алкілу; -С(=О)-Z-C1-6алкілу; -Y-C1-4 6. Сполука за п.1, яка відрізняється тим, що р доалкандіїл-С(=О)-Z-C1-6алкілу та R6; рівнює 1 або 2, а кожний R1 є атомом хлору. арил є фенілом; 7. Сполука за п.1, яка відрізняється тим, що R3 та 1 Гет є тіазолілом, піридинілом або оксадіазолілом, R4 обидва є метилом, -Х-R2 є необов„язково заміде вказані гетероцикли кожний незалежно є дизащеним 2-тіазолілом або 3-оксадіазолілом, складоміщені фенілом та або і) R11 або іі) С1-4алкілом, ва 6–азаурацилу є у парапозиції відносно атома заміщеним R11, де R11 є групою –С(=О)-О-R14; вуглецю, до якого приєднано -Х-R2, замісники R3 Гет5 є гетероциклом, вибраним з піролілу, піроліта R4, та р дорівнює 2, причому обидва замісники нілу, імідазолілу, імідазолінілу, піразолілу, піразоR1 представлені хлорними радикалами, знахолінілу, триазолілу, тетразолілу, фуранілу, тетрагідяться в ортопозиції відносно атома вуглецю, до дрофуранілу, тієнілу, тіоланілу, діоксоланілу, якого приєднані –Х-R2, замісники R3 та R4. оксазолілу, оксазолінілу, ізоксазолілу, тіазолілу, 8. Сполука за п. 7, яка відрізняється тим, що радитіазолінілу, ізотіазолілу, тіадіазолілу, оксадіазолікал –Х-R2 є двозаміщеним фенілом та або (і) R11, лу, піридинілу, піримідинілу, піразинілу, піранілу, де R11 є групою формули –С(=О)-Z-R14, у якій Z є піридазинілу, піролідинілу, піперидинілу, піперазиО, та R14 є С1-20алкілом, заміщеним гідроксигрупою нілу, морфолінілу, тіоморфолінілу, тетрагідропіраабо Гет5, де Гет5 є піперазинілом заміщеним нілу, діоксанілу, дитіанілу, тритіанілу, триазинілу, Гет6сульфонілом, або R14 є радикалом формули бензотієнілу, ізобензотієнілу, бензофуранілу, ізо(а), в якій Ri є С1-6алкілом та s дорівнює 2, або (іі) бензофуранілу, бензотіазолілу, бензоксазолілу, С1-6алкілом, заміщеним R11, де R11 є групою форбензодіоксанілу, індолілу, ізоіндолілу, індолінілу, мули –С(=О)-Z-R14, у якій Z є О та R14 є радикалом пуринілу, 1Н-піразоло[3,4-d]піримідинілу, бензіміформули (а), де Rі є С1-6алкілом та s дорівнює 2. дазолілу, хінолілу, ізохінолілу, цинолінілу, фтала9. Сполука за п.1, вибрана зі сполук формул (А), зинілу, хіназолінілу, хіноксалінілу, тіазолопіридині(В), (С), (D): лу, оксазолопіридинілу та імідазо[2,1-b]тіазолілу; 7 74791 H N O N HO O Cl N 8 N N Cl N , S N O O O Cl N Cl O , O H N O N N S Cl N O N S Cl O O O , (B) 10. Композиція, яка містить фармацевтично прийнятний носій та, як активний інгредієнт, терапевтично ефективну кількість сполуки за п.1. 11. Спосіб одержання композиції за п.10, який відрізняється тим, що фармацевтично прийнятний носій ретельно змішують з терапевтично ефективною кількістю сполуки за п.1. 12. Застосування сполуки за п.1 для виробництва медикаментів для лікування еозинофілзалежних запальних захворювань. 13. Спосіб одержання сполуки за п.1, який включає етапи: реакція проміжної сполуки формули (ІІ), де W1 є придатною для заміщення групою, з відповідним реагентом формули (ІІІ), необов„язково у інертному розчиннику та необов„язково у присутності основи при температурі від –70 o C до температури кипіння зі зворотним холодильником; R4 (R1)p W1 (R1)p R3 O C N N + NH H-XR2 R4 O C N N X O R2 NH O , (I) +W1H де R1, R2, R3, R4, р та Х визначені у п.1; та, якщо бажано, перетворення сполук формули (І) за допомогою відомих з рівня техніки перетворень, та далі, якщо бажано, перетворення сполуки формули (І) у терапевтично активну нетоксичну кислу адитивну сіль шляхом обробки кислотою або у терапевтично активну нетоксичну основну адитивну сіль шляхом обробки основою або, навпаки, перетворення кислої адитивної солі у вільну основу шляхом обробки лугом, або перетворення основної адитивної солі у вільну кислоту шляхом обробки кислотою; а також, якщо бажано, одержання їх стереохімічно ізомерних форм або форм N-оксиду. (II) (III) N S O Cl O R3 O (C) H N N N Cl O (A) O O N O S O H N O O . (D) 14. Спосіб одержання сполуки за п.1, який включає етапи: видалення групи Е триазиндіону формули (V) (R1)p R3 R4 R4 O C N N X (R1)p R3 NH N N X O R2 O C R2 NH O E , (V) (I) де Е є відповідною групою – акцептором електронів, та R1, R2, R3, R4, Х та число р визначені у п.1; та, якщо бажано, перетворення сполук формули (І) за допомогою відомих з рівня техніки перетворень, та далі, якщо бажано, перетворення сполуки формули (І) у терапевтично активну нетоксичну кислу адитивну сіль шляхом обробки кислотою або у терапевтично активну нетоксичну основну адитивну сіль шляхом обробки основою або, навпаки, перетворення кислої адитивної солі у вільну основу шляхом обробки лугом, або перетворення основної адитивної солі у вільну кислоту шляхом обробки кислотою; а також, якщо бажано, одержання їх стереохімічно ізомерних форм або форм N-оксиду. 15. Спосіб мічення рецептора, який містить етапи: а) мічення сполуки за п.1 радіоактивними ізотопами; б) введення зазначеної радіоктивноміченої сполуки до біологічного матеріалу; в) визначення випромінювання від радіоктивноміченої сполуки. 16. Спосіб візуалізації органа, який відрізняється тим, що вводять достатню кількість радіоактивноміченої сполуки формули (І) у складі відповідної композиції та визначають випромінювання від радіоактивної сполуки. 9 74791 10 Даний винахід стосується похідних 6азаурацилу, які пригнічують інтерлейкін-5 (ІЛ-5) та є ефективними в лікуванні еозинофіл-залежних запальних захворювань, процесу їх приготування та проміжним продуктам, а також фармацевтичним сполукам, які містять згадані похідні. Крім того, винахід пов'язаний із застосуванням цих похідних як медичного препарату, а також процесу мічення рецепторів та візуалізації органу із використанням вказаних похідних. Захоплення еозинофілів, що призводить до подальшого пошкодження тканини, вважається важливою патогенетичною ланкою бронхіальної астми та алергічних захворювань. Цитокін інтерлейкін-5 (ІЛ-5) за своєю природою є глікопротеїном, який продукується переважно Т-лімфоцитами та має здатність потенціювати диференціювання еозинофілів у кістковому мозку, стимулювати активацію незрілих еозинофілів у периферичній крові та підтримувати їх життєздатність у тканинах. Сам по-собі ІЛ-5 відіграє критичну роль у патогенезі еозинофільного запалення. Виходячи з цього, можливість зниження інгібіторами продукування ІЛ-5, у свою чергузнижує продукування активацію та/або життєздатності еозинофілів, становить певний терапевтичний підхід до лікування бронхіальної астми та інших алергічних захворювань, таких, як, наприклад, атопічні дерматити, алергічні риніти, алергічні кон'юнктивіти та інші еозинофілзалежні запальні хвороби. Стероїди, які потужно інгібують утворення ІЛ-5 in vitro, тривалий час застосовуються як єдині препарати з вираженою ефективністю стосовно бронхіальної астми та атопічних дерматитів, однак вони мають низку серйозних побічних реакцій, викликаючи, наприклад діабет, гіпертензія та катаракти. Тому дуже бажаним є пошук нестероїдних сполук, які б мали здатність пригнічувати утворення ІЛ-5 в Т-клітинах людини при мінімальних (або, навіть, відсутніх) побічних ефектах. Представлені в патенті US 4,631,278 -арил-4(4,5-дигідро-3,5-діоксо-1,2,4-тріазин-2(3Н)-іл)бензен-ацетонітрили та в патенті US 4,767,760 2(заміщений феніл)-1,2,4-тріазин-3,5(2Н,4Н)-діони мають антипротозойну активність, зокрема антикоккову активність. В патенти ЕР 831,088 як антикоккові агенти описуються 1,2,4-тріазин-3,5-діони. Заявка WO99/02505 представляє похідні 6азаурацилу, які мають потужну інгібуючу дію на утворення ІЛ-5. Представлений винахід стосується сполук, які мають формулу: ком, або радикали X-R2, разом взяті, можуть бути представлені ціаногрупою; Υ представлений О, S, NR5 або S(O)2; Кожний радикал R1 незалежно представляє 14 C(=O) Z-R , С1-6алкіл, гало, полігалоС1-6алкіл, гідрокси, меркапто, С1-6алкілокси, С1-6алкілтіо, С1-6 алкілкарбонілокси, арил, ціано, нітро, Het3, R6, NR7R8 або С1-4алкіл, заміщений C(=O) ZR14, Het3, R6 або NR7R8; R2 являє собою Het1, С3-7циклоалкіл, який необов'язково може бути заміщений на C(=O)-Z-R14, С1-6алкіл або С1-6алкіл, заміщений одним або двома замісниками, вибраними з C(=O) Z-R14, гідрокси, меркапто, ціано, аміно, моно- або ді(С1-4 алкіл)аміно, С1-6алкілокси, необов'язково заміщений C(=O)-Z-R14, С1-6алкілтіо, необов'язково заміщений C(=O)-Z-R14, С1-6алкілсульфонілокси, С3-7 циклоалкіл, необов'язково заміщений C(=O)-Z-R14, арил, арилокси, арилтіо, Het1, Het1-окси та Het1-тio; aбo якщо X представлений О, S або NR5, тоді R2 може також являти собоюамінотіокарбоніл, С1-4 алкілкарбоніл, необов'язково заміщений C(=O)-Z-R14, C1-4 алкілтіокарбоніл, необов'язково заміщений C(=O)Z-R14, арилкарбоніл, арилтіокарбоніл, Het11 карбоніл або Het -тіокарбоніл; R3 представляє водень, С1-6алкіл або С3-7 циклоалкіл; R4 представляє водень, С1-6алкіл або С3-7 циклоалкіл; або R3 та R4, разом взяті, формують С2-6алкандіїл; R5 представляє водень або С1-4алкіл; 6 кожний радикал R окремо представляє С1-6 алкілсульфоніл, аміносульфоніл, піперидинілсульфоніл, моно- або ді(С1-4алкіл)міносульфоніл, моно- або ди(бензил)аміносульфоніл, полігалоС1-6 алкілсульфоніл, С1-6алкілсульфініл, фенілС1-4 алкілсульфоніл, піперазинілсульфоніл, амінопіперидинілсульфоніл, піперидиніл-аміносульфоніл, NС1-4алкіл-N-піперидиніламіносульфоніл, Y-R14, моно- або ді- (С1-4алкіл)аміноС1-4алкілсульфоніл, Неt6сульфоніл або С3-7циклоалкілсульфоніл; кожен з радикалів R7 та R8 незалежно вибрані з водню, С1-4алкілу, гідроксиС1-4алкілу, меркаптоС1-4алкілу, дигідроксиС1-4алкілу, арилу, арилС1-4 алкілу, С1-4алкілоксиС1-4алкілу, С1-4алкілкарбонілу, С1-4алкіл-тіокарбонілу, арилкарбонілу, арилтіокарбонілу, Неt3тіокарбонілу, Het3карбонілу, моно- або ді(С1-4алкіл)аміноС1-4алкілу, ариламінокарбонілу, ариламінотіокарбонілу, Неt3амінокарбонілу, Неt3амінотіокарбонілу, С3-7циклоалкілу, піридинілС1-4алкілу, С1-4алкандіїл-С(=О)-Z-R14, -C(=O)-ZR14, -Y-C1-4алкандіїл -C(=O)-Z-R14, Het3, Het4 та R6; або R7 та R8 разом з атомом азоту, до якого вони приєднані, формують радикал, що відповідає формулі: їх N-оксидів, фармацевтично прийнятних адитивних солей та стереоізомеричних форм, де: p являє собою ціле число 0, 1, 2, 3 або 4; X представлений О, S, NR5 чи прямим зв'яз кожен з радикалів R9 та R10 незалежно вибраний з водню, С1-4алкілу, гідроксиС1-4алкілу, меркапто-С1-4алкілу, дигідроксиС1-4алкілу, фенілу, фенілС1-4алкілу, С1-4алкілоксиС1-4алкілу, 11 74791 12 С1-4алкілкарбонілу, арилкарбонілу, Неt3карбонілу, одним або більше замісниками, вибраними з наНеt3тіокарбонілу, моно- або ді(С1-4алкіл)аміноС1-4 ступних: гідрокси, меркапто, гало, меркаптоС1-4 алкілу, ариламінокарбонілу, ариламінотіокарбоніалкіл та гідроксиС1-4алкіл; Het5 або феніл, або R14 3 3 лу, Неt амінокарбонілу, Неt амінотіокарбонілу, С3-7 представлені радикалами, які відображаються циклоалкілу, піридинілС1-4алкілу, С1-4алкандіїлбудь-якою з наступних формул: 14 14 С(=О)-Z-R , -C(=O)-Z-R , -Y-C1-4алкандіїл-С(=О)Z-R14, Het3, Het4 та R6; або R9 та R10 разом з атомом азоту, до якого вони приєднані, формують радикал, що відповідає формулі: кожен радикал R11 незалежно вибраний з гідрокси, меркапто, ціано, нітро, гало, тригалометил, С1-4алкілокси, необов'язково заміщеного C(=O)-ZR14, С1-4алкілтіо, необов'язково заміщеного на C(=O)-Z-R14, форміл, тригалоС1-4 алкілсульфонілокси, R6, NR7R8, C(=O)NR15R16, -C(=O)-Z-R14, -Y-С1-4 алкандіїл-С(=О)-Z-R14, арилу, арилокси, арилкарбонілу, арилтіокарбонілу, С3-7циклоалкілу, необов'язково заміщеного з C(=O)-Z-R14, С3-7 циклоалкілокси, необов'язково заміщеного С(=О)-Z-R14, С3-7 циклоалкілтіо, необов'язково заміщеного C(=O)-ZR14, фталімід-2-ілу, Het3, Het4, C(=O)Het3, С(=О)С1-4 алкілу, необов'язково заміщеного одним або більше замісниками, незалежно вибраними з гідрокси, меркапто, гало та фенілу; кожен з радикалів R12 та R13 незалежно вибраний з водню, С1-4алкілу, гідроксиС1-4алкілу, меркапто-С1-4алкілу, дигідроксиС1-4 алкілу, фенілу, фенілС1-4алкілу, С1-4алкілоксиС1-4 алкілу, С1-4алкілкарбонілу, С1-4алкілтіокарбонілу, арилкарбонілу, моно- або ді(С1-4алкіл)аміноС1-4 алкілу, ариламінокарбонілу, ариламінотіокарбонілу, С3-7циклоалкілу, піридинілС1-4алкілу, С1-4 алкандіїл-С(=О)-Z-R14, -C(=O)-Z-R14, -Y-С1-4алкандіїлС(=О)-Z-R14 та R6; або R12 тa R13 разом із атомом азоту, до якого вони приєднані, формують радикал, що відповідає формулі: кожний радикал R14 незалежно представлений воднем; С1-20ацилом або С1-20алкілС1-20ацилом (з розгалуженою або нерозгалуженою структурою, з насиченим або ненасиченим вуглеводневим ланцюгом, який має у складі від 1 до 20 атомів вуглецю), необов'язково заміщеним одним або більше замісниками з наступних: гідрокси, меркапто гідроксиС1-4алкіл, меркаптоС1-4алкіл, NR17R18, арил, моно- або ді-(С1-4алкіл)аміно, ціано та Неt5;С1-20 алкіл, необов'язково заміщений одним або більше замісниками, вибраними з гідрокси, гало, меркапто, С1-4алкілоксиС1-4алкілокси, меркаптоС1-4алкілу, NR17R18, арилу, моно або ді-(С1-4алкіл)аміно, ціано, Неt5, С1-4алкілоксикарбонілу, арилС1-4 алкилоксикарбонілу, арилС1-4алкілокси, арилС1-4 алкілтіокарбоніл, арилС1-4алкілтіо, Неt5С1-4алкілокси, арилС1-4 алкілтіо, С3-7циклоалкілу та Неt5С1-4алкілтіо; С3-20 алкеніл, необов'язково заміщений фенілом; С3-20 алкініл; С3-7циклоалкіл, необов'язково заміщений в яких m - від 1 до 4, n - від 0 до 5, q - від 0 до 2, r - від 0 до 2 та s - від 0 до 4; Rb вибраний з водню, С1-6алкілу, фенілу, С3-7 циклоалкілу, С1-4алкілоксиС1-6алкілу та С1-4алкіл-YC1-4алкілу; кожний з радикалів Ra, Rc, Rd, Re та Rf незалежно вибраний з водню, С1-6алкілу, фенілу та С3-7 циклоалкілу або Re та Rf, разом взяті, можуть утворювати -СН2-СН2-, -СН2-СН2-СН2- або -CH2CH2-CH2-CH2-; кожен з радикалів Rg, Rh та Rk незалежно представлений воднем або С1-4алкілом; Ri вибраний з гідрокси, С3-7циклоалкілу та С1-4 алкілу або два радикали Ri, разом взяті, можуть формувати -СН2-СН2-, -СН2-СН2-СН2- або -СН2СН2-СН2-СН2- (утворюючи таким чином спірорадикал); Rj вибраний з -O-Rb; С1-6алкілу, необов'язково заміщеного фенільною групою або С3-7 циклоалкілом; фенілу; С3-7циклоалкілу, необов'язково заміщеного С1-4алкілокси та моно- або ді(С1-4 алкіл)аміно; Rm представлений воднем або С1-4алкілокси; Rn представлений воднем, С1-4алкілом, 13 74791 14 С3-7циклоалкілом, фенілом або фенілС1-4алкілом; наприклад, пірроліл, пирролініл, імідазоліл, імідата золініл, піразоліл, піразолініл, тріазоліл, тетразоW являє собою О або S; ліл, фураніл, тетрагідрофураніл, тієніл, тіоланіл, кожний з радикалів Ζ незалежно представледіоксоланіл, оксазоліл, оксазолініл, ізоксазоліл, ний О, S, ΝΗ, -СН2-О- або -СН2-S-, внаслідок чого тіазоліл, тіазолініл, ізотіазоліл, тіадіазоліл, оксадіСН2- приєднується до карбонільної групи; або азоліл, піридиніл, піримідиніл, піразиніл, піраніл, -Z-R14, разом взяті, формують радикал, що віпіридазиніл, пірролідиніл, піперидиніл, піперазиніл, дповідає формулі: морфолініл, тіоморфолініл, діоксаніл, дитіаніл, тритіаніл, тріазиніл, бензотієніл, ізобензотієніл, бензофураніл, ізобензофураніл, бензотіазоліл, бензоксазоліл, бензодіоксаніл, індоліл, ізоіндоліл, індолініл, пуриніл, 1H-піразоло[3,4-d]піримідиніл, бензімідазоліл, хіноліл, ізохіноліл, циннолініл, фталазиніл, хіназолініл, хіноксалініл, тіазолопірикожен з радикалів R15 та R16 незалежно вибдиніл, оксазолопіридиніл, та імідазо[2,1-b]тіазоліл; раний з водню; С1-4алкілу, необов'язково заміщев яких кожен з вищезазначених гетероциклів може ного одним або більше замісниками, незалежно бути необов'язково заміщений одним або, в тих вибраними з гідрокси, меркапто, арилу, моно- або випадках, коли це можливо, двома або трьома ді(С1-4алкіл)аміно та піридинілу; С1-4алкілокси; замісниками, кожен з яких незалежно вибраний з арилу; -C(=:O)-Z-R14; арилкарбонілу; арилтіокарHet2, R11 та С1-4алкілу, необов'язково заміщеного бонілу; ариламінокарбонілу; ариламінотіокарбоніодним або, якщо можливо, двома чи трьома заміслу; амінокарбонілметилену; моно- або ді(С1-4 алниками, кожен з яких незалежно вибраний з Het2 3 кіл)амінокарбонілметилену; Неt амінокарбонілу; тa R11; Неt3амінотіокарбонілу; піридинілС1-4алкілу; Het3 та Het2 являє собою тричленний, чотиричленний, R6; або R15 та R16 які, разом з атомом азоту, до п'яти- або шестичленний ароматичний або неароякого вони приєднані, формують радикал, що відматичний, моноциклічний або поліциклічний гетеповідає формулі: роцикл який містить один або більше, переважно від одного до чотирьох, гетероатомів, здебільшого обраних з азоту, кисню, сірки та фосфору, або замкнуту поліциклічнукільцеву систему, до складу якої входить вказаний гетероцикл (наприклад, замкнутий бензогетероцикл); до зразків подібних гетероцикл і в належать, але не обмужуються никожен з радикалів R17 та R18 незалежно вибми ,наприклад, пірроліл, пирролініл, імідазоліл, раний з водню, С1-6алкілу, необов'язково заміщеімідазолініл, піразоліл, піразолініл, тріазоліл, тетразоліл, фураніл. тетрагідрофураніл, тієніл, тіоланого одним або більше замісниками, незалежно обраними з гідрокси, меркапто, арилу, моно або ніл, діоксоланіл, оксазоліл, оксазолініл, ізоксазоліл, тіазоліл, тіазолініл, ізотіазоліл, тіадіазоліл, ді(С1-4алкіл) аміно, С1-4алкілокси та піридинілу; С1-4алкілоксикарбонілу; арилу; С1-4 алкілкарбооксадіазоліл, піридиніл, піримідиніл, піразиніл, піраніл, піридазиніл, діоксаніл, дитіаніл, тритіаніл, нілу; С1-4алкілтіокарбонілу; арилкарбонілу; арилтіокарбонілу; ариламінокарбонілу; ариламінотіокартріазиніл, бензотієніл, ізобензотієніл, бензофураніл, ізобензофураніл, бензотіазоліл, бензоксазобонілу; С3-7циклоалкілу; С1-4алкандіїл-С(=О)-Z-С1-6алкілу; -С(=О)-Z-С1-6 ліл, індоліл, ізоіндоліл, індолініл, пуриніл, 1Нпіразоло[3,4-d]піримідиніл, бензімідазоліл, хіноліл, алкілу; -Y-C1-4aлкaндiїл-C(=O)-Z-C1-6aлкiлy та R6; ізохіноліл, циннолініл, фталазиніл, хіназолініл, арил представлений фенілом, необов'язково хіноксалініл, тіазолопіридиніл, оксазолопіридиніл, заміщеним одним, двома або трьома замісниками, та імідазо[2,1-b]тіазоліл; в яких кожен з вищезакожен з яких незалежно вибраний з нітро, азидо, значених гетероциклів окремо може необов'язково ціано, гало, гідрокси, меркапто, С1-4алкілу, С3-7 цибути заміщеним одним або, в тих випадках, коли клоалкілу, С1-4алкілокси, С1-4алкілтіо, формілу, це можливо, двома чи трьома замісниками, кожен полігалоС1-4алкілу, NR9R10, C(=O)NR9R10, C(=O)-Zз яких незалежно вибраний з Het4, R11 та С1R14, R6, -O-R6, фенілу, Het3, C(=O)Het3 та С1-4 алкі4алкілу, необов'язково заміщеного одним або, яклу, заміщеного одним або більше замісниками, що припустимо, двома чи трьома замісниками, кожен з яких незалежно вибраний з гало, гідрокси, кожен з яких незалежно обраний з Het4 та R11; 14 меркапто, С1-4алкілокси, С1-4алкілтіо, C(O)-Z-R , Het3 представлений тричленним, чотиричлен14 3 9 10 Y-С1-4алкандіїл-С(=О)-Z-R , Het або NR R ; ним, п'ятичленним або шестичленним ароматичHet1 представляє тричленний, чотиричленний, ним або неароматичним, моноциклічним гетероцип'ятичленний або шестичленний ароматичний або клом який містить один або більше, переважно від неароматичний, моноциклічний або поліциклічний одного до чотирьох, гетероатомів, здебільшого гетероцикл, який містить один або більше, переобраних з азоту, кисню, сірки та фосфору; до зразважно від одного до чотирьох, гетероатомів, здеків подібних гетероциклів належать, але не обмебільшого обраних з азоту, кисню, сірки та фосфожуються ними, наприклад, пірролідиніл, піперидиру, або замкнуту поліциклічну кільцеву систему, до ніл, піперазиніл, морфолініл, тіоморфолініл, складу якої входить вказаний гетероцикл (напридіоксоланіл та тетрагідропіраніл; в яких кожен з клад, замкнутий бензогетероцикл); до подібних вищезазначених моноциклічних гетероциклів гетероциклів належать, але не обмежуються ними, окремо може бути необов'язково заміщений, де 15 74791 16 можливо, одним, двома, трьома або чотирма заміазаридиніл, піразолініл та піролініл, в яких кожен з сниками, кожен з яких незалежно вибраний з гідвищезазначених гетероциклів може бути необов'ярокси, С1-4алкілу, С1-4алкілокси, С1-4алкілкарбонілу, зково заміщений одним або, якщо припустимо, піперидинілу, NR12R13, C(=O)-Z-R14, R6 та С1-4 алкідвома чи трьома замісниками, кожен з яких незалу, заміщеного одним або двома замісниками, лежно вибраний з Het2, R11 та С1-4алкілу, необов'янезалежно обраними з гідрокси, карбоніл С1-4 алкізково заміщеного одним або більше замісниками, локси, фенілу, C(=O)-Z-R14, -Y-С1-4алкандіїл-С(=О)незалежно вибраними з Het2 та R11. 14 6 12 13 2-R ,R тa NR R ; однак за умов, що Het4 представлений тричленним, чотиричлен- R2 відмінний від С1-6алкілоксикарбоніл ним, п'ятичленним або шестичленним ароматичС1-6алкілу або амінокарбонілу та ним або неароматичним моноциклічним гетероци- R7, R8, R9 та R10 відмінні від амінокарбонілу, клом, який містить один або більше, переважно від С1-4алкілкарбонілокси-С1-4алкілкарбонілу, гідрокодного до чотирьох, гетероатомів, здебільшого сиС1-4алкілкарбонілу, С1-4 алкілоксикарбонілкарбообраних з азоту, кисню, сірки та фосфору; до зразнілу, C(=O)-O-R19, С1-4алкандіїлС(=О)-О-R19 або -Yків цих гетероциклів належать, але не обмежуютьС1-4алкандіїлС(=О)-О-R19 та ся ними, наприклад, пірроліл, імідазоліл, піразоліл, - R12 та R13 відмінні від С1-4 алкілкарбонілоктріазоліл, тетразоліл, фураніл, тієніл, оксазоліл, сиС1-4алкілкарбонілу, гідроксиС1-4 алкілкарбонілу ізоксазоліл, тіазоліл, ізотіазоліл, тіадіазоліл, оксаабо С1-4алкілкарбонілкарбонілу та діазоліл, піридиніл, піримідиніл, піразиніл, піраніл, - R11 відмінний від C(=O)-O-R19, -Y-С1-4 алкандіпіридазиніл та тріазиніл; їл-С(=О)-OR19, C(=O)NH2, С(=О)NHCI-4 алкілу або 5 Het представлений тричленним, чотиричленС(=О)NНС3-7циклоалкілу та ним, п'ятичленним або шестичленним ароматич- R15 та R16 відмінні від амінокарбонілу, С1-4 алним або неароматичним, моноциклічним або полікілкарбонілоксиС1-4алкілкарбонілу, гідрокси С1-4 циклічним гетероциклом, який містить один або алкілкарбонілу або С1-4алкілоксикарбонілбільше, переважно від одного до чотирьох, гетекарбонілу та роатомів, здебільшого обраних з азоту, кисню, - арил відмінний від фенілу, заміщеного C(=O)сірки та фосфору, або замкнуту поліциклічну кільO-R19, C(=O)NH2, C(=O)NHC1-4алкілом, цеву систему, до складу якої входить вказаний С(=О)NНС3-7циклоалкілом та/або С1-4алкілом, загетероцикл (наприклад, замкнутий бензогетероміщеним C(=O)-O-R19 або Y-С1-4алкандіїл-С(=О)-Оцикл); до зразків подібних гетероциклів належать, R14 та але не обмежуються ними, наприклад, пірроліл, - Het3 відмінний від моноциклічного гетероцикпирролініл, імідазоліл, імідазолініл, піразоліл, піралу, заміщеного C(=O) O-R19 та/або С1-4алкілом, 19 золініл, тріазоліл, тетразоліл, фураніл, тетрагідзаміщеним C(=O)-O-R та/або Y-С1-4алкандіїл 19 рофураніл, тієніл, тіоланіл, діоксоланіл, оксазоліл, C(=O)-O-R та оксазолініл, ізоксазоліл, тіазоліл, тіазолініл, ізотіа- у кожній з вищеперерахованих умов R19 золіл, тіадіазоліл, оксадіазоліл, піридиніл, піриміпредставляє собою водень, C1-4алкіл, диніл, піразиніл, піраніл, піридазиніл, пірролідиніл, С3-7циклоалкіл, амінокарбонілметилен або монопіперидиніл, піперазиніл, морфолініл, тіоморфолічи ді(С1-4алкіл)-амінокарбонілметилен та ніл, тетрагідропіраніл, діоксаніл, дитіаніл, тритіау яких вищезазначена сполука, що відповідає ніл, тріазиніл, бензотієніл, ізобензотієніл, бензоформулі (І), містить принаймні одну -C(=O)-Z-R14 фураніл, ізобензофураніл, бензотіазоліл, складову. бензоксазоліл, бензодіоксаніл, індоліл, ізоіндоліл, Вищеперераховані визначення, які використоіндолініл, пуриніл, 1Н-піразоло[3,4-d]піримідиніл, вуватимуться і надалі: бензімідазоліл, хіноліл, ізохіноліл, циннолініл, - термін "гало" використовується для познафталазиніл, хіназолініл, хіноксалініл, тіазолопіричення радикалів фтору, хлору, брому та йоду; диніл, оксазолопіридиніл та імідазо[2,1-b]тіазоліл; - термін "С3-7циклоалкіл" є загальним познав яких кожен з вищезазначених гетероциклів ченням сполук циклопропіл, циклобутил, циклопеокремо може необов'язково бути заміщений, де нтил, циклогексил та циклогептил; можливо, одним, двома, трьома або чотирма замі- терміном "С1-4алкіл" визначено нерозгалужесниками, кожен з яких незалежно вибраний з гідний або розгалужений ланцюг насичених вуглеворокси, меркапто, карбонілу, С1-4алкілу, С1-4 алкілодневих радикалів, які містять від 1 до 4 атомів вугкси, С1-4алкілтіо, С1-4алкілкарбонілу, піперидинілу, лецю, як, наприклад, метил, етил, пропіл, бутил, 1NR17R18, C(=O)-Z-C1-6алкілу, R6, сульфонамідо та метилетил, 2-метилпропіл, 2,2-диметилетил та С1-4алкілу, заміщеного одним або двома замісниподібні до них; ками, незалежно вибраними з гідрокси, С1-4 алкіло- термін "С1-6циклоалкіл" використовується для кси, меркапто, С1-4алкілтіо, фенілу, C(=O)-Z-C1-6 позначення С1-4алкільних та вищих гомологічних алкілу, -Y-C1-4алкандіїл-С(=О)-Z-С1-6алкілу, R6 сполук, що містять 5 або 6 атомів вуглецю, напри17 18 TaNR R ; клад, пентил, 2-метилбутил, гексил, 2Het6 представлений тричленним, чотиричленметилпентил та подібних до них; ним, п'ятичленним або шестичленним ароматич- термін "С1-20алкіл" використовується для позним або неароматичним моноциклічним гетероциначення С1-6алкілільних та вищих гомологічних клом, який містить один або більше, переважно від сполук, що містять від 7 до 20 атомів вуглецю, як, одного до чотирьох, гетероатомів, здебільшого наприклад, гептил, октил, ноніл, децил, ундецил, обраних з азоту, кисню, сірки та фосфору; до зраздодецил, тридецил, тетрадецил, пентадецил, окків цих гетероциклів належать, але не обмежуютьтадецил, нонадецил, ейкозил та подібних до них; ся ними, наприклад, пірролідиніл, піперидиніл, - термін "С5-20алкіл" призначений для 17 74791 18 С1-20алкільних сполук за виключенням С1-4алкілу; алкандіїлові радикали із розгалуженим або нероз- терміном "С3-20алкеніл" позначені розгалужегалуженим ланцюгом, які містять від 2 до 6 атомів ні та нерозгалужені ланцюги вуглеводневих радивуглецю, як, наприклад, 1,2-етандіїл, 1,3калів, які мають один подвійний зв'язок та містять пропандіїл, 1,4-бутандіїл, 1,5-пентандіїл, 1,6від 3 до 20 атомів вуглецю, як, наприклад, 2гександіїл та подібні до них. 1 2 3 4 5 пропеніл, 3-бутеніл, 2-бутеніл, 2-пентеніл, 3Позначення Het , Het , Het , Het та Het вклюпентеніл, 3-метил-2-бутеніл, 3-гексеніл та подібні чають всі можливі ізомерні форми гетероциклів, до них, атом вуглецю згаданих С3-20алкенільних означених у вищенаведених визначеннях, наприсполук, зв'язаний із залишком молекули, переважклад, пірроліл також вміщує 2Н-пірроліл; тріазоліл но насичений; включає 1,2,4-тріазоліл та 1,3,4-тріазоліл; оксадіа- терміном "С3-20алкініл" позначені розгалужезоліл включає 1,2,3-оксадіазоліл, 1,2,4ний та нерозгалужений ланцюги вуглеводневих оксадіазоліл, 1,2,5-оксадіазоліл та 1,3,4радикалів, які мають один потрійний зв'язок та оксадіазоліл; тіадіазоліл включає 1,2,3-тіадіазоліл, містять від 3 до 20 атомів вуглецю, як, наприклад, 1,2,4-тіадіазоліл, 1,2,5-тіадіазоліл та 1,3,42-пропініл, 3-бутиніл, 2-бутиніл,2-пентиніл, 3тіадіазоліл; піраніл включає 2Н-піраніл та 4Нпентиніл, 3-метил-2-бутиніл, 3-гексиніл та подібні піраніл. до них, атом вуглецю згаданих С3-20алкінільних Гетероцикли, позначені як Het1, Het2, Het3, Het4 сполук, зв'язаний із залишком молекули, переважта Het5, можуть бути приєднані до залишку молено насичений; кули, що описується формулою (1), за допомогою - термін "полігалоС1-4алкіл" визначає полігалобудь-якого відповідного вуглеводневого кільця або заміщений С1-4алкіл, зокрема заміщений С1-4алкіл гетероатому . Таким чином, наприклад, коли гетез 1-6 атомами галогену, частіше діфторо- або роцикл позначений як імідазоліл, він може бути 1трифторометил; імідазолілом, 2-імідазолілом, 4 імідазолілом та 5- термін "полігалоС1-6алкіл" визначає полігалоімідазолілом; коли він позначений як тіазоліл, він заміщений С1-6алкіл; може бути 2-тіазолілом, 4-тіазолілом та 5- термін "полігалоС1-20алкіл" визначає полігатіазолілом; коли він позначений як тріазоліл, він лозаміщений С1-20алкіл; може бути 1,2,4-тріазол-1-ілом, 1,2,4-тріазол-3- термін "С1-4алкандіїл" визначає двохвалентні ілом, 1,2,4-тріазол-5-ілом, 1,3,4-тріазол-1-ілом та алкандіїлові радикали із розгалуженим або нероз1,3,4-тріазол-2-ілом; коли гетероцикл представляє галуженим ланцюгом , які містять від 1 до 4 атомів бензотіазоліл, він може бути 2-бензотіазолілом, 4вуглецю, як, наприклад, метилен, 1,2-етандіїл, 1,3бензотіазолілом, 5-бензотіазолілом, 6пропандіїл, 1,4-бутандіїл та подібні до них; бензотіазолілом та 7-бензотіазолілом. - термін "С2-6алкандіїл" визначає двовалентні С1-20ацил є похідним наступних сполук: оцтова кислота Пропіонова кислота масляна кислота валеріанова кислота гексанова кислота гептанова кислота каприлова кислота нонанова кислота капронова кислота ундецилова кислота лаурилова кислота СН3СООН С2Н5СООН С3Н7СООН С4Н9СООН С5Н11СООН С6Н13СООН С7Н15СООН С8Н17СООН С9Н19СООН С10Н21СООН С11Н23СООН Вищезазначені фармацевтично прийнятні адитивні солі включають терапевтично активні нетоксичні кислі адитивні солі, здатні формувати сполуки, що відповідають формулі (1). Найзручніший спосіб отримання останніх полягає в обробці основних форм вказаними відповідними кислотами - неорганічними кислотами, наприклад галоводневими, такими як соляна, бромоводнева та подібними до них; сірчаною кислотою; азотною кислотою; фосфорною кислотою та подібними до Het ; або органічними кислотами, наприклад, оцтовою, пропіоновою, гідрооцтовою, 2гідропропіоновою, 2-оксопропіоновою, щавелевою, малоновою, бутандікислотою, 2-бутендкислотою, 2-гідроксибутандікислотою, 2,3дигідроксибутандікислотою, 2-гідрокси-1,2,3пропантрикарбоновою, метансульфоновою, етансульфонозою, бензенсульфоновою, 4метилбензенсульфоновою, циклогексансульфамі Трідеканоєва кислота Міристинова кислота Пентадеканова кислота Пальмітинова кислота Гептадеканова кислота Стеаринова кислота олеїнова кислота лінолева кислота Ліноленова кислота Нонадеканова кислота Айкозаноєва кислота С12Н25СООН С13Н27СООН С14Н29СООН С15Н31СООН С16Н33СООН С17Н35СООН С17н33СООН С17Н31СООН С17Н29СООН С18Н37СООН С19Н39СООН новою, 2-гідроксибензойною, 4-аміно-2гідроксибензойною або подібними до них. І навпаки, соль може бути перетворена на вільну основу шляхом обробки лугом. Сполуки, що відповідають формулі (1) та містять кислотні протони, можуть перетворюватись на їх терапевтично активні нетоксичні метало- або аміноформи адитивних солей шляхом взаємодії з відповідними органічними або неорганічними основами. До відповідних основних солей належать, наприклад, солі амонію, солі лужних та лужноземельних металів, наприклад, літію, натрію, калію, магнію, кальцію та подібні до них, солі органічних основ, наприклад, бензатин, N-метил-D-глюкамін, 2-аміно-2-(гідроксиметил)-1,3-пропандіол, гідрабамінові солі та солі природних амінокислот, наприклад, аргініну, лізину та подібні до них. Навпаки, сіль може перетворюватись на вільну кислотну форму шляхом взаємодії з кислотою. Поняття 19 74791 20 адитивна соль представлено також гідратами та ний C(=O)-Z-R14, С1-6алкілсульфонілокси, С3-7 цикрозчинними формами цих солей, які здатні форлоалкіл, необов'язково заміщений C(=O)-Z-R14, мувати сполуки, що відповідають формулі (1). арил, арилокси, арилтіо. Het1, Het1-окси та Het1-тio; Прикладами цих форм можуть виступати гідрати, та якщо X представлений О, S або NR5, тоді R2 алкоголяти та подібні до них. може також представляти амінотіокарбоніл, С1-4 14 N-оксиди представлених сполук включають алкіл карбоніл, можливо, заміщений C(=О)-Z-R , речовини, що відповідають формулі (1), в яких С1-4алкілтіокарбоніл, необов'язково заміщений один або декілька атомів азоту окислені до так C(=О)-Z-R14, арилкарбоніл, арилтіокарбоніл, Het1званої N-оксидної форми. Наприклад, один або карбоніл або Het1-тіокарбоніл; найбільш бажано, більше атомів азоту в будь-якому з гетероциклів, щоб R2 був представлений Het1; означених як Het1, Het2, Het3, Het4 та Het5, можуть - R3 представляє водень, метил, етил, пропіл бути N-окислені. або циклогексил, найбільш бажано - метил; Деякі із сполук, що відповідають формулі (1), - R4 представляє водень або метил, найбільш можуть також існувати у вигляді своїх таутомерних бажано - метил; форм. Хоча ці форми явно не наведені у вищеза- R3 тa R4 разом формують 1,4-бутандіїл; значеній формулі, вважається ,що вони належать - R6 представляє С1-6алкілсульфоніл, аміносудо об'єктів даного винаходу. Наприклад, складова льфоніл або Неt6сульфоніл, найбільш бажано гідроксизаміщеного тріазину може існувати у виНеt6сульфоніл; гляді тріазинонової складової складова гідрокси- кожен з paдикaлiв R7 та R8 незалежно предзаміщеного піримідину також існувати у вигляді ставлений воднем, С1-4алкілом, Het3 або R6; піримідинонової складової. - кожен з радикалів R9 та R10 незалежно предТерміном "стереохімічні ізомерні форми", який ставлений воднем, С1-4алкілоксиС1-4алкілом, амізгадувався раніше, описуються всі можливі стенокарбонілом, Het3 карбонілом, Het3 або R6; реоізомерні форми, в яких можуть існувати сполу- R11 представляє ціано, нітро, гало, С1-4 алкіки, що відповідають формулі (1). Якщо не вказано локси, форміл, NR7R8, C(=O)NR15R16, -C(=O)-Z-R14, інакше, то хімічне позначення сполуки означає арил, арилкарбоніл, Het3 або C(=O)Het3; найбільш суміш всіх можливих стереохімічних ізомерних бажано, щоб R11 був представлений фенілом, форм, ця суміш містить всі діастереомери та енанC(=O)-O-R14, -C(=O)-S-R14 або C(=O)-NH-R14. тіомери основної молекулярної структури. Зокре- кожен радикал R11 був незалежно вибраний з ма, стереогенні центри можуть мати R- або Sгідрокси, меркапто, ціано, нітро, гало, тригаломеконфігурацію, позначення яких наводиться у відтилу, С1-4алкілокси, можливо заміщеного C(=O)-Zповідності до Узагальненої Хімічної номенклатури. R14, С1-6алкілтіо, необов'язково заміщеного C(=O)14 Цей винахід обов'язково вміщує стереохімічні ізоZ-R , формілу, тригалоС1-4алкілсульфонілокси, 6 мерні форми сполук, що відповідають формулі (1). R , NR7R8, C(=O)NR15R16, -C(=O)-Z-R14, Сполуки, які відповідають формулі (1), та деякі -Y-С1-4алкандіїл-С(=О)-Z-R14, арилу, арилокси, проміжні продукти, що описуються в даному винаарилкарбонілу, арилтіокарбонілу, С3-7циклоалкілу, ході, містять один або більше асиметричних атонеобов'язково заміщеного C(=O)-Z-R14, мів вуглецю. Чисті стереоізомери та суміші стереС3-7циклоалкілокси, необов'язково заміщеного охімічних ізомерних форм сполук, що відповідають C(=О)-Z-R14, С3-7циклоалкілтіо, можливо заміщеноформулі (1), також входять до даного винаходу. го C(=О)-Z-R14, фталімід-2-ілу, Het3, C(=O)Het , Далі по тексту термін "сполука, що відповідає фоC(=O)C1-4алкілу, можливо заміщеного одним або рмулі (1)" включає також її N-оксидні форми, фардвома замісникам, незалежно обраними з гідрокмацевтично прийнятні адитивні солі та стереоізоси, меркапто, гало та фенілу; мерні форми. - R14 представляє дігідрофураніл, С5-20алкіл, Цікавою групою сполук, які відповідають форС3-20алкеніл, полігалоС1-6алкіл, Неt5, радикал формулі (1), є така, де складова 6-азаурацилу зв'язана мули (а) або С1-20алкіл заміщений одним або більз фенільним кільцем та знаходиться в пара- або ше замісниками, вибраними з наступних: феніл, мета-положенні відносно атому вуглецю, до якого С1-4алкіламіно, ціано, Het1, Het5, гідрокси та 2 3 4 приєднані замісники -X-R , R та R , здебільшого С3-7циклоалкілу, найбільш бажаним є радикал фов пара- положенні. До іншої цікавої групи належать рмули (а) ,в якому Rj є С1-6алкілом та s дорівнює 2, ті сполуки формули (І), які мають наступні обмеабо С1-20алкілом, заміщеним гідрокси або Het5; ження: - R17 та R18 незалежно представлені воднем - p представлений 0, 1 або 2; або фенілом; - X представлений S, NR5 чи прямим зв'язком; - арил являє собою феніл, необов'язково занайкраще - прямим зв'язком; міщений одним, двома або трьома замісниками, - кожний радикал R1 незалежно представляє кожен з яких незалежно обраний з нітро, ціано, гало, полігалоС1-6алкіл, С1-6алкіл, С1-6алкілокси або гало, гідрокси, С1-4алкілу, С3-7циклоалкілу, арил, бажано хлоро- або трифторометил, краще С1-4алкілокси, формілу, полігалоС1-4алкілу, NR9R10, хлоро; C(=O)NR9R10, C(=O)-O-R14, -O-R6, фенілу, 14 3 1-4 - як мінімум одна складова -C(=O)-Z-R , що C(=O)Het та С алкілу, заміщеного одним або міститься у сполуці, яка відповідає формулі (1), більше замісниками, кожен з яких незалежно вибутворена радикалом R2, раний з гало, гідрокси, С1-4алкілокси, C(=O)-O-R14, 2 1 - R являє собою Het або С1-6алкіл, заміщений Het3 тa NR9R10; одним або двома замісниками, вибраними з гідро- Het1 представляє моноциклічний гетероцикл, кси, ціано, аміно, моно- або ді(С1-4алкіл)аміно, вибраний з наступних: пірроліл, імідазоліл, піразоC(=O)-Z-R14, С1-6алкілокси, необов'язково заміщеліл, тріазоліл, тетразоліл, фураніл, тієніл, оксазо 21 74791 22 ліл, ізоксазоліл, тіазоліл, ізотіазоліл, тіадіазоліл, рема R2 може бути заміщений тіазолілом, піридиоксадіазоліл, піридиніл, піримідиніл, піразиніл, нілом або оксадіазолілом. піраніл, піридазиніл та тріазиніл, зокрема імідазоБажаними є сполуки, які відповідають формулі ліл, оксадіазоліл, тріазоліл, піримідиніл або піри(1), де обидва радикали R3 та R4 представлені мединіл, в яких кожен з вищезгаданих моноциклічних тилом та -X-R2 є Het1, де Het1 можливо заміщений гетероциклів незалежно може необов'язково бути тіазолілом, піридинілом або оксадіазолілом. заміщеним одним або, якщо можливо, двома чи Більш бажаними є сполуки, які відповідають трьома замісниками, незалежно вибраними з Het2, формулі (1), де обидва радикали R3 та R4 предR11 та С1-4алкілу, можливо заміщеного Het2 або ставлені метилом та -X-R2 можливо заміщений 211 1 R ; більш бажано, щоб Het був представлений тіазолілом або 3-оксадіазолілом, складова 6імідазолілом, оксадіазолілом, тіазолілом або піриазаурацилу знаходиться у парапозиції по віднодинілом, особливо тіазолілом, кожен з яких незашенню до атому вуглецю, до якого приєднані замілежно може бути заміщений одним або, при можсники -X-R2, R3 та R4, а р дорівнює 2, внаслідок ливості, двома чи трьома замісниками, з яких чого обидва замісники R1 є хлоро та знаходяться в 2 11 кожен незалежно вибраний з Het , R та С1-4 алкіортопозиції відносно атому вуглецю, до якого прилу, можливо заміщеного Het2 або R11, найбільш єднані замісники -X-R2, R3 та R4. Зокрема, найбажано - двома замісниками, кожен з яких незалебільш бажаними є ті сполуки, в яких-X-R2 двозаміжно вибраний з R11 та С1-4алкілу, заміщеного R11; щені фенілом та або (і) R11, де R11 представлений 2 - Het представляє ароматичний гетероцикл; групою -C(=O)-Z-R14, в якій Ζ представлений О, a зокрема фураніл, тієніл, піридиніл або бензотієніл, R14 є С1-20алкілом, заміщеним гідрокси або Неt5, де кожен із згаданих ароматичних гетероциклів особливо де Het5 являє собою піперазиніл, замінезалежно може бути заміщений одним або, за щений Неt6сульфонілом, особливо де Неt6 є пірможливості, двома чи трьома замісниками, кожен з ролідинілом, або R14 представлений радикалом, 11 яких незалежно вибраний з R та С1-4алкілу; що відповідає формулі (а), в якому Rj є С1-6 алкі- Het3 представлений піперидинілом, піперазилом, a s дорівнює 2, або (іі) С1-4алкілом, заміщенілом, морфолінілом або тетрагідропіранілом, коним R11, де R11 представлений групою -С(=О)-Zжен з яких незалежно заміщається, де можливо, R14, в якій Ζ є О, a R14 являє собою радикал, що одним, двома, трьома або чотирма замісниками, з описується формулою (а), де Rj є C1-6алкіл, a s яких кожен незалежно вибраний з гідрокси, дорівнює 2. С1-4алкілу, С1-4алкілкарбонілу, піперидинілу та Найбільш переважними речовинами є наступС1-4алкілу, заміщеного одним чи двома замісникані, які описуються нижченаведеними формулами ми, незалежно обраними з гідрокси, (А), (В), (С) та (D): С1-4алкілокси та фенілу; - Het4 представлений тієнілом; - Het5 представлений піперидинілом або піперазинілом, необов'язково заміщеним С1-4алкілом, сульфонамідо або R6, найбільш бажано - R6; - Het6 представлений пірролідинілом. В окремих речовинах, які належать до сполук, що відповідають формулі (1), р представлене числом 2 та обидва замісники R1 представлені хлоро-; найбільш бажано, якщо два хлорних замісники знаходяться в ортопозиції відносно атому вуглецю, до якого приєднані замісники -X-R2, R3 та R4. В інших окремих речовинах, що належать до сполук, які відповідають формулі (1), складова 6азаурацилу знаходиться в парапозиції відносно атому вуглецю, до якого приєднані замісники -XR2, R3 та R4, а р представлене числом 2, внаслідок чого обидва замісники R1 є хлоро- та знаходяться в ортопозиції відносно атому вуглецю, до якого приєднані замісники -X-R2, R3 та R4. В інших окремих речовинах, що належать до сполук формули (1), X представлений прямим зв'язком, a R2 є моноциклічним гетероциклом, вибраним з пірролілу, імідазолілу, піразолілу, тріазолілу, тетразолілу, фуранілу, тієнілу, оксазолілу, ізоксазолілу, тіазолілу, ізотіазолілу, тіадіазолілу, оксадіазолілу, піридинілу, піримідинілу, піразинілу, піранілу, піридазинілу та тріазинілу, зокрема імідазолілу, оксадіазолілу, тіазолілу, піримідинілу та піридинілу, в яких кожен з вищезгаданих моноциклічних гетероциклів може бути заміщеним одним або, де можливо, двома чи трьома замісниками, Прикладами сполук, які відповідають формулі кожен з яких незалежно вибраний з Het2, R11 та (І), в подальшому включають сполуки, що описуС1-4алкілу, можливо заміщеного Het2 або R11; зок 23 74791 24 1 2 3 4 5 бонілу, Неt3амінокарбонілу, Het3 амінотіокарбоніються формулою (l ), де р, Х, У, R , R , R , R , R , лу, С3-7циклоалкілу, піридиніл R6, R7, R8, R9, R10, R11, R12, R13, R14, n, m, Ra, Rb, Rc, С1-4алкілу, С1-4алкандіїл-С(=О)-Z-R14, -C(=O)-Z-R14, Rd, Re, Rf, Rg, Rh, R15, R16, Z, арил, Het1, Het2, Het3, 4 -Y-С1-4алкандіїл-С(=О)-Z-R14, Het3, Het4 та R6; Het коли вони використовуються по відношенню кожен з радикалів R9 та R10 незалежно вибрадо сполук, які відповідають формулі (1 ), мають ний з водню, С1-4алкілу, гідроксиС1-4алкілу, дигіднаступні значення: роксиС1-4алкілу, фенілу, фенілС1-4алкілу, Представлений винахід стосується сполук, які С1-4алкілоксиС1-4алкілу, C1-4алкілкарбонілу, фенілмають формулу: карбонілу, Неt3карбонілу, моно- або ді(С1-4 алкіл)аміноС1-4алкілу, феніламінокарбонілу, феніламінотіокарбонілу, Неt3амінокарбонілу, 3 Het амінотіокарбонілу, С3-7циклоалкілу, піридинілС1-4алкілу, С1-4алкандіїл-С(=О)-Z-R14, -C(=O)-ZR14, -Y-С1-4алкандіїл-С(=О)-Z-R14, Het3 та R6; кожен радикал R11 був незалежно вибраний з гідрокси, меркапто, ціано, нітро, гало, тригаломеїх N-оксидів, фармацевтично прийнятних адитилу, С1-4алкілокси, необов'язково заміщеного тивних солей та стереохімічно ізометрних форм, C(=O)-Z-R14, формілу, тригалоС1-4 алкілсульфоніде: локси, R6, NR7R8, C(=O)NR15R16, -C(=O)-Z-R14, -Yp являє собою ціле число 0, 1, 2, 3 або 4; C1-4алкандіїл-C(=O)-Z-R14, арил, арилокси, арилка5 X представлений О, S, NR чи прямим зв'язрбонілу, С3-7циклоалкілу, необов'язково заміщеноком, або радикали X-R2 разом можуть бути предго з C(=O)-Z-R14, С3-7циклоалкілокси, необов'язкоставлені ціаногрупою; во заміщеного C(=O)-Z-R14, фталімід-2-ілу, Het3, Υ представлений О, S, NR5 або S(O)2; Het4 та C(=O)Het3; кожен радикал R1 незалежно представляє кожен з радикалів R12 та R13 незалежно вибC(=O)-Z-R14, С1-6алкіл, гало, полігалоС1-6алкіл, гідраний з водню, С1-4алкілу, гідроксиС1-4алкілу, дигірокси, меркапто, С1-6алкілокси, С1-6алкілтіо, дроксиС1-4алкілу, фенілу, фенілС1-4алкілу, С1-4 алС1-6алкілкарбонілокси, арил, ціано, нітро, Неt3, R6, кілоксиС1-4алкілу, С1-4алкілкарбонілу, 7 8 14 3 NR R або С1-4алкіл, заміщений C(=O)-ZR , Het , фенілкарбонілу, моно- або ді(С1-4алкіл)аміноС1-4 R6 або NR7R8; алкілу, феніламінокарбонілу, феніламінотіокарбоR2 представляє Het1, С3-7циклоалкіл, який монілу, С3-7 циклоалкілу, піридинілС1-4алкілу, С1-4 алже бути заміщений C(=O)-Z-R14, С1-6алкіл або кандіїл-С(=О)-Z-R14, -C(=O)-Z-R14, -Y-С1-4 алкандіїл14 6 С1-6алкіл, заміщений одним або двома замісникаС(=О)-Z-R та R ; ми, вибраними з C(=O)Z-R14, гідрокси, ціано, аміно, кожний радикал R14 незалежно представлений моно- або ді(С1-4алкіл)аміно; С1-6алкілокси, можлиС1-4алкілом, заміщеним одним або більше замісво заміщений C(=O)-Z-R14, никами, вибраними з фенілу, ді- С1-4алкіламіно, С1-6алкілсульфонілокси, С3-7циклоалкіл, можливо ціано, Het1 та С3-7циклоалкілу, воднем, С1-20 аци14 заміщений C(=O)-Z-R , арил, арилокси, арилтіо, лом (з розгалуженою або нерозгалуженою струкHet1, Het1-окси та Het1-тіо; та якщо X представлетурою, з насиченим або ненасиченим вуглеводнений О, S або NR5, тоді R2 може також являти совим ланцюгом, який має у складі від 1 до 20 атомів бою амінотіокарбоніл, С1-4алкілкарбоніл, необов'явуглецю), С1-20алкілом, С3-7циклоалкілом, полігазково заміщений C(=O)-Z-R14, С1-4алкілтіокарбоніл, лоС1-20алкілом або радикалом, що відповідає фо14 можливо заміщений C(=O)-Z-R , арилкарбоніл, рмулі арилтіокарбоніл, Het1-карбоніл або Het1тіокарбоніл; R3 представляє водень, С1-6алкіл або С3-7циклоалкіл; R4 представляє водень, С1-6алкіл або С3-7циклоалкіл; або R3 та R4 разом формують С2-6алкандіїл; R5 представляє водень або С1-4алкіл; кожний радикал R6 окремо представляє С1-6алкілсульфоніл, аміносульфоніл, моно- або ді(С1-4алкіл)аміносульфоніл, моноабо ди(бензил)аміносульфоніл, полігало де n є ціле 0 до 5; С1-6алкілсульфоніл, С1-6алкілсульфініл, феніл кожен з радикалів Ra, Rb, Rc, Rd, Re та Rf незаС1-4алкілсульфоніл, піперазинілсульфоніл, амінолежно представлений воднем, С1-6алкілом або С3-7 піперидинілсульфоніл, піперидиніламіносульфоциклоалкілом; або Re та Rf разом взяті можуть ніл, N-С1-4алкіл-N-піперидиніламіносульфоніл або утворювати -СН2-СН2-, -CH2-CH2-CH2- або -СН2моно- чи ді(С1-4 алкіл)аміноС1-4алкілсульфоніл, СН2-СН2-СН2- або радикал, що описується формукожен з радикалів R7 та R8 незалежно вибрані лою з водню, С1-4алкілу, гідроксиС1-4алкілу, дигідроксиС1-4алкілу, арилу, арилС1-4алкілу, С1-4 алкілоксиС1-4алкілу, С1-4алкілкарбонілу, арилкарбонілу, Het3карбонілу, моно- або ді(С1-4алкіл)аміно С1-4алкілу, ариламінокарбонілу, ариламінотіокар 25 74791 26 бензофураніл, бензотіазоліл, бензоксазоліл, індоліл, ізоіндоліл, індолініл, пуриніл, 1Н-піразоло[3,4d]піримідиніл, бензімідазоліл, хіноліл, ізохіноліл, циннолініл, фталазиніл, квіназолініл, хіноксалініл, тіазолопіридиніл, оксазолопіридиніл та імідазо[2,1b]тіазоліл; в яких кожен з вищезазначених гетероде m є ціле від 0 до 4 циклів окремо може бути необов'язково заміщений кожен Ζ незалежно представлений О, S, NH, одним або, де можливо, двома чи трьома замісниСН2-О- або -CH2-S-, завдяки чому -СН2- приєднаками, кожен з яких незалежно вибраний з R11 та ний до карбонільної групи; С1-4алкілу, необов'язково заміщеного одним або -Z-R14 ,разом взяті, формують радикал, що двома замісниками, незалежно вибраними з R11; описується формулою Het3 представлений моноциклічним гетероциклом, вибраним з наступних: пірролідиніл, піперидиніл, піперазиніл, морфолініл, тіоморфолініл та тетрагідропіраніл; в яких кожен з вищезазначених моноциклічних гетероциклів незалежно може необов'язково бути заміщений, де можливо, одним, кожен з радикалів R15 та R16 незалежно вибдвома, трьома або чотирма замісниками, кожен з раний з дигідроксиС1-4алкілу, арилу, арилС1-4 алкіяких незалежно вибраний з гідрокси, С1-4алкілу, лу, С1-4алкілоксиС1-4алкілу, C(=O)-O-R14, арилкарС1-4алкілокси, С1-4алкілкарбонілу, піперидинілу, бонілу; моно- або ді(С1-4алкіл)аміноС1-4алкілу, NR12R13, C(=O)-Z-R14, R6 та С1-4алкілу, заміщеного 3 ариламінокарбонілу, ариламінотіокарбонілу, Het одним або двома замісниками, незалежно вибраамінокарбонілу; Неt3амінотіокарбонілу; піридиними з гідрокси, С1-4алкілокси, фенілу, C(=O)-ZнілС1-4алкілу; Het3 та R6; амінокарбонилметилену R14, -Y-С1-4алкандіїл-С(=O)-Z-R14, R6 та NR12R13; або моно- чи ді(С1-4 алкіл)амінокарбонилметилену; Het4 представлений моноциклічним гетероциарил представляє феніл, можливо заміщений одклом, вибраним з наступних: пірроліл, імідазоліл, ним, двома або трьома замісниками, кожен з яких піразоліл, тріазоліл, тетразоліл, фураніл, тієніл, незалежно вибраний з нітро, азидо, ціано, гало, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, тіадіагідрокси, С1-4 алкілу, С3-7циклоалкілу, С1-4алкілокси, золіл, оксадіазоліл, піридиніл, піримідиніл, піразиформілу, полігалоС1-4алкілу, NR9R10, C(=O)NR9R10, ніл, піраніл, піридазиніл та тріазиніл, однак за C(=O)-O-R14, R6, -O-R6, фенілу, Het3, C(=O)Het3 та умов, що: С1-4 алкілу, заміщеного одним або більше замісни- R2 відмінний від C1-6 алкілоксикарбонілС1-6 ками, кожен з яких незалежно вибраний з гало, алкілу, амінокарбонілу та гідрокси, С1-4 алкілокси, C(=O)-O-R14, -Y-С1-4 алкан- R7, R8, R9 та R10 відмінні від амінокарбонілу, діїл-С(=О)-Z-R14, Het3 або NR9R10; Het1 представС1-4алкілкарбонілокси-С1-4алкілкарбонілу, гідрокси ляє гетероцикл, вибраний з наступних: пірроліл, С1-4алкілкарбонілу, С1-4алкілоксикарбонілкарбоніл пирролініл, імідазоліл, імідазолініл, піразоліл, піраC(=O)-O-R14, С1-4алкандіїлС(=О)-О-R14 та -Y-С1-4 золініл, тріазоліл, тетразоліл, фураніл, тетрагідалкандіїлС(=О)-О-R14 ;та рофураніл, тієніл, тіоланіл, діоксоланіл, оксазоліл, - R12 та R13 відмінні від С1-4алкілкарбонілоксиоксазолініл, ізоксазоліл, тіазоліл, тіазолініл, ізотіаС1-4алкілкарбонілу, гідрокси С1-4алкілкарбонілу, золіл, тіадіазоліл, оксадіазоліл, піридиніл, піриміС1-4алкілкарбонілкарбонілу ;та диніл, піразиніл, піраніл, піридазиніл, пірролідиніл, - R11 відмінний від C(=O)-O-R14, Y-С1-4 алкандіпіперидиніл, піперазиніл, морфолініл, тіоморфоліїл-С(=O)-OR14, C(O)NH2, C(=O)NHC1-4алкілу або ніл, діоксаніл, дитіаніл, тритіаніл, тріазиніл, бензоС(=О)NНС3-7циклоалкілу ;та тієніл, ізобензотієніл, бензофураніл, ізобензофу- R14 відмінний від водню, С1-4алкілу, С3-7 цикраніл, бензотіазоліл, бензоксазоліл, індоліл, поалкілу, амінокарбонілметилену, моно- або ді ізоіндоліл, індолініл, пуриніл, 1H-піразоло[3,4(С1-4алкіл)амінокарбонілметилену у випадку, якщо d]піримідиніл, бензімідазоліл, хіноліл, ізохіноліл, Ζ дорівнює 0; та циннолініл, фталазиніл, хіназолініл, хіноксалініл, - R15 та R16 відмінні від амінокарбонілу, тіазолопіридиніл, оксазолопіридиніл та імідазо[2,1С1-4алкілкарбонілоксиС1-4алкілкарбонілу, гідрокси b]тіазоліл; в яких кожен з вищезазначених гетероС1-4алкілкарбонілу або Смалкілоксикарбонілкарциклів може бути необов'язково заміщений одним бонілу ;та або, коли це можливо, двома або трьома замісни- арил відмінний від фенілу, заміщеного C(=O)ками, кожен з яких незалежно вибраний з Het2, R11 O-R14 C(=O)NH2, C(=O)NHC1-4алкілом, С(=O)NHС3та С1-4алкілу, необов'язково заміщеного одним або та/або С1-4алкілом, заміщеним 7циклоалкілом двома замісниками, незалежно вибраними з Het2 C(=O)-O-R14 або Y-С1-4алкандіїл-С(=О)-О-R14 ;та та R11; - Het3 відмінний від моноциклічного гетероцик2 Het являє собою гетероцикл, вибраний з налу, заміщеного C(=O) O-R14 та/або С1-4алкілом, ступних: пірроліл, пирролініл, імідазоліл, імідазолізаміщеним C(=O)-O-R14 та/або Y-С1-4алкандіїл 14 ніл, піразоліл, піразолініл, тріазоліл, тетразоліл, (=O)-O-R ;та фураніл, тетрагідрофураніл, тієніл, тіоланіл, діок- Згадані сполуки, що описуються формулою соланіл, оксазоліл, оксазолініл, ізоксазоліл, тіазо(І), містять принаймні одну складову -C(=O)-Z-R14. ліл, тіазолініл, ізотіазоліл, тіадіазоліл, оксадіазоУ цікавлячій групі сполук, які відповідають фоліл, піридиніл, піриміідиніл, піразиніл, піраніл, рмулі (l ), складова 6-азаурацилу зв'язана з феніпіридазиніл, діоксаніл, дитіаніл, тритіаніл, тріазильним кільцем та знаходиться в пара- або метапоніл,бензотієніл, ізобензотієніл, бензофураніл, ізозиції відносно атому вуглецю, до якого приєднані 27 74791 28 замісники -X-R2, R3 та R4, здебільшого -в парапоніл, в яких кожен з вищезгаданих моноциклічних зиції. гетероциклів незалежно може необов'язково бути Наступні сполуки відповідно до винаходу вмізаміщеним одним або, де можливо, двома чи трьома замісниками, незалежно вибраними з Het2, щують такі за формулою (l ) ,які мають одне або R11 та С1-4алкілу, необов'язково заміщеного Het2 більше нижченаведених обмежень: 11 1 або R ; найбільш бажано, щоб Het був представ- p має значення 0, 1 або 2; 5 лений імідазолілом, оксадіазолілом, тіазолілом - X представлений S, NR чи прямим зв'язком; або піридинілом, кожен з яких незалежно необозокрема ΝΗ або прямим зв'язком; в'язково заміщений одним або, де можливо, двома - кожний радикал R1 незалежно представляє чи трьома замісниками, з яких кожен незалежно гало, полігалоС1-6алкіл, С1-6алкіл, C1-6алкілокси або вибраний з Het2, R11 та С1-4алкілу, необов'язково арил, бажано хлоро- або трифторометил, краще заміщеного Het2 або R11; хлоро-; 2 1 - Неt2 представляє ароматичний гетероцикл; - R представляє Het або С1-6алкіл, заміщений зокрема фураніл, тієніл, піридиніл або бензотієніл, одним або двома замісниками, вибраними з гідроде кожен із згаданих ароматичних гетероциклів кси, ціано, аміно, моно- або ді(С1-4алкіл)аміно, незалежно може необов'язково бути заміщений C(=O)-Z-R14, С1-6алкілокси, необов'язково заміщеодним або, за можливості, двома чи трьома замісний C(=O)-Z-R14, С1-6алкілсульфонілокси, С314 никами, кожен з яких незалежно вибраний з R11 та 7циклоалкіл, необов'язково заміщений C(=O)-Z-R , 1 1 1 С1-4алкілу; арил, арилокси, арилтіо, Het , Неt окси та Нet тіо; - Het3 представлений піперидинілом, піперазита якщо X представлений О, S або NR3, тоді R2 нілом, морфолінілом або тетрагідропіранілом, коможе також представляти амінотіокарбоніл, жен з яких незалежно необов'язково заміщається, С1-4алкілкарбоніл, необов'язково заміщений C(=O)якщо можливо, одним, двома, трьома або чотирма Z-R14, С1-4алкілтіокарбоніл, необов'язково заміщезамісниками, з яких кожен незалежно вибраний з ний С(=О)-Z-R14, арилкарбоніл, арилтіокарбоніл, гідрокси, С1-4алкілу, С1-4алкілкарбонілу, піперидиНеt1-карбоніл або Het1-тіокарбоніл; зокрема R2 нілу та С1-4алкілу, заміщеного одним чи двома запредставлений Het1 або у випадку, коли X предмісниками, незалежно вибраними з гідрокси, ставлений NH, R2 може також бути амінотіокарбоС1-4алкілокси та фенілу; нілом або Неt1карбонілом; - Het4 представлений тієнілом. - R3 представляє водень, метил, етил, пропіл або циклогексил, найбільш бажано - метил; До спеціальних сполук формули (l ), належать - R4 представляє водень або метил, найбільш ті, де p дорівнює 2 та обидва замісники R1 є хлоробажано - метил; ; найбільш бажано, щоб обидва хлорних замісники 3 4 - R та R , разом взяті, формують 1,4знаходились в ортопозиції відносно атому вуглебутандіїл; цю, до якого приєднані замісники -X-R2, R3 та R4. 6 - R представляє С1-6алкілсульфоніл або аміОкремими речовинами, які належать до сполук носульфоніл; формули (l ) є ті, в яких складова 6-азаурацилу - кожен з радикалів R7 та R8 незалежно предзнаходиться в парапозиції відносно атому вуглеставлений воднем, С1-4алкілом, Неt3 або R6; цю, до якого приєднані замісники -X-R2, R3 та R4, а 9 10 - кожен з радикалів R та R незалежно предр дорівнює 2, внаслідок чого обидва замісники R1 є ставлений воднем, С1-4алкілоксиС1-4алкілом, С1-4 хлоро- та знаходяться в ортопозиції по відношеналкілкарбонілом, амінокарбонілом, Неt3 карбоніню до атому вуглецю, до якого приєднані заміснилом, Het3 або R6; ки -X-R2, R3 та R4. - R11 представляє ціано, нітро, гало, С1-4 алкіВ інших окремих речовинах, які належать до локси, форміл, NR7R8, C(=O)NR15R16, -C(=O)-Z-R14, сполук формули (l ), Χ представлений прямим арил, арилкарбоніл, Het3, Het4 та C(=O)Het3; зв'язком, a R2 є моноциклічним гетероциклом, ви- R14 представляє дігідрофураніл, С5-20алкіл, браним з наступних: пірроліл, імідазоліл, піразоС1-4алкіл, заміщений одним або більше замісникаліл, тріазоліл, тетразоліл, фураніл, тієніл, оксазоми, вибраними з наступних: феніл, С1-4алкіламіно, ліл, ізоксазоліл, тіазоліл, ізотіазоліл, тіадіазоліл, ціано, Het1 та С3-7циклоалкіл; оксадіазоліл, піридиніл, піримідиніл, піразиніл, - арил представляє феніл, необов'язково запіраніл, піридазиніл та тріазиніл, зокрема імідазоміщений одним, двома або трьома замісниками, ліл, оксадіазоліл, тіазоліл, піримідиніл або піридикожен з яких незалежно обраний з нітро, ціано, ніл, в яких кожен з вищезгаданих моноциклічних гало, гідрокси, С1-4алкілу, С3-7циклоалкілу, гетероциклів незалежно може необов'язково бути С1-4алкілокси, формілу, полігалоС1-4алкілу, NR9R10, заміщеним одним або, де можливо, двома чи C(=O)NR9R10, C(=O)-O-R14, -O-R6, фенілу, трьома замісниками, незалежно вибраними з Het2, C(=O)Het3 та С1-4алкілу, заміщеного одним або R11 та С1-4алкілу, необов'язково заміщеного Het2 більше замісниками, кожен з яких незалежно вибабо R11; зокрема, R2 представлений тіазолілом, раний з гало, гідрокси, С1-4алкілокси, C(=O)-O-R14, піридинілом або оксадіазолілом, можливо заміщеHet3 та NR9R10; ним. 1 - Het представляє моноциклічний гетероцикл, Більш бажаними речовинами, що належать до вибраний з наступних: пірроліл, імідазоліл, піразосполук формули (l ), є ті, де обидва радикали R3 та ліл, тріазоліл, тетразоліл, фураніл, тієніл, оксазоR4 представлені метильними групами, a -X-R2 явліл, ізоксазоліл, тіазоліл, ізотіазоліл, тіадіазоліл, ляє собою Het1, де Het1 можливо заміщений тіазооксадіазоліл, піридиніл, піримідиніл, піразиніл, лілом, піридинілом або оксадіазолілом. піраніл, піридазиніл та тріазиніл, зокрема імідазоНайбільш переважнимиими речовинами, що ліл, оксадіазоліл, тіазоліл, піримідиніл або піридиналежать до сполук формули (l ), с ті, де обидва 29 74791 30 радикали R3 та R4 є метильними групами, -X-R2 С1-6алкілсульфоніл, С1-6алкілсульфініл, фенілС1-4 можуть бути заміщеними 2-тіазолілом або 3алкілсульфоніл, піперазинілсульфоніл, амінопіпеоксадіазолілом, складова 6-азаурацилу знахоридинілсульфоніл, піперидиніламіносульфоніл, Nдиться у парапозиції по відношенню до атому вугС1-4алкіл-N-піперидиніламіносульфоніл або монолецю, до якого приєднані замісники -X-R2, R3 та R4, чи ді-(С1-4алкіл)аміноС1-4алкілсульфоніл, 1 7 8 а р дорівнює 2, завдяки чому обидва замісники R кожен з paдикaлiв R та R незалежно вибрає хлоро та знаходяться в ортопозиції відносно ний з водню, С1-4алкілу, гідроксиС1-4алкілу, дигідатому вуглецю, до якого приєднані замісники -XроксиС1-4алкілу, арилу, арилС1-4алкілу, С1-4 алкілоR2, R3 та R4. ксиС1-4алкілу, С1-4алкілкарбонілу, арилкарбонілу, Приклади сполук формули (І) в подальшому Het3 карбонілу, моно- або ді(С1-4 алкіл)аміноС1-4 включають сполуки, що описуються формулою алкілу, ариламінокарбонілу, ариламінотіокарбонілу, Неt3амінокарбонілу, Het3амінотіокарбонілу, С3-7 (І ), в якій p, Χ, Υ, R1, R2, R3, R4, R5, R6, R7, R8, R9, 10 11 12 13 14 a b c d e циклоалкілу, піридинілС1-4алкілу, С1-4алкандіїлR , R , R , R , R , m, n, q, r, s R , R , R , R , R , C(=O)-Z-R14, -C(=O)-Z-R14, -Y-С1-4алкандіїл-С(=О)Rf, Rg, Rh, Rk, Ri, Rj, Rm, Rn, R15, R16, R17, R18, Ζ, 1 2 3 4 5 Z-R14, Het3, Het4 та R6; або R7 та R8, взяті разом з арил, Het , Het , Het , Het , Het так ,як вони викоатомом азоту, до якого вони приєднані, формують ристовуються для описання сполук формули (І ), радикал, що відповідає формулі: мають наступні значення:. Представлений винахід стосується сполук, які мають формулу: її N-оксидів, фармацевтично прийнятних адитивних солей та стереохімічно ізомерних форм, де: p являє собою ціле число 0, 1, 2, 3 або 4; X представлений О, S, NR5 чи прямим зв'язком або радикали -X-R2, разом взяті, можуть бути представлені ціаногрупою; Υ представлений О, S, NR5 або S(O)2; кожний радикал R1 незалежно представляє C(=O) Z-R14, С1-6алкіл, гало, полігалоС1-6алкіл, гідрокси, меркапто, С1-6алкілокси, С1-6алкілтіо, С1-6алкілкарбонілокси,арил, ціано, нітро, Het3, R6, NR7R8 або С1-4алкіл, заміщений C(=O)-Z-R14, Het3, R6 або NR7R8; R2 представляє Het1, С3-7циклоалкіл, можливо заміщений C(=O)-Z-R14, С1-6алкіл або С1-6алкіл, заміщений одним або двома замісниками, вибраними з C(=O) Z-R14, гідрокси, ціано, аміно, моноабо ді(С1-4алкіл)аміно, С1-6алкілокси, необов'язково заміщений C(=O)-Z-R14, С1-6алкілсульфонілокси, С3-7циклоалкіл, можливо заміщений C(=O)-Z-R14, арил, арилокси, арилтіо, Het1, Het1окси та Нet1тіо; якщо X представлений О, S або NR5, тоді R2 може також являти собою амінотіокарбоніл, С1-4алкілкарбоніл, необов'язково заміщений C(=O)Z-R14, С1-4алкілтіокарбоніл, можливо заміщений C(=O)-Z-R14, арилкарбоніл, арилтіокарбоніл, Неt1карбоніл або Het1тіокарбоніл; R3 представляє водень, С1-6алкіл або С3-7циклоалкіл; R4 представляє водень, С1-6алкіл або С3-7циклоалкіл; або R3 та R4, разом взяті, формують С2-6алкандіїл; R5 представляє водень або С1-4алкіл; кожний радикал R6 окремо представляє С1-6алкілсульфоніл, аміносульфоніл, піперидинілсульфоніл, моно- або ді(С1-4 алкіл)аміносульфоніл, моно- або ди(бензил)аміносульфоніл, полігало кожен з радикалів R9 та R10 незалежно вибраний з водню, С1-4алкілу, гідроксиС1-4алкілу, дигідроксиС1-4алкілу, фенілу, фенілС1-4алкілу, С1-4 алкілоксиС1-4алкілу, С1-4алкілкарбонілу, фенілкарбонілу, Het3карбонілу, моно- або ді(С1-4 алкіл)аміноС1-4алкілу, феніламінокарбонілу, феніламінотіокарбонілу, Het3аміно-карбонілу, 3 Het амінотіокарбонілу, С3-7циклоалкілу, піридинілС1-4алкілу, С1-4алкандіїл-С(=О)-Z-R14, -C(=O)-Z14 14 3 4 6 R , -Y-С1-4алкандіїл-С(=О)-Z-R , Het , Het та R ; 9 10 або R та R , взяті разом з атомом азоту, до якого вони приєднані, формують радикал, що відповідає формулі: кожен радикал R11 був незалежно вибраний з гідрокси, меркапто, ціано, нітро, гало, тригалометилу, С1-4алкілокси, необов'язково заміщеного C(=O)-Z-R14, формілу, тригалоС1-4 алкілсульфонілокси, R6, NR7R8, C(=O)NR15R16, -C(=O)-Z-R14, -YC1-4aлкaндiїл-C(=O)-Z-R14, арилу, арилокси, арилкарбонілу, С3-7циклоалкілу, необов'язково заміщеного C(=O)-Z-R14, С3-7 циклоалкілокси, необов'язково заміщеного C(=O)-Z-R14, фталімід-2-іл, Het3 та C(=O)Het3; кожен з радикалів R12 та R13 незалежно вибраний з водню, С1-4алкілу, гідроксиС1-4алкілу, дигідроксиС1-4алкілу, фенілу, фенілС1-4алкілу, С1-4 алкілоксиС1-4алкілу, С1-4алкілкарбонілу, фенілкарбонілу, моно- або ді(С1-4алкіл)аміноС1-4 алкілу, феніламінокарбонілу, феніламінотіокарбонілу, С3-7 циклоалкілу, піридинілС1-4алкілу, С1-4 алкандіїл-С(О)-Z-R14, -C(=O)-Z-R14, -Y-С1-4алкандіїлС(=О)-Z-R14, та R6; або R12 та R13 ,взяті разом із атомом азоту, до якого вони приєднані, формують радикал, що відповідає формулі: 31 кожний радикал R14 незалежно представлений воднем; С1-20ацилом (з розгалуженою або нерозгалуженою структурою, з насиченим або ненасиченим вуглеводневим ланцюгом, який має у складі від 1 до 20 атомів вуглецю), С1-20алкілом, С3-20 алкенілом, необов'язково заміщеним фенілом або С1-20алкілом, заміщеним одним або більше замісниками з наступних: гідрокси, NR17R18, фенілу, моно-або ді(С1-4алкіл)аміно, ціано, Het5, С1-4 алкілоксикарбонілу, фенілС1-4алкілоксикарбонілу та С3-7циклоалкілу, або R14 представляє радикал, що описується формулою де m представляє ціле число від 1 до 4, n - від 0 до 5, q - від 0 до 2, r - від 0 до 2 та s - від 0 до 4; Ra, Rb, Rc, Rd, Re та Rf незалежно представлені воднем, С1-6алкілом, фенілом або С3-7 циклоалкілом або Re та Rf разом можуть утворювати -СН2-СН2-, СН2-СН2-СН2- або -СН2-СН2-СН2-СН2; кожен з радикалів Rg, Rh та Rk незалежно представлений воднем або С1-4алкілом; Ri представлений С1-4алкілом; 74791 32 Rj представлений -O-Rb, С1-6алкілом, фенілом або С3-7циклоалкілом, необов'язково заміщеним С1-4алкілокси; де Rm представлений воднем або С1-4 алкілокси, a Rn є воднем, С1-4алкілом, С3-7 циклоалкілом, фенілом або фенілС1-4алкілом кожний Ζ незалежно представляє О, S, ΝΗ, СН2-О- або -CH2-S-, за допомогою чого -СН2- приєднується до карбонільної групи; або -Z-R14 разом формують радикал, що відповідає формулі: кожен з радикалів R15 та R16 незалежно вибраний з водню, С1-4алкілу, гідроксиС1-4алкілу, дигідроксиС1-4алкілу, арилу, арилС1-4алкілу, С1-4 алкілоксиС1-4алкілу, -C(=O)-Z-R14, арилкарбонілу, моно- або ді(С1-4алкіл)аміноС1-4алкілу, ариламінокарбонілу, ариламінотіокарбонілу, амінокарбонілметилену, моноабо ді(С1-4 алкіл)амінокарбонілметилену, Het3амінокарбонілу, Неt3амінотіокарбонілу, піридинілС1-4алкілу, Het3 або R6; або R15 та R16 ,взяті разом з атомом азоту, до якого вони приєднані, формують радикал, що відповідає формулі: кожен з радикалів R17 тa R18 незалежно вибраний з водню, С1-6алкілу, гідроксиС1-4алкілу, дигідроксиС1-4алкілу, фенілу, фенілС1-4алкілу, С1-4 алкілоксиС1-4алкілу, С1-4алкілкарбонілу, фенілкарбонілу, моно- або ді(С1-4алкіл)аміноС1-4 алкілу, феніламінокарбонілу, феніламінотіокарбонілу, С3-7 циклоалкілу, піридинілС1-4алкілу, С1-4 алкандіїл-С(=О)-Z-С1-6алкілу, -C(=O)-Z-C1-6алкілу, -YC1-4 алкандіїл-С(=О)-Z-С1-6алкілу та R6; арил представлений фенілом, необов'язково заміщеним одним, двома або трьома замісниками, кожен з яких незалежно вибраний з нітро, азидо, ціано, гало, гідрокси, С1-4алкілу, С3-7циклоалкілу, С1-4алкілокси, формілу, полігалоС1-4алкілу, NR9R10, C(=O)NR9R10, C(=O)-Z-R14, R6, -O-R6, фенілу, Het3, C(O)Het3 та С1-4алкілу, заміщеного одним або більше замісниками, кожен з яких незалежно вибраний з гало, гідрокси, С1-4алкілокси, C(=O)-Z-R14, -YС1-4алкандіїл-С(=О)-Z-R14, Het3 або NR9R10; Het представляє гетероцикл, вибраний з наступних сполук: пірроліл, пирролініл, імідазоліл, імідазолініл, піразоліл, піразолініл, тріазоліл, тетразоліл, фураніл, тетрагідрофураніл, тієніл, тіоланіл, діоксоланіл, оксазоліл, оксазолініл, ізоксазоліл, тіазоліл, тіазолініл, ізотіазоліл, тіадіазоліл, оксадіазоліл, піридиніл, піримідиніл, піразиніл, піраніл, піридазиніл, пірролідиніл, піперидиніл, піперазиніл, морфолініл, тіоморфолініл, діоксаніл, дитіаніл, тритіаніл, тріазиніл, бензотієніл, ізобензотієніл, бензофураніл, ізобензофураніл, бензотіазоліл, бензоксазоліл, бензодіоксаніл, індоліл, ізоі 33 74791 34 ндоліл, індолініл, пуриніл, 1Н-піразоло[3,4хіноксалініл, тіазолопіридиніл, оксазолопіридиніл d]піримідиніл, бензімідазоліл, хїіноліл, ізохіноліл, та імідазо[2,1-b]тіазоліл; в яких кожен з вищезациннолініл. фталазиніл, хіназолініл, хіноксалініл, значених гетероциклів окремо може бути заміщетіазолопіридиніл, оксазолопіридиніл, та іміданий, якщо можливо, одним, двома, трьома або зо[2,1-b]тіазоліл; в яких кожен з вищезазначених чотирма замісниками, кожен з яких незалежно вигетероциклів може бути необов'язково заміщений браний з гідрокси, С1-4алкілу, С1-4алкілокси, С1-4 одним або, коли це можливо, двома чи трьома алкілкарбонілу, піперидинілу, NR17R18, C(=O)-Z-C1-4 замісниками, кожен з яких незалежно вибраний з алкілу, R6, сульфонамідо та С1-4алкілу, заміщеного 2 11 Het , R та С1-4алкілу, необов'язково заміщеного одним або двома замісниками, незалежно обраодним або двома замісниками, кожен з яких незаними з гідрокси, С1-4алкілокси, фенілу, C(=O)-Z-C1-6 лежно вибраний з Het2 та R11; алкілу, -Y-С1-4алкандіїл-С(=О)-Z-С1-6алкілу, R6 тa 2 Het представлений гетероциклом, вибраним з NR17R18; однак за умов, що наступних: пірроліл, пирролініл, імідазоліл, іміда- R2 відмінний від С1-6 алкілоксикарбонілС1-6 золініл, піразоліл, піразолініл, тріазоліл, тетразоалкілу або амінокарбонілу; та ліл, фураніл, тетрагідрофураніл, тієніл, тіоланіл, - R7, R8, R9 та R10 відмінні від амінокарбонілу, діоксоланіл, оксазоліл, оксазолініл, ізоксазоліл, С1-6алкілкарбонілокси-С1-4алкілкарбонілу, гідрокси тіазоліл, тіазолініл, ізотіазоліл, тіадіазоліл, оксадіС1-4алкілкарбонілу, С1-4 алкілоксикарбонілкарбоніазоліл, піридиніл, піримідиніл, піразиніл, піраніл, лу, C(=O)-O-R19, С1-4 алкандіїлС(=О)-О-R19 або -Yпіридазиніл, діоксаніл, дитіаніл, тритіаніл. тріазиС1-4алкандіїлС(=O)-О-R1; та ніл, бензотієніл, ізобензотієніл, бензофураніл, ізо- R12 та R13 відмінні від С1-4алкілкарбонілоксибензофураніл, бензотіазоліл, бензоксазоліл, індоС1-4алкілкарбонілу, гідроксиС1-4алкілкарбонілу або ліл, ізоіндоліл, індолініл, пуриніл, 1H-піразоло[3,4С1-4алкілкарбонілкарбонілу ;та d]піримідиніл, бензімідазоліл, хіноліл, ізохіноліл, - R11 відмінний від C(=O)-O-R19, -Y-С1-4 алкандіциннолініл, фталазиніл, хіназолініл, хіноксалініл, їл-С(=О)-OR19, C(=O)NH2, С(=O)NHC1-4 алкілу або тіазолопіридиніл, оксазолопіридиніл, та імідаС(=О)NНС3-7циклоалкілу ;та зо[2,1-b]тіазоліл; в яких кожен з вищезазначених - R15 та R16 відмінні від амінокарбонілу, С1-4 алгетероциклів окремо може бути необов'язково закілкарбонілокси-С1-4алкілкарбонілу, гідрокси С1-4 міщений одним або, це можливо, двома чи трьома алкілкарбонілу або С1-4алкілоксикарбонілзамісниками, кожен з яких незалежно вибраний з карбонілу та Het4, R11 та С1-4алкілу, необов'язково заміщеного - арил відмінний від фенілу, заміщеного C(=O)одним або двома замісниками, незалежно обраO-R19, C(=O)NH2, C(=O)NHC1-4алкілом, ними з Het4 та R11; С(=О)NНС3-7циклоалкілом та/або С1-4алкілом, за3 19 Het представлений моноциклічним гетероциміщеним C(=O)-O-R або Y-С1-4алкандіїл-С(=О)-О14 клом, вибраним з наступних: пірролідиніл, піпериR ;та диніл, піперазиніл, морфолініл, тіоморфолініл та - Het3 відмінний від моноциклічного гетероциктетрагідропіраніл; в яких кожен з вищезазначених лу, заміщеного C(=O) O-R19 та/або С1-4алкілом, моноциклічних гетероциклів окремо може бути заміщеним C(=O)-O-R19 та/або Y-С1-4алкандіїл заміщений необов'язково, де припустимо, одним, C(=O)-O-R19 ;та двома, трьома або чотирма замісниками, кожен з - у кожній з вищеперерахованих умов R19 вияких незалежно вибраний з гідрокси, С1-4алкілу, значається як водень, С1-4алкіл, С3-7циклоалкіл, С1-4алкілокси, С1-4алкілкарбонілу, піперидинілу, амінокарбонілметилен або моно- чи ді(С1-4алкіл)NR12R13, C(=O)-Z-R14, R6 та С1-4алкілу, заміщеного амінокарбонілметилен; та одним або двома замісниками, незалежно обравищезазначена сполука, що відповідає форними з гідрокси, С1-4алкілокси, фенілу, C(=O)-Zмулі (І), містить принаймні одну складову -C(=O)-ZR14, -Y-С1-4алкандіїл-С(=О)-Z-R14, R6 тa NR12R13; R14. 4 Het представлений моноциклічним гетероциДо цікавлячої групи речовин належать сполуки клом, вибраним з наступних: пірроліл, імідазоліл, формули (І ), де складова 6-азаурацилу зв'язана з піразоліл, тріазоліл, тетразоліл, фураніл, тієніл, фенільним кільцем та знаходиться в пара- або оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, тіадіаметапозиції відносно атому вуглецю, до якого призоліл, оксадіазоліл, піридиніл, піримідиніл, піразиєднані замісники -X-R2, R3 та R4, переважно - в ніл, піраніл, піридазиніл та тріазиніл; парапозиції. До іншої цікавлячої групи належать ті Het5 представлений гетероциклом, вибраним з сполуки формули (І"), на які можуть поширюватись наступних: пірроліл, пирролініл, імідазоліл, імідаодне або більшеобмежень : золініл, піразоліл, піразолініл, тріазоліл, тетразо- p дорівнює 0, 1 або 2; ліл, фураніл, тетрагідрофураніл, тієніл, тіоланіл, - X представлений S, NR5 чи прямим зв'язком; діоксоланіл, оксазоліл, оксазолініл, ізоксазоліл, найкраще-прямим зв'язком; тіазоліл, тіазолініл, ізотіазоліл, тіадіазоліл, оксаді- кожний радикал R1 незалежно є гало, полігаазоліл, піридиніл, піримідиніл, піразиніл, піраніл, лоС1-4алкілом, С1-6алкілом, С1-6алкілокси або арил, піридазиніл, пірролідиніл, піперидиніл, піперазиніл, переважно хлоро- або трифлюорометил, більш морфолініл, тіоморфолініл, тетрагідропіраніл, діопереважно хлоро-; ксаніл, дитіаніл, тритіаніл, тріазиніл, бензотієніл, - як мінімум одна складова -C(=O)-Z-R14, що ізобензотієніл, бензофураніл, ізобензофураніл, міститься у сполуці, яка відповідає формулі (І"), бензотіазоліл, бензоксазоліл, бензодіоксаніл, інутворена радикалом R2, доліл, ізоіндоліл, індолініл, пуриніл, 1Н- R2 представляє Het1 або С1-6алкіл, заміщений піразоло[3,4-d]піримідиніл, бензімідазоліл, хіноліл, одним або двома замісниками, вибраними з гідроізохіноліл, циннолініл, фталазиніл, хіназолініл, кси, ціано, аміно, моно- або ді(С1-4алкіл)аміно, 35 74791 36 C(=O)-Z-R14, С1-6алкілокси, необов'язково заміщезокрема фураніл, тієніл, піридиніл або бензотієніл, ного C(=O)-Z-R14, С1-6алкілсульфонілокси, С3-7 цикде кожен із згаданих ароматичних гетероциклів лоалкіл, необов'язково заміщеного C(=O)-Z-R14, незалежно може необов'язково бути заміщений арила, арилокси, арилтіо, Het1, Het1окси та Het1тio; одним або, якщо можливості, двома чи трьома і якщо X представлений О, S або NR5, тоді R2 мозамісниками, кожен з яких незалежно вибраний з 11 же також представляти амінотіокарбоніл, С1-4 алкіR та С1-4алкілу; 14 лкарбоніл, необов'язково заміщений C(=O)-Z-R , - Het3 представлений піперидинілом, піперазиС1-4алкілтіокарбоніл, необов'язково заміщений нілом, морфолінілом або тетрагідропіранілом, коС(=О)-Z-R14, арилкарбоніл, арилтіокарбоніл, жен з яких незалежно необов'язково заміщається, Het1карбоніл або Het1тіокарбоніл; найбільш бажаде можливо, одним, двома, трьома або чотирма но, щоб R2 був представлений Het1; замісниками, серед яких кожен незалежно вибра- R3 представляє водень, метил, етил, пропіл ний з гідрокси, С1-4алкілу, С1-4алкілкарбонілу, піпеабо циклогексил, найбільш бажано - метил; ридинілу та С1-4алкілу, заміщеного одним чи двома - R4 представляє водень або метил, найбільш замісниками, незалежно обраними з гідрокси, С1-4 бажано - метил; алкілокси та фенілу; - R3 тa R4 разом формують 1,4-бутандіїл; - Het4 представлений тієнілом; 6 - R представляє С1-6алкілсульфоніл або амі- Het5 представлений піперидинілом або піпеносульфоніл; разинілом, необов'язково заміщеним С1-4алкілом, - кожен з радикалів R7 та R8 незалежно предсульфонамідо. ставлений воднем, С1-4алкілом, Het3 або R6; До спеціальних сполук формули (І"), належать - кожен з радикалів R9 та R10 незалежно предті, де р дорівнює 2 та обидва замісники R1 є хлороставлений воднем, С1-4алкілоксиС1-4алкілом, С1-4 ; найбільш бажано, щоб обидва хлорних замісники алкілкарбонілом, амінокарбонілом, знаходились в ортопозиції відносно атому вуглеНеt3карбонілом, Het3 або R6; цю, до якого приєднані замісники -X-R2, R3 та R4. - R11 представляє ціано, нітро, гало, С1-4 алкіОкремими речовинами, які належать до сполук локси, форміл, NR7R8, C(=O)NR15R16, -C(=O)-Z-R14, формули (І") є ті, в котрих складова 6-азаурацилу арил, арилкарбоніл, Het3 або C(=O)Het3; найбільш знаходиться в парапозиції відносно атому вуглебажано, щоб R11 був представлений фенілом, цю, до якого приєднані замісники -X-R2, R3 та R4, а 14 14 14 C(=O)-O-R , -C(=O)-S-R або C(=O)-NH-R . р дорівнює 2, внаслідок чого обидва замісники R1 є - R14 представляє дігідрофураніл, С5-20алкіл, хлоро та знаходяться в ортопозиції по відношенню С3-20алкеніл, полігалоС1-6алкіл, Het5 або С1-20алкіл, до атому вуглецю, до якого приєднані замісники заміщений одним або більше замісниками, вибраX-R2, R3 та R4. ними з наступних: феніл, С1-4алкіламіно, ціано, В інших окремих речовинах, які належать до Het1, гідрокси та С1-4циклоалкілу; сполук формули (І"), X представлений прямим - R17 та R18 незалежно представлені воднем зв'язком, a R2 є моноциклічним гетероциклом, виабо фенілом; браним з наступних: пірроліл, імідазоліл, піразо- арил являє собою феніл, необов'язково заліл, тріазоліл, тетразоліл, фураніл, тієніл, оксазоміщений одним, двома або трьома замісниками, ліл, ізоксазоліл, тіазоліл, ізотіазоліл, тіадіазоліл, кожен з яких незалежно вибраний з нітро, ціано, оксадіазоліл, піридиніл, піримідиніл, піразиніл, гало, гідрокси, С1-4алкілу, С3-7циклоалкілу, С1-4 алпіраніл, піридазиніл та тріазиніл, зокрема імідазокілокси, формілу, полігалоС1-4алкілу, NR9R10. ліл, оксадіазоліл, тіазоліл, піримідиніл або піридиC(=O)NR9R10, C(=O)-O-R14, -O-R6, фенілу, ніл, в яких кожен з вищезгаданих моноциклічних C(=O)Het3 та С1-4алкілу, заміщеного одним або гетероциклів незалежно може необов'язково бути більше замісниками, кожен з яких незалежно вибзаміщеним одним або, де можливо, двома чи раний з гало, гідрокси, С1-4алкілокси, C(=O)-O-R14, трьома замісниками, незалежно вибраними з Неt2, 3 9 10 Het тa NR R ; R11 та С1-4алкілу, необов'язково заміщеного Het2 - Het1 представляє моноциклічний гетероцикл, або R11; більш бажано, щоб R2 був представлений, вибраний з наступних: пірроліл, імідазоліл, піразозаміщеним необов'язково тіазолілом, піридинілом ліл, тріазоліл, тетразоліл, фураніл, тієніл, оксазоабо оксадіазолілом. ліл, ізоксазоліл, тіазоліл, ізотіазоліл, тіадіазоліл, Переважними речовинами, що належать до оксадіазоліл, піридиніл, піримідиніл, піразиніл, сполук формули (І"), є ті, де обидва радикали R3 та піраніл, піридазиніл та тріазиніл, зокрема імідазоR4 представлені метильними групами, a -X-R2 явліл, оксадіазоліл, тіазоліл, піримідиніл або піридиляє собою Het1, при цьому бажано, щоб Het1 був ніл, в яких кожен з вищезгаданих моноциклічних представлений необов'язково заміщеним тіазолігетероциклів незалежно може необов'язково бути лом, піридинілом або оксадіазолілом. заміщеним одним або, де можливо, двома чи Більш переважними речовинами, що належать трьома замісниками, незалежно вибраними з Het2, до сполук формули (І"), є ті, де обидва радикали R11 та С1-4алкілу, необов'язково заміщеного Het2 R3 та R4 представлені метильними групами, -X-R2 або R11; найбільш бажано, щоб Het1 був представє необов'язково заміщений 2-тіазоліл або 3лений імідазолілом, оксадіазолілом, тіазолілом оксадіазоліл, складова 6-азаурацилу знаходиться або піридинілом, кожен з яких незалежно необоу парапозиції по відношенню до атому вуглецю, до в'язково заміщений одним або, де можливо, двома якого приєднані замісники -X-R2, R3 та R4, а р дорічи трьома замісниками, з яких кожен незалежно внює 2, внаслідок чого обидва замісники R1 є хловибраний з Her, R11 та С1-4алкілу, необов'язково ро та знаходяться в ортопозиції відносно атому заміщеного Het2 або R11; вуглецю, до якого приєднані замісники -X-R2, R3 та 2 - Het представляє ароматичний гетероцикл; R4. 37 74791 38 З метою спрощення подання структури сполук ності основи, наприклад, ацетату калію. формули (І), група в подальшому буде представлятися символом D. Сполуки, що описуються формулою (І), можуть бути отримані шляхом низки реакцій, які включають етап взаємодії проміжної речовини, представленої формулою (II), у якій радикал W1 є придатною для заміщення групою, наприклад, атомом галогену, з відповідним реагентом, який описується формулою (III). Вищенаведена реакція може проходити в інертному відносно цієї реакції розчиннику, як, наприклад, ацетонітрил, N,N-диметилформамід, оцтова кислота, тетрагідрофуран, етанол або суміш вказаних сполук. Альтернативний спосіб за умов, що реагент формули (III) діє як розчинник, не вимагає додаткового інертного розчинника. Реакція може необов'язково відбуватись в присутності основи, наприклад, 1,8-діазабіцикло[5.4.0.]ундец-7-ену, бікарбонату натрію, метанолату натрію та подібних до них сполук. Прийнятний для реакції діапазон температур - від -70°С до температури дефлегмування. В наведеному та наступних способах приготування реагуючі продукти повинні бути ізольованими від середовища, в якому відбувається реакція, та, необов'язково, в подальшому очищені, у відповідності до загальноприйнятих методик, таких як, наприклад, екстракція, кристалізація, дистиляція, порошкування та хроматографія. Деякі сполуки та проміжні речовини, що використовуються в цьому винаході, можуть бути отримані відповідно (або аналогічно) до процедур, описаних в патентах ЕР-А-0,170,316, ЕР-А0,232,932 та заявці WO99/02505. Наприклад, альтернативний спосіб приготування сполук, що описуються формулою (І), включає циклізацію проміжної сполуки формули (IV), де L є групою, що відщеплюють ,наприклад, С1-6 алкілокси або гало, а Е представлений відповідною групою - акцептором електронів, наприклад, естером, амідом, цианідом, С1-6 алкілсульфонілокси або подібними до них групами; та видалення групи Ε цього отриманого тріазиндіону, який описується формулою (V). Прийнятним способом циклізації є її проведення шляхом реакції дефлегмування у проміжній речовині (IV), яке проходить у кислому середовищі, наприклад, оцтовій кислоті, у присут В залежності від природи групи Е, вона може бути видалена будь-якою з загальноприйнятих методик елімінації. Наприклад, коли Ε представлена амідом або ціано-складовою, її можна гідролізувати до карбоксильної складової шляхом, наприклад, заміщення у проміжній сполуці, до якої приєднана група Е, у соляній або оцтовій кислоті. Отримана таким чином проміжна речовина може потім реагувати з меркаптооцтовою кислотою або її функціональними похідними для отримання сполуки формули (І). Вказана реакція краще відбувається при підвищенні температури до температур дефлегмування. Прийнятний шлях приготування проміжних сполук, які описуються формулою (IV), вміщує реакцію проміжної сполуки формули (VI) з нітратом натрію або його функціональними похідними в кислому середовищі, наприклад, суміші соляною кислоти та оцтової кислот або, бажано, у подібній реакційній суміші, з подальшою взаємодією утвореної проміжної речовини з реагентом, який описується формулою (VII), де радикали L та Ε визначені вище, у присутності основи, наприклад, ацетату натрію. Значуща підгрупа в даному винаході - це підгрупа сполук формули (І), у якій -X-R2 є необов'язково заміщеною 2-тіазоліл складовою, такі сполуки можуть бути представлені формулою (l-а). Необов'язково заміщена 2-тіазоліл складова може бути включена в сполуки формули (l-а) на різних стадіях процесу її приготування. Наприклад, у схемі 1 представлені три описані вище шляхи приготування сполуки, що відповідає формулі (l-а). 39 Перший шлях залучає перетворення ціаноскладової проміжної сполуки формули (VIII) на відповідний тіоамід з використанням газоподібної речовини H2S у відповідному розчиннику, наприклад, піридині, та в присутності основи, такої як тріетиламін, таким чином отримуємо проміжну сполуку, що відповідає формулі (IX-а). Цей тіоамід може піддаватись циклізації з проміжною сполукою формули (XII), де W є групою, придатною для вивільнення, наприклад, галогеном (як бром-), у відповідному розчиннику, наприклад, етанолі. Аміноскладова утвореного похідного 2-тіазолілу, що відповідає формулі (ΘΧ-b), може потім реагувати, як описано вище, форміруючи 6-азаурацилове кільце, таким чином утворюється сполука, що відповідає формулі (l-а). Другий шлях утворення сполуки формули (l-а) включає по-перше захист аміноскладової в проміжній сполуці формули (VIII) за допомогою введення відповідної захисної групи Р, наприклад, алкілкарбонільної групи, з використанням загальноприйнятої методики протектування. У випадку, коли Ρ представлена алкілкарбонільною групою, проміжні сполуки формули (VII) можуть взаємодіяти з відповідним ангідридом, що описується формулою алкіл-С(=О)-О-С(=О)-алкіл, у відповідному розчиннику, наприклад, толуолі. Отримана таким чином проміжна сполука формули (Ха) може в подальшому вступати в реакцію у відповідності до першого шляху, описаного вище. Заключний етап перед утворенням кільця 6азаурацилу може ініціюватись після депротекції аміноскладової із застосуванням загальноприйнятої методики депротектування . У випадку, коли Ρ представлена алкілкарбонільною групою, проміжні сполуки формули (Х-с) можуть піддаватися депротекції шляхом їх взаємодії у відповідному розчиннику, наприклад, етанолі, у присутності кислоти, наприклад, соляної. Третій шлях включає на першому етапі утво 74791 40 рення кільця 6-азаурацилу, як описано вище, однак починаючи з проміжної сполуки формули (VIII), та наступну взаємодію утвореної в такий спосіб проміжної сполуки (ХІ-а) з H2S з подальшою взаємодією тіоаміду, що відповідає формулі (ΘΧ-b), з проміжною сполукою (XII), як описано в першому шляху, з формуванням наприкінці сполуки (l-а). Іншою значущою підгрупою в даному винаході є сполуки формули (І), де -X-R2 є необов'язково заміщеною складовою 1,2,4-оксадіазол-3-іл, вказані сполуки можуть бути представлені формулою (І-b-1). Необов'язково заміщена складова 1,2,4оксадіазол-3-іл може включатись на тих самих етапах процесу реагування, як це описано для похідних 2-тіазолілу в схемі 1. Наприклад, аналогічно одному з трьох шляхів, наведених у схемі 1, сполуки формули (І-b-1) можуть бути отримані за допомогою низки реакцій проміжної сполуки (VIII), як це представлено на схемі 2. У наведеній схемі 2 ціаногрупа проміжної сполуки (VIII) реагує з гідроксиламіном або його функціональним похідним у відповідному розчиннику, наприклад, метанолі, та у присутності основи, наприклад, метанолату натрію. Утворена таким чином проміжна речовина, що описується формулою (Хlll-а), далі реагує з проміжною сполукою (XIV), де W є придатною для вивільнення групою, наприклад, галогеном, зокрема хлоро-, у відповідному розчиннику, наприклад, дихлорметані, та у присутності основи, наприклад, N,N-(1метилетил)етанаміну. Утворена проміжна речовина (Хlll-b) потім піддається циклізації до похідного 3-оксадіазолілу, що описується формулою (Хlll-с). Аміноскладова проміжних сполук (Хlll-с) може в подальшому трансформуватись до кільця 6азаурацилу, як описано вище. Ще однією значущою підгрупою в даному винаході є сполуки формули (І), де -X-R2 є не обов'язково заміщеною складовою 1,3,4-оксадіазол-2-іл, ці сполуки можуть бути представлені формулою (Іb-2). Для прикладу, сполуки формули (І-b-2) можуть бути отримані, як це описано на схемі 3. 41 74791 42 наприклад, ізотіоціанатом, у відповідному розчиннику, наприклад, тетрагідрофурані. Проміжні речовини, що описуються формулою (VIII), можуть бути отримані, як це приведено на схемі 5. Проміжні сполуки, що описуються формулами (XIX) та (XX) можуть взаємодіяти у відповідному розчиннику, наприклад, диметилсульфоксіді, у присутності основи, наприклад, гідроксиду натрію, із утворенням проміжної сполуки (XV-a). Нітроскладова проміжних речовин (XV-a) може або одразу відновлюватись до аміногрупи шляхом загальноприйнятих методик відновлення, наприклад відновлення нітрогрупи з воднем в метанолі у присутності каталізатора, зокрема нікелевого каталізатора Ренея, або може спочатку, перед відновНітрильна складова проміжної сполуки (XV) ленням, реагувати з проміжною сполукою трансформується в складову карбонової кислоти формули R4 -W, де R4 є подібною до R4 групою, за допомогою загальноприйнятих методик. Наприяка, однак, відрізняється від водню, a W є відповіклад, похідне нітрилу може піддаватись зворотнодною групою, найбільш придатною для вивільненму захопленню в суміші сірчаної та оцтової кислоня, наприклад галогеном, зокрема йодо-, у відпоти з водою. Похідне карбонової кислоти, що відному розчиннику, наприклад N,Nописується формулою (XVI-a), може в подальшому диметилформаміді, у присутності відповідної осреагувати з хлоруючим агентом, наприклад, тіонінови, наприклад гідриду натрію перед відновленлхлоридом, з утворенням похідного ацилхлориду, ням нітро складової. що описується формулою (XVI-b). Надалі ацилхлорид може реагувати з похідним гідразину (XVII) у відповідному розчиннику, наприклад, дихлорметані, та у присутності основи, наприклад, N,N-(1метилетил)етанаміну. Утворена в такий спосіб проміжна сполука (XVI-c) може у присутності фосфорилхлориду піддаватись циклізації до похідного 1,2,4-оксадіазол-2-ілу, який описується формулою (XVI-d). Заключним етапом перед утворенням кільця 6-азаурацилу, як наведено вище, є відновлення нітрогрупи проміжної сполуки (XVI-e) до аміногрупи із застосуванням загальноприйнятих методик, наприклад, відновлення нітрогрупи з воСполуки, що описуються формулою (І) можуть днем в метанолі та у присутності каталізатора, також перетворюватись одна на одну шляхом зазокрема нікелевого каталізатора Ренея. гальноприйнятих методик трансформації функціоЩе однією значущою групою в даному винанальних груп, наприклад, згаданих у заявці ході є сполуки, що описуються формулою (І), де WO99/02505 та тих, що слугують прикладом у наX-R2 є -NH-R2, ці сполуки можуть бути представведеній нижче експериментальній частині. Зокрелені формулою (I-с-1). На схемі 4 приведений найма, сполуки формули (І), що містять як мінімум більш зручний шлях отримання сполук формули (Іодну -C(=O)-Z-R14 складову, утворену R2, де Ζ с-1). представлений О або S, a R14 відрізняється від водню, можуть найзручніше бути отримані шляхом взаємодії сполуки (XXI), що містить відповідну складову -C(=O)-Z-H, з відповідним реагентом (XXII), в якому W2 представлений придатною для вивільнення групою, як це показано нижче: У вищенаведеній схемі 4 ціаноскладова проміжної сполуки (ІХ-а) гідролізується до відповідного аміду із застосуванням загальноприйнятих методик, наприклад, гідролізу у присутності оцтової та сірчаної кислот. Утворений таким чином амід проміжної сполуки (XVIII-a) може перетворюватись на амін за допомогою (діацетоксийодо)бензену або його функціональних похідних у відповідному розчиннику, наприклад, суміші води та ацетонітрилу. Похідне аміну, що описується формулою (XVIIIb), може далі реагувати з бензотріазол-1ілокситрис-(диметиламіно)фосфоніум гексафлюоро-фосфатом, як це наведено в Tetrahedron Letters No. 14 (1975), с.1219-1222, до утворення сполуки, або із його функціональним похідним, Наприклад, перший спосіб такого отримання сполуки включає взаємодію речовини формули (XXI), яка містить відповідну складову -C(=O)-Z-H, з галідом, найкраще - бромідом, який відповідає формулі Br-R14, в реакційно-інертному розчиннику, наприклад такому, як описано вище, у присутності гідрогенокарбонату натрію. Згадана реакція проводиться при температурі нижче точки кипіння 43 74791 44 використаного розчинника на протязі, наприклад, лотою, алкілгідропероксидами, зокрема tвід 2 до 18 годин у випадку, коли в якості розчинбутилгідропероксидом. Придатними розчинниками ника застосовується диметилформамід. Другий можуть виступати, наприклад, вода, нижчі спирти, спосіб приготування включає взаємодію сполуки зокрема етанол та подібні до нього речовини, вугформули (XXI), яка містить відповідну -C(=O)-Z-H леводні, зокрема толуол, кетони, зокрема 214 складову, із спиртом, який відповідає формулі R бутанон, галогенізовані вуглеводні, зокрема діхлоOH, в реакційно-інертному розчиннику, наприклад рметан та суміші вищевказаних розчинників. Чисті стереоізомеричні форми сполук формутакому, як описано вище, у присутності 1,1 ли (І) можна отримати шляхом застосування загакарбонілбіс-1Н-імідазолу, який необов'язково може льноприйнятих методик. Діастереомери можуть змішуватись з 1,8-Діаза-7-біцикло (5.4.0) ундецебути виділені за допомогою фізичних методів, зокном. У випадку, коли в якості розчинника викорисрема селективної кристалізації та хроматографічтовується метиленхлорид, реакція може проходиних методик, наприклад протиплинного розподілу, ти при кімнатній температурі протягом декількох рідинної хроматографії та подібних до них метогодин. дик. Даний винахід стосується також нових сполук, Окремі сполуки формули (І) та деякі проміжні що описуються формулою: речовини даного винаходу можуть містити асиметричний атом вуглецю. Чисті стереоізомеричні форми цих сполук та проміжних речовин можна отримати за допомогою загальноприйнятих методик. Наприклад, діастереоізомери можуть бути виділені за допомогою фізичних методів, зокрема де кожен з радикалів R20 та R21 незалежно виселективної кристалізації та хроматографічних браний з водню чи С1-20алкілу або R20 та R21 ,взяті методик, наприклад протиплинного розподілу, ріразом з атомом вуглецю , до якого вони приєднані, динної хроматографії та подібних до них методик. утворюють циклоалкільний радикал. Ці нові речоЕнантіомери можна отримати з рацемічних сумівини є корисними для приготування сполуки, що шей за допомогою початкового перетворення цієї описується формулою (І), коли Het5 представлерацемічних сумішей відповідними розчинюючими ний сульфонамідо заміщеним піперазином. Такі агентами, наприклад, хіральними кислотами, на проміжні сполуки формули (XXIII) можуть бути суміш діастереомерних солей або сполук з подаотримані шляхом взаємодії Ν,Ν-диметил-1льшим фізичним відокремленням цих сумішей піперазинсульфонаміду з алкіленоксидом в реакдіастереомерних солей або сполук шляхом, наційно-інертному розчиннику, яким може виступати приклад, селективної кристалізації чи хроматогметанол та/або метиленхлорид. До придатних для рафічних методик, зокрема рідинної хроматографії цієї мети алкіленоксидів належать, наприклад, та подібних до неї методів, та заключним перетвоетиленоксид, пропіленоксид, 1,2-бутиленоксид, ренням цих виділених діастереоізомерних солей циклогексиленоксид та подібні до них речовини. або сполук на відповідні енантіомери. Чисті стереДаний винахід стосується також нових сполук, що оізомеричні форми можна також отримати з чисописуються формулами: тих стереоізомеричних форм відповідних проміжних сполук та вихідного матеріалу за умови, що реакції ,що мають місце, пройдуть стереоспецифічно. Альтернативним способом виділення енантіомерних форм сполук формули (І) та проміжних речовин є рідинна хроматографія, зокрема рідинна які є придатними проміжними речовинами для хроматографія із застосуванням хіральної стаціоприготування окремих сполук, які відвідають форнарної фази. мулі (І). Деякі проміжні сполуки та вихідні матеріали, Сполуки формули (І) можуть також бути перещо використовуються у вищенаведених методиках творені на відповідні N-оксидні форми за допомовзаємодії, є відомими речовинами та присутні на гою загальноприйнятих методик перетворення комерційному ринку або можуть бути отримані у тривалентного азоту на його N-оксидні форми. відповідності до загальноприйнятих методик. Вказана реакдія N-оксидації загалом може провоІЛ-5, відомий також як фактор диференціюдитись шляхом взаємодії початкового матеріалу вання еозинофілів (ФДЕ) або еозинофільний коформули (І) з 3-феніл-2-(феніллонієстимулюючий фактор (Ео-КСФ), є одним з сульфоніл)оксазиридином або відповідним органінайважливіших для еозинофілів факторів життєчним чи неорганічним пероксидом. До відповідних здатності та диференціювання і завдяки цьому в даному випадку неорганічних пероксидів налерозглядається як ключовий чинник еозинофільної жать, наприклад, пероксид водню, пероксиди лужінфільтрації тканин. Існує достатня кількість даних, них або лужноземельних металів, зокрема перокщо захват еозинофілів являє собою важливу патосид натрію, пероксид калію; відповідні органічні гену ланку у розвитку бронхіальної астми та алерпероксиди можуть бути представлені пероксокисгічних захворювань, таких як хейліти, хвороби "полотами, як, наприклад, бензолкарбопероксодразненого кишківника", екзема, кропив'янка, кислотою або гало-заміщеною бензолкарбоперокваскуліти, вульвіти, синдром "холодних кінцівок", сокислотою, зокрема 3атопічні дерматити, полінози, алергічні риніти та хлоробензолкарбопероксокислотою, пероксоалкаалергічні кон'юнктивіти, а також інших запальних новими кислотами, зокрема пероксооцтовою кис 45 74791 46 захворювань, зокрема еозинофільного синдрому, Представлений винахід пропонує також комалергічних ангіїтів, еозинофільних фасциїтів, еопозиції для лікування еозинофіл-залежних запальзинофільної пневмонії, PIE синдрому, ідіопатичної них захворювань, які містять ефективну кількість еозинофілії, еозинофільної міалгії, хвороби Крона, сполуки формули (І) та фармакологічно прийнятвиразкового коліту та подібних до них захворюний носій або розчинник. вань. Для приготування фармацевтичних композиПредставлені сполуки пригнічують також утвоцій, представлених у винаході, терапевтично еферення інших хемокінів, зокрема моноцитарного ктивну кількість даної сполуки, у формі основи або хемотаксичного протеїну-1 та -3 (МХП-1 та МХПадитивної солі в якості активного інгредієнту з'єд3). Відомо, що МХП-1 має здатність притягувати як нують, ретельно утворюючи суміш, з фармацевтиТ-клітини, в яких переважно і відбувається синтез чно прийнятним носієм, який може бути представІЛ-5, так і моноцити, відомі своїм синергізмом по лений різноманітними формами, в залежності від відношенню до еозинофілів [Саrr et al., 1994, бажаного шляху застосування препарату. Бажано, Immunology, 91, 3652-3656]. МХП-3 відіграє також щоб вказані фармацевтичні композиції були предважливу роль в алергічному запаленні завдяки ставлені в дозованих разових формах, особливо своїй здатності мобілізовувати та активувати бадля системного застосування, такого як парентезофільні та еозинофільні лейкоцити [Baggiolini et ральне введення; або місцевого застосування, як, al., 1994, Immunology Today, 15(3), 127-133]. наприклад інгаляції, назальні спреї або подібні Представлені сполуки практично не мають лікарські форми . Аплікації даних композицій мовпливу, або цей вплив досить незначний, на утвожуть наноситись у вигляді аерозолів з використанрення інших хемокінів, зокрема ІЛ-1, ІЛ-2, ІЛ-3, ІЛням витискаючого газу (наприклад азоту, діоксиду вуглецю, фреону) або без нього у вигляді насос4, ІЛ-6, ІЛ-10, -інтерферону ( -ΘΦ) та гранулоцитаних спреїв, крапель, лосьйонів або напівтвердих рно-макрофагального колонієстимулюючого факформ - густих композицій, які наносяться тампотора (ГМ-КСФ), що свідчить про відсутність широном. До напівтвердих композицій належать, зоккоспектрової імуносупресивної дії у інгібіторів ІЛ-5. рема, мазі, креми, гелі, лініменти та інші подібні Вибірковий пригнічуючий вплив представлених форми, які будуть зручні для застосування. сполук на хемокіни може бути продемонстрований Таке приготування вищезгаданих фармацевin vitro шляхом визначення кількості хемокінів в тичних композицій у вигляді дозованих разових крові людини. Спостереженні in vivo показали приформ має особливі переваги з точки зору легкості гнічення еозинофілії у вусі миші, пригнічення еозизастосування та рівномірності дозування. Під донофілії крові на моделі мишей виду Ascaris; знизованою разовою формою, як визначено у описі та ження продукції білку ІЛ-5 у сироватці та подальшій формулі винаходу, розуміється фізично підвищення експресії мРНК ІЛ-5 у селезінці мишей дискретна одиниця, придатна для вживання як під впливом анти-CD3 антитіл, а також пригнічення одноразова доза, кожна одиниця містить визначеалерген-індукованого або Сефадекс-індукованого ну кількість активного інгредієнту, розраховану для захвату еозинофілів легеневою тканиною у морсьспричинення бажаного терапевтичного ефекту, ких свинок, що свідчить про користь вказаних спопоєднану з певним фармацевтичним носієм. Прилук у лікуванні еозинофіл-залежних запальних кладом таких дозованих разових форм є таблетки захворювань. (включаючи таблетки з міткою для розподілення Представлені інгібітори утворення ІЛ-5 корисна більш дрібні дози та вкриті оболонкою таблетні, зокрема, при інгаляційному застосуванні. ки), капсули, пілюлі, пакетики з порошком, пастилПевний інтерес являють проміжні сполуки, які ки, розчини або суспензії для ін'єкцій, мірні чайні описуються формулою (ХІ-а). Вони мають не тільта столові ложки та інші подібні разові форми і їх ки значення як проміжні речовини в приготуванні сукупності. сполук формули (І), але й самі по собі володіють З метою підвищення розчинності та/або стабіцінною фармакологічною активністю. льності сполук формули (І) у фармацевтичних Зважаючи на описані фармакологічні властикомпозиціях найбільш вигідним є застосування -, вості, сполуки формули (І) можуть застосовуватись у медицині. Зокрема, представлені сполуки - або -циклодекстринів або їх похідних. Покраможуть використовуватись при виробництві медищувати розчинність та/або стабільність сполук каментів для лікування еозинофіл-залежних запаформули (І) у фармацевтичних композиціях мольних захворювань, як вказано вище, і серед них жуть також супутні розчинники, наприклад спирти. бронхіальної астми, атопічних дерматитів, алергіПри приготуванні водних композицій адитивні солі чних ринітів та алергічних кон'юнктивітів. основної складової сполуки є набагато прийнятЗ огляду на користь сполук формули (І), було ними внаслідок їх кращої розчинності у воді. запропоновано метод лікування теплокровних Придатними циклодекстринами можуть бути ссавців, включаючи людей, що страждають на -, -, -циклодекстрини або їх ефіри та змішані еозинофіл-залежні запальні захворювання, зокреефіри, в яких одна або більше гідроксильних груп ма бронхіальну астму, атопічні дерматити, алергіангідроглюкозних одиниць циклодекстрину замічні риніти та алергічні кон'юнктивіти. Цей метод щена С1-6алкілом, зокрема метилом, етилом або передбачає системне та місцеве застосування ізопропілом, наприклад випадково метильованим ефективної кількості сполуки формули (І), її N-ЦД; гідроксиС1-6алкілом, зокрема гідроксіетилом, оксидних форм та фармакологічно прийнятних гідроксипропілом або гідрокси бутилом; карбокадитивних солей або їх можливих стереоізомерисиС1-6алкілом, зокрема карбоксиметилом або карчних форм у теплокровних ссавців, включаючи боксиетилом; С1-6алкілкарбонілом, зокрема ацетилюдину. лом, С1-6алкілоксикарбонілС1-6алкілом або 47 74791 48 карбоксиС1-6алкілоксиС1-6алкілом, зокрема карбокформули (І) радіоактивними ізотопами, (b) переносиметоксипропілом або карбоксиетоксипропілом; су цих радіомічених сполук на біологічний матеріС1-6алкілкарбонілоксиС1-6алкілом, зокрема 2ал та подальшим (с) визначенням радіоактивного ацетилоксипропілом. Найбільш придатними в яковипромінювання мічених сполук. сті комплексантів та/або розчинників слід зазначиПід терміном "біологічний матеріал" розуміється любий різновид матеріалу, що має біологічну ти -ЦД, нерегулярно метильований -ЦД, 2,6природу. Зокрема, цей термін стосується зразків диметил- -ЦД, 2-гідроксиетил- -ЦД, 2тканин, плазми або інших рідких середовищ оргагідроксиетил- -ЦД, 2-гідроксипропіл- -ЦД, (2нізму, а також тварин, особливо теплокровних, або карбоксиметокси)пропіл- -ЦД та, зокрема, 2їх частин, наприклад, органів. гідроксипропіл- -ЦД (2-ΓΠ- -ЦД). Радіоактивні мічені сполуки формули (І) моПід терміном змішані ефіри розуміються похіжуть також бути корисними в якості агентів для дні циклодекстрину, де як мінімум визначення, в якій мірі речовина, що тестується, дві гідрокси групи циклодекстрину етерифікомає здатність займати або зв'язувати відповідну вані різними групами, наприклад, гідроксипропілом ділянку рецептора. Ступінь витіснення речовиною, та гідроксиетилом. що тестується, сполуки формули (І) з окремих діДля оцінки середньої кількості молей алкоксілянок рецептора буде демонструвати властивості одиниць на моль ангідроглюкози використовується речовини як агоніста, антагоніста або змішаного показник середнього молярного заміщення (М.З.). агоніста/антагоніста цього рецептора. Визначення показника М.З. проводиться з викориПри виконанні досліджень in vivo радіоактивні станням різноманітних аналітичних методик, пересполуки застосовувались на тваринах у вигляді вага при цьому надається методу масспектрометвідповідних композицій, а їх розподіл виявлявся із рії, М.З. діапазон 0,125-10. використанням візуалізаційних методів, зокрема Для оцінки середньої кількості заміщених гідоднопротонної емісійної комп'ютерної томографії роксилів на одиницю ангідроглюкози використову(ОЕКТ), позитронної емісійної томографії (ПЕТ) та ється показник середнього ступеня заміщення подібних до них методик. Таким чином визнача(С.З.). Визначення показника С.З. проводиться з лось розповсюдження окремих рецепторів по орвикористанням різноманітних аналітичних метоганізму та за допомогою вищевказаних візуалізадик, перевага при цьому надається методу массційних методик проводилось виявлення органів, пектрометрії, С.З. діапазон 0,125-3. що містять згадані рецептори. Подібний процес Завдяки своєму високому ступеню селективвізуалізації органу за допомогою сполуки формули ності у якості інгібіторів ІЛ-5, означені вище сполу(І), міченої радіоактивними ізотопами, із визначенки формули (І) також придатні для маркування або ням випромінювання цієї радіоактивної речовини ідентифікації рецепторів. Для реалізації цієї мети також складає частину представленого винаходу. сполуки, що розглядаються в даному винаході, В цілому спостерігалось, що ефективна з теповинні бути помічені, зокрема шляхом заміни, рапевтичної точки зору денна кількість сполуки часткової або повної, одного або більше атомів у складає від 0,01мг/кг до 50мг/кг маси тіла, зокрема молекулі їх радіоактивними ізотопами. Як прикла0,05-10мг/кг маси тіла. Метод лікування може тади мічених сполук, що викликають найбільшу зацікож включати застосування активного інгредієнту в кавленість, можна навести сполуки, які мають як терапевтичному режимі двох-трьох прийомів на мінімум один гало-радикал, яким є радіоактивний добу. ізотоп йоду, брому або фтору; або ті сполуки, що Експериментальна частина містять не менше одного атому 11С чи атому триУ наведених нижче зразках абревіатура ДМСО тію. стандартно використовується для позначення диОдна з таких груп складається з тих сполук метилсульфоксиду, КТ - кімнатної температури, формули (І), в яких R1 представлений атомом раДМФ - Ν,Ν-диметилформаміду, ЕтАц - етилацетадіоактивного галогену. В принципі, будь-яка сполуту, ДІПЕ - для позначення діізопропіленефіру та ка формули (І), що містить атом галогену, піддаТГФ -для тетрагідрофурану. ється радіоміченню шляхом заміни атому галогену А. Приготування проміжних сполук відповідним ізотопом. Найбільш придатними для Приклад A1 цієї мети галогеновими радіоізотопами є радіоак122 123 125 131 a) Суміш 2-хлорпропіонітрилу (0,2моль) та 1,3тивні иодіди, зокрема l, І, l, l; радіоактивні дихлоро-5-нітробензолу (0,2моль) в ДМСО (50мл) броміди, наприклад 75Вr, 76Вr, 77Вr та 82Вr, а також краплинно додавали при КТ до розчину NaOH радіоактивні фториди, зокрема 18F. Введення ра(1моль) в ДМСО (150мл), при цьому температура діоактивного атому галогену повинно проводитись підтримувалася нижче 30°С. Суміш перемішували шляхом відповідної реакції обміну або із викориспротягом 1 години при КТ, після чого поміщали на танням будь-якої вищеописаної методики приготулід та підкислювали НСl. Осад відфільтровували, вання галогенових похідних, що відповідають фопромивали Н2О та вносили в СН2Сl2. Органічний рмулі (І). розчин промивали Н2О, висушували, відфільтроІншою цікавою формою радіоактивного міченвували, після чого розчинник випаровували. Заня є заміщення атома вуглецю атомом "С або лишок очищували за допомогою колонкової хроатома водню атомом тритію. матографії на силікагелі (елюент: Отже, описані сполуки формули (І), мічені раСН2Сl2/циклогексан 70/30). Після збирання чистої діоактивними ізотопами, можуть використовувафракції розчинник випаровували, вихід - 19,5г тись у процесі специфічного мічення рецепторів у (40%) (±)-2,6-діхлоро- -метил-4біологічних матеріалах. Вказаний процес може нітробензолацетонітрилу (проміжна сполука 1). бути представлений етапами (а) мічення сполуки 49 74791 50 b) 80% NaH (0,0918моль) порціонно при темшар висушували, відфільтровували, після чого пературі 0°С під током N2 додавали до розчину розчинник випаровували. Додавали толуол, після проміжної речовини (1) (0,0612моль) у ДМФ чого проводилося азеотропне зневоднювання на (100мл). Суміш перемішували протягом 1 години ротаційному випарнику. Залишок очищували шляпри 0°С під током N2. Краплинно при температурі хом низькоколонкової хроматографії на силікагелі 0°С додавали СН3І (0,0918моль). Суміш перемішу(елюент: СН2СІ2/СН3ОН 98/2). Чисті фракції збиравали при температурі 50°С протягом 12 годин, ли, а розчинник випаровували. Залишок переміпісля чого поміщали на лід та екстрагували за дошували у ДІПЕ, відфільтровували, промивали ДІпомогою ЕтАц. Органічний шар виділяли, промиПЕ, після чого висушували, вихід - 36,8г (41%) 2,6вали Н2О, висушували, відфільтровували, після дихлоро-4-(4,5-дигідро-3,5-діоксо-1,2,4-тріазинчого розчинник випаровували, вихід - 17,1г 2,62(3Н)-іл)- , -диметилбензолацетонітрилу. Фільтдихлоро- , -диметил-4-нітробензолацетонітрилу рат перемішували в ДІПЕ, а отриманий преципітат (проміжна сполука 2). відфільтровували, промивали ДІПЕ та висушуваc) Суміш проміжної речовини (2) (0,066моль) в ли, вихід - 2,5г (3%) 2,6-дихлоро-4-(4,5-дигідро-3,5СН3ОН (200мл) гідрогенізували з нікелевим каталідіоксо-1,2,4-тріазин-2(3Н)-іл)- , затором Ренея (15г) при КТ під тиском 3бар протядиметилбензолацетонітрилу (проміжна сполука 7). гом 1 години. Після захвату Н2 каталізатор відфіе) Розчин проміжної сполуки (7) (0,107моль) та льтровували через целіт, промивали СН3ОН, а N,N-біс(1-метилетил)-етанаміну (0,315моль) в піфільтрат випаровували, вихід - 17,1г 4-аміно-2,6ридині (500мл) перемішували та підігрівали до дихлоро- , -диметилнітробензолацетонітрилу 80°С. Припускалося проходження пухирців H2S (проміжна сполука 3). через вказану суміш протягом 24 годин при 80°С. Приклад А2 Проходження газу H2S припиняли, а реакційна а) Розчин NaNO2 (0,36моль) в Н2О (50мл) досуміш залишалась для перемішування при КТ на давали до розчину проміжної сполуки (3) вихідні дні. Розчинник випаровували. Додавали (0,34моль) в оцтовій кислоті (700мл) та НСІ 500мл 9:1 суміші СН2Сl2/СН3OН, отриману суміш (102мл), перемішували при температурі 10°С. Ревливали в 2Н НСl (1000мл) при температурі 0°С та акційну суміш перемішували протягом 80 хвилин перемішували протягом 10 хвилин. Преципітат при 10°С. Додавали порошкоподібну суміш ацетавідфільтровували та висушували, вихід - 23,2г ту натрію (1,02моль) та діетил(1,3-діоксо-1,3(64%) 2,6-дихлоро-4-(4,5-дигідро-3,5-діоксо-1,2,4]пропандіїл)біскарбамату (0,374моль), реакційну , -диметилбензолетанетіоаміду (проміжна спосуміш перемішували протягом 40 хвилин. Реакційлука 8). ну суміш переливали на подрібнений лід. ПреципіПриклад A3 тат відфільтровували, промивали водою та вносиВ атмосфері азоту розчин проміжної речовини ли в СН2СІ2, після чого шари розділяли. (8) (0,0125моль) та Органічний шар висушували, відфільтровували, після чого розчинник випаровували, вихід - 138,5г (84%) діетил N,N -[2-[[3,5-дихлоро-4-(1-ціано-1метилетил)феніл]гідразоно]-1,3-діоксо-1,3пропандіїл]дікарбамат (проміжна сполука 4). b) Розчин проміжної сполуки (4) (0,28моль) та (0,0157моль) в етанолі (60мл) і ДМФ (30мл; ацетату калію (0,28моль) в оцтовій кислоті висушений скрізь молекулярні сита) перемішували (1000мл) змішували та дефлегмували протягом 3 протягом 6,5 годин при температурі 60°С, після годин. Реакційна суміш, яка містить етил[[2-[3,5чого суміш залишали при КТ на ніч. Розчинник дихлоро-4-(1-ціано-1-метилетил)феніл]-2,3,4,5випаровували. Залишок вносили у воду (100мл), тетрагідро-3,5,-діоксо-1,2,4-тріазин-6цю суміш екстрагували з СН2Сl2 (100мл). Відокреіл]карбоніл]карбамат (проміжна речовина 5) як млений органічний шар висушували (MgSO4), фітака використовувалась в наступному етапі. льтрували, після чого розчинник випаровували, а c) Проміжна сполука (5) (неочищена реакційна потім випаровували разом з толуолом. Залишок суміш) оброблялась 36% НСl (0,84моль). Реакцій(13г) очищували шляхом тонкошарової колонкової ну суміш перемішували та дефлегмували протяхроматографії на силікагелі (елюент: гом 4 годин, після чого залишали для перемішуСН2Сl2/СН3ОН 100/0, потім 99/1, насамкінець 98/2). вання при КТ на вихідні дні. Реакційна суміш Бажані фракції збирали, а розчинник випаровувавиливалась на подрібнений лід, після чого екстрали. Додавали толуол, після чого проводилося азегувалась СН2Сl2. Виділений органічний шар висуотропне зневоднювання на ротаційному випарнишували, відфільтровували, після чого розчинник ку. Залишок (6,5г) кристалізували з CH3CN. випаровували, вихід - 111,6г 2-[3,5-дихлоро-4-(1Преципітат відфільтровували, промивали CH3CN ціано-1-метилетил)феніл]-2,3,4,5-тетрагідро-3,5та ДІПЕ, а потім висушували у вакуумі при темпедіоксо-1,2,4-тріазин-6-карбонова кислоти (проміжратурі 50°С, вихід - 3,17г (46,5%) етил-2-[1-[2,6на сполука 6). дихлоро-4-(4,5-дигідро-3,5-діоксо-1,2,4-тріазинd) Суспензію проміжної речовини (6) 2(3Н)-іл]феніл]-1-метилетил]-4 феніл-5(0,28моль) у меркаптооцтовій кислоті (250мл) петіазолацетату (проміжна сполука 9) з температуремішували протягом 4 годин при температурі рою плавлення 148°С. 100°С, після чого їй давали остигнути до КТ та Приклад A4 продовжували змішування протягом ночі. РеакційСуміш проміжної сполуки (9) (0,00183моль) та ну суміш переливали на подрібнений лід, після 1Н NaOH (0,0055моль) в СН3ОН (25мл) та ТГФ чого екстрагували СН2СІ2. Виділений органічний 51 74791 52 (25мл) перемішували протягом ночі при КТ. Реакпроміжної сполуки 12, точка плавлення якої 130°С, ційну суміш підкислювали 1Н НСl (8мл), а отримасполука описується формулою ний продукт переносили в ЕтАц. Органічний шар промивали розсолом, висушували, фільтрували, розчинник випаровували. Залишок кристалізували з CH3CN. Преципітат відфільтровували, промивали ДІПЕ та висушували, вихід - 0,8г (79%) 2-[1-[2,6дихлоро-4-(4,5-дигідро-3,5-діоксо-1,2,4-тріазин2(3Н)іл)феніл]-1-метилетил]-4 феніл-5тіазолоцтової кислоти (проміжна сполука 10). Приклад А5. Приклад А7 На першому етапі розчин брому (0,02моль) в Проміжну сполуку 12 (0,00465моль) порціонно СН2Сl2 (20мл) краплинно при температурі 10°С при температурі 0-10°С додавали до трифтороцдодавався під потоком азоту до суміші сполук, які тової кислоти (35мл). Суміш перемішували при описуються формулою: кімнатній температурі протягом 3 годин, після чого переливали в Н2О. Преципітати відфільтровували, промивали Н2О та вносили в СН2СІ2. Органічний шар відокремлювали, висушували (MgSO4), профільтровували, а розчинник випаровували. Залишок (2,4г) очищували шляхом колонкової хроматографії на силікагелі (елюент: (0,0227моль) в СН2Сl2 (50мл). Суміш переміСН2Сl2/СН3ОН/NН4ОН 97/3/0,2; 15-40μΜ). Чисті шували при температурі 10°С протягом 1 години. фракції збирали, а розчинник випаровували. ЗаВ неї додавали Н2О та тверду форму К2СО3. Оргалишок кристалізували з CH3CN. Преципітат відфінічний шар відокремлювали, висушували (MgSO4), льтровували та висушували, вихід - 1,16г проміжфільтрували, а розчинник випаровували. Реакція ної сполуки 13, точка плавлення якої 232°С, проводилась чотири рази із використанням однасполука описується формулою кової кількості та складових залишку, вихід - 14г (51%) 1,1-диметилетил -бромо- -оксобензолпропаноату. Суміш проміжної сполуки (8) (0,0119моль), 1,1-диметилетил -бромо- -оксобензолпропаноату (0,0137 моль) та К2СО3 (0,0357 моль) в CH3CN (55мл) перемішували при кімнатній температурі протягом 3,5 годин. Додавали лід та ЕтАц. Суміш підкислювалась 3Н НСl. Органічний шар відокремлювали, висушували (MgSO4), профільтровували, а розчинник випаровували. Продукт використовувався без подальшого очищення, Приклад А8 вихід - 8г проміжної сполуки 11, яка описується 1,1 -карбонілбіс-1H-імідазол (0,0159моль) порформулою: ціонно при КТ під потоком азоту додавали до розчину проміжної речовини (13) (0,00795моль) в ДМФ (60мл). Суміш перемішували при КТ протягом ночі. На протязі 1 години через суміш пропускали пухирці H2S. Суміш перемішували при КТ протягом 1 години, після чого переливали у насичений розчин NaCl та двічі екстрагували СН2Сl2. Комбінований органічний шар висушували (MgSO4), профільтровували, а розчинник випаровували. Таким чином було отримано проміжну сполуку 14, яка описується формулою Приклад А 6 Проміжну сполуку (11) (0,0119моль) та третбутанол (24г) перемішували та дефлегмували протягом 2 годин. Суміш доводили до кімнатної температури. Розчинник випаровували. Залишок вносили в СН2Сl2. Органічний розчин промивали Н2О, висушували (MgSO4), профільтровували, а розчинник випаровували. Залишок (7,8г) очищували шляхом колонкової хроматографії на силікагелі та використовується без подальшого очищен(елюент: СН2СІ2/СН3ОН 99/1; 15-40μΜ). Збирали ня. дві фракції, а їх розчинники випаровували, вихід Приклад А9 2,66г (1-а фракція) та 0,7г (2-а фракція), відповідСуміш проміжної сполуки (8) (0,0158моль) та но. 2-у фракцію очищували за допомогою колонкової хроматографії (елюент CH3OH/NH4OAc 0,5% 80/20; колонка: HYPERSIL С18, 3μΜ). Чисті фракції збирали, а розчинники випаровували, вихід - 0,45г 53 74791 54 на протязі ночі. Розчинник випаровували. Залишок розподіляли між СН2Сl2 та водою. Органічний шар відокремлювали, висушували, фільтрували, а розчинник випаровували. Залишок перемішували з ДІПЕ, відфільтровували, промивали ДІПЕ та висушували, вихід - 3,7г (26%) 4-аміно-2,6-дихлоро(0,0237моль) в етанолі (60мл) та ДМФ (40мл) N -гідрокси- , -диметилбензолетанімідаміду (проперемішували при температурі 60°С протягом 4 міжна сполука 17). годин. Розчинник випаровували. Додавали ЕтАц. b) Розчин проміжної сполуки (17) (0,0323моль) Органічний розчин тричі промивали Н2О, висушута N,N-біс(метилетил)етанаміну (0,0339моль) в вали (MgSO4), профільтровували, а розчинник СН2СІ2 (190мл) перемішували при температурі випаровували. Залишок (11,2г) очищували шляхом 15°С. Краплинно додавали розчин 2колонкової хроматографії на силікагелі (елюент: метилбензоілхлориду (0,0323моль) в СН2Сl2 СН2СІ2/СН3ОН 98/2; 15-40цм). Бажані фракції зби(10мл), а отриману реакційну суміш перемішували рали, а розчинник випаровували, вихід - 4,2г (47%) протягом однієї години. Додавали воду. Органічпродукту, частина якого (1,5г) викристалізовуваний шар відокремлювали, висушували, фільтрувалась з петролейного ефіру та ДІПЕ. Преципітат ли, а розчинник випаровували. Додавали толуол, відфільтровували та висушували, вихід -1,15г після чого проводилося азеотропне зневоднюванпроміжної сполуки 15, точка плавлення якої 126°С, ня на ротаційному випарнику, вихід - 13,0г [1сполука описується формулою аміно-2-(4-аміно-2,6-дихлорфеніл)-2метилпропіліденіл]аміно 2-метилбензоату (проміжна сполука 18). c) Розчин проміжної речовини (18) (0,0323моль) та паратолуолсульфонової кислоти (0,0323моль) в ДМСО (100мл) перемішували протягом 30 хвилин при 150°С. Реакційну суміш охолоджували. Додавали воду і цю суміш екстрагували з толуолом. Виділений органічний шар висушували, фільтрували, а розчинник випаровували. Залишок очищували шляхом низькоколонкової хроматографії на силікагелі (елюент: СН2Сl2). Необхідні фракції збирали, а розчинник випаровуПриклад A10 вали. Концентрат випаровували разом з ЕтАц, Суміш проміжної сполуки (15) (0,0045моль) та вихід - 11,7г 3,5-дихлоро-4-[1-[5-(2-метилфеніл)NaOH (0,0135моль) в метанолі (30мл) та ТГФ 1,2,4-оксадіазол-3-іл]-1-метилетил]бензоламін (30мл) перемішували при кімнатній температурі (проміжна сполука 19). протягом 12 годин, поміщали на лід, підкислювали d) Розчин проміжної сполуки (19) (0,0302моль) НСl та екстрагували ЕтАц. Органічний шар відота концентрованої НСl (0,0906моль) в оцтовій кискремлювали, висушували (MgSO4), профільтровулоті (100мл) перемішували при 0°С. Краплинно вали, а розчинник випаровували. Залишок (2,2г) при температурі 0°С додавали розчин NaNO2 очищували шляхом колонкової хроматографії на (0,032моль) у воді (10мл). Реакційну суміш пересилікагелі (елюент: СН2Сl2/СН3ОН/NН4ОН 95/5/0,1; мішували протягом 1 години при 0°С. Окремими 15-40 м). порціями вносили порошкоподібну суміш ацетату Чисті фракції збирали, а розчинник випаровунатрію (0,0906моль) та діетил (1,3-діоксо-1,3вали, вихід - 1,5г (64%) продукту, частина якого пропандіїл)біскарбамату (0,0332моль). Суміші да(1г), кристалізували з діетилового ефіру. Преципівали нагрітися до КТ та перемішували протягом 1 тат відфільтровували та висушували, вихід - 0,5г години. Додавали воду і цю суміш екстрагували проміжної сполуки 16, точка плавлення якої 192°С, СН2Сl2. Відокремлений органічний шар висушувасполука описується формулою ли, фільтрували, а розчинник випаровували, вихід - діетил N,N'-[2-[[3,5-дихлоро-4-[1-[5-(метилфеніл)1,2,4-оксадіазол-3-іл]-1метилетил]феніл]гідразоно]-1,3-діоксо1,3пропандіїл]дикарбамат (проміжна сполука 20). е) Розчин проміжної сполуки (20) (0,0302моль) та ацетату натрію (0,0302моль) в оцтовій кислоті (200мл) перемішували та дефлегмували протягом 3 годин. Реакційну суміш переливали у воду і отриману суміш екстрагували СН2СІ2. Відокремлений органічний шар висушували, фільтрували, а Приклад A11 розчинник випаровували. Додавали толуол, після a) 30% NAОСН3 (0,592моль) додавали до розчого проводилося азеотропне зневоднювання на чину гідроксиламіну гідрохлориду (0,1085моль) в ротаційному випарнику, вихід - етил [[2-[3,5СН3ОН (200мл), перемішували при КТ. Суміш педихлоро-4-[1-[5-(2-метилфеніл)-1,2,4-оксадіазол-3ремішували протягом 10 хвилин. Проміжну сполуіл]-1-метилетил]феніл]-2,3,4,5-тетрагідро-3,5ку (3) (0,0542моль) додавали порціями, утворену діоксо-1,2,4-тріазин-6-іл]карбоніл]карбамат (прореакційну суміш перемішували та дефлегмували міжна сполука 21). 55 74791 56 f) Суміш проміжної сполуки (21) (0,0302моль) в HOАс (50мл), H2SO4 (50мл) та Н2О (50мл) перемі36% НСl (10мл) та оцтовій кислоті (200мл) перешували та дефлегмували протягом 2 годин. Реакмішували та дефлегмували протягом ночі. Реакційну суміш переливали в талу воду, утворений ційну суміш переливали на подрібнений лід, після преципітат відфільтровували, промивали та розчого цю суміш екстрагували СH2Сl2. Відокремлечиняли в СН2СІ2. Органічний розчин висушували, ний органічний шар висушували, фільтрували, а фільтрували, а розчинник випаровували. Залишок розчинник випаровували, вихід- 16,3г 2-[3,5очищували над силікагелем в скляному фільтрі дихлоро-4-[1-[5-[2-метилфеніл)-1,2,4-оксадіазол-3(елюент: СН2СІ2/СН3ОН 95/5). Необхідні фракції іл]-1-метилетил]феніл]-2,3,4,5-тетрагідро-3,5збирали, а розчинник випаровували. Залишок діоксо-1,2,4-тріазин-6-карбонова кислота (проміжочищували шляхом високочутливої рідинної хрона сполука 22). матографії над RB BDS Нурегргер С18 (100Å, 8 м; Приклад A12 градієнтна елюція при (0,5% NH4OAc у воді/СН3СN Суміш проміжної речовини (22) (0,0133моль) в 90/10)/CH3OH/CH3CN). Чисті фракції збирали, а меркаптооцтовій кислоті (7мл) перемішували при розчинник випаровували. Залишок перемішували температурі 175°С протягом 2 годин. Суміш охоу гексані, відфільтровували та висушували в вакулоджували, переливали у талу воду, злужнювали умі при температурі 60°С, вихід - 0,084г проміжної К2СО3 та екстрагували ЕтАц. Органічний шар відосполуки 26, яка описується формулою кремлювали, промивали Н2О, висушували, фільтрували, а розчинник випаровували. Залишок очищували шляхом колонкової хроматографії на силікагелі (елюент: СН2Сl2/СН3OН 99/1). Чисті фракції збирали, а розчинник випаровували, вихід - 2,2г (36%) проміжної сполуки 23, яка описується формулою Приклад А16 Розчин проміжної сполуки (26) (0,0014моль) в SOCl2 (15мл) перемішували та дефлегмували протягом 1 години. SOCl2 випаровували під зниженим тиском. Додавали толуол, після чого проводилося азеотропне зневоднювання на ротаційному випарнику, вихід - 100% проміжна сполука 27, яка описується формулою Приклад A13 Суміш проміжної сполуки (23) (0,0011моль), 1бромо-2,5-пірроліндіону (0,0011моль) та дибензоїлпероксиду (каталітична кількість) в ССl4 (30мл) перемішували та дефлегмували протягом 3 годин. Суміші давали остигнути до КТ. Суміш фільтрували скрізь інфузорну землю, доступну на комерційному ринки під торговою назвою Дикаліт, отриманий фільтрат містив 2-[4-[1-[5-[2(бромометил)феніл]-1,2,4-оксадіазол-3-іл]-1метилетил]-3,5-дихлорфеніл]-1,2,4-тріазин3,5(2Н,4Н)-діон (проміжна сполука 24). Приклад А14 Розчин проміжної сполуки (24) (0,017моль) та KCN (0,034моль) в етанолі (100мл) та Н2О (30мл) перемішували протягом 8 годин при температурі 60°С. Розчинник випаровували під зниженим тиском. Залишок вносили в СН2Сl2, після чого промивали водою, висушували (MgSO4), фільтрували, а розчинник випаровували, вихід - 8,2г проміжної сполуки 25, що описується формулою Приклад A15 Розчин проміжної сполуки (25) (0,017моль) в В. Приготування кінцевих сполук Приклад В1 Суміш 3-бромдигідро-2(3Н)-фуранону (0,0081моль) в ДМФ (16мл) краплинко при кімнатній температурі додавали в суміш проміжної сполуки (10) (0,00773моль) та NaHCO3 (0,0081моль) в ДМФ (30мл). Суміш перемішували при 70°С протягом 5 годин та доводили до кімнатної температури. Додавали Н2О та насичений розчин NaCl. Суміш екстрагували ЕтАц. Органічний шар відокремлювали, висушували (MgSO4), фільтрували, а розчинник випаровували. Залишок (5г) очищували шляхом колонкової хроматографії на силікагелі (елюент: СН2Сl2/СН3OН 98/2; 15-40μΜ). Чисті фракції збирали, а розчинник випаровували. Залишок вносили в ДІПЕ. Преципітат відфільтровували та висушували, вихід - 1,24г сполуки 1, точка плавлення якої 72°С, сполука описується формулою 57 Приклад В2 Розчин 1-бромпентандекану (0,0051моль) в ДМФ (18мл) краплинно при кімнатній температурі додавали до суміші проміжної сполуки (10) (0,00483моль) та NaHCO3 (0,0051моль) в ДМФ (10мл). Суміш перемішували при температурі 70°С протягом 5 годин, а потім при 45°С цілу ніч, після чого доводили до кімнатної температури. Додавали Н2О та NaCl. Суміш екстрагували ЕтАц. Органічний шар відокремлювали, промивали насиченим розчином NaCl, висушували (MgSO4), фільтрували, а розчинник випаровували. Залишок (3,8г) очищували шляхом колонкової хроматографії на силікагелі (елюент: СН2СІ2/СН3ОН 98/2; 15-40 м). Чисті фракції збирали, а розчинник випаровували, вихід - 0,49г сполуки 2, яка має точку плавлення 80°С та описується формулою Приклад В4 NaHCO3 (0,00835моль) краплинно при температурі 5°С під током азоту додавали до суміші проміжної сполуки (14) (0,00795моль) в ДМФ (22мл). Після цього краплинно додавали розчин 3бромдигідро-2(3Н)-фуранону (0,00835моль) в ДМФ (12мл). Суміш доводили до КТ та перемішували при КТ протягом 30 хвилин, потім переливали у воду та насичений розчин NaCl. Додавали малу кількість 3Н НСl. Органічний шар відокремлювали, висушували (MgSO4), фільтрували, а розчинник випаровували. Залишок (5,1г) очищували шляхом колонкової хроматографії на силікагелі (елюент: СН2Сl2/СН3OН 98,5/1,5; 15-40 м). Чисті фракції збирали, а розчинник випаровували. Залишок кристалізували з CH3CN, діетилового ефіру та ДІПЕ. Преципітат відфільтровували та висушували. Залишок кристалізували з CH3CN, діетилового ефіру та ДІПЕ. Преципітат відфільтровували та висушували, вихід - 0,85г сполуки 4, яка має точку плавлення 212°С та описується формулою 74791 58 Приклад В3 Розчин 3-бромдигідро-2(3Н)-фуранону (0,0073моль) в ДМФ (12мл) краплинно при КТ додавали до суміші проміжної сполуки (13) (0,00695моль) та NaHCO3 (0,0073моль) в ДМФ (22мл). Суміш перемішували при температурі 70°С на протязі 2,5 годин, доводили до КТ та переливали в Н2О. Преципітат відфільтровували та вносили в СН2СІ2. Органічний шар відокремлювали, промивали Н2О, висушували (MgSO4), фільтрували, а розчинник випаровували. Залишок (5,4г) очищували шляхом колонкової хроматографії на силікагелі (елюент: СH2Сl2/СН3ОН 98/2; 15-40 м). Необхідні фракції збирали, а розчинник випаровували. Залишок кристалізували з CH3CN, діетиловим ефіром та ДІПЕ. Преципітат відфільтровували та висушували. Вихід 1,3г. Цю фракцію викристалізовували з CH3CN, 2-пропанону та діетилового ефіру. Преципітат відфільтровували та висушували, вихід - 0,89г сполуки 3, яка має точку плавлення 208°С та описується формулою Приклад В5 Суміш 3-бромдигідро-2(3Н)-фуранону (0,00172моль) в ДМФ (5мл) краплинно при КТ додавали в суміш проміжної сполуки (16) (0,00172моль) тa NaHCO3 (0,00172моль) в ДМФ (5мл). Суміш перемішували при 70°С протягом 7 годин, після чого виливали у воду та насичений розчин NaCl і екстрагували ЕтАц. Органічний шар відокремлювали, промивали декілька разів водою, висушували (MgSO4), фільтрували, а розчинник випаровували. Залишок (1,2г) очищували шляхом колонкової хроматографії на силікагелі (елюент: СН2Сl2/СН3ОН 98/2; 15-40μΜ). Необхідні фракції збирали, а розчинник випаровували. Залишок знову очищували шляхом колонкової хроматографії на силікагелі (елюент: СН2Сl2/2-пропанол 97/3; 1540μΜ). Необхідні фракції збирали, а розчинник випаровували, вихід - 0,13г сполуки 5, яка має точку плавлення 110°С та описується формулою 59 Приклад В6 Розчин проміжної сполуки (27) (0,001моль) в етанолі (15мл) та дихлорметані (15мл) перемішували та дефлегмували протягом 1 години. Розчинник випаровували під зниженим тиском. Залишок розчиняли в СН2Сl2, промивали водою, висушували (MgSO4), фільтрували, а розчинник випаровували. Залишок очищували способом високочутливої рідинної хроматографії над Нурегргер С18 (елюент: ((0,5% NH4OAc в H2O)/CH3CN 90/10)CH3CN (0 хвил) 80/20, (44хвил) 20/80, (5761хвил) 0/100). Необхідні фракції збирали, а розчинник випаровували. Залишок перемішували у гексані, відфільтровували, промивали та висушували у вакуумі при 60°С, вихід - 0,059г сполуки 6, яка має точку плавлення 157°С та описується формулою Приклад В7 Суміш проміжної сполуки (10) (0,00387моль) та 1,1 -карбонілбіс-1Н-імідазола (0,0058моль) в дихлорметані (40мл) перемішували при КТ протягом 90 хвилин, після чого додавали циклогексилметанол (0,0058моль). Суміш перемішували при КТ цілу ніч, розводили СН2Сl2 та двічі промивали водним розчином NaCl. Органічний шар відокремлювали, висушували (MgSO4), фільтрували, а розчинник випаровували. Залишок очищували шляхом колонкової хроматографії на силікагелі (елюент: СН2Сl2/ЕтАц 50/50). Чисті фракції збирали, а розчинник випаровували. Залишок кристалізували з ЕтАц. Преципітат відфільтровували, промивали ДІПЕ та висушували при 50°С протягом ночі, вихід - 1,43г сполуки 7, яка має молекулярну вагу 613,5, точку плавлення 180°С та описується формулою де R14 представлений циклогексилметилом. Зразки від В8 до В53 У наведеній нижче таблиці 1 представлені 74791 60 сполуки формули (1А), які було приготовлено у відповідності до методики зразка В7, де циклогексилметанол, відновлений відповідним спиртом, представлений формулою R14ОН. Для синтезу сполук 8, 15-18, 21-23, 27, 32-34, 40-42 та 44 кількість дихлорметану збільшували до 50мл, а для сполуки 53 - до 60мл. Для синтезу сполуки 51 дихлорметан замінили 45мл ДМФ. В цій таблиці також вказано точки плавлення (у випадках, коли це можливо) - Т.П. (в °С) та вихід згаданих сполук - В (виражений у відсотках).
ДивитисяДодаткова інформація
Назва патенту англійською6-azauracil derivatives suppressing interleukin-5, a method for producing thereof, a composition based thereon and a method for producing thereof
Автори англійськоюFreyne Eddy Jean Edgard
Назва патенту російськоюПроизводные 6-азаурацила, угнетающие интерлейкин-5, способ их получения, композиция на их основании и способ ее получения
Автори російськоюФрейне Эдди Жан Эдгар
МПК / Мітки
МПК: A61P 37/08, A61P 17/06, C07D 417/10, A61K 31/5377, A61P 11/08, A61P 1/02, C07D 413/10, A61P 27/16, A61P 11/06, A61P 43/00, A61P 27/02, C07D 417/14, A61K 51/04, A61P 1/04, A61P 15/02, A61K 31/53
Мітки: композиція, спосіб, інтерлейкін-5, пригнічують, основі, одержання, 6-азаурацилу, похідні
Код посилання
<a href="https://ua.patents.su/50-74791-pokhidni-6-azauracilu-shho-prignichuyut-interlejjkin-5-sposib-kh-oderzhannya-kompoziciya-na-kh-osnovi-ta-sposib-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Похідні 6-азаурацилу, що пригнічують інтерлейкін-5, спосіб їх одержання, композиція на їх основі та спосіб її одержання</a>
Попередній патент: Спосіб лікування радіаційних ушкоджень кровоносних судин в експерименті
Наступний патент: Реверсивний стан для виробництва тонкої гарячекатаної штаби
Випадковий патент: Заміщені піридинони як модулятори р38 мар кінази