Морфолінотіазоли як позитивні алостеричні модулятори альфа 7
Номер патенту: 106636
Опубліковано: 25.09.2014
Автори: де Бек Бенойт Крістіан Альберт Гіслейн, Лінаертс Джозеф Елизабет, МакДональд Грегор Джеймс
Формула / Реферат
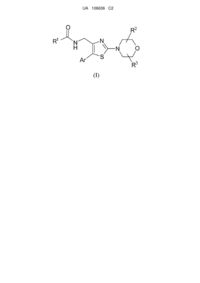
1. Сполука, що має формулу (І)
 , (І)
, (І)
або її стереохімічний ізомер, де
R1 є С1-6алкілом, С1-6алкілом, заміщеним 1, 2 або 3 галогеновими замісниками, С1-6алкілом, заміщеним 1 ціаногрупою, С1-6алкілом, заміщеним 1 гетероарильною групою, С3-6циклоалкілом, С3-6циклоалкілом, заміщеним 1, 2, 3 або 4 метильними групами, С3-6циклоалкілом, заміщеним 1 гідроксигрупою, (С3-6циклоалкіл)С1-6алкілом, (С1-6алкілоксі)С1-6алкілом, (галогенС1-4алкілоксі)С1-6алкілом, тетрагідрофурилом, арилом, гетероарилом, піролідинілом, піролідинілом, заміщеним 1 С1-4алкільною групою, або тетрагідрофурилом, заміщеним 1, 2 або 3 замісниками, вибраними з метилу і оксо;
арил є 2,2-дифтор-1,3-бензодіоксолілом; фенілом або фенілом, заміщеним 1, 2 або 3 замісниками, вибраними з галогену, трифторметилу, трифторметокси, ціано, С1-6алкілу, С1-4алкілокси і аміносульфонілу;
гетероарил є моно- або біциклічним ароматичним гетероциклічним радикалом, що містить щонайменше один гетероатом, вибраний з N, О і S, необов'язково заміщений 1, 2 або, коли можливо, 3 замісниками, вибраними з С1-4алкілу, С1-4алкілокси, С3-6циклоалкілу і трифторметилу;
R2 і R3 незалежно є Н, С1-4алкілом або трифторметилом;
або R2 і R3 узяті разом з утворенням 1,2-етандіїлу або 1,3-пропандіїлу;
Аr є 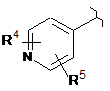 або
або 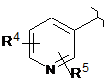 ;
;
R4 і R5 незалежно є H, С1-4алкілом, трифторметилом, С3-6циклоалкілом або С1-4алкілокси;
або її кислотно-адитивна сіль, або її сольват.
2. Сполука за п. 1, в якій
R1 є С1-6алкілом, С1-4алкілом, заміщеним 3 атомами фтору, метилом, заміщеним 1 ціаногрупою, метилом, заміщеним 3,5-диметил-4-ізоксазолілом, метилом, заміщеним 3-метил-5-ізоксазолілом, С3-6циклоалкілом, циклопропілом, заміщеним 1, 2, 3 або 4 метильними групами, циклопропілом, заміщеним 1 гідроксигрупою, (С3-6циклоалкіл)С1-2алкілом, метоксиметилом, метоксіетилом, (2,2,2-трифторетокси)метилом, тетрагідрофурилом, арилом, гетероарилом, піролідинілом, заміщеним 1 метильною групою, або тетрагідрофурилом, заміщеним 3 замісниками, вибраними з метилу і оксо;
арил є 2,2-дифтор-1,3-бензодіоксол-5-ілом; 2,2-дифтор-1,3-бензодіоксол-4-ілом; фенілом або фенілом, заміщеним 1, 2 або 3 замісниками, вибраними з фтору, хлору, трифторметилу, трифторметокси, ціано, метилу, метокси і аміносульфонілу;
гетероарил є фуранілом, оксазолілом, ізоксазолілом, оксадіазолілом, піролілом, піразолілом, імідазолілом, піридинілом, піримідинілом, піразинілом, піридазинілом, тієнілом, 1,2,3-тіадіазолілом, тіазолілом або бензізоксазолілом, кожен з яких не заміщений або заміщений 1, 2 або, коли можливо, 3 замісниками, вибраними з метилу, етилу, пропілу, ізопропілу, бутилу, ізобутилу, трет-бутилу, циклопропілу, метокси і трифторметилу.
3. Сполука за п. 1, в якій R2 є воднем або метилом.
4. Сполука за п. 1, в якій R3 є метилом.
5. Сполука за п. 1, в якій R4 є Н, метилом, трифторметилом, циклопропілом або метокси.
6. Сполука за п. 1, в якій R5 є воднем або метилом.
7. Сполука за п. 1, в якій
R1 є метилом, етилом, н-пропілом, ізопропілом, н-бутилом, ізобутилом, трет-бутилом, циклопропілом, 1-метилциклопропілом, 2,2,3,3-тетраметилпропілом, циклобутилом, циклопентилом, (циклопропіл)етилом, (циклопропіл)метилом, (циклобутил)метилом;
Het є 3-метилізоксазол-5-ілом, 3-метилізоксазол-4-ілом, 5-метилізоксазол-3-ілом, 2-метил-5-трифторметилоксазол-4-ілом, 2-метилоксазол-4-ілом.
8. Сполука за п. 1, в якій R2 і R3 є метилом і мають цис-конфігурацію.
9. Сполука за п. 1, в якій R5 є метилом.
10. Сполука за п. 1, яка вибрана з групи
N-[[2-[(2R,6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]циклопропанацетамід (сполука 1);
N-[2-[(2R,6S)-2,6-димeтил-4-мopфoлiнiл]-5-(2,6-димeтил-4-пipидинiл)-4-тіазоліл]метил]-3-метил-4-ізоксазолкарбоксамід (сполука 18);
N-[[2-[(2R,6S)-2,6-димeтил-4-мopфoлiнiл]-5-(2,6-димeтил-4-пipидинiл)-4-тіазоліл]метил]-3-метил-5-ізоксазолкарбоксамід (сполука 4) і
N-[[2-[(2R,6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]ацетамід (сполука 60).
11. Фармацевтична композиція, що містить як активний інгредієнт сполуку за будь-яким з пп. 1-10.
12. Продукт, що містить
(a) сполуку формули (І), визначену в п. 1, і
(b) агоніст нікотинового рецептора α7, вибраний з
моногідрохлориду 4-бромфенілового ефіру 1,4-діазабіцикло[3.2.2]нонан-4-карбонової кислоти (SSR180711А);
(-)-спіро-[1-азабіцикло[2.2.2]октан-3,5'-оксазолідин]-2'-ону;
(+)-N-(1-азабіцикло[2.2.2]окт-3-ил)бензо[b]фуран-2-карбоксаміду;
дигідрохлориду 3-[(2,4-диметокси)бензиліден]анабазеїну (GTS-21);
[гідрохлориду N-[(3R)-1-азабіцикло[2.2.2]окт-3-ил]-4-хлорбензаміду];
PNU-282987; нікотину; вареникліну; А-582941; AR-R17779; TС-1698; РНА-709829; тропізетрону; WAY-317538; МЕМ3454; EVP-6124; ТС-5619; МЕМ63908 і AZD-0328, як комбінований препарат для одночасного, роздільного або послідовного застосування для запобігання або лікування психотичних порушень, розумового розладу або запальних захворювань.
13. Сполука за будь-яким з пп. 1-10 для застосування як лікарського засобу.
14. Сполука за будь-яким з пп. 1-10, призначена для лікування хвороби Альцгеймера, деменції з тільцями Леві, синдрому дефіциту уваги, пов'язаного з гіперактивністю, тривожного стану, шизофренії, манії, біполярного розладу, хвороби Паркінсона, хвороби Хантінгтона, синдрому Жиля де ля Туретта, травми головного мозку, синдрому зміни часових поясів, нікотинової адикції, болю; ендотоксемії, ендотоксичного шоку, сепсису, ревматоїдного артриту, астми, розсіяного склерозу, псоріазу, кропив'янки, запального захворювання кишечнику, запального жовчного захворювання, хвороби Крона, неспецифічного виразкового коліту, післяопераційної непрохідності кишечнику, панкреатиту, серцевої недостатності, гострого легеневого пошкодження або відторгнення трансплантата; порушення пізнавальної здатності при шизофренії, порушення пізнавальної здатності при хворобі Альцгеймера, слабкої недостатності пізнавальної здатності, хвороби Паркінсона, синдрому дефіциту уваги, пов'язаного з гіперактивністю, неспецифічного виразкового коліту, панкреатиту, артриту, сепсису, післяопераційної непрохідності кишечнику або гострого легеневого пошкодження.
15. Спосіб отримання фармацевтичної композиції за п. 11, в якому здійснюють стадію ретельного змішування фармацевтично прийнятного носія з терапевтично ефективною кількістю сполуки за будь-яким з пп. 1-10.
Текст
Реферат: Даний винахід стосується похідних морфолінотіазолу і їх фармацевтично прийнятних солей, способів їх отримання, фармацевтичних композицій, що їх містять, і їх застосування в терапії. Винахід конкретно стосується позитивних алостеричних модуляторів нікотинових рецепторів ацетилхоліну, причому такі позитивні алостеричні модулятори мають здатність підвищувати ефективність агоністів нікотинових рецепторів. UA 106636 C2 (12) UA 106636 C2 UA 106636 C2 5 10 15 20 25 30 35 40 45 50 55 60 Область техніки, до якої відноситься винахід Даний винахід відноситься до похідних морфолінотіазола і їх фармацевтично прийнятним солям, способам їх отримання, фармацевтичним композиціям, що їх містять і їх застосуванню в терапії. Винахід конкретно відноситься до позитивних аллостеричних модуляторів нікотинових рецепторів ацетилхоліну, причому такі позитивні аллостеричні модулятори мають здатність підвищувати ефективність агоністів нікотинових рецепторів. Відомий рівень техніки У WO-2004/091480 описані похідні триазолу, які інгібують, регулюють та/або модулюють кінази, конкретно Tie-2, які можуть бути корисні для лікування або запобігання ракового і пов'язаного з раком захворювання. Рівень техніки винаходу Холінергічні рецептори зазвичай зв'язують ендогенний нейромедіаторний ацетилхолін (Аch), тим самим запускаючи відкриття іонних каналів. Рецептори АСh у центральній нервовій системі ссавців можна розділити на мускаринові (mAChR) і нікотинові (nAChR) підтипи на основі активностей агоністів мускарину і нікотину, відповідно. Нікотинові рецептори ацетилхоліну є відкриваємими лігандами іонними каналами, що містять п'ять субодиниць. Члени сімейства генів субодиниць nAChR розділені на дві групи на основі їх амінокислотної послідовності; причому одна група містить так звані альфа-субодиниці і друга група містить бета-субодиниці. Показано, що три типи альфа-субодиниць, альфа 7, альфа 8 і альфа 9, утворюють функціональні рецептори при експресуванні окремо, і таким чином, як передбачається, утворюють гомоолігомерні пентамерні рецептори. Була розроблена модель аллостеричного перехідного стану nAChR, яка включає щонайменше стан спокою, активований стан і стан "десенсибілізованого" закритого каналу, процесу, за допомогою якого рецептори стають нечутливими до агоніста. Різні ліганди nAChR можуть стабілізувати конформаційний стан рецептора, з яким вони бажано зв'язуються. Наприклад, агоністи AСh і (-)-нікотина, відповідно, стабілізують активні і десенсибілізовані стани. Зміни активності нікотинових рецепторів беруть участь у ряді захворювань. Деякі з них, наприклад, важка міастенія і аутосомальна домінантна нічна лобова епілепсія (ADNFLE), пов'язані із зниженнями активності нікотинового перенесення або внаслідок зменшення кількості рецепторів, або внаслідок підвищеної десенсибілізації. Була висловлена також гіпотеза, що зменшення нікотинових рецепторів опосередковує когнітивні дефіцити, що спостережуються в таких захворюваннях, як хвороба Альцгеймера і шизофренія. Дії нікотину з тютюну також опосередковуються нікотиновими рецепторами і так як дія нікотину повинна стабілізувати рецептори в десенсибілізованому стані, підвищена активність нікотинових рецепторів може зменшувати потяг до паління. Сполуки, які зв'язують nAChR, запропоновані для лікування ряду порушень, що включають знижену холінергічну функцію, таких як недостатність навчаємості, порушення пізнавальної здатності, синдром дефіциту уваги і втрата пам'яті. Передбачається, що модуляція активності нікотинового рецептора альфа 7 є корисною при ряду захворювань, що включають хворобу Альцгеймера, деменцію з тільцями Леві, синдром дефіциту уваги, пов'язаний з гіперактивністю, тривожний стан, шизофренію, манію, біполярний розлад, хворобу Паркінсона, хворобу Хантінгтона, синдром Жиля де ля Туретта, травму головного мозку і інші неврологічні, дегенеративні і психіатричні порушення, при яких є втрата холінергічних синапсів, у тому числі синдром зміни часових поясів, нікотинова аддикція і біль. Проте, лікування агоністами нікотинових рецепторів, які діють у тому ж сайті, що і ACh, є проблематичним, оскільки АСh не лише активує, але також і блокує активність рецептора за допомогою процесів, які включають десенсибілізацію і неконкурентну блокаду. Крім того, виявляється, що пролонгована активація індукує тривалу інактивацію. Тому передбачається, що агоністи AСh втрачають ефективність при постійному введенні. У нікотинових рецепторів загалом і, як особливо відмічено, у нікотинового рецептора альфа 7 десенсибілізація обмежує тривалість дії агоніста, що застосовується. Опис винаходу Авторами винаходу виявлено, що деякі похідні морфолінотіазола можуть підвищувати ефективність агоністів при нікотинових рецепторах ацетилхоліну (nAChR). Сполуки, що мають цей тип дії (що надалі називаються "позитивними аллостеричними модуляторами"), ймовірно є корисними для лікування станів, пов'язаних із зменшеннями в нікотиновому перенесенні. При терапевтичному застосуванні такі сполуки можуть відновлювати нормальну межнейрональную передачу без дії на тимчасовий профіль активації. Крім того, передбачається, що позитивні 1 UA 106636 C2 5 10 15 20 25 30 35 40 45 аллостеричні модулятори продукують тривалу інактивацію рецепторів, яка може мати місце при пролонгованому застосуванні агоністів. Позитивні модулятори nAChR даного винаходу є корисними для лікування і профілактики психотичних порушень, порушень і захворювань типа розумової недостатності, запальних захворювань і станів, для яких корисною є модуляція нікотинового рецептора альфа 7. Даний винахід відноситься до похідних морфолінотіазола, що мають властивості позитивних аллостеричних модуляторів, зокрема, таким, що підвищують ефективність агоністів при нікотиновому рецепторі альфа 7. Винахід далі відноситься до способів їх отримання і фармацевтичним композиціям, що їх містять. Винахід відноситься також до застосування цих похідних для виготовлення лікарського засобу для лікування і профілактики психотичних порушень, порушень і захворювань типа розумової недостатності, запальних захворювань і станів, для яких корисною є модуляція нікотинового рецептора альфа 7. Винахід далі відноситься до цих похідних, що застосовуються при лікуванні і профілактиці психотичних порушень, порушень і захворювань типа розумової недостатності, запальних захворювань і станів, для яких корисною є модуляція нікотинового рецептора альфа 7. Сполуки даного винаходу відрізняються структурно від сполук відомого рівня техніки і не проявляють активність відносно кіназ. У першому аспекті даний винахід відноситься до сполуки, що має формулу (I) або її стереохімічному ізомеру, де 1 R є С1-6алкілом, С3-6циклоалкілом, С3-6циклоалкілом, заміщеним 1, 2, 3 або 4 метильними групами, (С3-6циклоалкіл)С1-6алкілом, (С1-6алкілокси)С1-6алкілом, тетрагідрофурилом, арилом або гетероарилом; арил є 2,2-дифторбензодіоксанілом; фенілом або фенілом, заміщеним 1, 2 або 3 замісниками, вибраними з галогену, трифторметила, трифторметокси, ціано, С1-6алкіла, С14алкілокси і аміносульфонілу; гетероарил є моно- або біциклічним ароматичним гетероциклічним радикалом, що містить щонайменше один гетероатом, вибраний з N, O і S, необов'язково заміщений 1, 2 або, коли можливо, 3 замісниками, вибраними з С1-4алкіла, С1-4алкілокси, С3-6циклолкила або трифторметила; 2 3 R і R незалежно є H або С1-4алкілом; Ar є 4 5 R і R незалежно є H, С1-4алкілом, С3-6циклоалкілом або С1-4алкілокси; або її кислотно-аддитивній солі або її сольвату. 1 В одному прикладі R є С1-4алкілом, С3-6циклоалкілом, циклопропілом, заміщеним 1, 2, 3 або 4 метильними групами, (C3-6циклоалкіл)С1-2алкілом або метоксиметилом; арил є фенілом, заміщеним 1, 2 або 3 замісниками, вибраними з фтору, хлору, метилу, метокси, трифторметилу, трифторметокси, ціано і аміносульфонілу; гетероарил є фуранілом, оксазолілом, ізоксазолілом, оксадіазолілом, пірролілом, піразолілом, імідазолілом, піридинілом, піримідинілом, піразинілом, піридазинілом або бензізоксазолілом, кожен з яких не заміщений або заміщений 1, 2 або, коли можливо, 3 замісниками, вибраними з метилу, етилу, пропілу, ізопропілу, бутилу, ізобутилу, трет-бутилу, циклопропілу, метокси або трифторметила. 2 В іншому прикладі R є воднем або метилом. 2 UA 106636 C2 3 5 10 15 20 25 30 35 40 У іншому прикладі R є метилом. 4 У іншому прикладі R є воднем, метилом, циклопропілом або метокси. 5 В іншому прикладі R є воднем або метилом. 1 У іншому прикладі R є метилом, етилом, н-пропілом, ізопропілом, н-бутилом, ізобутилом, трет-бутилом, циклопропілом, 1-метилциклопропілом, 2,2,3,3-тетраметилпропілом, циклобутилом, циклопентилом, (циклопропіл)етилом, (циклопропіл)метилом, (циклобутил)метилом; Het є 3-метил-ізоксазол-5-ілом, 3-метилізоксазол-4-ілом, 5-метилізоксазол-3-ілом, 2-метил5-трифторметилоксазол-4-ілом, 2-метилоксазол-4-ілом. 2 3 У іншому прикладі R і R є метилом і мають цис-конфігурацію. 4 В іншому прикладі R є воднем, метилом, циклопропілом або метокси. 5 В іншому прикладі R є метилом. Конкретними сполуками є N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]циклопропанацетамід; N-[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]-3метил-4-ізоксазолкарбоксамід; N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]-3метил-5-ізоксазолкарбоксамід і N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]ацетамід. У другому аспекті даний винахід відноситься до сполуки, що має формулу (I) або її стереохімічному ізомеру, де 1 R є С1-6алкілом, С1-6алкілом, заміщеним 1, 2 або 3 галогеновими замісниками, С 1-6алкілом, заміщеним 1 ціаногрупою, С1-6алкілом, заміщеним 1 гетероарильною групою, C 3-6циклоалкілом, C3-6циклоалкілом, заміщеним 1, 2, 3 або 4 метильними групами, C 3-6циклоалкілом, заміщеним 1 гідроксигрупою, (C3-6циклоалкіл)С1-6алкілом, (С1-6алкілокси)С1-6алкілом, (галогенС1-4алкілокси)С1тетрагідрофурилом, арилом, гетероарилом, пірролідинілом, пірролідинілом, 6алкілом, заміщеним 1 С1-4алкільною групою, або тетрагідрофурилом, заміщеним 1, 2 або 3 замісниками, вибраними з метилу і оксо; арил є 2,2-дифтор-1,3-бензодіоксолілом; фенілом або фенілом, заміщеним 1, 2 або 3 замісниками, вибраними з галогену, трифторметила, трифторметокси, ціано, С 1-6алкілу, С14алкілокси і аміносульфонілу; гетероарил є моно- або біциклічним ароматичним гетероциклічним радикалом, що містить щонайменше один гетероатом, вибраний з N, O і S, необов'язково заміщений 1, 2 або, коли можливо, 3 замісниками, вибраними з С1-4алкіла, С1-4алкілокси, C3-6циклоалкіла і трифторметила; 2 3 R і R незалежно є H, С1-4алкілом або трифторметил; 2 3 або R і R взяті разом з утворенням 1,2-етандіїла або 1,3-пропандіїла; Ar є 4 45 5 R і R незалежно є H, С1-4алкілом, трифторметилом, C3-6циклоалкілом або С1-4алкілокси; або її кислотно-аддитивній солі або її сольвату. 1 В одному прикладі R є С1-4алкілом, C3-6циклоалкілом, циклопропілом, заміщеним 1, 2, 3 або 3 UA 106636 C2 5 10 15 20 25 30 35 40 45 50 55 4 метильними групами, (C3-6циклоалкіл)С1-2алкілом або метоксиметилом; арил є фенілом, заміщеним 1, 2 або 3 замісниками, вибраними з фтору, хлору, метилу, метокси, трифторметилу, трифторметокси, ціано і аміносульфонілу; гетероарил є фуранілом, оксазолілом, ізоксазолілом, оксадіазолілом, пірролілом, піразолілом, імідазолілом, піридинілом, піримідинілом, піразинілом, піридазинілом або бензізоксазолілом, кожен з яких не заміщений або заміщений 1, 2 або, коли можливо, 3 замісниками, вибраними з метилу, етилу, пропілу, ізопропілу, бутилу, ізобутилу, трет-бутилу, циклопропілу, метокси і трифторметилу. В іншому прикладі 1 R є С1-6алкілом, С1-4алкілом, заміщеним 3 атомами фтору, метилом, заміщеним 1 ціаногрупою, метилом, заміщеним 3,5-диметил-4-ізоксазолілом, метилом, заміщеним 3-метил-5ізоксазолілом, C3-6циклоалкілом, циклопропілом, заміщеним 1, 2, 3 або 4 метильними групами, циклопропілом, заміщеним 1 гідроксигрупою, (C3-6циклоалкіл)С1-2алкілом, метоксиметилом, метоксиетилом, (2,2,2-трифторетокси)метилом, тетрагідрофурилом, арилом, гетероарилом, пірролідинілом, заміщеним 1 метильною групою, або тетрагідрофурилом, заміщеним 3 замісниками, вибраними з метилу і оксо; арил є 2,2-дифтор-1,3-бензoдіоксол-5-ілом; 2,2-дифтор-1,3-бензoдіоксол-4-іл; фенілом або фенілом, заміщеним 1, 2 або 3 замісниками, вибраними з фтору, хлору, трифторметилу, трифторметокси, ціано, метилу, метокси і аміносульфонілу; зокрема, арил є фенілом, заміщеним 1, 2 або 3 замісниками, вибраними з фтору, хлору, трифторметилу, трифторметокси, ціано, метилу, метокси і аміносульфонілу; гетероарил є фуранілом, оксазолілом, ізоксазолілом, оксадіазолілом, пірролілом, піразолілом, імідазолілом, піридинілом, піримідинілом, піразинілом, піридазинілом, тієнілом, 1,2,3-тіадіазолілом, тіазолілом або бензізоксазолілом, кожен з яких не заміщений або заміщений 1, 2 або, коли можливо, 3 замісниками, вибраними з метилу, етилу, пропілу, ізопропілу, бутилу, ізобутилу, трет-бутилу, циклопропілу, метокси і трифторметилу; зокрема, гетероарил є фуранілом, оксазолілом, ізоксазолілом, піразолілом, піридинілом, піразинілом, тієнілом, 1,2,3-тіадіазолілом, тіазолілом або бензізоксазолілом, кожен з яких не заміщений або заміщений 1, 2 або, коли можливо, 3 замісниками, вибраними з метилу, ізопропілу, трет-бутилу, циклопропілу, метокси і трифторметилу. В іншому прикладі 1 R є С1-6алкілом, С1-4алкілом, заміщеним 3 атомами фтору, метилом, заміщеним 1 ціаногрупою, метилом, заміщеним 3,5-диметил-4-ізоксазолілом, метилом, заміщеним 3-метил-5ізоксазолілом, С3-6циклоалкілом, циклопропілом, заміщеним 1, 2, 3 або 4 метильними групами, циклопропілом, заміщеним 1 гідроксигрупою, (C 3-6циклоалкіл)С1-2алкілом, метоксиметилом, метоксиетилом, (2,2,2-трифторетокси)метилом, тетрагідрофурилом, арилом, гетероарилом, пірролідинілом,заміщеним 1 метильною групою, або тетрагідрофурилом, заміщеним 3 замісниками, вибраними з метилу і оксо; арил є 2,2-дифтор-1,3-бензoдіоксол-5-ілом; 2,2-дифтор-1,3-бензoдіоксол-4-ілом; фенілом або фенілом, заміщеним 1, 2 або 3 замісниками, вибраними з фтору, хлору, трифторметилу, трифторметокси, ціано, метилу, метокси і аміносульфонілу; зокрема, арил є фенілом, заміщеним 1, 2 або 3 замісниками, вибраними з фтору, хлору, трифторметилу, трифторметокси, ціано, метилу, метокси і аміносульфонілу; гетероарил є фуранілом, оксазолілом, ізоксазолілом, оксадіазолілом, пірролілом, піразолілом, імідазолілом, піридинілом, піримідинілом, піразинілом, піридазинілом, тієнілом, 1,2,3-тіадіазолілом, тіазолілом або бензізоксазолілом, кожен з яких не заміщений або заміщений 1, 2 або, коли можливо, 3 замісниками, вибраними з метилу, етилу, пропілу, ізопропілу, бутилу, ізобутилу, трет-бутилу, циклопропілу, метокси і трифторметила; зокрема, гетероарил є фуранілом, оксазолілом, ізоксазолілом, піразолілом, піридинілом, піразинілом, тієнілом, 1,2,3-тіадіазолілом, тіазолілом або бензізоксазолілом, кожен з яких не заміщений або заміщений 1, 2 або, коли можливо, 3 замісниками, вибраними з метилу, ізопропілу, трет-бутилу, циклопропілу, метокси і трифторметилу; 2 3 R і R є незалежно H, метилом або трифторметилом; 2 3 або R і R узяті разом з утворенням 1,2-етандіїла; Ar є 4 UA 106636 C2 4 5 10 15 20 25 30 35 40 45 5 R і R є незалежно H, метилом, трифторметилом, циклопропілом або метокси. 2 В іншому прикладі R є воднем або метилом. 3 У іншому прикладі R є метилом. 4 У іншому прикладі R є воднем, метилом, циклопропілом або метокси. 5 У іншому прикладі R є воднем або метилом. 1 У іншому прикладі R є метилом, етилом, н-пропілом, ізопропілом, н-бутилом, ізобутилом, трет-бутилом, циклопропілом, 1-метилциклопропілом, 2,2,3,3-тетраметилпропілом, циклобутилом, циклопентилом, (циклопропіл)етилом, (циклопропіл)метилом, (циклобутил)метилом; Het є 3-метилізоксазол-5-ілом, 3-метилізоксазол-4-ілом, 5-метилізоксазол-3-ілом, 2-метил-5трифторметилоксазол-4-ілом, 2-метилоксазол-4-ілом. 1 У іншому прикладі R є метилом, етилом, н-пропілом, ізопропілом, н-бутилом, ізобутилом, трет-бутилом, циклопропілом, 1-метилциклопропілом, 2,2,3,3-тетраметилциклопропілом, циклобутилом, циклопентилом, (циклопропіл)етилом, (циклопропіл)метилом, (циклобутил)метилом; Het є 3-метилізоксазол-5-ілом, 3-метилізоксазол-4-ілом, 5метилізоксазол-3-ілом, 2-метил-5-трифторметилоксазол-4-ілом, 2-метилоксазол-4-ілом. 1 У іншому прикладі R є циклопропілом або 3-метил-4-ізоксазолілом; зокрема, 3-метил-4ізоксазолілом. 1 У іншому прикладі R є С1-6алкілом, С1-6алкілом, заміщеним 1, 2 або 3 галогеновими замісниками, С1-6алкілом, заміщеним 1 ціаногрупою, С1-6алкілом, заміщеним 1 гетероарильною групою, C3-6циклоалкілом, C3-6циклоалкілом, заміщеним 1, 2, 3 або 4 метильними групами, C 36циклоалкілом, заміщеним 1 гідроксигрупою, (C 3-6циклоалкіл)С1-6алкілом, (С1-6алкілокси)С1(галогенС1-4алкілокси)С1-6алкілом, тетрагідрофурилом, арилом, гетероарилом, 6алкілом, пірролідинілом, пірролідинілом, заміщеним 1 С1-4алкільною групою, або тетрагідрофурилом, заміщеним 1 оксогрупою і 1 або 2 метильними групами. 2 3 В іншому прикладі R і R є метилом і мають цис-конфігурацію. 2 3 В іншому прикладі R і R є метилом і мають транс-конфігурацію. 2 3 2 3 В іншому прикладі R і R є незалежно H, С1-4алкілом або трифторметилом; зокрема, R і R незалежно є H, метилом або трифторметилом. 2 3 2 3 У іншому прикладі R і R незалежно є H, С1-4алкілом або трифторметилом або R і R взяті разом з утворенням 1,2-етандіїла; 2 3 зокрема, R і R незалежно є H, метилом або трифторметилом 2 3 або R і R взяті разом з утворенням 1,2-етандіїла. 4 5 В іншому прикладі R і R незалежно є H, метилом, трифторметилом, циклопропілом або метокси. 2 3 В іншому прикладі R і R незалежно є H, метилом або трифторметилом; 4 5 і R і R незалежно є H, метилом, трифторметилом, циклопропілом або метокси. 2 3 В іншому прикладі R і R незалежно є H, метилом або трифторметилом 2 3 або R і R взяті разом з утворенням 1,2-етандіїла 4 5 і R і R незалежно є H, метилом, трифторметилом, циклопропілом або метокси. 4 В іншому прикладі R є H, метилом, трифторметилом, циклопропілом або метокси, зокрема, H, метилом, циклопропілом або метокси. 5 В іншому прикладі R є метилом. 4 5 У іншому прикладі R і R є метилом. У іншому прикладі Ar є У іншому прикладі Ar є 5 UA 106636 C2 5 10 15 20 25 30 35 40 45 У іншому прикладі гетероарил є фуранілом, оксазолілом, ізоксазолілом, оксадіазолілом, пірролілом, піразолілом, імідазолілом, піридинілом, піримідинілом, піразинілом, піридазинілом, тієнілом, 1,2,3-тіадіазолілом, тіазолілом або бензізоксазолілом, кожен з яких не заміщений або заміщений 1, 2 або, коли можливо, 3 замісниками, вибраними з метилу, етилу, пропілу, ізопропілу, бутилу, ізобутилу, трет-бутилу, циклопропілу, метокси і трифторметилу; конкретніше, гетероарил є фуранілом, оксазолілом, ізоксазолілом, піразолілом, піридинілом, піразинілом, тієнілом, 1,2,3-тіадіазолілом, тіазоліл або бензізоксазолілом, кожен з яких не заміщений або заміщений 1, 2 або, коли можливо, 3 замісниками, вибраними з метилу, ізопропілу, трет-бутилу, циклопропілу, метокси і трифторметила; У іншому прикладі 1 R є циклопропілом або 3-метил-4-ізоксазолілом; зокрема, 3-метил-4-ізоксазолілом; 2 3 R і R є метилом і мають цис-конфігурацію; Ar є Конкретними сполуками є N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]циклопропанацетамід; N-[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]-3метил-4-ізоксазолкарбоксамід; N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]-3метил-5-ізоксазолкарбоксамід і N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]ацетамід; у тому числі будь-яка їх стереохімічна ізомерна форма і їх килотно-аддитивні солі і сольвати. Конкретними сполуками є N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]циклопропанацетамід; N-[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]-3метил-4-ізоксазолкарбоксамід; N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]-3метил-5-ізоксазолкарбоксамід і N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]ацетамід. Конкретними сполуками є N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]циклопропанацетамід і N-[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]-3метил-4-ізоксазолкарбоксамід. Конкретною сполукою є N-[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]-3метил-4-ізоксазолкарбоксамід, у тому числі будь-яка її стереохімічна ізомерна форма, і її кислотно-аддитивні солі і сольвати. Конкретною сполукою є N-[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]-3метил-4-ізоксазолкарбоксамід. Вважається, що всі можливі комбінації вищезгаданих цікавих сполук включені в обсяг даного винаходу. 6 UA 106636 C2 5 10 15 20 25 30 35 40 45 50 55 60 При описі сполук даного винаходу застосовані терміни слід тлумачити згідно наступним визначенням, якщо в контексті не вказується інакше. Термін "гало" або "галоген" як група або частина групи є родовим для фтору, хлору, брому, йоду, якщо не вказується інакше або ясно з контексту. Термін "C1-6алкіл" як група або частина групи відноситься до вуглеводневого радикала формули CnH2n+1, у якій n дорівнює числу, що становить від 1 до 6. C 1-6алкільні групи містять від 1 до 6 атомів вуглецю, бажано, від 1 до 4 атомів вуглецю, бажаніше, від 1 до 3 атомів вуглецю, ще бажаніше, 1 або 2 атоми вуглецю. Алкільні групи можуть бути нерозгалуженими або розгалуженими і можуть бути заміщені, як вказано в контексті. Коли нижній індекс застосовують у контексті після атома вуглецю, такий індекс належить до атомів вуглецю, які може містити названа група. Так, наприклад, C1-6алкіл включає всі нерозгалужені або розгалужені алкільні групи з числом атомів вуглецю від 1 до 6 і таким чином включає такі алкіли, як наприклад, метил, етил, н-пропіл, ізопропіл, 2-метилетил, бутил і його ізомери (наприклад, н-бутил, ізобутил і трет-бутил), пентил і його ізомери, гексил і його ізомери і тому подібне. Термін "C1-4алкіл" як група або частина групи відноситься до вуглеводневого радикала формули CnH2n+1, у якій n дорівнює числу, що становить від 1 до 4. C 1-4алкільні групи містять від 1 до 4 атомів вуглецю, бажано, від 1 до 3 атомів вуглецю, бажаніше, 1 або 2 атоми вуглецю. C 14алкіл включає всі нерозгалужені або розгалужені алкільні групи з числом атомів вуглецю від 1 до 4 і таким чином включає такі алкіли, як наприклад, метил, етил, н-пропіл, ізопропіл, 2метилетил, бутил і його ізомери (наприклад, н-бутил, ізобутил і трет-бутил) і тому подібне. Термін "C1-6алкілокси" як група або частина групи відноситься до радикала, що має формулу a a -OR , в якій R є C1-6алкілом. Необмежуючі приклади прийнятного алкілокси включають метилокси, етилокси, пропілокси, ізопропілокси, бутилокси, ізобутилокси, втор-бутилокси, третбутилокси, пентилокси і гексилокси. Термін "C1-4алкілокси" як група або частина групи відноситься до радикала, що має формулу b b -OR , в якій R є C1-4алкілом. Необмежуючі приклади прийнятного алкілокси включають метилокси (також метокси), етилокси (також етокси), пропілокси, ізопропілокси, бутилокси, ізобутилокси, втор-бутилокси і трет-бутилокси. Термін "галогенC1-4алкілокси" як група або частина групи відноситься до радикала C 14алкілокси, де вказаний радикал C1-4алкілокси додатково заміщений 1, 2 або 3 атомами галогену. Необмежуючі приклади прийнятних радикалів галогенC 1-4алкілокси включають трифторметилокси, трифторетилокси, трифторпропілокси і трифторбутилокси. Термін "C3-6циклоалкіл", окремо або в комбінації, відноситься до циклічного насиченого вуглеводневого радикала, що має від 3 до 6 атомів вуглецю. Необмежуючі приклади прийнятного циклоC3-6алкіла включають циклопропіл, циклобутил, циклопентил і циклогексил. Має бути очевидне, що деякі із сполук згідно формулі (I) і їх аддитивні солі, гідрати і сольвати можуть містити один або декілька центрів хіральності і можуть існувати у вигляді стереоізомерних форм. Термін "стереоізомерні форми", що вживається вище або нижче, означає всі можливі стереоізомерні форми, які можуть мати сполуки згідно формулі (I) і їх аддитивні солі. Якщо не згадується або не вказується інакше, хімічне найменування сполук означає суміш усіх можливих стереохімічних ізомерних форм, причому вказані суміші містять все діастереомери і енантіомери основної молекулярної структури, а також кожну з індивідуальних ізомерних форм згідно формулі (I) і їх солі, сольвати, що по суті не містять інші ізомери, тобто асоційовані менше, ніж з 10 %, бажано, менше, ніж з 5 %, зокрема, менше, ніж з 2 %, і найбажаніше, менше, ніж з 1 % інших ізомерів. Для терапевтичного застосування солями сполук згідно формулі (I) є солі, в яких протиіон є фармацевтично прийнятним. Проте, солі кислот і основ, які не є фармацевтично прийнятними, можуть також знайти застосування, наприклад, при отриманні або очищенні фармацевтично прийнятної сполуки. Всі солі, незалежно від того, чи є вони фармацевтично прийнятними чи ні, включені в межі обсягу даного винаходу. Мається на увазі, що фармацевтично прийнятні кислотно- і основно-аддитивні солі, що вказуються вище або нижче по контексту, містять терапевтично активні нетоксичні форми кислотно- і основно-аддитивних солей, які здатні утворювати сполуки згідно формулі (I). Фармацевтично прийнятні кислотно-аддитивні солі можна бажано отримувати обробкою форми основи такою прийнятною кислотою. Прийнятні кислоти містять, наприклад, неорганічні кислоти, такі як галогеноводневі кислоти, наприклад, хлористоводневу або бромистоводневу кислоту, сірчану, азотну, фосфорну і подібні кислоти; або органічні кислоти, такі як, наприклад, оцтова, пропанова, гідроксиоцтова, молочна, піровиноградна, щавлева (тобто етандіова), малонова, бурштинова (тобто бутандіова кислота), малеїнова, фумарова, яблучна, винна, лимонна, 7 UA 106636 C2 5 10 15 20 метансульфонова, етансульфонова, бензолсульфонова, п-толуолсульфонова, цикламова, саліцилова, п-аміносаліцилова, памоєва і подібні кислоти. Навпаки, вказані форми солей можна перетворити обробкою прийнятною основою у форму вільної основи. Термін "сольвати" відноситься до гідратів і алкоголятів, які можуть утворювати сполуки згідно формулі (I), а також їх солі. Хімічні назви сполук даного винаходу створювали згідно правилам номенклатури, що узгоджуються з Chemical Abstracts Service, Advanced Chemical Development, Inc., nomenclature software (ACD/Name product version 10.01; Build 15494, 1 Dec 2006). Деякі із сполук згідно формулі (I) можуть існувати також в їх таутомерній формі. Передбачається, що такі форми, хоча вони точно не вказані у вказаній вище формулі, включені в обсяг даного винаходу. Отримання сполук Сполуки формули (I) можна отримати взаємодією сполуки формули (II) 1 2 у якій Ar, R і R мають значення, вказані для формули (I), із сполукою формули (III) у якій R1 має значення, вказані для формули (I), у присутності прийнятного реагенту амідного сполучення, такого як HBTU, прийнятної основи, такої як DIPEA, у прийнятному розчиннику, такому як DCM, і при прийнятній температурі, такій як кімнатна температура. Альтернативно, реакцію ацилювання сполуки (II) можна проводити симетричним або несиметричним ангідридом або галогенангідридом карбонової кислоти (III). Сполуки формули (II) можна отримати взаємодією сполуки формули (IV) 2 25 30 3 у якій Ar, R і R мають значення, вказані для формули (I), з прийнятним відновлюючим агентом, таким як водень, у присутності прийнятного каталізатора, такого як нікель Ренея, у прийнятному розчиннику, такому як 7 М аміак у метанолі, при прийнятній температурі, такій як кімнатна температура. Сполуки формули (IV) можна отримувати взаємодією сполуки формули (V) 2 3 у якій R і R мають значення, вказані для формули (I), із сполукою формули (VI) 8 UA 106636 C2 5 у якій Ar має значення, вказані для формули (I), у присутності прийнятного каталізатора, такого як Pd(PPh3)4, з прийнятною основою, такою як карбонат натрію, у прийнятному розчиннику, такому як 1,4-діоксан і суміш етанол/вода (1:1), і при прийнятній температурі, такій як 130 °C, у запаяній трубці. Сполуки формули (V) можна отримати взаємодією сполуки формули (VII) 2 10 3 у якій R і R мають значення, вказані для формули (I), з N-бромсукцинімідом у прийнятному розчиннику, такому як ДМФА, і при прийнятній температурі, такій як кімнатна температура. Сполуки формули (VII) можна отримати взаємодією сполуки формули (VIII) 2 15 3 у якій R і R мають значення, вказані для формули (I), з ціанідом цинку у присутності прийнятного каталізатора, такого як суміш 10 % Pd на вугіллі, трифенілфосфіна і триметилсилілхлорида або суміш тетракис(трифенілфосфін)палладію і трифенілфосфіна, у прийнятному розчиннику, такому як ДМФА або ацетонітрил, і при прийнятній температурі, такій як 80 °C. Сполуки формули (VIII) можна отримати взаємодією сполуки формули (IX) із сполукою формули (Х) 20 25 2 3 у якій R і R мають значення, вказані для формули (I), у присутності прийнятної основи, такої як DIPEA, у прийнятному розчиннику, такому як ДМФА, при прийнятній температурі, такій як 75 °C, і у прийнятній інертній атмосфері, такій як аргон. Фармакологія Виявлено, що сполуки даного винаходу є позитивними аллостеричними модуляторами 9 UA 106636 C2 5 10 15 20 25 30 35 40 45 50 55 60 нікотинового рецептора альфа 7. Нікотиновий рецептор альфа 7 (nAChR альфа 7) відноситься до суперсімейства іонотропних, іонних каналів з цис-петлею, що відкриваються лігандом, які включають 5-HT3, GABAA і сімейства рецепторів гліцину. Він активується ацетилхоліном і його продуктом розщеплювання холіну, і основною особливістю nAChR альфа 7 є його швидка десенсибілізація при постійній присутності агоніста. Він є другим найбільш поширеним підтипом нікотинового рецептора в головному мозку і є важливим регулювальником вивільнення багатьох нейромедіаторів. Він має дискретне поширення в декількох структурах головного мозку, необхідних для процесів уваги і розумової діяльності, таких як гіпокамп і префронтальна коркова речовина, і бере участь у різних психіатричних і неврологічних порушеннях у людей. Він бере участь також у холінергичному запальному шляху. Генетичний доказ його зв'язку з шизофренією показаний у формі міцного зв'язку між маркером шизофренії (дефіцит сенсорного відкриття мембранного каналу) і локусом альфа 7 на 15q13-14 і поліморфізмом у центральній частині промотора гена альфа 7. Патологічна ознака вказує на втрату імунореактивности альфа 7 і скріплення αбунгаротоксина (Btx) у гіпокампі, фронтальній і цингулятній корковій речовині головного мозку при шизофренії, при хворобі Паркінсона і Альцгеймера і при паравентрикулярному ядрі і сполуках роз'єднаних ядер при аутизмі. Фармакологічна ознака, така як помітні звички до паління у шизофреніків у порівнянні із здоровими людьми, інтерпретували як спробу пацієнтами до самолікування для поповнення дефіциту нікотинергічної передачі альфа 7. Короткочасна нормалізація дефектів у сенсорному відкритті мембранного каналу (преімпульсне інгібування, PPI) як на тваринних моделях, так і у людини, при введенні нікотину і тимчасовому відновленні нормального сенсорного відкриття каналів у шизофреніків, коли холінергічна активність переднього мозку є низькою (наприклад, стадія 2 сну), обидва були інтерпретовані як результат короткочасної активації нікотинового рецептора альфа 7 з подальшою десенсибілізацією. Таким чином, є вагома підстава для припущення, що активація nAChR альфа 7 матиме терапевтично сприятливі дії для ряду порушень ЦНС (психіатричних і неврологічних). Як вже вказано, nAChR альфа 7 швидко десенсибілізується при короткочасній присутності природного медіатора ацетилхоліну, а також екзогенних лігандов, таких як нікотин. У десенсибілізованому стані рецептор залишається пов'язаним з лігандом, але функціонально неактивним. Цей факт не є значною проблемою для природних медіаторів, таких як ацетилхолін і холін, оскільки вони є субстратами для механізмів дуже сильного розкладання (ацетилхолінестераза) і кліренсу (переносник холіну). Ці механізми розкладання/кліренса медіаторів, ймовірно, підтримують баланс між активуємими і десенсибілізованими nAChR альфа 7 у фізіологічно застосовному діапазоні. Проте, зрозуміло, що синтетичні агоністи, які не є субстратами для природних механізмів розкладання і кліренсу, мають потенційну схильність як до надстимуляції, так і також зсуву рівноваги популяції nAChR альфа 7 у бік стійкого десенсибілізованого стану, який є небажаним при порушеннях, в яких відіграють роль дефіцити в експресії або функції nAChR альфа 7. Агоністи внаслідок їх природи повинні пригнічувати зв'язуючий карман ACh, який є високо консервативним для різних підтипів нікотинових рецепторів, призводячи таким чином до можливості шкідливих реакцій за допомогою неспецифічної активації інших підтипів нікотинових рецепторів. Тому, аби уникнути цих потенційних можливостей альтернативної терапевтичної стратегії для агонізму альфа 7, слід підвищувати сприйнятливість рецептора до природних агоністів позитивним аллостеричним модулятором (РАМ). РАМ визначають як агент, який зв'язується з сайтом, відмінним від сайту скріплення агоніста, і тому, як передбачається, не має властивості агоніста або десенсибілізації, але підвищує сприйнятливість nAChR альфа 7 до природного медіатора. Цінність цієї стратегії полягає в тому, що для даної кількості медіатора магнітуда реакції nAChR альфа 7 підвищується у присутності РАМ відносно рівня перенесення, можливого в його відсутність. Крім того, РАМ можуть також підвищувати ефективність природного медіатора. Тому для порушень, при яких є дефіцит білка nAChR альфа 7, РАМ-індуковане підвищення нікотинергічного перенесення альфа 7 може бути корисним. Оскільки РАМ залежить від присутності природного медіатора, потенціал для надстимуляції обмежується механізмами розкладання/кліренса для природного медіатора. Сполуки даного винаходу класифікують як типи 1-4 на основі кількісних кінетичних властивостей, що визначаються реєстрацією цілих клітин вольт-клампом. Ця класифікація заснована на дії сполуки РАМ альфа 7, як описано в контексті раніше, на сигнал, викликаний застосуванням агоніста. Зокрема, вказаним агоністом є холін при концентрації 1 мМ. У бажаному експериментальному способі вказану сполуку РАМ альфа 7 і холін одночасно наносять на клітину, як описано в контексті нижче. Десенсибілізацію визначають як закриття 10 UA 106636 C2 рецептору при активації під час нанесення агоніста при вимірах електрофізіології способом фіксації напруги цілих клітин, яка спостережується як зменшення зовнішнього струму після початкової активації агоністом. Визначення типів 1-4 РАМ описане нижче. 5 Тип 0 Тип 1 Тип 2 Тип 3 Тип 4 10 15 20 25 30 35 сполуки мінімально змінюють величину дії струму, викликаного 1 мМ холіном. сполуки підвищують величину дії струму, викликаного 1 мМ холіном, але мінімально змінюють кінетики рецептора. Зокрема, не впливають на швидкість і міру десенсибілізації і деактивації рецептора, викликаних агоністом. Модульована сполукою реакція на 1 мМ холін, отже, є близькою до лінійного виміру реакції 1 мМ холіну у відсутність сполуки РАМ альфа 7. сполуки підвищують величину дії струму, викликаного 1 мМ холіном, при зменшенні швидкості та/або міри десенсибілізації. На деактивацію рецептора сполуки зазвичай не впливають. сполуки підвищують величину дії струму, викликаного 1 мМ холіном. При випробуванні при вищих концентраціях аж до 10 мкМ вони повністю інгібують десенсибілізацію, зокрема, при застосуванні 1 мМ холіну протягом 250 мілісекунд. Деактивація рецептора може бути сповільнена. сполуки роблять можливою початкову десенсибілізацію рецептора з подальшим повторним відкриттям рецептора під час застосування агоніста. При концентраціях з низькою ефективністю сполуки РАМ альфа 7 індукована агоністом активація, за якою слідує десенсибілізація, може все ж відрізнятись від індукованого сполукою повторного відкриття як максимум початкового внутрішнього струму. При концентраціях сполуки РАМ альфа 7 з вищою ефективністю повторне відкриття відбувається швидше, ніж закриття внаслідок десенсибілізації, так що максимум початкового струму зникає. Вважається, що сполука має цікаву, подібну РАМ активність, коли потенціювання пікового струму було щонайменше 200 % у порівнянні з контрольною холіновою реакцією (=100 %). Такі сполуки класифікують як такі, що відносяться до конкретного РАМ-типу в експериментальній частині. Сполуки, що не задовольняють цій умові, класифікують як такі, що не відносяться до конкретного РАМ-типу. Ряд сполук згідно винаходу виявився активним у випробуванні на викликаний слуховим сигналом потенціал. Штам інбредної миші DBA/2, що застосовується в цьому випробуванні, показує недоліки сенсорних процесингів, подібні до недоліків пацієнтів з шизофренією, які корелюють також із зниженою присутністю нікотинових рецепторів альфа 7 у гіпокампі. Доведено, що миша DBA/2 є корисною моделлю подібних до шизофренії дефіцитів сенсорних процесингів. Дослідження за участю людей по впливах нікотину на сенсорний процесинг передбачили результати вивчення на миші DBA/2 і дослідження з селективним агоністом альфа 7, GTS-21, на мишах DBA/2 передбачили такі впливи у людей. Ця модель сенсорної здатності відкривати мембранний канал тому має трансляційну значущість. Відповідно цьому, завданням даного винаходу є забезпечення способів лікування, які включають введення позитивного аллостеричного модулятора як єдиної активної речовини, аби тим самим модулювати активність ендогенних агоністів нікотинових рецепторів, таких як ацетилхолін або холін, або введення позитивного аллостеричного модулятора разом з агоністом нікотинового рецептора. У конкретній формі цього аспекту винаходу спосіб лікування містить лікування позитивним аллостеричним модулятором нікотинового рецептора альфа 7, як описано в контексті, і агоністом або частковим агоністом нікотинового рецептора альфа 7. Приклади прийнятних сполук з агоністичною активністю відносно нікотинового рецептора альфа 7 включають - моногідрохлорид 4-бромфенілового ефіру 1,4-діазабіцикло[3.2.2]нонан-4-карбонової кислоти (SSR180711A); - (-)-спіро-[1-азабіцикло[2.2.2]октан-3,5'-оксазолідин]-2'-он; - дигідрохлорид 3-[(2,4-диметокси)бензиліден]анабазеїна (GTS-21); - [гідрохлорид N-[(3R)-1-азабіцикло[2.2.2]окт-3-іл]-4-хлорбензаміда]; - PNU-282987; - нікотин; - вареніклин; - MEM3454; 11 UA 106636 C2 5 10 15 20 25 30 35 40 45 50 55 60 - AZD-0328; - MEM63908; - (+)-N-(1-азабіцикло[2.2.2]окт-3-іл)бензo[b]фуран-2-карбоксамід; - A-582941; - AR-R17779; - TC-1698; - PHA-709829; - тропізетрон; - WAY-317538; - EVP-6124 і - TC-5619. Зокрема, приклади прийнятних сполук з агоністичною активністю відносно нікотинового рецептора α7 включають моногідрохлорид 4-бромфенілового ефіру 1,4діазабіцикло[3.2.2]нонан-4-карбонової кислоти (SSR180711A); (-)-спіро[1-азабіцикло[2.2.2]октан-3,5'-оксазолідин]-2'-он; дигідрохлорид 3-[(2,4-диметокси)бензиліден]-анабазеїна (GTS-21); [гідрохлорид N-[(3R)-1-азабіцикло[2.2.2]окт-3-іл]-4-хлорбензаміда]; PNU-282987; нікотин; вареніклин; MEM3454; AZD-0328 і МЕМ63908. Позитивні модулятори nAChR даного винаходу є застосовними для лікування або профілактики психотичних порушень, порушень і захворювань типа розумової недостатності, для яких корисною є модуляція активності нікотинового рецептора альфа 7. Конкретним аспектом способу винаходу є спосіб лікування недостатності виучуваності, порушення пізнавальної здатності, синдрому дефіциту уваги або втрати пам'яті, передбачається, що модуляція активності нікотинового рецептора альфа 7 є корисною для лікування ряду хвороб, що включають хворобу Альцгеймера, деменцію з тільцями Леві, синдром дефіциту уваги, пов'язаного з гіперактивністю, тривожний стан, шизофренію, манію, біполярний розлад, хворобу Паркінсона, хворобу Хантінгтона, синдром Жиля де ля Туретта, травму головного мозку або інші неврологічні, дегенеративні або психіатричні порушення, при яких є втрата холінергических синапсів, у тому числі синдром зміни часових поясів, нікотинова аддикція, біль. Сполуки можуть знайти також терапевтичне застосування як протизапальні лікарські засоби внаслідок того, що субодиниця альфа 7 нікотинового рецептора ацетилхоліну є важливою для інгібування синтезу цитокіна холінергічним запальним шляхом. Приклади показань, які можна лікувати такими сполуками, є ендотоксемія, ендотоксичний шок, сепсис, ревматоїдний артрит, астма, розсіяний склероз, псоріаз, кропив'янка, запальне захворювання кишечника, запальне жовчне захворювання, хвороба Крону, неспецифічний виразковий коліт, післяопераційна непрохідність кишечника, панкреатит, серцева недостатність, гостре легеневе ушкодження і відторгнення трансплантата. Сполуки винаходу можуть знайти терапевтичне застосування при таких наступних свідченнях, як порушення пізнавальної здатності при шизофренії, порушення пізнавальної здатності при хворобі Альцгеймера, легка недостатність пізнавальної здатності, хвороба Паркінсона, синдром дефіциту уваги, пов'язаний з гіперактивністю, неспецифічний виразковий коліт, панкреатит, артрит, сепсис, післяопераційна непрохідність кишечника і гостре легеневе пошкодження. Сполуки 22 оцінювали відносно дії на активність кінази в аналізі, що містить більш ніж 225 різних киназ; сполука не проявила активність проти будь-якої з застосованих у випробуванні кіназ. З точки зору описаних вище фармакологічних властивостей, сполуки згідно формулі (I) або будь-яка їх підгрупа, їх фармацевтично прийнятні аддитивні солі, сольвати і стереохімічно ізомерні форми можна застосовувати як лікарські засоби. Зокрема, дані сполуки можна застосовувати для виготовлення лікарського засобу для лікування або профілактики психотичних порушень, порушень розумових здібностей або захворювань або станів, для яких модуляція нікотинового рецептора альфа 7 є корисною. У варіанті здійснення даний винахід відноситься до сполук згідно формулі (I) для застосування при лікуванні або профілактиці, зокрема, для лікування психотичних порушень, порушень розумових здібностей або захворювань або станів, для яких модуляція нікотинового рецептора α7 є корисною. У варіанті здійснення даний винахід відноситься до сполук згідно формулі (I) для застосування при лікуванні або профілактиці, зокрема, при лікуванні психотичних порушень, порушень розумових здібностей або запальних захворювань. У варіанті здійснення даний винахід відноситься до сполук згідно формулі (I) для лікування 12 UA 106636 C2 5 10 15 20 25 30 35 40 45 50 55 60 або запобігання, зокрема, лікування вказаних захворювань або станів. З точки зору придатності сполук згідно формулі (I), тут запропонований спосіб лікування або запобігання у теплокровних тварин, у тому числі людей, захворювань, для яких корисною є модуляція нікотинового рецептора альфа 7, таких як шизофренія, манія, біполярний розлад, тривожний стан, хвороба Альцгеймера, синдром недостатності виучуваності, порушення пізнавальної здатності, синдром дефіциту уваги, втрата пам'яті, деменція з тільцями Леві, синдром дефіциту уваги, пов'язаний з гіперактивністю, хвороба Паркінсона, хвороба Хантінгтона, синдром Жиля де ля Туретта, травма головного мозку, синдром зміни часових поясів, нікотинова аддикція і біль. Вказані способи містять введення, тобто системне або місцеве введення, бажано, пероральне введення ефективної кількості сполуки згідно формулі (I), її стереохімічно ізомерної форми, її фармацевтично прийнятної аддитивної солі або сольвата теплокровним тваринам, у тому числі людям. Фахівцеві в даній галузі повинно бути зрозуміло, що терапевтично ефективною кількістю РАМ даного винаходу є кількість, достатня для модуляції активності нікотинового рецептора альфа 7, і що ця кількість змінюється inter alia (серед іншого) залежно від типа захворювання, концентрації сполуки в терапевтичному препараті і стану пацієнта. Звичайно кількість РАМ, яку вводять як терапевтичний агент для лікування захворювання, при якому корисною є модуляція нікотинового рецептора альфа 7, такого як шизофренія, манія і біполярний розлад, тривожний стан, хвороба Альцгеймера, синдром недостатності виучуваності, порушення пізнавальної здатності, синдром дефіциту уваги, втрата пам'яті, деменція з тільцями Леві, синдром дефіциту уваги, пов'язаний з гіперактивністю, хвороба Паркінсона, хвороба Хантінгтона, синдром Жиля де ля Туретта, травма головного мозку, синдром зміни часових поясів, нікотинова аддикція і біль, визначатиметься від випадку до випадку лікарем-консультантом. Добовою дозою зазвичай є доза, яка призводить до концентрації РАМ у місці лікування в діапазоні від 0,5 нМ до 200 мкМ і більш зазвичай від 5 нМ до 50 мкМ. Для отримання цих концентрацій при лікуванні пацієнтові, що потребує лікування, ймовірно вводитимуть між 0,01 мг/кг до 2,50 мг/кг маси тіла, зокрема, від 0,1 мг/кг до 0,50 мг/кг маси тіла. Кількість сполуки згідно даному винаходу, що також називається в контексті активним інгредієнтом, яка потрібна для досягнення терапевтичної дії, звичайно змінюватиметься від випадку до випадку, змінюватиметься залежно від конкретної сполуки, від шляху введення, віку і стану реципієнта і конкретного порушення, що піддається лікуванню, або захворювання. Спосіб лікування може включати також введення активного інгредієнта за схемою прийому між одним і чотирма прийомами на день. У цих способах лікування сполуки згідно винаходу бажано виготовляють у складі препарату перед прийомом. Як описано в контексті нижче, прийнятні фармацевтичні препарати отримують відомими процедурами із застосуванням добре відомих і легко доступних інгредієнтів. Фармацевтичні композиції Даний винахід пропонує також композиції для запобігання або лікування захворювань, при яких модуляція нікотинового рецептора альфа 7 є корисною, таких як шизофренія, манія і біполярний розлад, тривожний стан, хвороба Альцгеймера, синдром недостатності виучуваності, порушення пізнавальної здатності, синдром дефіциту уваги, втрата пам'яті, деменція з тільцями Леві, синдром дефіциту уваги, пов'язаний з гіперактивністю, хвороба Паркінсона, хвороба Хантінгтона, синдром Жиля де ля Туретта, травма головного мозку, синдром зміни часових поясів, нікотинова аддикція і біль. Вказані композиції містять терапевтично ефективну кількість сполуки згідно формулі (I) і фармацевтично прийнятний носій або розчинник. Хоча активний інгредієнт можна вводити як такий, бажаною є його присутність у складі фармацевтичної композиції. Згідно цьому, даний винахід далі пропонує фармацевтичну композицію, що містить сполуку згідно даному винаходу разом з фармацевтично прийнятним носієм або розчинником. Носій або розчинник має бути "прийнятним" у сенсі сумісності з іншими інгредієнтами композиції і не має бути шкідливим для його реципієнта. Фармацевтичні композиції даного винаходу можна отримати будь-якими способами, відомими в галузі фармації, наприклад, із застосуванням таких способів, які описані в публікації Gennaro et al. Remington's Pharmaceutical Sciences (18th ed., Mack Publishing Company, 1990, see especially Part 8: Pharmaceutical preparations and their Manufacture). Терапевтично ефективна кількість конкретної сполуки у формі основи або формі аддитивної солі як активного інгредієнта ретельно перемішують з фармацевтично прийнятним носієм, який може мати всілякі форми залежно від форми препарату, потрібного для введення. Ці фармацевтичні композиції бажані у вигляді стандартних лікарських форм, прийнятних бажано для системного введення, такого як пероральне, підшкірне або парентеральне введення, або місцевого введення, такого 13 UA 106636 C2 5 10 15 20 25 30 35 40 45 50 55 60 як введення за допомогою інгаляції, спрея для носа, очних крапель, або за допомогою крему, гелю, шампуня або тому подібного. Наприклад, при отриманні композицій в оральній лікарській формі можна застосовувати будь-яке із звичайних фармацевтичних середовищ, таке як, наприклад, вода, гліколі, масла, спирти і тому подібне, у разі оральних рідких препаратів, таких як суспензії, сиропи, еліксири і розчини; або тверді носії, такі як крохмалі, цукри, каолін, змащуючі речовини, зв'язуючі речовини, дезинтегруючі агенти і тому подібне, у разі порошків, пілюль, капсул і пігулок. Унаслідок легкості їх введення, пігулки і капсули є найбільш прийнятною оральною стандартною лікарською формою, в цьому випадку, вочевидь, застосовують тверді фармацевтичні носії. Для парентеральних композицій носій зазвичай містить стерильну воду, щонайменше як основну частину носія, хоча можуть бути включені інші інгредієнти, наприклад, для сприяння розчиненню. Наприклад, можна отримати розчини, що ін'єктуються, в яких носій містить сольовий розчин, розчин глюкози або суміш сольового розчину і розчину глюкози. Можна також отримувати суспензії, що ін'єктуються, в цьому випадку можна застосовувати прийнятні рідкі носії, суспендуючі агенти і тому подібне. У композиціях, прийнятних для підшкірного введення, носій необов'язково містить агент, що підвищує проникнення, та/або прийнятний змочуючий агент, необов'язково змішаний з прийнятними добавками будь-якої природи в невеликих кількостях, причому такі добавки не викликають жодних значних шкідливих дій на шкіру. Вказані добавки можуть полегшити введення в шкіру та/або можуть бути корисними для отримання необхідних композицій. Ці композиції можна вводити різними шляхами, наприклад, у вигляді черезшкірних пластирів, у вигляді нанесення плям на шкіру або у вигляді мазі. Особливо прийнятним є виготовлення вказаних вище фармацевтичних композицій у стандартній лікарській формі внаслідок легкості їх введення і однорідності дози. Стандартна лікарська форма, що застосовується в контексті опису і формули винаходу, відноситься до фізично дискретних доз, прийнятних як уніфіковані дози, причому кожна доза містить заздалегідь певну кількість активного інгредієнта, обчислену для продукування необхідної терапевтичної дії, у поєднанні з необхідним фармацевтичним носієм. Прикладами таких дозованих лікарських форм є пігулки (у тому числі пігулки з насічками (рисками) або пігулки з оболонками), капсули, пілюлі, пакетики з порошками, облатки, розчини, що ін'єктуються, або суспензії, наповнені чайні ложки, наповнені столові ложки і тому подібне і їх сегреговані багатократні дози. Точна доза і частота введення залежать від вживаної конкретної сполуки формули (I), конкретного стану, що піддається лікуванню, важкості стану, що піддається лікуванню, віку, маси, статі, міри порушення і загального фізичного стану конкретного пацієнта, а також іншої лікарської терапії, яку може отримувати індивідуум, що добре відоме фахівцеві в даній галузі. Крім того, вочевидь, що вказану ефективну добову кількість можна зменшити або збільшити залежно від реакції у відповідь суб'єкта, який піддається лікуванню, та/або залежно від оцінки лікаря, який прописує сполуки даного винаходу. Залежно від способу введення фармацевтична композиція міститиме від 0,05 до 99 % мас., бажано, від 0,1 до 70 % мас., бажаніше, від 0,1 до 50 % мас. активного інгредієнта і від 1 до 99,95 % мас., бажано, від 30 до 99,9 % мас., бажаніше, від 50 до 99,9 % мас. фармацевтично прийнятного носія, причому всі відсотки обчислені на основі загальної маси композиції. Кількість сполуки формули (I), яку можна змішати з речовиною-носієм для отримання однієї дозованої лікарської форми, змінюватиметься залежно від захворювання, що піддається лікуванню, виду ссавця і конкретного способу введення. Проте, як загальний критерій, прийнятні уніфіковані дози для сполук даного винаходу можуть, наприклад, бажано містити між 0,1 мг і приблизно 1000 мг активного інгредієнта. Бажана уніфікована доза складає від 1 мг до приблизно 500 мг. Бажаніша уніфікована доза складає від 1 мг до приблизно 300 мг. Ще бажаніша уніфікована доза складає від 1 мг до приблизно 100 мг. Такі уніфіковані дози можна вводити більше ніж один раз на день, наприклад, 2, 3, 4, 5 або 6 раз на день, але бажано 1 або 2 рази на день, так що загальна доза для 70 кг дорослого суб'єкта знаходиться в діапазоні від 0,001 до приблизно 15 мг на кг маси суб'єкта на одне введення. Бажана доза складає від 0,01 до приблизно 1,5 мг на кг маси суб'єкта для одного введення, і така терапія може продовжуватись протягом ряду тижнів або місяців і, в деяких випадках, років. Має бути зрозуміло, проте, що конкретний рівень дози для будь-якого конкретного пацієнта залежатиме від різних чинників, що включають активність конкретної сполуки, що застосовується; віку, маси тіла, загального стану здоров'я, статі і харчування індивідуума, який піддається лікуванню; часу і шляху введення; швидкості екскреції; інших лікарських засобів, які заздалегідь були введені, і важкості конкретного захворювання, що піддається терапії, що добре відоме фахівцеві в даній галузі. Типовою дозою може бути одна пігулка масою від 1 мг до приблизно 100 мг або від 1 мг 14 UA 106636 C2 5 10 15 20 25 30 35 40 45 50 55 60 до приблизно 300 мг, що вводиться один раз на день або кілька разів на день, або одна капсула або пігулка пролонгованої дії, що вводиться один раз на день і що має пропорційно вищий вміст активного інгредієнта. Пролонгованої дії можна досягти за допомогою речовин капсули, які розчиняються при різних величинах рН, за допомогою капсул, які вивільняють активний інгредієнт повільно за допомогою осмотичного тиску або за допомогою будь-якого іншого відомого способу регульованого вивільнення. Як має бути очевидне фахівцеві в даній галузі, в деяких випадках може бути необхідно застосовувати дози поза цими діапазонами. Крім того, слід зазначити, що клініцист або лікар, що лікує, повинні знати, як і коли почати, перервати, коректувати або закінчити терапію у зв'язку з реакцією окремого пацієнта. Дані сполуки можна застосовувати для системного введення, такого як пероральне, черезшкірне або парентеральне введення, або місцевого введення, такого як введення за допомогою інгаляції, спрея для носа, очних крапель або за допомогою крему, гелю, шампуня або тому подібного. Сполуки бажано вводять перорально. Точна доза і частота введення залежать від конкретної сполуки згідно формулі (I), що застосовується, конкретного стану, що піддається лікуванню, важкості стану, що піддається лікуванню, віку, маси, статі, міри порушення і загального фізичного стану окремого пацієнта, а також іншої лікарської терапії, яку може отримувати індивідуум, що добре відоме фахівцеві в даній галузі. Крім того, вочевидь, що вказану ефективну добову кількість можна зменшити або збільшити залежно від реакції у відповідь суб'єкта, який піддається лікуванню та/або залежно від оцінки лікаря, який прописує сполуки даного винаходу. Сполуки згідно формулі (I) можна також застосовувати в комбінації з іншими загальноприйнятими агоністами нікотинового рецептора альфа 7, такими як, наприклад моногідрохлорид 4-бромфенілового ефіру 1,4-діазабіцикло[3.2.2]нонан-4-карбонової кислоти (SSR180711A); (-)-спіро-[1-азабіцикло[2.2.2]октан-3,5'-оксазолідин]-2'-он; дигідрохлорид 3-[(2,4-диметокси)бензиліден]анабазеїна (GTS-21); [гідрохлорид N-[(3R)-1-азабіцикло[2.2.2]окт-3-іл]-4-хлорбензаміда]; PNU-282987; нікотин; вареніклін; MEM3454; AZD-0328 і MEM63908. Сполуки згідно формулі (I) можна також застосовувати в комбінації з іншими загальноприйнятими агоністами нікотинового рецептора α7, такими як, наприклад моногідрохлорид 4-бромфенілового ефіру 1,4-діазабіцикло[3.2.2]нонан-4-карбонової кислоти (SSR180711A); (-)-спіро-[1-азабіцикло[2.2.2]октан-3,5'-оксазолідин]-2'-он; дигідрохлорид 3-[(2,4-диметокси)бензиліден]анабазеїна (GTS-21); [гідрохлорид N-[(3R)-1-азабіцикло[2.2.2]окт-3-іл]-4-хлорбензаміда]; PNU-282987; нікотин; вареніклін; MEM3454; AZD-0328; MEM63908; (+)-N-(1-азабіцикло[2.2.2]окт-3-іл) бензo[b]фуран-2карбоксамід; A-582941; AR-R17779; TC-1698; PHA-709829; тропізетрон; WAY-317538; EVP-6124 і TC-5619. Таким чином, даний винахід відноситься також до комбінації сполуки згідно формулі (I) і агоніста нікотинового рецептора альфа 7. Вказану комбінацію можна застосовувати як лікарський засіб. Даний винахід відноситься також до продукту, що містить (а) сполуку згідно формулі (I) і (b) агоніст нікотинового рецептора альфа 7, як комбінований препарат для одночасного, роздільного або послідовного застосування при лікуванні захворювань, для яких модифікація нікотинового рецептора альфа 7 є корисною. Різні лікарські засоби можна комбінувати в одному препараті разом з фармацевтично прийнятними носіями. Експериментальна частина Декілька способів отримання сполук даного винаходу ілюструються в наступних прикладах. Якщо не вказано інакше, всі первинні речовини отримували від комерційних постачальників і застосовували без додаткового очищення. Нижче або вище в контексті "ДМФА" означає N, N-диметилформамід; "хв" означає хвилини; "МеОН" означає метанол; "EtOH" означає етанол; "Et2O" означає діетиловий ефір; "TFA" означає трифтороцтову кислоту; "iPrNH2" означає ізопропіламін; "NH4OAc" означає ацетат амонію; "SFC" означає надкритичну рідинну хроматографію; "HBTU" означає гексафторфосфат О-(бензотриазол-1-іл)-N, N, N",N’-тетраметилуронію; "DIPEA" означає діізопропілетиламін; "DCM" означає дихлорметан; "DIPE" означає діізопропіловий простий ефір. Реакції, яким сприяло мікрохвильове випромінювання, проводили в однорежимному реакторі: Initiator™ Sixty EXP microwave reactor (Biotage AB) або в багаторежимному реакторі: MICROSYNTH Labstation (Milestone, Inc.). Абсолютну стереохімічну конфігурацію деяких сполук визначали із застосуванням 15 UA 106636 C2 5 10 15 20 25 30 35 вібраційного кругового дихроїзма (VCD). Опис по застосуванню VCD для визначення абсолютної конфігурації можна знайти в публікації Dyatkin A.B. et. al, Chirality, 14: 215-219 (2002). Передбачається, що нижченаведені приклади ілюструють, але не обмежують обсяг даного винаходу. А. Отримання проміжних продуктів 4-(4-бромтіазол-2-іл)-цис-2,6-диметилморфолін (проміжний продукт 1) У 1 л колбу, забезпечену механічною мішалкою і термометром, завантажували 2,4дибромтіазол (60 г, 0,247 моль) і ДМФА (480 мл). Після розчинення в атмосфері азоту додавали цис-2,6-диметилморфолін (33,65 мл, 0,272 моль) і DIPEA (61,23 мл, 0,37 моль). Реакційну суміш нагрівали до 70 °C в атмосфері азоту і перемішували протягом ночі. Реакційну суміш охолоджували до 10 °C на бані крига/вода. Потім по краплях додавали воду (1 л) при температурному інтервалі 10-20 °C. Спостерігали слабку екзотермічну реакцію з утворенням не зовсім білого осаду. Після додавання реакційну суміш перемішували протягом 30 хв. Осад потім відділяли фільтруванням і промивали водою (50 мл). Зібрану тверду речовину сушили у вакуумній сушильній шафі при 50 °C, отримуючи при цьому 52,8 г (77 %) проміжного продукту 1 у вигляді не зовсім білої твердої речовини. 2-(цис-2,6-диметилморфолін-4-іл)тіазол-4-карбонітрил (Проміжний продукт 2) Суміш проміжного продукту 1 (52,8 г, 190,49 ммоль), трифенілфосфіну (4,99 г, 19,05 ммоль), ціаніду цинку (22,37 г, 190,49 ммоль) і сухого ацетонітрилу (360 мл) вводили в трубку високого тиску і дегазовували (видаляли повітря) азотом протягом 5 хв. Додавали тетракис(трифенілфосфін) палладій (11 г, 9,52 ммоль) і суміш додатково дегазовували протягом 5 хв. Трубку запаювали і реакційну суміш перемішували при 140 °C протягом 3 год. Суспензію упарювали і розчиняли в суміші вода/DCM. Об'єднаний органічний шар відділяли, фільтрували на шарі діатомової землі, сушили над MgSO 4, фільтрували і упарювали. Залишок очищали на 800 г колонці EasyVarioPrep (Merck) (елюент: DCM). Потрібні фракції концентрували у вакуумі і сушили у вакуумній сушильній шафі при 50 °C протягом ночі, отримуючи при цьому 25,6 г (60 %) проміжного продукту 2 у вигляді жовтої твердої речовини. 5-бром-2-(цис-2,6-диметилморфолін-4-іл)тіазол-4-карбонітрил (проміжний продукт 3) Колбу, завантажену проміжним продуктом 2 (25,61 г, 114,69 ммоль) і ДМФА (250 мл), охолоджували на бані крига/вода. По краплях додавали N-бромсукцинімід (24,49 г, 137,63 ммоль) (слабка екзотермічна реакція). Реакційну суміш перемішували при кімнатній температурі протягом 10 хв. Потім по краплях додавали воду (400 мл), що призводило до утворення жовтого осаду, з подальшим додаванням 1 M гідроксиду натрію (115 мл). Осад відділяли фільтруванням, промивали водою (50 мл) і DIPE (10 мл). Цю тверду речовину 16 UA 106636 C2 5 10 15 20 25 30 35 перекристалізовували з ацетонітрила. Фільтрування і сушіння протягом ночі у вакуумній сушильній шафі при 50 °C давали 25,5 г (73 %) проміжного продукту 3 у вигляді жовтої твердої речовини. 2-(цис-2,6-диметилморфолін-4-іл)-5-(2,6-диметилпіридин-4-іл)тіазол-4-карбонітрил (проміжний продукт 4) Суміш проміжного продукту 3 (20 г, 66,18 ммоль), пінаколового ефіру 2,6-диметилпіридин-4боронової кислоти ([325142-95-8], 20 г, 85,79 ммоль), тетракис(трифенілфосфін)паладію (4,59 г, 3,97 ммоль), 1,4-діоксану (120 мл), карбонату натрію (21,04 г, 198,55 ммоль) у суміші 1:1 етанол/вода (120 мл) перемішували і нагрівали в атмосфері азоту при 130 °C протягом 6 год. Розчинник випаровували. Залишок розчиняли в DCM і промивали двічі водою. Органічний шар відділяли, сушили MgSO4 і упарювали. Залишок очищали колонковою хроматографією на силікагелі (градієнт елюента від 100 % DCM до 98/2 суміші DCM/MeOH). Потрібні фракції збирали і упарювали. Залишок, що утворився, перекристалізовували з суміші DIPE/CH 3CN, отримуючи при цьому 18,5 г (85 %) проміжного продукту 4 після сушіння протягом ночі у вакуумі при 50 °C. [2-(цис-2,6-диметилморфолін-4-іл)-5-(2,6-диметилпіридин-4-іл)тіазол-4-іл]метиламін (проміжний продукт 5) Проміжний продукт 4 (18,5 г, 56,33 ммоль) додавали до суспензії нікелю Ренея (2 г) у 7 н розчині аміаку в MeOH (250 мл). Реакційну суміш перемішували при 14 °C в атмосфері водню до поглинання 2 еквівалентів водню. Каталізатор видаляли фільтруванням через діатомову землю. Розчинник випаровували, отримуючи при цьому проміжний продукт 5 з кількісним виходом. Проміжний продукт 5 застосовували без додаткового очищення. 2-метокси-6-метилпіридин-4-боронова кислота (проміжний продукт 6) Суміш 2-метокси-6-метилпіридину (4,9 г, 39,79 ммоль), біс(пінаколято) диборона ([73183-343], 10,1 г, 39,79 ммоль) і 4,4-ди-трет-бутил-2,2-дипіридила ([72914-19-3], 64 мг, 0,24 ммоль) у сухому октані (75 мл) перемішували при кімнатній температурі при барботуванні азоту через суміш протягом 15 хв. Додавали біс-(1,5-циклооктадієн) дііридій(I) дихлорид ([12112-67-3], 80 мг, 0,12 ммоль) і реакційну суміш доводили до кип'ятіння і кип'ятили із зворотним холодильником протягом 4 год. Реакційну суміш охолоджували, розбавляли DCM (100 мл) і переносили в хімічний стакан, забезпечений магнітною мішалкою. Порціями додавали воду (125 мл) при перемішуванні (виділення газу) і суміш енергійно перемішували протягом 15 хв. Органічний шар відділяли і шар води екстрагували 3 рази DCM. Об'єднані органічні шари сушили над MgSO 4, 17 UA 106636 C2 5 10 15 20 25 30 фільтрували і концентрували. Залишок очищали колонковою хроматографією на силікагелі із застосуванням градієнта елюента від 100 % DCM до 95/5 суміші DCM/MeOH, отримуючи при цьому відповідний боронатний ефір ([1083168-87-9]). Після декількох тижнів стояння при кімнатній температурі цей ефір повністю перетворювали на проміжний продукт 6 (3,5 г, 52 %), який застосовували без додаткового очищення. Пінаколовий ефір 2,5-диметилпіридин-4-боронової кислоти (проміжний продукт 7) Суміш 2,5-лутидина (5 г, 46,66 ммоль), біс(пінаколято)диборона ([73183-34-3], 11,85 г, 46,66 ммоль) і 4,4-ди-трет-бутил-2,2-дипіридила ([72914-19-3], 50 мг, 0,19 ммоль) у сухому октані (50 мл) перемішували при кімнатній температурі при барботуванні через суміш азоту протягом 10 хв. Додавали біс-(1,5-циклооктадієн) дііридій(I) дихлорид ([12112-67-3], 63 мг, 0,09 ммоль) і реакційну суміш нагрівали до кип'ятіння і кип'ятили із зворотним холодильником протягом ночі. Реакційну суміш охолоджували, розбавляли DCM (600 мл) і переносили в хімічний стакан, забезпечений магнітною мішалкою. Обережно додавали суміш крига/холодна вода (400 мл) при перемішуванні (спостерігали виділення газу) і суміш енергійно перемішували протягом 15 хв. Суміш фільтрували на діатомовій землі. Органічний шар відділяли і водний шар екстрагували двічі DCM. Об'єднані органічні шари промивали водою, сушили над MgSO 4, фільтрували і концентрували, отримуючи при цьому 2,1 г (17 %) проміжного продукту 7, який застосовували без додаткового очищення. Пінаколовий ефір 2-циклопропіл-6-метилпіридин-4-боронової кислоти (проміжний продукт 8) Суміш 2-циклопропіл-6-метилпіридину ([41765-00-8], 1,1 г, 8,26 ммоль), біс(пінаколято) диборона ([73183-34-3], 2,09 г, 8,26 ммоль) і 4,4-ди-трет-бутил-2,2-дипіридила ([72914-19-3], 9 мг, 0,03 ммоль) у сухому октані (20 мл) перемішували при кімнатній температурі при барботуванні азоту через суміш протягом 15 хв. Додавали біс-(1,5-циклооктадієн)дііридій(I) дихлорид ([12112-67-3], 11 мг, 0,02 ммоль) і реакційну суміш нагрівали до кип'ятіння і кип'ятили із зворотним холодильником протягом ночі. Реакційну суміш охолоджували, розбавляли DCM (50 мл) і переносили в хімічний стакан, забезпечений магнітною мішалкою. Порціями додавали воду (50 мл) при перемішуванні (відбувалося виділення газу) і суміш енергійно перемішували протягом 15 хв. Органічний шар відділяли і водний шар екстрагували 3 рази DCM. Об'єднані органічні шари сушили над MgSO4, фільтрували і концентрували, отримуючи при цьому проміжний продукт 8 (2,01 г, 91 %), який застосовували без додаткового очищення. Цис-2-трифторметил-6-метилморфолін (проміжний продукт 29) 18 UA 106636 C2 5 10 15 N-бензил-цис-2-трифторметил-6-метилморфолін [679839-97-5] (6,2 г, 23,91 ммоль) додавали до суспензії 10 % Pd/C (1 г) у метанолі (150 мл). Реакційну суміш перемішували при кімнатній температурі в атмосфері водню до поглинання 1 еквіваленту водню. Каталізатор видаляли фільтруванням через діатомову землю. Розчинник випаровували, отримуючи при цьому 3,1 г (77 %) проміжного продукту 29 у вигляді масла, який застосовували без додаткового очищення. Транс-2-трифторметил-6-метилморфолін (проміжний продукт 30) N-бензил-транс-2-трифторметил-6-метилморфолін [1223452-62-7] (7,5 г, 28,93 ммоль) додавали до суспензії 10 % Pd/C (1 г) у метанолі (150 мл). Реакційну суміш перемішували при кімнатній температурі в атмосфері водню до поглинання 1 еквіваленту водню. Каталізатор видаляли фільтруванням через діатомову землю. Розчинник випаровували, отримуючи при цьому 3,3 г (67 %) проміжного продукту 30 у вигляді масла, який застосовували без додаткового очищення. Таблиця 1 Наступні проміжні продукти отримували згідно процедурам, вживаним для проміжного продукту 5 (виходячи з проміжного продукту 3, через утворення проміжного продукту 4): Проміжний продукт Структура Виходячи з проміжного продукту 3 і гідрата 2піколін-5-боронової кислоти ([107295230-7]) 9 проміжного продукту 3 і проміжного продукту 6 10 проміжного продукту 3 і пінаколового ефіру 2-метилпіридин-4-боронової кислоти ([660867-80-1]) 11 19 UA 106636 C2 проміжного продукту 3 і піридин-4боронової кислоти ([1692-15-5]) 12 13 Проміжного продукту 3 і проміжного продукту 7 14 проміжного продукту 3 і проміжного продукту 8 22 проміжного продукту 3 і трифторметилпіридин-4-боронової кислоти ([1093407-58-9]) 2 Таблиця 2 Наступні проміжні продукти отримували згідно процедурам, що застосовувались для проміжного продукту 5 (виходячи з 2,4-дибромтіазола, через утворення проміжних продуктів 1, 2, 3 і 4): Проміжний продукт Структура Виходячи з 15 2,4-дибромтіазола і морфоліна 16 2,4-дибромтіазола і цис/транс-2,6диметилморфоліна з відділенням транс-ізомера від цис-ізомера в першій стадії колонковою хроматографією на силікагелі (елюент: суміш від 50/50 до 0/100 гептан/DCM 17 2,4-дибромтіазола і морфоліна і з застосуванням піридин-4-боронової кислоти ([1692-15-5]) замість пінаколового ефіру 2,6диметилпіридин-4-боронової кислоти 23 2,4-дибромтіазола диметилморфоліна 20 і 2,2 UA 106636 C2 і 3-(S) 24 2,4-дибромтіазола метилморфоліна 25 2,4-дибромтіазола продукту 29 і проміжного 26 2,4-дибромтіазола продукту 30 і проміжного 27 2,4-дибромтіазола трифторметилморфоліна 10 2 2,4-дибромтіазола і гідрохлорида 8окса-3-азабіцикло[3.2.1]октану 28 5 і Проміжні продукти 18(*R) і 19(*S) отримували згідно процедурі, що застосовувалась для проміжного продукту 4, виходячи з 2-метилморфоліна замість 2,6-диметилморфоліна. Два енантіомери розділяли препаративною надкритичною рідинною хроматографією (SFC) на колонці Chiralpak Diacel AD 30 × 250 мм із застосуванням суміші 81 % CО2 і 19 % MeOH з 0,2 % iPrNH2 як рухомої фази. Проміжні продукти 20(*R) і 21(*S) отримували згідно процедурі, що застосовувалась для проміжного продукту 5, виходячи з проміжних продуктів 18 і 19, відповідно. B. Отримання кінцевих сполук B1) Приклад 1 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]циклопропанацетамід (сполука 1) 21 UA 106636 C2 5 10 15 20 25 30 Суміш циклопропілоцтової кислоти (5 г, 49,94 ммоль), HBTU (19,16 г, 50,53 ммоль) і DIPEA (15,31 мл, 92,64 ммоль) у 250 мл дихлорметану перемішували протягом 15 хв при кімнатній температурі. По краплях додавали проміжний продукт 5 (14 г, 42,11 ммоль) у 80 мл дихлорметану і перемішування продовжували протягом 2 год. при кімнатній температурі. Реакційну суміш обробляли 1 н NaOH і органічний шар промивали три рази водою. Органічний шар відділяли, сушили MgSO4 і концентрували при зниженому тиску. Цей залишок очищали на колонці з діоксидом кремнію і з градієнтом елюента від 100 % DCM до 98/2 суміші DCM/MeOH. Відповідні чисті фракції збирали і упарювали. Продукт обробляли Et2O, фільтрували і сушили у вакуумі, отримуючи при цьому 11,8 г (68 %) сполуки 1. B2) Приклад 2 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]-3метил-5-ізоксазолкарбоксамід (сполука 4) DIPEA (0,16 мл, 0,97 ммоль) додавали до розчину проміжного продукту 5 (150 мг, 0,45 ммоль) у DCM (6 мл). Реакційну суміш охолоджували до 0 °C в атмосфері азоту. Потім по краплях додавали 3-метилізоксазол-5-карбонілхлорид (79 мг, 0,54 ммоль) і перемішування продовжували протягом 1 год. при кімнатній температурі. Реакційну суміш промивали бікарбонатом натрію і потім двічі водою. Органічний шар сушили над шаром сульфату магнію і упарювали. Залишок очищали препаративною ВЕРХ (RP Shandon Hyperprep C18 BDS-8 мкм, 250 г, 5 см; рухома фаза (0,25 % розчин NH4HCO3 у воді, CH3CN)), отримуючи при цьому 127 мг (64 %) сполуки 4. B3) Приклад 3 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]ацетамід (сполука 60) Суміш проміжного продукту 5 (150 мг, 0,45 ммоль) і триетиламіну (0,063 мл, 0,54 ммоль) перемішували в дихлорметані (6 мл) при кімнатній температурі. Додавали ангідрид оцтової кислоти (0,051 мл, 0,54 ммоль) і реакційну суміш перемішували при кімнатній температурі 22 UA 106636 C2 5 10 15 20 25 30 протягом 2 год. Реакційну суміш промивали розчином карбонату калію. Органічний шар сушили над MgSO4, фільтрували і упарювали. Залишок очищали препаративною ВЕРХ (RP Shandon Hyperprep C18 BDS-8 мкм, 250 г, 5 см; рухома фаза (0,25 % розчин NH4HCO3 у воді, MeOH+CH3CN)), отримуючи при цьому 100 мг (59 %) сполуки 60. B4) Приклад 4 N-[[5-(2,6-диметил-4-піридиніл)-2-[(2R, 6R)-2-метил-6-(трифторметил)-4-морфолініл]-4тіазоліл]метил]циклопропанацетамід (сполуки 203) і N-[[5-(2,6-диметил-4-піридиніл)-2-[(2S, 6S)2-метил-6-(трифторметил)-4-морфолініл]-4-тіазоліл]метил]циклопропанацетамід (сполука 204) Сполуку 202 (отримана за допомогою процедури, що аналогічна тій, що описується в B1) розділяли на її енантіомери препаративної SFC (на колонці Chiralpak® Daicel AD, 30 × 250 мм, сполученою з колонкою AD 20 × 250 мм; рухома фаза: CО 2, EtOH з 0,2 % iPrNH2). Дві фракції продукту збирали і розчинник випаровували в обох випадках. Залишки розчиняли в МеОН і розчинник знову випаровували в обох випадках. Сполука 203 була чистою після цих стадій, сполука 204 все ж містила деяку кількість іншого ізомеру, тому цю сполуку знову очищали тим же способом, отримуючи при цьому чисту сполуку 204. B5) Приклад 5 N-[[5-(2,6-диметил-4-піридиніл)-2-[2-метил-6-(трифторметил)-4-морфолініл]-4тіазоліл]метил]циклопропанацетамід (транс-енантіомер А) (сполука 206) N-[[5-(2,6-диметил-4-піридиніл)-2-[2-метил-6-(трифторметил)-4-морфолініл]-4тіазоліл]метил]циклопропанацетамід (транс-енантіомер В) (сполука 133) Сполуку 205 (отриману за допомогою процедури, що аналогічна тій, що описується в B1) розділяли на її енантіомери препаративною SFC (на колонці Chiralpak® Daicel AD, 30 × 250 мм, сполученою з AD 20 × 250 мм; рухома фаза: CО 2, МеOH з 0,2 % iPrNH2). Дві фракції продукту збирали і розчинник випаровували в обох випадках. Залишки розчиняли в МеОН і розчинник знову випаровували в обох випадках, отримуючи при цьому сполуку 206 і сполуку 133. B6) Приклад 6 N-[[5-(2,6-диметил-4-піридиніл)-2-[(2R)-2-(трифторметил)-4-морфолініл]-4тіазоліл]метил]циклопропанацетамід (сполука 191) N-[[5-(2,6-диметил-4-піридиніл)-2-[(2S)-2-(трифторметил)-4-морфолініл]-4тіазоліл]метил]циклопропанацетамід (сполука 192) 35 23 UA 106636 C2 5 Сполуку 190 (отриману за допомогою процедури, що аналогічна тій, що описується в B1) розділяли на її енантіомери препаративною SFC (на колонці Chiralpak® Daicel AD, 20 × 250 мм; рухома фаза: CО2, МеOH з 0,2 % iPrNH2). Дві фракції продукту збирали і розчинник упарювали в обох випадках. Залишки розчиняли в МеОН і розчинник знову випаровували в обох випадках, отримуючи при цьому сполуку 191 (білий порошок). Сполука 192 все ж не була чистою і її знову очищали препаративною SFC (на Chiralpak® Daicel AD, 20 × 250 мм; рухома фаза: CО 2, МеOH з 0,2 % iPrNH2). Потрібні фракції збирали і розчинник випаровували. Цей залишок розчиняли в МеОН і розчин знову упарювали, отримуючи при цьому сполуку 192 (білий порошок). 10 Таблиця 3 Кінцеві сполуки № спол. Хімічна назва 1 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4тіазоліл]метил]циклопропанацетамід 2 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4тіазоліл]метил]циклобутанкарбоксамід 3 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-5-метил-3ізоксазолкарбоксамід R1 № прикладу В1 В2 В1 4 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-3-метил-5ізоксазолкарбоксамід В2 5 2-хлор-N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]бензамід В2 6 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2фторбензамід В2 7 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-3фторбензамід В2 24 UA 106636 C2 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-4фторбензамід 3-хлор-N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]бензамід В2 10 2,4-дихлор-N-[[2-[(2R, 6S)-2,6-диметил-4морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]бензамід В2 11 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-4(трифторметокси)бензамід В2 12 3-ціано-N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]бензамід В2 13 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2,4дифторбензамід В2 14 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2,3,4трифторбензамід В2 15 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-3,5дифторбензамід В2 16 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4тіазоліл]метил]циклопентанкарбоксамід N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2-метил-3піридинкарбоксамід В2 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-3-метил-4ізоксазолкарбоксамід 4-хлор-N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]бензамід В1 20 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2-метил-5(трифторметил)-4-оксазолкарбоксамід В1 21 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2,4диметилбензамід В1 22 4-хлор-N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]-2метилбензамід В1 23 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-4(трифторметил)бензамід В1 8 9 17 18 19 25 В2 В1 В1 UA 106636 C2 24 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-4-фтор-2метилбензамід В1 25 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-3,5-диметил4-ізоксазолкарбоксамід В1 26 2,3-дихлор-N-[[2-[(2R, 6S)-2,6-диметил-4морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]бензамід В1 27 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]бензамід В1 28 (3S)-N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5(2,6-диметил-4-піридиніл)-4тіазоліл]метил]тетрагідро-3-фуранкарбоксамід N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2,4-диметил5-тіазолкарбоксамід В1 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-4метоксибензамід N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2-метил-4оксазолкарбоксамід В2 32 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2,3дифторбензамід В1 33 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-4-фтор-3(трифторметил)бензамід В1 34 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-1метилциклопропанкарбоксамід 3,4-дихлор-N-[[2-[(2R, 6S)-2,6-диметил-4морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]бензамід В1 36 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-3,4дифторбензамід В2 37 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2метоксиацетамід N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-3,4-дифтор2-метилбензамід В2 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]пропанамід N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2метилпропанамід В2 29 30 31 35 38 39 40 26 В1 В1 В2 В1 В2 UA 106636 C2 41 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]бутанамід В2 42 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-3метилбутанамід N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2,2,3,3тетраметилциклопропанкарбоксамід В2 44 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-3(трифторметил)бензамід В1 45 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2,2-дифтор1,3-бензoдіоксол-5-карбоксамід В1 46 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2,2-дифтор1,3-бензoдіоксол-4-карбоксамід В1 47 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2,2диметилпропанамід N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4тіазоліл]метил]циклопропанкарбоксамід N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4тіазоліл]метил]циклобутанацетамід В3 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4тіазоліл]метил]циклопропанпропанамід N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-4метилпентанамід В1 (2S)-N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5(2,6-диметил-4-піридиніл)-4-тіазоліл]метил]-1метил-2-пірролідинкарбоксамід В1 43 48 49 50 51 52 В1 В1 В1 В1 S-енантіомер 53 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-3метоксипропанамід В1 54 3-(1,1-диметилетил)-N-[[2-[(2R, 6S)-2,6-диметил-4морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]-1-метил-1H-піразол-5-карбоксамід В2 60 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6- -CH3 диметил-4-піридиніл)-4-тіазоліл]метил]ацетамід 5-циклопропіл-N-[[2-[(2R, 6S)-2,6-диметил-4морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]-3-ізоксазолкарбоксамід В3 127 27 В1 UA 106636 C2 128 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-4,4,4трифторбутанамід В1 129 1-(1,1-диметилетил)-N-[[2-[(2R, 6S)-2,6-диметил-4морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]-3-метил-1Н-піразол-5-карбоксамід В2 130 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-1,2бензізоксазол-3-карбоксамід В1 131 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-1,5-диметил1Н-піразол-3-карбоксамід В2 132 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-4оксазолкарбоксамід N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2,5-диметил4-оксазолкарбоксамід В1 135 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-5-(1метилетил)-3-ізоксазолкарбоксамід В1 136 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-1,3-диметил1Н-піразол-5-карбоксамід В2 137 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2піридинкарбоксамід В1 138 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-2піразинкарбоксамід 1-(1,1-диметилетил)-N-[[2-[(2R, 6S)-2,6-диметил-4морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]-5-метил-1Н-піразол-3-карбоксамід В2 140 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-6-метокси-2піридинкарбоксамід В1 141 N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-3фуранкарбоксамід N-[[2-[(2R, 6S)-2,6-диметил-4-морфолініл]-5-(2,6диметил-4-піридиніл)-4-тіазоліл]метил]-1-метил-1Нпіразол-3-карбоксамід В2 5-(1,1-диметилетил)-N-[[2-[(2R, 6S)-2,6-диметил-4морфолініл]-5-(2,6-диметил-4-піридиніл)-4тіазоліл]метил]-3-ізоксазолкарбоксамід В1 134 139 142 143 28 В1 В2 В1
ДивитисяДодаткова інформація
Назва патенту англійськоюMorpholinothiazoles as alpha 7 positive allosteric modulators
Автори англійськоюMacdonald, Gregor, James, de Boeck, Benoit, Christian, Albert, Ghislain, Leenaerts, Joseph, Elisabeth
Автори російськоюМакдональд Грегор Джеймс, де Бек Бенойт Кристиан Альберт Гислейн, Линаертс Джозеф Элизабет
МПК / Мітки
МПК: A61P 25/00, C07D 417/14, A61K 31/427
Мітки: модулятори, альфа, позитивні, алостеричні, морфолінотіазоли
Код посилання
<a href="https://ua.patents.su/55-106636-morfolinotiazoli-yak-pozitivni-alosterichni-modulyatori-alfa-7.html" target="_blank" rel="follow" title="База патентів України">Морфолінотіазоли як позитивні алостеричні модулятори альфа 7</a>
Попередній патент: Спосіб виготовлення обідка мундштука сигарети
Наступний патент: Птахозахищений ізолятор
Випадковий патент: Склопакет підвищеної жорсткості