Спосіб визначення загальної антиоксидантної ємності плазми крові
Номер патенту: 103605
Опубліковано: 25.12.2015
Автори: Зинченко Василь Демидович, Топчій Іван Іванович, Горяча Ірина Петрівна, Говор Ірина Вікторівна, Кірієнко Олександр Миколайович
Формула / Реферат
Спосіб визначення загальної антиоксидантної ємності плазми крові, який включає приготування двох зразків люмінолу з ініціатором люмінесценції, в один з яких додають плазму крові, і реєстрацію кривих висвічування обох зразків, який відрізняється тим, що як ініціатор люмінесценції використовують озонований фізіологічний розчин, а після одержання кривих висвічування визначають площу під цими кривими і вираховують загальну антиоксидантну ємність за формулою:
А=(1-∫Iл п/∫Iл)Соз×Vоз p/Mпл,
де А - загальна антиоксидантна ємність, ∫Iл п - площа під кривою висвічування для розчину люмінолу з додаванням плазми, ∫Iл - площа під кривою висвічування для розчину люмінолу без плазми, Соз - концентрація озону у озонованому фізіологічному розчині, Vоз p - об'єм уведеного озонованого фізіологічного розчину, Мпл - маса уведеної плазми.
Текст
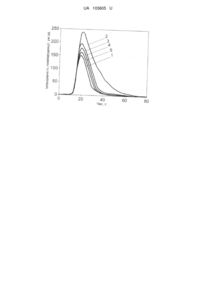
Реферат: Спосіб визначення загальної антиоксидантної ємності плазми крові включає приготування двох зразків люмінолу з ініціатором люмінесценції, в один з яких додають плазму крові, і реєстрацію кривих висвічування обох зразків. Як ініціатор люмінесценції використовують озонований фізіологічний розчин, а після одержання кривих висвічування визначають площу під цими кривими і вираховують загальну антиоксидантну ємність за формулою: А=(1-∫Iл п/∫Iл)СозVоз p/Mпл, де А - загальна антиоксидантна ємність, ∫Iл п - площа під кривою висвічування для розчину люмінолу з додаванням плазми, ∫Iл - площа під кривою висвічування для розчину люмінолу без плазми, Соз - концентрація озону у озонованому фізіологічному розчині, Vоз p - об'єм уведеного озонованого фізіологічного розчину, Мпл - маса уведеної плазми UA 103605 U (12) UA 103605 U UA 103605 U 5 10 15 20 25 30 35 40 45 50 55 60 Корисна модель належить до галузі клінічної біохімії і може бути використана для діагностики загального функціонального стану організму людини. Пошкодження клітин активними формами кисню (АФК) являють собою істотний фактор виникнення багатьох захворювань, включаючи захворювання серця, рак, ревматоїдні артрити, а також процеси старіння [1]. Існує ряд найбільш шкідливих АФК: пероксильні (ROO ) і гідроксильний (НО) радикали, - 1 супероксидіон (02 ), синглетний кисень ( О2), перекис водню (Н2О2), пеороксинітрит (OONO ), озон. При нормальному рівні АФК в клітинах беруть участь у ряді фізіологічних функцій, включаючи проліферацію, диференціацію і апоптоз. Разом з тим, АФК внаслідок їх високої реакційної здатності можуть пошкоджувати клітинні мембрани, білки, ДНК. В живих організмах існують захисні системи, що підтримують безпечний для організму рівень АФК. Відомо, що кров, включаючи клітини крові і плазму, мають системи захисту від АФК. завдяки дії яких підтримується баланс між продукцією АФК і їх нейтралізацією. У стані деяких захворювань цей баланс порушується внаслідок продукції надлишкових АФК або зниження ефективності роботи захисних механізмів. Порушення такого балансу викликає оксидативний стрес організму і порушення його фізіологічних функцій. Показником антиоксидантного стану організму може бути загальна антиоксидантна ємність (ЗАОЄ) або загальна антиоксидантна активність (ЗАОА) його біологічних рідин, зокрема плазми крові. Окрім поняття ЗАОЄ використовують також поняття антиоксидантна ємність (АОЄ), якщо мова йде про нейтралізацію не всіх активних форм кисню, а лише деяких з них, наприклад, гідроксильного радикала. Термін загальна антиоксидантна ємність означає кількість АФК, з якою здатна взаємодіяти жива система. Якщо кількість АФК в живій системі перевищує значення її антиоксидантної ємності, то захисні механізми не здатні повністю нейтралізувати АФК і це призводить до оксидативного стресу. Термін загальна антиоксидантна активність означає стартову динаміку антиоксидантного процесу. ЗАОА описується відповідною константою швидкості реакції антиоксиданту з активною формою кисню. В нинішній час широко використовують способи оцінки антиоксидантної ємності з застосуванням різних біомаркерів, які можуть бути індикаторами окисних реакцій, як, наприклад, окиснені біомолекули [21. Загальним недоліком цих способів є те, що для коректної оцінки антиоксидантної ємності організму необхідно проводити вимірювання панелі біомаркерів, наприклад, п'яти. Застосування великої кількості біомаркерів ускладнює і здорожує проведення аналізу антиоксидантного стану організму. Відомий спосіб визначення ЗАОА крові, заснований на реєстрації амплітуди піку хемілюмінесценції люмінолу [3]. Однак даний спосіб вимагає дуже тривалої надзвичайно складної підготовки реактивів і проб, обов'язкового вимірювання шумового сигналу перед дослідженням кожної проби, що призводить до значного збільшення часу аналізу. Оскільки процес багатостадійний, то виникає імовірність внесення похибок на кожній стадії, що, в кінцевому рахунку, призводить до значної сумарної похибки вимірювань. Ці причини знижують надійність кількісної оцінки ЗАОА. Відомий спосіб визначення АОЄ біологічних рідин шляхом кулонометричного титрування електрогенегованим окисником - бромом [4]. Електрохімічне окиснення бромід-іонів на платиновому електроді в кислих середовищах призводить до утворення Вr 2, Вr3, а також короткоживучих радикалів (Вr), адсорбованих на поверхні платинового електрода, які легко взаємодіють зі зразками, що досліджуються. Кількісно АОЄ виражається як електричний заряд на 1 мл зразка. Недоліком способу є те, що АОЄ зразка, який досліджується, визначається за його здатністю нейтралізувати окисну дію іонів брому, які не є природними АФК живої системи. Тому цей спосіб не придатний для точного віддзеркалювання реальної здатності зразка, що досліджується, нейтралізувати АФК. Відомий спосіб визначення ЗАОА плазми крові на підставі вимірювання поглинання плазмою пероксил-радикала [5]. Визначення ЗАОА проводять шляхом вимірювання часу, протягом якого плазма чинить опір окисненню в умовах атаки пероксильним радикалом. Моніторинг виконують за допомогою кисневого електрода. Хоча даний електрохімічний спосіб дозволяє отримувати інформацію про роль різних станів плазми, як антиоксиданту, він складний і тривалий, для проведення одного аналізу потрібно близько 90 хв. Реалізація даного способу потребує складного обладнання, яке не завжди доступне, вимірювання досить складне у виконанні. Найбільш близьким до способу, що заявляється, є спосіб вимірювання ЗАОЄ зразків плазми крові людини, у якому використовуються люмінесцентні реакції з люмінолом [6]. 1 UA 103605 U 5 10 15 20 25 30 35 40 45 50 Відповідно до способу готують 2 зразки розчину люмінолу, до кожного з яких додають ініціатор люмінесценції (парайодофенол, перекис водню в трис-буфері, рН 8.5 і кон'югат пероксидази хріну) і реєструють залежності інтенсивності люмінесценції від часу (криві висвічування). Після зниження інтенсивності люмінесценції на 10 % або виходу на плато, до одного зразка додають речовину з відомими антиоксидантними властивостями (TROLOX), а до другого - плазму крові і реєструють криві висвічування. На основі порівяння кривих висвічування визначають ЗАОЄ плазмі крові. Недоліком даного способу є його довготривалість. Це пов'язано з тривалістю реєстрації кривих висвічування. Внаслідок цього процес вимірювання ЗАОЄ одного зразка триває близько 1 години. В основу корисної моделі поставлено задачу удосконалити відомий спосіб вимірювання ЗАОЄ шляхом заміни ініціатора люмінесценції, що забезпечить можливість скорочення часу його здійснення. Поставлена задача вирішується тим, що в способі оцінки вимірювання ЗАОЄ плазми крові, який включає приготування двох зразків люмінолу з ініціатором люмінесценції, в один з яких додають плазму крові, і реєстрацію кривих висвічування обох зразків, згідно з корисною моделлю, як ініціатор люмінесценції використовують озонований фізіологічний розчин (ОФР), а після одержання кривих висвічування визначають площу під цими кривими і вираховують ЗАОЄ за формулою:, А=(1-∫lл п/∫lл)СозVоз p/Mпл, де А - ЗАОЄ, ∫lл п - площа під кривою висвічування для розчину люмінолу з додаванням плазми, ∫lл - площа під кривою висвічування для розчину люмінолу без плазми, С оз концентрація озону у ОФР, Vоз p - об'єм уведеного ОФР, Мпл - маса уведеної плазми. При використанні ОФР як ініціатора люмінесценції, скорочується тривалість реєстрації кривих висвічування. Час на проведення одного вимірювання складає близько 5 хв. Таким чином, час вимірювання скорочується порівняно з найближчим аналогом, приблизно, в 12 разів. -6 Спосіб здійснюють таким чином. Готують зразок розчину люмінолу (10 М, рН8.5) і ОФР, для чого фізіологічний розчин (150 мM NaCl) барботують озоно-кисневою сумішшю до досягнення концентрації розчиненого озону 5 мг/л. Розчин люмінолу об'ємом 1 мл поміщують у кювету люмінометра, вводять 0.1 мл ОФР і реєструють криву висвічування, починаючи з моменту уведення ОФР до моменту припинення люмінесценції. Вираховують площу під кривою висвічування. Готують другий зразок розчину люмінолу і додають 0.1 мл плазми крові та 0.1 мл ОФР. Реєструють криву висвічування і вираховують площу під нею. Використовуючи отримані площі під кривими висвічування, вираховують ЗАОЄ плазми крові за формулою: А=(1-∫lл п/∫lл)СозVоз p/Mпл, де А - ЗАОЄ, ∫lл п - площа під кривою висвічування люмінолу з додаванням плазми, ∫l л площа під кривою висвічування для розчину люмінолу без плазми, С оз - концентрація озону у ОФР, Vоз - об'єм уведеного ОФР, Мпл - маса уведеної плазми. Дослідження ефективності заявленого способу були проведені на здорових і хворих на гломерулонефрит пацієнтах. Результати наведені на графіку та у таблиці. З графіка видно, що площа під кривою висвічування у зразку з плазмою здорового донора (крива 1), менша, ніж відповідна площа у зразку без плазми (крива 2). Різниця між цими двома площами зумовлена тим, що частина активного кисню (озону) була нейтралізована антиоксидантними системами плазми і не брала участі у окисненні люмінолу і у генерації квантів світла. У присутності плазми пацієнта, хворого на гломерулонефрит на початку лікування (крива 3), ця різниця менша. Це означає, що антиоксиданті системи плазми хворого пацієнта нейтралізують менше активного кисню, тобто ЗАОЄ плазми менша, ніж у здорового донора. Після лікування протягом 10 днів різниця між площами збільшується, а через 21 день ця різниця стає ще більшою (відповідно, криві 4 і 5), однак вона не досягає значення, характерного для здорового донора. Одержані дані свідчать про те, що заявлений спосіб визначення ЗАОЄ плазми крові може ефективно використовуватись для контролю стану організму. 2 UA 103605 U Таблиця Показники ЗАОЄ плазми крові Площа під кривою спаду флуоресценції (умови, ЗАОЄ, мг О3/г плазми один.) Контрольний зразок (розчин люмінолу без плазми) Здоровий донор Гломерулонефрит на початку лікування Гломерулонефрит на 10 день лікування Гломерулонефрит на 21 день лікування 5 10 15 212±5 93±5 (2,8±0,06)10 ЗАОЄ, мкмоль О3/г плазми -3 56±1,5 -3 34±1,5 -3 43±1,5 -3 48±1,5 145±5 (1,7±0,06)10 121±5 (2,2±0,06)10 109±5 (2,4±0,06)10 Джерела інформації: 1. Sies H. Strategies of antioxidant defence// Eur. J. Biochem.-1993. - Vol. 215.-P. 213-219. 2. Dinardo J., Levis J.A. Method for characterizing the oxidative stress protective capacity of an antioxidative substance. Заявка WO 2006/083293, МПК A62K 49/00, публ. 10.08.2006. 3. Икконникова Е.И., Бурова М.Б. Способ определения суммарной антиоксидантной активности крови. Патент РФ № 2157531, МПК G01N33/52, публ. 10.10.2000. 4. Погорельцев В.И., Зиятдинова Г.К., Будников Г.К. Способ определения интегральной антиоксидантной емкости биологических жидкостей. заявка РФ № 2002134634/15, МПК G 01 N 33/48, публ. 27.05.2005. 5. Wainer D.D.M., Burton G.W., Ingold K.U., Barclay L.R.C., Locke S.J. The relative contribution of vitamin E, urate, ascorbate and proteins to the total peroxyl radical-trapping antioxidant activity of human blood plasma. //Biochim Biophys Acta.-1987. - Vol. 924, № 3. - P. 408-419. 6. Thrope G.H., Whitehead T.P. Патент Великобританії № 2245062, МПК G01N 21/76, C12Q 1/28; G01N 33/52/, публ. 18. 12. 1991. ФОРМУЛА КОРИСНОЇ МОДЕЛІ 20 25 30 Спосіб визначення загальної антиоксидантної ємності плазми крові, який включає приготування двох зразків люмінолу з ініціатором люмінесценції, в один з яких додають плазму крові, і реєстрацію кривих висвічування обох зразків, який відрізняється тим, що як ініціатор люмінесценції використовують озонований фізіологічний розчин, а після одержання кривих висвічування визначають площу під цими кривими і вираховують загальну антиоксидантну ємність за формулою: А=(1-∫Iл п/∫Iл)СозVоз p/Mпл, де А - загальна антиоксидантна ємність, ∫Iл п - площа під кривою висвічування для розчину люмінолу з додаванням плазми, ∫Iл - площа під кривою висвічування для розчину люмінолу без плазми, Соз - концентрація озону у озонованому фізіологічному розчині, Vоз p - об'єм уведеного озонованого фізіологічного розчину, Мпл - маса уведеної плазми. 3 UA 103605 U Комп’ютерна верстка Л. Бурлак Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 4
ДивитисяДодаткова інформація
МПК / Мітки
МПК: G01N 33/48
Мітки: антиоксидантної, ємності, визначення, плазми, крові, спосіб, загальної
Код посилання
<a href="https://ua.patents.su/6-103605-sposib-viznachennya-zagalno-antioksidantno-ehmnosti-plazmi-krovi.html" target="_blank" rel="follow" title="База патентів України">Спосіб визначення загальної антиоксидантної ємності плазми крові</a>
Попередній патент: Спосіб інгібіції проліферації стовбурових ракових клітин в старіючій популяції клітин аденокарциноми ерліха
Наступний патент: Пристрій для обкатування зовнішніх поверхонь обертання
Випадковий патент: Спосіб обробки інформації з використанням автоматичної штучної нейронної системи адаптованого резонансу з радіально-базисними функціями шару розпізнавання нейронної мережі