Солі азабіциклічних діарилових ефірів та способи їх одержання або одержання їх попередників
Номер патенту: 113409
Опубліковано: 25.01.2017
Автори: Бюргер Еккарт, Піньоне Массімо, Хар Дені, Ву Раеанн, Мартерер Вольфганг, Прашад Махавір, Уейкол Ліладхар Мурлідхар, Саттер Бертран, Віллхауер Едвін Бернард, Стінгелін Доріс, Карпінскі Піотр Х., Б'янкі Жан-Клод, Вівело Джеймс Ентоні
Формула / Реферат
1. Сіль (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану, де зазначена сіль являє собою солі фумарат, малеат, хлорид, фосфат, сукцинат або малонат (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану.
2. Сіль за п. 1, де зазначена сіль являє собою сіль монофумарат (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану у кристалічній формі.
3. Сіль за п. 2, де зазначена сіль характеризується практично такою ж дифрактограмою XRPD, що і дифрактограма XRPD, представлена на фіг. 1.
4. Сіль за п. 1, де зазначена сіль являє собою сіль монофумарат (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану у кристалічній формі, де середній розмір частинок кристалів становить щонайменше 15 мкм.
5. Сіль за будь-яким з пп. 2-4, де зазначена сіль являє собою сіль монофумарат (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану у кристалічній формі та де зазначена сіль існує у практично чистій формі.
6. Сіль за будь-яким з пп. 2-4, де зазначена сіль являє собою сіль монофумарат (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану у кристалічній формі та де зазначена сіль має ступінь чистоти вище ніж 90 мас. %.
7. Фармацевтична композиція, що містить сіль за будь-яким з пп. 1-6 як активний інгредієнт та щонайменше один фармацевтично прийнятний носій.
8. Фармацевтична композиція, що містить сіль за будь-яким з пп. 1-6 у комбінації з одним або більше інших терапевтичних агентів як активних інгредієнтів та щонайменше один фармацевтично прийнятний носій.
9. Фармацевтична композиція, що містить монофумарат (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану за будь-яким з пп. 2-6 як активний інгредієнт та щонайменше один фармацевтично прийнятний носій, де зазначена композиція має форму таблетки.
10. Фармацевтична композиція у формі таблетки, що містить
(a) монофумарат (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану за будь-яким з пп. 2-6 як активний інгредієнт;
(b) наповнювач;
(c) розпушувач;
(d) змащуючий агент; та
(e) агент, що надає властивість ковзкості;
де єдиним присутнім змащуючим агентом є змащуючий агент, вибраний з натрійстеарилфумарату, натрійлаурилсульфату, гліцерилбегенатів, гідрогенізованих рослинних олій, воску цетилових ефірів та тальку.
11. Фармацевтична композиція у формі таблетки, що містить
(a) до 10 мас. % монофумарату (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану за будь-яким з пп. 2-6 як активного інгредієнта;
(b) від 1 до 20 мас. % кукурудзяного крохмалю; від 15 до 35 мас. % мікрокристалічної целюлози та від 40 до 75 мас. % розпиленої лактози;
(c) від 0,5 до 5 мас. % натрійкарбоксиметилцелюлози XL;
(d) від 0,5 до 3 мас. % натрійстеарилфумарату; та
(e) від 0,1 до 1 мас. % аеросилу.
12. Фармацевтична композиція у формі таблетки, що містить від 1 до 10 мас. % монофумарату (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану за будь-яким з пп. 2-6 як активного інгредієнта та щонайменше один фармацевтично прийнятний носій;
де зазначена композиція включає шар активного інгредієнта, який містить монофумарат та допоміжний шар, який не містить монофумарату;
де масове співвідношення шару активного інгредієнта до допоміжного шару становить від 10:90 до 90:10.
13. Фармацевтична композиція у формі таблетки, що містить від 1 до 10 мас. % монофумарату (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану за будь-яким з пп. 2-6 як активного інгредієнта;
де зазначена композиція включає шар активного інгредієнта, який містить монофумарат,
та допоміжний шар, який не містить монофумарату;
де масове співвідношення шару активного інгредієнта до допоміжного шару становить від 10:90 до 90:10;
де шар зазначеного активного інгредієнта включає
(1а) від 11 до 25 мас. % від шару активного інгредієнта монофумарату (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану;
(1b) від 15 до 35 мас. % від шару активного інгредієнта мікрокристалічної целюлози та від 40 до 70 мас. % шару активного інгредієнта розпиленої лактози;
(1с) від 1 до 5 мас. % від шару активного інгредієнта натрійкарбоксиметилцелюлози XL;
(1d) від 1 до 5 мас. % від шару активного інгредієнта натрійстеарилфумарату; та
(1е) від 0,1 до 1 мас. % від шару активного інгредієнта аеросилу;
та де зазначений допоміжний шар включає
(2а) від 10 до 35 мас. % від зазначеного допоміжного шару мікрокристалічної целюлози та від 50 до 75 мас. % зазначеного допоміжного шару розпиленої лактози;
(2b) від 1 до 3 мас. % від зазначеного допоміжного шару натрійкарбоксиметилцелюлози XL;
(2с) від 1 до 5 мас. % від зазначеного допоміжного шару натрійстеарилфумарату; та
(2d) від 0,1 до 1 мас. % від зазначеного допоміжного шару аеросилу.
14. Спосіб профілактики, лікування та/або затримки розвитку захворювання або стану, в яких відіграє роль або залучена активація nAChRa7, у суб'єкта, який потребує такого лікування, який включає введення зазначеному суб'єкту терапевтично ефективної кількості солі за будь-яким з пп. 1-6.
15. Спосіб профілактики, лікування та/або затримки розвитку психіатричних або нейродегенеративних розладів у суб'єкта, який потребує такого лікування, який включає введення зазначеному суб'єкту терапевтично ефективної кількості солі за будь-яким з пп. 1-6.
16. Композиція, що містить щонайменше 90 мас. % солі за будь-яким з пп. 1-4, у розрахунку на масу зазначеної композиції.
17. Спосіб одержання солі монофумарату (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану у кристалічній формі, що включає стадії
(a) одержання розчину солі монофумарату (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану у суміші розчинників первинного спирту, вторинного спирту та води, де об'ємне співвідношення первинний спирт:вторинний спирт становить від 9:1 до 1:1, та де об'ємне співвідношення первинний спирт:вода становить від 17:1 до 7:1;
(b) нагрівання розчину, отриманого на стадії (а), до підвищеної температури;
(c) поступового додавання розчину, отриманого на стадії (b), до ефірного антирозчинника при температурі з інтервалу від кімнатної температури до 55 °С доти, поки об'ємне співвідношення первинний спирт:ефірний антирозчинник не досягає значення від 5:1 до 1:1; де, після того, як додають від 10% до 40% від повної кількості розчину зі стадії (b), у отриманий розчин вводять зародки із зародкових кристалів монофумарату (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану у кристалічній формі, де зародкові кристали суспендують у вторинному спирті;
(d) поступового охолодження розчину із введеними зародками зі стадії (с) до температури, нижчої за кімнатну; та
(e) виділення твердої речовини шляхом фільтрування до одержання монофумарату (R)-3-(6-(4-метилфеніл)піридин-3-ілоксі)-1-азабіцикло[2.2.2]октану у кристалічній формі.
18. Спосіб одержання сполуки формули II або її солі
 ; (II)
; (II)
що включає
а) здійснення взаємодії сполуки формули III
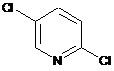 (III)
(III)
зі сполукою формули IV
 (IV) та/або
(IV) та/або
зі сполукою формули IVA
 , (IVА)
, (IVА)
де М1 являє собою лужний метал та n=1, або М1 являє собою лужноземельний метал та n=2;
у присутності паладієвого каталізатора; основи, вибраної з карбонатної основи, фосфатної основи, гідроксидної основи та алкоголятної основи; води та інертного розчинника;
до одержання сполуки формули II; та
b) необов'язкове перетворення сполуки формули II у її сіль.
19. Спосіб за п. 18, де зазначену реакцію здійснюють при рН від 10,5 до 13.
20. Спосіб за будь-яким з пп. 18 або 19, де зазначений інертний розчинник являє собою частково водорозчинний розчинник; де цистеїн додають до двофазної реакційної суміші після утворення сполуки формули II; фази розділяють та сполуку формули II виділяють з неводної фази.
21. Спосіб одержання сполуки формули І
 (I)
(I)
або її солі, що включає
с) здійснення взаємодії сполуки формули II
 (II)
(II)
або її солі зі сполукою формули V
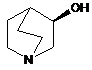 (V)
(V)
або її сіллю
при підвищеній температурі у присутності основи та інертного диполярного апротонного розчинника; де зазначена основа являє собою (M2)ОС(R)3, де М2 являє собою натрій або калій та кожен R незалежно являє собою С1-6алкіл, або два R разом з атомом вуглецю, з яким вони зв'язані, утворюють С4-6циклоалкіл, або зазначена основа являє собою гідроксидну основу; до одержання сполуки формули І; та
d) необов’язкове перетворення сполуки формули І у її сіль.
22. Спосіб за п. 21, де зазначену основу поступово додають до реакційної суміші.
23. Спосіб за будь-яким з пп. 21 або 22, де зазначена основа являє собою трет-бутанолат натрію або трет-бутанолат калію.
24. Спосіб за будь-яким з пп. 21-23, де зазначений інертний диполярний апротонний розчинник являє собою диметилсульфоксид.
25. Спосіб за п. 24, де зазначена реакційна суміш додатково включає толуол.
Текст
Реферат: Спосіб одержання гібридних кремнезем-желатинових матеріалів підвищеної гідрофобності включає розчинення желатини у дистильованій воді на водяній бані, додавання суспензії діоксиду кремнію та формування гелю, перемішування кремнезем-желатинової суспензії на магнітній мішалці та висушування кремнезем-желатинової суспензії у вигляді тонкого шару на полімерній підкладці при температурі приміщення. Крім цього кремнезем вводять у суспензію у кількості, що відповідає співвідношенню желатини до кремнезему від 1:1 до 4:1. UA 113409 U (54) СПОСІБ ОДЕРЖАННЯ ГІБРИДНИХ КРЕМНЕЗЕМ-ЖЕЛАТИНОВИХ МАТЕРІАЛІВ ПІДВИЩЕНОЇ ГІДРОФОБНОСТІ UA 113409 U UA 113409 U 5 10 15 20 25 30 35 40 45 50 55 60 Корисна модель належить до медицини, а саме до способів одержання біосумісних гібридних матеріалів на основі органічних і неорганічних речовин, зокрема з желатини та діоксиду кремнію, та може бути використана для репарації та реконструкції тканин, для іммобілізації ферментів і клітин, як лікарські форми, що забезпечують пролонговане вивільнення включених в пори матеріалу біологічно активних речовин тощо. Завдяки формуванню додаткових зв'язків між активними групами полімеру та діоксиду кремнію гібридні кремнезем-желатинові матеріали характеризуються підвищеною міцністю, покращеними механічними властивостями, підвищеною резистентністю до набухання та розчинення у водному середовищі, уповільненням десорбції активних речовин. Підвищення гідрофобності (зниження гідрофільності) гібридних матеріалів, що використовуються як лікарські форми, мало б сприяти додатковому покращенню їх властивостей. Дійсно, можна очікувати, що внаслідок послаблення взаємодії з водою такі матеріали будуть мати ще більшу стійкість до розчинення у біологічному середовищі, ще більш уповільнену десорбцію активних речовин, а також покращену біосумісність. Розробка способів одержання гібридних кремнезем-желатинових матеріалів підвищеної гідрофобності може мати і самостійну цінність; такі матеріали можуть бути використані як гідрофобні покриття чи покриття, що здатні до самоочищення. Гідрофобність/гідрофільність матеріалів може бути охарактеризована величиною крайового кута змочування. За ознакою, гідрофобними вважаються матеріали, для яких кут змочування (кут між нанесеною на поверхню краплею води та поверхнею) становить 90 градусів та вище. Відомо, що притаманні желатиновим матеріалам гідрофільні властивості пов'язані з присутністю в полімері амінокислот з полярними групами (лізин, аргінін, глютамінова кислота, аспарагінова кислота, гідроксипролін та гліцин), які мають високу спорідненість до молекул води. При створенні желатинових матеріалів частина цих груп бере участь у формуванні сітки гелю і виключається із взаємодії з водою. Сумарна гідрофільність/гідробофність матеріалу залежить від співвідношення гідрофобних груп полімеру та його полярних груп, які не приймають участь у формуванні сітки гелю і лишаються вільними для взаємодії з молекулами води [дивись статтю Gadomski W., Ratajska-Gadomska В.// Chemical Physics Letters. 2004. - V. 399. - P. 471]. У випадку гібридних матеріалів на загальну гідрофільність/гідрофобність матеріалів може впливати поява нових гідрофільних чи гідрофобних груп у результаті внесення в суспензію неорганічного матеріалу та зменшення кількості вільних полярних груп полімеру за рахунок формування додаткових зв'язків між органічною та неорганічною складовими гібридного матеріалу. Відомо про використання хімічно зшитих желатинових плівок з інкорпорованою в пори речовиною мелоксикамом в стоматології для лікування запальних процесів ясен. Плівки вводили в дентальну кишеню ротової порожнини для локального вивільнення активної речовини; у порівнянні з контролем, такі лікарські форми забезпечували рівномірне і довготривале вивільнення мелоксикаму та більш ефективне лікування пацієнтів [див. статтю Е.О. Cetin, N. Buduneli, E. Atlthan, L Kirilmaz. "In vitro studies of degradable device for controlled release of meloxicam", Journal of Clinical Periodontology, 200532 (7) (), 773-777]. Недоліком таких матеріалів є те, що в матеріалі залишаються незв'язані зшиваючі агенти або продукти їх хімічних реакцій з желатиною, які можуть проявляти токсичний ефект у готовому матеріалі. Відомий спосіб одержання кремнезем-желатинових матеріалів (Деклараційний патент України на корисну модель № 94703), який найбільш близький за технічним результатом та сукупністю суттєвих ознак, вибраний нами як прототип, який включає розчинення желатини у дистильованій воді на водяній бані при 60 °C при перемішуванні, додавання до розчину желатини суспензії діоксиду кремнію, перемішування суспензії за допомогою магнітної мішалки та висушування плівкоформуючої кремнезем-желатинової суспензії на полімерній підкладці при кімнатній температурі. Співвідношення желатини до кремнезему у суспензіях варіювалось від [Gel]/[SiO2]=100 до [Gel]/[SiO2]=5. Набухання отриманих плівок через 24 години (відношення кількості адсорбованої води до маси желатини у плівці) становило 190-350 %, крайовий кут змочування плівки дорівнював 78-85 градусам. Сукупними суттєвими ознаками відомого та заявленого способів є метод одержання желатинового гелю і гібридних кремнезем-желатинових матеріалів. Причиною, що перешкоджає одержанню технічного результату заявленого способу, є те, що, завдяки низькому вмісту діоксиду кремнію у суспензії, велика кількість полярних груп полімеру не приймає участі у взаємодії з силанольними групами кремнезему (чи з іншими групами полімеру) і лишається вільною для взаємодії з водою. 1 UA 113409 U 5 10 15 20 25 30 35 40 45 50 55 В основу корисної моделі поставлено задачу розробити спосіб одержання гібридних кремнезем-желатинових матеріалів, який би у результаті заявлених дій, забезпечив би підвищення їх гідрофобності, уповільнення набухання та пролонговане вивільнення інкорпорованих біологічно активних речовин. Поставлена задача вирішується тим, що спосіб включає розчинення желатини у дистильованій воді на водяній бані, додавання суспензії діоксиду кремнію та формування гелю, перемішування кремнезем-желатинової суспензії на магнітній мішалці та висушування кремнезем-желатинової суспензії у вигляді тонкого шару на полімерній підкладці при температурі приміщення. Згідно з корисною моделлю, кремнезем вводять у суспензію у кількості, що відповідає співвідношенню желатини до кремнезему від 1:1 до 4:1. За рахунок того, що діоксид кремнію вводять в суспензію у кількості, що відповідає співвідношенню желатини до кремнезему від [Gel]/[SiO2]= 1 ДО [Gel]/[SiO2]= 4, це приводить до зменшення кількості вільних полярних груп полімеру, що не приймають участь у формуванні зв'язків з іншими групами полімеру чи з силанольними групами кремнезему, та, відповідно, до підвищення гідрофобності матеріалу. При цьому співвідношення желатини до кремнезему в суспензії залишається досить високим для екранування надлишку гідрофільних силанольних груп введеного у суспензію кремнезему. (Адсорбція желатини па кремнеземі не перевищує 0,5 г/г, тобто навіть при співвідношенні [Gel]/[SiO2]=l кількість желатини в суспензії є більш ніж достатньою для формування моношару полімеру на поверхні частинок кремнезему та екранування надлишку полярних груп кремнезему). Для здійснення способу одержання кремнезем-желатинових матеріалів, який заявляється, використовували наступні реагенти: желатина (шкіра свині) фірма "Flukа"(Германія), 2006 р. діоксид кремнію ТУ У 24.6-05540209-003-2003 (кремнезем марки А-300) вода дистильована Н2О ГОСТ 6709-72 Гібридні кремнезем-желатинові матеріали з різним співвідношенням Gel:SiO2 одержували наступним чином. Для одержання розчину желатини наважку желатини розчиняли в певному об'ємі води і нагрівали на водяній бані до 60 °C при перемішуванні протягом 20 хв до повного розчинення желатини. Для приготування суспензії кремнезему до відповідної наважки кремнезему додавали дистильовану воду. Отриману суспензію перемішували на магнітній мішалці 20 хв. Для приготування кремнезем-желатинових матеріалів розчин желатини та суспензію кремнезему змішували і перемішували на магнітній мішалці ще протягом 5 хвилин, після чого певний об'єм кремнезем-желатинової суспензії виливали тонким шаром на полімерну підкладку та висушували при температурі приміщення (не нижче 15 °C) протягом кількох діб. При вивченні набухання плівок зразки зважували, занурювали у воду на 24 години, потім витягували їх з рідини та визначали приріст маси за рахунок поглинання води. Вимірювання крайового кута змочування проводили на установці з цифровим мікроскопом з 200-кратним збільшенням, об'єм краплі становив близько 10 мкл. Суть корисної моделі пояснюється конкретними прикладами виконання. Приклад 1. До 800 мг желатини додавали 5 мл дистильованої води та нагрівали на водяній бані (60 °C) при перемішуванні протягом 20 хв. до розчинення желатини. До наважки кремнезему 200 мг додавали 5 мл води. Отриману суспензію перемішували на магнітній мішалці 20 хв. До 5 мл розчину желатини при 60 °C додавали 5 мл суспензії кремнезему та перемішували суспензію протягом 5 хв. 2 мл плівкоформуючої кремнезем-желатинової суспензії виливали тонким шаром на полімерну підкладку та висушували при кімнатній температурі (не нижче 15 °C) протягом трьох діб. Концентрація желатини у плівкоформуючій кремнезем-желатиновій суспензії становила 80 мг/мл, концентрація кремнезему - 20 мг/мл. Співвідношення желатини до кремнезему в суспензії і в плівці дорівнювало [Gel]/[SiO2]=4. Набухання отриманих плівок (відношення кількості адсорбованої води до маси желатини у плівці) через 24 години становило 185 %, крайовий кут змочування для одержаної плівки становив 87 градусів. Приклад 2. Виконували згідно з прикладом 1, за винятком того, що наважка желатини при приготуванні розчину становила 600 мг. Концентрація желатини у плівкоформуючій суспензії становила 60 мг/мл, концентрація кремнезему 20 мг/мл. Співвідношення желатини до кремнезему в суспензії і в плівці дорівнювало [Gel]/[SiO2]=3. Крайовий кут змочування для 2 UA 113409 U 5 10 15 20 25 30 35 40 одержаної плівки становив 90 градусів, набухання плівки через 24 години становило 180 %. Одержана плівка, згідно з визначенням, може вважатися гідрофобною. Приклад 3. Виконували згідно з прикладом 1, за винятком того, що наважка желатини при приготуванні розчину становила 500 мг. Концентрація желатини у плівкоформуючій суспензії становила 50 мг/мл, концентрація кремнезему 20 мг/мл. Співвідношення желатини до кремнезему в суспензії і в плівці дорівнювало [Gel]/[SiO2]=2,5. Крайовий кут змочування для одержаної плівки становив 92 градуси, набухання плівки через 24 години - 170 %. Приклад 4 (желатинова плівка). До 500 мг желатини додавали 5 мл дистильованої води та нагрівали на водяній бані (60 °C) при перемішуванні протягом 20 хв. до розчинення желатини. Потім до розчину додавали ще 5 мл води і перемішували на мішалці ще 5 хв. Отриманий розчин виливали тонким шаром на полімерну підкладку та висушували при кімнатній температурі. Концентрація желатини у плівкоформуючій желатиновій суспензії суспензії становила 50 мг/мл. Крайовий кут змочування для одержаної плівки становив 75 градусів, набухання плівки через 24 години - 360 %. Приклад 5. Виконували згідно з прикладом 1, за винятком того, що наважка желатини при приготуванні розчину становила 400 мг. Концентрація желатини у плівкоформуючій суспензії становила 40 мг/мл, концентрація кремнезему 20 мг/мл. Співвідношення желатини до кремнезему в суспензії і в плівці дорівнювало [Gel]/[SiO2]=2. Крайовий кут змочування для одержаної плівки становив 92 градусів, набухання плівки через 24 години - 160 %. Приклад 6. Виконували згідно з прикладом 1, за винятком того, що наважка желатини при приготуванні розчину становила 200 мг. Концентрація желатини у плівкоформуючій суспензії становила 20 мг/мл, концентрація кремнезему 20 мг/мл. Співвідношення желатини до кремнезему в суспензії і в плівці дорівнювало [Gel]/[SiO2]= 1. Крайовий кут змочування для одержаної плівки становив 92 градусів, набухання плівки через 24 години – 160 %. Приклад 7. Виконували згідно з прикладом 1, за винятком того, що наважка желатини при приготуванні розчину становила 160 мг, а наважка кремнезему при приготуванні суспензії становила 200 мг. Концентрація желатини у плівкоформуючій суспензії становила 16 мг/мл, концентрація кремнезему - 20 мг/мл. Співвідношення желатини до кремнезему в суспензії і в плівці дорівнювало [Gel]/[SiO2]=0,8. Недоліком плівки є ії крихкість. Таким чином, приклад показує недоречність зменшення співвідношення желатини до кремнезему до значень, нижчих за [Gel]/[SiO2]=1. Приклад 8 (прототип). До 1 г желатини додавали 5 мл дистильованої води та нагрівали на водяній бані (60 °C) при перемішуванні протягом 20 хв до розчинення желатини. До наважки кремнезему 200 мг додавали 5 мл води. Отриману суспензію перемішували на магнітній мішалці 20 хв. До 5 мл розчину желатини при 60 °C додавали 5 мл суспензії кремнезему та перемішували суспензію протягом 5 хв. 2 мл плівкоформуючої кремнезем-желатинової суспензії виливали тонким шаром на полімерну підкладку та висушували при кімнатній температурі (не нижче 15 °C) протягом кількох діб. Концентрація желатини у плівкоформуючій кремнезем-желатиновій суспензії становила 100 мг/мл, концентрація кремнезему 20 мг/мл. Співвідношення желатини до кремнезему в суспензії і в плівці дорівнювало [Gel]/[SiO2]=5. Набухання отриманих плівок через 24 години становило 190 %, крайовий кут змочування для одержаної плівки становив 85 градусів. Дані за прикладами 1-8 наведені в таблиці. 45 Таблиця Приклади Приклад 1 Приклад 2 Приклад 3 Приклад 4 (желатинова плівка) Приклад 5 Приклад 6 Приклад 7 Приклад 8 (прототип) [Gel], г/л [SiO2], г/л 80 60 50 20 20 20 [Gel]/[SiO2], Набухання Крайовий кут Примітка г/г плівок, % змочування, град 4 180 87 3 170 90 2,5 165 92 50 40 20 16 100 360 20 20 20 20 2 1 0,8 5 де: 3 78 160 160 190 92 92 85 крихка UA 113409 U 5 10 15 20 -[Gel] - концентрація желатини у суспензіях; -[SiO2] - концентрація діоксиду кремнію у суспензіях; -|Gel]/[SiO2] - співвідношення желатини та діоксиду кремнію. Як видно із таблиці, гідрофобність гібридних кремнезем-желатинових матеріалів (крайовий кут змочування) залежить від співвідношення желатини та кремнезему в плівкоформуючій суспензії. Використання кремнезему у таких плівках, замість хімічних зшиваючих агентів, дозволяє уникнути появи у матеріалі потенційно токсичних речовин (зшиваючих агентів чи продуктів їх хімічних реакцій з желатиною), забезпечуючи при цьому необхідне уповільнення набухання композитів і, як наслідок, пролонговану десорбцію біологічно активних сполук. Приклади 1-6 демонструють, що суто желатинова плівка є гідрофільним матеріалом, тоді як додавання кремнезему поступово підвищує її гідрофобність. При низькому вмісті желатини в суспензії збільшується час гелеутворення, плівка довше застигає. Таким чином, з нашої точки зору, оптимальним співвідношенням желатини до кремнезему у суспензії є [Gel]/[SiO2]=2-2,5. Експериментально доведено, що зменшення співвідношення желатини та кремнезему |Gel]/[SiO2] від 5 до 2 приводить до поступового збільшення крайового кута змочування матеріалу. Підвищення гідрофобності плівок супроводжується уповільненням їх набухання. Зменшення співвідношення желатини до кремнезему до значень [Gel]/[SiO2] < 1 виявилося недоцільним, оскільки одержані гібридні кремнезем-желатинові матеріали стають крихкими. Таким чином, корисна модель дозволяє простим та дешевим способом одержувати гібридні кремнезем-желатинові матеріали з підвищеною гідрофобністю та уповільненим набуханням, при цьому ступінь гідрофобності матеріалів можна контролювати, змінюючи співвідношення желатини та кремнезему в плівкоформуючій суспензії. Одержані у такий спосіб матеріали можуть бути основою для створення препаратів з пролонгованим вивільненням інкорпорованих біологічно активних речовин. 25 ФОРМУЛА КОРИСНОЇ МОДЕЛІ 30 Спосіб одержання гібридних кремнезем-желатинових матеріалів підвищеної гідрофобності, який включає розчинення желатини у дистильованій воді на водяній бані, додавання суспензії діоксиду кремнію та формування гелю, перемішування кремнезем-желатинової суспензії на магнітній мішалці та висушування кремнезем-желатинової суспензії у вигляді тонкого шару на полімерній підкладці при температурі приміщення, який відрізняється тим, що кремнезем вводять у суспензію у кількості, що відповідає співвідношенню желатини до кремнезему від 1:1 до 4:1. 35 Комп’ютерна верстка Г. Паяльніков Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 4
ДивитисяДодаткова інформація
Назва патенту англійськоюSalts of aza-bicyclic di-aryl ethers and methods to make them or their precursors
Автори англійськоюMarterer, Wolfgang, Prashad, Mahavir, Villhauer, Edwin Bernard, Waykole, Liladhar Murlidhar, Vivelo, James Anthony, Sutter, Bertrand, Bianchi, Jean-Claude, Wu, Raeann, Har, Denis, Karpinski, Piotr H., Pignone, Massimo, Stingelin, Doris, Buerger, Eckart
Автори російськоюМартерер Вольфганг, Прашад Махавир, Виллхауер Эдвин Бернард, Уэйкол Лиладхар Мурлидхар, Вивело Джэймс Энтони, Саттер Бертран, Бьянки Жан-Клод, Ву Раеанн, Хар Дени, Карпински Пиотр Х., Пиньоне Массимо, Стингелин Дорис, Бюргер Эккарт
МПК / Мітки
МПК: C07D 453/02, A61K 31/439
Мітки: солі, ефірів, азабіциклічних, способи, діарилових, одержання, попередників
Код посилання
<a href="https://ua.patents.su/6-113409-soli-azabiciklichnikh-diarilovikh-efiriv-ta-sposobi-kh-oderzhannya-abo-oderzhannya-kh-poperednikiv.html" target="_blank" rel="follow" title="База патентів України">Солі азабіциклічних діарилових ефірів та способи їх одержання або одержання їх попередників</a>
Попередній патент: Комбінації активних сполук, що містить протіоконазол та іпродіон
Наступний патент: Пестицидні суміші, що включають похідні ізоксазоліну
Випадковий патент: Електрохімічний перетворювач теплоти в електроенергію










