Пептид і фармацевтична композиція, що здатні інгібувати секрецію пепсину
Номер патенту: 55369
Опубліковано: 15.04.2003
Автори: ДЕКРУА-ВАНЬ Монік, ТАРРАД Тьєрі, ПАНСЮ Даніель
Формула / Реферат
1. Пептид общей формулы I
A1-A2-A3-X, (І)
где A1 означает радикал L-Thr или D-Thr, или одну из следующих последовательностей,
Val-Thr,
Pro-Val-Thr,
Arg-Pro-Val-Thr,
Glu-Arg-Pro-Val-Thr,
His-Glu-Arg-Pro-Val-Thr,
Gln-His-Glu-Arg-Pro-Val-Thr,
Leu-Gln-His-Glu-Arg-Pro-Val-Thr,
Ile-Leu-Gln-His-Glu-Arg-Pro-Val-Thr,
Ser-Ile-Leu-Gln-His-Glu-Arg-Pro-Val-Thr,
Ser-Ser-Ile-Leu-Gln-His-Glu-Arg-Pro-Val-Thr,
Lys-Ser-Ser-Ile-Leu-Gln-His-Glu-Arg-Pro-Val-Thr,
Gly-Lys-Ser-Ser-Ile-Leu-Gln-His-Glu-Arg-Pro-Val-Thr,
Pro-Gly-Lys-Ser-Ser-Ile-Leu-Gln-His-Glu-Arg-Pro-Val-Thr,
Glu-Pro-Gly-Lys-Ser-Ser-Ile-Leu-Gln-His-Glu-Arg-Pro-Val-Thr,
в которой, по меньшей мере, один радикал аминокислоты может иметь D-конфигурацию;
A2 представляет собой последовательность Lys-Pro-Gln-Ala, в которой, по меньшей мере, один радикал аминокислоты может иметь D-конфигурацию;
A3 означает ковалентную связь или пептидную последовательность –Gly-A4-A5, где A4 и A5, независимо друг от друга, каждая представляет собой основный остаток аминокислоты;
X представляет собой гидрокси, амино, алкиламиногруппу, причем указанный пептид формулы I содержит, по меньшей мере, один радикал D-конфигурации и может содержать одну или больше одинаковых или различных защитных групп, или их фармацевтически приемлемые соли.
2. Пептид, отличающийся тем, что содержит последовательность аминокислот A1-A2-A3, в которой A1, A2 и А3 определены в соответствии с пунктом 1, при этом пептид содержит, по меньшей мере, один радикал аминокислоты D-конфигурации.
3. Пептид по п. 1 или 2, отличающийся тем, что содержит одну или больше одинаковых или различных защитных групп.
4. Пептид по п.3, отличающийся тем, что содержит, по меньшей мере, один радикал лизина, защищенный ацетильной группой.
5. Пептид по любому из пп.1 - 4, отличающийся тем, что содержит один радикал аминокислоты D-конфигурации.
6. Пептид по п. 5, отличающийся тем, что радикал аминокислоты D-конфигурации находится на С-конце или на N-конце.
7. Пептид по п. 6, отличающийся тем, что радикал аминокислоты D-конфигурации находится на С-конце.
8. Пептид по любому из пп. 4-6, отличающийся тем, что A2 обозначает Lys-Pro-Gln-D-Ala и A3 означает ковалентную связь.
9. Пептид по п. 8, отличающийся тем, что имеет формулу Thr-Lys-Pro-Gln-D-Ala-NH2 или Тhr-(ацетил)Lys-Рrо-Gln-D-Аla-NН2.
10. Пептид по п. 8, отличающийся тем, что имеет формулу Pro-Val-Thr-Lys-Pro-Gln-D-Ala-NH2 или Pro-Val-Thr-(ацетил)Lys-Pro-Gln-D-Ala-NH2 .
11. Пептид по п. 8, отличающийся тем, что имеет формулу His-Glu-Arg-Pro-Val-Thr-Lys-Pro-Gln-D-Ala-NH2.
12. Пептид по п. 8, отличающийся тем, что имеет формулу lle-Leu-Gln-His-Glu-Arg-Pro-Val-Thr-Lys-Pro-GIn-D-AIa-NH2.
13. Пептид по п. 8, отличающийся тем, что имеет формулу Glu-Pro-Gly-Lys-Ser-Ser-lle-Leu-Gln-His-Glu-Arg-Pro-Val-Thr-Lys-Pro-Gln-D-Ala-NH2.
14. Пептид по п. 6, отличающийся тем, что радикал аминокислоты D-конфигурации находится на N-конце.
15. Пептид по п. 14, отличающийся тем, что A1 обозначает D-Thr или вышеуказанную последовательность, в которой радикал аминокислоты на N-конце этой последовательности имеет D-конфигурацию.
16. Пептид по п. 15, отличающийся тем, что имеет формулу D-Pro-Val-Thr-Lys-Pro-Gln-Ala-NH2.
17. Пептид по любому из пп.1-4, отличающийся тем, что в нем содержатся два радикала аминокислоты D-конфигурации.
18. Пептид по п. 17, отличающийся тем, что радикал аминокислоты D-конфигурации располагается на С-конце.
19. Пептид по любому из пп. 17-18, отличающийся тем, что второй радикал аминокислоты D-конфигурации расположен на N-конце пептида.
20. Пептид по п.19, отличающийся тем, что имеет формулу D-Pro-Val-Thr-Lys-Pro-Gln-Ala-NH2.
21. Пептид по п.19, отличающийся тем, что имеет формулу D-Pro-Val-Thr-(ацетил)Lys-Pro-Gln-D-Ala-NH2.
22. Фармацевтическая композиция, ингибирующая высвобождение пепсина, содержащая активный компонент и фармацевтически приемлемый носитель или разбавитель, отличающаяся тем, что она содержит в качестве активного компонента эффективное количество, по меньшей мере, одного пептида по любому из пп. 1 – 21.
Текст
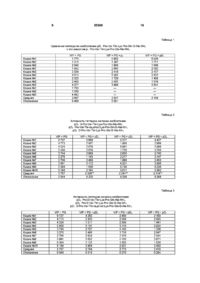
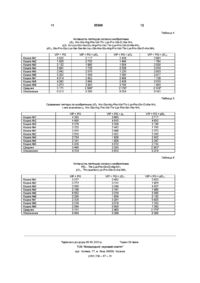
1 Пептид общей формулы І АгА2-Аз-Х, (І) где Аі означает радикал L-Thr или D-Thr, или одну из следующих последовательностей, Val Thr Pro Val Thr Arg Pro Val Thr Glu Arg Pro Val Thr His Glu Arg Pro Val Thr Gin His Glu Arg Pro Val Thr Leu Gin His Glu Arg Pro Val Thr lie Leu Gin His Glu Arg Pro Val Thr Ser lie Leu Gin His Glu Arg Pro Val Thr Ser Ser lie Leu Gn His Gu Arg Pro Val Thr i l Lys Ser Ser lie Leu Gin His Glu Arg Pro Val Thr Gly Lys Ser S r lie Leu Gn His Glu Arg Pro Val Thr e i Pro Gy Lys Ser Ser lie Leu Gin His Glu Arg Pro Val Thr l Glu Pro Gly Lys Ser Ser lie Leu Gn His Gu Arg Pro Val Thr i l в которой, по меньшей мере, один радикал аминокислоты может иметь D-конфигурацию, Аг представляет собой последовательность LysPro-Gln-Ala, в которой, по меньшей мере, один радикал аминокислоты может иметь Dконфигурацию, Аз означает ковалентную связь или пептидную последовательность -Gly-A4-As, где А4 и As, независимо друг от друга, каждая представляет собой основный остаток аминокислоты, X представляет собой гидрокси, амино, алкиламиногруппу, причем указанный пептид формулы I содержит, по меньшей мере, один радикал Dконфигурации и может содержать одну или больше одинаковых или различных защитных групп, или их фармацевтически приемлемые соли 2 Пептид, отличающийся тем, что содержит последовательность аминокислот А1-А2-А3, в которой А-і, Аг и Аз определены в соответствии с пунк том 1, при этом пептид содержит, по меньшей мере, один радикал аминокислоты Dконфигурации 3 Пептид по п 1 или 2, отличающийся тем, что содержит одну или больше одинаковых или различных защитных групп 4 Пептид по п 3, отличающийся тем, что содержит, по меньшей мере, один радикал лизина, защищенный ацетильной группой 5 Пептид по любому из пп 1 - 4, отличающийся тем, что содержит один радикал аминокислоты Dконфигурации 6 Пептид по п 5, отличающийся тем, что радикал аминокислоты D-конфигурации находится на С-конце или на N-конце 7 Пептид по п 6, отличающийся тем, что радикал аминокислоты D-конфигурации находится на С-конце 8 Пептид по любому из пп 4-6, отличающийся тем, что Аг обозначает Lys-Pro-Gln-D-Ala и Аз означает ковалентную связь 9 Пептид по п 8, отличающийся тем, что имеет формулу Thr-I_ys-Pro-Gln-D-Ala-NH2 или Thr(a4e™-|)Lys-Pro-Gln-D-Ala-NH2 10 Пептид по п 8, отличающийся тем, что имеет формулу Pro-Val-Thr-I_ys-Pro-Gln-D-Ala-NH2 или Pro-Val-Thr-(a4eTHn)Lys-Pro-Gln-D-Ala-NH2 11 Пептид по п 8, отличающийся тем, что имеет формулу His-Glu-Arg-Pro-Val-Thr-Lys-Pro-Gln-DAla-NH2 12 Пептид по п 8, отличающийся тем, что имеет формулу Ile-Leu-Gln-His-Glu-Arg-Pro-Val-Thr-LysPro-Gln-D-Ala-NH2 13 Пептид по п 8, отличающийся тем, что имеет формулу Glu-Pro-Gly-Lys-Ser-Ser-lle-Leu-Gln-HisGlu-Arg-Pro-Val-Thr-I_ys-Pro-Gln-D-Ala-NH2 14 Пептид по п 6, отличающийся тем, что радикал аминокислоты D-конфигурации находится на N-конце 15 Пептид по п 14, отличающийся тем, что Аі обозначает D-Thr или вышеуказанную последовательность, в которой радикал аминокислоты на Nконце этой последовательности имеет Dконфигурацию 16 Пептид по п 15, отличающийся тем, что имеет формулу D-Pro-Val-Thr-Lys-Pro-Gln-Ala-NH2 17 Пептид по любому из пп 1-4, отличающийся тем, что в нем содержатся два радикала амино О (О го ю ю 55369 кислоты D-конфигурации 18 Пептид по п 17, отличающийся тем, что радикал аминокислоты D-конфигурации располагается на С-конце 19 Пептид по любому из пп 17-18, отличающийся тем, что второй радикал аминокислоты Dконфигурации расположен на N-конце пептида 20 Пептид по п 19, отличающийся тем, что имеет формулу D-Pro-Val-Thr-I_ys-Pro-Gln-Ala-NH2 21 Пептид по п 19, отличающийся тем, что име Объектом изобретения являются пептиды, способные ингибировать высвобождение пепсина, их замещенные производные и их соли, а также фармацевтические композиции, содержащие эти пептиды Пептиды могут использоваться при лечении болезней, связанных с высвобождением пепсина, и, в частности, при лечении язв или эзофагита Известен пептид из кишечника свиньи этот пептид, названный сорбином, насчитывает 153 природные аминокислоты (WO 89/06241) Сорбин, также как и пептидные фрагменты С-концевой части сорбина (содержащие, кроме того, 40 аминокислот), способны вызывать увеличение поглощения слизистой оболочкой Однако модификация этих пептидных фрагментов путем включения по меньшей мере одного радикала аминокислоты D-конфигурации, оказалось, обладает новой биологической активностью, способной замедлять высвобождение пепсина, что не было присуще не модифицированным пептидам Эта активность представляет особый интерес Общие механизмы желудочной секреции у млекопитающих в настоящее время хорошо известны Желудочное пищеварение осуществляется под действием ферментов, соляной кислоты и пепсина Пепсин - это белок, который наряду с гастрином, является одним из основных компонентов желудочного сока Его основной физиологической функцией является инициация разложения белков Однако многочисленные исследования показали, что он способствует образованиюязв Следовательно, в определенных ситуациях желательно замедлить, по меньшей мере частично, высвобождение пепсина Объектом изобретения является пептид общей формулы I АгАз-Аз-Х, где Аі означает радикал L-Thr или D-Thr, или одну из следующих последовательностей, Val Thr Pro Val Thr Arg Pro Val Thr Glu Arg Pro Val Thr His Glu Arg Pro Val Thr Gin His Glu Arg Pro Val Thr L u Gin His Glu Arg Pro Val Thr e lie L u Gin His Glu Arg Pro Val Thr e Ser lie Leu Gin His Glu Arg Pro Val Thr Ser Ser lie L u Gin His Glu Arg Pro Val Thr e Lys Ser Ser lie L u Gin His Glu Arg Pro Val Thr e Gly Lys Ser S r lie L u Gn His Glu Arg Pro Val Thr e e i Pro Gy Lys Ser Ser lie L u Gin His Glu Arg Pro Val Thr l e Glu Pro Gly Lys Ser Ser lie L u Gin His Glu Arg Pro Val Thr e в которой, по меньшей мере, один радикал аминокислоты может иметь D-конфигурацию, Аг представляет собой последовательность Lys-Pro-Gln-Ala, в которой по меньшей мере один 4 ет формулу D-Pro-Val-Thr-^eTHn)l_ys-Pro-Gln-DAla-NH2 22 Фармацевтическая композиция, ингибирующая высвобождение пепсина, содержащая активный компонент и фармацевтически приемлемый носитель или разбавитель, отличающаяся тем, что она содержит в качестве активного компонента эффективное количество, по меньшей мере, одного пептида по любому из пп 1 - 21 радикал аминокислоты может иметь Dконфигурацию, Аз означает ковалентную связь или пептидную последовательность -Gly-A4-As, где А4 и As, независимо друг от друга, каждая представляют собой основный остаток аминокислоты, X представляет собой гидрокси, амино, алкиламиногруппу, причем указанный пептид формулы I содержит, по меньшей мере, один радикал Dконфигурации и может содержать одну или больше одинаковых или различных защитных групп, или их фармацевтически приемлемые соли Изобретение также касается замещенных производных пептидов общей формулы І, в которой один или несколько радикалов аминокислоты замещены одной или несколькими пептидными защитными группами, которые широко используются в химии и биологии, в случае замещения несколькими защитными группами их идентичность не обязательна Предпочтительно, защитные группы выбирают из групп низшего алкила, таких как метил или третичный бутил, фенил, бензил или замещенный бензил, такой как триметоксибензил, 2-хлорбензилоксикарбонил, 9фторенилметилоксикарбонил, третбутилоксикарбонил, ацетил, сульфонил и фосфорил Объектом изобретения также являются пептиды, содержащие последовательность аминокислот А1-А2-А3, в которой А-і, Аг и Аз являются такими, как они определены выше Изобретение касается также фармацевтически приемлемых солей пептидов, определенных выше Эти соли можно получить с органическими кислотами, такими как уксусная кислота, молочная, малеиновая, лимонная, яблочная, аскорбиновая, бензойная, салициловая, янтарная, метансульфокислота, тол уолсульфо кислота, или с минеральными кислотами, такими как соляная кислота, серная кислота или фосфорная кислота, или же с полимерными кислотами, такими как танин или карбоксиметилцеллюлоза А4 и As означают, независимо друг от друга, когда они присутствуют в пептидах по изобретению, радикалы основной аминокислоты конфигурации D или L Преимущественно А4 и As представляют, независимо, радикал аминовой кислоты Lys, D-Lys, Arg или D-Arg Вышеназванные пептиды по изобретению содержат один или несколько радикалов аминокислоты D-конфигурации Объектом изобретения, в частности, являются пептиды, содержащие радикал аминокислоты D-конфигурации, при этом на 55369 лоты Связывание осуществляется в основном в званные пептиды могут замещаться защитными присутствии агента связывания, такого как дицикгруппами, указанными в настоящем изобретении логексилкарбодиимид или диизопропилкарбодииМожно привести следующий пример пептидов мид Пептидная цепь, образованная таким обраThr Lys Pro Gin D Ala NH2 Thr Lys Pro Gin D Ala Gly l_ys Lys NH2 зом, включает две аминокислоты с защищенной Thr (ацетил )Lys Pro Gin 0 Ala NH аминогруппой Как указано выше, снимают защиту Pro Val Thr Lys Pro Gin D Ala NH Pro D Val Thr Lys Pro Gin Ala NH с концевой аминогруппы и затем осуществляют Pro Val Thr Lys Pro Gin Ala Gly Arg D Arg NH присоединение третьей аминокислоты Таким обPro Val Thr (ацетил)1уэ Pro Gin D Ala NH D Pro Val Thr Lys Pro Gin Ala NH разом, происходит последовательное присоедиHis Glu Arg Pro Val Thr Lys Pro Gin D Ala NH нение аминокислот одна за другой и построение lie Leu Gin His Glu Arg Pro Val Thr Lys Pro Gin D Ala NH Glu Pro Gly Lys Ser Ser lie Leu Gin His Glu Arg Pro Val Thr Lys Pro Gin D желаемой пептидной цепи После удаления всех Ala NH защитных групп пептид отщепляют от смолы Радикал аминокислоты D-конфигурации расНиже кратко описан синтез пептида по изополагается преимущественно на С-концевом или бретению, а именно Pro-Val-Thr-Lys-Pro-Gln-D-AlaN-концевом участке Предпочитаемые пептиды, NH2 Остальные пептиды по изобретению могут которые имеют радикал аминокислоты Dбыть получены соответствующими модификацияконфигурации на С-конце, являются пептидами, в ми описанного ниже пептидного синтеза, которые которых Аг означает Lys-Pro-Gln-D-Ala и аз ознахорошо знакомы специалистам в данной области чает ковалентную связь Предпочтительно, чтобы пептиды, которые имеют радикал аминокислоты Синтез осуществляется в твердой фазе при D-конфигурации на М-конце, представляли собой комнатной температуре Используемый рабочий пептиды, в которых Аі означает D-Thr или вышережим включает следующие этапы снятие защиуказанную последовательность, и радикал аминоты, нейтрализация и связывание Используется кислоты на N-конце этой последовательности смола типа полистирола, структурированного на имеет D-конфигурацию 1% дивинилбензолом (смола Мерифилда) Фиксация Boc-D-Ala на смоле Мерифилда производится Объектом изобретения также, в частности, в присутствии карбоната цезия в толуоле и димеявляются пептиды, которые имеют два радикала тилформамиде (ДМФ) Концевая аминогруппа исаминокислоты D-конфигурации, причем названпользуемых аминокислот защищается группой ные пептиды могут замещаться защитными групВое пами, определенными настоящим изобретением Можно привести следующий пример пептидов Эти группы Вое замещаются трифторуксуснои D Pro Val Thr Lys Pro Gin D Ala NH2 кислотой, затем производят несколько промываD Pro Val Thr Lys Pro Gin Ala Gly D Lys NH2 ний метиленхлоридом и изопропанолом АминоPro D Val Thr Lys Pro Gin D Ala NH2 D Pro Val Tnr (ацетил)Lys-Pro Gin D Ala NH группы нейтрализуются триэтиламином, затем Преимущественно, пептиды, содержащие два следует несколько промываний Треонин и валин радикала аминокислоты D-конфигурации, имеют перед связыванием превращаются в сложный один радикал на С-конце, а второй может распоэфир гидроксибензотриазола в присутствии диилагаться в любом месте на пептидной цепи, но зопропилкарбодиимида (DIPCDI), для глутамина преимущественно он находится на N-конце пептисложный эфир гидроксибензотриазола производа Предпочтительными пептидами являются те, в дится прямо в реакторе Лизин и оба пролина которых Аі представляет собой D-Thr или вышетрансформируются в симметричный ангидрид названную последовательность, в которой радиперед связыванием Во всех случаях связывание кал аминокислоты на N-конце этой последоваосуществляется в присутствии диизопропилэтительности имеет D-конфигурацию, Аг означает ламина Боковая цепь лизина защищается группой Lys-Pro-Gln-D-Ala, и аз означает ковалентную Fmoc, в то время как боковая цепь треонина не засвязь Такими пептидами, преимущественно, явщищается Когда заканчивается последнее связыляются пептиды, имеющие одну или несколько вание, группу Fmoc снимают с помощью пиперидизащитных групп, и, в частности, ацетильную зана в диметилформамиде перед замещением щитную группу на радикале Lys группы Вое N-концевой аминогруппы пролина Пептид получают отщеплением от смолы после Пептиды по изобретению могут быть получеобработки нашатырным спиртом в смеси метаны в соответствии с одним из известных классинол/ДМФ Полученный таким образом исходный ческих методов в области пептидных синтезов, продукт затем очищается например, с помощью твердофазного синтеза, который осуществляется по следующей схеме Объектом изобретения также являются фаробразование пептидной цепи начинается фиксамацевтические композиции, содержащие в качестцией первой аминокислоты с С-конца цепи, на ве активного ингредиента по меньшей мере один смоле, посредством ее карбоксильной группы, ее вышеназванный пептид формулы I, одно вышенааминогруппу защищают присоединением третзванное замещенное производное такого пептида бутилоксикарбонила (Вое) После присоединения или пептид, содержащий вышеназванную послеСООН-группы первой аминокислоты снимают задовательность аминокислоты А1-А2-А3, вместе с щиту с NH2-rpynnbi путем промывания смолы кифармацевтически приемлемым носителем или слотой В случае защитной группы Вое, снятие растворителем защиты может производиться с помощью трифтоПептиды настоящего изобретения могут вворуксуснои кислоты Вторая аминокислота с защидиться орально, внутривенно, парентерально, щенной аминогруппой присоединяется посредстподкожно, внутрибрюшинно или внутримышечно вом своей карбоксильной группы по Фармацевтическая композиция может быть в освободившейся аминогруппе первой аминокисвиде желатиновой капсулы, таблетки, лиофилиза2 2 2 2 2 2 2 2 2 2 55369 8 та или жидкости в соответствии с выбранным спокомпозиции собом введения Фармацевтическая композиция В виде лиофилизата также может быть в виде препарата с замедленПептид согласно изобретению 0,10мг ным выделением Маннит 25,00мг Пептид настоящего изобретения можно наХлористый натрий 4,50мг значать человеку для орального применения в В виде раствора дозе от 5 до 100мкг/кг в день Пептид согласно изобретению 0,30мг Внутривенно или подкожно соединение по Спирт 250,00мг изобретению можно назначать человеку в дозе от Вода 0,75мг 1 до 12мкг/кг от одного до трех раз в день В оргаВ виде эмульсии низме животных соединения настоящего изобреПептид согласно изобретению 0,30мг тения обнаруживались в значительных количестПолисорбат 5,00мг вах через несколько дней после инъекции, в Нейтральное масло 500,00мг частности, пептид Pro-Val-Thr-Lys-Pro-Gln-D-AlaВода 0,50мг NH2 обнаружен в количестве, превышающем 10% В виде таблеток Токсичность Пептид согласно изобретению 0,45мг Токсичность была изучена на крысах и собаГид роксипрол ил целлюлоза 22,00мг ках Через четыре недели после введения доз, Стеарат магния 0,10мг достигающих 4000мкг/кг/день, не было обнаружеПример 2 но никаких признаков токсичности и никаких приАминокислоты пептидов PD2-PD7 связывают знаков, говорящих о мутагенной способности Для друг с другом согласно указанному в описании человека подкожная или внутривенная инъекция классическому методу с использованием бутилокдозы 200мкг/кг не влечет за собой никакой биолосикарбонила (Вое), который применяли для полугической, клинической или патологической аномачения пептида pDi а также с использованием в лии качестве исходного смолы 4Фармакология метилбензгидриламина Терапевтический интерес соединений наСвязывание различных аминокислот произвостоящего изобретения определяется следующим дят в диметилформамиде (DMF) в присутствии экспериментом бензотриазол-1 -илокситрис(диметиламино)фосфонийИнтенсивность желудочной реакции измерягексафторфосфата (ВОР), 1ется при определении объема вызванной желудочной секреции гидроксибензотриазола (HOBt) и N,Nдиизопропилэтиламина (DIEA) Кошкам была проведена операция под общей анестезией Желудок был разделен на две части Процесс связывания и снятия защиты поэтапна так называемый карман Хайденхейма и желуно приведен ниже дочную фистулу Эти два кармана выводят наружу 1 - T F A - ( 1 х1мин) для сбора секреции соляной кислоты, пепсина и 2 - Т Р А - (1 хЗмин) желудочного сока как во время основной фазы, 3 - DCM - Быстрое отмывание так и после стимуляции Поскольку эти животные 4 - изопропиловый спирт - (1 х 1 мин) имели хронические фистулы, они подвергались 5 - О М Р - (1 хЗмин) определенному количеству тестов каждую неделю 6 - связывание/DMF - (1 х 12мин) и служили одновременно контрольными образца7-DMF-(1 х1мин) ми Стимулирование секреции пепсина достига8 - связывание/DMF - (1 х 12мин) лось путем перфузионного введения животным 9- DMF- ( 2 x 1 мин) пентагастрина (PG) и VIP (вазоактивный желудоч(TFA - три фтору ксусная кислота, DCM - диный пептид) в течение 2 часов из расчета 2 и хлорметан) На каждом этапе использовали по 4 м кг/кг/ч 10мл растворителя на 1г смолы В процессе синтеза пептидов использовали следующие защитЧерез час после стимулирования пентагастные группы боковых цепей рином и VIP перфузионно были добавлены пептиды в дозе 100пмоль/кг/ч Объем желудочного сока бензил для треонина измеряют в течение 30 минут до и после перфу2-CIZ для лизина зии Количество пепсина в желудочном соке опреацетил для лизина в пептидах pD? и рОз деляется протеолитическим спектрофотометричеДля прерывания процесса с помощью смолы к ским методом Результаты, полученные в 9 - 12 смеси добавляли по 10мл фтористоводородной экспериментах, представлены в нижеприведенных кислоты на 1 грамм пептидной смолы и инкубиротаблицах 1 - 6, секреция пепсина выражена в вали 45 минут при 0°С в присутствии паракрезола мг/15 минут, средняя величина двух периодов по в качестве очистителя 15 минут во время базальной секреции и средняя После выпаривания фтористоводородной кивеличина 6 периодов по 15 минут во время стимуслоты продукт синтеза отмывали в эфире, растволированной секреции ряли в TFA, осаждали эфиром и высушивали Некоторые пептиды изобретения, имеющие Фракции, достаточно очищенные, разделяли и хотя бы один радикал D-аминокислоты, сравнилиофилизировали Конечные продукты проверяли ваются со своими аналогами, у которых все радиметодами аналитической высокоэффективной калы аминокислот имеют L-конфигурацию жидкостной хроматографии (HPLC), массспектроскопии и аминокислотного анализа Пример 1 Конкретные примеры приготовления фарм 55369 10 Таблица 1 Сравнение пептида по изобретению pD] Pro-Val-Thr-Lys-Pro-Gln-D-Ala-NH; с его аналогом pi Pro-Val-Thr-Lys-Pro-Gln-Ala-NH2 VIP + PG 1 775 1 316 2 049 1 852 3 334 4 010 2 520 2 409 4 277 1 750 1 556 4 442 2 607 0 468 Кошка №1 Кошка №2 Кошка №3 Кошка №1 Кошка №2 Кошка №3 Кошка №1 Кошка №2 Кошка №3 Кошка №1 Кошка №2 Кошка №3 Среднее Отклонение VIP+ PG + p, 0 952 1 367 1 680 2 993 2 418 5 392 1 729 2 403 3 989 — — — 2 547 0 351 VIP+ PG + pD, 0 926 1 711 1 846 2 082 2 157 3 932 1 456 1 516 3 891 — — — 2 169 Таблица 2 Активность пептидов согласно изобретению pD2 D-Pro-Val-Thr-Lys-Pro-Gln-Ala-NH2 pD3 Pro^al-Thr-(aMeTYm)Lys-Pro-Gln-D-Ala-NH; pD4 D-Pro-Val-Thr-Lys-Pro-Gln-D-Ala-NH2 Кошка №1 Кошка №2 Кошка №3 Кошка №4 Кошка №5 Кошка №6 Кошка №7 Кошка №8 Кошка №9 Кошка №10 Среднее Отклонение VIP + PG 6 727 4 773 4 324 2 458 3 744 3 276 2 708 3 991 0 384 5 184 3 757 0 544 VIP + PG + pD2 2 689 2 007 2 576 2 076 2 689 1 143 2 409 3 172 1 036 3 164 2 296** 0 235 VIP + PG + pD3 2,317 1,860 0,891 1,725 2,630 2,217 1,899 4,321 0,738 3,811 2 241** 0,358 VIP + PG + pD4 4,427 2,999 2,898 3,780 3,740 3,147 2,452 3,996 0,236 3,362 3,104** 0,368 Таблица 3 Активность пептидов согласно изобретению pD5 Pro-D-Val-Thr-Lys-Pro-Gln-Ala-NH2, pD6 Pro-D-Val-Thr-Lys-Pro-Gln-D-Ala-NH2 pD7 D-Pro-Val-Thr-(aMeTYm)Lys-Pro-Gln-D-Ala-NH; Кошка №1 Кошка №2 Кошка №3 Кошка №4 Кошка №5 Кошка №6 Кошка №7 Кошка №8 Кошка №9 Кошка №10 Среднее Отклонение VIP + PG 6 727 4 773 4 324 2 458 3 744 3 276 2 708 3 991 0 384 5 184 3 757 0 544 VIP + PG + pD5 4 263 2 435 1 317 3 191 2 727 3 486 2 634 2 852 1 132 3 804 2 784 0 315 VIP + PG + pD6 2 480 2 544 2 589 3110 4 142 1 710 2 370 4 165 1 693 2 931 2 773 0 270 VIP + PG + pD7 2 163 2 995 1 441 2 834 1 236 2 047 2 544 3 971 1 520 3 402 2 415 0 284 11 55369 12 Таблица 4 Активность пептидов согласно изобретению pDB His-Glu-Arg-Pro-Val-Thr-Lys-Pro-Gln-D-Ala-NH2 pDg Ile-Leu-Gln-His-Glu-Arg-Pro-Val-Thr-Lys-Pro-Gln-D-Ala-NH2 pD, Glu-Pro-Gly-Lys-Ser-Ser-lle-Leu-Gln-His-Glu-Arg-Pro-Val-Thr-Lys-Pro-Gln-D-Ala-NH; Кошка №1 Кошка №2 Кошка №3 Кошка №4 Кошка №5 Кошка №6 Кошка №7 Кошка №8 Кошка №9 Среднее Отклонение VIP + PG 3 832 1 826 2 132 3 891 2 042 3 250 4 014 4 280 3 273 3 171 0 313 VIP + PG + pDB 3117 2 730 1 690 1 725 2 076 1 358 2 452 2 689 2 920 2 306* 0 206 VIP + PG + pDg 2 409 1 440 1 964 2 259 1 230 1 580 2 488 2 426 3 790 2 176* 0 254 VIP+ PG + pD 10 2 691 1 764 2 520 2 410 2 833 2 877 1 726 2 015 1 953 2 310* 0 151 Таблица 5 Сравнение пептида по изобретению pDB His-Glu-Arg-Pro-Val-Thr-Lys-Pro-Gln-D-Ala-NH; с его аналогом рв His-Glu-Arg-Pro-Val-Thr-Lys-Pro-Gm-Ala-NH2 Кошка №1 Кошка №2 Кошка №3 Кошка №4 Кошка №1 Кошка №2 Кошка №3 Кошка №4 Кошка №5 Среднее Отклонение VIP + PG 4 385 4 460 3 079 3 333 3 410 2 510 2 764 2 191 4 908 3 449 0 314 VIP + PG + рв 3 693 4 915 3 350 2 442 3 896 2 432 1 626 1 925 5 012 3 255 0 412 VIP + PG + pDB 2 717 4 630 2 198 1 746 2 270 2 245 2 452 2 247 2 739 2 583* 0 274 Таблица 6 Активность пептидов согласно изобретению PDn Thr-Lys-Pro-Gln-D-Ala-NH2 pD, 2 Тгіг-(ацетил)І_у5-Рго-СІп-0-АІа-МН2 Кошка №1 Кошка №2 Кошка №3 Кошка №4 Кошка №5 Кошка №6 Кошка №7 Кошка №8 Кошка №9 Среднее Отклонение VIP + PG 3 217 3 772 3 580 2 166 6 562 2 290 2 008 2 034 2 548 3 131 0 484 VIP+ PG + pD,, 3 452 3114 3 348 2 181 2 219 1 638 3 291 2 076 0 850 2 463 0 299 Підписано до друку 05 05 2003 р Тираж 39 прим ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)236-47-24 VIP+ PG + pD 12 2 620 1 925 4 037 1 896 3 585 2 192 0 625 1 339 1 385 2 178* 0 364
ДивитисяДодаткова інформація
Назва патенту англійськоюA peptide and a pharmaceutical composition able to inhibit the pepsin release
Назва патенту російськоюПептид и фармацевтическая композиция, которые способны ингибировать секрецию пепсина
МПК / Мітки
МПК: A61K 38/00, C07K 14/47, A61P 1/04
Мітки: пептид, інгібувати, здатні, фармацевтична, секрецію, композиція, пепсину
Код посилання
<a href="https://ua.patents.su/6-55369-peptid-i-farmacevtichna-kompoziciya-shho-zdatni-ingibuvati-sekreciyu-pepsinu.html" target="_blank" rel="follow" title="База патентів України">Пептид і фармацевтична композиція, що здатні інгібувати секрецію пепсину</a>
Попередній патент: Боросилікатне скло з високою хімічною стійкістю та низькою в’язкістю, яке містить оксид цирконію та оксид літію
Наступний патент: Виріб, що включає дозувальний контейнер
Випадковий патент: Пристрій для електромагнітної обробки рідини