N-[6-метоксі-5-(перфторалкін)-1-нафтоіл]-n-метілгліцин чи його тіонафтоільні аналоги як інгібітори албдозоредуктази
Формула / Реферат
Формула изобретения
N-[6-Метокси-5-(перфторалкил)-1-нафтоил]-N-метилглицин или его тионафтоильные аналоги формулы
где n=1 или 2, X=-S,
или n=2, X=-0,
в качестве ингибитора альдозоредуктазы.
Текст
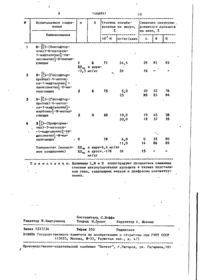
Изобретение касается замещенных аминокислот, в частности N- ) [б-ме Ї Изобретение относится к новым соединениям - перфторалкильным производным N-метилглицина общей формулы СН2-СООН СН,0 де п=1 или 2; X — S , їй п=2, Ч =-0; обладающим свойством ингибировать альдозоредуктазу, которые^ благодаря этому могут найти применение ттрн лечении сахарного диабета и связанных с ним заболеваний. Целью изобретения является изыскание в ряду производных N-нафтоилглицииа новых соединений, обладающих более высокой ингйбирующей альдозоредуктазу активностью. Пример 1. N- [[6-Иетокси-5-(пентафторэтил)-1-нафталенил^|-тиоксометшЛ-М-метилглицин (1). і Метиловый эфир N-([6~M6TOKCH-5-(пентафторэтил)-1-нафталенил]]-карбонил1-К-метилглицин (5,3 г или 4 00 1468897 13,ТГммоль) подвергают кипячению с обратным холодильником и перемешивают в 100 мл сухого пиридина совместно с 6 г пентасульфида фосфора в те- 5 чение 4 ч . После перемешивания в течение ночи при комнатной температуре смесь гидролизуют добавлением теплой воды, подвергают экстракционной обработке этилацетатом, а экстракт fQ промывают 3 н. водным раствором соляной кислоты, водой, бикарбонатом натрия и рассолом. После сушки и выпаривания неочищенный остаток растворяют в 25%-ном растворе этилацетате is а гексане и раствор профильтровывают через силикагель. Выпариванием фильтрата и сушкой получают 2,3 г метилового эфира Ы-|[(6-метокси~5-(пентафторэтил)-1-нафталенил]-тиоксометил1- 20 -N-метилглицина. 'Найдено,*: С 49,42; Н 3,58; N 3,40. П р и м е р 2. N- ][5-(гептафторпропил)-6-метокси-1-нафталенил]| карбонил]-М-метилглицин ( I I I ) . 5 г (0,0146 моль) б-метил-5-иодо-1-нафталинкарбоновой кислоты, метилового эфира, 8,9 г (4,35 мл, 0,03 моль) 1-иодгептафторпропана, 2,8 г (0,044 ат) активированной порошкообразной меди и 35 мл перегнанного диметилформамида выдерживают с перемешиванием в течение 4 ч при 150 С в автоклаве. Реакционную смесь охлаждают до комнатной температуры, осадок удаляют фильтрованием и промывают на фильтэе диэтиловым эфиром. Фильтрат промывают водой и высушивают над безводным сульфатом магния. Растворитель выпаривают и остаток оставляют в холодильнике, в резуль2,3 г (5,46 ммоль) метилового эфитате чего кристаллизуется 5,6 г ве,ра К-£(6-метокси-5-(пентафторэтил)щества. Небольшое количество мети-1-нафталенилтиоксометил]-N-метилгли- 25 лового эфира 5-(гептафторпропил)-6цина, 50 мл 2-метоксиэтанола и -метокси-1-нафталинкарбоновой кисло5,46 мл 2 н. водного раствора гидраты кристаллизуется из этанола, полута окиси натрия смешивают при 0 С чают продукт с т.пл. 74-75 Ct. и смесь подвергают перемешиванию при комнатной температуре в течение 3 ч дл 5,6 г (0,0146 моль) метилового (до исчезновения эфирного пятна при эфира 5-(гептафторпропил)-6~ме;гокси.тонкослойном хроматографическом ана-1-нафталинкарбоновой кислоты, 40 мл лизе с использованием смеси этилацеметанола и 7,3 мл 4 н. водного расттата с гексаном в соотношении 1:1). вора гидрата окиси натрия перемешиСмесь охлаждают до 0°С, нейтрализуют вают при комнатной температуре в тедо рН 8 добавлением 1 'н. водного чение 30 мин, после чего кипятят с раствора соляной кислоты, выпаривают, обратным холодильником в течение 4 ч . остаток растирают в воде, нейтральПосле выдержки в спокойном состояный материал экстрагируют этилацетании в течение ночи смесь охлаждают том и водный слой подкисляют добав- .Q до 0 С и нейтрализуют водным 1 н. ралением 1 н. водного раствора соляствором соляной кислоты. Метанол ной кислоты рН 3. Продукт экстрагивыпаривают, остаток растирают в воде руют этилацетатом, экстракт промываи смесь подкисляют до рН 3 добавлеют водой, высушивают над безводным нием 1 н. водного раствора соляной сульфатом магния. Остаток очищают .? кислоты. Пастообразный осадок подвергают экстракционной обработке этилкристаллизацией из смеси хлороформа ацетатом, органический слой промывают с гексаном, в результате чего полуводой, высушивают над безводным сульчают 700 мг в виде первой порции и фатом магния и выпаривают, 5,15 г дополнительно 568 мг сырого материасырого продукта 5-(гептафторпропил)ла из маточного раствора. Перекрис50 -б-метокси-1-нафталинкарбоновой кисталлизация первой порции позволила лоты используют на следующей стадии получить 400 мг чистого N- |£б~меток~ без дополнительной очистки. Одну си-5-(пентафторэтил)-1-нафталеншт]часть этого продукта перекристалли-тиоксометилі-і^-метилглицина. В резовывают из смеси хлороформа с гекзультате перекристаллизации маточно55 саном для спектральной идентификации. го раствора получают дополнительно 5,15 г (0,0139 моль) сырой кисло291 мг продукта с т.пл. 16Д-165°С» ты, 2,82 г (0,021 моль) 1-оксибенэоВычислено,%: С 50,13- Н 3,46; триазола, 40 мл сухого перегнанного N 3.44. 5 1 468897 6 диметилфомамида и 3,44 г (0,0167 моль) Еще теппую смесь выливают в теплую ( дкциклогексилкарбодиимида перемешиводу, подвергают экстракционной обвают в течение 1 ч при комнатной работке этилацетатом, экстракт про- • температуре. В указанную смесь добав- 5 мывают 3 н. водным раствором соляляют раствор 3,88 г (0,0278 моль) гиной кислоты, насыщенным раствором дрохлорида серокэинметилового эфира бикарбоната натрия и рассолом. Удав 30 мл диметилформамида, а затем ляют растворитель, маслоподобный 3,55 мл N-этилморфолина. Реакционную остаток растворяют в смеси гексана смесь перемешивают в течение ночи, 10 с этилацетатом в соотношении 3:1 и осадок (дициклогексилмочевкну) удараствор профильтровывают через силяю*т фильтрованием, фильтрат выпариликагель. После выпаривания раствовают досуха и остаток растворяют в рителя маслоподобиый продукт, метиэтилацетате. Раствор промывают биловый эфир' N- [[5~(гептафторпропил)-' карбонатом натрия и водой, высушива- 15 -6-метоксн-1-нафгаленил]-тиоксомеют над безводным сульфатом магния тнл]-1$-метилглицина, переводят в и выпаривают. Остаток очищают хроматвердое состояние (1,07 г) , полутографической обработкой смесью чив вещество с т.пл. 107—109°С. этилацетата с гексаном в соотношении В раствор 1,07 г (2,27 ммоль) метн1:1. В результате получают 3,3 г (масса очень чистой фракции составля- 20 левого эфира N- |[5-(гептафторпропнл)-6-метокси-1-нафталенил]-~тиокс-ометшіі ет 1,5 г) Я-{(гептафторпропил)-6-мэ-N-метилглицина в 15 мл 2-метокситоксн-1 -нафталеншГ|-карбонщЛ -N-меэтанола лри О С в токе азота добавтилглицин метилового эфира. ляют 2,27 мл 2 н. водного раствора В раствор 1,52 г (3,34 моль) мети- 25 гидрата окиси натрия. Смесь перемелового эфира N- {{5~гептафторпропил)~ шивают при комнатной температуре а -6-метокси-1-нафталенші]-карбонил)течение ночи, охлаждают до 0 С, ней-N-метилглицина в 20 мл 2-метокситрализуют до рН 7-8 водным 1 н. растэтанола при 0°С в токе азота добаввором соляной кислоты и выпаривают ляют 3,34 мл 2 н. водного раствора З" досуха. Остаток растирают в иоде, гидрата окиси натрия. подкисляют до рН 3, продукт экстраПеремешивание продолжают при комгируют этилацетатом, экстракт вторичнатной температуре в течение 2 ч. но промывают водой, высушивают над Смесь охлаждают до О С, нейтрализуют безводньэ-i сульфатом магния и выпаридобавлением 1 н. водного раствора 35 вают расгворигель. Маслоподобный соляной кислоты до рН 7, выпаривают остаток кристаллизуют из смеси хлорорастворитель, остаток растворяют в форма с гексаном, в результате чего воде и раствор подкисляют до рН 3. получают 484 мг > N- |[5-(гептафторПродукт выделяют фильтрованием, про( пр^опил)-6-метокси-ї-нзфталенил_|-тиокмывают водой и кристаллизуют из сме- 4 0 сометил}-М-метилглицина с т.пл. си хлороформа с гексаном, получив 162-163°С. 1,14 г N- [£5-(гептафторпропил)-6-меВычислено,%: С 47,27; Н 3,09; токси-1-нафталенилу-карбонил]-N-меN 3,06. тилглицина с т.пл. 195-197°С. Найдено,%: С 47,03; Н 3,08; Вычислено, %: С 49,02; Н 3,20; 45 N 3,03. N 3,18. Предлагаемые соединения обладают Найдено, %: С 48,29; Н 3,20; свойством ингнбировать альдозоредукN3,11. таэу, в связи с чем могут быть исГ г Пример 3. N-[{_5-(гептафторпользованы для предотвращения или пропил)-6-метокси-1-нафталенкгГ] -тиок- 50 ослабления осложнений, связанных с сометил|-її-метилглицин ( I I ) . диабетом'. 1,78 г (0,0039 моль) N[[5-(renTaСпособность предлагаемых соединефторпропил)-6-метокси-1-нафталенил iний ингибировать действие альдоэо-карбоншп-Л-метилглицин метилового 55 редуктазы и их использование для эфира, полученного согласно вышеизпредотвращения, ослабления или смягложенному, 30 мл сухого пиридина чения диабетических осложнений или 2 г (0,009 моль) пентасульфида люстрируется экспериментами с испольфосфора кипятят с обратным холодильзованием крыс, страдающих галактоником в токе азота в.течение 6 ч. •8 1468897 земией. Примеры таких экспериментов центное снижение степени аккумулироприведены ниже. вания дульцита в тканях хрусталиков В экспериментах использовали по глаз, седалищных нервов и диафрагмы четыре или более групп самцов крыс соответственно у подвергнутых лечевесом по 50-70 г расы Спрего-Доули, нию крыс в сравнении с животными, кокаждая из которых включала по 6 осо-> торые не подвергались такому лечению. бей. Животных первой группы, контКак видно из данных таблицы, соерольной группы, кормили смесью лабодинение 1 ( 1 ^ ^ = 3 , 5 мг/кг) превосхо-* раторного корма с глюкозой при 20%- JQ дит известное соединение (ВД =1 ной*по массе концентрации. Не под=6,4 мг/кг) в степени аккумулировавергаемых лечению животных, страдаю-' ния дульцита в нервах
ДивитисяДодаткова інформація
МПК / Мітки
МПК: A61K 31/195, A61P 27/02, A61P 15/00, A61P 3/08, C07C 327/00, A61P 3/10, C07C 235/66, C07C 233/83, A61P 27/12, A61P 13/02, C07C 325/00, C07C 67/00, A61P 25/18
Мітки: албдозоредуктази, аналоги, n-[6-метоксі-5-(перфторалкін)-1-нафтоіл]-n-метілгліцин, тіонафтоільні, інгібітори
Код посилання
<a href="https://ua.patents.su/6-7051-n-6-metoksi-5-perftoralkin-1-naftoil-n-metilglicin-chi-jjogo-tionaftoilni-analogi-yak-ingibitori-albdozoreduktazi.html" target="_blank" rel="follow" title="База патентів України">N-[6-метоксі-5-(перфторалкін)-1-нафтоіл]-n-метілгліцин чи його тіонафтоільні аналоги як інгібітори албдозоредуктази</a>
Попередній патент: Спосіб визначення сполученої активності пари антибіотиків
Наступний патент: Пристрій для голкотерапії
Випадковий патент: Подвійний кулірний пресовий трикотаж із пресових петель