(2-гідроксіетил)триметиламонію тіоктат (холіну тіоктат), що має гепатопротекторну, гіпоамоніємічну та детоксикуючу дію, спосіб його одержання, фармацевтична композиція на його основі
Формула / Реферат
1. (2-Гідроксіетил)триметиламонію тіоктат (холіну тіоктат) формули
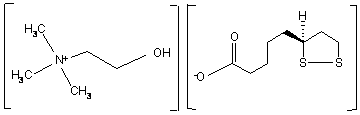 ,
,
що має гепатопротекторну, гіпоамоніємічну та детоксикуючу дію.
2. Спосіб одержання (2-гідроксіетил)триметиламонію тіоктату (холіну тіоктату), що включає розчинення у полярних розчинниках основи і органічної кислоти з подальшим виділенням цільового продукту, який відрізняється тим, що як основу використовують холіну основу, як органічну кислоту - тіоктову кислоту, як полярні розчинники використовують воду та/або спирт етиловий, а виділення цільового продукту здійснюють шляхом вилучення розчинника будь-яким відомим способом.
3. Фармацевтична композиція, що містить активну речовину і один або більше фармацевтично прийнятних носіїв або розчинників, яка відрізняється тим, що як активну речовину вона містить (2-гідроксіетил)триметиламонію тіоктат (холіну тіоктат) формули
 ,
,
що має гепатопротекторну, гіпоамоніємічну та детоксикуючу дію.
Текст
1. (2-Гідроксіетил)триметиламонію тіоктат (холіну тіоктат) формули C2 2 (13) 1 є сіллю холіну-основи і тіоктової кислоти, розчинної у воді та деяких полярних органічних розчинниках і має гепатопротекторну, гіпоамоніємічну та детоксикуючу дію. 3 86441 4 Проведені дослідження доводять перспективСтосовно гепатології до теперішнього часу ність створення комплексної фізіологічно активної значною залишається роль препаратів для лікуречовини на основі холіну і тіоктової кислоти, повання захворювань печінки і жовчовивідних шлядальше використання якої, зокрема, як гепатопрохів, і тих, що захищають печінку від ушкоджуючого тектора, істотно поліпшує якість життя хворих. впливу екзогенних або ендогенних факторів та/або Відомі гепатопротекторні лікарські засоби Леприскорюючих її природню регенерацію (гепатопгалон, Карсил, Силібор у формі таблеток, капсул, ротекторів). Група гепатопротекторів містить речодраже та ін., що містять як активні речовини флавини як рослинного, так і синтетичного походженвоноїди, одержані з плодів розторопші плямистої. ня, що мають різноспрямовану дію на метаболічні Застосовують ці засоби при гострих гепатитах, процеси. цирозах печінки, для підтримуючої терапії хронічАсортимент вітчизняних лікарських засобів гених захворювань печінки. При застосуванні цих патопротекторної, гіпоамоніємічної та детоксикуюпрепаратів можливі побічні прояви у вигляді прочої дії є недостатнім, тому пошук нових фізіологічносної дії, алергічних реакцій тканин шкіри (1). но активних речовин, що мають таку специфічну Відомий гепатопротекторний лікарський засіб активність, та створення на їх основі нових висо"Есенціале", що містить "есенціальні" фосфоліпіди коефективних засобів є актуальною проблемою. - дигліцеринові ефіри холінфосфорної кислоти і Структурним і фармакологічним аналогом хоненасичені жирні кислоти (лінолеву, ліноленовую ліну тіоктату є холіну хлорид - похідне холіну (гідта ін.) разом з вітамінами (піридоксином, ціанокороокису 2-оксиетилтриметиламонію), який є ліпотболаміном, нікотинамідом, пантотеновою кислоропною речовиною, що запобігає важким тою). Застосовують "Есенціале" у формі ампул захворюванням печінки, які виникають при її жироємністю 5 і 10мл, що містять відповідно 250 і вому переродженні. Холіну хлорид застосовують у 1000мг "есенціальних" фосфоліпідів, 2,5 і 5мг пімедицині для лікування захворювань печінки у ридоксину гідрохлориду, 10 і 15мкг ціанокоболаміскладі гепатопротекторних препаратів. Його ввону, 25 і 100мг нікотинаміду, 1,5 і 3мг пантотенату дять також до складу комбікормів сільськогоспонатрію, а також у формі капсул, що містять 175мг дарських тварин. До його недоліків слід віднести "есенціальних" фосфоліпідів, 3мг тіаміну, 3мг рінедостатньо високий рівень та обмежений спектр бофлавіну, 3мг піридоксину гідрохлориду, 3мг ціаспецифічної активності. На теперішній час у лікуванні метаболічних занокоболаміну, 15мг нікотинаміду і 3,3мг aхворювань печінки пильну увагу привертають претокоферолу ацетату. Застосовують засіб при хропарати тіоктової (a-ліпоєвої) кислоти (наприклад, нічних гепатитах, дистрофії і цирозі печінки, а таТіоктацид). Відомо, що тіоктовій кислоті (ТК) налекож при пораженнях печінки, пов'язаних з діабежить істотна роль у регуляції метаболічних процетом, алкоголізмом та ін. Можливі побічні ефекти у сів у печінці. Як кофермент вона приймає участь у вигляді диспептичних розладів (2). вуглеводному і білковому обміні, є однією з важВідомий гепатопротекторний лікарський засіб, ливих складових антиоксидантної системи органіщо містить як активну речовину 2-феніл-3зму. Тіоктова кислота відіграє важливу роль у реакарбетокси-4-диметиламінометил-5оксибензофурану гідрохлорид (вінборон, фенікакціях окислювального декарбоксилірування aберан), і допомагає збереженню балкової структукетокислот, включаючи перетворення піровиногри печінки (3). радної кислоти у ацетил-КоА - вихідну речовину у Відомий гепатопротекторний лікарський засіб циклі Кребса. У складному процесі окислення тіо"Гепабене" у формі капсул, який є комбінованим ктової кислоти в результаті утворюються 3 молепрепаратом і містить екстракти лікарських рослин, кули АТФ, що суттєво збільшує енергетичний поу тому числі екстракт плодів розторопші плямистої тенціал клітини. Тіоктова кислота активує процеси з не менш, ніж 22мг силібініну у капсулі (4). окислення жирних кислот у мітохондріях, що, окрім Відомий гепатопротекторний лікарський засіб енергозабезпечення клітини, зменшує вміст у ній "Гепабене" у формі розчину для інфузій, що міссубстратів для синтезу тригліцеридів і тим самим тить 5%-ний розчин суми найбільш прийнятних запобігає розвитку жирової дистрофії печінки і гідля організму амінокислот, у тому числі аргінін (5). перліпідемії. Відомий лікарський засіб Зиксорин, який заОсновними обґрунтуваннями для широкого стосовують у формі капсул при функціональній застосування тіоктової кислоти при захворюваннях гіпербілірубінемії у хворих хронічними дифузними печінки є : захворюваннями печінки, при жовтяницях, обумо- здатність знижувати ПОЛ (зв'язувати вільні влених ензимопатіями і доброякісним внутрішньорадикали і вільне тканинне залізо); печінковим холестазом (6). - участь у окисленні жирних кислот і ацетату Відомий лікарський засіб Гепатофальк, що мі(запобігає розвитку жирового стеатозу печінки); стить як активну субстанцію холіну оротат. Засто- участь у декарбоксилюванні a-кетокислот совують при токсичних ураженнях печінки (у тому (енергозабезпечення клітини і профілактика розчислі алкогольних і лікарських), при гострих і хровитку кетоацидозу); нічних гепатитах різної етіології і цирозі печінки як - підвищення трансмембранного транспорту підтримуючу терапію (7). глюкози у клітину (накопичення глікогену і збільВідомий лікарський засіб Ліповітан, що містить шення енергетичного балансу гепатоцитів); як активну субстанцію холіну тартрат. Застосову- пригнічення синтезу оксиду азоту гепатоциють при токсичних ураженнях печінки (8). тами (профілактика і купірування реологічних розВідомий лікарський засіб Глутаргін (L-аргініну ладів та судинних порушень). L-глутамат), що має гепатопротекторну, гіпоамоні 5 86441 6 ємічну та детоксикуючу дію, який застосовують у формі таблеток, капсул, порошків, розчинів для ін'єкцій і концентратів для інфузійних розчинів (9). Відомий спосіб одержання похідних амідів аргініну шляхом активації N-ациларгініну або його солі і ацилювання ним амінів формули NH2R у семає гепатопротекторну, гіпоамоніємічну та дередовищі органічного розчинника в присутності токсикуючу дію. основи і з подальшим виділенням цільового проПоставлене завдання вирішується тим, дукту, де як активуючий агент використовують дищо у способі одержання (2- гідроксиеметилформамідинійхлорид (10). тил)триметиламонію тіоктату (холіну тіоктату), що Відомий спосіб одержання глутамату 6включає розчинення у полярних розчинниках осамінокапронової кислоти -речовини, що має антинови і органічної кислоти з подальшим виділенням фібринолітичну, протизапальну і антимікробну цільового продукту, згідно з винаходом, як основу активність. Спосіб здійснюють шляхом розчинення використовують холіну основу, як органічну кислоу воді глутамінової кислоти і 6-амінокапронової ту - тіоктову кислоту, як полярні розчинники викокислоти. До одержаного розчину додають при перистовують воду та/або спирт етиловий, а видіремішуванні активоване вугілля. Одержаний розлення цільового продукту здійснюють шляхом чин солі глутамат 6-амінокапронової кислоти фільвилучення розчинника будь-яким відомим спосотрують, фільтрат охолоджують з метою бом. подальшого виділення осаду. Одержаний кристаПоставлене завдання вирішується тим, що лічний осад - сіль глутамату 6-амінокапронової фармацевтична композиція, що містить активну кислоти фільтрують, промивають і висушують. речовину і один або більше фармацевтично приВихід цільового продукту складає 86% (11). йнятні носії або розчинники, згідно з винаходом, як Найбільш близьким до заявляємого є спосіб активну речовину містить (2одержання водорозчинної солі L-аргініну Lгідроксиетил)триметиламонію тіоктат (холіну тіоглутамату, що включає розчинення у воді Lктат) формули аргініну-основи, додавання при перемішуванні до розчину L-аргініну-основи кислоти L-глутамінової до рН 6,6-6,8, фільтрацію одержаного водного розчину L-аргініну L-глутамату, введення водного розчину L-аргініну L-глутамату в етиловий спирт до випадання осаду (при співвідношенні вода фіщо має гепатопротекторну, гіпоамоніємічну та льтрату: спирт етиловий 1:(9,76-10,24), фільтрацію детоксикуючу дію. і промивання одержаного осаду L-аргініну LТехнічний результат, який отримують при глутамату, сушку L-аргініну L-глутамату під вакууздісненні винаходу, полягає у одержанні нової фімом при температурі не вище 60°С протягом 4зіологічно активної хімічної речовини (25год (12). гідроксиетил)триметиламонію тіоктату (холіну тіоДо недоліків способу-прототипу слід віднести ктату), що має гепатопротекторну, гіпоамоніємічну складність і довготривалість технологічного прота детоксикуючу дію, у розробці способу її одерцесу, необхідність дотримування жорстких темпежання, що забезпечує більш високий рівень і ратурних і часових режимів. більш широкий спектр специфічної активності, з В основу винаходу поставлено завдання ствоодночасним спрощенням і скороченням тривалості рення нової фізіологічно активної речовини холіну проведення технологічного процесу, а також у тіоктату, яка, проявляючи гепатопротекторну, гіпостворенні фармацевтичних композицій на основі амоніємічну та детоксикуючу активність, має більш нової фізіологічно активної речовини (2високий рівень і більш широкий спектр специфічгідроксиетил)триметиламонію тіоктату (холіну тіоної активності. ктату) у різних лікарських формах, використання В основу винаходу поставлено завдання розяких призводить до розширення асортименту геробки такого способу одержання нової хімічної патопротекторних засобів. речовини, що має гепатопротекторну, гіпоамонієНаводимо конкретні приклади здійснення вимічну та детоксикуючу активність, яка, завдячуючи находу. послідовності операцій по здійсненню процесу, Приклад 1. До суміші 0,8497г (0,004125 моль) підбору його режимів і параметрів, дає можливість тіоктової кислоти (з розрахунку на 100% речовину) одержати речовину з більш високим рівнем і більш в етиловому спирті додають 0,5г (0,004125 моль) широким спектром специфічної активності, з однохоліну основи (з розрахунку на 100% речовину) і часним спрощенням і скороченням тривалості перемішують до отримання прозорого розчину. проведення технологічного процесу. Для отримання цільового продукту - холіну тіоктаВ основу винаходу поставлено завдання по ту, із розчину відганяють спирт, одержаний осад створенню фармацевтичних композицій на основі сушать під вакуумом. нової біологічно активної речовини холіну тіоктату Приклад 2. До суспензії 0,8497г (0,004125 у різних лікарських формах. моль) тіоктової кислоти (з розрахунку на 100% Поставлене завдання вирішується тим, що, речовину) у воді додають 0,5г (0,004125 моль) згідно з винаходом, (2гідроксиехоліну основи (з розрахунку на 100% речовину) і тил)триметиламонію тіоктат (холіну тіоктат), форперемішують до отримання прозорого розчину. мули Для отримання цільового продукту - холіну тіоктату, розчин піддають ліофілізації. 7 86441 8 Приклад 3. Синтез здійснюють згідно з приПриклад 6. Синтез здійснюють згідно з прикладом 2. Для отримання цільового продукту кладом 2 при мольному співвідношенні тіоктова холіну тіоктату, розчин піддають розпилювальному кислота : холіну основа - 1:1-1,2. До одержаного сушінню. водного розчину цільового продукту додають фаПриклад 4. До суміші 0,5722г (0,004125 моль) рмацевтично прийнятні допоміжні речовини для холіну гідрохлориду (з розрахунку на 100% речоотримання ін'єкційного розчину відомим способом. вину) в етиловому спирті додають 0,165г (0,004125 Приклад 7. До фармацевтично прийнятних домоль) натрію гідроокису (з розрахунку на 100% поміжних речовин додають при перемішуванні речовину). Осад натрію хлориду, що випав, відфіконцентрований водний розчин холіну тіоктату, льтровують, до фільтрату додають 0,8497г який одержують згідно з прикладом 2, після чого (0,004125 моль) тіоктової кислоти (з розрахунку на гранулюють, висушують і таблетують або капсу100% речовину) і перемішують до отримання пролюють відомим способом. зорого розчину. Для отримання цільового продукту У випадку, якщо виробник має труднощі у при- холіну тіоктату, із розчину відганяють спирт, одедбанні субстанції - холіну основи, можливе отриржаний осад сушать під вакуумом. мання його згідно з прикладами 4-5. Приклад 5. До суміші 0,8497г (0,004125 моль) У відповідності з заявляємим способом одертіоктової кислоти (з розрахунку на 100% речовину) жують нову фізіологічно активну хімічну речовину в етиловому спирті додають 0,165г (0,004125 (2- гідроксиетил)триметиламонію тіоктат (холіну моль) натрію гідроокису (з розрахунку на 100% тіоктат), що має гепатопротекторну, гіпоамоніємічречовину) і перемішують. В отриманий розчин нану та детоксикуючу дію. Це аморфній продукт жовтрію тіоктату додають 0,5722г (0,004125 моль) хотуватого кольору (вихід біля 100%) з високим стуліну гідрохлориду (з розрахунку на 100% речовипенем чистоти (вміст основної речовини складає ну). Осад натрію хлориду, що випав, не менше 98,5%), розчинний у воді та полярних відфільтровують. Для отримання цільового продуорганічних розчинниках: С13Н27NO3S2 (М.м кту - холіну тіоктату, із розчину відганяють спирт, =309,53) одержаний осад сушать під вакуумом. Результати елементного аналізу Значення, % Розраховане Експериментальне С 50,4450,83 Взаємозв'язок та послідовність технологічних операцій заявляємого способу, підбір режимів і параметрів цілком забезпечують виконання поставленого завдання. Так, реакція солеутворення при одержанні холіну тіоктату найбільш ефективно проводиться у середовищі полярних розчинників Η 8,81 8,72 Ν 4,52 4,61 О 15,51 15,31 S 20,72 20,53 за рахунок їх специфічних властивостей (коли одночасно виконується функція розчинника і реакційного середовища), так і реактивних агентів: холіну основи і тіоктової кислоти. Вибрані співвідношення розчинників і холіну основи не обмежуються. Таблиця 1 Порівняльний аналіз заявляємого способу і способу-прототипу Заявляємий спосіб Спосіб одержання холіну тіоктату: 1. Змішування у розчиннику (у воді або/та спиртах) холіну основи і тіоктової кислоти до отримання розчину. 2. Виділення цільового продукту шляхом вилучення розчинника будь-яким відомим способом (відгін під вакуумом, ліофілізація, розпилювальне висушування та ін.). Спроби одержати холіну тіоктат у відповідності зі способом - прототипом не призвели до отримання цільового продукту, у зв'язку з тим, що вихідна субстанція розчиняється не тільки у воді, але й у етиловому спирті, який застосовують як висо Спосіб-прототип Спосіб одержання водорозчинної солі L-аргінину і Lглютамінової кислоти (L - аргінину L-глутамату): 1. Розчинення у воді L- аргінину основи. 2. Додавання при перемішуванні до розчину Lаргініну основи кислоти L-глутамінової до рН 6,6-6,8. 3. Фільтрація отриманого водного розчину L - аргініну L-глутамату. 4. Введення водного розчину L - аргініну L-глутамату в етиловий спирт до випадіння осаду (при співвідношенні вода фільтрату : спирт етиловий 1:(9,7610,24). 5. Фільтрація і промивання одержаного осаду L - аргініну L-глутамату. 6. Висушування L - аргініну L-глутамату під вакуумом при температурі не вище 60°С протягом 4-5год. лювальний агент при отриманні L-аргініну Lглутамату. Легкість проведення реакції солеутворення з вихідними реагентами достатнього ступеня чистоти, які використовують у еквівалентній кількості, гарантують високий рівень чистоти і ста 9 86441 10 більності не тільки цільового продукту, а й фармаслідження гепатозахисної активності таких цевтичних композицій при застосуванні цих розчикомплексів (склади №1-5), які містять у 1мл: нів (виключається операція виділення цільового Склад №1: 10,0мг холіну основи + 17,0мг aпродукту в сухому вигляді, внаслідок чого значно ліпоєвої (тіоктової) кислоти з хлоридом натрію спрощується технологічний цикл). Згідно з запро0,4%; понованим способом температурний режим солеСклад №2: 14,4мг аргініну основи + 17,0мг aутворення не впливає на чистоту продукту і обмеліпоєвої (тіоктової) кислоти; жується лише точкою замерзання і кипіння Склад №3: 10,0мг холіну основи + 17,0мг aрозчинників, які використовують як реакційне селіпоєвої (тіоктової) кислоти; редовище. Тільки задані параметри концентрації Склад №4: 9,98мг холіну основи +10,16мг ницільового продукту визначають кількість розчинникотинової кислоти; ка для солеутворення. Склад №5: 9,98мг холіну основи + 12,1мг глуФармацевтичні композиції на основі холіну тіотамінової кислоти; ктату одержують у формі таблеток, капсул, порошПрепарат Берлітіон («Berlin Chemie») 133мг ків, розчинів для ін'єкцій і концентратів для інфуліпоєвої (тіоктової) кислоти /12мл; зійних розчинів та інших лікарських формах. Препарат Глутаргін для ін'єкцій (ФК «ЗдороВибір активної субстанції здійснювали шляхом в'я») 200мг/5 мл (22мг аргініну + 18мг глутамінової фармакологічного скринінгу ряду одержаних комкислоти в 1мл). плексних сполук і проведення порівняльної фарЕкспериментальні дослідження проводились макологічної оцінки по відношенню до Глутаргіну на 48 білих безпородних щурах, самцях і самках (ін'єкційна форма). Були проведені попередні масою тіла 230-260г. Чотирьоххлористий вуглець скринінгові дслідження фармакологічної активності вводили тваринам у вигляді 50%-ної масляної нових комплексів на наявність у них гепатопротекемульсії однократно внутрішньошлунково у дозі торної дії. 0,8мл/100г маси тіла. Досліджувані зразки препаНа першому етапі досліджень була виявлена рату вводили тваринам внутрішньовенно, у хвоснайбільш активна сполука, на основі якої були тову вену, протягом трьох днів до введення токсипроведені подальші порівняльні дослідження. чного агента, а також протягом трьох днів після На моделі гепатиту у щурів, який було викливведення токсичного агента (тваринам, що вижикано внутрішньошлунковим введенням чотирьохли). Досліджувані зразки препарату вводили твахлористого вуглецю, проведено порівняльне доринам у таких дозах: Склад Склад №1 Склад №2 Склад №3 Склад №4 Склад №5 Берлітіон Глутаргін Доза, мг/кг 0,5 0,5 0,5 0,5 0,5 0,34 0,35 Доза діючих субстанцій, мг/кг холіну 5,1 + тіоктової кислоти 8,6 аргініну 7,2 + тіоктової кислоти 8,6 холіну 5,1 + тіоктової кислоти 8,6 холіну 5,1 + нікотинової кислоти 5,1 холіну 5,1 + глутамінової кислоти 7,2 тіоктової кислоти 8,6 аргініну 7,6 + глутамінової кислоти 6,4 У даній постановці досліду тварин розподілили на 8 груп по 6 голів у кожній: 1 - контроль патології; 2 - патологія + склад №1 у дозі 0,5мг/кг; 3 - патологія + склад №2 у дозі 0,5мг/кг; 4 - патологія + склад №3 у дозі 0,5мг/кг; 5 - патологія + склад №4 у дозі 0,5мг/кг; 6 - патологія + склад №5 у дозі 0,5мг/кг; 7 - патологія + Берлітіон у дозі 0,34мг/кг; 8 - патологія + Глутаргін у дозі 0,35мг/кг. При виборі доз виходили з того, що тварини мали отримувати субстанції у однакових дозах, наближених до рекомендованих у клініці дозам для людини. В результаті експериментальних досліджень встановлено, що на 3-5 добу після затравки у групі контролю патології відбувалася загибель 5-ти з 6ти щурів (таблиця 2), що співвідноситься з відомими з літератури даними і з власними дослідженнями, які свідчать про розвиток у щурів гострої печінкової патології і загибелі, як правило, 60-80% щурів. Таблиця 2 Досліджуваний зразок Контроль патології Склад №1 Склад №2 Склад №3 Склад№4 Склад №5 Берлітіон Глутаргін Кількість загиблих тварин 5/6 1/6 2/6 0/6 2/6 2/6 2/6 2/6 % виживання 16,7 83,3 66,7 100,0 66,7 66,7 66,7 66,7 11 86441 Введення щурам досліджуваних зразків виявило виразну гепатозахисну дію. Найбільший (100%-ний) ефект відмічався при введенні складу №3. Склад №1, що містить окрім холіну і ліпоєвої кислоти, 0,4% розчин натрію хлориду, виявив незначно меншу дію (83,3%). Решта досліджуваних складів і Глутаргін поступалися по рівню специфічної активності. При цьому доза Глутаргіну була майже у 3 рази вища, ніж доза найбільш активної досліджуваної сполуки. В результаті попередніх експериментів встановлено, що найбільш активний комплекс має 100%-ну гепатозахисну дію. Глутаргін у даній постановці досліду виявив 67%-ний ефект. Таким чином, можна зробити висновок про те, що фізіологічно активна хімічна сполука холіну тіоктат має виразний гепатозахисний ефект, що перевищує дію Глутаргіну, якій застосовували у більш високій дозі. Заявляємий комплекс є перспективним для створення на його основі монопрепаратів або комплексних лікарських засобів гепатозахисної дії. Література: 1. Машковский М.Д. Лекарственные средства. Харьков: Торсинг, 1997, Т.1.-С.514-516. Комп’ютерна верстка В. Мацело 12 2. Машковский М.Д. Лекарственные средства. Т.1. -Харьков: Торсинг, 1997.-С.514. 3. Патент Росссийской Федерации №2211034, класс МПК А61К31/3343, А61Р1/16. Опубл. Официальный бюллетень Роспатента "Изобретения, полезные модели" от 27.08.2003. 4. Справочник Видаль. Лекарственные препараты в России: Справочник. М.: АстраФармСервис, 2001, Б-132. 5. Справочник Видаль. Лекарственные препараты в России: Справочник. М.: АстраФармСервис, 2001, Б-472. 6. Машковский М.Д. Лекарственные средства. Харьков: Торсинг, 1997, Т.1.-С.516. 7. ROTE LISTE 2000, №48053. 8. ROTE LISTE 2000, №48056. 9. Патент України №54880, кл. C07C229/02, A61K31/195, A61P1/16, A61P39/00, опубл. офіц. бюл. "Промислова власність", 2003, №3. 10. Авторское свидетельство СССР №1266139. Кл. С07С103/187, опубл.03.07.84. 11. Авторское свидетельство СССР №1248212. Кл. С07С101/22, А61К31/195, опубл.27.07.83. 12. Патент України №54880, кл.С07С229/02, А61К31/195, А61Р1/16, А61Р39/00, опубл. офіц. бюл. "Промислова власність", 2003, №3. Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійською(2-hydroxyethyl)trimethylammonium thiooctate (choline thioctate), having hepatoprotective, hypoamoniemic and detoxic action, method for production thereof and pharmaceutical compositions based on it
Автори англійськоюNovik Ivan Ivanovych
Назва патенту російською(2-гидроксиэтил)триметиламмония тиоктат (холина тиоктат), имеющий гепатопротекторное, гипоаммониемическое и детоксицирующее действие, способ его получения, фармацевтическая композиция на его основе
Автори російськоюНовик Иван Иванович
МПК / Мітки
МПК: A61P 1/00, A61P 39/00, A61K 31/14, A61K 31/385
Мітки: спосіб, дію, 2-гідроксіетил)триметиламонію, тіоктат, холіну, детоксикуючу, гепатопротекторну, фармацевтична, композиція, гіпоамоніємічну, основі, має, одержання
Код посилання
<a href="https://ua.patents.su/6-86441-2-gidroksietiltrimetilamoniyu-tioktat-kholinu-tioktat-shho-maeh-gepatoprotektornu-gipoamoniehmichnu-ta-detoksikuyuchu-diyu-sposib-jjogo-oderzhannya-farmacevtichna-kompoziciya-na-jj.html" target="_blank" rel="follow" title="База патентів України">(2-гідроксіетил)триметиламонію тіоктат (холіну тіоктат), що має гепатопротекторну, гіпоамоніємічну та детоксикуючу дію, спосіб його одержання, фармацевтична композиція на його основі</a>
Попередній патент: Спосіб забезпечення насосом робочих характеристик морського ерліфта та система для його реалізації
Наступний патент: Пристрій для затягування пружинних запобіжних пристроїв
Випадковий патент: Спосіб одержання виробів із гомогенних алюмінідів титану










