Хінолізинонові похідні як інгібітори pi3k
Номер патенту: 115296
Опубліковано: 10.10.2017
Автори: Лагад Діпак Райчханд, Махангаре Сачхін Джайсінг, Джана Нірмал Кумар, Камбодж Раджендер Кумар, Відхате Прашант Попатрао, Кулкарні Санджеев Анант, Шукла Маноджкумар Рампрасад, Палле Венката П., Тараге Ананд Джаганнатх
Формула / Реферат
1. Сполука загальної формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль:
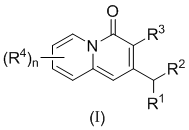 ,
,
де
R1 вибраний із
а)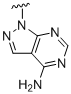 ,
, 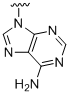 ,
, 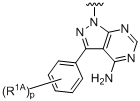 ,
, 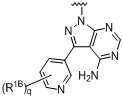 ,
,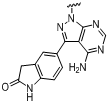 і
і 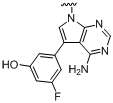 ,
,
де
R1A незалежно у кожному випадку вибраний із галогену, гідрокси, гідроксіалкілу та -NHSO2CH3;
R1B незалежно у кожному випадку вибраний із гідрокси, алкокси і -NHSO2CH3; або
b) -NH-R1a; де R1a вибраний із
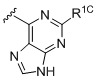 ,
, 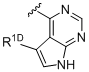 ,
, 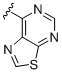 ,
, 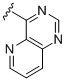 ,
, 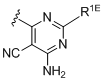 і
і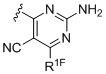 ,
,
де
R1C вибраний із водню, галогену і аміно; R1D вибраний із галогену та ціано; R1E вибраний із водню і аміно; R1F вибраний із водню, галогену і алкілу;
R2 вибраний із водню, заміщеного або незаміщеного алкілу, гідроксіалкілу, -OR5, -(CH2)mNR6R7 і -C(=O)-NR6R7;
R3 вибраний із заміщеного або незаміщеного арилу, заміщеного або незаміщеного циклоалкілу і заміщеного або незаміщеного циклоалкенілу;
R4 незалежно у кожному випадку вибраний із галогену, заміщеного або незаміщеного алкілу, заміщеного або незаміщеного арилу, заміщеного або незаміщеного гетероарилу, заміщеного або незаміщеного гетероциклу, заміщеного або незаміщеного карбоциклу і -OR5;
R5 являє собою заміщений або незаміщений алкіл;
кожен із R6 та R7 незалежно вибраний із водню та заміщеного або незаміщеного алкілу;
n являє собою ціле число, вибране з 0, 1 і 2;
m являє собою ціле число, вибране з 1, 2, 3 і 4;
p являє собою ціле число, вибране з 0, 1 і 2; та
q являє собою ціле число, вибране з 0, 1 і 2;
при цьому,
якщо алкільна група є заміщеною, то вона заміщена 1-3 замісниками, незалежно вибраними з оксо (=O), галогену, нітро, ціано, пергалогеналкілу, циклоалкілу, циклоалкенілу, арилу, гетероарилу, гетероциклілу, -OR8b, -SO2R8a, -C(=O)OR8a, -OC(=O)R8a, -C(=O)N(H)R8, -C(=O)N(алкіл)R8, -N(H)C(=O)R8a, -N(H)R8 і -N(алкіл)R8;
якщо циклоалкіл, циклоалкеніл і карбоцикл є заміщеними, то кожен із них заміщений 1-3 замісниками, незалежно вибраними з оксо (=O), галогену, нітро, ціано, алкілу, алкенілу, циклоалкілу, циклоалкенілу, пергалогеналкілу, арилу, гетероарилу, гетероциклілу, -OR8b, -SO2R8a, -C(=O)R8a, -C(=O)OR8a, -OC(=O)R8a, -C(=O)N(H)R8, -C(=O)N(алкіл)R8, -N(H)C(=O)R8a, -N(H)R8 і -N(алкіл)R8;
якщо арильна група є заміщеною, то вона заміщена 1-3 замісниками, незалежно вибраними з галогену, нітро, ціано, гідрокси, алкілу, алкенілу, пергалогеналкілу, циклоалкілу, циклоалкенілу, гетероциклілу, арилу, гетероарилу, -O-алкілу, -O-пергалогеналкілу, -N(алкіл)алкілу, -N(H)алкілу, -NH2, -SO2-алкілу, -SO2-пергалогеналкілу, -N(алкіл)C(=O)алкілу, -N(H)C(=O)алкілу, -C(=O)N(алкіл)алкілу, -C(=O)N(H)алкілу, -C(=O)N(H)циклоалкілу, -C(=O)NH2, -SO2N(алкіл)алкілу, -SO2N(H)алкілу, -SO2NH2, -C(=O)OH і -C(=O)O-алкілу;
якщо гетероарильна група є заміщеною, то вона заміщена 1-3 замісниками, незалежно вибраними з галогену, ціано, гідрокси, алкілу, алкенілу, пергалогеналкілу, циклоалкілу, циклоалкенілу, гетероциклілу, -O-алкілу, O-пергалогеналкілу, -N(алкіл)алкілу, -N(H)алкілу, -NH2, -SO2-алкілу, -SO2-пергалогеналкілу, -N(алкіл)C(=O)алкілу, -N(H)C(=O)алкілу, -C(=O)N(алкіл)алкілу, -C(=O)N(H)алкілу, -C(=O)NH2, -SO2N(алкіл)алкілу, -SO2N(H)алкілу, -SO2NH2, -C(=O)OH і -C(=O)O-алкілу;
якщо гетероцикліл і гетероцикл є заміщеними, то кожен із них заміщений або за атомом вуглецю в кільці, або за гетероатомом в кільці, та, якщо він є заміщеним за атомом вуглецю в кільці, то він заміщений 1-3 замісниками, незалежно вибраними з галогену, нітро, ціано, оксо (=O), алкілу, алкенілу, пергалогеналкілу, циклоалкілу, циклоалкенілу, арилу, гетероарилу, гетероциклілу, -SO2R8a, -OR8b, -C(=O)OR8a, -OC(=O)R8a, -C(=O)N(H)R8, -C(=O)N(алкіл)R8, -N(H)C(=O)R8a, -N(H)R8 і -N(алкіл)R8; та, якщо гетероциклічна група є заміщеною за атомом азоту в кільці, то вона заміщена замісниками, незалежно вибраними з алкілу, алкенілу, гідроксіалкілу, циклоалкілу, циклоалкенілу, арилу, гетероарилу, -SO2R8a, -C(=O)R8c, C(=O)OR8a, -C(=O)N(H)R8 і -C(=O)N(алкіл)R8;
R8 вибраний із групи, що включає водень, алкіл, алкеніл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл;
R8a вибраний із групи, що включає алкіл, алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл;
R8b вибраний із групи, що включає водень, алкіл, алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл; та
R8c вибраний із групи, що включає алкіл, гідроксіалкіл, алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл.
2. Сполука формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль за п. 1, причому R1 вибраний із
а)  ,
,  ,
,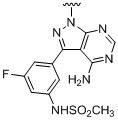 ,
, 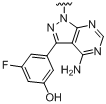 ,
, 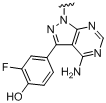 ,
, 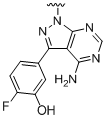 ,
, 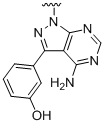 ,
, 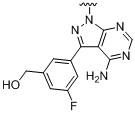 ,
, 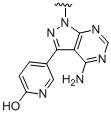 ,
, 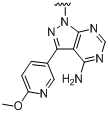 ,
, 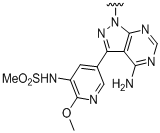 ,
, 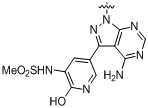 ,
, 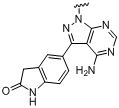 і
і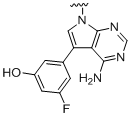 ; або
; або
b) -NH-R1a; де R1a вибраний із
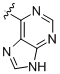 ,
, 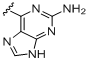 ,
, 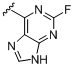 ,
, 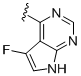 ,
, 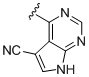 ,
, 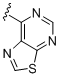 ,
, 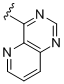 ,
, 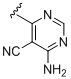 ,
, 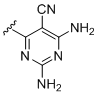 ,
, 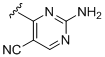 ,
, 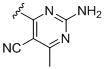 і
і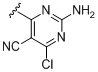 .
.
3. Сполука формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль за п. 1 або п. 2, де R2 вибраний із водню і алкілу.
4. Сполука формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль за будь-яким із пп. 1-3, де R3 являє собою заміщений або незаміщений арил.
5. Сполука формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль за будь-яким із пп. 1-4, де R3 вибраний із фенілу, 3-фторфенілу, 4-фторфенілу, 3,5-дифторфенілу, 3,4-дифторфенілу, 3-фтор-5-метилфенілу, 3-метилфенілу і 3-трифторметоксифенілу.
6. Сполука формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль за будь-яким із пп. 1-5, де R4 незалежно у кожному випадку вибраний із галогену і алкілу.
7. Сполука формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль за будь-яким із пп. 1-6, де R1 вибраний із
c)  ,
,  ,
, ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  і
і ; або
; або
d) -NH-R1a; де R1a вибраний із
 ,
,  ,
,  ,
,  ,
, 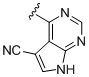 ,
,  ,
,  ,
,  ,
,  ,
, 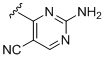 ,
, 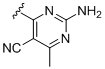 і
і  ;
;
R2 вибраний із водню і алкілу;
R3 являє собою заміщений або незаміщений арил; і
R4 незалежно у кожному випадку вибраний із галогену і алкілу.
8. Сполука формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль за будь-яким із пп. 1-7, де сполука вибрана з
2-(1-((9H-пурин-6-іл)аміно)етил)-3-феніл-4H-хінолізин-4-ону;
2-(1-((9H-пурин-6-іл)аміно)етил)-6-метил-3-феніл-4H-хінолізин-4-ону;
2-(1-((9H-пурин-6-іл)аміно)етил)-7-метил-3-феніл-4H-хінолізин-4-ону;
4-аміно-6-((1-(4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-(1-((9H-пурин-6-іл)аміно)етил)-3-(3-фторфеніл)-4H-хінолізин-4-ону;
4-аміно-6-((1-(3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
4-аміно-6-((1-(6-метил-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-6-метил-3-феніл-4H-хінолізин-4-ону;
2-(1-((2-фтор-9H-пурин-6-іл)аміно)етил)-6-метил-3-феніл-4H-хінолізин-4-ону;
4-аміно-6-((1-(3-(3-фторфеніл)-6-метил-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-(1-((9H-пурин-6-іл)аміно)етил)-3-(3-фторфеніл)-6-метил-4H-хінолізин-4-ону;
2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-3-(3-фторфеніл)-6-метил-4H-хінолізин-4-ону;
2-(1-((9H-пурин-6-іл)аміно)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
4-аміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-7-фтор-3-(3-фторфеніл)-4H-хінолізин-4-ону;
4-аміно-6-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
4-аміно-6-((1-(3-(3,5-дифторфеніл)-6-метил-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-3-(3,5-дифторфеніл)-6-метил-4H-хінолізин-4-ону;
4-аміно-6-((1-(3-(3,4-дифторфеніл)-6-метил-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-аміно-4-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-аміно-4-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)-6-метилпіримідин-5-карбонітрилу;
4-аміно-6-((1-(7-фтор-6-метил-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
4-аміно-6-((1-(7-фтор-3-(3-фторфеніл)-6-метил-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-(1-((9H-пурин-6-іл)аміно)етил)-7-фтор-6-метил-3-феніл-4H-хінолізин-4-ону;
(S)-2,4-діаміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2-аміно-4-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2-аміно-4-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)-6-метилпіримідин-5-карбонітрилу;
(S)-4-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)-7H-піроло[2,3-d]піримідин-5-карбонітрилу;
(S)-4-аміно-6-((1-(7-фтор-3-(3-фтор-5-метилфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2,4-діаміно-6-((1-(7-фтор-3-(3-фтор-5-метилфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-4-аміно-6-((1-(7-фтор-4-оксо-3-(м-толіл)-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2,4-діаміно-6-((1-(7-фтор-4-оксо-3-(м-толіл)-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
(S)-4-аміно-6-((1-(7-фтор-4-оксо-3-(3-(трифторметокси)феніл)-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-7-фтор-3-(3-(трифторметокси)феніл)-4H-хінолізин-4-ону;
(S)-4-аміно-6-((1-(7-фтор-3-(4-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2,4-діаміно-6-((1-(7-фтор-3-(4-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2-(1-((9H-пурин-6-іл)аміно)етил)-7-фтор-3-(4-фторфеніл)-4H-хінолізин-4-ону;
(S)-2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-7-фтор-3-(4-фторфеніл)-4H-хінолізин-4-ону;
(S)-7-фтор-2-(1-((5-фтор-7H-піроло[2,3-d]піримідин-4-іл)аміно)етил)-3-феніл-4H-хінолізин-4-ону;
4-аміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)пропіл)аміно)піримідин-5-карбонітрилу;
2,4-діаміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)пропіл)аміно)піримідин-5-карбонітрилу;
2-(1-((9H-пурин-6-іл)аміно)пропіл)-7-фтор-3-феніл-4H-хінолізин-4-ону;
4-аміно-6-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)пропіл)аміно)піримідин-5-карбонітрилу;
2,4-діаміно-6-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)пропіл)аміно)піримідин-5-карбонітрилу;
2-(1-((9H-пурин-6-іл)аміно)пропіл)-7-фтор-3-(3-фторфеніл)-4H-хінолізин-4-ону;
2-(1-((2-аміно-9H-пурин-6-іл)аміно)пропіл)-7-фтор-3-(3-фторфеніл)-4H-хінолізин-4-ону;
(S)-4-аміно-6-((1-(3-(3,5-дифторфеніл)-7-фтор-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2,4-діаміно-6-((1-(3-(3,5-дифторфеніл)-7-фтор-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2-(1-((9H-пурин-6-іл)аміно)етил)-3-(3,5-дифторфеніл)-7-фтор-4H-хінолізин-4-ону;
(S)-2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-3-(3,5-дифторфеніл)-7-фтор-4H-хінолізин-4-ону;
(S)-7-фтор-3-феніл-2-(1-(тіазоло[5,4-d]піримідин-7-іламіно)етил)-4H-хінолізин-4-ону;
(S)-2-аміно-4-хлор-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-7-фтор-3-феніл-2-(1-(піридо[3,2-d]піримідин-4-іламіно)етил)-4H-хінолізин-4-ону;
2-((4-аміно-1H-піразоло[3,4-d]піримідин-1-іл)метил)-6-метил-3-феніл-4H-хінолізин-4-ону;
2-((6-аміно-9H-пурин-9-іл)метил)-3-феніл-4H-хінолізин-4-ону;
2-(1-(4-аміно-1H-піразоло[3,4-d]піримідин-1-іл)етил)-3-(3-фторфеніл)-6-метил-4H-хінолізин-4-ону;
N-(3-(4-аміно-1-(1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)-1H-піразоло[3,4-d]піримідин-3-іл)-5-фторфеніл)метансульфонаміду;
2-(1-(4-аміно-3-(3-фтор-5-гідроксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
2-(1-(4-аміно-3-(3-фтор-4-гідроксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
2-(1-(4-аміно-3-(4-фтор-3-гідроксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
2-(1-(4-аміно-3-(3-гідроксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
2-(1-(4-аміно-5-(3-фтор-5-гідроксифеніл)-7H-піроло[2,3-d]піримідин-7-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
2-(1-(4-аміно-3-(6-метоксипіридин-3-іл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
2-(1-(4-аміно-3-(2-оксоіндолін-5-іл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
(S)-2-(1-(4-аміно-3-(6-гідроксипіридин-3-іл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
N-(5-(4-аміно-1-(1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)-1H-піразоло[3,4-d]піримідин-3-іл)-2-метоксипіридин-3-іл)метансульфонаміду;
(S)-N-(5-(4-аміно-1-(1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)-1H-піразоло[3,4-d]піримідин-3-іл)-2-гідроксипіридин-3-іл)метансульфонаміду та
2-(1-(4-аміно-3-(3-фтор-5-(гідроксиметил)феніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону.
9. Сполука формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль за будь-яким із пп. 1-8, де сполука вибрана з:
2-(1-((9H-пурин-6-іл)аміно)етил)-6-метил-3-феніл-4H-хінолізин-4-ону;
4-аміно-6-((1-(4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-(1-((9H-пурин-6-іл)аміно)етил)-3-(3-фторфеніл)-4H-хінолізин-4-ону;
4-аміно-6-((1-(3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
4-аміно-6-((1-(6-метил-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-6-метил-3-феніл-4H-хінолізин-4-ону;
2-(1-((2-фтор-9H-пурин-6-іл)аміно)етил)-6-метил-3-феніл-4H-хінолізин-4-ону;
4-аміно-6-((1-(3-(3-фторфеніл)-6-метил-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-(1-((9H-пурин-6-іл)аміно)етил)-3-(3-фторфеніл)-6-метил-4H-хінолізин-4-ону;
2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-3-(3-фторфеніл)-6-метил-4H-хінолізин-4-ону;
2-(1-((9H-пурин-6-іл)аміно)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
4-аміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-7-фтор-3-(3-фторфеніл)-4H-хінолізин-4-ону;
4-аміно-6-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
4-аміно-6-((1-(3-(3,5-дифторфеніл)-6-метил-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-3-(3,5-дифторфеніл)-6-метил-4H-хінолізин-4-ону;
4-аміно-6-((1-(3-(3,4-дифторфеніл)-6-метил-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-аміно-4-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-аміно-4-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)-6-метилпіримідин-5-карбонітрилу;
4-аміно-6-((1-(7-фтор-6-метил-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
4-аміно-6-((1-(7-фтор-3-(3-фторфеніл)-6-метил-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-(1-((9H-пурин-6-іл)аміно)етил)-7-фтор-6-метил-3-феніл-4H-хінолізин-4-ону;
(S)-2,4-діаміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2-аміно-4-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2-аміно-4-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)-6-метилпіримідин-5-карбонітрилу;
(S)-4-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)-7H-піроло[2,3-d]піримідин-5-карбонітрилу;
(S)-4-аміно-6-((1-(7-фтор-3-(3-фтор-5-метилфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2,4-діаміно-6-((1-(7-фтор-3-(3-фтор-5-метилфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-4-аміно-6-((1-(7-фтор-4-оксо-3-(м-толіл)-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2,4-діаміно-6-((1-(7-фтор-4-оксо-3-(м-толіл)-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
(S)-4-аміно-6-((1-(7-фтор-4-оксо-3-(3-(трифторметокси)феніл)-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-4-аміно-6-((1-(7-фтор-3-(4-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-7-фтор-2-(1-((5-фтор-7H-піроло[2,3-d]піримідин-4-іл)аміно)етил)-3-феніл-4H-хінолізин-4-ону;
4-аміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)пропіл)аміно)піримідин-5-карбонітрилу;
2,4-діаміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)пропіл)аміно)піримідин-5-карбонітрилу;
4-аміно-6-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)пропіл)аміно)піримідин-5-карбонітрилу;
2,4-діаміно-6-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)пропіл)аміно)піримідин-5-карбонітрилу;
2-(1-((2-аміно-9H-пурин-6-іл)аміно)пропіл)-7-фтор-3-(3-фторфеніл)-4H-хінолізин-4-ону;
(S)-4-аміно-6-((1-(3-(3,5-дифторфеніл)-7-фтор-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2,4-діаміно-6-((1-(3-(3,5-дифторфеніл)-7-фтор-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-2-(1-((9H-пурин-6-іл)аміно)етил)-3-(3,5-дифторфеніл)-7-фтор-4H-хінолізин-4-ону;
(S)-2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-3-(3,5-дифторфеніл)-7-фтор-4H-хінолізин-4-ону;
(S)-7-фтор-3-феніл-2-(1-(тіазоло[5,4-d]піримідин-7-іламіно)етил)-4H-хінолізин-4-ону;
(S)-2-аміно-4-хлор-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
(S)-7-фтор-3-феніл-2-(1-(піридо[3,2-d]піримідин-4-іламіно)етил)-4H-хінолізин-4-ону;
N-(3-(4-аміно-1-(1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)-1H-піразоло[3,4-d]піримідин-3-іл)-5-фторфеніл)метансульфонаміду;
2-(1-(4-аміно-3-(3-фтор-5-гідроксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
2-(1-(4-аміно-3-(3-фтор-4-гідроксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
2-(1-(4-аміно-3-(4-фтор-3-гідроксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
2-(1-(4-аміно-3-(3-гідроксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
2-(1-(4-аміно-5-(3-фтор-5-гідроксифеніл)-7H-піроло[2,3-d]піримідин-7-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
2-(1-(4-аміно-3-(6-метоксипіридин-3-іл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону;
2-(1-(4-аміно-3-(2-оксоіндолін-5-іл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону і
N-(5-(4-аміно-1-(1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)-1H-піразоло[3,4-d]піримідин-3-іл)-2-метоксипіридин-3-іл)метансульфонаміду.
10. Сполука формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль за будь-яким із пп. 1-9, де сполука вибрана з
4-аміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
4-аміно-6-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу;
2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-7-фтор-3-(3-фторфеніл)-4H-хінолізин-4-ону;
(S)-2,4-діаміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу і
2-(1-(4-аміно-3-(6-метоксипіридин-3-іл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону.
11. Фармацевтична композиція, що містить сполуку, її таутомерну форму, її стереоізомер або її фармацевтично прийнятну сіль за будь-яким із пп. 1-10 і фармацевтично прийнятний носій.
12. Спосіб лікування або попередження розладу, який є чутливим до інгібування активності PI3K, у ссавця, що страждає від нього, який включає введення ссавцю, що має потребу в такому лікуванні, терапевтично ефективної кількості сполуки, її таутомерної форми, її стереоізомера або її фармацевтично прийнятної солі за будь-яким із пп. 1-10.
13. Спосіб за п. 12, де вказаний розлад являє собою рак, розлади, пов'язані з запаленнями, або аутоімунні розлади.
14. Сполука формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль за будь-яким із пп. 1-10 для застосування у лікуванні або попередженні розладу, який є чутливим до інгібування активності PI3K, у ссавця, що страждає від нього.
15. Сполука формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль для застосування за п. 14, де вказаний розлад являє собою рак, розлади, пов'язані з запаленнями, або аутоімунні розлади.
Текст
Реферат: Розкриті сполуки формули (I), їхні таутомерні форми, стереоізомери і їхні фармацевтично прийнятні солі, , 1 4 де R -R і n визначені в описі, фармацевтичні композиції, що містять сполуку, її таутомер, стереоізомер або сіль, та способи лікування або попередження захворювань або розладів, UA 115296 C2 (12) UA 115296 C2 наприклад раку, які є такими, що піддаються лікуванню або попередженню шляхом інгібування ферменту PI3K суб’єкту. UA 115296 C2 5 10 15 20 25 30 35 40 45 50 55 60 ГАЛУЗЬ ТЕХНІКИ, ДО ЯКОЇ ВІДНОСИТЬСЯ ВИНАХІД Даний винахід відноситься до хінолізинонових похідних, їхніх таутомерних форм, їхніх стереоізомерів, їхніх фармацевтично прийнятних солей, комбінацій із придатним лікарським препаратом, фармацевтичних композицій, що містять їх, до способів одержання хінолізинонових похідних і до їх застосування як інгібіторів PI3K. ПЕРЕХРЕСНЕ ПОСИЛАННЯ НА СПОРІДНЕНУ ЗАЯВКУ Дана заявка заявляє пріоритет попередньої заявки на видачу патенту Індії № 2182/MUM/2014, поданої 4 липня 2014 року, розкриття якої включене у даний документ за допомогою посилання в повному обсязі. ПЕРЕДУМОВИ ВИНАХОДУ Онкогенна клітинна трансформація і рак пов’язані з посиленою передачею сигналів, опосередкованою PI3K, як наслідок мутаційної активації та надекспресії PI3K I класу та генетичної або епігенетичної інактивації PTEN (Ali et al., J. Natl. Cancer Inst. 1991, 1922–1932; Cantley et al., Science 2002, 296, 1655–1657; Campbell et al., Cancer Res. 2004, 64, 7678–7681; Cully et al., Nat. Rev. Cancer 2006, 6, 184–192; Vogt et al., Trends Biochem. Sci. 2007, 32, 342– 349). Фосфатидилінозитол-3-кінази (PI3K), сімейство ферментів, що діють на ліпіди, каталізують фосфорилювання 3–OH інозитольного кільця. Вони мають головну роль у регуляції широкого діапазону клітинних процесів, що включають метаболізм, виживання, рухливість, диференціацію і активацію клітин (Vanhaesebroeck et al., Annu. Rev. Biochem. 2001, 70, 535). За оцінками, сигнальний шлях PI3K має 50–100 подальших ефекторів у кожній еукаріотичній клітині. Дані ферменти, що діють на ліпіди, класифікують на 3 основних класи, I, II і III, в залежності від їхньої структури та субстратної специфічності in vitro (Wymann M. and Pirola L., Biochim. Biophys. Acta 1998, 1436, 127). Дані кінази PI3K I класу включають чотири ізоформи: PI3K α, β, γ і δ. Відомо, що як PI3K α, так і PI3K β експресуються всюди, тоді як PI3K γ і PI3K δ головним чином обмежуються гемопоетичними клітинами (Vanhaesebroeck et al., Proc. Natl. Acad. Sci. USA 1997, 94, 4330-4335). Каталітична субодиниця ізоформ p110α, p110β і p110δ конститутивно зв’язана з регуляторною субодиницею p85. Також важливо знати, що лише ізоформи I класу фосфорилюють ліпіди, які містять інозитол, з утворенням фосфоінозитидів, що являють собою вторинні месенджери, які безпосередньо перетворюють PIP2 в PIP3 у клітинній мембрані, що потім мобілізують білки низхідної передачі сигналів, як наприклад, тирозинкіназу Брутона (Btk), фосфатидилінозитол-залежну кіназу (Pdk), GRP1 і Akt (Vanhaesebroeck et al., Nat. Rev. Mol. Cell. Biol. 2010, 11, 329–41; Cantrell et al., J. Cell. Sci. 2001, 114, 1439–45; Ju He et al., J. Lipid Res. 2008, 48, 1807-1815). Активація шляху PI3K відбувається не лише за допомогою RTK, але також за допомогою RAS і GPCR (Irene Brana and Lillian L Siu., BMC Medicine 2012, 10, 161). Активація шляху PI3K за допомогою білку RAS відбувається шляхом безпосередньої взаємодії з субодиницями p110α, p110γ і p110δ, тоді як GPCR можуть взаємодіяти з субодиницями p110β і p110γ (Vanhaesebroeck et al., Nat. Rev. Mol. Cell Biol. 2010, 11, 329-341). Режим регулювання шляхом висхідної передачі сигналів також відрізняється серед чотирьох ізоформ PI3K. Ізоформа γ пов’язана зі спряженими з G-білком рецепторами, тоді як ізоформи PI3K α і PI3K δ активуються за допомогою сигналів від рецепторних тирозинкіназ. Однак, ізоформа PI3K β може приймати вхідні дані як від рецепторних тирозинкіназ, так і від спряжених із G-білком рецепторів (Kang et al., Proc. Natl. Acad. Sci. USA 2006, 103, 1289–94). Активність PI3K функціонально антагонізується гомологом фосфатази та тензину (PTEN), геном-супресором пухлини, який кодує ліпідну фосфатазу, що видаляє фосфат з положення 3OH 3-фосфоінозитидів, знижуючи клітинний пул PI(3,4,5)P3 шляхом його зворотного перетворення в PI(4,5)P2 (Liu et al., Nat. Rev. Drug Discov. 2009, 8, 627-44). Було показано, що втрата експресії PTEN активує шлях PI3K/Akt/mTOR, а також корелює з поганим прогнозом і, таким чином, зі зниженою виживаністю у випадку раку людини (LoPiccolo et al., Drug Resist. Updat. 2008, 11, 32-50). Повідомляється про мутації PIK3CA при декількох типах раку, що включають мультиформну гліобластому, рак молочної залози, рак ендометрію, колоректальний рак і гепатоцелюлярну карциному. Мутації PIK3CA є онкогенними, які per se сприяють утворенню пухлини в декількох доклінічних моделях без інших молекулярних відхилень (Ikenoue et al., Cancer Res. 2005, 65, 4562-4567; Isakoff et al., Cancer Res. 2005, 65, 10992-11000; Zhao et al., Proc. Natl. Acad. Sci. USA 2005, 102, 18443-18448). PI3Kα являє собою мутовану ізоформу, яка найбільш часто зустрічається при видах раку людини. Повідомляється, що в гені PIK3CA 80% мутацій зібрані у кластери у трьох гарячих точках мутагенезу в гені p110α, який кодує каталітичну субодиницю: дві у спіральному домені (E542K і E545K) та одну в кіназному домені (H1047R) (Zhao et al., Oncogene 2008, 27, 5486-5496). Однак дані соматичні мутації зібрані в кластери у двох гарячих точках мутагенезу: екзон 9 у спіральному домені p110α є поширеним у випадку колоректального 1 UA 115296 C2 5 10 15 20 25 30 раку, плоскоклітинного раку шийки матки та плоскоклітинного раку голови і шиї та екзон 20 в кіназному домені p110α є поширеним у випадку раку матки, раку молочної залози і типів раку яєчників (Janku et al., PLOS One 2011, 7, 6). Ізоформи PI3K I класу, відмінні від альфа-ізоформи, не мають специфічних відносно раку мутацій, але їхня диференційна експресія була виявлена при декількох видах раку. Повідомлені дані також вказують на залучення ізоформ PI3K I класу, відмінних від альфа-ізоформи, у щільних пухлинах. В останніх дослідженнях показано, що конкретні PTEN-дефіцитні лінії ракових клітин людини є більш чутливими до інактивації p110β, ніж p110α (Wee et al., Proc. Natl. Acad. Sci. USA 2008, 105, 13057–62; Torbett et al., Biochem. J. 2008, 415, 97–110). Однак дослідження in vivo вказують, що специфічна відносно ізоформи p110δ цілеспрямована дія може бути цитотоксичною до B-клітин з мінімальною токсичністю до інших типів гемопоетичних клітин. Для ясного розуміння функціональної ролі p110δ в B-клітинах виявили, що вимушена експресія p110δ поліпшує трансформаційний потенціал у лініях клітин (Kang et al., Proc. Natl. Acad. Sci. USA 2006, 103, 1289–94). При гострому мієлобластному лейкозі ізоформа p110δ завжди надекспресується та інгібітори p110δ специфічно перешкоджають росту даних лейкозних клітин, що вказує на роль p110δ у лейкемогенезі (Samuels et al., Science 2004, 304, 554; Sujobert et al., Blood 2005, 106, 1063–6). Однак P110γ особливо надекспресується при панкреатичній інтраепітеліальній неоплазії людини та внутрішньопротоковій карциномі, що корелює з підвищеними рівнями PIP3 і фосфорильованої Akt (Edling et al., Clin. Cancer Res. 2010, 16, 4928–4937; El Haibi et al., Mol. Cancer 2010, 9, 85). Підвищену експресію p110γ також спостерігали при хронічному мієлолейкозі (Hickey and Cotter., J. Biol. Chem. 2006, 281, 2441–50; Knobbe et al., Neuropathol. Appl. Neurobiol. 2005, 31, 486–90). Таким чином, очевидно, що PI3K I класу залучені до механізму виживання і до прогресування багатьох типів раку і, відтак, є одними з найбільш бажаних мішеней для терапевтичних засобів, які направлені проти раку. Отже цілеспрямована дія на саму PI3K або подальші ефектори PI3K являє собою підхід, який має можливість надати величезну терапевтичну перевагу. КОРОТКИЙ ОПИС ВИНАХОДУ В одному аспекті у даному винаході передбачені сполука формули (I), її таутомерна форма, її стереоізомер, її фармацевтично прийнятна сіль, її комбінація з придатним лікарським препаратом, фармацевтична композиція на її основі та її застосування як інгібітора PI3K, , де 1 R вибраний із 35 40 a) , , , , і , де 1A R незалежно у кожному випадку вибраний із галогену, гідрокси, гідроксиалкілу та NHSO2CH3; 1B R незалежно у кожному випадку вибраний із гідрокси, алкокси і -NHSO2CH3; або 1a 1a b) –NH-R ; де R вибраний із 2 UA 115296 C2 5 10 15 20 25 30 35 40 45 50 55 , , , , і , де 1C 1D 1E R вибраний із водню, галогену і аміно; R вибраний із галогену і ціано; R вибраний із 1F водню і аміно; R вибраний із водню, галогену і алкілу; 2 5 R вибраний із водню, заміщеного або незаміщеного алкілу, гідроксиалкілу, -OR , – 6 7 6 7 (CH2)mNR R і -C(=O)-NR R ; 3 R вибраний із заміщеного або незаміщеного арилу, заміщеного або незаміщеного циклоалкілу і заміщеного або незаміщеного циклоалкенілу; 4 R незалежно у кожному випадку вибраний із галогену, заміщеного або незаміщеного алкілу, заміщеного або незаміщеного арилу, заміщеного або незаміщеного гетероарилу, заміщеного 5 або незаміщеного гетероциклу, заміщеного або незаміщеного карбоциклу і –OR ; 5 R являє собою заміщений або незаміщений алкіл; 6 7 кожен із R та R незалежно вибраний із водню та заміщеного або незаміщеного алкілу; n являє собою ціле число, вибране з 0, 1 і 2; m являє собою ціле число, вибране з 1, 2, 3 і 4; p являє собою ціле число, вибране з 0, 1 і 2; та q являє собою ціле число, вибране з 0, 1 і 2; при цьому якщо алкільна група є заміщеною, то вона заміщена 1-3 замісниками, незалежно вибраними з оксо (=O), галогену, нітро, ціано, пергалогеналкілу, циклоалкілу, циклоалкенілу, арилу, 8b 8a 8a 8a 8 гетероарилу, гетероциклілу, -OR , -SO2R , -C(=O)OR , -OC(=O)R , -C(=O)N(H)R , 8 8a 8 8 C(=O)N(алкіл)R , -N(H)C(=O)R , -N(H)R і -N(алкіл)R ; якщо циклоалкіл, циклоалкеніл і карбоцикл є заміщеними, то кожен із них заміщений 1-3 замісниками, незалежно вибраними з оксо (=O), галогену, нітро, ціано, алкілу, алкенілу, 8b циклоалкілу, циклоалкенілу, пергалогеналкілу, арилу, гетероарилу, гетероциклілу, -OR , 8a 8a 8a 8a 8 8 8a SO2R , -C(=O)R , -C(=O)OR , -OC(=O)R , -C(=O)N(H)R , -C(=O)N(алкіл)R , -N(H)C(=O)R , 8 8 N(H)R і -N(алкіл)R ; якщо арильна група є заміщеною, то вона заміщена 1-3 замісниками, незалежно вибраними з галогену, нітро, ціано, гідрокси, алкілу, алкенілу, пергалогеналкілу, циклоалкілу, циклоалкенілу, гетероциклілу, арилу, гетероарилу, -O-алкілу, -O-пергалогеналкілу, N(алкіл)алкілу, -N(H)алкілу, -NH2, -SO2-алкілу, -SO2-пергалогеналкілу, -N(алкіл)C(=O)алкілу, N(H)C(=O)алкілу, -C(=O)N(алкіл)алкілу, -C(=O)N(H)алкілу, -C(=O)N(H)циклоалкілу, -C(=O)NH2, -SO2N(алкіл)алкілу, -SO2N(H)алкілу, SO2NH2, -C(=O)OH і -C(=O)O-алкілу; якщо гетероарильна група є заміщеною, то вона заміщена 1-3 замісниками, незалежно вибраними з галогену, ціано, гідрокси, алкілу, алкенілу, пергалогеналкілу, циклоалкілу, циклоалкенілу, гетероциклілу, -O-алкілу, O-пергалогеналкілу, -N(алкіл)алкілу, -N(H)алкілу, -NH2, -SO2-алкілу, -SO2-пергалогеналкілу, -N(алкіл)C(=O)алкілу, -N(H)C(=O)алкілу, C(=O)N(алкіл)алкілу, -C(=O)N(H)алкілу, -C(=O)NH2, -SO2N(алкіл)алкілу, -SO2N(H)алкілу, SO2NH2, -C(=O)OH і -C(=O)O-алкілу; якщо гетероцикліл і гетероцикл є заміщеними, то кожен із них заміщений або за атомом вуглецю в кільці, або за гетероатомом в кільці, та якщо він є заміщений за атомом вуглецю в кільці, то він заміщений 1-3 замісниками, незалежно вибраними з галогену, нітро, ціано, оксо (=O), алкілу, алкенілу, пергалогеналкілу, циклоалкілу, циклоалкенілу, арилу, гетероарилу, 8a 8b 8a 8a 8 8 гетероциклілу, -SO2R , -OR , -C(=O)OR , -OC(=O)R , -C(=O)N(H)R , -C(=O)N(алкіл)R , 8a 8 8 N(H)C(=O)R , -N(H)R і -N(алкіл)R ; та якщо гетероциклічна група є заміщеною за атомом азоту в кільці, то вона заміщена замісниками, незалежно вибраними з алкілу, алкенілу, гідроксиалкілу, 8a 8c 8a 8 циклоалкілу, циклоалкенілу, арилу, гетероарилу, -SO2R , -C(=O)R , C(=O)OR , -C(=O)N(H)R і 8 C(=O)N(алкіл)R ; 8 R вибраний із групи, що включає водень, алкіл, алкеніл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл; 8a R вибраний із групи, що включає алкіл, алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл; 8b R вибраний із групи, що включає водень, алкіл, алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл; та 8c R вибраний із групи, що включає алкіл, гідроксиалкіл, алкеніл, пергалогеналкіл, циклоалкіл, 3 UA 115296 C2 5 10 циклоалкеніл, арил, гетероарил і гетероцикліл. У другому аспекті у даному винаході передбачена фармацевтична композиція, що містить сполуку формули (I) та фармацевтично прийнятний носій. У третьому аспекті у даному винаході передбачений спосіб лікування або попередження розладу, який є чутливим до інгібування активності PI3K, у ссавця, що страждає від нього, який передбачає введення ссавцю, що має потребу в такому лікуванні, терапевтично ефективної кількості сполуки формули (I). ДОКЛАДНИЙ ОПИС ВИНАХОДУ В одному аспекті у даному винаході передбачені сполука формули (I), її таутомерна форма, її стереоізомер, її фармацевтично прийнятна сіль, її комбінація з придатним лікарським препаратом, фармацевтична композиція на її основі та її застосування як інгібітора PI3K, , де 1 R вибраний із 15 20 25 30 35 a) , , , , і , де 1A R незалежно у кожному випадку вибраний із галогену, гідрокси, гідроксиалкілу та NHSO2CH3; 1B R незалежно у кожному випадку вибраний із гідрокси, алкокси і -NHSO2CH3; або 1a 1a b) –NH-R ; де R вибраний із , , , , і , де 1C 1D 1E R вибраний із водню, галогену і аміно; R вибраний із галогену і ціано; R вибраний із 1F водню і аміно; R вибраний із водню, галогену і алкілу; 2 5 R вибраний із водню, заміщеного або незаміщеного алкілу, гідроксиалкілу, -OR , – 6 7 6 7 (CH2)mNR R і -C(=O)-NR R ; 3 R вибраний із заміщеного або незаміщеного арилу, заміщеного або незаміщеного циклоалкілу і заміщеного або незаміщеного циклоалкенілу; 4 R незалежно у кожному випадку вибраний із галогену, заміщеного або незаміщеного алкілу, заміщеного або незаміщеного арилу, заміщеного або незаміщеного гетероарилу, заміщеного 5 або незаміщеного гетероциклу, заміщеного або незаміщеного карбоциклу і –OR ; 5 R являє собою заміщений або незаміщений алкіл; 6 7 кожен із R і R незалежно вибраний із водню та заміщеного або незаміщеного алкілу; n являє собою ціле число, вибране з 0, 1 і 2; m являє собою ціле число, вибране з 1, 2, 3 і 4; p являє собою ціле число, вибране з 0, 1 і 2; та q являє собою ціле число, вибране з 0, 1 і 2; 4 UA 115296 C2 5 10 15 20 25 30 35 40 при цьому якщо алкільна група є заміщеною, то вона заміщена 1-3 замісниками, незалежно вибраними з оксо (=O), галогену, нітро, ціано, пергалогеналкілу, циклоалкілу, циклоалкенілу, арилу, 8b 8a 8a 8a 8 гетероарилу, гетероциклілу, -OR , -SO2R , -C(=O)OR , -OC(=O)R , -C(=O)N(H)R , 8 8a 8 8 C(=O)N(алкіл)R , -N(H)C(=O)R , -N(H)R і -N(алкіл)R ; якщо циклоалкіл, циклоалкеніл і карбоцикл є заміщеними, то кожен із них заміщений 1-3 замісниками, незалежно вибраними з оксо (=O), галогену, нітро, ціано, алкілу, алкенілу, 8b циклоалкілу, циклоалкенілу, пергалогеналкілу, арилу, гетероарилу, гетероциклілу, -OR , 8a 8a 8a 8a 8 8 8a SO2R , -C(=O)R , -C(=O)OR , -OC(=O)R , -C(=O)N(H)R , -C(=O)N(алкіл)R , -N(H)C(=O)R , 8 8 N(H)R і -N(алкіл)R ; якщо арильна група є заміщеною, то вона заміщена 1-3 замісниками, незалежно вибраними з галогену, нітро, ціано, гідрокси, алкілу, алкенілу, пергалогеналкілу, циклоалкілу, циклоалкенілу, гетероциклілу, арилу, гетероарилу, -O-алкілу, -O-пергалогеналкілу, N(алкіл)алкілу, -N(H)алкілу, -NH2, -SO2-алкілу, -SO2-пергалогеналкілу, -N(алкіл)C(=O)алкілу, N(H)C(=O)алкілу, -C(=O)N(алкіл)алкілу, -C(=O)N(H)алкілу, -C(=O)N(H)циклоалкілу, -C(=O)NH2, -SO2N(алкіл)алкілу, -SO2N(H)алкілу, SO2NH2, -C(=O)OH і -C(=O)O-алкілу; якщо гетероарильна група є заміщеною, то вона заміщена 1-3 замісниками, незалежно вибраними з галогену, ціано, гідрокси, алкілу, алкенілу, пергалогеналкілу, циклоалкілу, циклоалкенілу, гетероциклілу, -O-алкілу, O-пергалогеналкілу, -N(алкіл)алкілу, -N(H)алкілу, -NH2, -SO2-алкілу, -SO2-пергалогеналкілу, -N(алкіл)C(=O)алкілу, -N(H)C(=O)алкілу, C(=O)N(алкіл)алкілу, -C(=O)N(H)алкілу, -C(=O)NH2, -SO2N(алкіл)алкілу, -SO2N(H)алкілу, SO2NH2, -C(=O)OH і -C(=O)O-алкілу; якщо гетероцикліл і гетероцикл є заміщеними, то кожен із них заміщений або за атомом вуглецю в кільці, або за гетероатомом в кільці, та якщо він є заміщений за атомом вуглецю в кільці, то він заміщений 1-3 замісниками, незалежно вибраними з галогену, нітро, ціано, оксо (=O), алкілу, алкенілу, пергалогеналкілу, циклоалкілу, циклоалкенілу, арилу, гетероарилу, 8a 8b 8a 8a 8 8 гетероциклілу, -SO2R , -OR , -C(=O)OR , -OC(=O)R , -C(=O)N(H)R , -C(=O)N(алкіл)R , 8a 8 8 N(H)C(=O)R , -N(H)R і -N(алкіл)R ; та якщо гетероциклічна група є заміщеною за атомом азоту в кільці, то вона заміщена замісниками, незалежно вибраними з алкілу, алкенілу, гідроксиалкілу, 8a 8c 8a 8 циклоалкілу, циклоалкенілу, арилу, гетероарилу, -SO2R , -C(=O)R , C(=O)OR , -C(=O)N(H)R і 8 C(=O)N(алкіл)R ; 8 R вибраний із групи, що включає водень, алкіл, алкеніл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл; 8a R вибраний із групи, що включає алкіл, алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл; 8b R вибраний із групи, що включає водень, алкіл, алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл; та 8c R вибраний із групи, що включає алкіл, гідроксиалкіл, алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл. 1 У конкретних варіантах здійснення R вибраний із a) 45 , , , , і , де 1A R незалежно у кожному випадку вибраний із галогену, гідрокси, гідроксиалкілу і NHSO2CH3; 1B R незалежно у кожному випадку вибраний із гідрокси, алкокси і -NHSO2CH3; або 1a 1a b) –NH-R ; де R вибраний із 5 UA 115296 C2 5 , , , , і , де 1C 1D 1E R вибраний із водню, галогену і аміно; R вибраний із галогену і ціано; R вибраний із 1F водню і аміно; R вибраний із водню, галогену і алкілу. 1 Більш конкретно, R вибраний із a) , , , , , , , або 10 1a a) –NH-R ; де R , 15 20 , 1a , , , і , вибраний із , , , , , , , , , і . 2 У конкретних варіантах здійснення R вибраний із водню та алкілу. 2 Більш конкретно, R вибраний із водню, метилу та етилу. 3 У конкретних варіантах здійснення R являє собою заміщений або незаміщений арил. 3 Більш конкретно, R вибраний із фенілу, 3-фторфенілу, 4-фторфенілу, 3,5-дифторфенілу, 3,4-дифторфенілу, 3-фтор-5-метилфенілу, 3-метилфенілу та 3-трифторметоксифенілу. 4 У конкретних варіантах здійснення R незалежно у кожному випадку вибраний із галогену й алкілу. 4 Більш конкретно, R незалежно у кожному випадку вибраний із фтору та метилу. У конкретних варіантах здійснення n являє собою ціле число, вибране з 0-2. У конкретних варіантах здійснення p являє собою ціле число, вибране з 1 і 2. У конкретних варіантах здійснення q являє собою ціле число, вибране з 1 і 2. 1 У конкретних варіантах здійснення R вибраний із 6 UA 115296 C2 a) 5 10 15 , , , і , де 1A R незалежно у кожному випадку вибраний із галогену, гідрокси, гідроксиалкілу і NHSO2CH3; 1B R незалежно у кожному випадку вибраний із гідрокси, алкокси і -NHSO2CH3; або 1a 1a b) –NH-R ; де R вибраний із , , , , і , де 1C 1D 1E R вибраний із водню, галогену і аміно; R вибраний із галогену і ціано; R вибраний із 1F 2 3 водню і аміно; R вибраний із водню, галогену і алкілу; R вибраний із водню і алкілу; R являє 4 собою заміщений або незаміщений арил; R незалежно у кожному випадку вибраний із галогену і алкілу; n являє собою ціле число, вибране з 0-2; p являє собою ціле число, вибране з 1 і 2; та q являє собою ціле число, вибране з 1 і 2. 1 Більш конкретно, R вибраний із b) , , , , , 1a b) –NH-R ; де R 1a , , , або 20 , , вибраний із 7 , , і , UA 115296 C2 , 5 10 15 20 25 30 35 40 45 50 , , , , , , , , , і ; 2 3 R вибраний із водню, метилу та етилу; R вибраний із фенілу, 3-фторфенілу, 4-фторфенілу, 3,5-дифторфенілу, 3,4-дифторфенілу, 3-фтор-5-метилфенілу, 3-метилфенілу та 34 трифторметоксифенілу; R незалежно у кожному випадку вибраний із фтору та метилу; n являє собою ціле число, вибране з 0-2; p являє собою ціле число, вибране з 1 і 2; та q являє собою ціле число, вибране з 1 і 2. Термін «алкіл», застосовуваний у даному документі, означає вуглеводень з нерозгалуженим або нерозгалуженим ланцюгом, що містить від 1 до 20 атомів вуглецю. Переважно алкільний ланцюг може містити від 1 до 10 атомів вуглецю. Більш переважно алкільний ланцюг може містити не більше 6 атомів вуглецю. Ілюстративні приклади алкілу включають без обмеження метил, етил, н-пропіл, ізопропіл, н-бутил, втор-бутил, ізобутил, трет-бутил, н-пентил, ізопентил, неопентил і н-гексил. Термін «алкеніл», застосовуваний у даному документі, означає алкільну групу, що містить щонайменше один подвійний зв’язок. Терміни «алкіл» і «алкеніл», як визначено у даному документі вище, можуть передбачати заміщення 1-3 замісниками, незалежно вибраними з оксо (=O), галогену, нітро, ціано, 8b пергалогеналкілу, циклоалкілу, циклоалкенілу, арилу, гетероарилу, гетероциклілу, -OR , 8a 8a 8a 8 8 8a 8 SO2R , -C(=O)OR , -OC(=O)R , -C(=O)N(H)R , -C(=O)N(алкіл)R , -N(H)C(=O)R , -N(H)R і 8 8 N(алкіл)R ; R вибраний із групи, що включає водень, алкіл, алкеніл, циклоалкіл, циклоалкеніл, 8a арил, гетероарил і гетероцикліл; R вибраний із групи, що включає алкіл, алкеніл, 8b пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил, гетероцикліл; і R вибраний із групи, що включає водень, алкіл, алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл. Термін «пергалогеналкіл», застосовуваний у даному документі, означає алкільну групу, як визначено у даному документі вище, де всі атоми водню вказаної алкільної групи заміщенні галогеном. Прикладами пергалогеналкільної групи є трифторметил, пентафторетил тощо. Термін «аміно», застосовуваний у даному документі, означає –NH2. Термін «циклоалкіл», застосовуваний у даному документі, означає моноциклічну, біциклічну або трициклічну неароматичну кільцеву систему, що містить від 3 до 14 атомів вуглецю, переважно моноциклічне циклоалкільне кільце, яке містить від 3 до 6 атомів вуглецю. Приклади моноциклічних кільцевих систем включають циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил і циклооктил. Біцикличні кільцеві системи включають моноциклічну кільцеву систему, конденсовану за допомогою зв’язку з іншою циклічною системою, яка може являти собою аліциклічне кільце або ароматичне кільце. Біциклічні кільця також включають спіроциклічні системи, де друге кільце стає анельованим за одним атомом вуглецю. Також прикладом біциклічних кільцевих систем є місткова моноциклічна кільцева система, в якій два несуміжних атоми вуглецю моноциклічного кільця зв’язані за допомогою алкіленового містка. Ілюстративні приклади біциклічних кільцевих систем включають без обмеження біцикло[3.1.1]гептан, біцикло[2.2.1]гептан, біцикло[2.2.2]октан, біцикло[3.2.2]нонан, біцикло[3.3.1]нонан і біцикло[4.2.1]нонан, біцикло[3.3.2]декан, біцикло[3.1.0]гексан, біцикло[4.1.0]гептан, біцикло[3.2.0]гептани, октагідро-1H-інден, спіро[2.5]октан, спіро[4.5]декан, спіро[біцикло[4.1.0]гептан-2,1'-циклопентан], гексагідро-2'H-спіро[циклопропан-1,1'-пентален]. Трициклічні кільцеві системи являють собою системи, в яких біциклічні системи, що описані вище, додатково анельовані з третім кільцем, яким може бути аліциклічне кільце або ароматичне кільце. Також прикладом трициклічних кільцевих систем є біциклічна кільцева система, в якій два несуміжних атоми вуглецю з’єднані за допомогою зв’язку або алкіленового містка. Ілюстративні приклади трициклічних кільцевих систем включають без обмеження 3.7 3.7 трицикло[3.3.1.0 ]нонан і трицикло[3.3.1.1 ]декан (адамантан). Термін «циклоалкеніл», застосовуваний у даному документі, означає циклоалкільну групу, 8 UA 115296 C2 5 10 15 20 25 30 35 40 45 50 55 60 що містить щонайменше один подвійний зв’язок. Термін «карбоцикл», застосовуваний у даному документі, означає циклічну систему, що складається з атомів вуглецю, яка включає циклоалкіл, циклоалкеніл і арил. Циклоалкіл, циклоалкеніл і карбоцикл, як визначено у даному документі вище, можуть бути заміщені 1-3 замісниками, незалежно вибраними з оксо (=O), галогену, нітро, ціано, алкілу, алкенілу, циклоалкілу, циклоалкенілу, пергалогеналкілу, арилу, гетероарилу, гетероциклілу, 8b 8a 8a 8a 8a 8 8 OR , -SO2R , -C(=O)R , -C(=O)OR , -OC(=O)R , -C(=O)N(H)R , -C(=O)N(алкіл)R , 8a 8 8 8 N(H)C(=O)R , -N(H)R і -N(алкіл)R ; R вибраний із групи, що включає водень, алкіл, алкеніл, 8a циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл; R вибраний із групи, що включає алкіл, алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил, гетероцикліл; та 8b R вибраний із групи, що включає водень, алкіл, алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл. Термін «арил», застосовуваний у даному документі, відноситься до моновалентної моноциклічної, біциклічної або трициклічної ароматичної вуглеводневої кільцевої системи. Приклади арильних груп включають феніл, нафтил, антраценіл, флуореніл, інденіл, азуленіл тощо. Арильна група також включає частково насичені біциклічні та трициклічні ароматичні вуглеводні, наприклад, тетрагідронафтален. Арил, як визначено у даному документі вище, може бути заміщений 1-3 замісниками, вибраними з галогену, нітро, ціано, гідрокси, алкілу, алкенілу, пергалогеналкілу, циклоалкілу, циклоалкенілу, гетероциклілу, арилу, гетероарилу, -O-алкілу, -O-пергалогеналкілу, N(алкіл)алкілу, -N(H)алкілу, -NH2, -SO2-алкілу, -SO2-пергалогеналкілу, -N(алкіл)C(=O)алкілу, N(H)C(=O)алкілу, -C(=O)N(алкіл)алкілу, -C(=O)N(H)алкілу, -C(=O)N(H)циклоалкілу, -C(=O)NH2, SO2N(алкіл)алкілу, -SO2N(H)алкілу, -SO2NH2, -C(=O)OH і -C(=O)O-алкілу. Термін «гетероарил», застосовуваний у даному документі, відноситься до 5-14-членної моноциклічної, біциклічної або трициклічної кільцевої системи з 1-4 гетероатомами в кільці, вибраними з O, N або S, при цьому решта атомів кільця являють собою атоми вуглецю (з відповідними атомами водню, якщо не вказано інше), де щонайменше одне кільце в кільцевій системі є ароматичним. Гетероарильні групи можуть бути необов'язково заміщені одним або більше замісниками. В одному варіанті здійснення 0, 1, 2, 3 або 4 атоми кожного кільця гетероарильної групи можуть бути заміщені замісником. Приклади гетероарильних груп включають без обмеження піридил, 1-оксопіридил, фураніл, тієніл, піроліл, оксазоліл, оксадіазоліл, імідазоліл, тіазоліл, ізоксазоліл, хінолініл, піразоліл, ізотіазоліл, піридазиніл, піримідиніл, піразиніл, триазиніл. триазоліл, тіадіазоліл, ізохінолініл, бензоксазоліл, бензофураніл, індолізиніл, імідазопіридил, тетразоліл, бензимідазоліл, бензотіазоліл, бензотіадіазоліл, бензоксадіазоліл, індоліл, азаіндоліл, імідазопіридил, хіназолініл, пуриніл, піроло[2,3]піримідиніл, піразоло[3,4]піримідиніл і бензо(b)тієніл, 2,3-тіaдіазоліл, 1H-піразоло[5,1c]-1,2,4-триазоліл, піроло[3,4-d]-1,2,3-триазоліл, циклопентатриазоліл, 3H-піроло[3,4c]ізоксазоліл, 2,3-дигідробензо[1,4]діоксин-6-іл, 2,3-дигідробензо[1,4]діоксин-5-іл, 2,3дигідробензофуран-5-іл, 2,3-дигідробензофуран-4-іл, 2,3-дигідробензофуран-6-іл, 2,3дигідробензофуран-6-іл, 2,3-дигідро-1H-індол-5-іл, 2,3-дигідро-1H-індол-4-іл, 2,3-дигідро-1Hіндол-6-іл, 2,3-дигідро-1H-індол-7-іл, бензо[1,3]діоксол-4-іл, бензо[1,3]діоксол-5-іл, 1,2,3,4тетрагідрохінолініл, 1,2,3,4-тетрагідроізохінолініл, 2,3-дигідробензотієн-4-іл, 2-оксоіндолін-5-іл тощо. Термін «гетероарил», як визначено у даному документі вище, може передбачати необов'язкове заміщення 1-4 замісниками, вибраними з галогену, нітро, ціано, гідрокси, алкілу, алкенілу, пергалогеналкілу, циклоалкілу, циклоалкенілу, гетероциклілу, -O-алкілу, Oпергалогеналкілу, -N(алкіл)алкілу, -N(H)алкілу, -NH2, -SO2-алкілу, -SO2-пергалогеналкілу, N(алкіл)C(=O)алкілу, -N(H)C(=O)алкілу, -C(=O)N(алкіл)алкілу, -C(=O)N(H)алкілу, -C(=O)NH2, SO2N(алкіл)алкілу, -SO2N(H)алкілу, -SO2NH2, -C(=O)OH і -C(=O)O-алкілу. Термін «гетероцикл» або «гетероциклічний», застосовуваний у даному документі, означає «циклоалкільну» групу, де один або більше атомів вуглецю заміщені гетероатомом, вибраним із N, S і O. Гетероцикл може бути приєднаний до вихідного молекулярного фрагменту за допомогою будь-якого атома вуглецю або будь-якого атома азоту, що міститься у гетероциклі. Ілюстративні приклади моноциклічного гетероциклу включають без обмеження азетидиніл, азепаніл, азиридиніл, діазепаніл, 1,3-діоксаніл, 1,3-діоксоланіл, 1,3-дитіоланіл, 1,3-дитіаніл, імідазолініл, імідазолідиніл, ізотіазолініл, ізотіазолідиніл, ізоксазолініл, ізоксазолідиніл, морфолініл, оксадіазолініл, оксадіазолідиніл, оксазолініл, оксазолідиніл, піперазиніл, піперидиніл, піраніл, піразолініл, піразолідиніл, піролініл, піролідиніл, тетрагідрофураніл, тетрагідротієніл, тіадіазолініл, тіадіазолідиніл, тіазолініл, тіазолідиніл, тіоморфолініл, 1,1діоксидотіоморфолініл (тіоморфоліну сульфон), тіопіраніл і тритіаніл. Ілюстративні приклади 9 UA 115296 C2 5 10 15 20 25 30 35 40 45 50 55 60 біциклічного гетероциклу включають без обмеження 1,2,3,4-тетрагідроізохінолін-2-іл, 1,2,3,4тетрагідрохінолін-1-іл, 1,3-бензодіоксоліл, 1,3-бензодитіоліл, 2,3-дигідро-1,4-бензодіоксиніл, 2,3дигідро-1-бензофураніл, 2,3-дигідро-1-бензотієніл, 2,3-дигідро-1H-індоліл і 1,2,3,4тетрагідрохінолініл. Термін «гетероцикл» також включає місткові та спірогетероциклічні системи, як наприклад, азабіцикло[3.2.1]октан, азабіцикло[3.3.1]нонан, 8-окса-3азабіцикло[3.2.1]октан-3-іл, 3-окса-8-азабіцикло[3.2.1]октан-8-іл, 6-окса-3азабіцикло[3.1.1]гептан-3-іл, 8-азабіцикло[3.2.1]октан-8-іл, 3-азабіцикло[3.2.1]октан-3-іл, 3азабіцикло[3.1.0]гексан-3-іл, 6-азаспіро[2.5]октан-6-іл, 5-азаспіро[2.5]октан-5-іл, 4азаспіро[2.4]гептан-4-іл тощо. Гетероцикл, як визначено у даному документі вище, де атом вуглецю в кільці може бути необов'язково заміщений 1-3 замісниками, вибраними з галогену, нітро, ціано, оксо (=O), алкілу, алкенілу, пергалогеналкілу, циклоалкілу, циклоалкенілу, арилу, гетероарилу, гетероциклілу, 8a 8b 8a 8a 8 8 8a 8 SO2R , -OR , -C(=O)OR , -OC(=O)R , -C(=O)N(H)R , -C(=O)N(алкіл)R , -N(H)C(=O)R , -N(H)R і 8 8 -N(алкіл)R ; R вибраний із групи, що включає водень, алкіл, алкеніл, циклоалкіл, циклоалкеніл, 8a арил, гетероарил і гетероцикліл; R вибраний із групи, що включає алкіл, алкеніл, 8b пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил, гетероцикліл; та R вибраний із групи, що включає водень, алкіл, алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил і гетероцикліл. Термін «гетероцикл», як визначено у даному документі вище, де атом азоту в кільці може бути необов'язково заміщений замісником, вибраним із алкілу, алкенілу, гідроксиалкілу, 8a 8c 8a 8 циклоалкілу, циклоалкенілу, арилу, гетероарилу, -SO2R , -C(=O)R , C(=O)OR , -C(=O)N(H)R , 8 8 C(=O)N(алкіл)R ; R вибраний із групи, що включає водень, алкіл, алкеніл, циклоалкіл, 8a циклоалкеніл, арил, гетероарил і гетероцикліл; R вибраний із групи, що включає алкіл, 8c алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил, гетероцикліл; R вибраний із групи, що включає алкіл, гідроксиалкіл, алкеніл, пергалогеналкіл, циклоалкіл, циклоалкеніл, арил, гетероарил, гетероцикліл. Термін «оксо» означає двовалентний кисень (=O), який приєднаний до вихідної групи. Наприклад, оксо, приєднаний до вуглецю, утворює карбоніл, оксо, заміщений за циклогексаном, утворює циклогексанон тощо. Термін «анельований» означає кільцеву систему, яка при розгляді являє собою або анельовану з іншим кільцем за атомом вуглецю циклічної системи, або через зв’язок циклічної системи, як у випадку з конденсованими або спірокільцевими системами. Термін «містковий» означає кільцеву систему, яка при розгляді містить алкіленовий місток з 1-4 метиленовими ланками, що з’єднують два несуміжних атоми в кільці. Щоразу коли вказано діапазон числа атомів у структурі (наприклад, C 1-C20алкіл, C2C20алкеніл тощо) особливо передбачено, що також можна застосовувати будь-який піддіапазон або окреме число атомів вуглецю, які потрапляють у вказаний діапазон. Таким чином, наприклад, зазначення діапазону 1-6 атомів вуглецю (наприклад, C1-C6), 2-6 атомів вуглецю (наприклад, C2-C6), 3-6 атомів вуглецю (наприклад, C3-C6), застосовуване щодо будь-якої названої у даному документі хімічної групи (наприклад, алкіл, алкеніл тощо), охоплює і, зокрема, описує 1, 2, 3, 4, 5 і/або 6 атомів вуглецю, за необхідності, а також його будь-який піддіапазон (наприклад, 1-2 атомів вуглецю, 1-3 атомів вуглецю, 1-4 атомів вуглецю, 1-5 атомів вуглецю, 1-6 атомів вуглецю, 2-3 атомів вуглецю, 2-4 атомів вуглецю, 2-5 атомів вуглецю, 2-6 атомів вуглецю, 3-4 атомів вуглецю, 3-5 атомів вуглецю, 3-6 атомів вуглецю, 4-5 атомів вуглецю, 4-6 атомів вуглецю, за необхідності). Відповідно до одного варіанту здійснення у даному винаході передбачені сполука, її стереоізомери, рацемати і її фармацевтично прийнятна сіль, як описано в даному документі вище, де сполука загальної формули (I) вибрана з 2-(1-((9H-пурин-6-іл)аміно)етил)-3-феніл-4H-хінолізин-4-ону; 2-(1-((9H-пурин-6-іл)аміно)етил)-6-метил-3-феніл-4H-хінолізин-4-ону; 2-(1-((9H-пурин-6-іл)аміно)етил)-7-метил-3-феніл-4H-хінолізин-4-ону; 4-аміно-6-((1-(4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу; 2-(1-((9H-пурин-6-іл)аміно)етил)-3-(3-фторфеніл)-4H-хінолізин-4-ону; 4-аміно-6-((1-(3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу; 4-аміно-6-((1-(6-метил-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5карбонітрилу; 2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-6-метил-3-феніл-4H-хінолізин-4-ону; 2-(1-((2-фтор-9H-пурин-6-іл)аміно)етил)-6-метил-3-феніл-4H-хінолізин-4-ону; 4-аміно-6-((1-(3-(3-фторфеніл)-6-метил-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5карбонітрилу; 10 UA 115296 C2 5 10 15 20 25 30 35 40 45 50 55 60 2-(1-((9H-пурин-6-іл)аміно)етил)-3-(3-фторфеніл)-6-метил-4H-хінолізин-4-ону; 2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-3-(3-фторфеніл)-6-метил-4H-хінолізин-4-ону; 2-(1-((9H-пурин-6-іл)аміно)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону; 4-аміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5-карбонітрилу; 2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-7-фтор-3-(3-фторфеніл)-4H-хінолізин-4-ону; 4-аміно-6-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5карбонітрилу; 4-аміно-6-((1-(3-(3,5-дифторфеніл)-6-метил-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5карбонітрилу; 2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-3-(3,5-дифторфеніл)-6-метил-4H-хінолізин-4-ону; 4-аміно-6-((1-(3-(3,4-дифторфеніл)-6-метил-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5карбонітрилу; 2-аміно-4-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5карбонітрилу; 2-аміно-4-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)-6метилпіримідин-5-карбонітрилу; 4-аміно-6-((1-(7-фтор-6-метил-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5карбонітрилу; 4-аміно-6-((1-(7-фтор-3-(3-фторфеніл)-6-метил-4-оксо-4H-хінолізин-2іл)етил)аміно)піримідин-5-карбонітрилу; 2-(1-((9H-пурин-6-іл)аміно)етил)-7-фтор-6-метил-3-феніл-4H-хінолізин-4-ону; (S)-2,4-діаміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5карбонітрилу; (S)-2-аміно-4-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5карбонітрилу; (S)-2-аміно-4-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)-6-метилпіримідин-5карбонітрилу; (S)-4-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)-7H-піроло[2,3-d]піримідин-5карбонітрилу; (S)-4-аміно-6-((1-(7-фтор-3-(3-фтор-5-метилфеніл)-4-оксо-4H-хінолізин-2іл)етил)аміно)піримідин-5-карбонітрилу; (S)-2,4-діаміно-6-((1-(7-фтор-3-(3-фтор-5-метилфеніл)-4-оксо-4H-хінолізин-2іл)етил)аміно)піримідин-5-карбонітрилу; (S)-4-аміно-6-((1-(7-фтор-4-оксо-3-(м-толіл)-4H-хінолізин-2-іл)етил)аміно)піримідин-5карбонітрилу; (S)-2,4-діаміно-6-((1-(7-фтор-4-оксо-3-(м-толіл)-4H-хінолізин-2-іл)етил)аміно)піримідин-5карбонітрилу; (S)-2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-7-фтор-3-феніл-4H-хінолізин-4-ону; (S)-4-аміно-6-((1-(7-фтор-4-оксо-3-(3-(трифторметокси)феніл)-4H-хінолізин-2іл)етил)аміно)піримідин-5-карбонітрилу; (S)-2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-7-фтор-3-(3-(трифторметокси)феніл)-4Hхінолізин-4-ону; (S)-4-аміно-6-((1-(7-фтор-3-(4-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин-5карбонітрилу; (S)-2,4-діаміно-6-((1-(7-фтор-3-(4-фторфеніл)-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин5-карбонітрилу; (S)-2-(1-((9H-пурин-6-іл)аміно)етил)-7-фтор-3-(4-фторфеніл)-4H-хінолізин-4-ону; (S)-2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-7-фтор-3-(4-фторфеніл)-4H-хінолізин-4-ону; (S)-7-фтор-2-(1-((5-фтор-7H-піроло[2,3-d]піримідин-4-іл)аміно)етил)-3-феніл-4H-хінолізин-4ону; 4-аміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)пропіл)аміно)піримідин-5карбонітрилу; 2,4-діаміно-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)пропіл)аміно)піримідин-5карбонітрилу; 2-(1-((9H-пурин-6-іл)аміно)пропіл)-7-фтор-3-феніл-4H-хінолізин-4-ону; 4-аміно-6-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)пропіл)аміно)піримідин-5карбонітрилу; 2,4-діаміно-6-((1-(7-фтор-3-(3-фторфеніл)-4-оксо-4H-хінолізин-2-іл)пропіл)аміно)піримідин-5карбонітрилу; 2-(1-((9H-пурин-6-іл)аміно)пропіл)-7-фтор-3-(3-фторфеніл)-4H-хінолізин-4-ону; 11 UA 115296 C2 5 10 15 20 25 30 35 40 2-(1-((2-аміно-9H-пурин-6-іл)аміно)пропіл)-7-фтор-3-(3-фторфеніл)-4H-хінолізин-4-ону; (S)-4-аміно-6-((1-(3-(3,5-дифторфеніл)-7-фтор-4-оксо-4H-хінолізин-2-іл)етил)аміно)піримідин5-карбонітрилу; (S)-2,4-діаміно-6-((1-(3-(3,5-дифторфеніл)-7-фтор-4-оксо-4H-хінолізин-2іл)етил)аміно)піримідин-5-карбонітрилу; (S)-2-(1-((9H-пурин-6-іл)аміно)етил)-3-(3,5-дифторфеніл)-7-фтор-4H-хінолізин-4-ону; (S)-2-(1-((2-аміно-9H-пурин-6-іл)аміно)етил)-3-(3,5-дифторфеніл)-7-фтор-4H-хінолізин-4-ону; (S)-7-фтор-3-феніл-2-(1-(тіазоло[5,4-d]піримідин-7-іламіно)етил)-4H-хінолізин-4-ону; (S)-2-аміно-4-хлор-6-((1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)аміно)піримідин-5карбонітрилу; (S)-7-фтор-3-феніл-2-(1-(піридо[3,2-d]піримідин-4-іламіно)етил)-4H-хінолізин-4-ону; 2-((4-аміно-1H-піразоло[3,4-d]піримідин-1-іл)метил)-6-метил-3-феніл-4H-хінолізин-4-ону; 2-((6-аміно-9H-пурин-9-іл)метил)-3-феніл-4H-хінолізин-4-ону; 2-(1-(4-аміно-1H-піразоло[3,4-d]піримідин-1-іл)етил)-3-(3-фторфеніл)-6-метил-4H-хінолізин-4ону; N-(3-(4-аміно-1-(1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)-1H-піразоло[3,4d]піримідин-3-іл)-5-фторфеніл)метансульфонаміду; 2-(1-(4-аміно-3-(3-фтор-5-гідроксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3феніл-4H-хінолізин-4-ону; 2-(1-(4-аміно-3-(3-фтор-4-гідроксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3феніл-4H-хінолізин-4-ону; 2-(1-(4-аміно-3-(4-фтор-3-гідроксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3феніл-4H-хінолізин-4-ону; 2-(1-(4-аміно-3-(3-гідроксифеніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл-4Hхінолізин-4-ону; 2-(1-(4-аміно-5-(3-фтор-5-гідроксифеніл)-7H-піроло[2,3-d]піримідин-7-іл)етил)-7-фтор-3феніл-4H-хінолізин-4-ону; 2-(1-(4-аміно-3-(6-метоксипіридин-3-іл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3феніл-4H-хінолізин-4-ону; 2-(1-(4-аміно-3-(2-оксоіндолін-5-іл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3-феніл4H-хінолізин-4-ону; (S)-2-(1-(4-аміно-3-(6-гідроксипіридин-3-іл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7-фтор-3феніл-4H-хінолізин-4-ону; N-(5-(4-аміно-1-(1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)-1H-піразоло[3,4d]піримідин-3-іл)-2-метоксипіридин-3-іл)метансульфонаміду; (S)-N-(5-(4-аміно-1-(1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)-1H-піразоло[3,4d]піримідин-3-іл)-2-гідроксипіридин-3-іл)метансульфонаміду та 2-(1-(4-аміно-3-(3-фтор-5-(гідроксиметил)феніл)-1H-піразоло[3,4-d]піримідин-1-іл)етил)-7фтор-3-феніл-4H-хінолізин-4-ону. Відповідно до ознаки даного винаходу сполуку загальної формули I, де всі символи визначені раніше, можна одержувати за допомогою способів, що наведені на схемах 1 і 2 та у прикладах. На даних схемах або у прикладах показані без обмеження ілюстративні процедури. 1 1a 2 4 Сполуки формули (I), де R являє собою –NH-R і R -R визначені у даному документі вище, можна одержувати за допомогою наступної процедури, яка зображена на схемі 1. 45 12 UA 115296 C2 5 10 15 Сполуку формули (2), що являє собою піридинкарбоксиальдегід, вводять у реакцію Віттіга з фосфатною сполукою (3) з одержанням сполуки формули (4), яку піддають циклізації за допомогою придатного реагенту, як наприклад, p-TSA, PPA, з одержанням сполуки формули (6), що являє собою хінолізин-4-он. Сполуку формули (4) можуть також піддавати гідролізу в основних умовах, як наприклад, в присутності NaOH, KOH тощо, з одержанням сполуки (5). Шляхом циклізації сполуки (5) за допомогою EDC.HCl/HOBt/NEt3 або HATU/DIPEA одержують сполуку (6), що являє собою хінолізин-4-он. Шляхом бромування хінолізин-4-ону (6) за допомогою NBS одержують сполуку (7), яку піддають реакції сполучення Сузукі з бороновою кислотою (8) з одержанням сполуки формули (9). Сполуку (9) вводять у реакцію з сульфінамідом з утворенням іміну, який піддають реакції відновлювального амінування за допомогою NaBH4 з наступним гідролізом за допомогою хлороводневої кислоти з одержанням сполуки формули (10). Сполуку (10) сполучають зі сполукою (11) з одержанням сполуки формули (I). 1 1a 2 4 Сполуки формули (I), де R не являє собою –NH-R і R -R визначені у даному документі вище, можна одержувати за допомогою наступної процедури, що зображена на схемі 2. 13 UA 115296 C2 5 10 15 20 25 30 Сполуку формули (9) піддають гідролізу в основних умовах, як наприклад, в присутності NaOH, KOH тощо, з одержанням сполуки (12). Сполуку формули (12) вводять у реакцію з CDI/NaBH4 з утворенням сполуки формули (13). Сполуку формули (9) піддають реакції відновлення з утворенням сполуки формули (14). Сполуку формули 13 або 14 вводять у реакцію з метансульфонілхлоридом з утворенням мезилату, який сполучають зі сполукою формули (15) в умовах нагрівання з одержанням сполуки формули (I). Альтернативно, сполуку формули 14 вводять у реакцію з PPh3/DIAD і сполукою (16) в умовах нагрівання з одержанням сполуки формули (17), яку піддають реакції сполучення Сузукі зі сполукою формули (18) з одержанням сполуки формули (I). Проміжні сполуки та сполуки згідно з даним винаходом можна одержувати в чистій формі за допомогою будь-якого способу, відомим per se, наприклад, шляхом відгону розчинника у вакуумі та/або шляхом повторної кристалізації залишку, одержаного з придатного розчинника, як наприклад, пентан, діетиловий етер, ізопропіловий етер, хлороформ, дихлорметан, етилацетат, ацетон або їх комбінації, або шляхом піддавання її одному зі способів очищення, як наприклад, колонкова хроматографія (наприклад, флеш-хроматографія) на придатному матеріалі-основі, як наприклад, оксид алюмінію або силікагель, із застосуванням елюента, як наприклад, дихлорметан, етилацетат, гексан, метанол, ацетон і їх комбінації. Можна також застосовувати спосіб препаративної LC-MS для очищення молекул, що описані у даному документі. Якщо не зазначено інше, дослідження включає розподілення реакційної суміші між органічною і водною фазами, що вказані в дужках, розділення шарів і висушування органічного шару над сульфатом натрію, фільтрування і випарювання розчинника. Очищення, якщо не зазначено інше, включає очищення за допомогою хроматографічних методик із застосуванням силікагелю, використовуючи, в основному, рухому фазу з придатною полярністю. Солі сполуки формули I можна одержувати шляхом розчинення сполуки у придатному розчиннику, наприклад, у хлорованому вуглеводні, як наприклад, метилхлорид або хлороформ, або в низькомолекулярному аліфатичному спирті, наприклад, етанолі або ізопропанолі, який потім обробляють необхідною кислотою або основою, як описано в Berge S.M. et al., “Pharmaceutical Salts, a review article in Journal of Pharmaceutical sciences volume 66, page 1-19 (1977)” і в “Handbook of Pharmaceutical Salts - Properties, Selection, and Use,” P. H. Einrich 14 UA 115296 C2 5 10 15 20 25 30 35 40 45 50 55 60 Stahland Camille G.wermuth, Wiley- VCH (2002). Списки придатних солей також можна знайти в Remington’s Pharmaceutical Sciences, 18th ed., Mack Publishing Company, Easton, PA, 1990, p. 1445, і Journal of Pharmaceutical Science, 66, 2-19 (1977). Наприклад, це може бути сіль лужного металу (наприклад, натрієва або калієва), лужноземельного металу (наприклад, кальцієва) або сіль амонію. Сполуки згідно з даним винаходом або композицію на їх основі потенційно можна вводити у вигляді фармацевтично прийнятної солі приєднання кислоти, нейтралізованої основою солі або солі приєднання основи, що утворюються за допомогою реакції з неорганічними кислотами, як наприклад, хлороводнева кислота, бромоводнева кислота, перхлоратна кислота, азотна кислота, тіоціанатна кислота, сірчана кислота і фосфорна кислота, та органічними кислотами, як наприклад, мурашина кислота, оцтова кислота, пропіонова кислота, гліколева кислота, молочна кислота, піровиноградна кислота, щавлева кислота, малонова кислота, бурштинова кислота, малеїнова кислота і фумарова кислота, або шляхом реакції з неорганічною основою, як наприклад, гідроксид натрію, гідроксид калію. Перетворення у сіль досягають за допомогою обробки основної сполуки щонайменше стехіометричною кількістю відповідної кислоти. Як правило, вільну основу розчиняють в інертному органічному розчиннику, як наприклад, діетиловий етер, етилацетат, хлороформ, етанол, метанол тощо, а кислоту додають у подібний розчинник. Суміш підтримують за придатної температури (наприклад, від 0C до 50C). Одержана в результаті сіль осаджується самовільно або може бути виділена з розчину за допомогою менш полярного розчинника. Стереоізомери сполук формули I згідно з даним винаходом можуть бути одержані шляхом стереоспецифічного синтезу або розділення рацемічної сполуки з використанням оптично активного аміну, кислоти або засобу, що утворює комплекс, і відділення діастереомерної солі/комплексу шляхом фракційної кристалізації або колонкової хроматографії. Сполуки формули I згідно з даним винаходом можуть існувати в таутомерних формах, як наприклад, кето-енольні таутомери. Такі таутомерні форми розглядають як аспект даного винаходу, і такі таутомери можуть знаходитись у рівновазі або можуть переважно знаходитись в одній із форм. Таким чином, у даному винаході додатково передбачена фармацевтична композиція, що містить сполуки загальної формули (I), як визначено вище, їхню таутомерну форму, їхній стереоізомер або їхню фармацевтично прийнятну сіль і фармацевтично прийнятний носій. Таким чином, у даному винаході додатково передбачена фармацевтична композиція, що містить сполуки загальної формули (I), як визначено вище, їхні таутомерні форми, їхні стереоізомери та їхні фармацевтично прийнятні солі в комбінації з загальноприйнятими фармацевтично прийнятними носіями, розріджувачами, допоміжними засобами тощо. Фармацевтично прийнятний носій або допоміжний засіб переважно є хімічно інертним по відношенню до сполуки згідно з даним винаходом і не має шкідливих побічних ефектів або токсичності в умовах застосування. Такі фармацевтично прийнятні носії або допоміжні засоби ® включають фізіологічний розчин (наприклад, 0,9% фізіологічний розчин), Cremophor EL (який являє собою похідне рицинової олії і етиленоксиду, що постачається Sigma Chemical Co., СентЛуїс, Міссурі) (наприклад, 5% Cremophor EL/5% етанолу/90% фізіологічного розчину, 10% Cremophor EL/90% фізіологічного розчину або 50% Cremophor EL/50% етанолу), пропіленгліколь (наприклад, 40% пропіленгліколю/10% етанолу/50% води), поліетиленгліколь (наприклад, 40% PEG 400/60% фізіологічного розчину) і спирт (наприклад, 40% етанолу/60% води). Переважним фармацевтичним носієм є поліетиленгліколь, як наприклад, PEG 400, і конкретно композиція, що містить 40% PEG 400 і 60% води або фізіологічного розчину. Вибір носія буде частково визначатися конкретною обраною сполукою, а також конкретним способом, що використовується для введення композиції. Відповідно, існує широкий спектр придатних складів фармацевтичної композиції згідно з даним винаходом. Наступні склади для перорального, аерозольного, парентерального, підшкірного, внутрішньовенного, внутрішньоартеріального, внутрішьном’язового, інтратекального, інтраперитонеального, ректального і вагінального введення є винятково ілюстративними, а не обмежувальними. Фармацевтичні композиції можна вводити парентерально, наприклад, внутрішньовенно, внутрішньоартеріально, підшкірно, внутрішьношкірно, інтратекально або внутрішньом’язово. Таким чином, у даному винаході передбачені композиції для парентерального введення, які містять розчин сполуки згідно з даним винаходом, розчиненої або суспендованої у прийнятному носії, що є придатним для парентерального введення, у тому числі водні та неводні,ізотонічні стерильні ін'єкційні розчини. Загалом вимоги до ефективних фармацевтичних носіїв для парентеральних композицій 15 UA 115296 C2 5 10 15 20 25 30 35 40 45 50 55 60 добре відомі звичайним фахівцям у даній галузі. Див. Pharmaceutics and Pharmacy Practice, J. B. Lippincott Company, Philadelphia, PA, Banker and Chalmers, eds., pages 238-250 (1982), і ASHP Handbook on Injectable Drugs, Toissel, 4th ed., pages 622-630 (1986). Такі композиції включають розчини, що містять антиоксиданти, буфери, бактеріостатичні засоби та розчинні речовини, що приводять склад в ізотонічний стан з кров’ю очікуваного реципієнту, а також водні та неводні стерильні суспензії, які можуть включати суспендувальні засоби, солюбілізатори, згущувачі, стабілізатори і консерванти. Сполуку можна вводити у фізіологічно прийнятному розріджувачі у фармацевтичному носії, як наприклад, стерильна рідина або суміш рідин, що включають воду, фізіологічний розчин, водні розчини декстрози і споріднених цукрів, спирт, як наприклад, етанол, ізопропанол (наприклад, при місцевих застосуваннях) або гексадециловий спирт, гліколі, як наприклад, пропіленгліколь або поліетиленгліколь, диметилсульфоксид, кеталі гліцерину, як наприклад, 2,2-диметил-1,3-діоксолан-4-метанол, етери, як наприклад, полі(етиленгліколь) 400, масло, жирну кислоту, естер жирної кислоти, або гліцерид, або ацетильований гліцерид жирної кислоти, з додаванням або без додавання фармацевтично прийнятної поверхнево-активної речовини, як наприклад, мило або детергент, суспендувальний засіб, як наприклад, пектин, карбомери, метилцелюлоза, гідроксипропілметилцелюлоза або карбоксиметилцелюлоза, або емульгувальні засоби і інші фармацевтичні допоміжні речовини. Масла, що застосовуються у складах для парентерального введення, включають нафтове, масла тваринного походження, рослинне масло та синтетичні масла. Конкретні приклади масел, що застосовуються у таких складах, включають арахісове, соєве, кунжутне, бавовняне, кукурудзяне, оливкове, вазелінове та мінеральне масло. Придатні для застосування у складах для парентерального введення жирні кислоти включають олеїнову кислоту, стеаринову кислоту та ізостеаринову кислоту. Етилолеат та ізопропілміристат є прикладами придатних естерів жирних кислот. Придатні мила для застосування у складах для парентерального введення включають солі жирних кислот і лужних металів, амонієві та триетаноламінові солі, та придатні детергенти включають (a) катіонні детергенти, такі як наприклад, галогеніди диметилдіалкіламонію і галогеніди алкілпіридинію, (b) аніонні детергенти, такі як, наприклад, алкіл-, арил- і олефінсульфонати, алкіл-, олефін- і моногліцеридсульфат, сульфати етерів і сульфосукцинати, (с) неіонні детергенти, такі як наприклад, оксиди амінів жирного ряду, алканоламіди жирних кислот і співполімери поліоксиетилену і поліпропілену, (d) амфотерні детергенти, такі як наприклад, алкіл-β-амінопропіонати і четвертинні амонієві солі 2-алкіл-імідазоліну, а також (e) їх суміші. Склади для парентерального введення будуть, як правило, містити від приблизно 0,5% або менше до приблизно 25% або більше за вагою сполуки згідно з даним винаходом у розчині. Можна використовувати консерванти і буфери. Для мінімізації або усунення подразнення у місці ін’єкції такі композиції можуть містити один або більше неіонних поверхнево-активних речовин із гідрофільно-ліпофільним балансом (HLB) від приблизно 12 до приблизно 17. Кількість поверхнево-активної речовини в таких складах буде, як правило, знаходитись у діапазоні від приблизно 5% до приблизно 15% за вагою. Придатні поверхнево-активні речовини включають естери поліетиленсорбітану і жирної кислоти, як наприклад, сорбітанмоноолеат, і високомолекулярні продукти приєднання етиленоксиду до гідрофобної основи, що утворені шляхом конденсації пропіленоксиду з пропіленгліколем. Склади для парентерального введення можуть бути представлені в однодозових або багатодозових герметизованих контейнерах, як наприклад, ампули і флакони, і можуть зберігатись у висушеному за допомогою заморожування (ліофілізованому) стані, що потребує лише додавання стерильного рідкого допоміжного засобу, наприклад, води, для ін’єкцій, безпосередньо перед застосуванням. Приготовлені для негайного прийому ін’єкційні розчини і суспензії можна одержувати з стерильних порошків, гранул і таблеток. Склади для місцевого застосування, у том числі такі, що застосовуються для трансдермального вивільнення лікарського засобу, добре відомі фахівцям у даній галузі та в контексті даного винаходу є придатними для нанесення на шкіру. Придатні для перорального введення склади можуть складатись із (a) рідких розчинів, як наприклад, із ефективної кількості сполуки згідно з даним винаходом, розчиненої у розріджувачах, як наприклад, вода, фізіологічний розчин або апельсиновий сік; (b) капсул, саше, таблеток, льодяників і троше, при цьому в кожному міститься попередньо визначена кількість сполуки згідно з даним винаходом у вигляді твердих речовин або гранул; (c) порошків; (d) суспензій у відповідній рідині та (e) придатних емульсій. Рідкі склади можуть включати розріджувачі, як наприклад, воду і спирти, наприклад, етанол, бензиловий спирт і поліетиленові спирти, або з додаванням, або без додавання фармацевтично прийнятних поверхнево-активної 16 UA 115296 C2 5 10 15 20 25 30 35 40 45 50 55 60 речовини, суспендувального засобу або емульгувального засобу. Форми у вигляді капсул можуть знаходитись у стандартній желатиновій оболонці твердого або м’якого типу і при цьому містити, наприклад, поверхнево-активні речовини, змащувальні речовини та інертні наповнювачі, як наприклад, лактоза, сахароза, фосфат кальцію і кукурудзяний крохмаль. Таблетовані форми можуть включати одне або більше з лактози, сахарози, маніту, кукурудзяного крохмалю, картопляного крохмалю, альгінової кислоти, мікрокристалічної целюлози, камеді, желатину, гуарової камеді, колоїдного діоксиду кремнію, кроскармелози натрію, тальку, стеарату магнію, стеарату кальцію, стеарату цинку, стеаринової кислоти та інших допоміжних засобів, барвників, розріджувачів, буферних засобів, розпушувачів, зволожувальних засобів, консервантів, ароматизуючих засобів і сумісних у фармакологічному сенсі допоміжних засобів. Форми у вигляді льодяників можуть включати інгредієнт-сполуку зі смаком, як правило, сахарозу і камедь або трагакант, а також пастилки, що містять сполуку згідно з даним винаходом в інертній основі, як наприклад, желатин і гліцерин або сахароза і камедь, емульсії, гелі тощо, що містять окрім сполуки згідно з даним винаходом допоміжні засоби, які відомі з рівня техніки. Сполука згідно з даним винаходом окремо або в комбінації з іншими придатними компонентами може бути складена в аерозольні склади, що підлягають введенню шляхом інгаляції. Сполука або епімер згідно з даним винаходом переважно поставляється у тонкодисперсній формі разом з поверхнево-активною речовиною і пропелентом. Типові відсоткові вмісти сполук згідно з даним винаходом можуть складати від приблизно 0,01% до приблизно 20% за вагою, переважно від приблизно 1% до приблизно 10% за вагою. Відомо, що поверхнево-активна речовина повинна бути нетоксичною і переважно розчинною у пропеленті. Прикладами таких поверхнево-активних речовин є естери або неповні естери жирних кислот, що містять від 6 до 22 атомів вуглецю, як наприклад, капронова, октанова, лауринова, пальмітинова, стеаринова, лінолева, ліноленова, олестерова і олеїнова кислоти, з аліфатичним багатоатомним спиртом або його циклічним ангідридом. Можна використовувати змішані естери, як наприклад, змішані або природні гліцериди. Поверхнево-активна речовина може складати від приблизно 0,1% до приблизно 20% за вагою композиції, переважно від приблизно 0,25% до приблизно 5%. Композиція врівноважується стандартним пропелентом. За необхідності можна також включати носій, наприклад, лецитин, для інтраназальної доставки. Дані аерозольні склади можна помістити в прийнятні пропеленти, що знаходяться під тиском, як наприклад, дихлордифторметан, пропан, азот тощо. Вони також можуть бути складені у вигляді лікарських форм для препаратів, які не знаходяться під тиском, як наприклад, в аерозольному інгаляторі або розпилювачі. Такі склади для розпилювання можна використовувати для розпилення на слизову оболонку. Крім того, сполуки згідно з даним винаходом можуть бути складені в супозиторії шляхом змішування з рядом основ, як наприклад, емульгувальні основи або водорозчинні основи. Склади, які є придатними для вагінального введення, можуть бути представлені у вигляді песаріїв, тампонів, кремів, гелів, паст, пінок або складів для розпилення, що містять окрім інгредієнта-сполуки відповідні носії, які відомі з рівня техніки. Концентрація сполуки у фармацевтичних складах може знаходитись у діапазоні, наприклад, від менше приблизно 1% до приблизно 10%, від приблизно не менше 20% до приблизно 50% або більше за вагою і може бути переважно вибрана в залежності від об’ємів рідин та їхніх в’язкостей відповідно до вибраного конкретного шляху введення. Наприклад, типова фармацевтична композиція для внутрішньовенної інфузії може бути складена таким чином, щоб містити 250 мл стерильного розчину Рінгера і 100 мг щонайменше однієї сполуки згідно з даним винаходом. Сучасні способи одержання сполук згідно з даним винаходом для парентерального введення будуть відомі або очевидні для фахівців у даній th галузі і детально описані, наприклад, в Remington’s Pharmaceutical Science (17 ed., Mack Publishing Company, Easton, PA, 1985). Звичайному фахівцю у даній галузі буде зрозуміло, що крім описаних вище фармацевтичних композицій сполука згідно з даним винаходом може бути складеною у вигляді комплексів включення, як наприклад, комплекси включення на основі циклодекстрину, або у вигляді ліпосом. Ліпосоми можуть призначатися для цілеспрямованої дії сполуки згідно з даним винаходом на конкретну тканину, як наприклад, лімфоїдна тканина або ракові клітини печінки. Також ліпосоми можна використовувати для збільшення періоду напіввиведення сполуки згідно з даним винаходом. Безліч способів одержання ліпосом є доступними , як описано, наприклад, в Szoka et al., Ann. Rev. Biophys. Bioeng., 9, 467 (1980) і патентах США №№ 4235871, 4501728, 4837028 і 5019369. Сполуки згідно з даним винаходом можна вводити у дозі, що є достатньою для лікування 17 UA 115296 C2 5 10 15 20 25 30 35 40 45 50 55 60 захворювання, стану або розладу. Такі дози відомі з рівня техніки (см., наприклад, в Physicians’ Desk Reference (2004)). Сполуки також можна вводити з застосуванням методик, як такі, що описані, наприклад, в Wasserman et al., Cancer, 36, pp. 1258-1268 (1975) і Physicians’ Desk Reference, 58th ed., Thomson PDR (2004). Придатні дози та схеми дозування можна визначити за допомогою загальноприйнятих методик визначення діапазону терапевтичних доз, які відомі звичайному фахівцю у даній галузі. Як правило, лікування починають із менших дозувань, які менше оптимальної дози сполуки згідно з даним винаходом. Потім дозування підвищують шляхом невеликих додавань до досягнення оптимального ефекту за даних обстав. У способі згідно з даним винаходом може передбачатися введення від приблизно 0,1 мкг до приблизно 50 мг щонайменше однієї сполуки згідно з даним винаходом на кг ваги тіла індивідууму. Для пацієнта вагою 70 кг зазвичай будуть використовувати дозування від приблизно 10 мкг до приблизно 200 мг сполуки згідно з даним винаходом в залежності від фізіологічної реакції пацієнта. Як приклад і не обмежуючи даний винахід, доза фармацевтично активного(активних) засобу(засобів), який(які) описаний(описані) у даному документі для способів лікування або попередження захворювання або стану, що описані вище, може складати від приблизно 0,001 до приблизно 1 мг/кг ваги тіла суб’єкта на добу, наприклад, приблизно 0,001 мг, 0,002 мг, 0,005 мг, 0,010 мг, 0,015 мг, 0,020 мг, 0,025 мг, 0,050 мг, 0,075 мг, 0,1 мг, 0,15 мг, 0,2 мг, 0,25 мг, 0,5 мг, 0,75 мг або 1 мг/кг ваги тіла на добу. Доза фармацевтично активного(активних) засобу(засобів), який(які) описаний(описані) у даному документі для описаних способів, може складати від приблизно 1 до приблизно 1000 мг/кг ваги тіла суб’єкта, що підлягає лікуванню, на добу, наприклад, приблизно 1 мг, 2 мг, 5 мг, 10 мг, 15 мг, 0,020 мг, 25 мг, 50 мг, 75 мг, 100 мг, 150 мг, 200 мг, 250 мг, 500 мг, 750 мг або 1000 мг/кг ваги тіла на добу. Іншим аспектом даного винаходу є забезпечення способу лікування або попередження розладу, який є чутливим до інгібування активності PI3K, у ссавця, що страждає від нього, який включає введення ссавцю, що має потребу в такому лікуванні, терапевтично ефективної кількості сполуки формули I. Іншим аспектом даного винаходу є забезпечення способу лікування або попередження розладу, який є чутливим до інгібування активності PI3K, у ссавця, що страждає від нього, який включає введення ссавцю, що має потребу в такому лікуванні, терапевтично ефективної кількості сполуки формули I, її таутомерної форми, її стереоізомеру або її фармацевтично прийнятної солі. Сполука формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль для застосування у лікуванні або попередженні розладу, який є чутливим до інгібування активності PI3K, у ссавця, що страждає від нього. Сполука формули (I), її таутомерна форма, її стереоізомер або її фармацевтично прийнятна сіль для застосування в лікуванні або попередженні розладу, який є чутливим до інгібування активності PI3K, у ссавця, що страждає від нього, де вказаний розлад являє собою рак, розлади, пов'язані з запаленнями, або аутоімунні розлади. Інгібітори PI3K, що представлені у даному документі, можуть бути використані для лікування захворювань і/або розладів, які включають без обмеження рак, розлади, пов'язані з запаленнями, або аутоімунні розлади. Інгібітори PI3K, що згадуються у даному документі, можуть бути використані як окремі засоби і/або в комбінації з іншими хіміотерапевтичними засобами. Види раку, які можна лікувати і/або попереджати за допомогою інгібіторів PI3K, включають без обмеження гострий мієлолейкоз, рак тимусу, головного мозку, легень, плоскоклітинний рак, рак шкіри, ока, ретинобластому, інтраокулярну меланому, рак ротової порожнини і ротоглотки, сечового міхура, шлунково-кишкового тракту, шлунку, підшлункової залози, сечового міхура, молочної залози, шийки матки, голови, шиї, ренальний рак, рак нирки, печінки, яєчників, передміхурової залози, колоректальний рак, рак стравоходу, яєчка, гінекологічний рак, рак щитовидної залози, CNS, PNS, СНІД-асоційований рак (наприклад, лімфому і саркому Капоші) або рак, викликаний вірусами. У деяких варіантах здійснення вказаний спосіб відноситься до лікування гіперпроліферативного порушення, що не є злоякісним, як наприклад, доброякісна гіперплазія шкіри (наприклад, псоріаз), рестеноз або порушення, пов’язане з передміхуровою залозою (наприклад, доброякісна гіпертрофія передміхурової залози (BPH)). У деяких варіантах здійснення у даному розкритті передбачений спосіб лікування гіперпроліферативного розладу у суб’єкта, який включає введення вказаному суб’єкту терапевтично ефективної кількості сполуки або її фармацевтично прийнятної форми (наприклад, фармацевтично прийнятних солей, гідратів, сольватів, ізомерів, проліків та ізотопно мічених похідних) або фармацевтичних композицій, що передбачені у даному документі. У 18 UA 115296 C2 5 10 15 20 25 30 35 40 45 50 55 60 деяких варіантах здійснення вказаний спосіб відноситься до лікування раку, як наприклад, гострий мієлолейкоз, рак тимусу, головного мозку, легень, плоскоклітинний рак, рак шкіри, ока, ретинобластома, інтраокулярна меланома, рак ротової порожнини і ротоглотки, сечового міхура, шлунково-кишкового тракту, шлунку, підшлункової залози, сечового міхура, молочної залози, шийки матки, голови, шиї, ренальний рак, рак нирки, печінки, яєчників, передміхурової залози, колоректальний рак, рак стравоходу, яєчка, гінекологічний рак, рак щитовидної залози, CNS, PNS, СНІД-асоційований рак (наприклад, лімфому і саркому Капоші) або рак, що викликаний вірусами. У деяких варіантах здійснення вказаний спосіб відноситься до лікування гіперпроліферативного розладу, що відрізняється від раку, як наприклад, доброякісна гіперплазія шкіри (наприклад, псоріаз), рестеноз або розлад, який пов’язаний з передміхуровою залозою (наприклад, доброякісна гіпертрофія передміхурової залози (BPH)). Пацієнти, яких можна лікувати за допомогою сполук або їхньої фармацевтично прийнятної форми (наприклад, за допомогою фармацевтично прийнятних солей, гідратів, сольватів, ізомерів, проліків та ізотопно мічених похідних) або за допомогою фармацевтичних композицій, що передбачені в даному документі, згідно зі способами, які передбачені в даному документі, включають, наприклад, без обмеження пацієнтів, у яких діагностували наступні захворювання: псоріаз; рестеноз; атеросклероз; BPH; рак молочної залози, як наприклад, внутрішньопротокова карцинома у тканині протоків в молочній залозі, медулярні карциноми, колоїдні карциноми, тубулярні карциноми та рак молочної залози, що пов’язаний із запаленнями; рак яєчників, у тому числі епітеліальні пухлини яєчників, як наприклад, аденокарцинома в яєчнику і аденокарцинома, яка поширилась від яєчника в черевну порожнину; рак матки; рак шийки матки, як наприклад, аденокарцинома в епітелії шийки матки, у тому числі плоскоклітинна карцинома і аденокарциноми; рак передміхурової залози, як наприклад, рак передміхурової залози, що вибраний із наступного: аденокарцинома або аденокарцинома, яка поширилась до кістки; рак підшлункової, як наприклад, епітеліоїдна карцинома у тканині протоки підшлункової залози і аденокарцинома в протоці підшлункової залози; рак сечового міхура, як наприклад, перехідно-клітинна карцинома в сечовому міхурі, уротеліальні карциноми (перехідно-клітинні карциноми), пухлини в уротеліальних клітинах, які вистилають сечовий міхур, плоскоклітинні карциноми, аденокарциноми, і види дрібноклітинного раку; лейкоз, як наприклад, гострий мієлолейкоз (AML), гострий лімфоцитарний лейкоз, хронічний лімфоцитарний лейкоз, хронічний мієлолейкоз, волосатоклітинний лейкоз, мієлодисплазія, мієлопроліферативні розлади, NKклітинний лейкоз (наприклад, новоутворення з бластних плазмоцитоїдних дендритних клітин), гострий мієлогенний лейкоз (AML), хронічний мієлогенний лейкоз (CML), мастоцитоз, хронічний лімфоцитарний лейкоз (CLL), множинна мієлома (MM) і синдром мієлодисплазії (MDS); рак кісток; рак легень, як наприклад, недрібноклітинний рак легень (NSCLC), який поділяється на плоскоклітинні карциноми, аденокарциноми і великоклітинні недиференційовані карциноми, і дрібноклітинний рак легень; рак шкіри, як наприклад, базальноклітинна карцинома, меланома, плоскоклітинна карцинома і актинічний кератоз, що являє собою стан шкіри, який іноді розвивається у плоскоклітинну карциному; ретинобластома ока; меланома шкіри або інтраокулярна меланома (меланома ока) ; первинний рак печінки (рак, який починається у печінці); рак нирки; рак щитовидної залози, як наприклад, папілярний, фолікулярний, медулярний і анапластичний; лімфома, як наприклад, дифузна великоклітинна В-клітинна лімфома, B-клітинна імунобластна лімфома, NK-клітинна лімфома (наприклад, новоутворення з бластних плазмоцитоїдних дендритних клітин) і дрібноклітинна лімфома з нерозсіченими ядрами; саркома Капоші; види раку, що викликаються вірусами, у тому числі рак, який викликається вірусом гепатиту B (HBV), вірусом гепатиту C (HCV), і гепатоклітинна карцинома; лейкоз/лімфома, що викликається лімфотропним вірусом 1 типу людини (HTLV-1), і T-клітинний лейкоз/лімфома дорослих; і рак, який викликається папіломавірусом людини (HPV), і рак шийки матки; види раку центральної нервової системи (CNS), як наприклад, первинна пухлина головного мозку, яка включає гліоми (астроцитому, анапластичну астроцитому або мультиформну гліобластому), олігодендрогліому, епендимому, менінгіому, лімфому, шваному і медулобластому; види раку периферичної нервової системи (PNS), як наприклад, нейроми слухового нерву і злоякісна пухлина оболонок периферичних нервів (MPNST), у тому числі нейрофіброми і шваноми, злоякісна фіброцитома, злоякісна фіброзна гістіоцитоксантома, злоякісна менінгіома, злоякісна мезотеліома і злоякісна змішана пухлина Мюлера; рак ротової порожнини і ротоглотки, як наприклад, гіпофарингіальний рак, рак гортані, рак носоглотки і рак ротоглотки; рак шлунку, як наприклад, лімфоми, стромальні пухлини шлунково-кишкового тракту і карциноїдні пухлини; рак яєчка, як наприклад, ембріонально-клітинні пухлини (GCT), які включають семіноми і несеміомні пухлини і стромальні пухлини статевої залози, що включають пухлини з клітин Лейдіга і пухлини з клітин Сертолі; рак тимусу, як наприклад, тимоми, 19 UA 115296 C2 5 10 15 20 25 30 35 40 45 50 55 60 карциноми тимусу, хворобу Ходжкіна, карциноїди неходжкінської лімфоми або карциноїдні пухлини; ректальний рак і рак товстої кишки. Ілюстративні стани, що пов'язані з запаленнями, включають без обмеження запалення, пов’язане з акне, анемію (наприклад, апластичну анемію, гемолітичну аутоімунну анемію), астму, артеріїт (наприклад, поліартеріїт, артеріїт скроневих артерій, вузликовий периартериїт, синдром Такаясу), артрит (наприклад, кристалічний артрит, остеоартрит, псоріатичний артрит, загострення подагри, подагричний артрит, реактивний артрит, ревматоїдний артрит і артрит Рейтера), анкілозуючий спондиліт, амілоз, бічний аміотрофічний склероз, аутоімунні захворювання, алергії або алергічні реакції, атеросклероз, бронхіт, бурсит, хронічний простатит, кон’юнктивіт, хвороба Шагаса, хронічне обструктивне захворювання легень, дерматоміозит, дивертикуліт, діабет (наприклад, цукровий діабет I типу, цукровий діабет 2 типу), стан шкіри (наприклад, псоріаз, екзему, опіки, дерматит, свербіж (коросту)), ендометріоз, синдром ГієнаБарре, інфекцію, ішемічну хворобу серця, хворобу Кавасакі, гломерулонефрит, гінгівіт, гіперстезію, головні болі (наприклад, головні болі, що являють собою мігрень, головні болі напруги), непрохідність кишківника (наприклад, післяопераційну непрохідність кишківника і непрохідність кишківника під час сепсису), ідіопатичну тромбоцитопенічну пурпуру, інтерстиціальний цистит (больовий синдром сечового міхура), розлад шлунково-кишкового тракту (наприклад, вибраний із пептичних виразок, регіонарного ентериту, дивертикуліту, шлунково-кишкової кровотечі, еозинофільних розладів шлунково-кишкового тракту (наприклад, еозинофільного езофагіту, еозинофільного гастриту, еозинофільного гастроентериту, еозинофільного коліту), гастриту, діареї, гастроезофагеальної рефлюксної хвороби (GORD або її синдрому GERD), запального захворювання кишківника (IBD) (наприклад, хвороби Крона, виразкового коліту, колагенозного коліту, лімфоцитарного коліту, ішемічного коліту, коліту відключеної кишки, синдрому Бехчета, недиференційованого коліту) і синдрому подразненого кишківника (IBS)), вовчак, множинний склероз, кільцеподібну склеродермію, тяжку міастенію, ішемію міокарду, нефротичний синдром, звичайну пухирчатку, перніціозну анемію, пептичні виразки, поліміозит, первинний біліарний цироз, нейрозапалення, що пов’язане з розладами мозкової активності (наприклад, хвороба Паркінсона, хвороба Хантінгтона і хвороба Альцгеймера), простатит, хронічне запалення, яке пов’язане з радіаційним ураженням черепу, запалювальне захворювання тазових органів, ревматичну поліміалгію, реперфузійне ураження, регіонарний ентерит, ревматичну лихоманку, системний червоний вовчак, склеродермію, склеродому, саркоїдоз, спондилоартропатії, синдром Шегрена, тиреоїдит, відторгнення при трансплантації, тендиніт, травму або пошкодження (наприклад, обмороження, що викликане хімічними подразниками, токсинами, рубцювання, опіки, фізичне пошкодження), васкуліт, вітиліго і гранулематоз Вегенера. У конкретних варіантах здійснення розлад, пов'язаний з запаленнями, вибраний із артриту (наприклад, ревматоїдного артриту), запального захворювання кишківника, синдрому подразненого кишківника, астми, псоріазу, ендометріозу, інтерстиціального циститу і простатиту. У конкретних варіантах здійснення стан, пов'язаний з запаленнями, являє собою гострий стан, пов'язаний з запаленнями (як наприклад, запалення в результаті інфекції). У конкретних варіантах здійснення стан, пов'язаний з запаленнями, являє собою хронічний стан, пов'язаний з запаленнями (наприклад, стан в результаті астми, артриту і запального захворювання кишківника). Сполуки можуть також бути застосовані в лікуванні запалення, пов'язаного з травмою та незапальною міалгією. Імунні розлади, як наприклад, аутоімунні розлади, включають без обмеження артрит (у тому числі ревматоїдний артрит, спондилоартропатії, подагричний артрит, дегенеративні захворювання суглобів, як наприклад, остеоартрит, системний червоний вовчак, синдром Шегрена, анкілозуючий спондиліт, недиференційований спондиліт, синдром Бехчета, гемолітичні аутоімунні анемії, множинний склероз, бічний аміотрофічний склероз, амілоз, гострий плечокистьовий синдром, псоріатичний і ювенільний артрит), астму, атеросклероз, остеопороз, бронхіт, тендиніт, бурсит, стан шкіри (наприклад, псоріаз, екзему, опіки, дерматит, свербіж (коросту)), енурез, еозинофільне захворювання, розлад шлунково-кишкового тракту (наприклад, вибраний із пептичних виразок, регіонарного ентериту, дивертикуліту, шлунковокишкової кровотечі, еозинофільних розладів шлунково-кишкового тракту (наприклад, еозинофільного езофагіту, еозинофільного гастриту, еозинофільного гастроентериту, еозинофільного коліту), гастриту, діареї, гастроезофагеальної рефлюксної хвороби (GORD або її синдрому GERD), запального захворювання кишківника (IBD) (наприклад, хвороби Крона, виразкового коліту, колагенозного коліту, лімфоцитарного коліту, ішемічного коліту, коліту відключеної кишки, синдрому Бехчета, недиференційованого коліту) і синдрому подразненого кишківника (IBS)), рецидивуючий поліхондрит (наприклад, атрофічний поліхондрит і системну поліхондромаляцію), і розлади, що викликані підвищенням гастропрокінетичного засобу 20 UA 115296 C2 5 10 15 20 25 30 35 40 45 50 55 60 (наприклад, непрохідність кишківника, післяопераційна непрохідність кишківника і непрохідність кишківника під час сепсису; гастроезофагеальну рефлюксну хворобу (GORD або її синдром GERD); еозинофільний езофагіт, гастропарез, як наприклад, гастропарез при діабеті; непереносимості харчових продуктів і харчові алергії та інші функціональні розлади кишківника, як наприклад, невиразкова диспепсія (NUD) і біль у грудях несерцевого походження (NCCP, у тому числі запалення реберних хрящів)). У конкретних варіантах здійснення передбачений спосіб лікування запальних або аутоімунних захворювань, що включає введення суб'єкту (наприклад, ссавцю) терапевтично ефективної кількості сполуки або її фармацевтично прийнятної форми (наприклад, фармацевтично прийнятних солей, гідратів, сольватів, ізомерів, проліків і ізотопно мічених похідних) або фармацевтичних композицій, що передбачені у даному документі. Іншим аспектом даного винаходу є забезпечення сполуки формули (I), її таутомерної форми, її стереоізомеру або її фармацевтично прийнятної солі для застосування у лікуванні або попередженні розладу, який є чутливим до інгібування активності PI3K і PI3K, у ссавця, що страждає від нього. Додатковим аспектом даного винаходу є забезпечення сполуки формули (I), її таутомерної форми, її стереоізомеру або її фармацевтично прийнятної солі для застосування у лікуванні або попередженні розладу, який є чутливим до інгібування активності PI3K і PI3K, у ссавця, що страждає від нього, де вказаний розлад являє собою рак, розлади, пов'язані з запаленнями, або аутоімунні розлади. Ще одним аспектом даного винаходу є забезпечення сполуки формули (I), її таутомерної форми, її стереоізомера або її фармацевтично прийнятної солі для застосування у лікуванні або попередженні розладу, який є чутливим до інгібування активності PI3K, у ссавця, що страждає від нього. Додатковим аспектом даного винаходу є забезпечення сполуки формули (I), її таутомерної форми, її стереоізомеру або її фармацевтично прийнятної солі для застосування у лікуванні або попередженні розладу, який є чутливим до інгібування активності PI3K, у ссавця, що страждає від нього, де вказаний розлад являє собою рак, розлади, пов'язані з запаленнями, або аутоімунні розлади. Використовувані у даному документі терміни «лікувати», «попереджувати», «зменшувати інтенсивність» і «інгібувати», а також споріднені до них слова необов'язково на 100% означають або мають на увазі лікування, попередження, зменшення інтенсивності або інгібування. Точніше, існують різні ступені лікування, попередження, зменшення інтенсивності і інгібування, які відомі будь-якому звичайному фахівцю у даній галузі, як такі, що мають потенційну користь або терапевтичний ефект. У зв’язку з цим, розкриті способи можуть забезпечувати будь-яку ступінь будь-якого рівня лікування, попередження, зменшення інтенсивності або інгібування розладу у ссавця. Наприклад, розлад, у тому числі його симптоми або стани, можна зменшити, наприклад, на 100%, 90%, 80%, 70%, 60%, 50%, 40%, 30%, 20% або 10%. Крім того, лікування, попередження, зменшення інтенсивності або інгібування, що забезпечуються за допомогою способу згідно з даним винаходом, можуть включати лікування, попередження, зменшення інтенсивності або інгібування одного або більше станів або симптомів розладу, наприклад, раку. Крім того, для цілей, що передбачені у даному документі, «лікування», «попередження», «зменшення інтенсивності» або «інгібування» можуть охоплювати затримку прояву розладу або його симптому або стану. Терміни «ефективна кількість» або «терапевтично ефективна кількість», застосовувані у даному документі, відносяться до достатньої кількості засобу або сполуки, що підлягає введенню, яка буде послаблювати до певної міри один або більше симптомів захворювання або стану, що підлягає лікуванню. У деяких варіантах здійснення результатом є зниження та/або полегшення ознак, симптомів або причин захворювання або будь-яка інша бажана зміна біологічної системи. Наприклад, «ефективна кількість» для терапевтичних застосувань являє собою кількість композиції, що містить сполуку, які розкрита у даному документі, необхідну для забезпечення значного клінічно значущого зниження симптомів захворювання. У деяких варіантах здійснення відповідну «ефективну» кількість у будь-якому окремому випадку визначають із застосуванням методик, як наприклад, дослідження з підвищенням дози. Згідно з даним винаходом термін «суб'єкт» включає «тварину», яка, у свою чергу, передбачає ссавця, наприклад, без обмеження з ряду Rodentia, як наприклад, миші, і з ряду Lagomorpha, як наприклад, кролики. В одному аспекті ссавці відносяться до ряду Carnivora, у тому числі до Felines (кішки) і до Canines (собаки). В іншому аспекті ссавці відносяться до ряду Artiodactyla, у тому числі до Bovines (корови) і до Swine (свині), або до ряду Perssodactyla, у тому числі до Equines (коні). У додатковому аспекті ссавці відносяться до ряду Primates, Ceboids 21 UA 115296 C2 5 10 15 20 25 або Simoids (мавпи), або до ряду Anthropoids (люди і людиноподібні мавпи). У ще одному аспекті ссавець являє собою людину. Термін «пацієнт» охоплює ссавців і тварин, відмінних від ссавців. Приклади ссавців включають без обмеження будь-якого члена класу ссавців: людей, приматів, що не відносяться до людиноподібних, як наприклад, шимпанзе та інші людиноподібні мавпи, і видів мавп; сільськогосподарських тварин, як наприклад, велика рогата худоба, коні, вівці, кози, свині; домашні тварини, як наприклад, кролики, собаки і кішки; лабораторні тварини, у тому числі гризуни, як наприклад, щури, миші та морські свинки тощо. Приклади тварин, відмінних від ссавців, включають без обмеження птахів, риб тощо. В одному варіанті здійснення передбачених у даному документі способів і композицій ссавцем є людина. Іншим аспектом даного винаходу є забезпечення фармацевтичної композиції на основі сполуки формули I у комбінації щонайменше з одним іншим відомим протираковим засобом або фармацевтично прийнятною сіллю вказаного засобу. У тексті використані наступні скорочення: DMSO-d6: гексадейтеродиметилсульфоксид; DMF: N,N-диметилформамід, THF: тетрагідрофуран, J: константа взаємодії в одиницях Гц, HOBt: гідроксибензотриазол, pTsOH, p-TSA: п-толуолсульфонова кислота, NBS: N-бромсукцинімід, MeOH: метанол, EtOH: етанол, HCl: хлороводнева кислота, TEA: триетиламін, PPA: поліфосфорна кислота, CDI: 1,1'-карбонілдіімідазол, DIAD: діізопропілазодикарбоксилат, HATU: гексафторфосфат 1-[біс(диметіламіно)метилен]-1H-1,2,3-триазоло[4,5-b]піридиній-3-оксиду, DIPEA: N,N-діізопропілетиламін. У наступних прикладах додатково проілюстрований спосіб одержання сполук, що наведені у формулі I; однак, приклади не слід розглядати як такі, що обмежують будь-яким чином обсяг даного винаходу. Приклади Приклад 1. Одержання 2-(1-аміноетил)-3-феніл-4H-хінолізин-4-ону Стадія-1. Етил-4-оксо-3-(піридин-2-ілметилен)пентаноат 30 35 40 45 До перемішуваного розчину етил-3-(діетоксифосфорил)-4-оксопентаноату (14,39 г, 51,3 ммоль) і піколінальдегіду (5 г, 46,7 ммоль) у етанолі додавали етоксид натрію (4,76 г, 70,0 ммоль) при кімнатній температурі. Реакційну суміш перемішували при кімнатній температурі протягом 2 год., а потім нагрівали при 50°C протягом 1 год. Розчинник видаляли при зниженому тиску і одержаний в результаті залишок екстрагували за допомогою DCM (3 X 200 мл), об'єднаний органічний шар промивали водою (1 X 200 мл), висушували над безводним Na2SO4, фільтрували і концентрували при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт очищували за допомогою Combiflash із застосуванням 10% етилацетату-гексану як елюента з одержанням етил-4-оксо-3-(піридин-2-ілметилен)пентаноату (7,4 г, вихід 68,0%). Маса/заряд 234. Стадія-2. 2-Ацетил-4H-хінолізин-4-он Перемішуваний розчин етил-4-оксо-3-(піридин-2-ілметилен)пентаноату (1,7 г, 7,29 ммоль) і pTsOH (0,139 г, 0,729 ммоль) у ксилені (75 мл) нагрівали при 140°C протягом 2 год. Розчинник видаляли з реакційної суміші при зниженому тиску, потім одержаний в результаті залишок розводили холодною водою і екстрагували за допомогою DCM (2 X 200 мл), об'єднаний органічний шар промивали водою (1 X 200 мл), висушували над безводним Na2SO4, 22 UA 115296 C2 5 10 15 20 25 30 35 40 45 фільтрували і концентрували при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт очищували за допомогою Combiflash із застосуванням 2% MeOH-DCM як елюента з одержанням 2-ацетил-4H-хінолізин-4-ону (1,205 г, вихід 88%). Маса/заряд 188. Стадія-3. 2-Ацетил-3-бром-4H-хінолізин-4-он До перемішуваного розчину 2-ацетил-4H-хінолізин-4-ону (1,5 г, 8,01 ммоль) в CCl4 (30 мл) додавали NBS (1,426 г, 8,01 ммоль) при кімнатній температурі і перемішували протягом 45 хвилин. Реакційну суміш розводили водою і екстрагували за допомогою DCM (2 X 100 мл), об'єднаний органічний шар висушували над безводним Na 2SO4, фільтрували і концентрували при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт очищували за допомогою Combiflash із застосуванням 25% етилацетату-гексану як елюента з одержанням 2ацетил-3-бром-4H-хінолізин-4-ону (1,52 г, вихід 71,3%). Маса/заряд 266, 268. Стадія-4. 2-Ацетил-3-феніл-4H-хінолізин-4-он До перемішуваного розчину 2-ацетил-3-бром-4H-хінолізин-4-ону (1,59 г, 5,98 ммоль), фенілборонової кислоти (0,874 г, 7,17 ммоль) і Na2CO3 (1,900 г, 17,93 ммоль) у суміші вода:етанол:толуол (30 мл, 1:2:2) додавали тетракіс паладію (0,345 г, 0,299 ммоль) при продуванні азотом протягом 15 хвилин. Реакційну суміш нагрівали при 80°C протягом 12 год. Розчинник випарювали з реакційної суміші і залишок очищували за допомогою Combiflash із застосуванням 25% етилацетату-гексану як елюента з одержанням 2-ацетил-3-феніл-4Hхінолізин-4-ону (1,45 г, вихід 92%). Маса/заряд 264. Стадія-5. 2-(1-Аміноетил)-3-феніл-4H-хінолізин-4-он До перемішуваного розчину 2-ацетил-3-феніл-4H-хінолізин-4-ону (1,45 г, 5,51 ммоль) у ізопропоксиді титану (9,68 мл, 33,0 ммоль) додавали (S)-2-метилпропан-2-сульфінамід (0,667 г, 5,51 ммоль) при 0°C. Потім реакційну суміш нагрівали за 100°C протягом 12-18 год. Реакційну суміш екстрагували за допомогою DCM і випарювали при зниженому тиску з одержанням неочищеного залишку. Неочищений залишок розчиняли в MeOH і охолоджували до -78°C, потім додавали NaBH4 (0,833 г, 22,03 ммоль) і перемішували при -10°C протягом 2 год. Реакційну суміш розводили етилацетатом і холодною водою. Органічний шар відділяли і концентрували при зниженому тиску з одержанням неочищеної сполуки, яку потім перемішували в діоксані-HCl (4 M, 10 мл) протягом 15 хвилин. Підвищували основність реакційної суміші за допомогою бікарбонату натрію і екстрагували в етилацетаті (3 X 200 мл), об'єднаний органічний шар промивали водою (1 X 200 мл), висушували над безводним Na2SO4, фільтрували і концентрували при зниженому тиску з одержанням неочищеного продукту, який очищували за допомогою Combiflash із застосуванням 4-6% MeOH-DCM як елюента з одержанням 2-(1аміноетил)-3-феніл-4H-хінолізин-4-ону (402 мг, вихід 27,6%). Маса/заряд 265. Приклад 2. Наступні проміжні сполуки одержували із застосуванням процедури, що описана у прикладі 1, з відповідними змінами реагентів і умов реакції. 2-(1-Аміноетил)-3-(3-фторфеніл)-4H-хінолізин-4-он 23 UA 115296 C2 5 10 15 20 Маса/заряд 283. 2-(1-Аміноетил)-7-метил-3-феніл-4H-хінолізин-4-он Маса/заряд 279. 2-(1-Аміноетил)-7-фтор-3-(3-фторфеніл)-4H-хінолізин-4-он Маса/заряд 301. 2-(1-Аміноетил)-7-фтор-3-(м-толіл)-4H-хінолізин-4-он Маса/заряд 297. 2-(1-Аміноетил)-7-фтор-3-(3-фтор-5-метилфеніл)-4H-хінолізин-4-он Маса/заряд 315. 2-(1-Аміноетил)-7-фтор-3-(3-(трифторметокси)феніл)-4H-хінолізин-4-он Маса/заряд 367. 2-(1-Аміноетил)-7-фтор-3-(4-фторфеніл)-4H-хінолізин-4-он Маса/заряд 301. 2-(1-Аміноетил)-3-(3,5-дифторфеніл)-7-фтор-4H-хінолізин-4-он Маса/заряд 319. 2-(1-Амінопропіл)-7-фтор-3-феніл-4H-хінолізин-4-он Маса/заряд 297. 2-(1-Амінопропіл)-7-фтор-3-(3-фторфеніл)-4H-хінолізин-4-он Маса/заряд 315. 2-(1-Аміноетил)-7-фтор-3-феніл-4H-хінолізин-4-он Маса/заряд 283. Приклад 3. Одержання (S)-2-(1-аміноетил)-7-фтор-3-феніл-4H-хінолізин-4-ону Стадія-1. Етил-3-((5-фторпіридин-2-іл)метилен)-4-оксопентаноат 25 30 35 40 До перемішуваного розчину етил-3-(діетоксифосфорил)-4-оксопентаноату (224 г, 799 ммоль) і 5-фторпіколінальдегіду (100 г, 799 ммоль) у THF (250 мл) додавали розчин K2CO3 (122 г, 879 ммоль) в воді (250 мл) при кімнатній температурі та нагрівали при 45°C протягом 34 год. Реакційну суміш повільно виливали в охолоджену за допомогою льоду воду (2000 мл) при обробці ультразвуком. Осаджений твердий продукт фільтрували і висушували під вакуумом з одержанням етил-3-((5-фторпіридин-2-іл)метилен)-4-оксопентаноату (135 г, вихід 67,2%). Маса/заряд 252. Стадія-2. 3-((5-Фторпіридин-2-іл)метилен)-4-оксопентанова кислота До перемішуваного розчину етил-3-((5-фторпіридин-2-іл)метилен)-4-оксопентаноату (134 г, 533 ммоль) у суміші THF:вода:MeOH (2:2:1, 500 мл) додавали гідроксид літію (24,2 г, 587 ммоль) і перемішували при кімнатній температурі протягом 1 год. Розчинник видаляли при зниженому тиску і до залишку додавали воду (500 мл). Утворену таким чином суміш нейтралізували із застосуванням 1 н. розчину HCl, осаджений твердий продукт фільтрували і висушували під високим вакуумом з одержанням 3-((5-фторпіридин-2-іл)метилен)-4-оксопентанової кислоти (110 г, вихід 92%). Маса/заряд 224. Стадія-3. 2-Ацетил-7-фтор-4H-хінолізин-4-он 24 UA 115296 C2 5 10 15 20 25 30 35 40 Перемішуваний розчин 3-((5-фторпіридин-2-іл)метилен)-4-оксопентанової кислоти (109 г, 488 ммоль) у сухому DMF (300 мл) охолоджували до 0°C, до нього додавали EDC.HCl (112 г, 586 ммоль) і реакційну суміш перемішували протягом 10 хв. До реакційної суміші додавали HOBT (82 г, 537 ммоль) і TEA (102 мл, 733 ммоль) при даній температурі. Одержану в результаті реакційну суміш перемішували при кімнатній температурі протягом 18 год. Потім реакційну суміш виливали у воду з льодом, осаджений твердий продукт фільтрували, висушували під вакуумом з одержанням 2-ацетил-7-фтор-4H-хінолізин-4-ону (90 г, вихід 90%). Маса/заряд 206. Стадія-4. 2-Ацетил-3-бром-7-фтор-4H-хінолізин-4-он До перемішуваного розчину 2-ацетил-7-фтор-4H-хінолізин-4-ону (75 г, 366 ммоль) в DMF (400 мл) краплями додавали розчин NBS (65,1 г, 366 ммоль, 200 мл DMF) при 0-5°C і перемішували при 0-5°C протягом 15 хв. Реакційну суміш перемішували при кімнатній температурі протягом 10 хв. Потім реакційну суміш виливали в холодну воду; осаджений твердий продукт фільтрували і висушували під високим вакуумом з одержанням 2-ацетил-3бром-7-фтор-4H-хінолізин-4-ону (85 г, вихід 82%). Маса/заряд 284, 286. Стадія-5. 2-Ацетил-7-фтор-3-феніл-4H-хінолізин-4-он До перемішуваного розчину 2-ацетил-3-бром-7-фтор-4H-хінолізин-4-ону (85 г, 299 ммоль), фенілборонової кислоти (39,8 г, 329 ммоль) і Na2CO3 (95 г, 897 ммоль) у суміші вода:етанол:толуол (750 мл, 1:2:2) додавали тетракіс(трифенілфосфін)паладій(0) (8,63 г, 7,47 ммоль) при продуванні азотом протягом 10 хв. Потім реакційну суміш нагрівали при 85°C протягом 9 год. Розчинник видаляли з реакційної суміші при зниженому тиску і концентрат екстрагували етилацетатом (3 X 500 мл), об'єднаний органічний шар промивали водою (1 X 500 мл), висушували над безводним Na2SO4, фільтрували і концентрували при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт промивали 12% етилацетатомгексаном з одержанням 2-ацетил-7-фтор-3-феніл-4H-хінолізин-4-ону (77 г, вихід 92%). Маса/заряд 282. Стадія-6. 2-(1-Аміноетил)-7-фтор-3-феніл-4H-хінолізин-4-он До перемішуваного розчину 2-ацетил-7-фтор-3-феніл-4H-хінолізин-4-ону (77 г, 273 ммоль) в ізопропоксиді титану(IV) (321 мл, 1095 ммоль) додавали (S)-2-метилпропан-2-сульфінамід (38 г, 314 ммоль) при кімнатній температурі. Реакційну суміш нагрівали при 100°C протягом 9 год. Реакційну суміш розводили за допомогою DCM (2 л), насиченого розчину NaCl (750 мл), води (1,5 л) і перемішували протягом 25 хв. при кімнатній температурі. Органічний шар відділяли і водний шар знов перемішували з DCM (3 X 500 мл). Об'єднаний органічний шар фільтрували через подушку з целітом і шар промивали за допомогою DCM, потім об'єднаний фільтрат висушували над безводним Na2SO4, фільтрували і концентрували при зниженому тиску з 25 UA 115296 C2 5 10 15 20 25 30 35 40 45 одержанням неочищеного продукту. Неочищений продукт очищували за допомогою колонкової флеш-хроматографії, за допомогою якої одержували N-(1-(7-фтор-4-оксо-3-феніл-4H-хінолізин2-іл)етиліден)-2-метилпропан-2-сульфінамід (66 г, вихід 62,7%). До перемішуваної суспензії NaBH4 (6,35 г, 171,8 ммоль) у THF (500 мл) додавали N-(1-(7фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етиліден)-2-метилпропан-2-сульфінамід (66 г, 171,8 ммоль) при кімнатній температурі і реакційну суміш нагрівали при 45°C протягом 1-1,5 год. Реакційну суміш гасили розчином NH4Cl і екстрагували за допомогою етилацетату (3 X 500 мл), об'єднаний органічний шар промивали насиченим сольовим розчином (1 X 500 мл), висушували над безводним Na2SO4, фільтрували і концентрували при зниженому тиску з одержанням (S)-N1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)-2-метилпропан-2-сульфінаміду. У круглодонній колбі (S)-N-1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)-2-метилпропан2-сульфінамід (66 г, 171 ммоль) поміщали у воду (330 мл) і нагрівали при 45°C, потім додавали 330 мл етанолу і нагрівали при 80°C протягом 10 хв. Реакційну суміш перемішували при кімнатній температурі протягом 3 год. із наступним охолодження при 0-5°C протягом 1 год. Твердий продукт фільтрували і промивали охолодженою сумішшю вода-етанол (330 мл, 4:1) і висушували під високим вакуумом з одержанням чистого (S)-N-(S)-1-(7-фтор-4-оксо-3-феніл-4Hхінолізин-2-іл)етил)-2-метилпропан-2-сульфінаміду (36 г, вихід 54,5%, чистота = 99,28%, хіральна чистота =98,52%). Структуру підтверджували за допомогою рентгенівської дифрактометрії. До перемішуваного розчину (S)-N-(S)-(1-(7-фтор-4-оксо-3-феніл-4H-хінолізин-2-іл)етил)-2метилпропан-2-сульфінаміду (36 г, 93 ммоль) при 0°C повільно додавали розчин HCl у метанолі (140 мл, 421 ммоль) і перемішували при кімнатній температурі протягом 30 хв. Розчинник видаляли із суміші при зниженому тиску, після чого підвищували основність залишку за допомогою насиченого розчину NaHCO3 і екстрагували за допомогою етилацетату (5 X 300 мл), об'єднаний органічний шар промивали водою (1 X 100 мл), висушували над безводним Na2SO4, фільтрували і концентрували при зниженому тиску з одержанням жовтого твердої сполуки (S)-2(1-аміноетил)-7-фтор-3-феніл-4H-хінолізин-4-ону (23,6 г, вихід 90%). Маса/заряд 283. Приклад 4. Одержання 2-(1-аміноетил)-6-метил-3-феніл-4H-хінолізин-4-ону Стадія-1. Етил-3-((6-метилпіридин-2-іл)метилен)-4-оксопентаноат До перемішуваного розчину етил-3-(діетоксифосфорил)-4-оксопентаноату (12,72 г, 45,4 ммоль) і 6-метилпіколінальдегіду (5 г, 41,3 ммоль) в етанолі краплями додавали етоксид натрію (3,09 г, 45,4 ммоль) при 0°C і перемішували при даній температурі протягом 1 год. Розчинник видаляли з реакційної суміші при зниженому тиску і екстрагували за допомогою DCM (3 X 200 мл), об'єднаний органічний шар промивали водою (1 X 200 мл), висушували над безводним Na2SO4, фільтрували і концентрували при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт очищували за допомогою Combiflash із застосуванням 20% етилацетату-гексану як елюента з одержанням етил-3-((6-метилпіридин-2іл)метилен)-4-оксопентаноату (4,1 г, вихід 40,2%). Маса/заряд 248. Стадія-2. 3-((6-Метилпіридин-2-іл)метилен)-4-оксопентанова кислота До перемішуваного розчину етил-3-((6-метилпіридин-2-іл)метилен)-4-оксопентаноату (15 г, 26 UA 115296 C2 5 10 15 20 25 30 35 40 60,72 ммоль) у суміші THF-вода (200 мл) додавали гідроксид натрію (4,9 г, 121,44 ммоль) і перемішували при кімнатній температурі протягом 2 год. Реакційну суміш нейтралізували 1 н. безводним HCl і розчинник випарювали. Маса/заряд 220. Стадія-3. 2-Ацетил-6-метил-4H-хінолізин-4-он До перемішуваного розчину 3-((6-метилпіридин-2-іл)метилен)-4-оксопентанової кислоти (12 г, 54,7 ммоль) у сухому DMF (50 мл) додавали EDC.HCl (20,99 г, 109 ммоль) при кімнатній температурі і перемішували протягом 10 хвилин. До реакційної суміші додавали HOBT (12,57 г, 82 ммоль) і TEA (22,89 мл, 164 ммоль) і перемішували при кімнатній температурі протягом 18 год. Реакційну суміш гасили холодною водою і екстрагували за допомогою DCM (3 X 200 мл), об'єднаний органічний шар промивали водою (1 X 200 мл), висушували над безводним Na2SO4, фільтрували і концентрували при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт очищували за допомогою Combiflash із застосуванням 40% етилацетатугексану як елюента з одержанням 2-ацетил-6-метил-4H-хінолізин-4-ону (7,1 г, вихід 64,5%). Маса/заряд 202. Стадія-4. 2-Ацетил-3-бром-6-метил-4H-хінолізин-4-он До перемішуваного розчину 2-ацетил-6-метил-4H-хінолізин-4-ону (7 г, 34,8 ммоль) в DCM (50 мл) порціями додавали NBS (4,95 г, 27,8 ммоль) при -10°C і реакційну суміш перемішували при даній температурі протягом 45 хвилин. Потім реакційну суміш розводили водою і екстрагували за допомогою DCM (3 X 200 мл), об'єднаний органічний шар висушували над безводним Na2SO4, фільтрували і концентрували при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт очищували за допомогою Combiflash із застосуванням 25% етилацетату-гексану як елюента з одержанням 2-ацетил-3-бром-6-метил4H-хінолізин-4-ону (7,3 г, вихід 74,9%). Маса/заряд 280, 282. Стадія-5. 2-Ацетил-6-метил-3-феніл-4H-хінолізин-4-он До перемішуваного розчину 2-ацетил-3-бром-6-метил-4H-хінолізин-4-ону (5,8 г, 20,71 ммоль), фенілборонової кислоти (3,03 г, 24,85 ммоль) і Na2CO3 (6,58 г, 62,1 ммоль) у суміші вода:етанол:толуол (60 мл, 1:2:2) додавали тетракіс(трифенілфосфін)паладій(0) (1,196 г, 1,035 ммоль) при продуванні азотом протягом 15 хвилин. Потім реакційну суміш нагрівали при 80°C протягом 12 год. Розчинник випарювали з реакційної суміші і залишок очищували за допомогою Combiflash із застосуванням 25% етилацетату-гексану як елюента з одержанням 2ацетил-6-метил-3-феніл-4H-хінолізин-4-ону (5,41 г, вихід 94%). Маса/заряд 278. Стадія-6. 2-(1-Аміноетил)-6-метил-3-феніл-4H-хінолізин-4-он Спосіб A. До перемішуваного розчину 2-ацетил-6-метил-3-феніл-4H-хінолізин-4-ону (5,4 г, 19,47 ммоль) в ізопропоксиді титану (34,2 мл, 117 ммоль) додавали (S)-2-метилпропан-2 27 UA 115296 C2 5 10 15 20 25 30 35 сульфінамід (2,83 г, 23,37 ммоль) при 0°C. Реакційну суміш нагрівали за 100°C протягом 1218 год. Потім реакційну суміш екстрагували за допомогою DCM і випарювали при зниженому тиску з одержанням залишку. Потім залишок розчиняли в MeOH і охолоджували до -78°C, потім до суміші додавали NaBH4 (2,95 г, 78 ммоль) і перемішували при -10°C протягом 2 год. Реакційну суміш розводили етилацетатом і холодною водою. Органічний шар відділяли і концентрували при зниженому тиску, одержаний таким чином залишок перемішували в діоксаніHCl (4 M, 20 мл) протягом 15 хвилин. Підвищували основність реакційної суміші за допомогою бікарбонату натрію і екстрагували в етилацетаті (3 X 200 мл), об'єднаний органічний шар промивали водою (1 X 200 мл), висушували над безводним Na2SO4, фільтрували і концентрували при зниженому тиску з одержанням неочищеного продукту, який очищували за допомогою Combiflash із застосуванням 4-6% MeOH-DCM як елюента з одержанням 2-(1аміноетил)-6-метил-3-феніл-4H-хінолізин-4-ону (2,5 г) з виходом 46%. Маса/заряд 279. Спосіб B. До перемішуваного розчину 2-ацетил-6-метил-3-феніл-4H-хінолізин-4-ону (150 мг, 0,541 ммоль) у метанольному аміаку (5,02 мл, 35,2 ммоль) додавали NH4Cl (289 мг, 5,41 ммоль) при кімнатній температурі і нагрівали при 60°C протягом 9 год. Після утворення іміну реакційну суміш охолоджували до 0°C і додавали NaBH4 (30,7 мг, 0,811 ммоль) і перемішували при 0-5°C протягом 15 хвилин. Реакційну суміш гасили холодною водою і випарювали розчинник із реакційної суміші при зниженому тиску. Потім концентрат екстрагували етилацетатом (2 X 100 мл), висушували над безводним Na2SO4, фільтрували і концентрували при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт очищували за допомогою Combiflash із застосуванням 4-6% MeOH-DCM як елюента з одержанням 2-(1-аміноетил)-6метил-3-феніл-4H-хінолізин-4-ону (110 мг) з виходом 73,1%. Приклад 5. Наступні сполуки одержували із застосуванням процедури, що описана у прикладі 4, з відповідними змінами реагентів і умов реакції. 2-(1-Аміноетил)-3-(3-фторфеніл)-6-метил-4H-хінолізин-4-он Маса/заряд 297. 2-(1-Аміноетил)-3-(3,5-дифторфеніл)-6-метил-4H-хінолізин-4-он Маса/заряд 315. 2-(1-Аміноетил)-3-(3,4-дифторфеніл)-6-метил-4H-хінолізин-4-он Маса/заряд 315. 2-(1-Аміноетил)-7-фтор-6-метил-3-феніл-4H-хінолізин-4-он Маса/заряд 297. 2-(1-Аміноетил)-7-фтор-3-(3-фторфеніл)-6-метил-4H-хінолізин-4-он Маса/заряд 315. Приклад 6. 2-(Гідроксиметил)-6-метил-3-феніл-4H-хінолізин-4-он Стадія-1. Діетил-2-((6-метилпіридин-2-іл)метилен)сукцинат 40 45 50 До перемішуваного розчину діетил-2-(діетоксифосфорил)сукцинату (7,5 г, 24,17 ммоль) і етоксиду натрію (2,467 г, 36,3 ммоль) в етанолі додавали 6-метилпіколінальдегід (3,51 г, 29,0 ммоль) при кімнатній температурі. Реакційну суміш перемішували при кімнатній температурі протягом 2 год., а потім нагрівали при 50°C протягом 1 год. Розчинник видаляли при зниженому тиску і одержаний таким чином залишок розводили холодною водою і екстрагували за допомогою DCM (2 X 150 мл), об'єднаний органічний шар промивали водою (1 X 150 мл), висушували над безводним Na2SO4, фільтрували і концентрували при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт очищували за допомогою флеш-хроматографії із застосуванням 10% етилацетату-гексану як елюента з одержанням діетил-2-((6-метилпіридин-2-іл)метилен)сукцинату (2,5 г, вихід 37,3%). 28
ДивитисяДодаткова інформація
Назва патенту англійськоюQuinolizinone derivatives as pi3k inhibitors
Автори англійськоюShukla, Manojkumar, Ramprasad, Jana, Nirmal, Kumar, Mahangare, Sachin, Jaysing, Vidhate, Prashant, Popatrao, Lagad, Dipak, Raychand, Tarage, Anand, Jagannath, Kulkarni, Sanjeev, Anant, Palle, Venkata, P., Kamboj, Rajender, Kumar
Автори російськоюШукла Маноджкумар Рампрасад, Джана Нирмал Кумар, Махангаре Сачхин Джайсинг, Видхате Прашант Попатрао, Лагад Дипак Райчханд, Тараге Ананд Джаганнатх, Кулкарни Санджеев Анант, Палле Венката П., Камбодж Раджендер Кумар
МПК / Мітки
МПК: C07D 471/04, C07D 519/00
Мітки: хінолізинонові, похідні, інгібітори
Код посилання
<a href="https://ua.patents.su/64-115296-khinolizinonovi-pokhidni-yak-ingibitori-pi3k.html" target="_blank" rel="follow" title="База патентів України">Хінолізинонові похідні як інгібітори pi3k</a>
Попередній патент: Спосіб випалу сировини в обертовій печі
Наступний патент: Пристрій для впорядкування чисел
Випадковий патент: Дисковий оборотний плуг для гладкої оранки