Біциклічні піразинонові похідні
Номер патенту: 112795
Опубліковано: 25.10.2016
Автори: Бухшталлер Ханс-Петер, МУАНЕ Жерар, Дорш Дітер, Вегенер Ансгар
Формула / Реферат
1. Сполуки формули І
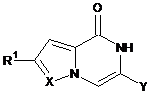 , I
, I
в якій
R1 являє собою Н, F, Сl, CN, CH3, CH2OH, CH2C1, CH2Br, CF3, CHF2 або CH2F,
R2 являє собою Η або А,
R3 являє собою Н, F, Сl, СН3, CF3 або CHF2,
X являє собою CR3 або N,
Υ являє собою Аr1, Carb, Het1 або Сус,
Аr1 являє собою феніл або нафтил, який незаміщений або моно-, ди- або тризаміщений за допомогою Hal, A, [C(R2)2]pOR2, [C(R2)2]pN(R2)2, [C(R2)2]pHet2, NO2, CN, [C(R2)2]pCOOR2, [C(R2)2]pCON(R2)2, NR2COA, NR2SO2A, [C(R2)2]pSO2N(R2)2, S(O)nA, COHet3, O[C(R2)2]mN(R2)2, O[C(R2)2]pAr2, O[C(R2)2]pHet2, NHCOOA, NHCON(R2)2, Сус, СНО і/або СОА,
Аr являє собою феніл, який незаміщений або моно- або дизаміщений за допомогою Hal, A, [C(R2)2]pOR2, [C(R2)2]pN(R2)2, [C(R2)2]pHet3, NO2, CN, [C(R2)2]pCOOR2, [C(R2)2]pN(R2)2, N(R2)2COA, NR2SO2A, [C(R2)2]pSO2N(R2)2, S(O)nA, COHet3, O[C(R2)2]mN(R2)2, O[C(R2)2]pHet3, NHCOOA, NHCON(R2)2, СНО і/або СОА,
Het1 являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3-бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з яких незаміщений або моно- або дизаміщений за допомогою Hal, A, [C(R2)2]pOR2, [C(R2)2]pN(R2)2, [C(R2)2]pHet2, [C(R2)2]pAr2, NO2, CN, [C(R2)2]pCOOR2, [C(R2)2]pCON(R2)2, NR2COA, NR2SO2A, [C(R2)2]pSO2N(R2)2, S(O)nA, COHet3, O[C(R2)2]mN(R2)2, O[C(R2)2]pAr2, O[C(R2)2]pHet2, NHCOOA, NHCON(R2)2, CHO, COA, =S, =NR і/або =O,
Carb являє собою інданіл або тетрагідронафтил, кожний з яких може бути незаміщений або моно-, ди-, три- або тетразаміщений за допомогою А,
Сус являє собою циклічний алкіл, який має 3, 4, 5, 6 або 7 атомів С, який може бути незаміщений або монозаміщений за допомогою А, ОН, Hal, CN або Аr або Het2,
Het2 являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3-бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з яких незаміщений або моно- або дизаміщений за допомогою Hal, A, [C(R2)2]pOR2, [C(R2)2]pN(R2)2, [C(R2)2]pHet3, [C(R2)2]pOHet3, [C(R2)2]pAr2, NO2, CN, [C(R2)2]pCOOR2, [C(R2)2]pCON(R2)2, NR2COA, NR2SO2A, [C(R2)2]рSO2N(R2)2, S(O)nA, COHet3, O[C(R2)2]mN(R2)2, O[C(R2)2]pAr2, O[C(R2)2]pHet3, NHCOOA, NHCON(R2)2, CHO, COA, =S, =NR і/або =O,
Het3 являє собою дигідропіроліл, піролідиніл, азетидиніл, оксетаніл, тетрагідроімідазоліл, дигідропіразоліл, тетрагідропіразоліл, тетрагідрофураніл, дигідропіридил, тетрагідропіридил, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, тетрагідропіраніл або піперазиніл, кожний з яких незаміщений або моно- або дизаміщений за допомогою Hal, CN, OR2, COOR2, CON(R2)2, S(O)nA, S(O)nAr, COA, А і/або =O,
А являє собою нерозгалужений або розгалужений алкіл, який має 1-10 атомів С, де дві розташовані поруч СН- і/або СН2-групи можуть утворювати подвійний зв'язок і де одна або дві СН- і/або СН2-групи, що не розташовані поруч, можуть бути замінені на атоми N-, О- і/або S, і де 1-7 атомів Η можуть бути замінені на F або Сl,
Hal являє собою F, Сl, Вr або І,
n являє собою 0, 1 або 2,
m являє собою 1, 2 або 3,
p являє собою 0, 1, 2, 3 або 4,
за умови, що, якщо R1 означає СН2ОН, то Аr1 не означає 2,4-дихлорфеніл, і їх фармацевтично прийнятні сольвати, солі, таутомери і стереоізомери, включаючи їх суміші у всіх співвідношеннях.
2. Сполуки за п. 1, в яких
Аr1 являє собою феніл, який незаміщений або моно-, ди- або тризаміщений за допомогою Hal, A, [C(R2)2]pOR2, [C(R2)2]pN(R2)2, [C(R2)2]pHet2, NO2, Cyc, [C(R2)2]pCOOR2, O[C(R2)2]pAr2 і/або O[C(R2)2]pHet2,
і їх фармацевтично прийнятні сольвати, солі, таутомери і стереоізомери, включаючи їх суміші у всіх співвідношеннях.
3. Сполуки за п. 1 або 2, в яких
Аr2 являє собою феніл, який незаміщений або монозаміщений за допомогою [C(R2)2]pOR2,
і їх фармацевтично прийнятні сольвати, солі, таутомери і стереоізомери, включаючи їх суміші у всіх співвідношеннях.
4. Сполуки за одним або декількома з п. 1-3, в яких
Het1 являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3-бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з яких незаміщений або моно- або дизаміщений за допомогою A, [C(R2)2]pOR2, [C(R2)2]pHet2 і/або [C(R2)2]pAr2,
і їх фармацевтично прийнятні сольвати, солі, таутомери і стереоізомери, включаючи їх суміші у всіх співвідношеннях.
5. Сполуки за одним або декількома з п. 1-4, в яких
Het2 являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3-бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з яких незаміщений або моно- або дизаміщений за допомогою A, [C(R2)2]pOR, [C(R2)2]pHet3 і/або [C(R2)2]pOHet3,
і їх фармацевтично прийнятні сольвати, солі, таутомери і стереоізомери, включаючи їх суміші у всіх співвідношеннях.
6. Сполуки за одним або декількома з п. 1-4, в яких
Het3 являє собою дигідропіроліл, піролідиніл, азетидиніл, оксетаніл, тетрагідроімідазоліл, дигідропіразоліл, тетрагідропіразоліл, тетрагідрофураніл, дигідропіридил, тетрагідропіридил, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, тетрагідропіраніл або піперазиніл,
і їх фармацевтично прийнятні сольвати, солі, таутомери і стереоізомери, включаючи їх суміші у всіх співвідношеннях.
7. Сполуки за одним або декількома з п. 1-6, в яких
R1 являє собою Н, F, Сl, CN, CH3, CH2OH, CH2Cl, CH2Br, CF3, CHF2 або CH2F,
R2 являє собою Η або А,
R3 являє собою Н, F, Сl, СН3, CF3 або CHF2,
X являє собою CR3 або N,
Υ являє собою Аr1, Carb, Het1 або Сус,
Аr являє собою феніл, який незаміщений або моно-, ди- або тризаміщений за допомогою Hal, A, [C(R2)2]pOR2, [C(R2)2]pN(R2)2, [C(R2)2]pHet2, NO2, Cyc, [C(R2)2]pCOOR2, O[C(R2)2]pAr2 і/або O[C(R2)2]pHet2,
Аr2 являє собою феніл, який незаміщений або монозаміщений за допомогою [C(R2)2]pOR2,
Het1 являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3-бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з яких незаміщений або моно- або дизаміщений за допомогою A, [C(R2)2]pOR2, [C(R2)2]pHet2 і/або [C(R2)2]pAr2,
Carb являє собою інданіл або тетрагідронафтил, кожний з яких може бути незаміщений або моно-, ди-, три- або тетразаміщений за допомогою А,
Сус являє собою циклічний алкіл, який має 3, 4, 5, 6 або 7 атомів С, який може бути незаміщений або монозаміщений за допомогою А, ОН, Hal, CN або Аr або Het2,
Het2 являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3-бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з яких незаміщений або моно- або дизаміщений за допомогою A, [C(R2)2]pOR2, [C(R2)2]pHet3 і/або [C(R2)2]pOHet3,
Het3 являє собою дигідропіроліл, піролідиніл, азетидиніл, оксетаніл, тетрагідроімідазоліл, дигідропіразоліл, тетрагідропіразоліл, тетрагідрофураніл, дигідропіридил, тетрагідропіридил, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, тетрагідропіраніл або піперазиніл,
А являє собою нерозгалужений або розгалужений алкіл, який має 1-10 атомів С, де дві розташовані поруч СН- і/або СН2-групи можуть утворювати подвійний зв'язок і де одна або дві СН- і/або СН2-групи, що не розташовані поруч, можуть бути замінені на атоми N-, О- і/або S, і де 1-7 атомів Η можуть бути замінені на F або Сl,
Hal являє собою F, Сl, Вr або І,
p являє собою 0, 1, 2, 3 або 4,
за умови, що, якщо R1 означає СН2ОН, то Аr1 не означає 2,4-дихлорфеніл,
і їх фармацевтично прийнятні сольвати, солі, таутомери і стереоізомери, включаючи їх суміші у всіх співвідношеннях.
8. Сполуки за одним або декількома з п. 1-7, в яких
R1 являє собою Н, F, Сl, CN, CH3, CH2OH, CH2Cl, CH2Br, CF3, CHF2 або CH2F,
R2 являє собою Η або А,
R3 являє собою Н, F, Сl, СН3, CF3 або CHF2,
X являє собою CR3 або N,
Υ являє собою Аr1, Carb, Het1 або Сус,
Аr1 являє собою феніл, який незаміщений або моно-, ди- або тризаміщений за допомогою Hal, A, [C(R2)2]pOR2, [C(R2)2]pN(R2)2, [C(R2)2]pHet2, NO2, Cyc, [C(R2)2]pCOOR2, O[C(R2)2]pAr2 і/або O[C(R2)2]pHet2,
Аr2 являє собою феніл, який незаміщений або монозаміщений за допомогою [C(R2)2]pOR2,
Het являє собою піролідиніл, піперидиніл, морфолініл, піразоліл, піридил, піримідил або 1,3-бензодіоксоліл, кожний з яких незаміщений або моно- або дизаміщений за допомогою A, [C(R2)2]pOR2, [C(R2)2]pHet2 і/або [C(R2)2]pAr2,
Carb являє собою інданіл або тетрагідронафтил, кожний з яких може бути незаміщений або моно-, ди-, три- або тетразаміщений за допомогою А,
Сус являє собою циклічний алкіл, який має 3, 4, 5, 6 або 7 атомів С, який може бути незаміщений або монозаміщений за допомогою А, ОН, Hal, CN або Аr2 або Het2,
Het2 являє собою піролідиніл, піперидиніл, морфолініл, піразоліл, оксазоліл, ізоксазоліл або оксадіазоліл, кожний з яких незаміщений або моно- або дизаміщений за допомогою A, [C(R2)2]pOR2, [C(R2)2]pHet3 і/або [C(R2)2]pOHet3,
Het3 являє собою піролідиніл, піперидиніл, морфолініл або тетрагідропіраніл,
А являє собою нерозгалужений або розгалужений алкіл, який має 1-10 атомів С, де дві розташовані поруч СН- і/або СН2-групи можуть утворювати подвійний зв'язок і де одна або дві СН- і/або СН2-групи, що не розташовані поруч, можуть бути замінені на атоми О, і де 1-7 атомів Η можуть бути замінені на F або Сl,
Hal являє собою F, Сl, Вr або І,
p являє собою 0, 1, 2, 3 або 4,
за умови, що, якщо R1 означає СН2ОН, то Аr1 не означає 2,4-дихлорфеніл,
і їх фармацевтично прийнятні сольвати, солі, таутомери і стереоізомери, включаючи їх суміші у всіх співвідношеннях.
9. Сполуки за п. 1, вибрані з групи
№
Назва
"А1"
3-(4-бензилоксифеніл)-2Н-піроло[1,2-а]піразин-1-он
"А2"
3-феніл-2Н-піроло[1,2-а]піразин-1-он
"A3"
3-(3-хлорфеніл)-2Н-піроло[1,2-а]піразин-1-он
"А4"
3-(3-метоксифеніл)-2Н-піроло[1,2-а]піразин-1-он
"А5"
3-(5,5,8,8-тетраметил-5,6,7,8-тетрагідронафталін-2-іл)-2Н-піроло[1,2-а]піразин-1-он
"А6"
3-(4-нітрофеніл)-2Н-піроло[1,2-а]піразин-1-он
"А7"
3-(4-метоксифеніл)-2Н-піроло[1,2-а]піразин-1-он
"А8"
3-(3,4-диметоксифеніл)-2Н-піроло[1,2-а]піразин-1-он
"А9"
3-бензо[1,3]діоксол-5-іл-2Н-піроло[1,2-а]піразин-1-он
"А10"
3-(4-фторфеніл)-2Н-піроло[1,2-а]піразин-1-он
"A11"
3-(4-трет-бутилфеніл)-2Н-піроло[1,2-а]піразин-1-он
"А12"
3-n-толіл-2Н-піроло[1,2-а]піразин-1-он
"А13"
3-(4-трифторметилфеніл)-2Н-піроло[1,2-а]піразин-1-он
"А14"
3-(1-метил-1Н-піразол-4-іл)-2Н-піроло[1,2-а]піразин-1-он
"А15"
6-(4-третет-бутилфеніл)-5Н-піразоло[1,5-а]піразин-4-он
"А16"
6-(4-трифторметоксифеніл)-5Н-піразоло[1,5-а]піразин-4-он
"А17"
6-(4-піролідин-1-ілфеніл)-5Н-піразоло[1,5-а]піразин-4-он
"А18"
6-(4-трет-бутилфеніл)-2-гідроксиметил-5Н-піразоло[1,5-а]піразин-4-он
"А19"
2-гідроксиметил-6-(4-піролідин-1-ілфеніл)-5Н-піразоло[1,5-а]піразин-4-он
"А20"
2-гідроксиметил-6-(4-ізопропоксифеніл)-5Н-піразоло[1,5-а]піразин-4-он
"А21"
2-гідроксиметил-6-[4-(5-метил-[1,2,4]оксадіазол-3-іл)феніл]-5Н-піразоло[1,5-а]піразин-4-он
"А22"
2-гідроксиметил-6-(1-ізопропіл-1Н-піразол-4-іл)-5Н-піразоло[1,5-а]піразин-4-он
"А23"
6-циклогексил-2-гідроксиметил-5Н-піразоло[1,5-а]піразин-4-он
"А24"
3-(4-бромфеніл)-2Н-піроло[1,2-а]піразин-1-он
"A25"
3-[4-(1-метил-1Н-піразол-4-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A26"
3-{4-[1-(2-метоксіетил)-1Н-піразол-4-іл]феніл}-2Н-піроло[1,2-а]піразин-1-он
"A27"
3-{4-[1-(2-піролідин-1-ілетил)-1Н-піразол-4-іл]феніл}-2Н-піроло[1,2-а]піразин-1-он
"A28"
складний метиловий ефір 4-(1-оксо-1,2-дигідропіроло[1,2-а]піразин-3-іл)-бензойної кислоти
"A29"
3-[4-(1-гідрокси-1-метилетил)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A30"
6-(4-трет-бутилфеніл)-2-метил-5Н-піразоло[1,5-а]піразин-4-он
"АЗІ"
3-(4-{1-[2-(тетрагідропіран-2-ілоксі)етил]-1Н-піразол-4-іл}феніл)-2Н-піроло[1,2-а]піразин-1-он
"А32"
3-{4-[1-(2-гідроксіетил)-1Н-піразол-4-іл]феніл}-2Н-піроло[1,2-а]піразин-1-он
"АЗЗ"
2-хлорметил-6-(4-трифторметоксифеніл)-5Н-піразоло[1,5-а]піразин-4-он
"А34"
2-метил-6-(4-трифторметоксифеніл)-5Н-піразоло[1,5-а]піразин-4-он
"А35"
3-(4-трет-бутилфеніл)-7-фтор-2Н-піроло[1,2-а]піразин-1-он
"А36"
2-бромметил-6-(4-бромфеніл)-5Н-піразоло[1,5-а]піразин-4-он
"А37"
2-метил-6-(4-піролідин-1-ілфеніл)-5Н-піразоло[1,5-а]піразин-4-он
"А38"
3-(4-трет-бутилфеніл)-7-метил-2Н-піроло[1,2-а]піразин-1-он
"А39"
6-(4-бромфеніл)-2-метил-5Н-піразоло[1,5-а]піразин-4-он
"А40"
6-(4-бромфеніл)-5Н-піразоло[1,5-а]піразин-4-он
"А41"
2-гідроксиметил-6-(6-піролідин-1-ілпіридин-3-іл)-5Н-піразоло[1,5-а]піразин-4-он
"А42"
6-(6-піролідин-1-ілпіридин-3-іл)-5Н-піразоло[1,5-а]піразин-4-он
"А43"
6-[4-(5-метил-[1,2,4]оксадіазол-3-іл)феніл]-5Н-піразоло[1,5-а]піразин-4-он
"А44"
6-(1-трет-бутил-1Н-піразол-4-іл)-5Н-піразоло[1,5-а]піразин-4-он
"А45"
2-(гідроксиметил)-6-[1-(4-метоксифеніл)-4-піперидил]-5Н-піразоло[1,5-а]піразин-4-он
"А46"
6-[4-(1-гідрокси-1-метилетил)феніл]-2-метил-5Н-піразоло[1,5-а]піразин-4-он
"А47"
6-[4-(1-гідрокси-1-метилетил)феніл]-5Н-піразоло[1,5-а]піразин-4-он
"А48"
2-метил-6-(6-піролідин-1-іл-3-піридил)-5Н-піразоло[1,5-а]піразин-4-он
"А49"
2-метил-6-[4-(5-метил-[1,2,4]оксадіазол-3-іл)феніл]-5Н-піразоло[1,5-а]піразин-4-он
"А50"
6-циклогексил-2-метил-5Н-піразоло[1,5-а]піразин-4-он
"Α51"
2-метил-6-(1-ізопропіл-1Н-піразол-4-іл)-5Н-піразоло[1,5-а]піразин-4-он
"A52"
2-метил-6-(1-тpeт-бутил-1Н-піразол-4-іл)-5Н-піразоло[1,5-а]піразин-4-он
"A53"
2-метил-6-[1-(4-метоксифеніл)-4-піперидил]-5Н-піразоло[1,5-а]піразин-4-он
"A54"
2-метил-6-(2-піролідин-1-ілпіримідин-5-іл)-5Н-піразоло[1,5-а]піразин-4-он
"A55"
6-(4-трет-бутилфеніл)-2-трифторметил-5Н-піразоло[1,5-а]піразин-4-он
"A56"
3-[4-(1-гідрокси-1-метилетил)феніл]-7-метил-2Н-піроло[1,2-а]піразин-1-он
"A57"
3-(1-трет-бутил-1Н-піразол-4-іл)-7-метил-2Н-піроло[1,2-а]піразин-1-он
"A58"
3-(4-бромфеніл)-7-фтор-2Н-піроло[1,2-а]піразин-1-он
"A59"
7-фтор-3-[4-(1-гідрокси-1-метилетил)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A60"
7-хлор-3-[4-(1-гідрокси-1-метилетил)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A61"
3-[4-(1-етил-1-гідроксипропіл)феніл]-7-фтор-2Н-піроло[1,2-а]піразин-1-он
"A62"
3-[4-(1-гідрокси-1-метилетил)феніл]-1-оксо-1,2-дигідропіроло[1,2-а]піразин-7-карбонітрил
"A63"
7-фтор-3-[4-(1-фтор-1-метилетил)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A64"
6-(4-трет-бутилфеніл)-2-фторметил-5Н-піразоло[1,5-а]піразин-4-он
"A65"
2-гідроксиметил-6-[4-(1-гідрокси-1-метилетил)феніл]-5Н-піразоло[1,5-а]піразин-4-он
"A66"
6-(4-трет-бутилфеніл)-2-дифторметил-5Н-піразоло[1,5-а]піразин-4-он
"A67"
6-(4-бромфеніл)-2-трифторметил-5Н-піразоло[1,5-а]піразин-4-он
"A68"
складний метиловий ефір 4-(4-оксо-2-трифторметил-4,5-дигідропіразоло[1,5-а]піразин-6-іл)бензойної кислоти
"A69"
6-[4-(1-гідрокси-1-метилетил)феніл]-2-трифторметил-5Н-піразоло[1,5-а]піразин-4-он
"A70"
7-фтор-3-{4-[1-(2-гідроксіетокси)-1-метилетил]феніл}-2Н-піроло[1,2-а]піразин-1-он
"Α71"
7-фтор-3-{4-[1-(2-метоксіетокси)-1-метилетил]феніл}-2Н-піроло[1,2-а]піразин-1-он
"A72"
3-[4-(1-аміно-1-метилетил)феніл]-7-фтор-2Н-піроло[1,2-а]піразин-1-он
"A73"
7-фтор-3-[4-(2-метилтетрагідрофуран-2-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A74"
7-фтор-3-[4-(4-гідрокси-1-метиленбутил)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A75"
3-(4-піперидин-4-ілфеніл)-2Н-піроло[1,2-а]піразин-1-он
"A76"
3-(4-піролідин-3-ілфеніл)-2Н-піроло[1,2-а]піразин-1-он
"A77"
7-фтор-3-(4-піперидин-4-ілфеніл)-2Н-піроло[1,2-а]піразин-1-он
"A78"
7-хлор-3-(4-піперидин-4-ілфеніл)-2Н-піроло[1,2-а]піразин-1-он
"A79"
3-[4-(1-метилпіперидин-4-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A80"
3-[4-(1-метилпіролідин-3-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A81"
7-фтор-3-[4-(1-метилпіперидин-4-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A82"
7-хлор-3-[4-(1-метилпіперидин-4-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A83"
6,7-дифтор-3-[4-(1-гідрокси-1-метилетил)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A84"
6-фтор-3-[4-(1-гідрокси-1-метилетил)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A85"
7-фтор-3-[4-(1-гідроксициклопентил)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A86"
гідрохлорид 3-[4-(3-гідроксіазетидин-3-іл)феніл]-2Н-піроло[1,2-а]піразин-1-ону
"A87"
3-[4-(1-гідрокси-1-метилетил)феніл]-6-метил-2Н-піроло[1,2-а]піразин-1-он
"A88"
7-хлор-3-[4-(1,3-дигідрокси-1-метилпропіл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A89"
6-(1-трет-бутил-1Н-піразол-4-іл)-2-гідроксиметил-5Н-піразоло[1,5-а]піразин-4-он
"A90"
7-фтор-3-[4-(1-метил-1Н-піразол-4-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"Α91"
7-метил-3-[4-(1-метил-1Н-піразол-4-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A92"
3-(4-трет-бутилфеніл)-1-оксо-1,2-дигідропіроло[1,2-а]піразин-7-карбонітрил
"A93"
7-фтор-3-феніл-2Н-піроло[1,2-а]піразин-1-он
"A94"
3-(4-бромфеніл)-6-метил-2Н-піроло[1,2-а]піразин-1-он
"A95"
3-[4-(1-гідрокси-1-метилетил)феніл]-6-метил-2Н-піроло[1,2-а]піразин-1-он
"A96"
6-(дифторметил)-3-[4-(1-гідрокси-1-метилетил)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A97"
6-(трифторметил)-3-[4-(1-гідрокси-1-метилетил)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A98"
3-[4-(3-гідроксипіролідин-3-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A99"
3-[4-(4-гідрокси-4-піперидил)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A100"
3-[4-(3-гідрокси-1-метилазетидин-3-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A101"
3-[4-(3-гідрокси-1-метилпіролідин-3-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A102"
3-[4-(4-гідрокси-1-метил-4-піперидил)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A103"
7-фтор-3-(4-піролідин-3-ілфеніл)-2Н-піроло[1,2-а]піразин-1-он
"A104"
7-фтор-3-[4-(1-метилпіролідин-3-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A105"
7-хлор-3-(4-піролідин-3-ілфеніл)-2Н-піроло[1,2-а]піразин-1-он
"A106"
7-хлор-3-[4-(1-метилпіролідин-3-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A107"
7-хлор-3-[4-(1,3-дигідрокси-1-метилпропіл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A108"
3-[4-(1,3-дигідрокси-1-метилпропіл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"A109"
7-фтор-3-[4-(1,3-дигідрокси-1-метилпропіл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"Α110"
3-[4-(3-гідроксіоксетан-3-іл)феніл]-2Н-піроло[1,2-а]піразин-1-он
"Α111"
3-[4-(1-гідроксициклобутил)феніл]-2Н-піроло[1,2-а]піразин-1-он
і їх фармацевтично прийнятні сольвати, солі, таутомери і стереоізомери, включаючи їх суміші у всіх співвідношеннях.
10. Спосіб одержання сполук формули І за пунктами 1-9 і їх фармацевтично прийнятних солей, сольватів, таутомерів і стереоізомерів, який відрізняється тим, що
а) сполуку формули II
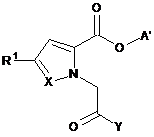 , ІІ
, ІІ
в якій R1, X і Υ мають значення, зазначені в п. 1,
і А' являє собою нерозгалужений або розгалужений алкіл, який має 1, 2, 3 або 4 атоми С,
піддають реакції з ΝΗ3, NH4OAс або (NH4)2CO3,
або
b) сполуку формули III
 , III
, III
в якій R1, X і Υ мають значення, зазначені в п. 1,
циклізують за допомогою Н2О2 за основних умов,
або
c) радикал R1 і/або Υ перетворюють на інший радикал R1 і/або Υ шляхом
і) перетворення СООН або СНО на Н,
іі) перетворення складноефірної групи на спиртову групу,
ііі) перетворення галогенованого фенільного кільця в реакції сполучення Сузукі на ариловане фенільне кільце,
iv) перетворення галогенованої алкільної групи на алкільну групу,
або
d) сполуку формули І вивільняють з однієї із її функціональних похідних шляхом обробки сольволізуючим або гідрогенолізуючим агентом,
і/або
основу або кислоту формули І перетворюють на одну з її солей.
11. Лікарський засіб, що містить принаймні одну сполуку формули І і/або її фармацевтично прийнятні солі, сольвати, таутомери і стереоізомери, включаючи їх суміші у всіх співвідношеннях, і необов'язково фармацевтично прийнятний носій, наповнювач або середовище для лікарського засобу.
12. Сполуки формули І і їх фармацевтично прийнятні солі, сольвати, таутомери і стереоізомери, включаючи їх суміші у всіх співвідношеннях, для застосування для лікування і/або запобігання злоякісному новоутворенню, розсіяному склерозу, серцево-судинним захворюванням, уражененям центральної нервової системи і різним формам запалення.
13. Сполуки за п. 12 для застосування для лікування і/або запобігання захворюванням, вибраним із групи раку голови, шиї, очей, рота, горла, стравоходу, бронхів, гортані, глотки, грудей, кісток, легенів, ободової кишки, прямої кишки, шлунка, передміхурової залози, сечового міхура, матки, шийки матки, молочної залози, яєчників, яєчок або інших репродуктивних органів, шкіри, щитовидної залози, крові, лімфатичних вузлів, нирок, печінки, підшлункової залози, головного мозку, центральної нервової системи, солідних пухлин і злоякісного переродження крові.
14. Лікарські засоби, що містять принаймні одну сполуку формули І і/або її фармацевтично прийнятні солі, сольвати і стереоізомери, включаючи їх суміші у всіх співвідношеннях, і принаймні один додатковий активний компонент лікарського засобу.
15. Комплект (набір),що складається з окремих упаковок
(a) ефективної кількості сполуки формули І і/або її фармацевтично прийнятних солей, сольватів, солей і стереоізомерів, включаючи їх суміші у всіх співвідношеннях,
і
(b) ефективної кількості додаткового активного компонента лікарського засобу.
Текст
Реферат: Сполуки формули І O R NH 1 N X 1 Y ,I в якій R , X і Υ мають значення, зазначені в п. 1, є інгібіторами танкірази і можуть застосовуватися, серед іншого, для лікування захворювань, таких як злоякісне новоутворення, серцево-судинні захворювання, ураження центральної нервової системи та різні форми запалення. UA 112795 C2 (12) UA 112795 C2 O N H 1 R XN Y I UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 ПЕРЕДУМОВИ СТВОРЕННЯ ВИНАХОДУ Задачею винаходу є виявлення нових сполук, які мають цінні властивості, зокрема, таких, які можна застосовувати для одержання лікарських засобів. Даний винахід відноситься до біциклічних піразинонових похідних, які інгібують активність танкіраз (TANK) і полі(ADP-рибоза)полімерази PARP-1. Таким чином, сполуки відповідно до даного винаходу придатні для лікування захворювань, таких як злоякісне новоутворення, розсіяний склероз, серцево-судинні захворювання, ураження центральної нервової системи та різні форми запалення. Даний винахід також забезпечує спосіб одержання цих сполук, фармацевтичні композиції, які містять ці сполуки, та способи лікування захворювань із застосуванням фармацевтичних композицій, які містять ці сполуки. Ядерний фермент полі(ADP-рибоза) полімераза-1 (PARP-1) є представником сімейства ферментів PARP. Це сімейство ферментів росту включає PARP, такі як, наприклад: PARP-1, PARP-2, PARP-3 і Vault-parp; і танкірази (TANK), такі як, наприклад: TANK-1 і TANK-2. PARP також позначається як полі(аденозин5'-дифосфорибоза) полімераза або PARS (полі(ADPрибоза) синтетаза). Вважають, що TANK-1 необхідна для полімеризації зв'язаної з мітотичним веретеном полі(ADP-рибози). Полі(ADP-рибозил)ююча активність TANK-1 повинна бути вирішальною для точного утворення й підтримки біполярності веретена. Крім того, вважають, що PARP активність TANK-1 необхідна для нормального поділу теломер перед анафазою. Інтерференція з танкіразною PARP активністю приводить до аберантного мітозу, який викликає тимчасову зупинку клітинного циклу, можливо, внаслідок активації контрольної точки веретена, з наступною клітинною загибеллю. Таким чином, вважають, що інгібування танкіраз має цитотоксичну дію на проліферуючі пухлинні клітини (WO 2008/107478). Інгібітори PARP описані M. Rouleau і ін. в Nature Reviews, том 10, 293-301 у клінічних дослідженнях злоякісних новоутворень (таблиця 2, сторінка 298). Відповідно до огляду Horvath і Szabo (Drug News Perspect 20(3), April 2007, 171-181) у останніх дослідженнях було показано, що PARP інгібітори підсилюють загибель ракових клітин головним чином у зв'язку з їх перешкоджанням репарації ДНК на різних рівнях. У останніх дослідженнях також було показано, що PARP інгібітори інгібують ангіогенез, або шляхом інгібування експресії фактора росту, або шляхом інгібування індукованих фактором росту клітинних проліферативних відповідей. Ці дані також можуть впливати на характер протиракових ефектів PARP інгібіторів in vivo. Також у дослідженні Tentori і ін. (Eur. J. Cancer, 2007, 43 (14) 2124-2133) було показано, що PARP інгібітори анулюють індуковану VEGF або плацентним фактором росту міграцію й запобігають утворенню трубочкоподібних мереж у клітинних системах, і ушкоджують ангіогенез in vivo. У дослідженні також показано, що індукований фактором росту ангіогенез є дефектним в PARP-1 "knock-out" мишей. Результати дослідження забезпечують підтвердження для націлювання PARP на анти-ангіогенез, додаючи нові терапевтичні показання для застосування PARP інгібіторів при лікуванні злоякісного новоутворення. Добре відомо, дефекти в консервативних шляхах передачі сигналів відіграють ключову роль у походженні й поведінці по суті всіх злоякісних новоутворень (E.A.Fearon, Cancer Cell, том 16, вид. 5, 2009, 366-368). Wnt шлях є мішенню для протиракової терапії. Ключовою особливістю Wnt шляху є регульований протеоліз (деградація) -катеніну за допомогою комплексу, що руйнує -катенін. Білки, такі як WTX, APC або Axin, задіяні в процес розкладання. Правильне розкладання -катеніну є важливим для уникнення невідповідної активації Wnt шляху, яка спостерігається при багатьох злоякісних новоутвореннях. Танкірази інгібують активність Axin і, отже, інгібують розкладання -катеніну. У результаті цього, інгібітори танкірази підвищують розкладання -катеніну. У недавньому виданні журналу Nature були запропоновані не тільки важливі нові відомості щодо білків, що регулюють Wnt передачу сигналів, а також додатково підтверджується підхід антагонізації рівнів -катеніну й локалізації за допомогою невеликих молекул (Huang і ін., 2009; Nature, том 461, 614-620). Сполука XAV939 інгібує ріст DLD-1ракових клітин. Вони виявили, що XAV9393 блокує Wnt-стимульоване накопичення -катеніну шляхом підвищення рівнів білків AXIN1 і AXIN2. У наступній роботі авторами було показано, що XAV939 регулює рівні AXIN за допомогою інгібування танкіраз 1 і 2 (TNKS1 і TNKS2), які обидві є членами сімейства білків полі(ADP-рибоза) полімерази (PARP) (S.J. Hsiao і ін., Biochimie 90, 2008, 83-92). Було виявлено, що сполуки відповідно до винаходу і їх солі мають надзвичайно хороші фармакологічні властивості, а також хорошу переносимість. 1 UA 112795 C2 5 10 15 20 25 30 Даний винахід, зокрема, відноситься до сполук формули I, які інгібують танкіразу 1 і 2, композицій, які містять ці сполуки, і способів їх застосування для лікування захворювань і ускладнень, індукованих TANK. Крім того, сполуки формули I можуть використовуватися для виділення й дослідження активності або експресії TANK. Додатково, вони особливо придатні для застосування в діагностичних методах для захворювань у зв'язку з нерегульованою або порушеною активністю TANK. Хазяїн або пацієнт може належати до будь-якого з видів ссавців, наприклад, видів приматів, зокрема, людей; гризунів, включаючи мишей, щурів і хом'яків; кроликів, коней, корів, собак, кішок і т. д. Тваринні моделі становлять інтерес для експериментальних досліджень, забезпечуючи модель для хвороб людини. Чутливість певної клітини до лікування за допомогою сполук відповідно до даного винаходу може визначатися за допомогою аналізів in vitro. Типово, до культури клітин додають сполуку відповідно до даного винаходу при різних концентраціях протягом періоду часу, який є достатнім для того, щоб дозволити активним агентам, таким, як анти Igm, індукувати клітинну відповідь, таку як експресія поверхневого маркера, звичайно від однієї години до одного тижня. In vitro аналіз може здійснюватися при використанні культивованих клітин, отриманих із крові або зі зразка біопсії. Кількість експресованого поверхневого маркера оцінюють за допомогою проточної цитометрії при використанні специфічних антитіл, які впізнають маркер. Доза змінюється залежно від використовуваної специфічної сполуки, специфічного захворювання, стану пацієнта, і т. д. Терапевтична доза типово є достатньою для того, щоб значно зменшити чисельність небажаної клітинної популяції в цільовій тканині при підтримці життєздатності пацієнта. Лікування в загальному випадку триває до виникнення значного зниження, наприклад, зниження, яке становить, принаймні, 50 % клітинного навантаження, і може тривати до відсутності істотного виявлення небажаних клітин в організмі. ВІДОМИЙ РІВЕНЬ ТЕХНІКИ Інші піролопіразинони описані як антагоністи рецептора V1b і як проміжні сполуки для одержання цих сполук в WO 2009/130231 A1 та в WO 2009/130232 A1. Інші піразолопіразинони описані як проміжні сполуки для одержання інгібіторів GSK3 в WO 2009/007029 A1. Інші піразолопіразинони описані як проміжні сполуки для одержання інгібіторів кінази PI3 в WO 2011/089400 A1. СТИСЛИЙ ВИКЛАД СУТІ ВИНАХОДУ Винахід відноситься до сполук формули I O NH 1 R 35 40 45 50 55 X N I Y в якій 1 R являє собою H, F, Cl, CN, CH3, CH2OH, CH2Cl, CH2Br, CF3, CHF2 або CH2F, 2 R являє собою H або A, 3 R являє собою H, F, Cl, CH3, CF3 або CHF2, 3 X являє собою CR або N, 1 1 Y являє собою Ar , Carb, Het або Cyc, 1 Ar являє собою феніл або нафтил, який незаміщений або моно-, ди- або тризаміщений за 2 2 2 2 2 2 2 2 допомогою Hal, A, [C(R )2]pOR , [C(R )2]pN(R )2, [C(R )2]pHet , NO2, CN, [C(R )2]pCOOR , 2 2 2 2 2 2 3 2 2 [C(R )2]pCON(R )2, NR COA, NR SO2A, [C(R )2]pSO2N(R )2, S(O)nA, COHet , O[C(R )2]mN(R )2, 2 2 2 2 2 O[C(R )2]pAr , O[C(R )2]pHet , NHCOOA, NHCON(R )2, Cyc, CHO і/або COA, 2 Ar являє собою феніл, який незаміщений або моно- або дизаміщений за допомогою Hal, A, 2 2 2 2 2 3 2 2 2 2 [C(R )2]pOR , [C(R )2]pN(R )2, [C(R )2]pHet , NO2, CN, [C(R )2]pCOOR, [C(R )2]pN(R )2, N(R )2COA, 2 2 2 3 2 2 2 3 NR SO2A, [C(R )2]pSO2N(R )2, S(O)nA, COHet , O[C(R )2]mN(R )2, O[C(R )2]pHet , NHCOOA, 2 NHCON(R )2, CHO і/або COA, 1 Het являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3-бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з яких 2 UA 112795 C2 2 5 10 15 20 25 30 35 2 2 2 незаміщений або моно- або дизаміщений за допомогою Hal, A, [C(R )2]pOR , [C(R )2]pN(R )2, 2 2 2 2 2 2 2 2 2 2 [C(R )2]pHet , [C(R )2]pAr , NO2, CN, [C(R )2]pCOOR , [C(R )2]pCON(R )2, NR COA, NR SO2A, 2 2 3 2 2 2 2 2 2 [C(R )2]pSO2N(R )2, S(O)nA, COHet , O[C(R )2]mN(R )2, O[C(R )2]pAr , O[C(R )2]pHet , NHCOOA, 2 NHCON(R )2, CHO, COA, =S, =NR і/або =O, Carb являє собою інданіл або тетрагідронафтил, кожний з яких може бути незаміщений або моно-, ди-, три- або тетразаміщений за допомогою А, Cyc являє собою циклічний алкіл, який має 3, 4, 5, 6 або 7 атомів C, який може бути 2 2 незаміщений або монозаміщений за допомогою А, OH, Hal, CN або Ar або Het , 2 Het являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3-бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з яких 2 2 2 2 незаміщений або моно- або дизаміщений за допомогою Hal, A, [C(R )2]pOR , [C(R )2]pN(R )2, 2 3 2 3 2 2 2 2 2 2 2 [C(R )2]pHet , [C(R )2]pOHet , [C(R )2]pAr , NO2, CN, [C(R )2]pCOOR , [C(R )2]pCON(R )2, NR COA, 2 2 2 3 2 2 2 2 2 3 NR SO2A, [C(R )2]pSO2N(R )2, S(O)nA, COHet , O[C(R )2]mN(R )2, O[C(R )2]pAr , O[C(R )2]pHet , 2 NHCOOA, NHCON(R )2, CHO, COA, =S, =NR і/або =O, 3 Het являє собою дигідропіроліл, піролідиніл, азетидиніл, оксетаніл, тетрагідроімідазоліл, дигідропіразоліл, тетрагідропіразоліл, тетрагідрофураніл, дигідропіридил, тетрагідропіридил, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, тетрагідропіраніл або піперазиніл, кожний з яких незаміщений або моно- або дизаміщений за 2 2 2 допомогою Hal, CN, OR , COOR , CON(R )2, S(O)nA, S(O)nAr, COA, A і/або =O, A являє собою нерозгалужений або розгалужений алкіл, який має 1-10 атомів C, де дві розташовані поруч CH- і/або CH2-групи можуть утворювати подвійний зв'язок і де одна або дві CH- і/або CH2-групи, що не розташовані поруч, можуть бути замінені на атоми N-, O- і/або S, і де 1-7 атомів H можуть бути замінені на F або Cl, Hal являє собою F, Cl, Br або I, n являє собою 0, 1 або 2, m являє собою 1, 2 або 3, p являє собою 0, 1, 2, 3 або 4, 1 1 за умови, що, якщо R означає CH2OH, то Ar не означає 2,4-дихлорфеніл, і їх фармацевтично прийнятних сольватів, солей, таутомерів і стереоізомерів, включаючи їх суміші у всіх співвідношеннях. Винахід також відноситься до оптично активних форм (стереоізомерів), енантіомерів, рацематів, діастереомерів і гідратів і сольватів цих сполук. Винахід відноситься до сполук формули I і їх таутомерів формули Ia OH N 1 R 40 45 50 55 X N Ia Y . Крім того, винахід відноситься до фармацевтично прийнятних похідних сполук формули I. Термін сольвати сполук позначає адукти молекул інертного розчинника на сполуках, які утворюються завдяки їх силі взаємного притягання. Сольвати являють собою, наприклад, моноабо дигідрати або алкоголяти. Мається на увазі, що винахід також відноситься до сольватів солей. Термін фармацевтично прийнятні похідні позначає, наприклад, солі сполук відповідно до винаходу й також так звані проліки сполук. Як використовується в даній заявці і якщо спеціально не вказано інакше, термін "проліки" позначає похідну сполуки формули I, яка може бути гідролізована, окиснена або по-іншому реагувати в біологічних умовах (in vitro або in vivo), забезпечуючи активну сполуку, зокрема сполуку формули I. Приклади проліків включають, але не обмежуючись тільки ними, похідні і метаболіти сполуки формули I, які включають здатні біогідролізуватися компоненти, такі як здатні біогідролізуватися аміди, здатні біогідролізуватися складні ефіри, здатні біогідролізуватися карбамати, здатні біогідролізуватися карбонати, здатні біогідролізуватися уреїди, і здатні біогідролізуватися аналоги фосфату. В певних варіантах здійснення, проліки сполук з карбоксильними функціональними групами являють собою нижчі алкілові складні ефіри карбонової кислоти. Карбоксилатні складні ефіри легко утворюються шляхом 3 UA 112795 C2 5 10 15 20 25 етерифікації будь-яких фрагментів карбонової кислоти, присутніх у молекулі. Проліки типово можна одержувати, використовуючи добре відомі методи, такі як методи, описані в Burger 's Medicinal Chemistry and Drug Discovery 6-е вид. (Donald J. Abraham ред., 2001, Wiley) і Design and Application of Prodrugs (H.Bundgaard ред., 1985, Harwood Academic Publishers Gmfh). Вираз "ефективна кількість" позначає кількість лікарського засобу або фармацевтичного активного компонента, яка викликає в тканині, системі, тварині або людині біологічну або медичну реакцію відповіді, яку передбачає або бажає отримати, наприклад, дослідник або лікар. Додатково, вираз "терапевтично ефективна кількість" означає ту кількість, яка має наступні наслідки в порівнянні з відповідним суб'єктом, який не одержував цієї кількості: поліпшення лікування, вилікування, запобігання або елімінація захворювання, синдрому, стану, скарги, розладу або побічних дій, або також зменшення прогресування захворювання, скарги або розладу. Термін "терапевтично ефективна кількість" також охоплює кількості, які ефективні для підвищення нормальної фізіологічної функції. Винахід також відноситься до застосування сумішей сполук формули I, наприклад, сумішей двох діастереомерів, наприклад, в співвідношенні 1:1, 1:2, 1:3, 1:4, 1:5, 1:10, 1:100 або 1:1000. Особливо кращими є суміші стереоізомерних сполук. "Таутомери" відносяться до ізомерних форм сполуки, які знаходяться у рівновазі одна з одною. Концентрації ізомерних форм будуть залежати від оточення, у якому знаходиться сполука, і можуть відрізнятися залежно від того, наприклад, чи буде сполука являти собою тверду речовину або знаходитися в органічному або водному розчині. Винахід відноситься до сполук формули I і їх солей та до способу одержання сполук формули I і їх фармацевтично прийнятних солей, сольватів, таутомерів і стереоізомерів, який відрізняється тим, що a) сполуку формули II O A' O 1 R X N O II Y 1 30 в якій R , X і Y мають значення, зазначені в пункті 1, і A' являє собою нерозгалужений або розгалужений алкіл, який має 1, 2, 3 або 4 атоми C, піддають реакції з NH3, NH4OAc або (NH4)2CO3, або b) сполуку формули III N 1 R X III N O Y 1 35 40 в якій R , X і Y мають значення, зазначені в пункті 1, циклізують за допомогою H2O2 за основних умов, або 1 1 c) радикал R і/або Y перетворюють на інший радикал R і/або Y шляхом i) перетворення COOH або CHO на H, ii) перетворення складноефірної групи на спиртову групу, iii) перетворення галогенованого фенільного кільця в реакції сполучення Сузукі на ариловане фенільне кільце, iv) перетворення галогенованої алкільної групи на алкільну групу, або 4 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 d) сполуку формули I вивільняють з однієї із її функціональних похідних шляхом обробки сольволізуючим або гідрогенолізуючим агентом, і/або основу або кислоту формули I перетворюють на одну з його(її) солей. 1 Вище і нижче радикали R , X і Y мають значення, вказані для формули I, якщо спеціально не вказано інше. A являє собою алкіл, який є нерозгалуженим (лінійним) або розгалуженим, і має 1, 2, 3, 4, 5, 6, 7, 8, 9 або 10 атомів C. A переважно являє собою метил, крім того, етил, пропіл, ізопропіл, бутил, ізобутил, втор-бутил або трет-бутил, крім того, також пентил, 1-, 2- або 3-метилбутил, 1,1-, 1,2- або 2,2-диметилпропіл, 1-етилпропіл, гексил, 1-, 2-, 3- або 4-метилпентил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- або 3,3-диметилбутил, 1- або 2-етилбутил, 1-етил-1-метилпропіл, 1-етил-2метилпропіл, 1,1,2- або 1,2,2-триметилпропіл, крім того, переважно, наприклад, трифторметил. A особливо бажано являє собою алкіл, який має 1, 2, 3, 4, 5 або 6 атомів C, переважно метил, етил, пропіл, ізопропіл, бутил, ізобутил, втор-бутил, трет-бутил, пентил, гексил, трифторметил, пентафторетил або 1,1,1-трифторетил. Крім того, A являє собою переважно CH2OCH3, CH2CH2OH або CH2CH2OCH3. Циклічний алкіл має 3-7 атомів C, переважно являє собою циклопропіл, циклобутил, циклопентил, циклогексил або циклогептил. 1 Ar являє собою переважно o-, м- або п-толіл, o-, м- або п-етилфеніл, o-, м- або ппропілфеніл, o-, м- або п-ізопропілфеніл, o-, м- або п-трет-бутилфеніл, o-, м- або пгідроксифеніл, o-, м- або п-нітрофеніл, o-, м- або п-амінофеніл, o-, м- або п-(Nметиламіно)феніл, o-, м- або п-(N-метиламінокарбоніл)феніл, o-, м- або п-метоксифеніл, o-, мабо п-етоксифеніл, o-, м- або п-етоксикарбонілфеніл, o-, м- або п-(N,N-диметиламіно)феніл, o-, м- або п-(N,N-диметиламінокарбоніл)феніл, o-, м- або п-(N-етиламіно)феніл, o-, м- або п-(N,Nдіетиламіно)феніл, o-, м- або п-фторфеніл, o-, м- або п-бромфеніл, o-, м- або п-хлорфеніл, o-, мабо п-(метилсульфонамідо)феніл, o-, м- або п-(метилсульфоніл)феніл, o-, м- або п-ціанофеніл, o-, м- або п-карбоксифеніл, o-, м- або п-метоксикарбонілфеніл, o-, м- або п-формілфеніл, o-, мабо п-ацетилфеніл, o-, м- або п-аміносульфонілфеніл, o-, м- або п-[2-(морфолін-4іл)етокси]феніл, o-, м- або п-[3-(N,N-діетиламіно)пропокси]феніл, крім того, бажано 2,3-, 2,4-, 2,5-, 2,6-, 3,4- або 3,5-дифторфеніл, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- або 3,5-дихлорфеніл, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- або 3,5-дибромфеніл, 2,4- або 2,5-динітрофеніл, 2,5- або 3,4-диметоксифеніл, 3-нітро4-хлорфеніл, 3-аміно-4-хлор-, 2-аміно-3-хлор-, 2-аміно-4-хлор-, 2-аміно-5-хлор- або 2-аміно-6хлорфеніл, 2-нітро-4-N, N-диметиламіно- або 3-нітро-4-N,N-диметиламінофеніл, 2,3діамінофеніл, 2,3,4-, 2,3,5-, 2,3,6-, 2,4,6- або 3,4,5-трихлорфеніл, 2,4,6-триметоксифеніл, 2гідрокси-3,5-дихлорфеніл, п-йодфеніл, 3,6-дихлор-4-амінофеніл, 4-фтор-3-хлорфеніл, 2-фтор-4бромфеніл, 2,5-дифтор-4-бромфеніл, 3-бром-6-метоксифеніл, 3-хлор-6-метоксифеніл, 3-хлор-4ацетамідофеніл, 3-фтор-4-метоксифеніл, 3-аміно-6-метилфеніл, 3-хлор-4-ацетамідофеніл або 2,5-диметил-4-хлорфеніл. 1 Ar , крім того, бажано являє собою феніл, який незаміщений або моно-, ди- або 2 2 2 2 2 2 тризаміщений за допомогою Hal, A, [C(R )2]pOR , [C(R )2]pN(R )2, [C(R )2]pHet , NO2, Cyc, 2 2 2 2 2 2 [C(R )2]pCOOR , O[C(R )2]pAr і/або O[C(R )2]pHet . 2 Ar являє собою переважно o-, м- або п-толіл, o-, м- або п-етилфеніл, o-, м- або ппропілфеніл, o-, м- або п-ізопропілфеніл, o-, м- або п-трет-бутилфеніл, o-, м- або пгідроксифеніл, o-, м- або п-нітрофеніл, o-, м- або п-амінофеніл, o-, м- або п-(Nметиламіно)феніл, o-, м- або п-(N-метиламінокарбоніл)феніл, o-, м- або п-метоксифеніл, o-, мабо п-етоксифеніл, o-, м- або п-етоксикарбонілфеніл, o-, м- або п-(N,N-диметиламіно)феніл, o-, м- або п-(N,N-диметиламінокарбоніл)феніл, o-, м- або п-(N-етиламіно)феніл, o-, м- або п-(N, Nдіетиламіно)феніл, o-, м- або п-фторфеніл, o-, м- або п-бромфеніл, o-, м- або п-хлорфеніл, o-, мабо п-(метилсульфонамідо)феніл, o-, м- або п-(метилсульфоніл)феніл, o-, м- або п-ціанофеніл, o-, м- або п-карбоксифеніл, o-, м- або п-метоксикарбонілфеніл, o-, м- або п-формілфеніл, o-, мабо п-ацетилфеніл, o-, м- або п-аміносульфонілфеніл, o-, м- або п-[2-(морфолін-4іл)етокси]феніл, o-, м- або п-[3-(N, N-діетиламіно)пропокси]феніл, крім того, бажано 2,3-, 2,4-, 2,5-, 2,6-, 3,4- або 3,5-дифторфеніл, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- або 3,5-дихлорфеніл, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- або 3,5-дибромфеніл, 2,4- або 2,5-динітрофеніл, 2,5- або 3,4-диметоксифеніл, 3-нітро4-хлорфеніл, 3-аміно-4-хлор-, 2-аміно-3-хлор-, 2-аміно-4-хлор-, 2-аміно-5-хлор- або 2-аміно-6хлорфеніл, 2-нітро-4-N, N-диметиламіно- або 3-нітро-4-N, N-диметиламінофеніл, 2,3діамінофеніл, 2,3,4-, 2,3,5-, 2,3,6-, 2,4,6- або 3,4,5-трихлорфеніл, 2,4,6-триметоксифеніл, 2гідрокси-3,5-дихлорфеніл, п-йодфеніл, 3,6-дихлор-4-амінофеніл, 4-фтор-3-хлорфеніл, 2-фтор-4бромфеніл, 2,5-дифтор-4-бромфеніл, 3-бром-6-метоксифеніл, 3-хлор-6-метоксифеніл, 3-хлор-4 5 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 60 ацетамідофеніл, 3-фтор-4-метоксифеніл, 3-аміно-6-метилфеніл, 3-хлор-4-ацетамідофеніл або 2,5-диметил-4-хлорфеніл. 2 Ar , крім того, бажано являє собою феніл, який незаміщений або монозаміщений за 2 2 допомогою [C(R )2]pOR . 1 Het переважно являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з 2 2 2 2 яких незаміщений або моно- або дизаміщений за допомогою A, [C(R )2]pOR , [C(R )2]pHet і/або 2 2 [C(R )2]pAr . 1 Het особливо бажано являє собою піролідиніл, піперидиніл, морфолініл, піразоліл, піридил, піримідил або 1,3-бензодіоксоліл, кожний з яких незаміщений або моно- або дизаміщений за 2 2 2 2 2 2 допомогою A, [C(R )2]pOR , [C(R )2]pHet і/або [C(R )2]pAr . 2 Het переважно являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з 2 2 2 3 яких незаміщений або моно- або дизаміщений за допомогою A, [C(R )2]pOR , [C(R )2]pHet і/або 2 3 [C(R )2]pOHet . 2 Het особливо бажано являє собою піролідиніл, піперидиніл, морфолініл, піразоліл, оксазоліл, ізоксазоліл або оксадіазоліл, кожний з яких незаміщений або моно- або дизаміщений 2 2 2 3 2 3 за допомогою A, [C(R )2]pOR , [C(R )2]pHet і/або [C(R )2]pOHet . 3 Het переважно являє собою дигідропіроліл, піролідиніл, азетидиніл, оксетаніл, тетрагідроімідазоліл, дигідропіразоліл, тетрагідропіразоліл, тетрагідрофураніл, дигідропіридил, тетрагідропіридил, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, тетрагідропіраніл або піперазиніл. 3 Het особливо бажано являє собою піролідиніл, піперидиніл, морфолініл або тетрагідропіраніл. Hal переважно являє собою F, Cl або Br, а також I, особливо краще F або Cl. Для всього винаходу, всі радикали, які зустрічаються більше одного разу, можуть бути однаковими або різними, тобто вони незалежні один від одного. Сполуки формули I можуть мати один або декілька хіральних центрів і тому можуть зустрічатися в різних стереоізомерних формах. Формула I охоплює всі ці форми. Відповідно, винахід відноситься, зокрема, до сполук формули I, в яких принаймні один із зазначених радикалів має одне з кращих значень, зазначених вище. Деякі кращі групи сполук можуть бути зображені за допомогою наступних підформул Ia-Ig, які відповідають формулі I і в яких радикали, не визначені більш детально, мають значення, вказані для формули I, але в яких 1 в Ia Ar являє собою феніл, який незаміщений або моно-, ди- або тризаміщений за 2 2 2 2 2 2 2 2 допомогою Hal, A, [C(R )2]pOR , [C(R )2]pN(R )2, [C(R )2]pHet , NO2, Cyc, [C(R )2]pCOOR , 2 2 2 2 O[C(R )2]pAr і/або O[C(R )2]pHet ; 2 в Ib Ar являє собою феніл, який незаміщений або монозаміщений за допомогою 2 2 [C(R )2]pOR ; 1 в Ic Het являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3-бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з яких 2 2 2 2 незаміщений або моно- або дизаміщений за допомогою A, [C(R )2]pOR , [C(R )2]pHet і/або 2 2 [C(R )2]pAr ; 2 в Id Het являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3-бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з яких 6 UA 112795 C2 2 5 10 15 20 25 30 35 40 45 50 55 60 2 2 3 незаміщений або моно- або дизаміщений за допомогою A, [C(R )2]pOR , [C(R )2]pHet і/або 2 3 [C(R )2]pOHet ; 3 в Ie Het являє собою дигідропіроліл, піролідиніл, азетидиніл, оксетаніл, тетрагідроімідазоліл, дигідропіразоліл, тетрагідропіразоліл, тетрагідрофураніл, дигідропіридил, тетрагідропіридил, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, тетрагідропіраніл або піперазиніл; 1 в If R являє собою H, F, Cl, CN CH3, CH2OH, CH2Cl, CH2Br, CF3, CHF2 або CH2F, 2 R являє собою H або A, 3 R являє собою H, F, Cl, CH3, CF3 або CHF2, 3 X являє собою CR або N, 1 1 Y являє собою Ar , Carb, Het або Cyc, 1 Ar являє собою феніл, який незаміщений або моно-, ди- або тризаміщений за допомогою 2 2 2 2 2 2 2 2 2 2 Hal, A, [C(R )2]pOR , [C(R )2]pN(R )2, [C(R )2]pHet , NO2, Cyc, [C(R )2]pCOOR , O[C(R )2]pAr і/або 2 2 O[C(R )2]pHet , 2 2 2 Ar являє собою феніл, який незаміщений або монозаміщений за допомогою [C(R )2]pOR , 1 Het являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3-бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з яких 2 2 2 2 незаміщений або моно- або дизаміщений за допомогою A, [C(R )2]pOR , [C(R )2]pHet і/або 2 2 [C(R )2]pAr , Carb являє собою інданіл або тетрагідронафтил, кожний з яких може бути незаміщений або моно-, ди-, три- або тетразаміщений за допомогою А, Cyc являє собою циклічний алкіл, який має 3, 4, 5, 6 або 7 атомів C, який може бути 2 2 незаміщений або монозаміщений за допомогою А, OH, Hal, CN або Ar або Het , 2 Het являє собою піролідиніл, азетидиніл, тетрагідроімідазоліл, тетрагідрофураніл, тетрагідропіразоліл, тетрагідропіраніл, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, піперазиніл, фурил, тієніл, піроліл, імідазоліл, піразоліл, оксазоліл, ізоксазоліл, оксадіазоліл, тіазоліл, триазоліл, тетразоліл, піридил, піримідил, піридазиніл, індоліл, ізоіндоліл, бензімідазоліл, індазоліл, хіноліл, 1,3-бензодіоксоліл, бензотіофеніл, бензофураніл, імідазопіридил або фуро[3,2-b]піридил, кожний з яких 2 2 2 3 незаміщений або моно- або дизаміщений за допомогою A, [C(R )2]pOR , [C(R )2]pHet і/або 2 3 [C(R )2]pOHet , 3 Het являє собою дигідропіроліл, піролідиніл, азетидиніл, оксетаніл, тетрагідроімідазоліл, дигідропіразоліл, тетрагідропіразоліл, тетрагідрофураніл, дигідропіридил, тетрагідропіридил, піперидиніл, морфолініл, гексагідропіридазиніл, гексагідропіримідиніл, [1,3]діоксоланіл, тетрагідропіраніл або піперазиніл, A являє собою нерозгалужений або розгалужений алкіл, який має 1-10 атомів C, де дві розташовані поруч CH- і/або CH2-групи можуть утворювати подвійний зв'язок і де одна або дві CH- і/або CH2-групи, що не розташовані поруч, можуть бути замінені на атоми N-, O- і/або S, і де 1-7 атомів H можуть бути замінені на F або Cl, Hal являє собою F, Cl, Br або I, p являє собою 0, 1, 2, 3 або 4, 1 1 за умови, що, якщо R означає CH2OH, то Ar не означає 2,4-дихлорфеніл; 1 в Ig R являє собою H, F, Cl, CN, CH3, CH2OH, CH2Cl, CH2Br, CF3, CHF2 або CH2F, 2 R являє собою H або A, 3 R являє собою H, F, Cl, CH3, CF3 або CHF2, 3 X являє собою CR або N, 1 1 Y являє собою Ar , Carb, Het або Cyc, 1 Ar являє собою феніл, який незаміщений або моно-, ди- або тризаміщений за допомогою 2 2 2 2 2 2 2 2 2 2 Hal, A, [C(R )2]pOR , [C(R )2]pN(R )2, [C(R )2]pHet , NO2, Cyc, [C(R )2]pCOOR , O[C(R )2]pAr і/або 2 2 O[C(R )2]pHet , 2 2 2 Ar являє собою феніл, який незаміщений або монозаміщений за допомогою [C(R )2]pOR , 1 Het являє собою піролідиніл, піперидиніл, морфолініл, піразоліл, піридил, піримідил або 1,3-бензодіоксоліл, кожний з яких незаміщений або моно- або дизаміщений за допомогою A, 2 2 2 2 2 2 [C(R )2]pOR , [C(R )2]pHet і/або [C(R )2]pAr , Carb являє собою інданіл або тетрагідронафтил, кожний з яких може бути незаміщений або моно-, ди-, три- або тетразаміщений за допомогою А, 7 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 60 Cyc являє собою циклічний алкіл, який має 3, 4, 5, 6 або 7 атомів C, який може бути 2 2 незаміщений або монозаміщений за допомогою А, OH, Hal, CN або Ar або Het , 2 Het являє собою піролідиніл, піперидиніл, морфолініл, піразоліл, оксазоліл, ізоксазоліл або оксадіазоліл, кожний з яких незаміщений або моно- або дизаміщений за допомогою A, 2 2 2 3 2 3 [C(R )2]pOR , [C(R )2]pHet і/або [C(R )2]pOHet , 3 Het являє собою піролідиніл, піперидиніл, морфолініл або тетрагідропіраніл, A являє собою нерозгалужений або розгалужений алкіл, який має 1-10 атомів C, де дві розташовані поруч CH- і/або CH2-групи можуть утворювати подвійний зв'язок і де одна або дві CH- і/або CH2-групи, що не розташовані поруч, можуть бути замінені на атоми O, і де 1-7 атомів H можуть бути замінені на F або Cl, Hal являє собою F, Cl, Br або I, p являє собою 0, 1, 2, 3 або 4, 1 1 за умови, що, якщо R означає CH2OH, то Ar не означає 2,4-дихлорфеніл, і включають їх фармацевтично прийнятні солі, сольвати, таутомери і стереоізомери, включаючи їх суміші у всіх співвідношеннях. Сполуки формули I, а також вихідні речовини для їх одержання можуть, крім того, бути одержані за допомогою методів, відомих per se, як описано в літературі (наприклад, в стандартних роботах, таких як Hоuben-Weyl, Methoden der organischen Chemie [Методи органічної хімії], Georg-Thieme-Verlag, Штутгарт) за умов реакцій, які відомі та є придатними для зазначених реакцій. Також при цьому можна застосовувати різноманітні модифікації, які відомі per se, але про які тут докладно не згадується. Вихідні сполуки формули II і формули III, як правило, відомі. Проте, якщо вони є новими, то їх можна одержати за допомогою методів, відомих per se. Сполуки формули I переважно можна одержати за реакцією сполуки формули II з NH 3, NH4OAc або (NH4)2CO3. Залежно від застосовуваних умов, час реакції знаходиться в інтервалі від декількох хвилин до 14 днів, температура реакції знаходиться в рамках між приблизно -10° і 140°, звичайно між 30° і 130°, зокрема між приблизно 60° і приблизно 120°. Реакцію проводять в інертному розчиннику. Прикладами придатних інертних розчинників є вуглеводні, такі як гексан, петролейний ефір, бензол, толуол або ксилол; хлоровані вуглеводні, такі як трихлоретилен, 1,2-дихлоретан, чотирихлористий вуглець, хлороформ або дихлорметан; спирти, такі як метанол, етанол, ізопропанол, н-пропанол, н-бутанол або трет-бутанол; прості ефіри, такі як діетиловий ефір, діізопропіловий ефір, тетрагідрофуран (ТГФ) або діоксан; гліколеві прості ефіри, такі як монометиловий або моноетиловий ефір етиленгліколю, диметиловий ефір етиленгліколю (диглим); кетони, такі як ацетон або бутанон; аміди, такі як ацетамід, диметилацетамід або диметилформамід (ДМФА); нітрили, такі як ацетонітрил; сульфоксиди, такі як диметилсульфоксид (ДМСО); сірковуглець; карбонові кислоти, такі як мурашина кислота або оцтова кислота; нітросполуки, такі як нітрометан або нітробензол; складні ефіри, такі як етилацетат, або суміші вищезазначених розчинників. Особливу перевагу надають метанолу або оцтовій кислоті. Крім того, сполуки формули I переважно можна одержати за реакцією сполуки формули III з H2O2 за основних умов. Реакцію проводять в інертному розчиннику, за присутності гідроксиду лужного або лужноземельного металу, карбонату або бікарбонату або іншої солі слабкої кислоти і лужного або лужноземельного металу, переважно калію, натрію, кальцію або цезію. Залежно від застосовуваних умов, час реакції знаходиться в інтервалі від декількох хвилин до 14 днів, температура реакції знаходиться в рамках між приблизно -10° і 140°, звичайно між 30° і 130°, зокрема між приблизно 60° і приблизно 120°. Прикладами придатних інертних розчинників є вуглеводні, такі як гексан, петролейний ефір, бензол, толуол або ксилол; хлоровані вуглеводні, такі як трихлоретилен, 1,2-дихлоретан, чотирихлористий вуглець, хлороформ або дихлорметан; спирти, такі як метанол, етанол, ізопропанол, н-пропанол, н-бутанол або трет-бутанол; прості ефіри, такі як діетиловий ефір, діізопропіловий ефір, тетрагідрофуран (ТГФ) або діоксан; гліколеві прості ефіри, такі як монометиловий або моноетиловий ефір етиленгліколю, диметиловий ефір етиленгліколю (диглим); кетони, такі як ацетон або бутанон; аміди, такі як ацетамід, диметилацетамід або диметилформамід (ДМФА); нітрили, такі як ацетонітрил; сульфоксиди, такі як диметилсульфоксид (ДМСО); сірковуглець; карбонові кислоти, такі як мурашина кислота або оцтова кислота; нітросполуки, такі як нітрометан або нітробензол; складні ефіри, такі як етилацетат, або суміші вищезазначених розчинників. 8 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 60 Особливу перевагу надають CH2Cl2 і воді або метанолу і диметилсульфоксиду. 1 Сполуки формули I, крім того, можна одержати шляхом перетворення радикала R і/або Y 1 на інший радикал R і/або Y шляхом i) перетворення COOH або CHO на H, ii) перетворення складноефірної групи на спиртову групу, iii) перетворення галогенованого фенільного кільця в реакції сполучення Сузукі на ариловане фенільне кільце, iv) перетворення галогенованої алкільної групи на алкільну групу. Стадія i): Перетворення COOH групи на H переважно проводять за допомогою мідного порошку за основних умов, переважно в органічному розчиннику; переважно в хіноліні за стандартних умов. Перетворення CHO групи на H переважно проводять в інертному розчиннику, переважно в диметиловому ефірі діетиленгліколю, за присутності 3дифенілфосфанілпропіл(дифеніл)фосфану і хлориду родію(III) за стандартних умов. Стадія ii): Перетворення складноефірної групи на спиртову групу переважно проводять за присутності хлориду церію(III) за допомогою алкілмагнійхлориду в ТГФ за стандартних умов або за допомогою алюмогідриду літію в ТГФ. Стадія iii): Перетворення галогенованого фенільного кільця на ариловане фенільне кільце, проводять за умов, стандартних для сполучення Сузукі. Стадія iv): Перетворення галогенованої алкільної групи на алкільну групу переважно проводять за допомогою LiAlH4 в ТГФ або за допомогою цинку в оцтовій кислоті за стандартних умов. Сполуки формули I, крім того, можна одержати шляхом вивільнення сполук формули I з однієї з їх функціональних похідних шляхом обробки сольволізуючим або гідрогенолізуючим агентом. Кращі вихідні речовини для сольволізу або гідрогенолізу являють собою речовини, які відповідають формулі I, але містять відповідні захищені аміно і/або гідроксильні групи замість однієї або декількох вільних аміно і/або гідроксильних груп, переважно, речовини, які несуть аміно-захисну групу замість атома H, зв'язаного з атомом N, зокрема речовини, які несуть R'-N групу, в якій R' означає аміно-захисну групу замість HN групи, і/або речовини, які несуть гідроксил-захисну групу замість атома H гідроксильної групи, наприклад, речовини, які відповідають формулі I, але несуть -COOR" групу, в якій R" означає гідроксил-захисну групу, замість -COOH групи. Кращі вихідні речовини також являють собою оксадіазольні похідні, які можуть бути перетворені на відповідні амідино сполуки. Також в молекулі вихідної речовини може бути присутньою множина – однакових або різних – захищених аміно і/або гідроксильних груп. Якщо присутні захисні групи відрізняються одна від одної, вони в багатьох випадках можуть бути відщеплені селективно. Термін "аміно-захисна група" відомий в загальних рисах і відноситься до груп, які придатні для захисту (блокування) аміногрупи від хімічних реакцій, але які легко видалити після проведення бажаної хімічної реакції в іншій частині молекули. Типовими такими групами є, зокрема, незаміщені або заміщені ацильні, арильні, аралкоксиметильні або аралкільні групи. Крім того, оскільки аміно-захисні групи видаляють після бажаної реакції (або послідовності реакцій), їх тип і розмір не є вирішальними; однак, перевага надається групам, що містять 1-20, зокрема 1-8, атомів вуглецю. Термін "ацильна група" слід розуміти в найширшому сенсі у зв'язку з даним способом. Він включає ацильні групи, одержані з аліфатичних, араліфатичних, ароматичних або гетероциклічних карбонових кислот або сульфонових кислот, і, зокрема, алкоксикарбонільні, арилоксикарбонільні і особливо аралкоксикарбонільні групи. Прикладами таких ацильних груп є алканоїл, такий як ацетил, пропіоніл і бутирил; аралканоїл, такий як фенілацетил; ароїл, такий як бензоїл і толіл; арилоксіалканоїл, такий як POA; алкоксикарбоніл, такий як метоксикарбоніл, етоксикарбоніл, 2,2,2-трихлоретоксикарбоніл, BOC (третбутоксикарбоніл) і 2-йодетоксикарбоніл; аралкоксикарбоніл, такий як CBZ ("карбобензокси"), 4метоксибензилоксикарбоніл і FMOC; і арилсульфоніл, такий як Mtr. Кращими аміно-захисними групами є BOC і Mtr, крім того, CBZ, Fmoc, бензил і ацетил. Термін "гідроксил-захисна група" також відомий в загальних рисах і відноситься до груп, які придатні для захисту гідроксильної групи від хімічних реакцій, але легко знімаються після проведення бажаної хімічної реакції в іншій частині молекули. Типовими такими групами є вищезазначені незаміщені або заміщені арильні, аралкільні або ацильні групи, крім того, також 9 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 60 алкільні групи. Природа і розмір гідроксил-захисних груп не є вирішальними, оскільки їх видаляють після бажаної хімічної реакції або послідовності реакцій; перевагу віддають групам, що містять 1-20, зокрема 1-10, атомів вуглецю. Прикладами гідроксил-захисних груп є, серед іншого, бензил, 4-метоксибензил, п-нітробензоїл, п-толуолсульфоніл, трет-бутил і ацетил, причому бензил, тетрагідропіраніл і трет-бутил є особливо кращими. Сполуки формули I вивільняють з їх функціональних похідних - в залежності від використовуваної захисної групи - наприклад, при застосуванні сильних кислот, переважно, при застосуванні ТФО або перхлорної кислоти, а також при застосуванні інших сильних неорганічних кислот, таких як хлористоводнева кислота або сірчана кислота, сильних органічних карбонових кислот, таких як трихлороцтова кислота, або сульфонових кислот, таких як бензол- або п-толуолсульфонова кислота. Присутність додаткового інертного розчинника можлива, але не завжди необхідна. Придатними інертними розчинниками переважно є органічні розчинники, наприклад, карбонові кислоти, такі як оцтова кислота, прості ефіри, такі як тетрагідрофуран або діоксан, аміди, такі як ДМФА, галогеновані вуглеводні, такі як дихлорметан, крім того, також спирти, такі як метанол, етанол або ізопропанол, і вода. Крім того, придатними є суміші вищезазначених розчинників. ТФО переважно використовують в надлишку, без додавання іншого розчинника, а перхлорну кислоту переважно використовують у вигляді суміші оцтової кислоти і 70 %-вої перхлорної кислоти в співвідношенні 9:1. Температури реакцій для відщеплення переважно знаходяться в діапазоні між приблизно 0 і приблизно 50°, переважно між 15 і 30° (кімнатна температура). Групи BOC, OBut і Mtr, наприклад, переважно можна відщепити при використанні ТФО в дихлорметані або при використанні приблизно 3 – 5 н. HCl в діоксані при температурі 15-30°, а FMOC групу можна відщепити при використанні приблизно 5-50 %-вого розчину диметиламіну, діетиламіну або піперидину в ДМФА при температурі 15-30°. Захисні групи, які можуть бути видалені гідрогенолітично (наприклад, CBZ, бензильна група, або при вивільненні амідиногрупи з її оксадіазольної похідної) можуть бути відщеплені, наприклад, шляхом обробки воднем за присутності каталізатора (наприклад, каталізатора на основі благородного металу, такого як паладій, переважно на носії, такому як вугілля). Придатними розчинниками в даному випадку є розчинники, які зазначені вище, зокрема, наприклад, спирти, такі як метанол або етанол, або аміди, такі як ДМФА. Гідрогеноліз звичайно проводять за температур між приблизно 0 і 100° і тисках між приблизно 1 і 200 бар, переважно за температур 20-30° і тисках 1-10 бар. Гідрогеноліз CBZ групи успішно виконують, наприклад, на 5-10 % Pd/C в метанолі або при застосуванні форміату амонію (замість водню) на Pd/C в суміші метанол/ДМФА при 20-30°. Прикладами придатних інертних розчинників є вуглеводні, такі як гексан, петролейний ефір, бензол, толуол або ксилол; хлоровані вуглеводні, такі як трихлоретилен, 1,2-дихлоретан, тетрахлорметан, трифторметилбензол, хлороформ або дихлорметан; спирти, такі як метанол, етанол, ізопропанол, н-пропанол, н-бутанол або трет-бутанол; прості ефіри, такі як діетиловий ефір, діізопропіловий ефір, тетрагідрофуран (ТГФ) або діоксан; гліколеві прості ефіри, такі як монометиловий або моноетиловий ефір етиленгліколю або диметиловий ефір етиленгліколю (диглим); кетони, такі як ацетон або бутанон; аміди, такі як ацетамід, диметилацетамід, Nметилпіролідон (NMP) або диметилформамід (ДМФА); нітрили, такі як ацетонітрил; сульфоксиди, такі як диметилсульфоксид (ДМСО); сірковуглець; карбонові кислоти, такі як мурашина кислота або оцтова кислота; нітросполуки, такі як нітрометан або нітробензол; складні ефіри, такі як етилацетат, або суміші вищезазначених розчинників. Складні ефіри можна омилити, наприклад, застосовуючи оцтову кислоту або застосовуючи NaOH або KOH у воді, суміші вода/ТГФ або вода/діоксан, за температур між 0 і 100°. Вільні аміногрупи, крім того, можна ацилювати звичайним способом, використовуючи хлорангідрид або ангідрид кислоти або алкілувати, використовуючи незаміщений або заміщений алкілгалогенід, або піддаючи реакції з CH 3-C(=NH)-OEt, переважно в інертному розчиннику, такому як дихлорметан або ТГФ і/або за присутності основи, такої як триетиламін або піридин, за температур між -60 і +30°. Фармацевтичні солі й інші форми Сполуки, розкриті у винаході, можуть використовуватися у своїй заключній, несольовій формі. З іншого боку, даний винахід також до застосування таких сполук у формі їх фармацевтично прийнятних солей, які можуть бути одержані за допомогою різноманітних органічних і неорганічних кислот і основ відповідно до способів, добре відомих в даній галузі техніки. Фармацевтично прийнятні форми солей сполук формули I готують, головним чином, при використанні традиційних способів. У випадку, якщо сполука формули I містить групу карбонової кислоти, то її прийнятна сіль може бути утворена за допомогою реакції сполуки із 10 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 60 прийнятною основою для одержання відповідної солі приєднання основи. Прикладами таких основ є гідроксиди лужних металів, включаючи гідроксид калію, гідроксид натрію й гідроксид літію; гідроксиди лужноземельних металів, такі, як гідроксид барію й гідроксид кальцію; алкоксиди лужних металів, наприклад, етанолят калію й пропанолят натрію; а також різні органічні основи, такі, як піперидин, діетанолaмін і N-метилглутамін. Сюди також включені солі алюмінію сполук формули I. Для деяких сполук формули I солі приєднання кислоти можуть бути утворені шляхом обробки вказаних сполук фармацевтично прийнятними органічними й неорганічними кислотами, наприклад, гідрогалогенідами, такими, як гідрохлорид, гідробромід або гідройодид; іншими мінеральними кислотами, і їх відповідними солями такими, як, сульфат, нітрат або фосфат, і ін.; і алкіл- і моноарилсульфонатами, такими, як етансульфонат, толуолсульфонат і бензолсульфонат; і іншими органічними кислотами і їх відповідними солями, такими, як ацетат, трифторацетат, тартрат, малеат, сукцинат, цитрат, бензоат, саліцилат, aскорбат і ін. Таким чином, фармацевтично прийнятні солі приєднання кислоти сполук формули I включають наступні солі, але не обмежуючись тільки ними: ацетат, адипат, aльгінат, aргінат, аспартат, бензоат, бензолсульфонат (безилат), бісульфат, бісульфіт, бромід, бутират, камфорат, камфорсульфонат, каприлат, хлорид, хлорбензоат, цитрат, циклопентанпропіонат, диглюконат, дигідрофосфат, динітробензоат, додецилсульфат, етансульфонат, фумарат, галактерат (зі слизової кислоти), галактуронат, глюкогептаноат, глюконат, глутамат, гліцерофосфат, гемісукцинат, гемісульфат, гептаноат, гексаноат, гіпурат, гідрохлорид, гідробромід, гідройодид, 2-гідроксіетансульфонат, йодид, ізетіонат, ізобутират, лактат, лактобіонат, малат, малеат, малонат, манделат, метафосфат, метансульфонат, метилбензоат, моногідрофосфат, 2-нафталінсульфонат, нікотинат, нітрат, оксалат, олеат, пальмоат, пектинат, персульфат, фенілацетат, 3-фенілпропіонат, фосфат, фосфонат, фталат. Крім того, оснóвні солі сполук відповідно до винаходу включають, але не обмежуючись тільки ними, солі алюмінію, амонію, кальцію, міді, заліза (III), заліза (II), літію, магнію, марганцю (III), марганцю (II), калію, натрію й цинку. Переважними серед перерахованих вище солей є амонійні; солі лужних металів натрію й калію; і солі лужноземельних металів кальцію й магнію. Солі сполук формули I, які мають походження від фармацевтично прийнятних органічних нетоксичних основ, включають, але не обмежуючись тільки ними, солі первинних, вторинних і третинних амінів, заміщених амінів, також включаючи природні заміщені аміни, циклічні аміни й основні іонообмінні смоли, наприклад, аргінін, бетаїн, кофеїн, хлорпрокаїн, холін, N,N'дибензилетилендіамін (бензатин), дициклогексиламін, діетаноламін, діетиламін, 2діетиламіноетанол, 2-диметиламіноетанол, етаноламін, етилендіамін, N-етилморфолін, Nетилпіперидин, глюкамін, глюкозамін, гістидин, гідрабамін, ізопропіламін, лідокаїн, лізин, меглумін, N-метил-d-глюкамін, морфолін, піперазин, піперидин, поліамінні смоли, прокаїн, пурини, теобромін, триетаноламін, триетиламін, триметиламін, трипропіламін і трис(гідроксиметил)метиламін (трометамін). Сполуки відповідно до даного винаходу, які включають основні азотовмісні групи, можуть бути кватернізовані за допомогою таких агентів, як C1-C4-алкілгалогеніди, наприклад, метил-, етил-, ізопропіл- і трет-бутилхлорид, бромід і йодид; ди-C1-C4-алкілсульфати, наприклад, диметил-, діетил- і діамілсульфат; C10-C18-алкілгалогеніди, наприклад, децил-, додецил-, лаурил-, міристил- і стеарилхлорид, бромід і йодид; і арил-C1-C4-алкілгалогеніди, наприклад, бензилхлорид і фенетилбромід. Вказані солі дозволяють одержувати як розчинні у воді, так і розчинні в маслі сполуки відповідно до винаходу. Переважні фармацевтичні солі, вказані вище, включають, але не обмежуючись тільки ними, ацетат, трифторацетат, безилат, цитрат, фумарат, глюконат, гемісукцинат, гіпурат, гідрохлорид, гідробромід, ізетіонат, манделат, меглумін, нітрат, олеат, фосфонат, півалат, фосфат натрію, стеарат, сульфат, сульфосаліцилат, тартрат, тіомалат, тозилат і трометамін. Особливо переважними є гідрохлорид, дигідрохлорид, гідробромід, малеат, мезилат, фосфат, сульфат і сукцинат. Кислотно-адитивні солі оснóвних сполук формули I одержують шляхом приведення в контакт форми вільних основ з достатньою кількістю бажаної кислоти для одержання солі традиційним способом. Вільну основу можна регенерувати шляхом приведення в контакт форми солі з основою й виділення вільної основи традиційним способом. Форми вільної основи до деякої міри відрізняються від своїх відповідних форм солей своїми певними фізичними властивостями, такими, як розчинність у полярних розчинниках, однак у всьому іншому солі є еквівалентними до своїх відповідних форм вільних основ для цілей даного винаходу. Як було вказано, фармацевтично прийнятні солі приєднання основи сполук формули I утворюються з металами або амінами, такими, як лужні метали й лужноземельні метали або органічні аміни. Переважні метали представляють собою натрій, калій, магній і кальцій. 11 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 60 Переважні органічні аміни представляють собою N,N'-дибензилетилендіамін, хлорпрокаїн, холін, діетаноламін, етилендіамін, N-метил-d-глюкамін і прокаїн. Солі приєднання основи кислих сполук відповідно до винаходу одержують шляхом приведення в контакт форми вільної кислоти з достатньою кількістю бажаної основи для одержання солі традиційним способом. Форма вільної кислоти може бути регенерована шляхом приведення в контакт форми солі з кислотою й виділення форми вільної кислоти відомим способом. Форми вільної кислоти до деякої міри відрізняються від своїх відповідних форм солей певними фізичними властивостями, такими, як розчинність у полярних розчинниках, однак у всім іншому солі є еквівалентними до своїх відповідних форм вільних кислот для цілей даного винаходу. Якщо сполука відповідно до винаходу включає більше, ніж одну групу, яка здатна до утворення фармацевтично прийнятних солей цього типу, то винахід також охоплює складені солі. Приклади типових складених форм солей включають, але не обмежуючись тільки ними, бітартрат, діацетат, дифумарат, димеглумін, дифосфат, динатрій і тригідрохлорид. У світлі описаного вище можна побачити, що вираз "фармацевтично прийнятна сіль" у контексті даної заявки призначений для позначення активного компонента, який включає сполуку формули I у формі однієї з її солей, особливо в тому випадку, якщо вказана форма солі забезпечує вказаному активному компоненту поліпшені фармакокінетичні властивості в порівнянні з вільною формою вказаного активного компоненту або будь-якою іншою сіллю вказаного активного компонента, які використовувалися раніше. Фармацевтично прийнятна форма солі активного компоненту може також спочатку забезпечувати бажану фармакокінетичну властивість вказаному активному компоненту, яку він раніше не мав, а також може навіть позитивно впливати на фармакодинаміку вказаного активного компоненту у відношенні його терапевтичної активності в організмі. Ізотопи Далі також передбачається, що сполука формули I включає її ізотопно-мічені форми. Ізотопно-мічена форма сполуки формули I є ідентичною до вказаної сполуки, за винятком того факту, що один або більше атомів вказаної сполуки були заміщені атомом або атомами, які мають атомну масу або атомне число, відмінне від атомної маси або атомного числа згаданого атома, яке звичайно існує в природі. Приклади ізотопів, які є легко доступними комерційно і які можуть бути введені в сполуку формули I відповідно до добре відомих способів, включають 2 3 13 14 15 ізотопи водню, вуглецю, азоту, кисню, фосфору, фтору й хлору, наприклад, H, H, C, C, N, 18 17 31 32 35 18 36 О, О, Р, Р, S, F і CI, відповідно. Сполука формули I, її пролікарська форма або фармацевтично прийнятна сіль, які містять один або більше вказаних вище ізотопів та/або інші ізотопи інших атомів також становлять обсяг даного винаходу. Ізотопно-мічена сполука формули I може використовуватися в ряді способів. Наприклад, мічена ізотопами сполука 3 14 формули I, наприклад, у яку введений радіоактивний ізотоп, такий, як H або C, буде корисною в аналізах дослідження розподілу лікарського засобу та/або субстрату в тканині. Такі 3 14 радіоактивні ізотопи, наприклад, тритій, ( Н) і вуглець-14, ( С), є особливо переважними внаслідок легкого одержання й високої здатності до виявлення. Введення більш важких ізотопів, 2 наприклад, дейтерію ( Н), у сполуку формули I, буде забезпечувати терапевтичні переваги, що ґрунтуються на більшій метаболічній стабільності вказаної сполуки, міченої ізотопами. Більша метаболічна стабільність представляється безпосередньо в підвищенні часу напіврозпаду in vivo або зниженні необхідної дози, що при більшості умов буде становити переважне втілення вказаного винаходу. Мічену ізотопом сполуку формули I звичайно одержують шляхом здійснення процедур, розкритих у схемах синтезу й в описі, що відноситься до них, у розділах, що стосуються прикладів, і способів одержання, описаних у даній заявці, шляхом заміни неміченого ізотопами реагенту його відповідним легко доступним реагентом, міченим ізотопом. 2 Дейтерій ( H) також може бути введений у сполуку формули I з метою зміни окисного метаболізму сполуки шляхом первинного кінетичного ізотопного ефекту. Первинний кінетичний ізотопний ефект являє собою зміну швидкості хімічної реакції, яка відбувається через заміщення ізотопного ядра, що, у свою чергу, викликається зміною енергій основного стану, що необхідно для утворення ковалентного зв'язку після вказаного ізотопного заміщення. Заміщення важким ізотопом буде звичайно приводити до зниження енергії основного стану для хімічного зв'язку, викликаючи, таким чином, зменшення швидкості швидкість-лімітуючого етапу руйнування зв'язку. Коли відбувається руйнування зв'язку в або поблизу ділянки сідлоподібної конфігурації вздовж координати реакції утворення декількох продуктів, коефіцієнт розподілу продуктів може суттєво змінюватися. Наприклад, у випадку, якщо дейтерій зв'язується з атомом вуглецю в положенні, у якому не відбувається обмін, відмінності швидкості k m/kd=2-7 є типовими. Така відмінність у швидкості, яку успішно застосовують до сполуки формули I, чутливої до 12 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 60 окиснення, може в значній мірі впливати на профіль вказаної сполуки in vivo і приводить до поліпшення фармакокінетичних властивостей. У процесі виявлення й удосконалення терапевтичних агентів середній спеціаліст у даній галузі шукає шляхи оптимізації фармакокінетичних параметрів доти, поки не одержить бажані in vitro властивості. Є раціональним припустити, що багато сполук зі слабкими фармакокінетичними профілями є нестійкими до окисного метаболізму. Аналізи in vitro мікросом печінки, які зараз є доступними, забезпечують цінну інформацію про процес окисного метаболізму, що, у свою чергу, дозволяє одержати раціональну модель мічених дейтерієм сполук формули I з поліпшеною стабільністю аж до резистентності до такого окисного метаболізму. Таким чином, одержують значне поліпшення фармакокінетичних профілів сполук формули I, що може бути кількісно виражене у величинах збільшення періоду напіврозпаду in vivo (t/2), у концентрації при максимальному терапевтичному ефекті (С mаx), площею під кривою відповіді на певну дозу (AUC) і F; у величинах зменшення кліренсу, дозі й матеріальних витрат. Наведене далі призначене для ілюстрації сказаного вище: сполуку формули I, яка має численні потенційні сайти для окисного метаболізму, наприклад, атоми водню бензилу й атоми водню, з'єднані з атомом азоту, одержують як серії аналогів, у яких різні комбінації атомів водню заміняються атомами дейтерію так, що деякі, більшість або всі вказані атоми водню заміняються на атоми дейтерію. Визначення періоду напіврозпаду забезпечує підходяще й точне визначення ступеня поліпшення резистентності до окисного метаболізму. У такий спосіб визначають, що період напіврозпаду вихідної сполуки може бути продовжений аж до 100 % як результат такого заміщення водню дейтерієм. Заміщення водню дейтерієм у сполуці формули I може також використовуватися для досягнення сприятливої зміни в профілі метаболіту вихідної сполуки як шляхів зменшення або усунення небажаних токсичних метаболітів. Наприклад, коли токсичний метаболіт виникає при окисному розщепленні вуглець-водневого зв'язку С-Н, то з достатньою ймовірністю передбачається, що мічений дейтерієм аналог значно зменшить або усуне вироблення небажаного метаболіту, навіть у випадку, коли окреме окиснення не є швидкість-лімітуючим етапом. Крім того, інформація, що відноситься до рівня техніки відносно заміщення водню дейтерієм, може бути знайдена в Hanzlik і ін., J. Org. Chem. 55, 3992-3997, 1990; Reider і ін., J. Org. Chem. 52, 3326-3334, 1987; Foster, Adv. Drug Res. 14, 1-40, 1985; Gillette і ін., Biochemistry 33 (10) 2927-2937, 1994; і Jarman і ін. Carcinogenesis 16 (4), 683-688, 1993. Крім того, винахід відноситься до лікарських засобів, що містять принаймні одну сполуку формули I та/або їх фармацевтично прийнятні похідні, сольвати й стереоізомери, включаючи їх суміші у всіх співвідношеннях, і необов'язково наповнювачі та/або допоміжні речовини. Фармацевтичні склади можуть вводитися у вигляді дозованих одиниць, які містять заздалегідь установлену кількість активного компоненту на дозовану одиницю. Така одиниця може включати, наприклад, від 0,5 мг до 1 г, переважно від 1 мг до 700 мг, більш переважно від 5 мг до 100 мг, сполуки відповідно до винаходу, залежно від стану, що піддається лікуванню, способу введення, а також віку, ваги тіла й стану пацієнта, або фармацевтичні склади можуть вводитися у вигляді дозованих одиниць, які містять заздалегідь установлену кількість активного компоненту на дозовану одиницю. Переважними дозованими одиницями лікарських препаратів є ті, які містять добову дозу або частину добової дози, як вказано вище, або відповідну порцію їх активного компонента. Фармацевтичні склади цього типу також можуть бути одержані способом, який добре відомий в галузі фармацевтики. Фармацевтичні склади можуть адаптуватися для введення за допомогою будь-якого підходящого способу, наприклад, шляхом перорального (включаючи букальне або під'язичне), ректального, назального, місцевого (включаючи букальне, під'язичне або трансдермальне), вагінального або парентерального (включаючи підшкірне, внутрішньом'язове, внутрішньовенне або внутрішньошкірне) введення. Такі препарати можуть бути приготовлені за допомогою будьякого способу, відомого в галузі фармацевтики, наприклад, шляхом об'єднання активного компоненту з наповнювачем(ами) або допоміжним(ими) речовиною(ами). Фармацевтичні склади, адаптовані для перорального введення, можуть вводитися у вигляді окремих одиниць, таких як, наприклад, капсули або таблетки; порошки або гранули; розчини або суспензії у водних або неводних рідинах; харчових пін або пінистих харчових продуктів; або рідких емульсій масло-в-воді або рідких емульсій вода-в-маслі. Так, наприклад, у випадку перорального введення у вигляді таблетки або капсули, активний компонент може бути об'єднаний з пероральним, нетоксичним і фармацевтично прийнятним інертним наповнювачем, таким як, наприклад, етанол, гліцерин, вода й т. п. Порошки одержують шляхом подрібнення сполуки до підходящого невеликого розміру й змішування її з фармацевтичним наповнювачем, подрібненим аналогічним способом, таким як, наприклад, 13 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 60 харчовий вуглеводень, такий як, наприклад, крохмаль або маніт. Також можна додавати ароматизатор, консервант, диспергуючу речовину й барвник. Капсули одержують шляхом приготування порошкової суміші, як описано вище, і заповнюють нею желатинові капсули певної форми. Перед заповненням капсул до порошкової суміші можна додавати ковзні й змащувальні речовини, такі як, наприклад, високодисперсна кремнієва кислота, тальк, стеарат магнію, стеарат кальцію або поліетиленгліколь у твердій формі. Для поліпшення доступності лікарського засобу, укладеного в капсулу, також можна додавати дезінтегруючу речовину або солюбілізатор, такий як, наприклад, агар-агар, карбонат кальцію або карбонат натрію. Додатково, якщо це є бажаним або необхідним, у суміш також можна додавати підходящі сполучні, змащувальні речовини, дезінтегратори, а також барвники. Підходящими сполучними є крохмаль, желатин, природні цукри, такі як, наприклад, глюкоза або бета-лактоза, підсолоджувачі, приготовлені з кукурудзи, природних і синтетичних смол, такі як, наприклад, аравійська камедь, трагакантова камедь або альгінат натрію, карбоксиметилцелюлоза, поліетиленгліколь, воски й т. п. Змащувальні речовини, які можуть застосовуватися в таких дозованих формах, включають олеат натрію, стеарат натрію, стеарат магнію, бензоат натрію, ацетат натрію, хлорид натрію й т. п. Дезінтегратори включають, але не обмежуючись тільки ними, крохмаль, метилцелюлозу, агар, бентоніт, ксантанову камедь і т. п. Лікарські засоби у вигляді таблеток одержують, наприклад, шляхом приготування порошкової суміші, гранулювання або сухого пресування суміші, додавання змащувальної речовини й дезінтегратора й пресування одержаної суміші в таблетки. Порошкову суміш готують шляхом змішування сполуки, подрібненої підходящим чином, з розріджувачем або основою, як описано вище, і необов'язково зі сполучним, таким як, наприклад, карбоксиметилцелюлоза, альгінат, желатин або полівінілпіролідон, сповільнювачем розчинення, таким як, наприклад, парафін, підсилювачем поглинання, таким як, наприклад, четвертинна сіль, та/або абсорбентом, таким як, наприклад, бентоніт, каолін або дикальційфосфат. Порошкову суміш можна гранулювати шляхом змочування зі сполучним, таким як, наприклад, сироп, крохмальна паста, слиз акації або розчини целюлози або полімерних речовин і пресування її через сито. Як альтернатива грануляції, порошкову суміш можна пропускати через таблетувальну машину, одержуючи шматки неправильної форми, які розпадаються, утворюючи гранули. Гранули можна замаслювати шляхом додавання стеаринової кислоти, стеарату, тальку або мінерального масла для запобігання злипання в таблетувальній ливарній формі. Після цього змащену суміш спресовують, одержуючи таблетки. Сполуки відповідно до винаходу також можна поєднувати із сипучим інертним наповнювачем і потім піддавати прямому пресуванню, одержуючи таблетки без здійснення стадій грануляції або сухого пресування. Таблетки також можна покривати прозорим або світлонепроникним захисним шаром, що складається із запечатувального шелакового шару, шару цукру або полімерної речовини й глянсового шару воску. До цих покриттів також можна додавати барвники для можливості розрізнення між різними дозованими одиницями. Рідини для перорального введення, такі як, наприклад, розчин, сиропи й еліксири, можуть бути приготовлені у вигляді дозованих одиниць таким чином, щоб вони містили заздалегідь установлену кількість сполуки. Сиропи можуть бути одержані шляхом розчинення сполуки у водному розчині з підходящим ароматизатором, тоді як еліксири готують із застосуванням нетоксичного спиртового наповнювача. Суспензії можуть бути приготовлені шляхом диспергування сполуки в нетоксичному наповнювачі. Також можна додавати солюбілізатори й емульсифікатори, такі як, наприклад, етоксиловані ізостеарилові спирти й поліоксіетиленові ефіри сорбіту, консерванти, ароматичні добавки, такі як, наприклад, масло м'яти перцевої, або натуральні замінники цукру або сахарин, або інші штучні замінники цукру й т. п. Лікарські препарати для перорального введення у вигляді дозованих одиниць можуть бути інкапсуловані в мікрокапсули, якщо це є бажаним. Також лікарський препарат може бути приготовлений таким чином, щоб пролонгувати або сповільнити вивільнення, наприклад, шляхом застосування покриттів або занурення необхідної речовини в полімери, віск і т. п. Сполуки формули I і їх солі, сольвати й фізіологічно функціональні похідні також можуть вводитися у вигляді ліпосомних систем доставки, таких як, наприклад, невеликі одношарові пухирці, більші одношарові пухирці й багатошарові пухирці. Ліпосоми можуть бути утворені за допомогою різних фосфоліпідів, таких як, наприклад, холестерин, стеариламін або фосфатидилхоліни. Сполуки формули I і їх солі, сольвати й фізіологічно функціональні похідні також можуть доставлятися за допомогою моноклональних антитіл як індивідуальних носіїв, до яких приєднані молекули сполуки. Сполуки також можуть бути з'єднані з розчинними полімерами як 14 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 60 націлювальними носіями лікарських засобів. Такими полімерами можуть бути полівінілпіролідон, співполімер пірану, полігідроксипропілметакриламідофенол, полігідроксіетиласпартамідофенол або поліетиленоксид полілізину, заміщений пальмітоїловими радикалами. Крім того, сполуки можна зв'язувати з біорозкладними полімерами, які придатні для забезпечення контрольованого вивільнення лікарського засобу, наприклад, полімолочною кислотою, полі-епсилон-капролактоном, полігідроксимасляною кислотою, поліортоефірами, поліацеталями, полідигідроксипіранами, поліціаноакрилатами й перехрестно-зшитими або амфіпатичними блок-співполімерами гідрогелів. Фармацевтичні склади, адаптовані для трансдермального введення, можуть вводитися у вигляді незалежних пластирів для подовженого, тісного контакту з епідермісом реципієнта. Таким чином, наприклад, активний компонент може доставлятися із пластиру шляхом іонофорезу, як у загальному описано в Pharmaceutical Research, 3(6), 318 (1986). Фармацевтичні композиції, адаптовані для місцевого введення, можуть бутиприготовлені у вигляді мазей, кремів, суспензій, лосьйонів, порошків, розчинів, паст, гелів, спреїв, аерозолів або масел. Для лікування очей або інших зовнішніх тканин, наприклад рота й шкіри, переважно застосовуються лікарські препарати у вигляді місцевої мазі або крему. Для приготування лікарського препарату у вигляді мазі активний компонент може застосовуватися з парафіновою або мазевою основою, що змішується з водою. Альтернативно, для одержання крему активний компонент може бути приготовлений з основою для крему типу масло-в-воді або основою водав-маслі. Фармацевтичні склади, адаптовані для місцевого введення в очі, включають очні краплі, у яких активний компонент розчинений або суспендований у підходящому носії, переважно у водному розчиннику. Фармацевтичні склади, адаптовані для місцевого введення в порожнину рота, включають коржі, пастилки й рідини для полоскання рота. Фармацевтичні склади, адаптовані для ректального введення, можуть вводитися у вигляді супозиторіїв або клізм. Фармацевтичні склади, адаптовані для інтраназального введення, у яких носій представляє собою тверду речовину, включають великий порошок, що має розмір частинок, наприклад, в інтервалі 20-500 мікронів, який вводиться шляхом вдихання, тобто шляхом швидкого вдиху через ніс із контейнера, що містить порошок, який притримують біля носа. Підходящі лікарські препарати для введення у вигляді інтраназального аерозолю або носових крапель із рідиною як носій включають розчини активної речовини у воді або в маслі. Фармацевтичні склади, адаптовані для введення шляхом інгаляції, включають тонкоподрібнені частинки у вигляді пилу або туману, які можуть бути одержані за допомогою різного диспергованого обладнання під тиском з аерозолями, розпилювачами або інсуфляторами. Фармацевтичні склади, адаптовані для вагінального введення, можуть вводитися у вигляді песаріїв, тампонів, кремів, гелів, паст, пін або аерозолів. Фармацевтичні склади, адаптовані для парентерального введення, включають водні або неводні стерильні розчини для ін'єкцій антиоксиданти, що містять, буфери, бактеріостатичні речовини й розчинені речовини, за допомогою яких лікарський засіб підтримується ізотонічним по відношенню крові реципієнта, що піддається лікуванню; і водні або неводні стерильні суспензії, які можуть містити суспензійну середовище й загусники. Лікарські препарати можуть вводитися за допомогою ємностей для однократного або багаторазового введення, наприклад, запечатаних ампул і флаконів, і зберігатися в ліофілізованому стані, при цьому безпосередньо перед введенням необхідно тільки додати стерильну рідину-носій, наприклад, воду для ін'єкцій. Розчини й суспензії для ін'єкцій, приготовлені згідно з рецептурою, можуть бути приготовлені зі стерильних порошків, гранул і таблеток. Також є очевидним, що додатково до переважних вищеописаних складових, лікарські препарати також можуть містити інші речовини, які використовуються в даній галузі для конкретних типів лікарських засобів; наприклад, лікарські препарати, придатні для перорального введення, можуть містити ароматизатори. Терапевтично ефективна кількість сполуки формули I залежить від багатьох факторів, включаючи, наприклад, вік і вагу тварини, певний стан, який необхідно лікувати, і його тяжкість, природу лікарського засобу й спосіб введення, і в кінцевому рахунку вона може бути визначена лікарем або ветеринаром. Проте, ефективна кількість сполуки відповідно до винаходу, як правило, знаходиться в інтервалі від 0,1 до 100 мг/кг ваги тіла реципієнта (ссавця) на добу й переважно звичайно знаходиться в інтервалі від 1 до 10 мг/кг ваги тіла в добу. Отже діюча 15 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 добова кількість для дорослого ссавця вагою 70 кг звичайно може становити від 70 до 700 мг, причому ця кількість може вводитися у вигляді окремої дози один раз на день або звичайно у вигляді циклів часткових доз (таких як, наприклад, два, три, чотири, п'ять або шість раз) на день, таким чином, що загальна добова доза є аналогічною. Ефективна кількість її солі, сольвату або фізіологічно функціональної похідної може бути визначена у вигляді частки ефективної кількості сполуки відповідно до винаходу per se. Також можна припустити, що аналогічні дози придатні для лікування інших станів, описаних вище. Комбіноване лікування цього типу можна здійснювати за допомогою одночасного, послідовного або окремого дозування індивідуальних компонентів лікування. У комбінованих продуктах такого типу застосовуються сполуки відповідно до винаходу. Крім того, винахід відноситься до лікарських засобів, що містять принаймні одну сполуку формули I та/або її фармацевтично прийнятні солі, сольвати й стереоізомери, включаючи їх суміші у всіх співвідношеннях, і принаймні один додатковий активний компонент лікарського засобу. Винахід також відноситься до комплекту (набору), що складається з окремих упаковок (a) ефективної кількості сполуки формули I та/або її фармацевтично прийнятних солей, сольватів і стереоізомерів, включаючи їх суміші у всіх співвідношеннях, і (b) ефективної кількості додаткового активного компоненту лікарського засобу. Комплект включає підходящі ємності, такі як коробки, індивідуальні пляшки, пакети або ампули. Комплект може включати, наприклад, окремі ампули, кожна з яких містить ефективну кількість сполуки формули I та/або її фармацевтично прийнятних солей, сольватів і стереоізомерів, включаючи їх суміші у всіх співвідношеннях, і ефективну кількість додаткового активного компоненту лікарського засобу в розчиненій або ліофілізованій формі. "Лікування", як використовується в даній заявці, означає полегшення, повністю або частково, симптомів, зв'язаних з порушенням або захворюванням, або сповільнення, або зупинку подальшого прогресування або погіршення цих симптомів, або запобігання або профілактику захворювання або порушення в суб'єкта, що має ризик розвитку такого захворювання або порушення. Термін "ефективна кількість" по відношенню до сполуки формули (I) може означати кількість, здатну полегшувати, повністю або частково, симптоми, пов'язані з порушенням або захворюванням, або сповільнення або зупинку подальшого прогресування або погіршення цих симптомів, або запобігати або забезпечувати профілактику захворювання або порушення в суб'єкта, що має або з ризиком розвитку захворювання, описаного в даній заявці, такого як запальні стани, імунологічні стани, злоякісне новоутворення або метаболічні стани. В одному варіанті здійснення ефективна кількість сполуки формули (I) представляє собою кількість, яка інгібує танкіразу в клітині, таку як, наприклад, in vitro або in vivo. У деяких варіантах здійснення, ефективна кількість сполуки формули (I) інгібує танкіразу в клітині на 10 %, 20 %, 30 %, 40 %, 50 %, 60 %, 70 %, 80 %, 90 % або 99 %, у порівнянні з активністю танкірази в необробленій клітині. Ефективна кількість сполуки формули (I), наприклад, у фармацевтичній композиції, може знаходитися на рівні, який перевищує бажаний ефект; наприклад, від приблизно 0,005 мг/кг ваги тіла суб'єкта до приблизно 10 мг/кг ваги тіла суб'єкта в одиничній лікарській формі як для перорального, так і для парентерального введення. ЗАСТОСУВАННЯ Сполуки згідно із даним винаходом придатні як фармацевтично активні компоненти для ссавців, особливо для людей, для лікування злоякісного новоутворення, розсіяного склерозу, серцево-судинних захворювань, уражень центральної нервової системи й різних форм запалення. Даний винахід охоплює застосування сполук формули I та/або їх фізіологічно прийнятних солей і сольватів для приготування лікарського засобу для лікування або запобігання злоякісного новоутворення, розсіяного склерозу, серцево-судинних захворювань, уражень центральної нервової системи й різних форм запалення. Приклади запальних захворювань включають ревматоїдний артрит, псоріаз, контактний дерматит, алергічну реакцію сповільненого типу й інші. Також охоплюється застосування сполук формули I та/або їх фізіологічно прийнятних солей і сольватів для приготування лікарського засобу для лікування або запобігання захворювання, індукованого танкіразою, або стану, індукованого танкіразою у ссавця, при якому у цьому способі терапевтично ефективну кількість сполуки відповідно до винаходу вводять хворому 16 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 ссавцеві, що потребує такого лікування. Терапевтична кількість змінюється залежно від конкретного захворювання й легко може бути визначена спеціалістом у даній галузі. Вираз "захворювання або стани, індуковані танкіразою" відноситься до патологічних станів, які залежать від активності однієї або декількох танкіраз. Захворювання, пов'язані з активністю танкірази, включають злоякісне новоутворення, розсіяний склероз, серцево-судинні захворювання, ураження центральної нервової системи й різні форм запалення. Даний винахід, зокрема, відноситься до сполук формули I і їх фармацевтично прийнятних солей, сольватів, таутомерів і стереоізомерів, включаючи їх суміші у всіх співвідношеннях, для застосування для лікування захворювань, при яких інгібування, регуляція та/або модуляція інгібування танкірази відіграє роль. Даний винахід, зокрема, відноситься до сполук формули I і їх фармацевтично прийнятних солей, сольватів, таутомерів і стереоізомерів, включаючи їх суміші у всіх співвідношеннях, для застосування для інгібування танкірази. Даний винахід, зокрема, відноситься до сполук формули I і їх фармацевтично прийнятних солей, сольватів, таутомерів і стереоізомерів, включаючи їх суміші у всіх співвідношеннях, для застосування для лікування злоякісного новоутворення, розсіяного склерозу, серцево-судинних захворювань, уражень центральної нервової системи й різних форм запалення. Даний винахід, зокрема, відноситься до способів лікування або запобігання злоякісного новоутворення, розсіяного склерозу, серцево-судинних захворювань, уражень центральної нервової системи й різних форм запалення, які включають введення суб'єкту, який цього потребує, ефективної кількості сполуки формули I або її фармацевтично прийнятної солі, таутомеру, стереоізомеру або сольвату. Характерні злоякісні новоутворення, для лікування або запобігання яких є корисними сполуки формули I, включають, але не обмежуються такими, рак голови, шиї, очей, рота, горла, стравоходу, бронхів, гортані, глотки, грудей, кісток, легенів, обідкової кишки, прямої кишки, шлунка, передміхурової залози, сечового міхура, матки, шийки матки, молочної залози, яєчників, яєчок або інших репродуктивних органів, шкіри, щитовидної залози, крові, лімфатичних вузлів, нирок, печінки, підшлункової залози, головного мозку, центральної нервової системи, солідних пухлин і злоякісного переродження крові. Характерні серцево-судинні захворювання, для лікування або запобігання яких є корисними сполуки формули I, включають, але не обмежуються такими, рестеноз, атеросклероз і його наслідки, такі як інсульт, інфаркт міокарда, ішемічні ушкодження серця, легенів, кишечнику, нирок, печінки, підшлункової залози, селезінки або мозку. Даний винахід відноситься до способу лікування проліферативного, аутоімунного, протизапального або інфекційного захворювання порушення, який включає введення суб'єкту, який цього потребує, терапевтично ефективної кількості сполуки формули I. Переважно, даний винахід відноситься до способу, де захворювання представляє собою злоякісне новоутворення. Особливо переважно, даний винахід відноситься до способу, де захворювання представляє собою злоякісне новоутворення, де введення є одночасним, послідовним або таким, що чергується із введенням принаймні одного іншого активного лікарського засобу. Описані сполуки формули I можуть вводитися в комбінації з іншими відомими лікарськими засобами, включаючи протиракові засоби. Як використовується в даному винаході, термін "протираковий засіб" відноситься до будь-якого засобу, який вводять пацієнтові зі злоякісним новоутворенням для лікування раку. Протипухлинне лікування, описане у винаході, може застосовуватися у вигляді монотерапії, або, додатково до сполуки за винаходом, можна також застосовувати звичайні хірургічні методи або радіотерапію або хіміотерапію. Така хіміотерапія може включати один або декілька наступних класів протипухлинних засобів: (i) антипроліферативні/протипухлинні/здатні ушкоджувати ДНК лікарські засоби та їх комбінації, які застосовуються в медичній онкології, такі як алкілувальні засоби (наприклад, цисплатин, карбоплатин, циклофосфамід, азотний іприт, мельфалан, хлорамбуцил, бусульфан і нітрозосечовини); антиметаболіти (наприклад, антифолати, такі як фторпіримідини, такі як 5фторурацил і тегафур, ралтитрексед, метотрексат, арабцнозид цитозину, гідроксисечовина й гемцитабін); протипухлинні антибіотики (наприклад, антрацикліни, такі як адріаміцин, блеоміцин, доксорубіцин, дауноміцин, епірубіцин, ідарубіцин, мітоміцин-C, дактиноміцин і мітраміцин); антимітотичні засоби (наприклад, алкалоїди барвінку, такі як вінкристин, вінбластин, віндезин і вінорелбін і таксоиди, такі як таксол і таксотер); інгібітори топоізомерази (наприклад, епіподофілотоксини, такі етопозид і теніпозид, амсакрин, топотекан, іринотекан і 17 UA 112795 C2 5 10 15 20 25 30 35 40 камптотецин); і засоби, що впливають на диференціацію клітин (наприклад, ретиноєва кислота, що повністю знаходиться в транс-конфігурації, 13-цис-ретиноєва кислота й фенретинід); (ii) цитостатичні засоби, такі як антиестрогени (наприклад, тамоксифен, тореміфен, ралоксифен, дролоксифен і йодоксифен), інгібітори рецептора естрогену (наприклад, фульвестрант); антиандрогени (наприклад, бікалутамід, флутамід, нілутамід і ципротерон ацетат), антагоністи LHRH або агоністи LHRH (наприклад, гозерелін, лейпрорелін і бузерелін), прогестогени (наприклад, мегестрол ацетат), інгібітори ароматази (наприклад, анастрозол, летрозол, воразол і ексеместан) і інгібітори 5-редуктази, такі як фінастерид; (iii) засоби, які інгібують інвазію злоякісних клітин (наприклад, інгібітори металопротеїнази, такі як маримастат, і інгібітори функції рецептора урокіназного активатора плазміногену); (iv) інгібітори дії фактора росту, наприклад, такі інгібітори включають антитіла до фактора росту, антитіла до рецептора фактора росту (наприклад, анти-erbb2 антитіло трастузумаб [Herceptin™] і анти-erbbl антитіло цетуксимаб [C225]), інгібітори фарнезилтрансферази, інгібітори тирозинкінази й інгібітори серин/треонін кінази, наприклад, інгібітори сімейства фактора росту епидермісу (наприклад, інгібітори EGFR сімейства тирозинкіназ, такі як N-(3хлор-4-фторфеніл)-7-метокси-6-(3-морфолінопропокси)хіназолін-4-амін (гефітиніб, АZD1839), N(3-етинілфеніл)-6,7-біс(2-метоксіетокси)хіназолін-4-амін (ерлотиніб, OSI-774) і 6-акриламідо-N(3-хлор-4-фторфеніл)-7-(3-морфолінопропокси)хіназолін-4-амін (CI 1033)), наприклад, інгібітори сімейства фактора росту похідних тромбоцитів і, наприклад, інгібітори сімейства фактора росту гепатоцитів; (v) антиангіогенні речовини, такі як ті, які інгібують дія фактора росту ендотелію судин, (наприклад, антитіло до фактора росту клітин ендотелію судин бевацизумаб [Avastin™], сполуки, які описані в опублікованих міжнародних заявках на патент WO 97/22596, WO 97/30035, WO 97/32856 і WO 98/13354) і сполуки, які діють за іншим механізмом (наприклад, ліномід, інгібітори дії інтегрину v3 і ангіостатин); (vi) речовини, що пошкоджують судини, такі як комбретастатин A4 і сполуки, описані в міжнародних заявках на патент WO 99/02166, WO 00/40529, WO 00/41669, WO 01/92224, WO 02/04434 і WO 02/08213; (vii) антисмислова терапія, наприклад, така, яка спрямована на перераховані вище мішені, така як ISIS 2503, антисмислова терапія на основі гена Ras; (viii) способи генної терапії, включаючи, наприклад, способи заміни аберантних генів, такі як способи аберації p53 або аберації BRCA1 або BRCA2, GDEPT (пролікарська терапія, спрямована на ген ферменту), способи з використанням деамінази цитозину, тімідинкінази або бактеріальної нітроредуктази й способи підвищення стійкості пацієнта до хіміотерапії або радіотерапії, такі як генна терапія резистентності до багатьох лікарських засобів; і (ix) способи імунотерапії, включаючи, наприклад, способи підвищення імуногенності пухлинних клітин пацієнта в умовах ex vivo і in vivo, такі як трансфекція цитокінами, такими як інтерлейкін 2, інтерлейкін 4 або фактор стимуляції колоній гранулоцитів-макрофагів, способи зниження активності T-клітин, способи з використанням трансфектованих імунних клітин, таких як цитокін-трансфектовані дендритні клітини, способи з використанням цитокінтрансфектованих ліній пухлинних клітин і способи з використанням анти-ідіотипових антитіл. Лікарські засоби, наведені нижче в таблиці 1, переважно, але не винятково, комбінують зі сполуками формули I. Таблиця 1 Алкілувальні агенти Циклофосфамід Бусульфан Іфосфамід Мелфалан Гексаметилмеламін Тіотепа Хлорамбуцил Дакарбазин Кармустин Ломустин Прокарбазин Алтретамін Естрамустин фосфат Мехлороетамін Стрептозоцин Темозоломід Семустин Платинові агенти Цисплатин Оксаліплатин Спіроплатин Карбоксифталатоплатинум Карбоплатин ZD-0473 (Anormed) Лобаплатин (Aetema) Сатраплатин (Johnson Matthey) 18 UA 112795 C2 Тетраплатин Орміплатин Іпроплатин BBR-3464 (Hoffrnann-la Roche) SМ-11355 (Sumitomo) AР-5280 (Access) Антиметаболіти Азацитидин Гемцитабін Капецитабін 5-фторурацил Флоксуридин 2-хлордезоксіаденозин 6-меркаптопурин 6-тіогуанін Цитарабін 2-фтордезоксицитидин Метотрексат Ідатрексат Томудекс Триметрексат Деоксикоформіцин Флударабин Пентостатин Ралтитрексед Гідроксисечовина Децитабін (Supergen) Клофарабин (Bioenvision) Ірофулвен (MGI Pharrna) DMDC (Hoffmann-la Roche) Етинілцитидин (Taiho) Інгібітори топоізомерази Амсакрин Епірубіцин Етопозид Теніпозид або мітоксантрон Іринотекан (CPT-11) 7-етил-10- гідроксикамптотецин Топотекан Дексразоксанет (Topotarget) Піксантрон (Novuspharrna) Аналог ребекаміцину (Exelixis) BBR-3576 (Novuspharrna) Рубітекан (Supergen) Ексатекан мезилат (Daiichi) Хінамед (Chemgenex) Гіматекан (Sigma-Tau) Дифломотекан (Beaufour-ipsen) TAS-103 (Taiho) Елзамітруцин (Spectrum) J-107088 (Merck & Co) BNР-1350 (Bionumerik) CKD-602 (Chong Kun Dang) KW-2170 (Kyowa Hakko) Протипухлинні антибіотики Дактиноміцин (Актиноміцин D) Доксорубіцин (Адріаміцин) Деоксирубіцин Валрубіцин Даунорубіцин (Дауноміцин) Епірубіцин Терарубіцин Ідарубіцин Рубідазон Плікаміцинп Порфіроміцин Ціаноморфолінодоксо-рубіцин Мітоксантрон (Новантрон) Амонафід Азонафід Антрапіразол Оксантразол Лозоксантрон Блеоміцин сульфат (Бленоксан) Блеоміцинова кислота Блеоміцин A Блеоміцин B Мітоміцин C MEN-10755 (Menarini) GPX-100 (Gem Pharmaceuticals) Антимітотичні агенти Паклітаксел Доцетаксел Колхіцин Вінбластин Вінкристин Вінорелбін Віндезин Доластатин 10 (NCI) Ризоксин (Fujisawa) Мівобулін (Warner-lambert) Цемадотин (BASF) RPR 109881A (Aventis) TXD 258 (Aventis) Епотилон B (Novartis) SB 408075 (Glaxosmithkline) E7010 (Abbott) PG-TXL (Cell Therapeutics) IDN 5109 (Bayer) A 105972 (Abbott) A 204197 (Abbott) LU 223651 (BASF) D 24851 (ASTA Medica) ER-86526 (Eisai) Комбретастатин A4 (BMS) Ізогомогаліхондрин-b (Pharmamar) ZD 6126 (Astrazeneca) Peg-паклітаксел (Enzon) 19 UA 112795 C2 T 900607 (Tularik) T 138067 (Tularik) Криптофіцин 52 (Eli Lilly) Вінфлунин (Fabre) Ауристатин PE (Teikoku Hormone) BMS 247550 (BMS) BMS 184476 (BMS) BMS 188797 (BMS) Таксопрексин (Protarga) AZ10992 (Asahi) !DN-5109 (Indena) AVLB (Prescient Neuropharma) Азаепотилон B (BMS) BNР-7787 (Bionumerik) CA-4-проліки (Oxigene) Доластатин-10 (Nrh) CA-4 (Oxigene) Інгібітори ароматази Аміноглутетімід Летрозол Анастразол Форместан Ексеместан Атаместан (Biomedicines) YМ-511 (Yamanouchi) Інгібітори тімідилатсинтази Пеметрексед (Eli Lilly) ZD-9331 (BTG) Нолатрексед (Eximias) Cofactor™ (Biokeys) Антагоністи ДНК Трабектедин (Pharmamar) Глуфосфамід (Baxter International) Альбумін + 32P (Isotope Solutions) Тимектацин (Newbiotics) Едотреотид (Novartis) Мафосфамід (Baxter International) Апазиквон (Spectrum Pharmaceuticals) O6-бензилгуанін (Paligent) Інгібітори фарнезилтрансферази Арглабін (Nuoncology Labs) Лонафарніб (Schering-plough) BAY-43-9006 (Bayer) Типіфарніб (Johnson & Johnson) Периліловий спирт (DOR Biopharma) Інгібітори помпи CBT-1 (CBA Pharma) Тариквідар (Xenova) MS-209 (Schering AG) Зосуквідар тригідрохлорид (Eli Lilly) Бірикодар дицитрат (Vertex) Інгібітори гістон-ацетилтрансферази Тацединалін (Pfizer) SAHA (Aton Pharma) MS-275 (Schering AG) Півалоїлоксиметил бутират (Titan) Депсипептид (Fujisawa) Інгібітори металопротеїнази Інгібітори рибонуклеозид- редуктази Неовастат (Aeterna Laboratories) Маримастат (British Biotech) Галію мальтолат (Titan) Триапін (Vion) CMT-3 (Collagenex) BMS-275291 (Celltech) Тезацитабін (Aventis) Дідокс (Molecules for Health) TNF-альфа агонисти/ антагоністи Вірулізин (Lorus Therapeutics) CDC-394 (Celgene) Ревімід (Celgene) Антагоністи рецептора ендотелін-А Атразентан (Abbot) ZD-4054 (Astrazeneca) YМ-598 (Yamanouchi) Агонисти рецептора ретиноєвої кислоти Фенретинід (Johnson & Johnson) LGD-1550 (Ligand) Алітретиноїн (Ligand) Імуномодулятори Інтерферон Онкофаг (Antigenics) GMK (Progenics) Аденокарциномна вакцина (Biomira) Дексосомна терапія (Anosys) Пентрикс (Australian Cancer Technology) JSF-154 (Tragen) Ракова вакцина (Intercell) 20 UA 112795 C2 CTР-37 (AVI Biopharma) JRX-2 (Immuno-rx) PEР-005 (Peplin Biotech) Синхроваксні вакцини (CTL Immuno) Меланомна вакцина (CTL Immuno) p21-RAS вакцина (Gemvax) Норелін (Biostar) BLР-25 (Biomira) MGV (Progenics) !3-алетин (Dovetail) Cll-тера (Vasogen) Гормональні та антигормональні агенти Естрогени Кон'юговані естрогени Етинілестрадіол хлортрианізен Іденестрол Гідроксипрогестерон капроат Медроксипрогестерон Тестостерон Тестостерон пропіонат Флуоксиместерон Метилтестостерон Діетилстилбестрол Мегестрол Тамоксифен Торемофин Дексаметазон Преднізон Метилпреднізолон Преднізолон Аміноглутетімід Леупролід Гозерелін Леупорелін Бікалутамід Флутамід Октреотид Нілутамід Мітотан Р-04 (Novogen) 2-метоксіестрадіол (Entremed) Арзоксифен (Eli Lilly) Фотодинамічні агенти Талапорфін (Light Sciences) Тералюкс (Theratechnologies) Мотексафін-гадоліній (Pharmacyclics) Pd-бактеріофеофорбід (Yeda) Лютецій-тексафірин (Pharmacyclics) Гіперицин Інгібітори тирозин-кінази Іматиніб (Novartis) Лефлуномід (Sugen/Pharmacia) Zdl839 (Astrazeneca) Ерлотиніб (Oncogene Science) Канерт'юніб (Pfizer) Скваламін (Genaera) SU5416 (Pharmacia) SU6668 (Pharmacia) ZD4190 (Astrazeneca) ZD6474 (Astrazeneca) Ваталаніб (Novartis) PKI166 (Novartis) GW2016 (Glaxosmithkline) EKB-509 (Wyeth) EKB-569 (Wyeth) SR-27897 (CCK-A інгібітор, Sanofi-synthelabo) Токладезин (цamф-агоніст, Ribapharm) Алвоцидіб (CDK інгібітор, Aventis) CV-247 (COX-2 інгібітор, Ivy Medical) P54 (COX-2 інгібітор, Phytopharm) Capcell™ (CYP450 стимулятор, Bavarian Nordic) GCS-IOO (gal3 антагоніст, Glycogenesys) Кахалід F (Pharmamar) CEР-701 (Cephalon) CEР-751 (Cephalon) MLN518 (Millenium) PKC412 (Novartis) Феноксодіол O Трастузумаб (Genentech) C225 (Imclone) rhu-маb (Genentech) MDX-H210 (Medarex) 2C4 (Genentech) MDX-447 (Medarex) ABX-EGF (Abgenix) IMC-1C11 (Imclone) Різні агенти 21 BCX-1777 (PNP інгібітор, Biocryst) Ранпірназа (стимулятор рибонуклеази, Alfacell) Галарубіцин (Інгібітор синтезу РНК, Dong-a) Тирапазамін (відновлюючий агент, SRI International) N-ацетилцистеїн (відновлюючий агент, Zambon) R-флурбіпрофен (Nf-каппаb інгібітор, Encore) 3CPA (Nf-каппаb інгібітор, Active Biotech) UA 112795 C2 G17DT імуноген (інгібітор гастрину, Aphton) Ефапроксирал (оксигенатор, Alios Therapeutics) PI-88 (інгібітор гепаранази, Progen) Тесміліфен (антагоніст гістаміну, YM Biosciences) Гістамін (агоніст рецептора гістаміну Н2, Maxim) Тіазофурин (IMPDH інгібітор, Ribapharm) Циленгітид (антагоніст інтегрину, Merck Kgaa) SR-31747 (IL-1 антагоніст, Sanofi-synthelabo) CCI-779 (інгібітор mtor кінази, Wyeth) Ексисулінд (PDE-V інгібітор, Cell Pathways) CР-461 (PDE-V інгібітор, Cell Pathways) AG-2037 (GART інгібітор, Pfizer) WX-UK1 (інгібітор активатора плазміногену, Wilex) PBI-1402 (PMN стимулятор, Prometic Lifesciences) Бортезоміб (інгібітор протеасоми, Millennium) SRL-172 (cтимулятор Т-клітин, SR Pharma) TLK-286 (інгібітор глутатіон-s трансферази, Telik) PT-100 (агоніст фактора росту, Point Therapeutics) Мідостаурин (PKC інгібітор, Novartis) Бріостатин-1 (PKC стимулятор, GPC Biotech) CDA-II (промотор апоптозу, Everlife) SDX-101 (промотор апоптозу, Salmedix) Цефлатонін (промотор апоптозу, Chemgenex) 5 10 15 Сеокальцитол (агоніст рецептора вітаміну D, Leo) 131-I-TМ-601 (ДНК антагоніст, Transmolecular) Ефлорнітин (ODC інгібітор, ILEX Oncology) Мінодронова кислота (інгібітор остеокласту, Yamanouchi) Індисулам (p53 стимулятор, Eisai) Аплідин (PPT інгібітор, Pharmamar) Ритуксимаб (CD20 антитіло, Genentech) Гемтузумаб (CD33 антитіло, Wyeth Ayerst) PG2 (промотор гематопоезу, Pharmagenesis) Immunol™ (триклозанова рідина для промивання ротової порожнини, Endo) Триацетилуридин (уридинові проліки, Welistat) SN-4071 (саркомний агент, Signature Bioscience) Transmid-107™ (імунотоксин, KS Biomedix) PCK-3145 (промотор апоптозу, Procyon) Доранідазол (промотор апоптозу, Pola) CHS-828 (цитотоксичний агент, Leo) Транс-ретинова кислота (диференціатор, NIH) MX6 (промотор апоптозу, MAXIA) Апомин (промотор апоптозу, ILEX Oncology) Уроцидин (промотор апоптозу, Bioniche) Ro-31-7453 (промотор апоптозу, La Roche) Бросталіцин (промотор апоптозу, Pharmacia) Наступні скорочення відносяться відповідно до визначень, наведених нижче: Наступні скорочення стосуються відповідно визначень, наведених нижче: водн. (водн), год. (година), г (грам), л (літр), мг (міліграм), МГц (мегагерц), хв. (хвилина), мм (міліметр), ммоль (мілімоль), мM (мілімолярний), t пл. (температура плавлення), екв. (еквівалент), мл (мілілітр), мкл (мікролітр), ACN (ацетoнітрил), AcОН (оцтова кислота), CdСl 3 (дейтерований хлороформ), CD3OD (дейтерований метанол), CH3CN (ацетoнітрил), c-hex (циклогексан), DCC (дициклогексил карбодіімід), ДХМ (дихлорметан), DIC (діізопропіл карбодіімід), DIEA (діізопропілетил-амін), ДМФА (диметилформамід), ДМСО (диметилсульфоксид), ДМСО-d6 (дейтерований диметилсульфоксид), EDC (1-(3-диметил-аміно-пропіл)-3-етилкарбодіімід), ЕРІ (електророзпилювальна іонізація), Etoac (етил ацетат), Et 2O (простий діетиловий ефір), Etoh (етанол), HATU гексафторфосфат (диметиламіно-([1,2,3]триазоло[4,5-b]піридин-3-ілокси)метилен]-диметил-амонію), ВЕРХ (високоефективна рідинна хроматографія), i-proh (2пропанол), K2CO3 (карбонат калію), РХ (рідинна хроматографія), MeOH (метанол), Mgso 4 (сульфат магнію), МС (мас-спектрометрія), MTBE (метил-трет-бутиловий ефір), Nahco3 22 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 60 (бікарбонат натрію), Nabh4 (борогідрид натрію), NMM (N-метилморфолін), ЯМР (ядерний магнітний резонанс), Pybop (гексафторфосфат бензотриазол-1-іл-окси-трис-піролідинoфосфонію), КТ (кімнатна температура), Rt (час утримання), SPE (твердофазова екстракція), TBTU (тетрафторборат 2-(1-h-бензотриазол-1-іл)-1,1,3,3-тетраметилуронію), TEA (триетиламін), ТФО (трифтороцтова кислота), ТГФ (тетрагідрофуран), ТШХ (тонкошарова хроматографія), УФ (ультрафіолет). Опис досліджень in vitro Скорочення: GST = глутатіон-s-трансфераза FRET= резонансний перенос енергії флуоресценції HTRF® = (гомогенна флуоресценція з розділенням у часі) HEPES = буфер 4-(2-гідроксіетил)-1-піперазин етансульфонова кислота DTT = дитіотреїтол BSA = бичачий сироватковий альбумін CHAPS = детергент; CHAPS=3-[(3-холамідопропіл)диметиламоніо]-1-пропансульфонат Стрептавідин-Xlent® являє собою кон'югат стрептавідин-Xl665, для якого були оптимізовані умови комбінації для одержання кон'югату з поліпшеними характеристиками для деяких досліджень, зокрема тих, для яких потрібна висока чутливість. Тестування біохімічної активності танкіраз 1 і 2: Дослідження аутопарсилування Дослідження аутопарсилування здійснюють за дві стадії: ферментативна реакція, в якій GST-мічена танкіраза-1, відпов. танкіраза-2 переносить біотиніловану ADP-рибозу на себе з біотинілованого NAD як ко-субстрату і реакція виявлення, де аналізують FRET з розділенням у часі між міченими криптатом анти-GST, які зв'язані з GST міткою ферменту і Xlent® міченимстрептавідин зв'язаним біотин-парсилованим залишком. Аутопарсилуючу активність визначають безпосередньо шляхом підвищення HTRF сигналу. Дослідження аутопарсилування здійснюють у форматі аналізу на 384 лунок HTRF® (Cisbio, Codolet, France) у мікротитрувальних низькооб'ємних планшетах на 384 лунки Greiner nb і використовують для екрану з високою пропускною здатністю. 250 нM GST-мічену танкіразу-1 (1023-1327 a/к), відповідно приблизно 250 нM GST-мічену танкіразу-2 (873-1166 a/к) і 5 мкM bioNAD (Biolog, Life science Inst., Bremen, Germany) як ко-субстрат інкубують в загальному об'ємі 5 мкл (50 мM HEPES, 4 мM Mg-хлорид, 0.05 % Pluronic F-68, 1.4 мM DTT, 0.5 % ДМСО, pH 7.7) за відсутності або за присутності тестованої сполуки (10 концентрацій розведення) впродовж 90 хв. при 30 °C. Реакцію зупиняють шляхом додавання 1 мкл 50 мМ EDTA розчину. Додають 2 мкл розчину для виявлення (1.6 мкM SA-Xlent® (Cisbio, Codolet, France), 7.4 нМ Анти-GST-K® (Euмічені анти-GST,Cisbio, Codolet, France) в 50 мМ HEPES, 800 мМ KF, 0.1 % BSA, 20 мМ EDTA, 0.1 % CHAPS, pH 7.0). Після інкубування впродовж 1 год. при кімнатній температурі HTRF вимірюють за допомогою багаторежимного планшет-рідера Envision (Perkin Elmer LAS Germany GmbH) при довжині хвилі збудження 340 нм (лазерний режим) і довжинах хвиль емісії 615 нм і 665 нм. Визначають співвідношення сигналів емісії. Повне використовуване значення являло реакцію без інгібітору. Використовуване значення фармакологічного нуля являло XAV-939 (Tocris) у кінцевій концентрації 5 мкM. Інгібуючі значення (IC50) визначають, використовуючи або програму Symyx Assay Explorer® або Condosseo® від GeneData. Вимірювання клітинного інгібування танкірази Оскільки було описано, що танкірази модулюють клітинний рівень Axin2 (Huang і ін., 2009; Nature), то підвищення рівня Axin2 використовують як аналізовані дані для визначення клітинного інгібування танкіраз в аналізі на основі Luminex. Клітини клітинної лінії карциноми обідкової кишки DLD1 висівають в планшети на 96 лунок 4 при густині 1,5×10 клітин на лунку. Наступного дня, клітини обробляють серійними розведеннями тестованої сполуки за сім стадій у вигляді трьох повторів з кінцевою концентрацією ДМСО 0,3 %. Через 24 години, клітини лізують в лізуючому буфері (20 мM Tris/HCl pH 8,0, 150 мM NaCl, 1 % NP40, 10 % гліцерин) і лізати очищають шляхом центрифугування через фільтрувальний планшет на 96 лунок (0,65 мкм). Білок Axin2 виділяють із клітинних лізатів шляхом інкубування з моноклональним анти-Axin2 антитілом (R&D Systems #MAB6078), яке зв'язується із флуоресцентними карбоксикульками. Після цього, зв'язаний Axin2 специфічно виявляють за допомогою поліклонального анти-Axin2 антитіла (Cell Signaling #2151) і підходящого PE-флуоресцентного вторинного антитіла. Кількість виділеного Axin2 білка 200 визначають за допомогою приладу Luminex (Luminex Corporation) відповідно до інструкцій виробника шляхом підрахування 100 подій на лунку. Інгібування танкірази тестованими сполуками приводить до більш високих рівнів Axin2, які прямо корелюють із підвищенням 23 UA 112795 C2 5 10 15 20 25 30 35 40 45 50 55 60 флуоресценції, що виявляється. Як контролі клітини обробляли тільки розчинником (нейтральний контроль) і порівняльним інгібітором танкірази IWR-2 (3E-06 M), який служить як контроль для максимального підвищення Axin2. Для аналізу, отримані дані нормалізують щодо необробленого контролю з розчинником і підганяють для визначення значень EC 50, використовуючи програмне забезпечення Assay Explorer (Accelrys). Опис дослідження PARP1 Тестування біохімічної активності PARP-1: Дослідження аутопарсилування Дослідження аутопарсилування здійснюють за дві стадії: ферментативна реакція, в якій Hisмічена Parp-1 переносить біотиніловану ADP-рибозу/ADP-рибозу на себе з біотинілованого NAD/NAD як ко-субстрату і реакція виявлення, де аналізують FRET з розділенням у часі між міченим криптатом анти-His антитілом, зв'язаним з His міткою ферменту і Xlent® міченим стрептавідин зв'язаним біотин-парсилованим залишком. Аутопарсилуючу активність визначають безпосередньо шляхом підвищення HTRF сигналу. Дослідження аутопарсилування здійснюють у форматі аналізу на 384 лунок HTRF® (Cisbio, Codolet, France) у мікротитрувальних низькооб'ємних планшетах на 384 лунки Greiner nb. 35 нМ His-мічену Parp-1 (людська, рекомбінантна, Enzo Life Sciences GmbH, Lörrach, Germany) і суміш 125 нМ bio-NAD (Biolog, Life science Inst., Bremen, Germany) і 800 нМ NAD як ко-субстрату інкубують в загальному об'ємі 6 мкл (100 мМ Tris/HCl, 4 мМ Mg-хлорид, 0,01 % IGEPAL® CA630, 1 мM DTT, 0,5 % ДМСО, pH 8, 13 нг/мкл активованої ДНК (BPS Bioscience, San Diego, US)) за відсутності або за присутності тестованої сполуки (10 концентрацій розведення) впродовж 150 хв. при 23 °C. Реакцію зупиняють шляхом додавання 4 мкл розчину стоп/виявлення (70 нМ SAXlent® (Cisbio, Codolet, France), 2.5 нМ анти-His-K® (Eu-мічені анти-His, Cisbio, Codolet, France) в 50 мМ HEPES, 400 мМ KF, 0,1 % BSA, 20 мМ EDTA, pH 7,0). Після інкубування впродовж 1 год. при кімнатній температурі HTRF вимірюють за допомогою багаторежимного планшет-рідера Envision (Perkin Elmer LAS Germany GmbH) при довжині хвилі збудження 340 нм (лазерний режим) і довжинах хвиль емісії 615 нм і 665 нм. Визначають співвідношення сигналів емісії. Повне використовуване значення являло реакцію без інгібітору. Використовуване значення фармакологічного нуля являло Olaparib (LClabs, Woburn, US) у кінцевій концентрації 1 мкМ. Визначають інгібуючі значення (IC50), використовуючи або програму Symyx Assay Explorer®, або Condosseo® від GeneData. Опис ELISA виявлення TNKS1 і TNKS2 Тестування біохімічної активності TNK 1 і 2: активності ELISA (дослідження аутопарсилування) Для аналізу аутопарсиліруючої активності TNKS 1 і 2 здійснюють ELISA: На першій стадії GST мічену TNKS захоплюють на покритому глутатіоном планшеті. Після цього здійснюють аналіз активності з біотинілованим NAD за відсутності /за присутності сполук. Впроцесі ферментативної реакції GST мічена TNKS переносить біотиніловану ADP-рибозу на себе з біотинілованого NAD як ко-субстрату. Для виявлення додають кон'югат стрептавідин-HRP, який зв'язується з біотинілованою TNKS і таким чином захоплюється на планшети. Визначають кількість біотинілованої відпов. аутопарсилованої TNKS з люмінесцентним субстратом для HRP. Рівень сигналу люмінесценції прямо корелюється з кількістю аутопарсилованої TNKS й, отже, з активністю TNKS. Активність ELISA здійснюють в мікротитрувальних планшетах на 384 лунки, покритих глутатіоном (планшети для захоплення Express, покриті глутатіоном, Biocat, Heidelberg, Germany). Планшети попередньо врівноважують за допомогою PBS. Потім планшети інкубують з 50 мкл 20 нг/лунку GST-міченої Tnks-1 (1023-1327 a/к, власного виробництва), відповідно GSTміченої Tnks-2 (873-1166 a/к, власного виробництва) в буфері для аналізу (50 мМ HEPES, 4 мМ Mg-хлорид, 0,05 % Pluronic F-68, 2 мМ DTT, pH 7.7) впродовж ночі при 4 °C. Планшети промивають 3 рази за допомогою PBS-Tween-20. Лунки блокують шляхом інкубування при кімнатній температурі впродовж 20 хвилин з 50 мкл блокувального буфера (PBS, 0,05 % Tween20, 0,5 % BSA). Після цього планшети промивають 3 рази за допомогою PBS-Tween-20. Ферментативну реакцію здійснюють в 50 мкл реакційного розчину (50 мМ HEPES, 4 мМ Mgхлорид, 0,05 % Pluronic F-68, 1,4 мМ DTT, 0,5 % ДМСО, pH 7,7) з 10 мкM bio-NAD (Biolog, Life science Inst., Bremen, Germany) як ко-субстратом за відсутності або присутності тестованої сполуки (10 концентрацій розведення) впродовж 1 години при 30 °C. Реакцію зупиняють шляхом промивання 3 рази з PBS-Tween-20. Для виявлення додають 50 мкл 20 нг/мкл стрептавідин, HRP кон'югату (MoBiTec, Göttingen, Germany) в PBS/0,05 %Tween-20/0,01 %BSA і планшети інкубують впродовж 30 хвилин при кімнатній температурі. Після триразового промивання PBSTween-20 додають 50 мкл SuperSignal ELISA Femto Maximum чутливого субстратного розчину (ThermoFisherScientific (Pierce), Bonn, Germany). Після інкубування впродовж 1 хвилини при 24 UA 112795 C2 5 10 15 20 25 30 35 40 45 кімнатній температурі, вимірюють люмінесцентні сигнали за допомогою багаторежимного планшет-рідера Envision (Perkin Elmer LAS Germany GmbH) при 700 нм. Повне використовуване значення являло реакцію без інгібітору. Використовуване значення фармакологічного нуля являло XAV-939 (Tocris) у кінцевій концентрації 5 мкM. Визначають інгібуючі значення (IC50), використовуючи або програму Symyx Assay Explorer®, або Condosseo® від GeneData. Вище і нижче, всі температури вказані в градусах Цельсію°C. В подальших прикладах "звичайна обробка" означає: при необхідності додають воду, pH встановлюють, при необхідності, на значення від 2 до 10, в залежності від складу кінцевого продукту, суміш екстрагують етилацетатом або дихлорметаном, фази розділяють, органічну фазу висушують над сульфатом натрію і упарюють, і залишок очищають за допомогою хроматографії на силикагелі і/або кристалізації. Rf значення на силікагелі; елюент: етилацетат/метанол 9:1. ВЕРХ/МС умови A 2 колонка: Chromolith Performance ROD RP-18e, 50 × 4,6 мм градієнт: A:B=96:4-0:100 за 2,8 хв. швидкість потоку: 2,40 мл/хв. елюент A: вода + 0,05 % мурашиної кислоти елюент B: ацетонітрил + 0,04 % мурашиної кислоти довжина хвилі: 220 нм мас-спектроскопія: позитивний режим ВЕРХ/МС умови B 2 колонка: Chromolith Performance ROD RP-18e, 100 × 3 мм градієнт: A:B=99:1-0:100 за 3,5 хв. швидкість потоку: 2,0 мл/хв. елюент A: вода + 0,05 % мурашиної кислоти елюент B: ацетонітрил + 0,04 % мурашиної кислоти довжина хвилі: 220 нм мас-спектроскопія: позитивний режим ВЕРХ/МС умови C 2 колонка: Chromolith Performance ROD RP-18e, 100 × 3 мм градієнт: A:B=99:1-0:100 за 1,8 хв. швидкість потоку: 2,0 мл/хв. елюент A: вода + 0,05 % мурашиної кислоти елюент B: ацетонітрил + 0,04 % мурашиної кислоти довжина хвилі: 220 нм мас-спектроскопія: позитивний режим 1 H ЯМР записували на спектрометрі Bruker DPX-300, DRX-400 або AVII-400, використовуючи залишковий сигнал дейтерованого розчинника як внутрішній стандарт. Хімічні зсуви (δ) представлені у вигляді м.ч. відносного залишкового сигналу розчинника (δ = 2,49 м.ч. для ЯМР 1 в ДМСО-d6). H ЯМР дані представлені таким чином: хімічний зсув (мультиплетність, константи взаємодії, і кількість воднів). Мультиплетність скорочували наступним чином: s (синглет), d (дублет), t (триплет), q (квартет), m (мультиплет), br (широкий). Мікрохвильову хімію здійснюють в однорежимному мікрохвильовому реакторі EmrysTM Optimiser від Personal Chemistry. Приклад 1 Синтез 3-(4-бензилоксифеніл)-2H-піроло[1,2-a]піразин-1-ону ("A1") O Br O Cs2CO3 O O O + N NH ДМФА O 50° C O O O NH3/MeOH 90°C H N O N 25 UA 112795 C2 5 10 Суспензію 200 мг (1.60 ммоль) складного метилового ефіру 1H-пірол-2-карбонової кислоти і 1,56 г (4,79 ммоль) карбонату цезію в 3 мл ДМФА нагрівають до 50 °C при перемішуванні. Потім впродовж 3-х хвилин додають розчин 488 мг (1,60 ммоль) 1-(4-бензилоксифеніл)-2-брометанону в 1 мл ДМФА. Реакційну суміш перемішують впродовж 18 годин при 50 °C. Реакційну суміш фільтрують з відсмоктуванням, і фільтрат упарюють. Залишок кристалізують з діетилового ефіру з одержанням складного метилового ефіру 1-[2-(4-бензилоксифеніл)-2-оксоетил]-1Hпірол-2-карбонової кислоти у вигляді бежевих кристалів; ВЕРХ/МС 2,51 хв. (A), [M+H] 350. Суспензію 100 мг (0.286 ммоль) складного метилового ефіру 1-[2-(4-бензилоксифеніл)-2оксоетил]-1H-пірол-2-карбонової кислоти в 7 M розчині аміаку в метанолі опромінюють в мікрохвильовому апараті при 90 °C впродовж 18 год. Реакційну суміш охолоджують до кімнатної температури і упарюють. Залишок хроматографують на колонці з силікагелем сумішшю петролейний ефір/етилацетат як елюентом з одержанням 3-(4-бензилоксифеніл)-2H-піроло[1,2a]піразин-1-ону у вигляді бежевих кристалів; ВЕРХ/МС 2,26 хв. (A), [M+H] 317. Аналогічно одержують наступні сполуки 15 сполука № назва і/або структура 3-феніл-2H-піроло[1,2-a]піразин-1-он O NH "A2" N 3-(3-хлорфеніл)-2H-піроло[1,2-a]піразин-1-он O NH "A3" Cl N 3-(3-метоксифеніл)-2H-піроло[1,2-a]піразин-1-он O NH "A4" O N 3-(5,5,8,8-тетраметил-5,6,7,8-тетрагідронафталін-2-іл)-2H-піроло[1,2a]піразин-1-он O "A5" NH N 3-(4-нітрофеніл)-2H-піроло[1,2-a]піразин-1-он O "A6" NH N NO2 "A7" 3-(4-метоксифеніл)-2H-піроло[1,2-a]піразин-1-он 26 UA 112795 C2 O NH N O ВЕРХ/МС 2,26 хв. (B), [M+H] 241; 1 H ЯМР (400 МГц, ДМСО-d6) δ [м.ч.] 10.67 (s, 1H), 7.63 (s, 1H), 7.60 (d, J=8.9, 2H), 7.43 (dd, J=2.5, 1.5, 1H), 7.02 (d, J=8.9, 2H), 6.89 (m, 1H), 6.55 (dd, J=3.9, 2.5, 1H), 3.80 (s, 3H) 3-(3,4-диметоксифеніл)-2H-піроло[1,2-a]піразин-1-он O "A8" NH O N O 3-бензо[1,3]діоксол-5-іл-2H-піроло[1,2-a]піразин-1-он O NH "A9" N O O 3-(4-фторфеніл)-2H-піроло[1,2-a]піразин-1-он O "A10" NH N F 3-(4-трет-бутилфеніл)-2H-піроло[1,2-a]піразин-1-он O NH "A11" N ВЕРХ/МС 2,79 хв. (B), [M+H] 267 1 H ЯМР (400 МГц, ДМСО-d6) δ [м.ч.] 10.68 (s, 1H), 7.69 (s, 1H), 7.60 (d, J=8.5, 2H), 7.47 (d, J=8.5, 2H), 7.45 (dd, J=2.4, 1.6, 1H), 6.90 (d, J=3.1, 1H), 6.56 (dd, J=3.9, 2.6, 1H), 1.31 (s, 9H) 3-п-толіл-2H-піроло[1,2-a]піразин-1-он O NH "A12" N 27 UA 112795 C2 Приклад 2 Синтез 3-(4-трифторметилфеніл)-2H-піроло[1,2-a]піразин-1-ону ("A13") O Br O O O O NH4OAc Cs2CO3 NH N O N AcOH + ацетонітрил NH O 80°C 35° C CF3 CF3 5 10 15 20 CF3 Розчин 1.15 г (9.19 ммоль) складного метилового ефіру 1H-пірол-2-карбонової кислоти і 2.70 г (10.1 ммоль) 2-бром-(1-(4-трифторметилфеніл)-етанону в 20 мл ацетонітрилу обробляють 3.30 г (10.1 ммоль) карбонату цезію. Одержану суспензію перемішують при 35 °C впродовж 18 годин. Реакційну суміш фільтрують і фільтрат упарюють. Залишок хроматографують на колонці з силікагелем сумішшю циклогексан/етилацетат як елюентом з одержанням складного метилового ефіру 1-[2-оксо-2-(4-трифторметилфеніл)-етил]-1H-пірол-2-карбонової кислоти у вигляді жовтого масла; ВЕРХ/МС 2.52 (A), [M+H] 312. Розчин 106 мг (0.34 ммоль) складного метилового ефіру 1-[2-оксо-2-(4-трифторметилфеніл)етил]-1H-пірол-2-карбонової кислоти і 789 мг (10.2 ммоль) ацетату амонію в 2 мл оцтової кислоти нагрівають до 80 °C при перемішуванні. Суміш перемішують при цій температурі впродовж 5 годин і потім охолоджують до кімнатної температури. Суміш розподіляють між ТГФ і насиченим розчином хлориду натрію. Органічну фазу два рази промивають 25 %-вим водним розчином аміаку і два рази насиченим розчином хлориду натрію. Органічну фазу сушать над сульфатом натрію і упарюють. Залишок хроматографують на колонці з силікагелем сумішшю циклогексан/етилацетат як елюентом з одержанням 3-(4-трифторметилфеніл)-2H-піроло[1,21 a]піразин-1-ону у вигляді безбарвних кристалів; ВЕРХ/МС 2.11 (A), [M+H] 279; H ЯМР (500 МГц, ДМСО-d6) δ [м.ч.] 10.91 (s, 1H), 7.90 (m, 3H), 7.82 (d, J=8.4, 2H), 7.49 (dd, J=2.4, 1.5, 1H), 6.95 (m, 1H), 6.61 (dd, J=3.8, 2.6, 1H). Аналогічно одержують наступні сполуки 3-(1-метил-1H-піразол-4-іл)-2H-піроло[1,2-a]піразин-1-он ("A14") O NH N N N 25 ВЕРХ/МС 1.66 хв. (B), [M+H] 215; 1 H ЯМР (400 МГц, ДМСО-d6) δ [м.ч.] 10.62 (s, 1H), 8.15 (s, 1H), 7.86 (d, J=0.6, 1H), 7.66 (s, 1H), 7.37 (dd, J=2.5, 1.5, 1H), 6.87 (m, 1H), 6.53 (dd, J=3.9, 2.5, 1H), 3.86 (s, 3H); 3-(4-трет-бутилфеніл)-7-метил-2H-піроло[1,2-a]піразин-1-он ("A38") O H N N 30 ВЕРХ/МС 2.94 хв. (B), [M+H] 281; 1 H ЯМР (400 МГц, ДМСО-d6) δ [м.ч.] 10.64 (s, 1H), 7.61 (s, 1H), 7.59 (d, J=8.6, 2H), 7.46 (d, J=8.6, 2H), 7.24 (dd, J=1.5, 0.8, 1H), 6.72 (m, 1H), 2.18 (s, 3H), 1.30 (s, 10H); 3-(4-трет-бутилфеніл)-1-оксо-1,2-дигідропіроло[1,2-a]піразин-7-карбонітрил ("A92") O H N N NC 35 ВЕРХ/МС 2,34 хв. (C), [M+H] 292. 28
ДивитисяДодаткова інформація
Назва патенту англійськоюBicyclic pyrazinone derivatives
Автори англійськоюDorsch, Dieter, Buchstaller, Hans-Peter, Moinet, Gerard, Wegener, Ansgar
Автори російськоюДорш Дитер, Бухшталлер Ханс-Пэтэр, Муанэ Жэрар, Вегэнэр Ансгар
МПК / Мітки
МПК: A61P 7/00, C07D 487/04, A61K 31/4985
Мітки: піразинонові, похідні, біциклічні
Код посилання
<a href="https://ua.patents.su/69-112795-biciklichni-pirazinonovi-pokhidni.html" target="_blank" rel="follow" title="База патентів України">Біциклічні піразинонові похідні</a>
Попередній патент: Спосіб контролю ступеневого перемикача
Наступний патент: Спосіб наддування паливного бака рушійної установки
Випадковий патент: Пристрій для зняття зовнішнього грату












