(8-n-бензиламінотеофілініл-7)ацетатної кислоти (1-фенілетиліден) гідразид, який виявляє антиоксидантну дію
Номер патенту: 71209
Опубліковано: 10.07.2012
Автори: Романенко Микола Іванович, Александрова Катерина В'ячеславівна, Бухтіярова Ніна Вікторівна, Бєленічев Ігор Федорович, Юрченко Дар'я Миколаївна
Формула / Реферат
(8-N-бензиламінотеофілініл-7)ацетатної кислоти (1-фенілетиліден) гідразид формули:
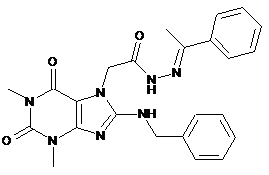 ,
,
який виявляє антиоксидантну дію.
Текст
Реферат: (8-N-бензиламінотеофілініл-7)ацетатної кислоти (1-фенілетиліден) гідразид формули: O O N N O N H N NH N N , який виявляє антиоксидантну дію. UA 71209 U (12) UA 71209 U UA 71209 U 5 10 15 20 25 Корисна модель належить до біологічно активних сполук і може бути використана у фармації та медицині. Результатами багатьох досліджень показано, що майже половина всіх патологічних станів супроводжується активацією процесів вільнорадикального окислення з формуванням так званого "оксидативного стресу" [Губський Ю.І. Жирнокислотний склад ліпідів головного мозку щурів при токсичному ураженні 1,2-дихлоретаном та введенні нікотинаміду / Ю. І. Губський, Л. В. Яніцька, Т. С Брюзгіна // Сучасність і пробл. токсикол.-2005. - № 1. - С 19-21]. Вільнорадикальні механізми беруть участь в патогенезі атеросклерозу та його тромбонекротичних фіналів (інфаркт, інсульт), цукрового діабету, хронічного неспецифічного захворювання легень, захворювань репродуктивної системи, гепатиту, зниження клітинного та гуморального імунітету та ін. Зважаючи на розповсюдженість захворювань, що перебігають за цим механізмом, розробка нових препаратів з антиоксидантною дією є актуальною проблемою сьогодення. Розвиток оксидативного стресу в умовах ішемії головного мозку перебігає у декілька стадій та найбільш важливою є продукція АФК (активних форм кисню) - супероксидрадикалу, гідроксирадикалу, NО-радикалу при роз'єднанні дихального ланцюгу та окисного фосфорилювання. В цих умовах АФК атакують макромолекули клітинної мембрани нейрону, що призводить до їх окислювальної модифікації та деструкції. При ішемії АФК також посилює експресію прозапальних цитокінів, що призводить, в свою чергу, до активації факторів транскрипції білка, які опосередковано, через активацію індуцибельної NO-синтази, ще більше посилюють утворення АФК. Необхідною задачею є створення препаратів, які б впливали на патогенетичні ланки та згальмували вільнорадикальні реакції, а також були малотоксичними та ефективними. Прототипом сполуки, що заявляється, може служити морфоліній (3-бензилксантиніл8)метилтіоацетат (Пат. 54957 Україна, МПК СО7В473/00. Водорозчинні солі 3-бензилксантиніл8-метилтіоацетатної кислоти, які виявляють антиоксидантну дію / Александрова К. В., Бєленічев І. Ф., Шкода О.С, Бухтіярова Н.В., Левіч С.В.; заявник та патентовласник Запорізький держ. мед. університет та автори. - № u 201007741; заявл. 21.06.2010; опубл. 25.11.2010, Бюл. № 22), який виявляє антиоксидантну дію. O O O- . HX+ H N HN O S N N CH2Ph 30 35 O X=HN . Сполука, що заявляється, та за структурою відрізняється від прототипу відсутністю в положенні 3 ксантинової молекули бензильної групи, у положенні 8 - залишку метилтіоацетатної кислоти та проявляє вищу антиоксидантну дію. До того ж прототип є сіллю. В основу корисної моделі поставлено задачу створення нової ефективної, малотоксичної речовини з антиоксидантною дією, яка після проведених фармакологічних досліджень може бути використана в медичній практиці. Поставлена задача вирішується синтезом (8-N-бензиламінотеофілініл-7)ацетатної кислоти (1-фенілетиліден) гідразиду (сполуки, що заявляється), формули: O O N N O N H N NH N N . 40 Приклад 1. Етап 1. Синтез 8-N-бензиламінотеофіліну 1 UA 71209 U 5 10 15 20 25 30 35 40 45 50 Розчин 13,0 г (0,05 моль) 8-бромотеофіліну (Хмелевский В. И. Получение 8-хлор- и 8бромтеофиллинов / В. И. Хмелевский, В. В. Павлова, О. И. Дурницына // Мед. пром-сть СССР.1966. - Т. 20, № і о. - С. 30-41) у 40 мл бензиламіну кип'ятять 30 хвилин, охолоджують до 70 °C і додають 100 мл ізопропілового спирту та 100 мл води, охолоджують. Через 24 години осад відфільтровують, промивають 1000 мл води, 100 мл 50 % ізопропілового спирту та 200 мл діетилового етеру. Кристалізують із водного діоксану. Вихід 9,5 г (67,8 %), Тпл.=203-5 °C. C14H15N5O2. Знайдено, %: С - 58,94; Н - 5,30; N - 24,55. Розраховано, %: С - 58,96; Н - 5,32; N 24,53. 7 ПМР-спектр (-шкала, розчинник - ДМСО, м.ч.): 11,61 (с, 1Н) - N H; 7,42 (м, 5Н) - СНаром; 7,78 1 3 (т, 1Н) - C8NH; 4,48 (д, 2Н) - CH2N; 3,35 (с, 3Н) – N CH3; 3,20(c1 3H) - N CH3. Етап 2. Синтез етилового естеру 8-N-бензиламінотеофілініл-7-ацетатної кислоти Суміш 2,85 г (0,01 моль) 8-N-бензиламінотеофілінілу, 1,4 г (0,012 моль) етилхлорацетату, 0,84 г (0,01 моль) NaHCO3, 30 мл диметилформаміду, кип'ятять 2 години і в гарячому стані фільтрують, фільтрат охолоджують, розводять водою 100 мл, осад відфільтровують, промивають водою та кристалізують із водного етанолу. Вихід 2,6 г (70,2 %), Тпл=164-6 °C. C18H21N5O4. Знайдено, %: С - 58,21; Н - 5,70; N - 18,86. Розраховано, %: С - 58,19; Н - 5,72; N 18,88. ПМР-спектр (-шкала, розчинник - ДМСО, м.ч.): 7,74 (т, 1Н) - C8NH; 7,32 (м, 5Н) - СНаром; 4,94 7 1 (с, 2Н) - N CH2; 4,57 (д, 2Н) - CH2N; 4,16 (кв, 2Н) - ОСН2; 3,36 (с, 3Н) – N CH3; 3,15 (с, 3Н) 3 N CH3. Етап 3. Синтез гідразиду 8-N-бензиламінотеофілініл-7-ацетатної кислоти До гарячого розчину 4,3 г (0,012 моль) етилового естеру 8-N-бензиламінотеофілініл-7ацетатної кислоти у 50 мл етанолу додають 4 мл (0,08 моль) гідразину гідрату, суміш кип'ятять 30 хвилин, охолоджують, осад відфільтровують, промивають водою та кристалізують із водного діоксану. Вихід 2,2 г (53,6 %), Тпл.=233-4 °C. C16H19N7O3. Знайдено, %: С - 53,77; Н - 5,36; N - 27,44. Розраховано, %: С - 53,75; Н - 5,34; N - 27,46. ПМР-спектр (-шкала, розчинник - ДМСО, м.ч.): 9,25 (пош.с, 1Н) - CONH; 7,54 (т, 1Н) - C8NH; 7 7,26 (м, 5Н) - СНаром; 4,73 (с, 2Н) - N CH2; 4,56 (д, 2Н) -CH2N; 4,26 (пош. с, 2Н) - NH2; 3,38 (с, 3Н) 1 3 – N CH3; 3,15 (с, 3Н) - N CH3. Етап 4. Синтез (8-N-бензиламінотеофілініл-7)ацетатної кислоти (1-фенілетиліден) гідразиду, сполуки, що заявляється Суміш 1,8 г (0,005 моль) гідразиду 8-N-бензиламінотеофілініл-7-ацетатної кислоти, 0,6 мл (0,005 моль) ацетофенону, 20 мл води та 20 мл діоксану кип'ятять 30 хв. При цьому додають 2 краплі хлористоводневої кислоти. Охолоджують, осад відфільтровують, промивають водою, 50 % ізопропіловим спиртом, ізопропіловим спиртом. Вихід 1,9 г (82,7 %), Тпл.=220-2 °C. C16H19N7O3. Знайдено, %: С - 62,73; Н - 5,48; N - 21,34. Розраховано, %: С - 62,75; Н - 5,46; N - 21,36. ПМР-спектр (-шкала, розчинник - ДМСО, м.ч.): 10,94 (пош.с, 1Н) - CONH; 7,81-7,15 - Ph (м, 8 7 1 10Н); 7,62-7,59 (т, 1Н) - C NH; 5,36 (с, 2Н) - N CH2; 4,59 (д, 2Н) - CH2NH; 2,27 (с, 3Н) – N CH3; 3 3,42 (с, 3Н) - N CH3. Приклад 2. Етап 1. Антиоксидантну активність досліджували за методом оцінки гальмування аутоокислення адреналіну в адренохром (Методи оцінки антиоксидантних властивостей фізіологічно активних сполук при ініціюванні вільнорадикальних процесів у дослідах in vitro / Губський Ю. І., Дунаев В.В., Бєленічев І.Ф. та інш. // Метод, реком. - Київ: ДФЦ МОЗ України, 2002. - 26 с.). Неферментативна реакція окислення адреналіну в адренохром в лужному середовищі супроводжується накопиченням супероксидрадикалу. У біологічних системах швидкість процесу залежить від активності ферменту супероксиддисмутази, але в хімічній системі in vitro ця реакція може бути застосовна для кількісної оцінки АОА досліджуваних сполук. Результати дослідження наведені в таблиці 1. 2 UA 71209 U Таблиця 1 -6 Антиоксидантна активність досліджуваних сполук (10 М) in vitro по інгібуванню супероксидрадикалу (М±m) Сполука (8-N-бензиламінотеофілініл-7)ацетатної кислоти (1фенілетиліден) гідразид Морфоліній (3-бензилксантиніл-8)метилтіоацетат Інтакт Контроль Тіотриазолін Емоксипін Оптична щільність 0,06±0,001* + + 0,068±0,002* 0,066±0,0008 0,2±0,001 0,072±0,001* 0,163±0,006* АОА % 70 66 35,8 18,5 Примітки: - р 0,05 по відношенню до інтакту; * - р 0,05 по відношенню до контролю; по відношенню до Емоксипіну. · 5 Етап 2. Оцінювання АОА сполук по інгібуванню NO -радикала (Ванин А.Ф. Динитрозольные комплексы железа и S-нитротиолы - две возможные формы стабилизации и транспорта оксида азота в биосистемах / А.Ф. Ванин // Биохимия.-1998. - Т.63, Вып.7. - С. 924-938). Фотоіндукція · натрію нітропрусиду супроводжується накопиченням NO -радикалу, про що судять за швидкістю окислення аскорбату, визначаючи спектрофотометрично оптичну щільність проби при 265 нм. Результати дослідження наведені в таблиці 2. Таблиця 2 -6 Антиоксидантна активність досліджуваних сполук (10 М) in vitro · по інгібуванню монооксиду азоту NO (M±m) Оптична щільність при 265 нм, Сполука (8-N-бензиламінотеофілініл-7)ацетатної кислоти (1фенілетиліден) гідразид Морфоліній (3-бензилксантиніл-8)метилтіоацетат Контроль N-АЦЦ Тіотриазолін 0,202±0,003* АОА % +# 65,7 +# 65,7 18,6 33,5 0,202±0,003* 0,59±0,03 0,48±0,002* + 0,392±0,006* Примітки: * - р 0,05 по відношенню до контролю; - р 0,05 по відношенню до Тіотриазоліну; р 0,05 по відношенню до N-АЦЦ. + 10 15 20 25 Етап 3. Метод оцінки АОА по інгібуванню окислювальної модифікації білка, що викликана реактивом Фентона (Ванин А.Ф. Динитрозольные комплексы железа и S-нитротиолы - две возможные формы стабилизации и транспорта оксида азота в биосистемах / А.Ф. Ванин // Биохимия.-1998. - Т.63, Вып.7. - С. 924-938). Для виявлення глибини патологічного процесу та ступеня розвитку окислювального стресу в тканинах головного мозку виявляли продукти окислювальної модифікації білка за реакцією взаємодії окислених амінокислотних залишків з 2,4-динітрофенілгідразином. Ініціацію окислювальної модифікації білка проводили в гомогенаті мозку нелінійних білих щурів з використанням серодовища Фентона. До 250 мг гомогенату тканини додають 7 мл 0,5 М фосфатного буферу (температура розведення 5 °C) та центрифугують при 11000g 30 хв. (при температурі 10 °C). До 0,1 мл підготовленого супернатанту додавали 0,1 мл досліджуваних -6 речовин (С = 10 М), 0,1 мл 2,8 % розчину феррум (II) сульфату, 0,1 мл 4 % гідроген пероксиду та інкубували при температурі 37 °C протягом 2 год. Потім додавали 0,1 мл 20 % розчину трихлороацетатної кислоти та центрифугували 30 хв. при 3000 об./хв. (при температурі 15 °C). До осаду, який залишився після центрифугування, додавали 1 мл 2,2 % 2,4динітрофенілгідразину (виготовленого на 7 % розчині хлоридної кислоти), інкубували 1 год. при температурі 37 °C та центрифугували 10 хв. при 3000 об/хв. Осад промивали 3 мл етилацетату, 3 UA 71209 U 5 висушували його та додавали 3 мл 8М розчину сечовини і 1 мл 2 М розчину хлоридної кислоти. Підготовлений розчин спектрофотометрували при довжині хвилі 274, 363 нм (розчин порівняння - 0,5 М фосфатний буфер). За показником екстинкції визначали кількість карбонільних і карбоксильних груп. Як еталон порівняння використовували емоксипін та тіотриазолін. Результати дослідження наведені в таблиці 3. Таблиця 3 -6 Антиоксидантна активність досліджуваних сполук (10 М) in vitro по інгібуванню окислювальної модифікації білка (М±m) Сполука (8-N-бензиламінотеофілініл-7)ацетатної кислоти (1-фенілетиліден) гідразид Морфоліній (3-бензилксантиніл8)метилтіоацетат Інтакт Контроль Емоксипін Тіотриазолін АФГ, у.о./г АОА, % КФГ, у.о./г 5,00±0,04* + 50,0 2,87±0,01* 5,61±0,01* + 43,7 3,52±0,02* ∆ 1,07±0,002 9,95±0,07 7,0±0,002* 6,00±0,01* 30 40 АОА, % + 58,3 + 48,8 ∆ 1,37±0,02 6,87±0,002 4,87±0,01* 3,75±0,01* 30,0 45,5 Примітки: - р 0,05 по відношенню до інтакту; * - р 0,05 по відношенню до контролю; - р 0,05 по відношенню до Емоксипіну. + 10 15 20 Дослідження АОА по інгібуванню супероксидрадикалу в системі аутоокислення адреналіну в адренохром показало, що синтезована сполука проявляє досліджувану активність і за силою антиоксидантного ефекту перевершує активність прототипу на 4 %, тіотриазоліну - на 34,2 % та емоксипіну - на 51,5 %. Сполука, що заявляється, за величиною антиоксидантної дії по інгібуванню монооксиду · азоту NO виявилась рівною прототипу, проте активнішою, ніж тіотриазолін та N-АЦЦ на 32,2 % та 47,1 % відповідно. Дослідження антиоксидантної активності (8-N-бензиламінотеофілініл-7)ацетатної кислоти (1фенілетиліден) гідразиду, сполуки, що заявляється, по відношенню до інгібування окислювальної модифікації білка виявило, що синтезована сполука проявляє заявлений вид активності та за величиною його перевищує активність прототипу на 6,3 % (при визначенні АФГ) та 9,5 % (при визначенні КФГ), а також активність еталонів порівняння. Таким чином, наведені вище дані свідчать про те, що після фармакологічних досліджень сполука, що заявляється, може бути використана як антиоксидантний засіб в медичній практиці. ФОРМУЛА КОРИСНОЇ МОДЕЛІ 25 (8-N-бензиламінотеофілініл-7)ацетатної кислоти (1-фенілетиліден) гідразид формули: O O N N O N H N NH N N , який виявляє антиоксидантну дію. 4 UA 71209 U Комп’ютерна верстка М. Ломалова Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 5
ДивитисяДодаткова інформація
Назва патенту англійською(8-n-benzylaminotheophyllinyl-7)acetic acid (1-phenylethylidene)hydrazide exhibiting antioxidant activity
Автори англійськоюYurchenko Daria Mykolaivna, Belenichev Igor Fedorovych, Aleksandrova Kateryna Viacheslavivna, Romanenko Mykola Ivanovych, Bukhtiiarova Nina Viktorivna
Назва патенту російською(8-n-бензиламинотеофиллинил-7)уксусной кислоты (1-фенилэтилиден) гидразид, который проявляет антиоксидантное действие
Автори російськоюЮрченко Дарья Николаевна, Беленичев Игорь Федорович, Александрова Екатерина Вячеславовна, Романенко Николай Иванович, Бухтиярова Нина Викторовна
МПК / Мітки
МПК: C07D 473/00
Мітки: кислоти, виявляє, 1-фенілетиліден, дію, гідразид, 8-n-бензиламінотеофілініл-7)ацетатної, антиоксидантну
Код посилання
<a href="https://ua.patents.su/7-71209-8-n-benzilaminoteofilinil-7acetatno-kisloti-1-feniletiliden-gidrazid-yakijj-viyavlyaeh-antioksidantnu-diyu.html" target="_blank" rel="follow" title="База патентів України">(8-n-бензиламінотеофілініл-7)ацетатної кислоти (1-фенілетиліден) гідразид, який виявляє антиоксидантну дію</a>
Попередній патент: Спосіб лікування м’якої та помірної артеріальної гіпертензії у хворих з абдомінальним ожирінням
Наступний патент: Спосіб визначення активності g-глютамілтранспептидази в паренхімі нирки в експерименті
Випадковий патент: Пристрій для лікування хвороб хребта











