Похідні піридазинону як агоністи рецептора тиреоїдного гормону
Номер патенту: 88104
Опубліковано: 10.09.2009
Автори: Кертеш Деніс Джон, П'єтраніко-Коле Шеррі Лінн, Тіллі Джефферсон Райт, Скотт Натан Роберт, Цянь Імінь, Тхаккар Кшітій Чхабільбхай, Со Сун-Сау, Хейнз Ненсі-Еллен
Формула / Реферат
1. Сполуки формули (І):
 , (I)
, (I)
де:
А являє собою О, СH2, S, SO або SO2;
Х та Y кожний незалежно вибраний із групи, яка складається з Br, C1 та -СН3;
R1 вибраний із групи, яка складається з:
-(СН2)nСООН;
-ОСН2СООН;
-NHC(=O)COOH;
-NHCH2COOH;
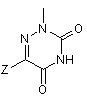 та
та ![]() ;
;
Z являє собою Н або ![]() ;
;
R2 являє собою нижчий алкіл;
R3 являє собою Н або нижчий алкіл;
n має значення 1, 2 або 3;
р має значення 1 або 2;
або їх фармацевтично прийнятні солі або складні ефіри.
2. Сполуки за п. 1, де Х та Y кожний являє собою Br.
3. Сполуки за п. 1, де Х та Y кожний являє собою Сl.
4. Сполуки за п. 1, де X та Y кожний являє собою -СН3.
5. Сполуки за п. 1, де Х являє собою Сl та Y являє собою -СН3.
6. Сполуки за п. 1, де R1 вибраний із групи, яка складається з:
-(СH2)nСООН;
-ОСН2СООН;
-NHC(=O)COOH і
-NHCH2COOH;
та їх складні ефіри.
7. Сполуки за п. 6, де R1 являє собою -(СH2)nСООН.
8. Сполуки за п. 7, де n означає 1.
9. Сполуки за п. 6, де R1 являє собою -NHC(=O)COOH.
10. Сполуки за п. 1, де R1 являє собою:
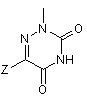 або
або ![]() .
.
11. Сполуки за п. 10, де R1 являє собою:
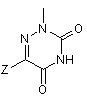 .
.
12. Сполуки за п. 11, де Z являє собою CN.
13. Сполуки за п. 1, де R2 являє собою нижчий алкіл, який містить від 1 до 3 атомів С.
14. Сполуки за п. 11, де R2 являє собою нижчий алкіл, який містить 3 атоми С.
15. Сполуки за п. 1, де R3 являє собою СН3.
16. Сполука за п. 1, яка являє собою:
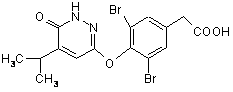 ,
,
або її фармацевтично прийнятна сіль або складний ефір.
17. Сполука за п. 1, яка являє собою:
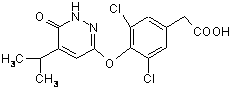 ,
,
або її фармацевтично прийнятна сіль.
18. Сполука за п. 1, яка являє собою:
 ,
,
або її фармацевтично прийнятна сіль або складний ефір.
19. Сполука за п. 1, яка являє собою:
 ,
,
або її фармацевтично прийнятна сіль або складний ефір.
20. Сполука за п. 1, яка являє собою:
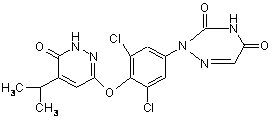 ,
,
або її фармацевтично прийнятна сіль або складний ефір.
21. Сполука за п. 2, яка являє собою:
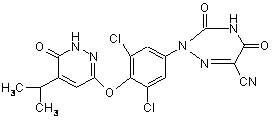 ,
,
або її фармацевтично прийнятна сіль або складний ефір.
22. Сполука за п. 1, вибрана із групи, яка складається з наступних сполук:
[4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілокси)-3,5-диметилфеніл]оцтова кислота,
[3-хлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілокси)-5-метилфеніл]оцтова кислота,
[3,5-дибром-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілокси)феніл]оцтова кислота,
[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілокси)феніл]оцтова кислота,
3-[3,5-дибром-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілокси)феніл]пропіонова кислота,
[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілокси)феніламіно]оцтова кислота,
N-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілокси)феніл]оксаламова кислота,
2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілокси)феніл]-3,5-діоксо-2,3,4,5-тетрагідро-[1,2,4]триазин-6-карбонітрил,
2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілокси)феніл]-2Н-[1,2,4]триазин-3,5-діон,
[3,5-дихлор-4-(5-ізопропіл-1-метил-6-оксо-1,6-дигідропіридазин-3-ілокси)феніл]оцтова кислота,
[3,5-дихлор-4-(5-ізопропіл-1-метил-6-оксо-1,6-дигідропіридазин-3-ілокси)феніл]оцтова кислота,
2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілметил)феніл]-3,5-діоксо-2,3,4,5-тетрагідро-[1,2,4]триазин-6-карбонітрил,
2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілметил)феніл]-[1,2,4]триазин-3,5-діон,
[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілметил)феніл]оцтова кислота,
[3,5-дибром-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілметил)феніл]оцтова кислота,
2-[3,5-дихлор-4-(5-ізопропіл-1-метил-6-оксо-1,6-дигідропіридазин-3-ілокси)феніл]-3,5-діоксо-2,3,4,5-тетрагідро[1,2,4]триазин-6-карбонітрил,
[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-ілсульфаніл)феніл]оцтова кислота,
[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-сульфініл)феніл]оцтова кислота,
[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-сульфоніл)феніл]оцтова кислота,
2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-сульфоніл)феніл]-3,5-діоксо-2,3,4,5-тетрагідро-[1,2,4]триазин-6-карбонітрил,
2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3-сульфоніл)феніл]-2Н-[1,2,4]триазин-3,5-діон та
2-[3,5-дихлор-4-(5-ізопропіл-1-метил-6-оксо-1,6-дигідропіридазин-3-ілметил)феніл]-3,5-діоксо-2,3,4,5-тетрагідро-[1,2,4]триазин-6-карбонітрил,
або її фармацевтично прийнятні солі або складні ефіри.
23. Сполуки за будь-яким з пп. 1-22 для застосування як терапевтично активних речовин.
24. Сполуки за будь-яким з пп. 1-22 для застосування як терапевтично активних речовин для лікування і/або профілактики захворювань, які модулюються аналогами тиреоїдного гормону.
25. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-22 та фармацевтично прийнятний носій і/або ад'ювант.
Текст
1. Сполуки формули (І): 2 (19) 1 3 88104 4 або її фармацевтично прийнятна сіль або складний ефір. O N N 22. Сполука за п. 1, вибрана із групи, яка складаNH ється з наступних сполук: Z [4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3O . ілокси)-3,5-диметилфеніл]оцтова кислота, 12. Сполуки за п. 11, де Z являє собою CN. [3-хлор-4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин13. Сполуки за п. 1, де R2 являє собою нижчий 3-ілокси)-5-метилфеніл]оцтова кислота, алкіл, який містить від 1 до 3 атомів С. [3,5-дибром-4-(5-ізопропіл-6-оксо-1,614. Сполуки за п. 11, де R2 являє собою нижчий дигідропіридазин-3-ілокси)феніл]оцтова кислота, алкіл, який містить 3 атоми С. [3,5-дихлор-4-(5-ізопропіл-6-оксо-1,615. Сполуки за п. 1, де R3 являє собою СН3. дигідропіридазин-3-ілокси)феніл]оцтова кислота, 16. Сполука за п. 1, яка являє собою: 3-[3,5-дибром-4-(5-ізопропіл-6-оксо-1,6H Br дигідропіридазин-3-ілокси)феніл]пропіонова кисO N лота, N COOH [3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілокси)феніламіно]оцтова кисH3C O лота, CH3 Br , N-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6або її фармацевтично прийнятна сіль або складдигідропіридазин-3-ілокси)феніл]оксаламова кисний ефір. лота, 17. Сполука за п. 1, яка являє собою: 2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6H Cl дигідропіридазин-3-ілокси)феніл]-3,5-діоксоO N 2,3,4,5-тетрагідро-[1,2,4]триазин-6-карбонітрил, N COOH 2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілокси)феніл]-2НH3C O [1,2,4]триазин-3,5-діон, CH3 Cl , [3,5-дихлор-4-(5-ізопропіл-1-метил-6-оксо-1,6або її фармацевтично прийнятна сіль. дигідропіридазин-3-ілокси)феніл]оцтова кислота, 18. Сполука за п. 1, яка являє собою: [3,5-дихлор-4-(5-ізопропіл-1-метил-6-оксо-1,6H Cl дигідропіридазин-3-ілокси)феніл]оцтова кислота, O N 2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6N COOH дигідропіридазин-3-ілметил)феніл]-3,5-діоксо2,3,4,5-тетрагідро-[1,2,4]триазин-6-карбонітрил, H3C O 2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6CH3 CH3 , дигідропіридазин-3-ілметил)феніл]-[1,2,4]триазинабо її фармацевтично прийнятна сіль або склад3,5-діон, ний ефір. [3,5-дихлор-4-(5-ізопропіл-6-оксо-1,619. Сполука за п. 1, яка являє собою: дигідропіридазин-3-ілметил)феніл]оцтова кислота, H H3C [3,5-дибром-4-(5-ізопропіл-6-оксо-1,6O N дигідропіридазин-3-ілметил)феніл]оцтова кислота, N COOH 2-[3,5-дихлор-4-(5-ізопропіл-1-метил-6-оксо-1,6дигідропіридазин-3-ілокси)феніл]-3,5-діоксоH3C O 2,3,4,5-тетрагідро[1,2,4]триазин-6-карбонітрил, CH3 CH3 , [3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6або її фармацевтично прийнятна сіль або складдигідропіридазин-3-ілсульфаніл)феніл]оцтова кисний ефір. лота, 20. Сполука за п. 1, яка являє собою: [3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6O дигідропіридазин-3-сульфініл)феніл]оцтова кислоH та, N H Cl [3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6O N N O N дигідропіридазин-3-сульфоніл)феніл]оцтова кисN лота, H3 C O 2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6CH3 Cl дигідропіридазин-3-сульфоніл)феніл]-3,5-діоксо, 2,3,4,5-тетрагідро-[1,2,4]триазин-6-карбонітрил, або її фармацевтично прийнятна сіль або склад2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6ний ефір. дигідропіридазин-3-сульфоніл)феніл]-2Н21. Сполука за п. 2, яка являє собою: O [1,2,4]триазин-3,5-діон та H 2-[3,5-дихлор-4-(5-ізопропіл-1-метил-6-оксо-1,6N H Cl дигідропіридазин-3-ілметил)феніл]-3,5-діоксоO O N N N 2,3,4,5-тетрагідро-[1,2,4]триазин-6-карбонітрил, N або її фармацевтично прийнятні солі або складні CN H3C O ефіри. CH3 Cl 23. Сполуки за будь-яким з пп. 1-22 для застосу, вання як терапевтично активних речовин. 5 88104 6 24. Сполуки за будь-яким з пп. 1-22 для застосу25. Фармацевтична композиція, яка містить сполування як терапевтично активних речовин для лікуку за будь-яким з пп. 1-22 та фармацевтично привання і/або профілактики захворювань, які модуйнятний носій і/або ад'ювант. люються аналогами тиреоїдного гормону. Даний винахід стосується нових лігандів тиреоїдного рецептора, зокрема аналогів піридазинону формули (І): де: А являє собою О, СН2, S, SO або SO2; X та Υ кожний незалежно вибраний із групи, яка складається з Br, СІ та -СН3; R1 вибраний із групи, яка складається з -(СН2)nСООН; -ОСН2СООН; -NHC(=O)COOH; -NHCH2COOH; Ζ являє собою Η або -O=N; R2 являє собою нижчий алкіл, який містить від 1 до 4 атомів С; R3 являє собою Η або нижчий алкіл; n має значення 1 або 2; p має значення 1 або 2; або їх фармацевтично прийнятних солей або складних ефірів. Винахід також стосується способів одержання таких сполук, які є корисними для лікування метаболічних захворювань, таких як ожиріння, гіперліпідемія, гіперхолестеринемія та діабети, та можуть використовуватися для лікування інших порушень та захворювань, таких як NASH (неалкогольний стеатогепатит), стеатоз печінки, атеросклероз, серцево-судинні захворювання, гіпотироїдизм, рак щитовидної залози та близькі порушення та захворювання. Всі документи, зазначені або наведені нижче, повністю наведені тут як посилання. Тиреоїдні гормони є критичними для нормального росту та розвитку та для підтримування метаболічного гомеостазу [Paul M. Yen Physiological reviews, 2001, Т. 81(3), cc. 1097-1126]. Циркулюючі рівні тиреоїдних гормонів в основному регулюються механізмами зворотного зв'язку в гіпоталамусній/пітуїтарній/тиреоїдній (НРТ) вісі. Дисфункція щитовидної залози, що приводить до гіпотироїдизму або гіпертиреоїдизму, ясно демонструє, що тиреоїдні гормони здійснюють глибокі дії на серцеву функцію, масу тіла, метаболізм, швидкість метаболізму, температуру тіла, холестерин, кісткову систему, м'язи та поведінку. Тиреоїдини гормон виробляється підшлунковою залозою та секретується в циркулюючу систему у вигляді двох різних форм, 3,5,3',5'-тетрайод-L-тиронін (Т4) та 3,5,3'-три-йод-L-тиронін (Т3). Хоча Т4 є переважною формою, що секретується щитовидною залозою, Т3 є більш біологічно активною формою. Т4 перетворюється на Т3 за допомогою тканиноспецифічних дейодиназ у всіх тканинах, але переважно в печінці та нирках. Біологічна активність тиреоїдних гормонів опосередкована рецепторами тиреоїдного гормону (TR) [М.А. Lazar Endocrine Reviews, 1993, Т. 14, cc. 348399]. TR належать до суперсімейства, відомого як ядерні рецептори. TR утворюють гетеродимери з ретиноїдним рецептором, який виступає як фактори транскрипції, що індукуються лігандом. TR містять лігандзв'язуючий домен, ДНК-зв'язуючий домен та амінотермінальний домен, та регулюють експресію гена шляхом взаємодії із ДНКвідповідними елементами та з різними ядерними співактиваторами та співрепресорами. Рецептори тиреоїдного гормону виходять із двох різних генів, a та b. Ці продукти різних генів виробляють множинні форми їх відповідних рецепторів за допомогою диференціального процесингу РНК. Основними ізоформами тиреоїдного рецептора є a1, a2, b1 та b2. Рецептори тиреоїдного гормону a1, b1 та b2 зв'язують тиреоїдини гормон. Було показано, що підтипи рецептора тиреоїдного гормону можуть розрізнятися за їх внеском в специфічні біологічні відповіді. Останні дослідження припустили, що TRb1 відіграє важливу роль у регулюванні TRH (гормон, що вивільняє тиротропін) та в регулюванні дій тиреоїдного гормону в печінці. TRb2 відіграє важливу роль у регулюванні TSH (тиреоїдстимулюючий гормон) [Abel та ін., J. Clin. Invest., 1999, Т. 104, cc. 291-300]. TRb1 відіграє важливу роль у регулюванні швидкості роботи серця [В. Gloss та ін., Endocrinology, 2001, Т. 142, сc. 544550; С. Johansson та ін., Am. J. Physiol., 1998, Т. 275, cc. R640-R646]. Деякі дії тиреоїдних гормонів можуть бути терапевтично вигідними, якщо побічні ефекти можуть бути мінімізовані або усунуті [Paul M. Yen, Physiological Reviews, 2001, Т. 81(3), cc. 1097-1126; Paul Webb, Expert Opin. Investig. Drugs, 2004, T. 13(5), cc. 489-500]. Наприклад, тиреоїдні гормони підвищують швидкість метаболізму, споживання кисню та вироблення тепла, і, отже, знижують масу тіла. Зниження маси тіла буде здійснювати сприятливу дію на пацієнтів з ожирінням завдяки поліпшенню захворювань, пов'язаних з ожирінням, 7 88104 8 та також можуть здійснювати сприятливу дію на Pharmaceutical Design, 2004, T. 10(28), cc. 3525глікемічний контроль у пацієнтів з ожирінням з діа3532; Expert Opin. Ther. Patents, 2004, T. 14, cc. бетом типу 2. 1169-1183; Thomas S. Scalan, Current Opinion in Іншою терапевтично сприятливою дією тиреоDrug Discovery & Development, 2001, T. 4 (5), cc. їдного гормону є зниження ліпопротеїну низької 614-622; Paul Webb, Expert Opinion on густини в сироватці (LDL) [Eugene Morkin та ін., Investigational Drugs, 2004, T. 13 (5), cc. 489-500]. 2004, Journal of Molecular and Cellular Cardiology, T. Розробка аналогів тиреоїдного гормону, які 37, cc. 1137-1146]. Було виявлено, що гіпертиреоїусувають побічні дії гіпертиреоїдизму та гіпотироїдизм пов'язаний з низьким загальним рівнем холедизму, у той же час підтримуючи сприятливі дії стерину в сироватці, що пояснюється підвищенням тиреоїдних гормонів, відкривають нові шляхи для тиреоїдним гормоном експресії рецептора печінлікування пацієнтів з метаболічними захворюванкового LDL та стимуляцією метаболізму холестенями, такими як ожиріння, гіперліпідемія, гіперхорину в жовчні кислоти [J.J. Abrams та ін., J. Lipid лестеринемія, діабети та інші порушення та захвоRes., 1981, Т. 22, cc. 323-38]. Гіпотироїдизм, у рювання, такі як стеатоз печінки та NASH, свою чергу, пов'язаний з гіперхолестеринемією, та атеросклероз, серцево-судинні захворювання, тиреоїдна гормонзамісна терапія, як відомо, знигіпотироїдизм, рак щитовидної залози, тиреоїдні жує загальний рівень холестерину [М. Aviram та захворювання та близькі порушення та захворюін., Clin. Biochem., 1982, Т. 15, cc. 62-66; J.J. вання. Abrams та ін., J. Lipid Res., 1981, T. 22, cc. 323-38]. Сполуки піридазинону, які структурно відрізНа тваринних моделях було показано, що тиреоїняються від сполук за даним винаходом, описані дини гормон здійснює сприятливу дію на підвираніше [Teruomi та ін., Agricultural and Biological щення холестерину HDL та поліпшення співвідноChemistry, 1974, Т. 38(6), cc. 1169-76; P.D. Leeson шення LDL з HDL шляхом підвищення експресії та ін., J. Med. Chem. Т., 1989, 32, cc. 320-326; EP апо-А-1, одного з основних аполіпопротеїнів HDL 188351 (1986); Damien John Dunnington WO [Gene С. Ness та ін., Biochemical Pharmacology, 9702023 (1997) та ЕР 728482 (1996)]. 1998, Т. 56, cc. 121-129; G.J. Grover та ін., Незважаючи на ці передумови, отже, все ще Endocrinology, 2004, Т. 145, cc. 1656-1661; G.J. існує потреба в нових міметиках тиреоїдного горGrover та ін., Proc. Natl. Acad. Sci. USA, 2003, T. мону, таких як, наприклад, нові піридазинонові 100, cc. 10067-10072]. Через їх дії на холестерин міметики тиреоїдного гормону, які проявляють LDL та HDL, можливо, що тиреоїдні гормони також покращені дії у відношенні тиреоїдного гормону, у можуть знижувати ризик атеросклерозу та інших той же час усуваючи побічні ефекти. серцево-судинних захворювань. Випадки атероСлід розуміти, що використовувана тут термісклеротичних васкулярних захворювань прямо нологія наведена з метою опису конкретних варіазв'язані з рівнем холестерину LDL. Крім того, існує нтів здійснення, та не призначена для обмеження. доказ того, що тиреоїдні гормони знижують рівні Крім того, хоча будь-які способи, пристрої та маліпопротеїну (а), важливого фактора ризику, що теріали, аналогічні або еквівалентні описаним тут підвищується в пацієнтів з атеросклерозом [Paul способам, пристроям та матеріалам, можуть викоWebb, Expert Opin. Investig. Drags, 2004, T. 13(5), ристовуватися для здійснення або перевірки винаcc. 489-500; de Bruin та ін., J. Clin. Endo. Metab., ходу, кращі способи, пристрої та матеріали описа1993, T. 76, cc. 121-126]. ні далі. Враховуючи випадки ожиріння та супутніх заЯк тут використовується, термін "алкіл" ознахворювань, діабетів, метаболічного синдрому та чає, наприклад, розгалужену або нерозгалужену, атеросклеротичного васкулярного захворювання, циклічну або ациклічну, насичену або ненасичену які підвищуються зі швидкістю епідемії, корисність (наприклад алкеніл або алкініл) вуглеводневу грусполук, здатних лікувати ці захворювання, є незапу, яка може бути заміщеною або незаміщеною. У перечною. На сьогоднішній день терапевтичні завипадку циклічної групи, алкільна група є перевастосування природного тиреоїдного гормону обжно С3-С12 групою, більш краще С4-С10 групою, межені небажаними побічними діями, пов'язаними найкраще С4-С7 групою. У випадку ациклічної груз гіпертиреоїдизмом, та особливо із серцевопи, алкільна група являє собою переважно С1-С10 групу, більш краще С1-С6 групу, більш краще месудинною токсичністю. тил, етил, пропіл (н-пропіл або ізопропіл), бутил (нОтже, були зроблені спроби для одержання бутил, ізобутил або трет-бутил) або пентил (вклюаналогів тиреоїдного гормону, які проявляють підчаючи н-пентил та ізопентил), більш краще метил. вищену селективність до бета-рецептора тиреоїдЗрозуміло, що термін "алкіл" як тут використовуного гормону і/або тканеселективну дію. Такі мімеється включає алкіл (розгалужений або нерозгатики тиреоїдного гормону можуть приводити до лужений), заміщений алкіл (розгалужений або небажаних знижень маси тіла, рівня ліпідів, холестерозгалужений), алкеніл (розгалужений або рину та ліпопротеїнів, при зниженій дії на серцевонерозгалужений), заміщений алкеніл (розгалужесудинну функцію або нормальну функцію гіпотаний або нерозгалужений), алкініл (розгалужений ламусної/пітуїтарної/тиреоїдної вісі [А.Н. або нерозгалужений), заміщений алкініл (розгалуUnderwood та ін., Nature, 1986, Т. 324, cc. 425-429, жений або нерозгалужений), циклоалкіл, заміщеG. J. Grover та ін., PNAS, 2003, Т. 100, cc. 10067ний циклоалкіл, циклоалкеніл, заміщений циклоал10072; G.J. Grover, Endocrinology, 2004, T. 145, cc. кеніл, циклоалкініл та заміщений циклоалкініл. 1656-1661; Yi-lin Li та ін., WO 9900353 (1999); Як тут використовується, термін "нижчий алThomas S. Scanlan та ін., WO 9857919 (1998); Keith кіл" означає, наприклад, розгалужену або нерозгаA. Walker та ін., US 5,284,971 (1994); Mark D. Erion лужену, циклічну або ациклічну, насичену або нета ін., WO 2005051298 (2005); Malm Johan, Current 9 88104 10 насичену (наприклад алкеніл або алкініл) вуглевофоксиди та сульфони (наприклад алкілтіо, алкілдневу групу, де зазначена циклічна нижча алкільна сульфініл, алкілсульфоніл, алкілтіоалкіл, група є С5, С6 або С7 групою, та де зазначена ациалкілсульфінілалкіл, алкілсульфонілалкіл, арилтіо, клічна нижча алкільна група є С1, С2, С3, С4, С5 або арилсульфініл, арилсульфоніл, арилтіоалкіл, ариС6 групою, бажано містить від 1 до 4 атомів вуглелсульфінілалкіл, арилсульфонілалкіл); та гетероцю. Звичайні нижчі алкільні групи включають мециклічні групи, які містять один або декілька, перетил, етил, пропіл (н-пропіл або ізопропіл), бутил (нважно один гетероатом, (наприклад тієніл, бутил, ізобутил або трет-бутил), пентил та гексил. фураніл, піроліл, імідазоліл, піразоліл, тіазоліл, Отже, зрозуміло, що термін "нижчий алкіл" як тут ізотіазоліл, оксазоліл, оксадіазоліл, тіадіазоліл, використовується включає, наприклад, нижчий азиридиніл, азетидиніл, піролідиніл, піролініл, іміалкіл (розгалужений або нерозгалужений), нижчий дазолідиніл, імідазолініл, піразолідиніл, тетрагідалкеніл (розгалужений або нерозгалужений), нижрофураніл, піраніл, піроніл, піридил, піразиніл, чий алкініл (розгалужений або нерозгалужений), піридазиніл, піперидил, гексагідроазепініл, піперациклонижчийалкіл, циклонижчийалкеніл та циклозиніл, морфолініл, тіанафтил, бензофураніл, ізонижчийалкініл. При приєднанні до іншої функціобензофураніл, індоліл, оксііндоліл, ізоіндоліл, іннальної групи, нижчий алкіл як тут використовудазоліл, індолініл, 7-азаіндоліл, бензопіраніл, ється може бути дивалентним, наприклад, -нижчий кумариніл, ізокумариніл, хінолініл, ізохінолініл, алкіл-СООН. Ациклічні, розгалужені або нерозганафтиридиніл, цінолініл, хіназолініл, піридопірилужені нижчі алкільні групи є кращими. дил, бензоксазиніл, хіноксалініл, хроменіл, хромаУ положенні R2 формули (І), нижчий алкіл місніл, ізохроманіл, фталазиніл та карболініл). тить від 1 до 4 атомів вуглецю. Кращий R являє Нижчі алкільні групи можуть бути заміщеними собою нижчий алкіл, який містить 3 атоми вуглеабо незаміщеними, переважно незаміщеними. цю. Більш кращим є ізопропіл. Коли вони є заміщеними, звичайно є присутні, наЯк тут використовується, термін "арил" ознаприклад, 1-3 замісники, краще 2 замісники. чає, наприклад, заміщену або незаміщену карбоЯк тут використовується, термін "алкоксі" циклічну ароматичну групу, таку як феніл або нафозначає, наприклад, алкіл-О- та "алкоїл" означає, тил, або заміщену або незаміщену наприклад, алкіл-СО-. Групи алкоксизамісника або гетероароматичну групу, яка містить один або дегрупи алкоксивмісного замісника можуть бути закілька, краще один, гетероатом, такий як піридил, міщеними, наприклад, однією або декількома алкіпіроліл, фураніл, тієніл, тіазоліл, ізотіазоліл, оксальними групами. золіл, ізоксазоліл, оксадіазоліл, тіадіазоліл, піраЯк тут використовується, термін "галоген" золіл, імідазоліл, триазоліл, пирімідиніл, піридазиозначає, наприклад, групу фтору, хлору, брому ніл, піразиніл, триазиніл, індоліл, індазоліл, або йоду, переважно групу хлору або брому, та хіноліл, хіназоліл, бензімідазоліл, бензотіазоліл, більш краще групу хлору. бензізоксазоліл та бензізотіазоліл. "Фармацевтично прийнятний," такий як фарАлкільні та арильні групи можуть бути заміщемацевтично прийнятний носій, ексципієнт і т.д., ними або незаміщеними. Коли вони є заміщеними, означає фармакологічно прийнятний та по суті звичайно присутні, наприклад, 1-3 замісники, кранетоксичний для суб'єкта, якому вводять конкретще 2 замісники. Замісники можуть включати, нану сполуку. приклад: вуглець-вмісні групи, такі як алкіл, арил, "Фармацевтично прийнятна сіль" стосується арилалкіл (наприклад, заміщений та незаміщений звичайних кислотних адитивних солей або основфеніл, заміщений та незаміщений бензил); атоми них адитивних солей, які зберігають біологічну галогену та галоген-вмісні групи, такі як галогеналефективність та властивості сполук формули І та кіл (наприклад трифторметил); кисень-вмісні груутворюються з придатних органічних або неорганіпи, такі як спирти (наприклад, гідроксил, гідроксіачних кислот або органічних або неорганічних ослкіл, арил(гідроксил)алкіл), прості ефіри нов. Приклади кислотних адитивних солей вклю(наприклад алкоксі, арилоксі, алкоксіалкіл, арилокчають солі, одержані з неорганічних кислот, таких сіалкіл), альдегіди (наприклад, карбоксальдегід), як хлористоводнева кислота, бромистоводнева кетони (наприклад, алкіл карбоніл, алкіл карбонікислота, йодистоводнева кислота, сірчана кислолалкіл, арилкарбоніл, арилалкіл карбоніл, арилката, сульфамінова кислота, фосфорна кислота й рбонілалкіл), кислоти (наприклад, карбокси, карбоазотна кислота, та солі, одержані з органічних кисксіалкіл), похідні кислот, такі як складні ефіри лот, таких як n-толуолсульфонова кислота, салі(наприклад, алкоксикарбоніл, алкоксикарбонілалцилова кислота, метансульфонова кислота, щавкіл, алкіл карбонілоксі, алкіл карбонілоксіалкіл), лева кислота, бурштинова кислота, лимонна аміди (наприклад, амінокарбоніл, моно- або діалкислота, яблучна кислота, молочна кислота, фукіл амінокарбоніл, амінокарбонілалкіл, або діалкіл марова кислота та їм подібні. Приклади основних амінокарбонілалкіл, ариламінокарбоніл), карбамаадитивних солей включають солі, одержані з гідти (наприклад, алкоксикарбоніламіно, арилоксикароксидів амонію, калію, натрію та четвертинного рбоніламіно, амінокарбонілоксі, або діалкіл аміноамонію, такого як, наприклад, гідроксид тетрамекарбонілоксі, ариламінокарбонілокси) та сечовини тиламонію. Хімічна модифікація фармацевтичної (наприклад, моно- або діалкіл амінокарбоніламіно сполуки (тобто лікарського препарату) у сіль є доабо ариламінокарбоніламіно); азот-вмісні групи, бре відомою методикою, яка використовується для такі як аміни (наприклад, аміно, моно- або діалкіл поліпшення властивостей, включаючи фізичну або аміно, аміноалкіл, моно- або діалкіл аміноалкіл), хімічну стабільність, наприклад, гігроскопічність, азиди, нітрили (наприклад, ціано, ціаноалкіл), нітплинність або розчинність сполук. [Див., наприро; сірко-вмісні групи, такі як тіоли, тіоефіри, сульклад, Н. Ansel та ін., Pharmaceutical Dosage Forms 11 88104 12 and Drug Delivery Systems (6-е видання, 1995), cc. R3 являє собою Η або нижчий алкіл; 196 та 1456-1457]. n має значення 1, 2 або 3; "Фармацевтично прийнятні складні ефіри" p має значення 1 або 2; означають звичайним чином етерифіковану сполуабо їх фармацевтично прийнятних солей або ку формули І, яка містить карбоксильну групу, прискладних ефірів. чому складні ефіри зберігають біологічну ефектиСполуки формули (І) індивідуально є кращими вність та властивості сполук формули І, та та їх фізіологічно прийнятні солі індивідуально є розщеплюються in vivo (в організмі) у відповідну кращими та їх фармацевтично прийнятні складні активну карбонову кислоту. У даному винаході ефіри індивідуально є кращими, причому сполуки складні ефіри можуть бути присутніми, наприклад, формули (І) є особливо кращими. коли R1 являє собою -(СН2)nСООН, -ОСН2СООН, Сполуки формули (І) можуть мати один або NHC(=O)COOH або -NHCH2COOH. Прикладами декілька асиметричних атомів С або S, і отже, москладноефірних груп, які відщеплюються (у випаджуть існувати у вигляді енантіомерної суміші, суку гідролізу) in vivo у відповідні карбонові кислоти, міші стереоізомерів або у вигляді оптично чистих є групи, у яких водень заміщений -нижчим алкілом, сполук. який є необов'язково заміщеним, наприклад, гетеКращими сполуками формули (І), як описано роциклом, циклоалкілом та т.д. Прикладами замівище, є сполуки, де X та Υ кожний являє собою Br. щених нижчих алкілових ефірів є ефіри, у яких Іншими кращими сполуками є сполуки, де X та Υ нижчий алкіл є заміщений піролідином, піперидикожний являє собою СІ. Іншими кращими сполуканом, морфоліном, N-метилпіперазином і т.д. Груми є сполуки, де X та Υ кожний являє собою -СН3. пою, яка відщеплюється in vivo, може бути, наприКрім того, бажано, коли X являє собою СІ та Υ явклад, етил, морфоліноетил та діетиламіноетил. У ляє собою -СН3. контексті даного винаходу -CONH2 також розгляКращими сполуками формули (І) як описано дається як складний ефір, оскільки група -NH2 мовище є сполуки, де R1 вибраний із групи, яка склаже відщеплюватися in vivo та заміщуватися гідродається з: ксигрупою, з утворенням відповідної карбонової -(СН2)nСООН; кислоти. -ОСН2СООН; Інша інформація, яка стосується прикладів та -NHC(=O)COOH і використання складних ефірів для доставки фар-NHCH2COOH; та мацевтичних сполук, доступна зі збірника Design of їх складних ефірів. Prodrugs. Ред. Bundgaard Η. (Elsevier, 1985). хДив. Краще, коли R1 являє собою -(СН2)nСООН. також Η. Ansel та ін., Pharmaceutical Dosage Forms Переважно, n має значення 1. Іншими кращими and Drug Delivery Systems (6-е видання, 1995), cc. сполуками є сполуки, де R1 являє собою 108-109; Krogsgaard-Larsen та ін., Textbook of Drug NHC(=O)COOH. Іншими кращими сполуками є Design and Development (2-е видання, 1996), cc. сполуки, де R1 являє собою: 152-191ї. Більш конкретно, даний винахід стосується сполук формули (І): Більш краще, коли R1 являє собою: де: А являє собою О, СН2, S, SO або SO2; X та Υ кожний незалежно вибраний із групи, яка складається з Br, Cд та -СН3; R1 вибраний із групи, яка складається з: -(СН2)nСООН; -ОСН2СООН; -NHC(=O)COOH; -NHCH2COOH; Ζ являє собою Η або -CºN; R2 являє собою нижчий алкіл; Переважно, Ζ являє собою CN. У сполуках формули (І), як описано вище, краще, коли R2 являє собою нижчий алкіл, який містить від 1 до 4 атомів С Більш краще, R2 являє собою нижчий алкіл, який містить від 1 до 3 атомів С. Іншою кращою сполукою формули (І) як описано вище, є сполуки, де R3 являє собою СН3. Особливо кращою сполукою формули (І) як описано вище є: 13 або її фармацевтично прийнятна сіль або складний ефір. Іншою особливо кращою сполукою формули (І) як описано вище є сполука: або її фармацевтично прийнятна сіль. Іншою особливо кращою сполукою формули (І) як визначено вище є сполука: або її фармацевтично прийнятна сіль або складний ефір. Іншою особливо кращою сполукою формули (І) як визначено вище є сполука: або її фармацевтично прийнятна сіль або складний ефір. Іншою особливо кращою сполукою формули (І) як визначено вище є сполука: або її фармацевтично прийнятна сіль або складний ефір. Іншою особливо кращою сполукою формули (І) як визначено вище є сполука: або її фармацевтично прийнятна сіль або складний ефір. Кращими є сполуки як визначене вище, які містять складноефірну групу, що відповідає R1, яка являє собою -NHC(=O)COOR, де складноефірна група, яка відповідає зазначеному "R", являє собою NH2. 88104 14 Зокрема, кращими сполуками формули (І) як описано вище є сполуки, вибрані із групи, яка складається з наступних сполук: [4-(5-ізопропіл-6-оксо-1,6-дигідропіридазин-3ілокси)-3,5-диметилфеніл]оцтова кислота, [3-хлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілокси)-5-метилфеніл]оцтова кислота, [3,5-дибром-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілокси)феніл]оцтова кислота, [3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілокси)феніл]оцтова кислота, 3-[3,5-дибром-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілокси)феніл]пропіонова кислота, [3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілокси)феніламіно] оцтова кислота, N-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілокси)феніл]оксаламінова кислота, 2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілокси)феніл]-3,5-діоксо2,3,4,5-тетрагідро-[1,2,4]триазин-6-карбонітрил, 2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілокси)феніл]-2Н[1,2,4]триазин-3,5-діон, [3,5-дихлор-4-(5-ізопропіл-1-метил-6-оксо-1,6дигідропіридазин-3-ілокси)феніл]оцтова кислота, [3,5-дихлор-4-(5-ізопропіл-1-метил-6-оксо-1,6дигідропіридазин-3-ілокси)феніл]оцтова кислота, 2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілметил)феніл]-3,5-діоксо2,3,4,5-тетрагідро-[1,2,4]триазин-6-карбонітрил, 2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілметил)феніл]-[1,2,4]триазин3,5-діон, [3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілметил)феніл]оцтова кислота, [3,5-дибром-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілметил)феніл]оцтова кислота, 2-[3,5-дихлор-4-(5-ізопропіл-1-метил-6-оксо1,6-дигідропіридазин-3-ілокси)феніл]-3,5-діоксо2,3,4,5-тетрагідро[1,2,4]триазин-6-карбонітрил, [3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-ілсульфаніл)феніл]оцтова кислота, [3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-сульфініл)феніл]оцтова кислота, [3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-сульфоніл)феніл]оцтова кислота, 2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-сульфоніл)феніл]-3,5-діоксо2,3,4,5-тетрагідро-[1,2,4]триазин-6-карбонітрил, 2-[3,5-дихлор-4-(5-ізопропіл-6-оксо-1,6дигідропіридазин-3-сульфоніл)феніл]-2Н[1,2,4]триазин-3,5-діон та 2-[3,5-дихлор-4-(5-ізопропіл-1-метил-6-оксо1,6-дигідропіридазин-3-ілметил)феніл]-3,5-діоксо2,3,4,5-тетрагідро-[1,2,4]триазин-6-карбонітрил, або їх фармацевтично прийнятні солі або складні ефіри. Зрозуміло, що із сполук загальної формули (І) у даному винаході можуть бути одержані похідні з 15 88104 16 функціональних груп з одержанням похідних, які більш краще від близько 0,70мг/кг до близько здатні перетворюватися назад у вихідну сполуку in 3,5мг/кг на добу. vivo. Винахід також включає застосування сполуки Було виявлено, що нові сполуки за даним вияк визначено вище для терапевтичного і/або пронаходом як описано вище є аналогами тиреоїднофілактичного лікування захворювань, які модулюго гормону. Сполуки за даним винаходом, отже, ються аналогами тиреоїдного гормону, зокрема можуть використовуватися для лікування і/або метаболічних захворювань, таких як ожиріння, профілактики захворювань, які модулюються анагіперліпідемія, гіперхолестеринемія та діабети, та логами тиреоїдного гормону, зокрема метаболічNASH (неалкогольний стеатогепатит), атеросклених захворювань, таких як ожиріння, гіперліпідероз, серцево-судинні захворювання, гіпотироїдизм, мія, гіперхолестеринемія та діабети, та можуть рак щитовидної залози та близькі порушення та бути корисними для лікування інших захворювань, захворювання. таких як NASH (неалкогольний стеатогепатит), Винахід також стосується застосування сполук атеросклероз, серцево-судинні захворювання, як описано вище для виготовлення лікарських загіпотироїдизм, рак щитовидної залози та близькі собів для терапевтичного і/або профілактичного порушення та захворювання. Пацієнтом з ожирінлікування захворювань, які модулюються аналоням є людина з індексом маси тіла 25 або більше. гами тиреоїдного гормону, зокрема метаболічних Винахід, отже, також стосується фармацевтизахворювань, таких як ожиріння, гіперліпідемія, чних композицій, які включають сполуки як визнагіперхолестеринемія та діабети, та NASH (неалкочені вище й фармацевтично прийнятний носій гольний стеатогепатит), атеросклероз, серцевоі/або ад'ювант. судинні захворювання, гіпотироїдизм, рак щитовиВинахід також включає сполуки як описано дної залози та близькі порушення та захворюванвище для застосування як терапевтично активні ня. Такі лікарські засоби включають сполуку як речовини, особливо як терапевтично активні речоописано вище. вини для лікування і/або профілактики захворюПрофілактика і/або лікування метаболічних вань, які модулюються аналогами тиреоїдного захворювань є кращим показанням до застосувангормону, зокрема метаболічних захворювань, таня. Діабети є більш переважними, зокрема інсуких як ожиріння, гіперліпідемія, гіперхолестеринеліннезалежний діабет (типу 2). Ожиріння також є мія та діабети, та NASH (неалкогольний стеатогебільш переважним. Гіперліпідемія також є більш патит), атеросклероз, серцево-судинні переважною, зокрема гіперхолестеринемія. захворювання, гіпотироїдизм, рак щитовидної заСполуки за даним винаходом можуть бути лози та близькі порушення та захворювання. одержані виходячи з комерційно доступних вихідВ іншому кращому варіанті здійснення, винахід них реагентів, та використовуючи загальні методистосується способу терапевтичного і/або профілаки синтезу та методики, відомі спеціалісту в даній ктичного лікування захворювань, які моделюються галузі техніки. Хроматографічне устаткування та аналогами тиреоїдного гормону, зокрема метабоінструменти можуть бути придбані в таких вироблічних захворювань, таких як ожиріння, гіперліпіників, як, наприклад Analogix, Inc, Burlington, WI; демія, гіперхолестеринемія та діабети, та NASH Analytical Sales and Services, Inc., Pompton Plains, (неалкогольний стеатогепатит), атеросклероз, сеNJ; Teledyne Isco, Lincoln, ΝΈ; VWR International, рцево-судинні захворювання, гіпотироїдизм, рак Bridgeport, NJ та Rainin Instrument Company, щитовидної залози та близькі порушення та заWoburn, MA. Хімічні речовини можуть бути прихворювання, який включає введення сполуки як дбані у виробників, таких як, наприклад Aldrich, визначено вище людині або тварині. Переважно, Argonaut Technologies, VWR та Lancaster. Далі кількість сполуки, яка вводиться, становить від наведені реакційні схеми, які придатні для одер0,01мг/кг до близько 50мг/кг на добу, більш краще жання таких сполук. Інші зразкові втілення можуть від близько 0,3мг/кг до близько 10мг/кг на добу, ще бути виявлені в конкретних прикладах, наведених нижче. 17 88104 18 19 88104 20 Сполуки 10а та 10b одержували серією реакцій, наведених на схемах 1-3. Вихідним реагентом для синтезу сполуки 10а був метиловий ефір 4гідрокси-2,6-диметилфенілоцтової кислоти, 6а, який одержували п'ятистадійним синтезом з комерційно доступного 2,6-диметилфенолу як показано на схемі 1, використовуючи методику, описану в статті Gardner, P. D. та ін., J. Amer. Chem. Soc, 1959, 81, с. 3364. 3,6-Дихлорпіридазин алкілували з одержанням сполуки 7 (схема 2) [див., наприклад, статтю Organic Preparations and Procedures International, 1988, 20(1-2), cc. 117-121]. Сполуку ба конденсували із сполукою 7, використовуючи основу та каталітичну кількість металоорганічного галогеніду при підвищених температурах з одержанням сполуки 8а [див., наприклад, Yuhpyng L. С. та ін., WO 9639388 (1996)]. Основний гідроліз метилового ефіру 8а здійснювали звичайними методиками з одержанням сполуки 9а. Перетворення хлорпіридазину 9а на піридизинон 10а здійснювали в кислих умовах [див., наприклад, статтю J. Chem. Soc. Perkin Trans. 1: Org. and Bioorg. Chem., 1988, 12, cc. 3103-3111]. Сполуку 10b одержували тим же способом, що й сполуки 10а, виходячи із сполуки 6b. Сполуку 6b одержували аналогічним способом, що й сполуку 6а (схема 1), виходячи із сполуки 1b. Сполуку 14 одержували серією реакцій, наведених на схемі 4. Вихідним реагентом для синтезу сполуки 14 був 2-(4-гідроксифеніл)етанол, який перетворювали на 11 у звичайних умовах бромування [див., наприклад, статтю J. Amer. Chem. Soc, 1989, 111(24), cc. 8912-8914]. Конденсацію сполуки 7 та сполуки 11 здійснювали із третбутоксидом калію в N,N-диметилацетаміді при підвищеній температурі з одержанням сполуки 12. Сполуку 12 окиснювали з одержанням сполуки 13, використовуючи аналогічну методику, як описано в статті Anelli, P.L. та ін., J. Org. Chem., 1987, 52(12), 21 88104 22 cc. 2559-2562. Хлорпіридазин 13 перетворювали на піридизинон 14 в умовах, як описано вище. Сполуку 19 одержували серією реакцій, наведених на схемі 5. Вихідним реагентом для синтезу сполуки 19 був метил 4гідроксифенілацетат, який перетворювали на сполуку 15 у звичайних умовах хлорування [див., наприклад, статтю Maeda, R. та ін., Chem. Pharm Bull, 1983, 31(10), cc. 3424-3445]. Сполуку 15 відновлювали в сполуку 16, використовуючи літійалюмогідрид у тетрагідрофурані при низькій температурі та невеликому часі реакції. Сполуку 16 перетворювали тристадійним способом на піридизинон 19 в умовах, які описані раніше. 23 88104 24 Сполуку 23 одержували серією реакцій, наведених на схемі 6. Бромування 2-(4гідроксифеніл)етанолу з одержанням сполуки 20 здійснювали в описаних вище умовах. Сполуку 20 конденсували із сполукою 7, використовуючи трет-бутоксид калію в N,N-диметилацетаміді при підвищеній температурі з одержанням сполуки 21. Сполуку 21 окиснювали в сполуку 22 окисненням за Джонсом [див., наприклад, статтю Bowden, K. та ін., J. Chem Soc, 1946, cc. 39-45]. Хлорпіридазиновий аналог 22 потім перетворювали на піридазинон 23 в описаних вище умовах. 3,5-дихлорфенільний аналог сполуки 23, 3,5диметилфенільний аналог сполуки 23, 3-хлор-5метилфенільний аналог сполуки 23, 3-бром-5метилфенільний аналог сполуки 23 та 3-бром-5хлорфенільний аналог сполуки 23 можуть бути одержані аналогічними способами. Сполуку 26 одержували серією реакцій, наведених на схемі 7. Вихідний реагент, 4-аміно2,6-дихлорфенол, конденсували із сполукою 7 з одержанням сполуки 24 описаною вище методикою. Хлорпіридазин 24 перетворювали на піридазинон описаною вище методикою. Гідроліз одержаного ацетаміду здійснювали в стандартних водних основних умовах з одержанням сполуки 25. Сполуку 25 потім перетворювали на сполуку 26 відновним амінуванням, використовуючи ціа ноборгідрид на смолі (МР-ціаноборгідрид, комерційно доступний від Argonaut Technologies) та гліоксилатну кислоту. 3,5-дибромфенільний аналог сполуки 26, 3,5-диметилфенільний аналог сполуки 26, 3-хлор-5-метилфенільний аналог сполуки 26, 3-бром-5-метилфенільний аналог сполуки 26 та 3-бром-5-хлорфенільний аналог сполуки 26 можуть бути одержані аналогічним способом. 25 88104 26 Сполуку 29 одержували серією реакцій, наведених на схемі 8. Сполуку 24 перетворювали на сполуку 27 ацилюванням аміну метилоксалілхлоридом [див., наприклад, статтю Sellstedt. J.H. та ін., J. Med. Chem., 1975, 18(9), cc. 926-933]. Сполуку 27 перетворювали на сполуку 28 гідролізом a-кетоефіру в a-кетокислоту, використовуючи стандартні умови [див., наприклад, статтю Minisci, F. та ін., J. Org. Chem., 1995, 60, cc. 5430 5433]. Хлорпіридазин 28 перетворювали на піридазинон 29 описаною вище методикою. 3,5дибромфенільний аналог сполуки 29, 3,5диметилфенільний аналог сполуки 29, 3-хлор-5метилфенільний аналог сполуки 29, 3-бром-5метилфенільний аналог сполуки 29 та 3-бром-5хлорфенільний аналог сполуки 29 можуть бути одержані аналогічними способами. Сполуку 31 одержували серією реакцій, наведених на схемі 9. Сполуки 25 перетворювали на ціаноацетилуретан 30, використовуючи методику, описану в статті Carroll, R.D. та ін., J. Med. Chem., 1983, 26, cc. 96-100. Циклізацію уретану сполуки 30 з одержанням ціаноазаурацилу 31 здійснювали, використовуючи методику, описану в статті Carroll, R.D. та ін., J. Med. Chem., 1983, 26, cc. 96-100. 3,5-дибромфенільний аналог сполуки 31, 3,5-диметилфенільний аналог сполуки 31, 3-хлор-5-метилфенільний аналог сполуки 31, 3-бром-5-метилфенільний аналог сполуки 31 та 3-бром-5-хлорфенільний аналог сполуки 31 можуть бути одержані аналогічними способами. 27 88104 28 Сполуку 33 одержували серією реакцій, наведених на схемі 10. Сполуку 31 перетворювали на сполуку 32 гідролізом ціаногрупи у карбонову кислоту методикою, описаною в статті Carroll, R.D. та ін., J. Med. Chem., 1983, 26, cc. 96-100. Сполуку 32 потім перетворювали на сполуку 33 декарбоксилюванням, використовуючи методику, описану в статті Carroll, R.D. та ін., J. Med. Chem., 1983, 26, cc. 96-100. 3,5-Дибромфенільний аналог сполуки 33, 3,5-диметилфенільний аналог сполуки 33, 3-хлор-5-метилфенільний аналог сполуки 33, 3-бром-5-метилфенільний аналог сполуки 33 та 3-бром-5-хлорфенільний аналог сполуки 33 можуть бути одержані аналогічними способами. Сполуку 37 одержували серією реакцій, наведених на схемі 11. Хлорпіридазин 17 перетворювали на піридазинон 34 методикою, описаною раніше. Піридазинон 34 алкілували, використовуючи основу та метилйодид, з одержанням сполуки 35, використовуючи методику, аналогічну описаній в статті J. Med. Chem., 1989, 32(10), cc. 2381-2388. Ацетат 35 піддавали гідролізу з одержанням спирту 36 у стандартних основних умовах [див., наприклад, Hauser, С. R. та ін., J. Amer. Chem. Soc, 1945, 67, cc. 409-412]. Сполуку 36 потім окиснювали в сполуку 37 окисненням за 29 88104 30 Джонсом. 3,5-Дибромфенільний аналог сполуки бром-5-метилфенільний аналог сполуки 37 та 337, 3,5-диметилфенільний аналог сполуки 37, 3бром-5-хлорфенільний аналог сполуки 37 можуть хлор-5-метилфенільний аналог сполуки 37, 3бути одержані аналогічними способами. Сполуку 42 одержували серією реакцій, наведених на схемі 12. Сполуку 11 перетворювали на сполуку 42 п'ятистадійним синтезом, використовуючи описані вище умови. 3,5Дихлорфенільний аналог сполуки 42, 3,5 диметилфенільний аналог сполуки 42, 3-хлор-5метилфенільний аналог сполуки 42, 3-бром-5метилфенільний аналог сполуки 42 та 3-бром-5хлорфенільний аналог сполуки 42 можуть бути одержані аналогічними способами. 31 Сполуку 48 одержували серією реакцій, наведених на схемі 13. Вихідний реагент, 1,2,3трихлор-5-нітробензол, перетворювали на сполуку 43 селективним заміщенням хлором у положенні 2 аніоном, який утвориться із третбутилціаноацетату [див., наприклад, Salturo, F. та ін., WO 00/17204]. Нітрогрупу сполуки 43 відновлювали до аміну, використовуючи стандартні умови. Трет-бутиловий ефір сполуки 43 піддавали гідролізу та декарбоксилювали з одержанням сполуки 44 [див., наприклад, Salturo, F. та ін., WO 00/17204]. Аніон сполуки 44 конденсували із сполукою 7 з одержанням сполуки 45, використовуючи методику, аналогічну описаній в Salturo, F. та ін., WO 00/17204. Хлорпіридазин 45 перетворю 88104 32 вали на піридазинон 46 у кислих умовах при підвищеній температурі. У цих умовах ціаногрупу піддавали гідролізу з одержанням карбонової кислоти і потім декарбоксилювали, використовуючи методику, описану в статті Carroll, R. D. та ін., J. Med. Chem., 1983, 26, cc. 96-100. Сполуку 46 перетворювали на сполуку 48 двостадійним способом, описаним раніше. 3,5Дибромфенільний аналог сполуки 48, 3,5диметилфенільний аналог сполуки 48, 3-хлор-5метилфенільний аналог сполуки 48, 3-бром-5метилфенільний аналог сполуки 48 та 3-бром-5хлорфенільний аналог сполуки 48 можуть бути одержані аналогічними способами. 33 Сполуку 50 одержували серією реакцій, наведених на схемі 14. Сполуку 50 одержували із сполуки 48 двостадійним способом, описаним раніше. 3,5-Дибромфенільний аналог сполуки 50, 3,5-диметилфенільний аналог сполуки 50, 3 88104 34 хлор-5-метилфенільний аналог сполуки 50, 3бром-5-метилфенільний аналог сполуки 50 та 3бром-5-хлорфенільний аналог сполуки 50 можуть бути одержані аналогічними способами. 35 88104 36 Сполуку 56 одержували серією реакцій, наведених на схемі 15. Аміногрупу сполуки 46 перетворювали на бромід сполуки 51, використовуючи стандартні умови [див., наприклад, статтю Doyle, М.Р. та ін., J. Org. Chem., 1977, 42(14), cc. 2426-2431]. Бромід 51 перетворювали на метиловий ефір 52 карбонілюванням, що каталізується паладієм у метанолі [див., наприклад, Takatori, К. та ін., Tetrahedron, 1998, 54, сс. 15861-15869]. Сполуку 52 відновлювали в сполуку 53 стандартними умовами відновлення, обробкою гідридом діізобутилалюмінію в тетрагідрофурані [див., наприклад, статтю Yoon, N.M. та ін., J. Org. Chem., 1985, 50, cc. 2443-2450]. Спирт 53 перетворювали на бромід 54, використовуючи стандартні умо ви [див., наприклад, статтю Lan, Aj. J. Υ. та ін., J. Amer. Chem. Soc, 1987, 109, cc. 2738-2745]. Бромід 54 заміщали ціанідом натрію з одержанням нітрилу 55, використовуючи методику, описану в статті Law, Η. та ін. J. Med. Chem., 1998, 41, cc. 2243-2251. Нітрил 55 піддавали гідролізу з одержанням кислоти 56 звичайною методикою гідролізу нітрилу в карбонову кислоту у водних кислих умовах [див., наприклад, Wenner, О., Org. Synth.; Coll. Т. IV, 1963, с. 760]. 3,5-Диметилфенільний аналог сполуки 56, 3-хлор-5-метилфенільний аналог сполуки 56, 3-бром-5-метилфенільний аналог сполуки 56 та 3-бром-5-хлорфенільний аналог сполуки 56 можуть бути одержані аналогічними способами. Сполуку 64 одержували серією реакцій, наведених на схемі 16. Вихідний реагент, метил 3,5-дибром-4-метилбензоат, бромували з одер жанням сполуки 57 у стандартних умовах бромування [див., наприклад, статтю Buu-Hoy, P. та ін., J. Org. Chem., 1953, 18, cc. 649-652]. Сполуку 57 37 88104 38 перетворювали на сполуку 59 двостадійним спопри підвищеній температурі. Ці реакційні умови собом, описаним вище. Спирт 59 перетворювали приводять до перетворення хлорпіридазину в на простий ефір 60 звичайною методикою перепіридинон, гідроліз нітрильної групи з одержантворення спирту на тетрагідропіранільний ефір ням карбонової кислоти, потім декарбоксилюван[див., наприклад, статтю Miyashita, Μ. та ін., J. ня кислоти та перетворення захищеного тетрагіOrg. Chem., 1977, 42, cc. 3882-3774]. Конденсацію дропіранілом спирту в бензилхлорид сполуки 62. сполуки 7 та сполуки 60 здійснювали гідридом Хлорид сполуки 62 заміщали ціанідом натрію з натрію в Ν,Ν-диметилформаміді при підвищеній одержанням нітрилу 63, використовуючи методитемпературі з одержанням сполуки 61, викориску, аналогічну описаній в статті Law, Η. та ін., J. товуючи методику, аналогічну описаній в міжнаMed. Chem., 1998, 41, cc. 2243-2251. Сполуку 64 родній заявці на патент Salturo, F. та ін., WO одержували із сполуки 63, використовуючи мето00/17204. Сполуку 61 обробляли в кислих умовах дику, описану раніше. Сполуку 69 одержували серією реакцій, наведених на схемі 17. Вихідний реагент, 4-аміно2,6-дихлорфенол, конденсували із сполукою 7, використовуючи трет-бутоксид калію в N,Nдиметилацетаміді при підвищеній температурі. Одержану проміжну сполуку потім обробляли ангідридом фталевої кислоти при підвищеній температурі з одержанням фталіміду. Одержаний фталімід нагрівали в льодяній оцтовій кислоті з ацетатом натрію з одержанням сполуки 65. Атом азоту піридизинону сполуки 65 метилювали в умовах, аналогічних описаним у статті Sotelo, E. та ін., Synth. Commun., 2002, 32(11), cc. 1675 1680 з одержанням сполуки 66. Фталімідну захисну групу сполуки 66 видаляли, використовуючи бутиламін у метанолі при підвищеній температурі з одержанням сполуки 67. Сполуку 67 потім перетворювали на сполуку 68, використовуючи описані вище способи. Сполуку 68 перетворювали на сполуку 69, використовуючи ацетат калію в Ν,Νдиметилацетаміді при підвищеній температурі. 3,5-Дибромфенільний аналог сполуки 69, 3,5диметилфенільний аналог сполуки 69, 3-хлор-5метилфенільний аналог сполуки 69, 3-бром-5метилфенільний аналог сполуки 69 та 3-бром-5 39 88104 40 хлорфенільний аналог сполуки 69 можуть бути одержані аналогічними способами. Сполуку 76 одержували серією реакцій, наведених на схемі 18. Спирт 16 захищали третбутилдифенілсилільним ефіром з одержанням сполуки 70, використовуючи стандартну методику, описану в статті Chaudhary, S.K. та ін., Tet. Lett., 1979, 20(2), cc. 99-102. Фенол 70 перетворювали на тіофенол 73, використовуючи тристадійну методику, як описано в статті D.M. Springer та ін., Bioorg Med. Chem., 2003, 11, cc. 265-279. Конденсацію сполуки 7 та сполуки 73 здійснюва ли з карбонатом калію в диметилсульфоксиді при підвищеній температурі з одержанням сполуки 74. Сполуку 74 перетворювали на піридизинонову кислоту 76 у дві стадії, описані раніше. 3,5Дибромфенільний аналог сполуки 76, 3,5диметилфенільний аналог сполуки 76, 3-хлор-5метилфенільний аналог сполуки 76, 3-бром-5метилфенільний аналог сполуки 76 та 3-бром-5хлорфенільний аналог сполуки 76 можуть бути одержані аналогічними способами. 41 Сполуки 77 та 78 одержували серією реакцій, наведених на схемі 19. Тіоефір 76 окиснювали, використовуючи мурашину кислоту й пероксид водню, з одержанням розділюваної суміші сульфоксиду 77 та сульфонілу 78 [див., наприклад, Cragoe, Ε. J. та ін., US4582842, 15.04.1986]. 3,5Дибромфенільний аналог сполуки 77 та 78, 3,5 88104 42 диметилфенільний аналог сполуки 77 та 78, 3хлор-5-метилфенільний аналог сполуки 77 та 78, 3-бром-5-метилфенільний аналог сполуки 77 та 78 та 3-бром-5-хлорфенільний аналог сполуки 77 та 78 можуть бути одержані аналогічними способами. 43 88104 44 Сполуку 88 одержували серією реакцій, наведених на схемі 20. Вихідний реагент, 2,6,дихлор-4-нітрофенол, перетворювали на сполуку 79 в умовах, описаних раніше. Сполуку 79 перетворювали на сполуку 80 в умовах, описаних раніше. Нітрогрупу сполуки 80 відновлювали з одержанням аміну 81, використовуючи стандартні умови реакції, порошок заліза в кислому середовищі [див., наприклад, статтю Org. Syn. Coll., 1943, Т. 2, с. 471]. Сполуку 81 потім перетворювали на сполуку 88 в умовах, описаних раніше. 3,5-Дибромфенільний аналог сполуки 88, 3,5диметилфенільний аналог сполуки 88, 3-хлор-5метилфенільний аналог сполуки 88, 3-бром-5метилфенільний аналог сполуки 88 та 3-бром-5хлорфенільний аналог сполуки 88 можуть бути одержані аналогічними способами. Сполуку 91 одержували серією реакцій, наведених на схемі 21. Сполуку 87 перетворювали на сполуку 91 в умовах, описаних раніше. 3,5Дибромфенільний аналог сполуки 91, 3,5диметилфенільний аналог сполуки 91, 3-хлор-5 метилфенільний аналог сполуки 91, 3-бром-5метилфенільний аналог сполуки 91 та 3-бром-5хлорфенільний аналог сполуки 91 можуть бути одержані аналогічними способами. 45 Сполуку 96 одержували серією реакцій, наведених на схемі 22. Амін 46 обробляли ангідридом фталевої кислоти в кислих умовах при підвищеній температурі з одержанням фталіміду 92 [див., наприклад, статтю Vera, L.M.S. та ін., Farmaco, 2003, 58(12), сс. 1283-1288]. Атом азоту піридизинону сполуки 92 метилювали в умовах, наведених у статті Sotelo, Ε. та ін., Synth. Commun., 2002, 32(11), сс. 1675-1680. Захисну групу фталіміду сполуки 93 видаляли в кислих 88104 46 умовах при підвищеній температурі з одержанням сполуки 94. Сполуку 94 перетворювали на сполуку 96 в умовах, описаних раніше. 3,5Дибромфенільний аналог сполуки 96, 3,5диметилфенільний аналог сполуки 96, 3-хлор-5метилфенільний аналог сполуки 96, 3-бром-5метилфенільний аналог сполуки 96 та 3-бром-5хлорфенільний аналог сполуки 96 можуть бути одержані аналогічними способами. Запропоновані способи синтезу 47 Спирт 17 може бути перетворений на бромід 97, використовуючи стандартні умови [див., наприклад, статтю Lan, Aj. J. Υ. та ін., J. Amer. Chem. Soc, 1987, 109, cc. 2738-2745]. Бромід сполуки 97 може бути заміщений ціанідом натрію з одержанням нітрилу 98, використовуючи методику, аналогічну описаній в статті Law, Η. та ін. J. Med. Chem., 1998, 41, cc. 2243-2251. Нітрили, такі як 98, можуть бути перетворені в тетразоли, такі як 98, використовуючи відомі методики, наприклад, обробкою сполуки 98 хлоридом амонію та азидом натрію при підвищеній температурі [див., 88104 48 наприклад, статтю Synthesis, 1998, 6, сс. 910914]. Конверсія хлорпіридазину 99 у піридизинон 100 може здійснюватися в кислих умовах [див., наприклад, статтю J. Chem. Soc. Perkin Trans. 1: Org. and Bioorg. Chem., 1988, 12, cc. 3103-3111]. 3,5-Дибромфенільний аналог сполуки 100, 3,5диметилфенільний аналог сполуки 100, 3-хлор-5метилфенільний аналог сполуки 100, 3-бром-5метилфенільний аналог сполуки 100 та 3-бром-5хлорфенільний аналог сполуки 100 можуть бути одержані аналогічними способами. 49 88104 50 Складний ефір метил 3,5-дихлор-4гідроксибензоату може бути відновлений з одержанням спирту 101, використовуючи відновний агент, такий як літійалюмогідрид, при низькій температурі [див., наприклад, статтю J. Org. Chem., 1998, 63, cc. 5658-5661]. Сполука 101 потім може бути конденсована із сполукою 7, використовуючи основу, при підвищеній температурі з одержанням сполуки 102 [див., наприклад, міжнародну заявку на патент Yuhpyng L. С. та ін., (1996) WO 9639388]. Спирт 102 може бути перетворений на сполуку 106, використовуючи описані раніше умови. 3,5-Дибромфенільний аналог сполуки 106, 3,5-диметилфенільний аналог сполуки 106, 3-хлор-5-метилфенільний аналог сполуки 106, 3-бром-5-метилфенільний аналог сполуки 106 та 3-бром-5-хлорфенільний аналог сполуки 106 можуть бути одержані аналогічними способами. Із броміду 54 може бути одержаний гомолог складного ефіру 107, використовуючи умови, описані в статті Can. J. Chem., 2001, 79(5-6), сс. 752-759. Складні ефіри, такі як 107, можуть бути перетворені на спирти, такі як 108, використовуючи відомі методики, наприклад, обробкою сполуки 107 гідридом діізобутиламонію в тетрагідрофурані [див., наприклад, статтю Yoon, N.M. та ін., J. Org. Chem., 1985, 50, сс. 2443-2450]). Пере творення спирту 108 натетразол 111 може здійснюватися в описаних раніше умовах. 3,5Дибромфенільний аналог сполуки 111, 3,5диметилфенільний аналог сполуки 111, 3-хлор-5метилфенільний аналог сполуки 111, 3-бром-5метилфенільний аналог сполуки 111 та 3-бром-5хлорфенільний аналог сполуки 111 можуть бути одержані аналогічними способами. 51 88104 52 Перетворення нітрилу 55 натетразол 112 можна здійснити, використовуючи описані раніше умови. 3,5-Дибромфенільний аналог сполуки 112, 3,5-диметилфенільний аналог сполуки 112, 3 хлор-5-метилфенільний аналог сполуки 112, 3бром-5-метилфенільний аналог сполуки 112 та 3бром-5-хлорфенільний аналог сполуки 112 можуть бути одержані аналогічними способами. Перетворення сполуки 74 на сполуку 116 можна здійснити, використовуючи описані раніше умови. 3,5-Дибромфенільний аналог сполуки 116, 3,5-диметилфенільний аналог сполуки 116, 3 хлор-5-метилфенільний аналог сполуки 116, 3бром-5-метилфенільний аналог сполуки 116 та 3бром-5-хлорфенільний аналог сполуки 116 можуть бути одержані аналогічними способами. 53 Перетворення сполуки 116 на сполуку 117 та 118 можна здійснити, використовуючи описані раніше умови. 3,5-Дибромфенільний аналог сполуки 117 та 118, 3,5-диметилфенільний аналог сполуки 117 та 118, 3-хлор-5-метилфенільний 88104 54 аналог сполуки 117 та 118, 3-бром-5метилфенільний аналог сполуки 117 та 118 та 3бром-5-хлорфенільний аналог сполуки 117 та 118 можуть бути одержані аналогічними способами. 55 88104 56 Перетворення сполуки 101 на сполуку 127 можна здійснити, використовуючи описані раніше умови. 3,5-Дибромфенільний аналог сполуки 127, 3,5-диметилфенільний аналог сполуки 127, 3 хлор-5-метилфенільний аналог сполуки 127, 3бром-5-метилфенільний аналог сполуки 127 та 3бром-5-хлорфенільний аналог сполуки 127 можуть бути одержані аналогічними способами. Перетворення сполуки 127 на сполуку 128 та 129 можна здійснити, використовуючи описані раніше умови. 3,5-Дибромфенільний аналог сполуки 128 та 129, 3,5-диметилфенільний аналог сполуки 128 та 129, 3-хлор-5-метилфенільний аналог сполуки 128 та 129, 3-бром-5метилфенільний аналог сполуки 128 та 129 та 3бром-5-хлорфенільний аналог сполуки 128 та 129 можуть бути одержані аналогічними способами. Вихідний реагент, 2,6-дихлорбензол-1,4-діол, може бути оброблений метиловим ефіром бромоцтової кислоти та основою при підвищеній температурі з одержанням сполуки 130, використовуючи методику, аналогічну описаній в статті J. Het. Chem., 1994, 31(6), cc. 1439-43. Перетворення сполуки 130 на сполуку 131 можна здійснити, використовуючи описані раніше умови. Гідроліз складного ефіру 131 у сполуку 132 можна здійс нити, використовуючи стандартні водні лужні умови. Перетворення сполуки 132 на сполуку 133 можна здійснити, використовуючи описані раніше умови. 3,5-Дибромфенільний аналог сполуки 133, 3,5-диметилфенільний аналог сполуки 133, 3хлор-5-метилфенільний аналог сполуки 133, 3бром-5-метилфенільний аналог сполуки 133 та 3бром-5-хлорфенільний аналог сполуки 133 можуть бути одержані аналогічними способами. 57 88104 58 Сполука 46 може бути перетворена в сполуку 134 в аналогічних умовах, як описано в статті Gattermann, L., Die Praxis des organischen Chemikers, 1914 (12), с 228. Перетворення сполуки 134 на сполуки 136 можна здійснити, використовуючи описані раніше умови. 3,5 Дибромфенільний аналог сполуки 136, 3,5диметилфенільний аналог сполуки 136, 3-хлор-5метилфенільний аналог сполуки 136, 3-бром-5метилфенільний аналог сполуки 136 та 3-бром-5хлорфенільний аналог сполуки 136 можуть бути одержані аналогічними способами. Перетворення сполуки 130 на сполуку 141 можна здійснити, використовуючи описані раніше умови. 3,5-Дибромфенільний аналог сполуки 141, 3,5-диметилфенільний аналог сполуки 141, 3 59 88104 60 хлор-5-метилфенільний аналог сполуки 141, 3бром-5-хлорфенільний аналог сполуки 141 мобром-5-метилфенільний аналог сполуки 141 та 3жуть бути одержані аналогічними способами. Перетворення сполуки 141 на сполуку 142 та 143 можна здійснити, використовуючи описані раніше умови. 3,5-Дибромфенільний аналог сполуки 142 та 143, 3,5-диметилфенільний аналог сполуки 142 та 143, 3-хлор-5-метилфенільний аналог сполуки 142 та 143, 3-бром-5метилфенільний аналог сполуки 142 та 143 та 3бром-5-хлорфенільний аналог сполуки 142 та 143 можуть бути одержані аналогічними способами. Перетворення сполуки 94 на сполуку 149 можна здійснити, використовуючи описані раніше умови. 3,5-Дибромфенільний аналог сполуки 149, 3,5-диметилфенільний аналог сполуки 149, 3 хлор-5-метилфенільний аналог сполуки 149, 3бром-5-метилфенільний аналог сполуки 149 та 3бром-5-хлорфенільний аналог сполуки 149 можуть бути одержані аналогічними способами.
ДивитисяДодаткова інформація
Назва патенту англійськоюPyridazinone derivatives as thyroid hormone receptor agonists
Автори англійськоюHaynes Nancy-Ellen, Kertesz Denis John, Pietranico-Cole Sherrie Lynn, Qian Yimin, Scott Nathan Robert, So Sung-Sau, Thakkar Kshitij Chhabilbhai, Tilley Jefferson Wright
Назва патенту російськоюПроизводные пиридазинона как агонисты рецептора тиреоидного гормона
Автори російськоюХейнз Ненси-Эллен, Кертеш Денис Джон, Пьетранико-Коле Шерри Линн, Цянь Иминь, Скотт Натан Роберт, Со Сун-Сау, Тхаккар Кшитий Чхабильбхай, Тилли Джефферсон Райт
МПК / Мітки
МПК: C07D 403/10, C07D 237/18, C07D 237/16, A61P 5/16, A61K 31/501, C07D 237/14, C07D 403/12
Мітки: похідні, піридазинону, тиреоїдного, рецептора, агоністи, гормону
Код посилання
<a href="https://ua.patents.su/74-88104-pokhidni-piridazinonu-yak-agonisti-receptora-tireodnogo-gormonu.html" target="_blank" rel="follow" title="База патентів України">Похідні піридазинону як агоністи рецептора тиреоїдного гормону</a>












