Стероїди, заміщені в положенні 11, спосіб їх одержання (варіанти) та фармацевтична композиція
Номер патенту: 54483
Опубліковано: 17.03.2003
Автори: ТЕТШ Жан-Жорж, Ван Де Вельд Патрік, НІК Франсуа, БУАЛІ Іаміна
Формула / Реферат
1. Сполуки загальної формули (І):
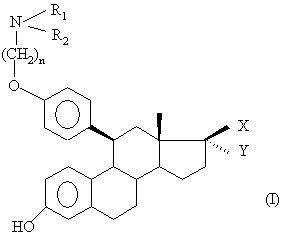 ,
,
де:
n - ціле число, що дорівнює 2 або З,
або R1 і R2, ідентичні чи різні, означають атом водню або радикал алкіл, що містить від 1 до 4 атомів вуглецю,
або R1 і R2 утворюють разом з атомом азоту, з яким вони зв’язані, моно або поліциклічний гетероцикл, що має від 5 до 15 ланок, ароматичний або не ароматичний, який містить, при необхідності, від 1 до 3 додаткових гетероатомів, що вибираються з кисню, сірки і азоту, заміщений або незаміщений,
Х означає гідроксильний радикал, при необхідності, етерифікований, а
Y означає заміщений або незаміщений алкільний радикал, що містить від 1 до 4 атомів вуглецю, а також їх адитивні солі з фармацевтично прийнятними кислотами.
2. Сполуки загальної формули (І) за пунктом 1, де n дорівнює 2, а також їх адитивні солі з фармацевтично прийнятними кислотами.
3. Сполуки загальної формули (І), визначеної у пунктах 1 або 2, де n дорівнює 2, або R1 і R2, ідентичні чи різні, означають радикал алкіл, який містить від 1 до 4 атомів вуглецю, або R1 і R2 утворюють разом з атомом азоту, з яким вони зв'язані, групу піперидино, піролідино або 2-азабіцикло(2.2.1)гепт-2-ил, Х означає гідроксильний радикал, а Y означає радикал метил чи етил, а також їх адитивні солі з фармацевтично прийнятними кислотами.
4. Сполуки формули (І) за одним з пунктів 1-3, а також їх адитивні солі з фармацевтично прийнятними кислотами, що мають такі назви:
11![]() -[4-[2-(1-піперидиніл)етокси]феніл]-19-нор-17
-[4-[2-(1-піперидиніл)етокси]феніл]-19-нор-17![]() -прегна-1,3,5(10)-триєн-3,17
-прегна-1,3,5(10)-триєн-3,17![]() -діол,
-діол,
17![]() -метил-11
-метил-11![]() -[4-[2-(1-піперидиніл)етокси]феніл]-естра-1,3,5(10)-триєн-3,17
-[4-[2-(1-піперидиніл)етокси]феніл]-естра-1,3,5(10)-триєн-3,17![]() -діол,
-діол,
17![]() -метил-11
-метил-11![]() -[4-[2-(діетиламіно)етокси]феніл]-естра-1,3,5(10)-3,17
-[4-[2-(діетиламіно)етокси]феніл]-естра-1,3,5(10)-3,17![]() -діол,
-діол,
17![]() -метил-11
-метил-11![]() -[4-[2-(1-піролідиніл)етокси]феніл]-естра-1,3,5(10)-триєн-3,17
-[4-[2-(1-піролідиніл)етокси]феніл]-естра-1,3,5(10)-триєн-3,17![]() -діол,
-діол,
17![]() -метил-11
-метил-11![]() -[4-[2-(2-азабіцикло(2.2.1)гепт-2-ил)етокси]феніл]-естра-1,3,5(10)-триєн-3,17
-[4-[2-(2-азабіцикло(2.2.1)гепт-2-ил)етокси]феніл]-естра-1,3,5(10)-триєн-3,17![]() -діол,
-діол,
11![]() -[4-[2-(2-азабіцикло(2.2.1)гепт-2-ил)етокси]феніл]-19-нор-17
-[4-[2-(2-азабіцикло(2.2.1)гепт-2-ил)етокси]феніл]-19-нор-17![]() -прегна-1,3,5(10)-триєн-3,17
-прегна-1,3,5(10)-триєн-3,17![]() -діол,
-діол,
17![]() -(трифторметил)-11
-(трифторметил)-11![]() -[4-[2-(1-піперидиніл)етокси]феніл]-естра-1,3,5(10)-триєн-3,17
-[4-[2-(1-піперидиніл)етокси]феніл]-естра-1,3,5(10)-триєн-3,17![]() -діол.
-діол.
5. Спосіб одержання сполук загальної формули (І), визначеної у пункті 1, який відрізняється тим, що сполуку загальної формули (II) :
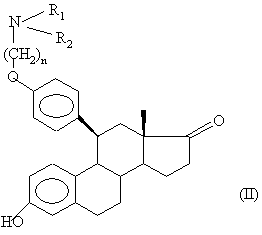 ,
,
де n, R1 та R2 мають значення, подані в пункті 1, піддають дії металоорганічної сполуки, похідної радикалу алкілу, що містить від 1 до 4 атомів вуглецю, з одержанням сполуки формули (І), в якій Х - гідроксильна група, a Y - алкільна група, що містить від 1 до 4 атомів вуглецю, одержану сполуку, у разі необхідності, піддають реакції етерифікації групи 17-ОН або реакції солеутворення.
6. Спосіб одержання сполук загальної формули (І), визначеної у пункті 1, де Y являє собою алкіл, що містить від 2 до 4 атомів вуглецю, який відрізняється тим, що сполуку загальної формули (III):
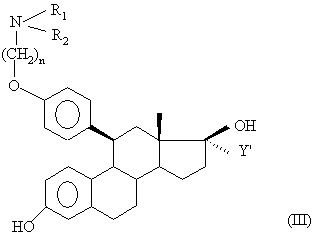 ,
,
в якій n, R1 та R2 мають названі вище значення і де Y’ позначає алкенільну або алкінільну групу, що містить від 2 до 4 атомів вуглецю, піддають дії агента відновлення подвійного або потрійного зв'язку з одержанням сполуки формули (І), у якій Х - гідроксильна група, а Y - алкільна група, яка містить від 2 до 4 атомів вуглецю, яку, у разі необхідності, піддають реакції етерифікації 17-ОН групи і/або реакції солеутворення.
7. Сполуки загальної формули (І) за пунктом 1 як лікарські засоби.
8. Сполуки загальної формули (І) за пунктами 2, 3 або 4 як лікарські засоби.
9. Сполуки формули (І) за п. 1 як лікарські засоби, призначені для гормонального замісного лікування менопаузи або перименопаузи, зокрема для профілактики або лікування остеопорозу, і які не мають або майже не мають естрогенної активності відносно матки.
10. Сполуки загальної формули (І) за п. 1 як лікарські засоби, призначені для гормонального замісного лікування менопаузи або перименопаузи, зокрема для профілактики або лікування остеопорозу у жінок з ризиком виникнення пухлини грудей.
11. Фармацевтичні композиції, що містять лікарські засоби за будь-яким з пунктів 7-10 в ефективній кількості та фармацевтично прийнятний носій.
Текст
1 Сполуки загальної формули (І) (I) Де п - ціле число, що дорівнює 2 або З, або Ri і F?2, ідентичні чи різні, означають атом водню або радикал алкіл, що містить від 1 до 4 атомів вуглецю, або Ri і R2 утворюють разом з атомом азоту, з яким вони зв'язані, моно або ПОЛІЦИКЛІЧНИЙ гетероцикл, що має від 5 до 15 ланок, ароматичний або не ароматичний, який містить, при необхідності, від 1 до 3 додаткових гетероатомів, що вибираються з кисню, сірки і азоту, заміщений або незаміщений, X означає гідроксильний радикал, при необхідності, етерифікований, а Y означає заміщений або незаміщений алкільний радикал, що містить від 1 до 4 атомів вуглецю, а також їх адитивні солі з фармацевтично прийнятними кислотами 2 Сполуки загальної формули (І) за пунктом 1, де п дорівнює 2, а також їх адитивні солі з фармацевтично прийнятними кислотами 3 Сполуки загальної формули (І), визначеної у пунктах 1 або 2, де п дорівнює 2, або Ri і R2, ідентичні чи різні, означають радикал алкіл, який містить від 1 до 4 атомів вуглецю, або Ri і R2 утворюють разом з атомом азоту, з яким вони зв'язані, групу піперидино, пірол ід ино або 2азабіцикло(2 2 1)гепт-2-ил, X означає гідроксильний радикал, a Y означає радикал метил чи етил, а також їх адитивні солі з фармацевтично прийнятними кислотами 4 Сполуки формули (І) за одним з пунктів 1-3, а також їх адитивні солі з фармацевтично прийнятними кислотами, що мають такі назви 11 Р -[4-[2-(1 -піперидиніл)етокси]феніл]-19-нор17 а -прегна-1,3,5(10)-триєн-3,17р-дюл, 17а -метил-11 р -[4-[2-(1 -піперидиніл)етокси]феніл] -естра-1,3,5(10)-триєн-3,17 р -дюл, 17 а -метил-11 р-[4-[2-(діетиламшо)етокси]феніл]естра-1,3,5(10)-3,17 р -дюл, 17 а -метил-11 р-[4-[2-(1-піролідиніл)етокси]феніл]естра-1,3,5(10)-триєн-3,17 р -дюл, 17 а -метил-11 р -[4-[2-(2-азабіцикло(2 2 1)гепт-2ил)етокси]феніл]-естра-1,3,5(10)-триєн-3,17 р -дюл, 11 р-[4-[2-(2-азабіцикло(2 2 1)гепт-2-ил)етокси] феніл]-19-нор-17 а -прегна-1,3,5(10)-триєн-3,17 р дюл, 17 а -(трифторметил)-і 1 р-[4-[2-(1-піперидиніл) етокси]феніл]-естра-1,3,5(10)-триєн-3,17 р -дюл 5 Спосіб одержання сполук загальної формули (І), визначеної у пункті 1, який відрізняється тим, що сполуку загальної формули (II) О со 00 ю 54483 (II) де n, Ri та F 2 мають значення, подані в пункті 1, ? піддають дії металоорганічної сполуки, похідної радикалу алкілу, що містить від 1 до 4 атомів вуглецю, з одержанням сполуки формули (І), в якій X - гідроксильна група, a Y - алкільна група, що містить від 1 до 4 атомів вуглецю, одержану сполуку, у разі необхідності, піддають реакції етерифікації групи 17-ОН або реакції солеутворення 6 Спосіб одержання сполук загальної формули (І), визначеної у пункті 1, де Y являє собою алкіл, що містить від 2 до 4 атомів вуглецю, який відрізняється тим, що сполуку загальної формули (III) де У позначає алкенільну або алкінільну групу, що містить від 2 до 4 атомів вуглецю, піддають дії агента відновлення подвійного або потрійного зв'язку з одержанням сполуки формули (І), у якій X - гідроксильна група, a Y - алкільна група, яка містить від 2 до 4 атомів вуглецю, яку, у разі необхідності, піддають реакції етерифікації 17-ОН групи і/або реакції солеутворення 7 Сполуки загальної формули (І) за пунктом 1 як лікарські засоби 8 Сполуки загальної формули (І) за пунктами 2, З або 4 як лікарські засоби 9 Сполуки формули (І) за п 1 як лікарські засоби, призначені для гормонального замісного лікування менопаузи або перименопаузи, зокрема для профілактики або лікування остеопорозу, і які не мають або майже не мають естрогенної активності відносно матки 10 Сполуки загальної формули (І) за п 1 як лікарські засоби, призначені для гормонального замісного лікування менопаузи або перименопаузи, зокрема для профілактики або лікування остеопорозу у жінок з ризиком виникнення пухлини грудей 11 Фармацевтичні композиції, що містять лікарські засоби за будь-яким з пунктів 7-10 в ефективній КІЛЬКОСТІ та фармацевтично прийнятний носій в якій n, Ri та F 2 мають названі вище значення і ? Даний винахід стосується стероїдних сполук, заміщених в положенні 11, способу їх одержання, їх застосування в якості лікарського засобу та фармацевтичних композицій, що їх містять Остеопороз є патологією, яка характеризується КІЛЬКІСНИМ і якісним ослабленням кісткової тканини, достатнім, щоб потягти за собою хребетні або периферійні переломи, які виникають спонтанно або внаслідок незначних травм Хоча це захворювання має багато факторів його виникнення, у жінок основним фактором виникнення кісткової недостатності або остеопенм є менопауза Остеопенія виявляється в розрідженні та ЗМІНІ побудови спонпозної кістки, наслідком чого є збільшення крихкості скелету і ризик переломів Кісткова недостатність сильно збільшується після менопаузи внаслідок припинення роботи яєчників і сягає 3 - 5% за рік, потім після 65 років швидкість збільшення кісткової недостатності уповільнюється В терапії постменопаузний гормональний дефіцит може компенсуватись замісною гормонотерапією, де головну роль відіграє естроген, що збе рігає кісткову тканину Але тривала естрогенотерапія інколи супроводжується небажаним впливом на статеві органи (ендометріальна гіперплазія, грудна пухлина ), що є серйозним недоліком і обмежує и використання Отже, необхідно знайти ІНШІ сполуки, окрім естрадюлу, які мали б роз'єднану естрогенну активність, а саме, естрогенну активність відносно до кістки, і зовсім не мали б або мали б дуже незначну активність щодо ендометріальної гіперплазії або розростання грудної пухлини Заявка на патент FR 2640977 А (29 червня 1990) описує стероїди, які мають антиестрогенну активність і/або естрогенну активність Ці сполуки відрізняються від сполук ВІДПОВІДНО до винаходу тим, що вони заміщені групою алкініл або не заміщені в положенні 17 альфа Журнал про стероїди (Lu jm et al Vol 60 № 8 серпень 1995, 512-518) описує не заміщений в положенні 17 альфа аналог (RU39411), що має змішану активність, як естрогенну, так і антиестрогенну, пригнічує зростання пухлинних клітин грудей MCF- 7 і, отже, використовується в лікуванні раку грудей 54483 Таким чином, об'єктом винаходу є сполуки загальної формули (І) щений або не заміщений, X означає гідроксил, можливо етерифікований і Y означає алкіл, заміщений або не заміщений, що містить від 1 до 4 атомів вуглецю, а також їх адитивні солі з фармацевтичне прийнятними кислотами Алкільним радикалом, що містить від 1 до 4 атомів вуглецю називають радикали метил, етил, пропіл, ізопропіл, н бутил, ізобутил, трет -бутил Коли Y означає алкіл, йдеться, зокрема, про алкіл, заміщений одним чи кількома атомами галогену Більш прийнятне, Y може означати групу три фтор метил Коли Ri і R2 утворюють разом з атомом азоту, з яким вони з'єднані гетероцикл, йдеться зокрема про насичені моно або біциклічні гетероцикли, що містять, при необхідності, ще один гетероатом, який вибирається з кисню та азоту, такі як гетероцикли, що вибираються з піролілу, імідазолілу, індолілу, піридилу, піразинілу, піримідинілу, піридазинілу, тіазолілу, оксазолілу, фуразонілу, піразолінілу, тіазолінілу, і, зокрема, такі насичені гетероцикли (І) Де п - ціле число, що дорівнює 2 або З, або Ri і F?2, ідентичні чи різні, означають атом водню або радикал алкіл, що містить від 1 до 4 атомів вуглецю, або Ri і F 2 утворюють разом з атомом азоту, з ? яким вони з'єднані, гетероцикл, моно або поліциклічний, насичений або ненасичений, 5-15-членний ароматичний або не ароматичний, який містить, при необхідності, від 1 до 3 додаткових гетероатомів, що вибираються з кисню, сірки і азоту, замі/ Ч H N Коли цей гетероцикл заміщений, він заміщений зокрема, алкільною групою, що містить від 1 до 4 атомів вуглецю на рівні атому азоту Коли X - гідроксильний радикал, можливо етерифікований, йдеться про групи OCO-alciF, в яких alc-iF- алкіл, що містить від 1 до 8 атомів вуглецю і, більш прийнятне, про групи -ОСОМе або OCOEt Адитивними солями з фармацевтичне прийнятними кислотами називають адитивні солі, утворені мінеральними або органічними кислотами з аміногрупами Так, мова може йти про кислоти соляна, бромистоводнева, азотна, сірчана, фосфорна, оцтова, мурашина, пропюнова, бензойна, малеїнова, фумарова, бурштинова, винна, лимонна, щавлева, глюксилова, аспарагінова, алкінсульфонові, такі як метансульфонова або етансульфонова, арилсульфонові, такі як бензолсульфонова або паратолуолсульфонова і бензоларилкарбонова чи паратолуоларилкарбонова Зокрема, об'єктом даного винаходу є сполуки названої вище формули (І), де п дорівнює 2, та їх адитивні солі з фармацевтичне прийнятними кислотами Більш прийнятно, об'єктом винаходу є сполуки названої вище формули (І), де п дорівнює 2, або Ri і F?2, ідентичні чи різні, означають радикал алкіл, який містить від 1 до 4 атомів вуглецю, або Ri і R2 утворюють разом з атомом азоту, з О N яким вони звязані, групу піперидино, піролідино або 2-азабіцик-ло(2 2 1)гепт-2-ил, X означає гідроксильний радикал, та Y означає радикал метил чи етил Зокрема об'єктом винаходу є сполуки формули (І), та їх адитивні солі з фармацевтичне прийнятними кислотами, що мають такі назви -11 р-[4-[2[(1 -піперидиніл)етокси]феніл]-19-нор17а-прегна-1,3,5(10)-триен-3,17р-дюл, -17а-метил-11р- [4- [2 [ (1-піперидиніл) етокси] феніл] -естра-1,3,5(10)-триен-3,17р-дюл, -17а-метил-11р- [4- [2- (діетиламшо) етокси] феніл] -естра-1,3,5(10)-3,17р-дюл, -17а-метил-11р-[4-[2-(1піролідиніл)етокси]феніл]-естра-1,3,5(10)-триен3,17р-дюл, -17а-метил-1ір-[4-[2-(2-аза-біцикло(2,2,1)гепт2-ил)етокси] феніл]-естра-1,3,5(10)-триен-3,17рдюл, -11р-[4-[2-(2-аза-біцикло(2 2 1)гепт-2-ил) етокси]феніл]-19-нор-17а-прегна-1,3,5(10)-триен-3,17рдюл, -17а-(трифторметил)-1ір-[4-[2-(1-піперидиніл) етокси]феніл] -естра-1,3,5(10)-триен-3,17р-дюл Об'єктом винаходу також є спосіб одержання сполук названої вище загальної формули (І), який полягає втому, що сполуку загальної формули (II) 54483 (її) де n, Ri та F 2 мають названі вище значення, ? піддають взаємодії з металоорганічною сполукою, похідною алкілу, що містить від 1 до 4 атомів вуглецю, і одержують сполуку формули (І), у якій X гідроксильна група та Y - алкільна група, що містить від 1 до 4 атомів вуглецю, яку, у разі необхідності, піддають реакції етерифікації групи 17-ОН і/або реакції солеутворення Дія металоорганічної сполуки на групу 17-кето дає змогу одержати сполуки формули (І), де X гідроксильна група і Y -алкільна група, що містить від 1 до 4 атомів вуглецю Металоорганічну похідну алкілу, що містить від 1 до 4 атомів вуглецю, вибирають з магнійорганічних сполук формули Y-MgHal і літійорганічних сполук формули Y-Li, в яких Y має назване вище значення, a Hal означає атом галогену Більш прийнятно, реакцію проводять в присутності хлориду церію В більш прийнятному варіанті втілення способу Hal позначає атом хлору, брому або йоду, більш прийнятно, брому Щоб одержати сполуки формули (І), в яких X гідроксильний радикал, a Y - це група CF3, реакцію проводять при дії СРзЄіМез на групу 17-кето, потім обробляють агентом зняття захисту, таким як фторид тетрабутиламонію Об'єктом винаходу є також спосіб одержання сполук загальної формули (І), де Y являє собою алкіл, що містить від 2 до 4 атомів вуглецю, який полягає в тому, що сполуку загальної формули (III) (III) у якій п, R1 та F 2 мають названі вище значен? ня і де Y1 позначає алкенільну або алкінільну групу, що містить від 2 до 4 атомів вуглецю, піддають дії агента відновлення подвійного або потрійного зв'язку, з одержанням сполуки формули (І), у якій X - гідроксильна група і Y - алкільна група, яка містить від 2 до 4 атомів вуглецю, яку, у разі необхідності, піддають реакції етерифікації з групою 17ОН і/або реакції солеутворення Реакцію повного відновлення можна здійсню 8 вати за допомогою водню в присутності каталізатора, такого як паладій на вугіллі, або родієвого каталізатора, такого як реактив Вілкінсона Реакції етерифікації і солеутворення проводять у звичайні способи, широко ВІДОМІ фахівцю Сполуки загальної формули (І), та їх адитивні солі з фармацевтичне прийнятними кислотами, мають естрогенну активність, а також антиестрогеннута антипроліферативну активність Завдяки своїй активності сполуки формули (І) можуть використовуватись при лікуванні хвороб, пов'язаних з ппофолікулінією, наприклад, аменорей, диспенорей, повторних викиднів, передменструальних болів, у лікуванні деяких естрогенозалежних патолопй, таких як простатичні аденоми або карциноми, грудні карциноми та їх метастази або при лікуванні доброякісних пухлин грудей, в якості антиустеротрофічного засобу, а також в замісній терапії менопаузи або перименопаузи Серед симптомів і наслідків, пов'язаних з менопаузою, частіше за все називають припливи крові до обличчя, потіння, атрофію та сухість піхви, сечові симптоми і тривале зменшення кісткової маси та підвищення ризику переломів, а також втрату СТІЙКОСТІ серцево-судинної системи, що спричинюється естрогенами Зокрема, сполуки формули (І), а також їх адитивні солі з фармацевтичне прийнятними кислотами можуть також застосовуватись у профілактиці або лікуванні остеопорозу Сполуки формули (І), а також їх адитивні солі з фармацевтичне прийнятними кислотами можуть також використовуватись в профілактиці і лікуванні остеопорозу у ЧОЛОВІКІВ Вони, також, можуть використовуватися в профілактиці і лікуванні вторинних (побічних) остеопорозів (наприклад, кортизонових, пов'язаних з нерухомістю) Сполуки формули (І), а також їх адитивні солі з фармацевтичне прийнятними кислотами мають, зокрема, роз'єднану естрогенну активність Роз'єднаною естрогенною активністю називають естрогенну активність відносно до кісткового апарату і мінімальну активність відносно до матки, що не спричинює ендометріальну проліферацію (активність значно нижча від активності естрадюлу) Сполуки ВІДПОВІДНО до винаходу мають такі переваги Вони мають антиестрогенну активність відносно до клітин грудних залоз На протилежність естрадюлу вони не стимулюють зростання пухлинних клітин грудних залоз у людини і навіть можуть пригнічувати їх зростання Сполуки ВІДПОВІДНО ДО винаходу, таким чином, є більш прийнятними при лікуванні менопаузи у жінок, схильних до раку грудей (родинний анамнез), для яких, таким чином, виключається замісне лікування естрадюлом Ці сполуки можуть, також, використовуватися при лікуванні раку грудей Вони ведуть до зниження сироваткового холестерину до рівня, еквівалентного рівню при лікуванні естрадюлом, посилюючи завдяки цьому СТІЙКІСТЬ серцево-судинної системи Нарешті, їх не прописують для прийому разом з прогестоміметичною сполукою, тому що вони не 54483 мають естрогенної аісгивності відносно до матки Таким чином, об'єктом винаходу є сполуки загальної формули (І), а також їх адитивні солі з фармацевтичне прийнятними кислотами, в якості лікарських засобів Зокрема, об'єктом винаходу є сполуки формули (І), а також їх адитивні солі з фармацевтичне прийнятними кислотами, в якості лікарських засобів, призначених для профілактики та лікування остеопорозу Також, об'єктом винаходу є сполуки загальної формули (І), а також їх адитивні солі з фармацевтичне прийнятними кислотами, в якості лікарського засобу, призначеного для профілактики або лікування остеопорозу, який не має або майже не має естрогенної активності відносно до матки Нарешті, об'єктом винаходу є сполуки загальної формули (І), а також їх адитивні солі з фармацевтичне прийнятними кислотами, в якості лікарського засобу, призначеного для профілактики або лікування остеопорозу, у жінок, схильних до пухлин грудей Винахід стосується фармацевтичних композицій, що мають в якості активної основи, принаймні, один з вищеназваних лікарських засобів Сполуки формули (І), а також їх адитивні солі з фармацевтично прийнятними кислотами застосовують через травний тракт, парентерально або місцево, наприклад, черезшкірно Вони можуть призначатися у вигляді простих або дражованих таблеток, желатинованих капсул, гранул, свічок, вапнальних шариків, ІН'ЄКЦІЙ мазей, кремів, гелів, мікросфер, імплантатів, внутрішньовапнальних кілець, пластирів, спреїв, які готують згідно з звичайними методиками Одна чи кілька активних основ можуть вводитися у фармацевтичні композиції разом з звичайно використовуваними в них ексципієнтами, такими як тальк, гуміарабік, лактоза, крохмаль, стеарат магнію, олія какао, водні і не водні зв'язувальні речовини, жирові речовини тваринного або рослинного походження, ПОХІДНІ парафінів, ГЛІКОЛІ, різні змочувальні речовини, диспергатори або емульгатори, консерванти Прийнятна доза варіюється залежно від захворювання і від способу введення засобу, вона може становити, наприклад, від 0,5 до ЮОмг на день для дорослих при прийомі всередину Сполуки загальної формули (II) і (III) ВІДОМІ І описані в таких патентах ЕР-В-0097572, FR-B2640977, ЕР-В-305942 Наведені нижче приклади ілюструють винахід, але не обмежують його Приклад 1 17а-метил-11р-[4-[2-[(1піперидиніл)етокси]феніл]-естра- 1,3,5(10)-триен3,17р-дюл Після дегідратації 1,06г СеСІз(ІІІ), 7НгО за пониженого тиску при t°=140°C додають в інертній атмосфері і при кімнатній температурі 10,6мл тетрапдрофурану (ТГФ), потім, після перемішування протягом 2 годин додають при температурі -70°С 1,89мл ефірного розчину метиллітію 1,6М і перемішують протягом ЗО хвилин при температурі 75°С Потім додають до цієї суспензії 268мг 3пдрокси-1ір-[4-[2-(1-піперидиніл)етокси]феніл] 10 естра-1, 3, 5 (10) -триен-3, 17р-ону в розчині в Змл тетрапдрофурану/ силіпоритута перемішують при цій температурі протягом 1 години Після додання 15мл насиченого розчину хлориду амонію і 20мл етилацетату, фільтрують, промивають, сушать і випарюють за пониженого тиску, щоб отримати 277мг неочищеного цільового продукту Цей продукт очищають хроматографією на ДІ-ОКСИДІ кремнію, елююючи сумішшю метиленхлорид 90/ метанол 10/ гідроксид амонію 0,5 Одержують 232мг продукту, який перекристалізовують з суміші дихлорметан/ ізопропіловий ефір, і одержують 180мг цільового продукту Т пл =155°С ІЧ спектр (СНСІз) -ОН 3602см 1 + загальна абсорбція ароматична 1610см \ 1580см \ 1512см ЯМР (CDCI3) 0,51 (s) 1,29 (s) M e в положенні 18 M e в положенні 17 3.98 (m) 6,41 O - C H 2 - C H 2 - N , C H - P h (Нц) Н2, Н4 цикл А, Н'з, Н'5 фенілу в положенні 11 Hi циклу А Н'2, Н'б фенілу в положенні 11 6,78 (d) 6,94 Приклад 2 11 р-[4-[2[-(1 -піперидиніл)етокси]феніл]-19-нор17а-прегна-1,3,5(10)-триен-3,17р-дюл До розчину в інертній атмосфері з 192мг 11р[4- [2 [ (1 -піперидиніл)етокси]феніл]-19-нор-17апрегна-1,3,5(10)-триен-20-ін-3,17р-дюлу в бмл етанолу додають 20мг паладію на вугіллі (9,5%) і перемішують під тиском водню в 1660мбар протягом 1 години 45 хвилин Суспензію фільтрують та випарюють за пониженого тиску Одержують 193мг неочищеного продукту, який очищають хроматографією на колонці з дюксиду кремнію (Lichrosorb RP18) елююючи сумішшю метанолу 90/ вода 10 Одержують 137мг продукту, який скристалізують в суміші дихлорметан/ ізопропіловий ефір, і одержують 114мг чистого цільового продукту Т пл = 231 °С ІЧ спектр (СНСІз) -ОН 3600см 1 + загальна абсорбція ароматична 1610см \ 1581см \ 1512см ЯМР (CDCI3+ 2 краплі C5D5N) 0,47 (s) Me в положенні 18 1.01 (t) 2 2 > 47 71 СН2-СН3 СН 2 - N - СН 2 - піперидин > O-CH2-CH2-N 3.99 (m) о - СН 2 - СН 2 - N, СН - Рп (Ии) 6,48 (dd) H2 6,59 Н'з, Н'б (феніл в положенні 11) 6,63 Н4 (цикл А) , 6,80 (d) Hi (цикл А) 6,96 Н'2, Н'б фенілу в положенні 11 9,94 з-ОН Приклад З 11р-[4-[2-[2-азабіцикло(2 2 1)гепт-2ил]етокси]феніл]-17а-метил-естра-1,3,5(10)-триен3-17р-діол 11 54483 Діють ЯК В прикладі 1, використовуючи в якості вихідної речовини 3,70г СеСІз, 7 ЬЬО і 37мл тетрапдрофурану та 6,7мл ефірного розчину метиллітію (1,6М) До одержаної суспензії, охолодженої до 78°С додають повільно 966мг 11р-{4-[2-[2азабіцикло(2 2 1)гепт-2-ил]етокси]феніл]3-пдроксиестра-1,3,5(10)-триен-17-ону в розчині 8мл тетрапдрофурану, перемішують протягом 45 хвилин і продовжують синтез, як в прикладі 1 Одержують 874мг неочищенного продукту Після хроматографії на дюксиді кремнію (елююючи СН2СІ2-СН3ОНNH 4 OH 90-10-0,7 потім AcOEt-TEA 88-12), одержують 442мг цільового продукту Т пл = 163-164°С ІЧ спектр (СНСІз) -ОН ароматична ЯМР (CDCI 3 ) 0,51 (s) 1,29 (s) 3,85-4,05 3602см 1 + загальна абсорбція 1610см \ 1581см \ 1512см Me в положенні 18 Me в положенні 17 O-CH2-CH2-N,CH-Ph (Нц) 6,41 Н 2 , Н 4 цикл А, 6,77 (d) Hi циклу А 6,46-6,95 Н фенілу в положенні 11 Одержання 1ір-[4-[2-[2-азабіцикло(2 2 1)гепт2-ил]етокси]феніл]-3-пдрокси-естра-1,3,5(10)триен-17-ону, що використовується в якості вихідної речовини в прикладі З Змішують 1,1г 3-пдрокси 11р-[4(йодоетокси)феніл]-естра-1,3,5(10)-триен-17-ону розчиненого в 20мл тетрапдрофурану і 1,03г 2азабіцикло[2 2 1 ]гептанута перемішують протягом 1 години ЗО хвилин при температурі дефлегмації в атмосфері азоту Випарюють тетрапдрофуран, обробляють залишок в етилацетаті, додають води, екстрагують етилацетатом, сушать, випарюють розчинник і одержують після хроматографії на дюксиді кремнію (елююючи СН2СІ2-СН3ОН-МН4ОН 90-10-0,5) 0,97г цільового продукту Rf=0,27 Приклад 4 17а-метил-1ір-[4-[2-(1-піролідиніл)етокси] феніл]-естра-1,3,5(10)-триен-3,17р-дюл Діють ЯК В прикладі 1, використовуючи в якості вихідної речовини 3,24г СеСІз, 7 ЬЬО, ЗОмл тетрапдрофурану, 5,85мл метиллітію, потім 850мг 3пдрокси-1ір-[4-[2-(1-пірол ідиніл)етокси]феніл]естра-1,3,5(10)-триен-17-ону, розчиненого в 8,5мл тетрапдрофурану Після хроматографії на дюксиді кремнію (елююючи CH 2 CI-CH 3 OH-NH 4 OH 92-8-0,5), одержують 615мг цільового продукту Т п л = 155-157°С ІЧ спектр (СНзСІз) -ОН 3603см 1 + загальне поглинання ароматична 1610см \ 1581см \ 1512см ЯМР (CDCI 3 ) 0,51 (s) Me в положенні 18 1,29 (s) Me в положенні 17 3." O-CH2-CH2-N,CH-Ph (Нц) 6,38 (dd) Н 2 цикл А, 6,40 (d) H 4 циклу А 6,77 Ні фенілу в положенні 11 6,49-6,95 Н фенілу в положенні 11 Одержання 3-пдрокси-11р- [4-[2- (іпіролідиніл) етокси] феніл] -естра-1,3,5(10)-триен-17-ону, що 12 використовується в якості вихідної речовини в прикладі 4 Діють ЯК при одержанні вихідного продукту прикладу 3, використовуючи 1,1г стероїдної йодвмісної похідної в 20мл тетрапдрофурану та 1мл піролідину Одержують 864мг цільового продукту після хроматографії на дюксиді кремнію (елююючи СН2СІ2-СН3ОН-МН4ОН 92-8-0,2) Rf=0,29 Приклад 5 1ір-[4-[2-(діетиламшо)етокси]феніл] 17аметил-естра-1,3,5(10)- триен-3,17р-дюл Діють ЯК В прикладі 1, використовуючи в якості вихідного продукту 3,62г хлориду СеСІз, 7 НгО, Збмл тетрапдрофурану і 6,5мл метиллітію в простому ефірі (1,6М) / потім 898мг 3-пдрокси 11 р-[4-[2(діетиламшо)етокси]феніл]-естра-1,3,5(10)-триен17-ону, розчиненого в 9мл тетрапдрофурану Після хроматографії на дюксиді кремнію (елююючи CH2CI2-CH3OH-NH4OH 92-8-0,5), одержують 686мг цільового продукту Т пл = 159-160°С ІЧ спектр (СНСІз) 1 -ОН 3602см + загальне поглинання, ароматична 1610см \ 1581см \ 1512см 1 (F), 1500см 1 (ер) ЯМР (CDCI 3 ) 0,47 (s) Me в положенні 18 1.05 (t) 1,28 (s) _N_(CH2-CH3)2 Me в положенні 18 2,65 (m) -N-(CH2-CH3)2 3,95 (t) O-CH2-CH2-N, 6,31 (d) H 4 (цикл А) 6,38 (dd) H 2 (цикл А) 6,80 (d) Hi (цикл А) 6,56 та 6, 93 H фенілу в положенні 11 Одержання 3-пдрокси 1ір-[4-[2-(діетиламшо) етокси]феніл]-естра-1,3,5(10)-триен-17-ону Діють ЯК при одержанні вихідного продукту прикладу 3, використовуючи 1,1г йодвмісної стероїдної похідної в 20мл тетрапдрофурану і 2мл діетиламіну Одержують 898мг цільового продукту після хроматографії на дюксиді кремнію (елююючи CH2CI2-CH3OH-NH4OH 92-8-0,2) Rf=0,24 Приклад 6 17а-(трифторметил)-1ір-[4-[2-(1-піперидиніл) етокси]феніл]-естра-1,3,5(10)-триен-3,17р-дюл Нагрівають протягом 2 годин при 120°С під тиском 10 2 мбар 83мг фториду тетрабутиламонію (Me4NH, 4H2O) , потім доводять температуру до кімнатної в інертній атмосфері Додають 237мг 3пдрокси 1ір-[4-[2-(піперидиніл)етокси]феніл]- естра- 1,3,5(10)-триен-17-ону, розчиненого в Змл тетрапдрофурану, охолоджують до +4°С та додають 0,3мл триметил (трифторметил)-силану, після цього перемішують 2 години при цій температурі Додають 4мл фториду тетрабутиламонію в розчині у тетрапдрофурані, перемішують 3 години ЗО хвилин при кімнатній температурі, додають воду, екстрагують метиленхлоридом, промивають водою, сушать і випарюють розчинники за пониженого тиску Залишок хроматографують на дюксиді кремнію (елююючи CH 2 CI 2 -MeOH-NH 4 OH 90-10-0,1) та 14 13 54483 одержують 127мг цільового продуїсгу (0,Змг/кг/д), ІЧ спектр (СНСІз) - КІЛЬКІСТЬ введень 1 раз/день, 5 1 протягом 4 тижнів, -ОН 3602см + загальна абсорбція ароматична 1610см \ 1580см \ 1512см - спосіб введення оральне введення, ЯМР (CDCI3) - об'єм 5мл/кг (р о ), 0,56 (s) Me в положенні 18 - термін між останньою ІН'ЄКЦІЄЮ та умертвінням 24 години, 4,00 (m) О - СН 2 - СН 2 - N, СН - Ph (Hu) 6,37 (dd) H2 (цикл А) 6,41-6,93 Н'2 Н'з (феніл в положенні 11) 6,41 (d) H4 (цикл А) 6,77 (d) Hi (цикл А) Фармакологічні тести 1) Дія на проліферацію клітин грудної залози Проліферативна активність молекул досліджувалась шляхом порівняння з проліферативною активністю естрадюлу на культурі грудної залози людини MCF-7 Щоб виявити агоністичну активність естрадюлу і/або досліджуваних сполук, культуральне середовище, в якому підтримують клітини (багате на фактори росту та стероїди), замінюють збідненим середовищем, позбавленим також і стероїдів (середовище DEMEM, доповнене 5% сироватки, що не містить стероїдів і без фенольного червоного) Клітини приміщують у збіднене середовище за 2 дні до початку тестів Через 7 днів культивування в присутності досліджуваних сполук клітинну проліферацію оцінюють шляхом аналізу ДНК В кожному тесті ефект естрадюлу при концентрації 10 1 0 М (зростання клітин у присутності естрадюлу мінус зростання клітин в присутності розчинника) приймають за 100% агоністичної активності Активність сполук визначають у порівнянні з цим внутрішнім контролем Сполуки, що викликають зростання клітин, ідентичне до зростання, що спостерігається в присутності лише одного розчинника, класифікуються як "неактивні", а сполуки, що спричинюють більш слабке зростання клітин, ніж при розчиннику, класифікуються, як "інгібітори" Таблиця 1 Е2 Пр 2 Активність Агоністична Неактивний Пр 3 Інгібітор 2) Сполуки ВІДПОВІДНО до винаходу тестують з метою визначення їх впливу на кісткову масу і на активність утворення та резорбції на моделі щура з видаленим яєчником у ВІЦІ 3 МІСЯЦІВ Тварин обробляють з профілактичною метою Таблиця 2 Тварини Вид Штам Стать Вага КІЛЬКІСТЬ тварин/група Щур Sprague-Dawley жіноча 250г - 280г 8 Сполуки 1 Тестовані сполуки сполука прикладу 1 - носій(ї) кукурудзяне масло, метилцелюлоза 0,5%, - доза(и) одна доза на тестовану речовину - КІЛЬКІСТЬ введень 20, 2 Контрольна сполука 17р естрадюл вводили підшкірне при дозі, що дорівнює 0,1мг/кг/день у розчині з сумішшю масло проростків кукурудзи бензиловий спирт (99 1, об/об) в обсязі 0,2мл/кг Протокол експерименту Тварини Дослідження проводять на самицях щурів з видаленими яєчниками у ВІЦІ 3 МІСЯЦІВ Тварини знаходяться в кімнаті, де підтримується певний температурний режим (20°С ± 2°С) , їх тримають в коробках групами по 4 Тварини одержують, ad libitum, демшералізовану воду і харчові таблетки (пробки AO4CR-10UAR) Хірургія У самиць щурів у ВІЦІ 3 МІСЯЦІВ вагою приблизно 250г видаляють яєчники під анестезією з імальгеном 100, доза якого дорівнює 100мг/кг і який вводять внутрішньочеревно (і р) та в об'ємі 1мл/кг Вони одержують також Нембутал (Змг/кг внутрішньочеревно, у об'ємі 0,Змл/кг) Після бокового розрізу шкірний і м'язовий шари поділяють Видалення кожного яєчника здійснюють після перев'язування маткової труби Контрольні зразки щура "SHAM" анестезують за тих самих умов Після розрізу шкірного і м'язового шарів кожен яєчник виймають, потім вертають на місце Лікування Активність сполук визначають при профілактичному лікуванні, їх вводять безпосередньо після видалення яєчників Тварин розподіляють на групи по 8 Група 1 контрольні зразки щура "SHAM", які отримують один чи кілька носив (розчинників) Група 2 контрольні зразки щурів "OVX", які одержують один чи кілька носив (розчинників) Групи X щури "OVX", які одержують ВІДПОВІДНО певні дози одного чи кількох тестованих сполук Взяття крові По закінченні 4 тижнів (тривалість тесту) тварин обезголовлюють за допомогою гільйотини Зібрану сироватку після центрифугування зберігають при -20°С ЛІПІДНИЙ баланс встановлюють, виходячи з аналізу сироватки на загальний холестерин, тригліцериди і фосфоліпіди на аліквотному об'ємі сироватки 500мкл Пониження рівня сироваткового холестерину виражено у % відносно до його рівня у тварин з видаленими яєчниками, які одержують лише розчинник Видалення органів Після умертвіння тварин здійснюють видалення таких органів - генітальний тракт Здійснюють видалення маток, їх зважують Збільшення ваги виражене у % від ваги маток тварин з видаленими яєчниками, які одержують лише розчинник 15 54483 - кісткова тканина Кісткову масу (МКЩ або мінеральна кісткова ЩІЛЬНІСТЬ) вимірюють за допомогою біфотонної абсорбціометри рентгенівського випромінювання подвійної енергії (DEXA) Вимірювання здійснюють на видалених кістках, з яких усунено усі м'які тканини BMD (кісткову мінеральну ЩІЛЬНІСТЬ) вимірюють на всій КІСТЦІ, а також на метафізарній частині проксимального кінця лівої великої гомілкової кістки Ця зона найбільш багата на трабекулярну кістку і, отже, найбільш чутлива до змін кісткового об'єму і мінеральної кісткової ЩІЛЬНОСТІ Результати виражено у % згідно з формулою МКЩ тестованого продукту - МКЩ OVXx 100 МКЩ SHAM-МКЩ OVX Таблиця З 16 Доза Велика гомілкова кістка мг/кг Е2 0/1 sc Пр 1 0,3 ро Пр 3 0,3 ро OVX SHAM ЩІЛЬНІСТЬ% 105 75 46 0 100 Матка Холестерин вага% 359 76 37 % -35 -43 -40 Висновки Сполуки ВІДПОВІДНО до винаходу забезпечують ефективний кістковий захист (= 75%), при цьому виявляють мінімальну уетеротрофічну активність порівняно з названою активністю, що викликається естрадюлом Крім того/ спостерігається значне зменшення загального рівня холестерину Підписано до друку 03 04 2003 р Тираж 39 прим ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)236-47-24
ДивитисяДодаткова інформація
Назва патенту англійськоюSteroids, substituted in position 11, a process for prepararion thereof, their application as a medicine and the pharmaceutical compositions containing them
Автори англійськоюTeutsch Jean-Georges
Назва патенту російськоюСтероиды, замещенные в положении 11, способ их получения, их применение в качестве лекарственного средства и фармацевтические композиции, содержащие их
Автори російськоюТетш Жан-Жорж
МПК / Мітки
МПК: A61P 19/10, A61K 31/565, C07J 41/00
Мітки: заміщені, стероїди, одержання, спосіб, положенні, композиція, фармацевтична, варіанти
Код посилання
<a href="https://ua.patents.su/8-54483-sterodi-zamishheni-v-polozhenni-11-sposib-kh-oderzhannya-varianti-ta-farmacevtichna-kompoziciya.html" target="_blank" rel="follow" title="База патентів України">Стероїди, заміщені в положенні 11, спосіб їх одержання (варіанти) та фармацевтична композиція</a>
Попередній патент: Спосіб вирощування деревостанів сосни на крупномірний пиловник
Наступний патент: Поглинальний апарат, зокрема для залізничних пасажирських вагонів
Випадковий патент: Стоматологічна паста для лікування захворювань пародонта












