Похідні 5-(піридин-3-іл)-1-азабіцикло[3,2,1]октану, фармацевтична композиція на їх основі
Номер патенту: 77229
Опубліковано: 15.11.2006
Автори: Неделек Ален, аллі Фредерік, Леклерк Оділь, Локгед Алістер
Формула / Реферат
1. Сполука у формі чистого енантіомера або у формі суміші енантіомерів загальної формули
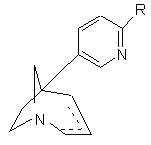 , (І)
, (І)
в якій R представляє атом галогену або (С3-С6) циклоалкіл або феніл, заміщений одною або більше групами, вибраними з атома галогену або (С1-С6)алкілу, (С1-С6)алкоксилу, нітрогрупи, аміногрупи, (С1-С3)діалкіламіногрупи, трифлуорметилу, трифлуорметоксилу, ціаногрупи, гідроксилу, ацетилу або метилендіоксилу, або піперидинілу, морфолін-4-ілу, піролідин-1-ілу, азетидин-1-ілу, азепін-1-ілу, піридинілу, хінолінілу, тієнілу, піразинілу, фурилу, бензофурилу, бензотієнілу, індолілу, піримідинілу, ізоксазолілу, феноксазинілу, феноксатіїнілу, дибензотієнілу, дибензофурилу, піролілу, нафтилу, де кожна з цих груп може, як варіант, бути заміщеною одною або більше групами, вибраними з атомів галогену, (С1-С6)алкілу, (С1-С6)алкоксилу, трифлуорметоксилу, трифлуорметилу, нітрогрупи, ціаногрупи, гідроксигрупи, аміногрупи, (С1-С3)діалкіламіногрупи або (С3-С8)циклоалкіламіногрупи, та де з двох представлених ![]() зв'язків карбон-карбон, один є простим, а інший може бути простим або подвійним,
зв'язків карбон-карбон, один є простим, а інший може бути простим або подвійним,
у формі основи або солі, похідної від додавання до кислоти, та за умови, що цією сполукою не є :
5-(2-бромпіридин-5-іл)-1-азабіцикло[3,2,1]окт-3-ан,
5-(2-хлорпіридин-5-іл)-1-азабіцикло[3,2,1]окт-3-ан,
5-(2-флуорпіридин-5-іл)-1-азабіцикло[3,2,1]окт-3-ан.
2. Сполука за п. 1, яка відрізняється тим, що R представляє атом галогену або феніл, заміщений одною або більше групами, вибраними з атомів галогену та (С1-С6)алкілу, (С1-С6)алкоксилу, нітрогрупи, аміногрупи, трифлуорметилу, ціаногрупи, гідроксилу, ацетилу або метилендіоксилу, або представляє піридиніл, тієніл, індоліл або піримідиніл, що як варіант, заміщено одною або більше (С1-С6)алкоксигрупами.
3. Медикамент, який відрізняється тим, що містить сполуку за п. 1.
4. Фармацевтична композиція, яка відрізняється тим, що містить сполуку за п. 1, разом з ексципієнтом.
Текст
1. Сполука у формі чистого енантіомера або у формі суміші енантіомерів загальної формули R 2 (19) 1 3 77229 4 3. Медикамент, який відрізняється тим, що міс4. Фармацевтична композиція, яка відрізняється тить сполуку за п. 1. тим, що містить сполуку за п. 1, разом з ексципієнтом. Представлений винахід стосується сполук, які є лігандами нікотинових рецепторів та є корисними при лікуванні чи попередженні розладів, пов'язаних з дисфункцією нікотинових рецепторів, зокрема на рівні центральної нервової системи. Сполуки представленого винаходу мають загальну формулу (І) в якій R представляє атом галогену або (С3С6)циклоалкіл або феніл, заміщений одною або більше групами, вибраними з атому галогену, або (С1-С6)алкілу, (С1-С6)алкоксилу, нітрогру-пи, амінофупи, (С1-С3)діалкіламіногрупи, трифлуорметилу, трифлуорметоксилу, ціаногрупи, гідроксилу, ацетилу або метилендіоксилу, або піперидиніл, або морфолін-4-іл, або піролідин-1-іл, або азетидин-1-іл, або азепін-1-іл, або піридиніл, або хінолініл, або тієніл, або піразиніл, або фурил, або бензофурил, або бензотієніл, або індоліл, або піримідиніл, або ізоксазоліл, або феноксазиніл, або феноксатіїніл, або дибензотієніл, або дибензофурил, або піроліл, або нафтил, де кожна з цих груп може, як варіант, бути заміщеною одною або більше групами, вибраними з атомів галогену, (С1С6)алкілу, (С1-С6)алкоксилу, трифлуорметоксилу, трифлуорметилу, нітрогрупи, ціаногрупи, гідроксигрупи, аміногрупи, (С1-С3)діалкіламіногрупи або (С3-С6)циклоалкіламіногрупи. З двох зв'язків карбон-карбон, представлених , один є простим, а інший може бути простим або подвійним. Крім того, атом карбону у позиції 5 є асиметричним, а відтак сполуки можуть існувати у формі двох енеантіомерів або їх сумішей. Сполуки винаходу можуть існувати у формі основ або солей, що походять від додавання до кислот. Підгрупою кращих сполук є сполуки загальної формули (І), в яких R представляє атом галогену або феніл, заміщений одною або більше групами, вибраними з атомів галогену та (С1-С6)алкілу або (С1-С6)алкоксилу, нітрогрупи, аміногрупи, трифлуорметилу, ціаногрупи, гідроксилу, ацетилу або метилендіоксилу, або представляє піридиніл, або тієніл, або індоліл, або піримідиніл, що, як варіант, заміщено одною або більше (С1С6)алкоксифупами. Сполуки загальної формули (І) можна отримувати способом, ілюстрованим наступною схемою. 3-Оксо-1,4-азабіцикло[2,2,2]октан формули (II), реагує з піридиновим похідним загальної формули (III), в якій R визначено вище, a W представляє атом галогену. Також можливо проводити реакцію конденсації між 3-оксо-1-азабіцикло[2,2,2]октаном та літійованим похідним сполуки загальної формули (III), отриманим обміном галоген-метал з ал-кіллітієвим похідним. Це дає сполуки загальної формули (IV), які при нагріванні у кислотному середовищі дають сполуки загальної формули (І), в яких один з двох представлених зв'язків карбон-карбон є подвійним. Каталітичне гідрування подвійного зв'язку дає сполуки загальної формули (І), в яких усі зв'язки азабіциклооктанового кільця є насиченими. 3-Оксо-1-азабіцикпо[2,2,2] октан є у продажу. Сполуки загальної формули (III) є у продажу або доступні способами, описаними у літературі. Для деяких сполук замісники R не представлено у вихідній сполуці загальної формули 5 (III); залежно від їх природи ці замісники можна уводити на кінцеву сполуку загальної формули (І). Отже, наприклад, сполуки загальної формули (І), в яких R представляє арил, можна отримувати виходячи з відповідних сполук, в яких R представляє атом галогену, використовуючи будь-які з відомих способів, як-то сполучення Сузукі у присутності боронової кислоти та паладієвого каталізатору, наприклад, тетракіс(трифенілфосфін)паладію, або сполучення Стилла з прийнятними реагентами. Наступні приклади ілюструють отримання деяких сполук винаходу. 5 77229 6 Аналізи на мікроелементи та спектри ІЧ та дної кислоти в оцтовій кислоті. Це дає 0,22г дигідЯМР підтверджують структури отриманих сполук. роброміду. Температура плавлення: 273-274°С. Число у дужках у назвах прикладів відповідає Приклад 2 (сполука №2). номеру у першій колонці нижченаведеної таблиці. Гідробромід 5-(2-фенілпіридин-5-іл) -1У назвах сполук, "дефіс" є частиною слова, а азабіцикло[3,2,1]октану(2:1) переніс "__" використано тільки при розриві у кінці 0,14г (0,33ммоль) дигідроброміду 5-(2строки, його слід позбавлятися у відсутність розфенілпіридин-5-іл)-1-азабіцикпо[3,2,1] окт-3-ену у риву, та не слід заміняти стандартним дефісом чи розчині у 20мл метанолу уводять у посудину Парпроміжком. ра на 250мл, та додають 0,14г 10% паладію, нанеПриклад 1 (сполука №1). сеного на вугілля. Реакційну суміш далі піддають Гідробромід 5-(2-фенілпіридин-5-іл)-1тиску водню 0,35МПа з перемішуванням протягом азабіцикло[3,2,1]окт-3-ену (2:1). 5 годин. Каталізатор збирають фільтруванням че1,1. 5-Бром-2-фенілпіридин рез діатомову землю та розчинник концентрують 30г (0,127моль) 2,5-дибромпіридин у суспензії під зниженим тиском. Це дає 0,058г продукту. у 100мл толуолу, 15,4г (0,127моль) фенілбороноТемпература плавлення: 272-277°С. вої кислоти, 4,4г (0,0038моль) тетраПриклад 3 (сполука №8). кіс(трифенілфосфін)паладію, 90мл 2М водного Етандіоат 5-[2-(3-метилфеніл)піридин-5-іл)-1розчину натрій карбонату та 4мл етанолу уводять азабіцикло[3,2,1]октану(1:1). послідовно у тригорлу колбу на 500мл, та суміш 3,1. 3-Гідрокси-3-(2-бромпіридин-5-іл)-1гріють при 90°С протягом 22 годин. азабіцикло[2,2,2] октан. Суміш декантують, органічну фазу промива27,6г (0,116моль) 2,5-дибромпіридин у 1000мл ють 100мл води сушать і концентрують під знижеетилового етеру уводять у тригорлу колбу на ним тиском, та залишок очищають хроматографі2000мл, реакційну суміш охолоджують до -67°С та єю на колонці з силікагелем, елюючи 30/70 56мл (0,140моль) 2,5Μ розчин бутиллітію у гексані сумішшю циклогексану та дихлорметану. Це дає додають краплями протягом 10 хвилин. Суміш 22,4г кристалів. перемішують при -67°С протягом 45 хвилин перед Температура плавлення: 69-72°С. додаванням 14,5г (0,116моль) 11,2. 3-Гідрокси-3-(2-фенілпіридин-5-іл)-1азабіцикло[2,2,2]октан-3-ону у розчині у 150мл азабіцикло[2,2,2]октан. етилового етеру протягом 45 хвилин та суміш пе2,5г (0,0107моль) 5-бром-2-фенілпіридину у ремішують при -67°С протягом 3 годин. Додають розчині у 40мл етилового етеру уводять у тригорлу 300мл насиченого водного розчину амоній хлориколбу на 100мл, та реакційну суміш охолоджують ду, а потім 200мл концентрованого водного розчидо -60°С перед додаванням краплями протягом 10 ну натрій гідроксиду, водну фазу екстрагують хлохвилин 5, 6мл (0,0139моль) 2,5Μ розчину нроформом, а органічні фази сушать та бутиллітію у гексан, та температур тримають при концентрують під зниженим тиском. Залишок очи70°С протягом 1 годин. щають хроматографією на колонці з силікагелем, 1,34г (0,0107моль) 1-азабіцикло[2,2,2]октан-3елюючи 95/5/0,5, далі 80/15/1,5, сумішшю хлороону у розчині у 20мл тетрагідрофурану додають форму, метанолу та аміаку. Це дає 19,7г продукту протягом 10 хвилин, та суміш перемішують протяу формі аморфного твердого продукту. гом 30 хвилин при -70°С далі при кімнатній темпе3,2. 5-(2-бромпіридин-5-іл)-1ратурі протягом 4 годин. азабіцикло[3,2,1]окт-3-ен. Реакційну суміш гідролізують додаванням 9,4г (0,033моль) 3-гідрокси-3-(2-бромпіридин100мл метанолу та концентрують під зниженим 5-іл)-1-азабіцикло [2,2,2] октану та 35мл конценттиском. Залишок переносять у 100мл насиченого рованої сульфатної кислоти уводять у тригорлу водного розчину амоній хлориду та водну фазу колбу на 100 мл та суміш гріють при 190°С протяекстрагують хлороформом. Органічні фази сушать гом 1 годин 45. Суміш охолоджують та виливають та концентрують під зниженим тиском та залишок у 400мл охолодженого льодом водного розчину очищають хроматографією на колонці з силікагенатрій гідроксиду, водну фазу екстрагують хлоролем, елюючи 90/10/1 сумішшю хлороформу, метаформом, та органічні фази сушать та випарюють нолу та аміаку. Це дає 0,8г кристалів. під зниженим тиском. Залишок очищають хроматоТемпература плавлення: 214°С. графією на колонці з силікагелем, елюючи 90/10/1 1,3. Гідробромід 5-(2-фенілпіридин-5-іл)-1сумішшю хлороформу, метанолу та аміаку. Це дає азабіцикло[3,2,1]окт-3-ен (2:1). 3,9г продукту у формі блідо-жовтого твердого про0,8г (2,85ммоль) 3-гідрокси-3-(2-фенілпіридиндукту. Температура плавлення: 73-75°С. 5-іл)-1-азабіцикло[2,2,2]окгану та далі 10мл метан3,3. Етандіоат 5-[2-(3-метилфеніл)піридин-5сульфонової кислоти уводять у тригорлу колбу на іл)-1-азабіцикло[3,2,1]окт-3-ен (1:1). 25мл та суміш гріють до 180°С протягом 24 годин. 0,2г (0,75ммоль) 5-(2-бромпіридин-5-іл)-1Суміш виливають на лід та підлужують додаазабіцикло[3,2,1]окт-3-ену, 3мл толуолу, 0,7мл 2Μ ванням концентрованого водного розчину натрій водного розчину натрій карбонату, 0,147г гідроксиду, водну фазу екстрагують хлороформом, (1,05ммоль) 3-метилбензолборонової кислоти, а органічну фазу сушать та концентрують під зни0,042г (0,04ммоль) тетраженим тиском. Залишок очищають хроматографікіс(трифенілфосфіно)паладію та 0,7мл етанолу єю на колонці з силікагелем, елюючи 98/2/0,2 сууводять послідовно у тубу на 10 мл та суміш грімішшю хлороформу, метанолу та аміаку. ють при 100°С протягом 15 годин. Водну фазу виЦе дає 0,25г продукту, дигідробромід якого даляють декантуванням та сирий продукт екстраотримують додаванням 5 ,7 Μ розчину гідробромігують на колонці зі смолою Dowex® послідовною 7 77229 8 промивкою метанолом та далі хлороформом песиду, та водну фазу екстрагують хлороформом, і ред елюванням розчином аміаку. Залишок очисирий продукт очищають хроматографією на кощають хроматографією на колонці з силікагелем, лонці з силікагелем, елюючи сумішшю 80/20/2 елюючи сумішшю 90/10/1 хлороформу, метанолу хлороформу, метанолу та аміаку. Це дає 0,085г та аміаку. Це дає 0,167г продукту у формі масла, продукту, дигідробромід якого отримують додаяке розчиняють у 2мл ізопропанолу для утворення ванням 0,107мл 33% розчину гідробромідної кисетандіоату додаванням 0,051г (0,057ммоль) етанлоти в оцтовій кислоті. Це дає 0,097г кристалів. діонової кислоти у розчині в ізопропанолі. Це дає Температура плавлення: 98-100°С. 0,188г кристалізованого продукту. Температура Нижченаведена таблиця ілюструє хімічні струплавлення: 173-174°С. ктури та фізичні властивості деяких сполук винаПриклад 4 (сполука №26) ходу. У колонці "R"," (+)" показує правообертальГідробромід 5-[2-(3-флуорфеніл)піридин-5-іл)ний енантіомер, а" (-)" лівообертальний 1-азабіцикло[3,2,1]октан/2:1. енантіомер; сполуки, не представлені у цій колон0,18г (0,51ммоль) етандіоату 5-[2-(3ці, є рацематами. У колонці "=" число стосується флуорфеніл)піридин-5-іл)-1-азабіцикло[3,2,1]окт-3позиції подвійного зв'язку у випадку 1ену у розчині у 20мл метанолу уводять у посудину азабіциклооктену, а "-" стосується насиченого геПарра на 250мл, та додають 0,36г 10% паладію, тероцикл. У колонці "сіль","-" стосується сполуки у нанесеного на вугілля, та реакційну суміш далі формі основи, "НВr" стосується гідроброміду, а піддають тиску 0,42МПа водню з перемішуванням "окс." стосується оксалату. Показано відповідне при 45°С протягом 6 годин. Каталізатор збирають молярне співвідношення кислота:основа. У колонфільтруванням через діатомову землю, фільтрат ці "М(°С)"," (d)" стосується температури плавлення концентрують під зниженим тиском, залишок пез розкладанням. реносять у 10мл Η водного розчину натрій гідрок 9 77229 10 11 Сполуки представленого винаходу вивчені стосовно їх спорідненості до нікотинових рецеп 77229 12 торів, що містять субелемент 4 2, використовуючи способи, описані Anderson та Arneric у Eur. J. 13 77229 14 Pharmacol. (1994), 253 .261 та Hall et al. у Brain Res. (1993), 600, 127. 1нМ [3Н] -бунгаротоксину у кінцевому об'ємі Самців щурів Sprague Dawley масою від 150 до 250мкл 20мМ буферу ГЕПЕС, 0,05% поліетиле200г обезголовлюють та цілий мозок швидко виніміну. Реакцію зупиняють фільтруванням через даляють, гомогенізують у 15 об'ємах 0,32Μ розфільтри Whatman GF/C™, попередньо оброблені чину сахарози при 4°С та далі центрифугують поліетиленіміном протягом 3 годин 0,05% поліепри 1000g протягом 10 хвилин. Гранулу видалятиленіміну. Фільтри промивають двічі, кожного ють та супернатант центрифугують при 20000g разу 5мл буферу при 4°С, а радіоактивність на протягом 20 хвилин при 4°С. Гранулу збирають кожному фільтрі вимірюють рідинною сцинтиграта гомогенізують за допомогою млина Polytron™ фією. Неспецифічне зв'язування у присутності у 15 об'ємах бідистиляту при 4°С, далі центрифу1мкМ α-бунгаротоксину визначають; неспецифічгують при 8000g протягом 20 хвилин. Гранулу не зв'язування представляє приблизно 60% загавидаляють та супернатант і зовнішній шар (світльного зв'язування, зібраного на фільтрі. Процент лий шар кров'яного згустку) центрифугують при інгібування специфічного зв'язування [3Н] 40000g протягом 20 хвилин та гранулу збирають і бунгаротоксину визначають для кожної концентсуспендують у 15мл бідистиляту та центрифугурації дослідженої сполуки, а далі розраховують ють знов при 40000g перед зберіганням при величину ІК50, концентрацію сполуки, яка інгібує 80°С. На добу експерименту тканину повільно 50% специфічного зв'язування. розморожують та суспендують у 3 об'ємах буфеВеличини ІК50 для сполук винаходу з найвиру. 150мкл цієї суспензії мембран інкубують при щою спорідненістю складають від 0,005 до 4°С протягом 120 хвилин у присутності 100мкл 20мкМ. 1нМ [3Н]-цитизину у кінцевому об'ємі буферу Вищенаведені результати свідчать, що спо500мкл, у присутності або відсутності тестлуки винаходу є лігандами нікотинових рецептосполуки. Реакцію зупиняють фільтруванням черів. Деякі з них є селективними стосовно рецепрез фільтри Whatman GF/B™, попередньо оброторів, що містять субелементи 7, a мають блені поліетиле-німіном, фільтри промивають змішану природу стосовно рецепторів типу 4 2 двічі, кожного разу 5мл буферу при 4°С, та радіота 7. активність на фільтрі вимірюють рідинною сцинРезультати тестів підказують застосування тиграфією. Неспецифічне зв'язування у присутсполук при лікуванні чи попередженні розладів, ності 10мкМ (-)-нікотину визначають; пов'язаних з дисфункцією нікотинових рецептонеспецифічне зв'язування представляє від 75 до рів, зокрема на рівні центральної нервової систе85% загального зв'язування, зібраного на фільтрі. ми. Для кожної концентрації дослідженої сполуки Ці розлади включають шкідливі когнитивні визначають процент інгібування специфічного зміни, більш конкретно шкідливі зміни пам'яті, а 3 зв'язування [ Н]-цитизину, та далі розраховують також шкідливі зміни уваги, пов'язані з хворобою величину ІК50, концентрацію сполуки, яка інгібує Альцгеймера, патологічним старінням (асоційо50% специфічного зв'язування. вані з віком порушення пам'яті, ААМІ), синдромом Величина ІК50 для сполук винаходу з найвиПаркінсона, тризомією 21 (синдромом Дауна), щою спорідненістю складає від 0,01 до 10мкМ. алкогольним синдромом Козакова або мультіінСполуки винаходу також досліджували стофарктною деменцією, MDI. совно їх спорідненості до нікотинових рецепторів, Сполуки винаходу могли б також бути корисщо містять субелемент а7, використовуючи споними при лікуванні моторних розладів, що способи, описані Mark та Collins у J. Pharmacol. Exp. стерігають при хворобі Паркінсона або інших неTher. (1982), 22, 564 та Marks et al. у Моl. врологічних хворобах, як-то хорея Гентингтона, Pharmacol. (1986), 30, 427. Самців щурів OFA синдром Туретта, пізня дискінезія та гіперкінезія. масою від 150 до 200г обезголовлюють та цілий Сполуки винаходу можуть також здійснювати мозок швидко видаляють, гомогенізують у 15 цілюще або симптоматичне лікування гострих об'ємах 0,32Μ розчину сахарози при 4°С та далі нейродегенеративних патологій, як-то інсульти та центрифугують при 1000g протягом 10 хвилин. випадки церебральної гіпоксії, та хронічних нейГранулу видаляють та супернатант центрифугуродегенеративних патологій, як-то хвороба Альцють при 8000g протягом 20 хвилин при 4°С. Грагеймера та хвороба Паркінсона. їх можна застонулу збирають та гомогенізують за допомогою совувати у випадках психіатричної патології: млина Polytron™ у 15 об'ємах бідистиляту при шизофренія, депресія, тривожність, приступи 4°С, далі центрифугують при 8000g протягом 20 паніки, або нав'язлива або компульсивна поведіхвилин. Гранулу видаляють та супернатант і зовнка. нішній шар (світлий шар кров'яного згустку) Вони можуть попереджати симптоми внасліцентрифугують при 40000g протягом 20 хвилин, док відвикання від тютюну або спирту, або різних та гранулу збирають та суспендують у 15мл бідиречовин, що викликають звикання, як-то кокаїн, стиляту та центрифугують знов при 40000g перед ЛСД, конопля, бензодіазепіни. зберіганням при -80°С. На добу експерименту Відтак представлений винахід також стосутканину повільно розморожують та суспендують у ється фармацевтичних композицій, що містять 5 об'ємах буферу. 150мкл цієї суспензії мембран ефективну дозу щонайменше одної сполуки випопередньо інкубують при 37°С протягом 30 хвинаходу у формі основи або солі або фармацевлин у темряві у присутності або відсутності тесттично прийнятного сольвату, або у суміші, де сполуки. Мембрани далі інкубують протягом 60 прийнятно, з придатними ексципієнтами. хвилин при 37°С у темряві у присутності 50мкл Вибір вказаних ексципієнтів залежить від по 15 77229 16 трібного способу застосування та фармацевтичми наповнювачами. Желатинові капсули можуть ного формату. бути твердими або м'якими та можуть мати покФармацевтичні композиції винаходу можуть риття з тонкої плівки, так, щоб мати швидку, повідтак бути призначеними для перора-льного, довжену або затриману активність (наприклад, сублінгвального, підшкірного, внутрішньом'язоводля форми з ентеросолюбільним покриттям). го, внутрішньовенного, місцевого, інтратрахеальКомпозиція у формі сиропу чи еліксиру або ного, інтраназального, трансдермального, ректадля застосування у формі крапель може включального, або внутрішньоочного застосування. ти активну речовину у поєднанні з підсолоджуваПрикладами можливих унітарних форм зачем, переважно малокалорійним підсолоджувастосування є таблетки, желатинові капсули, грачем, метилпарабеном або пропілпарабеном, як нули, порошки, розчини або суспензії для пероантисептиком, ароматизатори та барвники. рального застосування або ін'єкцій, Водо-дисперсивні гранули та порошки мотрансдермальні пластири або супозиторії. Мазі, жуть включати активну речовину у суміші з дислосьйони та колірит можуть бути призначеними пергувальними або змочувальними засобами, для місцевого застосування. або диспергувальними засобами, як-то полівінілВказані унітарні форми дозують для забезпепіролідон, а також з підсолоджувачами та аромачення добового застосування від 0,01 до 20мг тизаторами. активної речовини на кг маси тіла, залежно від Для ректального застосування отримують суфармацевтичної дозованої форми. позиторії, отримані із зв'язуючими, які плавляться Для отримання таблетки до активної речовипри ректальній температурі, наприклад масло ни додають наступні матеріали, мікронізовані або какао або поліетиленгліколі. немікронізовані: фармацевтичний наповнювач, Для парентерального застосування отримуякий може складатися з розріджувачів, як-то лакють водні суспензії, ізотонічні розчини солі або тоза, крохмаль, або мікрокристалічна целюлоза, стерильні розчини для ін'єкцій, що містять фарабо композиційні ад'юванти, як-то зв'язуючі (полімакологічно сумісні диспергувальні засоби та/або вінілпіролідон, гідроксипропілметилцелюлоза, змочувальні засоби, наприклад пропіленгліколь тощо), ковзні засоби, як-то оксид силіцію, змащуабо бутиленгліколь. вачі, як-то магній стеарат, стеаринова кислота, Активну речовину можна також формувати як гліцерин-трибегенат, натрій стеарилфумарат. мікрокапсули, як варіант, з одним або більше Змочувальні або поверхнево-активні засоби, якнаповнювачами або адитивами або крім того з то натрій лаурилсульфат, можна додавати також. полімерною матрицею або з циклодекстрином Можливими способами отримання є безпо(трансдермальні пластири або форми з подовжесереднє таблетування, сухе гранулювання, волоним вивільненням). ге гранулювання або гаряче плавлення. Таблетки Місцеві композиції винаходу включають семожуть бути непокритими, покритими цукром, редовище, сумісне зі шкірою. їх можна забезпенаприклад сахарозою, або покритими різними чити зокрема у формі водних, спиртових або вополімерами чи іншими прийнятними матеріаладно-спиртових розчинів, гелів, емульсій вода-уми, їх можна створювати для забезпечення швимаслі або масло-у-воді, що мають вигляд крему дкого, затриманого або подовженого вивільнення або гелю, мікроемульсій чи аерозолів, або у фоактивної речовини за допомогою полімерних мармі везикулярних дисперсій, що містять іонні триць або конкретних полімерів, застосовуваних та/або неіонні ліпіди. Ці фармацевтично дозовані у покритті. форми отримують звичайними способами. Для отримання желатинових капсул, активну Кінцево, фармацевтичні композиції винаходу речовину змішують з сухими фармацевтичними можуть включати на додаток до сполук загальної наповнювачами (просте змішування, сухе або формули (І), інші активні речовини, які можна вологе гранулювання, або гаряче плавлення), використовувати при лікуванні вищезазначених або рідкими або напівтвердими фармацевтичнирозладів та хвороби. Комп’ютерна верстка Л. Купенко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійською5-(pyridinyl-3-yl)-1-azabicyclo[3,2,1]octane derivatives and pharmaceutical composition
Автори англійськоюLeclerc Odile
Назва патенту російськоюПроизводные 5-(пиридин-3-ил)-1-азабицикло[3,2,1]октана, фармацевтическая композиция на их основе
Автори російськоюЛеклерк Одиль
МПК / Мітки
МПК: A61P 25/28, A61P 25/14, A61P 25/18, A61P 25/16, C07D 471/08, A61K 31/4709, A61K 31/4545, A61P 25/30, A61K 31/444, A61K 31/506, A61P 25/24, A61P 25/00, A61P 25/22
Мітки: похідні, основі, фармацевтична, композиція, 5-(піридин-3-іл)-1-азабіцикло[3,2,1]октану
Код посилання
<a href="https://ua.patents.su/8-77229-pokhidni-5-piridin-3-il-1-azabiciklo321oktanu-farmacevtichna-kompoziciya-na-kh-osnovi.html" target="_blank" rel="follow" title="База патентів України">Похідні 5-(піридин-3-іл)-1-азабіцикло[3,2,1]октану, фармацевтична композиція на їх основі</a>
Наступний патент: Пристрій для кріплення заземлення
Випадковий патент: Спучувана вогнезахисна епоксидна композиція












