Спосіб одержання феноксизаміщених 2-піридинових сполук
Номер патенту: 78333
Опубліковано: 15.03.2007
Автори: Тохіама Йосітомо, Фурукава Такасі, Мацуо Норітада
Формула / Реферат
1. Спосіб одержання феноксизаміщених 2-піридинових сполук формули (2):
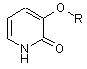 , (2)
, (2)
де R визначений нижче,
який включає взаємодію амідної сполуки формули (1):
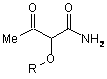 , (1)
, (1)
де R являє собою необов'язково заміщений феніл
щонайменше з одною сполукою, вибраною з групи, що включає 3-алкоксипропеналь формули (3), 3,3-діалкоксипропаналь формули (4), 1,3,3-триалкокси-1-пропен формули (5), 1,1,3,3-тетраалкоксипропан формули (6) і малоновий альдегід:
![]() (3)
(3) ![]() (4)
(4)
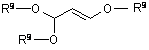 (5)
(5) 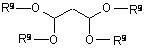 (6),
(6),
де R являє собою алкіл (наприклад, С1-С3алкіл, такий як метокси, етокси і т.п.);
в присутності протонної кислоти.
2. Спосіб за п. 1, де щонайменше одна сполука являє собою 3-алкоксипропеналь формули (3) або 1,1,3,3-тетраалкоксипропан формули (6).
3. Спосіб за п. 1, де щонайменше одна сполука являє собою 3-метоксипропеналь або 1,1,3,3-тетраметоксипропан.
4. Спосіб за п. 1, де протонна кислота являє собою галогенводень, фосфорну кислоту, поліфосфорну кислоту, сірчану кислоту, тригалогеноцтову кислоту або сульфонову кислоту.
5. Спосіб за п. 1, де R, в амідній сполуці формули (1) і в піридоновій сполуці формули (2), являє собою радикал наступної формули:
 ,
,
де R1 являє собою атом галогену або нітро і R2 являє собою водень або атом галогену.
Текст
1. Спосіб одержання феноксизаміщених 2піридинових сполук формули (2): O R 2 3 78333 4 отримані взаємодією 3-оксобутанаміду з різними кетонами. Зокрема, 4,6-диметил-2-піридон отриманий взаємодією 3-оксобутанаміду з ацетоном в присутності поліфосфорної кислоти; 3-ацетил-4,6диметил-2-піридон отриманий взаємодією 3оксобутанаміду з пентан-2,4-діоном в присутності хлористого водню або поліфосфорної кислоти; і 5де R9 являє собою алкіл (наприклад, С1етоксикарбоніл-4,6-диметил-2-піридон отриманий С3алкіл, такий як метокси, етокси і т.п.); взаємодією 3-оксобутанаміду з етилацетатом в в присутності протонної кислоти. присутності поліфосфорної кислоти [Chem. Pharm. Крім того, в даному винаході пропонується таBull. 28(7) 2244-2247 (1989), J. Chem. Soc. (3), кож спосіб отримання піридонової сполуки форму1967, 1836-1839]. ли (В): де R1 і R2 визначені нижче; з використанням амідної сполуки формули (А): Автори даного винаходу інтенсивно вивчили спосіб отримання 2-піридонової сполуки, заміщеної в положенні 3 необов'язково заміщеним фенокси, яка застосовна як проміжний продукт для отримання медичного і сільськогосподарського препарату, зокрема гербіцидної сполуки. У результаті автори встановили, що 3-фенокси-2-піридон, що має один замісник в положенні 3, може бути отриманий взаємодією 2-фенокси-3оксобутанаміду, в якому фенокси може бути заміщеним, з певним похідним малонового альдегіду або з малоновим альдегідом, що складає даний винахід. У даному винаході пропонується спосіб (який надалі називається як даний спосіб) отримання піридонової сполуки формули (2) (яка надалі називається як дана піридонова сполука): де R визначений нижче; який включає взаємодію амідної сполуки формули (1) (яка надалі називається як дана амідна сполука): де R1 являє собою атом галогену або нітрогруп у і R2 являє собою атом водню або атом галогену; як дану амідну сполуку. Замісник в необов'язково заміщеному фенокси даної амідної сполуки, яка є вихідною сполукою для даного способу, і дана піридонова сполука включають, наприклад, атом галогену (тобто атом фтор у, атом хлору, атом брому і т.п.); алкіл (наприклад, С1-С4алкіл, такий як метил, етил, пропіл, ізопропіл т.п.); алкокси (наприклад, С1-С4алкокси, такий як метокси, етокси, пропокси, ізопропокси і т.п.); галогеналкіл (наприклад, трифторметил, пентафторетил); нітро; ціано; і 5-6-членний гетероциклічний радикал (наприклад, 1,2,3,6-тетрагідро2,6-диоксопіримідин-1-іл, 1,6-дигідро-6оксопіридазин-1-іл і т.п.). Необов'язково заміщений фенокси включає, наприклад, фенокси і фенокси, показані на схемі: де R1 і R2 визначені вище. Дана амідна сполука включає, наприклад, сполуку, показану на схемі: де R являє собою необов'язково заміщений феніл; щонайменше, з однією сполукою (що надалі іменується як дане похідне малонового альдегіду), вибраною з групи, що включає 3алкоксипропеналь формули (3), 3,3діалкоксипропаналь формули (4), 1,3,3триалкокси-1-пропен формули (5), 1,1,3,3тетраалкоксипропан формули (6) і малоновий альдегід: Дане похідне малонового альдегіду являє собою малоновий альдегід або звичайні продукти конденсації малонового альдегіду і спирту, серед яких, зокрема, щонайменше, одне похідне малонового альдегіду вибране з групи, що включає 3алкоксипропеналь формули (3), 3,3діалкоксипропаналь формули (4), 1,3,3 5 78333 6 триалкокси-1-пропен формули (5), 1,1,3,3переважно, дану амідну сполуку і даний малонотетраалкоксипропан "формули (6). 3вий альдегід потрібно додавати поступово відповіАлкоксипропеналь формули (3) включає, напридно до проходження реакції. клад, 3-метоксипропеналь і 3-етоксипропеналь. Хід реакції можна контролювати, наприклад, 3,3-Діалкоксипропаналь формули (4) включає, відбираючи пробу з реакційної суміші і досліджуюнаприклад, 3,3-диметоксипропаналь і 3,3чи її хроматографічно (наприклад, за допомогою диетоксипропаналь. 1,3,3-Триалкокси-1-пропен тонкошарової хроматографії, високоефективної формули (5) включає, наприклад, 1, 3,3рідинної хроматографії і т.п.) для аналізу залишкотриметокси-1-пропен і 1,3,3-триетокси-і-пропен. вих кількостей амідної сполуки формули (1) в реа1,1,3,3-Тетраалкоксипропан формули (6) включає, кційній суміші. наприклад, 1,1,3,3-тетраметоксипропан і 1,1,3,3Дана піридонова сполука може бути виділена тетраетоксипропан. з реакційної суміші після завершення реакції за Для даного способу 1,1,3,3допомогою наступних процедур, які включають: тетраалкоксипропан формули (6) є переважною 1) Розбавлення реакційної суміші після заверсполукою як похідне малонового альдегіду внаслішення реакції гідрофобним органічним розчиннидок його доступності і іншого. ком; промивання суміші насиченим водним розчиПротонна кислота, призначена для застосуном хлориду натрію, насиченим водним розчином вання за даним способом, являє собою сполуку, бікарбонату натрію або т.п.; сушіння отриманого що володіє сильною тенденцією віддавати протон, органічного шару; і концентрування органічного відповідно до теорії кислот і основ Бренстеда, осшару для повного видалення розчинника. нованої на наданні і акцептуванні протона. Зокре2) Розбавлення реакційної суміші після заверма, протонна кислота включає галогеноводні (нашення реакції гідрофобним органічним розчинниприклад, хлористий водень, бромистий водень і ком; промивання суміші насиченим водним розчит.п.), фосфорну кислоту, поліфосфорну кислоту, ном хлориду натрію, насиченим водним розчином сірчану кислоту, тригалогеноцтову кислоту (наприбікарбонату натрію або т.п.; часткове концентруклад, трихлороцтову кислоту, трифтороцтову кисвання органічного шару при температурі від 80 до лоту і т.п.), сульфонову кислоту (наприклад, хлор120°С і охолоджування; фільтрування і сушіння сульфонову кислоту, метансульфонову кислоту, потриманої твердої речовини. толуолсульфонову кислоту, трифторметансуль3) Часткове концентрування реакційної суміші фонову кислоту і т.п.) і їх суміші, причому перевапісля завершення реакції; вилиття реакційної сужно протонні кислоти мають значення рКа (консміші в суміш води і гідрофільного органічного розтанта дисоціації кислоти у воді), меншу або рівну чинника, взятої в будь-якому співвідношенні; філь2,5. трування і сушіння отриманої твердої речовини. Реакція за даним способом може бути прове4) Виливання реакційної суміші після завердена в розчиннику. Розчинник, призначений для шення реакції у воду; доведення рН водного шару застосування, включає, наприклад, ароматичні приблизно до нейтральних значень; видалення вуглеводні, такі як толуол, ксилол і т.п.; галогеноорганічного розчинника азеотропною перегонкою; і вані ароматичні вуглеводні, такі як хлорбензол, сушіння отриманої твердої речовини. дихлорбензол, бензотрифторид і т.п.; галогеновані Гідрофобний органічний розчинник, призначеаліфатичні вуглеводні, такі як хлороформ, 1,2ний для застосування в процедурі подальшої обдихлоретан і т.п.; спирти, такі як гексафторізопроробки, включає, наприклад, ефіри, такі як етилапанол і т.п.; і їх суміші. цетат і т.п.; галогеновані аліфатичні вуглеводні, У реакції звичайно використовують від 1 до такі як хлороформ і т.п.; галогеновані ароматичні 10моль даного похідного, малонового альдегіду і вуглеводні, такі як хлорбензол, дихлорбензол, кількість кислоти від каталітичної до надмірної бензотрифторид і т.п.; кетони, такі як метилізобу(наприклад, від 0,1 до 1000моль, переважно, від 1 тилкетон і т.п.; і їх суміші. Гідрофільний органічний до 10моль), по відношенню до 1моль даної амідної розчинник включає спирти, такі як метанол, етасполуки. нол, ізопропіловий спирт, трет-бутиловий спирт і Температура проведення реакції звичайно т.п. знаходиться в інтервалі від 0 до 150°С, переважВиділена дана піридонова сполука може бути но, від 20 до 100°С, час реакції звичайно складає очищена хроматографічно, перекристалізацією, від 0,5 до 72 годин, причому вказані умови реакції промиванням невеликою кількістю розчинника і залежать від кількості і типів протонних кислот, що т.п. застосовуються. Дана амідна сполука, призначена для застосуРеакцію проводять при доданні даного похідвання в даному способі, може бути отримана, наного амідної сполуки і даного похідного малоновоприклад, взаємодією фенольної сполуки формули го альдегіду до протонної кислоти або до протон(7) з амідною сполукою формули (8) (наприклад, з ної кислоти, розбавленої вищезазначеним 2-хлор-3-оксобутанамідом): розчинником. У цьому випадку допустимо, що вся протонна кислота застосовується відразу на початку реакції; і частина протонної кислоти застосовується на початку реакції, а залишок додають по ходу проведення реакції. Дана амідна сполука і де X являє собою атом галогену, a R визначеданий малоновий альдегід можуть бути додані ний вище. відразу в протонну кислоту або в протонну кислоДану реакцію звичайно проводять в розчинниту, розбавлену згаданим вище розчинником; але, ку в присутності основи. Розчинник, призначений 7 78333 8 для застосування, включає, наприклад, ароматич0,05 по відношенню до 1моль сполуки формули ні вуглеводні, такі як толуол, ксилол і т.п.; аміди (В). Ці кількості можуть бути змінені відповідно до кислот, такі як Ν,Ν-диметилформамід і т.п. Основа, умов реакції. Сіль родію (II), призначена для запризначена для застосування, включає, напристосування, включає, наприклад, димер трифтоклад, неорганічні основи, такі як карбонат натрію, рацетату родію (II). карбонат калію і т.п.; третинні аміни, такі як триПісля завершення реакції піридинова сполука етиламін, трибутиламін і т.п. формули (D) може бути виділена з реакційної суУ реакції звичайно використовують від 1 міші подальшою обробкою, такою як фільтрування до 1,5моль амідної сполуки формули (8) і від 1 до реакційної суміші і концентрування фільтрату; 3моль основи по відношенню до 1моль фенольної розбавлення реакційної суміші органічним розчинсполуки формули (7). ником і відділення від водного розчину бікарбонату Температура проведення реакції звичайно натрію; сушіння і концентрування отриманого орзнаходиться в інтервалі від 20 до 150°С, час реакганічного шару і т.п. Виділена піридинова сполука ції звичайно складає від 0,5 до 24 годин. може бути очищена хроматографічно і т.п. Дана амідна сполука може бути виділена з реДаний винахід далі буде проілюстрований наакційної суміші після завершення реакції, наприступними прикладами отримання і т.п.; однак даклад, розбавленням реакційної суміші органічним ний винахід не обмежується даними прикладами. розчинником, промиванням суміші насиченим водКрім того, в наступному описі слово «частина» ним розчином хлориду натрію, насиченим водним означає масову частину. розчином бікарбонату натрію або т.п., сушінням і Приклад отримання 1 концентруванням отриманого органічного шару. В атмосфері азоту 57мг 3-оксо-2Виділена амідна сполука може бути очи щена хрофеноксибутанаміду і 49мг 1,1,3,3матографічно, перекристалізацією. тетраметоксипропану додавали до 2мл 25% розДане похідне малонового альдегіду, призначину бромистого водню в оцтовій кислоті, суміш чене для застосування в даному способі, являє перемішували при 50°С протягом 2,5 годин і при собою відому сполуку або може бути отримано 100°С протягом 2 годин. У реакційну суміш додаспособом, описаним в літературі. вали 80мл етилацетату і 30мл насиченого водного Як публікації вказані нижченаведені матеріарозчину хлориду натрію і суміш розділяли. Органіли. чний шар промивали послідовно один раз 30мл Japanese Publication of unexamined application насиченого водного розчину хлориду натрію, двічі S52-97905, для 3-алкоксипропеналю формули (3); 20мл насиченого водного розчину бікарбонату J. Chem. Soc, Chem. Commun., (20) 1421-1422 натрію і один раз 30мл насиченого водного розчи(1991), для 3,3-діалкоксипропаналю формули (4); ну хлориду натрію; сушили над безводним сульTetrahedron Lett., 29 (29) 3597-3598 (1988), для фатом магнію і концентрували. Залишок очищали 1,3,3-триалкокси-1-пропену формули (5); колонковою хроматографією на силікагелі (елюJ. Org. Chem., 53 (13) 2920-2925 (1988), для ент: метанол/етилацетат = 5/95) і отримували 36мг 1,1,3,3-тетраалкоксипропану формули (6); 3-фенокси-2-піридону. 1H-ЯМР (395,75МГц, CDCl3) J. Org. Chem., 50 3585-3592 (1985), для малоδ (ч/млн.): 6,18 (т, J=6,9Гц, 1Н), 6,92 (дд, J=7,5, нового альдегіду. 1,7Гц, 1H), 7,08 (шир.д, J=7,8Гц, 2H), 7,15 (шир.т, Дана піридонова сполука, отримана даним J=7,5Гц, 1Н), 7,19 (дд, J=6,7, 1,7Гц, 1Н), 7,36 способом, застосовна як проміжний продукт для (шир.т, J=7,5Гц, 2Н), 13,7 (шир.с, 1Н). медичного і сільськогосподарського продукту. НаПриклад отримання 2 приклад, піридинова сполука формули (D) може В атмосфері азоту 108мг амідної сполуки фобути отримана взаємодією сполуки формули (В) з рмули (F): ефірною сполукою діазооцтової кислоти формули (С) в присутності солі родію (II), трифториду бору, п-толуолсуль фонової кислоти або т.п. Отримана піридинова сполука формули (D) застосовується як активний інгредієнт гербіцидної композиції [Публікація європейської патентної заявки ЕРІ 122244А1]. де R3 являє собою С 1-С6алкокси. Реакцію в присутності солі родію (II) звичайно проводять в розчиннику, при температурі від 60 до 120°С і тривалість реакції від хвилини до 72 годин. Розчинник, призначений для застосування, включає, наприклад, галогеновані вуглеводні, такі як 1,2-дихлоретан і т.п. Звичайно, кількість діазоацетатної сполуки формули (С) складає від 0,5 до 2моль і кількість солі родію (II) складає від 0,01 до і 53мг 1,1,3,3-тетраметоксипропану додавали до 2мл 85% водного розчину фосфорної кислоти і суміш перемішували при 50°С протягом 9 годин. Реакційну суміш залишали охолоджуватися до кімнатної температури. У реакційну суміш додавали 80мл етилацетату і насиченого водного розчину хлориду натрію і суміш розділяли. Органічний шар промивали послідовно один раз 30мл насиченого водного розчину хлориду натрію, двічі 20мл насиченого водного розчину бікарбонату натрію і один раз 30мл насиченого водного розчину хлориду натрію; сушили над безводним сульфатом магнію і концентрували. Залишок очищали колонковою хроматографією на силікагелі (елюент: метанол/етилацетат = 5/95) і отримували 30мг піридо 9 нової сполуки формули (G): 78333 10 шок очищали колонковою хроматографією на силікагелі (елюент: метанол/етилацетат = 5/95) і отримували 96мг піридонової сполуки формули (G). Приклад отримання 6 В атмосфері азоту 103мг амідної сполуки формули (F) і 50мг 1,1,3,3-тетраметоксипропану до1 H- ЯМР (395,75МГц, CDCl3) δ (ч/млн.): 3,52 (с, давали до 1мл 48% бромистоводневої кислоти, суміш перемішували при 80°С протягом 4 годин. 3Н), 6,21 (т, J=6,9Гц, 1Н), 6,31 (с, 1H), 6,95 (с, 1H), 7,00 (дд, J=7,3, 1,5Гц, 1H), 7,26 (дд, J=6,5, 1,7Гц, Реакційну суміш охолоджували до кімнатної тем1Н), 7,38 (д, J=9,1Гц, 1H), 13,4 (шир.с, 1Н). ператури. У реакційну суміш додавали 80мл етиПриклад отримання 3 лацетату і 30мл насиченого водного розчину хлоВ атмосфері азоту 100мг амідної сполуки фориду натрію і суміш розділяли. Органічний шар промивали послідовно один раз 30мл насиченого рмули (F) і 49мг 1,1,3,3-тетраметоксипропану додавали до 1,4г поліфосфорної кислоти і суміш певодного розчину хлориду натрію, двічі 20мл насиремішували при 100°С протягом 3 годин. ченого водного розчину бікарбонату натрію і один Реакційну суміш залишали охолоджуватися до раз 30мл насиченого водного розчину хлориду кімнатної температури. У реакційну суміш додаванатрію; сушили над безводним сульфатом магнію і концентрували. Залишок очищали колонковою ли 150мл етилацетату і 10мл насиченого водного розчину хлориду натрію і суміш розділяли. Органіхроматографією на силікагелі (елюент: метачний шар промивали послідовно один раз 50мл нол/етилацетат = 5/95) і отримували 31мг піридонасиченого водного розчину хлориду натрію, двічі нової сполуки формули (G). 50мл насиченого водного розчину бікарбонату Приклад отримання 7 В атмосфері азоту 104мг амідної сполуки фонатрію і один раз 35мл насиченого водного розчину хлориду натрію; сушили над безводним сульрмули (F) і 51мг 1,1,3,3-тетраметоксипропану дофатом магнію і концентрували. Залишок очищали давали до 2мл 1моль/л хлористого водню в оцтоколонковою хроматографією на силікагелі (елювій кислоті, суміш перемішували при 80°С ент: метанол/етилацетат = 5/95) і отримували 38мг протягом 1,5 годин і при 100°С протягом 6 годин. Реакційну суміш охолоджували до кімнатної темпіридонової сполуки формули (G). Приклад отримання 4 ператури. У реакційну суміш додавали 80мл етиВ атмосфері азоту 101мг амідної сполуки фолацетату і 30мл насиченого водного розчину хлормули (F) і 38мг 1,1,3,3-тетраметоксипропану дориду натрію і суміш розділяли. Органічний шар давали до 2мл трифтороцтової кислоти, суміш промивали послідовно один раз 30мл насиченого водного розчину хлориду натрію, двічі 20мл насиперемішували при 70°С протягом 9 годин. У вказаний період часу в суміш додавали 38мг 1,1,3,3ченого водного розчину бікарбонату натрію і один тетраметоксипропану кожні 1,5 години (загальна раз 30мл насиченого водного розчину хлориду кількість 1,1,3,3-тетраметоксипропану становила натрію; сушили над безводним сульфатом магнію і 228мг). Реакційну суміш залишали охолоджуватиконцентрували. Залишок очищали колонковою хроматографією на силікагелі (елюент: метася до кімнатної температури. У реакційну суміш додавали 80мл етилацетату і 30мл насиченого нол/етилацетат = 5/95) і отримували 34мг піридоводного розчину хлориду натрію і суміш розділяли. нової сполуки формули (G). Органічний шар промивали послідовно один раз Приклад отримання 8 30мл насиченого водного розчину хлориду натрію, В атмосфері азоту 109мг амідної сполуки фодвічі 20мл насиченого водного розчину бікарбонармули (F) і 53мг 1,1,3,3-тетраметоксипропану доту натрію і один раз 30мл насиченого водного роздавали до 0,89г трихлороцтової кислоти, суміш чину хлориду натрію; сушили над безводним суперемішували при 100°С протягом 6 годин. Реакльфатом магнію і концентрували. Залишок ційну суміш охолоджували до кімнатної темпераочищали колонковою хроматографією на силікагетури. У реакційну суміш додавали 80мл етилацелі (елюент: метанол/етилацетат = 5/95) і отримутату і 30мл насиченого водного розчину хлориду вали 44мг піридонової сполуки формули (G). натрію і суміш розділяли. Органічний шар промиПриклад отримання 5 вали послідовно один раз 30мл насиченого водноВ атмосфері азоту 102мг амідної сполуки фого розчину хлориду натрію, двічі 20мл насиченого рмули (F) і 50мг 1,1,3,3-тетраметоксипропану доводного розчину бікарбонату натрію і один раз давали до 2мл 12,5% розчину бромистого водню в 30мл насиченого водного розчину хлориду натрію; оцтовій кислоті, суміш перемішували при 50°С сушили над безводним сульфатом магнію і концепротягом 2,5 годин і при 80°Спротягом 4 годин. нтрували. Залишок очищали колонковою хроматоРеакційну суміш охолоджували до кімнатної темграфією на силікагелі (елюент: метаператури. У реакційну суміш додавали 80мл етинол/етилацетат = 5/95) і отримували 24мг лацетату і 30мл насиченого водного розчину хлопіридонової сполуки формули (G). риду натрію і суміш розділяли. Приклад отримання 9 Органічний шар промивали послідовно один В атмосфері азоту 119мг амідної сполуки фораз 30мл насиченого водного розчину хлориду рмули (F) і 34мг 3-метоксипропеналю додавали до натрію, двічі 20мл насиченого водного розчину 2мл 12,5% розчину бромистого водню в оцтовій бікарбонату натрію і один раз 30мл насиченого кислоті, суміш перемішували при 80°С протягом 2 водного розчину хлориду натрію; сушили над безгодин. Реакційну суміш охолоджували до кімнатної водним сульфатом магнію і концентрували. Залитемператури. У реакційну суміш додавали 80мл 11 78333 12 етилацетату і 30мл насиченого водного розчину бікарбонату натрію і один раз 1200 частинами нахлориду натрію і суміш розділяли. Органічний шар сиченого водного розчину хлориду натрію; сушили промивали послідовно один раз 30мл насиченого над безводним сульфатом натрію і концентрували. водного розчину хлориду натрію, двічі 20мл насиЗалишок очищали колонковою хроматографією на ченого водного розчину бікарбонату натрію і один силікагелі (елюент: метанол/етилацетат = 5/95) і раз 30мл насиченого водного розчину хлориду отримували 65 частин піридонової сполуки форнатрію; сушили над безводним сульфатом магнію і мули (G). концентрували. Залишок очищали колонковою Приклад отримання 13 хроматографією на силікагелі (елюент: метаВ атмосфері азоту суміш 48 частин амідної нол/етилацетат = 5/95) і отримували 100мг піридосполуки формули (F), 21 частини 1,1,3,3нової сполуки формули (G). тетраметоксипропану, 33 частин метансульфоноПриклад отримання 10 вої кислоти і 1037 частин хлорбензолу перемішуВ атмосфері азоту суміш 117 частин амідної вали при 80°С протягом 1 години. Реакційну суміш сполуки формули (F), 57 частин 1,1,3,3охолоджували до кімнатної температури. У реактетраметоксипропану і 211 частин оцтової кислоти ційну суміш додавали 2250 частин етилацетату і додавали до 628 частин 30% розчину бромистого 2500 частин крижаної води і суміш розділяли. Орводню в оцтовій кислоті, який заздалегідь охологанічний шар послідовно промивали двічі 1200 джували до 10-15°С, і суміш перемішували при частинами води, один раз 1200 частинами насиче50°С протягом 8 годин. Реакційну суміш охолоного водного розчину бікарбонату натрію і один джували до кімнатної температури і концентрувараз 1200 частинами насиченого водного розчину ли при зниженому тиску до 240 масових частин. хлориду натрію; сушили над безводним сульфаСуміш залишку і 69 частин метанолу додавали по том натрію і концентрували. Залишок очищали краплях до суміші 1160 частин крижаної води і 316 колонковою хроматографією на силікагелі (елючастин метанолу при 0-3°С. Доводили рН суміші ент: метанол/етилацетат = 5/95) і отримували 34 до 7,3 за допомогою 40% водного розчину гідрочастини піридонової сполуки формули (G). ксиду натрію і насиченого водного розчину бікарПриклад отримання 14 бонату натрію. Суміш перемішували при кімнатній В атмосфері азоту суміш 112 частин амідної температурі півдня і потім фільтрували. Відфільтсполуки формули (F), 49 частин 1,1,3,3рований осад промивали три рази 240 частинами тетраметоксипропану, 78 частин метансульфоноводи і сушили при зниженому тиску. До сухого вої кислоти і 1894 частин толуолу перемішували осаду додавали 343 частини метанолу, вміст пепри 80°С протягом 2 годин. Реакційну суміш о хоремішували протягом 1 години при нагріванні із лоджували до кімнатної температури. У реакційну зворотним холодильником, охолоджували до кімсуміш додавали 2250 частин етилацетату і 2500 натної температури і фільтрували. Відфільтровачастин крижаної води і суміш розділяли. Органічний осад промивали 114 частинами метанолу, ний шар послідовно промивали двічі 1200 частисушили при зниженому тиску і отримували 96 часнами води, один раз 1200 частинами насиченого тин піридонової сполуки формули (G) (вміст: 94%). водного розчину бікарбонату натрію і один раз Приклад отримання 11 1200 частинами насиченого водного розчину хлоВ атмосфері азоту суміш 48 частин амідної риду натрію; сушили над безводним сульфатом сполуки формули (F), 21 частини 1,1,3,3натрію і концентрували. Залишок очищали колонтетраметоксипропану, 36 частин сірчаної кислоти і ковою хроматографією на силікагелі (елюент: ме1037 частин хлорбензолу перемішували при 80°С танол/етилацетат = 5/95) і отримували 85 частин протягом 1 години. Реакційну суміш охолоджували піридонової сполуки формули (G). до кімнатної температури. У реакційну суміш доПриклад отримання 15 давали 2250 частин етилацетату і 2500 частин В атмосфері азоту суміш 96 частин амідної крижаної води і суміш розділяли. Органічний шар сполуки формули (F), 42 частин 1,1,3,3послідовно промивали двічі 1200 частинами води, тетраметоксипропану, 55 частин хлорсульфонової один раз 1200 частинами насиченого водного розкислоти і 746 частин хлороформу перемішували чину бікарбонату натрію і один раз 1200 частинами при 60°С протягом 2,5 годин. Реакційну суміш охонасиченого водного розчину хлориду натрію; сулоджували до кімнатної температури. У реакційну шили над безводним сульфатом натрію і концентсуміш додавали 2255 частин етилацетату, 500 рували. Залишок очищали колонковою хроматогчастин крижаної води і 1200 частин насиченого рафією на силікагелі (елюент: метанол/етилацетат водного розчину бікарбонату натрію і суміш розді= 5/95) і отримували 32 частини піридонової споляли. Органічний шар послідовно промивали двічі луки формули (G). 1200 частинами води, один раз 1200 частинами Приклад отримання 12 насиченого водного розчину бікарбонату натрію і В атмосфері азоту суміш 96 частин амідної один раз 1200 частинами насиченого водного розсполуки формули (F), 42 частин 1,1,3,3чину хлориду натрію; сушили над безводним сутетраметоксипропану, 49 частин сірчаної кислоти і льфатом натрію і концентрували. Залишок очища1618 частин толуолу перемішували при 60°С проли колонковою хроматографією на силікагелі тягом 3 годин. Реакційну суміш охолоджували до (елюент: метанол/етилацетат = 5/95) і отримували кімнатної температури. У реакційну суміш додава73 частини піридонової сполуки формули (G). ли 2250 частин етилацетату і 2500 частин крижаПриклад отримання 16 ної води і суміш розділяли. Органічний шар посліВ атмосфері азоту суміш 96 частин амідної довно промивали двічі 1200 частинами води, один сполуки формули (F), 42 частин 1,1,3,3раз 1200 частинами насиченого водного розчину тетраметоксипропану, 81 частини хлорсульфоно 13 78333 14 вої кислоти і 2070 частин хлорбензолу перемішуоксобутанаміду, 20,3г сполуки формули (Η): вали при 80°С протягом 2 годин. Реакційну суміш охолоджували до кімнатної температури. У реакційну суміш додавали 2250 частин етилацетату і 2500 частин крижаної води і суміш розділяли. Органічний шар послідовно промивали двічі 1200 частинами води, один раз 1200 частинами насиченого водного розчину бікарбонату натрію і один раз 1200 частинами насиченого водного розчину і 16,7мл триетиламіну додавали до 120мл Ν,Νхлориду натрію; сушили над безводним сульфадиметилформаміду, суміш перемішували при 70°С том натрію і концентрували. Залишок очищали протягом 1 години і при 100°С протягом 4,5 годин. колонковою хроматографією на силікагелі (елюРеакційну суміш залишали охолоджуватися до ент: метанол/етилацетат = 5/95) і отримували 73 кімнатної температури. У реакційну суміш додавачастини піридонової сполуки формули (G). ли 200мл етилацетату і 30мл насиченого водного Приклад отримання 17 розчину хлориду натрію і суміш розділяли. ОрганіВ атмосфері азоту суміш 48 частин амідної чний шар промивали послідовно один раз 30мл сполуки формули (F), 21 частини 1,1,3,3насиченого водного розчину хлориду натрію, двічі тетраметоксипропану, 41 частини моногідрату п30мл хлористоводневої кислоти (1моль/л) і один толуолсульфонової кислоти і 1037 частин хлорбераз 30мл насиченого водного розчину хлориду нзолу перемішували при 80°С протягом 2 годин. натрію; сушили над безводним сульфатом магнію і Реакційну суміш охолоджували до кімнатної темконцентрували. Залишок очищали колонковою ператури. У реакційну суміш додавали 2250 часхроматографією на силікагелі (елюент: гектин етилацетату і 2500 частин крижаної води і сусан/етилацетат = 6/4) і отримували 17,9г сполуки міш розділяли. Органічний шар послідовно формули (F). промивали двічі 1200 частинами води, один раз Сполука формули (F) 1200 частинами насиченого водного розчину бікат.пл.: 192,3°С рбонату натрію і один раз 1200 частинами насичеНаступний спосіб отримання гербіцидної споного водного розчину хлориду натрію; сушили над луки із застосуванням сполуки формули (G) як безводним сульфатом натрію і концентрували. вихідної сполуки, отриманої в довідковому приЗалишок очищали колонковою хроматографією на кладі, представленому вище, буде проілюстровасилікагелі (елюент: метанол/етилацетат = 5/95) і ний довідковим прикладом. отримували 32 частини піридонової сполуки форДовідковий приклад 3 мули (G). У 15мл дихлоретану додавали 0,5г сполуки Наступний спосіб отримання вихідної сполуки, формули (G) і 8мг димеру трифторацетату родію що використовується в Прикладі отримання, пред(II), потім до суміші додавали по краплях 0,15г меставленому вище, буде проілюстрований довідкотилдіазоацетату при 80°С протягом 3 годин, після вим прикладом. чого суміш перемішували при 80°С протягом 1 Довідковий приклад 1 години і концентрували. Залишок очищали колонВ атмосфері азоту 1,57г 2-хлор-3ковою хроматографією на силікагелі (елюент: гекоксобутиламіду, 1,08г фенолу і 1,7мл триетиламісан/етилацетат = 3/1-0/1) і отримували 0,18г вихідну додавали до 20мл Ν,Ν-диметилформаміду, ної сполуки формули (G), що не прореагувала, і суміш перемішували при 80°С протягом 6 годин і 0,34г 3-(2-хлор-4-фтор-5-[3-метил-2,6-діоксо-4при 100°С протягом 4 годин. Реакційну суміш за(трифторметил)-1,2,3,6-тетрагідропіримідин-1-іл] лишали охолоджуватися до кімнатної температуфенокси)-2-(метоксикарбонілметокси)піридину: ри. У реакційну суміш додавали 100мл етилацетату і 30мл насиченого водного розчину хлориду натрію і суміш розділяли. Органічний шар промивали послідовно один раз 20мл насиченого водного розчину хлориду натрію, двічі 20мл хлористоводневої кислоти (1моль/л) і один раз 20мл насиченого водного розчину хлориду натрію; сушили над безводним сульфатом магнію і концент1 рували. Залишок очищали колонковою хроматогН-ЯМР (300МГц, CDCІ3, TMS δ (ч/млн.): 3,50 рафією на силікагелі (елюент: гексан/зтилацетат = (3Н, кв, J=1,0Гц), 3,70 (3Н, с), 4,90 (1Н, д, 6/4) і отримували 0,44г 3-оксо-2J=15,8Гц), 4,97 (1H, д, J=15,8Гц), 6,29 (1H, с), 6,90феноксибутиламіду. 6,95 (2Н, м), 7,32 (1H, дд, J=1,9Гц, 7,7Гц), 7,37 (1H, 3-Оксо-2-феноксибутиламід д, J=8,7Гц), 7,92 (1H, дд, J=1,9Гц, 4,9Гц). Промислове застосування Представлена піридонова сполука може бути отримана з даної амідної сполуки за даним способом. Довідковий приклад 2 В атмосфері азоту 8,92г 2-хлор-3 15 Комп’ютерна в ерстка Л. Купенко 78333 Підписне 16 Тираж 26 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for production of phenoxy-substituted 2-pyridone compounds
Назва патенту російськоюСпособ получения феноксизамещенных 2-пиридиновых соединений
МПК / Мітки
МПК: C07D 213/69, C07D 213/64, C07D 401/12
Мітки: спосіб, феноксизаміщених, одержання, сполук, 2-піридинових
Код посилання
<a href="https://ua.patents.su/8-78333-sposib-oderzhannya-fenoksizamishhenikh-2-piridinovikh-spoluk.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання феноксизаміщених 2-піридинових сполук</a>
Попередній патент: Спосіб та пристрій для виробництва рулону пакувального ламінату визначеної форми
Наступний патент: Спосіб покращення наповнюваності тютюну
Випадковий патент: Насос вібраційний побутовий












