4-імідазопіридазин-1-ілбензаміди і 4-імідазотриазин-1-ілбензаміди як втк-інгібітори
Номер патенту: 115312
Опубліковано: 25.10.2017
Автори: Раймакерс Ханс К.А., Ревінкел Йоханнес Бернардус Марія, Барф Тьєрд А., Стерренбург Ян-Герард, Ман де Адріанус Петрус Антоніус, Аубрі Артур А., Янс Хрістіан Герардус Йоханнес Марія, Вейкманс Якобус К. Х. М.
Формула / Реферат
1. Сполука, яка являє собою (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-а]піразин-1-іл)-N-(піридин-2-іл)бензамід формули
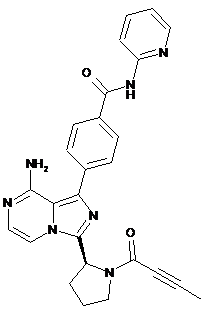 .
.
2. Фармацевтична композиція, що включає фармацевтично прийнятний носій або розчинник і сполуку за п. 1.
3. Фармацевтична композиція за п. 2, сформульована для перорального введення.
4. Фармацевтична композиція за п. 3, яка являє собою таблетку, капсулу, порошок, гранулят, розчин або суспензію.
5. Комбінація сполуки за п. 1 і додаткового терапевтичного засобу.
6. Фармацевтично прийнятна сіль (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-а]піразин-1-іл)-N-(піридин-2-іл)бензаміду формули
 .
.
7. Фармацевтично прийнятна сіль за п. 6, де сіль вибирають з групи, яка складається з ацетату, аскорбату, бензоату, бензолсульфонату, бісульфату, борату, бутирату, цитрату, камфорату, камфорсульфонату, фумарату, гідрохлориду, гідроброміду, гідройодиду, лактату, малеату, метансульфонату, нафталінсульфонату, нітрату, оксалату, фосфату, пропіонату, саліцилату, сукцинату, сульфату, тартрату, тіоціанату і толуолсульфонату.
8. Фармацевтична композиція, що включає фармацевтично прийнятний носій або розчинник і фармацевтично прийнятну сіль за п. 6.
9. Фармацевтична композиція, що включає фармацевтично прийнятний носій або розчинник і фармацевтично прийнятну сіль за п. 7.
10. Фармацевтична композиція за п. 9, сформульована для перорального введення.
11. Фармацевтична композиція за п. 10, що являє собою таблетку, капсулу, порошок, гранулят, розчин або суспензію.
12. Комбінація фармацевтично прийнятної солі за п. 6 і додаткового терапевтичного засобу.
13. Сполука, що являє собою (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-а]піразин-1-іл)-2-метокси-N-(піридин-2-іл)бензамід формули
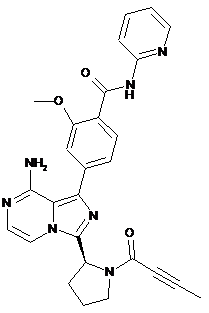 .
.
14. Фармацевтична композиція, що включає фармацевтично прийнятний носій або розчинник і сполуку за п. 13.
15. Фармацевтична композиція за п. 14, сформульована для перорального введення.
16. Фармацевтична композиція за п. 15, що являє собою таблетку, капсулу, порошок, гранулят, розчин або суспензію.
17. Комбінація сполуки за п. 13 і додаткового терапевтичного засобу.
18. Фармацевтично прийнятна сіль (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-а]піразин-1-іл)-2-метокси-N-(піридин-2-іл)бензаміду формули
 .
.
19. Фармацевтично прийнятна сіль за п. 18, де сіль вибирають з групи, яка складається з ацетату, аскорбату, бензоату, бензолсульфонату, бісульфату, борату, бутирату, цитрату, камфорату, камфорсульфонату, фумарату, гідрохлориду, гідроброміду, гідройодиду, лактату, малеату, метансульфонату, нафталінсульфонату, нітрату, оксалату, фосфату, пропіонату, саліцилату, сукцинату, сульфату, тартрату, тіоціанату і толуолсульфонату.
20. Фармацевтична композиція, що включає фармацевтично прийнятний носій або розчинник і фармацевтично прийнятну сіль за п. 18.
21. Фармацевтична композиція, що включає фармацевтично прийнятний носій або розчинник і фармацевтично прийнятну сіль за п. 19.
22. Фармацевтична композиція за п. 21, сформульована для перорального введення.
23. Фармацевтична композиція за п. 22, що являє собою таблетку, капсулу, порошок, гранулят, розчин або суспензію.
24. Комбінація фармацевтично прийнятної солі за п. 18 і додаткового терапевтичного засобу.
25. Спосіб лікування розладу, опосередкованого тирозинкіназою Брутона (Btk), у суб'єкта, що включає введення суб'єкту сполуки за п. 1 в кількості, ефективній для лікування розладу, опосередкованого Btk, здійснюючи, таким чином, лікування суб'єкта,
де розлад, опосередкований Btk, вибирають з групи, що включає ревматоїдний артрит, псоріатичний артрит, інфекційний артрит, прогресивний хронічний артрит, деформуючий артрит, остеоартрит, травматичний артрит, подагричний артрит, синдром Рейтера, поліхондрит, гострий синовіт і спондиліт, гломерулонефрит (з або без нефротичного синдрому), аутоімунні гематологічні захворювання, гемолітичну анемію, апластичну анемію, ідіопатичну тромбоцитопенію і нейтропенію, аутоімунний гастрит і аутоімунні запальні захворювання кишечнику, виразковий коліт, хворобу Крона, реакцію "трансплантат проти хазяїна", відторгнення алотрансплантата, хронічний тиреоїдит, хворобу Грейвса, склеродермію, діабет (І типу і II типу), активний гепатит (гострий і хронічний), панкреатит, первинний біліарний цироз, важку міастенію, розсіяний склероз, системний червоний вовчак, псоріаз, атопічний дерматит, контактний дерматит, екзему, сонячні опіки шкіри, васкуліт (наприклад, хвороба Бехчета), хронічну ниркову недостатність, синдром Стівенса-Джонсона, запальний біль, ідіопатичний синдром мальабсорбції, кахексію, саркоїдоз, синдром Гієна-Барре, увеїт, кон'юнктивіт, кератокон'юнктивіт, середній отит, пародонтоз, легеневий інтерстиціальний фіброз, астму, бронхіт, риніт, синусит, пневмоконіоз, синдром легеневої недостатності, емфізему легенів, легеневий фіброз, силікоз, хронічне запальне захворювання легенів, хронічне обструктивне захворювання легенів, проліферативне захворювання, неходжкінську лімфому, дифузну великоклітинну В-клітинну лімфому (DLBCL), лімфому з клітин мантійної зони (MCL), В-клітинний хронічний лімфолейкоз, гострий лімфобластний лейкоз, гострий лімфобластний лейкоз із зрілими В-клітинами, В-клітинну лімфому, проліферативний мастоцитоз і враження кістки, пов'язані з множинною мієломою.
26. Спосіб за п. 25, де розлад, опосередкований Btk, являє собою неходжкінську лімфому, дифузну великоклітинну В-клітинну лімфому (DLBCL), лімфому з клітин мантійної зони (MCL), В-клітинний хронічний лімфолейкоз, гострий лімфобластний лейкоз, гострий лімфобластний лейкоз зі зрілими В-клітинами або В-клітинну лімфому, що виникають в результаті постійного активного сигналу В-клітинного рецептора.
27. Спосіб за п. 25, де розлад, опосередкований Btk, являє собою В-клітинний хронічний лімфолейкоз або лімфому з клітин мантійної зони (MCL).
28. Спосіб лікування розладу, опосередкованого тирозинкіназою Брутона (Btk), у суб'єкта, що включає введення суб'єкту фармацевтично прийнятної солі за п. 6 в кількості, ефективній для лікування розладу, опосередкованого Btk, здійснюючи, таким чином, лікування суб'єкта,
де розлад, опосередкований Btk, вибирають з групи, що включає ревматоїдний артрит, псоріатичний артрит, інфекційний артрит, прогресивний хронічний артрит, деформуючий артрит, остеоартрит, травматичний артрит, подагричний артрит, синдром Рейтера, поліхондрит, гострий синовіт і спондиліт, гломерулонефрит (з або без нефротичного синдрому), аутоімунні гематологічні захворювання, гемолітичну анемію, апластичну анемію, ідіопатичну тромбоцитопенію і нейтропенію, аутоімунний гастрит і аутоімунні запальні захворювання кишечнику, виразковий коліт, хворобу Крона, реакцію "трансплантат проти хазяїна", відторгнення алотрансплантата, хронічний тиреоїдит, хворобу Грейвса, склеродермію, діабет (І типу і II типу), активний гепатит (гострий і хронічний), панкреатит, первинний біліарний цироз, важку міастенію, розсіяний склероз, системний червоний вовчак, псоріаз, атопічний дерматит, контактний дерматит, екзему, сонячні опіки шкіри, васкуліт (наприклад, хвороба Бехчета), хронічну ниркову недостатність, синдром Стівенса-Джонсона, запальний біль, ідіопатичний синдром мальабсорбції, кахексію, саркоїдоз, синдром Гієна-Барре, увеїт, кон'юнктивіт, кератокон'юнктивіт, середній отит, пародонтоз, легеневий інтерстиціальний фіброз, астму, бронхіт, риніт, синусит, пневмоконіоз, синдром легеневої недостатності, емфізему легенів, легеневий фіброз, силікоз, хронічне запальне захворювання легенів, хронічне обструктивне захворювання легенів, проліферативне захворювання, неходжкінську лімфому, дифузну великоклітинну В-клітинну лімфому (DLBCL), лімфому з клітин мантійної зони (MCL), В-клітинний хронічний лімфолейкоз, гострий лімфобластний лейкоз, гострий лімфобластний лейкоз із зрілими В-клітинами, В-клітинну лімфому, проліферативний мастоцитоз і ураження кістки, пов'язані з множинною мієломою.
29. Спосіб за п. 28, де розлад, опосередкований Btk, являє собою неходжкінську лімфому, дифузну великоклітинну В-клітинну лімфому (DLBCL), лімфому з клітин мантійної зони (MCL), В-клітинний хронічний лімфолейкоз, гострий лімфобластний лейкоз, гострий лімфобластний лейкоз зі зрілими В-клітинами або В-клітинну лімфому, що виникають в результаті постійного активного сигналу В-клітинного рецептора.
30. Спосіб за п. 28, де розлад, опосередкований Btk, являє собою В-клітинний хронічний лімфолейкоз або лімфому з клітин мантійної зони (MCL).
31. Спосіб лікування розладу, опосередкованого тирозинкіназою Брутона (Btk), у суб'єкта, що включає введення суб'єкту сполуки за п. 13 в кількості, ефективній для лікування розладу, опосередкованого Btk, здійснюючи, таким чином, лікування суб'єкта,
де розлад, опосередкований Btk, вибирають з групи, що включає ревматоїдний артрит, псоріатичний артрит, інфекційний артрит, прогресивний хронічний артрит, деформуючий артрит, остеоартрит, травматичний артрит, подагричний артрит, синдром Рейтера, поліхондрит, гострий синовіт і спондиліт, гломерулонефрит (з або без нефротичного синдрому), аутоімунні гематологічні захворювання, гемолітичну анемію, апластичну анемію, ідіопатичну тромбоцитопенію і нейтропенію, аутоімунний гастрит і аутоімунні запальні захворювання кишечнику, виразковий коліт, хворобу Крона, реакцію "трансплантат проти хазяїна", відторгнення алотрансплантата, хронічний тиреоїдит, хворобу Грейвса, склеродермію, діабет (І типу і II типу), активний гепатит (гострий і хронічний), панкреатит, первинний біліарний цироз, важку міастенію, розсіяний склероз, системний червоний вовчак, псоріаз, атопічний дерматит, контактний дерматит, екзему, сонячні опіки шкіри, васкуліт (наприклад, хвороба Бехчета), хронічну ниркову недостатність, синдром Стівенса-Джонсона, запальний біль, ідіопатичний синдром мальабсорбції, кахексію, саркоїдоз, синдром Гієна-Барре, увеїт, кон'юнктивіт, кератокон'юнктивіт, середній отит, пародонтоз, легеневий інтерстиціальний фіброз, астму, бронхіт, риніт, синусит, пневмоконіоз, синдром легеневої недостатності, емфізему легенів, легеневий фіброз, силікоз, хронічне запальне захворювання легенів, хронічне обструктивне захворювання легенів, проліферативне захворювання, неходжкінську лімфому, дифузну великоклітинну В-клітинну лімфому (DLBCL), лімфому з клітин мантійної зони (MCL), В-клітинний хронічний лімфолейкоз, гострий лімфобластний лейкоз, гострий лімфобластний лейкоз із зрілими В-клітинами, В-клітинну лімфому, проліферативний мастоцитоз і ураження кістки, пов'язані з множинною мієломою.
32. Спосіб за п. 31, де розлад, опосередкований Btk, являє собою ревматоїдний артрит, псоріатичний артрит або остеоартрит.
33. Спосіб лікування розладу, опосередкованого тирозинкіназою Брутона (Btk), у суб'єкта, що включає введення суб'єкту фармацевтично прийнятної солі за п. 18 в кількості, ефективній для лікування розладу, опосередкованого Btk, здійснюючи, таким чином, лікування суб'єкта,
де розлад, опосередкований Btk, вибирають з групи, що включає ревматоїдний артрит, псоріатичний артрит, інфекційний артрит, прогресивний хронічний артрит, деформуючий артрит, остеоартрит, травматичний артрит, подагричний артрит, синдром Рейтера, поліхондрит, гострий синовіт і спондиліт, гломерулонефрит (з або без нефротичного синдрому), аутоімунні гематологічні захворювання, гемолітичну анемію, апластичну анемію, ідіопатичну тромбоцитопенію і нейтропенію, аутоімунний гастрит і аутоімунні запальні захворювання кишечнику, виразковий коліт, хворобу Крона, реакцію "трансплантат проти хазяїна", відторгнення алотрансплантата, хронічний тиреоїдит, хворобу Грейвса, склеродермію, діабет (І типу і II типу), активний гепатит (гострий і хронічний), панкреатит, первинний біліарний цироз, важку міастенію, розсіяний склероз, системний червоний вовчак, псоріаз, атопічний дерматит, контактний дерматит, екзему, сонячні опіки шкіри, васкуліт (наприклад, хвороба Бехчета), хронічну ниркову недостатність, синдром Стівенса-Джонсона, запальний біль, ідіопатичний синдром мальабсорбції, кахексію, саркоїдоз, синдром Гієна-Барре, увеїт, кон'юнктивіт, кератокон'юнктивіт, середній отит, пародонтоз, легеневий інтерстиціальний фіброз, астму, бронхіт, риніт, синусит, пневмоконіоз, синдром легеневої недостатності, емфізему легенів, легеневий фіброз, силікоз, хронічне запальне захворювання легенів, хронічне обструктивне захворювання легенів, проліферативне захворювання, неходжкінську лімфому, дифузну великоклітинну В-клітинну лімфому (DLBCL), лімфому з клітин мантійної зони (MCL), В-клітинний хронічний лімфолейкоз, гострий лімфобластний лейкоз, гострий лімфобластний лейкоз із зрілими В-клітинами, В-клітинну лімфому, проліферативний мастоцитоз і ураження кістки, пов'язані з множинною мієломою.
34. Спосіб за п. 33, де розлад, опосередкований Btk, являє собою ревматоїдний артрит, псоріатичний артрит або остеоартрит.
Текст
Реферат: Даний винахід стосується 6-5-членних конденсованих з піридиновим кільцем сполук відповідно до формули І UA 115312 C2 (12) UA 115312 C2 Y R5 X N O B3 N NH B1 B4 NH2 Z B2 N A N R1 R4 R3 N R2 Формула І або їх фармацевтично прийнятних солей або фармацевтичних композицій, що містять ці сполуки, і їх застосування в терапії. Зокрема, даний винахід стосується застосування 6-5членних конденсованих з піридиновим кільцем сполук відповідно до формули І для лікування розладів, опосередкованих тирозинкіназою Брутона (Btk). UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 Галузь техніки, до якої належить винахід Даний винахід стосується 6-5-членних конденсованих з піридиновим кільцем сполук, фармацевтичних композицій, що містять ці сполуки, і їх застосування в терапії. Зокрема, даний винахід стосується застосування 6-5-членних конденсованих з піридиновим кільцем сполук при лікуванні розладів, опосередкованих тирозинкіназою Брутона (BTK). Передумови створення винаходу Активація B-лімфоцитів є ключовим фактором у генерації адаптивної імунної відповіді. Порушена активація B-лімфоцитів є відмітною рисою багатьох аутоімунних захворювань і тому модуляція цієї імунної відповіді викликає терапевтичний інтерес. Нещодавно було виявлено, що терапія з використанням В-клітин в аутоімунних захворюваннях має успіх. Лікування пацієнтів з ревматоїдним артритом (RA) за допомогою Ритуксимабу (анти-CD20 терапія) на даний момент є загальноприйнятою клінічною терапією. Більш пізні дослідження з використанням клінічних випробувань показують, що лікування за допомогою Ритуксимабу також поліпшує симптоми захворювання у пацієнтів з рецидивуючим ремітуючим розсіяним склерозом (RRMS) і системним червоним вовчаком (SLE). Цей успіх підтверджує потенційну можливість майбутнього застосування для лікування аутоімунних захворювань зі спрямованою дією на Вклітинний імунітет. Тирозинкіназа Брутона (Btk) являє собою нерецепторну протеїнкіназу Tec-сімейства, експресовану у В-клітинах і мієлоїдних клітинах. Добре відомо, що функція Btk у сигнальних шляхах активується шляхом заняття В-клітинного рецептора (BCR) і FcεR1 на тучних клітинах. Крім того, були припущення про функцію Btk як мішені у сигнальному шляху Toll-подібного рецептора. Функціональні мутації в Btk у людини приводять до захворювань первинного імунодефіциту, називаних XLA, які характеризуються дефектом у розвитку В-клітин із блокуванням між про- і пре-В-клітинною стадією. Це приводить до майже повної відсутності Влімфоцитів в організмі людини, що викликає виражене зниження сироваткового імуноглобуліну всіх класів. Ці відкриття підтверджують ключову роль Btk у регуляції продукції аутоантитіл в аутоімунних захворюваннях. Крім того, регуляція Btk може впливати на BCR-індуковану продукцію прозапальних цитокінів і хемокінів В-клітинами, що вказує на широкий потенціал для Btk у лікуванні аутоімунних захворювань. З урахуванням регуляторної ролі, описаної для Btk у FcεR-опосередкованій активації тучних клітин, інгібітори Btk можуть також показувати потенціал для лікування алергічних реакцій [Gilfillan et al. Immunological Reviews, 288 (2009), pp. 149-169]. Крім того, також повідомлялося, що Btk беруть участь у RANKL-індукованій диференціації остеокластів [Shinohara et al. Cell, 132 (2008), pp. 794-806] і тому також можуть становити інтерес для лікування розладів резорбції кісток. Інші захворювання, у яких важливу роль грають дисфункціональні B-клітини, являють собою В-клітинні злоякісні новоутворення. Дійсно, анти-CD20 терапія ефективно використовується в клініці для лікування фолікулярної лімфоми, дифузійної великоклітинної В-клітинної лімфоми і хронічного лімфоцитарного лейкозу [Lim et al. Haematologica, 95 (2010), pp. 135-143]. Повідомлялося про роль Btk у регуляції проліферації й апоптозу B-клітин і це вказує, що також існує потенціал для інгібіторів Btk у лікуванні В-клітинних лімфом. Інгібування Btk, як видно, буде корисним, зокрема, при В-клітинних лімфомах через постійну активну передачу сигналу BCR [Davis et al. Nature, 463 (2010), pp. 88-94]. Деякі класи 6-5-членних конденсованих піридинових кільцевих сполук були описані як інгібітори кінази, наприклад імідазо[1,5-f][1,2,4]триазинові сполуки були описані в WO 2005097800 і WO 2007064993; імідазо[1,5-a]піразинові сполуки були описані в WO 2005037836 і WO 2001019828 як інгібітори IGF-1R-ферменту. Деякі з Btk-інгібіторів, про які повідомлялося, не є селективними відносно кіназ Srcсімейства. Існуючі серйозні побічні ефекти, описані для "нокаутів" кіназ Src-сімейства, особливо для подвійних і потрійних "нокаутів", розглядають як перешкоду для розробки інгібіторів Btk, що не є селективними відносно кіназ Src-сімейства. І Lyn-дефіцитні, і Fyn-дефіцитні миші демонструють аутоімунітет, імітуючи фенотип люпус-нефриту людини. Крім того, Fyn-дефіцитні миші також демонструють виражені неврологічні дефекти. Миші з Lyn-"нокаутом" також демонструють подібний алергічному фенотип і це говорить про те, що Lyn є широким негативним регулятором IgE-опосередкованої алергічної відповіді, контролюючи реактивність тучних клітин і асоційовані з алергією ознаки [Odom et al. J. Exp. Med., 199 (2004), pp. 14911502]. Крім того, у старих мишей з Lyn-"нокаутом" розвивалася важка спленомегалія (мієлоїдна експансія) і дисеміновані моноцитарні/макрофагальні пухлини [Harder et al. Immunity, 15 (2001), pp. 603-615]. Ці спостереження знаходяться у відповідності з гіперреспонсивними B-клітинами, 1 UA 115312 C2 5 10 15 20 25 30 35 тучними клітинами і мієлоїдними клітинами і підвищеними Ig-рівнями, що спостерігаються у Lynдефіцитних мишей. Самки мишей з Src-"нокаутом" є безплідними через зменшений розвиток фолікулів і овуляції [Roby et al. Endocrine, 26 (2005), pp. 169-176]. -/-/-/-/Подвійні "нокаути" Src Fyn і Src Yes демонструють важкий фенотип з ефектами на рух і -/-/-/дихання. Тварини з потрійними "нокаутами" Src Fyn Yes вмирали в день 9,5 [Klinghoffer et al. -/-/EMBO J., 18 (1999), pp. 2459-2471]. Що стосується подвійного "нокауту" Src Hck , дві третини мишей умирали при народженні, при цьому у мишей, що вижили, спостерігали розвиток остеопорозу, екстрамедулярного гемопоезу, анемії, лейкопенії [Lowell et al. Blood, 87 (1996), pp. 1780-1792]. Отже, інгібітор, що інгібує декілька або всі кінази з Src-сімейства кіназ, одночасно може викликати серйозні побічні ефекти. Докладний опис винаходу Задачею даного винаходу є забезпечення 6-5-членних конденсованих піридинових кільцевих сполук, фармацевтичних композицій, що містять ці сполуки, і їх застосування в терапії. Зокрема, даний винахід стосується застосування 6-5-членних конденсованих піридинових кільцевих сполук для лікування розладів, опосередкованих тирозинкіназою Брутона (Btk). Більш конкретно, даний винахід забезпечує 6-5-членні конденсовані піридинові кільцеві сполуки відповідно до формули I або їх фармацевтично прийнятні солі. . У цій формулі замісники визначені наступним чином: X являє собою CH, N, O або S; Y являє собою C(R6), N, O або S; Z являє собою CH, N або зв'язок; A являє собою CH або N; B1 являє собою N або C(R7); B2 являє собою N або C(R8); B3 являє собою N або C(R9); B4 являє собою N або C(R10); R1 являє собою R11C(O), R12S(O), R13SO2 або (1-6C)алкіл, необов'язково заміщений групою R14; R2 являє собою H, (1-3C)алкіл або (3-7C)циклоалкіл; R3 являє собою H, (1-6C)алкіл або (3-7C)циклоалкіл; або R2 і R3 утворюють разом з атомами N і C, до яких вони приєднані, (3-7C)гетероциклоалкіл, необов'язково заміщений одним або декількома атомами фтору, гідроксилом, (1-3C)алкілом, (13C)алкокси або оксо; R4 являє собою H або (1-3C)алкіл; 2 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 60 R5 являє собою H, галоген, ціано, (1-4C)алкіл, (1-3C)алкокси, (3-6C)циклоалкіл; всі алкільні групи R5 необов'язково заміщені одним або декількома атомами галогену; або R5 являє собою (6-10C)арил або (2-6C)гетероциклоалкіл; R6 являє собою H або (1-3C)алкіл; або R5 і R6 разом можуть утворювати (3-7C)циклоалкеніл або (2-6C)гетероциклоалкеніл; причому кожен необов'язково заміщений (1-3C)алкілом або одним або декількома атомами галогену; R7 являє собою H, галоген або (1-3C)алкокси; R8 являє собою H або (1-3C)алкіл; або R7 і R8 утворюють разом з атомом вуглецю, до якого вони приєднані, (6-10C)арил або (19C)гетероарил; R9 являє собою H, галоген або (1-3C)алкокси; R10 являє собою Н, галоген або (1-3C)алкокси; R11 незалежно вибирають із групи, що включає (1-6C)алкіл, (2-6C)алкеніл і (2-6C)алкініл, причому кожен алкіл, алкеніл або алкініл необов'язково заміщений однією або декількома групами, вибраними з гідроксилу, (1-4C)алкілу, (3-7C)циклоалкілу, [(1-4C)алкіл]аміно, ді[(14C)алкіл]аміно, (1-3C)алкокси, (3-7C)циклоалкокси, (6-10C)арилу або (3-7C)гетероциклоалкілу; або R11 являє собою (1-3C)алкіл-C(O)-S-(1-3C)алкіл; або R11 являє собою (1-5C)гетероарил, необов'язково заміщений однією або декількома групами, вибраними з галогену або ціано; R12 і R13 незалежно вибирають із групи, що складається з (2-6C)алкенілу або (26C)алкінілу, причому обидва необов'язково заміщені однією або декількома групами, вибраними з гідроксилу, (1-4C)алкілу, (3-7C)циклоалкілу, [(1-4C)алкіл]аміно, ді[(1-4C)алкіл]аміно, (13C)алкокси, (3-7C)циклоалкокси, (6-10C)арилу або (3-7C)гетероциклоалкілу; або (1-5C)гетероарилу, необов'язково заміщеного однією або декількома групами, вибраними з галогену або ціано; R14 незалежно вибирають із групи, що включає галоген, ціано або (2-6C)алкеніл або (26C)алкініл, причому обидва необов'язково заміщені однією або декількома групами, вибраними з гідроксилу, (1-4C)алкілу, (3-7C)циклоалкілу, [(1-4C)алкіл]аміно, ді[(1-4C)алкіл]аміно, (13C)алкокси, (3-7C)циклоалкокси, (6-10C)арилу, (1-5C)гетероарилу або (3-7C)гетероциклоалкілу; за умови, що: - від 0 до 2 атомів груп X, Y, Z одночасно можуть являти собою гетероатом; - коли один атом, вибраний із груп X, Y, являє собою O або S, тоді Z являє собою зв'язок, а інший атом, вибраний із груп X, Y, не може являти собою O або S; - коли Z являє собою C або N, тоді Y являє собою C(R6) або N, і X являє собою C або N; - від 0 до 2 атомів груп B1, B2, B3 і B4 являють собою N. Терміни, використовувані в даній заявці, стосуються наступного. (1-2C)алкіл означає алкільну групу, що містить від 1 до 2 атомів вуглецю, таку як метил або етил. (1-3C)алкіл означає розгалужену або нерозгалужену алкільну групу, що містить 1-3 атоми вуглецю, таку як метил, етил, пропіл або ізопропіл. (1-4C)алкіл означає розгалужену або нерозгалужену алкільну групу, що містить 1-4 атоми вуглецю, таку як метил, етил, пропіл, ізопропіл, бутил, ізобутил, втор-бутил і трет-бутил, переважними є (1-3C)алкільні групи. (1-5C)алкіл означає розгалужену або нерозгалужену алкільну групу, що містить 1-5 атомів вуглецю, наприклад метил, етил, пропіл, ізопропіл, бутил, ізобутил, втор-бутил, трет-бутил, пентил і ізопентил, переважними є (1-4C)алкільні групи. (1-6C)алкіл означає розгалужену або нерозгалужену алкільну групу, що містить 1-6 атомів вуглецю, наприклад метил, етил, пропіл, ізопропіл, бутил, трет-бутил, н-пентил і н-гексил. Переважними є (1-5C)алкільні групи, найбільш переважним є (1-4C)алкіл. (1-2C)алкокси означає алкоксигрупу, що містить 1-2 атоми вуглецю, при цьому алкільна група має значення, визначене вище. (1-3C)алкокси означає алкоксигрупу, що містить 1-3 атоми вуглецю, при цьому алкільна група має значення, визначене вище. Переважними є (1-2C)алкоксигрупи. (1-4C)алкокси означає алкоксигрупу, що містить 1-4 атоми вуглецю, при цьому алкільна група має значення, визначене вище. Переважними є (1-3C)алкоксигрупи, найбільш переважними є (1-2C)алкоксигрупи. (2-4C)алкеніл означає розгалужену або нерозгалужену алкенільну групу, що містить 2-4 атоми вуглецю, таку як етеніл, 2-пропеніл, ізобутеніл або 2-бутеніл. 3 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 60 (2-6C)алкеніл означає розгалужену або нерозгалужену алкенільну групу, що містить 2-6 атомів вуглецю, таку як етеніл, 2-бутеніл і н-пентеніл. Переважними є (2-4C)алкенільні групи. (2-4C)алкініл означає розгалужену або нерозгалужену алкінільну групу, що містить 2-4 атоми вуглецю, таку як етиніл, 2-пропініл або 2-бутиніл. (2-6C)алкініл означає розгалужену або нерозгалужену алкінільну групу, що містить 2-6 атомів вуглецю, таку як етиніл, пропініл, н-бутиніл, н-пентиніл, ізопентиніл, ізогексиніл або нгексиніл. Переважними є (2-4C)алкінільні групи. (3-6C)циклоалкіл означає циклоалкільну групу, що містить 3-6 атомів вуглецю, таку як циклопропіл, циклобутил, циклопентил або циклогексил. (3-7C)циклоалкіл означає циклоалкільну групу, що містить 3-7 атомів вуглецю, таку як циклопропіл, циклобутил, циклопентил, циклогексил або циклогептил. (2-6C)гетероциклоалкіл означає гетероциклоалкільну групу, що містить 2-6 атомів вуглецю, переважно 3-5 атомів вуглецю, і один або два гетероатоми, вибрані з N, O і/або S, яка може бути приєднана через гетероатом, якщо це можливо, або вуглецевий атом. Переважними гетероатомами є N або O. Переважними є піперидин, морфолін, піролідин і піперазин. Найбільш переважний (2-6C)гетероциклоалкіл являє собою піролідин. Гетероциклоалкільна група може бути приєднана через гетероатом, якщо це можливо. (3-7C)гетероциклоалкіл означає гетероциклоалкільну групу, що містить 3-7 атомів вуглецю, переважно 3-5 атомів вуглецю, і один або два гетероатоми, вибрані з N, O і/або S. Переважними гетероатомами є N або O. Переважні (3-7C)гетероциклоалкільні групи являють собою азетидиніл, піролідиніл, піперидиніл, гомопіперидиніл або морфолініл. Більш переважні (3-7C)гетероциклоалкільні групи являють собою піперидин, морфолін і піролідин. Гетероциклоалкільна група може бути приєднана через гетероатом, якщо це можливо. (3-7C)циклоалкокси означає циклоалкільну групу, що містить 3-7 атомів вуглецю, з тим же значенням, як визначено раніше, приєднану через кільцевий вуглецевий атом до екзоциклічного атома кисню. (6-10C)арил означає ароматичну вуглеводневу групу, що містить 6-10 атомів вуглецю, таку як феніл, нафтил, тетрагідронафтил або інденіл. Переважна (6-10C)арильна група являє собою феніл. (1-5C)гетероарил означає заміщену або незаміщену ароматичну групу, що містить 1-5 атомів вуглецю і 1-4 гетероатоми, вибрані з N, O і/або S. (1-5C)гетероарил може бути необов'язково заміщеним. Переважні (1-5C)гетероарильні групи являють собою тетразоліл, імідазоліл, тіадіазоліл, піридил, піримідил, триазиніл, тієніл або фурил, більш переважно, коли (1-5C)гетероарил являє собою піримідил. (1-9C)гетероарил означає заміщену або незаміщену ароматичну групу, що містить 1-9 атомів вуглецю і 1-4 гетероатоми, вибрані з N, O і/або S. (1-9C)гетероарил може бути необов'язково заміщеним. Переважні (1-9C)гетероарильні групи являють собою хінолін, ізохінолін і індол. [(1-4C)алкіл]аміно означає аміногрупу, монозаміщену алкільною групою, що містить 1-4 атоми вуглецю, яка має значення, визначене вище. Переважна [(1-4C)алкіл]аміногрупа являє собою метиламіно. Ді[(1-4C)алкіл]аміно означає аміногрупу, дизаміщену алкільною групою (групами), при цьому кожна містить 1-4 атоми вуглецю і має значення, визначене вище. Переважна ді[(14C)алкіл]аміногрупа являє собою диметиламіно. Галоген означає фтор, хлор, бром або йод. (1-3C)алкіл-C(O)-S-(1-3C)алкіл означає алкілкарбонілтіоалкільну групу, при цьому кожна з алкільних груп містить від 1 до 3 атомів вуглецю і має значення, визначене вище. (3-7C)циклоалкеніл означає циклоалкенільну групу, що містить 3-7 атомів вуглецю, переважно 5-7 атомів вуглецю. Переважні (3-7C)циклоалкенільні групи являють собою циклопентеніл або циклогексеніл. Циклогексенільні групи є найбільш переважними. (2-6C)гетероциклоалкеніл означає гетероциклоалкенільну групу, що містить 2-6 атомів вуглецю, переважно 3-5 атомів вуглецю; і 1 гетероатом, вибраний з N, O і/або S. Переважні (26C)гетероциклоалкенільні групи являють собою оксициклогексенільну й азациклогексенільну групу. У наведених вище визначеннях з багатофункціональними групами точка приєднання знаходиться на останній групі. Коли у визначенні замісника зазначено, що "усі з алкільних груп" зазначеного замісника є необов'язково заміщеними, це також включає в себе алкільний фрагмент алкоксигрупи. Коло в кільці формули I указує, що кільце є ароматичним. Залежно від утвореного кільця, азот, якщо він присутній у X або Y, може нести водень. 4 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 Термін "заміщений" означає, що один або декілька атомів водню на позначеному атомі/атомах є заміщеним і замісник вибраний із зазначеної групи, за умови, що нормальна валентність зазначеного атома в рамках існуючих обставин не перевищена, і що заміщення приводить до стабільної сполуки. Комбінації замісників і/або змінних припустимі, тільки якщо такі комбінації приводять до стабільних сполук. "Стабільна сполука" або "стабільна структура" визначені як сполука або структура, яка досить стійка, щоб витримати виділення з реакційної суміші з придатним ступенем чистоти і формулювання в композицію ефективного терапевтичного засобу. Термін "необов'язково заміщений" означає необов'язкове заміщення зазначеними групами, радикалами або фрагментами. Аспекти винаходу В одному аспекті даний винахід стосується сполуки відповідно до формули I, де B 1 являє собою C(R7); B2 являє собою C(R8); B3 являє собою C(R9); і B4 являє собою C(R10). В іншому аспекті даний винахід стосується сполуки відповідно до формули I, де B 1 являє собою C(R7); B2 являє собою C(R8); B3 являє собою C(R9); B4 являє собою C(R10); R7, R9 і R10, кожний, являють собою H; і R8 вибраний із групи, що складається з водню і метилу. В одному аспекті даний винахід стосується сполуки відповідно до формули I, де R8 являє собою водень або метил, зокрема R8 являє собою водень. В іншому аспекті даний винахід стосується сполуки відповідно до формули I, де R7 являє собою водень, фтор або (1-3C)алкокси. Зокрема, R7 являє собою водень, фтор або метокси. Ще конкретніше, аспект даного винаходу стосується сполуки відповідно до формули I, де R7 являє собою водень. У ще одному аспекті даний винахід стосується сполуки відповідно до формули I, де R9 являє собою водень, фтор або (1-3C)алкокси. Зокрема, R9 являє собою водень, фтор або метокси. Ще конкретніше, аспект даного винаходу стосується сполуки відповідно до формули I, де R9 являє собою водень. В іншому аспекті даний винахід стосується сполуки відповідно до формули I, де R10 являє собою водень, фтор або (1-3C)алкокси. Зокрема, R10 являє собою водень, фтор або метокси. Ще конкретніше, аспект даного винаходу стосується сполуки відповідно до формули I, де R10 являє собою водень. У ще одному аспекті даний винахід стосується сполуки відповідно до формули I, де R7 і R8 утворюють разом з атомом вуглецю, до якого вони приєднані, індол або хінолін, або нафтил. В іншому аспекті даний винахід стосується сполуки відповідно до формули I, де B 1 являє собою C(R7); B2 являє собою C(R8); B3 являє собою C(R9); B4 являє собою C(R10); і R7, R8, R9 і R10, кожний, являють собою H. У ще одному аспекті даний винахід стосується сполуки відповідно до формули I, де R4 являє собою водень або метил. Зокрема, R4 являє собою водень. У ще одному аспекті даний винахід стосується сполуки відповідно до формули I, де A являє собою N. В іншому аспекті даний винахід стосується сполуки відповідно до формули I, де A являє собою CH. В іншому аспекті даний винахід стосується сполуки відповідно до формули I, де кільце, що містить X, Y і Z, вибрано з групи, що включає піридил, піримідил, піридазил, триазиніл, тіазоліл, оксазоліл і ізоксазоліл. Зокрема, винахід стосується сполуки відповідно до формули I, де кільце, що містить X, Y і Z, вибирають із групи, що включає піридил, піримідил і тіазоліл. Визначення R5 і R6 не залежить від вибору X, Y і Z. Місце приєднання R5 і, необов'язково, R6 до цих гетероарильних кілець випливає з формули I. Винахід також стосується сполуки відповідно до формули I, де R5 вибирають із групи, що включає водень, галоген, ціано, (1-4C)алкіл, (1-3C)алкокси і (3-6C)циклоалкіл. Всі алкільні групи R5 необов'язково заміщені одним або декількома атомами галогену. Зокрема, (1-4C)алкільна група в R5 необов'язково заміщена одним або декількома атомами галогену. В іншому аспекті даний винахід стосується сполуки відповідно до формули I, де R5 вибирають із групи, що включає водень, фтор, хлор, (1-3C)алкіл і (1-2C)алкокси, всі алкільні групи R5 необов'язково заміщені одним або декількома атомами галогену. Зокрема, (13C)алкільна група в R5 необов'язково заміщена одним або декількома атомами фтору. Ще конкретніше, винахід стосується сполуки відповідно до формули I, де R5 являє собою водень, фтор, метил, етил, пропіл, метокси або трифторметил. У ще одному аспекті даний винахід стосується сполуки відповідно до формули I, де R5 являє собою піролідин або феніл. 5 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 60 В іншому аспекті винахід стосується сполуки відповідно до формули I, де R6 являє собою водень або (1-3C)алкіл, переважно R6 являє собою водень. У ще одному аспекті даний винахід стосується сполуки відповідно до формули I, де R5 і R6 разом утворюють (3-7C)циклоалкеніл або (2-6C)гетероциклоалкеніл, обидва необов'язково заміщені (1-3C)алкілом або одним або декількома атомами галогену. Зокрема, (37C)циклоалкенільні групи являють собою циклогексеніл і циклопентеніл. Зокрема, (26C)гетероциклоалкенільні групи являють собою азациклогексеніл і оксоциклогексеніл. Ще більш конкретно, винахід стосується сполуки відповідно до формули I, де (3-7C)циклоалкеніл у R5 являє собою циклогексеніл. В іншому аспекті винахід стосується сполуки відповідно до формули I, де R2 являє собою водень або (1-3C)алкіл. Зокрема, R2 являє собою водень або метил. Найбільш переважним є R2, що являє собою водень. У ще одному аспекті даний винахід стосується сполуки відповідно до формули I, де R3 являє собою (1-6C)алкіл. Зокрема, R3 являє собою (1-3C)алкіл. Найбільш переважним є R3, що являє собою метил. В іншому аспекті даний винахід стосується сполуки відповідно до формули I, де R3 являє собою (3-7C)циклоалкіл. В іншому аспекті даний винахід стосується сполуки відповідно до формули I, де R2 являє собою водень або (1-3C)алкіл, і R3 являє собою (1-6C)алкіл. Зокрема, R2 являє собою водень або метил, і R3 являє собою (1-3C)алкіл. Ще конкретніше, винахід стосується сполуки відповідно до формули I, де R2 являє собою водень, і R3 являє собою метил. У ще одному аспекті даний винахід стосується сполуки відповідно до формули I, де R2 або R3 незалежно вибирають із групи, що включає циклопропіл, циклобутил і циклопентил. В іншому аспекті даний винахід стосується сполуки формули I, де R2 і R3 утворюють разом з атомами N і C, до яких вони приєднані, (3-7C)гетероциклоалкіл, необов'язково заміщений одним або декількома атомами галогену, гідроксилом, (1-3C)алкілом. Зокрема, R2 і R3 утворюють разом з атомами N і C, до яких вони приєднані, азетидинільне, піролідинільне, піперидинільне, гомопіперидинільне або морфолінільне кільце, кожне з яких необов'язково заміщене одним або декількома атомами галогену, гідроксилом, (1-3C)алкілом, (1-3C)алкокси або оксо, переважний галогеновий замісник являє собою фтор. У ще одному аспекті даний винахід стосується сполуки формули I, де R2 і R3 утворюють разом з атомами N і C, до яких вони приєднані, азетидинільне, піролідинільне, піперидинільне, гомопіперидинільне або морфолінільне кільце, кожне з яких необов'язково заміщене фтором, гідроксилом, (1-3C)алкілом, (1-3C)алкокси або оксо. Зокрема, R2 і R3 разом з атомами N і C, до яких вони приєднані, утворюють піролідинільне, піперидинільне, морфолінільне або гомопіперидинільне кільце. У ще одному аспекті даний винахід стосується сполуки відповідно до формули I, де R1 являє собою R11C(O), і R11 являє собою (1-6C)алкіл, (2-6C)алкеніл або (2-6C)алкініл, кожен необов'язково незалежно заміщений однією або декількома групами, вибраними з гідроксилу, (1-4C)алкілу, (3-7C)циклоалкілу, (3-7C)гетероциклоалкілу, [(1-4C)алкіл]аміно, ді[(14C)алкіл]аміно, (1-3C)алкокси, (3-7C)циклоалкокси, (6-10C)арилу, (1-5C)гетероарилу або (13C)алкіл-S-C(O)-(1-3C)алкілу. Зокрема, (1-5C)гетероарильна група являє собою піримідил або триазиніл, необов'язково заміщений однією або декількома групами, вибраними з галогену або ціано. Зокрема, (3-7C)гетероциклоалкіл являє собою піролідиніл. Ще конкретніше, винахід стосується сполуки відповідно до формули I, де (3-7C)циклоалкільний замісник групи R11 являє собою циклопропіл. Зокрема, (6-10C)арильний замісник групи R11 являє собою феніл. У ще одному аспекті даний винахід стосується сполуки відповідно до формули I, де R1 являє собою C(O)R11, і R11 являє собою (2-6C)алкеніл або (2-6C)алкініл, кожен необов'язково заміщений однією або декількома групами, вибраними з гідроксилу, (1-4C)алкілу, (37C)циклоалкілу, (3-7C)гетероциклоалкілу, (ді)[(1-4C)алкіл]аміно, (1-3C)алкокси або (37C)циклоалкокси. Зокрема, (3-7C)гетероциклоалкільний замісник групи R11 являє собою піролідиніл, і (3-7C)циклоалкільний замісник групи R11 являє собою циклопропіл. В іншому аспекті даний винахід стосується сполуки відповідно до формули I, де R1 являє собою C(O)R11, і R11 являє собою (2-4C)алкеніл або (2-4C)алкініл, кожен необов'язково заміщений однією або декількома групами, вибраними з (1-4C)алкілу, (3-7C)циклоалкілу, (37C)гетероциклоалкілу, (ді)[(1-4C)алкіл]аміно або (1-3C)алкокси. Зокрема, (37C)гетероциклоалкільний замісник групи R11 являє собою піролідиніл, і (3-7C)циклоалкільний замісник являє собою циклопропіл. Ще конкретніше, R11 являє собою (2-4C)алкеніл або (24C)алкініл, кожен необов'язково заміщений однією або декількома групами, вибраними з метилу, етилу, циклопропілу, піролідинілу, диметиламіно, метокси або етокси. 6 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 У наступному аспекті винахід стосується сполук відповідно до формули I, де R1 являє собою C(O)R11, де R11 являє собою (1-5C)гетероарил, необов'язково заміщений однією або декількома групами, вибраними з галогену або ціано. Зокрема, (1-5C)гетероарильний замісник являє собою піримідил або триазиніл, піримідильні кільця є переважними, необов'язково заміщений однією або декількома групами, вибраними з галогену або ціано. Зокрема, галогеновий замісник являє собою хлор. В іншому аспекті винахід стосується сполук відповідно до формули I, де R1 являє собою R13SO2, де R13 являє собою (2-6C)алкеніл або (2-6C)алкініл. Зокрема, R13 являє собою (24C)алкеніл. Ще конкретніше, R13 являє собою етеніл. В іншому аспекті винахід стосується сполук відповідно до формули I, де R1 являє собою R12S(O), де R12 являє собою (2-6C)алкеніл або (2-6C)алкініл. Зокрема, R13 являє собою (24C)алкеніл. Ще конкретніше, R12 являє собою етеніл. У ще одному аспекті винахід стосується сполук відповідно до формули I, де R1 являє собою (1-3C)алкіл, необов'язково заміщений групою R14, де R14 являє собою (2-4C)алкеніл або (24C)алкініл. У ще одному аспекті даний винахід стосується сполуки відповідно до формули I, вибраної з групи, що включає: (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-(піролідин-1-іл)бут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(піридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-(диметиламіно)бут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(піридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-(диметиламіно)бут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(4-фторпіридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-метилпіридин-2іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4пропілпіридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4(трифторметил)піридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4етилпіридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4,5,6,7тетрагідробензо[d]тіазол-2-іл)бензамід, (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-2-фтор-N-(піридин-2іл)бензамід, (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-2-метокси-N-(піридин-2іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-(диметиламіно)бут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(тіазол-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піридин-2-іл)бензамід, (S)-4-(3-(1-акрилоїлпіперидин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(4-фторпіридин-2іл)бензамід, (S)-4-(3-(1-акрилоїлпіперидин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(4-ціанопіридин-2іл)бензамід, (S)-4-(8-аміно-3-(1-(вінілсульфоніл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4(трифторметил)піридин-2-іл)бензамід, (S)-4-(3-(1-акрилоїлпіперидин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(піримідин-2іл)бензамід, (S)-4-(3-(1-акрилоїлпіперидин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(4-метилпіримідин-2іл)бензамід, 7 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 (S)-4-(8-аміно-3-(1-бут-2-иноїлпіперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піримідин-4іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридазин-3іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(ізоксазол-3іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(5етилтіазол-2-іл)бензамід, (S)-4-(3-(1-акрилоїлпіперидин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-2-фтор-N-(4пропілпіридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-(диметиламіно)бут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)2-метокси-N-(4-пропілпіридин-2-іл)бензамід, 4-(8-аміно-3-((S)-1-бут-2-иноїлпіперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-3-метил-N-(піридин2-іл)бензамід, 4-(3-(акриламідометил)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-инамідоетил)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2-іл)бензамід, (S)-S-2-(2-(8-аміно-1-(4-(піридин-2-ілкарбамоїл)феніл)імідазо[1,5-a]піразин-3-іл)піролідин-1іл)-2-оксоетилетантіоат, (S)-4-(8-аміно-3-(1-(4-гідрокси-4-метилпент-2-иноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(6-хлорпіримідин-4-карбоніл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-пент-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід, (S)-4-(8-аміно-3-(1-(3-циклопропілпропіолоїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-гекс-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід, 4-(3-(1-акрилоїлазепан-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(піридин-2-іл)бензамід, (R)-4-(8-аміно-3-(4-бут-2-иноїлморфолін-3-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід, (S)-4-(8-аміно-3-(1-(N-метилбут-2-инамідо)етил)імідазо[1,5-a]піразин-1-іл)-N-(4(трифторметил)піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(4-(диметиламіно)бут-2-иноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(4-метоксибут-2-иноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піридин-2-іл)бензамід, (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(4-фторпіридин-2іл)бензамід, (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(4-(піролідин-1іл)піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-фторпіридин-2іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід, (S)-4-(3-(1-акрилоїлпіперидин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-пропілпіридин-2іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метокси-N-метилбут-2-енамідо)етил)імідазо[1,5-a]піразин-1-іл)-N-(4пропілпіридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(вінілсульфоніл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4пропілпіридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-2-фтор-N-(піридин-2іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4метоксипіридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-2-фторN-(4-метоксипіридин-2-іл)бензамід, 8 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 60 (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4фторпіридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(ізоксазол-3-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піримідин-2-іл)бензамід, 4-(8-аміно-3-((S)-1-(2-хлорпіримідин-4-карбоніл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-3метил-N-(піридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4метилпіридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4ізопропілпіридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-(диметиламіно)бут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(4-метилпіридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(тіазол-2іл)бензамід, (S)-4-(3-(1-акрилоїлпіперидин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(4-пропілпіридин-2іл)бензамід, (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(4(трифторметил)піридин-2-іл)бензамід,(S)-4-(8-аміно-3-(1-бут-2-иноїлпіперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4(трифторметил)піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-пропілпіридин-2іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-(диметиламіно)бут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(4-ізопропілпіридин-2-іл)бензамід, 4-(8-аміно-3-((S)-1-(вінілсульфоніл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-3-метил-N(піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-2-фтор-N-(4пропілпіридин-2-іл)бензамід, 4-(3-((S)-1-акрилоїлпіперидин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-3-метил-N-(піридин-2іл)бензамід, (E)-4-(8-аміно-3-((4-(диметиламіно)бут-2-енамідо)метил)імідазо[1,5-a]піразин-1-іл)-N(піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(4-ізопропілпіридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(4,5,6,7-тетрагідробензо[d]тіазол-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піридазин-3-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-(диметиламіно)бут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(піридазин-3-іл)бензамід, (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піридазин-3-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метокси-N-метилбут-2-енамідо)етил)імідазо[1,5-a]піразин-1-іл)-N-(4(трифторметил)піридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-(диметиламіно)-N-метилбут-2-енамідо)етил)імідазо[1,5-a]піразин-1іл)-N-(4-пропілпіридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-(піролідин-1-іл)бут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(4-пропілпіридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-(диметиламіно)бут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(4-пропілпіридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(4-фторпіридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4фторпіридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(4,5,6,7-тетрагідробензо[d]тіазол-2-іл)бензамід, 9 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-2метокси-N-(піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-2фтор-N-(піридин-2-іл)бензамід, 4-(8-аміно-3-((S)-1-((E)-4-метоксибут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-3метил-N-(піридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піримідин-4-іл)бензамід, 4-(8-аміно-3-((S)-1-((E)-4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-3метил-N-(4-пропілпіридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4метилпіримідин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-метилпіримідин2-іл)бензамід, (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піримідин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-метакрилоїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід, (S)-4-(8-аміно-3-(1-(2-(трифторметил)акрилоїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піридин-2-іл)бензамід, (S, E)-4-(8-аміно-3-(1-бут-2-еноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід, (S)-4-(8-аміно-3-(1-(ціанометил)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід, (E)-4-(8-аміно-3-((4-метоксибут-2-енамідо)метил)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-(піролідин-1іл)піридин-2-іл)бензамід, (E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)азепан-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4ціанопіридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-2-метокси-N-(піридин2-іл)бензамід, (S)-4-(3-(1-акриламідоетил)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(піридин-2-іл)бензамід, (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(тіазол-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-ізопропілпіридин2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-2метокси-N-(піридин-2-іл)бензамід, (S, E)-4-(8-аміно-3-(1-цинамоїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід, (S)-N-(1-(8-аміно-1-(4-(піридин-2-ілкарбамоїл)феніл)імідазо[1,5-a]піразин-3-іл)етил)-2хлорпіримідин-4-карбоксамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-фторпіридин-2іл)бензамід, (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(4-пропілпіридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4(трифторметил)піридин-2-іл)бензамід, (S)-4-(3-(1-акрилоїлпіперидин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(4(трифторметил)піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-2-метокси-N-(4пропілпіридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-2метокси-N-(4-пропілпіридин-2-іл)бензамід, 4-(8-аміно-3-(бут-2-инамідометил)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(N-метилбут-2-инамідо)етил)імідазо[1,5-a]піразин-1-іл)-N-(4пропілпіридин-2-іл)бензамід, 10 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 60 (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-2-фторN-(4-пропілпіридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(4-(трифторметил)піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(5-етилтіазол-2іл)бензамід, (S)-4-(3-(1-акрилоїлпіперидин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(5-етилтіазол-2іл)бензамід, (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(5-етилтіазол-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(4-(трифторметил)піридин-2-іл)бензамід, (R,E)-4-(8-аміно-3-(4-(4-метоксибут-2-еноїл)морфолін-3-іл)імідазо[1,5-a]піразин-1-іл)-N(піридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піперидин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4пропілпіридин-2-іл)бензамід, (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(4-ціанопіридин-2іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-метоксипіридин2-іл)бензамід, (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(4-метилпіридин-2іл)бензамід, (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(4-пропілпіридин-2іл)бензамід, (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(4-етилпіридин-2іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-(диметиламіно)бут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(піридин-2-іл)бензамід, (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4(трифторметил)піридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(4-метилпіридин-2-іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-ціанопіридин-2іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-етилпіридин-2іл)бензамід, (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-фенілпіридин-2іл)бензамід і (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(4-фенілпіридин-2іл)бензамід. Винахід також стосується таких сполук, де всі конкретні визначення для R1-R14 і всіх груп замісників у різних аспектах винаходу, визначених вище в даній заявці, зустрічаються в будьякій комбінації в рамках визначення 6-5-членних конденсованих піридинових кільцевих сполук, тобто як 8-аміноімідазо[1,5-a]піразинові і 4-аміноімідазо[1,5-f][1,2,4]триазинові сполуки формули I. 6-5-членні конденсовані піридинові кільцеві сполуки, такі як 8-аміноімідазо[1,5-a]піразинові і 4-аміноімідазо[1,5-f][1,2,4]триазинові сполуки за даним винаходом, інгібують активність Btkкінази. Усі сполуки за даним винаходом мають значення EC50 10 мкM або нижче. В іншому аспекті винахід стосується сполук формули I, що мають значення EC50 менше 100 нМ. У ще одному аспекті винахід стосується сполук формули I, що мають значення EC50 менше 10 нМ. Термін "EC50" означає концентрацію випробовуваної сполуки, яка необхідна для 50 % інгібування її максимального ефекту in vitro. Інгібування активності кінази можна виміряти з використанням аналізу іммобілізованого металу для фосфовмісних хімічних речовин (Immobilized Metal Assay for Phosphochemicals (IMAP)). IMAP являє собою гомогенний аналіз поляризації флуоресценції (FP), оснований на уловлюванні фосфорилованих пептидних субстратів за принципом спорідненості. Для IMAP використовують мічені флуоресцеїном пептидні субстрати, які при фосфорилуванні протеїнкіназою зв'язуються з так званими наночастинками IMAP, що дериватизовані з використанням комплексів тривалентних металів. Зв'язування приводить до зміни швидкості 11 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 60 молекулярного руху пептиду і приводить до збільшення значення FP, спостережуваного для флуоресцеїнової мітки, приєднаної до пептидного субстрату (Gaudet et al. A homogeneous fluorescence polarization assay adaptable for a range of protein serine/threonine and tyrosine kinases. J. Biomol. Screen (2003), 8, 164-175). Сполуки формули (I) можуть утворювати солі, які також входять в обсяг даного винаходу. Варто розуміти, що посилання на сполуку формули (I) у даній заявці включає посилання на її солі, якщо не зазначене інше. Термін "сіль (солі)", як він використовується в даній заявці, означає кислотні солі, утворені з неорганічними і/або органічними кислотами, а також основні солі, утворені з неорганічними і/або органічними основами. Крім того, коли сполука формули (I) містить як основну групу, таку як, але не обмежуючись цим, піридин або імідазол, так і кислотну групу, таку як, але не обмежуючись цим, карбонову кислоту, можуть бути утворені цвітер-іони ("внутрішні солі"), і вони включені в термін "сіль (солі)", використовуваний у даній заявці. Такі кислотні й основні солі, використовувані в рамках даного винаходу, є фармацевтично прийнятними (тобто нетоксичними, фізіологічно прийнятними) солями. Солі сполук формули (I) можуть бути утворені, наприклад, взаємодією сполуки формули (I) з кількістю кислоти або основи, такою як еквівалентна кількість, у середовищі, такому як середовище, у якому осаджується сіль, або у водному середовищі з наступною ліофілізацією. Типові кислотно-адитивні солі включають ацетати, аскорбати, бензоати, бензолсульфонати, бісульфати, борати, бутирати, цитрати, камфорати, камфорсульфонати, фумарати, гідрохлориди, гідроброміди, гідройодиди, лактати, малеати, метансульфонати, нафталінсульфонати, нітрати, оксалати, фосфати, пропіонати, саліцилати, сукцинати, сульфати, тартрати, тіоціанати, толуолсульфонати (також відомі як тозилати) тощо. Крім того, кислоти, які звичайно вважаються придатними для утворення фармацевтично застосовних солей з основних фармацевтичних сполук, обговорюються, наприклад, у Stahl P. et al. Camille G. (eds.) Handbook of Pharmaceutical Salts. Properties, Selection and Use. (2002) Zurich: Wiley-VCH; Berge S. et al. Journal of Pharmaceutical Sciences (1977) 66(1) 1-19; Gould P., International J. of Pharmaceutics (1986), 33 201-217; Anderson et al. The Practice of Medicinal Chemistry (1996), Academic Press, New York; і в The Orange Book (Food & Drug Administration, Washington, D.C. на їх сайті). Ці розкриття включені в дану заявку як посилання. Типові основні солі включають солі амонію, солі лужних металів, такі як солі натрію, літію і калію, солі лужноземельних металів, такі як солі кальцію і магнію, солі з органічними основами (наприклад, органічні аміни), такими як дициклогексиламіни, трет-бутиламіни, і солі з амінокислотами, такими як аргінін, лізин і т. п. Основні азотовмісні групи можуть бути квартернізовані за допомогою речовин, таких як нижчі алкілгалогеніди (наприклад, метил-, етилі бутилхлориди, броміди і йодиди), діалкілсульфати (наприклад, диметил-, діетил- і дибутилсульфати), галогеніди з довгим ланцюгом (наприклад, децил-, лаурил- і стеарилхлориди, броміди і йодиди), аралкілгалогеніди (наприклад, бензил- і фенетилброміди) і інші. Сполуки формули I можуть містити асиметричні або хіральні центри і, отже, існують у різних стереоізомерних формах. Передбачається, що всі стереоізомерні форми сполук формули (I), а також їх суміші, включаючи рацемічні суміші, складають частину даного винаходу. Крім того, даний винахід охоплює всі геометричні ізомери й ізомери положення. Наприклад, якщо сполука формули (I) включає подвійний зв'язок або конденсоване кільце, цис- і транс-форми, а також їх суміші включені в обсяг даного винаходу. Суміші діастереомерів можуть бути розділені на їх індивідуальні діастереомери на основі їх фізико-хімічних відмінностей способами, добре відомими фахівцям у даній галузі техніки, наприклад за допомогою хроматографії і/або фракційної кристалізації. Енантіомери можуть бути розділені шляхом перетворення енантіомерної суміші в діастереомерну суміш шляхом взаємодії з відповідною оптично активною сполукою (наприклад, хіральним допоміжним елементом, таким як хіральний спирт або хлорангідрид кислоти Мошера), розділенням діастереомерів і перетворенням (наприклад, гідролізом) окремих діастереомерів на відповідні чисті енантіомери. Крім того, деякі сполуки формули (I) можуть являти собою атропоізомери (наприклад, заміщені біарили), і вони розглядаються як частина даного винаходу. Енантіомери також можуть бути розділені з використанням хіральної ВЕРХ-колонки. Крім того, можливо, що сполуки формули (I) можуть існувати в різних таутомерних формах, і всі такі форми включені в обсяг даного винаходу. Крім того, у винахід включені, наприклад, усі кето-енольні і імін-енамінові форми сполук. Усі стереоізомери (наприклад, геометричні ізомери, оптичні ізомери і т. п.) сполук за даним винаходом (включаючи солі, сольвати, складні ефіри і проліки сполук, а також солі, сольвати і складні ефіри проліків), такі як ті, котрі можуть існувати завдяки асиметричним атомам вуглецю 12 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 60 на різних замісниках, включаючи енантіомерні форми (які можуть існувати навіть за відсутності асиметричних атомів вуглецю), ротамерні форми, атропоізомери і діастереомерні форми, розглядаються як охоплювані обсягом даного винаходу, також як і ізомери положення. Окремі стереоізомери сполук за даним винаходом можуть, наприклад, бути по суті вільними від інших ізомерів або можуть бути змішані, наприклад, у вигляді рацематів або зі всіма іншими або з вибраними іншими стереоізомерами. Хіральні центри за даним винаходом можуть мати конфігурацію R або S, як визначено в Рекомендаціях IUPAC 1974. Використання термінів "сіль", "сольват", "складний ефір", "проліки" і подібних в однаковій мірі стосується солі, сольвату, складного ефіру і проліків енантіомерів, стереоізомерів, ротамерів, таутомерів, ізомерів положення, рацематів або проліків сполук за даним винаходом. Обговорення проліків представлене в Higuchi T. and Stella V. Pro-drugs as Novel Delivery Systems (1987) 14 °F the A.C.S. Symposium Series, і в Bioreversible Carriers in Drug Design, (1987) Edward B. Roche, ed., American Pharmaceutical Association and Pergamon Press. Термін "проліки" означає сполуку (наприклад, попередник лікарського засобу), яка перетворюється in vivo з утворенням сполуки формули (I) або фармацевтично прийнятної солі, гідрату або сольвату сполуки. Перетворення може відбуватися за допомогою різних механізмів (наприклад, метаболічних або хімічних процесів), таких як, наприклад, через гідроліз у крові. Обговорення використання проліків представлене в Higuchi T. and Stella W. "Pro-drugs as Novel Delivery Systems", Vol. 14 °F the A.C.S. Symposium Series, і в Bioreversible Carriers in Drug Design, ed. Edward B. Roche, American Pharmaceutical Association and Pergamon Press, 1987. Сполуки за даним винаходом можуть утворювати гідрати або сольвати. Фахівцям у даній галузі відомо, що заряджені сполуки утворюють гідратовані види при ліофілізації з водою або утворюють сольватовані види при концентрації в розчині з придатним органічним розчинником. Сполуки за даним винаходом включають гідрати або сольвати перерахованих сполук. Одна або декілька сполук за даним винаходом можуть існувати в несольватованих, а також у сольватованих формах з фармацевтично прийнятними розчинниками, такими як вода, етанол і подібні, і передбачається, що даний винахід охоплює як сольватовані, так і несольватовані форми. "Сольват" означає фізичну асоціацію сполуки за даним винаходом з однією або декількома молекулами розчинника. Ця фізична асоціація включає різні ступені іонного і ковалентного зв'язування, включаючи водневе зв'язування. У деяких випадках, сольват може бути здатний до виділення, наприклад, коли одна або декілька молекул розчинника включені в кристалічну решітку кристалічної твердої речовини. "Сольват" охоплює як сольвати, що знаходяться у фазі розчину, так і виділювані сольвати. Необмежувальні приклади придатних сольватів включають етаноляти, метаноляти і подібні. "Гідрат" являє собою сольват, де молекулою розчинника є H2O. Даний винахід також стосується фармацевтичної композиції, що включає 6-5-членні конденсовані піридинові кільцеві сполуки, такі як імідазопіразинові і імідазотриазинові сполуки, або їх фармацевтично прийнятні солі, що мають загальну формулу I, у суміші з фармацевтично прийнятними допоміжними речовинами і, необов'язково, з іншими терапевтичними засобами. Допоміжні речовини повинні бути "прийнятними" у тому розумінні, що вони повинні бути сумісними з іншими інгредієнтами композиції і не повинні бути шкідливими для їх реципієнтів. Даний винахід, крім того, включає сполуку формули I у комбінації з одним або декількома іншими лікарськими засобами. Композиції включають, наприклад, такі, котрі є придатними для перорального, сублінгвального, підшкірного, внутрішньовенного, внутрішньом'язового, назального, місцевого або ректального введення і т. п., усі в одиничній дозованій формі для введення. Для перорального введення, активний інгредієнт може бути представлений у вигляді дискретних одиниць, таких як таблетки, капсули, порошки, грануляти, розчини, суспензії і подібні. Для парентерального введення, фармацевтична композиція за даним винаходом може бути представлена в однодозових або багатодозових контейнерах, наприклад, у вигляді рідини для ін'єкцій у попередньо визначених кількостях, наприклад у герметично закритих флаконах і ампулах, і також може зберігатися у висушеному заморожуванням (ліофілізованому) стані, що вимагає тільки додавання стерильного рідкого носія, наприклад, такого як вода, перед використанням. Змішану з такими фармацевтично прийнятними допоміжними речовинами, наприклад, як описано в довідковій літературі Gennaro A.R. et al. Remington: The Science and Practice of Pharmacy (20th Edition., Lippincott Williams & Wilkins, 2000, див., зокрема, Part 5: Pharmaceutical Manufacturing), активну речовину можна пресувати у тверду одиничну дозовану форму, таку як пігулки, таблетки, або переробити в капсули або супозиторії. За допомогою фармацевтично 13 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 60 прийнятних рідин активну речовину можна застосовувати у вигляді рідкої композиції, наприклад у вигляді препарату для ін'єкцій, у формі розчину, суспензії, емульсії або у вигляді спрею, наприклад назального спрею. Для одержання твердих одиничних дозованих форм передбачається використання традиційних добавок, таких як наповнювачі, барвники, полімерні зв'язуючі і подібні. Як правило, можна використовувати будь-яку фармацевтично прийнятну добавку, яка не надає несприятливого впливу на функцію активної сполуки. Придатні носії, за допомогою яких активний засіб за даним винаходом можна вводити у вигляді твердих композицій, включають лактозу, крохмаль, похідні целюлози і подібні або їх суміші, які використовують у придатних кількостях. Для парентерального введення можна використовувати водні суспензії, ізотонічні сольові розчини і стерильні розчини для ін'єкцій, що містять фармацевтично прийнятні диспергуючі речовини і/або змочувальні речовини, такі як пропіленгліколь або бутиленгліколь. Даний винахід, крім того, включає фармацевтичну композицію, описану в цій заявці вище, у сполученні з пакувальним матеріалом, придатним для зазначеної композиції, при цьому зазначений пакувальний матеріал включає інструкції по застосуванню композиції для використання, описаного в даній заявці вище. Точна доза і схема введення активного інгредієнта або фармацевтичної композиції, що його включає, можуть варіювати залежно від конкретної сполуки, шляху введення і віку і стану конкретного суб'єкта, якому можна вводити цей лікарський засіб. Як правило, для парентерального введення вимагаються більш низькі дози, ніж для інших способів введення, які більшою мірою залежать від абсорбції. Однак доза для людини переважно містить 0,0001-25 мг на кг маси тіла. Бажана доза може бути представлена у вигляді однієї дози або у вигляді декількох субдоз, що вводяться з придатними інтервалами протягом дня, або, у випадку реципієнтів-жінок, у вигляді доз, що вводяться з придатними добовими інтервалами протягом менструального циклу. Доза, а також схема введення можуть відрізнятися у реципієнтів чоловічої і жіночої статі. У сполуках загальної Формули I атоми можуть демонструвати їх природний відносний вміст ізотопів або один або декілька атомів можуть бути штучно збагаченими конкретним ізотопом, що має такий же атомний номер, але атомну масу або масове число, відмінні від атомної маси або масового числа, що переважно присутні у природі. Передбачається, що даний винахід включає всі придатні ізотопні варіанти сполук родової Формули I. Наприклад, різні ізотопні 1 2 форми водню (H) включають протій ( H) і дейтерій ( H). Протій являє собою переважний ізотоп водню, присутній у природі. Збагачення дейтерієм може дати певні терапевтичні переваги, такі як збільшення періоду напіврозпаду in vivo або зниження рівня необхідних доз, або може забезпечити сполуку, корисну як стандарт для характеристики біологічних зразків. Ізотопно збагачені сполуки, охоплювані родовою Формулою I, можна одержати без надмірного експериментування традиційними способами, добре відомими фахівцям у даній галузі, або способами, аналогічними тим, що описані в Схемах і Прикладах у даній заявці, з використанням придатних ізотопно збагачених реагентів і/або проміжних сполук. Сполуки відповідно до даного винаходу можна використовувати в терапії. Ще один аспект даного винаходу стосується застосування 6-5-членних конденсованих піридинових кільцевих сполук або їх фармацевтично прийнятних солей, що мають загальну формулу I, для одержання лікарського засобу, який можна використовувати для лікування Btkопосередкованих захворювань або Btk-опосередкованих станів. Ще один аспект даного винаходу стосується застосування 6-5-членних конденсованих піридинових кільцевих сполук або їх фармацевтично прийнятних солей, що мають загальну формулу I, для одержання лікарського засобу, який можна використовувати для лікування хронічних B-клітинних розладів, у яких T-клітини відіграють помітну роль. У ще одному аспекті даний винахід стосується застосування 6-5-членних конденсованих піридинових кільцевих сполук, таких як 8-аміноімідазо[1,5-a]піразинові і 4-аміноімідазо[1,5f][1,2,4]триазинові сполуки, що мають загальну формулу I, для одержання лікарського засобу, призначеного для лікування Btk-опосередкованих захворювань або станів. Такі застосування включають, але не обмежуються цим, лікування В-клітинних лімфом, що розвиваються в результаті постійної активної передачі сигналу B-клітинного рецептора. Таким чином, сполуки за даним винаходом можуть бути використані в терапії для лікування або попередження захворювань, опосередкованих тирозинкіназою Брутона (Btk). Захворювання, опосередковані Btk, або стани, опосередковані Btk, при використанні в даній заявці, означають будь-який хворобливий стан або інший небезпечний стан, у якому центральну роль грають В-клітини, тучні клітини, мієлоїдні клітини або остеокласти. Ці захворювання включають, але не обмежуються ними, імунні, аутоімунні і запальні 14 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 захворювання, алергії, інфекційні захворювання, резорбції кісток і проліферативні захворювання. Імунні, аутоімунні і запальні захворювання, які можна лікувати або попереджати за допомогою сполук за даним винаходом, включають ревматичні захворювання (наприклад, ревматоїдний артрит, псоріатичний артрит, інфекційний артрит, прогресивний хронічний артрит, деформуючий артрит, остеоартрит, травматичний артрит, подагричний артрит, синдром Рейтера, поліхондрит, гострий синовіт і спондиліт), гломерулонефрит (з або без нефротичного синдрому), аутоімунні гематологічні розлади (наприклад, гемолітична анемія, апластична анемія, ідіопатична тромбоцитопенія і нейтропенія), аутоімунний гастрит і аутоімунні запальні захворювання кишечнику (наприклад, виразковий коліт і хвороба Крона), реакцію "трансплантат проти хазяїна", відторгнення алотрансплантата, хронічний тиреоїдит, хворобу Грейвса, склеродермію, діабет (тип I і тип II), активний гепатит (гострий і хронічний), панкреатит, первинний жовчний цироз, важку міастенію, розсіяний склероз, системний червоний вовчак, псоріаз, атопічний дерматит, контактний дерматит, екзему, сонячні опіки шкіри, васкуліт (наприклад, хвороба Бехчета), хронічну ниркову недостатність, синдром Стівенса-Джонсона, запальний біль, ідіопатичний синдром мальабсорбції, кахексію, саркоїдоз, синдром ГійєнаБарре, увеїт, кон'юнктивіт, кератокон'юнктивіт, середній отит, пародонтоз, легеневий інтерстиціальний фіброз, астму, бронхіт, риніт, синусит, пневмоконіоз, синдром легеневої недостатності, емфізему легень, легеневий фіброз, силікоз, хронічне запальне захворювання легень (наприклад, хронічне обструктивне захворювання легень) і інші запальні або обструктивні захворювання дихальних шляхів. Алергічні захворювання, які можна лікувати або попереджати, включають, серед іншого, алергію на харчові продукти, харчові добавки, отрути комах, пилових кліщів, пилок, тваринні матеріали і контактні алергени, алергічну бронхіальну астму I типу, алергічний риніт, алергічний кон'юнктивіт. Інфекційні захворювання, які можна лікувати або попереджати, включають, серед іншого, сепсис, септичний шок, ендотоксиновий бактеріально-токсичний шок, сепсис, викликаний грамнегативними бактеріями, шигельоз, менінгіт, церебральну малярію, пневмонію, туберкульоз, вірусний міокардит, вірусний гепатит (гепатит А, гепатит В і гепатит С), ВІЛінфекцію, ретиніт, викликаний цитомегаловірусом, грип, герпес, лікування інфекцій, пов'язаних з важкими опіками, міалгію, викликану інфекціями, кахексію, вторинну відносно інфекції, і ветеринарні вірусні інфекції, такі як лентивірус, вірус козячого артриту, вірус меді-вісна, вірус імунодефіциту котячих, бичачий вірус імунодефіциту або вірус імунодефіциту собак. Розлади, такі як резорбція кістки, які можна лікувати або попереджати, включають, серед іншого, остеопороз, остеоартрит, травматичний артрит, подагричний артрит і кісткові захворювання, пов'язані з множинною мієломою. Проліферативні захворювання, які можна лікувати або попереджати, включають, серед іншого, неходжкінську лімфому (зокрема, підтипи дифузійної великоклітинної В-клітинної лімфоми (DLBCL) і лімфому з клітин мантійної зони (MCL)), В-клітинний хронічний лімфоцитарний лейкоз і гострий лімфобластний лейкоз (ALL) зі зрілими В-клітинами, особливо ALL. Зокрема, сполуки за даним винаходом можна використовувати для лікування В-клітинних лімфом, що виникають в результаті постійного активного сигналу В-клітинного рецептора. Інгібування активності кінази можна виміряти з використанням аналізу іммобілізованого металу для фосфовмісних хімічних речовин (Immobilized Metal Assay for Phosphochemicals (IMAP)). IMAP являє собою гомогенний аналіз поляризації флуоресценції (FP), оснований на уловлюванні фосфорилованих пептидних субстратів за принципом спорідненості. Для IMAP використовують мічені флуоресцеїном пептидні субстрати, які при фосфорилуванні протеїнкіназою зв'язуються з так званими наночастинками IMAP, що дериватизовані з використанням комплексів тривалентних металів. Зв'язування приводить до зміни швидкості молекулярного руху пептиду і приводить до збільшення значення FP, спостережуваного для флуоресцеїнової мітки, приєднаної до пептидного субстрату. Активність Btk також можна визначити у В-клітинних лініях, таких як клітини Ramos, або в первинних клітинних аналізах, наприклад, з використанням PBMC або цільної крові людини, мавпи, щура або миші або ізольованих спленоцитів мавпи, щура або миші. Інгібування активності Btk можна досліджувати шляхом вимірювання анти-IgM-індукованої продукції MIP1β (Ramos, PBMC, спленоцити), H2O2-індукованого Btk і PLCγ2 фосфорилування (клітини Ramos) або анти-IgM-індукованої B-клітинній проліферації або експресії CD86 на первинних B-клітинах (PBMC і спленоцити). 15 UA 115312 C2 5 10 15 20 25 30 35 40 Регуляцію активності Btk також можна визначити на тучних клітинах людини, мавпи, щура або миші, після дегрануляції, індукованої активацією FcεR, продукції цитокінів і експресії на клітинній поверхні, індукованої CD63. Крім того, регуляцію активності Btk можна визначити на CD14+ моноцитах, диференційованих після обробки за допомогою M-CSF до остеокластів і активованих за допомогою RANKL. Активність інгібіторів Btk можна досліджувати в спленоцитах миші після введення in vivo. У типовому експерименті миші можуть бути умертвлені через 3 години після введення сполуки. Селезінки видаляють у оброблених мишей для виділення спленоцитів. Спленоцити можна помістити в 96-ямкові культуральні планшети і стимулювати за допомогою анти-IgM, без подальшого додавання сполук. Стимуляцію В-клітин, індуковану анти-IgM, і їх інгібування Btkінгібіторами можна виміряти на основі В-клітинної проліферації, продукції MIP1β або експресії CD86 на спленоцитних B-клітинах CD19+. Ефективність інгібіторів Btk також можна досліджувати в мишачій моделі індукованого колагеном артриту з використанням терапевтичного протоколу при початку лікування після виникнення захворювання, з використанням вимірювальної оцінки хвороби, рентгенівського аналізу деструкції кісткової тканини, руйнування хряща і гістології суглобів. Ефективність інгібіторів Btk на регуляцію активованих тучних клітин можна досліджувати in vivo з використанням моделі пасивної шкірної анафілаксії. Ефект інгібіторів Btk на резорбцію кістки in vivo можна досліджувати з використанням щурячої моделі OVX. У цій моделі у оваріектомованих тварин розвиваються симптоми остеопорозу, які можна регулювати з використанням інгібітору Btk. Загальний синтез 8-Аміноімідазо[1,5-a]піразинові і 4-аміноімідазо[1,5-f][1,2,4]триазинові похідні за даним винаходом можна одержати способами, добре відомими в галузі органічної хімії. Див., th наприклад, March J. "Advanced Organic Chemistry" 4 Edition, John Wiley and Sons. При послідовному здійсненні синтезу може бути необхідним і/або бажаним захистити чутливі або реактивні групи в будь-якій з відповідних молекул. Це досягається за допомогою звичайних захисних груп, таких як ті, котрі описані в Greene T.W. and Wutts P.G.M. "Protective Groups in rd Organic Synthesis" 3 Edition, John Wiley and Sons, 1999. Захисні групи необов'язково видаляють на зручній для цього наступній стадії з використанням способів, добре відомих у даній галузі. Продукти реакцій необов'язково виділяють і очищають, при бажанні, з використанням звичайних способів, таких як, але не обмежуючись ними, фільтрування, перегонка, кристалізація, хроматографія і подібні. Для характеристики таких речовин необов'язково використовують звичайні засоби, включаючи фізичні константи і спектральні дані. 8-Аміноімідазо[1,5-a]піразинові сполуки формули I, де R1-R5 мають раніше визначені значення, можна одержати загальним шляхом синтезу, показаним на схемі I. Відновлення 3-хлорпіразин-2-карбонітрилу (II) можна здійснити шляхом гідрування в присутності придатної системи каталізаторів і розчинника, наприклад нікелю Ренея, з 16 UA 115312 C2 5 10 15 20 25 30 35 40 одержанням (3-хлорпіразин-2-іл)метанаміну (III). Цю сполуку потім можна піддати взаємодії з відповідним чином амінзахищеною амінокислотою. Реакцію Cbz-N(R2)(CR3R4)COOH можна здійснювати в розчиннику, такому як DMF, ТГФ або DCM, у присутності основи, такої як DIPEA, N-метилморфолін, 4-DMAP або триетиламін, і в присутності зв'язуючого реагенту, такого як PyBOP, TBTU, EDCI або HATU, з утворенням N-((3-хлорпіразин-2-іл)метил)аміду (IV). Циклізацію хлорпіразину (IV) можна здійснити з використанням агентів конденсації, таких як фосфороксихлорид, в умовах нагрівання з одержанням 8-хлорімідазо[1,5-a]піразинових похідних (V). Наступне бромування можна здійснити з використанням брому або Nбромсукциніміду в придатному розчиннику, такому як DCM або DMF, при відповідній температурі, з одержанням сполук формули (VI). 8-Аміноімідазо[1,5-a]піразинові похідні (VII) можна одержати зі сполук (VI) з використанням аміаку (газ) у ізопропанолі при підвищеній температурі в посудині високого тиску (>4 атм). Сполуки формули (IX) можна одержати зі сполук формули (VII) з використанням придатної боронової кислоти або пінаконового складного ефіру (VIII), у присутності придатної паладієвої каталітичної системи і розчинника, наприклад комплексу біс(дифенілфосфіно)фероценпаладій(II)хлориду або тетракис(трифенілфосфін)паладію(0), у присутності карбонату калію в суміші діоксан/вода, з одержанням сполук формули (IX). Нарешті, відщіплення захисної групи сполук з формулою (IX) дає незахищений амін, який після функціоналізації з використанням способів, добре відомих у цій галузі техніки, і відповідних реакційноздатних груп, що мають визначені вище значення, дає сполуки формули (I). Прикладом такої захисної стратегії є використання бензилоксикарбонільної захисної групи для захисту аміну від використовуваних амінокислот, що після зняття захисту з використанням 33 % HBr/HOAc або концентрованої HCl давало в результаті аміни. Амінокислоти HN(R2)(CR3R4)COOH є або комерційно доступними, або їх можна легко одержати з використанням способів, добре відомих фахівцям у даній галузі органічної хімії, для введення захисних груп, таких як бензилоксикарбоніл або трет-бутилоксикарбоніл. Паладієві каталізатори й умови для утворення пінаконових ефірів або для зв'язування боронових кислот або пінаконових ефірів з 1-бромімідазо[1,5-a]піразин-8-аміном добре відомі фахівцям в галузі органічної хімії, див., наприклад, Ei-ichi Negishi (Editor), Armin de Meijere (Associate Editor), Handbook of Organopalladium Chemistry for Organic Synthesis, John Wiley and Sons, 2002. 4-Аміноімідазо[1,5-f][1,2,4]триазинові сполуки формули I, де R1-R5 мають раніше визначені значення, можна одержати загальним синтетичним способом, показаним на схемі II. Вихідну речовину 3-аміно-6-(амінометил)-1,2,4-триазин-5(4H)-он (X) можна одержати за допомогою реакції конденсації етилбромпірувату, дибензиламіну й аміногуанідинкарбонату, з наступним дебензилуванням шляхом гідрування над Pd-C-каталізатором [Mitchel W.L. et al. J. Heterocycl. Chem. 21 (1984), pp. 697]. Ця сполука може потім взаємодіяти з відповідним чином амінзахищеною амінокислотою. Реакцію Cbz-N(R2)(CR3R4)COOH можна здійснювати в розчиннику, такому як DMF, ТГФ або DCM, у присутності основи, такої як DIPEA, Nметилморфолін, 4-DMAP або триетиламін, і в присутності зв'язуючого реагенту, такого як 17 UA 115312 C2 5 10 15 20 25 30 35 40 45 50 55 60 PyBOP, TBTU, EDCI або HATU, з утворенням N-((3-аміно-5-оксо-4,5-дигідро-1,2,4-триазин-6іл)метил)аміду (XI). Циклізацію амінотриазинону (XI) можна здійснити з використанням агентів конденсації, таких як фосфороксихлорид, в умовах нагрівання з одержанням похідних 2аміноімідазо[1,5-f][1,2,4]триазин-4(3H)-ону (XIІ). Наступне йодування можна здійснити з використанням йоду або N-йодсукциніміду в придатному розчиннику, такому як DCM або DMF, при відповідній температурі з одержанням сполук формули (XIII). Видалення 2-аміногрупи в похідних 2-аміноімідазо[1,5-f][1,2,4]триазин-4(3H)-ону (XIII) можна здійснити з використанням трет-бутилнітриту в розчинниках, таких як DMF/ТГФ, при кімнатній температурі з утворенням похідних імідазо[1,5-f][1,2,4]триазин-4(3H)-ону (XIV). Похідні 4-аміноімідазо[1,5-f][1,2,4]триазину (XV) можна одержати зі сполук (XIV) з використанням фосфороксихлориду, 1,2,4-триазолу в піридині і наступним амонолізом з використанням аміаку (газ) у ізопропанолі при кімнатній температурі. Сполуки формули (XVI) можна одержати зі сполук формули (XV) з використанням придатної боронової кислоти або пінаконового ефіру (VIII), у присутності придатної паладієвої каталітичної системи і розчинника, наприклад комплексу біс(дифенілфосфіно)фероценпаладій(II)хлориду або тетракис(трифенілфосфін)-паладію(0) у присутності карбонату калію в суміші діоксан/вода, з одержанням сполук формули (XVI). Нарешті, відщіплення захисної групи сполук формули (XVI) дає незахищений амін, що після функціоналізації з використанням способів, добре відомих у цій галузі техніки, і відповідних реакційноздатних груп, що мають визначені вище значення, дає сполуки формули (I). Прикладом такої захисної стратегії є використання бензилоксикарбонільної захисної групи для захисту аміну від використовуваних амінокислот, що після зняття захисту з використанням 33 % HBr/HOAc або концентрованої HCl давало в результаті аміни. Амінокислоти HN(R2)(CR3R4)COOH є або комерційно доступними, або їх можна легко одержати з використанням способів, добре відомих фахівцям у даній галузі органічної хімії, для введення захисних груп, таких як бензилоксикарбоніл або трет-бутилоксикарбоніл. Паладієві каталізатори й умови для утворення пінаконових ефірів або для зв'язування боронових кислот або пінаконових ефірів з 1-бромімідазо[1,5-a]піразин-8-аміном добре відомі фахівцям в галузі органічної хімії, див., наприклад, Ei-ichi Negishi (Editor), Armin de Meijere (Associate Editor), Handbook of Organopalladium Chemistry for Organic Synthesis, John Wiley and Sons, 2002. Даний винахід також охоплює усі стереоізомерні форми 8-аміноімідазо[1,5-a]піразинових і 4аміноімідазо[1,5-f][1,2,4]триазинових похідних відповідно до даного винаходу, що є результатом, наприклад, конфігураційної або геометричної ізомерії. Такі стереоізомерні форми являють собою енантіомери, діастереоізомери, цис- і транс-ізомери і т. д. Наприклад, коли азепан-2карбонову кислоту використовують як амінокислоту, існує суміш двох енантіомерів. У випадку окремих стереоізомерів сполук формули I або їх солей або сольватів, даний винахід включає вищевказані стереоізомери, по суті вільні від, тобто зв'язані з менше ніж 5 %, переважно менше 2 % і, зокрема, менше 1 %, іншого стереоізомера. Суміші стереоізомерів у будь-якій пропорції, наприклад рацемічна суміш, що містить по суті рівні кількості двох енантіомерів, також включені в обсяг даного винаходу. Для хіральних сполук добре відомі в даній галузі методи асиметричного синтезу, у результаті чого одержують чисті стереоізомери, наприклад синтез з хіральною індукцією, синтез, виходячи з хіральних проміжних сполук, енантіоселективні ферментативні перетворення, розділення стереоізомерів з використанням хроматографії на хіральному середовищі. Такі способи описані в Chirality in Industry (за редакцією A.N. Collins, G.N. Sheldrake and J. Crosby, 1992; John Wiley). Таким же чином, у даній галузі добре відомі способи синтезу геометричних ізомерів. 8-Аміноімідазо[1,5-a]піразинові і 4-аміноімідазо[1,5-f][1,2,4]триазинові похідні за даним винаходом, що можуть бути у формі вільної основи, можна виділити з реакційної суміші у вигляді фармацевтично прийнятної солі. Фармацевтично прийнятні солі також можна одержати шляхом обробки вільної основи формули I органічною або неорганічною кислотою, такою як хлористоводнева, бромистоводнева, йодистоводнева, сірчана кислота, фосфорна кислота, оцтова кислота, пропіонова кислота, гліколева кислота, малеїнова кислота, малонова кислота, метансульфонова кислота, фумарова кислота, бурштинова кислота, винна кислота, лимонна кислота, бензойна кислота й аскорбінова кислота. 8-Аміноімідазо[1,5-a]піразинові і 4-аміноімідазо[1,5-f][1,2,4]триазинові похідні за даним винаходом також існують у вигляді аморфних форм. Також можливі декілька кристалічних форм. Усі фізичні форми включені в обсяг даного винаходу. Загальновідоме одержання сольватів. Таким чином, наприклад, Caira M. et al. J. Pharmaceutical Sci., 93(3), 601-611 (2004), описує одержання сольватів протигрибкового 18 UA 115312 C2 5 10 15 20 25 30 35 40 45 флуконазолу в етилацетаті, а також з води. Подібні одержання сольватів, напівсольватів, гідратів і т. п. описані в van Tonder E. C. et al. AAPS PharmSciTech., 5(1), article 12 (2004); і в Bingham A. L. et al, Chem. Commun. 603-604 (2001). Типовий необмежувальний спосіб включає розчинення сполуки за даним винаходом в бажаних кількостях бажаного розчинника (органічної речовини або води або їх суміші) при температурі, більш високій, ніж температура навколишнього середовища, і охолодження розчину зі швидкістю, достатньою для утворення кристалів, які потім виділяють стандартними способами. Аналітичні методи, такі як, наприклад, ІЧ-спектроскопія, показують присутність розчинника (або води) у кристалах у вигляді сольвату (або гідрату). Даний винахід також охоплює ізотопно мічені сполуки за даним винаходом, які ідентичні тим, що зазначені в даній заявці, але при цьому один або декілька атомів заміщені атомом, що має атомну масу або масове число, відмінні від атомної маси або масового числа, які звичайно зустрічаються в природі. Приклади ізотопів, що можуть бути включені в сполуки за даним винаходом, включають ізотопи водню, вуглецю, азоту, кисню, фосфору, фтору і хлору, такі як 2 3 13 14 15 17 18 31 32 35 18 36 H, H, C, C, N, O, O, P, P, S, F і Cl, відповідно. 3 14 Деякі мічені ізотопами сполуки формули I (наприклад, мічені ізотопами H і C) є корисними 3 в аналізах розподілу сполуки і/або тканин субстрату. Ізотопи тритію (тобто H) і вуглецю-14 14 (тобто C) є особливо переважними через простоту їх одержання і можливість виявлення. Крім 2 того, заміщення більш важкими ізотопами, такими як дейтерій (тобто H), може давати певні терапевтичні переваги в результаті більш високої метаболічної стабільності (наприклад, збільшений період напіврозпаду in vivo або зниження рівня необхідних доз), і, отже, вони можуть бути переважними в деяких обставинах. Ізотопно мічені сполуки формули I звичайно можна одержати, додержуючись процедур, аналогічних тим, що розкриті далі в Схемах і/або в Прикладах, шляхом заміщення не міченого ізотопом реагенту відповідним ізотопно міченим реагентом. Винахід проілюстрований наступними прикладами. Приклади Наступні приклади являють собою ілюстративні варіанти втілення даного винаходу, при цьому ніяким чином не обмежуючи обсяг даного винаходу. Реагенти є комерційно доступними або їх одержують відповідно до процедур, описаних в літературі. Мас-спектрометрія: спектри, одержувані методом електронного розпилення, реєстрували на мас-спектрометрі Applied Biosystems API-165 з однією квадрупольною лінзою в режимі чергування позитивних і негативних іонів, з використанням проточно-інжекційного методу. Масовий діапазон складав 120-2000 Да, і сканування здійснювали з розміром кроку 0,2 Да, і капілярну напругу встановлювали на 5000 В. Для розпилення використовували N 2-газ. LC-MS спектрометр (Waters) детектор: PDA (200-320 нм), мас-детектор: ZQ. Елюенти: A: ацетонітрил з 0,05 % трифтороцтової кислоти, B: ацетонітрил/вода=1/9 (об./об.) з 0,05 % трифтороцтової кислоти. Метод LCMS (A) Колонка 1: Chromolith Performance, RP-18e, 4,6×100 мм, градієнтний метод: потік: 4 мл/хв. Час (хв.) A (%) B (%) 0,00 100 0 3,60 0 100 4,00 0 100 4,05 100 0 6,00 100 0 Метод LCMS (B) Колонка 2: XBridge C18, 3,5 мкм, 4,6×20 мм, градієнтний метод: потік: 4 мл/хв. Час (хв.) A (%) B (%) 0,0 100 0 1,60 0 100 3,10 0 100 3,20 100 0 5,00 100 0 UPLC: система Water acquity UPLC; колонка: BEH C18 1,7 мкм, 2,1×100 мм, детектор: PDA (200-320 нм), мас-детектор: SQD. Елюенти: A: ацетонітрил з 0,035 % трифтороцтової кислоти, B: ацетонітрил/вода=1/9 (об./об.) з 0,035 % трифтороцтової кислоти. 19 UA 115312 C2 Метод Час (хв.) 0,0 3,00 3,20 3,69 3,70 5 10 UPLC (A) Метод 60_100 Потік: 0,75 мл/хв. A (%) B (%) 40 60 0 100 0 100 0 100 40 60 UPLC (B) Метод 40_80 Потік: 0,65 мл/хв. A (%) B (%) 60 40 20 80 0 100 0 100 60 40 UPLC (C) Метод 0_60 Потік: 0,60 мл/хв. A (%) B (%) 100 0 40 60 0 100 0 100 100 0 Препаративну ВЕРХ здійснювали на колонці (50×10 мм в. д., 5 мкм, Xterra Prep MS C18) при швидкості потоку 5 мл/хв., об'єм проби, що вводиться, 500 мкл, при кімнатній температурі й УФдетекції при 210 нм. Наступні скорочення використовують повсюдно в даній заявці відповідно до хімічної термінології. HATU O-(7-азабензотриазол-1-іл)-1,1,3,3-тетраметилуронію гексафторфосфат Cbz бензилоксикарбоніл DMF N,N-диметилформамід DCM дихлорметан EtOAc етилацетат DIPEA N,N-діізопропілетиламін ТГФ тетрагідрофуран EtOH етанол EDCI·HCl 1-(3-диметиламінопропіл)-3-етилкарбодііміду гідрохлорид 4-DMAP 4-диметиламінопіридин PyBOP O-бензотриазол-1-ілокситриспіролідинoфосфонію гексафторфосфат TBTU O-бензотриазол-1-іл-N,N,N',N'-тетраметилуронію тетрафторборат HBr бромистий водень HCl хлористий водень HOAc оцтова кислота Z бензилоксикарбоніл Pro пролін POCl3 фосфороксихлорид ВЕРХ високоефективна рідинна хроматографія UPLC надпродуктивна рідинна хроматографія LiHMDS гексаметилдисилазид літію MeOH метанол Gly гліцин Ala аланін n-BuLi н-бутиллітій CO2 діоксид вуглецю Назви кінцевих продуктів у прикладах були одержані з використанням Chemdraw Ultra (версія 9.0.7). Проміжна сполука 1 20 UA 115312 C2 5 10 15 20 25 30 35 40 (S)-бензил-2-(8-аміно-1-бромімідазо[1,5-a]піразин-3-іл)піролідин-1-карбоксилат (a) (3-Хлорпіразин-2-іл)метанаміну гідрохлорид До розчину 3-хлорпіразин-2-карбонітрилу (160 г, 1,147 моль) в оцтовій кислоті (1,5 л) додавали нікель Ренея (50 % суспензія у воді, 70 г, 409 ммоль). Одержану суміш перемішували 2 під тиском 4 бари (4,079 кг/см ) водню при кімнатній температурі протягом ночі. Нікель Ренея видаляли за допомогою фільтрації через декаліт і фільтрат концентрували при зниженому тиску й упарювали разом з толуолом. Тверду коричневу речовину, що залишилася, розчиняли в етилацетаті при 50 °C і охолоджували на бані з льодом. Додавали 2M розчин хлористого водню в діетиловому ефірі (1,14 л) протягом 30 хвилин. Суміш залишали перемішуватися при кімнатній температурі протягом уїк-енду. Кристали збирали за допомогою фільтрації, промивали діетиловим ефіром і сушили при зниженому тиску при 40 °C. Одержану тверду коричневу речовину розчиняли в метанолі при 60 °C. Суміш фільтрували і частково концентрували, охолоджували до кімнатної температури, і додавали діетиловий ефір (1000 мл). Суміш залишали перемішуватися при кімнатній температурі протягом ночі. Утворені тверді речовини збирали за допомогою фільтрації, промивали діетиловим ефіром і сушили при зниженому тиску при 40 °C з одержанням 153,5 г (3-хлорпіразин-2-іл)метанаміну гідрохлориду у вигляді коричневої твердої речовини (74,4 %, вміст 77 %). (b) (S)-бензил-2-((3-хлорпіразин-2-іл)метилкарбамоїл)піролідин-1-карбоксилат До розчину (3-хлорпіразин-2-іл)метанамінHCl (9,57 г, 21,26 ммоль, 40 % ваг.) і Z-Pro-OH (5,3 г, 21,26 ммоль) у дихлорметані (250 мл) додавали триетиламін (11,85 мл, 85 ммоль) і реакційну суміш охолоджували до 0 °C. Через 15 хвилин перемішування при 0 °C додавали HATU (8,49 г, 22,33 ммоль). Суміш перемішували протягом 1 години при 0 °C і потім протягом ночі при кімнатній температурі. Суміш промивали 0,1M розчином HCl, 5 % розчином NaHCO3, водою і насиченим сольовим розчином, сушили над сульфатом натрію і концентрували у вакуумі. Продукт очищали з використанням хроматографії на силікагелі (гептан/етилацетат=1/4 об./об. %) з одержанням 5 г (S)-бензил-2-((3-хлорпіразин-2-іл)метилкарбамоїл)піролідин-1карбоксилату (62,7 %). (c) (S)-бензил-2-(8-хлорімідазо[1,5-a]піразин-3-іл)піролідин-1-карбоксилат (S)-бензил-2-((3-хлорпіразин-2-іл)метилкарбамоїл)піролідин-1-карбоксилат (20,94 ммоль, 7,85 г) розчиняли в ацетонітрилі (75 мл), додавали 1,3-диметил-2-імідазолідинон (62,8 ммоль, 6,9 мл, 7,17 г) і реакційну суміш охолоджували до 0C перед додаванням POCl3 (84 ммоль, 7,81 мл, 12,84 г) по краплях, підтримуючи при цьому температуру близько 5C. Реакційну суміш кип'ятили зі зворотним холодильником при 60-65 °C протягом ночі. Реакційну суміш виливали обережно в 25 % розчин гідроксиду амонію у воді (250 мл)/колотий лід (500 мл) з одержанням жовтої суспензії (pН ~8-9), яку перемішували протягом 15 хвилин доти, поки в суспензії більше не залишалося льоду. Додавали етилацетат, шари розділяли і водний шар екстрагували етилацетатом (3×). Органічні шари об'єднували і промивали насиченим сольовим розчином, сушили над сульфатом натрію, фільтрували й упарювали з одержанням 7,5 г неочищеного продукту. Неочищений продукт очищали з використанням хроматографії на силікагелі (гептан/етилацетат=1/4 об./об. %) з одержанням 6,6 г (S)-бензил-2-(8-хлорімідазо[1,5-a]піразин3-іл)піролідин-1-карбоксилату (88 %). (d) (S)-бензил-2-(1-бром-8-хлорімідазо[1,5-a]піразин-3-іл)піролідин-1-карбоксилат 21 UA 115312 C2 5 10 15 20 25 30 35 40 N-бромсукцинімід (24,69 ммоль, 4,4 г) додавали до перемішуваного розчину (S)-бензил-2-(8хлорімідазо[1,5-a]піразин-3-іл)піролідин-1-карбоксилату (24,94 ммоль, 8,9 г) у DMF (145 мл). Реакційну суміш перемішували 3 години при кімнатній температурі. Суміш виливали (повільно) у перемішувану суміш води (145 мл), етилацетату (145 мл) і насиченого сольового розчину (145 мл). Суміш потім переносили в ділильну лійку й екстрагували. Водний шар екстрагували за допомогою 2×145 мл етилацетату. Об'єднані органічні шари промивали за допомогою 3×300 мл води, 300 мл насиченого сольового розчину, сушили над сульфатом натрію, фільтрували й упарювали. Продукт очищали з використанням хроматографії на силікагелі (етилацетат/гептан=3/1 об./об. %) з одержанням 8,95 г (S)-бензил-2-(1-бром-8-хлорімідазо[1,5a]піразин-3-іл)піролідин-1-карбоксилату (82,3 %). (e) (S)-бензил-2-(8-аміно-1-бромімідазо[1,5-a]піразин-3-іл)піролідин-1-карбоксилат (S)-бензил-2-(1-бром-8-хлорімідазо[1,5-a]піразин-3-іл)піролідин-1-карбоксилат (20,54 ммоль, 8,95 г) суспендували в 2-пропанолі (113 мл) у посудині високого тиску. 2-Пропанол (50 мл) охолоджували до -78C у попередньо зваженій колбі (із пробкою і магнітним стрижнем) і завантажували газоподібний аміак (646 ммоль, 11 г) протягом 15 хвилин. Одержаний розчин додавали до суспензії в посудині високого тиску. Посудину закривали і перемішували при кімнатній температурі і спостерігали невелике збільшення тиску. Потім суспензію нагрівали до 2 110 °C, що приводило до підвищення тиску до 4,5 барів (4,589 кг/см ). Чистий розчин перемішували при 110 °C, 4,5 барах протягом ночі. Через 18 годин тиск залишався 4 бари. Реакційну суміш концентрували у вакуумі, залишок суспендували в етилацетаті і далі промивали водою. Шари розділяли і водний шар екстрагували етилацетатом. Об'єднані органічні шари промивали водою, насиченим розчином хлориду натрію, сушили над сульфатом натрію і концентрували з одержанням 7,35 г (S)-бензил-2-(8-аміно-1-бромімідазо[1,5-a]піразин-3іл)піролідин-1-карбоксилату (86 %). Проміжна сполука 2 (S)-4-(8-аміно-3-(піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2-іл)бензамід (a) (S)-бензил-2-(8-аміно-1-(4-(піридин-2-ілкарбамоїл)феніл)імідазо[1,5-a]піразин-3іл)піролідин-1-карбоксилат (S)-бензил-2-(8-аміно-1-бромімідазо[1,5-a]піразин-3-іл)піролідин-1-карбоксилат (0,237 ммоль, 98,5 мг) і 4-(піридин-2-іламінокарбоніл)-бензолборонову кислоту (0,260 ммоль, 63,0 мг) суспендували в суміші 2N водного розчину карбонату калію (2,37 ммоль, 1,18 мл) і діоксану (2,96 мл). Азот барботували через суміш з наступним додаванням 1,1'біс(дифенілфосфіно)фероценпаладій(ІІ)хлориду (0,059 ммоль, 47,8 мг). Реакційну суміш нагрівали протягом 20 хвилин при 140 °C у мікрохвильовій печі. У реакційну суміш додавали воду з наступною екстракцією етилацетатом (2×). Об'єднаний органічний шар промивали насиченим сольовим розчином, сушили над сульфатом магнію й упарювали. Продукт очищали з використанням силікагелю і суміші дихлорметан/метанол=9/1 об./об. % як елюенту з одержанням 97,1 мг (S)-бензил-2-(8-аміно-1-(4-(піридин-2-ілкарбамоїл)феніл)імідазо[1,5a]піразин-3-іл)піролідин-1-карбоксилату (77 %). (b) (S)-4-(8-аміно-3-(піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2-іл)бензамід До (S)-бензил-2-(8-аміно-1-(4-(піридин-2-ілкарбамоїл)феніл)імідазо[1,5-a]піразин-3іл)піролідин-1-карбоксилату (0,146 ммоль, 78 мг) додавали розчин 33 % бромистоводнева 22 UA 115312 C2 5 10 15 20 25 кислота/оцтова кислота (11,26 ммоль, 2 мл) і суміш залишали при кімнатній температурі протягом 1 години. Суміш розбавляли водою й екстрагували дихлорметаном. Водну фазу нейтралізували з використанням 2N розчину гідроксиду натрію і потім екстрагували дихлорметаном. Органічний шар сушили над сульфатом магнію, фільтрували й упарювали з одержанням 34 мг (S)-4-(8-аміно-3-(піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензаміду (58 %). (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(піридин-2-іл)бензамід До розчину (S)-4-(8-аміно-3-(піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензаміду (0,626 ммоль, 250 мг) у дихлорметані (25 мл) при 0 °C додавали триетиламін (0,626 ммоль, 0,087 мл, 63,3 мг) і по краплях додавали акрилоїлхлорид (0,657 ммоль, 0,053 мл, 59,5 мг). Одержану суміш перемішували при 0 °C протягом 2 годин. Суміш промивали водою, сушили над сульфатом магнію. Після упарювання залишок очищали за допомогою препаративної ВЕРХ. Фракції, що містять продукт, збирали і ліофілізували з одержанням 126 мг (S)-4-(3-(1-акрилоїлпіролідин-2-іл)-8-аміноімідазо[1,5-a]піразин-1-іл)-N-(піридин-2-іл)бензаміду + (44,4 % вихід). Дані: UPLC (C) Rt: 1,50 хв.; m/z 454,3 (M+H) . (S,E)-4-(8-аміно-3-(1-(4-(піролідин-1-іл)бут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(піридин-2-іл)бензамід До розчину (S)-4-(8-аміно-3-(піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензаміду (проміжна сполука 2b, 19,7 мг, 0,049 ммоль), триетиламіну (20 мг, 0,197 ммоль, 0,027 мл) і гідрохлориду (E)-4-(піролідин-1-іл)бут-2-енової кислоти (9,45 мг, 0,049 ммоль) у дихлорметані (2 мл) додавали HATU (18,75 мг, 0,049 ммоль). Суміш перемішували протягом 30 хвилин при кімнатній температурі. Суміш промивали водою, сушили над сульфатом магнію і концентрували у вакуумі. Залишок очищали за допомогою препаративної ВЕРХ. Фракції, що містять продукт, збирали й упарювали досуха з одержанням 7,1 мг (S, E)-4-(8-аміно-3-(1-(4(піролідин-1-іл)бут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2-іл)бензаміду + (26,8 % вихід). Дані: UPLC (C) Rt: 1,25 хв.; m/z 537,4 (M+H) . 23 UA 115312 C2 5 10 15 (S,E)-4-(8-аміно-3-(1-(4-(диметиламіно)бут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(піридин-2-іл)бензамід Цю сполуку одержували способом, аналогічним описаному у Прикладі 2, зі сполуки, описаної в проміжній сполуці 2b, і (E)-4-(диметиламіно)бут-2-енової кислоти, з одержанням + зазначеної в заголовку сполуки (11,8 мг, 46,6 %). Дані: UPLC (C) Rt: 1,29 хв.; m/z 511,0 (M+H) . Проміжна сполука 3 (E)-4-метоксибут-2-енова кислота Метоксид натрію (30 %/метанол, 30,3 ммоль, 5,68 мл) додавали через скляний шприц до перемішуваного розчину 4-бромкротонової кислоти (6,06 ммоль, 1 г) у метанолі (60 мл) при кімнатній температурі. Ясно-жовтий розчин перемішували протягом 30 хвилин при кімнатній температурі і протягом 2 годин при кип'ятінні зі зворотним холодильником. Після охолодження реакційної суміші розчинник видаляли при зниженому тиску. Залишок розподіляли між водою (50 мл) і діетиловим ефіром (50 мл). Додавали 2M водний розчин гідрохлориду (3,5 мл) доти, поки рН не досягав ~1. Водний шар відділяли й екстрагували діетиловим ефіром (3×20 мл). Об'єднані органічні шари промивали насиченим сольовим розчином, сушили над сульфатом натрію, фільтрували і концентрували у вакуумі, з одержанням 650 мг (E)-4-метоксибут-2-енової кислоти (92 %). 20 25 (S,E)-4-(8-аміно-3-(1-(4-метоксибут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піридин-2-іл)бензамід Цю сполуку одержували способом, аналогічним описаному у Прикладі 2, зі сполуки, описаної в проміжній сполуці 2b, і (E)-4-метоксибут-2-енової кислоти (проміжна сполука 3), з одержанням зазначеної в заголовку сполуки (11 мг, 29,9 %). Дані: UPLC (C) Rt: 1,58 хв.; m/z + 498,3 (M+H) . 24 UA 115312 C2 5 10 (S)-4-(8-аміно-3-(1-(2-хлорпіримідин-4-карбоніл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N(піридин-2-іл)бензамід Цю сполуку одержували способом, аналогічним описаному у Прикладі 2, зі сполуки, описаної в проміжній сполуці 2b, і 2-хлорпіримідин-4-карбонової кислоти, з одержанням + зазначеної в заголовку сполуки (8,3 мг, 40,4 %). Дані: UPLC (C) Rt: 1,64 хв.; m/z 540,1 (M+H) . (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(піридин-2іл)бензамід Цю сполуку одержували способом, аналогічним описаному у Прикладі 2, зі сполуки, описаної в проміжній сполуці 2b, і 2-бутинової кислоти, з одержанням зазначеної в заголовку + сполуки (10,5 мг, 18,0 %). Дані: LCMS (B) Rt: 2,08 хв.; m/z 466,1 (M+H) . Проміжна сполука 4 15 20 N-(4-фторпіридин-2-іл)-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)бензамід (a) 4-(4,4,5,5-Тетраметил-1,3,2-діоксаборолан-2-іл)бензоїлхлорид До холодного (0 °C) розчину 4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)бензойної кислоти (40,3 ммоль, 10,01 г) у дихлорметані (206 мл) додавали каталітичну кількість DMF. Розчин оксалілхлориду (101 ммоль, 8,66 мл, 12,8 г) додавали по краплях. Після перемішування 25 UA 115312 C2 5 10 протягом 30 хвилин при 0 °C реакційну суміш залишали нагріватися до кімнатної температури і суміш перемішували протягом додаткових 3 годин. Реакційну суміш концентрували з одержанням 10,9 г неочищеного 4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)бензоїлхлориду (101 %). (b) N-(4-фторпіридин-2-іл)-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)бензамід До розчину 4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)бензоїлхлориду (1,688 ммоль, 450 мг) в ацетонітрилі (24,8 мл) додавали 2-аміно-4-фторпіридин (4,22 ммоль, 473 мг). Реакційну суміш перемішували при кімнатній температурі протягом 1,5 години. Реакційну суміш концентрували до невеликого об'єму, додавали 3 % водний розчин лимонної кислоти (18 мл) і суміш екстрагували дихлорметаном (2×15 мл). Об'єднаний органічний шар промивали 3 % водним розчином лимонної кислоти, сушили над сульфатом магнію, фільтрували й упарювали з одержанням 542,2 мг N-(4-фторпіридин-2-іл)-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2іл)бензаміду (94 %) у вигляді не зовсім білої твердої речовини. Проміжна сполука 5 15 20 25 (S)-4-(8-аміно-3-(піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-фторпіридин-2-іл)бензамід Цю проміжну сполуку одержували способом, аналогічним описаному для проміжної сполуки 2b, з (S)-бензил-2-(8-аміно-1-бромімідазо[1,5-a]піразин-3-іл)піролідин-1-карбоксилату (проміжна сполука 1e) і N-(4-фторпіридин-2-іл)-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)бензаміду (проміжна сполука 4b), з одержанням зазначеної в заголовку сполуки (331 мг, 93 %). (S,E)-4-(8-аміно-3-(1-(4-(диметиламіно)бут-2-еноїл)піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)N-(4-фторпіридин-2-іл)бензамід Цю сполуку одержували способом, аналогічним описаному у Прикладі 2, зі сполуки, описаної в проміжній сполуці 5, і (E)-4-(диметиламіно)бут-2-енової кислоти, з одержанням + зазначеної в заголовку сполуки (33,4 мг, 54,1 %). Дані: UPLC (C) Rt: 1,72 хв.; m/z 529,3 (M+H) . Проміжна сполука 6 26 UA 115312 C2 5 10 15 20 N-(4-метилпіридин-2-іл)-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)бензамід До перемішуваного розчину 4-метилпіридин-2-аміну (7,86 ммоль, 850 мг) у ТГФ (50 мл) при кімнатній температурі додавали по краплях розчин 1M LiHMDS у ТГФ (8,0 ммоль, 8 мл). Коли реакційна суміш ставала темно-зеленою, додавали по краплях розчин 4-(4,4,5,5-тетраметил1,3,2-діоксаборолан-2-іл)бензоїлхлориду (9,6 ммоль, 2,56 г) у дихлорметані (55 мл). Суміш перемішували при кімнатній температурі протягом 2,5 годин і потім концентрували. Додавали 3 % водний розчин лимонної кислоти (18 мл) і суміш екстрагували дихлорметаном (2×15 мл). Об'єднаний органічний шар промивали 3 % водним розчином лимонної кислоти, сушили над сульфатом магнію, фільтрували й упарювали. Залишок розчиняли в ТГФ (15 мл) і додавали 6M розчин NaOH (15 мл). Суміш перемішували протягом 4 годин при кімнатній температурі. Додавали етилацетат і шари розділяли. Органічний шар промивали водою і насиченим сольовим розчином, сушили над сульфатом натрію, фільтрували й упарювали. Залишок очищали за допомогою хроматографії на силікагелі (елюент: DCM/MeOH=98/2 до DCM/MeOH=95/5) з одержанням 1,1 г N-(4-метилпіридин-2-іл)-4-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)бензаміду (40,7 %). Проміжна сполука 7 (S)-4-(8-аміно-3-(піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-метилпіридин-2-іл)бензамід Цю проміжну сполуку одержували способом, аналогічним описаному для проміжної сполуки 2, з (S)-бензил-2-(8-аміно-1-бромімідазо[1,5-a]піразин-3-іл)піролідин-1-карбоксилату (проміжна сполука 1e) і N-(4-метилпіридин-2-іл)-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)бензаміду (проміжна сполука 6), з одержанням зазначеної в заголовку сполуки (125,5 мг, 82 %). 27 UA 115312 C2 5 10 (S)-4-(8-аміно-3-(1-бут-2-иноїлпіролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-метилпіридин-2іл)бензамід Цю сполуку одержували способом, аналогічним описаному у Прикладі 2, з (S)-4-(8-аміно-3(піролідин-2-іл)імідазо[1,5-a]піразин-1-іл)-N-(4-метилпіридин-2-іл)бензаміду (проміжна сполука7) і 2-бутинової кислоти, з одержанням зазначеної в заголовку сполуки (6,3 мг, 27,2 %). Дані: UPLC + (C) Rt: 1,56 хв.; m/z 480,3 (M+H) . Проміжна сполука 8 N-(4-пропілпіридин-2-іл)-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)бензамід Цю сполуку одержували способом, аналогічним описаному для проміжної сполуки 6, виходячи з 4-пропілпіридин-2-аміну, з одержанням зазначеної в заголовку сполуки (371,5 мг, 54,1 %). Проміжна сполука 9 28
ДивитисяДодаткова інформація
Назва патенту англійською4-imidazopyridazin-1-yl-benzamides and 4-imidazotriazin-1-yl-benzamides as btk- inhibitors
Автори англійськоюBarf, Tjeerd A., Jans, Christiaan, Gerardus, Johannes, Maria, Man, de Adrianus, Petrus, Antonius, Oubrie, Arthur A., Raaijmakers, Hans C.A., Rewinkel, Johannes, Bernardus, Maria, Sterrenburg, Jan-Gerard, Wijkmans, Jacobus C. H. M.
Автори російськоюБарф Тьерд А., Янс Христиан Герардус Йоханнес Мария, Ман де Адрианус Петрус Антониус, Аубри Артур А., Раймакерс Ханс К.А., Ревинкел Йоханнес Бернардус Мария, Стерренбург Ян-Герард, Вейкманс Якобус К. Х. М.
МПК / Мітки
МПК: A61K 31/4985, C07D 519/00, C07D 487/04
Мітки: втк-інгібітори, 4-імідазотриазин-1-ілбензаміди, 4-імідазопіридазин-1-ілбензаміди
Код посилання
<a href="https://ua.patents.su/85-115312-4-imidazopiridazin-1-ilbenzamidi-i-4-imidazotriazin-1-ilbenzamidi-yak-vtk-ingibitori.html" target="_blank" rel="follow" title="База патентів України">4-імідазопіридазин-1-ілбензаміди і 4-імідазотриазин-1-ілбензаміди як втк-інгібітори</a>
Попередній патент: Геміфумарат тенофовіру алафенаміду
Наступний патент: Пристрій для аналізу проб
Випадковий патент: Спосіб профілактики та лікування доброякісних дисплазій молочних залоз у жінок з ранніми втратами вагітності












