Застосування сполук діосметину у лікуванні і запобіганні тромботичним патологіям
Номер патенту: 91848
Опубліковано: 10.09.2010
Автори: Сансільвестрі-Морель Патрісія, Вієрзбікі Мішель, Рюпен Ален, Буссар Марі-Франсуаз, Верберен Тоні, Валлє Марі-Оділь
Формула / Реферат
1. Застосування сполук діосметину формули (І)
 , (I)
, (I)
в якій:
R1 являє собою атом водню або радикал пропілу або алілу;
R2 являє собою атом водню або радикал пропілу, алілу, 2,3-дигідроксипропілу, (2,2-диметил-1,3-діоксол-4-іл)метилу або 3-ацетилокси-2-гідроксипропілу;
R3 являє собою атом водню або радикал пропілу або алілу;
R4 являє собою атом водню або радикал метилу, пропілу, алілу, 2,3-дигідроксипропілу або (2,2-диметил-1,3-діоксол-4-іл)метилу або радикал формули -COR'4, в якій R'4 являє собою лінійний або розгалужений (С1-С5)алкільний радикал або радикал фенілу;
R5 являє собою атом водню або радикал пропілу або алілу, і
R6 являє собою атом водню або радикал метилу, пропілу, алілу, 2,3-дигідроксипропілу або (2,2-диметил-1,3-діоксол-4-іл)метилу, радикал формули -COR'6 (в якій R'6 являє собою лінійний або розгалужений (С1-С5)алкільний радикал або радикал фенілу) або радикал формули (I’):
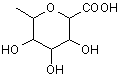 , (I’)
, (I’)
за умови, що:
щонайменше одна з груп R1, R2, R3, R4, R5 і R6 є іншою, ніж атом водню, і
якщо R1, R2 і R3 кожний одночасно являє собоюатом водню, тоді R4 також являє собою атом водню,
їх діастереоізомерів та енантіомерів, а також адитивних солей з фармацевтично прийнятною кислотою або основою,
в одержанні фармацевтичних композицій, призначених для запобігання і/або лікування тромботичних патологій.
2. Застосування 6,8-діаліл-5,7-дигідроксі-2-(2-аліл-3-гідрокси-4-метоксифеніл)-4Н-1-бензопіран-4-ону формули (XVII):
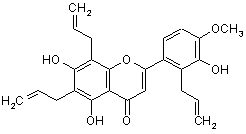 (XVII)
(XVII)
в одержанні фармацевтичних композицій, призначених для запобігання і/або лікування тромботичних патологій.
3. Застосування сполук діосметину за п. 1 або 2 в одержанні фармацевтичних композицій, призначених для запобігання і/або лікування патологій з ризиком тромбозу.
4. Застосування сполук діосметину за будь-яким з пп. 1-3 в одержанні фармацевтичних композицій для орального введення, призначених для запобігання і/або лікування тромботичних патологій або патологій з ризиком тромбозу.
5. Застосування сполук діосметину за будь-яким з пп. 1-4 в комбінації з одним або більше фармацевтично прийнятними наповнювачами в одержанні фармацевтичних композицій, призначених для запобігання і/або лікування тромботичних патологій або патологій з ризиком тромбозу.
6. Фармацевтична композиція, яка містить сполуку діосметину за будь-яким з пп. 1-3 в комбінації з одним або більше фармацевтично прийнятними наповнювачами, призначена для запобігання і/або лікування тромботичних патологій або патологій з ризиком тромбозу.
Текст
1. Застосування сполук діосметину формули (І) 2 3 91848 4 гання і/або лікування тромботичних патологій або патологій з ризиком тромбозу. 5. Застосування сполук діосметину за будь-яким з пп.1-4 в комбінації з одним або більше фармацевтично прийнятними наповнювачами в одержанні фармацевтичних композицій, призначених для запобігання і/або лікування тромботичних патологій або патологій з ризиком тромбозу. 6. Фармацевтична композиція, яка містить сполуку діосметину за будь-яким з пп.1-3 в комбінації з одним або більше фармацевтично прийнятними наповнювачами, призначена для запобігання і/або лікування тромботичних патологій або патологій з ризиком тромбозу. Даний винахід стосується застосування сполук діосметину в одержанні фармацевтичних композицій, призначених для запобігання і/або лікування тромботичних патологій і патологій з ризиком тромбозу. Винахід стосується, зокрема, застосування сполуки діосметину 6,8-діаліл-5,7-дигідрокси-2-(2аліл-3-гідрокси-4-метоксифеніл)-4Н-1-бензопіран4-ону в одержанні фармацевтичних композицій, призначених для запобігання і/або лікування тромботичних патологій. Фізіологічний процес гемостазу ініціюється несприятливою зміною в ендотеліальних клітинах кровоносних судин, або через несуттєві причини або через більш складні патологічні причини. Його метою є блокувати і перешкоджати виділенню крові за допомогою двох шляхів, які відмінні один від одного, але пов'язані і залежні один від одного: первинний гемостаз і коагуляція плазми. Первинно гемостаз є допоміжним механізмом, який залучає циркулюючі тромбоцити, що прилипають до ендотелію, щоб утворити білий тромб або тромбоцитарну пробку. Окрім того, тромбоцитарний тромб укріплюється утворенням сітки фібрину, що охоплює агреговані тромбоцити своїми нитками. Нерозчинний фібрин генерується, починаючи з розчинного білка плазми крові, фібриногену, під дією тромбіну, кінцевого продукту каскаду ферментатичної активації системи коагуляції. Нарешті, фібриновий/тромбоцитарний тромб резорбується за допомогою явища фібринолізу. Фактично, через свою здатність зменшувати кількість фібрину в судинному кругообігу, фібриноліз дозволяє тілу "битись" з появою тромбозів, також як і руйнувати тромб, що початково зупинив кровотечу. Фібриноліз головним чином залучає плазмін, протеолітичний фермент, який розбиває довгі ланцюги полімеризованого фібрину на D-димери. Цей фермент присутній у плазмі у формі зимогену, плазміногену, який активується в плазмін різними сериновими протеазами, присутніми на поверхні фібринового/тромбоцитарного згустку. Ці серинові протеази є, зокрема, активаторами плазміногену тканинного типу (t-PA), які по суті вивільняються активованими ендотеліальними клітинами, і типу урокінази (u-ΡΑ), чиє вивільнення у формі проурокіназ є набагато більш повсюдним. Фібриноліз є сам негативно регульованою трикомпонентною системою, яка включає інгібітори плазміну (α2-антиплазмін і α2-макроглобулін), інгібітори активації плазміногену (РАІ-1 або Інгібітор Активатора Плазміногену типу 1; РАІ-2) та інгібітор тромбін-активовуваного фібринолізу (TAFI). Головний інгібітор активатора плазміногену являє собою РАІ-1. Білок РАІ-1, який належить до суперсімейства серпінів (інгібітори серинової протеази), являє собою глікопротеїн 379 амінокислот (47кДа) з нестачею цистеїну, але дуже багатий на залишки метіоніну. Білок РАІ-1, який продукується численними типами клітин, таких як ендотеліальні клітини, моноцити, гепатоцити, фібробласти, адипоцити і мегакаріоцити, присутній в плазмі і тромбоцитах. Активна ділянка РАІ-1, розміщена в С346 347 кінці білка у положенні (Arg -Met ), поводить себе як псевдосубстрат для активаторів плазміногену тканинного типу. Головними мішенями білків РАІ-1 є, таким чином, t-PA і u-РА. Беручи до уваги механізми, які регулюють гемостаз і фібриноліз, в масштабі тіла цілком, було виявлено позитивний взаємозв'язок між підвищеним рівнем РАІ-1 і збільшеним ризиком венозних і артеріальних тромбозів. Цей позитивний взаємозв'язок повідомляється, зокрема, у випадку патологій, чиїм походженням є венозний або артеріальний тромбоз, таких як інфаркт міокарда (Hamsten et al. Plasminogen activator inhibitor in plasma: risk factor for recurrent myocardial infarction, 1987, Lancet 2, 3-9), стенокардія (Wieczorek et al. Tissuetype plasminogen activator and tissue plasminogen activator inhibitor activities as predictor of adverse events in unstable angina, 1994, Am J Cardiol, 74, 424-429), переміжна кульгавість, інсульт, тромбоз глибоких вен (Schulman et al. The significance of hypofibrinolysis for the risk of venous thromboembolism, 1996, Thromb Haemost, 75, 307611), легенева емболія, а також патології, при яких збільшується ризик тромбозів, такі як гіпертензія, гіперхолестеринемія, діабет, ожиріння, генетичні аномалії коагуляції крові або набуті аномалії коагуляції крові. Плазмовий рівень РАІ-1, фактично, підіймається на 30% у пацієнтів, які хворі на венозну тромбоемболію (Tabernero ef al. Incidence of increased plasminogen activator inhibitor in patients with deep venous thrombosis and/or pulmonary embolism, 1989, Thromb Res, 56, 565-570). Наслідком цього є загальна дисфункція фібринолітичної системи і 5 особливо падіння t-PA. Такі ж спостереження були зроблені відносно пацієнтів, які страждають на легеневу гіпертензію, що є результатом емболії (Huber et al. Fibrinogen, t-PA and PAI-1 plasma levels in patients with primary pulmonary hypertension, 1994, Am J Grit Care Med, 150, 929933). У цьому конкретному випадку, зростання рівня РАІ-1 відбувається завдяки ендотеліальним клітинам, розташованим в зоні тромбозу, які проявляють збільшення у вивільненні РАІ-1, що асоційоване з індукуванням або тромбіном, або посередником, який вивільняється тромбоцитами. За умови, що збільшений рівень РАІ-1 є шкідливим в контексті серцево-судинних синдромів, вважалось, що відновлення нормальної фібринолітичної активності повинне запобігти появі тромботичних подій у пацієнтів з таким ризиком. Регулювання процесу фібринолізу, відповідно, складає центральну проблему у медичних серцево-судинних патологіях. Антикоагулянти і антитромбоцити складають звичайне лікування при різноманітних серцевосудинних патологіях. їх значення в контексті запобігання серцево-судинним випадкам, а також для серцево-судинних критичних станів, демонструвалось на епідеміологічних дослідженнях. Однак, співвідношення ризик/перевага повинне завжди бути урівноважене через те, що ці випадки, асоційовані з антикоагулянтами і антитромбоцитами, знаходяться під впливом кровотеч, що може поставити під питання функціональний або життєвий прогноз. Дійсно, головне ускладнення антикоагулянтного і антитромбоциатрного лікування являє собою кровотечу. Антикоагулянти, які вводять парентеральним шляхом, являють собою, зокрема, нефракціонований гепарин (NFH), фракціоновані гепарини (LMWH) і сінкумар (Sintrom®). Епідеміологічні дослідження показали, що терапевтичний клас фракціонованих і нефракціонованих гепаринів в контексті лікування тромбоемболічного приступу викликає значну кровотечу у від 0 до 7% випадків зі смертністю в діапазоні від 0 до 2%. Антикоагулянт Sintrom®, розроблений при профілактичному і радикальному лікуванні тромбоемболічних симптомів, також призводить до значних геморагічних подій, які загрожують життю, у до 2,2% випадків. Беручи до уваги критичне зростання геморагічних ризиків при комбінації Sintrom® з антитромбоцитом, таким як аспірин, співвідношення ризик/перевага цієї комбінації не повинне недооцінюватись, коли робиться вибір терапевтичного лікування. Були розроблені останні лікування, які мали фібринолітичну або тромболітичну дію; вони прискорюють розчинення внутрішньосудинних згустків за допомогою сприяння перетворенню неактивного плазміногену в активний плазмін (Marder VJ., Thrombolytic therapy: foundations and clinical results in «Haemostasis and Thrombosis», Fourth Edition 2001, Editors Colman RW et al.). Ці фібринолiтичні або тромболітичні засоби вводять виключно паре 91848 6 нтеральним шляхом, або загальним внутрішньовенним шляхом в перфузії або як болюсне введення, або місцевим, наприклад інтракоронарним або внутрішньоартеріальним шляхом. Ці фармацевтичні композиції повинні, крім того, бути введені якомога скоріше після утворення тромбу для того, щоб спробувати розчинити його і таким чином видалити закупорку в судині. Ці нові тромболітичні засоби, відповідно, складаються з аналогів тканинного активатора плазміногену або t-PA, такого як, наприклад: альтеплаза, яку одержують за допомогою генної інженерії, і вона є ідентичною tPA; ретеплаза, яка являє собою спрощений аналог людського t-PA; або тенектеплаза, яка являє собою рекомбінантний білок, подібний до ендогенного t-PA і який має більшу афінність до фібрину тромбу. Ці фібринолітичні засоби швидко показали свої обмеження щодо їх застосування у лікарнях швидкої допомоги і проблеми з їх введенням, наприклад, введення катетера в тромбовану артерію. Інші потенційні лікування розглядались для того, щоб змінити рівень РАІ-1, збільшення якого корелює з тромбоемболічними випадками. Зокрема, були розроблені моноклональні антитіла як інгібітори активності РАІ-1. МАІ 12 являє собою мишаче антитіло, специфічне до людського РАІ-1, який не перешкоджає або РАІ-2 або t-PA або α2антиплазміну. За допомогою блокування взаємодії РАІ-1 з t-РА, це моноклональне антитіло збільшує фібриноліз in vitro та in vivo (Levi et al. Inhibition of plasminogen activator inhibitor-1 activity results in promotion of endogenous thrombolysis and inhibition of thrombus extension in models of experimental thrombosis, 1992, Circulation, 85, 305-312). У випадку моноклонального антитіла CLB-2C, це антитіло зв'язується між позиціями 128 і 145 в амінокислотній послідовності вітронектину і, відповідно, запобігає зв'язуванню білка РАІ-1, таким чином прискорюючи його інактивацію. Незважаючи на ефективність цих моноклональних антитіл на in vitro і in vivo моделях, ці специфічні інгібітори РАІ-1 не можна використовувати з медичної точки зору, через труднощі, асоційовані з відсутністю гуманізації антитіл, ризиками імуногенності і витратами на розробку. Даний винахід, відповідно, націлений на пропонування альтернативної стратегії до вже доступних механізмів удосконалення фібринолізу, з метою запобіжного і радикального лікування тромботичних патологій, з метою подолати, щонайменше частково, недоліки відомого лікування тромбоемболічних випадків. Ця альтернативна стратегія основується на інгібуванні експресії гена РАІ-1. Для цього як винахід пропонується застосування сполук діосметину в одержанні фармацевтичних композицій, призначених для запобігання і/або лікування тромботичних патологій. Сполуки діосметину відповідно до винаходу являють собою сполуки загальної формули (І): 7 91848 (І) в якій: - R1 являє собою атом водню або радикал пропілу або алілу; - R2 являє собою атом водню або радикал пропілу, алілу, 2,3-дигідроксипропілу, (2,2диметил-1,3-діоксол-4-іл)метилу або 3-ацетил окси-2-гідроксипропілу; - R3 являє собою атом водню або радикал пропілу або алілу; - R4 являє собою атом водню або радикал метилу, пропілу, алілу, 2,3-дигідроксипропілу або (2,2-диметил-1,3-діоксол-4-іл)метилу або радикал формули -COR'4, в якій R'4 являє собою лінійний або розгалужений (С1-С5)алкільний радикал або радикал фенілу; - R5 являє собою атом водню або радикал пропілу або алілу, і - R6 являє собою атом водню або радикал метилу, пропілу, алілу, 2,3-дигідроксипропілу або (2,2-диметил-1,3-діоксол-4-іл)метилу, радикал формули -СОR'6 (в якій R'6 являє собою лінійний або розгалужений (С1-С5)алкільний радикал, або радикал фенілу) або радикал формули (І'): (І') за умови, що: - щонайменше одна з груп R1, R2, R3, R4, R5 і R6 є іншою, ніж атом водню і, - якщо R1, R2 і R3 кожний одночасно являють собою атом водню, тоді R4 також являє собою атом водню, їх діастереоізомери та енантіомери, а також адитивні солі з фармацевтично прийнятною кислотою або основою. Одержання сполук загальної формули (І) розкрито в описі патенту ЕР 0 709 383. Більш конкретно, сполуки діосметини, застосовані відповідно до даного винаходу, являють собою наступні сполуки, розкриті в описі патенту ЕР 0 709 383, формул (II)-(XVII): (II) 7-алілокси-5-гідрокси-2-(3-гідрокси-4метоксифеніл)-4Н-І-бензопіран-4-он 8 (ІІІ) (IV) (R,S)-5-гідрокси-2-(3-гідрокси-4метоксифеніл)-7-(2,3-дигідроксипропіл-окси)-4Н-1бензопіран-4-он (IV) (V) 5,7-ди-(2,3-Дигідроксипропілокси)-2-(3гідрокси-4-метоксифеніл)-4Н-1-бензопіран-4-он (V) (VI) 5-гідрокси-2-(4-метокси-3півалоїлоксифеніл)-7-(2,3-дигідроксипропіл-окси)4Н-1-бензопіран-4-он (VI) (VII) 5-алілокси-2-(3-алілокси-4-метоксифеніл)7-(2,3-дигідроксипропіл-окси)-4Н-1-бензопіран-4-он (VII) (VIII) 6-аліл-5-гідрокси-2-(2-аліл-3-гідрокси-5метоксифеніл)-7-(2,3-дигідроксипропілокси)-4Н-1бензопіран-4-он (VIII) (IX) 5-гідрокси-2-(3-гідрокси-4-метокси-2пропілфеніл)-6-пропіл-7-(2,3дигідроксипропілокси)-4Н-1-бензопіран-4-он (ІІ) (IX) (III) 5,7-дигідрокси-2-[3-(2,3дигідроксипропілокси)-4-метоксифеніл]-4Н-1бензопіран-4-он (X) (R,S)-5-гідрокси-2-(3-гідрокси-4-метокси-2пропілфеніл)-7-(2,3-дигідроксипропілокси)-4Н-1бензопіран-4-он 9 91848 10 (X) (І) (XI) (R)-5-гідрокси-2-(3-гідрокси-4-метокси-2пропілфеніл)-7-(2,3-дигідроксипропілокси)-4Н-1бензопіран-4-он (XII) (S)-5-гідрокси-2-(3-гідрокси-4-метокси-2пропілфеніл)-7-(2,3-дигідроксипропілокси)-4Н-1бензопіран-4-он (XIII) (R,S)-5-гідрокси-2-(3-гідрокси-4-метокси2-пропілфеніл)-7-(3-ацетилокси-2гідроксипропілокси)-4Н-1-бензопіран-4-он (XIII) (XIV) 5-гідрокси-2-[4-метокси-2-пропіл-3-(6карбокси-3,4,5-тригідрокси-тетрагідропіран-2-ілокси)феніл]-7-(2,3-дигідроксипропілокси)-4Н-1бензопіран-4-он (XIV) (XV) 5-гідрокси-2-[4-метокси-3-(2,3дигідроксипропілокси)феніл]-7-(2,3дигідроксипропілокси)-4Н-1-бензопіран-4-он (XV) (XVI) 5,7-дигідрокси-2-(3-гідрокси-4-метокси-2пропілфеніл)-6,8-дипропіл-4Н-1-бензопіран-4-он (XVI) Більш переважно, переважна сполука формули (І) відповідно до даного винаходу являє собою 6,8-діаліл-5,7-дигідрокси-2-(2-аліл-3-гідрокси-4метоксифеніл)-4Н-1-бензопіран-4-он формули (XVII): (XVII) Даний винахід, відповідно, стосується застосування сполук діосметину формули (І): в якій: - R1являє собою атом водню або радикал пропілу або алілу; - R2 являє собою атом водню або радикал пропілу, алілу, 2,3-дигідроксипропілу, (2,2диметил-1,3-діоксол-4-іл)метилу або 3-ацетил окси-2-гідроксипропілу; - R3 являє собою атом водню або радикал пропілу або алілу; - R4 являє собою атом водню або радикал метилу, пропілу, алілу, 2,3-дигідроксипропілу або (2,2-диметил-1,3-діоксол-4-іл)метилу або радикал формули -COR'4, в якій R'4 являє собою лінійний або розгалужений (С1-С5)алкільний радикал або радикал фенілу; - R5 являє собою атом водню або радикал пропілу або алілу, і - R6 являє собою атом водню або радикал метилу, пропілу, алілу, 2,3-дигідроксипропілу або (2,2-диметил-1,3-діоксол-4-іл)метилу, радикал формули -COR'6 (в якій R'6 являє собою лінійний або розгалужений (С1-С5)алкільний радикал або радикал фенілу) або радикал формули (I'): (І') за умови, що: - щонайменше одна з груп R1, R2, R3, R4, R5 і R6 є іншою, ніж атом водню і, - якщо R1, R2 і R3 кожний одночасно являють собою атом водню, тоді R4 також являє собою атом водню, їх діастереоізомерів та енантіомерів, а також адитивних солей з фармацевтично прийнятною кислотою або основою, в одержанні фармацевтичних композицій, призначених для запобігання і/або лікування тромботичних патологій. Відповідно до звичайного значення в рамках даного винаходу, вираз "тромботичні патології" означає будь-яку патологію, викликану утворенням тромбозу в серцево-судинній системі (вени, артерії, серце, мікроциркуляція). Місцева закупорка судини згустком або закупорка у віддаленому місцезнаходженні, що виникає через емболізацію згустку, відповідальні за клінічні ознаки тромботичних патологій. Тромбози глибоких вен з'являються суттєво в ногах; якщо вони емболізують до легень вони викличуть легеневу емболію. Артеріальні тромбози відбуваються найбільш часто в поєднанні з судинною патологією, що найчастіше являє собою атеросклероз. Вони відповідальні за ішемію тканин через зупинення кровотоку в артерії, наприклад інфаркт міокарду у випадку коронарного тромбозу або тром 11 91848 бозу далі в мікроциркуляції після емболізації, або в контексті, наприклад, інсульту (CVA) після емболізації внутрішньосерцевого або каротидного тромбу. Нарешті, мікроциркулюючий тромбоз звичайно являє собою ускладнення розповсюдженої внутрішньосудинної коагуляції, при якому мікротромб продукує ішемічний некроз. Термін "запобіжний" відповідно до даного винаходу відповідає лікуванню з метою запобігання, ціллю якого є зменшення ризику розвитку тромбозу у сприяючих такому розвитку станах, таких як атеросклеротичні захворювання, діабет або метаболічний синдром. Крім того, термін "запобіжний" може бути зрозумілий, як вторинне запобігання, яке призначене для зменшення поширення за допомогою зменшення розвитку і тривалості захворювання. Вторинне запобігання є суттєвим після інфаркту міокарда та інсультів для того, щоб зменшити ризик повторної появи. Термін "лікування" розуміється як радикальне лікування, яке призначається з метою лікування тромбозу, який може бути або може не бути ускладнений емболією. Винахід переважно стосується застосування 6,8-діаліл-5,7-дигідрокси-2-(2-алiл-3-гідрокси-4метоксифеніл)-4Н-1-бензопіран-4-ону формули (XVII): (XVII) для одержання фармацевтичних композицій, призначених для запобігання і/або лікування тромботичних патологій. Даний винахід стосується, крім того, застосування сполук діосметину в одержанні фармацевтичних композицій, призначених для запобігання і/або лікування патологій з ризиком тромбозу. "Патології з ризиком тромбозу" означають будь-яку патологію, під час якої відбуваються тромботичні події. Патології, які загострюють атеросклероз, такі як гіперхолестеринемія, діабет, гіпертензія, ожиріння, тютюнопаління і також фібриляція передсердь, являють собою головні патології з ризиком артеріального тромбозу. Генетичні або набуті патології коагуляції білків і ортопедична хірургія являють собою головні патології з ризиком венозного тромбозу, але також можуть бути згадані ожиріння, лікування певними гормонами, певні види раку і їх лікування, вагітність і причини тривалої нерухомості іммобілізації. Нарешті, септичний шок являє собою головну патологію з ризиком мікро-циркулюючих тромбозів. Наприклад, збільшений рівень тригліцеридів, такий як при гіперхолестеринемії, являє собою особливо загострюючий маркер серцевосудинного ризику взагалі і тромбозу зокрема. Існує зв'язок між збільшеним рівнем VLDL і РАІ-1, який вивільняється гетапоцитами, і ендотеліальними клітинами (Allison et al. Effects of native triglycerideenriched and oxidatively modified LDL on 12 plasminogen activator inhibitor-1 expression in human endothelial cells, 1999, Arterioscler Thromb Vase Biol, 19, 1354-1360) (Mussoni et al. Hypertriglyceridemia and regulation of fibrinolytic activity, 1992, Arterioscler Thromb, 12, 19-27). Винахід стосується також застосування сполук діосметину як активного інгредієнта в комбінації з одним або більше фармацевтично прийнятним наповнювачем в одержанні фармацевтичних композицій, призначених для запобігання і/або лікування тромботичних патологій або патологій з ризиком тромбозу. Винахід переважно стосується фармацевтичної композиції, що містить сполуку діосметину відповідно до даного винаходу в комбінації з одним або більше фармацевтично прийнятним наповнювачем, яка призначена для запобігання і/або лікування тромботичних патологій або патологій з ризиком тромбозу. "Активний інгредієнт" означає будь-яку речовину, відповідальну за фармакодинамічні або терапевтичні властивості фармацевтичної композиції. В контексті даного винаходу, "наповнювачі" означають будь-яку речовину, в якій активний інгредієнт лікарського засобу включений для того, щоб полегшити його одержання і введення і також, щоб удосконалити його консистенцію, форму і об'єм. Фармацевтичні композиції, призначені для запобігання і/або лікування тромботичних патологій або патологій з ризиком тромбозу, знаходяться, крім того, у формі, придатній для орального, парентерального, назального, під- або через-шкірного, ректального, під'язикового, очного або респіраторного введення, особливо таблетки або драже, під'язикові таблетки, саше, порошки, капсули, коржики, супозиторії, креми, мазі, шкірні гелі і придатні для пиття або ін'єкцій ампули. Сполуки діосметину відповідно до даного винаходу переважно застосовують при одержанні фармацевтичних композицій для орального введення, призначених для запобігання і/або лікування тромботичних патологій або патологій з ризиком тромбозу. Введення оральним шляхом фармацевтичних композицій, призначених для лікування тромботичних патологій або патологій з ризиком тромбозу особливо придатні для лікування, яке має превентивну ціль в силу легкості введення пацієнту. Нарешті, корисне дозування змінюється відповідно до статі, віку і ваги пацієнта, шляху введення, природа терапевтичного призначення і будьякого пов'язаного лікування і знаходиться в діапазоні від 0,1мг до 1г на 24 години за одне або більше введень. Даний винахід ілюструється наступними прикладами, не маючи на увазі будь-якого обмеження. Приклад 1: In vitro інгібування експресії РАІ-1 1. Клітинна культура Дослідження проводять на лінії людських гепатоцитів HepG2 (ATCC, no. НВ-8065). Клітини культурують в середовищі MEM (мінімальне підтримуюче середовище) з глутамакс-1 (Gibco™), яке містить 10% PCS (фетальна теляча сироватка), 13 1% замінюваних амінокислот і 1% піруват натрію і доповненому пеніциліном і стрептоміцином. 2) Клонування промотору РАІ-1 а) Ампліфікація промотору за допомогою ПЛР Фрагмент 2,5т.п.н., який відповідає промотору РАІ-1, що тягнеться від нуклеотидів у положеннях від -2442 до +136, апліфікували за допомогою ПЛР і суб-клонували (Lopez et al., 2000, Atherosclerosis, 152, 359-366). В кінцевому реакційному об'ємі 50мкл 2,5 одиниць Platinum® TaqDNA Полімерази високоякісного відтворення (Invitrogen) розміщують у присутності 300нг людської геномної ДНК (Clontech), 300мкМ dNTP (дезоксинуклеотид трифосфат) (Clontech), 300нМ праймерів в середовищі, яке містить буфер, специфічний до ферменту, доповненому 1,5мМ MgCl2 і різними концентраціями ПЛР x Енхансерна Система (Invitrogen), що покращує ампліфікацію особливо важких послідовностей (0-4х). Набір праймерів, які використовують, (Chen et al. Differential mechanisms of PAI-1 gene activation by transforming growth factor beta and tumor necrosis factor alpha in endothelial cells, 2001, Thrmb Haemost, 86, 1563-72) є таким, як зазначено нижче: 5'-TTACGCGTGGGTTTGGGGCTGGACTTG-3' (SEQ ID NO.1) і 5'-CGAGATCTCAGAGGTGCCTTGCGATTGG-3' (SEQ ID NO.2). Програма ПЛР, на апараті Perkin Elmer 2400, включає ініціацію при підвищеній температурі при 94°С протягом 2хв. і потім ампліфікацію протягом 35 циклів. Продукт ПЛР потім осаджують протягом 1год. при -80°С у присутності 7,5М ацетату амонію і етанолу. Після центрифугування при 14000об./хв. при 4°С, осад повторно суспендують в 70% етанолу і знову центрифугують при 14000об./хв. при 4°С. Осад, який одержують, потім висушують і додають у воду. b) Розщеплення промоторної послідовності Ампліфіковану послідовність потім ферментативно гідролізують у два етапи за допомогою рестрикційних ферментів Bgl II і Мlu І. Ампліфіковану послідовність ферментативно гідролізують протягом 1год. 30хв. при 37°С у присутності 1 одиниці/мкл ферменту і 100мкг/мл BSA (Бичачий сироватковий альбумін). Після ферментативного гідролізу, продукт, який одержують, методично очищують на хроматографічних колонках Micro Bio-Spin® (Bio Rad) для того, щоб видалити солі буфера. c) Конструювання плазміди PGL3/РАІ-1 pGL3-Основну плазміду (Promega), яка містить ген люциферази світляка, ферментативно гідролізують рестрикційними ферментами Bgl II і Мlu І відповідно до того ж протоколу що і для вставки і потім очищують на 1% низькоплавким агарозним гелем. Лігування pGL3-Основного плазмідного вектора і вставки, яка відповідає промотору РАІ-1, проводять за допомогою Т4 ДНК Лігази Ligase (LigaFast™ Система швидкого лігування ДНК від Promega). Умовно, протягом лігування, використо 91848 14 вують надлишок вставки, який еквівалентний трикратній кількості вектора. До того ж, через те, що ця вставка вдвічі менша ніж вектор (2,5т.п.н. у порівнянні з 4,8т.п.н.), підтримування стехіометричної рівноваги вимагає подвійної маси вектора. 37,5нг вставки і 25нг pGL3-Ocновного вектора таким чином піддавали реакції у присутності 3 одиниць Т4 лігази, при температурі навколишнього середовища. 3) Трансфекція гепатоцитів PGL3/PAI-1 плазміду трансфекують у HepG2 клітини. Трансфекування проводять в планшетах з клітинами при 50% конфлюентності, відкладаючи Lipofectin® (1мг/мл) і 1,5мкг PGL3/PAI-1 плазміду в кожній з ямок. Lipofectin® активують протягом 30хв. в ОРТІ-MEM середовищі (GIBCO™) і потім приводять у взаємодію протягом 15хв. з плазмідами, який заздалегідь розбавляють середовищем. Клітини інкубують протягом 6 годин при 37°С в атмосфері, яка містить 5% СО2 і 95% О2. Трансфекційне середовище витягають і заміщують протягом ночі збагаченим культуральним середовищем для того, щоб стабілізувати клітини. Експресію репортерних генів індукують протягом 24год. в середовищі MEM без сироватки. Клітини зшкрябують і лізують в лізисному буфері (набір Dual-Luciferase®, Promega) і потім утримують при -20°С. Фаза індукування складає 24год. для клітин HepG2 у присутності TGFβ1 (1нг/мл). Протягом цієї фази індукування інгібітор експресії РАІ-1 може бути доданий за 4год. до TGFβ1 і його утримують у взаємодії з клітинами до кінця 24год. фази індукування. 4) Визначення активності промотору Активність промотору РАІ-1 визначають шляхом кількісного аналізу виробленої активності люциферази (набір Dual-Luciferase®, Promega). До кожної ямки додають розчин люциферину, субстрат люциферази світляка. Це приводить до виділення світла. Планшет інкубують протягом 10хв. в темряві, через те, що активність люциферази є чутливою до світла, і потім починають зчитування люмінометром для того, щоб визначити кількість виділених фотонів (Wallac, Perkin Elmer), одержаний результат являє собою середнє срm (відліків за хвилину) протягом періоду у 5сек. 5) Результати 6,8-Діаліл-5,7-дигідрокси-2-(2-аліл-3-гідрокси4-метоксифеніл)-4Н-1-бензопіран-4-он, довільно названий як сполука А, і Т686 формули 3(Е)бензиліден-4(Е)-(3,4,5триметоксибензиліден)піролідин-2,5-діону (інгібітор експресії РАІ-1 посилання, від Tanabe) досліджують при концентрації. 10мкМ на HepG2 клітинах в базисному стані і після індукування з TGFβ1. Активність промотору РАІ-1 вимірюють в контрольних умовах і у присутності інгібіторів, в базисному та індукованому станах. Активності, виражені в срm і як процент контрольних спостережень, показані у Таблиці 1. 15 91848 16 Таблиця 1 Вимірювання активності промотору РАІ-1 у присутності 6,8-діаліл-5,7-дигідрокси-2-(2-аліл-3-гідрокси-4-метоксифеніл)-4Н-1-бензопіран-4-ону або Т686 (24год.) в базисному стані або стані, індукованому TGFβ1 (1мг/мл) Базисний Індукований (TGFP) Контроль Сполука А (10мкМ) Т686 (10мкМ) Контроль Сполука А (10мкМ) Т686 (10мкМ) Активність в срm 1430±59 445±121 (**) 473±143 (**) 3440±242 765±138 ( ) 1641±173 ( ) % інгібування/ контроль 69 67 78 52 ** р
ДивитисяДодаткова інформація
Назва патенту англійськоюDiosmetin derivatives for the treatment and prevention of thrombotic pathologies
Автори англійськоюVerbeuren Tony, Rupin Alain, Sansilvestri-Morel Patricia, Vallez Marie-Odile, Boussard Marie-Francoise, Wierzbicki Michel
Назва патенту російськоюПрименение соединений диосметина в лечении и предотвращении тромботическим патологиям
Автори російськоюВерберен Тоне, Рюпен Ален, Сансильвестри-Морель Патрисия, Валле Мари-Одиль, Буссар Мари-Франсуаз, Виерзбики Мишель
МПК / Мітки
МПК: A61K 31/352, A61P 7/02
Мітки: застосування, тромботичним, діосметину, запобіганні, патологіям, сполук, лікуванні
Код посилання
<a href="https://ua.patents.su/9-91848-zastosuvannya-spoluk-diosmetinu-u-likuvanni-i-zapobiganni-trombotichnim-patologiyam.html" target="_blank" rel="follow" title="База патентів України">Застосування сполук діосметину у лікуванні і запобіганні тромботичним патологіям</a>
Попередній патент: Конвеєрний валик та спосіб його складання
Наступний патент: Спосіб і пристрій для керування виділенням ресурсів висхідної лінії зв’язку в системі зв’язку
Випадковий патент: Спосіб лікування первинного безсоння












