Спосіб синтезу сполук (2s, 3as, 7as)-1-[(s)-аланіл]-октагідро-1н-індол-2-карбонової кислоти і їх застосування у синтезі периндоприлу
Формула / Реферат
1. Спосіб одержання сполук формули (І)
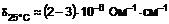
в якій R являє собою атом водню або захисну групу для амінофункції,
який відрізняється тим, що бензиловий ефір формули (IIIа) або (Шb):
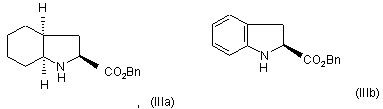
або адитивну сіль ефіру формули (IIIа) або (IIIb) з мінеральною кислотою або органічною кислотою піддають реакції зі сполукою аланіну формули (IV):
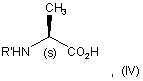
в якій R' являє собою захисну групу для амінофункції,
у присутності зв'язувального агента, який вибирають з наступних реагентів і пар реагентів:
O-(бензотриазол-1-іл)-1,1,3,3-біс(тетраметилен)уроній гексафторфосфат,
О-(бензотриазол-1-іл)-1,1,3,3-біс(тетраметилен)уроній тетрафторборат,
необов'язково у присутності основи,
з одержанням сполуки формули (Va) або (Vb), відповідно, в залежності від того, чи використовують сполуку формули (IIIа) або (IIIb) як вихідний матеріал:
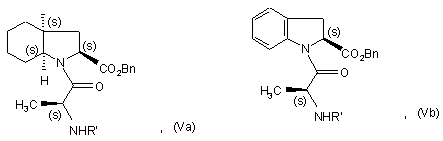
в яких R' є таким же, як визначено тут вище,
яку піддають реакції каталітичної гідрогенізації у присутності паладію з одержанням продукту формули (І).
2. Спосіб за п. 1, який відрізняється тим, що сполуку формули (IIIа) використовують як вихідний матеріал.
3. Спосіб за п. 1, який відрізняється тим, що сполуку формули (IIIb) використовують як вихідний матеріал.
4. Спосіб за п. 2, який відрізняється тим, що реакцію гідрогенізації сполуки формули (Va) проводять під тиском водню менше ніж 10 бар.
5. Спосіб за п. 3, який відрізняється тим, що реакцію гідрогенізації сполуки формули (Vb) проводять під тиском водню від 10 до 35 бар.
6. Спосіб одержання периндоприлу або його фармацевтично прийнятних солей, в якому бензиловий ефір формули (ІІІа) або (ІІІb):

або адитивну сіль ефіру формули (IIIа) або (IIIb) з мінеральною кислотою або органічною кислотою піддають дії способу за будь-яким з пп. 1-5, і сполуку формули (І), яку таким чином одержують, потім піддають, якщо вимагається, реакції зняття захисту амінофункції, з наступною реакцією сполучення або з етил 2-оксопентаноатом в умовах відновлювального амінування, або зі сполукою формули (VІ):
 , (VІ)
, (VІ)
в якій Х являє собою групу, що відходить, яку вибирають з галогену,
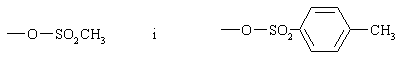 ,
,
з одержанням оптично чистого периндоприлу, який перетворюють, якщо бажано, у фармацевтично прийнятну сіль, таку як трет-бутиламінна сіль.
Текст
1. Спосіб одержання сполук формули (І) 2 3 84897 3. Спосіб за п. 1, який відрізняється тим, що сполуку формули (IIIb) використовують як вихідний матеріал. 4. Спосіб за п. 2, який відрізняється тим, що реакцію гідрогенізації сполуки формули (Va) проводять під тиском водню менше ніж 10 бар. 5. Спосіб за п. 3, який відрізняється тим, що реакцію гідрогенізації сполуки формули (Vb) проводять під тиском водню від 10 до 35 бар. 6. Спосіб одержання периндоприлу або його фармацевтично прийнятних солей, в якому бензиловий ефір формули (ІІІа) або (ІІІb): H H N H CO2 Bn , (IIIa) N H 4 тім піддають, якщо вимагається, реакції зняття захисту амінофункції, з наступною реакцією сполучення або з етил 2-оксопентаноатом в умовах відновлювального амінування, або зі сполукою формули (VІ): CH3 (VІ) X (R) CO2Et , в якій Х являє собою групу, що відходить, яку вибирають з галогену, O CO2Bn (IIIb) або адитивну сіль ефіру формули (IIIа) або (IIIb) з мінеральною кислотою або органічною кислотою піддають дії способу за будь-яким з пп. 1-5, і сполуку формули (І), яку таким чином одержують, по Даний винахід відноситься до способу синтезу сполук формули (І): в якій R являє собою атом водню або захисну груп у для аміно функції, і до їх застосування у синтезі периндоприлу формули (II): і його фармацевтично прийнятних солей. Периндоприл і його фармацевтично прийнятні солі, і більш конкретно його трет-бутиламінна сіль, володіють цінними фармакологічними властивостями. Їх головна властивість полягає в інгібуванні ангіотензин І перетворювального ферменту (або кінінази II), що дозволяє, з одного боку, запобігти перетворенню декапептид ангіотензину І в октапептид ангіотензин II (вазоконстриктор) і, з іншого боку, запобігти деградації брадикініну (вазодилататор) в неактивний пептид. SO2CH3 i O SO2 CH3 , з одержанням оптично чистого периндоприлу, який перетворюють, якщо бажано, у фармацевтично прийнятну сіль, таку як трет-бутиламінна сіль. Ці дві дії сприяють позитивному впливу периндоприлу на серцево-судинні захворювання, більш конкретно на артеріальну гіпертензію і параліч серця. Периндоприл, його приготування і застосування в терапії були розкриті в описі Європейського патенту EP 0 049 658. Беручи до уваги фармацевтичне значення цієї сполуки, було важливо спромогтись одержати її ефективним способом синтезу, легковідтворюваною у промисловому масштабі, що веде до одержання периндоприлу у хорошому ви ході і з відмінною мірою чистоти. Опис патенту EP 0 308 341 розкриває промисловий синтез периндоприлу шляхом зв'язування бензилового ефіру (2S,3аS,7аS)-октагідроіндол-2карбонової кислоти з етиловим ефіром N-[(S)-1карбоксибутил]-(S)-аланіну у присутності дициклогексилкарбодііміду, з наступним зняттям захисту карбонової групи ге тероциклу шляхом каталітичної гідрогенізації. Цей спосіб має недоліки, пов'язані із застосуванням дициклогексилкарбодііміду. Заявник розробив спосіб синтезу периндоприлу, який використовує інші зв'язувальні агенти. Більш конкретно, даний винахід відноситься до способу синтезу периндоприлу, який відрізняється тим, що бензиловий ефір формули (IIIa) або (IIIb): або адитивну сіль ефіру формули (IIIa) або (IIIb) з мінеральною кислотою або органічною кис 5 84897 лотою піддають реакції зі сполукою аланіну формули (IV): в якій R' являє собою захисну груп у для аміно функції, у присутності зв'язувального агента, який вибирають з наступних реагентів і пар реагентів: (1,3-диметиламінопропіл)-3-етил-карбодіімід гідрохлорид, (1,3-диметиламінопропіл)-3-етил-карбодіімід гідрохлорид / 1-гідроксибензо-триазол, (1,3-диметиламінопропіл)-3-етил-карбодіімід гідрохлорид / 1-гідрокси-7-аза-бензотриазол, (1,3-диметиламінопропіл)-3-етил-карбодіімід гідрохлорид / N-гідрокси-сукцинімід, (1,3-диметиламінопропіл)-3-етил-карбодіімід гідрохлорид / 3-гідрокси-3,4-дигідро-4-оксо-1,2,3бензотриазин, (1,3-диметиламінопропіл)-3-етил-карбодіімід гідрохлорид / N-гідроксифталімід, дициклогексилкарбодіімід /1-гідрокси-7азабензотриазол, дициклогексилкарбодіімід / Nгідроксисукцинімід, дициклогексилкарбодіімід/3-гідрокси-3,4дигідро-4-оксо-1,2,3-бензотриазин, дициклогексилкарбодіімід / Nгідроксифталімід, О-(бензотриазол-1-іл)-1,1,3,3тетраметилуроній гексафторфосфат, О-(7-азабензотриазол-1-іл)-1,1,3,3тетраметилуроній гексафторфосфат, О-(бензотриазол-1-іл)-1,1,3,3тетраметилуроній тетрафторборат, бензотриазол-1-іл-окситрипіролідинофосфоній гексафторфосфат, бензотриазол-1-іл-окситрис(диметиламіно)фосфоній гексафторфосфат, О-(бензотриазол-1-іл)-1,1,3,3біс(тетраметилен)уроній гексафторфосфат, О-(бензотриазол-1-іл)-1,1,3,3біс(пентаметилен)уроній гексафторфосфат, хлор-трипіролідинофосфоній гексафторфосфат, хлор-1,1,3,3-біс(тетраметилен)формамідиній гексафторфосфат, хлор-1,1,3,3-біс(пентаметилен)формамідиній гексафторфосфат, N-етоксикарбоніл-2-етокси-1,2-дигідрохінолін, О-[(етоксикарбоніл)-ціанометиленаміно]1,1,3,3-тетраметилуроній тетрафторборат, О-(3,4-дигідро-4-оксо-1,2,3-бензотриазин-3-іл)1,1,3,3-тетраметилуроній тетрафторборат, О-(3,4-дигідро-4-оксо-1,2,3-бензотриазин-3-іл)1,1,3,3-тетраметилуроній тетрафторборат / 1гідроксибензотриазол, О-(3,4-дигідро-4-оксо-1,2,3-бензотриазин-3-іл)1,1,3,3-тетраметилуроній тетрафторборат / Nметилморфолін, 6 О-(3,4-дигідро-4-оксо-1,2,3-бензотриазин-3-іл)1,1,3,3-тетраметилуроній тетрафторборат / колідин, О-(1,2-дигідро-2-оксо-1 -піридил)-1,1,3,3 тетраметилуроній тетрафторборат, О-(1,2-дигідро-2-оксо-1-піридил)-1,1,3,3тетраметилуроній тетрафторборат / 1 гідроксибензотриіізол, О-(1,2-дигідро-2-оксо-1 -піридил)-1,1,3,3біс(тетраметилен)уроній гексафтор-фосфат, О-(1,2-дигідро-2-оксо-1-піридил)-1,1,3,3біс(тетраметилен)уроній гексафтор-фосфа т/ 1гідрокси-бензотриазол, О-(N-сукцинімідил)-1,1,3,3-тетраметилуроній тетрафторборат, О-(N-сукцинімідил)-1,1,3,3біс(тетраметилен)уроній тетрафторборат, O-(N-сукцинімідил)-1,1,3,3біс(тетраметилен)уроній тетрафторборат / 1гідрокси-бензотриазол, О-(5-норборнен-2,3-дикарбоксімідо)-1,1,3,3тетраметилуроній тетрафторборат, пропанфосфоновий ангідрид, імід N-гідрокси-5-норборнен-2,3-дикарбонової кислоти, і N-гідрокси-1,2-дигідро-2-оксо-піридин, необов'язково у присутності основи, для того, щоб одержати сполуку формули (Va) або (Vb), відповідно, в залежності від того, чи використовують сполуку формули (IIIa) або (IIIb) як вихідний матеріал: в яких R' є таким же, як визначено тут вище, яку піддають реакції каталітичної гідрогенізації у присутності паладію для того, щоб одержати продукт формули (І). Серед захисних груп для аміно функції, які можуть бути використані в даному винаході, можуть бути згадані, без будь-якого обмеження, третбутилоксикарбонільна, бензильна і бензилоксикарбонільна групи. Каталітичну гідрогенізацію сполуки формули (Va) переважно проводять під тиском водню менше ніж 10 бар. Каталітичну гідрогенізацію сполуки формули (Vb) переважно проводять під тиском водню від 10 до 35 бар. Сполуку формули (І), яку таким чином одержують, потім піддають, якщо вимагається, реакції зняття захисту аміно функції, з наступною реакцією з'єднання або з етил 2-оксо-пентаноатом в умовах відновлювального амінування або зі сполукою формули (VI): 7 84897 в якій X являє собою відхідну груп у, яку вибирають з галогену, для того, щоб одержати оптично чистий периндоприл, який перетворюють, якщо бажано, у фармацевтично прийнятну сіль, таку як третбутиламінна сіль. Нижченаведені приклади ілюструють даний винахід. Приклад 1: (2S,3аS,7аS)-1-{(2S)-2-[(третБутилоксикарбоніл)аміно]-пропіоніл}октагідро-1Ніндол-2-карбонова кислота / спосіб 1: Стадія А: Бензил (2S,3аS,7аS)-1-{(2S)-2-[(третбутилоксикарбоніл)аміно]-пропіоніл}-октагідро-1Hіндол-2-карбоксилат: 200г (2S,3аS,7аS)-октагідроіндол-2-карбонової кислоти бензилового ефіру пара-толуолсульфонату, 65 мл триетиламіну і 1 літр етилацетату вміщують у реактор з мішалкою, з наступним додаванням, після перемішування протягом 10 хвилин при температурі навколишнього середовища, 87 г Ν-[трет-бутилоксикарбоніл]-(S)-аланіну і 175г О-(бензотриазол-1-іл)-1,1,3,3-біс(тетраметилен)уроній гексафторфосфату. Неоднорідну суміш потім нагрівають при 30°C протягом 3 годин, поки добре перемішуючи, і потім охолоджують до 0°C і фільтрують. Фільтрат потім промивають і згодом випаровують досуха для того, щоб одержати очікуваний продукт. Стадія В: (2S,3аS,7аS)-1-{(2S)-2-[(третБутилоксикарбоніл)аміно]пропіоніл}-октагідро-1Hіндол-2-карбонова кислота: Залишок, який одержують на попередній Стадії, (200 г), розчиняють в 200 мл метилциклогексану і переносять в гідрогенізатор; потім додають 26 г 5% паладію-на-вуглеці, суспендованого в 80 мл метилциклогексану, з наступним додаванням 640 мл води. Суміш потім гідрогенізують під тиском 0,5 Комп’ютерна в ерстка І.Скворцов а 8 бар при температурі від 15 до 30°C доти, доки не абсорбується теоретична кількість водню. Після відфільтровування каталізатора, водну фаз у фільтрату промивають метилциклогексаном і потім ліофілізують для того, щоб одержати очікуваний продукт з виходом 94%. Приклад 2: (2S,3аS,7аS)-1-{(2S)-2-[(третБутилоксикарбоніл)аміно]-пропіоніл}октагідро-1Ніндол-2-карбонова кислота / спосіб 2: Стадія А: Бензил (2S)-1-{(2S)-2-[(третбутилоксикарбоніл)аміно]пропіоніл}-2,3-дигідро1Н-індол-2-карбоксилат: 200г бензил 2,3-дигідро-1Н-індол-2карбоксилат пара-толуолсульфонату, 66 мл триетиламіну і 1 літр етилацетату вміщують у реактор з мішалкою, з наступним додаванням, після перемішування протягом 10 хвилин при температурі навколишнього середовища, 89г N-[третбутилоксикарбоніл]-(S)-аланіну і 151г O(бензотриазол-1-іл)-1,1,3,3біс(тетраметилен)уроній тетрафторборату. Неоднорідну суміш потім нагрівають при 30°C протягом 3 годин, поки добре перемішуючи, і потім охолоджують до 0°C і фільтрують. Фільтрат потім промивають і згодом випаровують досуха для того, щоб одержати очікуваний продукт. Стадія В: (2S,5аS,7аS)-1-{(2S)-2-[(третБутилоксикарбоніл)аміно]пропіоніл}-октагідро-1Ніндол-2-карбонова кислота: Залишок, який одержують на попередній Стадії, (200 г), розчиняють в 200 мл метилциклогексану - переносять в гідрогенізатор; потім додають 26 г 5% паладію-на-вуглеці, суспендованого в 80 мл метилциклогексану, з наступним додаванням 640 мл води. Суміш потім гідрогенізують під тиском 0,5 бар при температурі від 15 до 30°C доти, доки не абсорбується теоретична кількість водню, який вимагається для дебензилування; суміш потім нагрівають до температури від 50 до 100°C і гідрогенізують під тиском 30 бар доти, доки не абсорбується теоретична кількість водню, який вимагається для гідрогенізації. Після відфільтровування каталізатора, водну фазу фільтрату промивають метилциклогексаном і потім ліофілізують для того, щоб одержати очікуваний продукт. Підписне Тираж 28 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for the synthesis of derivatives of (2s, 3as, 7as)-1-[(s)-alanyl]-octahydro-1h-indole-2-carboxylic acid and use thereof for the synthesis of perindopril
Автори англійськоюDubuffet Thierry, Lecouve Jean-Pierre
Назва патенту російськоюСпособ синтеза соединений (2s, 3a, 7a)-1-[(s)-аланил]-октагидро-1н-индол-2-карбоновой кислоты и их применение в синтезе периндоприла
Автори російськоюДюбюффе Тьерри, Лекув Жан-Пьер
МПК / Мітки
МПК: C07K 5/06
Мітки: спосіб, 7as)-1-[(s)-аланіл]-октагідро-1н-індол-2-карбонової, кислоти, застосування, периндоприлу, синтезу, синтезі, сполук
Код посилання
<a href="https://ua.patents.su/4-84897-sposib-sintezu-spoluk-2s-3as-7as-1-s-alanil-oktagidro-1n-indol-2-karbonovo-kisloti-i-kh-zastosuvannya-u-sintezi-perindoprilu.html" target="_blank" rel="follow" title="База патентів України">Спосіб синтезу сполук (2s, 3as, 7as)-1-[(s)-аланіл]-октагідро-1н-індол-2-карбонової кислоти і їх застосування у синтезі периндоприлу</a>
Попередній патент: Похідні гідронополу як агоністи людських рецепторів orl1
Наступний патент: Спосіб синтезу периндоприлу і його фармацевтично прийнятних солей
Випадковий патент: Гусеничний ланцюг транспортного засобу








