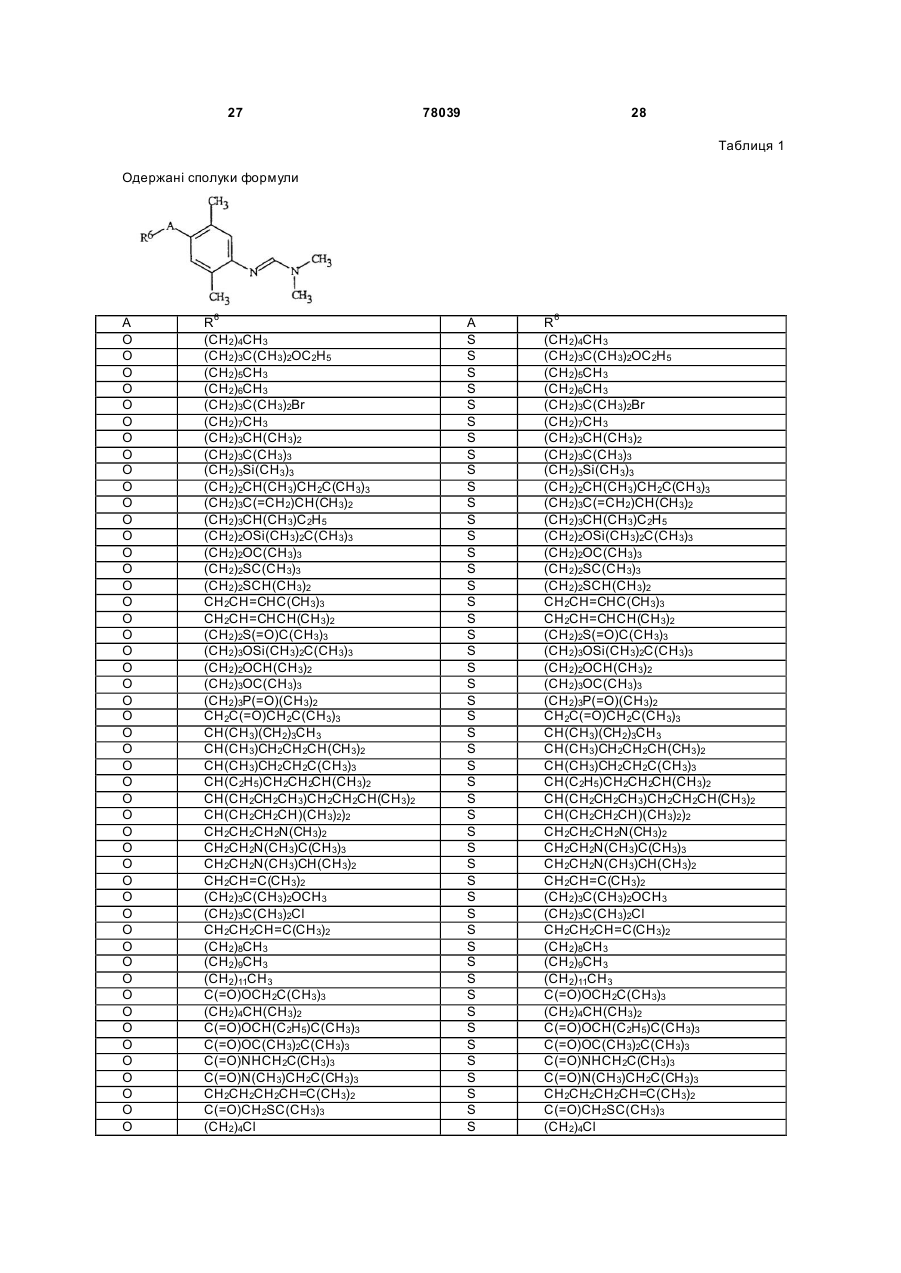
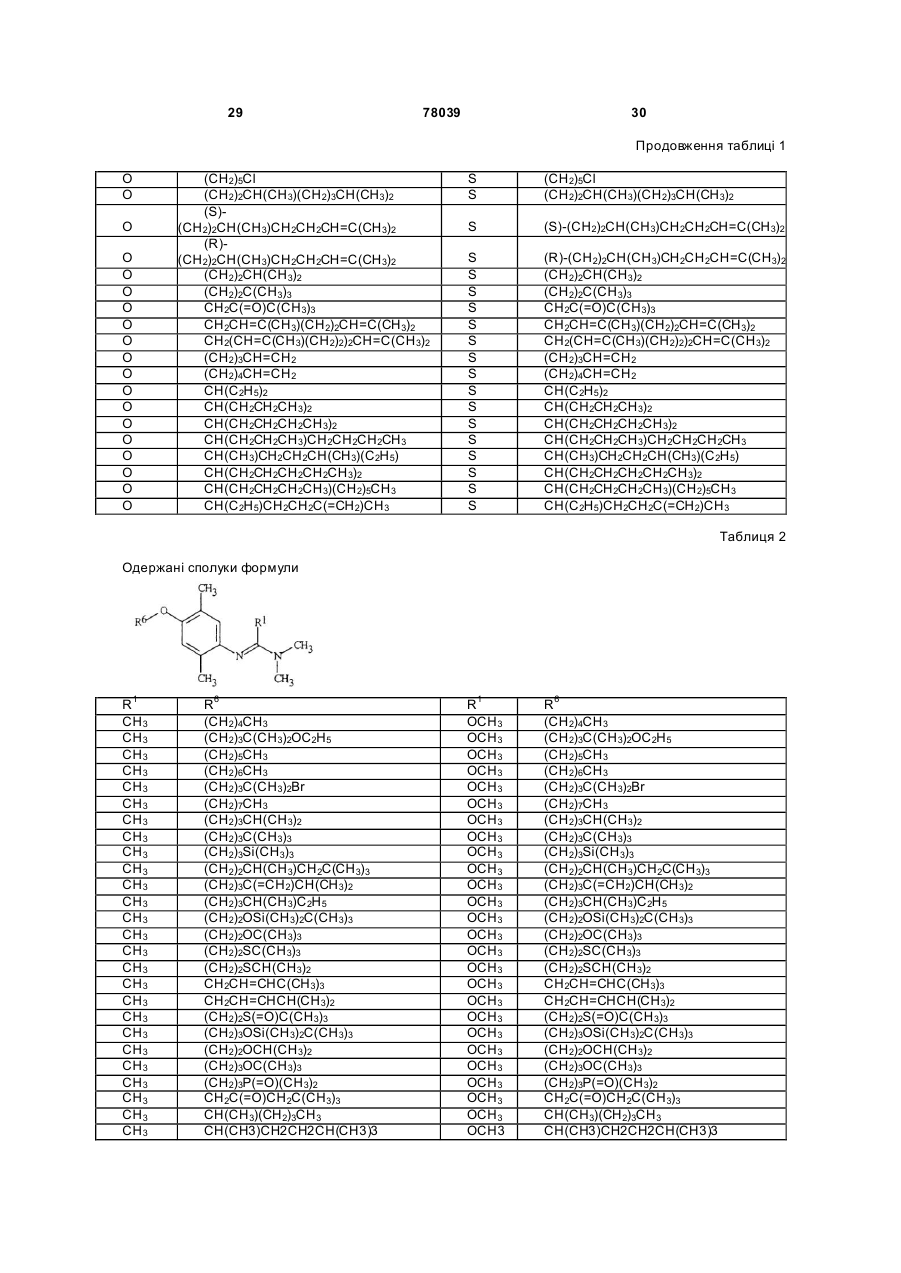
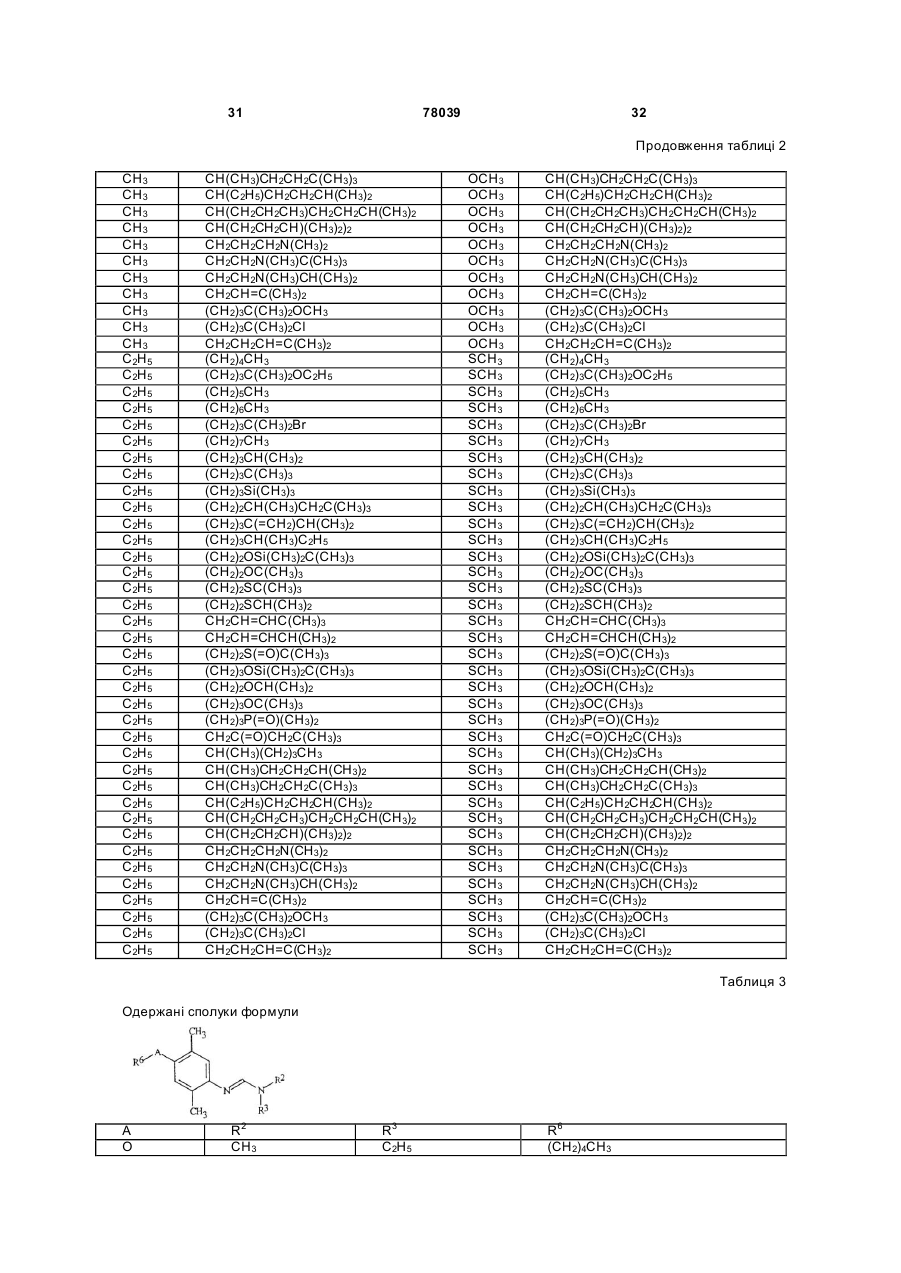
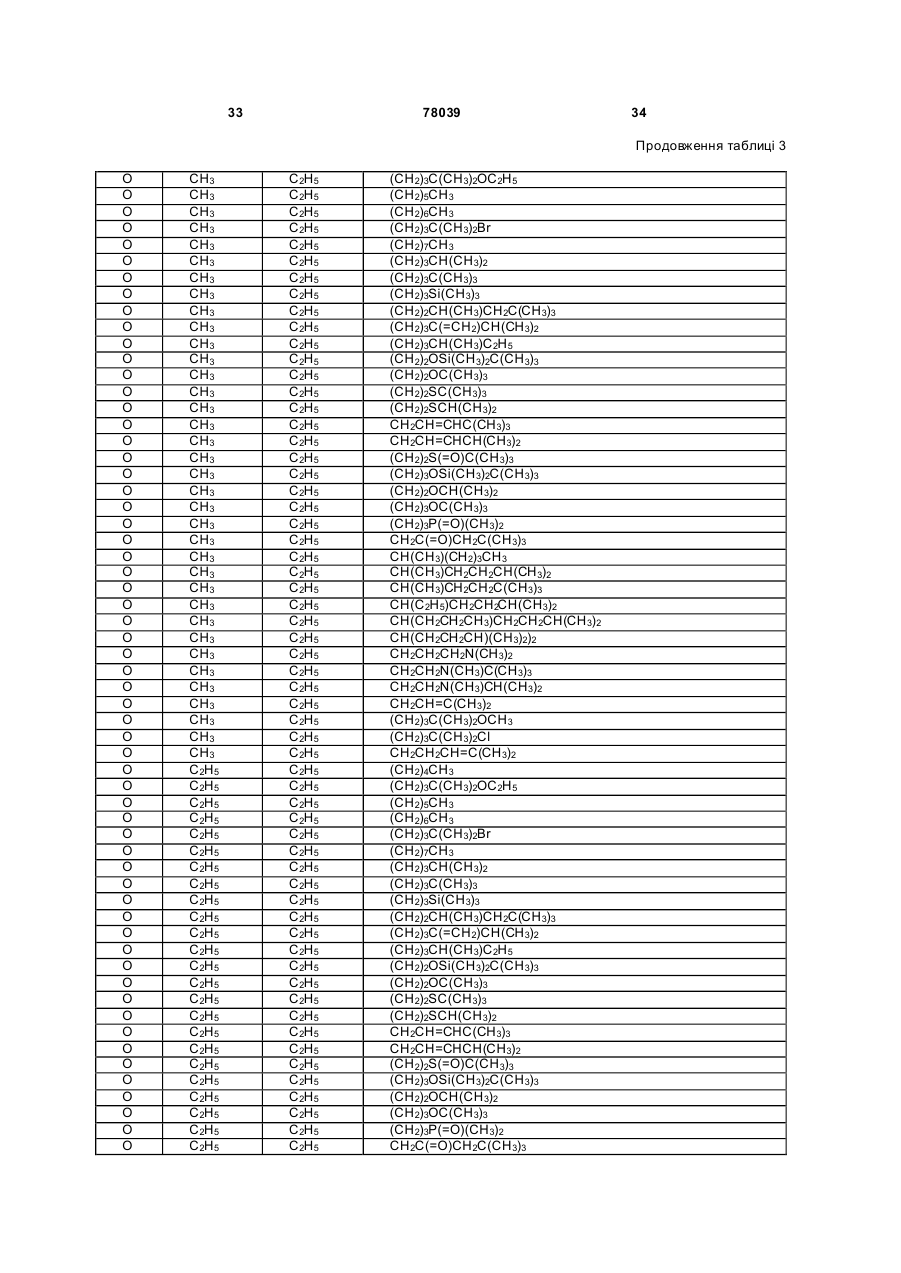
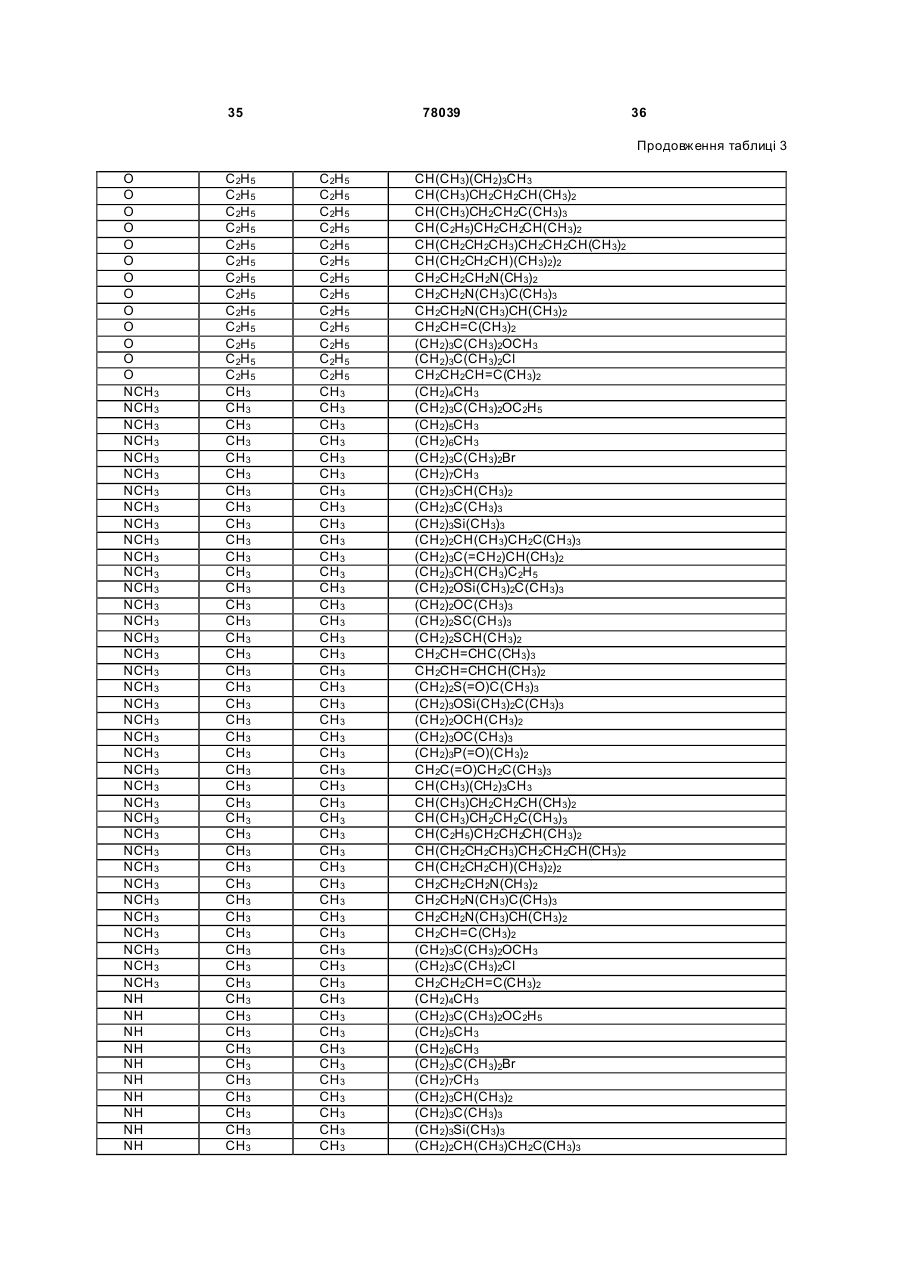
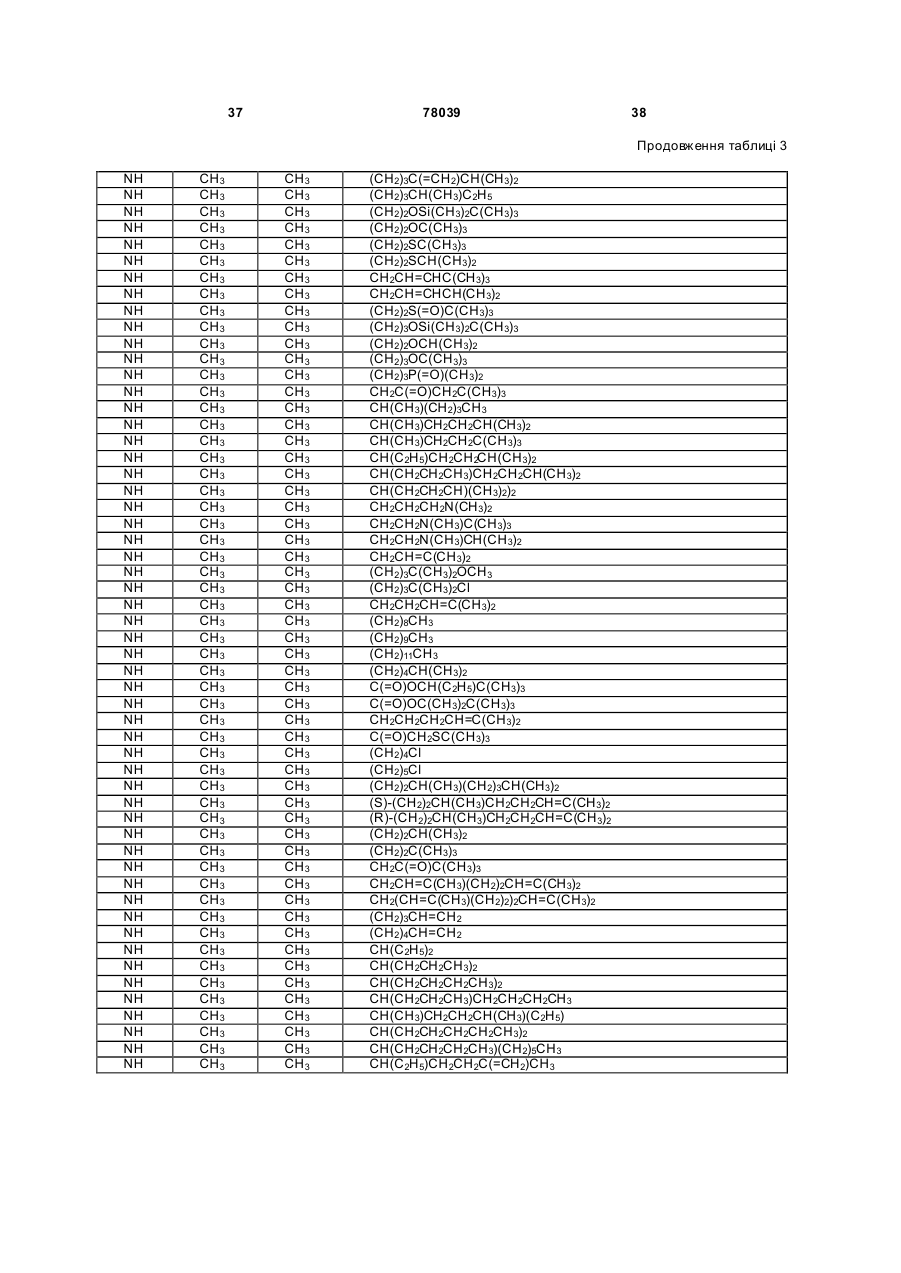
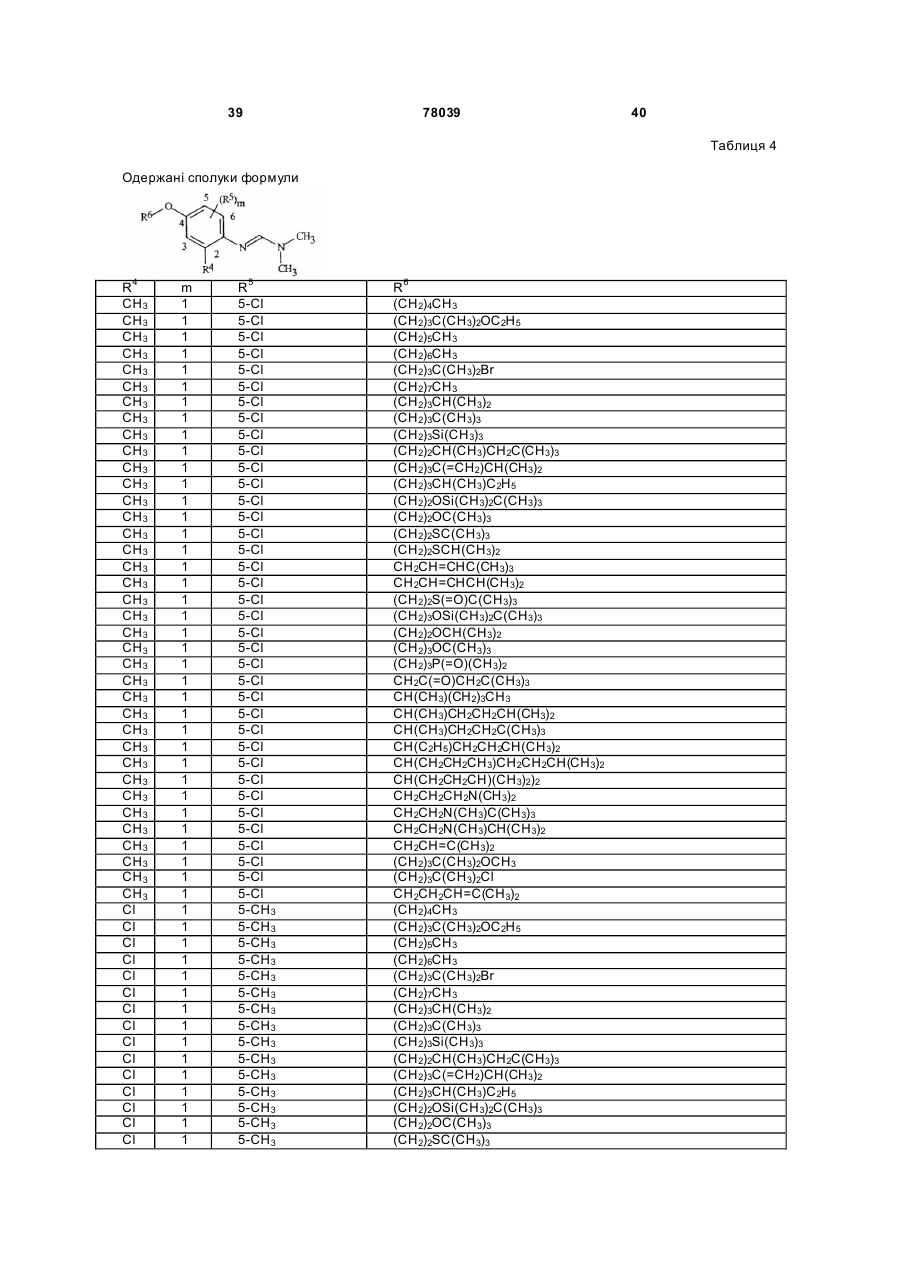
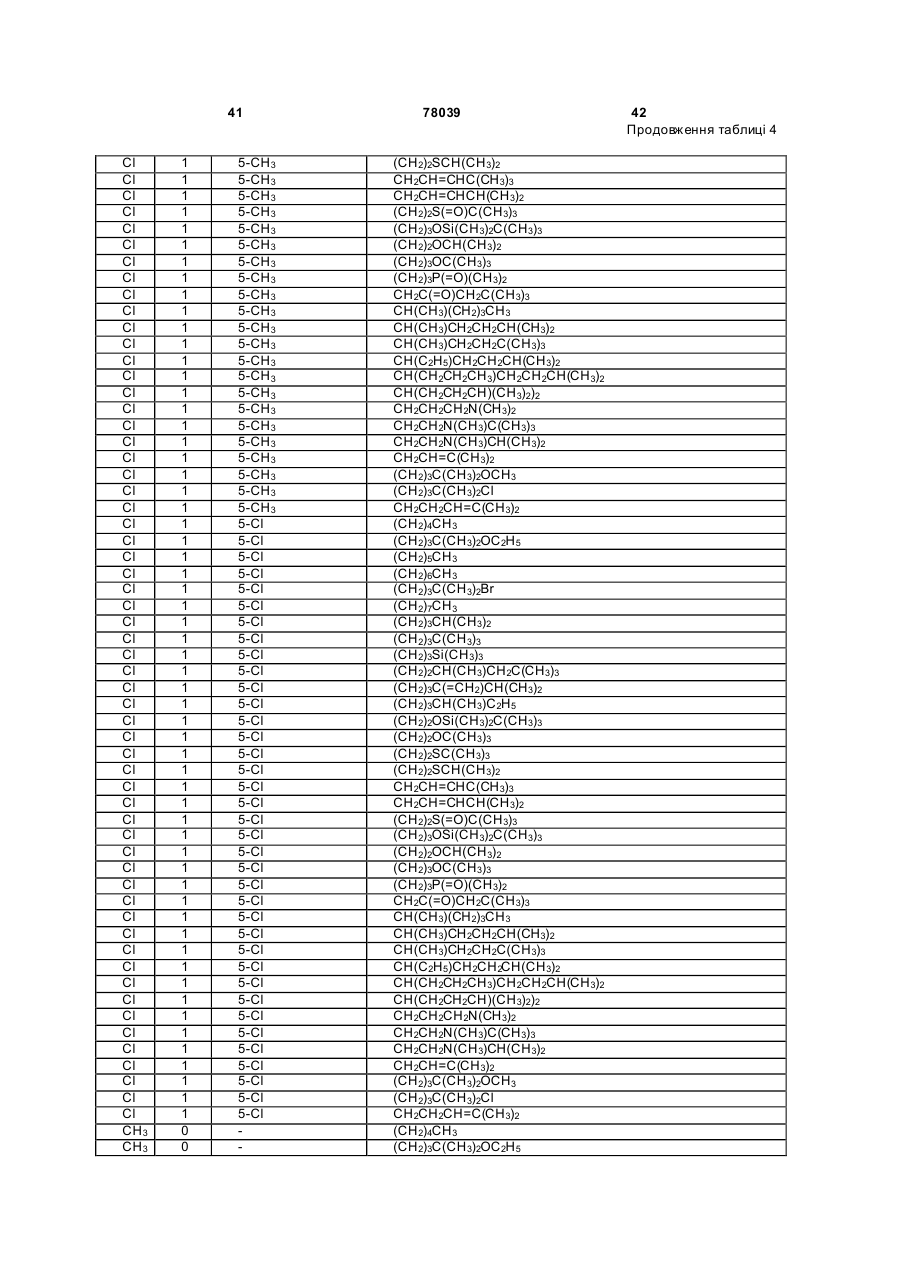
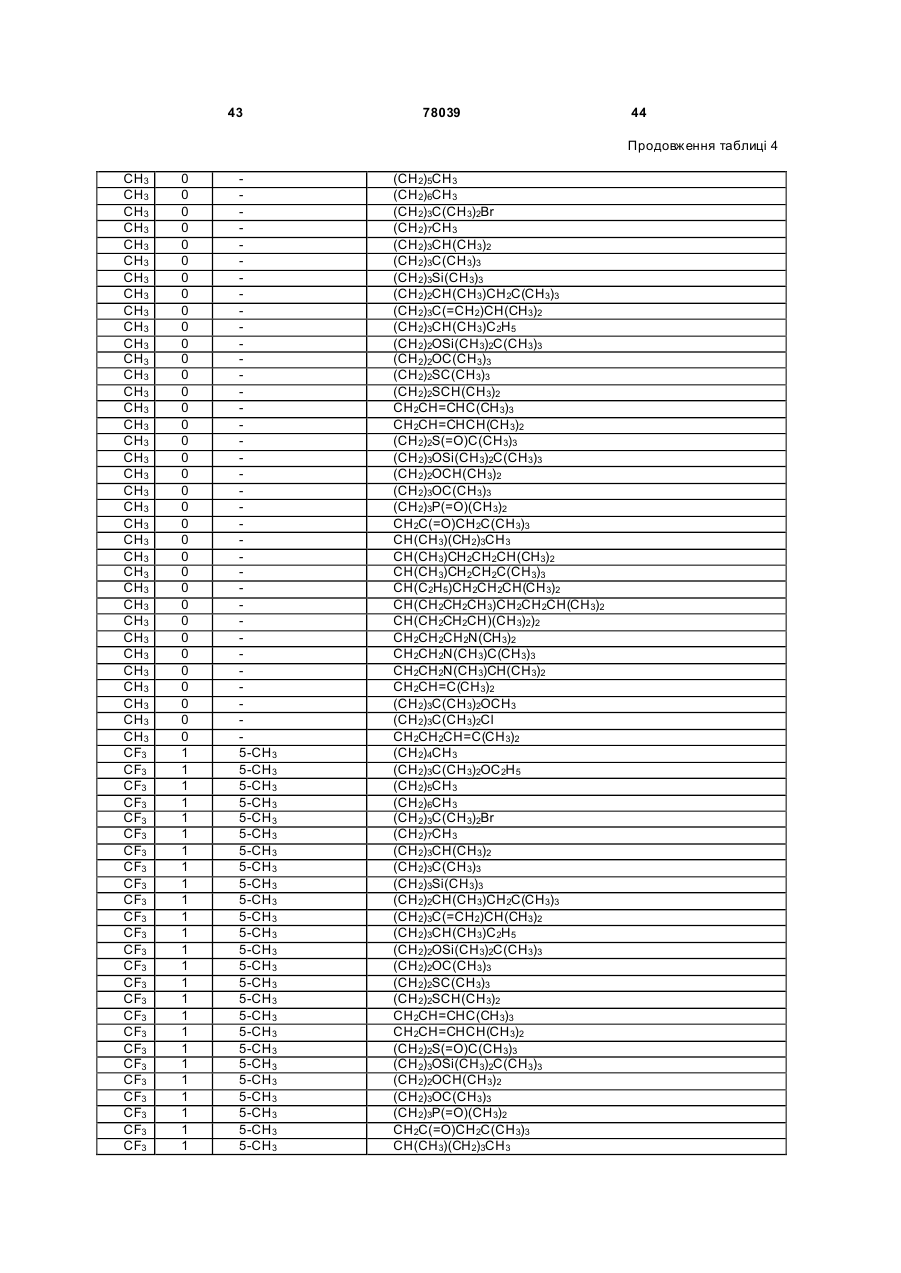
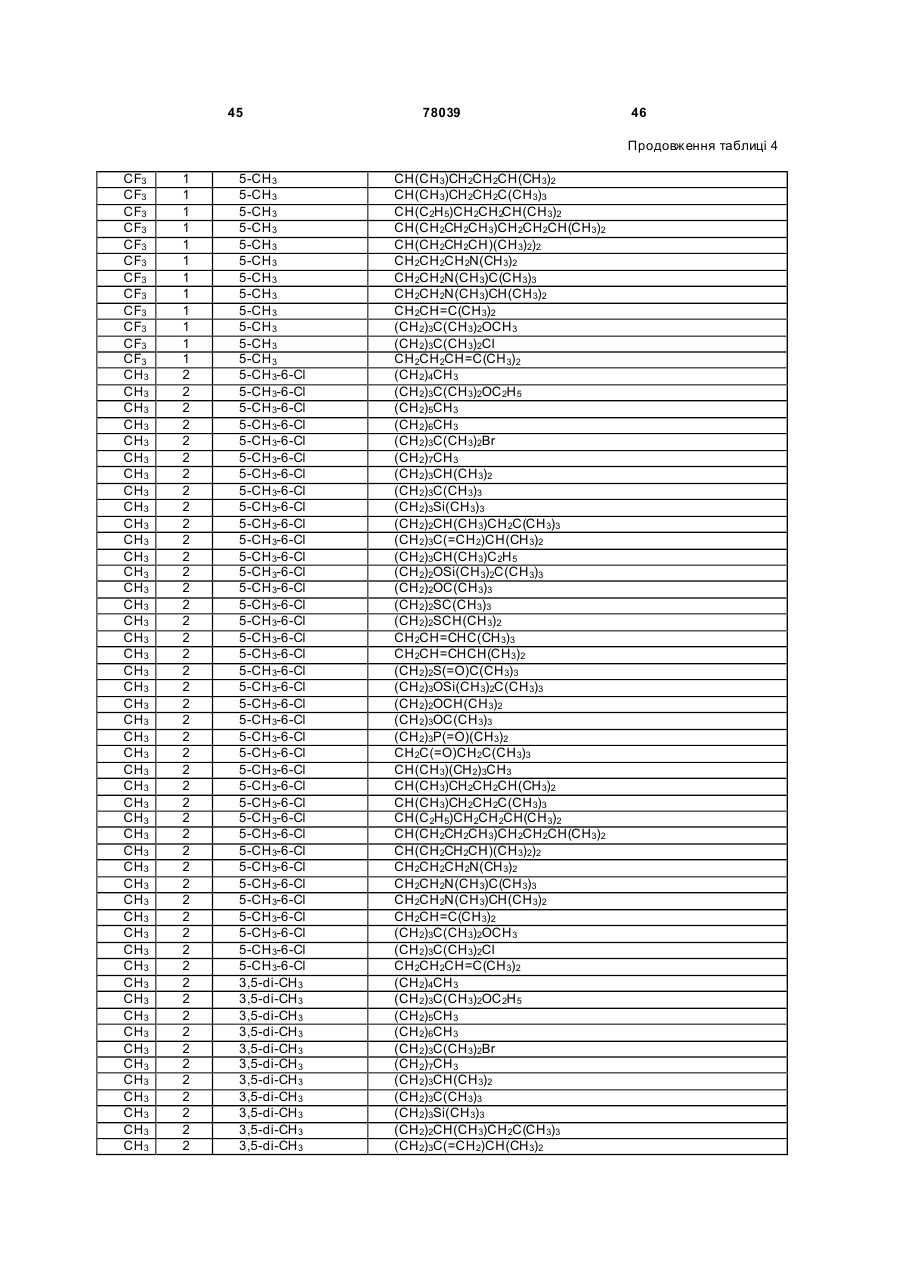
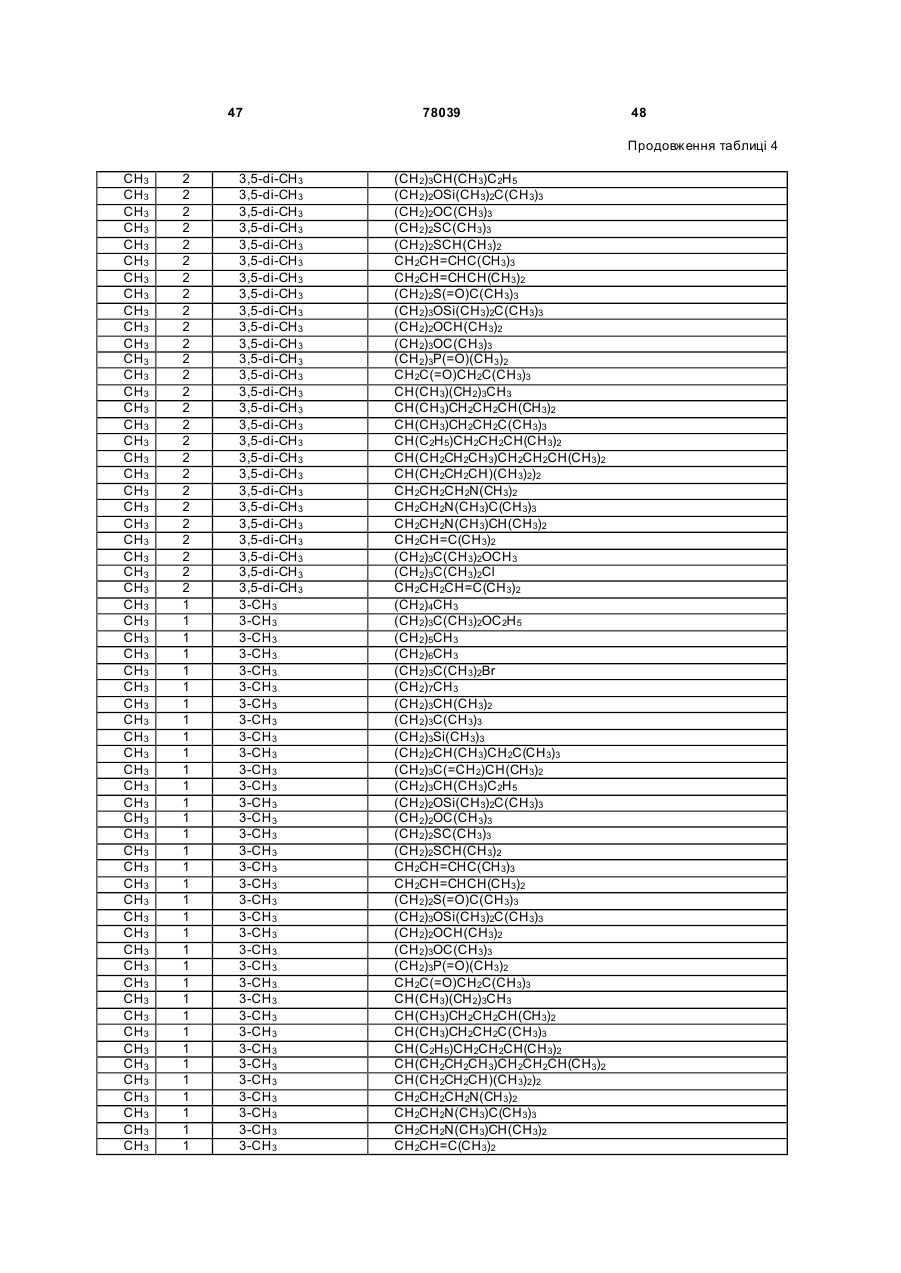
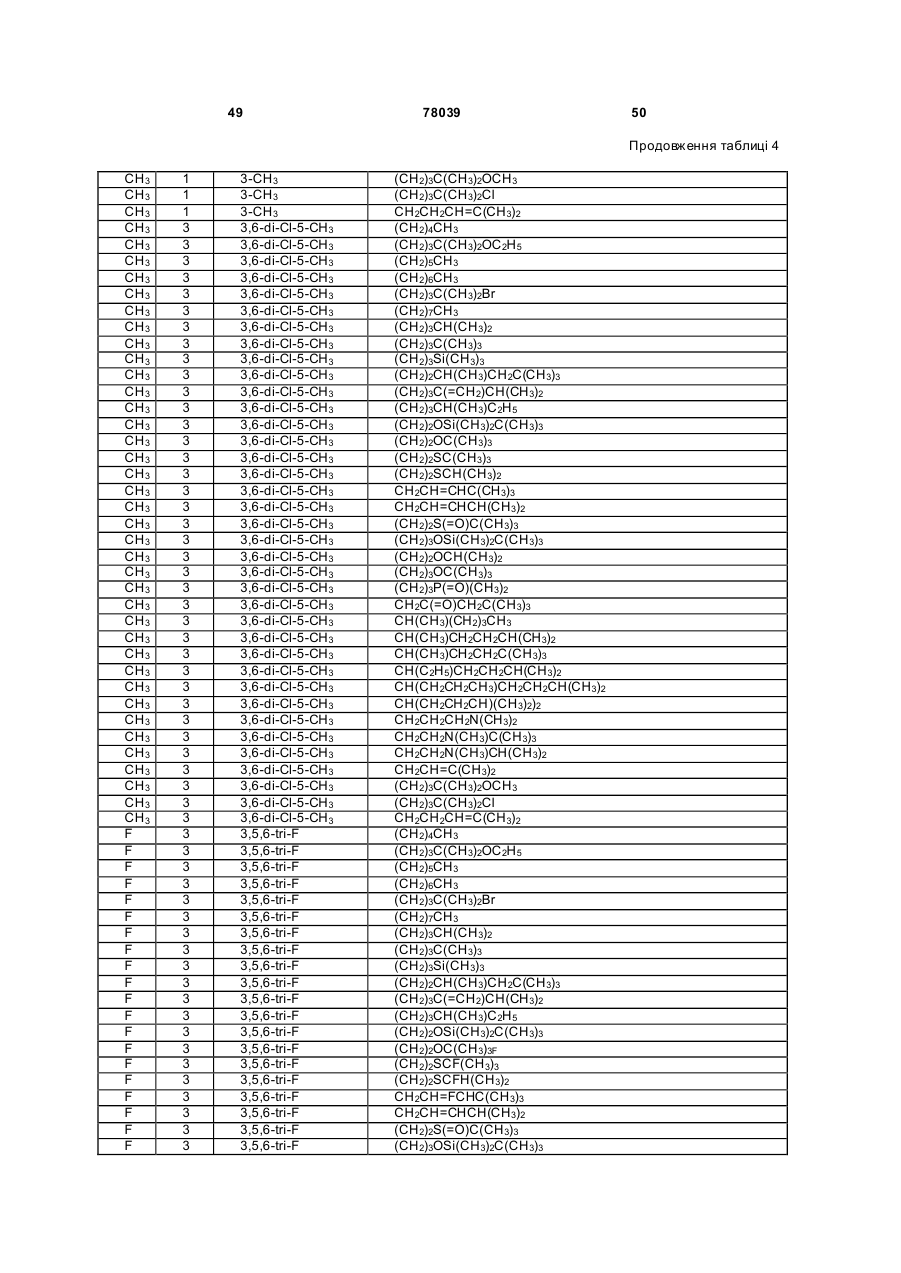
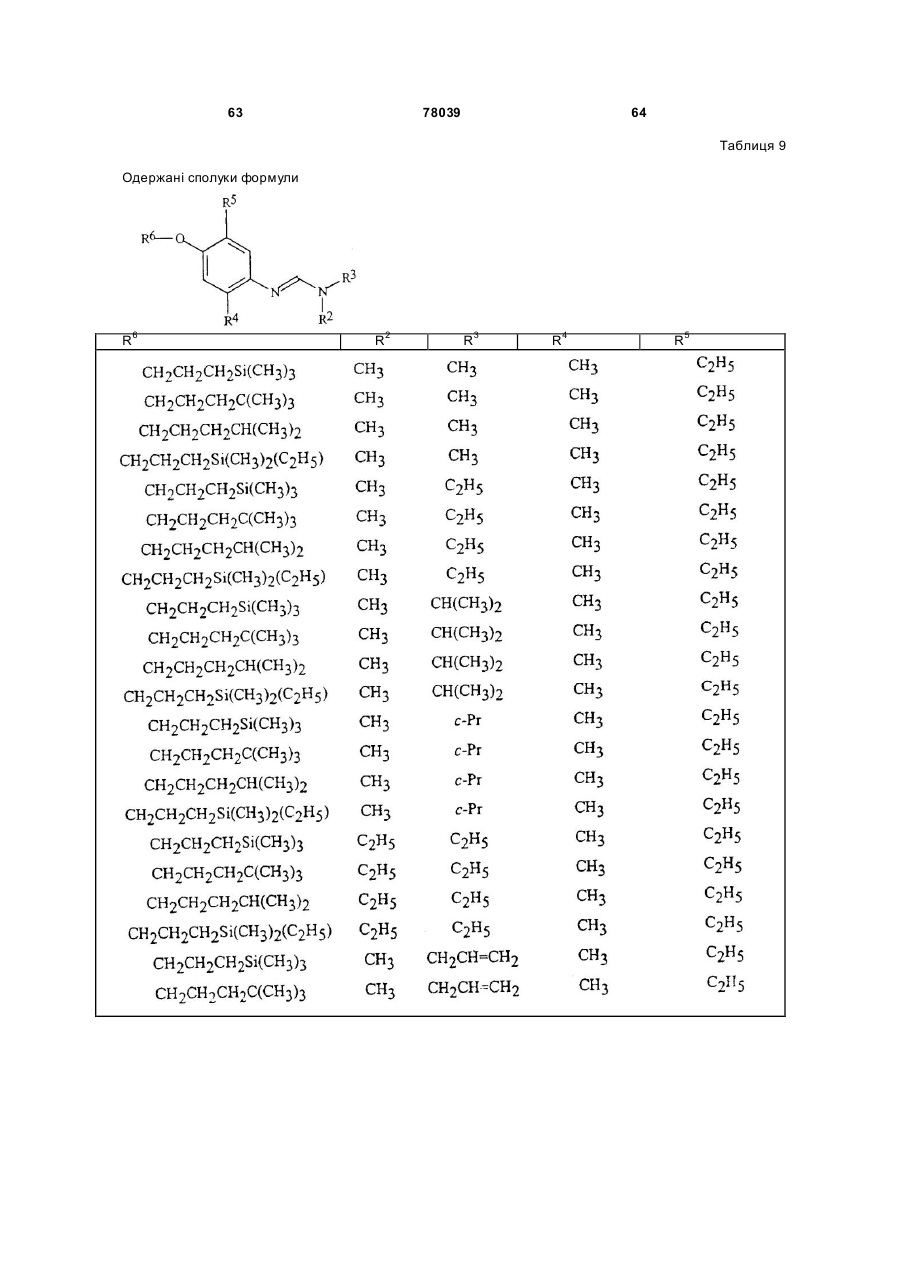
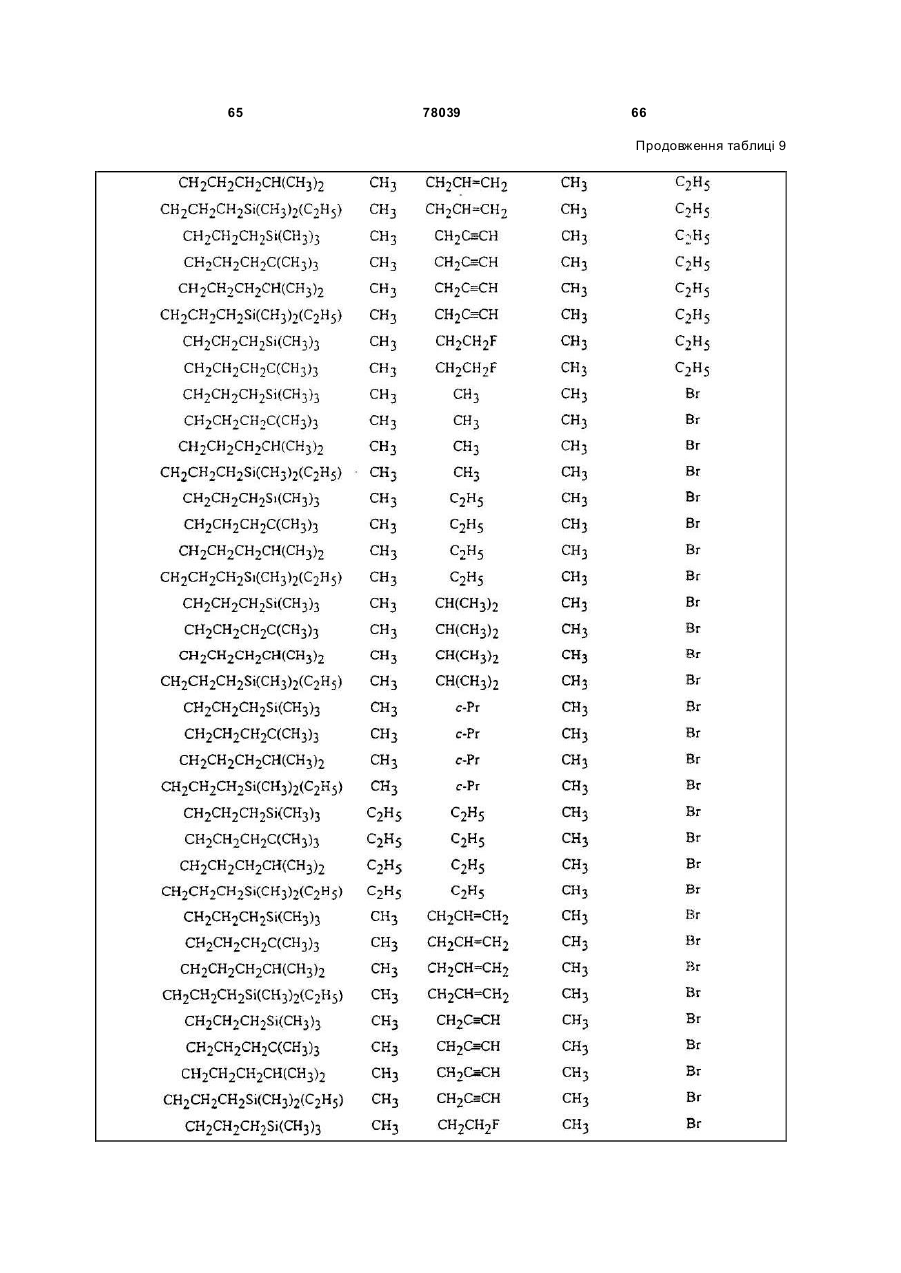
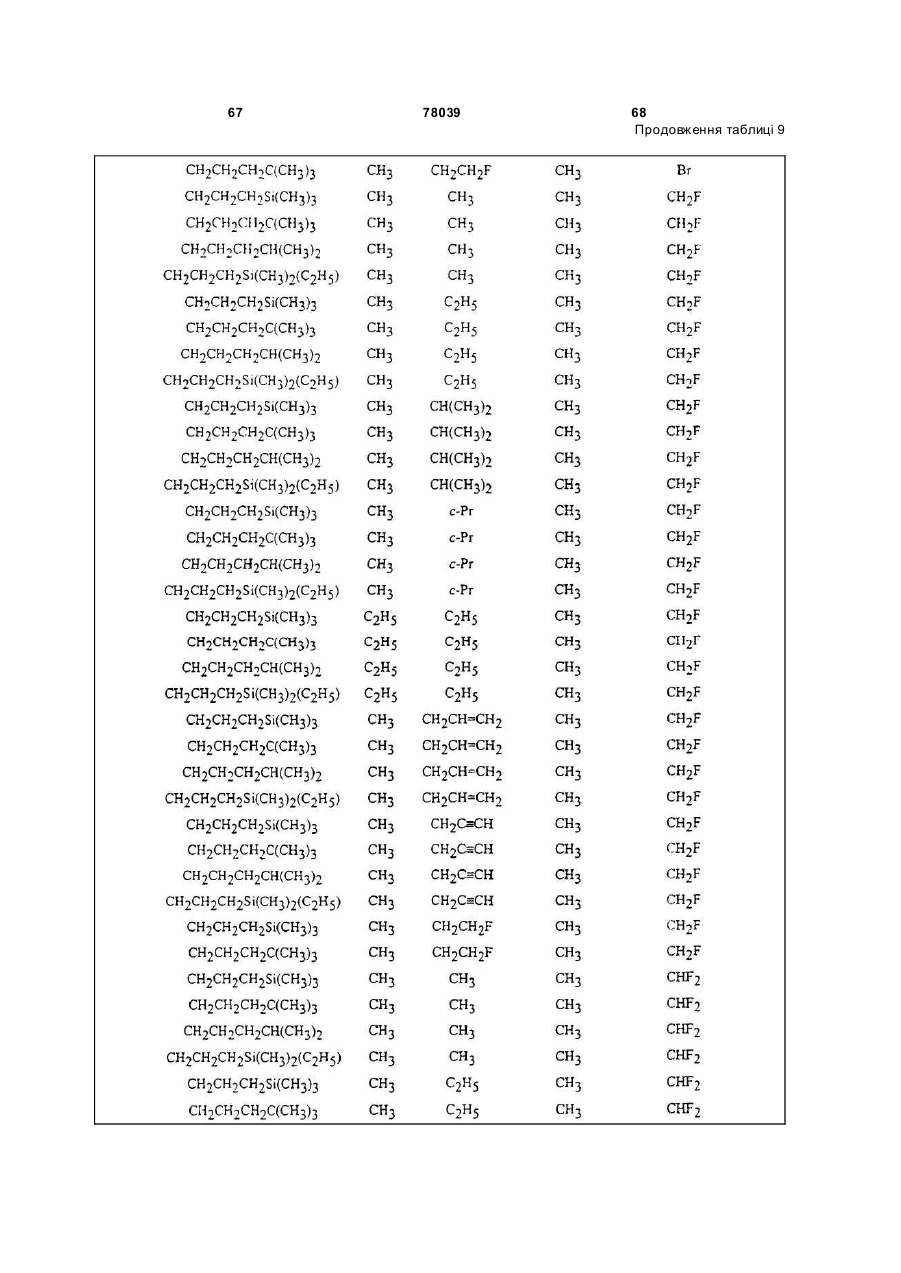
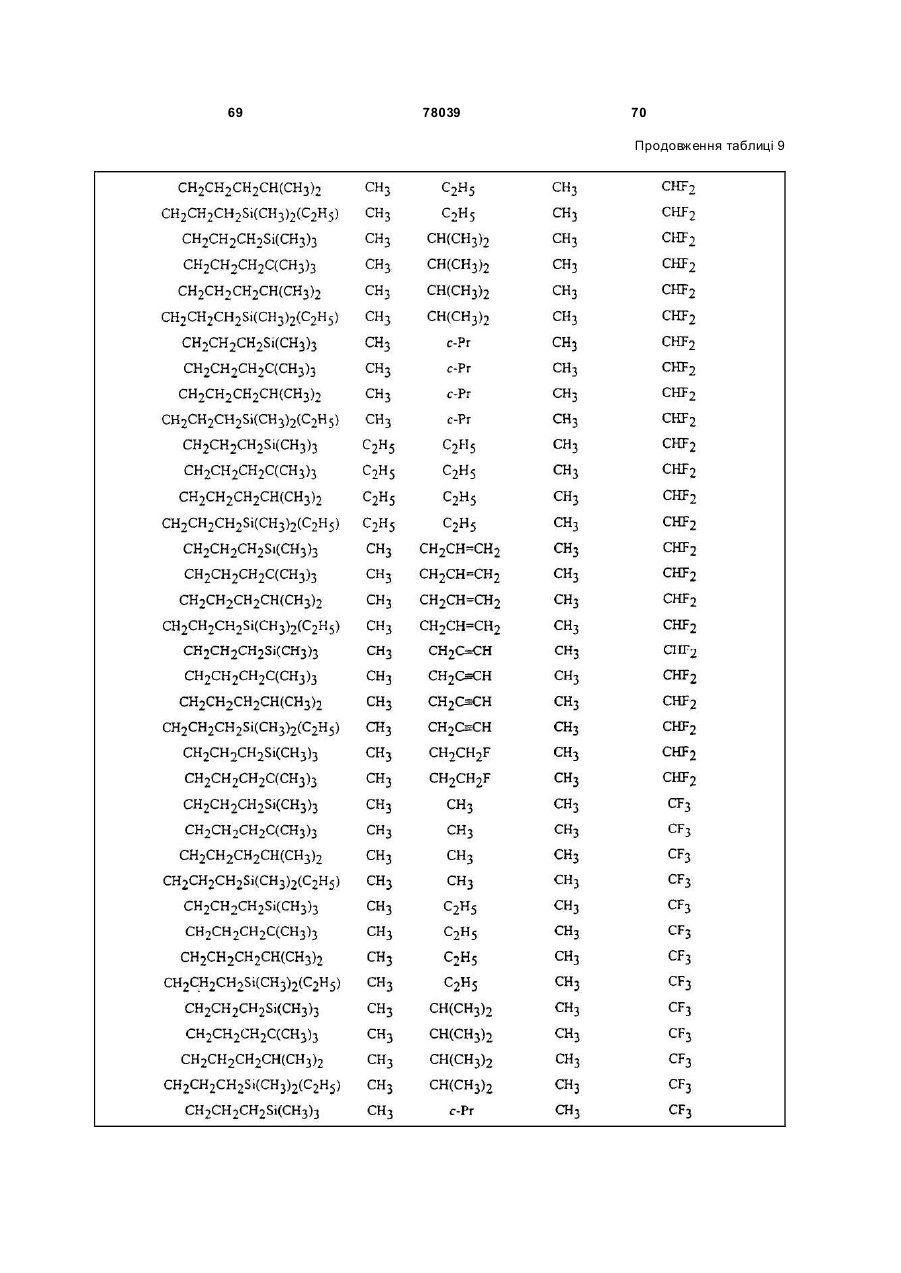
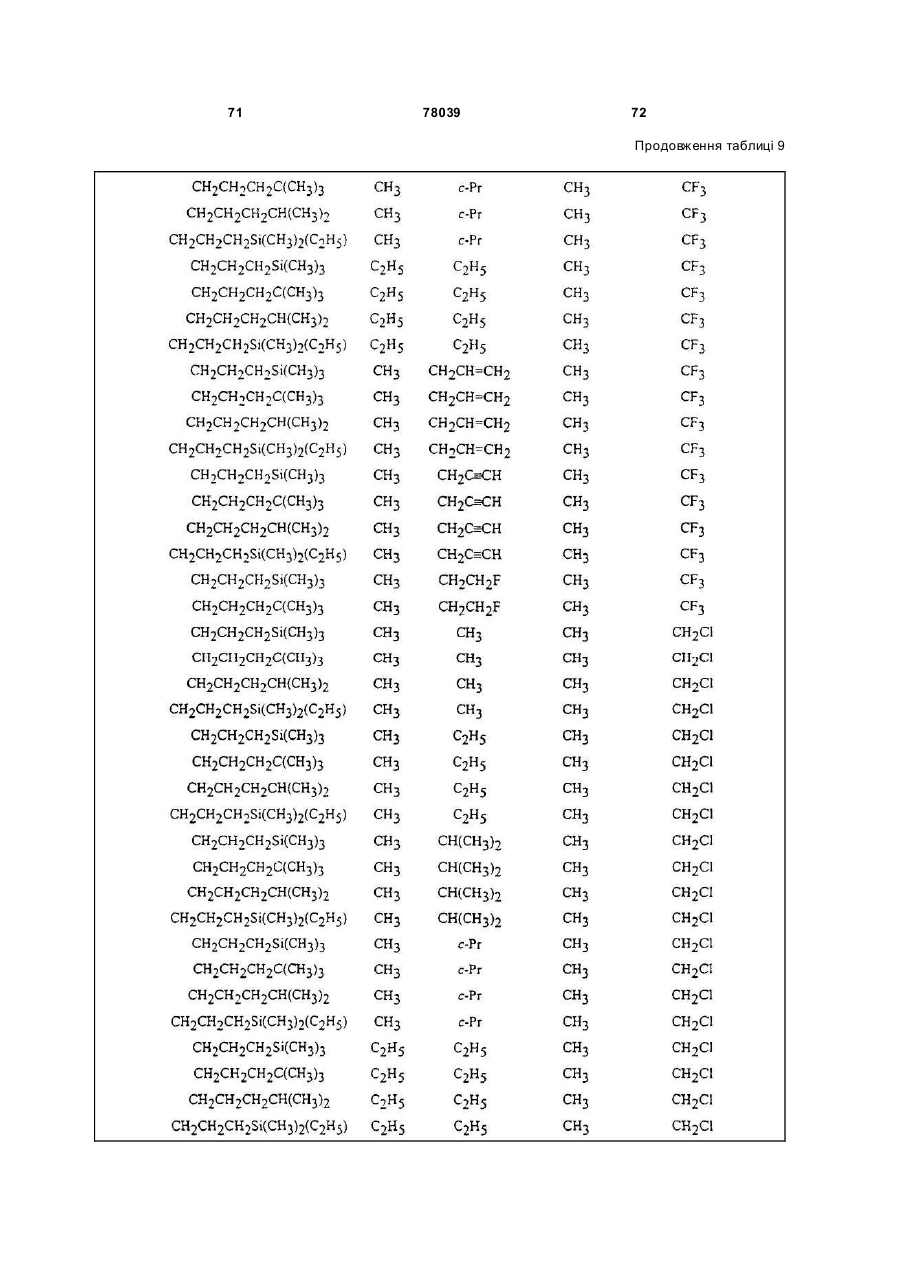
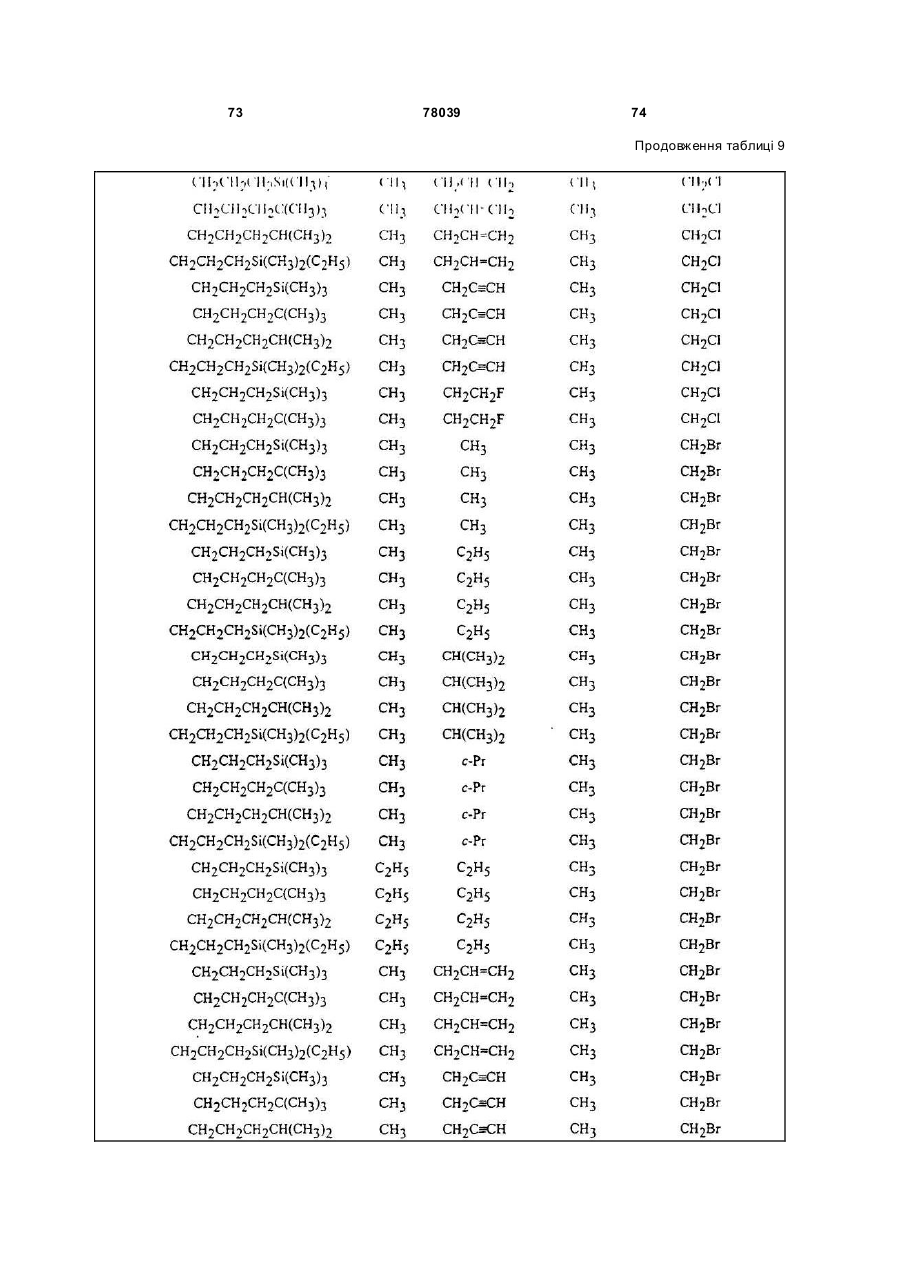
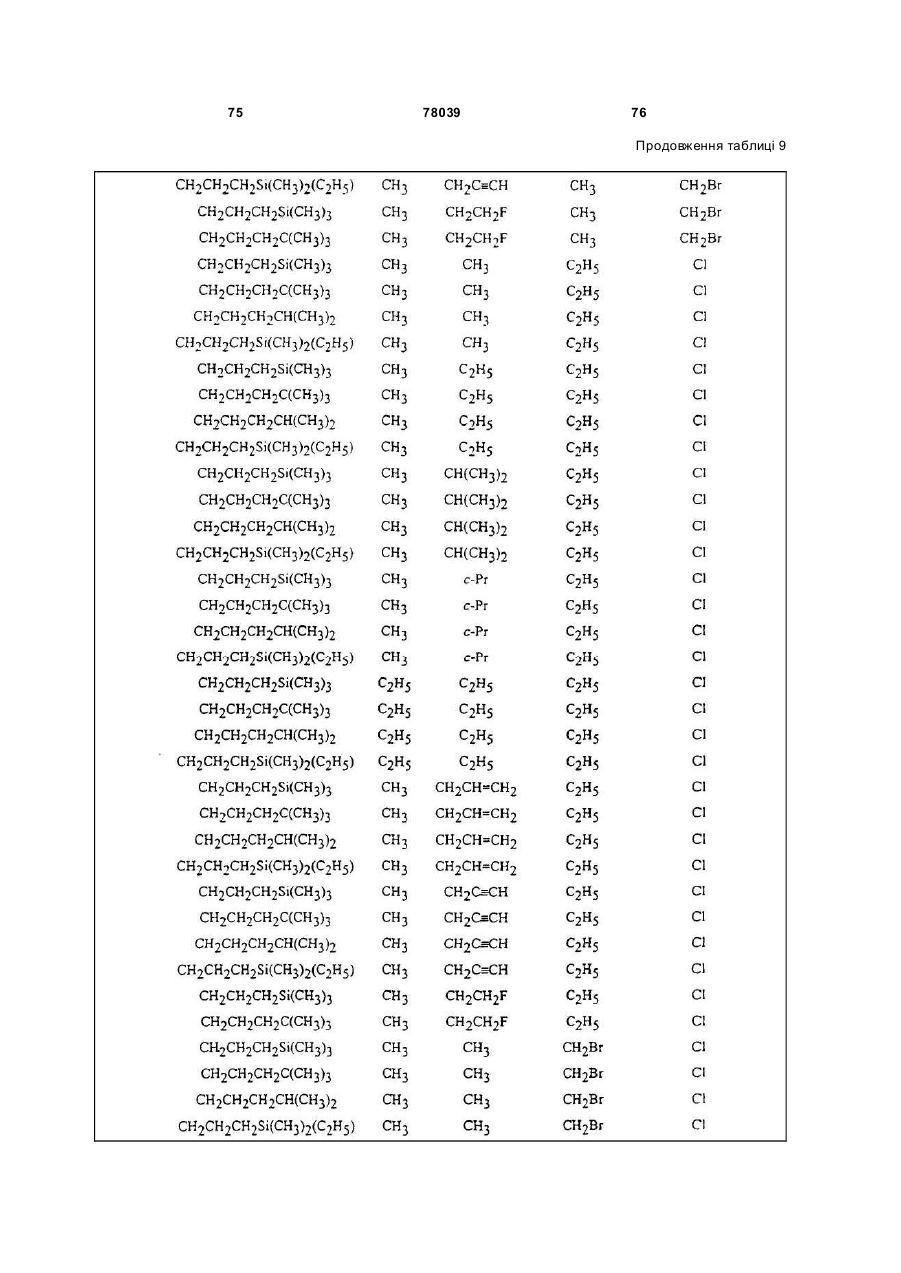
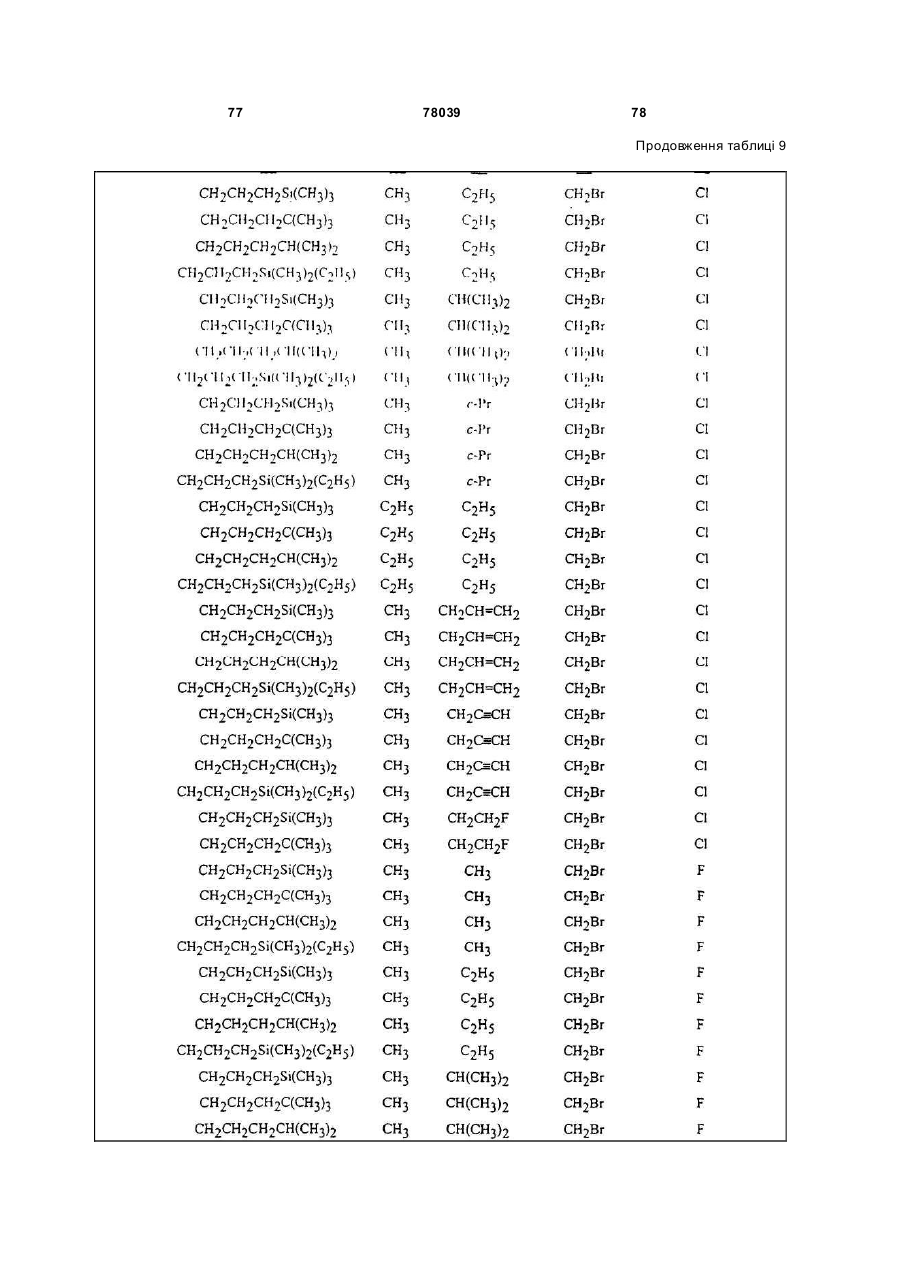
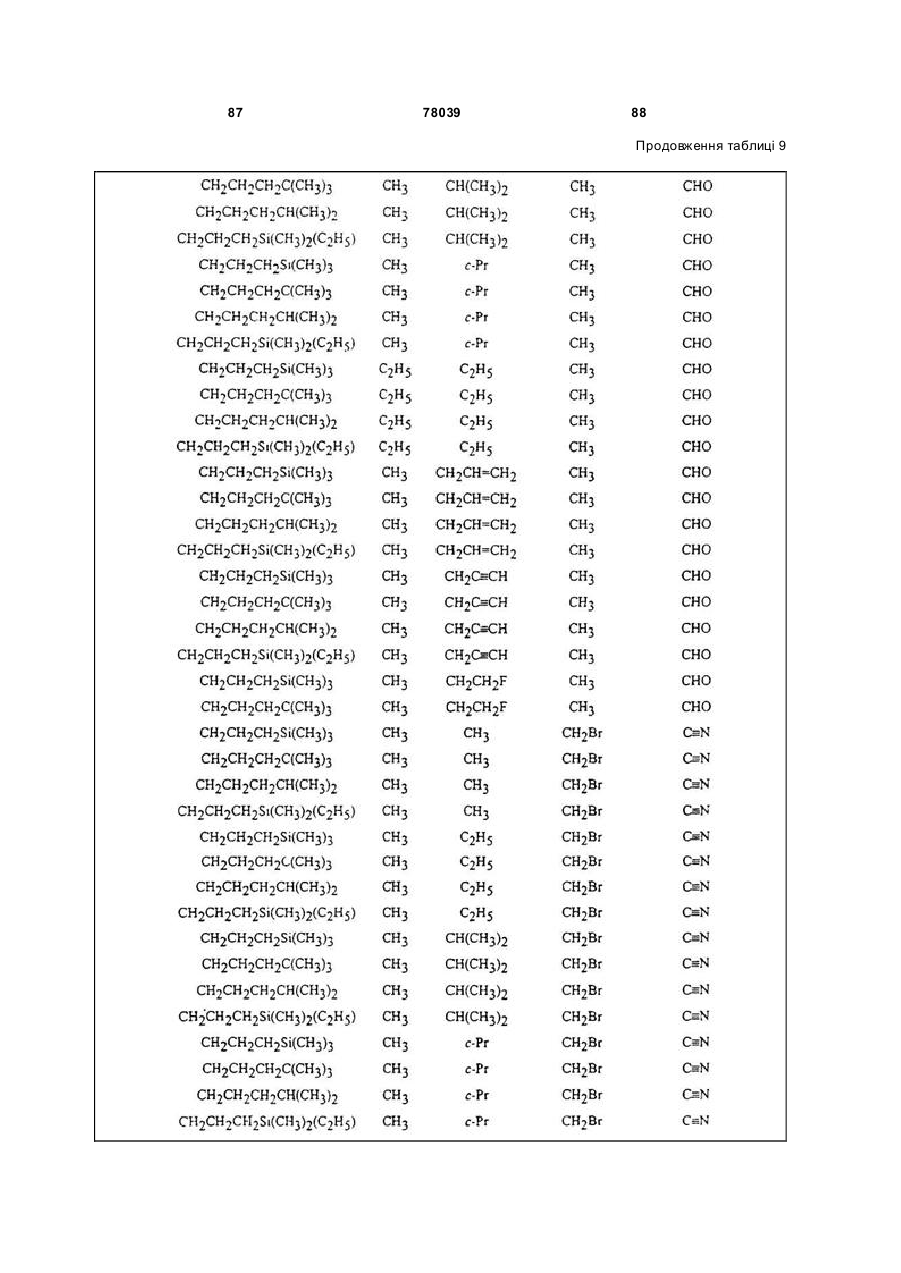
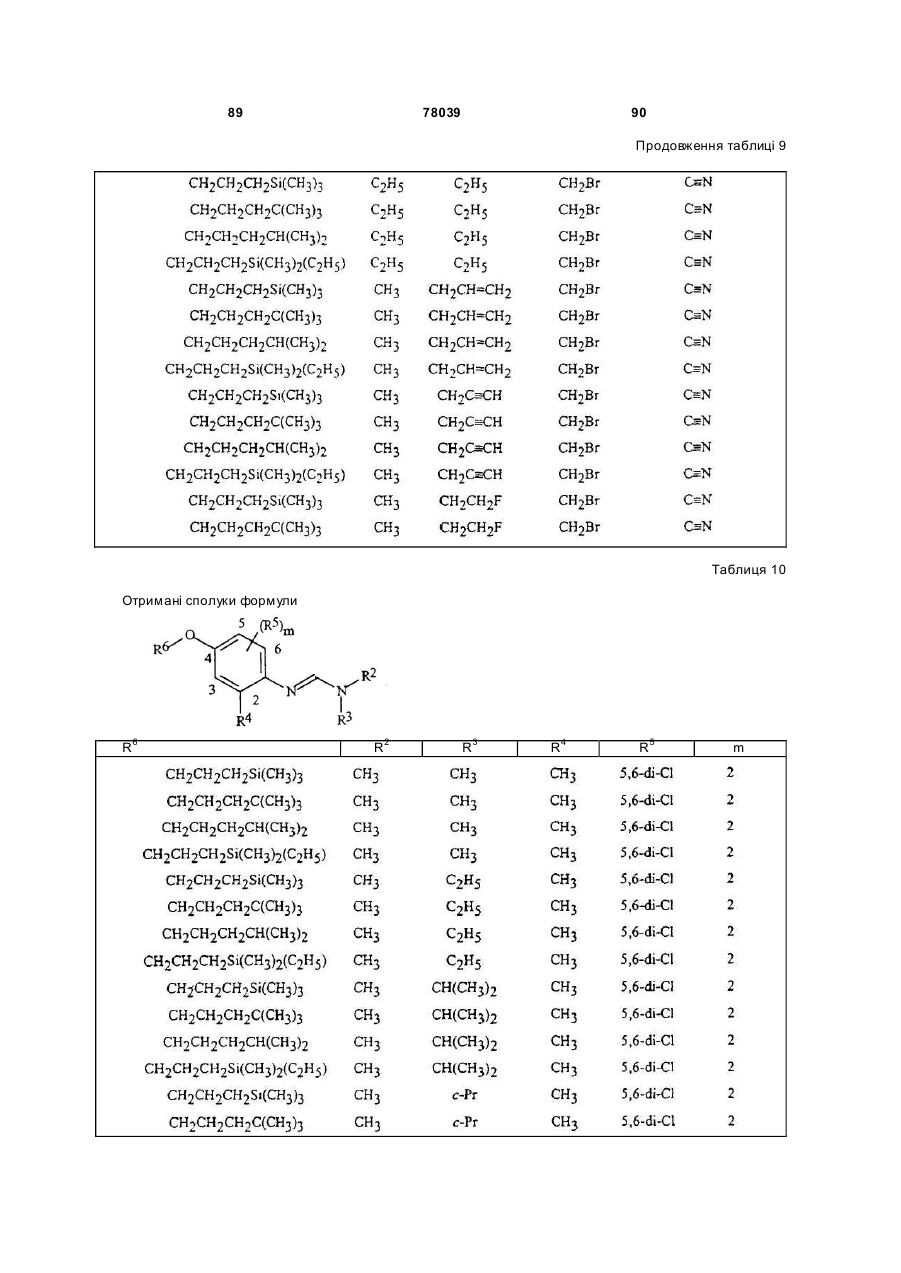
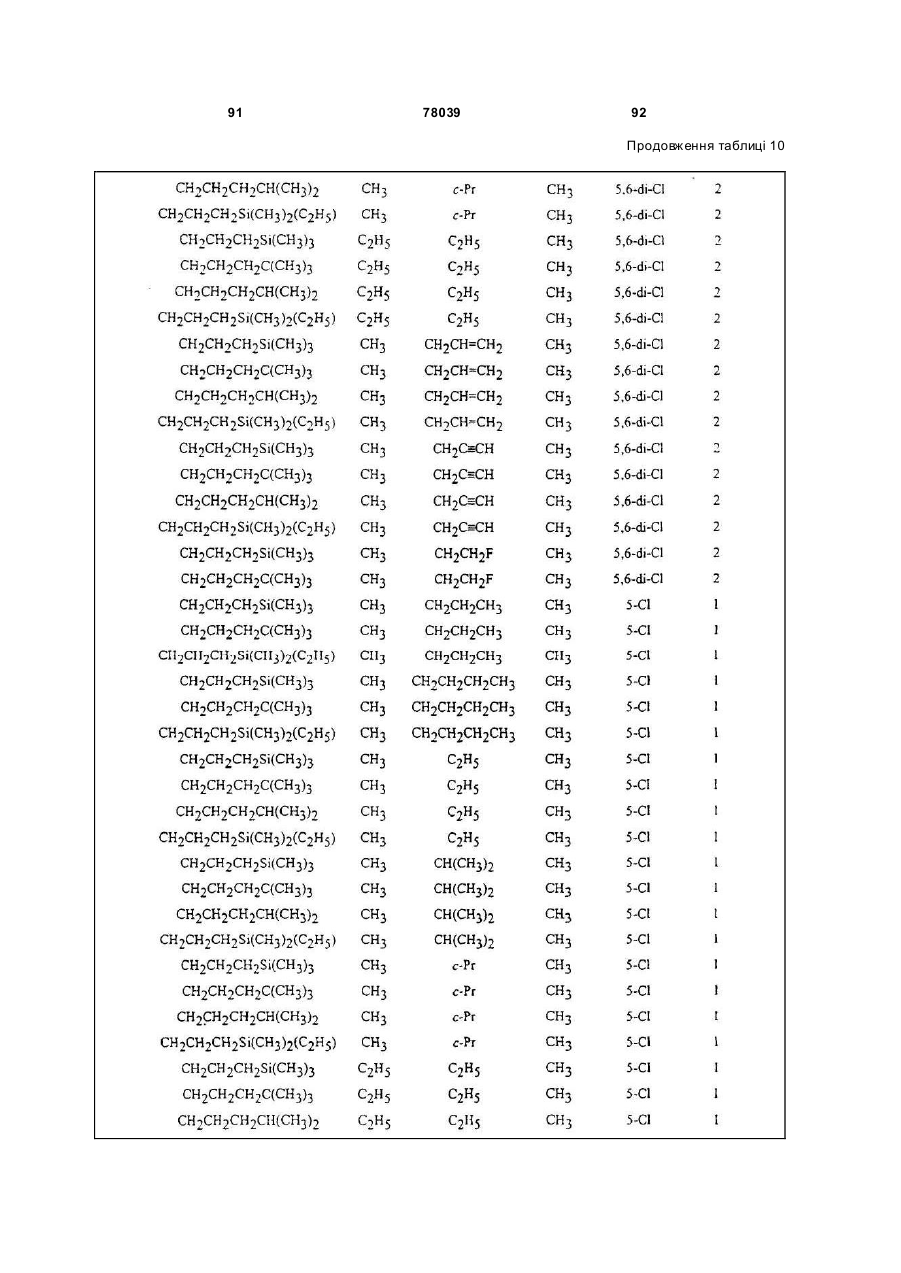
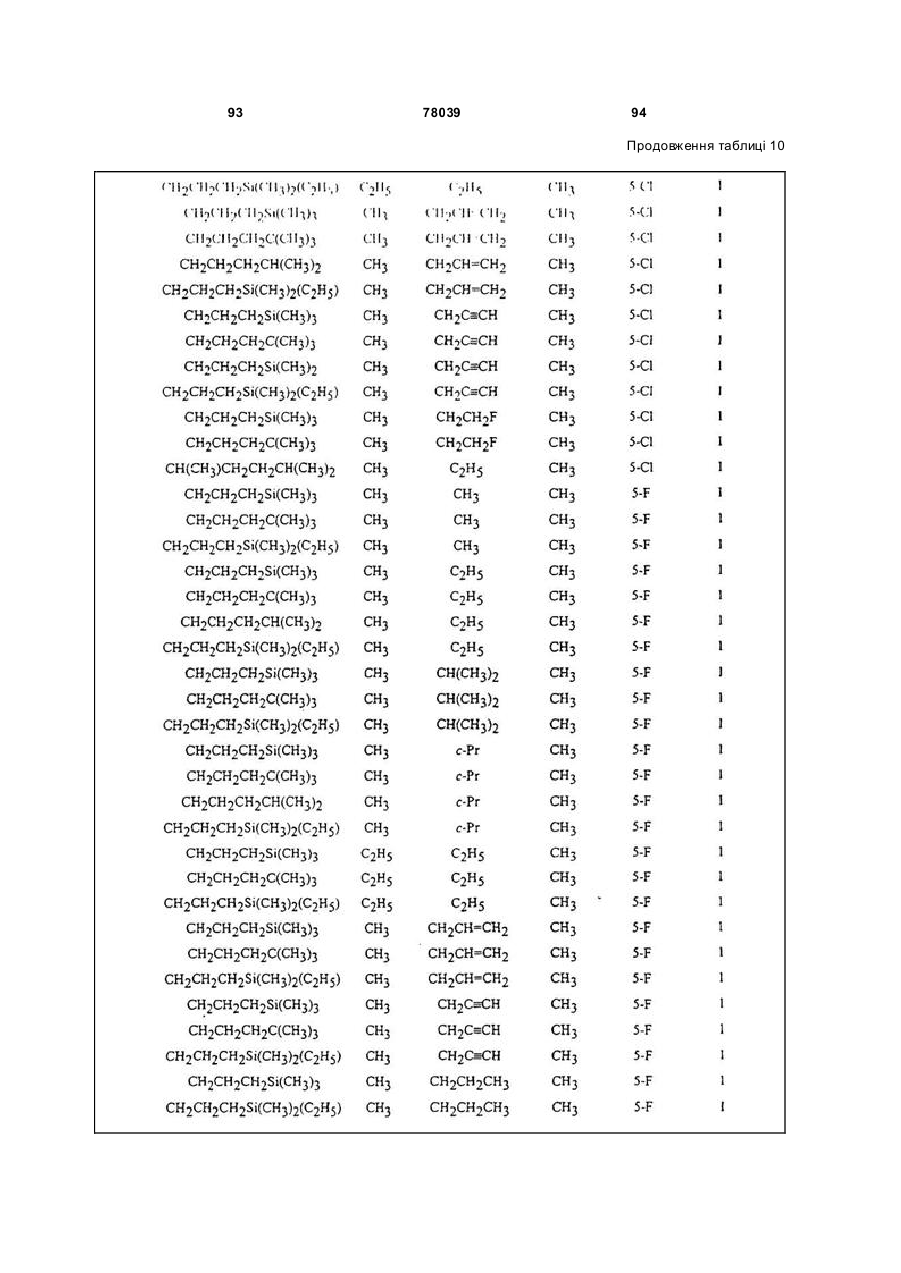
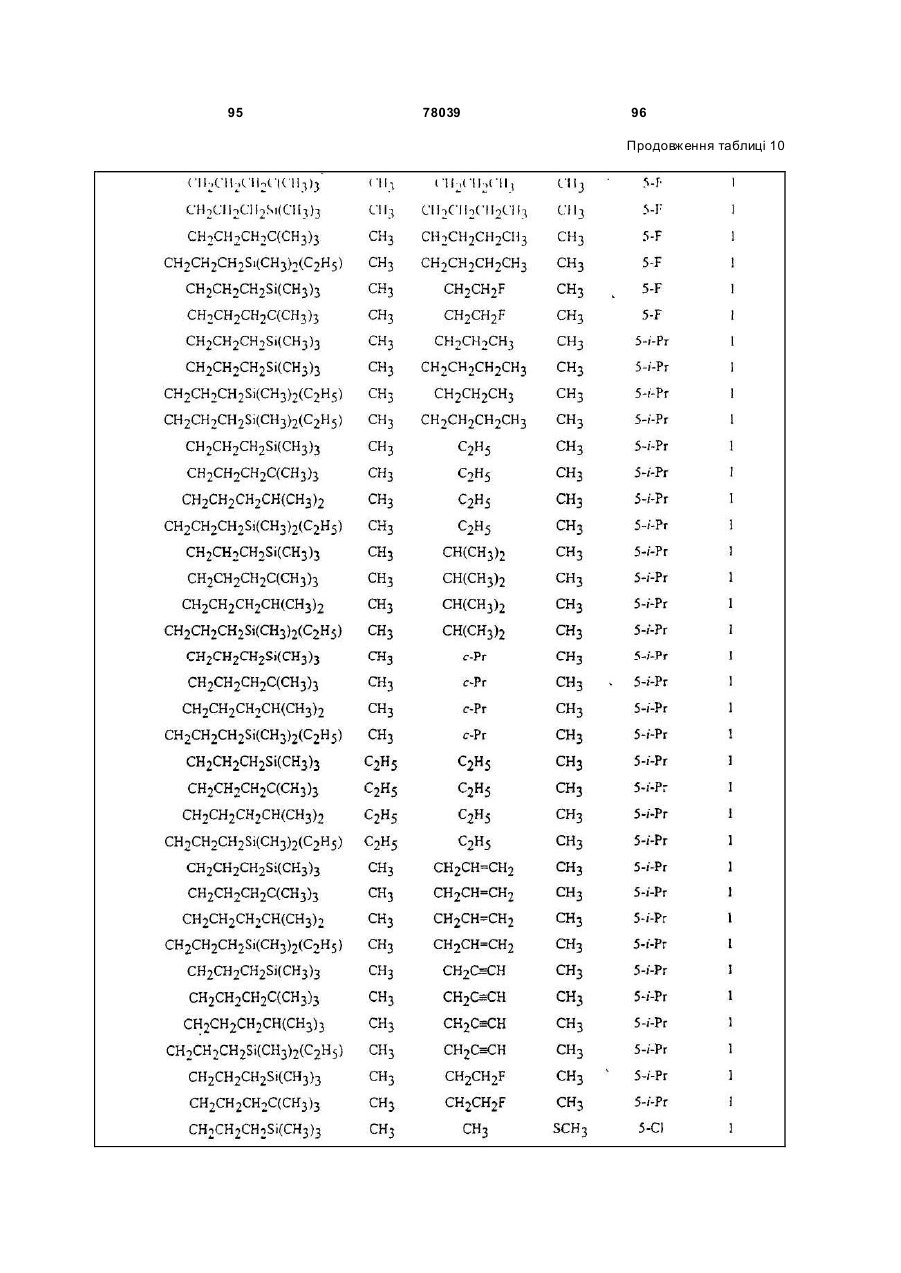
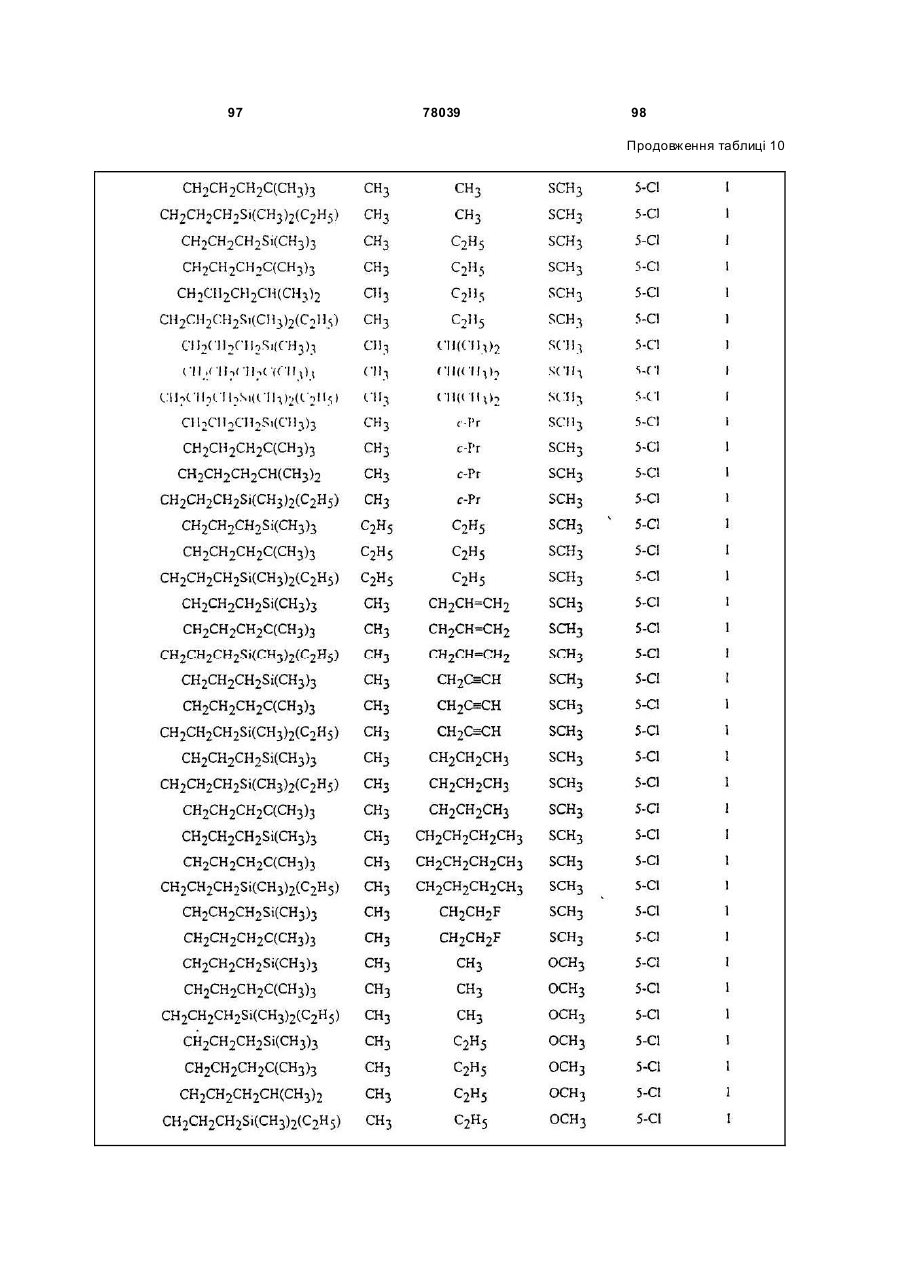
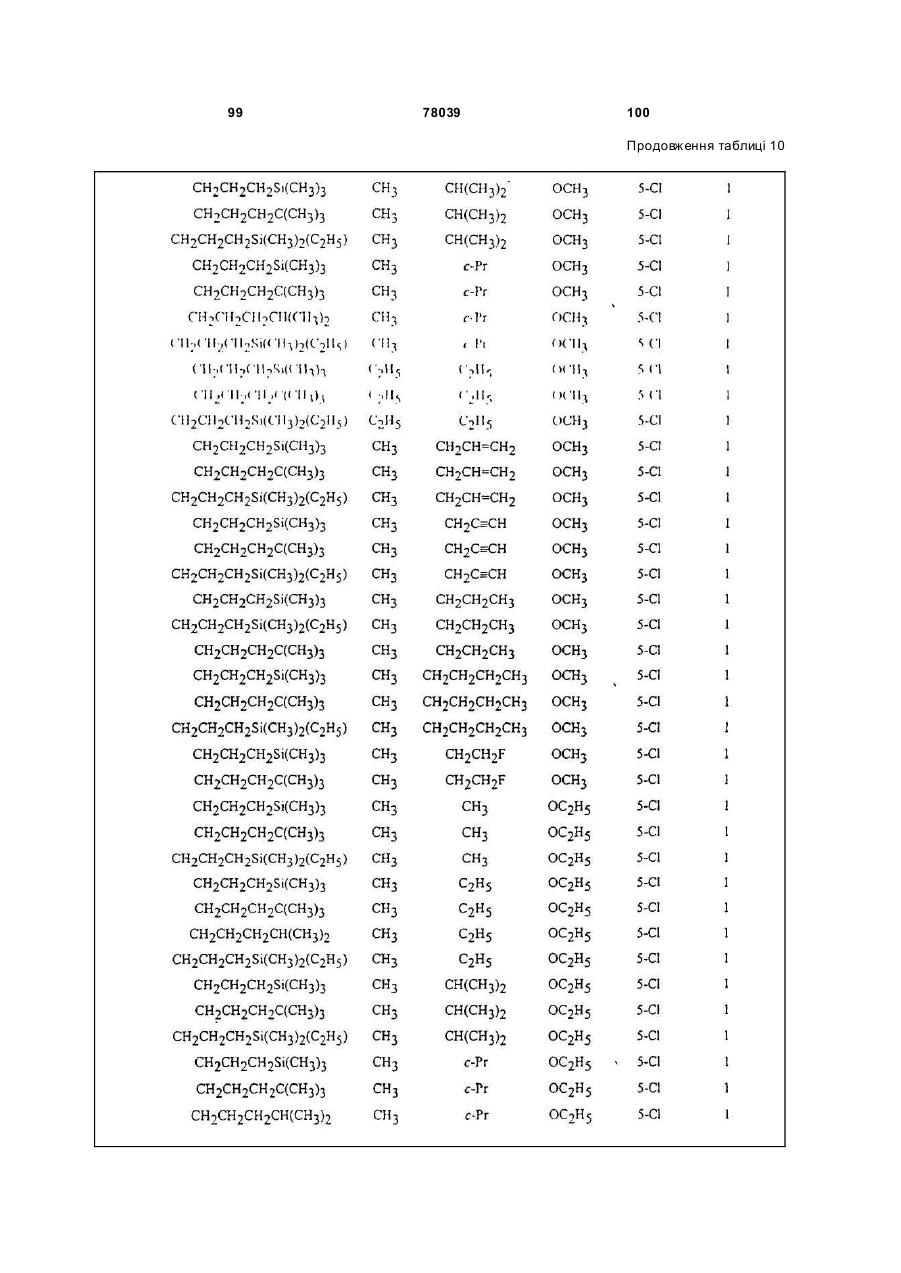
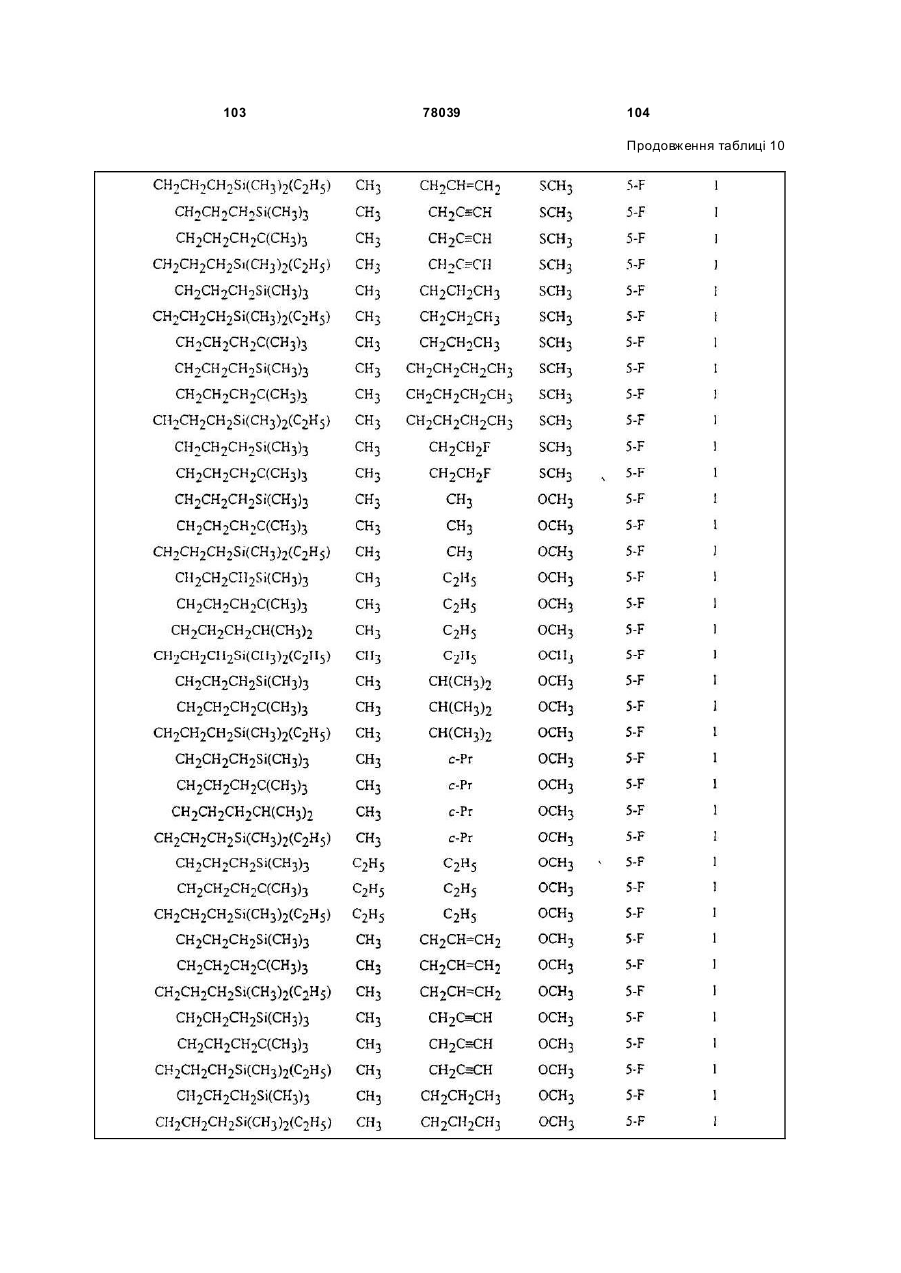
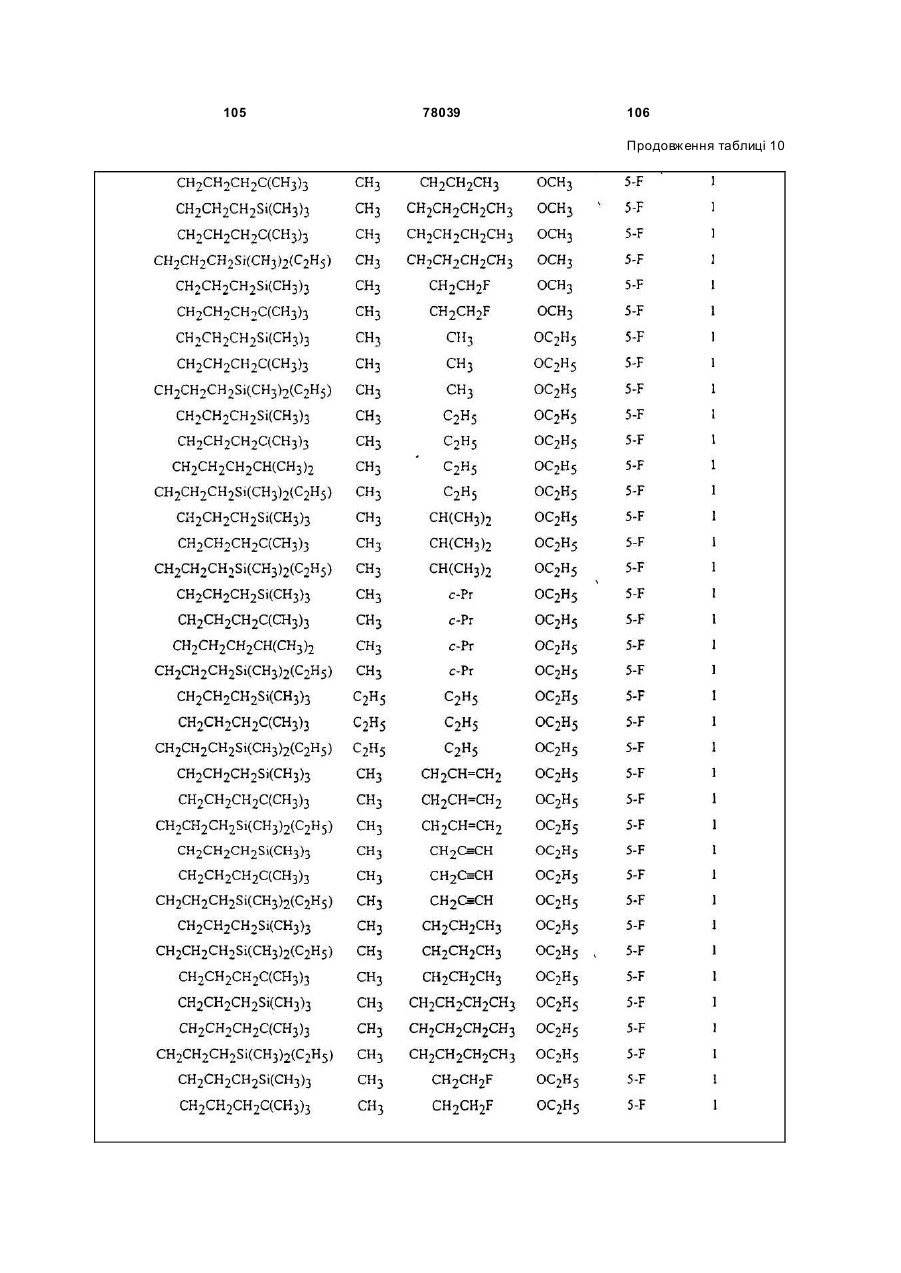
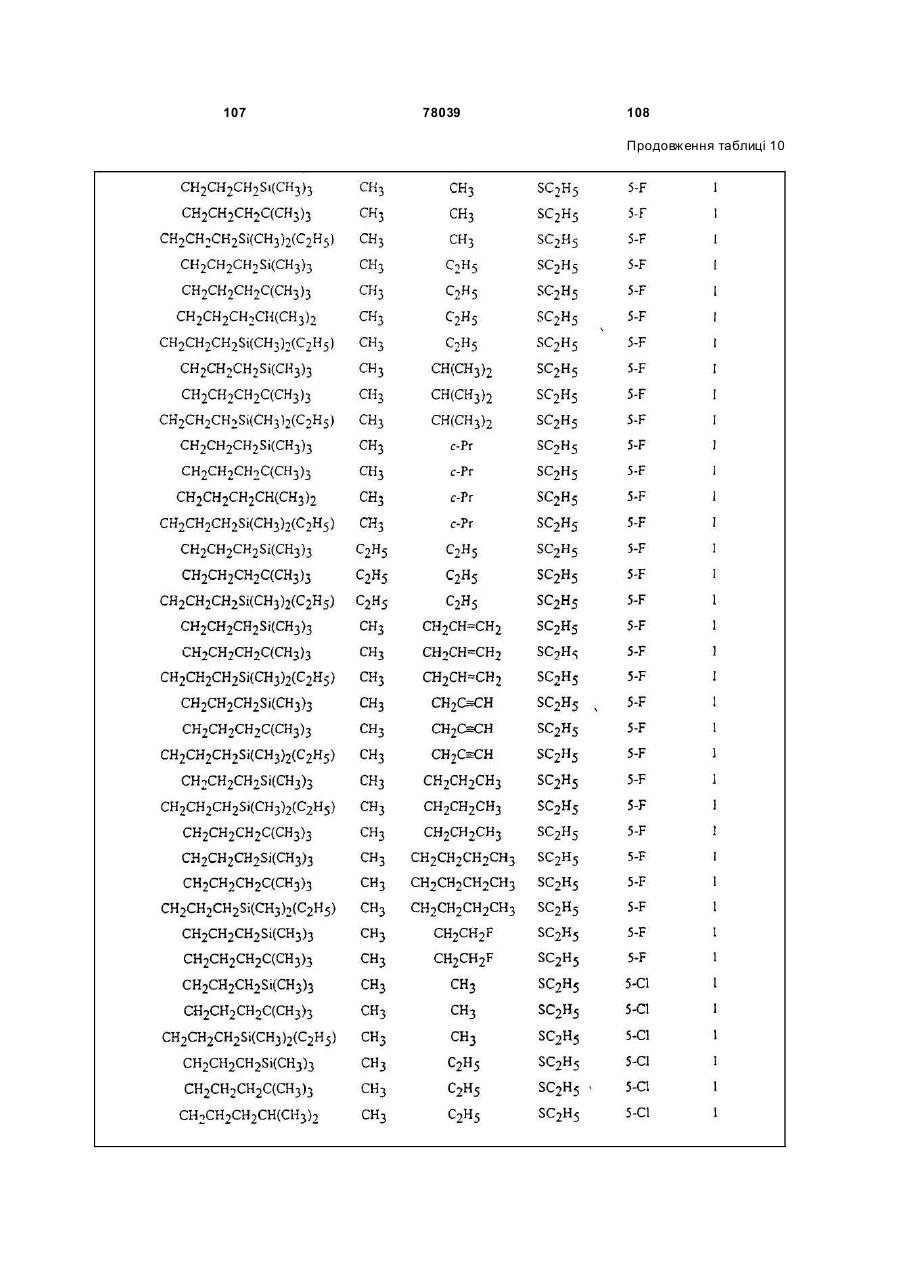
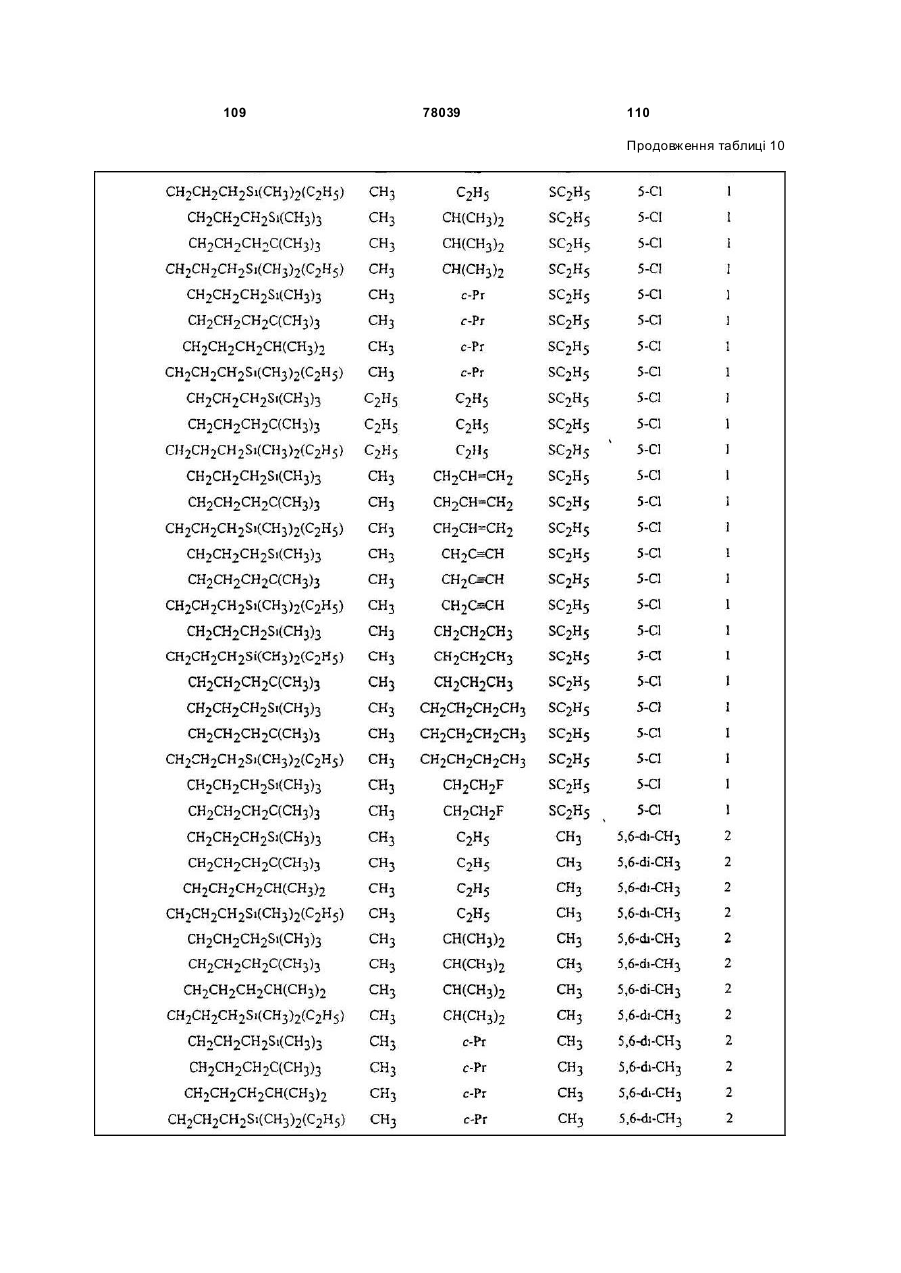
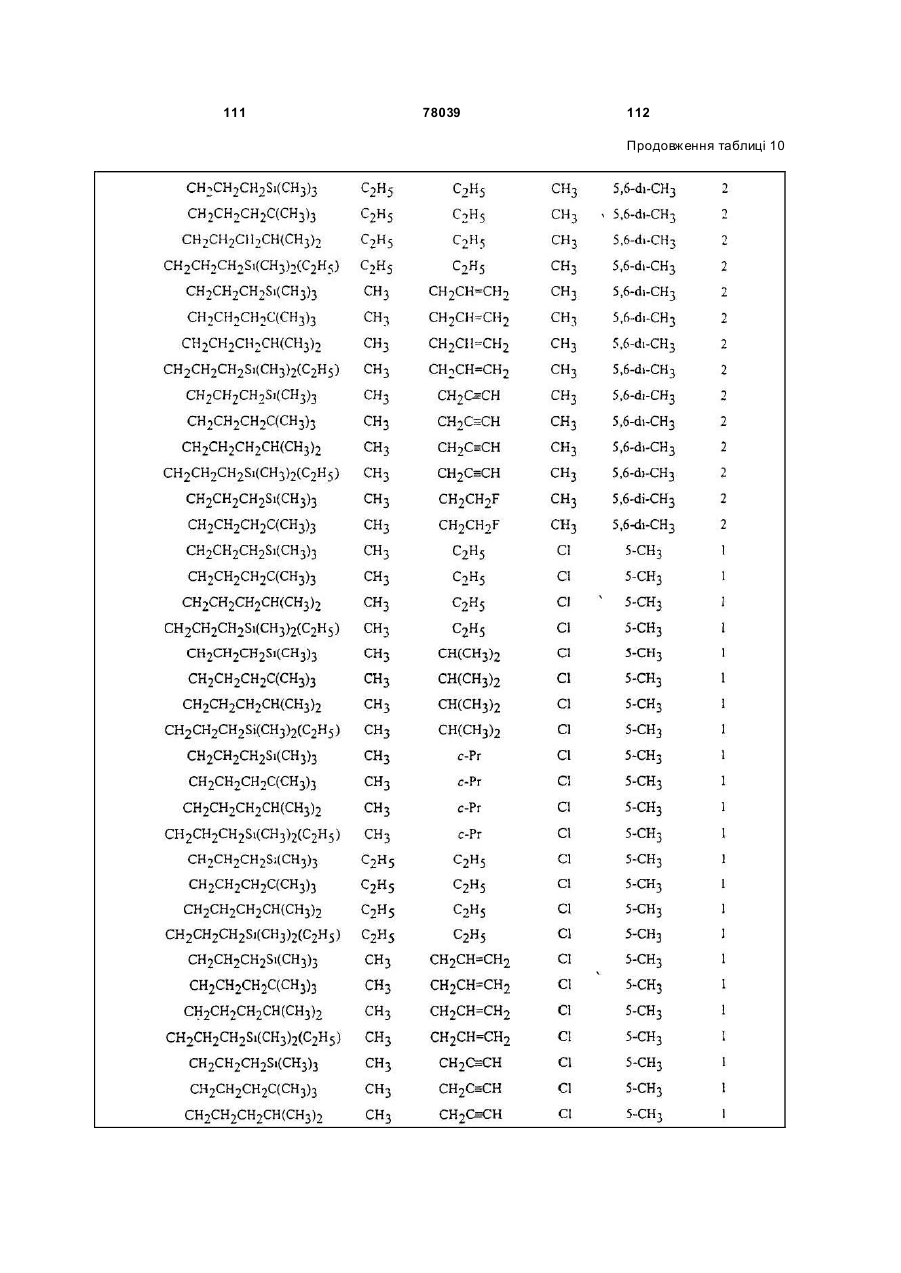
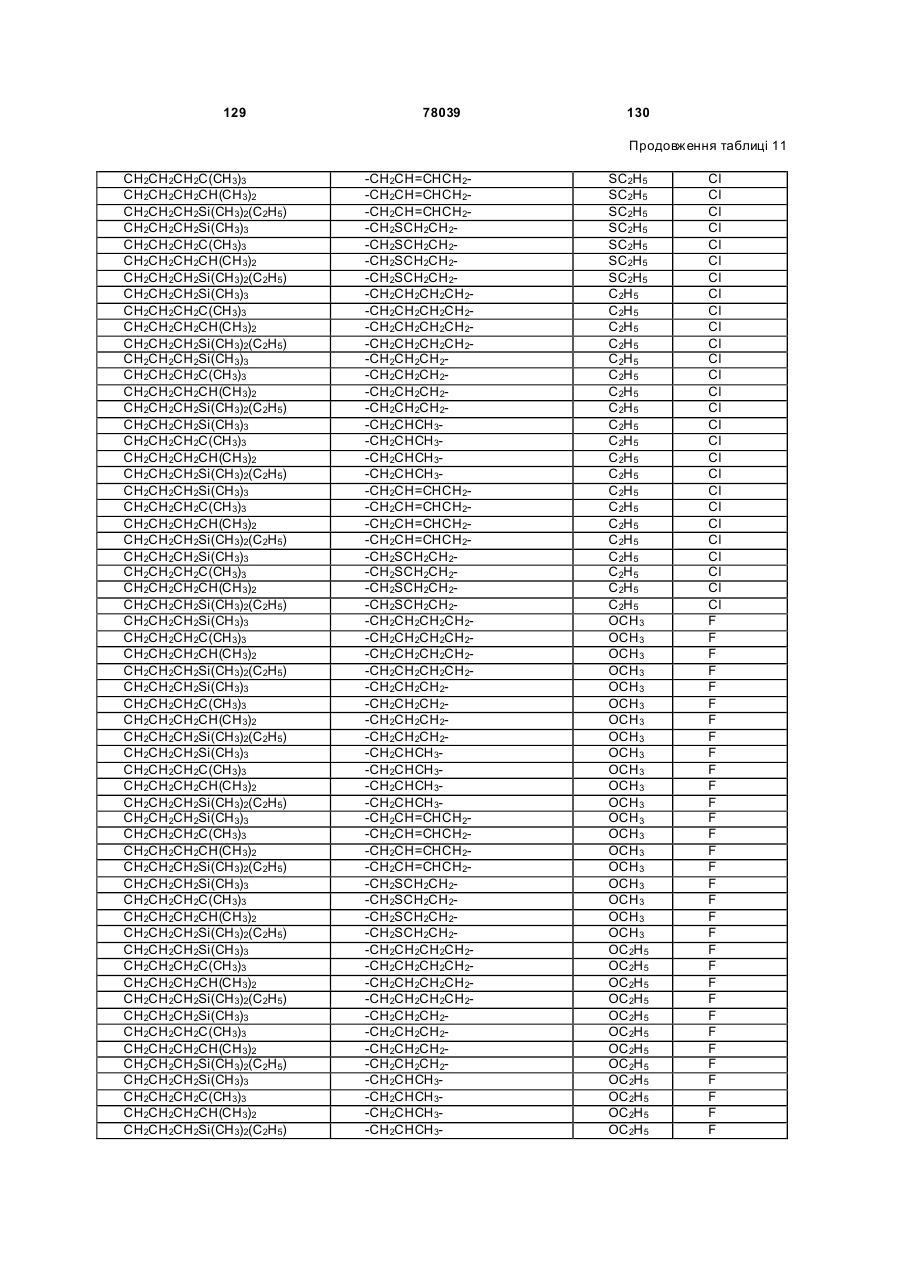
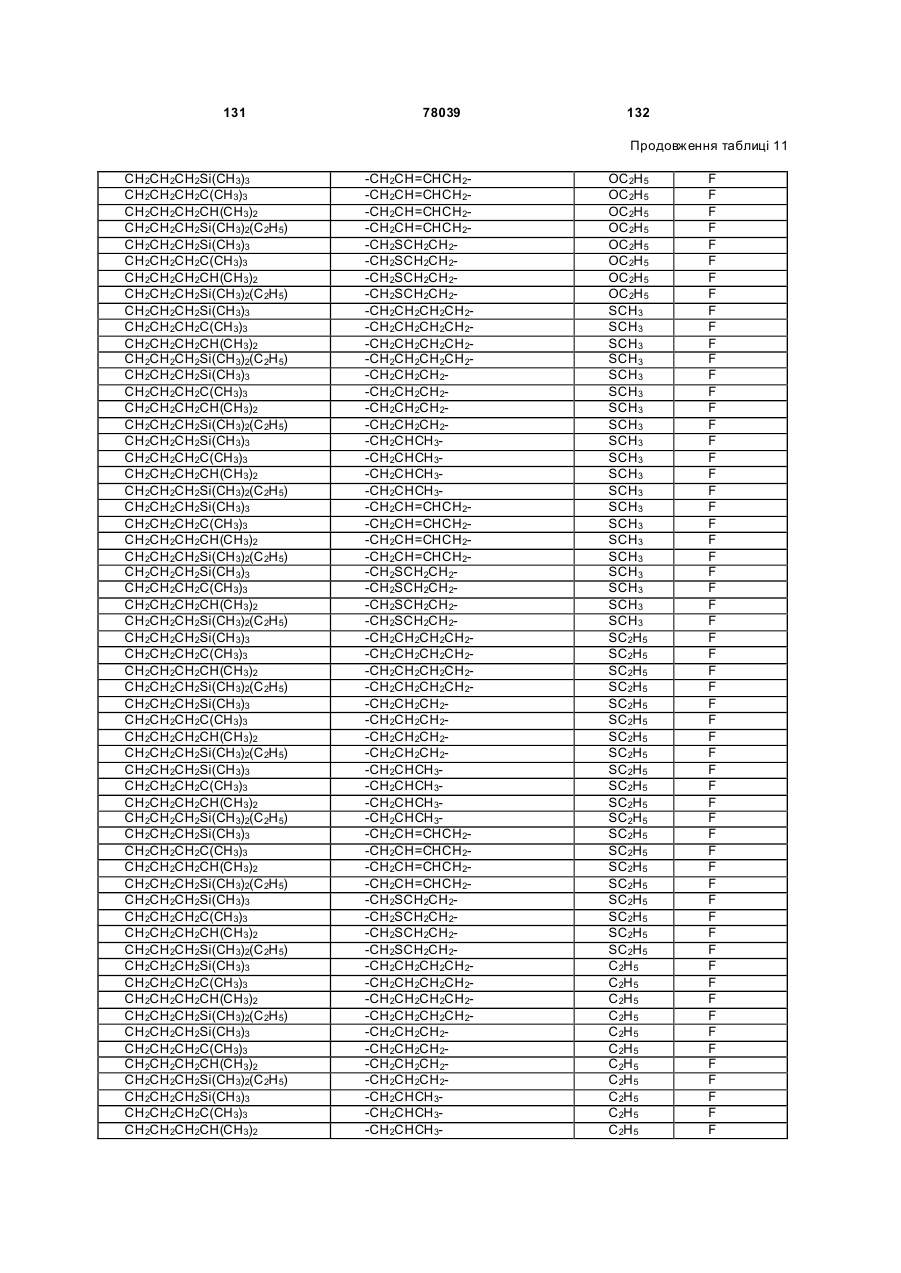
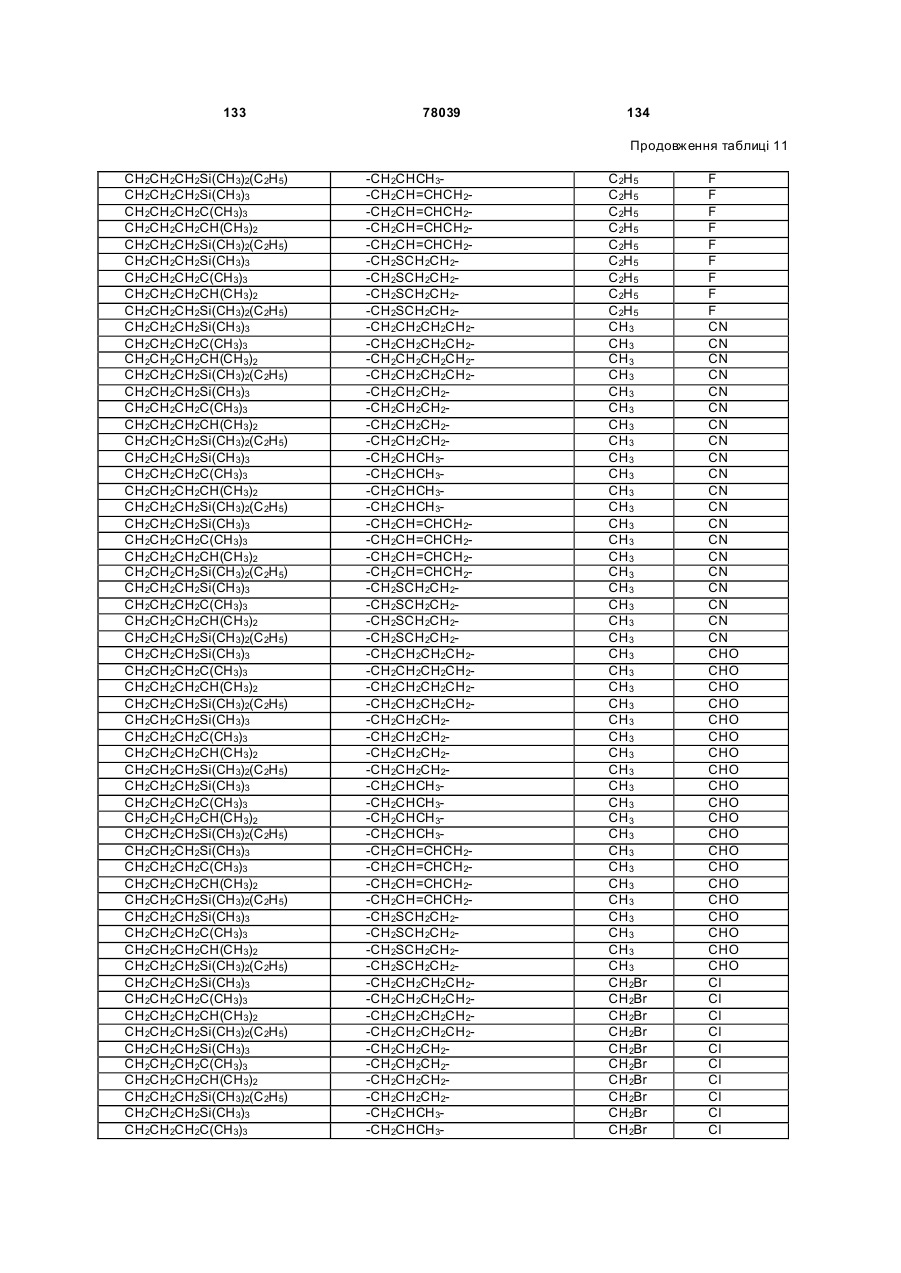
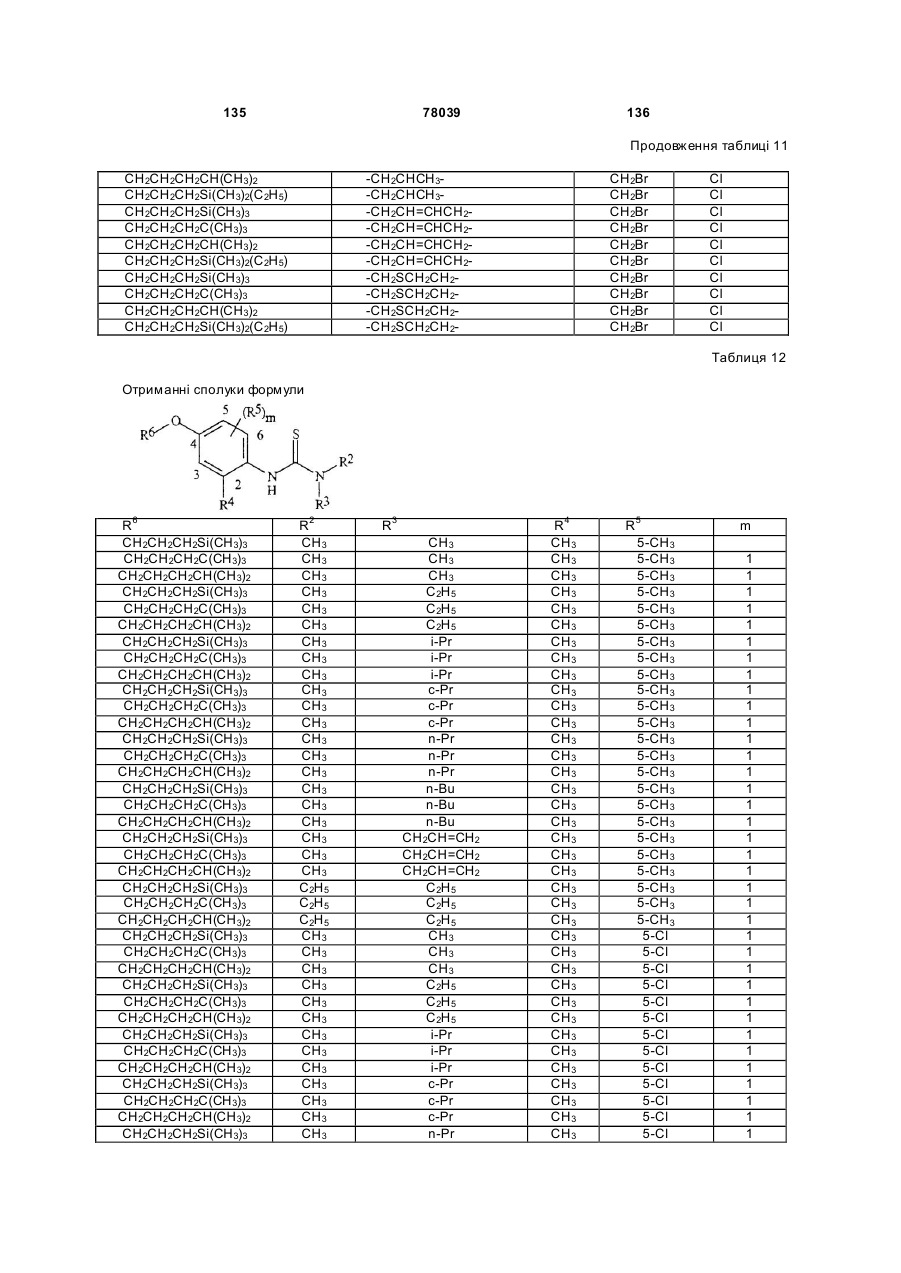
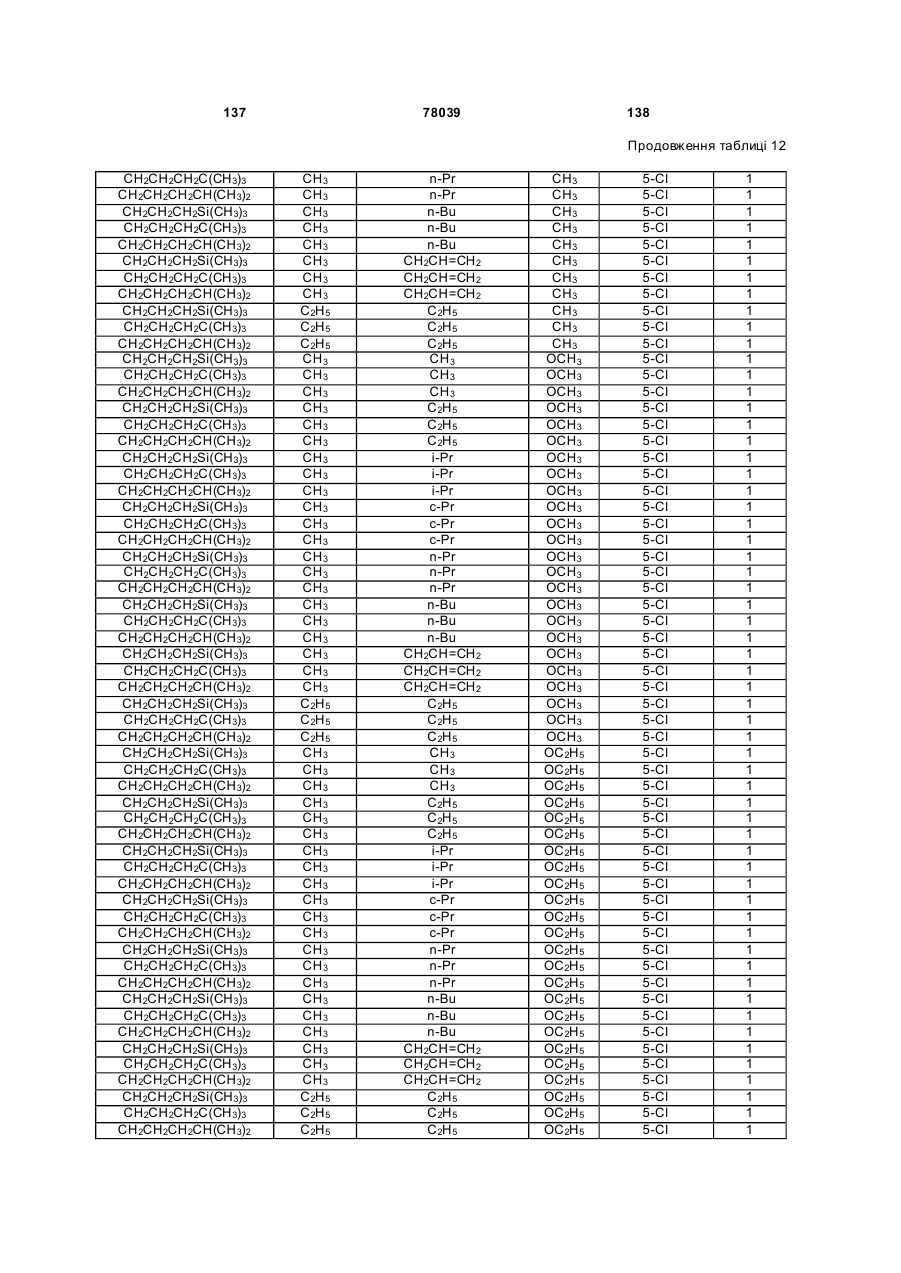
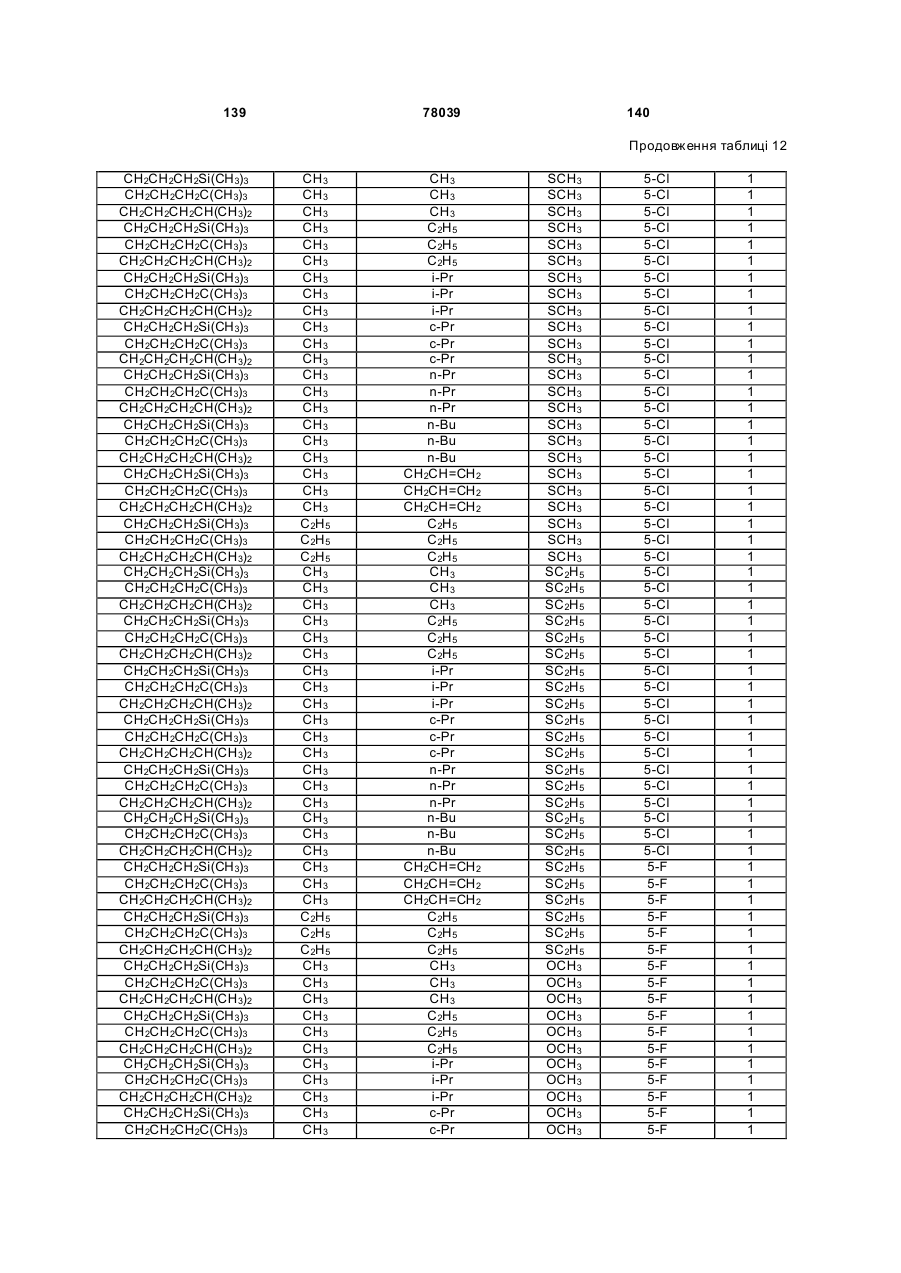
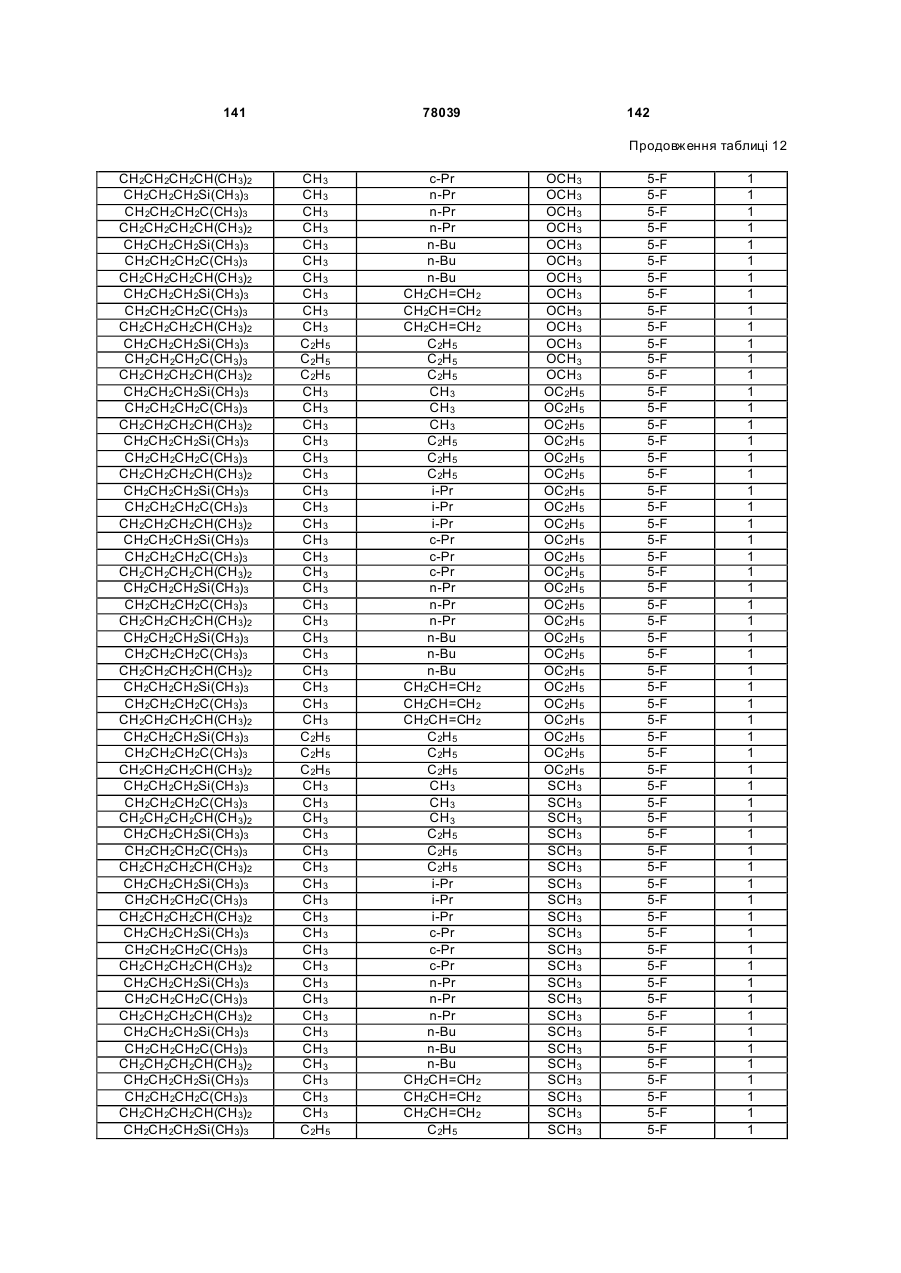
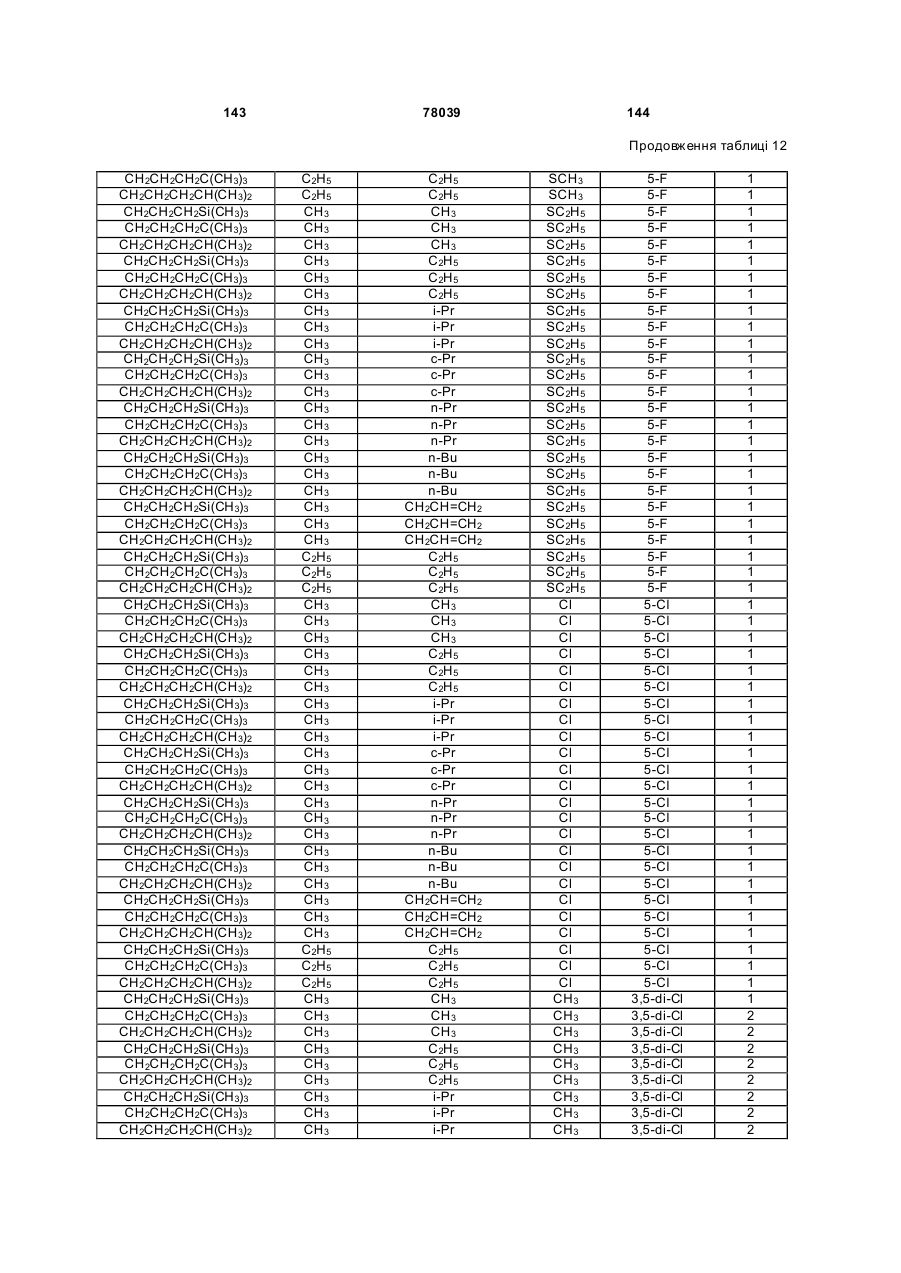
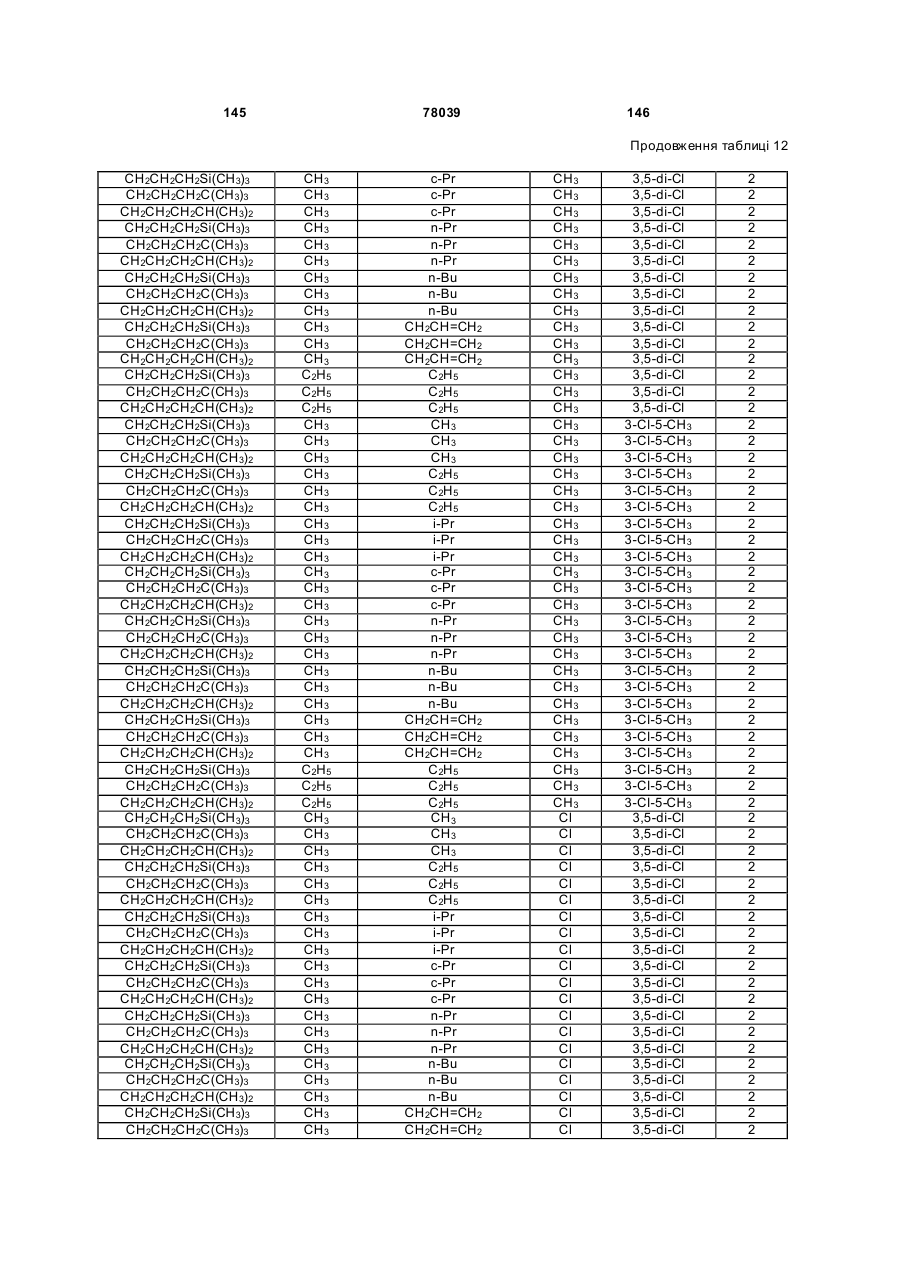
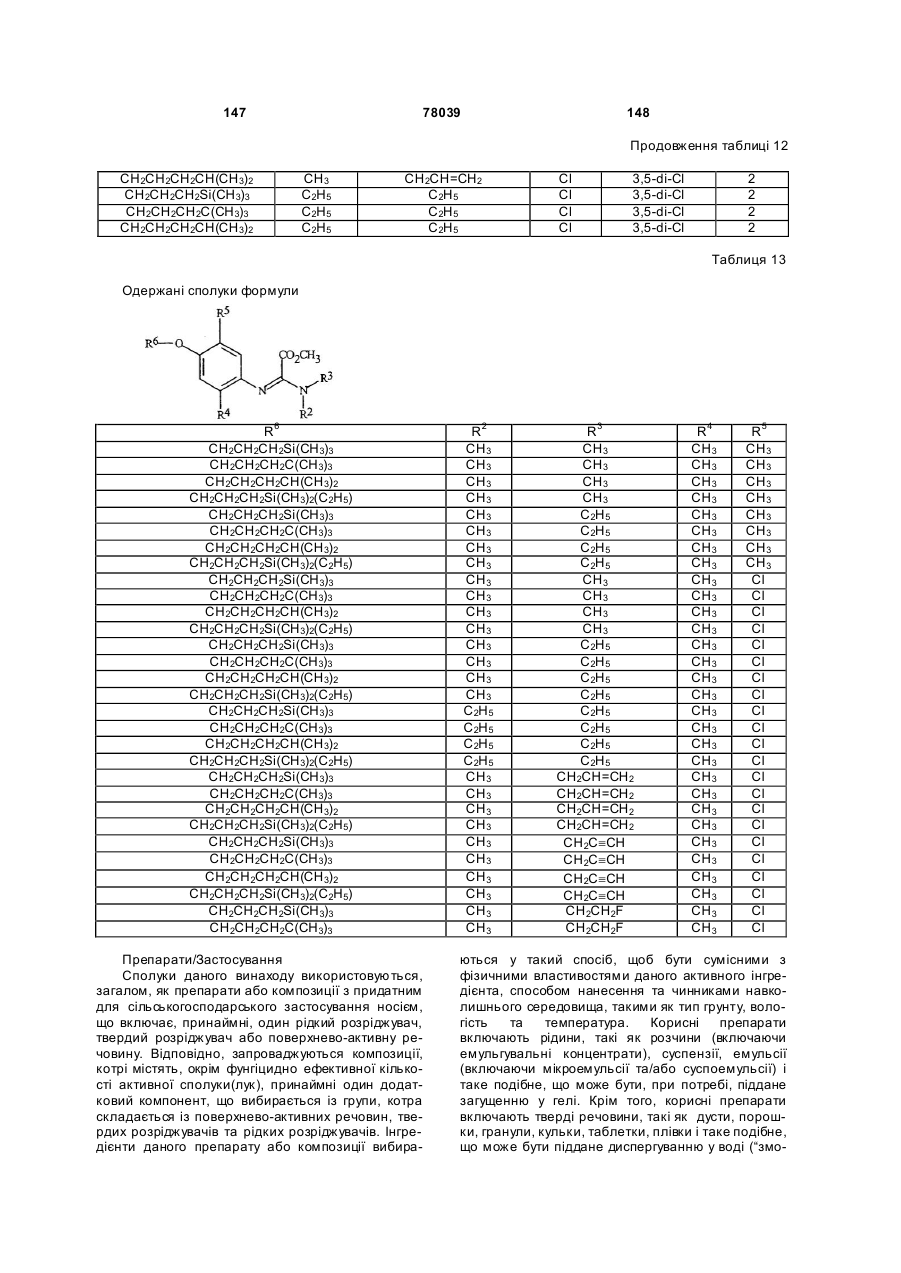
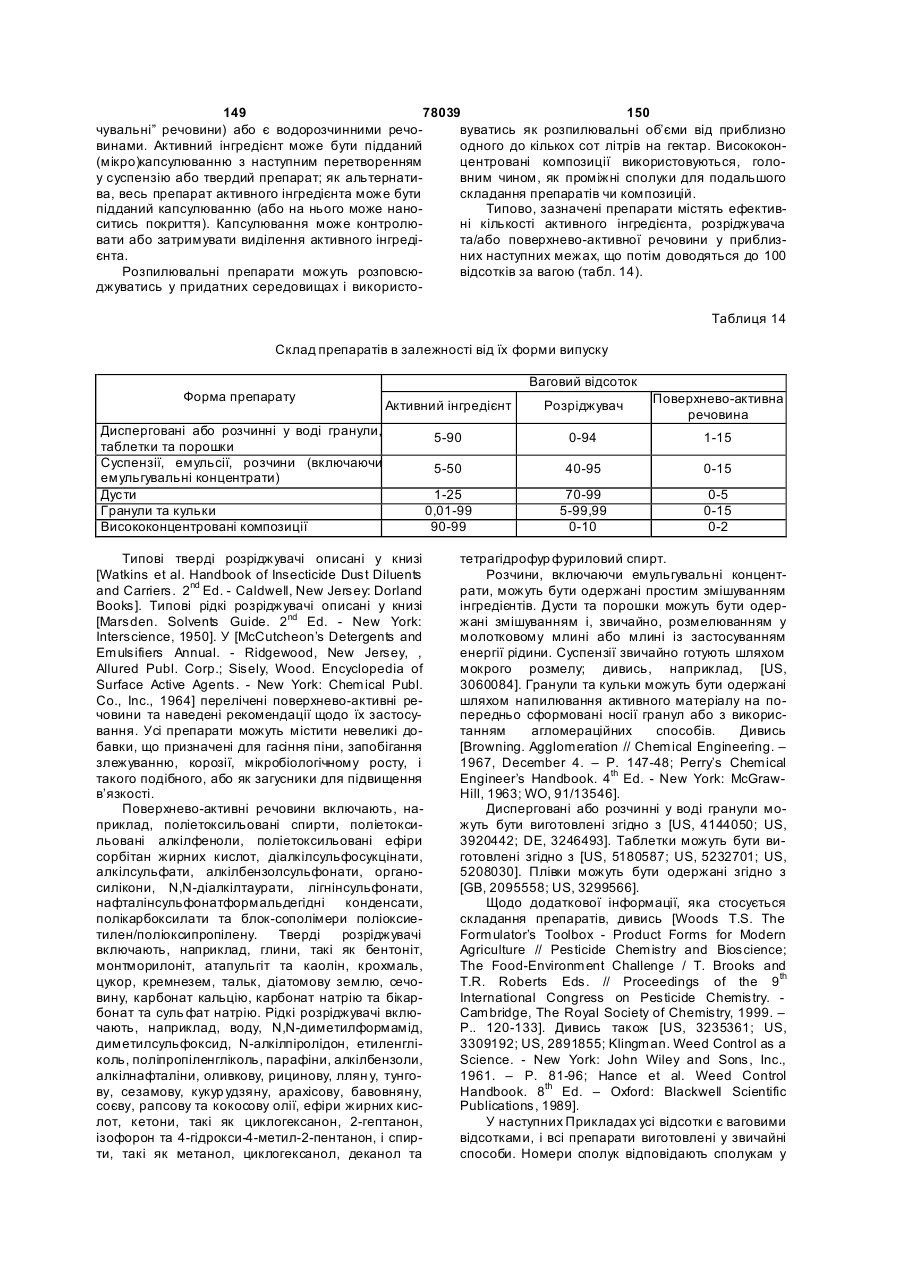
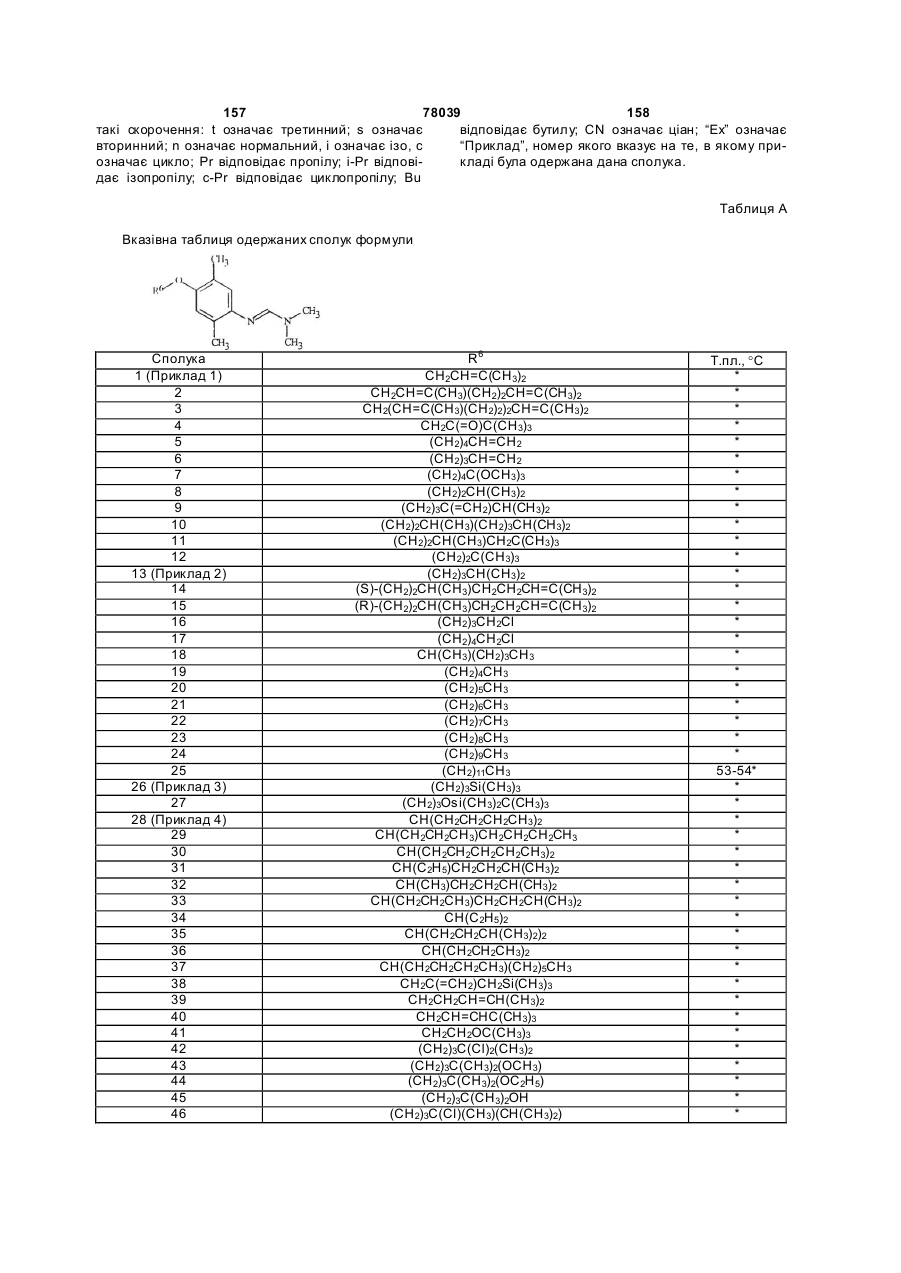
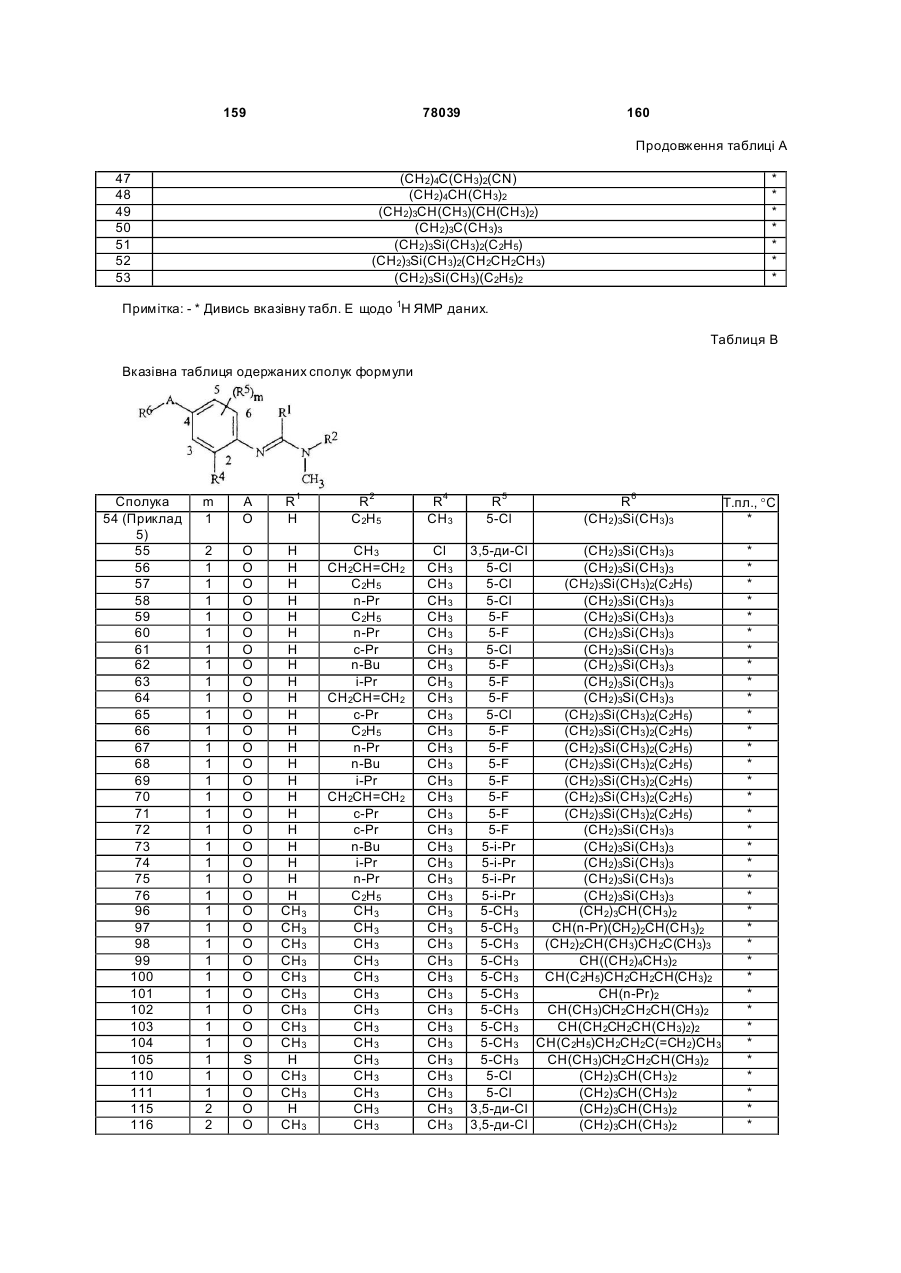
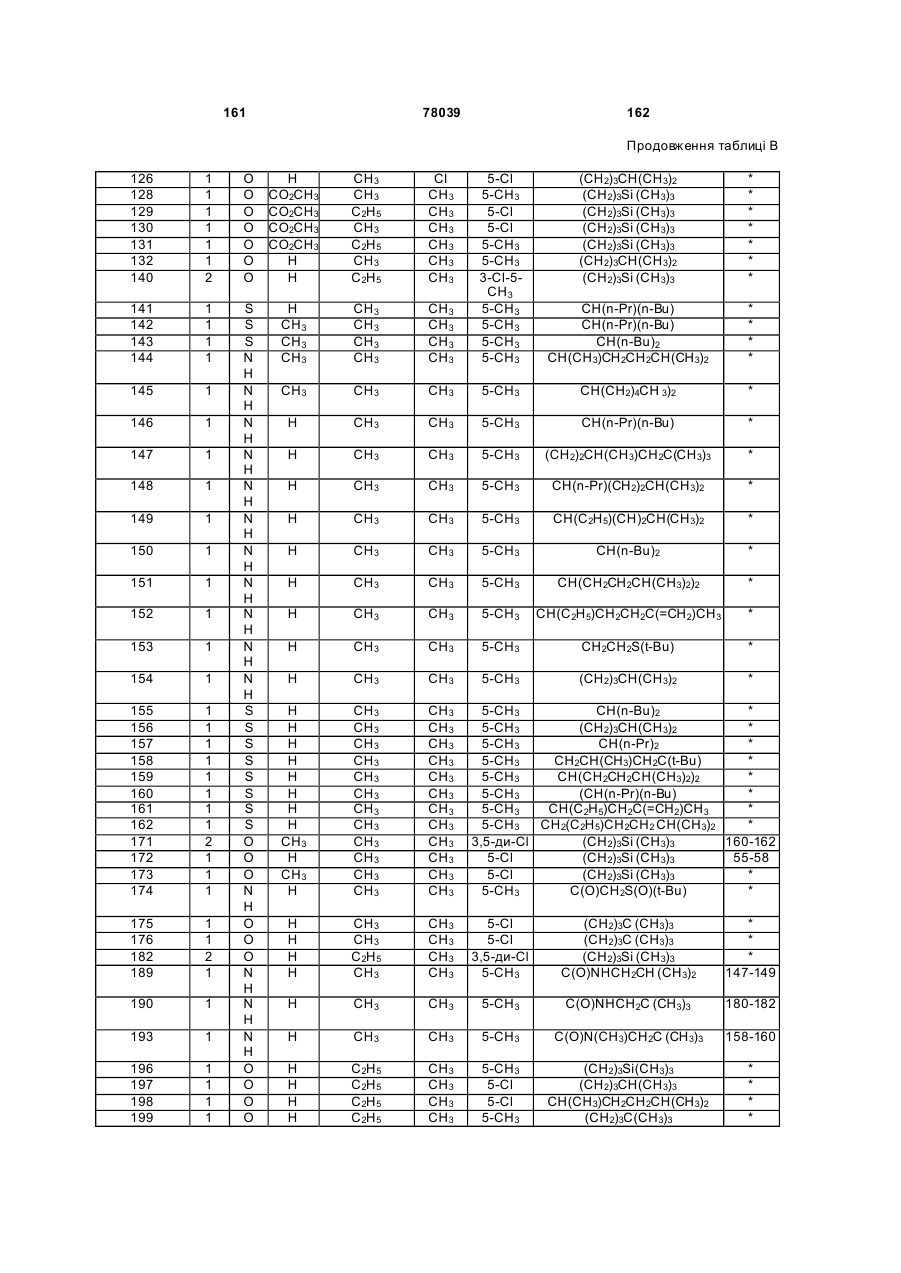
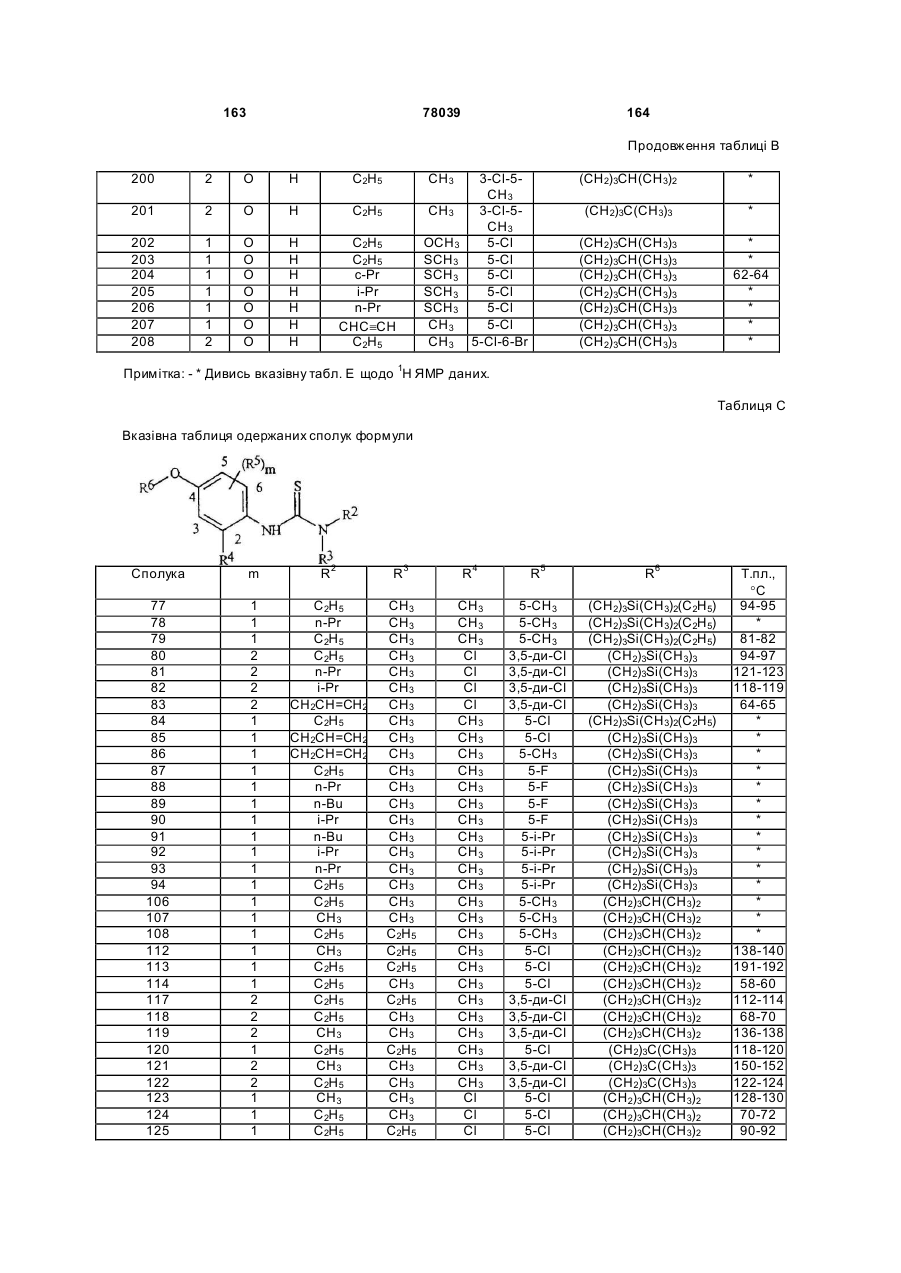
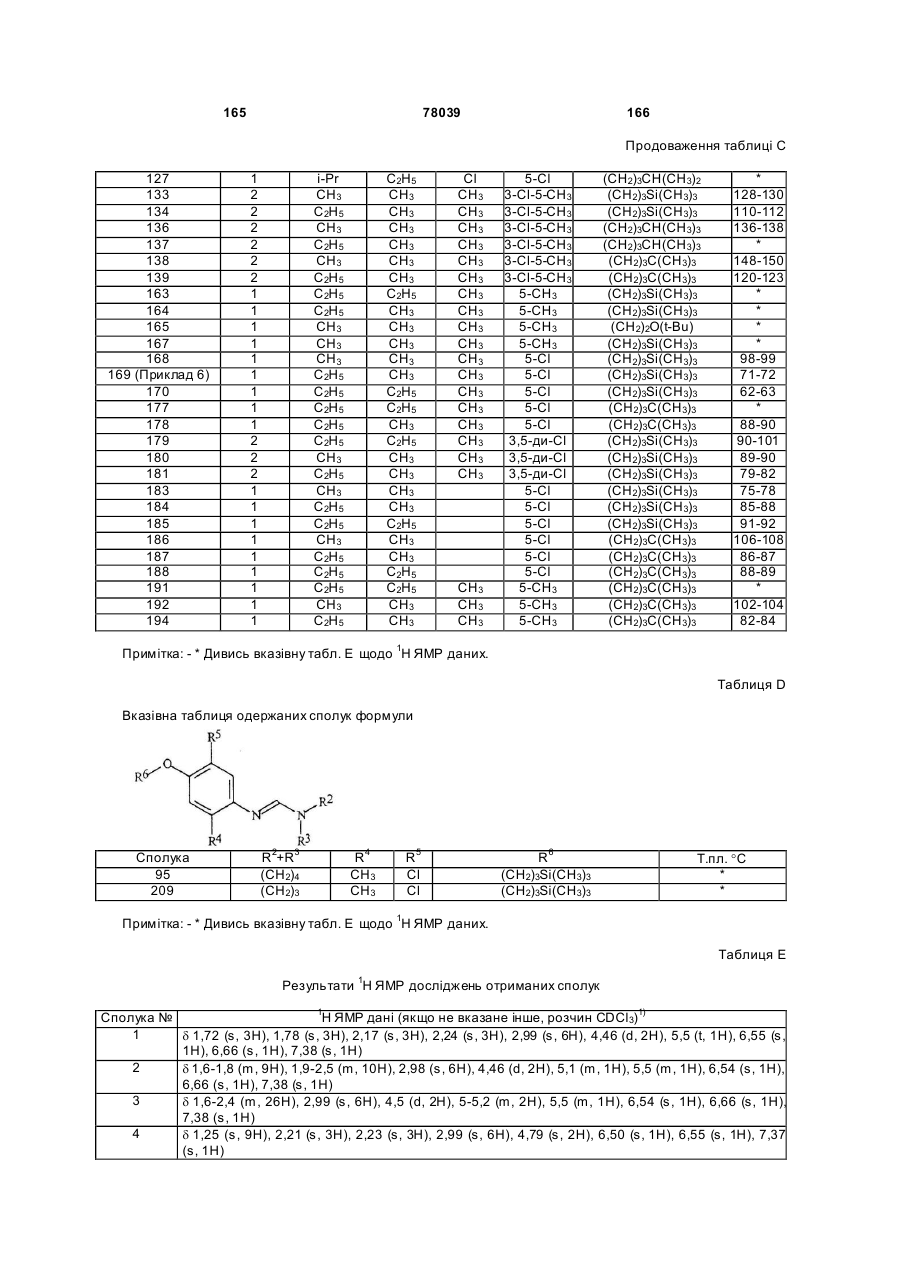
Амідинілфенілові сполуки, фунгіцидні композиції та спосіб контролю хвороб рослин
Формула / Реферат
1. Сполука формули І та або її прийнятна для сільськогосподарського застосування сіль
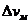 , (І)
, (І)
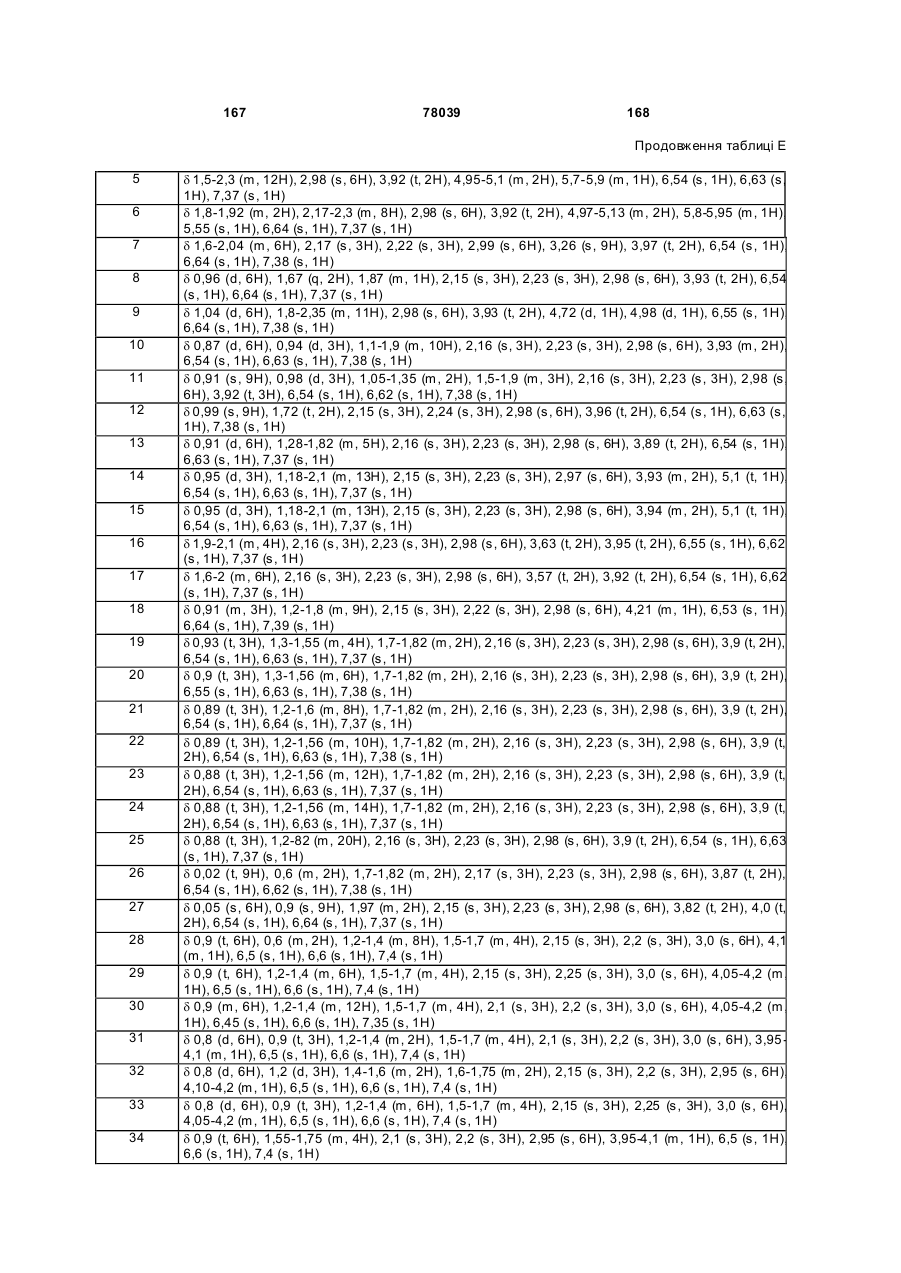
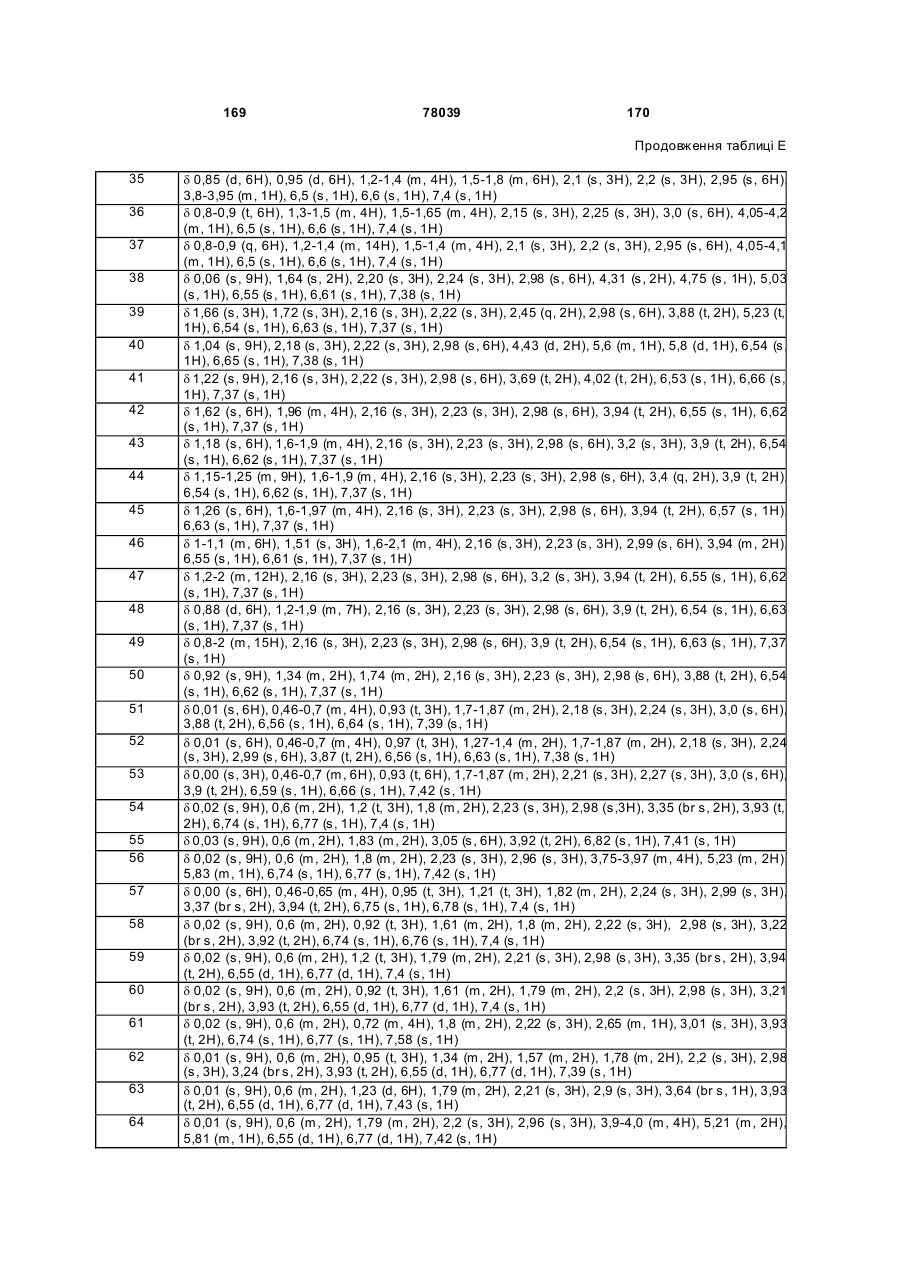
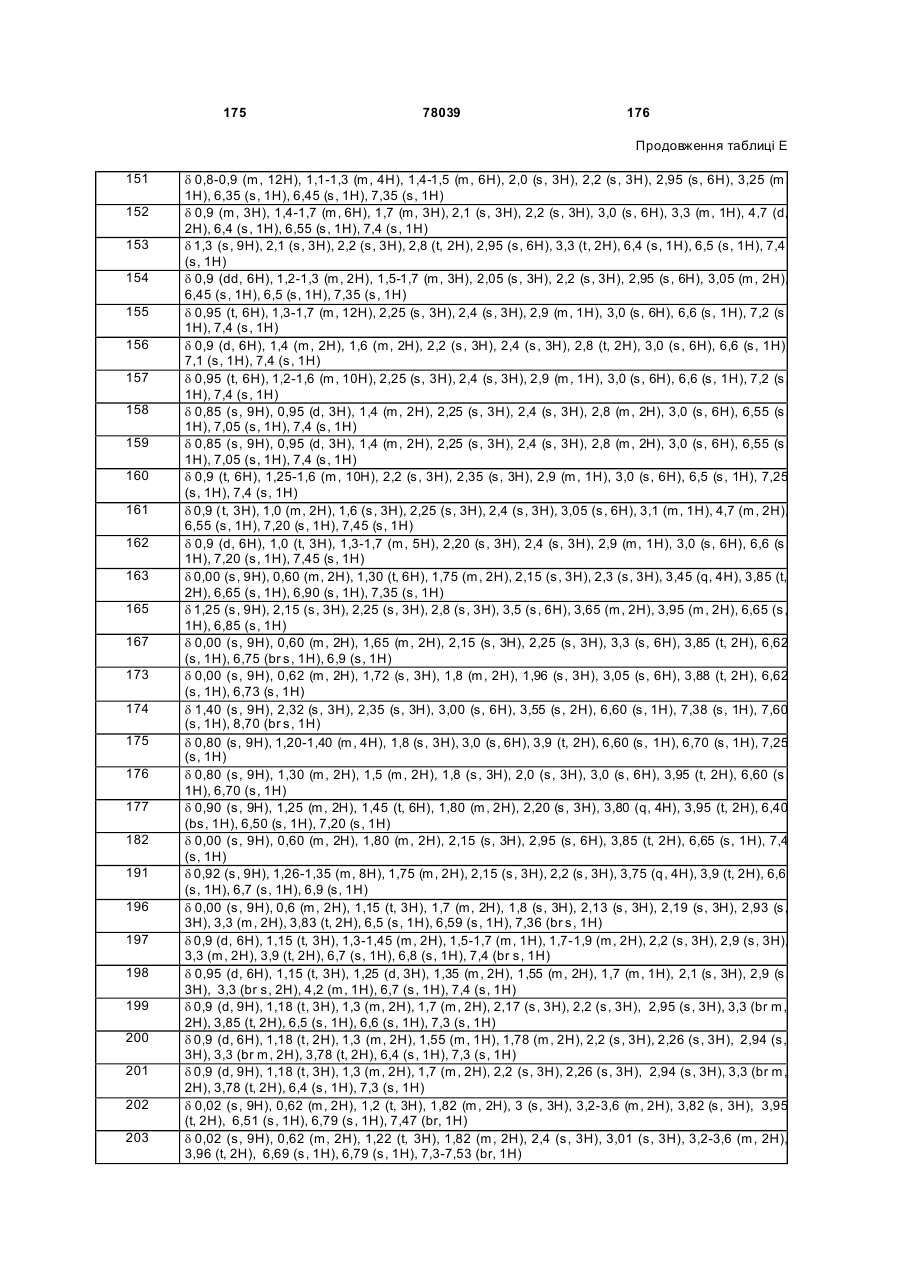
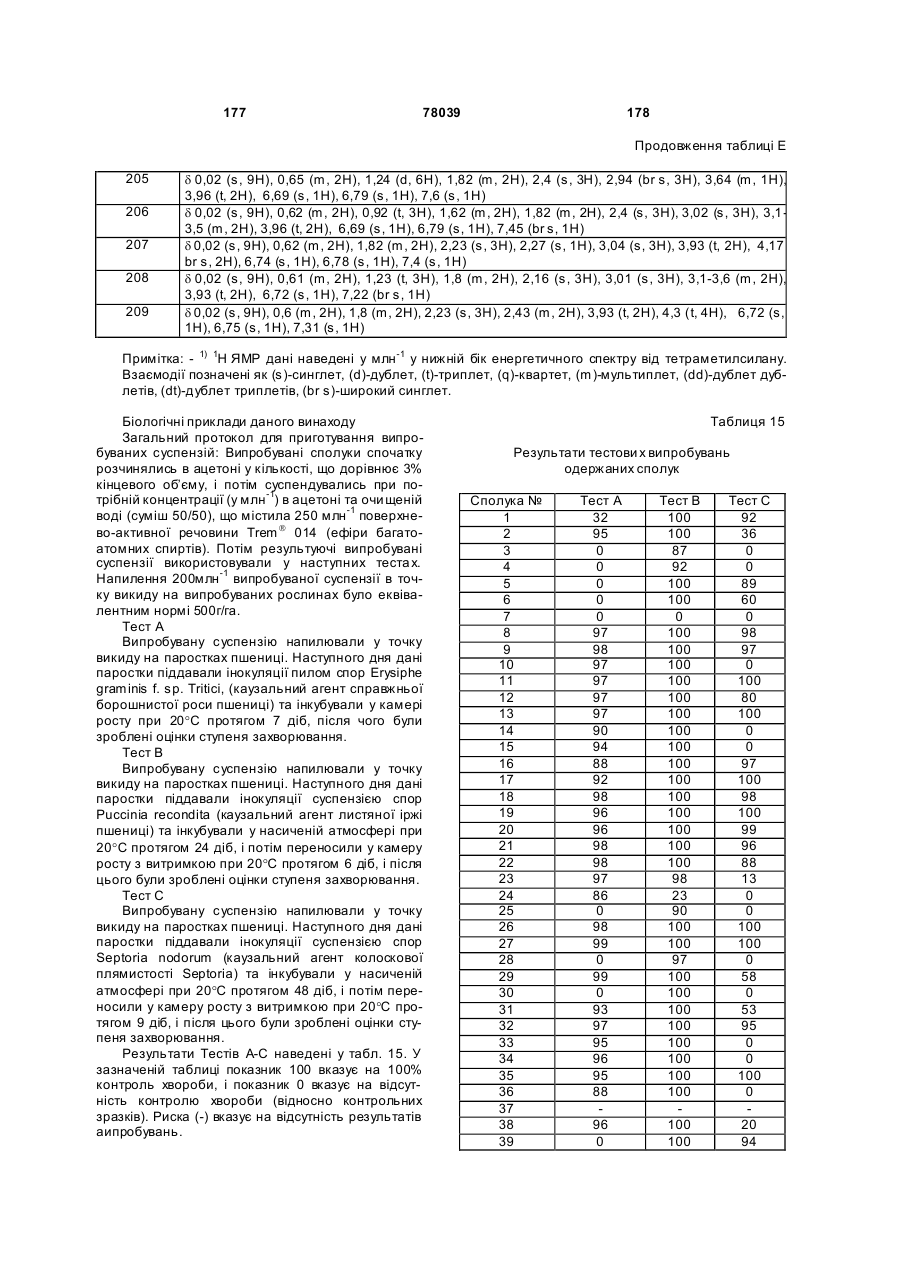
де
R1 являє собою Н, SH, метил або C2-C5 алкоксикарбоніл;
R2 являє собою С1-С10 алкіл, С2-С10 алкеніл або С2-С10 алкініл;
R3 являє собою С1-С10 алкіл; або, що їх зв'язує
R2 та R3, взяті разом з азотом, утворюють гетероциклічне кільце, що містить від 3 до 7 атомів, зазначене кільце складається із зазначеного зв'язуючого атома азоту та атомів вуглецю;
R4 та кожний з R5 кожний незалежно являє собою С1-С6 алкіл, галоген, С1-С4 алкоксигрупу або С1-С4 алкілтіогрупу;
R6 являє собою C5-C21 алкіл, С5-С21 алкеніл або С4-С6 алкіламінокарбоніл, кожний необов'язково заміщений; або R6 являє собою С1-С4 алкіл або С2-С9 алкілкарбоніл, кожний заміщений одним або декількома R12;
А являє собою О, S або NH;
кожний R12 незалежно являє собою С1-С6 алкілсульфініл, С2-С6 алкілкарбоніл, С3-С9 триалкілсиліл або С3-С9 триалкілсилілоксигрупу; та
m дорівнює 1 або 2.
2. Сполука за п. 1, яка відрізняється тим, що
R6 являє собою Н, SH або метил;
R6 являє собою C5-C21 алкіл, С5-С21 алкеніл або С4-С6 алкіламінокарбоніл, кожний необов'язково заміщений одним або декількома R11; або R6 являє собою С1-С4 алкіл або С2-С9 алкілкарбоніл, кожний заміщений одним або декількома R12; та
кожний R11 незалежно являє собою галоген, гідроксигрупу або С1-С6 алкоксигрупу.
3. Сполука, за п. 2, яка відрізняється тим, що
R6 являє собою С5-С15 алкіл або C5-C15 алкеніл, кожний необов'язково заміщений одним або декількома R11; або R6 являє собою С1-С4 алкіл, заміщений одним або декількома R12; та
А являє собою О або S.
4. Сполука за п. 3, яка відрізняється тим, що А приєднано до залишкової частини формули І у 4 положенні бензольного кільця.
5. Сполука за п. 4, яка відрізняється тим, що
кожний з R2 та R3 незалежно являє собою С1-С10 алкіл; або
R2 та R3, взяті разом з азотом, що їх зв'язує, утворюють гетероциклічне кільце, що містить від 3 до 7 атомів, зазначене кільце складається із зазначеного зв'язуючого атома азоту та атомів вуглецю;
та де один R5 приєднано до залишкової частини формули І у 5 положенні бензольного кільця, та необов'язково другий R5 приєднаний у 6 положенні бензольного кільця.
6. Сполука за п. 5, яка відрізняється тим, що
R1 являє собою Н; та
R6 являє собою С6-С15 алкіл, де принаймні один з четвертого та п'ятого атомів вуглецю з А має один або не має жодного приєднаного атома водню, або С5-С12 алкеніл, де четвертий або п'ятий атом вуглецю з А має один або не має жодного приєднаного атома водню.
7. Сполука за п. 5, яка відрізняється тим, що
R1 являє собою Н; та
R6 являє собою С1-С4 алкіл, заміщений одним або декількома R12.
8. Фунгіцидна композиція, що включає фунгіцидно ефективну кількість сполуки за п. 1 та принаймні один додатковий компонент, який вибрано з групи, що складається з поверхнево-активних речовин, твердих розріджувачів та рідких розріджувачів.
9. Фунгіцидна композиція, що включає суміш сполук за п. 1 та принаймні один інший фунгіцид, який має інакший спосіб дії.
10. Спосіб контролю хвороб рослин, що зумовлені грибковими рослинними патогенами, який включає нанесення на дану рослину або її частину, або на насіння чи розсаду фунгіцидно ефективної кількості сполуки за п. 1.
Текст
1. Сполука формули І та або її прийнятна для сільськогосподарського застосування сіль R (5) m C2 2 (19) 1 3 78039 4 або С5-С12 алкеніл, де четвертий або п'ятий атом що складається з поверхнево-активних речовин, вуглецю з А має один або не має жодного приєдтвердих розріджувачів та рідких розріджувачів. наного атома водню. 9. Фунгіцидна композиція, що включає суміш спо7. Сполука за п.5, яка відрізняється тим, що лук за п.1 та принаймні один інший фунгіцид, який R1 являє собою Н; та має інакший спосіб дії. R6 являє собою С1-С4 алкіл, заміщений одним або 10. Спосіб контролю хвороб рослин, що зумовлені декількома R12. грибковими рослинними патогенами, який включає 8. Фунгіцидна композиція, що включає фунгіцидно нанесення на дану рослину або її частин у, або на ефективну кількість сполуки за п.1 та принаймні насіння чи розсаду фунгіцидно ефективної кількоодин додатковий компонент, який вибрано з групи, сті сполуки за п.1. Даний винахід стосується деяких амідинів, їх солей, що придатні для сільськогосподарського застосування, та композицій і способів їх використання як фунгіцидів. Контроль хвороб рослин, що зумовлені грибковими рослинними патогенами, є надзвичайно важливим у плані досягнення високої ефективності врожаїв. Збитки, які завдають хвороби рослин декоративним, овочевим, польовим, злаковим та фр уктовим культурам, можуть спричинити суттєве зниження продуктивності і у такий спосіб призвести до підвищених витрат споживача. Для реалізації цих цілей щодо контролю хвороб рослин у продажу є багато продуктів. Проте існує потреба у нових сполуках, що є більш ефективними, більш дешевими, менш токсичними, більш безпечними для навколишнього середовища та/або характеризуються різнимим способами дії. У [WO, 00/46184] розкриті деякі феніламідини формули i як фунгіциди i де: A та R1- R5 є такими, як визначено у даній заявці; і R6 вляє собою заміщений, при потребі, карбоцикліл або гетероцикліл. Різні амідинілфенілові сполуки також розкриті у патента х [US, 3284289, A, 08.11.1966; US, 3993469; US, 4018814, A, 19.04.1977; US, 4154755; US, 4208411; US, 4209319; US, 5219868]. Даний винахід спрямований на сполуки формули І (включаючи усі геометричні, таутомерні та стереоізомери) та їх солі, що придатні для сільськогосподарського застосування, композиції сільськогосподарського призначення, що містять ці сполуки, та їх використання як фунгіцидів: I де: R1 являє собою H, OH, SH, SO3H, CN, -OR 7 або –SR7; C1-C10 алкіл, С2-С10 алкеніл, С2-С5 алкоксикарбоніл, С2-C10 алкініл, С3-С6 карбоцикл або 3-, 4-, 5- або 6-членний гетероцикл, кожен, при потребі, заміщений; за умови, що коли R1 являє собою гетероцикл, котрий містить азот як член кільця, він не приєднаний до залишкової частини Формули І через зазначений азотний член кільця; R2 являє собою H, CN, -OR7 або -SR7; C1-C10 алкіл, С2-С10 алкеніл, С2-C10 алкініл, С3-С6 карбоцикл, 3-, 4-, 5- або 6-членний гетероцикл, або С2С10 алкілкарбоніл, кожен, при потребі, заміщений; R3 являє собою Н; C1-C10 алкіл, С2-С10 алкеніл, С2-C10 алкініл, С3-С6 карбоцикл, 3-, 4-, 5- або 6членний гетероцикл, або С2-С10 алкілкарбоніл, кожен, при потребі, заміщений; або R3 та R3 , взяті разом з їх взаємозв’язуючим азотом, утворюють гетероциклічне кільце, що містить від 3 до 7 атомів, зазначене кільце складається із зазначеного взаємозв’язуючого атому азоту, вуглецю та, при потребі, із одного або двох додаткових атомів, котрі вибираються із групи, що складається із азоту, сірки та кисню, і зазначене кільце заміщене, при потребі, однією або більше R9; кожна із R4 та R5 являє собою, незалежно, С1С6 алкіл, С2-С6 алкеніл, С2-С6 алкініл, С3-С6 циклоалкіл, С1-С6 галоалкіл, С2-С6 галоалкеніл, С2-С6 галоалкініл, С3-С6 галоциклоалкіл, галоген, CN, CHO, CO2H, CONH2, SF5, C1-C 4 алкокси, C1-C4 галоалкокси, C1-C4 алкілтіо, C1-C4 алкілсульфініл, C1-C4 алкілсульфоніл, C1-C4 галоалкілтіо, C1-C4 галоалкілсульфініл, C1-C4 галоалкілсульфоніл, C1C4 алкіламіно, C2-C8 діалкіламіно, C3-C6 циклоалкіламіно, C2-C6 алкілкарбоніл, C2-C6 алкоксикарбоніл, C2-C6 алкіламінокарбоніл, C3-C8 діалкіламінокарбоніл або C3-C6 триалкілсиліл; R6 являє собою C5-C21 алкіл, C5-C21 алкеніл, C5-C21 алкініл, C4-C9 алкоксикарбоніл, C4-C6 алкіламінокарбоніл, C3-C10 діалкіламінокарбоніл або C3-C12 триалкілсиліл, кожна, при потребі, заміщена; або R6 являє собою C1-C4 алкіл або C2-C9 алкілкарбоніл, кожна заміщена однією або більшою кількістю R12; A являє собою прямий зв’язок, O, S(O)n або NR10; кожна R7 являє собою, незалежно, C1-C6 алкіл, C2-C6 алкеніл, C2-C6 алкініл, C3-C6 карбоцикл або 3-, 4-, 5- або 6-членний гетероцикл, кожен, при потребі, заміщений; кожна R9 являє собою, незалежно, галоген, 5 78039 6 CN, NO2, C1-C4 алкокси, C1-C4 алкіл, C1-C4 галоалподібне визначаються аналогічно до вищенаведекокси або C1-C4 алкілтіо; них прикладів. R10 являє собою Н, C1-C6 алкіл, C2-C6 алкеніл, Вираз “карбоцикл” включає вираз “ароматичC2-C6 алкініл, C1-C4 алкілсульфоніл, C1-C4 галоална карбоциклічна кільцева система”, що означає кілсульфоніл, C2-C6 алкілкарбоніл, C2-C6 алкоксицілком ароматичні карбоцикли та карбоцикли, в карбоніл, C2-C6 алкіламінокарбоніл, C3-C8 діалкіяких принаймні одне кільце поліциклічної кільцевої ламінокарбоніл або C3-C6 триалкілсиліл; системи є ароматичним (де вираз ароматичний кожна R12 являє собою, незалежно, CO2H, вказує на те, що правило Гюккеля виконується), та CONH2, NO2, C1-C6 галоалкокси, C2-C6 алкілтіо, C1вираз “неароматична карбоциклічна кільцева сисC6 алкілсульфініл, C1-C6 алкілсульфоніл, C1-C6 тема”, що відповідає цілком насиченим карбоцикгалоалкілтіо, C1-C6 галоалкілсульфініл, C1-C6 галам, так само як і частково або цілком ненасичелоалкілсульфоніл, C1-C6 алкіламіно, C2-C8 діалкіним карбоциклам, де правило Гюккеля не ламіно, C2-C6 алкілкарбоніл, C2-C6 алкоксикарбозадовольняється жодним кільцем у даній кільцевій ніл, C3-C9 алкоксиалкілкарбоніл, C2-C6 системі. “Циклоалкіл” включає, наприклад, циклоалкіламінокарбоніл, C3-C10 алкіламіноалкілкарбопропіл, циклобутил, циклопентил та циклогексил. ніл, C3-C8 діалкіламінокарбоніл, C4-C8 діалкіламіВираз “гетеро” у зв’язку з кільцями стосується ноалкілкарбоніл, C3-C9 алкілтіоалкілкарбоніл, C3кільця, в якому принаймні один кільцевий атом не C9 триалкілсиліл, C3-C9 галотриалкілсиліл, C4-C9 є вуглецем, і яке може містити від 1 до 4 гетероалкокситриалкілсиліл або C3-C9 триалкілсилілокси; атомів, що вибираються, незалежно, із групи, котn дорівнює 0, 1 або 2; і ра включає азот, кисень та сірку, за умови, що m дорівнює 0, 1, 2 або 3. кожне кільце містить не більше 4 атомів азоту, не Сполуки формули І, що проілюстровані вище, більше 2 атомів кисню та не більше 2 атомів сірки. можуть також бути описані як сполуки формули “Гетероцикл” включає вираз “ароматична гетеро(R5)m-(R6 A)-2-(R4)-1-[N=C(R 1)N(R2)(R3)]бензол, де циклічна кільцева система”, що відповідає цілком R1, R2, R3, R4, R5, R6, A, m є такими як визначено ароматичним гетероциклам та гетероциклам, в вище. яких принаймні одне кільце поліциклічної кільцевої У вищенаведеному переліку вираз “алкіл”, що системи є ароматичним (де вираз ароматичний використовується або окремо або у складних слоозначає, що правило Гюккеля виконується), та вах, таких як “алкілтіо” або “галоалкіл”, включає вираз “неароматична гетероциклічна кільцева сиспрямий або розгалужений алкіл, такий як метил, тема”, що відповідає цілком насиченим гетероцикетил, n-пропіл, і-пропіл, або різні бутилові, пентилам, так само як і частково або цілком ненасичелові або гексилові ізомери. “Алкеніл” включає пряним гетероциклам, де правило Гюккеля не мі або розгалужені алкени, такі як етеніл, 1задовольняється жодним кільцем у даній кільцевій пропеніл, 2-пропеніл, та різні бутенілові, пентенисистемі. Дані гетероциклічні кільцеві системи молові та гексенілові ізомери. “Алкеніл” також вклюжуть бути приєднані через будь-який наявний вугчає полієни, такі як 1,2-пропадієніл та 2,4лецевий або азотний атом шляхом заміни водню гексадієніл. “Алкініл” включає прямі або розгалуна зазначеному вуглецевому або азотному атомі. жені алкіни, такі як етиніл, 1-пропініл, 2-пропініл та Вираз “галоген”, що використовується або різні бутинілові, пентинілові та гексинілові ізомеокремо або у складних словах, таких як “галоалри. “Алкініл” може також включати складові, що кіл”, включає фтор, хлор, бром або йод. Крім того, містять множину потрійних зв’язків, наприклад, при використанні у таких складних слова х як “га2,5-гексадіініл. “Алкокси” включає, наприклад, мелоалкіл”, зазначений алкіл може бути частково або токси, етокси, n-пропілокси, ізопропілокси та різні цілком заміщений галогеновими атомами, які мобутокси, пентокси та гексилокси ізомери. “Алкокжуть бути однаковими або різними. Приклади “гасиалкіл” означає алкокси заміщення по алкілу. лоалкілу” включають F3C, ClCH2, CF3CH2 та Приклади “алкоксиалкілу” включають CH3OCH2, CF3CCl2. Вирази “галоалкеніл”, “галоалкініл”, “гаCH3OCH2CH2, CH3CH2OCH2, CH3CH2CH2CH2OCH2 лоалкокси”, “галоалкілтіо” і такі подібні визначата CH3CH2OCH2СН2. “Алкоксиалкокси” означає ються аналогічно до виразу “галоалкіл”. Приклади алкокси заміщення по алкокси. “Алкілтіо” включає “галоалкенілу” включають (Cl)2C=CHCH2 та розгалужені або прямі алкілтіо складові, такі як CF3CH2CH=CHCH2. Приклади “галоалкінілу” вклюметилтіо, етилтіо, та різні пропілтіо, бутилтіо, пенчають HCºCCHCl, CF3CºC, CCl3CºC та тилтіо та гексилтіо ізомери. “Алкілтіоалкіл” означає FCH2CºCCH2. Приклади “галоалкокси” включають алкілтіо заміщення по алкілу. Приклади “алкілтіоаCF3O, CCl3CH2O, HCF2CH2CH2O та CF3CH2O. Прилкілу” включають CH3SCH2, CH3SCH2CH2, клади “галоалкілтіо” включають CCl3S, CF3S, CH3CH2SCH2, CH3CH2CH2CH2SCH2 та CCl3CH2S та ClCH2CH2CH2S. Приклади “галоалкілCH3CH2SCH2СН2. “Алкілтіоалкокси” означає алкілсульфінілу” включають CF3S(O), CCl3S(O), тіо заміщення по алкокси. “Алкілсульфініл” вклюCF3CH2S(O) та CF3CF 2S(O). Приклади “галоалкілчає обидва енантіомери алкілсульфінільної групи. сульфонілу” включають CF3S(O)2, CCl3S(O)2, Приклади “алкілсульфінілу” включають CH3S(O), CF3CH2S(O)2 та CF3CF 2S(O) 2. CH3CH2S(O), CH3CH2CH2S(O), (CH3)2CHS(O) та Вираз “триалкілсиліл” включає 3-ланцюгові різні бутилсульфінілові, пентилсульфінілові та розгалужені та/або прямі алкіл-радикали, що пригексилсульфінілові ізомери. Приклади “алкілсульєднані та зв’язані через атом кремнію, такі як трифонілу” включають CH3S(O)2, CH3CH2S(O)2, метилсиліл, триетилсиліл та t-бутил-диметилсиліл. CH3CH2CH2S(O)2, (CH3)2CHS(O)2 та різні бутилсу“Галотриалкілсиліл” означає, що принаймні один із льфонілові, пентилсульфонілові та гексилсульфотрьох алкіл-радикалів частково або цілком замінілові ізомери. “Алкіламіно”, “діалкіламіно” і таке щений галогеновими атомами, які можуть бути 7 78039 8 однаковими або різними. “Алкокситриалкілсиліл” хівцеві у даній галузі зрозуміло, що один стереоозначає, що принаймні один із трьох алкілізомер може бути більш активним та/або може радикалів заміщений одним або більшою кількістю виявляти сприятливі ефекти при збагаченні ним алкокси радикалів, які можуть бути однаковими даної сполуки, відносно іншого стереоізомеру(ів), або різними. “Триалкілсилілокси” означає триалкіабо при його відокремленні від іншого стереоізолсилілову складову, що приєднана через кисень. меру(ів). Крім того, фахівцеві у даній галузі відомо, Приклади “алкілкарбонілу” включають як проводити розділення, збагачення та/або селеC(O)CH3, C(O)CH2CH2CH3 та С(О)СН(СН 3)2. Приктивне одержання зазначених стереоізомерів. Відклади “алкоксикарбонілу” включають СН 3ОС(=О), повідно, даний винахід включає сполуки, що вибСН3CH2ОС(=О), CH 3CH2CH2ОС(=О), рані із формули І, їх N-оксиди та придатні для (CH3)2CHОС(=О) та різні бутокси- або пентоксикасільськогосподарського застосування солі. Сполурбонільні ізомери. Приклади “алкіламінокарбонілу” ки даного винаходу можуть бути присутні як суміш включають CH3NHC(=O), CH 3CH2NHC(=O), стереоізомерів, окремі стереоізомери або як оптиCH3CH2CH2NHC(=O), (CH 3)2CHNHC(=O) та різні чно активна форма. бутиламіно- або пентиламінокарбонільні ізомери. Фахівцеві у даній галузі зрозуміло, що не всі Приклади “діалкіламінокарбонілу” включають гетероцикли, які містять азот, можуть утворювати (CH3)2NC(=O), (CH 3CH2)2NC(=O), N-оксиди, оскільки даний атом азоту потребує наCH3CH2(CH3)2NC(=O), CH3CH2CH2(CH3)2NC(=O) та явності окремої пари для окиснення до даного (CH3)2СНN(СН3)С(=O). Приклади “алкоксиалкілкаоксиду; фа хівець зможе розпізнати ті гетероцикли, рбонілу” включають СН 3ОСН2С(=О), що містять азот, які здатні утворювати N-оксиди. СН3ОСН2СН2С(=О), СН3СН2ОСН2С(=О), Крім того, фахівець у даній галузі розпізнає й ті СН3СН2СН2СН2ОСН2С(=О) та третинні аміни, що здатні утворити N-оксиди. СинСН3СН2ОСН2СН2С(=О). Приклади “алкілтіоалкілтетичні методи одержання N-оксидів гетероциклів карбонілу” включають CH3SCH2C(=O), та третинних амінів дуже добре відомі фахівцям у CH3SCH2CH2C(=O), CH 3CH2SCH2C(=O), даній галузі, включаючи окиснення гетероциклів та CH3CH2CH2CH2SCH2C(=O) та третинних амінів пероксикислотами, такими як СН3СН2SCH2CH2C(=O). Приклади “алкіламіноалкіпероцтова та m-хлоропербензойна кислота лкарбонілу” включають CH3NHCH2C(=O), (МСРВА), пероксидом водню, алкілгідропероксиCH3NHCH2CH2C(=O), CH 3CH2NHCH2C(=O), дами, такими як t-бутилгідропероксид, перборатом CH3CH2CH2CH2NHCH2C(=O) та натрію та діоксиранами, такими як диметилдіоксиCH3CH2NHCH2CH2C(=O). ран. Ці методи одержання N-оксидів детально Загальна кількість вуглецевих а томів у групі описані та оглянуті у літературі, дивись наприклад, замісника позначається префіксом “Ci-Cj”, де i та j [T.L. Gilchrist in Comprehensive Organic Synthesis, є числами від 1 до 21. Наприклад, С1-С3 алкілсуvol. 7, pp 748-750, S.V. Le y, Ed., Pergamon Press; льфоніл визначає групи від метилсульфонілу до M. Tisler and B. Stanovnik in Comprehensive Heteroпропілсульфонілу; С2 алкоксиалкіл визначає cyclic Chemistry, vol.3, pp 18-20, A.J. Boulton and A. СН3ОСН2; С3 алкоксиалкіл визначає, наприклад, McKillop, Eds., Pergamon Press; M.R. Grimmett and СН3СН(ОСН3), СН3ОСН2СН2 або СН 3СН2ОСН2; і С4 B.R.T. Keene in Advances in Heterocyclic Chemistry, алкоксиалкіл визначає різні ізомери алкільної груvol. 43, pp 149-161, A.R. Katritzky, Ed., Academic пи, заміщеної алкокси групою, що містить, загаPress; M. Tisler and B. Stanovnik in Advances in лом, чотири вуглецевих атоми, приклади включаHeterocyclic Chemistry, vol. 9, pp 285-291, A.R. ють СН 3СН2СН2ОСН2 та СН3СН2ОСН2СН2. У Katritzky and A.J. Boulton, Eds., Academic Press; вищезазначених переліках, коли сполука формулиand G.W.H. Cheeseman and E.S.G. Werstuik in AdІ складається із одного або більшої кількості гетеvances in Heterocyclic Chemistry, vol. 22, pp 390роциклічних кілець, усі замісники приєднані до цих 392, A.R. Katritzky and A.J. Boulton, Eds., Academic кілець через будь-який наявний вуглецевий або Press]. азотний атом шляхом заміни водню на зазначеноСолі сполук даного винаходу включають кислі му вуглецевому чи азотному атомі. солі приєднання з неорганічними або органічними Коли сполука заміщена замісником, котрий некислотами, такими як бромистоводнева, хлористосе підрядковий індекс, який вказує, що кількість воднева, азотна, фосфорна, сірчана, оцтова, масзазначених замісників може перевищувати 1, заляна, фумарова, молочна, малеїнова, малонова, значені замісники (коли їх кількість перевищує 1) щавлева, пропіонова, саліцилова, винна, 4вибираються, незалежно, із групи визначених затолуолсульфонова або валеріанова кислоти. Солі місників. Крім того, коли даний підрядковий індекс сполук даного винаходу також включають солі, що вказує на область, наприклад, (R)i-j, тоді кількість утворені з органічними основами (наприклад, пізамісників може вибиратись із цілих чисел від i до j ридин, амоній або триетиламін) або неорганічними включно. основами (наприклад, гідриди, гідроксиди або карКоли група містить замісник, що може бути вобонати натрію, калію, літію, кальцію, магнію або днем, наприклад, R1 або R2, і тоді, коли цим замісбарію), коли дана сполука містить кислотну групу, ником вибирають водень, вважається, що це еквітаку як карбонова кислота або фенол. валентно тому, що зазначена група не є Заслуговують на ува гу сполуки формули І, заміщеною. де: Сполуки даного винаходу можуть існувати як R1 являє собою Н, ОН, SH, SO3H, CN, -OR 7 один або більша кількість стереоізомерів. Різні або -SR7; C1-C10 алкіл, C2-C10 алкеніл, C2-C10 алкістереоізомери включають енантіомери, діастереніл, C3-C6 карбоцикл або 3-, 4-, 5- або 6-членний омери, атропоізомери та геометричні ізомери. Фагетероцикл, кожен, при потребі, заміщений; за 9 78039 10 умови, що коли R1 являє собою гетероцикл, котрий C3-C12 триалкілсиліл, кожна, при потребі, заміщена містить азот як член кільця, він не приєднаний до однією або більшою кількістю R11; або R6 являє залишкової частини Формули І через зазначений собою C1-C4 алкіл або C2-C9 алкілкарбоніл, кожна азотний член кільця; заміщена однією або більшою кількістю R12; кожна із R4 та R5 являє собою, незалежно, С1кожна R7 являє собою, незалежно, C1-C6 алкіл, С6 алкіл, С2-С6 алкеніл, С2-С6 алкініл, С3-С6 циклоC2-C6 алкеніл, C2-C6 алкініл, кожна, при потребі, алкіл, С1-С6 галоалкіл, С2-С6 галоалкеніл, С2-С6 заміщена однією або більшою кількістю R8; або галоалкініл, С3-С6 галоциклоалкіл, галоген, CO2H, C3-C6 карбоцикл чи 3-, 4-, 5- або 6-членний гетеCONH2, SF5, C1-C4 алкокси, C1-C4 галоалкокси, C1роцикл, кожен, при потребі, заміщений однією або C4 алкілтіо, C1-C4 алкілсульфініл, C1-C4 алкілсульбільшою кількістю R9; фоніл, C1-C4 галоалкілтіо, C1-C4 галоалкілсульфікожна R8 являє собою, незалежно, галоген, ніл, C1-C4 галоалкілсульфоніл, C1-C4 алкіламіно, CN, NO2, С1-С4 алкокси, С1-C4 галоалкокси або С 1C2-C8 діалкіламіно, C3-C6 циклоалкіламіно, C2-C6 С4 алкілтіо; і алкілкарбоніл, C2-C6 алкоксикарбоніл, C2-C6 алкікожна R11 являє собою, незалежно, галоген, ламінокарбоніл, C3-C8 діалкіламінокарбоніл або CO2H, CONH2, NO2, гідрокси, C1-C6 алкокси, C1-C6 C3-C6 триалкілсиліл; і галоалкокси, C2-C6 алкілтіо, C1-C6 алкілсульфініл, кожна R12 являє собою, незалежно, CO2H, C1-C6 алкілсульфоніл, C1-C6 галоалкілтіо, C1-C6 CONH2, NO2, C1-C6 галоалкокси, C2-C6 алкілтіо, C1галоалкілсульфініл, C1-C6 галоалкілсульфоніл, C1C6 алкілсульфініл, C1-C6 алкілсульфоніл, C1-C6 C6 алкіламіно, C2-C8 діалкіламіно, C2-C6 алкілкаргалоалкілтіо, C1-C6 галоалкілсульфініл, C1-C6 габоніл, C2-C6 алкоксикарбоніл, C3-C9 алкоксиалкіллоалкілсульфоніл, C1-C6 алкіламіно, C2-C8 діалкікарбоніл, C2-C6 алкіламінокарбоніл, C4-C10 алкілаламіно, C2-C6 алкілкарбоніл, C2-C6 алкоксикарбоміноалкілкарбоніл, C3-C8 діалкіламінокарбоніл, C4ніл, C3-C9 алкоксиалкілкарбоніл, C2-C6 C8 діалкіламіноалкілкарбоніл, C3-C9 алкілтіоалкілалкіламінокарбоніл, C4-C10 алкіламіноалкілкарбокарбоніл, С2-С8 діалкілфосфорил, С2-С8 діалкілніл, C3-C8 діалкіламінокарбоніл, C3-C8 діалкіламіфосфініл, C3-C9 триалкілсиліл або C3-C9 триалкілноалкілкарбоніл, C3-C9 алкілтіоалкілкарбоніл, C3силілокси. C9 триалкілсиліл або C3-C9 триалкілсилілокси. Заслуговують на увагу сполуки із розділу Сполуки, яким віддається перевага, виходячи “Сполуки, яким віддається перевага, 1”, із їх вартості, легкості синтезу та/або біологічної де: ефективності, є наступними: R2 являє собою H, CN, -OR7 або -SR7; C1-C10 “Сполуки, яким віддається перевага, 1” алкіл, С2-С10 алкеніл, С2-C10 алкініл або С2-С10 алСполуки вищенаведеної Формули І та їх солі, кілкарбоніл, кожен, при потребі, заміщений однією що придатні для сільськогосподарського застосуабо більшою кількістю R8; або С3-С6 карбоцикл чи вання, 3-, 4-, 5- або 6-членний гетероцикл, кожен, при де: потребі, заміщений однією або більшою кількістю R1 являє собою H, SH, SO3H, CN, -OR 7 або R9; 7 SR ; C1-C10 алкіл, С2-С10 алкеніл або С2-C10 алкініл, R3 являє собою Н; C1-C10 алкіл, С2-С10 алкеніл, кожен, при потребі, заміщений однією або більС2-C10 алкініл або С2-С10 алкілкарбоніл, кожен, при шою кількістю R8; або С3-С6 карбоцикл чи 3-, 4-, 5потребі, заміщений однією або більшою кількістю або 6-членний гетероцикл, кожен, при потребі, R8; або С3-С6 карбоцикл чи 3-, 4-, 5- або 6-членний заміщений однією або більшою кількістю R9; гетероцикл, кожен, при потребі, заміщений однією R2 являє собою H, CN, -OR7 або -SR7; C1-C10 або більшою кількістю R9; алкіл, С2-С10 алкеніл, С2-C10 алкініл або С2-С10 алкожна із R4 та R5 являє собою, незалежно, С1кілкарбоніл, кожен, при потребі, заміщений однією С6 алкіл, С2-С6 алкеніл, С2-С6 алкініл, С3-С6 циклоабо більшою кількістю R8; або С3-С6 карбоцикл чи алкіл, С1-С6 галоалкіл, С2-С6 галоалкеніл, С2-С6 3-, 4-, 5- або 6-членний гетероцикл, кожен, при галоалкініл, С3-С6 галоциклоалкіл, галоген, CO2H, потребі, заміщений однією або більшою кількістю CONH2, SF5, C1-C4 алкокси, C1-C4 галоалкокси, C1R9; C4 алкілтіо, C1-C4 алкілсульфініл, C1-C4 алкілсульR3 являє собою Н; C1-C10 алкіл, С2-С10 алкеніл, фоніл, C1-C4 галоалкілтіо, C1-C4 галоалкілсульфіС2-C10 алкініл або С2-С10 алкілкарбоніл, кожен, при ніл, C1-C4 галоалкілсульфоніл, C1-C4 алкіламіно, потребі, заміщений однією або більшою кількістю C2-C8 діалкіламіно, C3-C6 циклоалкіламіно, C2-C6 R8; або С3-С6 карбоцикл чи 3-, 4-, 5- або 6-членний алкілкарбоніл, C2-C6 алкоксикарбоніл, C2-C6 алкігетероцикл, кожен, при потребі, заміщений однією ламінокарбоніл, C3-C8 діалкіламінокарбоніл або або більшою кількістю R9; або C3-C6 триалкілсиліл; та R2 та R3 , взяті разом з їх взаємозв’язуючим кожна R12 являє собою, незалежно, CO2H, азотом, утворюють гетероциклічне кільце, що місCONH2, NO2, C1-C6 галоалкокси, C2-C6 алкілтіо, C1тить від 3 до 6 атомів, зазначене кільце складаC6 алкілсульфініл, C1-C6 алкілсульфоніл, C1-C6 ється із зазначеного взаємозв’язуючого атому азогалоалкілтіо, C1-C6 галоалкілсульфініл, C1-C6 гату, вуглецю та, при потребі, із одного або двох лоалкілсульфоніл, C1-C6 алкіламіно, C2-C8 діалкідодаткових атомів, котрі вибираються із групи, що ламіно, C2-C6 алкілкарбоніл, C2-C6 алкоксикарбоскладається із азоту, сірки та кисню, і зазначене ніл, C3-C9 алкоксиалкілкарбоніл, C2-C6 кільце заміщене, при потребі, однією або більше алкіламінокарбоніл, C4-C10 алкіламіноалкілкарбоR9; ніл, C3-C8 діалкіламінокарбоніл, C3-C8 діалкіламіR6 являє собою C5-C21 алкіл, C5-C21 алкеніл, ноалкілкарбоніл, C3-C9 алкілтіоалкілкарбоніл, C3C5-C21 алкініл, C4-C9 алкоксикарбоніл, C4-C6 алкіC9 триалкілсиліл або C3-C9 триалкілсилілокси. ламінокарбоніл, C3-C10 діалкіламінокарбоніл або “Сполуки, яким віддається перевага, 2” 11 78039 12 Сполуки із розділу “Сполуки, яким віддається лоалкілсульфоніл, C1-C6 алкіламіно, C2-C8 діалкіперевага, 1”, де ламіно, C2-C6 алкілкарбоніл, C2-C6 алкоксикарбоR2 являє собою H, CN, -OR7 або -SR7; C1-C10 ніл, C3-C9 алкоксиалкілкарбоніл, C2-C6 алкіл, С2-С10 алкеніл, С2-C10 алкініл, кожен, при алкіламінокарбоніл, C4-C10 алкіламіноалкілкарбопотребі, заміщений однією або більшою кількістю ніл, C3-C8 діалкіламінокарбоніл, C3-C8 діалкіламіR8; або феніл, заміщений, при потребі, 1-3 R 9; ноалкілкарбоніл, C3-C9 алкілтіоалкілкарбоніл, C3R3 являє собою Н; C1-C10 алкіл, С2-С10 алкеніл C9 триалкілсиліл або C3-C9 триалкілсилілокси. або С2-C10 алкініл, кожен, при потребі, заміщений “Сполуки, яким віддається перевага, 3” однією або більшою кількістю R8; або феніл, заміСполуки із розділу “Сполуки, яким віддається щений, при потребі, 1-3 R 9; або перевага, 2”, де: R2 та R3 , взяті разом з їх взаємозв’язуючим А приєднана до залишкової частини формули І азотом, утворюють гетероциклічне кільце, що місу 4 положенні даного бензольного кільця. тить від 3 до 6 атомів, зазначене кільце склада“Сполуки, яким віддається перевага, 3а” ється із зазначеного взаємозв’язуючого атому азоСполуки із розділу “Сполуки, яким віддається ту, вуглецю та, при потребі, із одного або двох перевага, 3”, де: додаткових атомів, котрі вибираються із групи, що R1 являє собою H, SH або С 1-С10 алкіл. складається із азоту, сірки та кисню, і зазначене Заслуговують на увагу сполуки із розділу кільце заміщене, при потребі, однією або більше “Сполуки, яким віддається перевага, 3”, де: R9; кожна із R1 та R2 являє собою, незалежно, H, 4 5 кожна із R та R являє собою, незалежно, С1CN, -OR 7 або -SR7; C1-C10 алкіл, С2-С10 алкеніл, С2С6 алкіл, С2-С6 алкеніл, С2-С6 алкініл, С1-С6 галоаC10 алкініл, кожен, при потребі, заміщений однією лкіл, галоген, CO2H, CONH2, С1-C4 алкокси, C1-C4 або більшою кількістю R8; або феніл, заміщений, галоалкокси, C1-C4 алкілтіо, C1-C4 алкілсульфініл, при потребі, 1-3 R9; C1-C4 алкілсульфоніл, C1-C4 галоалкілтіо, C1-C4 R3 являє собою Н; C1-C10 алкіл, С2-С10 алкеніл галоалкілсульфініл, C1-C4 галоалкілсульфоніл, C1або С2-C10 алкініл, кожен, при потребі, заміщений C6 алкілкарбоніл, C2-C6 алкоксикарбоніл, C2-C6 однією або більшою кількістю R8; або феніл, заміалкіламінокарбоніл, CN, CHO або C3-C8 діалкілащений, при потребі, 1-3 R 9; мінокарбоніл; кожна із R4 та R5 являє собою, незалежно, С1R6 являє собою C5-C15 алкіл, C5-C15 алкеніл С6 алкіл, С2-С6 алкеніл, С2-С6 алкініл, С1-С6 галоаабо C5-C15 алкініл, кожен, при потребі, заміщений лкіл, галоген, CO2H, CONH2, С1-C4 алкокси, C1-C4 однією або більшою кількістю R11; або R6 являє галоалкокси, C1-C4 алкілтіо, C1-C4 алкілсульфініл, собою C1-C4 алкіл, заміщений однією або більшою C1-C4 алкілсульфоніл, C1-C4 галоалкілтіо, C1-C4 кількістю R12; галоалкілсульфініл, C1-C4 галоалкілсульфоніл, C1кожна R7 являє собою, незалежно, C1-C6 алкіл, C6 алкілкарбоніл, C1-C6 алкоксикарбоніл, C1-C6 заміщений, при потребі, однією або більшою кільалкіламінокарбоніл або C2-C8 діалкіламінокарбокістю R8; ніл; і А являє собою прямий зв’язок, О або S(O)n; і кожна R12 являє собою, незалежно, CO2H, m дорівнює 0, 1 або 2. CONH2, NO2, C1-C6 галоалкокси, C2-C6 алкілтіо, C1“Сполуки, яким віддається перевага, 2а” C6 алкілсульфініл, C1-C6 алкілсульфоніл, C1-C6 Сполуки із розділу “Сполуки, яким віддається галоалкілтіо, C1-C6 галоалкілсульфініл, C1-C6 гаперевага, 2”, де: лоалкілсульфоніл, C1-C6 алкіламіно, C2-C8 діалкіR1 являє собою H, SH або С 1-С10 алкіл. ламіно, C2-C6 алкілкарбоніл, C2-C6 алкоксикарбоЗаслуговують на увагу сполуки із розділу ніл, C3-C9 алкоксиалкілкарбоніл, C2-C6 “Сполуки, яким віддається перевага, 2”, де алкіламінокарбоніл, C4-C10 алкіламіноалкілкарбокожна із R1 та R2 являє собою, незалежно, H, ніл, C3-C8 діалкіламінокарбоніл, C3-C8 діалкіламіCN, -OR 7 або -SR7; C1-C10 алкіл, С2-С10 алкеніл, С2ноалкілкарбоніл, C3-C9 алкілтіоалкілкарбоніл, C3C10 алкініл, кожен, при потребі, заміщений однією C9 триалкілсиліл або C3-C9 триалкілсилілокси. або більшою кількістю R8; або феніл, заміщений, “Сполуки, яким віддається перевага, 4” при потребі, 1-3 R9; Сполуки із розділу “Сполуки, яким віддається R3 являє собою Н; C1-C10 алкіл, С2-С10 алкеніл перевага, 3”, де: або С2-C10 алкініл, кожен, при потребі, заміщений R1 являє собою H, SH або С 1-С10 алкіл; 8 однією або більшою кількістю R ; або феніл, замікожна із R2 та R3 являє собою, незалежно, Н щений, при потребі, 1-3 R 9; або С1-С10 алкіл; або кожна із R4 та R5 являє собою, незалежно, С1R2 та R3 , взяті разом з їх взаємозв’язуючим С6 алкіл, С2-С6 алкеніл, С2-С6 алкініл, С1-С6 галоаазотом, утворюють гетероциклічне кільце, що міслкіл, галоген, CO2H, CONH2, С1-C4 алкокси, C1-C4 тить від 3 до 6 атомів, зазначене кільце складагалоалкокси, C1-C4 алкілтіо, C1-C4 алкілсульфініл, ється із зазначеного взаємозв’язуючого атому азоC1-C4 алкілсульфоніл, C1-C4 галоалкілтіо, C1-C4 ту, вуглецю та, при потребі, із одного додаткового галоалкілсульфініл, C1-C4 галоалкілсульфоніл, C1атому, котрий вибирається із групи, що складаєтьC6 алкілкарбоніл, C1-C6 алкоксикарбоніл, C1-C6 ся із азоту, сірки та кисню, і зазначене кільце заалкіламінокарбоніл або C2-C8 діалкіламінокарбоміщене, при потребі, однією або більше R9; ніл; і кожна із R4 та R5 являє собою, незалежно, гакожна R12 являє собою, незалежно, CO2H, логен, CN, CHO, С1-С6 алкіл, С1-C4 алкокси, C1-C4 CONH2, NO2, C1-C6 галоалкокси, C2-C6 алкілтіо, C1галоалкокси, C1-C4 алкілтіо, C1-C4 алкілсульфініл, C6 алкілсульфініл, C1-C6 алкілсульфоніл, C1-C6 C1-C4 галоалкілтіо, C1-C4 галоалкілсульфініл або галоалкілтіо, C1-C6 галоалкілсульфініл, C1-C6 гаС1-С6 галоалкіл; 13 78039 14 Одна R5 приєднана до залишкової частини алкенілів (СН2)= СН2, (СН2)= СН2, 3СН 4СН Формули І у 5 положенні даного бензольного кіль(СН2)= СН2, (СН2)6СН СН2, (СН2)7СН СН2, = = 5СН ця, і, при потребі, друга R5 приєднана у 6 поло(СН2)8СН СН2 та (СН2)9СН= СН2. Крім того, при= женні даного бензольного кільця; та клади включають такі сполуки, де R6 вибирається m дорівнює 1 або 2. із зазначених алкільних та алкенільних складових “Сполуки, яким віддається перевага 4а” (а), (b), (c) та (d), де принаймні один атом водню Сполуки із розділу “Сполуки, яким віддається замінений галогеном (наприклад, сполуки, де R6 перевага, 4”, де: вибирається із зазначених алкільних складових, кожна із R1, R2 та R3 являє собою, незалежно, де CH3 група замінена на CF3 групу; і сполуки, де Н або С 1-С10 алкіл; R6 вибирається із зазначених алкенільних складо4 5 кожна із R та R являє собою, незалежно, гавих, де =СН2 гр упа замінена на =CF2 групу). Прилоген, С1-С6 алкіл або С 1-С6 галоалкіл; клади також включають такі сполуки, де R6 виби5 R приєднана до залишкової частини Формули рається із зазначених алкільних складових (а) та І у 5 положенні даного бензольного кільця; (b), де принаймні один атом водню замінений на кожна R12 являє собою, незалежно, CO2H, ОСН3, ОС2Н5 , ОСН(СН3)2 або ОС(СН 3)3. CONH2, NO2, C1-C6 галоалкокси, C2-C6 алкілтіо, C1Заслуговують на особливу увагу сполуки форC6 алкілсульфініл, C1-C6 алкілсульфоніл, C1-C6 мули І (включаючи, але не обмежуючись цим, спогалоалкілтіо, C1-C6 галоалкілсульфініл, C1-C6 галуки із розділів “Сполуки, яким віддається перевалоалкілсульфоніл, C1-C6 алкіламіно, C2-C8 діалкіга, 1, 2, 2а, 3, 3а, 4 та 4а”), де: ламіно, C2-C6 алкілкарбоніл, C2-C6 алкоксикарбоR6 вибирається із групи, котра включає ніл, C3-C9 алкоксиалкілкарбоніл, C2-C6 (СН2)3С(СН3)2ОСН3, (СН2)3С(СН3)2ОС2Н5, алкіламінокарбоніл, C4-C10 алкіламіноалкілкарбо(СН2)3С(СН3)2ОСН(СН3)2, (СН2)3С(СН3)2ОС(СН3)3, ніл, C3-C8 діалкіламінокарбоніл, C3-C8 діалкіламі(СН2)3С(СН3)2F, (СН2)3С(СН3)2Cl та ноалкілкарбоніл, C3-C9 алкілтіоалкілкарбоніл, C3(СН2)3С(СН3)2Br. C9 триалкілсиліл або C3-C9 триалкілсилілокси; і “Сполуки, яким віддається перевага, 5” m дорівнює 1. Сполуки із розділу “Сполуки, яким віддається Заслуговують на увагу сполуки формули І перевага, 4”, де: (включаючи, але не обмежуючись цим, сполуки із R1 являє собою Н; і розділів “Сполуки, яким віддається перевага, 1, 2, R6 являє собою С6-С15 алкіл, де принаймні 2а, 3, 3а, 4 та 4а”), де: один із четвертого та п’ятого вуглецевих атомів від R6 являє собою алкіл, заміщений, при потребі, А має один або не має жодного приєднаного атому галогеном або С 1-С6 алкокси. Також заслуговують водню, або С5-С12 алкеніл, де четвертий або на увагу сполуки Формули І (включаючи, але не п’ятий вуглецевий атом від А має один або не має обмежуючись цим, сполуки із розділів “Сполуки, жодного приєднаного атому водню (іншими слояким віддається перевага, 1, 2, 2а, 3, 3а, 4 та 4а”), вами, R6 розгалужений у четвертого та/або п’ятого де R6 являє собою алкеніл, заміщений, при потреатомів вуглецю). бі, галогеном. Приклади включають сполуки, де R6 “Сполуки, яким віддається перевага, 5а” вибирається із групи, котра містить (а) складові із Сполуки із розділу “Сполуки, яким віддається розгалужених алкілів СН(СН 3)(СН2)3СН3, перевага, 5”, де: СН(СН3)(СН2)4СН3, СН(СН3)(СН2)5СН3, кожна із R2, R3, R4 та R5 являє собою метил, і СН(СН3)(СН2)6СН3, СН(СН3)(СН2)7СН3, m дорівнює 1. СН(СН3)(СН2)8СН3, СН(С2Н5)(СН2)4СН3, “Сполуки, яким віддається перевага, 5b” СН2СН(СН3)(СН2)2СН3, СН2СН(СН3)(СН2)4СН3, Сполуки із розділу “Сполуки, яким віддається СН2СН(С2Н5)СН2СН2СН3, перевага, 5”, де: (СН2)2СН(СН3)(СН2)3СН(СН3)2, кожна із R2 та R3 являє собою, незалежно, ме(СН2)2СН(СН3)СН2С(СН3)3, тил або етил. (СН2)2СН(СН3)(СН2)3С(СН3)3, (СН2)2С(СН3)3, Заслуговують на увагу сполуки формули І (СН2)3С(СН3)3, (СН2)3С(С2Н5)3 , (СН2)3СН(С2Н5)3, (включаючи, але не обмежуючись цим, сполуки із (СН2)3СН(СН3)2, (СН2)4СН(СН3)2, (СН2)5СН(СН3)2, розділів “Сполуки, яким віддається перевага, 1, 2, СН(СН2СН2СН2СН3)2, СН(СН2СН2СН3)(СН2)3СН3, 2а, 3, 3а, 4, 4а, 5, 5а та 5b”), де: СН(СН2СН2СН2СН2 СН3)2, R6 вибирається із групи, що включає (а) алкіСН(С2Н5)СН2СН2СН(СН3)2, льні складові (СН2)2СН(СН3)СН2С(СН3)3, СН(СН3)СН2СН2СН(СН3)2, СН(СН3)СН2СН2С(СН3)3, (СН2)3СН(СН3)2, СН(С2Н5)СН2СН2СН(СН3)2, СН(СН2СН2СН3)СН2СН2СН(СН3)2, СН(СН3)СН2СН2СН(СН3)2, СН(СН2СН2СН(СН3)2)2, СН(СН2СН2СН3)2 та СН(СН2СН2СН3)СН2СН2СН(СН3)2 та СН(СН2СН2СН2СН3)(СН2)5СН3, (b) складові із ліСН(СН2СН2СН(СН3)2)2 та (b) алкенільні складові нійних алкілів (СН2)4СН3, (СН2)5СН3, (СН2)6СН3, СН2СН= СНСН(СН3)2, СН2= СНСН2СН(СН3)2, СН (СН2)7СН3, (СН2)8СН3, (СН2)9СН3, (СН2)10СН3, (с) СН2= СНС(СН3)3 та СН2СН=СНСН2С(СН3)3. ТаСН складові із розгалужених алкенілів кож заслуговують на увагу сполуки Формули І (СН2)= С(СН3)2, (СН2)5C(СН3)=СН2, (включаючи, але не обмежуючись цим, сполуки із 2CН (СН2)6C(СН3)=СН2, (СН2)7C(СН3)=СН2, розділів “Сполуки, яким віддається перевага, 1, 2, = С(СН3)2, СН2СН= С(СН3)(СН2)2СН= С(СН3)2, СН2СН 2а, 3, 3а, 4, 4а, 5, 5а та 5b”), де R6 являє собою СН2(СН= С(СН3)(СН2)2)2СН= С(СН3)2, (СН2)3С(СН3)3 або СН(СН3)СН2СН2С(СН3)3. (СН2)3С(=СН2)СН(СН3)2, СН= СНСН(СН3)2, “Сполуки, яким віддається перевага, 6” 2СН СН= СНСН2СН(СН3)2, СН2СН СНС(СН3)3 та = Сполуки із розділу “Сполуки, яким віддається 2СН СН2СН СНСН2С(СН 3)3 та (d) складові із лінійних = перевага, 4”, де: 15 78039 16 R1 являє собою Н; і Даний винахід також стосується способу контR6 являє собою С1-С4 алкіл, заміщений одним ролю хвороб рослин, що зумовлені грибковими або більшою кількістю замісників, що вибираються рослинними патогенами, який включає нанесення із групи, котра включає С 2-С6 алкілтіо, С1-6 алкілна дану рослину або її частину, або на насіння чи сульфініл, С2-С6 алкоксикарбоніл, С2-С8 діалкіларозсаду фунгіцидно ефективної кількості сполук міно, С2-С6 алкілкарбоніл, С3-С9 алкоксиалкілкарданого винаходу (наприклад, як композицію, що боніл, С2-С6 алкіламінокарбоніл, С3-С8 описана у даному тексті). Способами, котрим віддіалкіламінокарбоніл, С3-С9 триалкілсиліл, С3-С9 дається перевага, є ті, що включають вищезазнагалотриалкілсиліл, С4-С9 алкокситриалкілсиліл або чені сполуки, яким віддається перевага. С3-С9 триалкілсилілокси. Сполуки формули І можуть бути одержані з “Сполуки, яким віддається перевага, 6а” використанням одного або більшої кількості настуСполуки із розділу “Сполуки, яким віддається пних способів та варіантів, як описано на схемах 1перевага, 6”, де: 9. Якщо окремо не зазначено, визначення R1 - R12, 2 3 4 5 кожна із R , R , R та R являє собою метил; і A, m та n у сполуках формул 1-13 нижче є такими, R6 являє собою С1-С4 алкіл, заміщений одним як визначено вище. Сполуки формул Ia-Ig являють або більшою кількістю замісників, що вибираються собою різні підмножини сполук формули І, і всі із групи, котра включає С 2-С6 алкілтіо, С1-6 алкілзамісники для формул Ia-Ig, якщо окремо не засульфініл, С2-С6 алкоксикарбоніл, С2-С8 діалкілазначено, є такими, як визначено вище для формуміно, С2-С6 алкілкарбоніл, С3-С9 алкоксиалкілкарли І. боніл, С2-С6 алкіламінокарбоніл, С3-С8 Як показано на схемі І, сполуки формули Іа діалкіламінокарбоніл, С3-С9 триалкілсиліл або С 3можуть бути одержані із анілінів формули 1. Є різС9 триалкілсилілокси. новид способів для проведення такого перетво“Сполуки, яким віддається перевага, 6b” рення. Особливо корисні наступні чотири способи. Сполуки із розділу “Сполуки, яким віддається Схема І перевага, 6”, де: кожна із R2 та R3 являє собою метил або етил. Заслуговують на увагу сполуки формули І (включаючи, але не обмежуючись цим, сполуки із розділів “Сполуки, яким віддається перевага, 1, 2, 2а, 3, 3а, 4, 4а, 5, 5а, 5b, 6, 6а та 6b”), де R6 являє де: R1 являє собою Н; С1-С10 алкіл, С2-С10 алсобою алкілтриалкілсиліл. Заслуговують також на кеніл, С2-С10 алкініл, С2-С5 алкоксикарбоніл, С3-С6 увагу сполуки Формули І (включаючи, але не обкарбоцикл або С3-С6 гетероцикл. межуючись цим, сполуки із розділів “Сполуки, яким Спосіб 1: Обробка аніліну формули 1 ацетавіддається перевага, 1, 2, 2а, 3, 3а, 4, 4а, 5, 5а, 5b, лем формули R2R3NC(R1)(OR13)2, де R13 являє 6, 6а та 6b”), де R6 являє собою алкілтриалкілсилісобою алкіл. Як основне посилання на цей спосіб локси. Приклади включають сполуки, де R6 вибидивись роботу [Toste et al. // Synth. Commun. – рається із групи, що включає (е) алкілтриалкілси1994. - 24(11). – P. 1617-1624]. лілові складові СН 2Si(CH3)3, CH2СН2Si(CH3)3, Спосіб 2: Обробка аніліну формули 1 амідом СН2CH2CH2Si(CH3)3, СН2CH2CH2CH2Si(CH3)3, формули R1C(=O)NR 2R3 у присутності агента галоCH2Si(C2H5)3, CH2CH2Si(C2H5)3, генування, такого як, але не обмежуючись цим, CH2CH2CH2Si(CH3)2(C2H5), CH2CH2CH2Si(C2H5)3, POCl3 або SOCl2. Як основне посилання на цей CH2CH2CH2CH2Si(C2H5)3, CH2Si(CH(CH3)2)3, спосіб дивись роботу [Bergman et al. // Tetrahedron. CH2CH2Si(CH(CH3)2)3, CH2CH2CH2Si(CH(CH3)2)3, – 1990. - 46(17). – P. 6058-6112]. CH2CH2CH2CH2Si(CH(CH3)2)3, CH2Si(CH3)2C(CH3)3, Спосіб 3: Обробка аніліну формули 1 ортоефіCH2CH2Si(CH3)2C(CH3)3, ром формули R1C(OR 13)3, де R13 являє собою алCH2CH2CH2Si(CH3)2C(CH3)3 та кіл, для одержання відповідного іміноефіру з наСН2CH2CH2CH2Si(CH3)2C(CH3)3 та (f) алкілтриалкіступним нагріванням даного іміноефіру з аміном лсилілокси складові СН 2OSi(CH3)3, формули HNR2R3. Як основне посилання на цей CН2СН2OSi(CH3)3, СН2СН2СН2OSi(CH3)3, спосіб дивись [US, 4209319]. СН2СН2СН2СН2OSi(CH3)3, СН2OSi(C2H5)3, Спосіб 4: Обробка аніліну формули 1 фосгеCH2СН2OSi(C2H5)3, CH2CH2СН2OSi(C2H5)3, ном для одержання ізоціанату з наступною реакціCH2CH2CH2СН2OSi(C2H5)3, CH2OSi(CH(CH3)2)3, єю зазначеного ізоціанату з амідом формули CH2CH2OSi(CH(CH 3)2)3, CH2CH2CH2OSi(CH(CH3)2)3, R1C(=O)NR 2R3. Як основне посилання на цей споCH2CH2CH2CH2OSi(CH(CH3)2)3, сіб дивись [WO, 00/46184]. CH2OSi(CH3)2C(CH3)3, CH2CH2OSi(CH3)2C(CH3)3, Спосіб 5: Обробка аніліну формули 1 CH2CH2CH2OSi(CH3)2C(CH3)3 та C2H5OCH=NCN для одержання N-ціаноамідину з СН2CH2CH2CH2OSi(CH3)2C(CH 3)3. наступною реакцією зазначеного N-ціаноамідину з Даний винахід також стосується фунгіцидних аміном формули НNR2R3. Як основне посилання композицій, що включають фунгіцидно ефективні на цей спосіб дивись [WO, 00/46184]. кількості сполук даного винаходу та, принаймні, Сполуки Формули Ib можуть бути одержані за один додатковий компонент, котрий вибирається із способом, що окреслений на cхемі 2. Обробка групи, що складається із поверхнево-активних респолуки формули 1 4,5-дихлоро-1,2,3човин, твердих розріджувачів та рідких розріджудитіазолійхлоридом (формула 2) дає відповідний вачів. Композиціями даного винаходу, котрим від4-хлоро-5-(феніліміно)-5Н-1,2,3-дитіазол (формула дається перевага, є ті композиції, що включають 3). Реакція зазначеного дитіазолу з аміном форвищезазначені сполуки, яким віддається перевага. 17 78039 18 мули 4 у придатному органічному розчиннику, тагрупи як визначено вище, шляхом обробки відпокому як, але не обмежуючись цим, дихлорометан, відним аміном або ацилювання чи алкілування, при кімнатній температурі дає сполуку формули Іb. коли R2 або R3 являє собою водень. Як основне посилання на цей спосіб дивись [J. Як проілюстровано на Схемі 5, сполука форOrg. Chem. // - 1993. - 58(25). – P. 7001-7008]. мули І може також бути одержана шляхом алкілуСхема 2 вання сполуки формули 8 агентом алкілування формули 9 у присутності основи. Сполуки формули 8 є відомими сполуками або можуть бути одержані за методами, що відомі із літератури [J. Med. Chem. – 1984. - 27(12). – P. 1705-10; EP, 94052; WO, 00/46184]. В агенті алкілування формули 9 Х являє собою відщеплювальну груп у нуклеофільної реакції, як визначено вище для формули 7. Дана реакція проводиться у присутності принаймні одного еквівалента основи, краще, від 1 до 2 еквівалентів. Придатні основи включають неорганічні основи, такі як гідриди лужних металів (таких як літій, натрій або калій), карбонати та гідроксиди, і Сполуки Формули Iс можуть бути одержані у органічні основи, такі як триетиламін, діізопропілеспосіб, що окреслений на Схемі 3. Реакція аніліну тиламін та 1,8-діазобіцикло[5,4,0]ундец-7-ен. Дана Формули 1 з карбамоїлхлоридом формули 5 дає реакція звичайно проводиться в розчиннику, котсечовину формули Ig. Потім сечовину Формули Ig рий може включати ароматичні розчинники, такі як піддають O-алкілуванню з утворенням сполуки бензол та толуол, е фіри, такі як тетрагідрофуран формули Іс шля хом контактування з агентом алкіта діетиловий ефір, і полярні апротонні розчинни7 лування формули 7 (R X) у присутності основи. В ки, такі як ацетонітрил, N,N-диметилформамід і агенті алкілування Формули 7 Х являє собою відтаке подібне. Дану реакцію, загалом, проводять в щеплювальну гр упу нуклеофільної реакції, таку як області температур від приблизно -20 до 150 оС, галоген (наприклад, Br, I), OS(O) 2CH3 (метансулькраще, від 20 до 140оС. Час реакції може варіювафонат), OS(O)2CF 3, OS(O) 2Ph-p-CH 3 (pти від 1год. до 7 діб. Сполука Формули І може бути толуолсульфонат) і таке подібне. Придатними освиділена з використанням звичайних способів, новами можуть бути, наприклад, але не обмежуютаких як екстракція. Додаткові експериментальні чись цим, карбонат калію (К2СО3) або оксид срібла подробиці способу за Схемою 5 проілюстровані у (Ag2O). Як основне посилання на цей спосіб диприкладі 1. вись роботу [Curtis et al. // Aust. J. Chem. – 1988. Схема 5 41(4). – P. 585-595]. Схема 3 де Х являє собою відщеплювальну груп у. Сполуки формули Id можуть бути одержані у спосіб, що окреслений на Схемі 4. Обробка аніліну формули 1 тіофосгеном (або його еквівалентом) дає відповідний ізотіоціанат. Потім даний ізотіоціанат піддають реакції з аміном формули 4 з одержанням тіосечовини Формули Ih. Потім тіосечовину формули Ih алкілують з одержанням сполуки формули Id шля хом контактування з агентом алкілування Формули 7 (R7X). Придатною основою може бути, наприклад, але не обмежуючись цим, гідроксид калію. Як основне посилання на цей спосіб дивись роботу [Filop et al. // Tetrahedron. – 1985. - 41(24). – P. 5981-5988]. Схема 4 де Х являє собою відщеплювальну груп у. Слід зазначити, що R2 та R3 групи у сполуках Формули І можуть бути перетворені в інші R2 та R3 де: A являє собою О, S або NR10; і Х являє собою відщеплювальну групу нуклеофільної реакції. Крім того, відновлювальне амінування сполуки формули 8, де А являє собою NH, у присутності альдегіду або кетону також може дати сполуку формули І, де R 6 являє собою заміщену, при потребі, алкільну груп у. Умови реакції відновлювального амінування вивчались у роботі [J. Med. Chem. – 1984. - 17(12). – P. 1705-1710] та у роботах, на які посилаються в цій роботі. Як альтернатива до способу, що проілюстрований на Схемі 3, сполука формули 1с може бути також одержана у спосіб, який окреслений на Схемі 6. Нагрівання фенілізоціаніддихлориду формули 10 з аміном формули 4 дає відповідну імідоїлову проміжну сполуку. Обробка даної імідоїлової проміжної сполуки спиртом формули 11 у присутності інертної основи, такої як, але не обмежуючись цим, триетиламін, дає сполуку формули Іс. Як посилання на цей спосіб дивись роботу [Filop et al. // Izv. Akad. Nauk SSSR, Ser. Khim. – 1989. - (11). – P. 2596-2601] та посилання, що наведені у цій роботі. Фенілізоціаніддихлорид формули 10 може бути одержаний у способи, що викладені у літера 19 78039 турі [J. Chem. Soc., Perkin Trans. 1. – 1987. - (5). – P. 1069-1076; Tetrahedron Lett. – 1982. - 23(35). – P. 3539-3542; Chem. Ber. – 1987. - 120(3). – P. 421424]. Схема 6 Сполуки формули 1f можуть бути одержані шляхом окиснення сполук формули Іе, як проілюстровано на Схемі 7. Агентом окиснення можуть слугувати пероцтова кислота, пероксид водню, перманганат калію, перйодат натрію або 3хлоропероксибензойна кислота. Розчинником може бути, наприклад, але не обмежуючись цим, дихлорометан, оцтова кислота або вода. Детальні умови для реалізації цього способу можна знайти у робота х [J. Med. Chem. – 1996. - 39(26). – P. 5072-5082; J. Med. Chem. – 1983. - 26(1). – P.107110] та посиланнях, що наведені в цих робота х. Схема 7 деn дорівнює 1 або 2. Сполуки формули 1 можуть бути одержані шляхом відновлення нітрогрупи у сполуках формули 12. Існ ує багато способів проведення цієї відновлювальної реакції. Способи, яким віддається перевага, включають відновлення хлоридом двовалентного олова у концентрованій хлористоводневій кислоті [J. Med. Chem. – 1984. - 24(12). – P. 1705-1710] та відновлення порошком заліза у розчині оцтової кислоти та води [J. Org. Chem. – 2001. - 66(13). – P. 4563-4575]. Схема 8 Як показано на Схемі 9, сполуки формули 12 можуть бути одержані шляхом алкілування сполук формули 13 агентом алкілування формули 9 у присутності основи. Умови реакції для цього алкілування вже описані для перетворення сполук формули 8 у сполуки Формули І на Схемі 5. Сполуки формули 13 є відомими сполуками або можуть бути одержані з використанням способів, що описані в літературі [Can. J. Chem. – 1984. - 62(8). – P. 1446-51; Aust. J. Chem. – 1991. - 44(1). – P. 151-6]. Схема 9 20 де: А являє собою O, S або NR10; і Х являє собою відщеплювальну групу нуклеофільної реакції. Як альтернатива, сполуки формули 12, де А являє собою O, S або NR10, і R6 є заміщеною, при потребі, алкільною групою, можуть бути також одержані із сполук формули 13 через реакцію Міцунобу, котра включає реакцію сполуки формули 13 з відповідним спиртом R6OH. Загальні умови реакції Міцунобу добре задокументовані у хімічній літературі. Огляд зазначеної реакції Міцунобу дивись у роботі [Hughes Org. React. – 1992. – 42. – P. 335-656] та наведених у цій роботі посиланнях. Сполуки формули 12, де А являє собою прямий зв’язок, можуть бути одержані з використанням множини відомих способів. Фахівець у даній галузі може одержати сполуки формули 12 з використанням способів, що широко висвітлені у літературі; дивись, наприклад, [Synth. Commun. – 2001. - 31(14). – P. 2113-2117; Synth. Commun. – 1999. - 29(12). – P. 2169-2174; J. Chem. Res. Synop. – 1998. - (8). – P. 410, 1701-1714; J. Chem. Soc. Perkin Trans. 1. – 1998. - (12). – P. 1903-1912; Synthesis. – 1982. - (10). – P. 836-9; J. Org. Chem. – 1977. - 42(24). – P. 3907-9]. Визнано, що деякі реагенти та умови реакцій, що описані вище для одержання сполук Формули І, можуть бути несумісними з деякими функціональними групами, котрі присутні у даних проміжних сполуках. У цих випадках уведення у схему даного синтезу послідовностей протектування/депротектування або взаємоперетворень функціональних гр уп буде сприяти одержанню потрібних продуктів. Використання та вибір зазначених протекторних груп є зрозумілим для фахівця у галузі хімічного синтезу (дивись, наприклад, [Greene T.W., Wuts, P.G.M. Protecti ve Groups in Organic Synthesis. 2nd ed. - New York: Wiley, 1991]). Фахівцеві у даній галузі також зрозуміло, що в деяких випадках після уведення даного реагенту, як це зображено на будь-якій окремій схемі, може виникнути потреба у проведенні додаткових звичайних синтетичних стадій, що детально не описані, для завершення синтезу сполук формули І. Фахівцеві у даній галузі також зрозуміло, що може виникнути потреба у комбінації кількох стадій, що проілюстровані на вищезазначених схемах, у порядку, який відрізняється від передбаченого конкретними наведеними послідовностями, для одержання сполук формули І. Фахівцеві у даній галузі також зрозуміло, що сполуки формули І та проміжні сполуки, котрі описані у даному тексті, можуть піддаватись різним електрофільним, нуклеофільним, радикальним, металоорганічним реакціям, реакціям окиснення та відновлення для додаткового уведення замісників або модифікування існуючих замісників. Можна вважати, що без будь-яких додаткових уточнень фахівець у даній галузі, використовуючи 21 78039 22 вищенаведений опис, зможе використати даний Приклад 3 винахід у повному обсязі. Тому наступні приклади Одержання N’-[2,5-диметил-4-[3слід розглядати як просто ілюстративні, без будь(триметилсиліл)пропокси]феніл]-N,Nяких обмежень у плані розкриття винаходу. Відсодиметилметанімідаміду тки наведені у вигляді вагових відсотків, за виклюДо суспензії N’-(4-гідрокси-2,5-диметилфеніл)ченням відсотків для хроматографічних сумішей N,N-диметилметанімідаміду (0,52г, 2,7ммоль) у ррозчинників або коли зазначене інше. Якщо окредіоксані (10мл) під атмосферою азоту при кімнатмо не зазначено, частини та відсотки для хроматоній температурі додавали 60% гідрид натрію у міграфічних сумішей розчинників наведені в неральному маслі (120мг, 3ммоль). Після додаоб’ємних одиницях. 1Н ЯМР спектри подані у млн -1 вання дану суміш перемішували при кімнатній долях у нижньому напрямі енергетичного спектру температурі протягом 21хв., і додавали (3від тетраметилсилану: s – син глет; d – дублет; t – хлоропропіл)триметилсилан (0,5г, 3,3ммоль). триплет; q – квартет; m – мультиплет; dd - дублет Утворену в результаті реакційну суміш нагрівали зі дублетів; dt - дублет триплетів; br s - широкий синзворотним холодильником протягом 4 діб і потім глет. охолоджували до кімнатної температури. Дану Приклад 1 реакційну суміш виливали у діетиловий ефір Одержання N’-[2,5-диметил-4-[(3-метил-2(100мл). Органічний шар промивали 1N водним бутеніл)-окси]феніл]-N,N-диметилметанімідаміду розчином гідроксиду натрію (3 х 100мл). Потім орТитульну сполуку одержували із N’-(4-гідроксиганічний шар осушували над MgSO4 та фільтрува2,5-диметилфеніл)-N,N-диметилметанімідаміду ли. Фільтрат концентрували і потім висушували у (одержаного як описано у [WO, 00/46184]. До сувакуумній печі при 90°С протягом ночі з одержанспензії N’-(4-гідрокси-2,5-диметилфеніл)-N,Nням титульної сполуки (0,16г), сполуки даного видиметилметанімідаміду (0,77г, 4ммоль) у тетрагіднаходу, у вигляді масла. 1 рофурані (34мл) під атмосферою азоту при кімнаH ЯМР (CDCl3): d 0,02 (t, 9H), 0,6 (m, 2H), 1,7тній температурі додавали 60% гідрид натрію у 1,82 (m, 2H), 2,17 (s, 3H), 2,23 (s, 3H), 2,98 (s, мінеральному маслі (170мг, 4,25ммоль). Потім 6H),3,87 (t, 2H), 6,54 (s, 1H), 6,62 (s, 1H), 7,38 (s, дану суміш перемішували при кімнатній темпера1H). турі протягом приблизно 45хв. з наступним доданПриклад 4 ням 4-бромо-2-метил-2-бутену (0,72г, 4,8ммоль). Одержання N’-[4-[(1-бутилпентил)окси]-2,5Результуючу реакційну суміш перемішували при диметилфеніл]-N,N-диметилметанімідаміду кімнатній температурі протягом 2 діб і потім вилиСтадія А: Одержання 1-[(1-бутилпентил)окси]вали у діетиловий ефір (250мл). Органічний шар 2,5-диметил-4-нітробензолу потім промивали 1N водним розчином гідроксиду Діізопропіл азодикарбоксилат (0,570г, натрію (2 х 200мл). Потім органічний шар осушу2,82ммоль) додавали по краплях до розчину тривали над MgSO4 та фільтрували. Фільтрат конценфенілфосфін у (0,739г, 2,82ммоль) у тетрагідрофутрували з одержанням титульної сполуки (1,02г), рані (15мл) при 0°С. Дану суміш перемішували при сполуки даного винаходу, у вигляді коричневого 0°С додатково протягом 30хв. До вищезазначеномасла. го холодного розчину по краплях додавали суміш 1 Н ЯМР (CDCl3): d 1,72 (s, 3H), 1,78 (s, 3H), 2,5-диметил-4-нітрофенолу (0,315г, 1,9ммоль) та 2,17 (s, 3H), 2,24 (s, 3H), 2,99 (s, 6H), 4,46 (d, 2H), 5-нонанолу (0,288г, 2ммоль) у тетрагідрофурані 5,5 (t, 1H), 6,55 (s, 1H), 6,66 (s, 1H), 7,38 (s, 1H). (10мл). Потім дану реакційну суміш перемішували Приклад 2 при 0°С протягом 30хв. та при кімнатній темпераОдержання N’-[2,5-диметил-4-[(4турі протягом 1год. Тетрагідрофуран вилучали під метилфеніл)окси]-феніл]-N,Nзниженим тиском, і залишок розтирали з гексаном диметилметанімідаміду (100мл) та фільтрували. Осад промивали гексаДо суспензії N’-(4-гідрокси-2,5-диметилфеніл)ном (50мл). Гексан вилучали під зниженим тиском, N,N-диметилметанімідаміду (0,52г, 2,7ммоль) у і залишок очищали методом колонкової хроматогтетрагідрофурані (~10мл) під атмосферою азоту рафії з елююванням дихлорометаном з одержанпри кімнатній температурі додавали 60% гідрид ням титульної сполуки (0,4г) у вигляді масла. 1 натрію у мінеральному маслі (120мг, 3ммоль). ПісH ЯМР (CDCl3): d 0,9 (t, 6H), 1,2-1,4 (m, 8H), ля додавання дану суміш перемішували при кімна1,6-1,7 (m, 4H), 2,15 (s, 3H), 2,6 (s, 3H), 4,35 (m, H), тній температурі протягом 30хв., і додавали 16,6 (s, 1H), 7,9 (s, 1H). бромо-4-метилпентан (0,55г, 3,3ммоль). Утворену Стадія В: Одержання 1-[(1-бутилпентил)окси]в результаті реакційну суміш нагрівали зі зворот2,5-диметил-4-бензоламіну ним холодильником протягом 24год., охолоджува1-[(1-бутилпентил)окси]-2,5-диметил-4ли до кімнатної температури та перемішували при нітробензол (тобто продукт зі стадії А) (0,4г, кімнатній температурі протягом ночі. Потім дану 1,39ммоль) відновлювали шляхом каталітичного реакційну суміш виливали у діетиловий ефір гідрування з використанням паладієвого (на вугіл(100мл). Органічний шар промивали 1N водним лі) каталізатора (10 % мас., 0,2г) в етанолі (~20мл) розчином гідроксиду натрію (3 х 100мл), осушувапід надлишковим тиском водню 40 фунтів на квадли над MgSO4 та фільтрували. Фільтрат концентратний дюйм (276кПа) відносно навколишнього рували з одержанням титульної сполуки (0,7 г), середовища протягом 8год. Даний каталізатор сполуки даного винаходу, у вигляді масла. вилучали фільтр уванням, і фільтрат концентрува1 H ЯМР (CDCl3): d 0,91 (d, 6H), 1,28-1,82 (m, ли під зниженим тиском. Залишок очищали мето5H), 2,16 (s, 3H), 2,23 (s, 3H), 2,98 (s, 6H),3,89 (t, дом колонкової хроматографії з елююванням дих2H), 6,54 (s, 1H), 6,63 (s, 1H), 7,37 (s, 1H). лорометаном з одержанням титульної сполуки 23 78039 24 (0,35г) у вигляді масла. ціанометанімідаміду 1 До розчину N-ціанометанімідного етилового H ЯМР (CDCl3): d 0,9 (t, 6H), 1,2-1,4 (m, 8H), ефіру (1,21г, 12,35ммоль) в етанолі (16мл) при 1,6-1,7 (m, 4H), 2,15 (s, 6H), 3,25 (m, 2H), 4,0 (m, кімнатній температурі додавали по краплях розчин 1H), 6,42 (s, 1H), 6,5 (s, 1H). 5-хлоро-2-метил-4-[3Стадія С: Одержання N’-[4-[(1(триметилсиліл)пропокси]бензоламіну (тобто пробутилпентил)окси]-2,5-диметилфеніл]-N,Nдукту зі стадії В) (2,93г, 10,77ммоль) в етанолі диметилметанімідаміду (16мл). Після додавання дану реакційну суміш Диметилформамід диметилацеталь (~5мл) перемішували при кімнатній температурі протягом додавали до 1-[(1-бутилпентил)окси]-2,5-диметилночі і потім концентрували під зниженим тиском. 4-бензоламіну (тобто продукту зі стадії В) (350мг) Залишок розтирали у розчині 25% етилацетату в під аргоном, і дану суміш нагрівали до 100°С прогексанах, і тверду речовину збирали шляхом фільтягом 2год. Дану реакційну суміш охолоджували трації з одержанням титульної сполуки (2,4г) у видо кімнатної температури та розподіляли між ефігляді білуватої твердої речовини, Т.пл. 143-144°С. ром (50мл) та водою (50мл). Органічний шар про1 мивали послідовно водою (50мл) та розсолом, H ЯМР (CDCl3): d 0,03 (s, 9H), 0,62 (m, 2H), осушували (Na2SO4), фільтрували та концентрува1,82 (m, 2H), 2,28 (m, 3H), 3,96 (m, 2H), 6,78-8,35 ли з одержанням титульної сполуки (300мг), спо(m, 3H). луки даного винаходу, у вигляді червонува того Стадія D: Одержання N’-[5-хлоро-2-метил-4-[3масла. (триметилсиліл)пропокси]феніл]-N-етил-N1 метилметанімідаміду H ЯМР (CDCl3): d 0,9 (t, 6H), 1,2-1,4 (m, 8H), До суспензії N-[5-хлоро-2-метил-4-[31,5-1,7 (m, 4H), 2,15 (s, 3H), 2,2 (s, 3H), 3,0 (s, 6H), (триметилсиліл]пропокси]феніл]-N’4,1 (m, H), 6,5 (s, 1H), 6,6 (s, 1H), 7,4 (s, 1H). ціанометанімідаміду (тобто продукту зі стадії С) Приклад 5 (174мг, 0,54ммоль) в ацетонітрилі (4мл) при кімнаОдержання N’-[5-хлоро-2-метил-4-[3тній температурі по краплях додавали N(триметилсиліл)пропокси]феніл]-N-етил-Nетилметиламін (0,23мл, 2,68ммоль). Після додаметилметанімідаміду вання дану реакційну суміш перемішували при Стадія А: Одержання [3-(2-хлоро-5-метил-4кімнатній температурі протягом ночі. Потім до реанітрофенокси)пропіл]триметилсилану кційної суміші додавали ефір (40мл). Утворену в Діізопропіл азодикарбоксилат (2,3мл, результаті суміш промивали водою (40мл) і потім 11,68ммоль), 3-триметилсилілпропанол (1,41г, розсолом (40мл). Органічний шар відокремлюва10,66ммоль), 2-хлоро-5-метил-4-нітрофенол (2,0г, ли, осушували над MgSO4 та концентрували з 10,64ммоль) та трифенілфосфін (3,24г, одержанням титульної сполуки (160мг), сполуки 12,35ммоль) додавали до тетрагідрофурану даного винаходу, у вигляді масла. (55мл) при -10°С. Потім дану суміш підігрівали до 1 H ЯМР (CDCl3): d 0,02 (s, 9H), 0,6 (m, 2H), 1,2 кімнатної температури та перемішували при кімна(t, 3H), 1,8 (m, 2H), 2,23 (s, 3H), 2,98 (s, 3H), 3,35 (br тній температурі протягом ночі. Тетрагідрофуран s, 2H), 3,93 (t, 2H), 6,74 (s, 1H), 6,77 (s, 1H), 7,4 (s, вилучали під зниженим тиском, і залишок очищали 1H). методом колонкової хроматографії (силікагель; елюювання розчином 5% етилацетату у гексанах) Приклад 6 Одержання N’-[5-хлоро-2-метил-4-[3з одержанням титульної сполуки (2,68г) у вигляді (триметилсиліл)пропокси]феніл]-N-етил-Nтвердої речовини жовтого кольору, Т.пл. 66-68°С. 1 метилтіосечовини H ЯМР (CDCl3): d 0,04 (s, 9H), 0,64 (m, 2H), Стадія А: Одержання [3-(2-хлоро-41,86 (m, 2H), 2,64 (s, 3H), 4,05 (t, 2H), 6,76 (s, 1H), ізотіоціанато-5-метилфенокси)пропіл]8,17 (s, 1H). триметилсилану Стадія В: Одержання 5-хлоро-2-метил-4-[3До розчину 5-хлоро-2-метил-4-[3(триметилсиліл)пропокси]бензоламіну (триметилсиліл)пропокси]бензоламіну (тобто проДо суміші [3-(2-хлоро-5-метил-4дукту із Прикладу 5, стадія В) (1,63г, 6ммоль) у нітрофенокси)пропіл]триметилсилану (тобто протолуолі (50мл) при 25°С додавали діетилкарбамілдукту зі стадії А) (3,5г, 11,6ммоль) та метанолу хлорид (1,2г, 7,8ммоль) з наступним додаванням (16мл) при кімнатній температурі додавали при N,N-діізопропілетиламіну (1,1г, 9ммоль). Утвореперемішуванні концентровану хлористоводневу ний в результаті гомогенний розчин нагрівали зі кислоту (16мл) та хлорид олова (ІІ) (6,64г, зворотним холодильником протягом 3год. Розчин35,02ммоль). Дану реакційну суміш нагрівали зі ник випарювали, і залишок піддавали хроматогзворотним холодильником протягом 4год. Після рафуванню на тонкому шарі силікагелю з викорисохолодження даної суміші до кімнатної температутанням етилацетат/гексану (1:40) як елюенту з ри до неї додавали дихлорометан (320мл). Суміш одержанням титульної сполуки (1,19г) у вигляді промивали 4N водним розчином гідроксиду натрію блідо-жовтої напіврідкої речовини. (110мл) а потім розсолом (3 х 320мл). Органічний 1 H ЯМР (CDCl3): d 0,00 (s, 9H), 0,60 (m, 2H), шар відокремлювали, осушували над MgSO 4 та 1,80 (m, 2H), 2,40 (s, 3H), 3,85 (t, 2H), 6,60 (s, 1H), концентрували з одержанням титульної сполуки 7,00 (s, 1H). (2,97г) у вигляді масла. 1 Стадія В: Одержання N’-[5-хлоро-2-метил-4-[3H ЯМР (CDCl3): d 0,02 (s, 9H), 0,61 (m, 2H), (триметилсиліл)пропокси]феніл]-N-етил-N1,76 (m, 2H), 2,13 (s, 3H), 3,4 (br s, 2H), 3,89 (t, 2H), метилтіосечовини 6,69 (s, 1H), 6,7 (s, 1H). До розчину [3-(2-хлоро-4-ізотіоціанато-5Стадія С: Одержання N-[5-хлоро-2-метил-4-[3метилфенокси)пропіл]-триметилсилану (тобто (триметилсиліл]пропокси]феніл]-N’ 25 78039 26 продукту зі стадії А) (310мг, 1ммоль) у те трагідрододавали хлорид олова (ІІ) (5,1г, 26,7ммоль). Дану реакційну суміш нагрівали зі зворотним холодильфурані (10мл) при 25°С додавали Nником протягом 4год. Реакційну суміш охолоджуетилметиламін (1г, 17ммоль). Дану реакційну сували до кімнатної температури, і метаноловий міш перемішували при 25°С протягом 30хв. Потім розчинник вилучали під зниженим тиском. Дану розчинник випарювали, і до залишку додавали реакційну суміш розподіляли між дихлорометаном гексан з метою індукувати кристалізацію. Тверду (~50мл) та 4N водним розчином гідроксиду натрію речовину збирали фільтруванням та промивали (4 х 50мл). Органічний шар відокремлювали, осурозчином ефір/гексан (1:5) (20мл) з одержанням шували над MgSO4 та концентрували з одержантитульної сполуки (255мг), сполуки даного винахоням титульної сполуки (2,0г) у вигляді коричневого ду, у вигляді білуватої твердої речовини, Т.пл. 71масла. 72°С. 1 1 H ЯМР (CDCl3): d 0,02 (s, 9H), 0,61 (m, 2H), H ЯМР (CDCl3): d 0,00 (s, 9H), 0,60 (m, 2H), 1,78 (m, 2H), 2,35 (s, 3H), 3,92 (t, 2H), 4,04 (br s, 1,25 (t, 3H), 1,80 (m, 2H), 2,20 (s, 3H), 3,20 (s, 3H), 2H), 6,78 (s, 1H), 6,98 (s, 1H). 3,85 (q, 2H), 3,90 (t, 2H), 6,70 (br s, 1H), 6,75 (s, 1H), Стадія D: Одержання N-[5-хлоро-2-(метилтіо)7,15 (s, 1H). 4-[3-(триметилсиліл)пропокси]феніл]-N’Приклад 7 ціанометанімідаміду Одержання N’-[5-хлоро-2-(метилтіо)-4-[3До розчину N-ціанометанімідного етилового (триметилсиліл)пропокси]феніл]-N-циклопропіл-Nефіру (0,84г, 8,6ммоль) в етанолі (5мл) додавали метилметанімідаміду по краплях при кімнатній температурі розчин 5Стадія А: Одержання [3-(2,5-дихлоро-4хлоро-2-(метилтіо)-4-[3нітрофенокси)пропіл]триметилсилану (триметилсиліл)пропокси]бензоламіну (тобто проДіізопропіл азодикарбоксилат (10,4мл, дукту зі стадії С) (2,0г, 6,6ммоль) в етанолі (10мл). 53ммоль), 3-триметилсилілпропанол (6,4г, Після додавання дану реакційну суміш перемішу48ммоль), 2,5-дихлоро-4-нітрофенол (10,0г, вали при кімнатній температурі протягом 2 діб і 48ммоль) та трифенілфосфін (12,6г, 48ммоль) потім концентрували під зниженим тиском. Залидодавали до тетрагідрофурану (100мл) при -10°С. шок очищали методом силікагелевої колонкової Потім дану суміш підігрівали до кімнатної темпехроматографії з використанням суміші етилацератури протягом ночі. Тетрагідрофуран вилучали тат/гексани (1:2) як елюенту з одержанням титульпід зниженим тиском, і залишок розтирали з гексаної сполуки (1,8г) у вигляді твердої речовини понами (~200мл). Тверду речовину відфільтровувамаранчевого кольору, Т.пл. 94-96°С. ли. Потім фільтрат концентрували, і залишок очи1 H ЯМР (CDCl3): d 0,03 (s, 9H), 0,62 (m, 2H), щали методом силікагелевої колонкової 1,84 (m, 2H), 2,39 (m, 3H), 3,96 (t, 2H), 6,97-8,37 (m, хроматографії з елююванням гексанами а потім 3H). 2% етилацетатом у гексанах з одержанням титуСтадія Е: Одержання N’-[5-хлоро-2-(метилтіо)льної сполуки (13,5г) у вигляді твердої речовини 4-[3-(триметилсиліл)пропокси]феніл]-Nжовтого кольору, Т.пл. 45-48°С. 1 циклопропіл-N-метилметанімідаміну H ЯМР (CDCl3): d 0,05 (s, 9H), 0,65 (m, 2H), До суспензії N-[5-хлоро-2-(метилтіо)-4-[31,89 (m, 2H), 4,07 (t, 2H), 7,00 (s, 1H), 8,12 (s, 1H). (триметилсиліл)пропокси]феніл]-N’Стадія В: Одержання [3-[2-хлоро-5-(метилтіо)ціанометанімідаміду (тобто продукту зі стадії D) 4-нітрофенокси]пропіл]триметилсилану (200мг, 0,56ммоль) в ацетонітрилі (5мл) при кімнаДо розчину [3-(2,5-дихлоро-4тній температурі додавали по краплях розчин Nнітрофенокси)пропіл]триметилсилану (4,6г, циклопропілметиламіну в ефірі (7,6мл, 0,74М, 14,3ммоль) (тобто продукту зі стадії А) у N,N5,6ммоль). Після додавання дану реакційну суміш диметилформаміді (40мл) додавали тіометоксид перемішували при кімнатній температурі протягом натрію (1,3г, 18,6ммоль) при кімнатній температуночі. Потім реакційну суміш концентрували під рі. Дану реакційну суміш нагрівали до 100°С прозниженим тиском, і залишок очищали методом тягом 2 діб. Потім дану реакційну суміш розподісилікагелевої колонкової хроматографії з викорислювали між ефіром (100мл) та водою (150мл). танням суміші етилацетат/гексани (1:2) як елюенОрганічний шар промивали водою (3 х 50мл), відоту з одержанням титульної сполуки (120мг), сполукремлювали, осушували над MgSO4, фільтр ували ки даного винаходу, у вигляді рудувато-коричневої та концентрували. Залишок очищали методом твердої речовини, Т.пл. 62-64°С. силікагелевої колонкової хроматографії з викорис1 H ЯМР (CDCl3): d 0,02 (s, 9H), 0,6-0,8 (m, 6H), танням суміші гексани/бутилхлорид (3:1) як елюе1,82 (m, 2H), 2,4 (s, 3H), 2,7 (m, 1H), 3,23 (s, 3H), нту з одержанням титульної сполуки (2,7г) у ви3,96 (t, 2H), 6,69 (s, 1H), 6,79 (s, 1H), 7,64 (s, 1H). гляді твердої речовини помаранчевого кольору, З використанням процедур, що описані у даТ.пл. 51-53°С. 1 ному тексті, та разом з методами, що відомі у даH ЯМР (CDCl3): d 0,05 (s, 9H), 0,65 (m, 2H), ній галузі, можуть бути одержані наступні сполуки, 1,89 (m, 2H), 2,49 (s, 3H), 4,09 (t, 2H), 6,69 (s, 1H),наведені у табл. 1-13. У зазначених табл. 1-13 ви8,35 (s, 1H). користані наступні скорочення: t означає третинСтадія С: Одержання 5-хлоро-2-(метилтіо)-4ний; s означає вторинний; n означає нормальний, і [3-(триметилсиліл)пропокси]бензоламіну відповідає ізо, с відповідає цикло; Pr означає проДо розчину [3-[2-хлоро-5-(метилтіо)-4піл; і-Pr означає ізопропіл; с-Pr означає циклопронітрофенокси]пропіл]триметилсилану (тобто пропіл; Bu означає бутил; CN означає ціано. дукту зі стадії В) (2.7г, 8,91ммоль) у метанолі (5мл) та концентрованій хлористоводневій кислоті (5мл) 27 78039 28 Таблиця 1 Одержані сполуки формули А O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O R6 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH 3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)8CH3 (CH2)9CH3 (CH2)11CH3 C(=O)OCH 2C(CH3)3 (CH2)4CH(CH3)2 C(=O)OCH(C 2H5)C(CH3)3 C(=O)OC(CH 3)2C(CH3)3 C(=O)NHCH2C(CH3)3 C(=O)N(CH 3)CH2C(CH 3)3 CH2CH2CH2CH=C(CH3)2 C(=O)CH 2SC(CH3)3 (CH2)4Cl A S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S S R6 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)8CH3 (CH2)9CH3 (CH2)11CH3 C(=O)OCH 2C(CH3)3 (CH2)4CH(CH3)2 C(=O)OCH(C 2H5)C(CH3)3 C(=O)OC(CH 3)2C(CH3)3 C(=O)NHCH2C(CH3)3 C(=O)N(CH 3)CH2C(CH3)3 CH2CH2CH2CH=C(CH3)2 C(=O)CH 2SC(CH3)3 (CH2)4Cl 29 78039 30 Продовження таблиці 1 O O O O O O O O O O O O O O O O O O O (CH2)5Cl (CH2)2CH(CH3)(CH2)3CH(CH3)2 (S)(CH2)2CH(CH3)CH2CH2CH=C(CH 3)2 (R)(CH2)2CH(CH3)CH2CH2CH=C(CH 3)2 (CH2)2CH(CH3)2 (CH2)2C(CH3)3 CH2C(=O)C(CH 3)3 CH2CH=C(CH3)(CH2)2CH=C(CH3)2 CH2(CH=C(CH3)(CH2)2)2CH=C(CH3)2 (CH2)3CH=CH2 (CH2)4CH=CH2 CH(C2H5)2 CH(CH2CH2CH3)2 CH(CH2CH2CH2CH3)2 CH(CH2CH2CH3)CH2CH2CH2CH3 CH(CH3)CH2CH2CH(CH3)(C2H5) CH(CH2CH2CH2CH2CH3)2 CH(CH2CH2CH2CH3)(CH2)5CH3 CH(C2H5)CH2CH2C(=CH2)CH3 S S (CH2)5Cl (CH2)2CH(CH3)(CH2)3CH(CH3)2 S (S)-(CH2)2CH(CH3)CH2CH2CH=C(CH 3)2 S S S S S S S S S S S S S S S S (R)-(CH2)2CH(CH3)CH2CH2CH=C(CH3)2 (CH2)2CH(CH3)2 (CH2)2C(CH3)3 CH2C(=O)C(CH 3)3 CH2CH=C(CH3)(CH2)2CH=C(CH3)2 CH2(CH=C(CH3)(CH2)2)2CH=C(CH3)2 (CH2)3CH=CH2 (CH2)4CH=CH2 CH(C2H5)2 CH(CH2CH2CH3)2 CH(CH2CH2CH2CH3)2 CH(CH2CH2CH3)CH2CH2CH2CH3 CH(CH3)CH2CH2CH(CH3)(C2H5) CH(CH2CH2CH2CH2CH3)2 CH(CH2CH2CH2CH3)(CH2)5CH3 CH(C2H5)CH2CH2C(=CH2)CH3 Таблиця 2 Одержані сполуки формули R1 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 СН3 R6 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)3 R1 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 R6 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)3 31 78039 32 Продовження таблиці 2 СН3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH 3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH 3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 OCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 SCH3 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 Таблиця 3 Одержані сполуки формули A O R2 CH3 R3 C2H5 R6 (CH2)4CH3 33 78039 34 Продовження таблиці 3 O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O O CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 35 78039 36 Продовження таблиці 3 O O O O O O O O O O O O O NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NCH3 NH NH NH NH NH NH NH NH NH NH C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 C2H5 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 37 78039 38 Продовження таблиці 3 NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH NH CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)8CH3 (CH2)9CH3 (CH2)11CH3 (CH2)4CH(CH3)2 C(=O)OCH(C 2H5)C(CH3)3 C(=O)OC(CH 3)2C(CH3)3 CH2CH2CH2CH=C(CH3)2 C(=O)CH 2SC(CH3)3 (CH2)4Cl (CH2)5Cl (CH2)2CH(CH3)(CH2)3CH(CH3)2 (S)-(CH2)2CH(CH3)CH2CH2CH=C(CH 3)2 (R)-(CH2)2CH(CH3)CH2CH2CH=C(CH3)2 (CH2)2CH(CH3)2 (CH2)2C(CH3)3 CH2C(=O)C(CH 3)3 CH2CH=C(CH3)(CH2)2CH=C(CH3)2 CH2(CH=C(CH3)(CH2)2)2CH=C(CH3)2 (CH2)3CH=CH2 (CH2)4CH=CH2 CH(C2H5)2 CH(CH2CH2CH3)2 CH(CH2CH2CH2CH3)2 CH(CH2CH2CH3)CH2CH2CH2CH3 CH(CH3)CH2CH2CH(CH3)(C2H5) CH(CH2CH2CH2CH2CH3)2 CH(CH2CH2CH2CH3)(CH2)5CH3 CH(C2H5)CH2CH2C(=CH2)CH3 39 78039 40 Таблиця 4 Одержані сполуки формули R4 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl m 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 R5 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 R6 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 41 Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl CH3 CH3 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 0 0 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 5-Cl 78039 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 42 Продовження таблиці 4 43 78039 44 Продовження таблиці 4 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 45 78039 46 Продовження таблиці 4 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CF3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 1 1 1 1 1 1 1 1 1 1 1 1 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 5-CH3-6-Cl 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 47 78039 48 Продовження таблиці 4 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3,5-di-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 3-CH3 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 49 78039 50 Продовження таблиці 4 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 F F F F F F F F F F F F F F F F F F F F 1 1 1 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3-CH3 3-CH3 3-CH3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,6-di-Cl-5-CH 3 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3F (CH2)2SCF(CH3)3 (CH2)2SCFH(CH3)2 CH2CH=FCHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 51 78039 52 Продовження таблиці 4 F F F F F F F F F F F F F F F F F Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl CH3 CH3 CH3 CH3 CH3 CH3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 1 1 1 1 1 1 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-F 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 3,5,6-tri-Cl 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SCF(CH3)3 (CH2)2SCFH(CH3)2 CH2CH=FCHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 53 78039 54 Продовження таблиці 4 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 CH3 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-CH(CH 3)2 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 55 78039 56 Продовження таблиці 4 CH3 CH3 CH3 CH3 CH3 CH3 1 1 1 1 1 1 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 5-C(CH3)3 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl Таблиця 5 Одержані сполуки формули A NH NH NH NH NH NH NH NH NH O O O R6 C(=O)CH 2SC(CH3)3 C(=O)CH 2S(=O)C(CH 3)3 C(=O)CH 2S(=O)2C(CH3)3 C(=O)OCH 2C(CH3)3 C(=O)NHCH2C(CH3)3 C(=O)N(CH 3)CH2C(CH 3)3 C(=O)OCH 2CH(CH3)2 C(=O)NHCH2CH(CH3)2 C(=O)N(CH 3)CH2CH(CH3)2 C(CH3)2CH2CH2CH(CH3)2 C(CH3)(CH2CH2CH2CH3)2 C(CH3)(CH2CH2CH3)2 Таблиця 6 Одержані сполуки формули R5 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 R6 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 57 78039 58 Продовження таблиці 6 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 5-CH3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 Таблиця 7 Одержані сполуки формули R2 + R3 -(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4 R6 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 59 78039 60 Продовження таблиці 7 -(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-(CH2)4-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-CH2CH2OCH2CH2-(CH2)5-(CH2)5-(CH2)5-(CH2)5-(CH2)5-(CH2)5-(CH2)5-(CH2)5-(CH2)5-(CH2)5-(CH2)5-(CH2)5-(CH2)5-(CH2)5-(CH2)5-(CH2)5 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2 CH2CH=CHC(CH3)3 CH2CH=CHCH(CH3)2 (CH2)2S(=O)C(CH 3)3 (CH2)3OSi(CH3)2C(CH3)3 (CH2)2OCH(CH3)2 (CH2)3OC(CH3)3 (CH2)3P(=O)(CH3)2 CH2C(=O)CH 2C(CH3)3 CH(CH3)(CH2)3CH3 CH(CH3)CH2CH2CH(CH3)2 CH(CH3)CH2CH2C(CH3)3 CH(C2H5)CH2CH2CH(CH3)2 CH(CH2CH2CH3)CH2CH2CH(CH3)2 CH(CH2CH2CH)(CH3)2)2 CH2CH2CH2N(CH3)2 CH2CH2N(CH3)C(CH3)3 CH2CH2N(CH3)CH(CH3)2 CH2CH=C(CH3)2 (CH2)3C(CH3)2OCH3 (CH2)3C(CH3)2Cl CH2CH2CH=C(CH3)2 (CH2)4CH3 (CH2)3C(CH3)2OC2H5 (CH2)5CH3 (CH2)6CH3 (CH2)3C(CH3)2Br (CH2)7CH3 (CH2)3CH(CH3)2 (CH2)3C(CH3)3 (CH2)3Si(CH3)3 (CH2)2CH(CH3)CH2C(CH3)3 (CH2)3C(=CH2)CH(CH3)2 (CH2)3CH(CH3)C2H5 (CH2)2OSi(CH3)2C(CH3)3 (CH2)2OC(CH3)3 (CH2)2SC(CH3)3 (CH2)2SCH(CH3)2
ДивитисяДодаткова інформація
Назва патенту англійськоюAmidinyl phenyl compounds, fungicide compositions and a method for controlling plants diseases
Назва патенту російськоюАмидинилфениловые соединения, фунгицидные композиции и способ контроля болезней растений
Автори російськоюTSENG, Chi-Ping
МПК / Мітки
МПК: A01N 47/28, A01N 47/40, C07C 257/00, A01N 37/52, A01P 3/00
Мітки: контролю, фунгіцидні, сполуки, амідинілфенілові, композиції, рослин, хвороб, спосіб
Код посилання
<a href="https://ua.patents.su/91-78039-amidinilfenilovi-spoluki-fungicidni-kompozici-ta-sposib-kontrolyu-khvorob-roslin.html" target="_blank" rel="follow" title="База патентів України">Амідинілфенілові сполуки, фунгіцидні композиції та спосіб контролю хвороб рослин</a>
Попередній патент: Ініціювальна вибухова речовина
Наступний патент: Похідні ацил-4-карбоксифенілмочевини, спосіб їх одержання (варіанти), лікарський засіб на їх основі та спосіб його одержання
Випадковий патент: Спосіб визначення характеристики тріщиностійкості кіс матеріалу