Похідні бензоїлгуанідину, спосіб їх отримання, фармацевтична композиція та спосіб її отримання
Номер патенту: 39118
Опубліковано: 15.06.2001
Автори: МІНК Клаус-Отто, БАУМГАРТ Манфред, ГЕРІКЕ Рольф, Дорш Дітер, Байєр Норберт
Формула / Реферат
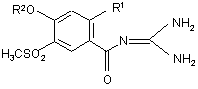
1. Производные бензоилгуанидина формулы (I):
 , (I)
, (I)
где R1 обозначает метил или этил, и R2 обозначает водород; линейный или разветвленный C1-C6 - алкильный или алкенильный остаток; С3-С7-циклоалкил, бензил или незамещенный, или одно-, двух- или трехкратно замещенный метилом, метокси-группой, амино-группой, F, Cl, Вг, или СF3 фенил, а также их физиологически приемлемые соли.
2. Производные бензоилгуанидина формулы (I) по п. 1, представляющие
собой:
N-диаминометилен-2-метил-4-фенокси-5-метилсульфонил-бензамид;
N-диаминометилен-2-этил-4-метокси-5-метилсульфонил-бензамид;
N-диаминометилен-2-метил-4-этокси-5-метилсульфонил-бензамид;
N-диаминометилен-2-метил-4-Х2-хлорфенокси-5-метилсульфонил-бензамид;
N-диаминометилен-2-метил-4-(4-хлорфенокси)-5-метилсульфонил-бензамид;
а также их физиологически приемлемые соли.
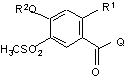
3. Способ получения производных бензоилгуанидина формулы (I) по п. 1, а также их солей, отличающийся тем, что соединение формулы (II):
 , (II)
, (II)
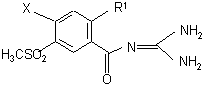
где R1 и R2 имеют вышеуказанные значения, и Q обозначает С1, Вг , ОА, O-СО-А, O-CO-Ph , ОН или другую реакционноспособную, этерифицированную до сложноэфирной, группу, соответственно, легко нуклеофильно замещаемую удаляемую группу; и А обозначает алкил с 1 - 6 С-атомами, вводят во взаимодействие с гуанидином; или беноилгуанидин формулы (III)
 , (III)
, (III)
где R' имеет вышеуказанные значения, и Х обозначает F, С1, Br, J или другую пригодную удаляемую группу, вводят во взаимодействие со спиртом, соответственно, с фенолом формулы (IV) R2 - ОН, где R2 имеет указанное значение, в случае необходимости после предварительного переведения в алкоголят; или спирт (фенол) формулы (I), где R2 = Н и R1 имеет указанное значение, вводят во взаимодействие с соединением формулы R2 - X, где R2 и Х имеют указанные значения; или обычно соответствующее формуле (I) соединение, которое, однако, вместо одного или нескольких атомов водорода содержит одну или несколько восстанавливаемых групп и/или одну или несколько дополнительных С-С- и/или C-N- связей, обрабатывают восстановителем; или обычно соответствующее формуле (I) соединение, которое, однако, вместо одного или нескольких атомов водорода содержит одну или несколько сольволизируемых групп, обрабатывают сольволизирующим средством; и/или полученное основание формулы (I) путем обработки с помощью кислоты переводят в одну из его солей.
4. Способ получения фармацевтической композиции, отличающийся тем, что соединение формулы (I) по п. 1 и/или одну из его физиологически приемлемых солей вместе, по меньшей мере, с одним твердым, жидким или полужидким носителем,или вспомогательным веществом доводят до пригодной дозировочной формы.
5. Фармацевтическая композиция, содержащая активный компонент и фармацевтически приемлемые добавки, отличающаяся тем, что в качестве активного компонента содержит эффективное количество производного бензоилгуанидина формулы (I) по п.1.
Текст
1. Производные бензоилгуанидина формулы (I): 39118 обычно соответствующее формуле (I) соединение, которое, однако, вместо одного или нескольких атомов водорода содержит одну или несколько сольволизируемых групп, обрабатывают сольволизирующим средством; и/или полученное основание формулы (I) путем обработки с помощью кислоты переводят в одну из его солей. 4. Способ получения фармацевтической композиции, отличающийся тем, что соединение формулы (I) по п. 1 и/или одн у из его физио логически приемлемых солей вместе, по меньшей мере, с одним твердым, жидким или полужидким носителем,или вспомогательным веществом доводят до пригодной дозировочной формы. 5. Фармацевтическая композиция, содержащая активный компонент и фармацевтически приемлемые добавки, отличающаяся тем, что в качестве активного компонента содержит эффективное количество производного бензоилгуанидина формулы (I) по п.1. ______________________________ Изобретение относится к производным бензоилгуа нидина формулы (I) Предлагаемые согласно изобретению вещества настоящей заявки обладают хо рошим кардиозащитным действием и поэтому особенно пригодны для лечения инфаркта, профилакти ки инфаркта и для лечения стенокардии. Далее, вещества противодействуют всем патологическим гипоксическим и ишемическим повреждениям, так что можно лечить вызываемые благо даря им первичные или вторичные заболевания. Биологически активные вещества также хорошо пригодны для профилакти ческих применений. Из защитной активности эти х ве ществ при гетологических гипоксических или ише мических ситуа циях вытекают дальнейшие возможности применения при хирургических вмешательствах для защиты вре менно менее снабжаемых (кровью) органов, при трансплантациях органов для защи ты извлекаемых органов, при ангиопластических вмешательствах в сосуды или сердце, при ишемиях нервной системы, при терапии шоковых состояний и для профи лактического препятствования эссенциальной гиперто нии. Далее, соединения также можно использовать в качестве терапевти ческих средств в случае обусловленных пролифе рацией клеток заболеваний, как артериосклероз, диабетические поздние осложнения, опухо левые заболевания, фибротические заболевания, в особенности легких, печени и почек, а также гипертрофии и гиперплазии органов. Сверх того, вещества пригодны для диагностики с целью распознавания заболеваний, которые сопровождаются повышенной активностью Na+/H+ – антипереносчика, например, в эритроцитах, тромбоцитах или лейкоцитах. Активность соединений можно определять с помощью само по себе известных методов, которые, например, указываются в N.Escobales и J. Figueroa в J. Membrane Biol. 120, 41–49 (1991) или L. Counillon, W. Scholg, H.J. Lang, и J. Ponyssegur. Mol. Pharmacol. 44, 1041–1045 (1993). В качестве подопытных животных пригодны, например, мыши, крысы, морские свинки, собаки, кошки, обезьяны или свиньи. Соединения поэтому можно применять в качестве биологически активных веществ лекарственных средств в медицине и ветеринарии. Далее, они могут найти применение в качестве промежуточных продуктов для получения других ценных биологически активных ве ществ ле карственных средств. R2 предпочти тельно обозначает метил, этил или фенил; далее, однако также предпочти тельно , (I) 1 где R обозначает метил или этил; R2 обозначает водород, линейный или разветвленный С1-С6-алкильный или алкенильный остаток, С3-С7-циклоалкил, бензил или незамещенный или одно-, двух- или трехк ратно замещенный метилом, метокси-группой, амино-группой, F, Cl, Br, или CF3 фе нил; а также к их фи зиологически приемлемым солям. В основу изобретения положена задача получения новых сое динений с ценными свойствами, в особенности таких, которые можно применять для приготовления лекарственных средств. Найдено, что соединения формулы (I) и их фи зиологически приемлемые соли при хорошей совместимости обладают ценными фармакологическими свойства ми. В случае но вы х соеди нений речь иде т об ингиби торах кле точного Na+/H+ – антипереносчика, т.е . о био логически акти вных ве щества х, кото рые инги бируют ме ха низм Na+/H+ – обмена в клетках (Düsing и др., Med. Klin . 87, 378–384 (1992)) и ко торые та ким образом представляют собой хо рошие ан тиаритмические средства. В особенности они пригодны для ле че ния аритмий, кото рые появляются как следствие не достатка кисло рода. Самым известным биологически активным веществом из группы ацилгуа нидинов является амилорид. Это вещество, однако, в первую очередь обладает понижающим кровяное давление и салуретическим действием, что в особенности нежелательно при лечении наруше ний сердечного ритма, в то время как антиаритмические свойства выражены только очень слабо. Сверх того, известны структурно-подобные соединения, например, из европейского патента ЕР-04 16 499. Предметом изобретения являются соединения формулы (I), а также их физиологически приемлемые соли. 2 39118 бензил или циклоалкил с 3-, 5-или 6-атомами углерода, в особенности, следовательно, циклопропил, циклопентил или циклогексил. Если R2 обозначает фенил, то он предпочти тельно незамещен или однократно замещен фтором или хлором. Соответственно этому, предметом изобретения являются в частности те соединения формулы (I), в кото рых по меньшей мере один из указанных остатков имеет одно из вышеуказанных предпочтительных значений. Некоторыми предпочти тельными соединениями формулы (I) являются следующие: N-диаминометилен-2-метил-4-фенокси-5-метилсульфо нилбензамид; N-диаминометилен-2-этил-4-фе нокси-5-метилсульфо нилбензамид; N-диаминометилен-2-метил-4-гидрокси-5-метилсульфо нилбензамид; N-диаминометилен-2-этил-4-гидрокси-5-метилсульфо нилбензамид; N-диаминометилен-2-метил-4-бензилокси-5метилсульфо нилбензамид; N-диаминометилен-2-этил-4-бензилокси-5-метилсульфо нилбензамид; N-диаминомети лен-2-этил-4-ме токси-5-метилсульфо нилбензамид; N-диаминометилен-2-этил-4-циклопропилокси-5- метилсульфо нилбензамид; N-диаминометилен-2-этил-4-циклопентилокси-5- метилсульфо нилбензамид; N-диаминометилен-2-этил-4-циклогексилокси-5- метилсульфо нилбензамид. Предметом изобретения, далее, является способ получения соединений формулы (I) по п. 1 формулы изобретения, а также их со лей, отличающийся тем, что соединение формулы (II): вводят во взаимодействие со спиртом, соответственно фенолом, формулы (IV): R2 – OH где R2 имеет указанное значение, в случае необходимости после предшествующего переведения в алкоголят; или спирт (фенол) формулы (I), где R2 = Н, а R1 имеет указанное значение, вводят во взаимодействие с соединением формулы R2 – Х, где R2 и Х имеют указанные значения; или обычно соответствующее фор муле (I) соединение, которое, однако, вместо одного или нескольких ато мов водорода содержит одну или несколько восстанавливаемых групп и/или одну или несколько дополнительных С-С и/или С-Nсвязей, обрабатывают восстанови телем; или обычно соответствующее фор муле (I) соединение, которое, однако, вместо одного или нескольких ато мов водорода содержит одну или несколько сольволизируемых групп, обрабатывают с помощью сольволизирующе го средства; и/или полученное основание формулы (I) путем обработки с помощью кислоты превращают в одну из его солей. Соединения формулы (I) впрочем получают само по себе известными способами, которые описываются в лите ратуре (например, в стандартных работах, как Губен-Вейл, Ме тоды органической химии, изд. Georg-Thieme, Штутгарт; Органические реакции, John Wiley and Sons, Inc., НьюЙорк; а также в вышеуказанной заявке на патент), а именно при реакционных условиях, которые известны и пригодны для указанных взаимодействий. При этом также можно использовать само по себе известные, здесь подробнее не упомянутые, варианты. Исходные вещества в желательном случае также можно получать in situ, таким образом, что их не выделяют из реакционной смеси, а тотчас вводят во взаимодействие далее до получения соединений формулы (I). Предпочти тельно, соединения формулы (I) получают тем, что активированное производное карбоновой кислоты фор мулы (II), причем Q особенно предпочти тельно обозначает хлор или -О-СН3, вво дят во взаимодействие с гуанидином. Особенно пригодны также варианты реакции, в случае кото рых свободная карбоновая кислота формулы (II) (Q=OH) само по себе известным образом превращается в соответствующее активированное производное и его затем непосредственно, без промежуточного выделения, вводят во взаимодействие с гуа нидином. Способы, при которых излишне промежуточное выделение, представляют собой, например, активирование с помощью карбонилдиимидазола, дициклогексилкарбодиимида или по варианту Maka yama (Angew. Chem., 91, 788–812 (1979)). Карбоновые кислоты и производные карбоновых кислот формулы (II) как прави ло известны. В особенности их получают тем, что соответствующее производное 2-алкил-4-галоген-5-метилсуфо нилбензойной кислоты вво дят во взаимодействие с алкого лятом или фенолятом, который производится от спирта или фенола формулы (IV). Н3 СО2 S , (II) где R1 и R2 имеют вы шеуказанные значения и Q обозначает Cl, Br, OA, O-CO-A, O-CO-Ph, ОН или другую реакционноспособную, эте рифи цированную до сложноэфирной ОН-группу, соответственно, легко нуклеофильно замещаемую уда ляемую груп пу; и А обозначает алкил с 1–6 С-атомами, вводят во взаимодействие с гуанидином; или бензоилгуа нидин формулы (III): H3 CO2 X (IV), , (III) где R1 имеет выше указанные значения, а Х обозначает F, Cl, Br, J или другую пригодную удаляемую гр уппу, 3 39118 Взаимодействие осуществляют по аналогии с реакцией соединения формулы (III) с соединением формулы (IV). Оно описывается ниже. Взаимодействие реакционноспособного производного карбоновой кислоты формулы (II) с гуа нидином осуществляют само по себе известным образом, предпочтительно в протонном или апротонном, полярном или неполярном, инертном органическом растворите ле. Пригодные растворители указываются ниже для взаимодействия соединений формул (III) и (IV). Особенно предпочтительными растворителями, однако, являются метанол, ТГФ, диметоксиэтан, диоксан или приготовляемые из них смеси, а также вода. В качестве реакционной температуры пригодны, например, температуры от 20оС до температуры кипения растворите ля. Времена реакций составляют от 5 минут до 12 часов. Целесообразно при реакции использовать улавливатель кислоты. Для этой цели пригодны любые виды оснований, которые сами не мешают реакции. Особенно пригодно, однако, применение неорганических оснований, как карбонат калия, или органических оснований, как триэтиламин или пиридин, или, однако, избыток гуа нидина. Соединения формулы (I) по п. 1, далее, можно получать тем, что бензоилгуанидин формулы (III) вво дят во взаимодействие с соединением формулы (IV). Исходные вещества фор мулы (III) можно получать путем взаимодействия соответствующим образом замещенных бензойных кислот или производимых от них реакционноспособных производных кислот, как, например, галоидангидриды, сложные эфиры или ангидриды, с гуанидином, при реакционных условиях, которые сами по себе известны и общеприняты для получения амидов. Опять особенно пригодны такие варианты реакции, которые указаны выше для взаимодействия соединения формулы (II) с гуанидином. Получение соединения формулы (II), а также взаимодействие соединения формулы (III) с соединением формулы (IV), осуществляют само по себе известным образом, предпочти тельно в протонном или апротонном полярном инертном органическом растворите ле. При получении соединения формулы (II) или при взаимодействии соединения формулы (III) с соединением формулы (IV) также целесообразно работать в присутствии основания или с избытком основной компоненты. В качестве оснований предпочти тельно пригодны, например, гидроксиды, карбонаты, алкоголяты ще лочных или щелочноземельных металлов или органические основания, как триэтиламин или пиридин, которые также применяются в избытке и тогда одновременно могут служить в качестве растворителя. В качестве инертных растворите лей в частности пригодны спирты, как метанол, этанол, изопропанол, н-бутанол или трет.-бута нол; простые эфи ры, как диэтиловый эфир, диизопропиловый эфир, тетрагидрофуран (ТГФ) или диоксан; простые гликолевые эфи ры, как этиленгликольмонометиловый или -моноэтиловый простой эфир (метилгликоль или этилгликоль), этиленгликольдиметиловый простой эфир (диглим); кетоны, как ацетон или бутанон; нитрилы, как ацетонитрил; нитросоединения, как нитрометан или натробензол; сложные эфиры, как этилацетат; амиды, как гексаметилтриамид фосфорной кислоты; сульфоксиды, как диметилсульфоксид (ДМСО); хло рированные углеводороды, как дихлорметан, хло роформ, трихлорэти лен, 1,2-дихлорэтан, или тетрахлорид углерода; углеводороды, как бензол, толуол или ксилол. Далее, пригодны смеси этих растворителей друг с др угом. Также соединения формулы (I) можно получать тем, что их высво бождают из их функциональных производных путем сольволиза, в особенности гидролиза, или путем гидрогенолиза. Предпочти тельными исходными веществами для сольволиза, соответственно, гидрогенолиза, являются такие, которые обычно соответствуют формуле (I), однако, вместо одной или нескольких свободных амино- и/или гидроксильных групп содержат соответствующие защищенные амино- и/или гидроксильные группы, предпочтительно такие, которые вместо Н-атома, который связан с N-атомом, содержат защитную для амино-функции группу, в особенности такие, которые вместо NH-груп пы содержат R' – N-группу, где R' обозначает защи тную для амино-функции группу, и/или такие, которые вместо Н-атома гидроксильный группы содержат защитную для гидроксильной функции группу, например, такие, которые соответствуют формуле (I), однако, вместо ОНгруп пы содержит OR''-груп пу, где R'' обозначает защитную для гидроксильной функции группу. В молекуле исходного вещества могут такженахо диться несколько – одинаковых или разных – защи щенных амино- и/или гидроксильных групп. В случае, если имеющиеся защитные группы отличаются друг от др уга, то во многих случаях их можно отщеплять селективно. Выражение "защитная для амино-функции груп па" общеизвестно и относится к группам, которые пригодны для защиты (блокирования) аминофункции от химических взаимодействий и которые, однако, легко удаляются, после того, как в другом месте молекулы прошла желательная химическая реакция. Типичными для таких групп являются в частности незамещенные или замещенные ацильные, арильные (например, как 2,4-динитрофе нил [DNP]), аралкоксиметильные (например, как бензилоксиметил [BOM]) или аралкильные группы (например, бензил, 4-нитробензил, трифенилметил). Так как защитные для аминофункции группы после желательной реакции (или последовательности реакций) удаляются, их род и величина, впрочем, не критические; предпочтительно, однако, груп пы с 1–20, в особенности 1–8 С-атомами. Выражение "ацильная группа" в связи с настоящим способом нужно понимать в самом широком смысле. Оно охватывает производимые от алифати ческих, аралифа тических, ароматических или гетероциклических карбоновых кислот или сульфо кислот ацильные группы, также, как в особенности алкоксикарбонильные, арилоксикарбонильные или прежде всего аралкоксикарбонильные группы. Примерами такого рода ацильных групп являются алканоильная группа, как ацетил, пропионил, бутирил; аралканоильная группа, как фе нилацетил; ароильная группа, как бензоил или толуил; арилоксиалканоильная группа, как феноксиацетил; алкоксикарбонильная группа, как меток 4 39118 сикарбонил, этоксикарбонил, 2,2,2-трихлорэтоксикарбонил, изопропоксикарбонил, трет.-бутоксикарбонил (ВОС), 2-иодэтоксикарбонил; аралкилоксикарбонил, как бензилоксикарбонил (CВZ), 4-метоксибензилоксикарбонил, 9-флуо ренилметоксикарбонил (FМОС). Предпочти тельными защитными для амино-функции группами являются ВОС, DNP и ВОМ, да лее, CBZ, бензил и ацетил. Выражение "защитная для гидроксильной функции группа" также общеизвестно и относится к группам, которые пригодны для защи ты гидроксильной группы от химических взаимодействий, которые, однако, легко удаляются, после то го, как в другом месте молекулы прошла желательная хи мическая реакция. Типичными для таких групп являются вышеуказанные, незамещен ные или замещенные, арильные, аралкильные или ацильные груп пы, далее, также алкильные группы. Природа и величина защитных для гидроксильной функции групп не критические, так как они снова удаляются после протекания желательной химической реакции или последовательности реакций; предпочтительны группы с 1–20, в особенности с 1–10 С-атомами. Примерами защитных для гидроксильной функции групп являются, между прочим, трет.бутил, бензил, п-нитробензоил, п-толуолсульфонил и ацетил, причем бензил и ацетил особенно предпочтительным. Применяемые в качестве исходных веществ функциональные производные соединений формулы (I) можно получать обычными способами, которые описываются, например, в указанных стандартных работах и патентной заявке, например, путем взаимодействия соединений, которые соответствуют формулам (II) и (III), причем, однако, по меньшей мере одно из этих соединений содержит защитную груп пу вместо Н-атома. Высвобождение соединений формулы (I) из их функциональных производных – в зави симости от используемой защитной группы – осуществляют, например, с помощью сильных кислот, целесообразно с помощью трифторуксусной кислоты или хлорной кислоты, однако, также с помощью других сильных неорганических кислот, как соляная кислота, или серная кислота, сильных органических карбоновых кислот, как трихлоруксусная кислота, или сульфокислот, как бензол- или п-толуолсульфо кислота. Присутствие дополнительного инертного растворителя возможно, но не всегда требуется. В качестве инертных растворителей предпочти тельно пригодны органические, например, карбоновые, каислоты, как уксусная кислота; простые эфиры, как тетрагидрофуран (ТГФ) или диоксан; амиды, как диметилформамид (ДМФ); га логенированные углеводороды, как дихлорметан; далее, также спирты, как метанол, этанол или изопропанол, а также вода. Далее, принимают во внимание смеси вышеуказанных растворителей. Трифторуксусную кислоту предпочтительно применяют в избытке без другого растворите ля, хлорную кислоту применяют в фор ме смеси из уксусной кислоты и 70%-ной хлорной кислоты в соотношении 9:1. Температуры реакции отщепления целесообразно составляют примерно 0: примерно 50оС; предпочтительно работают в температур ном интервале 15–30оС (комнатная температура). ВОС-груп пу можно отщеплять, например, предпочтительно с помощью 40%-ной трифторуксусной кислоты в дихлорметане или с помощью примерно 3–5 н HCl в диоксане при 15–60оС; FМОС-груп пу – с помощью примерно 5–20%-ного раствора диметиламина, диэтиламина или пиперидина в ДМФ при 15–50оС. Отщепление DNPгруп пы осуществляли, например, также с помощью примерно 3–10%-ного раствора 2-меркаптоэтанола в смеси ДМФ с водой при 15–30оС. Гидрогенолитически удаляемые защитные груп пы (например, ВОМ, CBZ или бензил) можно отщеплять, например, путем обработки водородом в присутствии катализатора (например, катализатора на основе благородного металла, как палладий, целесообразно на носителе, как уголь). В качестве растворителей при этом пригодны вышеуказанные, в особенности, например, спирты, как метанол, или этанол, или амиды, как ДМФ. Гидрогенолиз, как правило, осуществляют при температуре примерно 0–100оС и давлениях примерно 1–200 бар, предпочтительно при 20–30оС и давлении 1–10 бар. Гидрогенолиз CBZ-группы хорошо протекает, например, на 5–10%-ном палладии-на-угле в метаноле при 20–30оС. Основа ние формулы (I), далее, с помощью кислоты можно переводить в соответствующую соль присоединения кислоты. Для это го взаимодействия применяют кислоты, кото рые дают физиологи чески приемлемые соли. Так, можно применять неорганические кислоты, например, серную кислоту, азотную кислоту; га логенво дородные кислоты, как соляная кислота или бро моводородная кислота; фосфор ные кислоты, как ортофосфор ная кислота; сульфа миновую кислоту; далее, орга нические кислоты, в особенности алифа тические, алициклические, аралифа ти ческие, ароматические или гетероциклические одно- или многоосновные карбоновые, суль фо новые или серные кислоты, например, как муравьиная кислота, уксусная кислота, пропионовая кислота, пивалиновая кислота, диэти лук сусная кислота, малоновая кислота, янтар ная кислота, пимелиновая кислота, фумаровая кислота, ма леиновая кислота, молочная кислота, вин ная кислота, яб лочная кислота, бен зойная кислота, са лициловая кислота, 2- или 3-фе нил-пропионовая кислота, ли монная кислота, глюконовая кислота, аскорбиновая кислота, никоти новая кислота, изо никоти новая кислота, метан- или этан -суль фо кислота, этандисуль фо кислота, 2-гидрокси-этан сульфо кислота, бензолсульфо кислота, п-толуолсульфо кислота, нафталин-моно- и дисуль фокислоты, ла урилсерная кислота. Соединения формулы (I) и и х фи зиологически приемлемые соли можно применять для получения фармацевтических композиций, в частности нехи мическим путем. При этом их вместе по меньшей мере с одним твердым, жидким и/или полужидким носителем или вспомога тельным веществом и, в случае необхо димости, в комбинации с одним или несколькими други ми биологически активными веществами можно доводить до пригодной дозировочной формы. Предметом изобрете ния, далее, являются средства, в особенности фар мацевтические композиции, содержащие по меньшей мере одно сое 5 39118 динение формулы (I) и/или одну из его физиологически приемлемых солей. Эти композиции можно применять в качестве лекарственных средств в медицине или ветеринарии. В качестве носите лей принимают во внимание органические или неорганические вещества, которые пригодны для кишечного (например, орального), парентерального или топического введения и не реаги руют с новыми соединениями, например, воду, растительные масла, бензиловые спирты, полиэтиленгликоли, триацетат гли церина, желати ну, углеводы, как лактоза или крахмал, стеарат магния, тальк, ланолин, вазелин. Для орального применения служат в особенности таблетки, драже, капсулы, сиропы, соки или капли; для ректального применения служат свечи; для парентерального применения служат растворы, предпочтительно масляные или водные растворы, далее, суспензии, эмульсии или импланта ты; для топического применения служат мази, кремы, пасты, лосьоны, гели, пульверизуемые препараты, пены, аэрозоли, растворы (например, растворы в спиртах, как этанол или изопропанол, ацетонитриле, ДМФ, ди метилацетамиде, пропан-1,2-диоле или их смесях друг с другом и/или с водой) или пудры. Новые соединения можно также лиофи лизировать и полученные лиофи лизаты применять, например, для приготовления препаратов для инъекций. В особенности для топического применения принимают во внимание также липосомальные композиции. Указанные композиции могут быть стерилизова ны и/или могут со держать вспомогательные вещества, как вещества, придающие скользкость; консерванты, ста билизато ры и/или смачиватели, эмульгаторы, соли для влияния на осмотическое давление, буферные вещества, красители, вкусовые вещества и/или аромати зирующие ве щества. Если желательно, они могут со держать также одно или несколько других био логически активных веществ, например, один или несколько витаминов. Соединения формулы (I) и и х фи зиологически приемлемые соли можно вводить людям или животным, в частности млекопитающим, как обезьяны, собаки, кошки, крысы или мыши, и применять при терапии человеческого или животного организма, а также при борьбе с заболева ниями, в особенности при лечении и/или профи лакти ке нарушений сердечно-сосудистой системы. Поэтому они пригодны для лечения аритмий, в особенности когда они вызываются недостатком кислорода, стенокардий, инфарктов, ише мий нервной системы, как, например, инсульт или отек головного мозга, шоковых состояний, и для профилактики. Вещества, далее, можно использовать в качестве терапевти ческих средств при заболеваниях, при которых играют роль пролиферации клеток, как артериосклерозы, диабетические поздние осложнения, опухолевые заболевания, фиброзы, а также гипертрофии и ги перплазии орга нов, в особенности при заболеваниях простаты. При этом предлагаемые согласно изобретению вещества вво дят по аналогии с известными антиаритмическими средствами, как, например, Ап риндин, предпочтительно в дозах примерно 0,01–5 мг, в особенности 0,02–0,5 мг на дозиро вочную единицу. С уточная доза предпочти тельно составляет примерно 0,0001–0,1, в особенности 0,0003–0,01 мг/кг веса тела. Специальная доза для каждого определенного пациента, однако, зависит от са мых различных факторов, например, от эффективности используемого специального соединения, от возраста, веса тела, общего состояния здоровья, пола, стоимости, момента и пути введения, от скорости выделения, комбинации лекарственных веществ и тя жести соответствующего заболевания, которое имеет значение для терапии. Предпочтительно оральное применение. В нижеследующих примерах "обычная обработка" обозначает: Добавляют, если необхо димо, воду; экстрагируют ор ганическим растворителем, как этилацетат; ор ганическую фазу о тделяют, сушат над сульфа том натрия, отфильтровывают, выпаривают и очищают путем хроматографии и/или кристаллизации. Пример 1. Раствор 1,4 г мети лового эфира 2-метил-4этокси-5-метилсульфо нил- бензойной кислоты (получают путем взаимодействия 2-метил-4-хлор-5метилсульфо нил-бензойной кислоты с этилатом натрия и последующей этерификации до сложного эфи ра) и 1,5 г гуанидина в 50 мл метанола кипятят в те чение 5 часов и после это го растворитель удаляют. Остаток обрабатывают во дой, образующиеся кристаллы отсасывают и обрабатывают разбавленным раствором гидроксида натрия. Твердый остаток отфильтровывают, перекристаллизовывают из этанола и получают N-диаминометилен-2метил-4-этокси-5-метилсульфо нил-бензамид. Т. пл. = 201–203оС. Аналогичным образом, путем введения во взаимодействие гуанидина с метиловым эфиром 2-этил-4-этокси-5-метилсульфо нил-бензойной кислоты получают Nдиаминометилен-2-этил-4-этокси-5- метилсульфонил-бензамид; с метиловым эфиром 2-метил-4-изопропокси-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-метил-4-изопропокси5-метилсульфо нил-бензамид; т.пл. 185–188 оС; с мети ловым эфиром 2-метил-4-трет.-бутокси-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-метил-4-трет.-бутокси5-метилсульфо нил-бензамид, т. пл. 205–207 оС; с метиловым эфиром 2-этил-4-бутокси-5-метилсульфо нил-бензойной кислоты получают Nдиаминометилен-2-метил-4-бутокси-5-метилсульфо нил-бензамид; с метиловым эфиром 2-метил-4(2-бутокси)5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-метил-4-(2-бутокси)-5-метилсульфо нил-бензамид; с метиловым эфиром 2-метил-4-циклопентокси-5-метилсульфо нил- бензойной кислот получают N-диаминометилен-2-метил-4-циклопентокси-5-метилсульфонил-бензамид; т. пл. 238–241оС; с метиловым эфиром 2-метил-4-(2-пентокси)-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-метил-4-(2-пентокси)-5метилсульфо нил-бензамид; с метиловым эфиром 2-метил-4-(3-пентокси)-5-метилсульфонил-бензойной кислоты полу 6 39118 чают N-диаминометилен-2-метил-4-(3-пентокси)-5метилсульфо нил-бензамид; с метиловым эфиром 2-метил-4-циклогексилокси-5-метилсуль фонил- бензойной кислоты получают N-диаминометилен-2-метил-4-циклогексилокси-5-метилсуль фонил-бензамид, т.пл. 224– 226оС; с метиловым эфиром 2-метил-4-циклопропокси-5-метилсульфо нил- бензойной кислоты получают N-диаминометилен-2-метил-4-циклопропокси-5-метилсульфо нил-бензамид; с мети ловым эфиром 2-этил-4-метокси-5метилсульфо нил-бензойной кислоты получают Nдиаминометилен-2-этил-4-метокси-5-метилсульфо нил-бензамид, т. пл. 192–195оС; с метиловым эфиром 2-этил-4-изопропокси5-метилсульфо нил- бензойной кислоты получают N-диаминометилен-2-этил-4-изопропокси-5-метилсульфо нил-бензамид; с мети ловым эфиром 2-этил-4-пропокси-5метилсульфо нил-бензойной кислоты получают Nдиаминометилен-2-этил-4-пропокси-5-метилсульфо нил-бензамид; с метиловым эфиром 2-этил-4-бутокси-5-метилсульфо нил-бензойной кислоты получают Nдиаминометилен-2-этил-4-бутокси-5-метилсульфо-нил-бензамид; с метиловым эфиром 2-этил-4-(2-бутокси)-5метилсульфо нил- бензойной кислоты получают Nдиаминометилен-2-этил-4-(2-бутокси)-5-метилсульфо нил-бензамид; с мети ловым эфи ром 2-этил-4-трет.-бутокси-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-метил-4-трет.-бутокси5-метилсульфо нил-бензамид; с метиловым эфиром 2-этил-4-пентокси-5метилсульфо нил-бензойной кислоты получают Nдиаминометилен-2-этил-4-пентокси-5-метилсульфо нил-бензамид; с метиловым эфиром 2-этил-4-(2-пентокси)5-метилсульфо нил- бензойной кислоты получают N-диаминометилен-2-этил-4-(2-пентокси)-5-метилсульфо нил-бензамид; с метиловым эфиром 2-этил-4-(3-пентокси)5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-этил-4-(3-пентокси)-5-метилсульфо нил-бензамид; с мети ловым эфиром 2-этил-4-циклопропокси-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-этил-4- циклопропокси5-метилсульфо нил-бензамид; с метиловым эфиром 2-этил-4-циклопентокси-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-этил-4-циклопентокси5-метилсульфо нил-бензамид; с метиловым эфиром 2-этил-4-циклогексилокси-5-метилсуль фонил-бензойной кислоты получают N-диаминометилен-2-этил-4-циклогексил5-метилсульфо нил-бензамид. Пример 2. 3,0 г N-диаминометилен-2-этил-4-фтор-5метилсульфо нил-бензамида [получают путем взаимодействия метилового эфи ра 2'-этил-4фтор-5-метилсульфонил-бензойной кислоты с гуанидином] и 1,5 г метилата натрия в 25 мл метанола кипятят в те чение 16 ч. После обычной обработки получают N-диаминометилен-2-этил-4-ме токси-5-метилсульфо нил-бензамид, т. пл. 192– 195оС. Аналогичным образом, путем взаимодействия мети лата натрия с N-диаминометилен-2-метил-4-хлор-5-метилсульфо нил-бензамидом получают N-диаминометилен-2-метил-4-метокси-5-метилсульфо нил- бензамид. Т. пл. 189–190оС. Пример 3. 700 мг N-диаминометилен-2-этил-4-метокси5-метилсульфо нил-бензамида (получают согласно примеру 2) суспендируют в 50 мл воды и при перемеши вании смешивают с 1,8 мл 1 н HCl. После отфильтровывания и лиофи лизации получают Nдиаминометилен-2-этил-4-метокси-5-метилсульфонил-бензамид-гидрохлорид. Т. пл. 217–220оС. Аналогичным образом, из свободного основания получают: N-диаминометилен-2-метил-4-этокси-5-метилсульфо нил-бензамид-гидрохлорид; т. пл. 218– 219оС; N-диаминометилен-2-метил-4-изопропокси5-метилсуль фонил-бензамид-гидрохлорид; т. пл. 219–220оС; N-диаминометилен-2-метил-4-циклопентокси-5-метилсуль фонил-бензамид-гидрохлорид, т. пл. >250оС; N-диа миномети лен-2-ме тил-4-цик ло гексилокси-5-метилсульфо нил-бензамид-гидрохлорид, т. пл. 185–187оС; N-диаминометилен-2-метил-4-бензилокси-5метилсульфо нил-бензамид-гидрохлорид; аморфный; N-диаминометилен-2-метил-4-метокси-5-метилсульфонил-бензамид-гидрохлорид, аморфный. Пример 4. 1,8 г 2-метил-4-фенокси-5-метилсульфо нилбензойной кислоты (получают путем взаимодействия 2-метил-4-хлор-5-метилсульфо нил- бензойной кислоты с фе нолятом натрия при 180оС) вместе с 25 мл SOCl2 кипятят в те чение 3-х часов. Прозрачный раствор концентрируют и остаток растворяют в 20 мл этиленгликольдиметилового простого эфи ра. Эту реакционную смесь медленно при комнатной температуре добавляют к 2,5 г гуанидина, растворенным в 30 мл этиленгликольдимети лового простого эфира, и дополнительно перемешивают три ча са. Затем раствор концентрируют наполовину, смешивают с 50 мл воды, подкисляют и обрабаты вают как обычно. Получают N-диаминомети лен-2-метил-4-фе нокси-5-метилсуль фо нилбензамид. Т. пл. 248–250оС. После суспендирования основа ния в 50 мл воды и обработки с помощью 1,8 мл 1 н HCl при перемеши вании, получают, после фильтрации и лиофи лизации, N-диаминометилен-2-метил-4-фенокси-5-метилсульфо нил-бензамид в виде гидрохлорида. Т. пл. >250оС. Пример 5. Аналогично примеру 4 путем взаимодействия 2-метил-4-(2-хлорфе нокси)-5-метилсульфонил-бензойной кислоты (получают путем взаимодействия 2-метил-4-хлор-5-метилсульфонил- бензойной кислоты с 2-хлор-фенолятом натрия при 180оС) с SOCl2 и последующе го взаимодействия с гуа нидином получают N-диаминометилен-2-метил-4-(2-хлор-фе нокси)-5-метилсуль фо нилбензамид, т. пл. 188–191оС. 7 39118 Аналогичным образом при использовании 2-метил-4-(3-хлор-фенокси)-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-метил-4-(3-хлор-фенокси)-5-метилсуль фонил-бензамид, т. пл. 205–207оС; 2-метил-4-(4-хлор-фенокси)-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-метил-4-(4-хлор-фенокси)-5-метилсуль фонил-бензамид, т. пл. 219–221оС; 2-метил-4-(2,4-дихлор-фенокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-метил-4-(2,4-дихлор-фенокси)-5-метилсульфо нил-бензамид; 2-метил-4-(2-фтор-фенокси)-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-метил-4-(2-фтор-фе нокси)-5-метилсульфонил-бензамид; 2-метил-4-(3-фтор-фенокси)-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-метил-4-(3-фтор-фе нокси)-5-метилсульфонил-бензамид; 2-метил-4-(4-фтор-фенокси)-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-метил-4-(4-фтор-фе нокси)-5-метилсульфонил-бензамид; 2-метил-4-(2,4-дифтор-фенокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-метил-4-(2,4-дифтор-фе нокси)-5-метилсульфо нил-бензамид; 2-метил-4-бензилокси-5-метилсуль фонилбензойной кислоты получают N-диаминометилен2-метил-4-бензилокси-5-метилсуль фонил-бензамид, т. пл. 212–217оС; 2-метил-4-(3-метокси-фенокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-метил-4-(3-метокси-фенокси)-5-метилсульфо нил-бензамид; 2-метил-4-(4-метокси-фенокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-метил-4-(4-метокси-фенокси)-5-метилсульфо нил-бензамид; 2-метил-4-(2,4-диметокси-фе нокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-метил-4-(2,4-диметокси-фенокси)-5метилсульфо нил-бензамид; 2-метил-4-(2-метокси-фенокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-метил-4-(2-метокси-фенокси)-5-метилсульфо нил-бензамид; 2-метил-4-(3-трифторметил-фенокси)-5-метилсульфо нил-бензойной кислоты получают Nдиаминометилен-2-метил-4-(3-трифторметил-фенокси)-5-метилсульфо нил-бензамид; 2-метил-4-(4-трифторметил-фенокси)-5-метилсульфо нил-бензойной кислоты получают Nдиаминометилен-2-метил-4-(4-трифторметил-фенокси)-5-метилсульфо нил-бензамид; 2-метил-4-(2-трифторметил-фенокси)-5-метилсульфо нил-бензойной кислоты получают Nдиаминометилен-2-метил-4-(2-трифторметил-фенокси)-5-метилсульфо нил-бензамид; 2-метил-4-(3-метил-фе нокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-метил-4-(3-метил-фенокси)-5-метилсульфо нил-бензамид; 2-метил-4-(4-метил-фе нокси)-5-метилсульфо нил-бензойной кислоты получают N-диамино метилен-2-метил-4-(4-метил-фенокси)-5-метилсульфо нил-бензамид; 2-метил-4-(2,4-диметил-фе нокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-метил-4-(2,4-диметил-фенокси)-5-метилсульфо нил-бензамид; 2-метил-4-(2-метил-фе нокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминомети лен-2-метил-4-(2-ме тил-фе нокси)-5-ме тилсульфо нил-бензамид. Пример 6. Аналогично примеру 4, п утем взаимодействия 2-этил-4-(2-хлор-фенокси)-5-метилсуль фонилбензойной кислоты (получают путем взаимодействия 2-этил-4-хлор-5-метилсульфо нил-бензойной кислоты с 2-хлор-фенолятом натрия при 180оС) с SOCl2 и последующе го взаимодействия с гуанидином получают N-диаминометилен-2-этил-4-(2хлор-фе нокси)-5-метилсульфо нил-бензамид. Аналогичным образом при использовании 2-этил-4-фенокси-5-метилсуль фонил-бензойной кислоты получают N-диаминометилен-2этил-4-фе нокси-5-метилсульфонил-бензамид; 2-этил-4-(3-хлор-фенокси)-5-метилсуль фонил-бензойной кислоты получают N-диаминометилен-2-этил-4-(3-хлор-фенокси)-5-метилсульфонилбензамид; 2-этил-4-(4-хлор-фенокси)-5-метилсуль фонил-бензойной кислоты получают N-диаминометилен-2-этил-4-(4-хлор-фенокси)-5-метилсульфонилбензамид; 2-этил-4-(2,4-дихлор-фенокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-этил-4-(2,4-дихлор-фенокси)-5-метилсульфо нил-бензамид; 2-этил-4-(2-фтор-фе нокси)-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-этил-4-(2-фтор-фенокси)-5-метилсульфонил-бензамид; 2-этил-4-(3-фтор-фе нокси)-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-этил-4-(3-фтор-фенокси)-5-метилсульфонил-бензамид; 2-этил-4-(4-фтор-фе нокси)-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-этил-4-(4-фтор-фенокси)-5-метилсульфонил-бензамид; 2-этил-4-(2,4-дифтор-фенокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-этил-4-(2,4-дифтор-фе нокси)-5-метилсульфо нил-бензамид; 2-этил-4-бензилокси-5-метилсульфонил-бензойной кислоты получают N-диаминометилен2-этил-4-бен зилокси-5-ме тилсульфо нил-бен замид; 2-этил-4-(3-метокси-фенокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-этил-4-(3-метокси-фенокси)-5-метилсульфо нил-бензамид; 2-этил-4-(4-метокси-фенокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-этил-4-(4-метокси-фенокси)-5-метилсульфо нил-бензамид; 2-этил-4-(2,4-диметокси-фе нокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-этил-4-(2,4-диметокси-фенокси)-5метилсульфо нил-бензамид; 8 39118 2-этил-4-(2-метокси-фенокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-этил-4-(2-метокси-фенокси)-5-метилсульфо нил-бензамид; 2-этил-4-(3-трифторметил-фе нокси)-5-метилсульфо нил-бензойной кислоты получают Nдиаминометилен-2-этил-4-(3-трифторметил-фенокси)-5-метилсульфо нил-бензамид; 2-этил-4-(4-трифторметил-фе нокси)-5-метилсульфо нил-бензойной кислоты получают Nдиаминометилен-2-этил-4-(4-трифторметил-фенокси)-5-метилсульфо нил-бензамид; 2-этил-4-(2-трифторметил-фе нокси)-5-метилсульфо нил-бензойной кислоты получают Nдиаминометилен-2-этил-4-(2-трифторметил-фенокси)-5-метилсульфо нил-бензамид; 2-этил-4-(3-метил-фе нокси)-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-этил-4-(3-метил-фенокси)-5-метилсуль фонил-бензамид; 2-этил-4-(4-метил-фе нокси)-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-этил-4-(4-метил-фенокси)-5-метилсуль фонил-бензамид; 2-этил-4-(2,4-диметил-фе нокси)-5-метилсульфо нил-бензойной кислоты получают N-диаминометилен-2-этил-4-(2,4-диметил-фе нокси)-5-метил-сульфо нил-бензамид; 2-этил-4-(2-метил-фе нокси)-5-метилсульфонил-бензойной кислоты получают N-диаминометилен-2-этил-4-(2-метил-фенокси)-5-метилсуль фонил-бензамид. Пример 7. 600 мг N-диаминометилен-2-метил-4-метокси-5-метилсульфонил- бензамида (получают согласно примеру 2) в 80 мл пиридина вместе с 1 г пиридин гидрохлорида кипятят в течение 3-х часов. Охлаждают, выпаривают, обрабаты вают как обычно и получают N-диаминомети лен-2-метил-4гидрокси-5-метил-сульфо нил-бензамид, т. пл. >260оС. Пример 8. 1,1 г N-диаминометилен-2-этил-4-бензилокси-5-метилсульфонил-бензамида (получают согласно примеру 6) растворяют в 30 мл то луо ла и при комнатной температуре в течение часа обрабатывают га зообразным водородом (р=1 атм) при каталитическом воздействии 150 мг палладия-наугле (содержание палладия = 1%). Затем реакционную смесь отфильтровывают и после обычной обработки получают N-диаминометилен-2этил-4-гидрокси-5-метилсульфо нил- бензамид. Пример 9. Аналогично примеру 3, путем воздействия с 1 н. раствором метансульфоната получают следующие метансуль фонаты: N-диаминометилен-2-метил-4-этокси-5-метилсульфо нил-бензамид- метансульфо нат; N-диаминометилен-2-метил-4-изопрококси5-метилсульфо нил-бензамид- метансуль фонат; N-диаминометилен-2-метил-4-циклопентокси-5-метилсульфонил-бензамид- метансульфо нат; N-диаминометилен-2-метил-4-циклогексилокси-5-метилсуль фонил-бензамид-метансульфонат; N-диаминометилен-2-метил-4-бензилокси-5метилсульфо нил-бензамид- метансульфо нат; N-диаминометилен-2-метил-4-фенокси-5-ме-тилсульфонил-бензамид-метансульфо нат, т.пл. 260–262оС; N-диаминометилен-2-метил-4-трет.-бутокси5-метилсульфо нил-бензамид-метансульфо нат, т.пл. 164–167оС; N-диаминометилен-2-метил-4-(3-хлорфе нокси)-5-метилсульфонил-бензамид-метансульфонат, т.пл. 144оС; N-диаминометилен-2-метил-4-гидрокси-5метилсульфо нил-бензамид-метансуль фонат, аморфный; N-диаминометилен-2-метил-4-(4-хлорфе нокси)-5-метилсульфонил-бензамид-метансульфонат, т.пл. 260оС; N-диаминометилен-2-метил-4-(2-хлорфе нокси)-5-метилсульфонил-бензамид-метансульфонат, т.пл. 217–219оС. Пример 10. Аналогично примеру 1, п утем взаимодействия метилового эфи ра 2- метил-4-(3-пропен-1-ил)5-метилсульфо нил-бензойной кислоты с гуанидином получают N-диаминометилен-2-метил-4-(3пропен-1-ил)- 5-метилсульфонил-бензамид, т. пл. 207–209оС. Соответствующий метансуль фонат получают по аналогии с примером 9 и он плавится при 187–189оС. Нижеследующие примеры относятся к фармацевтическим композициям: Пример А: Стеклянные пузырьки с препаратом для инъекции В растворе 100 г биологически активного вещества формулы (I) и 5 г динатрийгидрофосфата в 3 л дважды перегнанной воды с помощью 2 н соляной кислоты устанавливают рН = 6,5, раствор стерильно фильтруют, заполняют им стеклянные пузырьки (емкости) для препарата для инъекции, лиофи лизируют в сте рильных условиях и стерильно закрывают. Каждый стеклянный пузырек с препаратом для инъекции содержит 5 мг биологически активного ве щества. Пример Б: Свечи Расплавляют смесь 20 г биологически активного вещества формулы (I) со 100 г соевого лецитина и 1400 г масла какао, разливают в формы и оставляют охлаждаться. Каждая свеча содержит 20 мг биологически активного вещества. Пример В: Раствор Готовя т раствор из 1 г биологически активного ве щества фор мулы (I), 9,38 г NaH 2PO4 x x 2H 2O, 28,48 г Na 2HPO4 · 12H2 O и 0,1 г бен зальконий хлорида в 940 мл дважды перегнанной воды. Устанавливают рН = 6,8, до ли вают до общего объема 1 литр и сте рилизуют п утем облучения. Это т раствор можно применять в фор ме глаз ных ка пель. Пример Г: Ма зь 500 мг биологи чески активного вещества формулы (I) смеши вают с 99,5 г ва зелина при асептических условиях. Пример Д: Таблетки 9 39118 Смесь 1 кг биологически активного вещества формулы (I), 4 кг лактозы, 1,2 кг картофельного крахмала, 0,2 кг талька и 0,1 кг стеарата магния обычным образом прессуют в таблетки, таким образом, что каждая таблетка содержит 10 мг биологически активного ве щества. Пример Е: Драже Аналогично примеру Д, прессуют таблетки, на которые затем обычным образом наносят покрытие из сахарозы, картофельного крахмала, талька, траганта и красите ля. Пример Ж: Капсулы с лекарством 2 кг биологически активного вещества формулы (I) обычным образом наносят в капсулы из твердой желатины, так, что каждая капсула содержит 20 мг биологически активного ве щества. Пример З: Ампулы Раствор 1 кг биологически активного вещества формулы (I) в 60 л дважды перегнанной воды стерильно фильтруют, заполняют им ампулы, лиофилизируют в стерильных условиях и стерильно закрывают. Каждая ампула содержит 10 мг биологически активного ве щества. Тираж 50 екз. Відкрите акціонерне товариство «Патент» Україна, 88000, м. Ужгород, вул. Гагаріна, 101 (03122) 3 – 72 – 89 (03122) 2 – 57 – 03 10
ДивитисяДодаткова інформація
Назва патенту англійськоюBenzoylguanidine derivatives, method for preparation thereof, pharmaceutical composition and method for preparation thereof
Автори англійськоюGericke Rolf, Dorsch Dieter, Baumgarth Manfred, Minck Klaus-Otto, Bayer Norbert
Назва патенту російськоюПроизводные бензоилгуанидина, способ их получения, фармацевтическая композиция и способ ее получения
Автори російськоюГерике Рольф, Дорш Дитер, Баумгарт Манфред, Минк Клаус-Отто, Байер Норберт
МПК / Мітки
МПК: A61P 9/06, A61P 9/00, C07C 317/44, C07C 315/00, C07C 317/50, A61P 9/08, A61K 31/165, A61P 9/10
Мітки: спосіб, отримання, бензоїлгуанідину, похідні, композиція, фармацевтична
Код посилання
<a href="https://ua.patents.su/10-39118-pokhidni-benzolguanidinu-sposib-kh-otrimannya-farmacevtichna-kompoziciya-ta-sposib-otrimannya.html" target="_blank" rel="follow" title="База патентів України">Похідні бензоїлгуанідину, спосіб їх отримання, фармацевтична композиція та спосіб її отримання</a>
Попередній патент: Спосіб лікування цитомегаловірусної інфекції у жінок та дітей
Наступний патент: Плоский зрівноважувальний канат
Випадковий патент: Сполуки оксабіспідину, що корисні при лікуванні серцевих аритмій