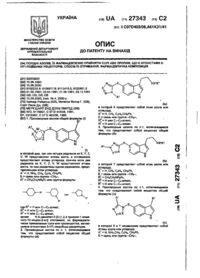
Нуклеозидмонофосфатні похідні, спосіб їх отримання та фармацевтична композиція, що має протипухлинну активність
Номер патенту: 45339
Опубліковано: 15.04.2002
Автори: ХЕРРМАНН Дітер, ОПІТЦ Ханс-Георг, ЦІЛЬХ Харальд, МЕРТЕНС Альфред
Формула / Реферат
1. Нуклеозидмонофосфатные производные формулы I
в которой
R1 представляет собой линейную или разветвленную насыщенную алкильную цепь, содержащую 1-20 атомов углерода,
R2 представляет особой линейную или разветвленную насыщенную алкильную цепь, содержащую 1-20 атомов углерода,
R3 представляет собой водород или гидроксильную группу,
R4 представляет собой гидроксильную группу,
R5 представляет собой водород или гидроксильную группу,
Χ представляет собой атом серы, сульфинильную или сульфонильную группу,
Υ представляет собой атом кислорода,
В представляет собой пуриновое или пиримидиновое основание формулы IIIа или IIIг
в которых
R6 представляет собой водород или галоген,
R6' представляет собой атом водорода,
R9 представляет собой водород,
R10 представляет собой водород, меркаптогруппу, (С1-С6)-алкилмеркаптогрупу,
при условии, что по крайней мере один из остатков R3 или R5 представляет собой водород, их таутомеры, их оптически активные формы и рацемические смеси, или их физиологически приемлемые соли неорганических и органических кислот или оснований.
2. Нуклеозидмонофосфатные производные формулы I по п. 1, отличающиеся тем, что R1 представляет собой линейную (С8-С15)-алкильную группу.
3. Нуклеозидмонофосфатные производные формулы I по п. 1 или 2, отличающиеся тем, что R2 представляет собой линейную (С8-С15)-алкильную группу.
4. Нуклеозидмонофосфатные производные формулы I по любому из пп. 1-3, отличающиеся тем, что R5 представляет собой водород.
5. Нуклеозидмонофосфатные производные формулы I по любому из пп. 1-4, отличающиеся тем, что R3 представляет собой гидроксильную группу.
6. Нуклеозидмонофосфатные производные формулы I по любому из пп. 1-5, отличающиеся тем, что R6 представляет собой атом водорода.
7. Нуклеозидмонофосфатные производные формулы І по любому из пп. 1-6, отличающиеся тем, что R10 представляет собой атом водорода или (С1-С6)-алкилмеркаптогруппу.
8. Нуклеозидмонофосфатные производные формулы I по любому из пп. 1-7, отличающиеся тем, что
R1 представляет собой линейную (С9-С13)-алкильную группу,
R2 представляет собой линейную (С8-С14)-алкильную группу,
R3 представляет собой гидроксильную группу,
R4 представляет собой гидроксильную группу,
R5 представляет собой водород,
R6 представляет собой водород или атом фтора, хлора или брома,
R6' представлет собой атом водорода,
R10 представляет собой водород, меркаптогруппу, метилмеркаптогруппу, этилмеркаптогруппу, бутилмеркаптогруппу, гексилмеркаптогруппу.
9. Нуклеозидмонофосфатные производные формулы I по любому из пп. 1-8, отличающиеся тем, что нуклеозидную часть выбирают из группы, в которую входят 6-меркаптопурин-9--D-рибофуранозид, 5-фторуридин, 5-хлоруридин, 6-метилмеркаптопурин-9--D-рибофуранозид,2'-дезокси-5-фторуридин.
10. Нуклеозидмонофосфатное производное формулы I по любому из пп. 1-9, отличающееся тем, что оно является (3-додецилмеркапто-2-децилокси)пропиловым эфиром (5-фторуридин)-5'-фосфорной кислоты или его солью.
11. Нуклеозидмонофосфатные производные формулы по любому из пп. 1-10, обладающие противоопухолевой активностью.
12. Способ получения нуклеозидмонофосфатных производных формулы 1 по любому из пп. 1-11, отличающийся тем, что вводят во взаимодействие соединение общей формулы V
в которой R1, R2, Χ, Υ имеют вышеуказанные значения,
с соединением общей формулы VI
в которой R1, R2, R5 и В имеют вышеуказанные значения,
в присутствии активного хлорангидрида, такого, как хлорангидрид 2,4,6-триизопропилбензолсульфоновой кислоты, и азотистого основания, например, пиридина или лутидина, в инертном растворителе, таком как толуол, или непосредственно в безводном пиридине.
13. Фармацевтическая композиция, обладающая противоопухолевой активностью, отличающаяся тем, что содержит по крайней мере одно соединение формулы 1 по любому из пп. 1-11 в эффективном количестве, а также фармацевтические адъюванты или носители.
Текст
1 Нуклеозидмонофосфатные производные формулы I D! v К A Э 2 _ , п„ t-H2 Шг н 2 с—о—Р—о—сн 2 он I Y& в которой R1 представляет собой линейную или разветвленную насыщенную алкильную цепь, содержащую 120 атомов углерода, R2 представляет особой линейную или разветвленную насыщенную алкильную цепь, содержащую 1-20 атомов углерода, R представляет собой водород или гидроксильную группу, R4 представляет собой гидроксильную группу, R5 представляет собой водород или гидроксильную группу, X представляет собой атом серы, сульфинильную или сульфонильную группу, Y представляет собой атом кислорода, В представляет собой пуриновое или пиримидиновое основание формулы Ilia или Шг в которых R6 представляет собой водород или галоген, R6' представляет собой атом водорода, R9 представляет собой водород, R10 представляет собой водород, меркаптогруппу, (Сі-Сє)-алкилмеркаптогрупу, при условии, что по крайней мере один из остатков R3 или R5 представляет собой водород, их таутомеры, их оптически активные формы и рацемические смеси, или их физиологически приемлемые соли неорганических и органических кислот или оснований 2 Нуклеозидмонофосфатные производные формулы І по п 1, отличающиеся тем, что R1 представляет собой линейную (С8-Сі5)-алкильную группу 3 Нуклеозидмонофосфатные производные формулы І по п 1 или 2, отличающиеся тем, что R2 представляет собой линейную (С8-Сі5)-алкильную группу 4 Нуклеозидмонофосфатные производные формулы I по любому из пп 1-3, отличающиеся тем, что R5 представляет собой водород 5 Нуклеозидмонофосфатные производные формулы I по любому из пп 1-4, отличающиеся тем, что R3 представляет собой гидроксильную группу 6 Нуклеозидмонофосфатные производные фор О го го ю 45339 мулы I по любому из пп 1-5, отличающиеся тем, производных формулы 1 по любому из пп 1-11, что R6 представляет собой атом водорода отличающийся тем, что вводят во взаимодейст7 Нуклеозидмонофосфатные производные форвие соединение общей формулы V мулы I по любому из пп 1-6, отличающиеся тем, RX что R представляет собой атом водорода или (Сі-Сє)-ал кил меркаптогруппу 8 Нуклеозидмонофосфатные производные формулы I по любому из пп 1-7, отличающиеся тем, -p—он С что он R1 представляет собой линейную (Сд-С-із)алкильную группу, R2 представляет собой линейную (Сз-Си)в которой R1, R2, X, Y имеют вышеуказанные знаалкильную группу, чения, R3 представляет собой гидроксильную группу, с соединением общей формулы VI R4 представляет собой гидроксильную группу, 5 но—сн2 R представляет собой водород, 6 R представляет собой водород или атом фтора, хлора или брома, R6' представлет собой атом водорода, R10 представляет собой водород, меркаптогруппу, метил меркаптогруппу, этил меркаптогруппу, бутил меркаптогруппу, гексил меркаптогруппу VI 9 Нуклеозидмонофосфатные производные форв которой R1, R2, R5 и В имеют вышеуказанные мулы I по любому из пп 1-8, отличающиеся тем, значения, что нуклеозидную часть выбирают из группы, в в присутствии активного хлорангидрида, такого, которую входят 6-меркаптопурин-9- ft -Dкак хлорангидрид 2,4,6рибофуранозид, 5-фторуридин, 5-хлоруридин, 6триизопропилбензолсульфоновой кислоты, и азометилмеркаптопурин-9- ft -О-рибофуранозид,2'тистого основания, например, пиридина или лутидина, в инертном растворителе, таком как толуол, дезокси-5-фторуридин или непосредственно в безводном пиридине 10 Нуклеозидмонофосфатное производное фор13 Фармацевтическая композиция, обладающая мулы I по любому из пп 1-9, отличающееся тем, противоопухолевой активностью, отличающаяся что оно является (З-додецилмеркапто-2тем, что содержит по крайней мере одно соединедецилокси)пропиловым эфиром (5-фторуридин)-5'ние формулы 1 по любому из пп 1-11 в эффекфосфорной кислоты или его солью тивном количестве, а также фармацевтические 11 Нуклеозидмонофосфатные производные форадъюванты или носители мулы по любому из пп 1-10, обладающие противоопухолевой активностью 12 Способ получения нуклеозидмонофосфатных Настоящее изобретение относится к новым нуклеозидмонофосфатным производным с остатками липидных сложных эфиров общей формулы в которой R1 может представлять собой линейную или разветвленную, насыщенную или ненасыщенную алкильную цепь, содержащую 1 - 20 атомов углерода, необязательно моно- или полизамещенную галогеном, (Сі-Сб)-алкоксигруппой, (С-і-Сє)алкилмекаптогруппой, (СгСбЭ-алкоксикарбонилом, (СгСб)-алкилсульфинильной или (С-і-Сє)алкилсульфонильной группами, R может представлять собой водород, линейную или разветвленную, насыщенную или ненасыщенную алкильную цепь, содержащую 1 - 20 атомов углерода, необязательно моно- или полизамещенную галогеном, (СгСб)-алкоксигруппой, (Сі-Сє)-алкилмеркаптогруппой, (С-і-Сє)алкокси карбон илом или (С-і-Сє)алкилсульфонильной группой, R3, представляет собой водород, гидроксильную группу, азидогруппу, аминогруппу, цианогруппу или галоген, R4 представляет собой гидроксильную группу, азидогруппу, аминогруппу, цианогруппу или галоген, R5 представляет собой водород, гидроксильную группу, азидогруппу, аминогруппу, цианогруппу или галоген, X представляет собой валентную связь, атом кислорода, атом серы, сульфинильную или сульфонильную группу, Y представляет собой валентную связь, атом кислорода или атом серы, 45339 В представляет собой пуриновое и/или пирикак AZT (азидотимидин) и ddC (2',3'дидезоксицитидин), включающие в свою структуру мидиновое основание формулы III (a - г) остатки сложных эфиров жирных кислот В J Med Chem 33, 1380 (1990), описываются нуклеозидные конъюгаты липидов - простых тиоэфиров - с цитидиндифосфатом, которые обладают противоопухолевой активностью и могут найти применение в онкологии В Chem Pharm Bull 36, 209, (1988), описываются 5'-(3-snфосфатидил)нуклеозиды, обладающие противолейкозной активностью, а также их ферментативный синтез из соответствующих нуклеозидов и фосфохолинов в присутствии фосфолипазы D с активностью трансферазы Подобным образом, в в которых J Med Chem 34, 1408 (1991), описываются нукR может представлять собой водород, аллеотидные конъюгаты, обладающие активностью кильную цепь, содержащую 1 - 6 атомов углерода, против ВИЧ 1, которые замещены метокси- или которая может быть замещена галогеном, алкеэтоксигруппами в sn-положении липидной части В нильную и/или алкинильную группу, содержащую заявке на патент ВОИС 92/03462 описываются 2 - 6 атомов углерода, необязательно замещенконъюгаты тиоэфирных липидов, обладающие ную галогеном, или галоген, противовирусной активностью, в частности, для R6 может представлять собой атом водорода, лечения ВИЧ-инфекций или бензил, или фенилтиогруппу, Соединения настоящего изобретения облаR7 может представлять собой водород, алдают ценными фармакологическими свойствами кильную цепь, содержащую 1 - 6 атомов углерода, В частности, они пригодны для лечения и профикоторая может быть замещена галогеном, или лактики злокачественных опухолей, таких как негалоген, оплазмы, карциномы, саркомы, или лейкозов R8 может представлять собой водород, алКроме того, соединения обнаруживают иммунодекильную цепь, содержащую 1 - 6 атомов углерода, прессивную активность и, следовательно, могут галоген или гидроксильную или аминогруппу, применяться при лечении органоспецифических 9 R может представлять собой водород, амиили системных аутоиммунных заболеваний, таких ногркппу или атом галогена, и как ревматоидный артрит, системная красная вол10 R может представлять собой водород, галочанка, хроническая гомологичная болезнь, рассеген, меркаптогруппу, гидроксильную группу, (Сг янный склероз, и т п , или для предупреждения Сб)-алкокси группу, (Сі-Сє)-ал кил меркаптогруппу отторжения аллотрансплантата или полуалили аминогруппу, которая может быть моно- или лотрансплантата, например, почек, печени, легдизамещена (Сі-Сє)-ал килом, (Сі-Сє)ких, сердца, и т п Кроме того, соединения облаалкоксигруппой, гид рокси-(С2-Сє)-ал килом и/или дают противовирусной, противоретровирусной (Сз-Сб)-циклоал килом, арилом, гетероарилом, или противоопухолевой активностью и, таким обарал килом или гетероарилалкильной группой, разом, являются также подходящими средствами необязательно замещенными в арильном или гепри профилактике и лечении заболеваний, индутероарильном остатке одной или несколькими цированных/вызванных вирусами и онкогенно (тамеркаптогруппами, гидроксильными группами, (Сг ких как СПИД и т п) По сравнению с соединеСб)-алкоксигруппами или (СгСб)-алкильными ниями, используемыми до настоящего времени группами или галогенами, или (С2-Сє)-алкенил, при лечении злокачественных опухолей, соединенеобязательно замещенный моно- или диалкильния по настоящему изобретению обладают повыной группой или алкоксигруппой, шенной эффективностью или меньшей токсичнопри условии, что по крайней мере один из осстью, и, таким образом, имеют более широкий татков R или R5 представляет собой водород, терапевтический спектр действия По этой причик их таутомерам и их физиологически приемне, они имеют то преимущество, что введение лемым солям неорганических и органических килекарственных средств, содержащих эти соединеслот и/или оснований, а так же к способам их пония, может продолжаться непрерывно в течение лучения и к лекарственным средствам, продолжительного периода времени, и можно изсодержащим упомянутые соединения бежать синдрома отмены препарата или дробного введения, которое в настоящее время часто исТак как соединения общей формулы 1 содерпользуется с цитостатическими средствами при жат асимметричные атомы углерода, настоящее лечении опухолей, или бывает необходимым изобретение также относится ко всем оптически вследствие их нежелательных побочных дейстактивным формам и рацемическим смесям упомявий нутых соединений В J BioL Chem 265, 6112 (1990), и в европейСоединения по настоящему изобретению своском патенте ЕР 0350287 описывается получение бодны от таких недостатков Их действие в фари применение липонуклеотидов в качестве протимакологически необходимых дозах является имвовирусных лекарственных средств Однако, в муносупрессивным или противовирусным, не этих работах проверены и синтезированы только будучи неспечифическим цитотоксичным соединения, в которых димиристоилфосфатиПодобным образом, соединения настоящего дильный и дипальмитоилфосфатидильный остатизобретения и содержащие их фармацевтические ки сочетаются с семействами нуклеозидов, такими 45339 8 представляет собой октильную, нонильную, десоставы могут использоваться в сочетании с друцильную, ундецильную, додецильную, тридецильгими лечебными средствами для лечения и проную или тетрадецильную группу Метоксигруппа, филактики упомянутых выше заболеваний Приэтоксигруппа, пропоксигруппа, бутоксигруппа и мерами таких других лекарственных средств гексилоксигруппа являются предпочтительными являются такие средства, как, например, ингиби(СгСб)-алкоксизаместителями R2 В случае, когда торы митоза, такие как колхицин, митоподозид, R2 замещен (Сі-Сє)-алкилмеркаптогруппой, подравинбластин, алкилирующие цитостатические зумевается, что эта группа представляет собой, в средства, такие как циклофосфамид, мелфалан, частности, метил меркатогруппу, этилмеркаптомилеран или цисплатин, антиметаболиты, такие группу, бутил меркаптогруппу и гексил меркаптокак антагонисты фолиевой кислоты (метотрексат) группу и антагонисты пуриновых и пиримидиновых оснований (меркаптопурин, 5-фторуридин, цитарабин), Предпочтительно, X представляет собой атом цитостатически активные антибиотики, такие как серы, сульфинильную или сульфонильную группу, антрациклины (например, доксорубицин, дауноруи Y представляет собой кислород бицин), гормоны, такие как фосфэстрол, тамоксиПодобным образом, предпочтительными явфен, другие цитостатически/цитотоксически акляются соединения, в которых X и Y представлятивные химиотерапевтические средства и другие ют собой валентные связи, R2 представляет собой иммунодепрессивные лекарственные средства водород, и R1 представляет собой (С1-С20)(такие как циклоспорины, FK 506, рапамицины, алкильную цепь, необязательно замещенную ( d дезоксиспергуалин, и т п) Сб)-алкоксигруппой или (С-і-Сб)Возможные соли соединений общей формулы алкилмеркаптогруппой 1 представляют собой, прежде всего, соли щелочПредпочтительно, R5 представляет собой воных и щелочноземельных металлов и аммония дород, азидогруппу, цианогруппу или галоген, тафосфатной группы Предпочтительными солями кой как фтор, хлор или бром щелочных металлов являются литиевые, натриеПредпочтительно, каждый из R3 и R4 предвые и калиевые соли Возможными солями щеставляет собой гидроксильную группу, или цианолочноземельных металлов являются магниевые и группу, или азидогруппу, или атом галогена, такого кальциевые соли, в особенности В соответствии с как фтор, хлор, бром или азидогруппу, или атом изобретением, под аммониевыми солями подрагалогена, такого как фтор, хлор, бром или йод, при зумеваются соли, содержащие аммониевый ион, этом группы могут быть одинаковыми или разкоторый может замещаться до четвертой степени ными алкильными остатками, имеющими 1-4 атома угОсобенно предпочтительными являются солерода, и/или аралкильными остатками, предпочединения, в которых R5 представляет собой атом тительно, бензильными остатками Заместители водорода, и R3, и R4 являются гидроксильными могут быть одинаковыми или различными группами, циангруппами, азидогруппами или атомами фтора Соединения общей формулы 1 могут содержать группы основного характера, в частности, На основаниях общей формулы (III) группы R6 7 аминогруппы, которые могут быть превращены в и R , предпочтительно, представляют собой атосоли присоединения кислот с помощью соответстмы водорода, метильные, трифторметильные, вующих неорганических или органических кислот этильные, пропильные или бутильные группы, или В таком случае, подходящими кислотами являютатомы галогена, такие как атомы фтора, хлора, ся, в частности, хлористоводородная кислота, брома или йода, а также алкенильные группы, фумаровая кислота, янтарная кислота, винная которые могут быть замещены галогеном кислота, лимонная кислота, молочная кислота, Особенно предпочтительными значениями R6 7 малеиновая кислота или м етан сул ьфо новая кии R являются атомы водорода, метильные, трифслота торметильные или этильные группы, и атомы фтора, хлора или брома, и/или винильные, пропеВ общей формуле 1 R1, предпочтительно, нильные, этинильные или пропинильные группы, представляет собой линейную (С8-Сі5)-алкильную необязательно замещенные галогеном группу, которая также может быть замещена ( d Сб)-алкоксигруппой или (С-і-Сє)Группа R8, предпочтительно, представляет 1 собой атом водорода, метильную, этильную, проалкилмеркапрогруппой Точнее, R представляет пильную или бутильную группу, аминогруппу или собой нонильную, децильную, ундецильную, доатом галогена, такого как фтор, хлор, бром или децильную, тридецильную или тетрадецильную йод, предпочтительно - атом хлора или брома группу Метоксигруппа, этоксигруппа, бутоксигруппа и гексилоксигруппа являются, предпочтительR10, предпочтительно, представляет собой но, возможными (СгСб)-алкоксизаместителями R1 атом водорода, фтора или брома, (С-і-Сє)В случае, когда R1 замещен (С-і-Сє)алкоксигруппу, конкретнее - метоксигруппу, этокалкилмеркаптогруппой, подразумевается, что эта сигруппу, пропоксигруппу, бутоксигруппу или гекгруппа представляет собой, в частности, метилсилоксигруппу, меркаптогруппу, (С-і-Сє)меркатогруппу, этилмеркаптогруппу, пропилмерал кил меркаптогруппу, точнее - метил меркаптокаптогруппу, бутилмеркаптогруппу и гексилмергруппу, этилмеркаптогруппу, бутилмеркаптогруппу каптогруппу или гексилмеркаптогруппу, или аминогруппу, которая может быть моно- или дизамещенной (С-і-Сб)R2, предпочтительно, представляет собой лиалкильной группой, такой как метильная, этильнейную (Св-Сі5)-алкильную группу, которая также ная, бутильная или гексильная группа, гидроксиможет быть замещена (Сі-Сє)-алкоксигруппой или (С2-Сб)-алкильной группой, такой как гидрокси(Сі-Сє)-алкилмеркаптогруппой Конкретнее, R2 45339 10 этильная, гидроксипропилыная, гид роке и бути л ьная или гидроксигексильная группа, (Сз-Сб)циклоалкилыной группой, такой как циклопропиль(У1Ї, ная, циклопентилыная или циклогексильная группа, арилом, предпочтительно - фенилом, аралкильной группой, такой как, в частности, бензил, 3 4 5 необязательно замещенный одной или нескольв которой R , R , R , и В имеют установленные кими гидроксильными или метоксильными группавыше значения, или представляют собой гидроми, (СгСб)-алкильными группами, такими как мексильную группу, защищенную защитной для гидтил ьная, этильная, пропильная, бутильная или роксильной функциональности группой, привычгексильная группы, или атомами галогена, такими ной для специалиста, в присутствии активного как атомы фтора, хлора или брома Подобным хлорангидрида, такого как хлорид 2,4,6образом, аминогруппа может быть замещена гетриизопропилбензолсульфоновой кислоты, и четтероалкильной или гетероарильной группой, такой вертичного азотистого основания, например, пикак, в частности, тиенильная, фурильная или пиридина или лутидина, в инертном растворителе, ридильная группа, например Под гетероарильной таком как толуол, или непосредственно в безводгруппой подразумевается, предпочтительно, тиеном пиридине, и, необязательно, с последующим нилметильная, фурилметильная или пиридилмегидролизом, удаляющим защитные группы, в сотильная группа ответствии со способами, принятыми в химии нуклеозидов, или Нуклеозидами, подходящими в качестве компонентов сочетания для получения липиднуклеотидных конъюгатов формулы (1), являются 6-меркаптопурин-9-р-О-рибофуранозид, 5-фторуридин, инозин, 5-метилуридин, 2',3'-дидезокси-2',3'-дифтортимидин, 5-хлоруридин, 5-трифторметилуридин, 5-этинилуридин, 5-этинилцитидин, 5-проп-1 -енилуридин, 5-проп-2-енилуридин, аденозин, гуанозин, 2,6-диаминопурин-9-р-О-рибофуранозид, 2-амино-6-меркаптопурин-9-р-Орибофуранозид, 2-амино-6-меркаптометилпурин-9-р-Орибофуранозид, 2-амино-6-хлорпурин-9-р-О-рибофуранозид, 2'-дезокси-2'-аминоаденозин, 2'-дезокси-2'-азидоаденозин, 2'-дезокси-2'-азидоцитидин, 2'-дезокси-5-фторуридин, 2-хлораденозин, 2-бромаденозин, З'-дезокси-З'-фтораденозин, 6-метилмеркаптопурин-9-р-О-рибофуранозид, 2-фтораденозин, 2-фтор-2'-дезоксиаденозин Соединения общей формулы (1) могут быть получены 1) взаимодействием соединения общей формулы У гч -~- \_ |*І_ О СМг-0-Р (У), в которой R1, R2, X и Y имеют установленные выше значения, с соединением общей формулы VI 2) взаимодействием соединения общей формулы VII в которой R1, R2, X и Y имеют установленные выше значения, с соединением общей формулы VI, в которой R3, R4, R5 и В имеют вышеустановленные значения, в присутствии фосфолипазы D из Streptomyces инертном растворителе, таком как флороформ, в присутствии подходящего буфера, и, необязательно, с последующей реакцией, удаляющей защитные группы, в соответствии с методами, принятыми в химии нуклеозидов Получение соединений общих формул V и VII осуществляют по аналогии с методами в Lipids 22, 947 (1987), и в J Med Chem 34, 1377 (1991) Получение соединений общей формулы VI описано, например, в ЕР-А-0286028 и в ВОИС 90/08147 Некоторые из перечисленных нуклеозидов являются коммерчески доступными соединениями Соединения, подобные соединениям формулы 1, описываются в ЕР-А-0350287 В этом патенте описываются соответствующие сложные 1,2диэфиры глицерина Лекарственные средства для лечения вирусных инфекций, содержащие соединения формулы 1, могут применяться в жидкой или твердой формах интестинальным или парентеральным способом Возможно использование обычных форм, таких как таблетки, капсулы, таблетки с покрытием, сиропы, растворы или суспензии В качестве инъекционной среды применяют, предпочтительно, воду, содержащую такие добавки, как стабилизаторы, солюбилизаторы и буферы, которые обычны для растворов для инъекций Такие добавки представляют собой, например, тартратные или цитратные буферные растворы, этанол, комплексообразующие агенты, такие как этилендиаминтетрауксусная кислота и ее нетоксичные соли, высокомолекулярные полимеры, такие как жидкие 11 45339 12 полиэтиленоксиды для регулирования вязкости фосфорной кислоты Жидкие носители для растворов для инъекций 11 (З-Додецилсульфонил-2должны быть стерильными, и, предпочтительно, децилокси)пропиловый эфир (5-хлор-уридин)-5'разливаются в ампулы Твердыми носителями фосфорной кислоты являются, например, крахмал, лактоза, маннит, 12 (З-Додецилсульфонил-2метилцеллюлоза, тальк, высокодисперсные кремдецилокси)пропиловый эфир (6-меркаптопурин-9ниевые кислоты, высокомолекулярные жирные р-О-рибофуранозид)-5'-фосфорной кислоты кислоты, такие как стеориновая кислота, желатин, 13 (3-Додецилокси-2-децилокси)пропиловый агар-агар, фосфат кальция, стеарат магния, жиэфир (5-фтор-уридин)-5'-фосфорной кислоты вотные и растительные жиры, твердые высокомо14 (3-Додецилокси-2-децилокси)пропиловый лекулярные полимеры, такие как полиэтиленглиэфир (6-меркаптопурин-9-р-О)-рибофуранозид)-5'коль, и т п Если желательно, составы, пригодные фосфорной кислоты для перорального применения, могут включать 15 (З-Додецилмеркапто-2корригенты и подслащиватели децилмеркапто)пропиловый эфир (5-фторуридин)5'-фосфорной кислоты Дозировка может зависеть от различных факторов, таких как способ введения, вид, возраст 16 (З-Ундецилмеркапто-2или индивидуальное состояние Обычно, соедиундецилокси)пропиловый эфир (5-фторуридин)-5'нения по настоящему изобретению применяют в фосфорной кислоты количестве 0,1 - 100мг, предпочтительно - 0,2 17 (З-Ундецилмеркапто-280мг, в сутки и на кг массы тела Предпочтительно ундецилокси)пропиловый эфир (5разделять суточную дозу на 2 - 5 применений, трифторметилуридин)-5'-фосфорной кислоты причем при каждом применении принимают таб18 (З-Ундецилмеркапто-2летки, имеющие содержание активного ингредиундецилокси)пропиловый эфир (6-меркаптопуринента 0,5 - 500мг Подобным образом, таблетки 9-р-О-рибофуранозид)-5'-фосфорной кислоты могут обладать продолжительным выделением 19 (З-Децилмеркапто-2лекарственного средства, что снижает число додецилокси)пропиловый эфир (5приемов до 1 - 3 раз в сутки Содержание активнотрифторметилуридин)-5'-фосфорной кислоты го ингредиента в таблетках с длительным выде20 (З-Ундецилмеркапто-2лением может составлять 2 - 1000мг Активный додецилокси)пропиловый эфир (5-фторуридин)-5'ингредиент также может вводиться непрерывными фосфорной кислоты инфузиями, при которых обычно достаточным 21 (З-Ундецилмеркапто-2является количество 5 - 1000мг в сутки децилокси)пропиловый эфир (5трифторметилуридин)-5'-фосфорной кислоты Помимо соединений, упомянутых в примерах, для целей настоящего изобретения можно ис22 (З-Тетрадецилмеркапто-2пользовать соединения формулы 1, перечислендецилокси)пропиловый эфир (6-меркаптопурин-9ные ниже р-О-рибофуранозид)-5'-фосфорной кислоты 1 (З-Додецилмеркапто-223 (З-Тридецилмеркапто-2децилокси)пропиловый эфир (5-фторуридин)-5'децилокси)пропиловый эфир (5-хлор-уридин)-5'фосфорной кислоты фосфорной кислоты 2 (З-Додецилмеркапто-224 (З-Додецилмеркапто-2децилокси)пропиловый эфир (2-фтораденозин)-5'децилокси)пропиловый эфир (5фосфорной кислоты трифторметилуридин)-5'-фосфорной кислоты 3 (З-Додецилмеркапто-225 (З-Додецилмеркапто-2дециклоси)пропиловый эфир (6-меркаптопурин-9децилокси)пропиловый эфир (2-дезокси-2р-О-рибофуранозид)-5'-фосфорной кислоты фтораденозин)-5'-фосфорной кислоты 4 (З-Додецилмеркапто-226 Додециловый эфир (6-меркаптопурин-9-рдецилокси)пропиловый эфир (5-фтор-уридин)-5'О-рибофуранозид)-5'-фосфорной кислоты фосфорной кислоты 27 Гексадециловый эфир (5-фторуридин)-5'фосфорной кислоты 5 (З-Додецилмеркапто-2децилокси)пропиловый эфир (5-проп-128 Эйкозиловый эфир (5енилуридин)-5'-фосфорной кислоты трифторметилуридин)-5'-фосфорной кислоты 6 (З-Додецилмеркапто-229 Додециловый эфир (5-фторуридин)-5'децилокси)пропиловый эфир (5-этинил-цитидин)фосфорной кислоты 5'-фосфорной кислоты 30 Додециловый эфир (6-меркаптопурин-9-рО-рибофуранозид)-5'-фосфорной кислоты 7 (З-Додецилмеркапто-2децилокси)пропиловый эфир (2-амино-6Пример 1 меркаптопурин-9-р-О-рибофуранозид)-5'(3-Додецилмеркапто-2-децилокси)пропиловый фосфорной кислоты эфир (5-фторуридин)-5'-фосфорной кислоты 8 (З-Додецилмеркапто-2Обрабатывают 3,6г (6,1ммоль) (3децилокси)пропиловый эфир (2,6-диаминопуриндодецилмеркапто-2-децилокси)пропилового эфи9-р-О-рибофуранозид)-5'-фосфорной кислоты ра фосфорной кислоты, дважды, 30мл безводного пиридина, и концентрируют путем упаривания 9 (З-Додецилмеркапто-2Остаток растворяют в 30мл безводного пиридина, децилокси)пропиловый эфир (5-проп-2обрабатывают в атмосфере азота 2,76г енилуридин)-5'-фосфорной кислоты (9,1ммоль) хлорангидрида 2,4,610 (З-Додецилсульфонил-2децилокси)пропиловый эфир (5-фтор-уридин)-5'триизопропилбензолсульфоновой кислоты и пе 13 45339 14 ремешивают при комнатной температуре в течешивают до полного растворения в органической ние 30 минут Затем добавляют 1,60г (6,1ммоль) фазе Органическую фазу отделяют, промывают 5-фторуридина (Fluka), и загрузку оставляют стонасыщенным раствором хлорида натрия и конценять в атмосфере N2 в течение 24 часов трируют в роторном испарителе Остаток вносят в Гидролиз осуществляют, используя 15мл во80г LChroprep RP-18 (обрабатывают RP-18 расды, смесь перемешивают еще в течение 2 часов твор сырого продукта в МТБ, упаривают и сушат), при комнатной температуре, освобождают от раси разделяют на части на форколонке с RP-18 Катворителя в вакууме, и дважды очищают от расждый раз в качестве элюента служит смесь 3,7л творителя, используя небольшое количество тометанола, 400мл воды, Змл ледяной уксусной килуола Остаток очищают колоночной слоты и 2г ацетата натрия Фракции, содержащие хроматографией на LiChroprep® RP-18 с линейным продукт, объединяют, осаждают нужное соединеградиентом элюента от метанола с водой (7/1) до ние путем добавления 20г оцетата кальция в метанола Выход составляет 3,1 г (69% от теоре100мл воды, и фильтруют отсасыванием Выход тического количества), масло Rf = 0,24 32г (43% от теоретического количества) (СН2СІ2/Ме0Н 8/2), Rf = 0,55 (СН2СІ2/МеОН/Н20 Кальциевую соль суспендируют в 250мл МТБ, 6,5/2,5/0,4) на пластинах для ТХС Merk 5715, сиэкстрагируют 80мл 2N HCI путем встряхивания, и ликагель 60F органическую фазу дважды промыванию насыщенным раствором хлорида натрия После удале(3-Додецилмеркапто-2-децилокси)пропиловый ния растворителя остаток растворяют в 200мл эфир фосфорной кислоты получают в соответсттолуола, и доводят рН до 7 против Fnscolyt элеквии с описанием в ВОИС 92/03462 трода 30% раствором метилата натрия НатриеПример 2 вую соль осаждают путем перемешивания в (3-Додецилмеркапто-2-децилокси)пропиловый 200мл ацетона, фильтруют отсасыванием и сушат эфир (6-меркаптопурин-9-р-О-рибофуранозид)-5'в печи для вакуумной сушки Выход 29г (37% от фосфорной кислоты теоретического количества) Обрабатывают 6,2г (12,5ммоль) (3додецилмеркапто-2-децилокси)пропилового эфиВеличина Rf 0,18 (силикагель, элюент изопрора фосфорной кислоты 5,7г (18,75ммоль) хлоранпанол/бутилацетат/вода/конц аммиак 50/30/15/5) гидрида 2,4,6-триизопропилбензолсульфоновой Пример 4 кислоты, как описано в примере 1, и затем 3,55г Натриевая соль (З-додецилмеркапто-2(11,25ммоль) б-меркаптопурин-9-p-D)децилокси)пропилового эфира (6-меркаптопурин9-р-О-рибофуранозид)-5'-фосфорной кислоты рибофуранозида, и через 24 часа осуществляют гидролиз водой Аналогично примеру 3, получают сырой конъюгат из 40г б-меркаптопурин-9-p-DЗатем к полученной смеси постепенно прикалывают раствор 2,85г ацетата кальция в 15мл рибофуранозида Сырой продукт очищают коловоды, осаждая сырую кальциевую соль конъюгата ночной хроматографией, используя каждый раз 8г, После продолжительного перемешивания с ацена колонке с фазой DIOL (диаметр 4см, длина тоном (1/10) получают 6г сырого аморфного про25см) (детекция при 254нм, элюент метанол/МТВ дукта, имеющего площадь в 72% по ВЭЖХ 10/4) Внесенный образец образует в элюенте прозрачный раствор Фракции из различных выКальциевую соль суспендируют в 350мл меделений, содержащие продукт, объединяют, упатанола, обрабатывают 150г амберлита IR 120 в ривают и осаждают в виде натриевой соли из тоформе Na+, и перемешивают в течение 2 суток луола и ацетона, как в при мере 3 Выход 64,5г После этого удаляют ионообменную смолу, (51% от теоретического количества) фильтрат упаривают, и остаток очищают колоночной хроматографией на LiChroprep® RP-18 с лиЗначение Rf 0,85 (фаза DIOL, элюент метанейным градиентом метанола с водой от 5 /1 до 9 нол) / 1 Фракции, содержащие продукт, упаривают в Пример 5 вакууме, и остаток перемешивают с ацетоном и Натриевая соль (З-додецилмеркапто-2сушат Выход 3,52г (41% от теоретического колидецилокси)пропилового эфира (6чества) метилмеркаптопурин-р-О-рибофуранозид)-5'фосфорной кислоты DC Rf = 0,45 (изопропанол/бутилацетат/конц аммиак/вода 50/30/5/15) Аналогично примеру 1, вводят во взаимодейПример 3 ствие 14,9г б-метилмеркаптопурин-9-p-Dрибофуранозида (50ммоль) со смешанным ангидНатриевая соль (З-додецилмеркапто-2ридом, полученным из 27,Зг (3-додецилмеркаптодецилокси)пропилового эфира (6-меркаптопурин2-децилокси)-пропилового эфира фосфорной ки9-р-О-рибофуранозид)-5'-фосфорной кислоты слоты и 25г хлорангидрида 2,4,6Аналогично примеру 2, в 400мл безводного триизопропилбензолсульфоновой кислоты в пиридина вводят во взаимодействие 41,4г (3250мл безводного пиридина, гидролизуют и кондодецилмеркапто-2-децилокси)пропилового эфицентрируют путем выпаривания Аналогично прира фосфорной кислоты с 42,9г хлорангидрида меру 3, сырой продукт (ВЭЖХ 67% площадь) 2,4,6-триизопропилбензолсульфоновой кислоты, и очищают хроматографией на RP-18, осаждают в затем с 23,7г б-меркаптопурин-9-p-Dвиде кальциевой соли, и превращают в натриевую рибофуранозида Сырую кальциевую соль, котосоль Выход 15,2г (38% от теоретического количерую отфильтровывают отсасыванием после гидства) ролиза и осаждения 25г ацетата кальция в 160мл воды, распределяют между 500мл МТБ (метилЗначение Rf 0,22 (силикагель, элюент изопротретбутиловый эфир) и 250мл 2N HCI, и перемепанол/бутилацетат/вода/конц аммиак 50/30/15/5) 45339 16 15 Пример 6 меркаптопурина (6-МР), 6Натриевая соль (З-додецилмеркапто-2меркаптопуринрибозида, ВМ 92 0729 и доксорубиа децилокси)пропилового эфира (5-фторуридин)-5'цина при анализах КОЕ-Э и КОЕ-ГМ фосфорной кислоты Соединение КОЕ-Э КОЕ-ГМ Аналогично примеру 1, 50г 5-фторуридина Азатиоприн 0,0004 + 0,0001 (41 0,0043 -г 0,0019 !31 превращают в сырой конъюгат, осаждают в виде 6-МР 0,0003 ± 060001 (4} 0,0023 + 0,00009 ІЗІ кальциевой соли, как описано в примере 3, и затем, чтобы конвертировать ее в свободную кисло6-МР-риеоэил 0,0003 ± 0,0001 {4) С.0О23 + 0,00013 (3) ту, очищают сырой продукт хроматографией, анаВ 32 0729 М 0,056 ± 0,013 !5І 0,247 + 0,044 Ш логично примеру 4, на фазе DIOL, используя в Доксорубишн 0.Q017 *_ 0,0005 [4! 0,050 + 0,004 Ш качестве элюента метанол/МТВ 10/4 Натриевую соль, полученную как в примере 3, извлекают с а среднее ± ст отклонение, п - число разных выходом 69% экспериментов Значение Rf 0,35 (пластины DIOL, элюент меПример 8 танол/МТВ 10/4) Токсичность ВМ 92 0729, азатиоприна, 6Пример 7 меркаптопурина и 6-меркаптопуринрибозида для Значения IC50 (мкг/мл) для азатиоприна, 6костного мозга у самок мышей Balb/c, на 4 сутки меркаптопурина (6-МР), 6(эксп 930740) меркаптопуринрибозида, ВМ 92 0729 и доксорубиЭксп 930740 показывает токсичность для коцина при анализах КОЕ-Э и КОЕ-ГМ стного мозга ВМ 92 0729, азатиоприна, 6В таблице этого примера приводятся величимеркаптопурина и 6-меркаптопуринрибозида in ны ІСбо, мкг/мл, для азатиоприна, 6vivo на самках мышей Balb/c, которым препараты меркаптопурина (6-МР) и 6давались один раз в сутки, р о , четыре дня подмеркаптопуринрибозида в сравнении с (3ряд (сутки 0 - сутки + 3) Животных умерщвляют додецилмеркапто-2-децилокси)пропиловым эфина 4 сутки (сутки +4), и определяют насыщенность ром (6-меркаптопурин-9-[3-О-рибофуранозид)-5'клетками костного мозга (клетки/бедр кость) Рефосфорной кислоты - ВМ 92 0729 - для цитотокзультаты показывают отсутствие токсичности для сичности in vitro для стволовых муриновых клеток костного мозга в случае конъюгата 6костного мозга, полученные при анализах отношемеркаптопуринрибозида с простым эфиром липиний колониеобразующих единиц к эритроцитам да ВМ 92 0729 вплоть до самых высоких прове(КОЕ-Э) и колониеобразующих единиц к гранулоренных доз, т е , до 100мг кг1сутки \ что соответцитам-макрофагам (КОЕ-ГМ) В качестве вещестствует, в молярном отношении, 30мг кг 1сутки 1 6ва для сравнения также включено цитостатичемеркаптопуринрибозида Это последнее соединеское-цитотоксическое соединение доксорубицин ние, в отличие от простого эфирного липидного Все соединения проверяются при 3 - 6 различных конъюгата ВМ 92 0729, показывает отчетливое, концентрациях при, по крайней мере, двух- трехзависящее от дозы, снижение насыщенности кратном повторении для каждой проверяемой клетками костного мозга Такие же результаты концентрации получают для других веществ, в том числе, для азатиоприна и 6-меркаптопурина Как можно видеть из результатов ВМ 92 0729 значительно лучше переносится стволовыми клетками костного мозга по сравнению со всеми другими тестируемыми соединениями, в частности, по сравнению с 6-меркаптопуринрибозидом Значения IC50 (мкг/мл) для азатиоприна, 6 Токсичность ВМ 92 0729, азатиоприна, 6меркаптопурина и 6-меркаптопуринрибозида для костного мозга у самок мышей Balb/c, на 4 сутки (эксп 930740) Таблица Соединение Контроль (0,5% тилоза) Азатиоприн Азатиоприн 6-Меркаптопурин 6-Меркаптопурин 6-Меркаптопуринрибозид 6-Меркаптопуринрибозид ВМ 92 0729 ВМ 92 0729 Доза(мг кг ' сутки ') 10 30 10 30 10 30 30 100 а среднее ± ст откл , обработка один раз в сутки, р о , сутки 0 - сутки +3, умерщвление на 4 сутки (сутки +4) Р •£ 0,01 Пример 9 Клетки/бедр кость(10°) 15,9 ± 1,4 (8) 11,6 ± 0,4 (9) 9,6 ±0,9 (9) 13,0 ±1,5 (8) 6,5 ±0,7 (9) 12,6 ±0,5 (9) 9,3 ±0,5 (9) 15,4 ±0,9 (9) 13,0 ±0,6 (9) а * ** ** ** ** 17 45339 18 Токсичность ВМ 92 0729, азатиоприна, 6циклоспорин А Результаты эксп 940026 подтвермеркаптопурина, 6-меркаптопуринрибозида и цикждают результаты, полученные в эксп 930740 in лоспорина А для костного мозга у самок мышей vivo Balb/c, на 4 сутки (эксп 940026) Токсичность ВМ 92 0729, азатиоприна, 6меркаптопурина, 6-меркаптопуринрибозида и цикЭксп 940026 является экспериментом с целоспорина А для костного мозга у самок мышей лью воспроизведения результатов, полученных в Balb/c, на 4 сутки (эксп 940026) эксп 930740 (пример 8) В этот эксперимент в качестве соединения для сравнения так же включен Таблица Соединение Контроль (0,5% тилоза) Азатиоприн Азатиоприн 6-Меркаптопурин 6-Меркаптопурин 6-Меркаптопуринрибозид 6-Меркаптопуринрибозид ВМ 92 0729 ВМ 92 0729 Циклоспорин А Циклоспорин А Доза(мг кг ' сутки ') 10 30 10 30 10 30 30 100 5 10 а среднее ± ст откл , обработка один раз в сутки, р о , сутки 0 - сутки +3, умерщвление на 4 сутки (сутки +4) тест Малп Пример 10 Токсичность (мкМ) ВМ 92 07 и 5-FU при анализах КОЕ-Э и КОЕ-ГМ для костного мозга В приведенной ниже таблице даются значения IC50 для 5-фторуридина (5-FU) и (3додецилмеркапто-2-децилокси)пропилового эфи Клетки/бедр кость(10°) 15,6 ±0,8 (10) 11,1 ±0,6 (10) 9,1 ±0,5 (10) 10,9 + 0,9 (10) 6,2 ±0,5 (10) (10) 13,7 ± 1 , 4 8,4 ±0,4 (10) 14,3 ±0,5 (10) 13,0 ±0,4 (10) 13,0 ±0,4 (10) 7,6 ±1,4 (10) а ** ** * ** * ** ** ра (5-фторуридин)-5'-фосфорной кислоты ВМ 92 0700) для токсичности для костного мозга при анализах in vitro КОЕ-Э и КОЕ-ГМ Условия испытаний см в примере 7 Результаты показывают, что конъюгат простого эфира липида и 5-фторуридина ВМ 92 0700 в 610 раз и в 238 раз менее токсичен для эритроцитных и гранулоцитных/макрофаговых стволовых клеток костного мозга, соответственно, чем сам 5FU Токсичность (мкМ) ВМ 92 0700 и 5-FU при анализах КОЕ-Э и КОЕ-ГМ для костного мозга Таблица Соединение ВМ 92 0700 3 3 КОЕ-Э 0,372 (3) КОЕ-ГМ 1,178(7) 610х 5-FU 0,00061 (3) а среднее, п - число экспериментов Пример 11 Влияние конъюгата простого эфира липида с 5FU (ВМ 92 0700) (рис 1) и 5-FU (рис 2) на лейкоз L 1210 in vitro время жизни Мышей инокулируют клетками лейкоза L 1210 в день 0 (п = 10 животных/группу), и затем дают лечебные препараты один раз в сутки, ip , от дня 0 (+1 час) до дня +41 (6 недель) еженедельными циклами, указанными на рис 1 и рис 2, соответственно Из графиков времени выживания контрольных и обрабатываемых групп, приведенных на рис 2, очевидно, что 5-FU, как сообщалось в литературе, имеет весьма узкий профиль зависимости дозаэффективность, т е , увеличение дозы, например, от 2 х 10 / 5 х 0,1мг кг 1 сутки 1 до 2 х 10 / 5 х 0,3мг кг 1 сутки 1 или даже до более высоких доз 238 х 0,00496(10) ведет к пониженным коэффициентам выживаемости Напротив, в случае конъюгата 5-FU и простого эфира липида (ВМ 92 0700) получают отчетливое, зависящее от дозы возрастание времени жизни, по сравнению с контролем 1 и 11 (рис 1), указывающее, что эквимолярные дозы ВМ 92 0700 являются явно более эффективными, при сравнении дозы ВМ 92 0700 являются явно более эффективными, при сравнении со стандартным соединением 5-FU, в этой модели лейкоза Учитывая, что ВМ 92 0700 является более эффективным (рис 1 и 2) и значительно менее токсичным для клеток костного мозга, можно сделать вывод, что ВМ 92 0700 обладает значительно более высоким терапевтическим индексом/коэффициентом, чем стандартный цитостатический 5-FU ДП «Український інститут промислової власності» (Укрпатент) вул Сім'ї Хохлових, 15, м Київ, 04119, Україна (044)456-20- 90 ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)216-32-71
ДивитисяДодаткова інформація
Автори англійськоюMertens Alfred
Автори російськоюМертенс Альфред
МПК / Мітки
МПК: A61P 31/12, A61P 37/06, A61K 31/7068, A61K 31/7076, A61K 31/7064, A61K 31/7042, A61K 31/708, A61K 31/70, A61K 31/7052, C07H 19/10, A61K 31/7072, C07H 19/20, A61P 35/00
Мітки: композиція, отримання, має, спосіб, фармацевтична, протипухлинну, активність, похідні, нуклеозидмонофосфатні
Код посилання
<a href="https://ua.patents.su/10-45339-nukleozidmonofosfatni-pokhidni-sposib-kh-otrimannya-ta-farmacevtichna-kompoziciya-shho-maeh-protipukhlinnu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">Нуклеозидмонофосфатні похідні, спосіб їх отримання та фармацевтична композиція, що має протипухлинну активність</a>
Попередній патент: Спосіб діагностики абляційної хвороби в довідшаровній стадії
Наступний патент: Спосіб з’єднання деталей з використанням мікрошарових матеріалів
Випадковий патент: Спосіб лікування гіперпігментації шкіри мікродозами аскорбінової кислоти за індріксоном-йовбак