Вакцина для великої рогатої худоби проти респіраторних патологій, спосіб вакцинації та набір для вакцинації великої рогатої худоби
Номер патенту: 70914
Опубліковано: 15.11.2004
Автори: Одонне Жан-Крістоф, Рівьєр Мішель, Бушардон Аннабель, Бодю Філіпп
Формула / Реферат
1. Вакцина для великої рогатої худоби, яка включає плазміду, що містить одну або більше нуклеїнових кислот, що кодує F та/або G білок респіраторного синцитіального вірусу великої рогатої худоби.
2. Вакцина за п. 1, яка відрізняється тим, що вказана плазміда містить нуклеїнову кислоту, яка кодує обидва гени F та G.
3. Вакцина за п. 1, яка відрізняється тим, що вказана плазміда містить нуклеїнову кислоту, яка кодує F ген, і при цьому вакцина містить другу плазміду, що містить нуклеїнову кислоту, яка кодує G ген.
4. Вакцина за будь-яким з пунктів 1-3, яка відрізняється тим, що плазміда включає ранній промотор CMV-IE цитомегаловірусу.
5. Вакцина за будь-яким з пунктів 1-3, яка відрізняється тим, що плазміда включає промотор, вибраний з раннього промотору SV40, пізнього промотору SV40, промотору LTR вірусу саркоми Рауса та промотору цитоскелета.
6. Вакцина за п. 5, яка відрізняється тим, що промотор цитоскелета являє собою промотор десміну або промотор актину.
7. Вакцина за будь-яким з пунктів 1-6, яка відрізняється тим, що її поєднують з живою цільною вакциною, інактивованою цільною вакциною, рекомбінантною вакциною або субодиницею вакцини.
8. Вакцина за будь-яким з пунктів 1-7, яка відрізняється тим, що додатково включає плазміду, що містить, принаймні, один ген іншого патогену великої рогатої худоби.
9. Вакцина за п. 8, яка відрізняється тим, що ген вибирають з gB та gD вірусу герпесу великої рогатої худоби, E2, C+E1+E2 та E1+E2 вірусу захворювання слизової оболонки, HN та F вірусу парагрипу типу 3.
10. Спосіб вакцинації великої рогатої худоби, який полягає у введенні великій рогатій худобі однієї або більше плазмід, описаних у будь-якому з пунктів 1-9, у поєднанні з інактивованою цільною вакциною, рекомбінантною вакциною або субодиничною вакциною.
11. Спосіб вакцинації великої рогатої худоби, який полягає у введенні однієї або більше плазмід, описаних у будь-якому з пунктів 1-9, великій рогатій худобі, яку спочатку вакцинують першою вакциною, вибраною з групи, яка складається з живої цільної вакцини, інактивованої цільної вакцини, субодиничної вакцини, рекомбінантної вакцини, при цьому вказана перша вакцина містить один або більше антигенів, що кодуються плазмідою, або один або більше антигенів, які забезпечують перехресний імунітет.
12. Набір для вакцинації великої рогатої худоби, що містить вакцину за будь-яким з пунктів 1-9, та іншу вакцину, вибрану з групи, яка складається з живої цільної вакцини, інактивованої цільної вакцини, субодиничної вакцини, рекомбінантної вакцини, при цьому перша вакцина містить антиген, що кодується плазмідою, або антиген, що забезпечує перехресний імунітет, для введення спочатку вказаної другої вакцини та введення вакцини за будь-яким з пунктів 1-9 як допоміжного засобу.
Текст
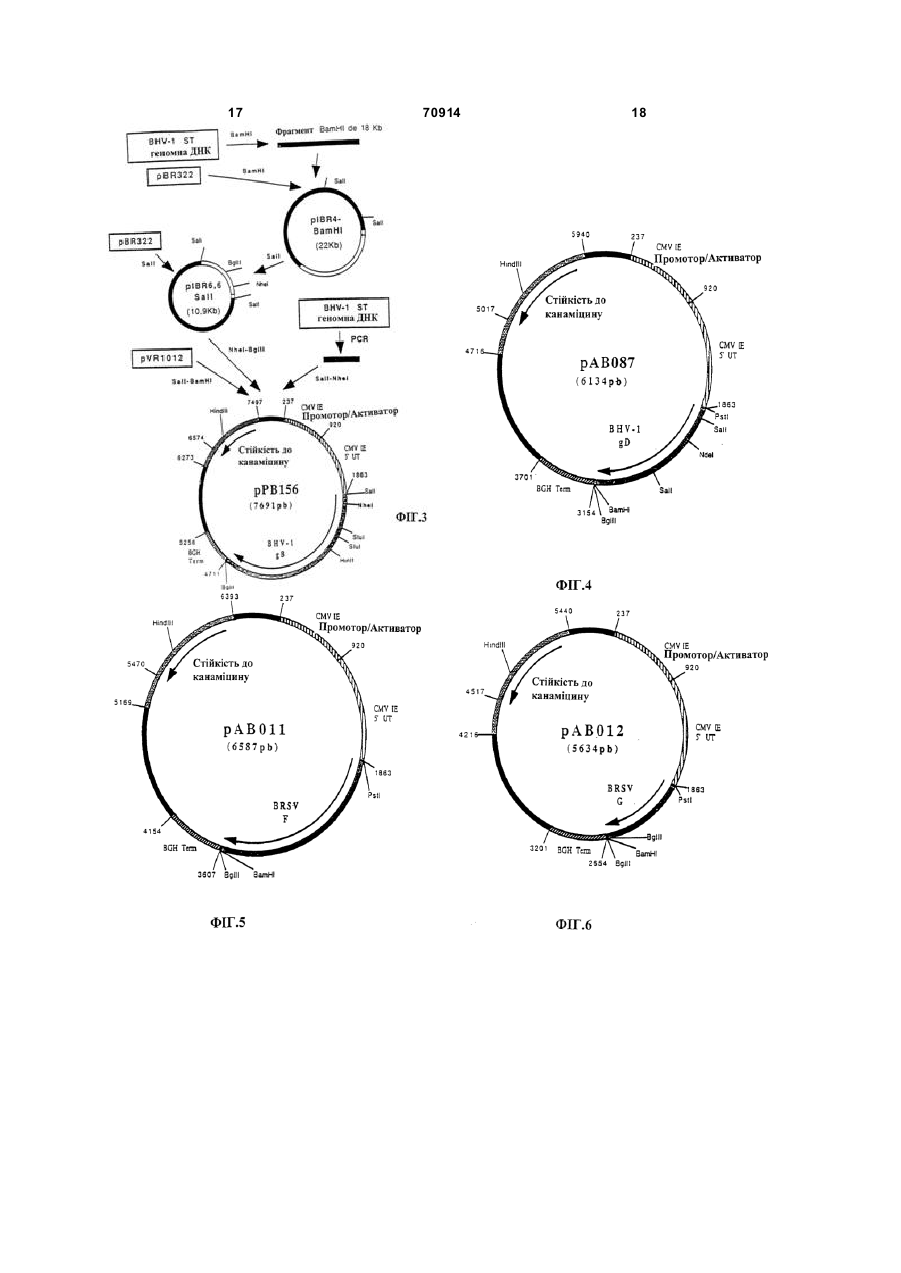
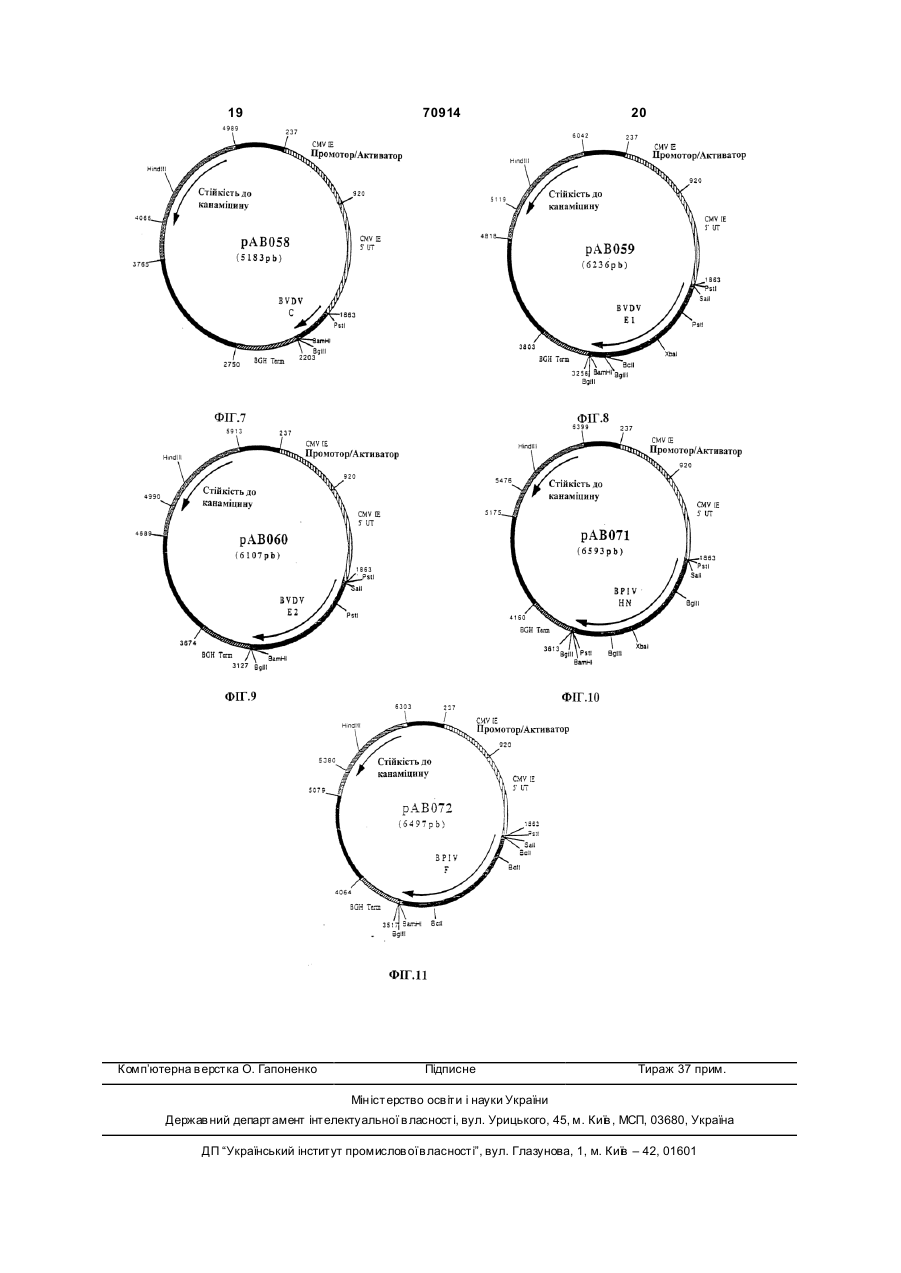
1. Вакцина для великої рогатої худоби, яка включає плазміду, що містить одну або більше нуклеїнових кислот, що кодує F та/або G білок респіраторного синцитіального вірусу великої рогатої худоби. 2. Вакцина за п. 1, яка відрізняється тим, що вказана плазміда містить нуклеїнову кислоту, яка кодує обидва гени F та G. 3. Вакцина за п. 1, яка відрізняється тим, що вказана плазміда містить нуклеїнову кислоту, яка кодує F ген, і при цьому вакцина містить другу плазміду, що містить нуклеїнову кислоту, яка кодує G ген. 4. Вакцина за будь-яким з пунктів 1-3, яка відрізняється тим, що плазміда включає ранній промотор CMV-IE цитомегаловірусу. 5. Вакцина за будь-яким з пунктів 1-3, яка відрізняється тим, що плазміда включає промотор, вибраний з раннього промотору SV40, пізнього промотору SV40, промотору LTR вірусу саркоми Рауса та промотору цитоскелета. 6. Вакцина за п. 5, яка відрізняється тим, що промотор цитоскелета являє собою промотор десміну або промотор актину. 2 (19) 1 3 70914 Даний винахід стосується формули вакцини, яка дозволяє провести вакцинацію великої рогатої худоби, зокрема, проти респіраторних патологій. Він також стосується відповідної методики вакцинації. Велика рогата худоба є носієм потенційно патогенних вірусів і бактерій із різним ступенем патогенності. Віруси можуть розмножуватися у випадку ослаблення специфічного імунітету і у випадку ушкоджень дихальних шляхів. Далі вони виділяються тваринами і можуть заражувати інши х тварин. Серед вірусів, які зустрічаються, можна, зокрема, назвати вірус парагрипу типу 3 (РІ-3), помірної власної патогенності, респіраторний вірус сінцітія великої рогатої худоби (RSV) і бичачий вірус герпесу (BHV), називаний також вірусом інфекційного ринотрахеіту великої рогатої худоби (IBR), високої власної патогенності. Іншим вірусом, що заслуговує особливої уваги через свою роль імунодепресанта і несприятливого впливу на репродукцію, є вірус захворювання слизових оболонок, або пестивірус великої рогатої худоби (BVDV). Ці віруси виявляються в цілому у первинній фазі підвищення температур, грипозного синдрому і дихательних порушень, з порушеннями травлення (діареями) у випадку BVD. Ця фаза може супроводжуватися вторинною фазою з виникненням бронхопневмоній, зв'язаних із бактеріальними інфекціями, зокрема, з такими як Pasteurella, які можуть призвести до смерті. Цей феномен особливо підсилюється придушенням імунної системи інфекцією BVD або зараженням макрофагів вірусом РІ3. Можуть проявитися і інші симптоми, такі як викидень плоду при BVD і BHV. Необхідно, отже, постаратися налагодити ефективний спосіб попередження респіраторних патологій великої рогатої худоби, які викликаються основними вірусами. В минулому вже пропонувалися сполучення вакцин проти деяких вірусів, які викликають респіраторні патології великої рогатої худоби. Такі сполучення, розроблені дотепер, були створені на основі інактивованих вакцин або живих вакцин, а також на основі сумішей таких вакцин. Їх створення ставить проблеми сумісності валентності і стабільності. Дійсно, необхідно забезпечити одночасно сумісність різних валентностей вакцин як у плані відмінності використовуваних антигенів, так і в плані самих таких складів, зокрема, при сполученні інактивованих вакцин і живих вакцин. Також виникають проблеми збереження таких комбінованих вакцин і їхньої нешкідливості, зокрема, у присутності добавок. Такі вакцини в цілому досить дорогі. У заявках WO-A-90 11092, WO-A-93 19183, WO-A-94 21797 і WO-A-95 20660 відображене використання недавно розробленої технології полінуклеотидних вакцин. Відомо, що в ци х вакцинах використовують плазміду, здатну здійснювати в клітинах хазяїна експресію антигену, вмонтованого в цю плазміду. Були запропоновані всі шляхи уведення (внутрішньочеревинний, внутрішньовенний, 4 внутрішньом'язовий, черезшкірний, внутрішньошкірний, крізь слизову і т.п.). Також можуть бути використані різні засоби вакцинації, такі як ДНК, розміщена на поверхні частинок золота і яка наноситься таким чином, і щоб вона проникала в шкіру тварини (Tang та ін., Nature 356, 152-154, 1992) і рідкоструменний впорскувач, які дозволяють здійснити трасфекцію одночасно в шкіру, м'язи, жирову тканину і у тканини молочних залоз (Furth та ін., Analytical Biochemistry, 205, 365-368, 1992). У полінуклеотидних вакцинах можуть використовуватися як неодягнуті ДНК, так і ДНК усередині ліпосом або катіонних ліпідів. G.J.M.COX вже пропонував полінуклеотидну вакцинацію проти бичачого вірусу герпесу типу 1 у J. of Virology, том 67, №9, вересень 1993, 56645667. Авторами були описані, зокрема, плазміди, що несуть гени gl (gB), gІll (gС) і Giv (gС). У "Vaccine", том 13 №4 415-421, 1995, J.E. CROWE подає загальний огляд різних методик вакцинації проти респіраторного вірусу сінцітія і проти вірусу парагрипу типу 3. Цей огляд відображає усі можливості, які надаються сучасною технікою вакцинації, і у ньому уточнюється тільки те, що технологія полінуклеотидної імунізації може бути корисна в стратегії імунізації проти RSV і PI-3. Hi плазмідні конструкції, ні результати вакцинації великої рогатої худоби проти цих вірусів у даному документі не описані. Задачею винаходу є, таким чином, створення формули полівалентної вакцини, яка дозволяє здійснити вакцинацію проти деякого числа патогенних вірусів, які викликають, зокрема, респіраторні патології у великої рогатої худоби, і забезпечити, таким чином, ефективну вакцинацію проти цих патологій. Іншою метою винаходу є створення такої формули вакцини, що поєднує у собі різні валентності при збереженні всіх необхідних критеріїв взаємної сумісності і стабільності валентностей. Іншою метою винаходу є створення такої формули вакцини, яка дозволяє сполучити різні валентності в одному і тому ж носії. Іншою метою винаходу є створення такої вакцини, яка була б проста в застосуванні і була б недорогою. Ще однією метою винаходу є створення такої формули вакцини і методики вакцинації великої рогатої худоби, які дозволяють домогтися високоефективного і довгострокового полівалентного захисту, а також нешкідливості препарату і відсутність відходів. Таким чином, об'єктом даного винаходу є формула вакцини, зокрема, проти респіраторних патології великої рогатої худоби, що включає, щонайменше, три валентності полінуклеотидних вакцин, кожна з яких включає плазміду, що містить (і яка забезпечує його експресію in vivo в клітинах хазяїна) ген однієї валентності респіраторного патогену великої рогатої худоби, причому ці валентності вибирають з групи, яка подана бичачим вірусом герпесу, респіраторним вірусом сінцітія великої рогатої худоби, вір усом захворювання слизових оболонок і вірусом парагрипу типу 3, при цьому плазміди містять в собі, для кожної валент 5 70914 6 ності, один або декілька генів, вибраних із групи, миші, або, можливо, від інших тварин, таких як представленої gВ і gD для бичачого вірусу герпепацюк, свиня, морська свинка. су, F і G для респіраторного вірусу сінцітія великої У цілому промотор може мати як вірусне, так і рогатої худоби, Е2, С+Е1+Е2 і Е1+Е2 для вірусу клітинне походження. В якості вірусного промотозахворювання слизових оболонок, HN і F для віруру, крім CMV-IE, можна назвати ранній або пізній су парагрипу типу 3. Під валентністю в даному промотор вірусу SV40 або промотор LTR вірусу винаході розуміють, щонайменше, один антиген, саркоми Рауса. Це може бути також промотор, який забезпечує захист проти патогенного вірусу, який походить від того ж вірусу, від якого походить причому валентність може містити в собі в якості ген, наприклад, власний промотор даного гену. підвалентності один або декілька природних або В якості клітинного промотора можна назвати змінених генів одного або декількох штамів даного промотор гену цитоскелета, наприклад, промотор патогену. десміну (Bolmont і ін., Journal of Submicroscopic Під геном патогенного агента розуміють не Cytology and Patology, 1990, 22,117-122; і ZHENLIN тільки повний ген, але і різні нуклеотидні послідові ін., Gene, 1989, 78, 243-254) або промотор актину. ності, включаючи фрагменти, які зберігають здатЯкщо одна плазміда містить декілька генів, ність індукувати захисну відповідь. Поняття гена вони можуть знаходитися в одній одиниці транспоширюється на нуклеотидні послідовності, еквікрипції або в двох різних одиницях. валентні в точності наведеним у прикладах, тобто Комбінація різних валентностей вакцини згідно на різні, але кодуючі один і той же протеїн. Воно з винаходом може бути отримана, переважно, також поширюється на нуклеотидні послідовності змішуванням полінуклеотидних плазмід, що заінших штамів розглянутого патогену, що забезпебезпечують експресію одного або декількох античують перехресний захист або захист, специфічгенів кожної валентності, але можна також здійсний для штаму або групи штамів. Воно також понити експресію антигенів декількох валентностей ширюється на нуклеотидні послідовності, змінені з за допомогою однієї і тієї ж плазміди. метою полегшення експресії in vivo в організмі Також об'єктом винаходу є формули одноватварина-хазяїна, але кодуючі той же протеїн. лентної вакцини, які включають одну або декілька Переважно, формула вакцини згідно з винахоплазмід, кодуючих один або декілька генів одного дом включає усі чотири валентності. з вірусів, вибраних з групи, представленої BRSV, Щодо валентності BHV, краще використовуваBVD і РІ-3, при цьому гени відповідають описаним ти обидва гени, які кодують gВ і gD, у різних плазвище. Не вважаючи їхнього одновалентного харамідах або в одній плазміді. Можна також викорисктеру, ці формули можуть мати вищенаведені хатовувати, що є менш бажаним, один або інший із рактеристики в плані вибору генів, їх комбінацій, цих генів. композиції плазмід, об'ємів доз, доз і т.д. Для валентності RSV переважно використоФормули одновалентної вакцини можуть бути вують, обидва гени G і F, які вмонтовані у дві різні використані. плазміду або в одну плазміди. Можна використо(I) для одержання формули полівалентної вавувати, що є менш бажаним, тільки ген F. кцини як вона описана вище, Для валентності BVD переважно використо(II) в індивідуальному порядку проти певної вують плазміду, яка включає ген Е2. Можна викопатології, ристовувати , що є менш бажаним, плазміду, яка (III) у сполученні з вакциною іншого типу (сукодує Е1 і Е2 або С, Е1 і Е2. цільною живою або інактивованою, рекомбінантДля валентності РІ-3 переважно використовуною, субодиниці) проти іншої патології або ють обидва гени HN і F у двох різних плазмідах (IV) як вакцини для повторного уведення після або в одній плазміде. Також можна використовувакцини, описаної нижче. вати тільки ген HN. Дійсно, ще одним об'єктом винаходу є застоФормула вакцини згідно з винаходом в її красування однієї або декількох плазмід згідно з вищому варіанті забезпечує експресію вмонтованих находом для одержання вакцини, яка призначена у неї генів gВ і gD (BHV), G і F (RSV), E2 (BVD) і для вакцинації великої рогатої худоби, первинно HN і F(PI-3). вакцинованої першою, звичайною вакциною відоОб'єм дози формули вакцини згідно з винахомого типу, вибраною, зокрема, з групи, представдом може складати від 0,1 до 10мл, зокрема, від 1 леною суцільною живою вакциною, суцільною індо 5мл. активованою вакциною, субодиничною вакциною, Доза складає, в цілому, від 10нг до 1мг, перерекомбінантною вакциною, причому ця перша вакважно, від 100нг до 500мкг, ще краще від 1мкг до цина містить (або здійснює їх експресію) один або 250мкг на кожен тип плазміди. декілька антигенів, кодуємих однією або декількоВикористовують, переважно, неодягнені плазма використовуваними плазмідами, або антигенів, міди, вміщені в носій, який вакцинує, такий як фізіякі забезпечують перехресний захист. ологічний розчин (NaCI 0,9%), ультрачиста вода, Заслуговує на увагу той факт, що полінуклеобуфер ТЕ і т.п. Можна, зрозуміло, використовувати тидна вакцина справляє сильну дію в якості другої будь-які форми полінуклеотидних вакцин, які опивакцини, яка проявляється в посиленні імунної сані в практиці минулого. відповіді і у встановленні довгострокового імунітеКожна плазміда містить у собі промотор, який ту. забезпечує експресію підпорядкованого йому гена У цілому вакцини для первинної вакцинації в клітинах-хазяїв. Це може бути сильний еукаріоможуть бути вибрані з вакцин, які випускаються тичний промотор і, зокрема, ранній промотор цидля продажу різними виробниками ветеринарних томегаловірусу CMV-IE, узятий від людини або від вакцин. 7 70914 8 Також об'єктом винаходу є набір для вакцинаSEQ ID №13: Олігон уклеотид АВ115 ції, у який входять вакцина для первинної вакциSEQ ID №14: Олігон уклеотид АВ116 нації, як вона описана вище, і формула вакцини SEQ ID №15: Олігон уклеотид АВ117 згідно з винаходом для вторинної вакцинації. Він SEQ ID №16: Олігон уклеотид АВ130 (винахід) також відноситься до формули вакцини SEQ ID №17: Олігон уклеотид АВ131 згідно з винаходом з прикладеною до неї інструкSEQ ID №18: Олігон уклеотид АВ132 цією по застосуванню цієї формули при вторинній SEQ ID №19 Олігонуклеотид АВ133 вакцинації після первинної вакцинації як вона опиПриклади: сана вище. Приклад 1 Також об'єктом винаходу є методика вакцинаКультура вирусів ції великої рогатої худоби проти респіраторних Віруси культивують на відповідній системі кліпатологій, включаючи уведення формули ефектитин до проявлення цитопатичного ефекту. Систевної вакцини, як вона описана вище. Ця методика ми клітин, які використовуються для кожного вірувакцинації включає уведення однієї або декількох су, добре відомі фахівцям. Коротко кажучи, доз формули вакцини, причому ці дози можуть клітини, чутливі до використовуваного вірусу, які бути уведені послідовно за короткий проміжок часу культивуються в мінімальному необхідному серета/або послідовно через тривалий проміжок часу. довищі Ігла (середовище "MEM") або в іншому Формули вакцини згідно з винаходом можуть відповідному середовищі, заражають досліджувабути уведені, у рамках даної методики вакцинації, ним вірусним штамом, використовуючи множинрізними шляхами уведення, передбаченими для ність зараження 1. Інфіковані клітини інкубують полінуклеотидної вакцинації, і за допомогою будьпри 37°С протягом часу, необхідного для проявів якої відомої техніки уведення. повного цитопатичного ефекту (у середньому 36 Також об'єктом винаходу є методика вакцинагодин). ції, яка полягає в тому, що проводять первинну Приклад 2 вакцинацію, як описано вище, і вторинну вакцинаЕкстракція геномних вірусних ДНК цію формулою вакцини згідно з винаходом. Після культивації збирають зруйновані клітини Відповідно до кращої форми здійснення споі їх уламки, що плавають на поверхні, і центрифусобу згідно з винаходом, спочатку тварині уводять гують вірусну суспензію при 1.000g і +4°С на проефективну дозу вакцини класичного типу, зокрема, тязі 10 хвилин для видалення уламків клітин. Поінактивованої, живої, ослабленої або рекомбінанттім осаджують вірусні частинки за допомогою ної, або субодиничну вакцину, таким чином, щоб ультрацентрифугування при 400.000g і +4°С на забезпечити первинну вакцинацію, і, переважно протязі 1 години. Осад збирають у мінімальному через 2-6 неділь, уводять полівалентну або однооб'ємі буфера (Tris 10мМ, EDTA 1мМ). Цю конценвалентну вакцину згідно з винаходом. тровану вірусн у суспензію обробляють протеїнаВинахід також стосується методики приготузою К (в кінцевій концентрації 100мкг/мл) у присутвання формул вакцини, а саме одержання валентності додецилсульфату натрію (SDS) (кінц. конц. ностей і їхніх сумішей, як випливає з даного опису. 0,5%) протягом 2 годин при 37°С. Потім екстрагуДалі випливає більш детальний опис у спосоють вірусну ДНК за допомогою суміші фебах здійснення винаходу, що обпирається на манол/хлороформ, потім осаджують 2 об'ємами аблюнки додатка. солютного етанолу. Залишають на ніч при -20°С, Список Фігур потім центрифугують ДНК при 10.000g і +4°С на Фігура 1 Плазміда pVR 1012 протязі 15 хвилин. Висушують осаджену ДНК, поФігура 2 Послідовність гену BHV-I ST gB тім збирають у мінімальному об'ємі стерильної Фігура 3 Конструкція плазміди рРВ 156 ультрачистої води. Тепер вона може піддаватися Фігура 4 Плазм іда рАВ 087 дії ферментів рестрикції. Фігура 5 Плазміда рАВ 011 Приклад 3 Фігура 6 Плазміда рАВ 012 Виділення геномних вірусни х РНК Фігура 7 Плазміда рАВ 058 РНК - які містять віруси очищають відповідно Фігура 8 Плазміда рАВ 059 до добре відомих фахівцям технологіям. Потім Фігура 9 Плазміда рАВ 060 виділяють геномну вірусну РНК кожного вірусу, Фігура 10 Плазміда рАВ 071 використовуючи те хніку екстракції "тіоціанат гуаніФігура 11 Плазміда рАВ 072 дію/фенолхлороформ", описану P. Chomczynski, Список послідовностей SEQ ID № N.Sacchi (Anal Biochem. 1987, 162, 156-159). SEQ ID №1: Послідовність гену BHV-I gB Приклад 4 (штам ST) Технології молекулярної біології SEQ ID №2: Олігонуклеотид РВ234 Усі плазмідні конструкції були отримані при SEQ ID №3: Олігонуклеотид РВ235 використанні стандартних технологій молекулярSEQ ID №4: Олігонуклеотид АВ162 ної біології, описаних J. Sambrook; і ін. (Molecular SEQ ID №5: Олігонуклеотид АВ163 Cloning: A Laboratory Manual 2-е вид. Cold Spring SEQ ID №6: Олігонуклеотид АВ026 Harbor Laboratory. Cold Spring Harbor. New York. SEQ ID №7: Олігонуклеотид АВ027 1989). Усі рестрикційні фрагменти, використовуваSEQ ID №8: Олігонуклеотид АВ028 ні уданому винаході були ізольовані за допомогою SEQ ID №9: Олігонуклеотид АВ029 набору "Geneclean" (BIO 101 Inc. La Jolla, CA). SEQ ID №10: Олігон уклеотид АВ110 Приклад 5 SEQ ID №11: Олігон уклеотид АВ111 Технологія полімеразної ланцюгової реакції із SEQ ID №12: Олігон уклеотид АВ114 зворотною транскриптазою (RT-PCR.) 9 70914 10 Специфічні олігонуклеотиди (несучі на 5'Конструювання плазміди рАВ087 (ген BHV-1 кінцях сайти рестрикції для полегшення клонуванgD) ня ампліфікованих фрагментів) синтезують таким Провели реакцію ПЛР із геномною ДНК бичачином, що вони повністю охоплюють кодуючі ділячого вірусу герпесу (BHV-1) (Штам ST) (P.Leungнки генів, які повинні бути ампліфіковані (див. спеTack і ін. Virology. 1994. 199. 409-421), отриманою цифічні приклади). Полімеразну ланцюгову реакза технологією, описаною у прикладі 2 і з наступцію (ПЛР) із зворотною транскриптазою (RT) ними олігонуклеотидами: здійснюють по стандартним технологіях (J. Sambrook і ін. Molecular Cloning: A Laboratory Manual. 2-е видання. Cold Spring Harbor Laboratory. Cold Spring Harbor. New York. 1989). Кожну реакцію RT-ПЛР проводять із парою специфічних амплімерів, використовуючи в якості матриці екстраговану вірусну геномну РНК. Комплементарну ампліфіковану ДНК екстрагували фенощоб ампліфікувати частину 5'-гену, що кодує лом/хлороформом/ізоаміловим спиртом (25:24:1) глікопротеїн gD бичачого вірусу герпесу (BHV-1) перед розщепленням рестрикційними фермента(№ доступу послідовности в Gen Bank'e = L 26360) ми. у ви гляді фрагмента ПЛР 338 п.н. Після очищення Приклад 6 цей фрагмент розщепили за допомогою Pstl і NdeІ, Плазміда рVR 1012 щоб ізолювати фрагмент Pstl-Ndel317 п.н. (фрагПлазміда pVR 1012 (фігура 1) була отримана мент А). при Vical Inc. San Diego, CA, USA. Її конструювання Плазміду pBHV 001 (P.Leung-Tack і ін. Virology. було описано у J. Hartikka і ін. (Human Gene 1994. 199. 409-421) розщепили за допомогою Ndel Therapy. 1996. 7. 1205-1217). і Styl, щоб визволити фрагмент 942 п.н., який місПриклад 7 тить частину 3'-ген у, що кодує глікопротеїн gD віКонструювання плазміди рРВ 156 (ген BHV-1 русу BH V-1 (фрагмент В). gB) Фрагменти А і В зшили разом із вектором pvR ДНК генома бичачого вірусу герпесу BHV-I 1012 (приклад 6), попередньо розщепленим Pstl і (Штам ST) (Leung-Tack P. і ін. Virology. 1994. 199. Xbal, і одержали плазміду рАВ 087 (6134 п.н.) (фі409-421) була отримана за технологією, описаною гура 4). в прикладі 2, і розщеплена ВатНІ. Після очищення Приклад 9 фрагмент BamHI-BamHI з 18 т.п.н. був клонований Конструювання плазміди рАВ 011 (ген BRSV у векторі pBR 322, попередньо розщепленим за F) допомогою ВатНІ, для одержання плазміди plBR-4За технологією, описаною у прикладі 5, провеBamHI (22 т.п.н.). ли реакцію RT-ПЛР із геномною РНК респіраторноПотім плазміду plBR-4-BamHI розщепили за го вірусу сінцітія великої рогатої худоби (BRSV) допомогою Sall, щоб вивільнити фрагмент Sall-Sall (Штам 391-2) (R.Lerch і ін. Virology. 1991. 181. 1186,6 т.п.н. який містить ген, що кодує глікопротеїн 131), отриманої, як зазначено в прикладі 3, і з наgB вірусу BH V-1 (фігура 2 і SEQ ID №1). Цей фраступними олігонуклеотидами: гмент клонували у векторі pBR 322, попередньо розщепленому за допомогою Sall, і одержали плазміду plBR-6, 6-Sall (10,9 т.п.н.). Плазміду plBR-6, 6-Sall розщепили за допомогою Nhel і Bglll, щоб визволити фрагмент Nhel-Bglll (2676 п.н.), який містить ген, що кодує глікопротеїн gB бичачого вірусу герпесу (BH V-1) (фрагмент А). Провели реакцію ПЛР із геномною ДНК бичащоб виділити ген, що кодує глікопротеїн злитчого вірусу герпесу (BHV-1) (Штам ST) і з наступтя F (BRSV F) у формі фрагмента ПЛР 1734 п.н. ними олігонуклеотидами: Після очищення цей фрагмент розщепили Pstl і ВатНІ, щоб ізолювати фрагмент Pstl -BamHI 1717 п.н. Цей фрагмент зшили з вектором pVR 1012 (приклад 6), попередньо розщепленим Pstl і ВатНІ, і одержали плазміду рАВ 011 (6587 п.н.) (фігура 5). Приклад 10 Конструювання плазміни рАВ 012 (ген BRSV G) щоб виділити частину 5'-гену, що кодує глікопЗа технологією, описаною в прикладі 5, проверотеїн gB (BHV-1). ли реакцію RT-ПЛР із геномною РНК респіраторноПісля очищення продукт ПЛР (153 п.н.) розщего вірусу сінцітія великої рогатої худоби (BRSV) пили за допомогою Sall і Nhel, щоб ізолювати фра(Штам 391-2) (R.Lerch і ін. J.Virology. 1990. 64. гмент Sall-NheІ 145 п.н. (фрагмент В). 5559-5569) і з наступними олігонуклеотидами: Фрагменти А і В зшили разом із вектором pvR 1012 (приклад 6), попередньо розщепленим за допомогою SaІl і ВатНІ, і одержали плазміду ррВ 156 (7691 п.н.) (Фігура 3). Приклад 8 11 70914 12 ної діареї великої рогатої худоби (BVDV) (Штам Osloss) (L.De Moerlooze і ін. J.Gen. Virol. 1993. 74. 1433-1438) і з наступними олігонуклеотидами: щоб виділити ген, що кодує протеїн G (BRSV G) у формі фрагмента ПЛР 780 п.н. Після очищення цей фрагмент розщепили за допомогою Pstl і ВатНІ, щоб ізолювати фрагмент Pstl -BamHI 763 п.н. Цей фрагмент зшили з вектором pVR 1012 (приклад 6), попередньо розщепленим Pstl і ВатНІ, і одержали плазміду pAB012 (5634 п.н.) (фігура 6). Приклад 11 Конструювання плазміди рАВ058 (ген BVDV С) За технологією, описаною в прикладі 5, провели реакцію RT-ПЛР із геномною РНК вірусу вірусної діареї великої рогатої худоби (BVDV) (Штам Osloss) (L.De Moerlooze і ін. J.Gen.Virol. 1993. 74. 1433-1438), отриманою за технологією, описаною в прикладі 3, і з наступними олігонуклеотидами: щоб ампліфікувати фрагмент у 342 п.н., який містить ген, що кодує протеїн капсиду С вірусу BVD V. Після очищення продукт реакції RT-ПЛР розщепили за допомогою Pstl і ВатНІ і одержали фрагмент Pstl-BamHI 324 п.н. Цей фрагмент зшили з вектором pVR 1012 (приклад 6), попередньо розщепленим за допомогою Pstl і ВатНІ, і одержали плазміду рАВ 058 (5183 п.н.) (фігура 7). Приклад 12 Конструювання плазміди рАВ 059 (ген BVDV E1) За технологією, описаною в прикладі 5, провели реакцію RT-ПЛР із РНК геному вірусу вір усної діареї великої рогатої худоби (BVD V) (Штам Osloss) (L.De Moerlooze і ін. J.Gen. Virol. 1993. 74. 1433-1438) і з наступними олігонуклеотидами: щоб виділити послідовність, яка кодує протеїн Е1 вірусу BVD V, у формі фрагмента ПЛР 1381 п.н. Після очищення цей фрагмент розщепили за допомогою SaІl і ВатНІ і одержали фрагмент Sall-BamHI 1367 п.н. Цей фрагмент зшили з вектором pVR 1012 (приклад 6), попередньо розщепленим за допомогою SaІl і ВатНІ, і одержали плазміду рАВ 059 (6236 п.н.) (Фігура 8). Приклад 13 Конструювання плазміди рАВ 060 (ген BVDV E2) За технологією, описаною в прикладі 5, провели реакцію RT-ПЛР із геномною РНК вірусу вірус щоб ізолювати послідовність, яка кодує протеїн Е2 вірусу BVD V, у формі фрагмента ПЛР 1252 п.н. Після очищення цей фрагмент розщепили Sall і ВатНІ і одержали фрагмент SallBamH11238 п.н. Цей фрагмент зшили з вектором pVR 1012 (приклад 6), попередньо розщепленим за допомогою Sall і ВатНІ, і одержали плазміду рАВ (6107 п.н.) (Фігура 9). Приклад 14 Конструювання плазміди рАВ 071 (ген BPIV HN) За технологією, описаною в прикладі 5, проводять реакцію RT-ПЛР з геномною РНК вірусу парагрипу великої рогатої худоби типу З (PI3=BPIV) і з наступними олігонуклеотидами: щоб виділити ген, який кодує глікопротеїн HN BPIV (послідовність гену HN, заявлена H.Shibuta у 1987 № доступу послідовності в Gen Bank'e = Y00115) у формі фрагмента ПЛР 1737 п.н. Після очищення цей фрагмент розщепили за допомогою Sall і ВатНІ, щоб ізолювати фрагмент Sall і ВатНІ 1725 п.н. Цей фрагмент зшили з вектором pVR 1012 (приклад 6), попередньо розщепленим за допомогою Sall і ВатНІ, і одержали плазміду р АВ 071 (6593 п.н.) (фігура 10). Приклад 15 Конструювання плазміди рАВ072 (ген BPIV F) За технологією, описаною в прикладі 5, провели реакцію RT-ПЛР із геномною РНК вірусу парагрипу великої рогатої худоби типу 3 (PI3=BPIV) і з наступними олігонуклеотидами: щоб виділити ген, який кодує протеїн F вірусу BPIV (послідовність гену F, заявлена H.Shibuta у 1987. №. доступу послідовності в Gen Bank'e = Y00115) у формі фрагмента ПЛР 1641 п.н. Після очищення цей фрагмент розщепили за допомогою Sall і BamHI, щоб ізолювати фрагмент Sall-BamHI 1629 п.н. Цей фрагмент зшили з вектором pVR 1012 (приклад 6), попередньо розщепленим за допомогою Sall і BamHI, і одержали плазміду рАВ 13 70914 14 072 (6497 п.н.) (фігура 11). ультрачистій воді або в буфері ТЕ (Tris-HCI 10мМ; Приклад 16 EDTA 1мм, рН 8,0). Одержання і очищення плазмід Приклад 17 Для одержання плазмід, призначених для вакОдержання асоційованих вакцин цинації тварин, можна використовувати будь-яку Різні плазміди, необхідні для одержання асотехнологію, яка дозволяє одержати суспензію ційованої вакцини, змішують у їхніх концентроваочищених плазмід, здебільшого у зверхскрученій них розчинах (приклад 16). Суміші готують таким формі. Такі технології добре відомі фахівцям. Мочином, що кінцева концентрація кожної плазміди жна назвати, зокрема, техніку лужного лізису з відповідає ефективній дозі кожної плазміди. Для наступним дворазовим центрифугуванням у градіточного доведення кінцевої концентрації вакцини єнті хлориду цезію в присутності броміду етідія, як використовують розчин 0,9% NaCI або буфер PBS. вона описана J.Sambrook і ін. (Molecular Cloning: A Такі особливі компоненти як ліпосоми, катіонні Laboratory Manual 2-е вид. Cold Spring Harbor ліпіди можуть також бути використані для одерLaboratory. Cold Spring Harbor. New York. 1989). жання вакцин. Також можна звернутися до матеріалів заявок РСТ Приклад 18 WO 95/21250 і РСТ WO 96/02658, де описані меВакцинація великої рогатої худоби тодики одержання у промисловому масштабі плаВелику рогату худобу вакцинують дозами змід для вакцинації. Для одержання вакцин (див. 100мкг, 250мкг або 500мкг на плазміду. Ін'єкцію приклад 17) очищені плазміди поміщають у супроводять за допомогою голки внутрішньом'язово спензію таким чином, щоб одержати розчини висов м'яз gluteus або в м'язи шиї. Дози вакцинації кої концентрації (>2мг/мл), придатні для зберевводять в об'ємах від 1 до 5мл. ження. Для цього готують суспензію плазмід в 15 70914 16 17 70914 18 19 Комп’ютерна в ерстка О. Гапоненко 70914 Підписне 20 Тираж 37 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюFormula of polynucleotide vaccine against respiratory pathogens of the cattle
Автори англійськоюBouchardon, Annabelle, Baudu,Philippe, Riviere, Michel
Назва патенту російськоюФормула полинуклеотидной вакцины против респираторных патологий крупного рогатого скота
Автори російськоюБушардон Аннабель, Бодю Филипп, Ривьер Мишель
МПК / Мітки
МПК: C07K 14/06, C07K 14/115, A61K 39/12, A61P 31/22, A61K 39/155, C07K 14/18, C12P 21/02, A61P 31/20, C12N 15/45, C07K 14/135, A61K 39/245, C12N 15/09, A61K 39/295
Мітки: рогатої, великої, вакцинації, спосіб, респіраторних, набір, патологій, вакцина, худоби
Код посилання
<a href="https://ua.patents.su/10-70914-vakcina-dlya-veliko-rogato-khudobi-proti-respiratornikh-patologijj-sposib-vakcinaci-ta-nabir-dlya-vakcinaci-veliko-rogato-khudobi.html" target="_blank" rel="follow" title="База патентів України">Вакцина для великої рогатої худоби проти респіраторних патологій, спосіб вакцинації та набір для вакцинації великої рогатої худоби</a>