Спосіб одержання кополіестеретерів двоосновних природних a-амінокислот
Номер патенту: 87934
Опубліковано: 25.02.2014
Автори: Фігурка Наталія Володимирівна, Воронов Андрій Станіславович, Дронь Ірина Анатоліївна, Носова Наталія Геріанівна, Самарик Володимир Ярославович, Воронов Станіслав Андрійович, Варваренко Сергій Миколайович, Тарнавчик Ігор Тарасович
Формула / Реферат
Спосіб одержання кополіестеретерів двоосновних природних a-амінокислот, що включає взаємодію двоосновної N-захищеної амінокислоти та поліетердіолу-поліоксіетилену (ПЕГ) з утворенням діестеру та його кополіконденсацію з утворенням кополіестеретеру та наступним видаленням захисних труп трифлуороцтовою кислотою в метилені хлористому, який відрізняється тим, що як N-захищену амінокислоту використовують 2-[(трет-бутоксикарбоніл)аміно]пентандіонову кислоту (Glu(Boc)), взаємодію проводять при мольному співвідношенні Glu(Boc):ПЕГ не менше як 1:2,2, діестер отримують з кінцевими гідроксильними групами формули
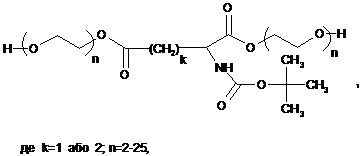
і кополіконденсують його за реакцією Стегліха з 2-(алканоїламіно)пентандіоновою кислотою (Glu-R) з одержанням кополіестеретеру
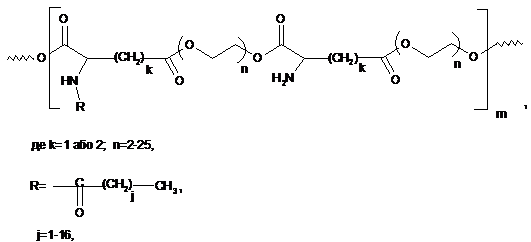
з первинними аміногрупами.
Текст
Реферат: Спосіб одержання кополіестеретерів двоосновних природних -амінокислот включає взаємодію двоосновної N-захищеної амінокислоти та поліетердіолу-поліоксіетилену (ПЕГ) з утворенням діестеру та його кополіконденсацію з утворенням кополіестеретеру та наступним видаленням захисних груп трифлуороцтовою кислотою в метилені хлористому. Як N-захищену амінокислоту використовують 2-[(трет-бутоксикарбоніл)аміно]пентандіонову кислоту (Glu(Boc)), взаємодію проводять при мольному співвідношенні Glu(Boc):ПЕГ не менше як 1:2,2, та отримують діестер. Кополіконденсують його за реакцією Стегліха з 2-(алканоїламіно)пентандіоновою кислотою (Glu-R) з одержанням кополіестеретеру. UA 87934 U (12) UA 87934 U UA 87934 U 5 10 15 20 25 30 35 Корисна модель належить до галузі хімії високомолекулярних сполук, а саме до способу одержання кополіестеретерів альтернатної будови з ліпофільними та гідрофільними фрагментами, що забезпечує їх амфіфільність, які відрізняються наявністю первинних аміногруп. Завдяки використанню похідних природних двоосновних α-амінокислот глутамінової/аспарагінової та поліетердіолів оксіетиленового ряду, як мономерних ланок для синтезу, отримані кополіестеретери є біосумісними і біодеградабельними. Такі полімери можуть бути використані при створенні нових типів засобів для інженерії тканин, а також для створення нових полімерних систем транспорту ліків з можливістю ковалентного приєднання по первинній аміногрупі молекул спейсорів, маркерів та діючої речовини ліків. Відомий спосіб [Won C.Y. Novel biodegradable copolymers containing pendant amine functional groups based on aspartic acid and poly(ethyleneglycol) / C.Y. Won, C.C. Chu, J.D. Lee // Polymer.1998. - №39(25). - P.6677-6681.] одержання кополіестеретерів природних двоосновних аамінокислот та поліетердіолів (ПЕГ). На першій стадії проводили поліконденсацію ангідриду Nкарбоксибензил-захищеної аспарагінової кислоти з ПЕГ при 403 К в присутності nтолуолсульфокислоти, як каталізатора. При цьому отримували низькомолекулярні кополіестеретери. Поліконденсацією в розплаві цих низькомолекулярних кополіестеретерів при 433 К в присутності тетраїзопропоксититану, як каталізатора, отримували високомолекулярні кополіестеретери і після видалення захисної групи каталітичним гідрогенолізом на паладієвому каталізаторі отримували кополіестеретери з первинною аміногрупою. До недоліків способу можна віднести проведення синтезу при високій температурі, що не дає можливості використовувати складні мономери з естерним зв'язком у структурі молекули через можливість конкуруючого протікання реакцій неконтрольованої переестерифікації. Крім того, за цим способом нема можливості регулювати колоїдно-хімічні властивості отриманих кополіестеретерів, оскільки вони не містять фрагментів ліпофільної природи - після видалення захисної групи, отриманий кополіестеретер є водорозчинним і не має амфіфільних властивостей. Найбільш близьким до запропонованого є спосіб одержання кополіестеретерів двоосновних природних α-амінокислот, що включає взаємодію двоосновної N-захищеної амінокислоти та поліетердіолу-поліоксіетилену (ПЕГ) з утворенням діестеру та його кополіконденсацію з утворенням кополіестеретеру та наступним видаленням захисних груп трифлуороцтовою кислотою в метилені хлористому. Отриманий кополіестер з первинними аміногрупами був випробуваний для зв'язування ДНК та доставки генів [Caracciolo P. C. Novel bioresorbable cationic polyester for gene delivery / P. С Caracciolo, F. Parra, G.A. Abraham [et. al.] // IX Simposio Argentino de Polimeros (SAP'2011), 15-18 denoviembre, 2011. Abstract Book.-2011.-P. 63.]. Але за цим способом взаємодією N-захищеної піроглутамінової кислоти з поліетердіолом при мольному співвідношенні кислота:ПЕГ як 2:0,8, отримували діестер, який містить два фрагменти N-захищеної глутамінової кислоти (Glu(Boc)), що визначає кінцеві карбоксильні групи діестеру формули: O O HO (CH2) O O O k n NH O O CH3 (CH2) O OH k NH O O CH3 CH3 CH3 CH3 40 45 CH3 , де k=2, n=4. Кополіконденсацією діестеру як комономер з поліетердіолом - (ПЕГ200) та після видалення Вос-захисної групи отримували кополіестеретер, який містить первинну аміногрупу, але є водорозчинним і не має амфіфільних властивостей. Крім того, невисокі виходи кополіестеретеру, низька молярна маса та складна очистка не дозволяє за цим способом конструювати кополіестеретери складної архітектури з заданими властивостями. В основу корисної моделі поставлена задача - створити спосіб одержання кополіестеретерів двоосновних природних α-амінокислот, в якому використання нової двоосновної N-захищеної амінокислоти з поліетердіолом (ПЕГ), що забезпечив би утворення діестеру з кінцевими 1 UA 87934 U гідроксильними групами та його кополіконденсацію за новим механізмом з одержанням кополіестеретеру формули O O (CH2) O HN O O k n O (CH2) O H2N n k O O R m , де k=1 або 2; n=2-25, C R= (CH2) j CH3 , O j=1-16, 5 10 15 з первинними аміногрупами та заданою альтернантною структурою складної будови і визначеними колоїдно-хімічними властивостями. Поставлена задача вирішується тим, що у способі одержання кополіестеретерів двоосновних природних α-амінокислот, що включає взаємодію двоосновної N-захищеної амінокислоти та поліетердіолу -поліоксіетилену (ПЕГ) з утворенням діестеру та його кополіконденсацію з утворенням кополіестеретеру та наступним видаленням захисних груп трифлуороцтовою кислотою в метилені хлористому, згідно з корисною моделлю, як N-захищену амінокислоту використовують 2-[(трет-бутоксикарбоніл)аміно]пентандіонову кислоту Glu(Boc), взаємодію проводять при мольному співвідношенні Glu(Вос):ПЕГ не менше як 1:2,2, діестер отримують з кінцевими гідроксильними групами формули O H O O O (CH2) n k O O n CH3 NH O O H CH3 , CH3 де k=1 або 2; n=2-25, (1) і кополіконденсують його за реакцією Стегліха з 2-(алканоїламіно)пентандіоновою кислотою (Glu-R) з одержанням кополіестеретеру 20 O O (CH2) O HN O O k O n (CH2) O H2N R k n O O , m де k=1 або 2; n=2-25, R= C (CH2) j CH3 , O j=1-16 , (2) 2 UA 87934 U 5 10 15 20 25 30 35 з первинними аміногрупами. Такий спосіб при мольному співвідношенні комономерів, близький до еквімольного (GluR:діестер=1:1,05), забезпечує отримання кополіестеретерів альтернантної будови, в яких кожна елементарна ланка складається з фрагменту N-захищеної амінокислоти Glu(Boc), у якому після видалення захисної групи утворюється первинна аміногрупа, фрагменту Nалканоїлзахищеної двоосновної α-амінокислоти GluR (кількість атомів вуглецю у алкільному фрагменті R=248) з ліпофільними властивостями і гідрофільного фрагменту поліетердіолу (ПЕГ). Наявність у структурі макромолекули гідрофільних та ліпофільних фрагментів, що чергуються забезпечує амфіфільні властивості синтезованих кополіестеретерів та дозволяє зміною молярної ваги поліетердіолу та величиною алкільного замісника у ліпофільному комономері регулювати їх колоїдно-хімічні властивості. Лабільний естерний з'язок, що зв'язує фрагменти у кополіестеретері забезпечує його здатність до біодеградації, а аміногрупа дозволяє ковалентне приєднання молекул спейсорів, діючої лікарської речовини, фрагментів специфічної взаємодії для створення нових систем транспорту лікарських препаратів в живому організмі, а також в інженерії тканин. Для одержання кополіестеретерів природних двоосновних α-амінокислот були використані: N-захищені природні двоосновні амінокислоти 2-[(третбутокси-карбоніл)аміно]пентандіонова кислота (Glu-Boc) (Aldrich); 2-(алканоїламіно)пентадіонові кислоти (Glu-R), такі як 2(гептадеканоїл-аміно)пентандіонова кислота (Glu-St), 2-(додеканоїламіно)пентандіонова кислота (Glu-L) (Aldrich). Перед використанням сушили у вакуумі над фосфорним ангідридом до постійної ваги. Трифлуороцтова кислота (TFA) (Aldrich). Використовували без додаткового очищення. Поліетердіоли (ПЕГ) молярної ваги 100, 600, 1000 г/моль (Aldrich). Для очищення від домішок води до відповідного поліетердіолу (ПЕГ) додавали бензол та відганяли азеотропну суміш бензол-вода. Залишки бензолу видаляли у вакуумі до постійної ваги. N, N'-дициклогексилкарбодіімід (ДЦК) (Aldrich); 4-Диметиламінопіридин (ДМАП), 99 % (Alfa Aesar). Використовували без додаткового очищення. Метилен хлористий, бензол очищали за відомими методиками [Вайсберг А., Проскауэр Э., Риддис Д. и др. Органические растворители. - М.: Иностранная литература.-1976. -с. 285-286, 389] Структуру отриманих мономерів та полімерів підтверджували ПМР спектроскопією. Молекулярну масу визначали гельпроникною хроматографією (GPC). Кількість первинних аміногруп визначали потенціометричним титруванням. Суть корисної моделі пояснюється прикладами. Приклад 1. Синтез діестеру 2-[(трет-бутоксикарбоніл)аміно]-пентандіонової кислоти (GluBoc) та діетиленгліколю (ПЕГ-100) (ПЕГ-100-Glu-Boc-ПЕГ-100) проводили згідно з загальною реакцією O O O (CH2) HO k CH3 H3C O OH + 2 HO NH O H n O 2DCC DMAP H - 2DCU O (CH2) O CH3 n H3C O H3C H3C k O O O H n NH O , де n=2-25, k=1 або 2. 40 45 50 У двогорлий реактор об'ємом 250 мл, обладнаний крапельною лійкою та насадкою ДінаСтарка зі зворотним холодильником, вносили 0,06 моль (15,1 г) 99,5 % GluBoc, 0,3 моль (31,8г) ПЕГ-100 і 70мл метилену хлористого. Реакційну суміш нагрівали до 318 К і через насадку ДінаСтарка відбирали 30 мл азеотропної суміші для видалення води. Після охолодження до 278-280 К при перемішуванні повільно прикапували розчин дициклогексилкарбодііміду 0,13 моль (27 г) в 25 мл метилену хлористого та розчин 4-диметиламінопіридину 0,02 моль (2,44 г) в 15 мл метилену хлористого. Реакційну суміш перемішували при температурі 288 К протягом 2-3 год., піднімали температуру до 308 К і витримували ще 3 години. По завершенні, реакційну масу фільтрували, а фільтрат упарювали. Висушений неочищений продукт розчиняли в 150-200 мл бензолу і промивали 5 разів по 30-40 мл насиченим розчином NaCl, підкисленим хлороводневою кислотою до рН 2,5-3. Промитий від непрореагованого ПЕГ-100 бензольний розчин упарювали до об'єму 100 мл. Діестер з бензольного розчину екстрагували водою 5-6 разів об'ємом по 100 мл. Водні витяжки об'єднували і упарювали при 313 К. Сухий залишок 3 UA 87934 U 5 10 розчиняли в ацетоні, фільтрували від залишків солей і фільтрат упарювали. Отримували діестер ПЕГ-100 2-[(трет-бутоксикарбоніл)аміно] пентандіонової кислоти (ПЕГ-100-Glu-Boc-ПЕГ100) формули (1) при n=2 в кількості 22,6 г. Вихід 88 %. Приклад 2. Здійснювали аналогічно прикладу 1, але як діол використовували поліетердіол з молярною масою 600 г/моль (ПЕГ-600). Отримували діестер ПЕГ-600 в кількості 73,7 г 2-[(третбутоксикарбоніл)аміно]пентандіонової кислоти ПЕГ-600-Glu-Вос-ПЕГ-600 формули (1) при n=1314. Вихід 85 %. Приклад 3. Здійснювали аналогічно прикладу 1, але як діол використовували поліетердіол з молярною масою 1000 г/моль (ПЕГ-1000). Отримали 110,4 г діестеру ПЕГ-1000 2-[(третбутоксикарбоніл)-аміно]пентандіонової кислоти ПЕГ-1000-Glu-Boc-ПЕГ-1000 формули (1) при п=22-23. Вихід 82 %. Структуру отриманого діестеру підтверджували Н-ЯМР спектроскопією: O O J I HO CH2 G O CH2 C CH2 B CH2 D C CH n G C O CH2 CH2 OH n NH E J I E O C O C H3C A CH3 CH3 CH2 Таблиця 1 Віднесення сигналів протонів Н1-NMR-спектру в дейтероацетоні діестеру 2-[(трет-бутоксикарбоніл)аміно]пентандіонової кислоти та ПЕГ 100 А 1,41 с Фрагмент мономеру O C (H3C)3 8,96 9 Glu 1,00 1 Glu 2,02 2 Glu, Glu HC NH C к-сть протонів у фрагменті Воc Віднесення Інтеграл 2,01 2 PEG, PEG Позн. Зсув Тип 3,98 4 PEG PEG PEG 84,23 3,88 2,11 88 4 2 O CH2 В 4,6 С 1,92,0 CH NH м O C шм 2,42 G 4,24,3 м м ш O CH2 CH O C NH CH2 O C O м 3,65 3.2 3.5 CH2 CH NH CH2 C м D O O O O C Е І J O O CH2 CH2 C O O CH2 O (CH2 CH2)n O CH2 O (CH2 CH2)n O CH2 CH2 OH O (CH2 CH2)n O CH2 CH2 OH 4 UA 87934 U Продовження таблиці 1 CH2 6,36,5 К 5 CH NH ш O C O Glu 1 Хороше узгодження між кількостями протонів, що відповідають формулі (1) та визначеними інтегралами їх сигналів у спектрі підтверджує структуру отриманого продукту. Приклад 4. Синтез кополіестеретеру здійснювали кополіконденсацією синтезованого діестеру (приклад 1) ПЕГ-ЮО-Оіи-Вос-ПЕГ-ЮО (гідрофільний фрагмент) та 2-(гептадеканоїламіно)пентадіоновою кислотою (Glu-St) (ліпофільний фрагмент) як мономерів згідно з наступною загальною реакцією: O O H O O (CH2) n O O k + H O n NH O H3C CH2 HO O DCC, DMAP CH3 O OH NH -DCU R1 CH3 O O O O O (CH2) n O k NH O O O NH R1 O H3C O CH2 n , m CH3 CH3 де k=1 або 2; n=2-25, C (CH2) CH3 , R1= j O j=1-16. 10 15 20 В двогорлий реактор об'ємом 50 мл, обладнаний крапельною лійкою та зворотним холодильником з хлоркальцієвою трубкою, вносили 0,005 моль (2,068 г) Glu-St та 0,0055 моль діестеру діетиленгліколю 2-[(трет-бутоксикарбоніл)аміно]пентандіонової кислоти ПЕГ-100-GluBoc-ПЕГ-100 формули 1 при n=2 (2,32 г) і 15 мл метилену хлористого. Реакційну масу охолоджували до 278-280 К і в реактор повільно протягом 45 хв прикапували розчин дициклогексилкарбодііміду 0,0055 моль (1,13 г) в 5 мл метилену хлористого та розчин 4диметиламінопіридину 5,5-10"4 моль (0,067 г) в 1 мл метилену хлористого. Реакційну суміш витримували при 288 К протягом 3 год., потім 3 години при 308 К. Реакційну масу охолоджували і фільтрували, а фільтрат упарювали. Для очищення висушений залишок розчиняли в бензолі, створюючи 10 %-й розчин і промивали насиченим розчином NaCl. Після упарювання бензолу та сушіння над фосфорним ангідридом у вакуумі отримували 3,35 г кополіестеретеру формули (3). Вихід 76,3 %. 5 UA 87934 U O O C O O O O O C C O O O HN O NH C O (CH2) CH3 CH3 O O C CH3 m CH3 5 (3) Для видалення третбутилоксикарбонільної (Вос-) захисної групи зі складу полімеру 2 г сухого поліестеретеру розчиняли у 10 мл 50 %-го розчину трифлуороцтової кислоти в метилені хлористому. Розчин перемішували протягом 2 год. і упарювали розчинник у вакуумі. Висушений поліестеретер розчиняли в метилені хлористому і осаджували в гексан. Переосадження повторювали двічі. Продукт сушили до постійної ваги і отримували кополіестеретер з первинною аміногрупою у вигляді солі трифлуороцтової кислоти - [ПЕГ-100-Glu-NH2+(TFA-)ПЕГ-100-Glu-St]m. Одержували 1,72 г кополіестеретеру формули (4). Вихід 85 %. 10 O O C CH2 CH2 CH C O ( CH2 CH2 NH C H2 C O O C O O) n CH2 CH2 C CH O + F CH2 CH2 O) n NH3 O F O ( CH2 m O F CH3 15 20 25 (4) Приклад 5. Здійснювали аналогічно прикладу 4, але як діол використовували діестер на основі поліетердіолу ПЕГ-600 та 2-[(трет-бутоксикарбоніл)аміно]пентандіонової кислоти ПЕГ600-FluВос-ПЕГ600 формули (4 при n=12-13). Отримували 8,3 г кополіестеретеру. Вихід 70 %. Приклад 6. Здійснювали аналогічно прикладу 4, але як діол використовували діестерну основу поліетердіолу ПЕГ-1000 та 2-[(трет-бутоксикарбоніл)аміно] пентандіонової кислоти ПЕГ1000Glu-Boc-ПЕГ1000 формули (4 при n=22-23), а як дикислоти 2-[додеканоїламіно]-пентандіонову. Отримували 9,51 г кополіестеретеру. Вихід 68 %. Для вивільнення аміногрупи з її сольової форми (приклади 4-6) кополіестеретер розчиняли в хлороформі насичували осушеним аміаком і після відділення аміачної солі трифлуороцтової кислоти фільтруванням, упарення фільтрату та сушіння у вакуумі до постійної маси практично кількісно одержували кополіестеретери з первинною аміногрупою. O O G E J O C CH2 CH2 CH C K NH D H2C C O O ( CH2 CH2 O) G E J CH2 CH2 CH H (I) O C H (I) C K1 n NH2 O ( CH2 CH2 O ) n O m CH2 F B CH3 A (5) 6 UA 87934 U Таблиця 2 Віднесення сигналів протонів H1-NMR-спектра в дейтероацетоні кополіестеретеру 2[додеканоїламіно]пентандіонової кислоти (GluL) та ПЕГ1000 з первинною аміногрупою, елементарна ланка якого відповідає формулі (5) Віднесення Зсув Тип А 0,87 т H3C CH2 CH2 Lauroyl 1,00 3 В 1,24 м H3C (CH2)8 CH2 Lauroyl 5,3 16 С 1,41 с Boc 0,2 0 Lauroyl 0.70 2 Glu, Glu 1,41 4 Lauroyl 0.68 2 Glu, Glu 1.40 4 PEG 31,8 96 PEG 2,69 8 Glu 0,69 2 (H3C)3C O Фрагмент Інтеграл Кількісткість протонів у фрагменті Позн. N H C O D 1,61 м (CH2)7 CH2 CH2 NH C O O Е 1,9-2,0 C шм O (CH2)7 F 2,20 CH2 O C O C CH2 CH2 м CH NH CH2 NH O O G 2,42 м Н 3,65 м C 4,2-4,3 CH2 O CH2 O І CH O CH2 (CH2 C NH CH2 O CH2)n CH2 O O O CH2 C м O CH2 J 4,6 CH2 К 6,5-6,8 6,8-7,0 ш O O CH C NH ш CH2 К1 C NH м CH O CH C O + NH3 7 1 Glu O Glu 1 O UA 87934 U Таблиця 3 Характеристики поліестеретерів, отриманих у прикладах 4-6 № Прикладу 5 6 5 Вміст аміногруп % -OH 2,2 12050 78 -OH 0,89 10500 22 -OH 0,6 7500 12 [ПЕГ-100-Glu-NH2-ПЕГ-100Glu-St]m [ПЕГ-600-Glu-NH2-ПЕГ-600Glu-St]m [ПЕГ-1000-Glu-NH2-ПЕГ1000-Glu-L]m 4 Молярна маса Ступінь поліестеретеру поліконденсації (GPC), г/моль Кінцеві групи Поліестеретер (ф-ла 5) Вміст аміногруп встановлений потенціометричним титруванням становить від 2,2 % у кополіестеретері, отриманому в прикладі 4 до 0,6 % у поліестеретері, отриманому у прикладі 6, що добре узгоджується з їх вмістом у кожній елементарній ланці кополіестеретеру формула (2). ФОРМУЛА КОРИСНОЇ МОДЕЛІ 10 15 Спосіб одержання кополіестеретерів двоосновних природних -амінокислот, що включає взаємодію двоосновної N-захищеної амінокислоти та поліетердіолу-поліоксіетилену (ПЕГ) з утворенням діестеру та його кополіконденсацію з утворенням кополіестеретеру та наступним видаленням захисних труп трифлуороцтовою кислотою в метилені хлористому, який відрізняється тим, що як N-захищену амінокислоту використовують 2-[(третбутоксикарбоніл)аміно]пентандіонову кислоту (Glu(Boc)), взаємодію проводять при мольному співвідношенні Glu(Boc):ПЕГ не менше як 1:2,2, діестер отримують з кінцевими гідроксильними групами формули O H O O O (CH2) n k O O n CH3 NH O H CH3 O , CH3 де k=1 або 2; n=2-25, і кополіконденсують його за реакцією Стегліха з 2-(алканоїламіно)пентандіоновою кислотою (Glu-R) з одержанням кополіестеретеру O O (CH2) O HN O O k O n (CH2) O H2N k n O O R m , де k=1 або 2; n=2-25, R= C (CH2) j CH3 , O 20 j=1-16, з первинними аміногрупами. Комп’ютерна верстка Г. Паяльніков Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 8
ДивитисяДодаткова інформація
Автори англійськоюVarvarenko Serhii Mykolaiovych, Samaryk Volodymyr Yaroslavovych, Voronov Andrii Stanislavovych, Nosova Natalia Herianivna, Tarnavchyk Ihor Tarasovych, Voronov Stanislav Andriiovych
Автори російськоюВарваренко Сергей Николаевич, Самарик Владимир Ярославович, Воронов Андрей Станиславович, Носова Наталия Гериановна, Тарнавчик Игорь Тарасович, Воронов Станислав Андреевич
МПК / Мітки
МПК: C08G 63/12, C08G 63/685
Мітки: кополіестеретерів, природних, a-амінокислот, одержання, двоосновних, спосіб
Код посилання
<a href="https://ua.patents.su/10-87934-sposib-oderzhannya-kopoliestereteriv-dvoosnovnikh-prirodnikh-a-aminokislot.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання кополіестеретерів двоосновних природних a-амінокислот</a>
Попередній патент: Робоче обладнання драглайна
Наступний патент: Спосіб утилізації двоокису вуглецю у морських газогідратних родовищах
Випадковий патент: Батутний комплекс «sky park»












