Спосіб одержання препарату із пробіотичними властивостями “епібактерин” для лікування хворих із захворюваннями шкіри
Номер патенту: 53782
Опубліковано: 25.10.2010
Автори: Димент Галина Семенівна, Янковський Дмитро Станіславович, Широбоков Володимир Павлович
Формула / Реферат
1. Спосіб одержання препарату з пробіотичними властивостями для лікування хворих із захворюваннями шкіри, що передбачає спільне культивування в молочному середовищі полівидового мультисимбіозу біфідобактерій, лактобацил і пропіоновокислих бактерій, культивування клітин і відділення біомаси, який відрізняється тим, що у складі препарату з біфідобактерій використовують штами Bifidobacterium adolescentis ІMB В-7148 й В. adolescentis ІMB В-7112, з лактобацил -Lactobacillus fermentum ІMB В-7133, L. fermentum ІMB В-7146, L. acidophilus ЦМПМ В-2846, L. delbrueckii ssp. bulgaricus ВКПМ В-5810, L. casei ВКПМ В-5724, L. plantarum ІMB В-7116, L. helveticus IMB-7115, із пропіоновокислих бактерій - Propionibacterium freudenreichii ssp. shermanii ВКПМ B-4544 і ВКПМ В-4545 й P. acidipropionici ВКПМ В-5723 і ВКПМ В-5800, а співвідношення між лактобацилами, біфідобактеріями й пропіоновокислими бактеріями встановлюють 2:1:1, при цьому одержану біомасу змішують у співвідношенні 1:1-1:2 з 5-6 %-ою суспензією гелю дрібнодисперсного бентоніту.
2. Спосіб за п. 1, який відрізняється тим, що до складу препарату вводять спиртовий екстракт прополісу.
3. Спосіб за п. 1, який відрізняється тим, що до складу препарату вводять йод у вигляді водного або спиртового розчину дрібнокристалічного йоду і йодиду калію.
4. Спосіб за п. 1, який відрізняється тим, що до складу препарату вводять протимікозні препарати.
Текст
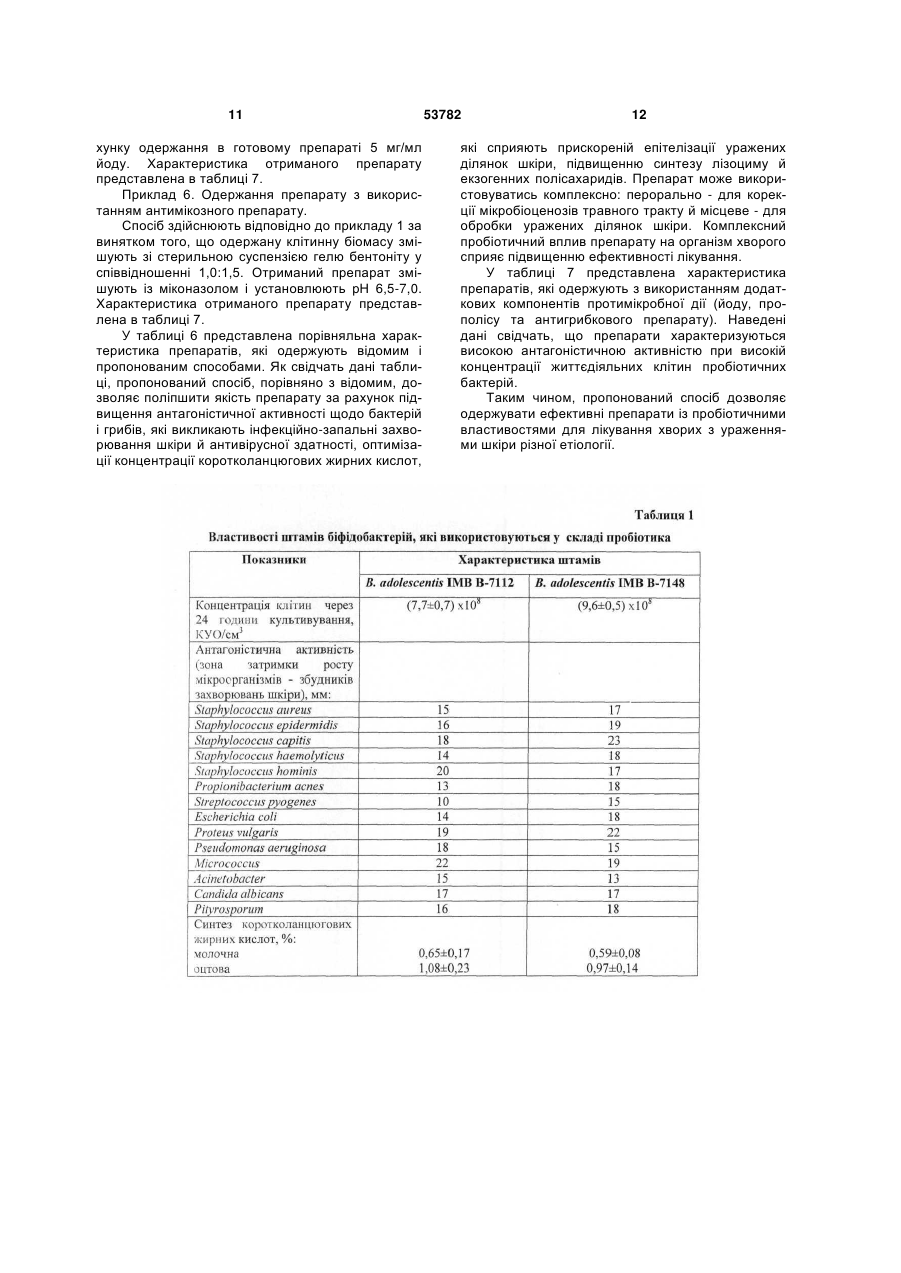
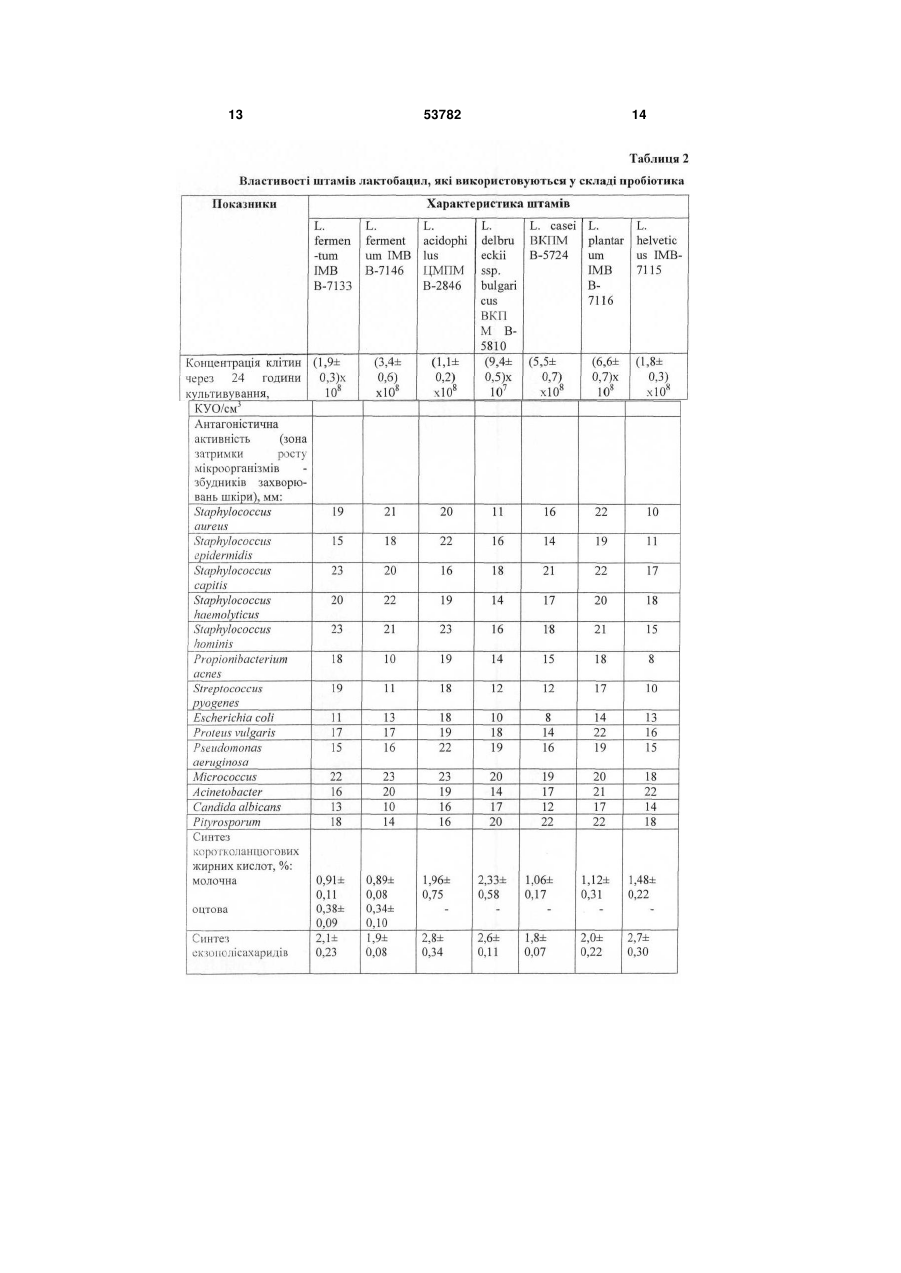
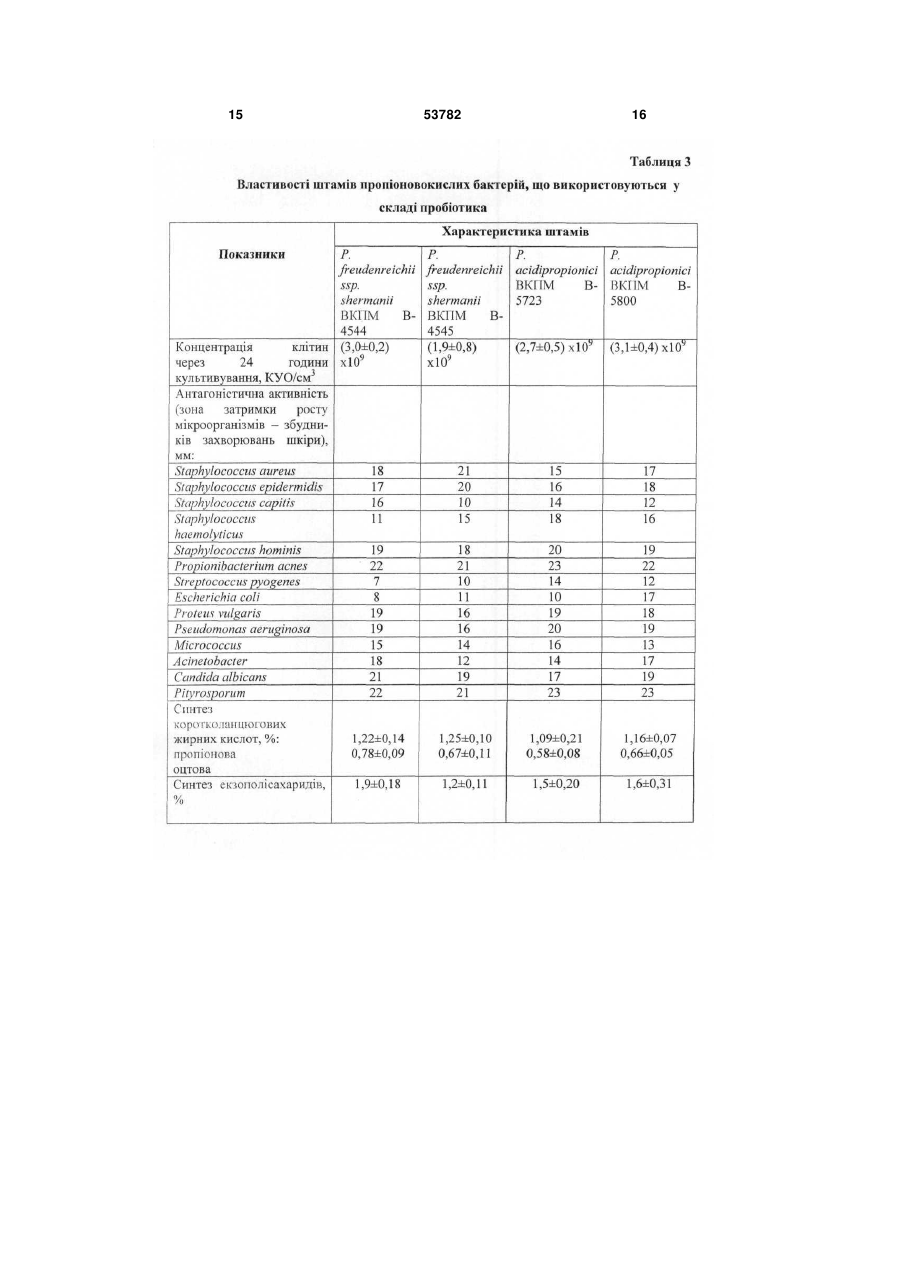
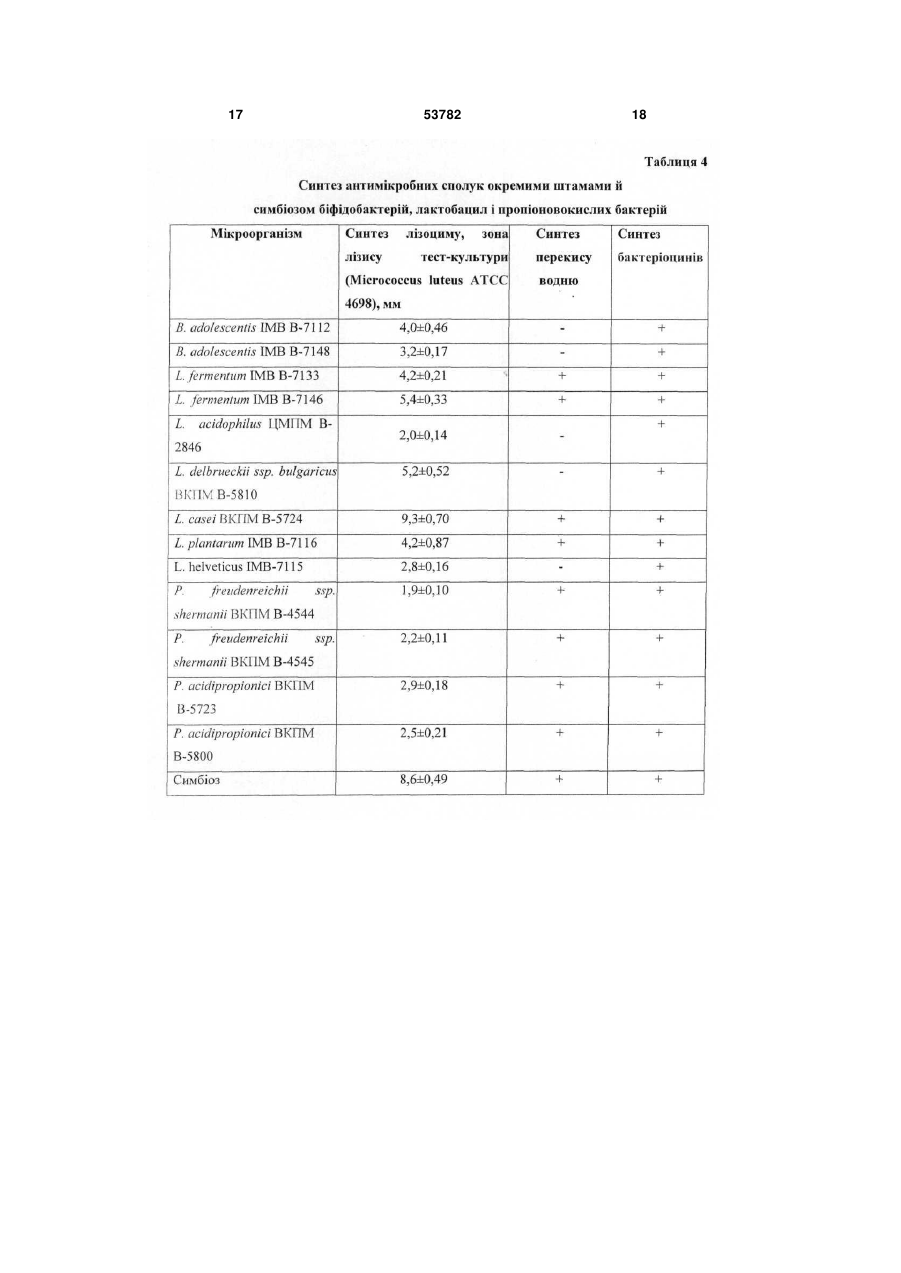
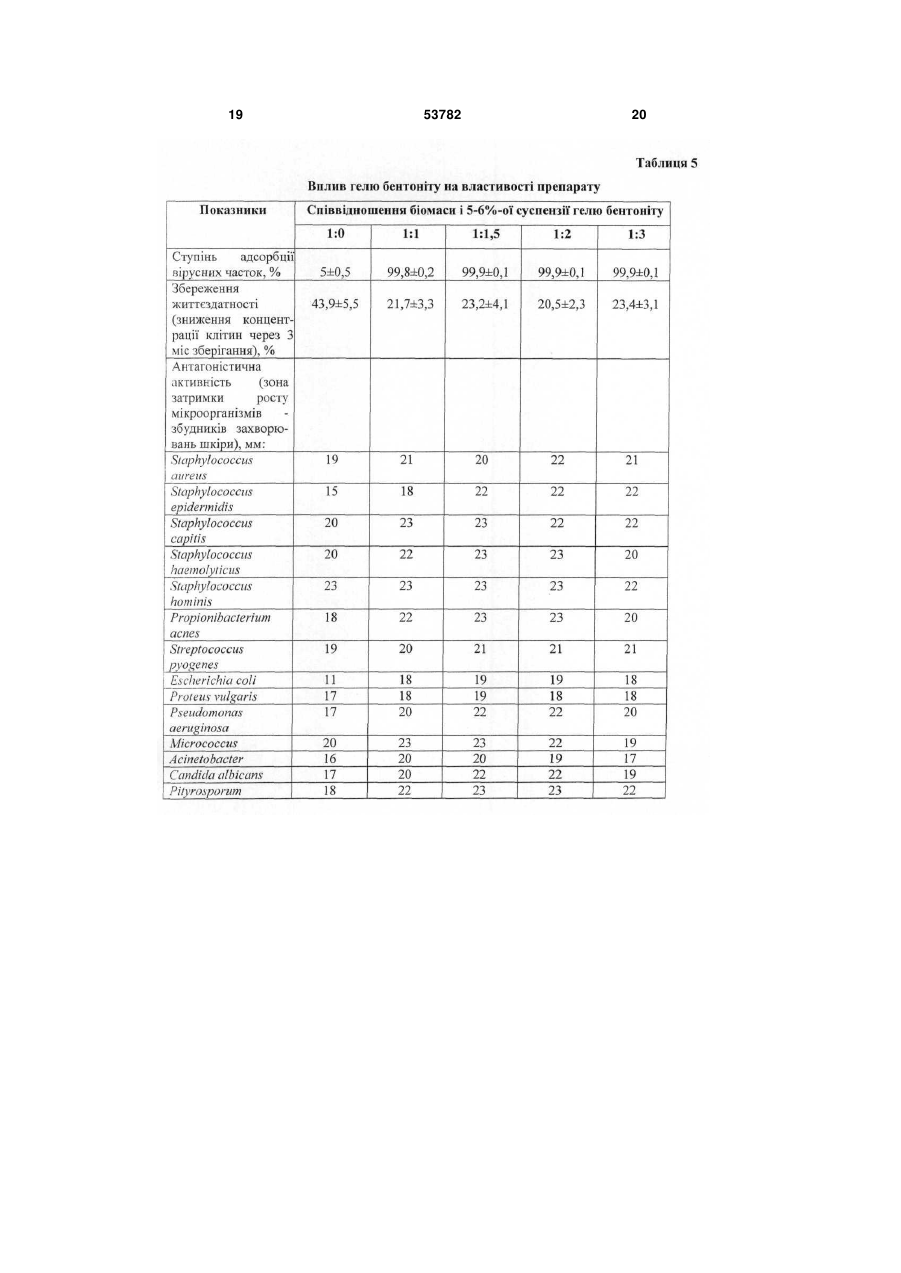
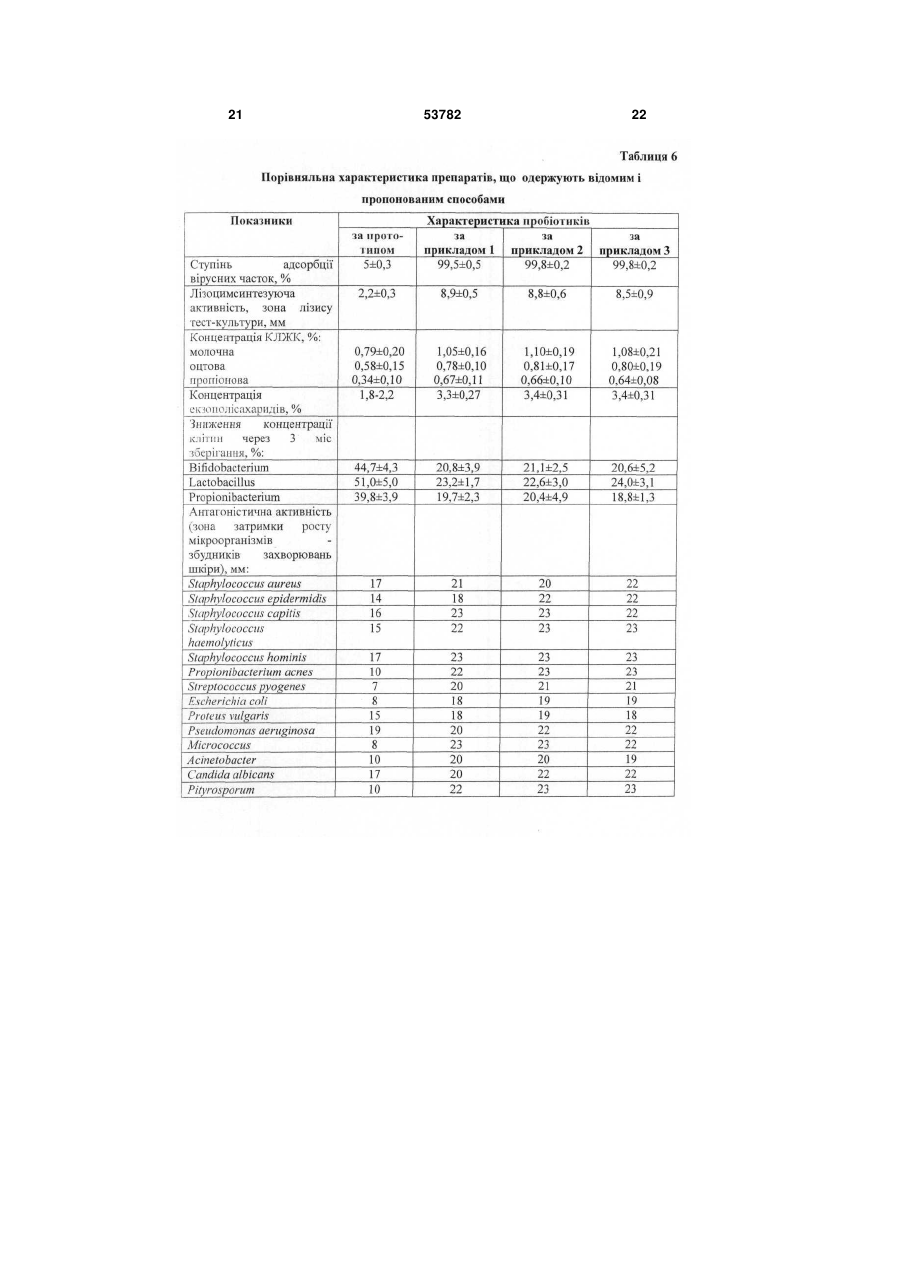
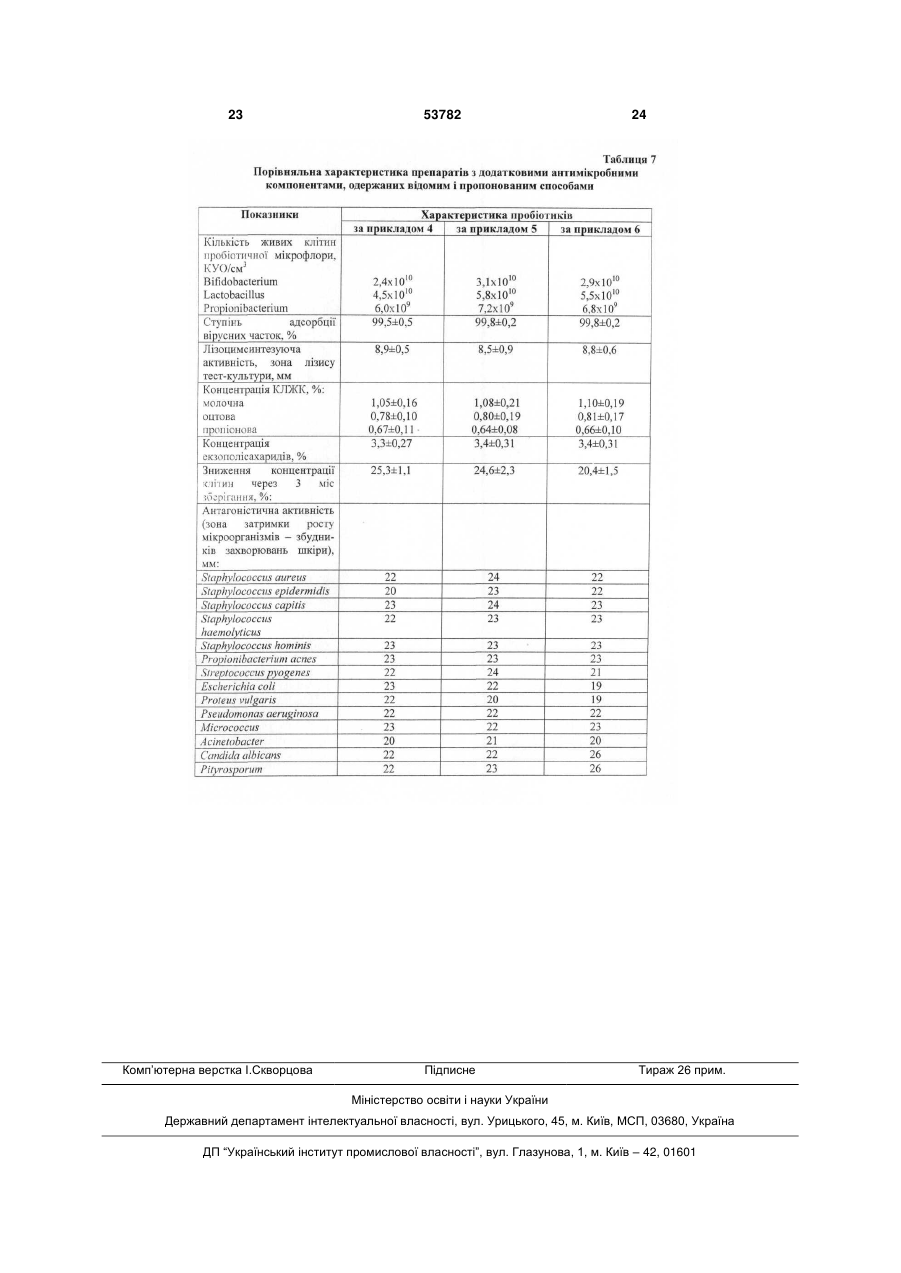
1. Спосіб одержання препарату з пробіотичними властивостями для лікування хворих із захворюваннями шкіри, що передбачає спільне культивування в молочному середовищі полівидового мультисимбіозу біфідобактерій, лактобацил і пропіоновокислих бактерій, культивування клітин і відділення біомаси, який відрізняється тим, що у складі препарату з біфідобактерій використовують штами Bifidobacterium adolescentis ІMB В-7148 й В. adolescentis ІMB В-7112, з лактобацил -Lactobacillus fermentum ІMB В-7133, L. fermentum ІMB В-7146, L. acidophilus ЦМПМ В U 2 (19) 1 3 ційних інфекційно-запальних ускладнень. Комплексний пробіотичний вплив на мікрофлору шкіри й інших мікробних екосистем, насамперед, травного тракту, що грає важливу патогенетичну роль у розвитку дерматозів, а також у запаленні післяопераційних, опікових й інших ран, є одним з найбільш перспективних підходів до відновлення складу й функцій нормофлори організму в цілому. Це, у свою чергу, дозволить підвищити ефективність лікування хворих з ураженнями шкіри різної етіології. Відома мазь «Настасія» для лікування опікових ран, що включає 90-95 % основи й 5-10 % рідкого біфідобактерину, при цьому основа містить медичний вазелін, емульгатор й очищену воду (патент України №26538, А61К35/74, 1999). Використання в складі мазі життєдіяльних клітин біфідобактерій сприяє підвищенню її ефективності й зниженню ризику розвитку ускладнень, однак обмеження бактеріального складу препарату тільки біфідобактеріями, не пристосованими до життя в аеробних умовах, не забезпечує достатній ступінь санації області ураження й загоєння шкіри. Крім того, обмеження лікування місцевою обробкою області ураженої шкіри без нормалізації мікробної екосистеми хворого в цілому не може забезпечити ефективного лікування. Відома мазь «Емулакт» для лікування й профілактики інфекційно-запальних гінекологічних захворювань і дисбактеріозів, що містить як активний біологічний компонент стабілізовану рідку ку7 льтуру лактобактерій з концентрацією клітин 10 1010 КУО/мл у кількості 5-50 %, при цьому стабілізація культури досягається за рахунок її переводу в гелеподібний стан за допомогою додавання поверхнево-активних речовин в кількості 3-5 % і мазевої основи до 100 % (Патент РФ №2183963, А61К35/74, 9/06, А61Р31/04, 2002). Використання в складі мазі одного або декількох штамів лактобактерій видів Lactobacillus plantarum, Lactobaciluus fermentum й Lactobacillus acidophilus збільшує її бактерицидні властивості. Недоліком мазі є обмеженість сфери її застосування лікуванням гінекологічних захворювань. Найбільш близьким до способу, що заявляється, є спосіб одержання пробіотика «Симбітер-2», який передбачає спільне культивування в молочному середовищі багатовидового симбіозу молочнокислих бактерій, біфідобактерій, пропіоновокислих й оцтовокислих бактерій видів Bifidobacterium bifidum, В. longum, В. infantis, В. breve, В. adolescentis, Lactococcus lactis, Streptococcus salivarius ssp. thermophilus, Lactobacillus acidophilus, L. casei, L. plantarum, L. gasseri, L. brevis, Propionibacterium frendenreichii, P. acidipropionici й Acetobacter aceti, при цьому попередньо одержаний консорціум молочнокислих стрептококів і лактобацил поєднують із консорціумом біфідобактерій, пропіоновокислих й оцтовокислих бактерій у співвідношенні 1:4 (Патент України № 28040, А23С9/12, C12N1/20, 2000) -прототип. Пробіотик, одержаний відомим способом, пригнічує ріст широкого кола патогенних й умовнопатогенних мікроорганізмів, які викликають розвиток дисбіозів й інфекцій кишечнику й сечостатевої 53782 4 системи. У зв'язку з цим пробіотик проявляє високу ефективність при лікуванні хворих даними захворюваннями. Вміст у складі пробіотика широкого спектра мікроорганізмів з високою антагоністичною активністю дозволяє усувати вогнища мікроекологічних розладів у кишечнику й урогенітальному тракті, а також поліпшувати стан шкіри при обробці препаратом області її ураження. Однак у зв'язку з тим, що антагоністична активність препарату спрямована на пригнічення росту патогенних й умовно-патогенних мікроорганізмів вагінального й кишкового походження, він недостатньо ефективно загоює ураження шкіри при його місцевому використанні через низьку активність інгібування ряду збудників шкірних інфекційно-запальних процесів. Препарат не містить додаткових компонентів, що сприяють більш ефективній санації уражених ділянок шкіри від мікробних і тканинних токсинів, шкідливих метаболітів і ферментів, а також інших агресивних сполук. Завданням корисної моделі є створення способу одержання препарату із пробіотичними властивостями для лікування хворих із інфекційнозапальними, алергійними, опіковими й іншими ураженнями шкіри, у якому шляхом зміни складу мікроорганізмів і використання гелю дрібнодисперсного бентоніту забезпечується розширення спектра антагоністичної активності препарату й сфери його застосування. Поставлене завдання вирішується тим, що в способі одержання препарату із пробіотичними властивостями, що передбачає спільне культивування полівидового мультисимбіозу біфідобактерій, лактобацил і пропіоновокислих бактерій, культивування клітин і відділення біомаси, відповідно до корисної моделі, у складі пробіотика з біфідобактерій використовують штами Bifidobacterium adolescentis IMB В-7148 й В. adolescentis IMB В7112, з лактобацил - Lactobacillus fermentum IMB В-7133, L. fermentum IMB В-7146, L. acidophilus ЦМПМ В-2846, L. delbrueckii ssp. bulgaricus ВКПМ В-5810, L. casei ВКПМ В-5724, L. plantarum IMB В7116, L. hefveticus ІМВ-7115, із пропіоновокислих бактерій - Propiombacterium freudenreichii ssp. shermanii ВКПМ B-4544, P. freudenreichii ssp. shermanii ВКПМ B-4545, P. acidipropionici ВКПМ В5723 й P. acidipropionici ВКПМ В-5800, співвідношення між лактобацилами, біфідобактеріями й пропіоновокислими бактеріями становить 2:1:1, а отриману біомасу пробіотичних бактерій змішують у співвідношенні 1:1-1:2 з 5-6 %-м гелем дрібнодисперсного бентоніту. Крім того, до складу препарату може вводитися спиртовий екстракт прополісу із розрахунку одержання в готовому препараті прополісу; або йод у вигляді водного або спиртового розчину; або протимікозні препарати. Пропонований спосіб передбачає використання в складі пробіотика штамів біфідобактерій Bifidobacterium adolescentis IMB В-7148 й В. adolescentis IMB B-7112; штамів лактобацил Lactobacillus fermentum IMB В-7133, L. fermentum IMB B-7146, L. acidophilus ЦМПМ B-2846, L. delbnieckii ssp. bulgaricus ВКПМ B-5810, L. casei ВКПМ B-5724, L. plantarum IMB B-7116 й L. helveticus IMB-7115; штамів пропіоновокислих бак 5 терій -Propionibacterium freudenreichii ssp. shermanii ВКПМ В-4544, P. freudenreichii ssp. shermanii ВКПМ B-4545, P. acidipropionici ВКПМ В5723 й P. acidipropionici ВКПМ В-5800. Властивості штамів представлені в табл. 1-4. Як видно з даних таблиць 1 й 4, штами біфідобактерій, відібрані до складу препарату, активно пригнічують ріст патогенних й умовно-патогенних мікроорганізмів, що є етіологічним фактором розвитку інфекційно-запальних захворювань шкіри, синтезують бактеріоцини, молочну й оцтову кислоти, які мають високі бактерицидні властивості щодо гнильної мікрофлори, а також сприяють прискоренню процесів репарації ушкодженої шкіри. Властивості штамів лактобацил, що використовуються у пропонованому способі, представлені в таблицях 2 і 4. Штами характеризуються здатністю формувати високі рівні клітинних популяцій, активно пригнічують розвиток збудників шкірних інфекцій, синтезують екзополісахариди, молочну кислоту або суміш молочної й оцтової кислот, бактеріоцини, лізоцим і перекис водню. Пропіоновокислі бактерії, відібрані для використання в складі препарату, інгібують ріст патогенних й умовно-патогенних мікроорганізмів, які вегетують на шкірі при її патологічних змінах. Штами синтезують бактеріоцини (пропіоніни), пропіонову й оцтову кислоти, які характеризуються високими бактерицидними властивостями. Зокрема, пропіонова кислота активно пригнічує розвиток грибів й «шкірних» видів пропіоновокислих бактерій, що є збудниками акне й інших інфекційнозапальних уражень шкіри. Крім того, пропіонова й оцтова кислоти сприяють прискоренню процесу епітелізації ушкодженої тканини. Завдяки даним властивостям, пропіоновокислі бактерії вносять значний вклад у сумарну антагоністичну активність пропонованого препарату (табл. 3, 4). Співвідношення між лактобацилами, біфідобактеріями й пропіоновокислими бактеріями становить 2:1:1. Дане співвідношення є найбільш оптимальним для досягнення позитивного ефекту. Зміна співвідношення у бік зниження концентрації лактобацил негативно позначається на антагоністичній активності препарату щодо гнильних мікроорганізмів. Збільшення концентрації лактобацил приводить до зниження кількості біфідобактерий і пропіоновокислих бактерій і внаслідок цього до зниження антагоністичної активності щодо збудників мікозних дерматитів і вугрової висипки, наприклад акне. Зміна співвідношення між бактеріальними групами в будь-якому іншому напрямку негативно позначається на спектрі антагоністичної активності препарату й здатності інтенсифікувати процес репарації ушкоджених шкірних покривів. Пропонований спосіб передбачає використання в складі пробіотика гелю дрібнодисперсного бентоніту. Бентоніт, очищений від забруднюючих компонентів, є абсолютно безпечним для здоров'я людини. Він відноситься до природних глин і йому властиві всі позитивні ефекти, об'єднані в поняття «глинотерапія». Одержана спеціальним способом, дрібнодисперсна натрієва форма цього природного матеріалу, очищеного від сторонніх домішок і грубих часток бентоніту, має високі вологоутриму 53782 6 ючі, іонообмінні й адсорбційні властивості. Зокрема, гель дрібнодисперсного бентоніту має високі адсорбційні властивості щодо вірусів, мікробних і тканинних токсинів й інших шкідливих сполук, що утворюються внаслідок перебігу інфекційнозапального процесу на шкірі. Гель не зв'язує бактеріальні клітини, тому не здатний порушувати нормальний мікробний баланс шкірного біотопу й поглиблювати мікроекологічні порушення. Разом з тим він інактивує деякі ферменти патогенності збудників хвороб, зокрема, нуклеази. Відповідно до пропонованого способу, гель дрібнодисперсного бентоніту змішують із концентрованою біомасою клітин про біотичних бактерій. При цьому дрібнодисперсний сорбент зв'язується з поверхневими структурами бактеріальних клітин і покриває їх захисним шаром, захищаючи від впливу інгібуючих факторів. Це поліпшує умови для прояву бактеріями препарату пробіотичної активності й продовжує строк зберігання препарату. Завдяки здатності активно зв'язувати воду, набухати й формувати гелі, бентоніт не здатний впливати на ушкоджену ділянку шкіри, а навпроти, має обволікаючі властивості й сприяє його санації й прискоренню загоєння шляхом зв'язування й «витягування» з рани агресивних і токсичних сполук. За рахунок здатності нормалізувати кислотнолужний баланс, бентоніт оптимізує перебіг біохімічних процесів. Перелічені особливості гелю бентоніту дозволяють довгостроково використовувати одержаний пропонованим способом комплексний бактеріально-бентонітовий препарат, у тому числі при лікуванні дітей раннього віку, імунокомпроментованих осіб й хворих з підвищеною чутливістю до антибіотиків й інших засобів медикаментозної хіміотерапії без небезпеки розвитку негативних ефектів. У той же час здатність гелю бентоніту активно адсорбувати віруси дозволяє ефективно використовувати препарат при вірусних ураженнях шкіри. Як показали спеціально проведені дослідження, гель бентоніту має високі протекторні властивості щодо біомаси багатовидового симбіозу, що є бактеріальною основою препарату. Зв'язуючи кисень і його токсичні похідні, гель бентоніту оптимізує умови для розвитку анаеробної пробіотичної флори. З огляду на проліферацію аеробних і факультативно-анаеробних умовно-патогенних мікроорганізмів на уражених ділянках шкіри, використання бентоніту в складі препарату інгібує їхній розвиток за рахунок зв'язування кисню й сприяє пригніченню інфекційно-запального процесу або попередженню його розвитку. У той же час, анаеробна мікрофлора препарату, що перебуває під захистом гелю бентоніту, активно пригнічує патогенну анаеробну бактеріальну флору. Таким чином, пропонований спосіб забезпечує синергізм позитивного впливу гелю бентоніту й пробіотичних бактерій, зокрема за рахунок збільшення спектра антагоністичної активності щодо патогенних й умовно-патогенних мікроорганізмів. Гель бентоніту впливає на якість препарату. У присутності гелю бентоніту, який одержують спеціальним способом, значно краще зберігається бактеріальний склад й активність пробіотичної біомаси (табл. 5). 7 Пропонований спосіб передбачає використання гелю бентоніту з концентрацією сухих речовин 5-6 %. Зниження концентрації бентоніту в гелі менш 5 % зменшує ефективність препарату за рахунок зниження в ньому концентрації життєдіяльних клітин пробіотичних бактерій, а також зниження антивірусної активності й терміну зберігання препарату. Збільшення концентрації бентоніту в гелі понад 6 % недоцільно, оскільки не впливає на ефективність препарату, але ускладнює технологію одержання гелю. Клітинну біомасу змішують із 5-6 %-им гелем бентоніту в співвідношенні 1:1-1:2. Дане співвідношення є найбільш оптимальним. Зміна співвідношення у бік зменшення частки гелю бентоніту приводить до погіршення лікувальних властивостей препарату. Збільшення кількості гелю бентоніту недоцільно, оскільки приводить до зниження концентрації клітин у препараті і його активності. Спосіб передбачає можливість додаткового введення до складу препарату компонентів антимікробної дії, таких як йод, прополіс або протимікозні засоби. Введення даних компонентів сприяє підвищенню антагоністичної активності препарату щодо збудників інфекційно-запальних захворювань шкіри без пригнічення пробіотичних бактерій. Як показали спеціально проведені дослідження, незважаючи на високу антимікробну активність йоду й спиртового екстракту прополісу, за наявності гелю бентоніту, який одержують спеціальним способом, концентрація життєдіяльних клітин пробіотичних бактерій у препараті, що містить до 50 мг/мл прополісу або до 5 мг/мл йоду, залишається незмінною протягом 2-3 місяців зберігання. Спосіб здійснюють таким чином. Як середовище культивування використовують молоко із вмістом сухих речовин 4-5 %, у яке додають 10 % молока, гідролізованого панкреатином, або 5 % гідролізату казеїну й 1-2 % натрію лимоннокислого 3-заміщеного. Середовище стерилізують, охолоджують до температури культивування, інокулюють симбіозом пробіотичних бактерій і ферментують для накопичення біомаси, яку відокремлюють від культуральної рідини центрифугуванням. Для готування інокуляту використовують мультикомпонентний симбіоз лактобацил, пропіоновокислих і біфідобактерій. Для створення симбіозу використовують культури нижчеперелічених штамів: Bifidobacterium adolescentis IMB В-7148 Bifidobacterium adolescentis IMB В-7112 Lactobacillus fermentum IMB B-7133 Lactobacillus fermentum IMB B-7146 Lactobacillus acidophilus ЦМПМ B-2846 Lactobacillus helveticus IMB B-7115 Lactobacillus delbrueckii ssp. bulgaricus ВКПМ B-5810 Lactobacillus casei ВКПМ В-5724 Lactobacillus plantarum IMB B-7116 Propionibacterium freudenreichii ssp. shermanii ВКПМ В-4544 Propionibacterium freudenreichii ssp. shermanii ВКПМ В-4545 53782 8 Propionibacterium acidipropionici ВКПМ В-5723 Propionibacterium acidipropionici ВКПМ В-5800. Культури з'єднують із розрахунку одержання співвідношення між лактобацилами, біфідобактеріями й пропіоновокислими бактеріями 2:1:1. Отриманий комплекс штамів вносять у стерильне знежирене молоко зі вмістом сухих речовин 10 %. Інокульоване молоко ферментують протягом 16-24 годин при температурі 34-37 °С. Спеціально проведеними дослідженнями встановлено, що при з'єднанні штамів у зазначеному співвідношенні вони формують стійкий мультикомпонентний симбіоз. Одержаний симбіоз використовують як посівний матеріал для одержання інокуляту, який вносять в основну масу середовища культивування. Біомасу клітин, відділену від культуральної рідини, змішують у співвідношенні 1:1-1:2 з 5-6 %-м гелем дрібнодисперсного бентоніту. Для одержання гелю бентоніту сухий бентоніт диспергують у воді з додаванням вуглекислого натрію, центрифугують. Осад суспендують у воді, центрифугують для відділення забруднюючих речовин і грубих часток бентоніту. Після багаторазового фракціонування одержують дрібнодисперсну фракцію бентоніту, яку суспендують у бідистильованій воді до одержання 5-6 %-ої суспензії гелеподібної консистенції, а потім стерилізують. Корисна модель пояснюється прикладами. Приклад 1. Одержання препарату із пробіотичними властивостями для лікування хворих з опіковими ураженнями шкіри. Для приготування інокуляту до 25 л стерильного знежиреного молока з 10 % сухих речовин вносять 1,25 л культури мультикомпонентного симбіозу лактобацил, пропіоновокислих і біфідобактерій при наступному співвідношенні штамів: Bifidobacterium adolescentis IMB В-7148 - 6 Bifido bacter ium adolescentis IMB B-7112-6 Lactobacillus fermentum IMB B-7133 - 4 Lactobacillus fermentum IMB B-7146 - 4 Lactobacillus acidophilus ЦМПМ B-2846 - 4 Lactobacillus helveticus IMB B-7115-2 Lactobacillus delbrueckii ssp. Bulgaricus BKПM B-5810-2 Lactobacillus casei ВКПМ B-5724 - 4 Lactobacillus plantarum IMB B-7116 - 4 Propionibacterium freudenreichii ssp. shermanii ВКПМ В-4544 - 3 Propionibacterium freudenreichii ssp. shermanii ВКПМ В-4545 - 3 Propionibacterium acidipropionici ВКПМ B-5723 3. Propionibacterium acidipropionici ВКПМ B-5800 3. Інокульоване молоко ферментують протягом 18 годин при температурі 34 °С. Готовий інокулят характеризується густою в'язкою консистенцією, кислотністю 102°Т, рН 4,4, концентрацією живих клітин -7,9 х 108 КУО/см3. Для готування середовища культивування 25 кг сухого знежиреного молока розчиняють в 100 л водопровідної води. До розчиненого молока доливають воду (до 500 л) з розрахунку одержання відновленого молока зі вмістом сухих речовин 5 %. Відновлене молоко стерилізують при температурі 9 121 °С із витримкою протягом 25 хвилин, охолоджують до 37 °С і вносять 5 % інокуляту. Одночасно з інокулятом уводять 10 % стерильного панкреатичного гідролізату молока й 2 % натрію лимоннокислого 3-заміщеного (у вигляді стерильного 50 %-го розчину). Процес культивування проводять 24 години при температурі 36 °С і рН6,0. Концентрація життєдіяльних клітин наприкінці культивування становить 1,5х1010 КУО/см3. Клітинну біомасу відокремлюють центрифугуванням і змішують її в співвідношенні 1:1 з 5 %-ю суспензією гелю бентоніту. Характеристика одержаного препарату представлена в таблиці 6. Приклад 2. Одержання препарату із пробіотичними властивостями для лікування хворих з дерматитами. Для готування інокуляту до 50 л стерильного знежиреного молока з 10 % сухих речовин вносять 2,5 л культури мультикомпонентного симбіозу лактобацил, пропіоновокислих і біфідобактерій при наступному співвідношенні штамів: Bifidobacterium adolescentis IMB В-7148 - 8 Bifidobacterium adolescentis IMB B-7112-4 Lactobacillus fermentumIMB B-713 3 - 3 Lactobacillus fermentum IMB В-7146 - 5 Lactobacillus acidophilus ЦМПМ B-2846 - 2 Lactobacillus helveticus IMB B-7115 - 4 Lactobacillus delbrueckii ssp. bulgaricus ВКПМ B-5810 - 3 Lactobacillus casei ВКПМ B-5724 - 4 Lactobacillus plantarum IMB B-7116 - 3 Propionibacterium freudenreichii ssp. shermanii ВКПМ B-4544 - 2 Propionibacterium freudenreichii ssp. shermanii ВКПМ B-4545 - 4 Propionibacterium acidipropionici ВКПМ B-5723 5. Propionibacterium acidipropionici ВКПМ B-5800 1. Інокульоване молоко ферментують протягом 20 годин при температурі 37 °С. Готовий інокулят має густу, в'язку консистенцію, кислотність 94°Т, рН 4,5, концентрація живих клітин - 8,9х108 КУО/см3. Для готування середовища культивування 40 кг сухого знежиреного молока розчиняють у 100 л водопровідної води. До розчиненого молока додають воду (до 1000 л) з розрахунку одержання відновленого молока зі вмістом сухих речовин 4 %. Відновлене молоко стерилізують при температурі 121 °С із витримкою протягом 30 хвилин. Охолоджують до температури 36 °С і вносять 4 % інокуляту. Одночасно з інокулятом уводять 10 % стерильного панкреатичного гідролізату молока й 1 % натрію лимоннокислого 3-заміщеного (у вигляді стерильного 50 %-го розчину). Процес культивування проводять 22 години при температурі 37 °С і рН 6,5. Концентрація життєдіяльних клітин наприкінці культивування становить 1,2х1010 КУО/см3. Клітинну біомасу відокремлюють центрифугуванням і змішують її в співвідношенні 1:2 з 6 %-м гелем бентоніту. Характеристика отриманого препарату представлена в таблиці 6. 53782 10 Приклад 3. Одержання препарату із пробіотичними властивостями для обробки хірургічних ран. Для готування інокуляту до 30 л стерильного знежиреного молока з 10 % сухих речовин вносять 1,5 л культури мультикомпонентного симбіозу лактобацил, пропіоновокислих і біфідобактерій при наступному співвідношенні штамів: Bifidobacterium adolescentis IMB B-7148 - 5 Bifidobacterium adolescentis IMB B-7112- 7 Lactobacillus fermentum IMB B-7133 - 3 Lactobacillus fermentum IMB B-7146 - 4 Lactobacillus acidophilus ЦМПМ B-2846 - 3 Lactobacillus helveticus IMB B-7115-3 Lactobacillus delbrueckii ssp. bulgaricus ВКПМ B-5810 - 4 Lactobacillus casei ВКПМ В-5724 - 3 Lactobacillus plantarum IMB B-7116 - 4 Propionibacterium freudenreichii ssp. shermanii ВКПМ B-4544 - 4 Propionibacterium freudenreichii ssp. shermanii ВКПМ В-4545 - 3 Propionibacterium acidipropionici ВКПМ B-5723 4. Propionibacterium acidipropionici ВКПМ B-5800 1. Інокульоване молоко ферментують протягом 24 годин при температурі 35 °С. Готовий інокулят характеризується густою, в'язкою консистенцією, кислотністю 91°Т, рН 4,6, концентрацією живих клітин -1,1х109 КУО/см3. Для готування середовища культивування 27 кг сухого знежиреного молока розчиняють у 100 л водопровідної води. До розчиненого молока додають воду (до 600 л) з розрахунку одержання відновленого молока зі вмістом сухих речовин 4,5 %. Відновлене молоко стерилізують при температурі 121 °С із витримкою протягом 35 хвилин, охолоджують до 35 °С і вносять 5 % інокуляту. Одночасно з інокулятом уводять 10 % стерильного панкреатичного гідролізату молока й 1,5 % натрію лимоннокислого 3-заміщеного (у вигляді стерильного 50 %-го розчину). Процес культивування проводять 23 години при температурі 37 °С і рН 6,2. Концентрація життєдіяльних клітин наприкінці культивування становить 2,0х1010 КУО/см3. Клітинну біомасу відокремлюють центрифугуванням і змішують її в співвідношенні 1,0:1,5 з 5,5 %-м гелем бентоніту. Характеристика отриманого препарату представлена в таблиці 6. Приклад 4. Одержання препарату з використанням спиртового екстракту прополісу. Біомасу пробіотичних бактерій і суспензію гелю бентоніту одержують відповідно до приклада 3, за винятком того, що в отриману суміш клітинної біомаси й гелю бентоніту додають спиртовий екстракт прополісу з розрахунку одержання в готовому препараті прополісу в концентрації 50 мг/мл. Характеристика отриманого препарату представлена в таблиці 7. Приклад 5. Одержання препарату з використанням йоду. Спосіб здійснюють відповідно до прикладу 2 за винятком того, що в препарат уводять препарат йоду у вигляді водного або спиртового розчину дрібнокристалічного йоду і йодиду калію з розра 11 хунку одержання в готовому препараті 5 мг/мл йоду. Характеристика отриманого препарату представлена в таблиці 7. Приклад 6. Одержання препарату з використанням антимікозного препарату. Спосіб здійснюють відповідно до прикладу 1 за винятком того, що одержану клітинну біомасу змішують зі стерильною суспензією гелю бентоніту у співвідношенні 1,0:1,5. Отриманий препарат змішують із міконазолом і установлюють рН 6,5-7,0. Характеристика отриманого препарату представлена в таблиці 7. У таблиці 6 представлена порівняльна характеристика препаратів, які одержують відомим і пропонованим способами. Як свідчать дані таблиці, пропонований спосіб, порівняно з відомим, дозволяє поліпшити якість препарату за рахунок підвищення антагоністичної активності щодо бактерій і грибів, які викликають інфекційно-запальні захворювання шкіри й антивірусної здатності, оптимізації концентрації коротколанцюгових жирних кислот, 53782 12 які сприяють прискореній епітелізації уражених ділянок шкіри, підвищенню синтезу лізоциму й екзогенних полісахаридів. Препарат може використовуватись комплексно: перорально - для корекції мікробіоценозів травного тракту й місцеве - для обробки уражених ділянок шкіри. Комплексний пробіотичний вплив препарату на організм хворого сприяє підвищенню ефективності лікування. У таблиці 7 представлена характеристика препаратів, які одержують з використанням додаткових компонентів протимікробної дії (йоду, прополісу та антигрибкового препарату). Наведені дані свідчать, що препарати характеризуються високою антагоністичною активністю при високій концентрації життєдіяльних клітин пробіотичних бактерій. Таким чином, пропонований спосіб дозволяє одержувати ефективні препарати із пробіотичними властивостями для лікування хворих з ураженнями шкіри різної етіології. 13 53782 14 15 53782 16 17 53782 18 19 53782 20 21 53782 22 23 Комп’ютерна верстка І.Скворцова 53782 Підписне 24 Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for prodicing of “epibacterin” preparation having probiotic properties for treatment of patients with skin diseases
Автори англійськоюShyrobokov Volodymyr Pavlovych, Yankovskyi Dmytro Stanislavovych, Dyment Halyna Semenivna
Назва патенту російськоюСпособ получения препарата с пробиотическими свойствами 'эпибактерин' для лечения больных с заболеваниями кожи
Автори російськоюШиробоков Владимир Павлович, Янковский Дмитрий Станиславович, Димент Галина Семеновна
МПК / Мітки
МПК: A23C 9/12, C12N 1/20, A61K 35/74
Мітки: спосіб, одержання, шкіри, пробіотичними, епібактерин, захворюваннями, хворих, властивостями, препарату, лікування
Код посилання
<a href="https://ua.patents.su/12-53782-sposib-oderzhannya-preparatu-iz-probiotichnimi-vlastivostyami-epibakterin-dlya-likuvannya-khvorikh-iz-zakhvoryuvannyami-shkiri.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання препарату із пробіотичними властивостями “епібактерин” для лікування хворих із захворюваннями шкіри</a>
Попередній патент: Спосіб лікування хворих на хронічне обструктивне захворювання легень, сполучене з неалкогольним стеатогепатитом, на тлі туберкульозу легень
Наступний патент: Спосіб діагностики больових синдромів у хворих на розсіяний склероз
Випадковий патент: Гідрооб`ємна трансмісія транспортного засобу