Похідні ди- або трифторметансульфоніланіліду, спосіб їх одержання і гербіциди, що містять вказані похідні як активні інгредієнти
Номер патенту: 56338
Опубліковано: 15.05.2003
Автори: Дандзо Такесі, Йосімура Такумі, Оно Юкімаса, Тамару Масатосі, Накатані Масао, Янасігава Кацутада
Формула / Реферат
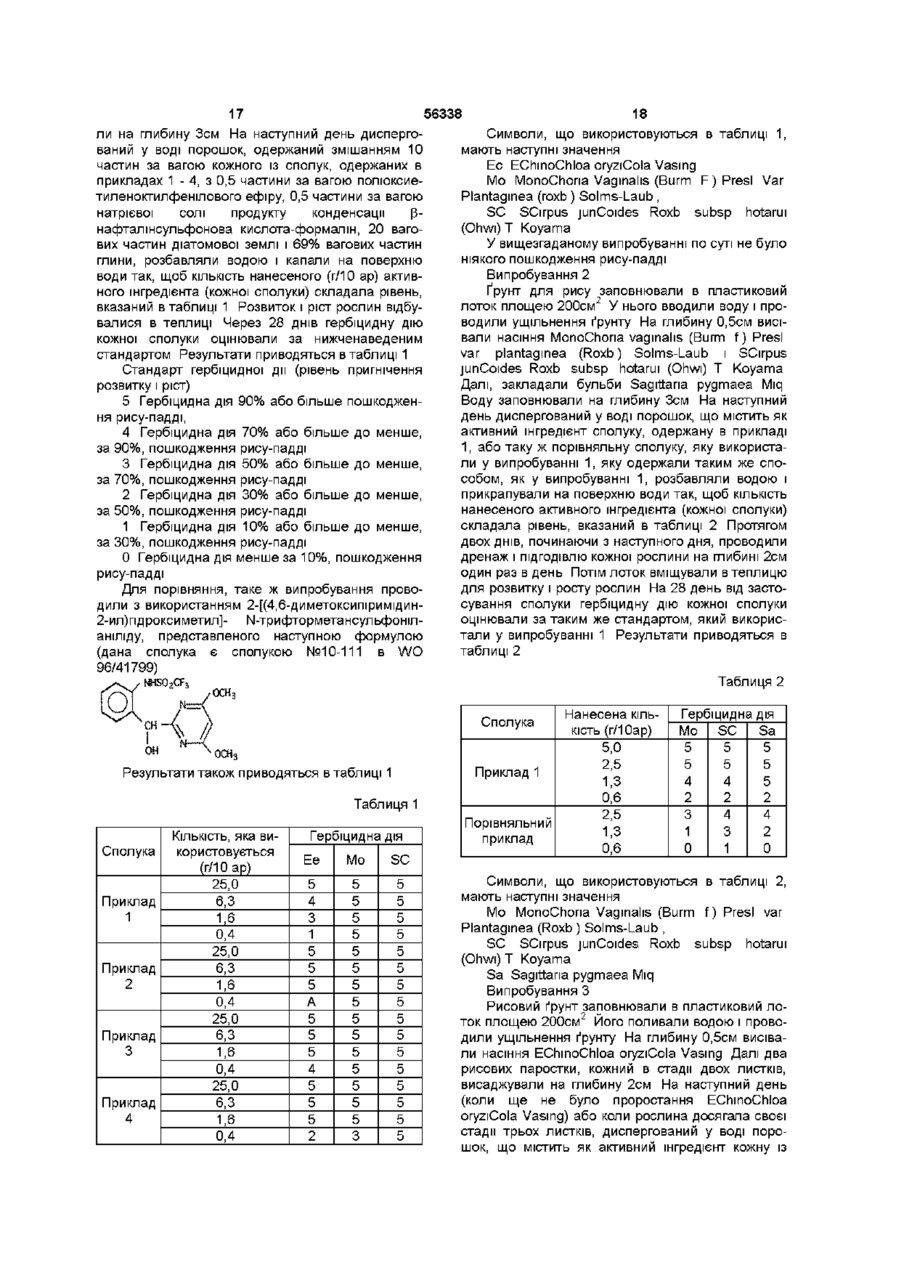
1. Похідне ди- або трифторметансульфоніланіліду, представлене наступною загальною формулою:
,
де R1 являє атом водню, алкільну групу або алкоксіалкільну групу; і R2 являє атом водню, коли R1 являє атом водню або алкільну групу, і являє атом водню або атом фтору, коли R1 являє алкоксіалкільну групу, або його сіль.
2. Похідне ди- або трифторметансульфоніланіліду або його сіль за п. 1, в якому R1 являє атом водню.
3. Похідне ди- або трифторметансульфоніланіліду або його сіль за п. 1, в якому R1 являє алкільну групу.
4. Похідне ди- або трифторметансульфоніланіліду або його сіль за п. 3, в якому алкільна група являє собою етильну групу.
5. Похідне ди- або трифторметансульфоніланіліду або його сіль за п. 1, в якому R1 являє алкоксіалкільну групу.
6. Похідне ди- або трифторметансульфоніланіліду або його сіль за п. 5, в якому алкоксіалкільна група являє собою метоксиметильну групу.
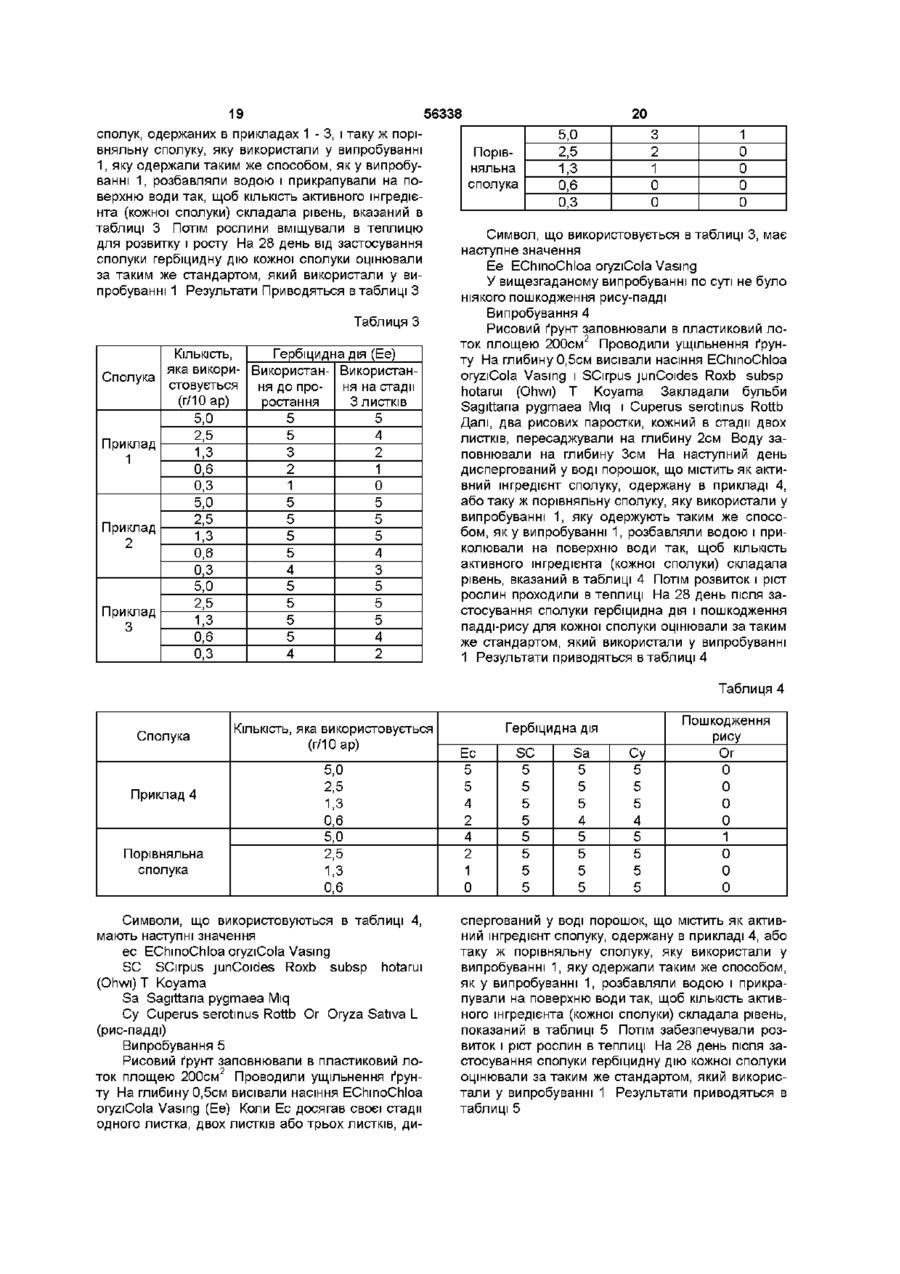
7. Спосіб одержання похідного ди- або трифторметансульфоніланіліду, представленого наступною загальною формулою:
,
де R1 являє атом водню, алкільну групу або алкоксіалкільну групу; і R2 являє атом водню, коли R1 являє атом водню або алкільну групу, і являє атом водню або атом фтору, коли R1 являє алкоксіалкільну групу, або її солі, що включає взаємодію 2-заміщеного похідного аніліну, представленого наступною загальною формулою:
,
де R1 має те ж визначення, що наводиться вище, з ди- або трифторметансульфонілгалогенідом або ангідридом трифторметансульфонової кислоти і потім, якщо необхідно, перетворенням продукту реакції в його сіль.
8. Спосіб одержання похідного ди- або трифторметансульфоніланіліду, представленого наступною загальною формулою:
,
де R1 являє атом водню, алкільну групу або алкоксіалкільну групу; і R2 являє атом водню, коли R1 являє атом водню або алкільну групу, і являє атом водню або атом фтору, коли R1 являє алкоксіалкільну групу, або її солі, який включає відновлення похідного ди- або трифторметансульфоніланіліду, представлену наступною загальною формулою:
,
де R1 і R2 мають те ж визначення, що наводиться вище і потім, якщо необхідно, перетворення продукту реакції в його сіль.
9. Гербіцид, що містить як активний інгредієнт похідне ди- або трифторметансульфоніланіліду, представленого наступною загальною формулою:
,
де R1 - являє атом водню, алкільну групу або алкоксіалкільну групу; і R2 являє атом водню, коли R1 являє атом водню або алкільну групу, і являє атом водню або атом фтору, коли R1 являє алкоксіалкільну групу) або його сіль.
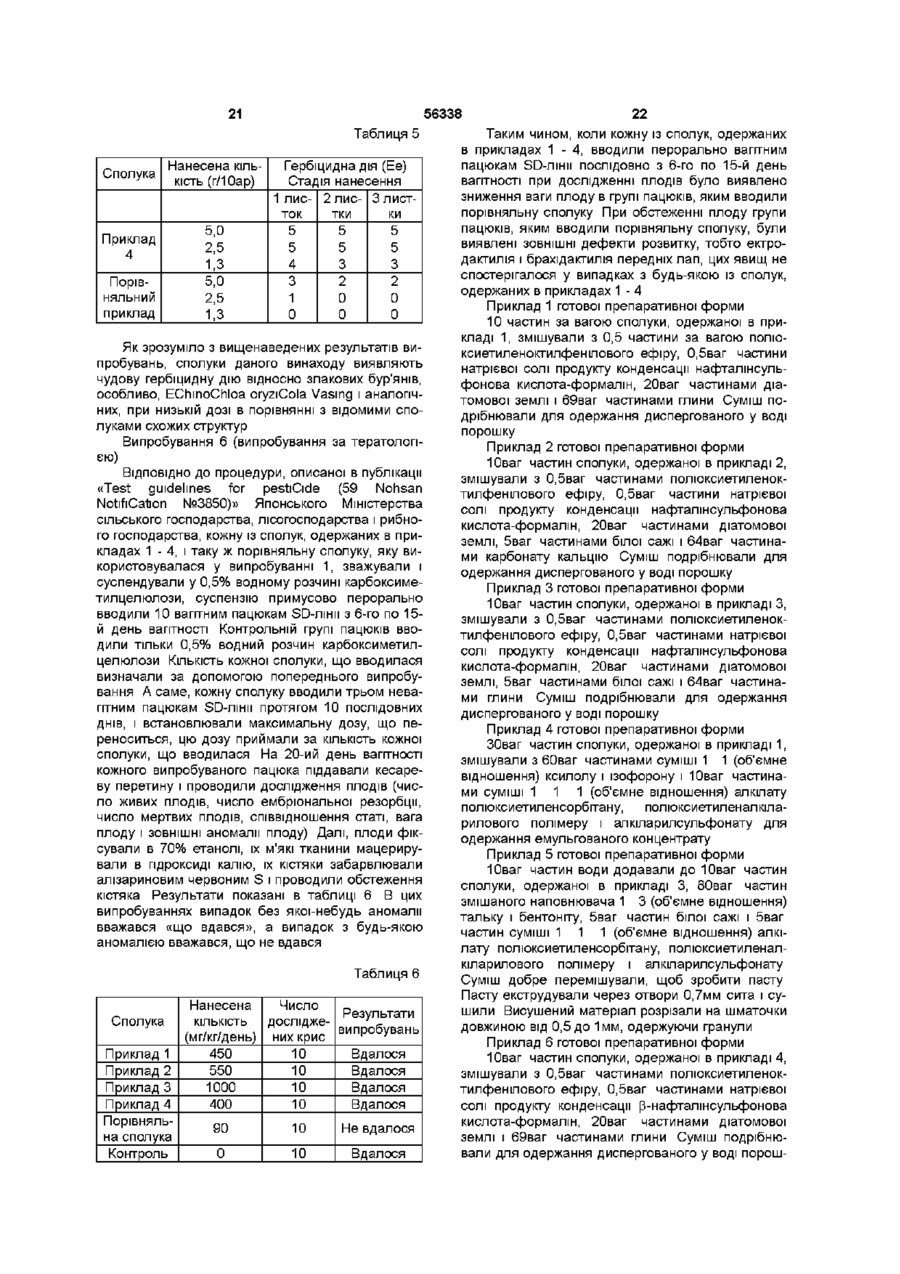
10. 2- Заміщене похідне аніліну, представлене наступною загальною формулою:
,
де R1 являє атом водню, алкільну групу або алкоксіалкільну групу.
11. Похідне ди- або трифторметансульфоніланіліду, представлене наступною загальною формулою:
,
де R1 являє атом водню, алкільну групу або алкоксіалкільну групу; і R2 являє атом водню, коли R1 являє атом водню або алкільну групу, і являє атом водню або атом фтору, коли R1 являє алкоксіалкільну групу.
Текст
1 Похідне ди- або трифторметансульфоніланіліду, представлене наступною загальною формулою R1 осн= осн. 1 де R являє атом водню, алкільну групу або алкоксіалкільну групу, і R являє атом водню, коли R1 являє атом водню або алкільну групу, і являє атом водню або атом фтору, коли R1 являє алкоксиалкільну групу, або його сіль 2 Похідне ди- або трифторметансульфоніланіліду або його сіль за п 1, в якому R1 являє атом водню 3 Похідне ди- або трифторметансульфоніланіліду або його сіль за п 1, в якому R1 являє алкільну групу 4 Похідне ди- або трифторметансульфоніланіліду або його сіль за п 3, в якому алкільна група являє собою етильну групу 5 Похідне ди- або трифторметансульфоніланіліду або його сіль за п 1, в якому R1 являє алкоксиалкільну групу 6 Похідне ди- або трифторметансульфоніланіліду або його сіль за п 5, в якому алкоксиалкільна група являє собою метоксиметильну групу 7 Спосіб одержання похідного ди- або трифтор метансульфоніланіліду, представленого наступною загальною формулою 1 R R Js. ,NHSO2CF2 О * -осн= f л\ / / он де R1 являє атом водню, алкільну групу або алкоксіалкільну групу, і R являє атом водню, коли R1 являє атом водню або алкільну групу, і являє атом водню або атом фтору, коли R1 являє алкоксіалкільну групу, або и солі, що включає взаємодію 2заміщеного похідного аніліну, представленого наступною загальною формулою осн. О осн3 де R1 маете ж визначення, що наводиться вище, з ди- або трифторметансульфонілгалогенідом або ангідридом трифторметансульфонової кислоти і потім, якщо необхідно, перетворенням продукту реакції в його сіль 8 Спосіб одержання похідного ди- або трифторметансульфоніланіліду, представленого наступною загальною формулою Вг ОСН, • 1 де R являє атом водню, алкільну групу або алкоксиалкільну групу, і R2 являє атом водню, коли R1 являє атом водню або алкільну групу, і являє атом водню або атом фтору, коли R1 являє алкоксиалкільну групу, або и солі, який включає відновлення похідного ди- або трифторметансульфоніланіліду, представлену наступною загальною формулою 00 со го (О ю 56338 ОСН Ч осн, 0СН3 1 2 де R і R мають те ж визначення, що наводиться вище і потім, якщо необхідно, перетворення продукту реакції в його сіль 9 Гербіцид, що містить як активний інгредієнт похідне ди- або трифторметансульфоніланіліду, представленого наступною загальною формулою f 1 де R являє атом водню, алкільну групу або алкоксіалкільну групу 11 Похідне ди- або трифторметансульфоніланіліду, представлене наступною загальною формулою осн, осн= ОСН, • 1 де R - являє атом водню, алкільну групу або алкоксіалкільну групу, і R являє атом водню, коли R1 являє атом водню або алкільну групу, і являє атом водню або атом фтору, коли R1 являє алкоксіалкільну групу) або його сіль 10 2- Заміщене похідне аніліну, представлене наступною загальною формулою Даний винахід стосується нових похідних диабо трифторметансульфоніланіліду або їх солей, способу їх одержання, гербіциду, що містить вказане похідне або його сіль як активний інгредієнт, і нових, сполук, які є початковими матеріалами, що використовуються у вказаному способі Відомо, ЩО ПОХІДНІ N-фторметансульфоніланіліду, що мають піримідинілутримуючу групу в положенні 2, наприклад, N-трифторметансульфоніланілідне похідне 2-піримідинілметил-заміщеного або 2-піримідинілокси- або -тюкси-заміщеного аніліну, мають гербіцидну активність (див Національну публікацію Міжнародної патентної заявки №7-501053 і WO 93/09099) Відомо також, що N-трифторметансульфоніланілідне похідне 2-піримідинілпдроксиметилзаміщеного аніліну має активність, яка регулює ріст рослин (див WO 96/41799) Однак, ще не відомо, що будь-який з N-ди- або трифтор-метансульфонілпохідних аніліну, що мають піримідинілутримуючу групу в положенні 2, має гербіцидну активність При культивуванні рису-падді важливою задачею в останні роки є боротьба з шкідливими бур'янами, які сходять на рисовому полі з якими важко ефективно боротися загальноприйнятими гербіцидами, тобто важкими для пригнічення бур'янами Ці бур'яни сходять протягом тривалого періоду часу і, отже, боротися, з ними необхідно протягом тривалого періоду часу Злакові бур'яни (ІНШІ, НІЖ рисові рослини), що належать до того ж самого сімейства, що і рисові рослини, наприклад, Echinochloa oryzicola Vasmg і т д , сходять протягом тривалого періоду часу, а також активно і швидко ростуть, отже, боротьба з ними також важлива До теперішнього часу не розроблений гербіцид, який має високу активність для вищезгаданих бур'янів і може пригнічувати їх Отже, бажано осн. де R1 являє атом водню, алкільну групу або алкоксиалкільну групу, і R2 являє атом водню, коли R1 являє атом водню або алкільну групу, і являє атом водню або атом фтору, коли R1 являє алкоксиалкільну групу розробити ХІМІЧНИЙ агент, який має високу гербіцидну активність не тільки для бур'янів, що погано піддаються пригніченню, але також і для злакових бур'янів, який може пригнічувати велику різноманітність бур'янів, що сходять на рисових полях протягом тривалого періоду часу, і який у високій мірі безпечний для ссавців При вищезгаданому стані справ даний винахід має на меті надання нових сполук, які ефективні для видалення широкої різноманітності бур'янів, включаючи бур'яни, що погано піддаються пригніченню, які сходять на рисовому полі, і які безпечні для ссавців, способу одержання їх, гербіциду, що містить вказану сполуку, як активний інгредієнт, і нових, сполук, що є початковими матеріалами, що використовуються в даному способі Автори даного винаходу провели інтенсивні дослідження для розробки нової сполуки, що має гербіцидну активність Внаслідок цього автори даного винаходу виявили, що N-ди- або трифторметансульфонільне похідне 2-піримідинілпдроксиметил-заміщеногоного аніліну має гербіцидну активність проти широкої різноманітності бур'янів при низькій дозі, дуже ефективну, особливо для злакових бур'янів і, крім того, високо безпечну для ссавців Даний винахід був завершений на основі вищезгаданого відкриття Даний винахід представляє похідне ди- або трифторметансульфоніланіліду, представлене наступною загальною формулою (І) ост (І) ON C, (де R1 представляє атом водню, алкільну гру 56338 пу або алкоксиалкільну групу, і R представляє атом водню, коли R представляє атом водню або алкільну групу, і представляє атом водню або атом фтору, коли R представляє алкоксиалкільну групу) або їх солі, причому і вказані ПОХІДНІ, І вказані солі мають гербіцидну активність Кожну із сполук, представлених загальною формулою (І), можна одержати, наприклад, за реакцією 2-заміщеного похідного аніліну (II) з ди- або трифторметансульфонілгалогенідом або ангідридом трифторметансульфонової кислоти за наступною схемою реакції (1) F" t MM. GH C= 4 0И N OCHg де X представляє атом галогену і R1 і R2, кожний, мають такі ж визначення, які зазначені вище, або відновленням похідного 2-(4,6диметоксипіримідин-2-іл карбоніл)N-ди- або трифторметансульфоніланіліду (III) за наступною схемою реакції (2) осн, 0) 1 2 (де R і R , кожний, мають такі ж визначення, які зазначено вище) Сполуки, представлені загальною формулою (II) або (III), одержання, що використовуються у вищезгаданих способах, також є новими сполуками, не описаними в будь-якій літературі В даній сполуці, представленій загальною формулою (І), R1 представляє атом водню, алкільну групу або алкоксіалкільну групу Алкільна група, переважно, представляє алкільну групу з нерозгалуженим або розгалуженим ланцюгом, що мас віл 1 до 5 атомів вуглецю, таку як метильна група, стильна група, н-пропільна група, ізопропільна група, н-бутильна група, ізобутильна група, вторбутильна група, трет-бутильна група, н-пентильна група, 1-метилбутильна група, н-гексильна група або аналогічні Алкоксіалкільна група, переважно, представляє алкоксіалкільну групу з нерозгалуженим або розгалуженим ланцюгом, що має від 2 до 6 атомів вуглецю, таку як метоксиметильна група, метоксіетильна група, етоксіетильна група, 3етоксипропільна група, 1-метил-З-метоксибутильна група або аналогічні У сполуці, представленій загальною формулою (І), R2 представляє атом водню, коли R1 представляє атом водню або алкільну групу, і предста 6 вляє атом водню або атом фтору, коли R1 представляє алкоксіалкільну групу Коли R2 представляє атом водню, сполука, представлена загальною формулою (І), є похідним дифторметансульфоніланіліду, коли R2 представляє атом фтору, сполука, представлена загальною формулою (1), є похідним трифторметансульфоніланіліду Сіль сполуки, представленої загальною формулою (І), є сіллю між сульфоніламідною частиною цієї сполуки і основою Як основу можна навести сіль натрію і сіль калію Як приклади похідних ди- або трифторметансульфоніланіліду, представлені загальною формулою (І), можна згадати 2-[(4,6-диметоксипіримідин-2-ил)пдроксиметил]-6-метоксиметил-І\Ідифторметансульфоніланілід, 2-[(4,6-диметоксипіримідин-2-ил)пдроксиметил]-6-метоксиетил-Мдифторметансульфоніланілід, 2-[(4,6-диметоксипіримідин-2-ил)пдроксиметил]-6-етоксиметил-Мдифторметансульфоніланілід, 2-[(4,6-диметоксипіримідин-2-ил)пдроксиметил]-І\І-дифторметансульфоніланілід, 2-[(4,6-диметоксипіримідин-2-ил)пдроксиметил]-6-етил-І\І-дифторметансульфоніланілід, 2-[(4,6-диметоксипіримідин-2-ил)пдроксиметил]-6метоксиметил-ІЧ-трифторметансульфоніланіл, 2[(4,6-диметоксипіримідин-2-ил)пдроксиметил]-6метоксиетил-ІЧ-трифторметансульфоніланілід і 2[(4,6-диметоксипіримідин-2-ил)пдроксиметил]-6етоксиметил-ІЧ-трифторметансульфоніланілід Сполуку, представлену загальною формулою (І), можна одержати, наприклад, за реакцією 2заміщеного похідного аніліну, представленого загальною формулою (II), з ди- або трифторметансульфонілгалогенідом або ангідридом трифторметансульфонової кислоти за вищезгаданою схемою реакції (1) або відновленням похідного 2-(4,6диметоксипіримідин-2-іл карбоніл)- N-ди- або трифторметансульфоніланіліду, представленого загальною формулою (III), за вищенаведеною схемою реакції (2) Перший спосіб проводять звичайно в присутності основи в інертному розчиннику, такому як аліфатичний або аліциклічний вуглеводень (наприклад, пентан, гексан або циклогексан), ароматичний вуглеводень (наприклад, толуол або ксилол), галогенований вуглеводень (наприклад, дихлорметан або хлороформ), простий ефір (наприклад, діетиловий ефір, тетрапдрофуран або 1,4-дюксан), складний ефір (наприклад, метилацетат або етилацетат), нітрил (наприклад, ацетонітрил або пропюнітрил), апротонний полярний розчинник (наприклад, N, N-диметилформамид, N, Nд и мети л сульфоксид або сульфолан) або їх суміші Основою, що використовується вище є основа, що звичайно використовується в реакції між аніліном і галогенанпдридом кислоти, таким як гідроксид лужного металу (наприклад, гідроксид натрію або гідроксид калію), гідроксид лужноземельного металу (наприклад, гідроксид кальцію) або органічна основа (наприклад, триметиламін, триетиламш, N, N-диметиланілін або піридин) Температуру реакції вибирають в діапазоні від -70 до 250°С, переважно, від -70 до 40°С Час реакції змінюється в залежності від виду, що використовується як початковий матеріал сполук, температури реакції, що використовується і т д , і 56338 8 складає приблизно від 5 хвилин до 7 днів Сполуку загальної формули (II) можна одержати, наприклад, таким чином Похідне 2Останній спосіб звичайно проводять в інертнітрофенілацетонітрилу піддають реакції з 2ному розчиннику, такому як спирт (наприклад, мегалоген- або -алкілсульфоніл-4,6-диметоксипіримітанол або етанол), простий ефір (наприклад, діедином в присутності основи або похідне 2тиловий ефір, тетрапдрофуран або 1,4-дюксан), гал о ген нітробензолу піддають реакції з 2-(4,6складний ефір (наприклад, метилацетат або етидиметрксипіримідин-2-ил)ацетонітрилом в присутлацетат), нітрил (наприклад, ацетонітрил або проності основи з одержанням 2-(4,6-диметоксипюнітрил), апротонний полярний розчинник (напіримідин-2-ил)-2-(2-нітрофеніл)ацетонітрилу (IV) приклад, N, N-диметилформамід, N, N-диметилСполуку (IV) піддають окислювальному деціанусульфоксид або сульфолан) або їх суміші ванню з одержанням сполуки загальної формули Відновлення проводять в присутності поновлюючого агента, наприклад, комплексної сполуки (V) Нітрогрупу сполуки (V) відновлюють для перелужний метал-водень (наприклад натріиборгідрид) творення її в аміногрупу з одержанням сполуки в температурному в інтервалі від -70°С до точки загальної формули (VI) Карбонільну групу сполуки кипіння розчинника, що використовується, пере(VI) відновлюють в пдроксиметильну групу з одерважно, від -20 до 40°С Час реакції змінюється в жанням сполуки загальної формули (II) залежності від виду початкових матеріалів сполук, Окислювальне деціанування для перетворенщо використовуються температури реакції, що ня сполуки загальної формули (IV) в сполуку загавикористовується і т д , і складає приблизно від 5 льної формули (V) проводять, на першій стадії, хвилин до 7 днів окисленням окисляючим агентом і, на другій стадії, обробленням основою Сполуки загальної формули (II) або (III), що використовуються як початковий матеріал у вищеДану реакцію проводять звичайно в інертному згаданих процесах, також є новими сполуками, не розчиннику, такому як аліфатичний або аліциклічописаними в будь-якій літературі ний вуглеводень (наприклад, пентан, гексан або циклогексан), ароматичний вуглеводень (наприЦі сполуки можна легко одержати з ВІДПОВІДНОклад, толуол або ксилол), галогенований вуглевоГО 2-(4,6-диметоксипіримідин-2-ил)-2-(2-нітрофедень (наприклад, дихлорметан або хлороформ), ніл)ацетонітрилу (IV) за нижченаведеною реакційпростий ефір (наприклад, діетиловий ефір, тетраною схемою у ВІДПОВІДНОСТІ зі способом одержанпдрофуран або 1,4-дюксан), кетон (наприклад, ня, описаним, наприклад, в J Org Food Chem, ацетон або метилетилкетон), складний ефір (наVol 22, №6, crop 1111 (1974), J Chem приклад, метилацетат або етилацетат), нітрил Researchers, 1977, crop 186, або Heterocycles, vol (наприклад, ацетонітрил або пропюнітрил), апро38, №1, crop 125 тонний полярний розчинник (наприклад, N, Nдиметилформамід, N, N-д и мети л сульфоксид або сульфолан), вода або їх суміші Як окисляючий агент, що використовується на першій стадії, можна указати, наприклад, органічні перкислоти, такі як м-хлорпербензойна кислота і аналогічні Основу, що використовується на другій стадії, можна без обмежень вибрати з основ, що звичайно використовуються при деціануванні даного виду Такі основи включають, наприклад, гідроксиди лужних металів, такі як гідроксид натрію, гідроксид калію і аналогічні, гідроксиди лужноземельних металів, такі як гідроксид кальцію і аналогічні, і органічні основи, такі як триметиламін, триетиламш, N, N-диметиланілш, піридин і аналогічні Температуру, що використовується у вищезгаданій реакції, вибирають в діапазоні від -70 до 250°С, переважно, від -20 до 40°С Час реакції змінюється в залежності від видів окисляючого агента, що використовується і основи і температури реакції, що застосовується, але звичайно він складає від 5 хвилин до 7 днів Реакцію відновлення нітрогрупи сполуки загальної формули (V) для перетворення її в аміногрупу для одержання похідного аніліну загальної формули (IV) можна провести поновлюючим агентом в присутності каталізатора в інертному розчиннику Інертний розчинник включає, наприклад, спирти, такі як метанол, етанол і аналогічні, простий ефір, такий як діетиловий ефір, тетрапдрофуран, 0) 1,4-дюксан і аналогічні, складний ефір, такий як (де R1, R2 і X, кожний, має такі ж визначення, метилацетат, етилацетат і аналогічні, нітрили, такі які зазначені вище) 56338 10 диметилформамід, N, N-диметилсульфоксид або як ацетонітрил, пропюнітрил і аналогічні, апротонні сульфолан), вода або їх суміші полярні розчинники, такі як N, N-диметилформаЯк окисляючий агент можна згадати, напримід, N, N-диметилсульфоксид, сульфолан і аналоклад, органічні перкислоти, такі як м-хлорпербенгічні, воду і змішані розчинники з них зойна кислота і аналогічні Як поновлюючий агент використовують, наприклад, метали, такі як залізо, цинк і олово Як Як основу використовують основи, що звичайкаталізатор використовують, наприклад, органічні но використовуються в реакції даного вигляду, кислоти, такі як оцтова кислота наприклад, гідроксиди лужних металів, такі як гідроксид натрію, гідроксид калію і тому подібне, гідВищезгадану реакцію проводять при темперароксиди лужноземельних металів, такі як гідроксид турі в діапазоні звичайно від 20°С до точки кипіння кальцію і тому подібне, і органічні основи, такі як розчинника, що використовується Час реакції змітриметиламін, триетиламш, N, N-диметиланілш, нюється в залежності від поновлюючого агента, піридин і аналогічні що використовується, каталізатора і температури реакції, і звичайно складає від 5 хвилин до 7 днів Температуру реакції вибирають в діапазоні від -70 до 250°С, переважно, від -20 до 40°С Час реаВідновлення для перетворення карбонільної кції змінюється в залежності від основи, що викогрупи сполуки загальної формули (VI), одержаної ристовується і температури реакції, звичайно вище, в пдроксиметильну групу можна провести складає від 5 хвилин до 7 днів таким же способом, який використовується при вищезгаданому відновленні сполуки загальної фоГербіцид, що містить сполуку, представлену рмули (III), для одержання сполуки (І) загальною формулою (І), як активний інгредієнт, можна виготовити в різних готових препаративних Сполуку загальної формули (III) можна одерформах, що звичайно використовуються в звичайжати, наприклад, відновленням нітрогрупи 2-(4,6них гербіцидах, таких як дуст, диспергований у диметоксипіримідин-2-ил)-2-(2-нітрофеніл)ацетоніводі порошок, емульгований концентрат, дрібні трилу (IV) для перетворення її в аміногрупу для гранули, гранули і тому подібне Як гербіцид можодержання сполуки загальної формули (VII), потім на використати саме сполуку (І) реакцією сполуку (VII) з ди- або тр и фтор метан сульфонілгалогенідом або ангідридом трифтормеНосій І добавки, що використовуються в гототансульфонової кислоти в присутності основи для вій препаративній формі вищезгаданого гербіциду одержання індольної сполуки загальної формули можна вільно вибрати з носив і добавок, що зви(VIII) і підданням індольної сполуки (VIII) окисленчайно використовуються в гербіцид них готових ню для розкриття кільця препаративних формах, в залежності від мети застосування виготовленого гербіциду Реакцію відновлення нітрогрупи сполуки загальної формули (IV) для перетворення її в аміноЯк носій в готовій препаративній формі вищегрупу проводять гідруванням в присутності каталізгаданого гербіциду можна указати, наприклад, затора в інертному розчиннику Інертний тверді носи, такі як тальк, бентоніт, глина, каолін, розчинник може бути тим же розчинником, який діатомова земля, біла сажа, вермикуліт, карбонат використовують при одержанні сполуки загальної кальцію, гашене вапно, кремнеземний пісок, сульформули (V) Каталізатор можна вільно вибрати з фат амонію, сечовина і тому подібне, і рідкі носи, каталізаторів, що звичайно використовуються в такі як ізопропіловий спирт, ксилол, циклогексан, каталітичному відновленні, таких як платина, паметилнафталін і аналогічні ладій, паладій на вугіллі і аналогічні Як поверхово-активну речовину або диспергатор можна указати, наприклад, алкілбензолсульРеакцію сполуки загальної формули (VII) з дифонати металів, динафтилметандисульфонати або трифторметансульфонілгалогенідом або ангіметалів, солі алкілсульфатів, продукти конденсадридом трифторметансульфонової кислоти можна ції, сіль алкіларилсульфонової кислоти-формалін, провести таким же способом, як у вищезгаданій солі лігнінсульфонових кислот, полюксиетиленгліреакції сполуки загальної формули (II) з ди- або колевий ефір, полюксиетиленалкілариловий ефір і трифторметансульфонілгалогенідом або ангідримоноалкілати полюксиетиленсорбітану дом трифторметансульфонової кислоти для одержання сполуки (І) Як допоміжний агент можна указати, наприклад, карбоксиметилцелюлозу, поліетиленгліколь і Реакцію піддання похідного індолу загальної аравійську камедь формули (VIII) окисленню для розкриття кільця проводять, на першій стадії, обробленням сполуки Гербіцид застосовують шляхом розбавлення окисляючим агентом і, на другій стадії, обробленйого до відповідної концентрації і розбризкування ням основою матеріалу, що одержується або застосовують безпосередньо Дану реакцію звичайно проводять в інертному розчиннику, такому як аліфатичний або аліциклічГербіцид даного винаходу застосовують до ний вуглеводень (наприклад, пентан, гексан або листя, грунту, поверхні води і т д циклогексан), ароматичний вуглеводень (наприКІЛЬКІСТЬ активного інгредієнта в даному гербіклад, толуол або ксилол), галогенований вуглевоциді ВІДПОВІДНИМ чином визначають в залежності день (наприклад, дихлорметан або хлороформ), від мети застосування гербіциду, його можна вибпростий ефір (наприклад діетиловий ефір, тетрапрати в діапазоні від 0,01 до 10% за масою, передрофуран або 1,4-дюксан), кетон (наприклад, ацеважно, від 0,05 до 5% за масою, коли гербіцид тон або метилетилкетон), складний ефір (наприявляє собою дуст або гранули, і в діапазоні від 1 клад, метилацетат або етилацетат), нітрил до 50% за масою, переважно, від 5 до 30% за ма(наприклад, ацетонітрил або пропюнітрил), апросою, коли гербіцид являє собою емульгований тонний полярний розчинник (наприклад, N, Nконцентрат або диспергований у воді порошок 12 11 56338 КІЛЬКІСТЬ застосування даного гербіциду змінсульфонілхлориду Розчин перемішують при кімнюється в залежності від вигляду сполуки, що міснатній температурі протягом ночі Реакційну суміш титься в гербіциді, бур'яну(ів), що підлягають випромивають розбавленою хлористоводневою кисдаленню, режиму появи паростків бур'яну(ів), умов лотою і насиченим водним розчином хлориду нанавколишнього середовища, типу гербіцидної готрію з подальшим сушінням над безводним сультової препаративної форми і т д Однак, КІЛЬКІСТЬ фатом магнію Суміш, що одержують піддають можна вибрати в діапазоні від 0,1г до 5кг, перевавакуумній дистиляції для видалення розчинника жно, від 1 г до 1 кг на 10ар, виходячи з КІЛЬКОСТІ акЗалишок піддають колоночній хроматографії на тивного інгредієнта, коли гербіцид являє собою, силікагелі (елюентний розчинник етилаценаприклад, дуст або гранули, і його використовутат/гексан = 1/3) для розділення і очищення, одерють безпосередньо Коли гербіцид являє собою, жуючи 2,0г (вихід 35%) 2-амшо-1-дифторметаннаприклад, емульгований концентрат або дисперсульфоніл-3-(4,6-диметоксипіримідин-2-ил)шдолу гований у воді порошок і використовується в рідкій у вигляді світло-жовтого порошку (точка плавленформі, КІЛЬКІСТЬ активного інгредієнта може вибиня 156-158°С) ратися в діапазоні від 0,1 до 50000м д , переважОдержані дані 1 но, від 10 до 10000м д Н ЯМР 300МГц CDCI ТМС 8,57 (д, 1Н), 7,81 Гербіцид даного винаходу можна, коли необхідно, використати в поєднанні з інсектицидом, фунгіцидом, іншим гербіцидом, регулювальником росту рослин, добривом і т д Даний винахід описується нижче більш детально за допомогою прикладів Однак, даний винахід не обмежується цими прикладами Посилальний приклад 1 Одержання 2-(4,6-диметоксипіримідин-2ілкарбоніл)-І\І-дифторметансульфоніланіліду (1) 50г (0,31 М) 2-(2-Нітрофеніл)ацетонітрилу розчиняють в 500мл диметилформаміду До нього додають 24,7г (0.62М) 60% гідриду натрію Суміш перемішують при кімнатній температурі протягом 2 годин Потім додають 68г (0,31 М) 4,6-диметокси-2метансульфонілпіримідину Суміш перемішують при 80°С протягом 1 години, щоб викликати реакцію Реакційну суміш виливають у воду з подальшою нейтралізацією розбавленою хлористоводневою кислотою Суміш піддають екстракції етилацетатом Екстракт промивають водою, сушать і піддають вакуумній дистиляції для видалення розчинника Залишок перекристалізовують з етанолу, одержуючи 73,3г (вихід 79%) 2-(4,6диметоксипіримідин-2-ил)-2-(2нітрофеніл)ацетонітрилу у вигляді білого порошку (точка плавлення 88 - 89°С) Одержані дані 1 Н ЯМР 60МГц CDCI3 ТМС 7,5 - 8,2 (м, 4Н), 6,4(с,1Н), 5,9 (с, 1Н), 3,8 (с, 6Н) (2) 3,0г (ЮмМ) 2-(4, Диметоксипіримідин-2-ил)2-(2-нітрофеніл)ацетонітрилу, одержаного вище на стадії (1), і 0,3г 10% паладії на вугіллі суспендують в ЮОмл метанолу У той час як суспензію перемішують при кімнатній температурі протягом ночі, до неї додають водень Твердий матеріал видаляють фільтруванням Фільтрат піддають вакуумній дистиляції для видалення метанолу Залишок піддають очищенню колоночною хроматографією на силікагелі (елюентний розчинник етилацетат/гексан = 1/1), одержуючи 1,8г (вихід 67%) 2-(2амшофеніл)-2-(4,6-диметоксипіримідин-2ил)ацетонітрилу у вигляді світло-жовтої, подібної до льодяників речовини Одержані дані 1 Н ЯМР60 МГц CDCI3 ТМС 6,5 - 7,6 (м, 4Н), 6,9 (с, 1Н), 5,3 (с, 1Н), 4,6 (шир , 2Н), 3,9 (с, 6Н) (3) У ЮОмл хлороформу розчиняють 4,0г (14,8мМ) 2-(2-амшофеніл)-2-(4,6-диметоксипіримідин-2-ил)ацетонітрилу, одержаного на стадії (2), 2,5г (31,6мМ) піридин і 2,8г (18,6мМ) дифтормета 3 (д, 1Н), 7,56 (шир, 2Н), 7,34 (т, 1Н), 7,15 (т, 1Н), 6,43 (т, 1Н), 5,84 (с, 1Н), 4,05 (с, 6Н) (4) У ЗОмл хлороформу розчиняють 2,0г (5,2мМ) 2-амшо-1-дифторметансульфоніл-3-(4,8диметоксипіримідин-2-илу)шдолу, одержаного на вищезгаданій стадії (3), і 2,0г (5,8мМ) 50% мхлорпербензойної кислоти Розчин перемішують при кімнатній температурі протягом 12 годин Потім додають 15мл 10% водного розчину гідроксиду натрію Суміш перемішують при кімнатній температурі протягом 1 години Додають 50мл хлороформу Органічний шар промивають 5% розбавленою хлористоводневою кислотою і насиченим водним розчином хлориду натрію з подальшим сушінням Розчин, що одержують піддають вакуумній дистиляції для видалення розчинника Залишок піддають колоночній хроматографії на силікагелі (елюентний розчинник етил а цетат/н-гексан = 1/5) для очищення, одержуючи 1,0г (вихід 52%) 2(4,6-диметоксипіримідин-2-ілкарбоніл)Nдифторметансульфоніланіліду у вигляді білого порошку (точка плавлення 131 -133°С) Одержані дані 1 Н ЯМР 300МГц CDCI3 ТМС 11,36 (шир , 1Н), 7,86 (д, 1Н), 7,70 (д, 1Н), 7,62 (т , 1Н), 7,18 (т, 1Н), 6,35 (т, 1Н), 6,19 (с, 1Н), 3,97 (с, 6Н) Посилальний приклад 2 Одержання 2-[(4,6-диметоксипіримідин-2ил)пдроксиметил]-6-метоксиметиланілшу (1) 11,2г (0.28М) 60% гідриду натрію суспендують в ЮОмл N, N-диметилформаміду У той час як суспензію охолоджують до Ю°С або нижче в бані з льодом і водою і перемішують, до неї додають по краплях розчин 25г (0,14М) 2-(4,6-диметоксипіримідин-2ил)ацетонітрилу, розчиненого в ЮОмл N, Nдиметилформаміду Після завершення прикапування суміш перемішують при кімнатній температурі доти, поки не припиниться виділення водню У той час як суміш охолоджують до Ю°С або нижче в бані з крижаною водою і перемішують, до неї додають по краплях розчин 28г (0.14М) 2-хлор-6метоксиметилнітробензолу, розчиненого в ЮОмл диметилформаміду Потім суміш перемішують при кімнатній температурі протягом 12 годин Реакційну суміш виливають в крижану воду Суміш підкисляють 10% хлористоводневою кислотою з подальшою екстракцією етилацетатом Органічний шар промивають насиченим водним розчином хлориду натрію і водою, сушать і концентрують при зниженому тиску Кристали, що одержують промивають 14 13 56338 змішаним розчинником з етанолу і ізопропілового собу для фільтрування Органічний шар промиваефіру, одержуючи 31г (вихід 64%) 2-(4,6ють насиченим водним розчином хлориду натрію, диметоксипіримідин-2-ил)-2-(3-метоксиметил-2-нітсушать і піддають вакуумній дистиляції для видарофеніл)ацетонітрилу у вигляді червонувато - колення розчинника Залишкові кристали промиваричневого порошку (точка плавлення 112 - 113°С) ють диїзопропіловим ефіром, одержуючи 2,4г (вихід 80%) 2-(4,6-диметоксипіримідин-2-ілкарбоніл)Одержані дані 1 6- метоксиметиланіліну у вигляді жовтих кристалів Н ЯМР 300МГц CDCI3 ТМС 7,83 (м, 1Н), 7,58 (точка плавлення Ю0-Ю1°С) (м, 2Н), 5,91 (с, 1Н), 5,72 (с, 1Н), 4,53 (с, 2Н), 3,90 (с, 6Н), 3,39 (с, ЗН) Одержані дані 1 (2) 11,2г (0.28М) 60% гідриду натрію суспенН ЯМР 300МГц CDCI3 ТМС 7,37 (д, 1Н), 7,24 дують в ЮОмл N, N-диметилформаміду У той час (д, 1Н), 7,14 (шир, 2Н), 6,53 (т, 1Н), 6,11 (с, 1Н), як суспензію охолоджують до 10°С або нижче у 4,55 (с, 2Н), 3,96 (с, 6Н), 3,35 (с, ЗН) ванні з крижаною водою і перемішують, до неї до(5) 3,1г (ЮмМ) 2-(4, Диметоксипіримідин-2дають по краплях розчин 29г (0.14М) 3-метоксиілкарбоніл)-6-метоксиметиланілшу, одержаного на метил-2-нітрофенілацетонітрилу, розчиненого в стадії (4), розчиняють в 50мл змішаного розчинниЮОмл N, N-диметилформаміду Після завершення ка 1 1 (об'ємне відношення) тетрапдрофурану і додання по краплях суміш перемішують при кімнаводи У той час як розчин перемішують при кімнатній температурі доти, поки не припиниться видітній температурі, до нього додають 0,6г (16мМ) лення водню У той час як суміш охолоджують до натрій-борпдриду Суміш перемішують при кімнат10°С або нижче у ванні з крижаною водою і переній температурі протягом 2 годин Додають 50мл мішують, до неї додають 30г (0,14М) 4,6крижаної води з подальшою екстракцією етилацедиметокси-2-метилсульфонілпіримідину Суміш татом Органічний шар промивають насиченим перемішують при кімнатній температурі протягом водним розчином хлориду нагрію, сушать і підда12 годин Реакційну суміш виливають в крижану ють вакуумній дистиляції для видалення розчинводу Суміш підкисляють 10% хлористоводневою ника Залишкові кристали промивають диїзопропікислотою Сирі кристали, що одержують збирають ловим ефіром, одержуючи 2,8г (вихід 92%) 2-[(4,6фільтруванням, промивають водою і змішаним диметоксипіримідин-2-ил)пдроксиметил]-6-меторозчинником з етанолу і ізопропілового ефіру, ксиметиланіліну у вигляді білого порошку (точка одержуючи 42г (вихід 87%) 2-(4,6-диметоксипіриплавлення 40 - 42°С) мідин-2-ил)-2-(3-метоксиметил-2-нітрофеніл)ацеОдержані дані тонітрилу у вигляді червонувато-коричневого по1 Н ЯМР 300МГц CDCI3 ТМС 7,30 (д, 1Н), 7,01 рошку (точка плавлення 112-113°С) (д, 1Н), 6,73 (т, 1Н), 5,93 (с, 1Н), 5,84 (д, 1Н), 5,17 (шир , 2Н), 4,68 (д, 1Н), 4,51 (до, 2Н), 3,94 (с, 6Н), Одержані дані 1 3,32 (с, ЗН) Н ЯМР 300МГц CDCI3 ТМС 7,83 (м, 1Н), 7,58 (м, 2Н), 5,91 (с, 1Н), 5,72 (с, 1Н), 4,53 (с, 2Н), 3,90 Посилальний приклад З (с, 6Н), 3,39 (с, ЗН) Одержання 2-[(4,6-диметоксипіримідин-2ил)пдроксиметил]-6-етиланілшу (3) У ЗОмл хлороформу розчиняють 3,5г (ЮмМ) 2-(4,6-диметоксипіримідин-2-ил)-2-(3-мето(1) Операцію (1) посилального прикладу 2 поксиметил-2-нітрофеніл)-ацетонітрилу, одержаного вторюють, за винятком того, що 2-хлор-6на вищезгаданій стадії (1) або (2), і 6,0г (17мМ) метоксиметилнітробензол, що використовується 50% м-хлорпербензойної кислоти Розчин переміна стадії (1) посилального прикладу 2, замінюють шують при кімнатній температурі протягом 12 го2-етил-6-фторнітробензолом, за допомогою чого дин До нього додають 15мл 10% водного розчину одержують 2-(4,6-диметоксипіримідин-2-ил)-2-(3гідроксиду натрію з подальшим перемішуванням етил-2-нітрофеніл)ацетонітрил у вигляді червонупри кімнатній температурі протягом 1 години Довато-коричневого порошку (точка плавлення 113 дають 50мл хлороформу Органічний шар проми114°С) Вихід 66,6% вають 5% розбавленою хлористоводневою кислоОдержані дані 1 тою і насиченим водним розчином хлориду натрію, Н ЯМР 300МГц CDCI3 ТМС 7,73 (д, 1Н), 7,50 сушать і піддають вакуумній дистиляції для вида(т, 1Н), 7,36 (д, 1Н), 5,92 (с, 1Н), 5,52 (с, 1Н), 3,91 лення розчинника Кристали, що залишилися про(с, 6Н), 2,56 - 2,76 (м, 2Н), 1,26 (т, ЗН) мивають сумішшю етанолдиїзопропілового ефіру, (2) 2-(4,6-диметоксипіримідин-2-ил)-2-(3-етилодержуючи 2,8г (вихід 84%) (4,6-диметоксипіри2-нітрофеніл)ацетонітрил, одержаний за вищезгамідин-2-ил)-3-метоксиметил-2-нітрофенілкетону у даною процедурою (1), піддають такій же обробці, вигляді білого порошку (точка плавлення від 111 як на стадії (3) посилального прикладу 2, за доподо113°С) могою чого одержують 2-(4,6-диметоксипіримідин2-илу)- З-етил-2-нітрофенілкетон у вигляді білого Одержані_дані 1 порошку (точка плавлення 116 - 117°С) Вихід Н ЯМР 300МГц CDCI3 ТМС 7,90 (д, 1Н), 7,72 100% (т, 1Н), 7,61 (д, 1Н), 6,13 (с, 1Н), 4,78 (с, 2Н), 3,90 (с, 6Н), 3,47 (с, ЗН) Одержані дані 1 (4) 3,3г (ЮмМ) (4, Диметоксипіримідин-2-ил)-3Н ЯМР 300МГц CDCI3 ТМС 7,51 - 7,63 (м, метоксиметил-2-нітрофенілкетону, одержаного на ЗН), 6,13 (с, 1Н), 3,92 (с, 6Н), 2,88 (до, 2Н), 1,32 (т, стадії (3), Зг (54мМ) порошку заліза, 20мл води і ЗН) суміш 150мл етилацетату і 1мл оцтової кислоти (3) 2-(4,6-диметоксипіримідин-2-ил)- З-етил-2піддають реакції при 50°С протягом 5 годин Ненітрофенілкетон, одержаний на стадії (2), піддають розчинні речовини в реакційній суміші ВІДДІЛЯЮТЬ такій же обробці, як на стадії (4) посилального фільтруванням з використанням допоміжного заприкладу 2, за допомогою чого одержують 2-(4,6 16 15 56338 диметоксипіримідин-2-ілкарбоніл)-6- етиланілін у 7,67 (д, 1Н), 7,49 (д, 1Н), 7,36 (т, 1Н), 6,53 (т, 1Н), вигляді жовтого порошку (точка плавлення 122 6,24 (д, 1Н), 5,98 (с, 1Н), 4,92 (д , 1Н), 4,68 (д, 2Н), 123°С) Вихід 64% 3.98 (с, 6Н), 3,39 (с, ЗН) Одержані дані Приклад З 1 Н ЯМР 300МГц CDCI3 ТМС 6,67 (шир, 2Н), У ЗОмл дихлорметану розчиняють 4,0г 6,56 (т, 1Н), 6,11 (с, 1Н), 3,95 (с, 6Н), 2,56 (до, 2Н), (13,81мМ) 2-[(4,6-диметоксипіримідин-2-ил)пдро1,30 (т, ЗН) ксиметил]-6- етиланіліну, одержаного в посилальному прикладі 3, і 2,0г (25,ЗмМ) піридин У той час (4) 2-(4, Диметоксипіримідин-2-ілкарбоніл)-6як розчин перемішують при -10°С, до нього додаетиланілін, одержаний на вищезгаданій стадії (3), ють по краплях 3,6г (23,9мМ) дифторметансульпіддають такій же обробці, як на стадії (5) посилафонілхлориду Суміш перемішують при кімнатній льного прикладу 2, за допомогою чого одержують температурі протягом 3 днів Реакційну суміш ви2-[(4,6-диметоксипіримідин-2-ил)пдроксиметил]-6ливають в крижану воду з подальшою екстракцією етил анілін у вигляді білого порошку (точка плавдихлорметаном Органічний шар промивають 5% лення 85 - 86°С) Вихід 93,7% розбавленою хлористоводневою кислотою і насиОдержані дані 1 ченим водним розчином хлориду натрію, сушать і Н ЯМР 300МГц CDCI3 ТМС 7,19 (д, 1Н), 7,03 піддають вакуумній дистиляції для видалення роз(д, 1Н), 6,76 (т, 1Н), 5,93 (с, 1Н), 5,87 (д, 1Н), 4,71 чинника Залишок піддають колоночній хроматог(шир , 2Н), 4,69 (д, 1Н), 3,93 (с, 6Н), 2,56 (до, 2Н), рафії на силікагелі (елюентний розчинник етила1,25 (т, ЗН) цетат/гексан = 1/3) для розділення і очищення, Приклад 1 одержуючи 2,4г (вихід 43%) 2-[(4,6-диметоксипіри1,0г (2,7мМ) 2-(4, Диметоксипіримідин-2мідин-2-ил)пдроксиметил] - б-етил-Ы-дифтормеілкарбоніл)- N-дифторметанульфоніланіліду, одетансульфоніланіліду у вигляді білого порошку (торжаного в посилальному прикладі 1, розчиняють в чка плавлення 120-121 °С) 50мл змішаного розчинника 1 1 (об'ємне відно шення) тетрапдрофурану і води У той час як розчин перемішують при кімнатній температурі, до нього додають 0,2г (5,4мМ) натрійборпдриду Суміш перемішують при кімнатній температурі протягом 2 годин Додають 50мл води з подальшою екстракцією етилацетатом Органічний шар промивають насиченим водним розчином хлориду натрію, сушать і піддають вакуумній дистиляції для видалення розчинника Залишкові кристали промивають диїзопропіловим ефіром, одержуючи 0,8г (вихід 80%) 2-[(4,6-диметоксипіримідин-2-ил)пдроксиметил]- N-дифторметансульфоніланіліду у вигляді білого порошку (точка плавлення 103 105°С) Одержані дані 1 Н ЯМР 300МГц CDCI3 ТМС 10,89 (шир , 1Н), 7,70 (м, 1Н), 7,60 (м, 1Н), 7,30 (м, 2Н), 6,32 (т, 1Н), 6,10 (д, 1Н), 5,99 (с, 1Н), 4,92 (д , 1Н), 4,00 (с, 6Н) Приклад 2 У ЗОмл дихлорметану розчиняють 4,0г (13,1 мМ) 2-[(4,6-диметоксипіримідин-2-ил)пдроксиметил]-6- метоксиметиланіліну, одержаного в посилальному прикладі 2, і 2,0г (25,ЗмМ) піридину У той час як розчин перемішують при -10°С, до нього додають по краплях 3,6г (23,9мМ) дифторметансульфонілхлориду Суміш перемішують при кімнатній температурі протягом 7 днів Реакційну суміш виливають в крижану воду з подальшою екстракцією дихлорметаном Органічний шар промивають 5% розбавленою хлористоводневою кислотою і насиченим водним розчином хлориду натрію, сушать і піддають вакуумній дистиляції для видалення розчинника Залишок піддають колоночній хроматографії на силікагелі (елюентний розчинник етил ацетат/гексан = 1/3) для розділення і очищення, одержуючи 2,0г (вихід 36%) 2-[(4,6диметоксипіримідин-2-ил)пдроксиметил] 6метоксиметил-ІЧ-дифторметансульфоніланілід у вигляді безбарвних гранульованих кристалів у вигляді гранул (точка плавлення 76 - 77°С) Одержані дані 1 Н ЯМР 300МГц CDCI3 ТМС 10,53 (шир , 1Н), Одержані дані 1 Н ЯМР 300МГц CDCI3 ТМС 10,34 (шир, 1Н), 7,56 (до, 1Н), 7,27 - 7,32 (м, 2Н), 6,40 (т, 1Н), 6,27 (д, 1Н), 5,97 (с, 1Н), 4,93 (д , 2Н), 3,98 (с, 6Н), 2,95 3,07 (м, 1Н), 2,76 - 2,89 (м, 1Н), 1,23 (до, ЗН) Приклад 4 У ЗОмл дихлорметану розчиняють 4,0г (13,1 мМ) 2-[(4,6-диметоксипіримідин-2-ил)пдроксиметил]-6- метоксиметиланіліну, одержаного в посилальному прикладі 2, і 1,5г (14,8мМ) триетиламіну У той час як розчин перемішують при -50°С, до нього додають по краплях 4,0г (14,2мМ) ангідриду трифторметансульфонової кислоти Суміш перемішують при -50°С - 0°С протягом 3 годин Реакційну суміш виливають в крижану воду з подальшою екстракцією дихлорметаном Органічний шар промивають 5% розбавленою хлористоводневою кислотою і насиченим водним розчином хлориду натрію, сушать і піддають вакуумній дистиляції для видалення розчинника Залишок піддають колоночній хроматографії на силікагелі (елюентний розчинник етил ацетат/гексан = 1/3) для розділення і очищення, одержуючи 3,8г (вихід 66%) 2-[(4,6-диметоксипіримідин-2-ил)пдроксиметил]-6-метоксиметилтрифторметансульфоніланіліду у вигляді безбарвних гранульованих кристалів (точка плавлення 91 - 92°С) Одержані дані 1 Н ЯМР 300МГц CDCI3 ТМС 11,12 (шир, 1Н), 7,69 (д, 1Н), 7,56 (д, 1Н), 7,41 (т, 1Н), 6,08 (д, 1Н), 5.99 (с, 1Н), 4,91 (д , 1Н), 4,69 (до, 2Н), 3,99 (с, 6Н), 3,42 (с, ЗН) Випробування 1 Ґрунт для рису заповнювали в пластиковий горщик площею 100см2 До нього додавали воду і проводили ущільнення ґрунту На глибину 0,5см висівали насіння EChinoChloa oryziCola Vasing , MonoChirola Vagmahs (Burin, f ) Presl var Plantagmea (Roxb ) Solms-Laub і SCirpus junCoides Roxb subsp hotarui (Ohwi) T Koyama Далі, два рисових паростки, кожний на стадії двох листків, пересаджували на глибину 2см Воду заповнюва 18 17 56338 ли на глибину Зсм На наступний день диспергоСимволи, що використовуються в таблиці 1, ваний у воді порошок, одержаний змішанням 10 мають наступні значення частин за вагою кожного із сполук, одержаних в Ес EChinoChloa oryziCola Vasing прикладах 1 - 4, з 0,5 частини за вагою полюксиеMo MonoChona Vagmahs (Burm F) Presl Var ти л енокти л фенілового ефіру, 0,5 частини за вагою Plantagmea (roxb ) Solms-Laub , натрієвої солі продукту конденсації рSC SCirpus junCoides Roxb subsp hotarui нафталінсульфонова кислота-формалін, 20 ваго(Ohwi) T Koyama вих частин діатомової землі і 69% вагових частин У вищезгаданому випробуванні по суті не було глини, розбавляли водою і капали на поверхню ніякого пошкодження рису-падді води так, щоб КІЛЬКІСТЬ нанесеного (г/10 ар) активВипробування 2 ного інгредієнта (кожної сполуки) складала рівень, Ґрунт для рису заповнювали в пластиковий вказаний в таблиці 1 Розвиток і ріст рослин відбулоток площею 200см2 У нього вводили воду і провалися в теплиці Через 28 днів гербіцидну дію водили ущільнення ґрунту На глибину 0,5см висікожної сполуки оцінювали за нижченаведеним вали насіння MonoChona vagmahs (Burm f ) Presl стандартом Результати приводяться в таблиці 1 var plantagmea (Roxb) Solms-Laub і SCirpus junCoides Roxb subsp hotarui (Ohwi) T Koyama Стандарт гербіцидної дії (рівень пригнічення Далі, закладали бульби Sagittana pygmaea Miq розвитку і ріст) Воду заповнювали на глибину Зсм На наступний 5 Гербіцидна дія 90% або більше пошкоджендень диспергований у воді порошок, що містить як ня рису-падді, активний інгредієнт сполуку, одержану в прикладі 4 Гербіцидна дія 70% або більше до менше, 1, або таку ж порівняльну сполуку, яку використаза 90%, пошкодження рису-падді ли у випробуванні 1, яку одержали таким же споЗ Гербіцидна дія 50% або більше до менше, собом, як у випробуванні 1, розбавляли водою і за 70%, пошкодження рису-падді прикрапували на поверхню води так, щоб КІЛЬКІСТЬ 2 Гербіцидна дія 30% або більше до менше, нанесеного активного інгредієнта (кожної сполуки) за 50%, пошкодження рису-падді складала рівень, вказаний в таблиці 2 Протягом 1 Гербіцидна дія 10% або більше до менше, двох днів, починаючи з наступного дня, проводили за 30%, пошкодження рису-падді дренаж і ПІДГОДІВЛЮ кожної рослини на глибині 2см 0 Гербіцидна дія менше за 10%, пошкодження один раз в день Потім лоток вміщували в теплицю рису-падді для розвитку і росту рослин На 28 день від застоДля порівняння, таке ж випробування провосування сполуки гербіцидну дію кожної сполуки дили з використанням 2-[(4,6-диметоксипіримідиноцінювали за таким же стандартом, який викорис2-ил)пдроксиметил]N-трифторметансульфонілтали у випробуванні 1 Результати приводяться в аніліду, представленого наступною формулою таблиці 2 (дана сполука є сполукою №10-111 в WO 96/41799) Таблиця 2 t< -OCH3 Сполука 0СН 3 Приклад 1 Результати також приводяться в таблиці 1 Таблиця 1 КІЛЬКІСТЬ, яка ви Сполука Приклад 1 Приклад 2 Приклад 3 Приклад 4 користовується (г/10 ар) 25,0 6,3 1,6 0,4 25,0 6,3 1,6 0,4 25,0 6,3 1,6 0,4 25,0 6,3 1,6 0,4 Гербіцидна дія Ее Мо SC 5 4 3 1 5 5 5 А 5 5 5 4 5 5 5 2 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 3 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 Порівняльний приклад Нанесена КІЛЬКІСТЬ (г/Юар) 5,0 2,5 1,3 0,6 2,5 1,3 0,6 Гербіцидна Мо SC 5 5 5 5 4 4 2 2 3 4 1 3 0 1 дія Sa 5 5 5 2 4 2 0 Символи, що використовуються в таблиці 2, мають наступні значення Мо MonoChona Vagmahs (Burm f ) Presl var Plantagmea (Roxb ) Solms-Laub , SC SCirpus junCoides Roxb subsp hotarui (Ohwi) T Koyama Sa Sagittana pygmaea Miq Випробування З Рисовий ґрунт заповнювали в пластиковий ло2 ток площею 200см Його поливали водою і проводили ущільнення ґрунту На глибину 0,5см висівали насіння EChinoChloa oryziCola Vasing Далі два рисових паростки, кожний в стадії двох листків, висаджували на глибину 2см На наступний день (коли ще не було проростання EChinoChloa oryziCola Vasing) або коли рослина досягала своєї стадії трьох листків, диспергований у воді порошок, що містить як активний інгредієнт кожну із 20 19 56338 сполук, одержаних в прикладах 1 - 3, і таку ж порі5,0 3 1 вняльну сполуку, яку використали у випробуванні 2,5 2 0 Порів1, яку одержали таким же способом, як у випробуняльна 1,3 1 0 ванні 1, розбавляли водою і прикрапували на посполука 0,6 0 0 верхню води так, щоб КІЛЬКІСТЬ активного інгредіє0,3 0 0 нта (кожної сполуки) складала рівень, вказаний в таблиці 3 Потім рослини вміщували в теплицю Символ, що використовується в таблиці 3, має для розвитку і росту На 28 день від застосування наступне значення сполуки гербіцидну дію кожної сполуки оцінювали Ее EChinoChloa oryziCola Vasmg за таким же стандартом, який використали у виУ вищезгаданому випробуванні по суті не було пробуванні 1 Результати Приводяться в таблиці З ніякого пошкодження рису-падді Випробування 4 Таблиця З Рисовий ґрунт заповнювали в пластиковий ло2 ток площею 200см Проводили ущільнення ґрунКІЛЬКІСТЬ, Гербіцидна дія (Ее) ту На глибину 0,5см висівали насіння EChinoChloa яка викори- Використан- ВикористанoryziCola Vasmg і SCirpus junCoides Roxb subsp Сполука стовується ня до про- ня на стадії hotarui (Ohwi) T Koyama Закладали бульби (г/Юар) ростання 3 ЛИСТКІВ Sagittana pygmaea Miq і Cuperus serotmus Rottb 5,0 5 5 Далі, два рисових паростки, кожний в стадії двох 2,5 5 4 листків, пересаджували на глибину 2см Воду заПриклад повнювали на глибину Зсм На наступний день 1,3 3 2 1 диспергований у воді порошок, що містить як акти0,6 2 1 вний інгредієнт сполуку, одержану в прикладі 4, 0,3 1 0 або таку ж порівняльну сполуку, яку використали у 5,0 5 5 випробуванні 1, яку одержують таким же спосо2,5 5 5 бом, як у випробуванні 1, розбавляли водою і приПриклад 1,3 5 5 колювали на поверхню води так, щоб КІЛЬКІСТЬ 2 0,6 5 4 активного інгредієнта (кожної сполуки) складала 0,3 4 3 рівень, вказаний в таблиці 4 Потім розвиток і ріст 5,0 5 5 рослин проходили в теплиці На 28 день після за2,5 5 5 стосування сполуки гербіцидна дія і пошкодження Приклад падді-рису для кожної сполуки оцінювали за таким 1,3 5 5 3 же стандартом, який використали у випробуванні 0,6 5 4 1 Результати приводяться в таблиці 4 0,3 4 2 Таблиця 4 Символи, що використовуються в таблиці 4, мають наступні значення ес EChinoChloa oryziCola Vasmg SC SCirpus junCoides Roxb subsp hotarui (Ohwi) T Koyama Sa Sagittana pygmaea Miq Су Cuperus serotmus Rottb Or Oryza Sativa L (рис-падді) Випробування 5 Рисовий ґрунт заповнювали в пластиковий лоток площею 200см2 Проводили ущільнення ґрунту На глибину 0,5см висівали насіння EChinoChloa oryziCola Vasmg (Ее) Коли Ес досягав своєї стадії одного листка, двох листків або трьох листків, ди SC 5 Sa 5 5 5 4 5 Су 5 5 5 4 5 Пошкодження рису Or о о оо Ес 5 5 4 2 4 2 1 0 ел ел ел 5,0 2,5 1,3 0,6 5,0 2,5 1,3 0,6 ел ел ел Порівняльна сполука (г/Юар) ел ел ел ел Приклад 4 Гербіцидна дія КІЛЬКІСТЬ, яка використовується ел ел ел Сполука 1 0 0 0 спергований у воді порошок, що містить як активний інгредієнт сполуку, одержану в прикладі 4, або таку ж порівняльну сполуку, яку використали у випробуванні 1, яку одержали таким же способом, як у випробуванні 1, розбавляли водою і прикрапували на поверхню води так, щоб КІЛЬКІСТЬ активного інгредієнта (кожної сполуки) складала рівень, показаний в таблиці 5 Потім забезпечували розвиток і ріст рослин в теплиці На 28 день після застосування сполуки гербіцидну дію кожної сполуки оцінювали за таким же стандартом, який використали у випробуванні 1 Результати приводяться в таблиці 5 21 56338 Таблиця 5 Порівняльний приклад 5,0 2,5 1,3 5,0 2,5 1,3 Гербіцидна дія (Ее) Стадія нанесення 1 лис- 2 лис- 3 листток тки ки 5 5 4 3 1 0 о о ю со ел ел Приклад 4 Нанесена КІЛЬКІСТЬ (г/Юар) о о to со ел ел Сполука Як зрозуміло з вищенаведених результатів випробувань, сполуки даного винаходу виявляють чудову гербіцидну дію відносно злакових бур'янів, особливо, EChinoChloa oryziCola Vasmg і аналогічних, при низькій дозі в порівнянні з відомими сполуками схожих структур Випробування 6 (випробування за тератологією) ВІДПОВІДНО ДО процедури, описаної в публікації «Test guidelines for pestiCide (59 Nohsan Notification №3850)» Японського Міністерства сільського господарства, лісогосподарства і рибного господарства, кожну із сполук, одержаних в прикладах 1 - 4, і таку ж порівняльну сполуку, яку використовувалася у випробуванні 1, зважували і суспендували у 0,5% водному розчині карбоксиметилцелюлози, суспензію примусово перорально вводили 10 вагітним пацюкам SD-лінм з 6-го по 15й день вагітності Контрольній групі пацюків вводили тільки 0,5% водний розчин карбоксиметилцелюлози КІЛЬКІСТЬ кожної сполуки, що вводилася визначали за допомогою попереднього випробування А саме, кожну сполуку вводили трьом неваптним пацюкам SD-лінм протягом 10 послідовних днів, і встановлювали максимальну дозу, що переноситься, цю дозу приймали за КІЛЬКІСТЬ кожної сполуки, що вводилася На 20-ий день вагітності кожного випробуваного пацюка піддавали кесареву перетину і проводили дослідження плодів (число живих плодів, число ембріональної резорбції, число мертвих плодів, співвідношення статі, вага плоду і ЗОВНІШНІ аномалії плоду) Далі, плоди фіксували в 70% етанолі, їх м'які тканини мацерирували в гідроксиді калію, їх кістяки забарвлювали алізариновим червоним S і проводили обстеження кістяка Результати показані в таблиці 6 В цих випробуваннях випадок без якоі-небудь аномалії вважався «що вдався», а випадок з будь-якою аномалією вважався, що не вдався Таблиця 6 Нанесена Число Результати досліджевипробувань (мг/кг/день) них крис Приклад 1 450 10 Вдалося Приклад 2 550 10 Вдалося Приклад 3 1000 10 Вдалося Приклад 4 400 10 Вдалося Порівняль90 10 Не вдалося на сполука Контроль 0 10 Вдалося Сполука КІЛЬКІСТЬ 22 Таким чином, коли кожну із сполук, одержаних в прикладах 1 - 4, вводили перорально вагітним пацюкам SD-лінм послідовно з 6-го по 15-й день вагітності при дослідженні плодів було виявлено зниження ваги плоду в групі пацюків, яким вводили порівняльну сполуку При обстеженні плоду групи пацюків, яким вводили порівняльну сполуку, були виявлені ЗОВНІШНІ дефекти розвитку, тобто ектродактилія і брахідактилія передніх лап, цих явищ не спостерігалося у випадках з будь-якою із сполук, одержаних в прикладах 1 - 4 Приклад 1 готової препаративної форми 10 частин за вагою сполуки, одержаної в прикладі 1, змішували з 0,5 частини за вагою полюксиетиленоктилфенілового ефіру, 0,5ваг частини натрієвої солі продукту конденсації нафталінсульфонова кислота-формалін, 20ваг частинами діатомової землі і 69ваг частинами глини Суміш подрібнювали для одержання диспергованого у воді порошку Приклад 2 готової препаративної форми Юваг частин сполуки, одержаної в прикладі 2, змішували з 0,5ваг частинами полюксиетиленоктилфенілового ефіру, 0,5ваг частини натрієвої солі продукту конденсації нафталінсульфонова кислота-формалін, 20ваг частинами діатомової землі, 5ваг частинами білої сажі і 64ваг частинами карбонату кальцію Суміш подрібнювали для одержання диспергованого у воді порошку Приклад 3 готової препаративної форми Юваг частин сполуки, одержаної в прикладі З, змішували з 0,5ваг частинами полюксиетиленоктилфенілового ефіру, 0,5ваг частинами натрієвої солі продукту конденсації нафталінсульфонова кислота-формалін, 20ваг частинами діатомової землі, 5ваг частинами білої сажі і 64ваг частинами глини Суміш подрібнювали для одержання диспергованого у воді порошку Приклад 4 готової препаративної форми ЗОваг частин сполуки, одержаної в прикладі 1, змішували з бОваг частинами суміші 1 1 (об'ємне відношення) ксилолу і ізофорону і Юваг частинами суміші 1 1 1 (об'ємне відношення) алкілату полюксиетиленсорбітану, полюксиетиленалкіларилового полімеру і алкіларилсульфонату для одержання емульгованого концентрату Приклад 5 готової препаративної форми Юваг частин води додавали до Юваг частин сполуки, одержаної в прикладі 3, 80ваг частин змішаного наповнювача 1 3 (об'ємне відношення) тальку і бентоніту, 5ваг частин білої сажі і 5ваг частин суміші 1 1 1 (об'ємне відношення) алкілату полюксиетиленсорбітану, полюксиетиленалкіларилового полімеру і алкіларилсульфонату Суміш добре перемішували, щоб зробити пасту Пасту екструдували через отвори 0,7мм сита і сушили Висушений матеріал розрізали на шматочки довжиною від 0,5 до 1мм, одержуючи гранули Приклад 6 готової препаративної форми Юваг частин сполуки, одержаної в прикладі 4, змішували з 0,5ваг частинами полюксиетиленоктилфенілового ефіру, 0,5ваг частинами натрієвої солі продукту конденсації р-нафталінсульфонова кислота-формалін, 20ваг частинами діатомової землі і 69ваг частинами глини Суміш подрібнювали для одержання диспергованого у воді порош 23 56338 24 алкілату полюксиетиленсорбітану, полюксиетилеку налкіларилового полімеру і алкіларилсульфонату Приклад 7 готової препаративної форми для одержання емульгованого концентрату 10 вагових частин сполуки, одержаної в приПриклад 10 готової препаративної форми кладі 4, змішували з 0,5ваг частинами полюксиети л енокти л фенілового ефіру, 0,5ваг частинами 10 вагових частин додавали до Юваг частин натрієвої солі продукту конденсації рсполуки, одержаної в прикладі 4, 80ваг частин нафталінсульфонова кислота-формалін, 20ваг змішаного наповнювача 1 3 (об'ємне відношення) частинами діатомової землі, 5ваг частинами білої тальку і бетоніту, 5ваг частин білої сажі і 5ваг сажі і 64ваг частинами глини Суміш подрібнювачастин суміші 1 1 1 (об'ємне відношення) алкіли для одержання диспергованого у воді порошку лату полюксиетиленсорбітану, полюксиетиленалПриклад 8 готової препаративної форми кіларилового полімеру і алкіларилсульфонату 10 вагових частин сполуки, одержаної в приСуміш добре перемішували з одержанням пасти кладі 4, змішували з 0,5ваг частинами полюксиеПасту екструдували через отвори 0,7мм сита і сутиленоктилфенілового ефіру, 0,5ваг частинами шили Висушений матеріал розрізали на шматочки натрієвої солі продукту конденсації рдовжиною 0,5 -1 мм, одержуючи гранули нафталінсульфонова кислота-формалін, 20ваг Промислова застосовність частинами діатомової землі, 5ваг частинами білої Дана сполука має гербіцидну активність при сажі і 64ваг частинами карбонату кальцію Суміш низькій дозі стосовно різних бур'янів протягом різподрібнювали для одержання диспергованого у них сезонів, надає сильну переважну дію, особливоді порошку во на злакові бур'яни, безпечна для ссавців (наприклад, не викликає мальформацію) і є новою Приклад 9 готової препаративної форми речовиною, корисною як гербіцид або як початкоЗО вагових частин сполуки, одержаної в привий матеріал для його одержання кладі 4, змішували з бОваг частинами суміші 1 1 (об'ємне відношення) ксилолу і ізофорону і Юваг частинами суміші 1 1 1 (об'ємне відношення) Підписано до друку 05 06 2003 р Тираж 39 прим ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)236-47-24
ДивитисяДодаткова інформація
Назва патенту англійськоюDerivatives of di-or trifluorinesulfonilanilide, a method for preparing thereof and herbicides containing the mentioned derivatives as active ingredients
Назва патенту російськоюПроизводные ди- или трифторметансульфониланилида, способ их получения и гербициды, содержащие указанные производные в качестве активных ингредиентов
МПК / Мітки
МПК: A01N 43/54, C07C 317/36, A01N 41/06, C07D 239/52
Мітки: інгредієнти, похідні, гербіциди, одержання, дії, трифторметансульфоніланіліду, спосіб, вказані, містять, активні
Код посилання
<a href="https://ua.patents.su/12-56338-pokhidni-di-abo-triftormetansulfonilanilidu-sposib-kh-oderzhannya-i-gerbicidi-shho-mistyat-vkazani-pokhidni-yak-aktivni-ingrediehnti.html" target="_blank" rel="follow" title="База патентів України">Похідні ди- або трифторметансульфоніланіліду, спосіб їх одержання і гербіциди, що містять вказані похідні як активні інгредієнти</a>
Попередній патент: Двокорпусне рятувальне судно окран і вітрильне озброєння ок
Наступний патент: Роторний сферичний двигун
Випадковий патент: Механізм керування поворотом напівпричепа автопоїзда з важелями поворотних цапф різної довжини та електрогідравлічним приводом