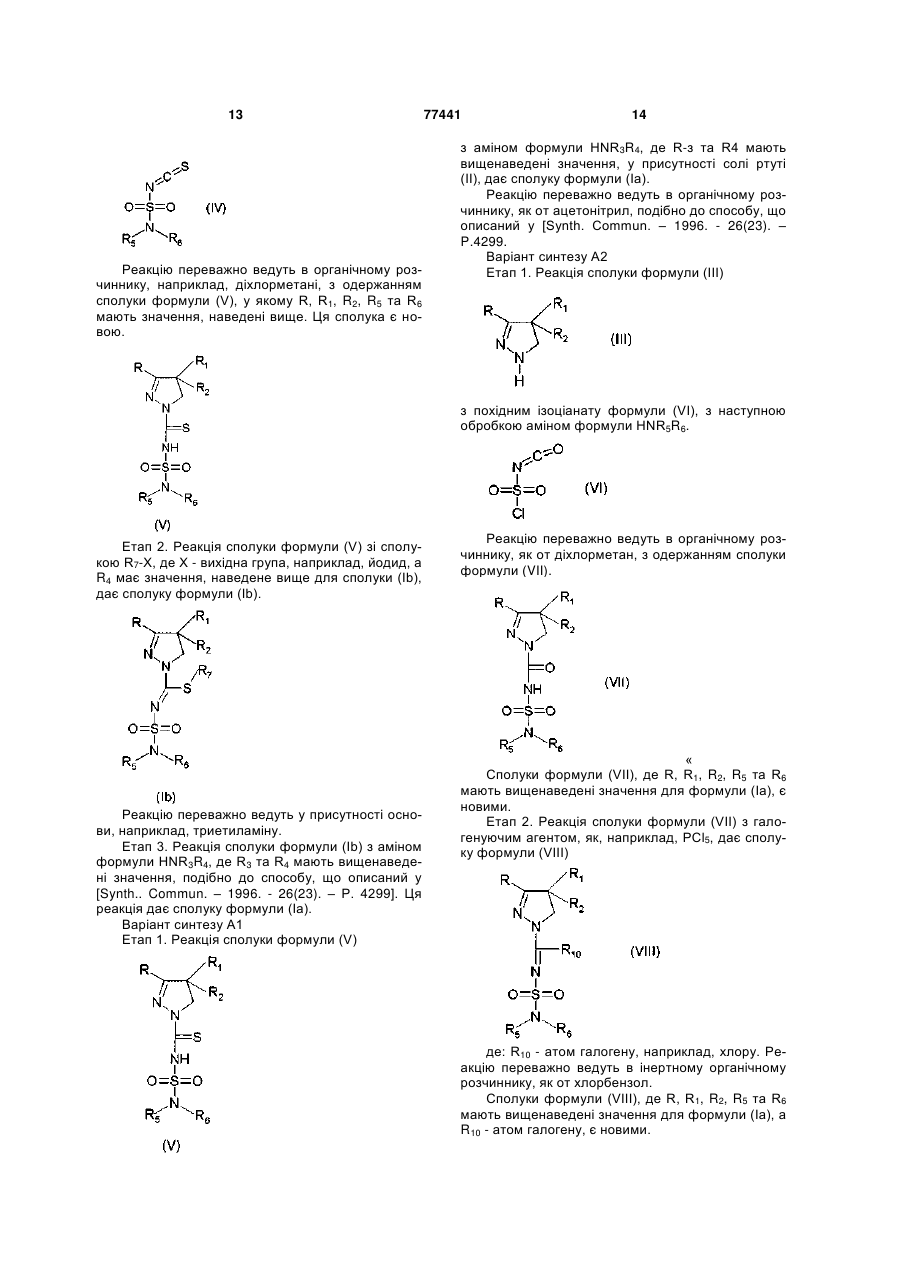
Похідні 4,5-дигідро-1н-піразолу з сильнодіючою антагоністичною активністю щодо рецепторів св-1, спосіб їх одержання (варіанти), проміжні сполуки, фармацевтична композиція та спосіб її одержання
Номер патенту: 77441
Опубліковано: 15.12.2006
Автори: ван Стюйвенберг Герман Г., Тіпкер Якобус, Герреманс Арнольдус Г.Й., Крузе Корнеліс Г., Ланге Йозефус Х.М.
Формула / Реферат
1. Сполуки загальної формули (Iа) або (Іb)
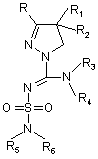 (Iа),
(Iа), 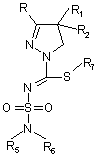 , (Іb)
, (Іb)
де
- R та R1 незалежно являють собою феніл, тієніл або піриділ, групи яких можуть бути заміщені 1, 2 або 3 однаковими або різними замісниками Y з групи С1-3-алкіл або алкокси, гідрокси, галоген, трифторметил, трифторметилтіо, трифторметокси, нітро, аміно, моно- або діалкіл(С1-2)-аміно, моно- або діалкіл(С1-2)-амідо, (С1-3)-алкілсульфоніл, диметилсульфамідо, С1-3-алкілоксикарбоніл, карбоксил, трифторметилсульфоніл, ціано, карбамоїл, сульфамоїл та ацетил, або R та/або R1 представляють нафтил;
- R2 являє собою водень, гідрокси, С1-3 алкокси, ацетилокси або пропіонілокси,
- R3 являє собою атом водню або розгалужену чи нерозгалужену C1-8 алкільну групу або С3-7 циклоалкільну групу, причому алкільна або циклоалкільна група може бути заміщена гідроксигрупою;
- R4 являє собою атом водню або розгалужений чи нерозгалужений C1-8 алкіл, С3-8 циклоалкіл, С2-10 гетероалкіл, С3-8 неароматичний гетероциклоалкіл або С4-10 неароматичну гетероциклоалкілалкільну частину, причому такі частини можуть містити один або кілька гетероатомів з групи (О, N, S) і бути заміщені кетогрупою, трифторметильною групою, С1-3 алкільною групою, гідрокси, аміно, моноалкіламіно- або діалкіламіногрупою або атомом фтору, або ж R4 являє собою аміно, гідрокси, фенокси чи бензилоксигрупу, або ж R4 являє собою розгалужену чи нерозгалужену C1-8 алкокси, С3-8 алкеніл, C5-8 циклоалкеніл або С6-9 циклоалкеналкіл групу, які можуть містити атом сірки, азоту або кисню, кетогрупу або -SO2- групу, і зазначені C1-8 алкокси, С3-8 алкеніл, C5-8 циклоалкеніл або С6-9 циклоалкенілалкілгрупи можуть бути заміщені гідроксигрупою, трифторметильною групою, аміногрупою, моноалкіламіногрупою або діалкіламіногрупою або атомом фтору, або ж R4 являє собою феніл, бензил, піридил, тієніл, піридилметил або фенетилгрупу, у яких ароматичні кільця можуть бути заміщені 1, 2 або 3 замісниками Y, де Y має значення, наведені вище, або
- R4 являє собою групу NR8R9 за умови, що R3 є атомом водню або метилгрупою, тоді як R8 та R9 є однакові або різні й являють собою С1-4 алкіл або C2-4 трифторалкіл, або ж R8 та R9 разом з атомом водню, до якого вони приєднані, утворюють насичену або ненасичену гетероциклічну частину, яка має від 4 до 8 атомів у кільці, і ця гетероциклічна частина може містити атом кисню або сірки, кетогрупу або -SO2-групу, або додатковий атом азоту, причому насичена або ненасичена гетероциклічна частина може бути заміщена С1-4 алкілгрупою, або
R3 та R4 разом з атомом азоту, до якого вони приєднані, утворюють насичену або ненасичену, моноциклічну або біциклічну гетероциклічну частину з 4-10 атомами у кільці, причому зазначена гетероциклічна частина може містити один або більше гетероатомів з групи (О, N, S) або кетогрупу, або -SO2-групу й може бути заміщена С1-4 алкіл, гідроксіалкіл, феніл, тієніл, піридил, аміно, моноалкіламіноалкіл, діалкіламіноалкіл, моноалкіламіно, діалкіламіно, аміноалкіл, азетидініл, піролідиніл, піперідиніл або гексагідро-1Н-азепінілгрупою;
- R5 та R6 незалежно один від одного являють собою атом водню або розгалужену чи нерозгалужену C1-8 алкільну чи алкенільну групу, причому такі групи можуть містити один або кілька гетероатомів з групи (О, N, S), кетогрупу або -SO2-групу й можуть бути заміщені гідрокси або аміногрупою, або ж R5 та R6, незалежно один від одного являють собою С3-8 циклоалкільну групу або С3-8 циклоалкенільну групу, які можуть містити один або кілька гетероатомів з групи (О, N, S) або -SO2-групу, й ці групи можуть бути заміщені гідроксигрупою, алкіл (С1-3), -SO2-групою, кетогрупою, аміногрупою, моно-алкіламіногрупою (С1-3), або діалкіламіногрупою (С1-3), або
R5 являє собою нафтильну або фенільну групу, причому фенільна група може бути заміщена 1, 2 або 3 замісниками Y, де Y має значення, наведені вище, за умови, що R6 являє собою атом водню або розгалужену чи нерозгалужену алкільну групу (C1-5), причому алкільна група може містити один або кілька гетероатомів з групи (О, N, S) aбo -SO2-групу й алкільна група може бути заміщена гідрокси, кето або аміногрупою,
або R5 та R6 разом з атомом азоту, до якого вони приєднані, утворюють моноциклічну, біциклічну або трициклічну алкільну чи алкенільну групу, яка може містити кільцеві гетероатоми з групи (О, N, S), кетогрупу або -SO2-групу, і ця моноциклічна, біциклічна або трициклічна алкільна чи алкенільна група може бути заміщена гідроксигрупою, алкіл (С1-3), -SO2-групою, кетогрупою, аміногрупою, моноалкіламіногрупою (С1-3), діалкіламіногрупою (С1-3), піролідинілгрупою або піперидинілгрупою, причому моноциклічна, біциклічна або трициклічна алкільна чи алкенільна група може містити анельовану фенільну групу, яка, у свою чергу, може бути заміщена 1 або 2 замісниками Y, де Y має значення, наведені вище,
R7 являє собою розгалужений або нерозгалужений С1-3 алкіл,
та їхні таутомери, стереоізомери, пролікарські форми та солі.
2. Сполука за п. 1, яка представляє (-)-(4S)-3-(4-хлорфеніл)-N-метил-4-феніл-N’-((піперидин-1-іл)сульфоніл)-4,5-дігідро-1Н-піразол-1-карбоксамідин, що має формулу (X):
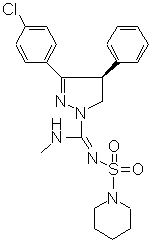 , (X)
, (X)
та її солі.
3. Фармацевтична композиція, яка містить фармацевтично активну кількість принаймні однієї сполуки за п.1 як діючу речовину.
4. Спосіб одержання фармацевтичної композиції за п. 2, який відрізняється тим, що сполуці за п.1 надають форму, придатну для введення до організму.
5. Спосіб одержання сполук формули (Іb)
 , (Іb)
, (Іb)
який відрізняється тим, що одержують сполуку, в якій R, R1-2, R5-6 та R7 мають значення, наведені в п. 1, шляхом
(1) реакції в органічному розчиннику сполуки формули (III)
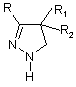 (III)
(III)
зі сполукою формули (IV)
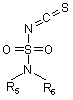 (IV)
(IV)
з одержанням сполуки формули (V)
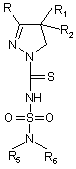 , (V)
, (V)
яку піддають реакції в присутності основи зі сполукою формули R7-X, де Х - відхідна група, наприклад йодид, або
(2) реакції сполуки формули (ІІІ)
 (III)
(III)
зі сполукою формули (IX)
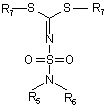 . (IX)
. (IX)
6. Спосіб одержання сполук формули (Iа)
 , (Iа)
, (Iа)
який відрізняється тим, що одержують сполуку, в якій R та R1-R6 мають значення, наведені в п.1, шляхом
(1) реакції сполуки формули (Іb)
 (Іb)
(Іb)
з аміном формули HNR3R4, або
(2) реакції сполуки формули (V)
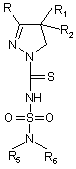 (V)
(V)
з аміном формули HNR3R4 у присутності солі Hg++ (II), або
(3) реакції сполуки формули (III)
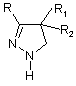 (III)
(III)
зі сполукою формули (VI)
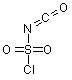 (VI)
(VI)
з наступною обробкою в органічному розчиннику з аміном формули HNR5R6 з одержанням сполуки формули (VII)
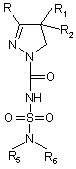 , (VII)
, (VII)
яку піддають реакції з галогенізуючим агентом, як наприклад РСl5, з одержанням сполуки формули (VIII)
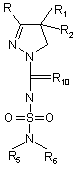 , (VIII)
, (VIII)
яку піддають реакції в інертному органічному розчиннику з аміном формули HNR3R4.
7. Сполуки загальної формули (V)
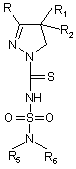 , (V)
, (V)
де R, R1, R2, R5 та R6 мають значення, наведені в п.1.
8. Сполуки загальної формули (VII)
 , (VII)
, (VII)
де R, R1, R2, R5 та R6, мають значення, наведені в п.1.
9. Сполуки загальної формули (VIII)
 , (VIII)
, (VIII)
де R, R1, R2, R5 та R6 мають значення, наведені в п.1, a R10 - атом галогену.
10. Застосування сполуки за п.1 для одержання фармацевтичної композиції для лікування розладів, пов'язаних з нейротрансмісією канабіноїдів.
11. Застосування за п. 10, яке відрізняється тим, що зазначені розлади являють собою психічні розлади, як то психози, збентеженість, депресія, дефіцит уваги, розлади пам'яті, пізнавальні розлади, розлади апетиту, опасистість, згубні звички, гіперсексуальність, наркозалежність, неврологічні розлади, як то недоумство, дистонія, м'язова спастичність, тремтіння, травматичне пошкодження мозку, інсульт, хвороба Паркінсона, хвороба Альцгеймера, епілепсія, хвороба Гантінгтона, синдром Турета, церебральна ішемія, церебральна апоплексія, черепно-мозкова травма, удар, пошкодження хребта, нейрозапальні хвороби, бляшковий склероз, вірусний енцефаліт, хвороби, пов'язані з демієлінізацією, а також для лікування болів, включаючи невропатичні больові прояви, та інших хвороб, що пов'язані з нейротрансмісією канабіноїдів, як то септичний шок, глаукома, рак, діабет, блювання, нудота, астма, респіраторні захворювання, шлунково-кишкові розлади, виразка шлунку, діарея та серцево-судинні розлади.
Текст
1. Сполуки загальної формули (Iа) або (Іb) UA 2 (19) 1 C2 (54) ПОХІДНІ 4,5-ДИГІДРО-1Н-ПІРАЗОЛУ З СИЛЬНОДІЮЧОЮ АНТАГОНІСТИЧНОЮ АКТИВНІСТЮ ЩОДО РЕЦЕПТОРІВ СВ-1, СПОСІБ ЇХ ОДЕРЖАННЯ (ВАРІАНТИ), ПРОМІЖНІ СПОЛУКИ, ФАРМАЦЕВТИЧНА КОМПОЗИЦІЯ ТА СПОСІБ ЇЇ ОДЕРЖАННЯ 3 моноалкіламіно- або діалкіламіногрупою або атомом фтору, або ж R4 являє собою аміно, гідрокси, фенокси чи бензилоксигрупу, або ж R4 являє собою розгалужену чи нерозгалужену C1-8 алкокси, С3-8 алкеніл, C5-8 циклоалкеніл або С6-9 циклоалкеналкіл групу, які можуть містити атом сірки, азоту або кисню, кетогрупу або -SO2- групу, і зазначені C1-8 алкокси, С3-8 алкеніл, C5-8 циклоалкеніл або С69 циклоалкенілалкілгрупи можуть бути заміщені гідроксигрупою, трифторметильною групою, аміногрупою, моноалкіламіногрупою або діалкіламіногрупою або атомом фтору, або ж R4 являє собою феніл, бензил, піридил, тієніл, піридилметил або фенетилгрупу, у яких ароматичні кільця можуть бути заміщені 1, 2 або 3 замісниками Y, де Y має значення, наведені вище, або - R4 являє собою групу NR8R9 за умови, що R3 є атомом водню або метилгрупою, тоді як R8 та R9 є однакові або різні й являють собою С1-4 алкіл або C2-4 трифторалкіл, або ж R8 та R9 разом з атомом водню, до якого вони приєднані, утворюють насичену або ненасичену гетероциклічну частину, яка має від 4 до 8 атомів у кільці, і ця гетероциклічна частина може містити атом кисню або сірки, кетогрупу або -SO2-групу, або додатковий атом азоту, причому насичена або ненасичена гетероциклічна частина може бути заміщена С1-4 алкілгрупою, або R3 та R4 разом з атомом азоту, до якого вони приєднані, утворюють насичену або ненасичену, моноциклічну або біциклічну гетероциклічну частину з 4-10 атомами у кільці, причому зазначена гетероциклічна частина може містити один або більше гетероатомів з групи (О, N, S) або кетогрупу, або SO2-групу й може бути заміщена С1-4 алкіл, гідроксіалкіл, феніл, тієніл, піридил, аміно, моноалкіламіноалкіл, діалкіламіноалкіл, моноалкіламіно, діалкіламіно, аміноалкіл, азетидініл, піролідиніл, піперідиніл або гексагідро-1Н-азепінілгрупою; - R5 та R6 незалежно один від одного являють собою атом водню або розгалужену чи нерозгалужену C1-8 алкільну чи алкенільну групу, причому такі групи можуть містити один або кілька гетероатомів з групи (О, N, S), кетогрупу або -SO2-групу й можуть бути заміщені гідрокси або аміногрупою, або ж R5 та R6, незалежно один від одного являють собою С3-8 циклоалкільну групу або С3-8 циклоалкенільну групу, які можуть містити один або кілька гетероатомів з групи (О, N, S) або -SO2-групу, й ці групи можуть бути заміщені гідроксигрупою, алкіл (С1-3), -SO2-групою, кетогрупою, аміногрупою, моно-алкіламіногрупою (С1-3), або діалкіламіногрупою (С1-3), або R5 являє собою нафтильну або фенільну групу, причому фенільна група може бути заміщена 1, 2 або 3 замісниками Y, де Y має значення, наведені вище, за умови, що R6 являє собою атом водню або розгалужену чи нерозгалужену алкільну групу (C1-5), причому алкільна група може містити один або кілька гетероатомів з групи (О, N, S) aбo -SO2групу й алкільна група може бути заміщена гідрокси, кето або аміногрупою, або R5 та R6 разом з атомом азоту, до якого вони приєднані, утворюють моноциклічну, біциклічну або трициклічну алкільну чи алкенільну групу, яка може містити кільцеві гетероатоми з групи (О, N, 77441 4 S), кетогрупу або -SO2-групу, і ця моноциклічна, біциклічна або трициклічна алкільна чи алкенільна група може бути заміщена гідроксигрупою, алкіл (С1-3), -SO2-групою, кетогрупою, аміногрупою, моноалкіламіногрупою (С1-3), діалкіламіногрупою (С13), піролідинілгрупою або піперидинілгрупою, причому моноциклічна, біциклічна або трициклічна алкільна чи алкенільна група може містити анельовану фенільну групу, яка, у свою чергу, може бути заміщена 1 або 2 замісниками Y, де Y має значення, наведені вище, R7 являє собою розгалужений або нерозгалужений С1-3 алкіл, та їхні таутомери, стереоізомери, пролікарські форми та солі. 2. Сполука за п. 1, яка представляє (-)-(4S)-3-(4хлорфеніл)-N-метил-4-феніл-N’-((піперидин-1іл)сульфоніл)-4,5-дігідро-1Н-піразол-1карбоксамідин, що має формулу (X): Cl N N H N (X) N O S O N , та її солі. 3. Фармацевтична композиція, яка містить фармацевтично активну кількість принаймні однієї сполуки за п.1 як діючу речовину. 4. Спосіб одержання фармацевтичної композиції за п.2, який відрізняється тим, що сполуці за п.1 надають форму, придатну для введення до організму. 5. Спосіб одержання сполук формули (Іb) R N R1 R2 N S N O S R7 (Іb) O N R5 R6 , який відрізняється тим, що одержують сполуку, в якій R, R1-2, R5-6 та R7 мають значення, наведені в п.1, шляхом (1) реакції в органічному розчиннику сполуки формули (III) R R1 N R2 N H , зі сполукою формули (IV) (III) 5 N O S 77441 з аміном формули HNR3R4, або (2) реакції сполуки формули (V) S С R O N R6 , з одержанням сполуки формули (V) R O (V) NH O N R6 , яку піддають реакції в присутності основи зі сполукою формули R7-X, де Х - відхідна група, наприклад йодид, або (2) реакції сполуки формули (ІІІ) R R1 R2 N (III) N S , з аміном формули HNR3R4 у присутності солі Hg++ (II), або (3) реакції сполуки формули (III) R R1 N H , зі сполукою формули (VI) O С N R N R5 N R6 , 6. Спосіб одержання сполук формули (Iа) R N O (Iа) , який відрізняється тим, що одержують сполуку, в якій R та R1-R6 мають значення, наведені в п.1, шляхом (1) реакції сполуки формули (Іb) R R1 S N O S N R2 N R10 S (VIII) O N R5 R7 (Іb) O R6 R1 N O N R5 , яку піддають реакції з галогенізуючим агентом, як наприклад РСl5, з одержанням сполуки формули (VIII) R2 N O R6 R R6 N S R5 R3 N R5 (VII) N R4 O N O R2 N R2 NH R1 N (VI) O R1 (IX) O (III) N , з наступною обробкою в органічному розчиннику з аміном формули HNR5R6 з одержанням сполуки формули (VII) R7 S O S O S R2 Cl N N O R6 O S H , зі сполукою формули (IX) R7 S R5 S R5 (V) N N S N NH R2 O R2 S R1 N R1 (IV) N R5 6 , R6 , яку піддають реакції в інертному органічному розчиннику з аміном формули HNR3R4. 7. Сполуки загальної формули (V) 7 R N R2 N N O O R5 , де R, R1, R2, R5 та R6 мають значення, наведені в п.1. 8. Сполуки загальної формули (VII) N R1 R2 N O NH O S (VII) O N R5 N S (VIII) O N R6 R R2 N N R5 R1 R10 (V) NH S 8 R R1 S O 77441 R6 , де R, R1, R2, R5 та R6, мають значення, наведені в п.1. 9. Сполуки загальної формули (VIII) Винахід стосується групи нових енантіомерів похідних 4,5-дігідро-1Н-піразолу, що мають Sконфігурацію у 4-й позиції 4,5-дігідропіразольного кільця, способів одержання таких сполук та фармаційних композицій, що містять одну або кілька таких сполук у якості діючих речовин. Зазначені (S)-4,5-дігідро-1Н-піразоли є сильнодіючими антагоністами рецепторів канабіноїду (СВ1) і можуть використовуватися для лікування психічних та нервових розладів, пов'язаних з нейротрансмісією канабіноїду. Канабіноїди знаходяться у індійських коноплях Cannabis sativa L й використовуються у медицині протягом століть [Mechoulam R., Fegenbaum J..J. // Prog. Med. Chem. – 1987. – 24. – P.. 159]. Втім, лише в останньому десятиріччі досліди канабіноїдів висвітлили ключові дані щодо рецепторів канабіноїдів та їхніх (ендогенних) агоністів та антагоністів. Відкриття та наступне клонування двох різних підтипів рецепторів канабіноїдів (СВ1) та СВ2) стимулювали пошуки нових антагоністів рецепторів канабіноїдів [Munro S. et al. // Nature. – 1993. – 365. – P. 61; Matsuda L..A., Bonner Τ..I., Cannabinoid R6 , де R, R1, R2, R5 та R6 мають значення, наведені в п.1, a R10 - атом галогену. 10. Застосування сполуки за п.1 для одержання фармацевтичної композиції для лікування розладів, пов'язаних з нейротрансмісією канабіноїдів. 11. Застосування за п.10, яке відрізняється тим, що зазначені розлади являють собою психічні розлади, як то психози, збентеженість, депресія, дефіцит уваги, розлади пам'яті, пізнавальні розлади, розлади апетиту, опасистість, згубні звички, гіперсексуальність, наркозалежність, неврологічні розлади, як то недоумство, дистонія, м'язова спастичність, тремтіння, травматичне пошкодження мозку, інсульт, хвороба Паркінсона, хвороба Альцгеймера, епілепсія, хвороба Гантінгтона, синдром Турета, церебральна ішемія, церебральна апоплексія, черепно-мозкова травма, удар, пошкодження хребта, нейрозапальні хвороби, бляшковий склероз, вірусний енцефаліт, хвороби, пов'язані з демієлінізацією, а також для лікування болів, включаючи невропатичні больові прояви, та інших хвороб, що пов'язані з нейротрансмісією канабіноїдів, як то септичний шок, глаукома, рак, діабет, блювання, нудота, астма, респіраторні захворювання, шлунково-кишкові розлади, виразка шлунку, діарея та серцево-судинні розлади. Receptors / Pertwee R..G. Ed. – London: Academic Press, 1995. – 117 p.]. Крім того, фармаційні фірми зацікавилися розробкою ліків для хвороб, пов'язаних з розладами канабоідної системи Велике поширення рецепторів СВ1 у мозку поряд з суворо периферійною локалізацією рецепторів СВ2 робить рецептори СВ1 дуже привабливою молекулярною мішенню для розробки спрямованих на ЦНС ліків від психічних та нервових розладів [Consroe Ρ. // Neurobiology of Disease. – 1998. – 5. – P. 534; Pop Ε. // Curr. Opin. in CPNS Investigational Drugs. – 1999. – 1. – P.. 587; Greenberg D..A. // Drug News Perspect. – 1999. – 12. – P. 458; Pertwee R.G. // Progress in Neurobiology. – 2001. – 63. – P. 569] Наразі відомі кілька типів антагоністів рецепторів СВ1. Фірма "Санофі" встановила, що деякі з її діарилпіразолів діють як селективні антагоністи рецепторів СВ1. Прикладом може бути SR-141716A, який зараз проходить другу фазу клінічних випробувань проти психічних розладів [Dutta А.К. et al. // Med. Chem. Res. – 1994. – 5. – P.. 54; Lan R. et al. // J. Med. Chem. – 1999. – 42. – P. 769; NakamuraPalacios Ε..Μ. et al. // CNS Drug Rev. – 1999. – 5. – 9 P. 43].. CP-272871 - це похідне піразолу, подібне до SR-141716А, але менш сильнодіюче й менш селективне до підтипів рецепторів СВ1, ніж SR141716A [Meschler J..P. et al. // Biochem. Pharmacol. – 2000. – 60. – P. 1315]. Встановлено, що антагоністами рецепторів СВ1 є аміноалкіліндоли Прикладом є іодоправадолін (АМ-630), впроваджений 1995ρ. АМ-630 є антагоністом рецепторів СВ1, але іноді поводиться як частковий агоніст [Hosohata К.. et al. // Life Sc. – 1997. – 61. – P.. PL115]. Пізніше дослідники фірми "Елі Лілі" описали арил-ароїлзаміщені бензофурани як селективні антагоністи рецепторів СВ1 (наприклад, LY320135) [Felder С.С. et al. // Pharmacol. Exp. Ther. – 1998. – 284. – P. 291].. Нещодавно з'явилися повідомлення, що 3-алкіл-5,5'діфенілімідазолідиндіони - це ліганди рецепторів канабіноїдів з ознаками антагонізму до канабіноїдів [Капуопуо Μ. et al. // Bioorg. Med. Chem. Lett. – 1999. – 9. – P.. 2233]. Фірма "Авентіс-Фарма" заявила аналоги діарилметиленазетидіну як антагоністи рецепторів СВ1 [FR, 2783246]. Трициклічні піразоли заявлені фірмою "Санофі-Синтелабо" як антагоністі СВ1 [WO, 0132663]. Цікаво, що багато з антагоністів рецепторів СВ1 поводяться як зворотні агоністи in vitro [Landsman R..S. et al. // Eur. J. Pharmacol. – 1997. – 334. – P. R1]. В останніх публікаціях містяться непогані огляди сучасного стану досліджень у галузі канабіноїдів [Mechoulam R. et al. // Prog. Med. Chem. – 1998. – 35. – P. 199; Lambert D.Μ. // Curr. Med. Chem. – 1999. – 6. –P. 635; Mechoulam R. et al. // Eur. J. Pharmacol. – 1998. - 359, - P.1; Williamson Ε..Μ.., Evans F.J. // Drugs. – 2000. – 60. – P. 1303; Pertwee R.G. // Addiction Biology. – 2000. – 5. – P. 37; Robson Ρ. // Br. J. Psychiatry. – 2001. – 178. – P. 107; Pertwee R.G. // Prog. Neurobiol. – 2001. – 63. – P. 569; Goya P., Jagerovic N. // Exp. Opin. Ther. Patents. – 2000. – 10. – P. 1529; Pertwee R.G. // Gut. – 2001. – 48. – P. 859].. Нами несподівано виявлено, що сильнодіючий та селективний антагонізм до рецепторів канабіноїдів СВ1 виявляють нові похідні 4,5-дігідро-1Нпіразолу формули (Iа) або (Іb), їхні пролікарські форми, таутомери та солі де: - R та R1 незалежно являють собою феніл, тієніл або іридій, групи яких можуть бути заміщені 1, 2 або З однаковими або різними замінниками Υ з групи С1-3-алкіл або алкоксі, гідроксі, галоген, трифторметил, трифторметилтіо, трифторметоксі, нітро, аміно, моно- або діалкіл(С1-2)-аміно, моноабо діалкіл(С1-2)-амідо, (С1-3)-алкілсульфонил, ді 77441 10 метил-сульфамідо, С1-3-алкілоксікарбоніл, карбоксил, трифторметилсульфоніл, ціано, карбамоїл, сульфамоїл та ацетил, або R та/або R1 представляють нафтил; - R2 являє собою водень, гідроксі, С1-3 алкоксі, ацетилоксі або пропіонилоксі, - R3 являє собою атом водню або розгалужену чи нерозгалужену С1-8 алкільну групу або С1-7 циклоалкільну групу, причому алкільна або циклоалкільна група може бути заміщена гідроксігрупою; - R4 являє собою атом водню або розгалужений чи нерозгалужений С1-8 алкіл, С3-8 циклоалкіл, С2-10 гетероалкіл, С3-8 неароматичний гетероциклоалкіл або С4-10 неароматичну гетероциклоалкілалкільну частину, причому такі частини можуть містити один або кілька гетероатомів з групи (О, N, S) і бути заміщені кетогрупою, трифторметильною групою, С1-3 алкільною групою, гідроксі, аміно, моноалкіламіно- або діалкіламіногрупою або атомом фтору, або ж R4 являє собою аміно, гідроксі, феноксі чи бензилоксігрупу, або ж R4 являє собою розгалужену чи нерозгалужену С1-8 алкоксі, С3-8 алкеніл, С5-8 циклоалкеніл або С6-9 циклоалкеналкіл групу, які можуть містити атом сірки, азоту або кисню, кетогрупу або -SO2- групу, і зазначені С1-8 алкоксі, С3-8 алкеніл, С5-8 циклоалкеніл або С6-9 циклоалкенілалкіл групи можуть бути заміщені гідроксігрупою, трифторметильною групою, аміногрупою, моноалкіламін-групою або діалкіламіногрупою або атомом фтору, або ж R4 являє собою феніл, бензил, піридил, тієніл, піридилметил або фенетилгрупу, у яких ароматичні кільця можуть бути заміщені 1, 2 або 3 замінниками Y, де Υ має значення, наведені вище, або - R4 являє собою групу NR8R9 за умови, що R3 є атомом водню або метилгрупою, тоді як R8 та R9 є однакові або різні й являють собою С1-4 алкіл або С2-4 трифторалкіл, або ж R8 та R9 разом з атомом водню, до якого вони прив'язані, утворюють насичену або ненасичену гетероциклічну частину, яка має від 4 до 8 атомів у кільці, і ця гетероциклічна частина може містити атом кисню або сірки, кетогрупу або -SO2- групу, або додатковий атом азоту, причому насичена або ненасичена гетероциклічна частина може бути заміщена С1-4 алкілгрупою або R3 та R4 разом з атомом азоту, до якого вони прив'язані, утворюють насичену або ненасичену, моноциклічну або біциклічну гетероциклічну частину з 4-10 атомами у кільці, причому зазначена гетероциклічна частина може містити один або більше гетероатомів з групи (О, N, S), або кетогрупу, або – SO2- групу й може бути заміщена С1-4 алкіл, гідроксі-алкіл, феніл, тієніл, піридил, аміно, моноалкіламіноалкіл, діалкіламіноалкіл, моноалкіламіно, діалкіламіно, аміноалкіл, азетидініл, піролідиніл, піперідиніл або гексагідро-1Н-азепінил групою; - R5 та R6 незалежно один від одного являють собою атом водню, або розгалужену чи нерозгалужену С1-8 алкільну чи алкенільну групу, причому такі групи можуть містити один або кілька гетероатомів з групи (О, N, S), кетогрупу, або -SO2- групу й можуть бути заміщені гідроксі або аміногрупою, або ж R5 та R6 незалежно один від одного являють собою С3-8 циклоалкільну групу або С3-8 циклоалкенільну групу, які можуть містити один або кілька 11 гетероатомів з групи (О, N, S), або –SO2- групу, й ці групи можуть бути заміщені гідроксігрупою, алкіл (С1-3), -SO2- групою, кетогрупою, аміногрупою, моно-алкіламіногрупою (С1-3), або діалкіламіногрупою (С1-3), або R5 являє собою нафтильну або фенільну групу, причому фенільна група може бути заміщена 1, 2 або 3 замінниками Y, де Υ має значення, наведені вище, за умови, що R6 являє собою атом водню, або розгалужену чи нерозгалужену алкільну групу (C1-5), причому алкільна група може містити один або кілька гетероатомів з групи (О, N, S), або –SO2- групу й алкільна група може бути заміщена гідроксі, кето або аміногрупою, або R5 та R6 разом з атомом азоту, до якого вони прив'язані, утворюють моноциклічну, біциклічну або трициклічну алкільну чи алкенільну групу, яка може містити кільцеві гетероатоми з групи (О, N, S), кетогрупу, або SO2 групу, і ця моноциклічна, біциклічна або трициклічна алкільна чи алкенільна група може бути заміщена гідроксігрупою, алкіл (С1-3), S02 групою, кетогрупою, аміногрупою, моноалкіламіногрупою (С1-3), діалкіламіногрупою (С1-3), піролідинілгрупою або піперидинілгрупою, причому моноциклічна, біциклічна або трициклічна алкільна чи алкенільна група може містити анельовану фенільну групу, яка, у свою чергу, може бути заміщена 1 або 2 замінниками Y, де Υ має значення, наведені вище; - R7 являє собою розгалужений або нерозгалужений С1-3 алкіл. У сполуках формули (Ia) та (ІЬ) присутній принаймні один центр хіральності (у позиції С4 4,5дігідро-1Н-піразольної частини). Винахід охоплює усі рацемати, суміші діастереомерів та окремі стереоізомери сполук, що мають формули (Ia) або (Іb) Особливо цікаві серед сполук формули (Ia) або (Іb) ті, що мають абсолютну стереоконфігурацію у позиції С4 4,5-дігідро-1Н-піразольної частини, як видно з формул (Ia*) та (Ib*). Сполукам за винаходом можна надати форму, придатну для введення до організму, відомими способами за допомогою допоміжних речовин та/або рідких чи твердих носіїв. Завдяки потужній антагоністичній активності до СВ1 сполуки за винаходом можуть використовуватися для лікування психічних розладів, як от психози, збентеженість, депресія, дефіцит уваги, розлади пам'яті та апетиту, опасистість, алкоголізм, гіперсексуальність, наркозалежність, нервових розладів, як от недоумство, дистонія, м'язова еластичність, дрижавка, травматичне пошкодження мозку, інсульт, хвороба Паркінсона, хвороба Альцгеймера, епілепсія, хвороба Гантінгтона, синдром Турета, церебральна ішемія, церебральна апоплексія, черепно-мозкова травма, пошкодження хребта, нейрозапалювальні хвороби, бляшковий склероз, вірусний енцефаліт, хвороб, пов'язаних з деміелінізацією, а також для лікування болів, включаючи невропатичні больові прояви, та інших хвороб, що пов'язані з нейротрансмісією канабіноїдів, як от септичний шок, глаукома, рак, діабет, блювання, нудота, астма, респіраторні захворювання, шлунково-кишкові розлади, виразка шлунку, діарея та серцево-судинні розлади. 77441 12 Спорідненість сполук за винаходом до рецепторів канабіноїдів СВ1 визначалася за допомогою препаратів клітинних мембран яєчників китайського хом'яка (ЯКХ), до яких стабільно трансфектувався людський рецептор канабісу СВ1 у сполученні з [3Н]СР-55940 в якості радіоліганду Після інкубації свіжо приготованих препаратів клітинних мембран з [3Н]-лігандом, з доданням сполук за винаходом або без, зв'язані та вільні ліганди відокремлювали на фільтрах зі скловолокна. Радіоактивність на фільтрі вимірювали рідинним сцинтиляційним лічильником. Антагоністична активність сполук за винаходом щодо СВ1 канабіноїдів визначалася функціональними дослідженнями за допомогою клітин ЯКХ, у яких були постійно виражені людські рецептори СВ1 канабіноїдів. Аденилілциклазу стимулювали форсколіном та вимірювали квантифікацією циклічного АМФ, що накопичився. Супутня активація рецепторів СВ1 агоністами рецепторів СВ1 (наприклад, СР-55940 або (R)-WIN-55212-2) може придушувати ініційоване форсколіном накопичення цАМФ у залежності від концентрації. Ця викликана рецепторами СВ1 реакція може придушуватися антагоністами рецепторів СВ1, наприклад, сполуками за винаходом. Проміжні сполуки формули (II) можна одержувати відомими способами, наприклад [Francotte Ε., Tong Z. // Chem.. Abstr.. – 126. – 213598; Rempfler Η.., Kunz W. // Chem. Abstr.. – 113. – 40432; Rempfler Η.., Kunz W. // Chem. Abstr. – 107. – 217473]. Проміжні сполуки формули (III), де R2 - водень, можна одержувати способами відомими, наприклад, з [ЕР, 0021506; DE, 2529689; Grosscurt A..C. et al. // J. Agric. Food. Chem. – 1979. – 27(2). – P. 406]. Проміжні сполуки формули (ІІІ), де R2 - гідроксігрупа, можна одержувати реакцією сполуки формули (II) з гідразином або гідразингідратом. Цю реакцію переважно здійснюють в органічному розчиннику, як от етанол, одержуючи сполуку формули (ІІІ), де R2 – гідроксігрупа. Синтезувати сполуки за винаходом можна декількома варіантами. Варіант синтезу А Етап 1. Реакція сполуки формули (III) зі сполукою формули (IV) 13 Реакцію переважно ведуть в органічному розчиннику, наприклад, діхлорметані, з одержанням сполуки формули (V), у якому R, R1, R2, R5 та R6 мають значення, наведені вище. Ця сполука є новою. 77441 14 з аміном формули HNR3R4, де R-з та R4 мають вищенаведені значення, у присутності солі ртуті (II), дає сполуку формули (Іa). Реакцію переважно ведуть в органічному розчиннику, як от ацетонітрил, подібно до способу, що описаний у [Synth. Commun. – 1996. - 26(23). – P.4299. Варіант синтезу А2 Етап 1. Реакція сполуки формули (III) з похідним ізоціанату формули (VI), з наступною обробкою аміном формули HNR5R6. Етап 2. Реакція сполуки формули (V) зі сполукою R7-X, де X - вихідна група, наприклад, йодид, a R4 має значення, наведене вище для сполуки (Іb), дає сполуку формули (Іb). Реакцію переважно ведуть у присутності основи, наприклад, триетиламіну. Етап 3. Реакція сполуки формули (Іb) з аміном формули HNR3R4, де R3 та R4 мають вищенаведені значення, подібно до способу, що описаний у [Synth.. Commun. – 1996. - 26(23). – P. 4299]. Ця реакція дає сполуку формули (Іа). Варіант синтезу А1 Етап 1. Реакція сполуки формули (V) Реакцію переважно ведуть в органічному розчиннику, як от діхлорметан, з одержанням сполуки формули (VII). « Сполуки формули (VII), де R, R1, R2, R5 та R6 мають вищенаведені значення для формули (Іа), є новими. Етап 2. Реакція сполуки формули (VII) з галогенуючим агентом, як, наприклад, РСl5, дає сполуку формули (VIII) де: R10 - атом галогену, наприклад, хлору. Реакцію переважно ведуть в інертному органічному розчиннику, як от хлорбензол. Сполуки формули (VIII), де R, R1, R2, R5 та R6 мають вищенаведені значення для формули (Іа), a R10 - атом галогену, є новими. 15 Етап 3. Реакція, переважно в інертному органічному розчиннику, як от діхлорметан, сполуки формули (VIII) з аміном формули HNR3R4, де R3 та R4 мають вищенаведені значення, дає сполуку формули (Іа). Варіант синтезу A3 Етап 1. Реакція сполуки формули (ІІІ) зі сполукою формули (IX) дає сполуку формули (Ib) [Chem. Ber. – 1966. – 99. – P. 2885; Chem. Ztg. – 1984. - 108(12). – P. 404]. Приготування сполук ілюструється наступними прикладами Приклад 1. Приготування 3-(4-хлорфеніл)-N’(((етил)пропиламін)сульфоніл)-N-метил-4-феніл4,5-дігідро-1Н-піразол-1-карбоксамідину Частина А. До розчину 5,98г (25,4ммоля) ((етил)пропиламін)сульфонілізоціанату в сухому діхлорметані в атмосфері азоту додають з перемішуванням 6,52г (25,4ммоля) 3-(4-хлорфеніл)-4феніл-4,5-дігідро-1Н-піразолу. Після 90хв. перемішування одержаний розчин концентрують у вакуумі та очищують колонковою хроматографією (СН2Сl2, силікагель, Rf ~0,45). Отриману тверду фазу перекристалізують з діетилетеру й одержують 6,57г (вихід 56%) 3-(4-хлорфеніл)-N(((етил)пропиламін)сульфоніл)-4-феніл-4,5-дігідро1Н-піразол-1-тіокарбоксамиду. Точка топлення 144-146°С. Частина В.. До суспензії 2,32г (5ммоля) 3-(4хлорфеніл)-N-(((етил)пропиламін) сульфоніл)-4феніл-4,5-дігїдро-1Н-піразол-1-тіокарбоксамиду в 20мл ацетонітрилу додають з перемішуванням 4мл холодного метиламіну. До одержаного розчину додають розчин 1,5г HgCl2 у 10мл ацетонітрилу. Одержану чорну суспензію перемішують 4год. Осад видаляють фільтрацією.. Фільтрат концентрують у вакуумі, розчиняють у діхлорметані й послідовно промивають водним розчином 0,5N NaOH та водою, сушать над Na2SO4, відфільтровують та концентрують у вакуумі. Одержану олію кристалізують з діетилетеру і мають 1,78г 3-(4-хлорфеніл)N’-(((етил) пропиламін)сульфоніл)-N-метил-4феніл-4,5-дігідро-1Н-піразол-1-карбоксамідину (вихід 77%) Точка топлення 129-131°С. Аналогічним чином одержують інші сполуки формули (Іа): 2. 3-(4-хлорфеніл)-N’(((етил)метиламін))сульфоніл)-N-метил-4-феніл4,5-дігідро-1Н-піразол-1-карбоксамідин. Точка топлення 112-115°С. 3. 3-(4-хлорфеніл)-N'-((діетиламін)сульфоніл)N-(2-гідроксіетил)-4-феніл-4,5-дігідро-1Н-піразол1-карбоксамідин. Точка топлення 104-106°С. 4. 3-(4-хлорфеніл)-N-(2-гідроксіетил)-N'(((етил)метиламін))сульфоніл)-4-феніл-4,5-дігідро1Н-піразол-1-карбоксамідин. Мас-спектрометрія (ESI+): 490МН+. 77441 16 5. 3-(4-хлорфеніл)-N'-((діетиламін)сульфоніл)N-(2-морфолін-4-іл)етил)-4-феніл-4,5-дігідро-1Нпіразол-1-карбоксамідин. Мас-спектрометрія (ESI+): 547МН+. 6. 3-(4-хлорфеніл)-N'-((діметиламін)сульфоніл)-N-(2-морфолін-4-іл)етил)-4-феніл-4,5-дігідро1Н-піразол-1-карбоксамідин. Аморфний. 7. 3-(4-хлорфеніл)-N’-((діетиламін)сульфоніл)N-(2-діметиламін)етил)-4-феніл-4,5-дігідро-1Нпіразол-1-карбоксамідин. Мас-спектрометрія (ESI+): 505МН+. 8. 3-(4-хлорфеніл)-N-(3-(діметиламін)пропил)N'-((діметиламін))сульфоніл)-4-феніл-4,5-дігідро1Н-піразол-1-карбоксамідин. Аморфний. 9. 3-(4-хлорфеніл)-N-(2-піперидін-1-іл)етил)-N'((піперидін-1-іл)сульфоніл)-4-феніл-4,5-дігідро-1Нпіразол-1-карбоксамідин. Мас-спектрометрія (ESI+): 557МН+. 10. 3-(4-хлорфеніл)-N-(2-морфолін-4-іл)етил)N’-((піперидін-1-іл)сульфоніл)-4-феніл-4,5-дігідро1Н-піразол-1-карбоксамідин. Мас-спектрометрія (ESI+): 559МН+. Точка топлення 174-176°С. 11. 3-(4-хлорфеніл)-N-(2-(діметиламін)етил)N'-((діметиламін)сульфоніл)-4-феніл-4,5-дігідро1Н-піразол-1-карбоксамідин. Аморфний. 12. 3-(4-хлорфеніл)-N-(2-(діетиламін)етил)-N’((діметиламін)сульфоніл)-4-феніл-4,5-дігідро-1Нпіразол-1-карбоксамідин. Аморфний. 13. 3-(4-хлорфеніл)-N-(3-(діметиламін)пропил)N’-((діметиламін)сульфоніл)-4-феніл-4,5-дігідро1Н-піразол-1-карбоксамідин. Мас-спектрометрія + (ESI+): 519МН . 14. 3-(4-хлорфеніл)-N-(2-(діетиламін)етил)-N'((діетиламін)сульфоніл)-4-феніл-4,5-дігідро-1Нпіразол-1-карбоксамідин геміфумарат. Точка топлення 182-185°С. 15. 3-(4-хлорфеніл)-N-(2-(діметиламін)етил)N’-((піперидін-1-іл)сульфоніл)-4-феніл-4,5-дігідро1Н-піразол-1-карбоксамідин. Аморфний. 16. 3-(4-хлорфеніл)-N-(2-(діетиламін)етил)-N’((пірролідин-1-іл)сульфоніл)-4-феніл-4,5-дігідро1Н-піразол-1-карбоксамідин. Аморфний. 17. 3-(4-хлорфеніл)-N’-((діетиламін)сульфоніл)-N-(1-метилпіперидін-4-іл)-4-феніл-4,5-дігідро1Н-піразол-1-карбоксамідин. Аморфний. 18. 3-(4-хлорфеніл)-N’-((діметиламін)сульфоніл)-N-(2-гідроксіетил)-4-феніл-4,5-дігідро-1Нпіразол-1-карбоксамідин. Точка топлення 123126°С. 19. 3-(4-хлорфеніл)-N'-((діетиламін)сульфоніл)-N-1-Meтил-4-феніл-4,5-дігідро-1H-піразол-1карбоксамідин. Аморфний. Rf~0,4 (діетилетер). 20. 3-(4-хлорфеніл)-N’-(((етил)пропиламін)сульфоніл)-N-метил-4-феніл-4,5-дігідро-1H-піразол1-карбоксамідин. Точка топлення 129-131°С. 21. 3-(4-хлорфеніл)-N-метил-N'-((пірролідин-1іл)сульфоніл)-4-феніл-4,5-дігідро-1Н-піразол-1карбоксамідин. Аморфний. Rf~0,3 (МТБЕ). 22. 3-(4-хлорфеніл)-N-метил-N'-(((метил)пропиламін)сульфоніл)-4-феніл-4,5-дігідро-1Н-піразол-1-карбоксамідин. Точка топлення 132-134°С. 23. 3-(4-хлорфеніл)-N,N-діметил-N'-((пірролідин-1-іл)сульфоніл)-4-феніл-4,5-дігідро-1Нпіразол-1-карбоксамідин. Аморфний. Rf~0,25 (МТБЕ). 17 24. 3-(4-хлорфеніл)-N-метил-N'-((піреридин-1іл)сульфоніл)-4-феніл-4,5-дігідро-1Н-піразол-1карбоксамідин. Точка топлення 175-177°С. 25. 3-(4-хлорфеніл)-N'-((гексагідро-1Н-азепин1-іл)сульфоніл)-N-метил-4-феніл-4,5-дігідро-1Нпіразол-1-карбоксамідин. Аморфний. 26. 3-(4-хлорфеніл)-N'-((діпропиламін)сульфоніл)-N-метил-4-феніл-4,5-дігідро-1Н-піразол-1карбоксамідин. Точка топлення 141-142°С. 27. 3-(4-хлорфеніл)-N’-(((ізопропил)метиламін) сульфоніл)-N-метил-4-феніл-4,5-дігідро-1Hпіразол-1-карбоксамідин. Точка топлення 134136°С. 28. 3-(4-хлорфеніл)-N-метил-N’-((октагідроазоцин-1-іл)сульфоніл)-4-феніл-4,5-дігідро-1Нпіразол-1-карбоксамідин. Точка топлення 165168°С. 29. 3-(4-хлорфеніл)-N-етил-N'-((піперидин-1іл)сульфоніл)-4-феніл-4,5-дігідро-1Н-піразол-1карбоксамідин. Аморфний. 30. 3-(4-хлорфеніл)-N’-((діметиламін)сульфоніл)-N-метил-4-феніл-4,5-дігідро-1Н-піразол-1карбоксамідин. Точка топлення 166-168°С. Приклад 31. Приготування 3-(4-хлорфеніл)-N’((діметиламін)сульфоніл)-N-пропил-4-феніл-4,5дігідро-1H-піразол-1-карбоксамідин Частина А. До розчину 1,73мл (20ммоля) хлорсульфоніл ізоціанату в 20мл сухого діхлорметану дуже повільно додають з перемішуванням розчин 5,13г (20ммоля) 3-(4-хлорфеніл)4-феніл-4,5дігідро-1Н-піразолу в 125мл сухого діхлорметану при -5°С. Після 30хв. перемішування реакційній суміші дають досягти кімнатної температури й перемішують ще 2год. Після охолодження до 0°С додають 5мл рідкого діметиламіну, одержаний розчин перемішують 1годину при 0°С і 2год. при кімнатній температурі. Розчин промивають водою, фільтрують на фільтрі Гіфло і концентрують у вакуумі. Випарювальна хроматографія (МТБЕ, Rf ~0,3) дає 4,75г (вихід 58%) 3-(4-хлорфеніл)-N((діметиламін)сульфоніл)-4-феніл-4,5-дігідро-1Hпіразол-1-карбоксаміду. Точка топлення 210-212°С Частина В. Суміш 1,47г (3,62ммоля) 3-(4хлорфеніл)-N-((діметиламін)сульфоніл)-4-феніл4,5-дігідро-1H-піразол-1-карбоксаміду з 0,80г (3,84ммоля) пентахлориду фосфору в 20мл хлорбензолу нагрівають зі зворотним холодильником 1год. Після ретельного концентрування у вакуумі одержаний 3-(4-хлорфеніл)-N-((діметиламін) сульфоніл)-4-феніл-4,5-дігідро-1Н-піразол-1карбоксамідоілхлорид суспендують у сухому діхлорметані та обробляють 1,0мл холодного nпропиламіну при 0°С Після 1год. перемішування суміш розчиняють в етилацетаті, промивають водою та концентрують у вакуумі Осад очищують колонковою хроматографією (співвідношення діхлорметан:ацетон як 19:1 (об.:об.), Rf ~0,35), одержуючи 0,82г олії. Після кристалізації з діетилетеру з наступною перекристалізацією з етанолу одержують 0,38г 3-(4-хлорфеніл)-N’-((діметиламін)сульфоніл)-N-пропил-4-феніл-4,5-дігідро-1H-піразол-1карбоксамідину (вихід 23%), точка топлення 127129°С. Аналогічним чином одержують інші сполуки формули (Іа): 77441 18 32. 3-(4-хлорфеніл)-N'-((діметиламін)сульфоніл)-N-(2-фторетил)-4-феніл-4,5-діпдро-1Нпіразол-1-карбоксамідин. Точка топлення 128131°С. 33. 3-(4-хлорфеніл)-N'-((діметиламін)сульфоніл)-4-феніл-N-(2,2,2-трифтор-етил)-4,5-дігідро-1Нпіразол-1-карбоксамідин. Точка топлення 158159°С. 34. 3-(4-хлорфеніл)-N'-((діметиламін)сульфоніл)-N-метоксі-4-феніл-4,5-дігідро-1Н-піразол-1карбоксамідин. Точка топлення 170-172°С. Приклад 35. Приготування метилефіру 3-(4хлорфеніл)-N-((піперидин-1-іл)сульфоніл)-4-феніл4,5-дігідро-1Н-піразол-1-карбоксімідотіокислоти Частина А. До розчину 54,77г (266ммоля) (піперидин-1-іл)сульфонілізотіоціанату в 900мл сухого діхлорметану в атмосфері азоту додають 68,3г (266ммоля) 3-(4-хлорфеніл)-4-феніл-4,5-дігідро1Н-піразолу. Після 16год. перемішування додають ще діхлорметану. Одержаний розчин двічі промивають водою, сушать над Na2SO4 та концентрують у вакуумі. Після додання МТБЕ осад кристалізується. Кристалічний матеріал збирають і промивають МТБЕ, одержуючи 77,6г 3-(4-хлорфеніл)-4феніл-N-((піперидин-1-іл)сульфоніл)-4,5-дігідро1H-піразол-1-тіокарбоксаміду (вихід 63%). Частина В.. До розчину 30г (64,9ммоля) 3-(4хлорфеніл)-4-феніл-N-((піперидин-1-іл)сульфоніл)4,5-дігідро-1H-піразол-1-тіокарбоксаміду в 1л ацетону додають 18,0 мл (130ммоля) триетиламіну. До одержаного жовтого розчину додають 9,12г (64ммоля) метил-йодиду, одержаний розчин перемішують 16год. при кімнатній температурі. Осад відфільтровують, фільтрат промивають водою, концентрують у вакуумі й одержують жовту тверду фазу. Перекристалізація з МТБЕ дає 27,9г метилефіру 3-(4-хлорфеніл)-N-((піперидин-1-іл)сульфоніл)-4-феніл-4,5-дігідро-1Н-піразол-1-карбоксімідотіокислоти (вихід 90%), точка топлення 192-194°С. Аналогічним чином одержують інші сполуки формули (Іb): 36. Метилефір 3-(4-хлорфеніл)-N-((діметиламін)сульфоніл)-4-феніл-4,5-дігідро-1H-піразол-1карбоксімідотіокислоти. Точка топлення 159160°С. 37. Метилефір 3-(4-хлорфеніл)-N-((діетиламін)сульфоніл)-4-феніл-4,5-дігідро-1H-піразол-1карбоксімідотіокислоти. Точка топлення 141143°С. 38. Метилефір 3-(4-хлорфеніл)-4-феніл-N((1,2,3,4-тетрагідроізохінолин-2-іл)сульфоніл)-4,5дігідро-1Н-піразол-1-карбоксімідотіокислоти. Точка топлення 143-145°С. 39. Метилефір 3-(4-хлорфеніл)-N-(((етил) феніламін)сульфоніл)-4-феніл-4,5-дігідро-1Н-піразол1-карбоксімідотіокислоти. Точка топлення 143146°С. 40. Метилефір 3-(4-хлорфеніл)-N-((діетиламін) сульфоніл)-4-гідроксі-4-феніл-4,5-дігідро-1Нпіразол-1-карбоксімідотіокислоти. Аморфний. 41. Метилефір 3-(4-хлорфеніл)-N-((діетиламін) сульфоніл)-4-(піридин-4-іл)-4,5-дігідро-1Н-піразол1-карбоксімідотіокислоти. Аморфний. 42. Метилефір 3-(4-хлорфеніл)-N-((піперидин1-іл)сульфоніл)-4-(3-трифторметил)феніл)-4,5 19 дігідро-1Н-піразол-1-карбоксімідотіокислоти. Аморфний. 43. Метилефір 3-(4-хлорфеніл)-N-((діметиламін)сульфоніл)-4-(3-трифторметил)феніл)-4,5дігідро-1Н-піразол-1-карбоксімідотіокислоти. Аморфний. 44. Метилефір 3-(4-хлорфеніл)-N-(((етил) метиламін)сульфоніл)-4-(піридин-3-іл)-4,5-дігідро-1Нпіразол-1-карбоксімідотіокислоти. Точка топлення 133-136°С. 45. Метилефір 3-(4-хлорфеніл)-N-((піперидин1-іл)сульфоніл)-4-(піридин-3-іл)-4,5-дігідро-1Нпіразол-1-карбоксімідотіокислоти. Точка топлення 182-185°С. 46. Метилефір 3-(4-хлорфеніл)-N-((морфолин4-іл)сульфоніл)-4-феніл-4,5-дігідро-1Н-піразол-1карбоксімідотіокислоти. 202-204 47. Метилефір 3-(4-хлорфеніл)-4-(2-фторфеніл)-N-((морфолин-4-іл)сульфоніл)-4,5-дігідро-1Нпіразол-1-карбоксімідотіокислоти. Точка топлення 205-207°С. 48. Метилефір 3-(4-хлорфеніл)-4-(2-фторфеніл)-N-((піперидин-1-іл)сульфоніл)-4,5-дігідро-1Нпіразол-1-карбоксімідотіокислоти. Точка топлення 196-198°С. 49. Метилефір 3-(4-хлорфеніл)-4-(2-фторфеніл)-N-((діметиламін)сульфоніл)-4,5-дігідро-1Нпіразол-1-карбоксімідотіокислоти. Точка топлення 181-183°С. 50. Метилефір 3-(4-хлорфеніл)-4-(2,6-діфторфеніл)-N-((морфолин-4-іл)сульфоніл)- 4,5-дігідро1Н-піразол-1-карбоксімідотіокислоти. Точка топлення 231-233°С. 51. Метилефір 3-(4-хлорфеніл)-4-(2,6-діфторфеніл)-N-(піперидин-1-іл)сульфоніл)- 4,5-дігідро1Н-піразол-1-карбоксімідотіокислоти. Точка топлення 221-225°С. 52. Метилефір 3-(4-хлорфеніл)-4-(2,6діфторфеніл)-N-((діметиламін)сульфоніл)4,5дігідро-1H-піразол-1-карбоксімідотіокислоти. Точка топлення 181-185°С. 53. Метилефір 3-(4-хлорфеніл)-N-((1,1-діоксидотіоморфолин-4-іл)сульфоніл)-4-феніл-4,5дігідро-1Н-піразол-1-карбоксімідотіокислоти. Точка топлення 216-217°С. 54. Метилефір 3-(5-хлортієн-2-іл)-N-((діетиламін)сульфоніл)-4-феніл-4,5-дігідро-1H-піразол-1карбоксімідотіокислоти. Аморфний. Приклад 55. Приготування 3-(4-хлорфеніл)-Nметил- 4-феніл-N'-((піперидин-1-іл)сульфоніл) -4,5дігідро-1H-піразол-1-карбоксамідин До охолодженої суміші (
ДивитисяДодаткова інформація
Назва патенту англійською4,5-dihydro-1h-pyrazole derivatives as potent cb1 receptor antagonists, methods for their preparation (variants), intermediate, pharmaceutical composition and method for its preparation
Автори англійськоюKruse Cornelis G., Kruse, Cornelis G., Lange, Josephus, H., M.
Назва патенту російськоюПроизводные 4,5-дигидро-1н-пиразола с выраженной антагонистической активностью в отношении рецепторов св-1, способ их получения (варианты), промежуточные соединения, фармацевтическая композиция и способ ее получен
Автори російськоюКрузе Корнелис Г., Ланге Йозефус Х.М.
МПК / Мітки
МПК: A61K 31/4725, C07D 403/12, A61K 31/415, A61P 3/10, A61P 1/12, A61P 25/08, A61K 31/4545, A61P 29/00, A61K 31/4155, A61P 25/22, A61K 31/4439, A61P 1/08, A61P 1/04, A61P 25/16, A61K 31/541, A61P 27/06, C07D 403/06, A61P 25/24, A61K 31/194, A61P 25/14, C07D 409/04, A61P 25/02, A61P 3/04, A61P 11/06, A61P 9/10, A61K 31/55, A61P 25/00, A61K 31/5377, A61K 31/551, C07D 401/04, A61P 1/14, A61P 25/28, A61K 31/496, A61P 43/00, A61P 31/04, A61K 31/454, C07D 401/12, A61P 25/18, C07D 231/06, A61P 25/30, A61P 35/00, A61P 31/12, A61P 9/00
Мітки: 4,5-дигідро-1н-піразолу, фармацевтична, похідні, активністю, антагоністичною, св-1, спосіб, композиція, рецепторів, сполуки, варіанти, сильнодіючою, одержання, проміжні
Код посилання
<a href="https://ua.patents.su/12-77441-pokhidni-45-digidro-1n-pirazolu-z-silnodiyuchoyu-antagonistichnoyu-aktivnistyu-shhodo-receptoriv-sv-1-sposib-kh-oderzhannya-varianti-promizhni-spoluki-farmacevtichna-kompoziciya-ta.html" target="_blank" rel="follow" title="База патентів України">Похідні 4,5-дигідро-1н-піразолу з сильнодіючою антагоністичною активністю щодо рецепторів св-1, спосіб їх одержання (варіанти), проміжні сполуки, фармацевтична композиція та спосіб її одержання</a>