Похідні тіазоло[4,5-d]піримідину, спосіб їх одержання (варіанти), проміжні сполуки, фармацевтична композиція на їх основі та спосіб виготовлення такої композиції
Номер патенту: 73521
Опубліковано: 15.08.2005
Автори: Вілліс Пол Ендрю, Волтерс Айен Алістер Ст'юарт, Боннерт Роджер Віктор, Гант Саймон Фрейзер
Формула / Реферат
1. Похідні тіазоло[4,5-d]піримидину формули (І) чи його фармацевтично прийнятна сіль чи сольват:
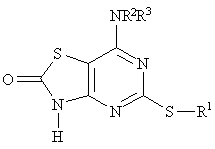 , (I)
, (I)
де
R1 являє собою С3-С7 карбоциклічну групу, С1-С8алкіл, С2-С6алкеніл чи С2-С6алкініл, кожна з цих груп, як варіант, заміщена одним чи більше замісниками, що незалежно вибрані з атомів галогену, -OR4, -NR5R6, -CONR5R6, -COOR7, -NR8COR9, -SR10, -SO2R10, -SO2NR5R6, -NR8S02R9, фенілу, нафтилу чи 5- чи 6-членного ароматичного кільця, що містить один чи більше гетероатомів, які вибрано з N, S та О, феніл, нафтил та ароматичні кільця, як варіант, заміщені одним чи більше замісниками, що незалежно вибрані з атомів галогену, ціаногрупи, нітрогрупи, -OR4, -NR5R6, -CONR5R6, -COOR7, -NR8COR9, -SR10, -SO2R10, -SO2NR5R6, -NR8SO2R9, С1-С6алкілу чи трифлуорметилу;
R2 та R3, кожний незалежно, являють собою атом гідрогену чи С3-С7 карбоциклічну групу, С1-С8алкіл, С2-С6алкеніл чи С2-С6алкініл, останні чотири групи можуть бути, як варіант, заміщені одним чи більше замісниками, що незалежно вибрані з:
(a) атомів галогену, -OR4, -NR5R6 -CONR5R6, -COOR7, -NR8COR9, -SR10, -SO2R10, -SO2NR5R6, -NR8S02R9;
(b) 3-8-членного кільця, що містить, як варіант, один чи більше атомів, що вибрані з О, S, NR8, та, як варіант, заміщено С1-С3алкілом чи галогеном; або
(c) арилу чи гетероарилу, кожний з яких може бути, як варіант, заміщено одним чи більше замісниками, що незалежно вибрані з атомів галогену, ціаногрупи, нітрогрупи, -OR4, -NR5R6, -CONR5R6, -NR8COR9, -SO2NR5R6, -NR8SO2R9, С1-С6алкілу та трифлуорметилу;
R4 являє собою гідроген, С1-С6алкіл чи феніл, останні два з яких можуть бути, як варіант, заміщені одним чи більше замісниками, що незалежно вибрані з атомів галогену, фенілу, -OR11 та -NR12R13;
R5 та R6 незалежно являють собою атом гідрогену, С1-С6алкіл чи феніл, останні два з яких можуть бути, як варіант, заміщені одним чи більше замісниками, що незалежно вибрані з атомів галогену, фенілу, -OR14 та -NR15R16, -CONR15R16, -NR15COR16, -SONR15R16, NR15SO2R16, чи
R5 та R6 разом з атомом нітрогену, до якого вони приєднані, утворюють 4-7-членну насичену гетероциклічну систему, що містить, як варіант, ще гетероатом, що вибрані з атомів оксигену та нітрогену, ця кільцева система може бути, як варіант, заміщена одним чи більше замісниками, які незалежно вибрано з фенілу, -OR14, -COOR14, -NR15R16, -CONR15R16, -NR15COR16, -SONR15R16, NR15SO2R16, чи С1-С6алкілом, що сам, як варіант, заміщений одним чи більше замісниками, які незалежно вибрано з атомів галогену та груп -NR15R16 та -OR17;
R10 являє собою атом гідрогену, С1-С6алкіл чи феніл, останні два з яких можуть бути, як варіант, заміщені одним чи більше замісниками, що незалежно вибрані з атомів галогену, фенілу, -OR17 та -NR15R16; a
кожний з R7, R8, R9, R11, R12, R13, R14 R15, R16 та R17 незалежно являє собою атом гідрогену чи С1-С6алкіл, чи феніл.
2. Сполука за п. 1, в якій R1 являє собою, як варіант, заміщений бензил.
3. Сполука за п. 1 чи п. 2, в якій один з R2 та R3 є гідрогеном, а інший - С2-С8алкіл, заміщений гідроксилом.
4. Сполука за п. 1, яку вибрано з групи:
7-[(2-гідрокси-1,1-диметилетил)аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
(R)-7-[[1-(гідроксиметил)пропіл]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
(R)-7-[(2-гідрокси-1-метилетил)аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[(2-гідрокси-1,1-диметилетил)аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-(гідроксіетоксі)етил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]тіазоло-[4,5-d]піримідин-2(3H)-он,
7-[(2-аміноетил)аміно]-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[(2-гідроксіетил)аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
N-[2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2,3-дигідро-2-оксотіазоло[4,5-d]піримідин-7-іл]аміно]етил]метансульфонамід,
(+/-)-5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-(2-гідроксіетокси)-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
7-[[(1R)-2-аміно-1-метилетил]аміно]-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-[(2-гідроксіетил)аміно]-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-(диметиламіно)-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[[4-(2-аміноетокси)-3-хлорфеніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазолo[4,5-d]піримідин-2(3H)-он,
5-[[3-хлор-4-метоксифеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[3-хлор-2-флуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(3R,4R)-4-гідроксипіролідин-3-іл]аміно]-тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[(3R)-піролідин-3-іламіно]тіазолo[4,5-d]піримідин-2(3H)-он,
7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло [4,5-d]піримідин-2(3H)-он,
7-[(2-гідрокси-1,1-диметилетил)аміно]-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
7-[(2-гідрокси-1,1-диметилетил)аміно]-5-[[(2-метилфеніл)метил)тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[(2-фуранілметил)тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
7-[[(1R)-2-аміно-1-метилетил]аміно]-5-[[(3-хлор-2-флуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
(2S)-2-[[5-[[2,3-дифлуорфеніл)метил]тіо]2,3-дигідро-2-оксотіазоло[4,5-d]піримідин-7-іл]аміно]-3-гідроксипропанамід,
7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(2-тієнілметил)тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5[[[3-метил-4-(метилсульфоніл)феніл]метил]тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[[3-хлор-4-(трифлуорметокси)феніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[[2-флуор-3-(трифлуорметил)феніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[2-[(диметиламіно)етил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2-флуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[[(2-метоксифеніл)метил]тіо]тіазолo[4,5-d]піримідин-2(3H)-он,
7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(2-феноксіетил)тіо]тіазолo[4,5-d]піримідин-2(3H)-он,
7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[[(3-метилфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2-флуор-3-метилфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(3-хлорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(3-бромфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[[4-(дифлуорметокси)феніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
(+/-)-5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-гідрокси-1-(метоксиметил)етил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2-бромфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[[3-хлор-2-флуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
(+/-)-5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-гідрокси-1-(метоксиметил)етил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он,
7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3H)-он,
5-[(5-хлор-1,2,3-тіадіазол-4-іл)тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]-тіазоло[4,5-d]піримідин-2(3H)-он, та
її фармацевтично прийнятні солі та сольвати.
5. Сполука за п. 1, яку вибрано з групи:
сіль натрію 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-гiдpoкcи-1-мeтилeтил]-аміно]тіазоло[4,5-d]піримідин-2(3Н)-ону,
сіль натрію 5-[[3-хлор-2-флуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]-аміно]тіазоло[4,5-d]піримідин-2(3Н)-ону,
сіль натрію (+/-)-5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-гідрокси-1-
(метоксиметил)етил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-ону,
сіль натрію 7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-5-[(фенілметил)тіо]-тіазоло[4,5-d]піримідин-2(3Н)-ону чи
сіль натрію 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d)піримідин-2(3Н)-ону.
6. Сполука за п. 1, яку вибрано з групи:
трифлуорацетат 7-[[(1R)-2-aміно-1-метилетил]аміно]-5-[[(2,3-дифлуорфеніл)метил]-
тіо]тіазоло[4,5-d]піримідин-2(3Н)-ону,
трифлуорацетат 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-[(2-гідроксіетил)аміно]-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-ону,
5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-(диметиламіно)-1-метилетил]аміно]-тіазоло[4,5-d]піримідин-2(3Н)-он,
трифлуорацетат 5-[[[4-(2-аміноетокси)-3-хлорфеніл]метил]тіо]-7-[[(1R)-2-гідрокси-1 -метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-ону,
моногідрохлорид 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[2-[(диметиламіно)етил]-
аміно]тіазоло[4,5-d]піримідин-2(3Н)-ону, чи
дигідрохлорид 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[(3R)-піролідин-3-іламіно]-тіазоло[4,5-d]піримідин-2(3Н)-ону.
7. Сполука формули (І) чи її фармацевтично прийнятна сіль, чи сольват за будь-яким одним з пп.1-6 для використання у терапії.
8. Сполука формули (І) чи її фармацевтично прийнятна соль, чи сольват за будь-яким одним з пп.1-6 для використання у виробництві лікувального засобу для застосування у терапії.
9. Сполука, сіль чи сольват за п. 7 для використання при лікуванні опосередкованої хемокінами хвороби, де хемокіни з'єднують один чи більше рецепторів хемокінів.
10. Сполука, сіль чи сольват за п. 9, в якій рецептор хемокінів належить до підродини СХС рецепторів хемокінів.
11. Сполука, сіль чи сольват за пп. 9 та 10, в якій рецептором хемокінів є рецептор CXСR2.
12. Сполука, сіль чи сольват за п. 7 для використання при лікуванні запальної хвороби у пацієнта, що страждає від вказаної хвороби, чи у якого існує ризик захворіти нею.
13. Сполука, сіль чи сольват за п. 7 для використання при лікуванні хвороби, у якій ангіогенез залежить від підвищення рівнів хемокінів CXCR2.
14. Сполука, сіль чи сольват за п. 7 для використання при лікуванні псоріазу.
15. Сполука, сіль чи сольват за п. 7 для використання при лікуванні хронічного обструктивного захворювання легенів.
16. Сполука, сіль чи сольват за п. 7 для використання при лікуванні раку.
17. Сполука, сіль чи сольват за п. 7 для використання при лікуванні хвороби шлунково-кишкового тракту.
18. Спосіб одержання сполуки формули (І), яку визначено у п. 1, що включає обробку сполуки формули (ІІА):
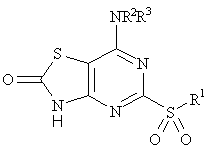 , (IIA)
, (IIA)
де R1, R2 та R3 визначено у формулі (І), тіолом R1SH у присутності придатної основи.
19. Спосіб одержання сполуки формули (І), яку визначено в п. 1, що включає обробку сполуки формули (ІІВ )
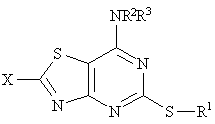 , (IIB)
, (IIB)
де R1 , R2 та R3 визначено у формулі (І), а X - відщеплювана група, алкоксидом металу з наступною обробкою кислотою чи основою, та, як варіант, після обробки, утворення фармацевтично прийнятної солі.
20. Проміжна сполука формули (ІІА)
 , (IIA)
, (IIA)
де R1, R2 та R3 як визначено у формулі (І).
21. Проміжна сполука формули (ІІВ)
 , (IIB)
, (IIB)
де R1, R2 та R3 такі, як визначено у формулі (І), а Х – відщеплювана група
за умови, що сполуками формули (ІІВ) не є:
і) 2-[[2-бром-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-2-метил-1-пропанол;
іі) 2[[2-бром-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-2-метил-1-пропанол.
22. Проміжна сполука формули (ІІІА)
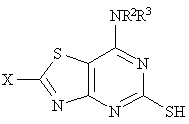 , (IIIA)
, (IIIA)
де R2 та R3 визначено у формулі (I), a X - NH2.
23. Фармацевтична композиція, що містить сполуку формули (І) чи її фармацевтично прийнятну сіль, чи сольват за будь-яким одним з пп. 1-6 у поєднанні з фармацевтично прийнятним ад'ювантом, розріджувачем чи носієм.
24. Спосіб виготовлення фармацевтичної композиції за п. 23, що включає змішування сполуки формули (І) чи її фармацевтично прийнятної солі, чи сольвату за будь-яким одним з пп.1-6 з фармацевтично прийнятним ад'ювантом, розріджувачем чи носієм.
Текст
Винахід стосується деяких сполук тіазолопіримідинону, способу їх виготовлення та інтермедіатів при їх виготовленні, фармацевтичних композицій, що їх містять та їх використання у терапії. У кожному з WO 98/08847 та ЕР0778277 розкрито серії 6,5-гетеродициклічних сполук, про які сказано, що вони корисні як антагоністи CRF. Хемокіни грають важливу роль в імунній та запальній реакціях при різних хворобах та розладах, включаючи астму та алергічні хвороби, а також автоімунні патології, як-то ревматоїдний артрит та атеросклероз. Ці малі секретовані молекули належать до збільшуваної надродини білків розміром 8-14кДа, що характеризуються чотирма збереженими цистеїновими функціональними послідовностями. Надродину хемокінів можна розділити на дві головні групи, що характеризуються структурними функціональними послідовностями, родини Cys-X-Cys (C-X-C) та Cys-Cys (C-C). Їх відрізняють на основі одиничної амінокислотної вставки між NH-проксимальною парою цистеїнових залишків та подібністю послідовностей. Хемокіни С-Х-С включають кілька потужних хемоатрактантів та активаторів нейтрофілів, як-то інтерлейкін8 (IL-8) та нейтрофіл-активаторний пептид 2 (NAP-2). Хемокіни С-С включають потужні хемоатрактанти моноцитів та лімфоцитів, але не нейтрофілів, як-то хемотактичні білки моноцитів людини 1-3 (МСР-1, МСР-2 та МСР-3), RANTES (Regulated on Activation, Normal T Expressed та Secreted), еотаксин та запальні білки макрофагів 1a та 1b (МІР-1a та ΜΙΡ-1b). Дослідження продемонструвало, що дію хемокінів опосередковано підродиною G сполучальних з білком рецепторів, серед яких є рецептори, позначені як CCR1, CCR2, CCR2A, CCR2B, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CCR10, CXCR1, CXCR2, CXCR3, CXCR4 та CX3CR1. Ці рецептори представляють гарні цілі для розробки ліків, оскільки засоби, що модулюють ці рецептори, могли б бути корисними при лікуванні розладів та хвороб, як-то тих, що згадано вище. Згідно з представленим винаходом запропоновано тому сполуку формули (І) чи її фармацевтично прийнятну сіль чи сольват: де R1 представляє С3-С7, карбоциклічну групу, С1-С8алкіл, С2-С6алкеніл чи С2-С6алкініл, кожну з цих груп, як варіант, заміщено одним чи більше замісниками, що незалежно вибрано з атомів галогену, -OR4, -NR5R6, CONR5R6, -COOR7, -NR8COR9, -SR10, -SO2R10, -SO2NR5R6, -NR8SO2R9, арилу чи гетероарилу, обидва з яких можуть бути, як варіант, заміщені одним чи більше замісниками, що незалежно вибрано з атомів галогену, ціаногрупи, нітрогрупи -OR4, -NR5R6, -CONR5R6, -COOR7, -NR8COR9, -SR10, -SO2R10, -SO2NR5R6. -NR8SO2R9, СгС6алкілу чи трифлуорметилу; R2 та R3, кожний незалежно, представляють атом гідрогену, чи С 3-С7 карбоциклічну групу, С1-С8алкіл, С2С6алкеніл чи С2-С6алкініл, останні чотири групи можуть бути, як варіант, заміщені одним чи більше замісниками, що незалежно вибрано з: (a) атомів галогену, -OR4, -NR5R6 -CONR5R6, -COOR7, -NR8COR9, -SR10, -SO2R10, -SO2NR5R6, -NR8SO2R9; (b) 3-8-членного кільця, що містить, як варіант, один чи більше атомів, що вибрано з О, S, NR8, тa само, як варіант, заміщено С1-С3алкілом чи галогеном; або (c) арилу чи гетероарилу, кожний з яких може бути, як варіант, заміщено одним чи більше замісниками, що незалежно вибрано з атомів галогену, ціаногрупи, нітрогрупи, -OR4, -NR5R6, -CONR5R6, - NR8COR9, -SO2NR5R6. -NR8SO2R9, С1-С6алкілу та трифлуорметилу; R4 представляє гідроген, С1-С6алкіл чи феніл, останні два з яких можуть бути, як варіант, заміщені одним чи більше замісниками, що незалежно вибрано з атомів галогену, фенілу, -OR11 та -NR12R13, R5 та R6 незалежно представляють атом гідрогену, С1-С6алкіл чи феніл, останні два з яких можуть бути, як варіант, заміщені одним чи більше замісниками, що незалежно вибрано з атомів галогену, фенілу, -OR14 та NR15R16, -CONR1-R16, -NR15COR16, -SONR15R16, NR15SO2R16, чи R5 та R6 разом з атомом нітрогену, до якого вони приєднані, утворюють 4-7-членну насичену гетероциклічну систему, що містить, як варіант, ще один гетероатом, який вибрано з атомів оксигену та нітрогену, ця кільцева система може бути, як, варіант, заміщена одним чи більше замісниками, що незалежно вибрано з фенілу, -OR14, -COOR14, -NR15R16, -CONR15R16, -NR15COR16, -SONR15R16, NR15SO2R16 чи С1С6алкілом, що сам, як варіант, заміщений одним чи більше замісниками, які незалежно вибрано з атомів галогену та груп -NR15R16 та -OR17; R10 представляє атом гідрогену, С1-С6алкіл чи феніл, останні два з яких можуть бути, як варіант, заміщено одним чи більше замісниками, що незалежно вибрано з атомів галогену, фенілу, -OR17 та -NR15R16; а кожний з R7, R8, R9, R11, R12, R13, R14 R15, R16 та R17 незалежно представляє атом гідрогену чи С1-С6алкіл чи феніл. В контексті представленого опису, якщо не сказано інше, алкіл чи алкеніл, або алкіл чи алкеніл у заміснику можуть бути лінійними чи розгалуженими. Арили включають феніл та нафтил. Гетероарили включають 5- ми 6-членні -ароматичні кільця, що містятьодин чи більше гетероатомів, які вибрано з N, S, О. Приклади включають піридин, піримідин, тіазол, оксазол, піразол, імідазол, фуран. Деякі сполуки формули (І) можуть бути у формі стереоізомерів. Слід розуміти, що винахід охоплює усі геометричні та оптичні ізомери сполук формули (І) та їх суміші, включаючи рацемати. Таутомери та їх суміші також утворюють аспект представленого винаходу. У вищенаведеній формулі (І) група R1 представляє С3-С7, карбоциклічну групу, С1-С8алкіл, С2-С6алкеніл чи С2-С6алкініл, кожну з цих груп, як варіант, заміщено одним чи більше замісниками, що незалежно вибрано з атомів галогену, -OR4, -NR5R6, -CONR5R6, -COOR7, -NR8COR9, -SR10, -SO2R10, -SO2NR5R6, -NR8SO2R9, арилу чи гетероарилу, обидва з яких можуть бути, як варіант, заміщені одним чи більше замісниками, що незалежно вибрано з атомів галогену, ціаногрупи, нітроігрупи -OR4, -NR5R6, -CONRSR6, -COOR7, -NR8COR9, -SR10, SO2R10, -SO2NR5R6. -NR8SO2R9, С1-С6алкілу чи трифлуорметилу. Особливо кращими сполуками формули (І) є ті, в яких R1 представляє заміщений, як варіант, бензил. Ще краще, коли R1 представляє бензил чи бензил, заміщений одним чи більше С1-С6алкілом, С1-С6алкоксилом чи атомами галогену. Коли R2 та R3 представляють групу, заміщену одним чи більше 3-8-членними кільцями, що містять, як варіант, один чи більше атомів, які вибрано з О, S чи NR8, приклади таких груп включають піперидин, піролідин, піперазин та морфолін. Переважно, один з R2 та R3 є гідрогеном, а інший - С1-С8алкілом, заміщеним гідроксилом та одним чи більше метилом чи етилом. Краще, коли один з R2 та R3 є гідрогеном, а інший - СН(СН3 )СН2ОН, CH(Et)CH2OH, C(CH3)2CH2OH чи СН(СН2ОН)2. Коли один з R2 та R3 є гідрогеном, а інший - СН(СН3)СН2OН чи CH(Et)CH2OH, сполуки формули (І) переважно існують у формі (R) ізомеру. Особливо кращі сполуки згідно з винаходом включають: 7-[(2-гідрокси-1,1-диметилетил)аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-он, (R)-7-[[1-(гiдpoкcимeтил)пpoпiл]aмiнo]-5-[(фeнілмeтил)тio]тiaзoлo[4,5-d]пipимiдин-2(3H)-он, (R)-7-[(2-гідрокси-1-метилетил)аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(ЗН)-он, 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[(2-гідрокси-1,1-диметилетил)аміно]тіазоло[4,5-d]піримідин-2(3Н)-он, 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-гiдpoкcи-1-мeтилeтил]aмiнo]тiaзoлo [4,5-d]піримідин-2(3Н)-он, 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-(гідроксіетокси)етил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он, 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]тіазоло-[4,5-d]піримідин-2(3Н)он, 7-[(2-аміноетил)аміно]-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2(3Н)-он, 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[(2-гідроксіетил)аміно]тіазоло[4,5-d]піримідин-2(3Н)-он, N-[2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2,3-дигідро-2-оксотіазоло[4,5-d]піримідин-7іл]аміно]етил]метансульфонамід, (+/-)-5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-(2-гідроксіетокси)-1-метилетил]аміно]тіазоло[4,5-d]піримідин2(3Н)-он, 7-[[(1R)-2-аміно-1-метилетил]аміно]-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2(3Н)-он, 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-[(2-гідроксіетил)аміно]-1-метилетил]аміно]тіазоло[4,5d]піримідин-2(3Н)-он, 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-(диметиламіно)-1-метилетил]аміно]тіазоло[4,5-d]піримідин2(3Н)-он, 5-[[[4-(2-аміноетокси)-3-хлорфеніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин2(3Н)-он, 5-[[3-хлор-4-метоксифеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)он, 5-[[3-хлор-2-флуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он, 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(3R,4R)-4-гідроксипіролідин-3-іл]аміно]-тіазоло[4,5-d]піримідин-2(3Н)он, 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[(3R)-піролідин-3-іламіно]тіазоло[4,5-d]піримідин-2(3Н)-он, 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-2(3Н)-он, 7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-2(3Н)он, 7-[(2-гідрокси-1,1-диметилетил)аміно]-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-2(3Н)-он, 7-[(2-гідрокси-1,1-диметилетил)аміно]-5-[[(2-метилфеніл)метил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-он, 5-[(2-фуранілметил)тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он, 7-[[(1R)-2-аміно-1-метилетил]аміно]-5-[[(3-хлор-2-флуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2(3Н)-он (2S)-2[[5-[[2,3-дифлуорфеніл)метил]тіо]2,3-дигідро-2-оксотіазоло[4,5-d]піримідин-7-іл]аміно]-гідроксипропанамід, 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(2-тієнілметил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-он, 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5[[[3-метил-4-(метилсульфоніл)феніл]метил]тіо]тіазоло[4,5d]піримідин-2(3Н)-он, 5-[[[3-хлор-4-(трифлуорметокси)феніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-етилетил]аміно]тіазоло[4,5d]піримідин-2(3Н)-он, 5-[[[2-флуор-3-(трифлуорметил)феніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5d]піриіиідин-2(3Н)-он, 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[2-[(диметиламіно)етил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он, 5-[[(2-флуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он, 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[[(2-метоксифеніл)метил]тіо]тіазоло[4,5-d]піримідин-2(3Н)-он, 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(2-феноксіетил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-он, 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[[(3-метилфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2(3Н)-он, 5-[[(2-флуор-3-метилфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)он, 5-[[(3-хлорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он, 5-[[(3-бромфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он, 5-[[[4-(дифлуорметокси)феніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин2(3Н)-он, (+/-)-5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-гідрокси-1-(метоксиметил)етил]аміно]тіазоло[4,5-d]піримідин2(3Н)-он, 7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-он, 5-[[(2-бромфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он, 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он, 5-[[3-хлор-2-флуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(ЗН)-он, (+/-)-5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-гідрокси-1-(метоксиметил)етил]аміно]тіазоло[4,5-d]піримідин2(3Н)-он, 7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-он, 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(ЗН)-он, 5-[(5-хлор-1,2,3-тіадіазол-4-іл)тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]-тіазоло[4,5-d]піримідин-2(3Н)-он, та їх фармацевтично прийнятні солі та сольвати. Особливі солі сполук формули (І) включають: Сіль натрію 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5d]піримідин-2(3Н)-ону, Сіль натрію 5-[[3-хлор-2-флуорфеніл)метид]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5d]піримідин-2(3Н)-ону, Сіль натрію (+/-)-5-[[(2,3-дифлуорфеніл)метил]тіо]-7-{[2-гідрокси-1-(метоксиметил)етил]аміно]тіазоло[4,5d]піримідин-2(3Н)-ону, Сіль натрію 7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3Н)ону, чи Сіль натрію 7-[[(1-R)-2-гідрокси-1-метилетил]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-ону. Наступні особливі солі сполук формули (І) включають: Трифлуорацетат 7-[[(1R)-2-аміно-1-метилетил]аміно]-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5d]піримідин-2(3Н)-ону, Трифлуорацетат 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-[(2-гідроксіетил)аміно]-1метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-ону, 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-(диметиламіно)-1-метилетил]аміно]тіазоло[4,5-d]піримідин2(3Н)-он, Трифлуорацетат 5-[[[4-(2-аміноетокси)-3-хлорфеніл]метил]тіо]-7-[[(1R)-2-гідрокси-1метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-ону, Моногідрохлорид 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[2-[(диметиламіно)етил]аміно]тіазоло[4,5-d]піримідин2(3Н)-ону, чи Дигідрохлорид 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[(3R)-піролідин-3-іламіно]тіазоло[4,5-d]піримідин-2(3Н)ону. Згідно з винаходом запропоновано також спосіб виготовлення сполуки формули (І), що включає : Або обробку сполуки формули (llА) де R1, R2 та R3 визначено у формулі(І), тіолом R1SH у присутності придатної основи та, як варіант, утворення фармацевтично прийнятної солі. Реакцію можна проводити у змішаному розчиннику з диметилсульфоксиду та етанолу при температурі між 0°С та 100°С, використовуючи борогідрид натрію як основу. Сполуки формули (llА) де R1, R2 та R3, що визначено у формулі (І), можна виготовити обробкою сполук формули (І) придатним окисником, як-то оксон. Реакцію можна проводити у розчиннику, як-то ацетонітрил, при температурі між 0°С та 100°С. Чи обробкою сполуки формули (ІIB); де R1, R2 та R3 визначено у формулі (І), а X - відщеплювана група, алкоксидом металу, з наступною обробкою кислотою чи основою та, як варіант, утворенням фармацевтично прийнятної солі X - будь-яка придатна відщеплювана група, як-то галоген. Реакцію можна проводити у спиртовому розчиннику, як-то метанол, а депротектування проводити у такому розчиннику, як 1,4-діоксан. Приклади алкоксидів металу включають метоксид калію. Приклади придатних кислот включають гідрохлоридну кислоту. Переважно сполуку формули (ІІВ) обробляють алкоксидом металу, як-то метоксид калію, а потім кислотою, якто конц. HCL у розчиннику, як-то 1,4-діоксан. Сполуки формули (ІІВ), де R1, R2 та R3 визначено у формулі (І), а X - галоген, можна виготовити з відповідних сполук (ІІВ), де R1, R2 та R3 визначено у формулі (І), а X - NH2; обробкою діазотувальним засобом, як-то ізоамілнітрит та галогенувальним засобом, як-то бромоформ. Сполуки формули (ІІВ), де R1, R2 та R3 визначено у формулі (І), а X - NH2, можна виготовити обробкою сполуки формули (ІІІА): де R2 and R3 визначено у формулі (І), а X -NH, сполукою формули R1X, де R1 визначено вище, а X відщеплювана група, як-то бромідна, у присутності такої основи, як діізопропілетиламін, в такому інертному розчиннику, як ДМСО/N-метилпіролідинон при температурі між 0°С та 100°С. Сполуки формули (llΙΑ), де R2 та R3 визначено у формулі (І), а X - ΝΗ, можна виготовити обробкою сполуки формули (ІІВ), де R2 та R3 визначено у формулі (І), X - ΝΗ, a R1 - придатна бензильна група, як-то бензил чи 2,3-дифлуорбензил, відновником, як-то розчин металевого натрію у рідкому аміаку, чи обробкою сполуки формули (ІІІВ): де R1 визначено у формулі(І), a L - відщеплювана група, як-то хлор, з аміном HNR2R3, де R2 та R3 визначено у формулі (І). Реакцію можна проводити у розчиннику, як-то N-метилпіролідин, при температурі між 0°С та 150°С. Сполуки формули (ІІІВ), де R1 визначено у формулі (І), a L - галогені можна виготовити обробкою сполуки формули (ІІІВ), де R1 визначено у формулі (І), a L - гідроксил, галогенувальним засобом, як-то оксихлорид фосфору. Реакцію можна проводити у присутності диметиланіліну, гріючи під зворотним холодильником. Сполуки формули (ІІІВ), де R1 визначено у формулі (І), a L - гідроксил, можна утворити обробкою сполуки формули (IVA) сполукою формули R1X, де R1 визначено вище, а X - відщеплювана група, як-то бромід у присутності основи, як-то трет-бутоксиду калію, в інертному розчиннику, як-то диметилсульфоксид при температурі довкілля. Чи нагріванням сполуки формули(IVB), де R1 визначено вище Реакцію переважно проводять у придатному розчиннику, як-то диметилформамід при підвищеній температурі, наприклад, приблизно при 120°С. Сполуки формули (IVB) можна легко виготовити реакцією сполуки загальної формули (V), де R1 визначено вище, з тіоціанатом калію та бромом в інертному розчиннику, як-то диметилформамід/піридин. Сполуки формули (V) зручно виготовляють реакцією сполуки формули (VI): зі сполукою формули R X, де R визначено вище, а X - відщеплювана група, як-то бромідна, у присутності такої основи, як гідрид натрію в інертному розчиннику, як-то диметилформамід, при температурі довкілля. Сполуки формул (IVA) та (VI) комерційно доступні чи добре відомі з літератури. Фахівцям буде зрозуміло, що у описаних вище способах функціональні групи (наприклад, гідроксили) проміжних сполук можуть потребувати протектування протектувальними групами. Кінцевий етап при виготовленні сполук згідно з винаходом може включати видалення одної чи більше протектувальних груп. Протектування та депротектування функціональних груп повністю [описано у Protective Groups in Organic Chemistry, вид. J.W.F.McOmie, Plenum Press (1973), та Protective Groups in Organic Synthesis, 2-е вид., Т.W.Greene & P.G.M.Wuts, Wiley-lnterscience (1991)]. Нові проміжні сполуки створюють наступний аспект винаходу. Зокрема, сполуки формул (llA), (ІІВ) та (lllА) є новими та створюють аспект винаходу. Сполуки вищенаведеної формули (І) можна перетворити у їх фармацевтично прийнятну сіль чи сольват, переважно основно-адитивну сіль, як-то натрію, калію, кальцію, алюмінію, літію, магнію, цинку, бензатину, хлорпрокаїну, холіну, діетаноламіну, етаноламіну, етилдіаміну, меглуміну, трометамін чи прокаїну, чи кислотно-адитивну сіль, як-то гідрохлорид, гідробромід, фосфат, ацетат, фумарат, малеат, тартрат, цитрат, оксалат, метансульфонат чи п-толуолсульфонат. Сполуки формули (І) мають фармацевтичну активність, зокрема, як модулятори рецепторів хемокінів, та їх можна використовувати при лікуванні (терапевтичному чи профілактичному) станів/хвороб організмів людини та нелюдини, які посилено чи викликано надлишковим чи нерегульованим продукуванням хемокінів. Приклади таких станів/хвороб включають: (1) (респіраторного тракту) обструктивні хвороби дихальних шляхів, включаючи хронічну обструктивну хворобу легенів (COPD); астму, як-то бронхіальну, алергічну, притаманну, сторонню та від пилу, особливо, хронічну чи застарілу астму (наприклад, пізню астму та гіперчутливість дихальних шляхів); бронхіти; гострий, алергічний, атрофічний риніт та хронічний риніт, включаючи казеозний риніт, гіпертрофічний риніт, гнійний риніт, сухий риніт та медикаментозний риніт; плівковий риніт, включаючи крупозний, фібринозний та псевдоплівковий риніт та золотушний риніт; сезонний риніт, включаючи риніт на нервовому ґрунті (сінна лихоманка) та вазомоторний риніт; саркоїдоз, легені фермера та споріднені хвороби, фіброїдні легені та ідіопатична інтерстиціальна пневмонія; (2) (кісток та суглобів) ревматоїдний артрит, сироваточнонегативні спонділоартропатії (включаючи анкілозний спондиліт, псоріатичний артрит та хворобу Рейтера), хворобу Бекета, синдром Сьйоргена та системний склероз; (3) (шкіри) псоріаз, атопічний дерматит, контактний дерматит та інші екзематозні дерматити, себорейний дерматит, лишай, пухирчатка, бульозна пухирчатка, бульозний епідермоліз, кропивниця, ангіодермія, васкулітид, еритема, шкірна еозинофілія, ювеїт, алопеція та кон'юнктивіт; (4) (шлунково-кишкового тракту) хвороба Куліака, проктит, еозинофільний гастроентерит, мастоцитоз, хвороба Крона, виразковий коліт, залежні від їжі алергії, що впливають на віддалені від кишечнику ділянки, наприклад, мігрень, риніт та екзема; (5) (хвороби інших тканин та системні хвороби) розсіяний склероз, атеросклероз, синдром набутого імунодефіциту (СНІД), червоний вовчак, системний червоний вовчак, еритроматоз, тироїдит Хашимото, важка міастенія, діабети типу 1, нефротичний синдром, еозинофілія, синдром гіпер-lgE, лепра, синдром сезарі та ідіопатична тромбопенія пурпура; післяопераційні спайки та сепсис; (6) (відторгнення) гострі та хронічні після, наприклад, трансплантації нирок, серця, печінки, легенів, кісткового мозку, шкіри та роговиці та хронічна хвороба хазяїна як реакція на трансплантат; (7) Рак, особливо рак немаленьких клітин легенів (NSCLC), злоякісна меланома, рак простати та сквамозна саркома, та пухлинні метастази; (8) хвороби, при яких ангіогенез асоційований з підвищеними рівнями хемокіну CXCR2 (наприклад, NSCLC, діабетична ретинопатія); (9) циститний фіброз, параліч, проникаючі поранення серця, мозку, периферійних членів та інших органів; (10) опіки та хронічні виразки шкіри; (11) хвороби репродуктивності (наприклад, розлади овуляції, менструації та імплантації, передчасні пологи, ендометріоз). Отже, згідно з представленим винаходом запропоновано сполуку формули (І), чи її фармацевтично прийнятну сіль чи сольват, що визначено вище, для використання у терапії. Переважно сполуки винаходу використовують для лікування хвороб, у яких рецептор хемокіну належить до підродини рецепторів хемокіну СХС, кращим цільовим рецептором хемокіну є рецептор CXCR2. Певні стани, які можна лікувати сполуками згідно з винаходом є псоріазом, хвороба, при якій ангіогенез асоційований з підвищеними рівнями хемокіну CXCR2 та хронічне обструктивне захворювання легенів. Краще використовувати сполуки згідно з винаходом . для лікування псоріазу. Згідно з наступним аспектом представленого винаходу запропоновано використання сполуки формули (І), чи вищенаведених її фармацевтично прийнятної солі чи сольвату у виробництві лікувального засобу для використання у терапії. Згідно з ще одним аспектом представленого винаходу запропоновано використання сполуки формули (І), чи вищенаведених її фармацевтично прийнятної солі чи сольвату у виробництві лікувального засобу для лікування хвороб чи станів людини, при яких корисною є модуляція активності рецепторів хемокінів. В контексті представленого опису, термін "терапія" також включає "профілактику", якщо не сказано інше. Терміни "терапевтичний" та "терапевтично" слід розуміти відповідно. Згідно з винаходом крім того запропоновано спосіб лікування опосередкованих хемокіном хвороб, де хемокін приєднується до рецептору хемокіну (особливо CXCR2), що включає застосування пацієнтом терапевтично ефективної кількості сполуки формули (І), чи вищенаведених її фармацевтично прийнятної солі чи сольвату. Згідно з винаходом запропоновано також спосіб лікування запальних хвороб, особливо псоріазу, у пацієнта, що потерпає від вказаної хвороби, чи має ризик захворіти нею, який включає застосування пацієнтом терапевтично ефективної кількості сполуки формули (І), чи вищенаведених її фармацевтично прийнятної солі чи сольвату. Для вищезазначених терапевтичних використань застосовувані дози безумовно залежатимуть від використовуваної сполуки, способу застосування, потрібного лікування та природи розладу. Сполуки формули (І) та їх фармацевтично прийнятні солі та сольвати можна використовувати самі по собі, але звичайно їх використовують у формі фармацевтичної композиції, в якій сполука/сіль/сольват формули (І) (активний інгредієнт) поєднаний з фармацевтично прийнятним ад'ювантом, розріджувачем чи носієм. Залежно від способу застосування фармацевтична композиція переважно вміщуватиме 0,05-99мас мас% (процентів за масою), краще 0,05-80мас%, ще краще 0,10-70мас%, найкраще 0,10-50мас%, активного інгредієнту, усі проценти за масою стосуються всієї композиції. Згідно з представленим винаходом запропоновано також фармацевтичну композицію, що містить сполуку формули (І), чи вищенаведені її фармацевтично прийнятні сіль чи сольват у поєднанні з фармацевтично прийнятним ад'ювантом, розріджувачем чи носієм. Згідно з винаходом далі запропоновано спосіб виготовлення фармацевтичної композиції згідно з винаходом, що включає змішування сполуки формули (І), чи вищенаведених її фармацевтично прийнятної солі чи сольвату з фармацевтично прийнятним ад'ювантом, розріджувачем чи носієм. Фармацевтичні композиції можна застосовувати локально (наприклад, до легенів та/чи дихальних шляхів чи до шкіри) у формі розчинів, суспензій, гептафлуоралканових аерозолів та композицій з сухого порошку; чи системно, наприклад, пероральним застосуванням у формі таблеток, капсул, сиропів, порошків чи гранул, чи парентеральним застосуванням у формі розчинів чи суспензій, чи підшкірним застосуванням чи ректальним застосуванням у формі супозиторіїв, чи трансдермально. Переважно сполуки згідно з винаходом вживають перорально. Винахід далі ілюстровано з посиланням на наступні приклади. У прикладах спектри ядерного магнітного резонансу (ЯМР) вимірювали на спектрометрі Varian Unity Inova 300 чи 400МГц, а мас-спектрометричні спектри (МС) вимірювали на спектрометрі Finnigan Mat SSQ7000 чи Micromass Platform, де потрібно, реакції проводили в інертній атмосфері азоту чи аргону. Хроматографію загалом проводили, використовуючи силікагель Matrex Silica 60 (35-70 мікрон) чи Prolabo Silica gel 60 (35-70 мікрон), придатні для імпульсної хроматографії на силікагелі. Очистку високоефективною рідинною хроматографією проводили, використовуючи · Waters Micromass LCZ з контролером насосу Waters 600, детектор Waters 2487 та колектор фракцій Gilson FC024 чи Waters Delta Prep 4000. Скорочення т.пл. та ДМСО у прикладах означають точку плавлення та диметилсульфоксид, відповідно. Приклад 1 7-[(2-гідрокси-1,1-диметилетил)аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-он (a) Тіоціанатний естер 6-аміно-1,4-дигідро-4-оксо-2-[(фенілметил)тіо]-5-піримідинілу 6-аміно-2[(фенілметил)тіо]-4(1Н)-піримідинон (10,5г) [виготовлено як описано у WO 9635678] та тіоціанат калію (25г) у Ν,Ν-диметилформаміді (200мл) гріли разом при 65°С. Піридин (6,3мл) додавали та розчин охолоджували до 5°С. Бром (2,2мл) додавали повільно та реакційну суміш перемішували протягом 2 годин при 5-10°С. Реакційну суміш виливали у льодяну воду, перемішували протягом 1 години та тверду речовину виділяли фільтруванням. Після промивки водою та етером, чистий зразок отримали після розтирання з гарячим метанолом. МС(АРСІ)291 (М+Н, 100%). (b) 2-аміно-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7(4Н)-он Продукт з етапу а) прикладу 1 (7,35г) гріли при 120°С у Ν,Ν-диметилформаміді (40мл)/воді (10мл) протягом 10 годин. Після охолодження утворену тверду речовину відфільтровували, промивали водою, далі етилацетатом, одержавши потрібну сполуку. Т.пл. 325°С МС (АРСІ) 291 (М+Н, 100%). (c) 7-хлор-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2-амін Продукт з етапу b) прикладу 1 (0,89г), оксихлорид фосфору (12мл) та Ν,Ν-диметиланілін (1,2мл) гріли під зворотним холодильником протягом 2 годин. Охолоджену реакційну суміш виливали у льодяну воду та перемішували протягом 2 годин. Хроматографія (SiO2, метанол/дихлорметан як елюент) дала потрібну сполуку. Т.пл. 217-218,5°C МС (АРСІ) 309 (М+Н, 100%). (d)2-[[2-аміно-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-2-метил-1-пропанол Продукт з етапу с) прикладу 1 (0,6г) та 1-аміно-2-метил-пропан-2-ол (1,1г) у тетрагідрофурані (10мл) гріли у закритій посудині при 100°С протягом 18 годин. Суміш випарювали досуха та очищали (SiO2, етилацетат як елюент), одержавши потрібну сполуку (0,46г). МС (АРСІ) 362 (М+Н+, 100%). (e) 2-[[2-бром-5-[(феніл метил )тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-2-метил-1-пропанол До розчину продукту з етапу d) прикладу 1 (0,1г) у бромоформі (5мл) додавали ізоамілнітрит (0,13мл) та суміш гріли при 60°С протягом 10 хвилин. Суміш випарювали досуха та очищали (SiO2, етилацетат:дихлорметан 1:9 як елюент), одержавши потрібну сполуку як безбарвну тверду речовину (0,043г). МС (АРСІ) 427 (М+Н+, 100%). (f) 2-[[2-метокси-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-2-метил-1-пропанол До розчину продукту з етапу e) прикладу 1 (0,36г) у метанолі (5мл) додавали гідроксид калію (0,095г) та суміш перемішували протягом 30 хвилин. Суміш нейтралізували концентрованою гідрохлоридною кислотою далі випарювали досуха та очищали (SiO2, етилацетат:дихлорметан 1:9 як елюент), одержавши потрібну сполуку як безбарвну тверду речовину (0,245г). МС (АРСІ) 377 (М+Н+, 100%). (g) 7-[(2-гідрокси-1,1-диметилетил)аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]-піримідин-2(3Н)-он До розчину продукту з етапу f) прикладу 1 (0,21 г) у 1,4-діоксані (5мл) додавали воду (0,1мл) та концентровану гідрохлоридну кислоту (1 краплю). Суміш гріли при 45°С протягом 3 годин, далі випарювали досуха. Перекристалізація (ацетонітрил) дала потрібну сполуку (0,110г). Т.пл. 207-8°С МС (АРСІ) 363 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 12,37 (1Н, s), 7,43-7,23 (5Н, m), 6,61 (1Н, bs),4,81 (1Н, t),4,34 (2Н, s), 3,55 (2Н, bs), 1,32 (6Н, s). ПРИКЛАД 2 (R)-7-[[1-(гідроксиметил)пропіл]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-он (а) (R)-2-[[2-аміно-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1-бутанол До суміші продукту з етапу с) прикладу 1 (2,5г) та (R)-(-)-2-аміно-1-бутанолу (5г) у розчиннику Nметилпіролідинон (10мл) додавали Ν,Ν-діізопропілетиламін (5мл) та утворену суміш гріли при 100°С протягом 10 годин. Суміш виливали у воду та продукт збирали фільтруванням, одержавши потрібну сполуку (2,5г) МС (АРСІ) 362 (М+Н+, 100%). (b) (R)-2-[[2-бром-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1-бутанол Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу а) прикладу 2. МС (АРСІ) 427 (М+Н+, 100%). (c) (R)-2-[(2-метокси-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1-бутанол Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 2. МС (АРСІ) 377 (М+Н+, 100%). (d) (R)-7-[[1-(гідроксиметил)пропіл]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]-піримідин-2(3Н)-он Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу с) прикладу 2. Т.пл. 217-8°С МС (АРСІ) 363 (М+Н+, 100%). ЯМР δΗ (d6-диметилсульфоксид) 12,37 (1Н, s), 7,43-7,21 (6Н, m), 4,68(1Н, t), 4,32 (2Н, q), 4,09 (1Н, bs), 3,47-3,32 (2Н, m), 1,69-1,59 (1Н, m), 1,48-1,41 (1Н, m), 0,82 (3Н, t). ПРИКЛАД 3 (R)-7-[(2-гідрокси-1-метилетил)аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-он (a) (R)-2-[(2-аміно-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1-пропанол Виготовлено способом з етапу а) прикладу 2, використовуючи продукт з етапу с) прикладу 1 та (R)-(-)-2аміно-1-пропанолу. МС (АРСІ) 412 (М+Н+, 100%). (b) (R)-2-[[2-бром-5[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1-пропанол Виготовлено способом з етапу є) прикладу 1, використовуючи продукт з етапу а) прикладу 3 МС (АРСІ) 348 (М+Н+, 100%). (с) (R)-2-[[2-метокси-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1-пропанол Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 3. МС (АРСІ) 363 (М+Н+, 100%). (d) (R)-7-[(2-гідрокси-1-метилетил)аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-он Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу c) прикладу 3. МС (АРСІ) 349 (М+Н+,100%). ЯМР dН (d6-диметилсульфоксид) 12,38 (1Н, s), 7,44-7,20 (6Н, m), 4,72 (1Н, t), 4,32 (2Н, m), 4,23 (1Н, m), 3,49-3,29 (2Н, m). 1,11(3H, d). ПРИКЛАД 4 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[(2-гідрокси-1,1-диметилетил)аміно]тіазоло-[4,5-d]піримідин-2(3-Н)-он (a) 2-аміно-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-а]піримідин-7(4Н)-он Розчин трет-бутоксиду калію (0,45мл 1Μ розчину у тетрагідрофурані) додавали до перемішуваного розчину 2-аміно-5,6-дигідро-5-тіоксотіазоло[4,5-d]піримідин-7(R)-ону (0,09г) [цитовано: Indian J. Chem., Sect. В (1989), 28В(11), 964-5.] та 2,3-дифлуорбензилброміду у диметилсульфоксиді (2мл). Після перемішування протягом 3 діб, реакційну суміш виливали у воду, одержавши потрібну сполуку, яку виділяли фільтруванням. МС (АРСІ) 327 (М+Н+,100%). (b) 7-хлор-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2-амін Виготовлено способом з етапу с) прикладу 1, використовуючи продукт з етапу а) прикладу 4. МС (АРСІ) 345 (М+Н+, 100%). (c) 2-[(2-аміно-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-2-метил-1-пропанол Виготовлено способом з етапу а) прикладу 2, використовуючи продукт з етапу b) прикладу 4 та 2-аміно-2метилпропанол. МС (АРСІ) 398 (М+Н+, 100%). (d) 2-[[2-бром-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-2-метил-1-пропанол Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу с) прикладу 4. МС (АРСІ) 462 (М+Н+, 100%). (e) 2-[{5-[[(2,3-дифлуорфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7-іл]аміно]-2-метил-1-пропанол Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу d) прикладу 4. МС (АРСІ) 413 (М+Н+, 100%). (f) 5-[{(2,3-дифлуорфеніл)метил]тіо]-7-[(2-гідрокси-1,1-диметилетил)аміно]-тіазоло[4,5-d]піримідин-2(3Н)-он Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу e) прикладу 4. МС (АРСІ) 399 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 12,41 (1Н, s), 7,41-7,30 (2Н, m), 7,21-7,13 (1Н, m), 6,64 (1Н, bs), 4,79 (1Η, t), 4,41 (2Н, s), 3,53 (2Н, d), 1,29 (6Н, s). ПРИКЛАД 5 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он (a) (2R)-2-[[2-аміно-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1-пропанол Виготовлено способом з етапу а) прикладу 2, використовуючи продукт з етапу b) прикладу 4 та (R)-(-)-2аміно-1-пропанол. МС (АРСІ) 384 (М+Н+, 100%). (b) (2R)-2-[[2-бром-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1-пропанол Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу а) прикладу 5. МС (АРСІ) 448 (М+Н+, 100%). (c) (2R)-2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7-іл]аміно]-1-пропанол Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 5. МС (АРСІ) 398 (М+Н+, 100%). (d) 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]-тіазоло[4,5-d]піримідин-2(3Н)он Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу с) прикладу 5. МС (АРСІ) 385 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 12,41 (1Н, s), 7,41-7,11 (4Н, m), 4,72 (1Н, t), 4,39 (2Н, m), 4,21 (1Н, m), 3,47-3,29 (2Н, m), 1,09 (ЗН, d). ПРИКЛАД 6 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-(гідроксіетоксі)етил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он (а) 2-[2-[[2-аміно-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]етоксі]етанол, Виготовлено способом з етапу а) прикладу 2, використовуючи продукт з етапу b) прикладу 4 та 2-(2аміноетоксі)етанол. МС (АРСІ) 414 (М+Н+, 100%). (b) 2-(2-[[2-бром-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]-аміно]етоксі]етанол, Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу а) прикладу 6. МС (АРСІ) 478 (М+Н+, 100%). (c) 2-[2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7-іл]аміно]етоксі]етанол, Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 6. МС (АРСІ) 429 (М+Н+, 100%). (d) 5-[[(23-дифлуорфеніл)метил]тіо]-7-[[2-(2-гідроксіетоксі)етил]аміно]тіазоло-[4,5-d]піримідин-2(3Н)-он Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу с) прикладу 6. Т.пл. 213-4°С МС (АРСІ) 415 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,41 (1Н, s), 7,39-7,11 (4Н, m), 4,57 (1Н, t), 4,39 (2Н, s), 3,57-3,38 (8Н, m). ПРИКЛАД 7 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]тіазоло[4,5-d]піримідин-2(Н)он, (a) 2-[[2-аміно-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]-аміно]-1,3-пропандіол, Виготовлено способом з етапу а) прикладу 2, використовуючи продукт з етапу b) прикладу 4 та 2-аміно1,3-пропандіол. МС (АРСІ) 400 (М+Н+, 100%). (b) 2-[(2-бром-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1,3-пропандіол, Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу а) прикладу 7. МС (АРСІ) 464 (М+Н+, 100%). (c) 2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2-метокситіазоло(4,5-d]піримідин-7-іл]аміно]-1,3-пропандіол, Виготовлено способом з етапу f) прикладу 1, використовуючи продукт 7 з етапу b) прикладу 7. МС (АРСІ) 415 (М+Н+, 100%). d) 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-тіазоло[4,5-d]піримідин2(3Н)-он, Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу с) прикладу 7. Т.пл. 178-9°С МС (АРСІ) 401 (М+Н+,100%). ЯМР dН (d6-диметилсульфоксид) 12,41 (1Н, s), 7,42-7,11 (4Н, m), 4,66 (2Н, s), 4,40 (2Н, s), 4,19 (1Н, m),3,49(4Н, m). ПРИКЛАД 8 7-[(2-аміноетил)аміно]-5-[[(2,3-дифлуорфеніл)метилІтіо]тіазоло[4,5-d]піримідин-2(3Н)-он, (а) 1,1-диметилетиловий естер(2-[[2-аміно-5-[[(2,3-дифлуорфеніл)метил]тіо]-тіазоло[4,5-d]піримідин-7іл]аміно]етил]карбамової кислоти Виготовлено способом з етапу а) прикладу 2, використовуючи продукт з етапу b) прикладу 4 та 1,1диметилетиловий естер (2-аміноетил)-карбамової кислоти. МС (АРСІ) 469 (М+Н+,100%). b) 1,1-диметилетиловий естер(2-[[2-бром-5-[[(2,3-дифлуорфеніл)метил]тіо]-тіазоло[4,5-d]піримідин-7іл]аміно]етил]-карбамової кислоти Виготовлено способом з етапу є) прикладу 1, використовуючи продукт з етапу а) прикладу 8. МС (АРСІ) 533 (М+Н+, 100%). c) 1,1-диметилетиловий естер [2-[(5-[[(2,3-дифлуорфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7іл]аміно]етил]-карбамової кислоти Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 8. МС (АРСІ) 489 (М+Н+, 100%). d) 7-[(2-аміноетил)аміно]-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2(3Н)-он, Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу с) прикладу 8. Т.пл. 215-6°С МС (АРСІ) 370 (М+Н+,100%). ЯМР dН (d6-диметилсульфоксид) 12,00 (1Н, s), 7,45-7,11 (3Н, m), 6,35 (1Н, bs), 4,37 (2Н, s), 3,48 (2Н, m),2,92(2Н, t) ПРИКЛАД 9 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[(2-гідроксіетил)аміно]тіазоло[4,5-d]піримідин-2(3Н)-он, (а) 2-[[2-аміно-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]етанол Виготовлено способом з етапу а) прикладу 2, використовуючи продукт з етапу b) прикладу 4 та етаноламін. МС (АРСІ) 370 (М+Н+, 100%). (b) 2-[[2-бром-5-[[2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]етанол Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу а) прикладу 9. МС (АРСІ) 434 (М+Н+, 100%). c) 2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7-іл]аміно]етанол, Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 9. МС (АРСІ) 385 (М+Н+, 100%). d) 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[(2-гідроксіетил)аміно]тіазоло[4,5-d]піримідин-2(3Н)-он, Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу с) прикладу 9. Т.пл. 217-9°С МС (АРСІ) 371 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 12,43 (1Н, s), 7,67-7,64 (1Н, m), 7,39-7,33 (2Н, m), 7,16-7,12 (1Н, m), 4,73 (1Н, t), 4,40 (2Н, s), 3,52-3,42 (4Н, m). ПРИКЛАД 10 N-2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2,3-дигідро-2-оксотіазоло[4,5-d]піримідин-7іл]аміно]етил]метансульфонамід, (а) N-(2-[[2-аміно-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7іл]аміно]етил]метансульфонамід, Виготовлено способом з етапу а) прикладу 2, використовуючи продукт з етапу b) прикладу 4 та N-[2аміноетил]-метансульфонаміду. МС (АРСІ) 448 (М+Н+, 100%). b) N-(2-[[2-бром-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7іл]аміно]етил]метансульфонамід, Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу а) прикладу 10. МС (АРСІ) 511 (М+Н+, 100%). c) N-[2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7іл]аміно]етил]метансульфонамід, Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 10. МС (АРСІ) 462 (М+Н+, 100%). d) N-[2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2,3-дигідро-2-оксотіазоло[4,5-d]піримідин-7іл]аміно]етил]метансульфонамід, Виготовлено способом з етапу д) прикладу 1, використовуючи продукт з етапу с) прикладу 10. Т.пл. 225-6°C МС (АРСІ) 448 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 12,49 (1Н, s), 7,72 (1Н, t), 7,41-7,13 (4Н, m), 4,43 (2Н, bs), 3,49 (2Н, m), 3,13 (2Н, m), 2,89 (3Н, s). ПРИКЛАД 11 (+/-)-5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-(2-гідроксіетокси)-1-метилетил]аміно]тіазоло[4,5-d]піримідин2(3Н)-он, (а)-2-[2-[(2-аміно-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]пропоксі]етанол, Виготовлено способом з етапу а) прикладу 2, використовуючи продукт з етапу b) прикладу 4 та (+/-)-2-[2амінопропоксі]етанол, МС (АРСІ) 428 (М+Н+, 100%). b) (+/-)-2-[2-[(2-бром-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]пропоксі]етанол, Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу а) прикладу 11. МС (АРСІ) 492 (М+Н+, 100%). c) (+/-)-2-[2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7-іл]аміно]пропоксі]етанол, Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 11. МС (АРСІ) 443 (М+Н+, 100%). d) (+/-)-5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-(2-гідроксіетокси)-1-метилетил]аміно]тіазоло[4,5-d]піримідин2(3Н)-он, Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу с) прикладу 11. Т.пл. 221-2°C МС (АРСІ) 429 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 12,43 (1Н, s), 7,47-7,30 (3Н, m), 7,17-7,13 (1Н, m), 4,56 (1Н, t), 4,40 (2Н, s), 4,35 (1Н, m), 3,49-3,32 (6Н, m), 1,10 (3Н, d). ПРИКЛАД 12: Трифлуорацетат 7-[[(1R)-2-аміно-1-метилетил]аміно]-5-[[(2,3-дифлуорфеніл)-метил]тіо]тіазоло[4,5d]піримідин-2(3Н)-ону, (а) (2R)-2-[[2-аміно-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]пропанамід, Виготовлено способом з етапу а) прикладу 2, використовуючи продукт з етапу b) прикладу 4 та гідрохлорид (2R)-2-амінопропанаміду. МС (АРСІ) 397 (М+Н+, 100%). (b) N7-[(1R)-2-аміно-1-метилетил]-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2,7-діамін До розчину продукту з етапу а) прикладу 12 (0,3г) у сухому тетрагідрофурані (10мл) додавали 2М боран у ТГФ (10мл) та суміш гріли під зворотним холодильником протягом 6 годин. Гасили гарячим метанолом (30мл), випарювали досуха та залишок переносили у метанол (30мл), що містить кілька крапель концентрованої гідрохлоридної кислоти. Суміш далі гріли під зворотним холодильником протягом ще 1 години, випарювали досуха, одержавши блідо-жовту тверду речовину. МС (АРСІ) 383 (М+Н+, 100%). (c) 1,1-диметилетиловий естер[(2R)-2-[[2-аміно-5-[[(2,3-дифлуорфеніл)метил]-тіо]тіазоло[4,5-d]піримідин-7іл]аміно]пропіл]карбамової кислоти До розчину продукту з етапу b) прикладу 12 (1,6г) у ТГФ (50мл) додавали ди-трет-бутилдикарбонат (0,91г) та суміш перемішували протягом 2 діб. Випарювали досуха, одержавши 2,0г. МС (АРСІ) 483 (М+Н+, 100%). (d) 1,1-диметилетиловий естер [(2R)-2-[[2-бром-5-[[(2,3-дифлуорфеніл)метил]тіо]-тіазоло[4,5-d]піримідин-7іл]аміно]пропіл]карбамової кислоти Виготовлено способом з етапу с) прикладу 1, використовуючи продукт з етапу с) прикладу 12. МС (АРСІ) 547 (М+Н+, 100%). (e) 1,1-диметилетиловий естер [(2R)-2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2-метокситіазоло[4,5d]піримідин-7-іл]аміно]пропіл]карбамової кислоти Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу d) прикладу 12. МС (АРСІ) 498 (М+Н+, 100%). (f) Трифлуорацетат 7-[[(1R)-2-аміно-1-метилетил]аміно]-5-[[(2,3-дифлуорфеніл)-метил]тіо]тіазоло[4,5d]піримідин-2(3Н)-ону, Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу e) прикладу 12, та очищено способом з етапу f) прикладу 15. МС (АРСІ) 384 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 12,55 (1Н, s),7,81 (3Н, bs), 7,45-7,31 (4Н, m), 7,18-7,13 (1Н, m), 4,51-4,34 (3Н, m). 2,95 (2Н, m), 1,14 (3Н, d). ПРИКЛАД 13 Трифлуорацетат 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-[(2-гідроксіетил)-аміно]-1метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-ону, До розчину продукту з етапу f) прикладу 12 (100мг) у сухому ТГФ (5мл) додавали [[(1,1диметилетил)диметилсиліл]окси]-ацетальдегід (49мг), а потім триацетоксиборогідрид натрію (61мг) та суміш перемішували протягом 1 години. Суміш підкислювали концентрованою гідрохлоридною кислотою, перемішували при кімнатній температурі протягом 1 години, а далі випарювали досуха. Продукт очищали (ВЕРХ, колонка Novapak® СІ 8, 0,1% водна ТРА:ацетонітрил, градієнтне елюювання 75:25-5:95 протягом 15 хвилин), одержавши потрібну сполуку (0,021г). МС (АРСІ) 428 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 7,39-7,29 (2Н, m), 7,17-12 (1Н, m). 6,92 (1Н, m), 4,91 (1Н, s), 4,48-4,32 (3Н, m), 3,54 (2Н, m), 2,94-2,82 (4Н, m), 1,12 (3Н, m). ПРИКЛАД 14 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-(диметиламіно)-1-метилетил]аміно]тіазоло[4,5-d]піримідин2(3Н)-он, Виготовлено способом з прикладу 13, використовуючи продукт з етапу f) прикладу 12, та 40% водний розчин формальдегіду. МС (АРСІ) 412 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 12,00 (1Н, s), 7,39-7,31 (2Н, m), 7,18-7,09 (2Н, m), 4,39 (2Н, q ), 4,30 (1Н, m). 3,31 (6Н, bs), 2,43-2,38 (1Н, m), 2,24-20 (1Н, m), 1,07 (3Н, d). ПРИКЛАД 15 Трифлуорацетат 5-[[[4-(2-аміноетокси)-3-хлорфеніл]метил]тіо]-7-[[(1R)-2-гідрокси-1метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-ону (a) 2-(2-хлор-4-формілфенокси)ацетамід До розчину 3-хлор-4-гідроксибензальдегіду (10г) у метанолі (100мл) додавали 1,0Μ трет-бутоксид калію (64мл). До суміші додавали 2-хлорацетамід (5,96г) та суміш гріли під зворотним холодильником протягом ночі. Суміш випарювали, залишок розтирали з водою (500мл) та тверду речовину збирали, одержавши потрібну сполуку (4,4г). ЯМР dΗ (CDCI 3) 9,89 (1Н, s), 7,97 (1Н, d), 7,82 (1Н, dd ), 7,04 (1Н, d), 6,73 (1Н, s), 25 5,87(1Η, s). 4,63 (2H, s). (b) 2-[2-хлор-4-(гідроксиметил)фенокси]ацетамід, До розчину продукту з етапу а) прикладу 15 (4,4г) у етанолі (500мл) додавали борогідрид натрію (1,56г) та суміш перемішували протягом 1 години. Підкислювали льодяною оцтовою кислотою, випарювали досуха та екстрагували етилацетатом, промивали водою, одержавши потрібну сполуку (4,3г). ЯМР dΗ (CDCI 3) 7,44 (1Н, d), 7,29 (1Н, d), 6,90 (1Н, d ), 6,81 (1Н, s), 5,85 (1Н, s), 4,63 (2Н, s). 4,48 (2H,s), 1,96(1Η, s). (с) 2-[4-[(ацетилтіо)метил]-2-хлорфенокси]ацетамід, Діізопропілазодикарбоксилат (5,5мл) додавали до перемішуваного розчину трифенілфосфіну (7,31г) у ТГФ при 0°С. При закінченні додавання випадав безбарвний осад. До цієї суспензії додавали суміш продукту з етапу b) прикладу 15 (3,0г) та тіооцтову кислоту (2,00мл) у ТГФ (30мл) при 0°С. Суміші давали досягти кімнатної температури протягом ночі, випарювали досуха та залишок очищали (SiO2, 10% етилацетату:90% ефіру як елюент), одержавши потрібну сполуку (3,5г). ЯМР dΗ (CDCI 3) 7,35 (1Н, d), 7,17 (1Н, dd), 6,84 (1Н. d), 6,76 (1Н, s), 5,81 (1Н, s), 4,54 (2Н, s), 4,04 (2Н, s ), 2,35 (3Н, s). (d) 2-[2-хлор-4-(меркаптометил)фенокси]ацетамід, До розчину продукту з етапу с) прикладу 15 (1,0г) у метанолі (50мл) додавали гранули гідроксиду натрію (0,15г) та суміш перемішували протягом 2 діб. Суміш розбавляли водою та потрібну сполуку збирали фільтруванням (0,7г). ЯМР dΗ (d6-диметилсульфоксид) 7,44 (1Н, s), 7,38 (1Н, d), 7-21 (1Н, dd ), 6,98(1Η, d), 4,55 (2Н, s), 3,76 (2H, s). (e) 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(фенілметил)сульфоніл]тіазоло[4,5-d]піримідин-2(3Н)-он, До розчину продукту з етапу d) прикладу 3 (240мг) у ацетонітрилі (100мл) та воді (100мл) додавали оксон (2,4г) та суміш гріли при 40°С протягом 2 годин. Ацетонітрил видаляли роторним випарюванням та потрібну сполуку збирали фільтруванням (235мг) МС (АРСІ) 381 (М+Н+, 100%). (f) Трифлуорацетат 5-[[(4-(2-аміноетокси)-3-хлорфеніл]метил]тіо]-7-[[(12?)-2-гідрокси-1метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-ону Суміш продукту з етапу e) прикладу 15 (100мг), продукту з етапу d) прикладу 15 (329мг) та борогідриду натрію (50мг) у розчині диметилсульфоксиду (1мл) та етанолу (10мл) гріли при 55-60°С протягом 12 годин. Реакційну суміш випарювали досуха та залишок очищали (ВЕРХ, колонка Novapak® С18, 0,1% водн. TFA:ацетонітрил, градієнтне елюювання 95:5-5:95 протягом 15 хвилин), одержавши потрібну сполуку (0,023г). МС (АРСІ) 442 (М+Н+, 100%). ЯМР dΗ {D2O) 7,46 (1Н, bs), 7,32 (1Н, d), 7,00 (1Н, d), 4,36-4,20 (5Н, m), 3,61 (2Н, m), 3,46(2Н, m), 1,20(3H, d). ПРИКЛАД 16 5-[[3-хлор-4-метоксифеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)он а) 3-хлор-4-метоксибензолметантіол Тіосечовину (3,04г, 0,04моль) додавали до розчину 3-хлор-4-метоксибензилброміду (4,0г, 0,02моль) у етанолі (200мл) та гріли під зворотним холодильником протягом 16 годин. Реакційну суміш концентрували у вакуумі та залишок далі розчиняли у водному розчині гідроксиду натрію (30г, 0,75моль у 300мл води) та гріли при 80°С протягом одної години. Реакційну суміш охолоджували льодяною банею та підкислювали додаванням концентрованої гідрохлоридної кислоти. Продукт виділяли триразовою екстракцією діетиловим етером. Поєднані органічні фази сушили безводним сульфатом магнію, фільтрували та концентрували у вакуумі, одержавши потрібну сполуку як безбарвне масло з виходом 83%. ЯМР dΗ (CDCI 3) 7,34 (1Н, m,), 7,18 (1Н, dd,), 6,86 (1Н, d), 3,89 (3Н, s), 3,68 (2Н, d), 1,76(1H,t). b) 5-[[3-хлор-4-метоксифеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]-тіазоло[4,5-d]піримідин2(3Н)-он 3-хлор-4-метоксибензолметантіол (0,128г, 0,68ммоль), виготовлений на етапі а) прикладу 16, продукт з етапу e) прикладу 15 (0,130г, 0,349ммоль), та борогідрид натрію (0,026г, 0,68ммоль) гріли під зворотним холодильником при 50°С у суміші диметилсульфоксиду (6мл) та етанолу (10мл). Через 3 години та знов через п'ять годин перебігу реакції додавали до реакційної суміші наступні порції борогідриду натрію (0,05г, 1,3ммоль) у етанолі (2мл) та нагрів під зворотним холодильником при 50°С продовжували до завершення перетворення, контролюючи ВЕРХ-МС (загалом 15 годин). Реакційну суміші нейтралізували додаванням концентрованої гідрохлоридної кислоти та етанол видаляли у вакуумі. Залишок очищали обернено-фазовою хроматографією на Symmetry C8, елююючи з градієнтом 25%-95% ацетонітрилу у 0,1Μ водному ацетаті амонію протягом 10 хвилин. Продукт сушили сублімацією метанолу/води/ацетонітрилу, одержавши потрібну сполуку з виходом 33% як білий ліофілат (0,046г). МС (АРСІ) 413 (М+Н+, 100%). ЯМР dΗ (d6-ДМCO) 12,39 (1Н, bs), 7,47 (1Н, m), 7,36 (1Н, m), 7,25 (1Н, d), 7,06 (1Н, d). 4,72 (1Н, t), 4,32-4,21 (3Н, m), 3,82 (3Н, s). 3,49-3,30 (2Н, m), 1,11 (ЗН, d), ПРИКЛАД 17 5-[[3-хлор-2-флуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло [4,5-d]піримідин-2(3Н)-он a) 3-хлор-2-флуорбензолметантіол Потрібну сполуку виготовляли як безбарвне масло з виходом 65% (2,51г) способом, що описано у етапі а) прикладу 16 з 3-хлор-2-флуорбензилброміду (5,0г, 0,022моль). ЯМР dΗ (CDCI 3) 7,32-7,21 (2Н, m), 7,04 (1Н, t), 3,75 (2Н, d), 1,90 (1Н, t). b) 5-[(3-хлор-2-флуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]-тіазоло[4,5-d]піримідин-2(3Н)он Потрібну сполуку виготовляли способом з етапу b) прикладу 16 з 3-хлор-2-флуорбензолметантіолу з етапу а) прикладу 17 та продукту з етапу e) прикладу 15. Продукт отримали з виходом 12% як білий ліофілат (0,038г). Т.пл. 234-5°С МС (АРСІ) 401 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,4 (1Н, bs), 7,55 (1Н, m), 7,48 (1Н, t), 7,26 (1Н, d), 7,17 (1Н, t), 4,72 (1Н, bs), 4,38 (2Н, m), 4,19 (1Н, m), 3,3 (2Н, m), 1,08 (3Н, d). ПРИКЛАД 18 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(3R,4R)-4-гідроксипіролідин-3-іл]аміно]-тіазоло{[4,5-d]піримідин-2(3Н)он (a) 1,1-диметилетиловий естер 3-[[2-аміно-5-[[(2,3-дифлуорфеніл)метил]-тіо]тіазоло[4,5-d]піримідин-7іл]аміно]-4-гідрокси-(3R,4R)-1-піролідинкарбонової кислоти 1,1-диметилетиловий естер (3R,4R)-3-аміно-4-гідрокси-1-піролідинкарбонової кислоти (0,73г), діізопропілетиламін (1,0мл) та продукт з етапу b) прикладу 4 перемішували у N-метилпіролідиноні (10мл) при 100°С протягом 28 годин. Охолоджену реакційну суміш виливали у воду та утворену тверду речовину збирали, промивали водою та сушили на повітрі. Сирий матеріал очищали (SiO2, етилацетат як елюент), одержавши потрібну сполуку як безбарвну тверду речовину (0,58г). Т.пл. 182-5°С МС (АРСІ) 511 (М+Н+, 100%). (b) 1,1-диметилетиловий естер 3-[[2-бром-5-[[(2,3-дифлуорфеніл)метил]тіо]-тіазоло[4,5-d]піримідин-7іл]аміно]-4-гідрокси-(3R,4R)-1-піролідинкарбонової кислоти Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу а) прикладу 18. МС (АРСІ) 572 (М-Н+, 100%). (c) 1,1-диметилетиловий естер 3-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7іл]аміно]-4-гідрокси-(3R,4R)-1-піролідинкарбонової кислоти Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 18. МС (АРСІ) 526 (М+Н+, 100%). (d) 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(3R,4R)-4-гідроксипіролідин-3-іл]аміно]-тіазоло[4,5-d]піримідин2(3Н)-он Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу с) прикладу 18. Т.пл. 270°С(розкл.) МС (АРСІ) 412 (М+Н+,100%). ЯМР dΗ (d6-диметилсульфоксид) 7,32 (2Н, m), 7,14 (1Н, m), 6,46 (1Н, d), 5,57 (1Н, s), 4,39 (2Н, S), 4,30 (2Н, m), 3,39 (2Н, m), 3,12 (1Н. dd). 2,98 (1Н, d). ПРИКЛАД 19 Дигідрохлорид 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[(3R)-піролідин-3-іламіно]-тіазоло[4,5-d]піримідин-2(3Н)ону (а) 1,1-диметилетиловий естер 3-[[2-аміно-5-[[(2,3-дифлуорфеніл)метил]-тіо]тіазоло[4,5-d]піримідин-7іл]аміно]-(3R)-1-піролідинкарбонової кислоти Виготовлено способом з етапу а) прикладу 18, використовуючи 1,1-диметилетиловий естер (R)-3-аміно-1піролідинкарбонової кислоти та продукт з етапу b) прикладу 4. МС (АРСІ) 495 (М+Н+, 100%). (b) 1,1-диметилетиловий естер 3-[[2-бром-5-[[(2,3-дифлуорфеніл)метил]тіо]-тіазоло[4,5-d]піримідин-7іл]аміно]-(3R)-1-піролідинкарбонової кислоти Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу а) прикладу 19. МС (АРСІ) 559 (М+Н+, 100%). (c) 1,1-диметилетиловий естер 3-[(5-[((2,3-дифлуорфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7іл]аміно]-(3R)-1-піролідинкарбонової кислоти Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 19. МС (АРСІ) 510 (М+Н+, 100%). (d) Дигідрохлорид 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[(3R)-піролідин-3-іламіно]-тіазоло[4,5-d]піримідин2(3Н)-ону Виготовлено способом з етапу д) прикладу 1, використовуючи продукт з етапу с) прикладу 19, далі його перетворено у сіль. Т.пл. 178-181°C МС (АРСІ) 396 (М+Н, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,75 (1Н, s), 9,19 (2Н, bd), 7,91 (1Н, d), 7,37 (2H,m). 7,17 (1Н, m), 4,66 (1Н, m), 4,43 (2Н, dd), 3,10-3,50 (4Н, m), 2,17 (1Н, m), 1,96 (1Н, m). ПРИКЛАД 20 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[[(2-метил-4-тіазоліл)метил]тіо]-тіазоло[4,5-d]піримідин-2(3H)-он (a) 6-аміно-2-[[(2-метил-4-тіазоліл)метил]тіо]-4(3Н)-піримідинон Гідрат 4-аміно-6-гідрокси-2-меркаптопіримідину (16,1г) та порошок гідроксиду натрію (8,0г) перемішували у сухому диметилформаміді (100мл) протягом 20 хвилин. Порціями додавали моногідрат гідрохлориду 4хлорметил-2-метилтіазолу (20г) та утворену суспензію перемішували протягом 18 годин. Суміш виливали у воду та тверду речовину збирали, промивали водою та сушили, одержавши потрібну сполуку (24,3г) МС (АРСІ) 255 (М+Н+, 100%). (b) 2-аміно-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-7(6Н)-он Продукт з етапу а) прикладу 20 (24,3г) та тіоціанат калію (37,1г) перемішували у сухому диметилформаміді (400мл) з піридином (13,1мл) при 0°С. Бром (4,5мл) додавали протягом 1 години. Після перемішування протягом 2 годин суміш виливали у воду. Утворений розчин концентрували до малого об'єму, далі додавали воду. Утворену тверду речовину збирали, переносили у 2М гідрохлоридну кислоту та осаджували додаванням насиченого розчину гідрокарбонату натрію. Тверду речовину збирали, промивали водою та сушили, одержавши потрібну сполуку, (8,7г). МС (АРСІ) 312 (М+Н+, 100%). (с) 7-хлор-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-2-амін Виготовлено способом 1 з етапу с) прикладу , використовуючи продукт з етапу b) прикладу 20 (4,3г). МС (АРСІ) 330/332 (М+Н+), 330 (100%). (d) (2R)-2-[[2-аміно-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1-пропанол Виготовлено способом з етапу а) прикладу 18, використовуючи продукт з етапу с) прикладу 20. Т.пл. 220-2°С МС (АРСІ) 369 (М+Н, 100%). (e) (1R)-2-[[2-бром-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1-пропанол Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу d) прикладу 20. МС (АРСІ) 433 (М+Н+, 100%). (f) (2R)-2-[[2-метокси-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1-пропанол Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу e) прикладу 20. МС (АРСІ) 384 (М+Н+, 100%). (g) 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло [4,5-d]піримідин-2(3Н)он Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу f) прикладу 20. Т.пл. 208-9°С МС (АРСІ) 370 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 12,37 (1Н, s), 7,35 (1Н, s), 7,32 (1Н, d), 4,73 (1Н, t), 4,36 (2Н, s), 4,21 (1Н, m), 3,38 (2Н, m), 2,62 (3Н, s), 1,10 (3Н, d). ПРИКЛАД 21 7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-5-[[(2-метил-4-тіазоліл)метил]тіо]-тіазоло[4,5-d]піримідин-2(3Н)он (a) 2-[(2-аміно-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1,3-пропандіол Виготовлено способом з етапу а) прикладу 18, використовуючи продукт з етапу с) прикладу 20 та 2-аміно1,3-пропандіол. Т.пл, 158-160°С МС (АРСІ) 385 (М+Н, 100%). (b) 2-[[2-бром-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]-аміно]-1,3-пропандіол Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу а) прикладу 21. МС (АРСІ) 448 (М+Н+, 100%). (с) 2-[[2-метокси-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1,3-пропандіол Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 21. МС (АРСІ) 400 (М+Н+, 100%). (d) 7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-5-[[(2-метил-4-тіазоліл)метил]-тіо]тіазоло[4,5-d] піримідин2(3Н)-он Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу с) прикладу 21. Т.пл. 239-243°С МС (АРСІ) 386 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,37 (1Н, s), 7,38 (1Н, s), 7,24 (1Н, d), 4,67 (2Н, t), 4,36 (2Н, s), 4,20 (1Н, m), 3,50 (4Н, m), 2,62 (ЗН, s). ПРИКЛАД 22 7-[(2-гідрокси-1,1-диметилетил)аміно]-5-[[(2-метил-4-тіазоліл)метил]тіо]-тіазоло[4,5-d]піримідин-2(3H)-OH (a) 2-[[2-аміно-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]-аміно]-2-метил-1-пропанол Виготовлено способом з етапу а) прикладу 18, використовуючи продукт з етапу с) прикладу 20 та 2-аміно2-метилпропанол. Т.пл. 250-252°С МС (АРСІ) 383 (М+Н, 100%). (b) 2-[[2-бром-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-2-метил-1-пропанол Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу а) прикладу 22. МС (АРСІ) 446 (М+Н+, 100%). (c) 2-[[2-метокси-5-[[(2-метил-4-тіазоліл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-2-метил-1-пропанол Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 22. МС (АРСІ) 39S (М+Н+, 100%). (d) 7-[(2-гідрокси-1,1-диметилетил)аміно]-5-[[(2-метил-4-тіазоліл)метил]тіо]-тіазоло[4,5-d]піримідин-2(3Н)-он Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу с) прикладу 22. Т.пл. 231-2°C МС (АРСІ) 384 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,36 (1Н, s), 7,37 (1Н, s), 6,61 (1Н, bs). 4,80 (1Н, t), 4,37 (2Н, s), 3,55 (2Н, d), 2,62 (3Н, s), 1,31 (6Н, s). ПРИКЛАД 23 7-[(2-гідрокси-1,1-диметилетил)аміно]-5-[[(2-метилфеніл)метил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-он. (a) 7-[(2-гідрокси-1,1-диметилетил)аміно]-5-[(фенілметил)сульфоніл]тіазоло[4,5-d]піримідин-2(3Н)-он. Перемішуваний розчин продукту з етапу g) прикладу 1 (0,14г) у льодяній оцтовій кислоті (30мл) обробляли пероцтовою кислотою (36/40% у оцтовій кислоті, 2мл), перемішували протягом 2 годин, далі при 50°С протягом 1 години. Розчин гасили надлишком диметилсульфіду та випарювали, одержавши смолу. МС (АРСІ) 395 (М+Н+, 100%). (b) 7-[(2-гідрокси-1,1-диметилетил)аміно]-5-[[(2-метилфеніл)метил)тіо]тіазоло-[4,5-d]піримідин-2(3Н)-он. Продукт з етапу (а) прикладу 23 переносили у диметилсульфоксид (1,73мл), обробляли бутоксидом калію та поділяли на 3 порції. Одну порцію обробляли 2-метилфенілметилмеркаптаном (0,053г), перемішували при 50°С протягом 1 години протягом 2 годин, нейтралізували льодяною оцтовою кислотою та піддавали препаративній ВЕРХ з оберненими фазами на симетричній колонці С8 розміром 19´50мм, використовуючи 1060% ацетонітрил у 0,1% водному ацетаті амонію протягом 6 хвилин при 20мл/хвилину, одержавши потрібну сполуку. МС (АРСІ) 377 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 1,33 (s, 6Н); 2,35 (s, 3Н); 3,57 (d, 2H); 4,33 (s, 2H); 4,82 (t, 1H); 6,57 (шир. s, 1Н); 7,12-7,20 (m, 3Н); 7,41 (d, 1Н); 12,37 (шир. s, 1Н) ПРИКЛАД 24 5-[(2-фуранілметил)тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он (a) 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(фeнілметил)сульфоніл]тіазоло[4,5-d]піримідин-2(3Н)-он. Потрібну сполуку виготовляли з продукту з етапу d) прикладу 3, використовуючи спосіб з етапу (а) прикладу 23. МС (ES) 381 (М+Н+, 100%). (b) 5-[(2-фуранілметил)тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло(4,5-d]піримідин-2(3H)-он Потрібну сполуку виготовляли з продукту з етапу (а) прикладу 24, використовуючи спосіб з етапу (b) прикладу 23, використовуючи фурфурилмеркаптан МС (АРСІ) 339 (М+Н+, 100%). ЯМР dΗ (d6-метанол) 1,12 (d, 3Н); 3,41-3,45 (m, 1Н); 3,49-3,53 (m, 1Н); 4,24-4,32 (m, 3Н); 6,18-6,22 (m, 2Н); 7,29 (шир. s, 1H). ПРИКЛАД 25 7-[[(1R)-2-аміно-1-метилетил]аміно]-5-[[(3-хлор-2-флуорфеніл)метил]тіо]тіазоло-[4,5-d]піримідин-2(3Н)-он (a) 9Н-флуорен-9-ілметиловий естер [(1R)-2-аміно-1-метил-2-оксоетил]-карбамової кислоти Розчин гідрохлориду D-аланінаміду (3г) у 10% розчині карбонату натрію (50мл) та діоксані (50мл) обробляли флуоренілметоксикарбонілхлоридом (6,24г) у діоксані (40мл) та перемішували протягом ночі. Суміш розбавляли водою (500мл) та продукт збирали фільтруванням і сушили у вакуумі, одержавши 9,0г потрібної сполуки. МС (ESI) ВР 311 (+Н) (b) 9Н-флуорен-9-ілметиловий естер [(1R)-2-аміно-1-метилетил]карбамової кислоти До розчину продукту з етапу а) прикладу 25 (6,9г) у ТГФ (100мл) додавали боран-метилсульфідний комплекс (4,4мл) та суміш гріли під зворотним холодильником протягом 2 годин. Суміш обережно гасили додаванням метанолу (100мл), випарювали досуха та залишок переносили у метанол (100мл).та підкислювали до рН1-2 концентрованою гідрохлоридною кислотою. Гріли під зворотним холодильником протягом 30 хвилин, а далі випарювали досуха. Залишок розтирали з ефіром, одержавши тверду речовину, яку збирали фільтруванням, розчиняли у воді та осаджували вільну основу додаванням водного розчину гідрокарбонату натрію, одержавши потрібну сполуку (3,1г). МС (ESI) ВР 297 (+Н) (c) 1,1-диметилетиловий естер (2R)-[2-(9Н-флуорен-9-ілметоксикарбоніламіно)-пропіл]карбамової кислоти. До перемішуваного розчину продукту з етапу b) прикладу 25 (3,0г) у ТГФ (100мл) додавали ди-третбутилдикарбонат (2,2г) та суміш перемішували при кімнатній температурі протягом 30 хвилин. Суміш випарювали досуха та сирий продукт очищали (SiO2, дихлорметан як елюент), одержавши потрібну сполуку (3,8г). ЯМР dН (CDCI 3) 7,76 (2Н, m), 7,42 (2Н, m), 7,39-26 (4Н, s), 5,01 (1Н, s), 4,85 (1Н, s), 4,38 (2Н, d), 4,19 (1Н, t), 3,77 (1Н, m), 3,18 (2Н, m), 1,27 (9Н, s). (d) 1,1-диметилетиловий естер [(2R)-2-амінопропіл]карбамової кислоти До розчину продукту з етапу с) прикладу 25 (3,8г) у ТГФ (100мл) додавали піперидин (5мл) та суміш залишали протягом 1 години при кімнатній температурі. Суміш випарювали досуха та залишок очищали (SiO2, 5% метанол:дихлорметан як елюент), одержавши потрібну сполуку як безбарвне масло (1,7г). ЯМР dΗ (CDCl3) 4,95 (1Н, s), 3,13 (1Н, m), 2,99 (1Н, m), 2,87 (1Н, m), 1,38 (9Н, s), 1,08 (3H, d). (e) 1,1-диметилетиловий естер [(2R)-2-[[2-аміно-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7іл]аміно]пропіл]карбамової кислоти Продукт 1 з етапу с) прикладу (2,0г) та продукт з етапу d) прикладу 25 (1,3г) у розчиннику Nметилпіролідинон (10мл), що містить основу Хуніга (3мл) гріли при 110°С протягом 10 годин. Суміш випарювали досуха та очищали (SiO2, (1:1) дихлорметан:етилацетат як елюент), одержавши потрібну сполуку (1,9г). МС (ESI) ВР 447 (+Н) (f) 1,1-диметилетиловий естер [(2R)-2-[[2-аміно-5-[(фенілметил)сульфоніл]-тіазоло[4,5-d]піримідин-7іл]аміно]пропіл]карбамової кислоти До розчину оксону (7,0г) у воді (400мл) додавали гідрокарбонат натрію до рН7,4. До цього розчину додавали розчин продукту з етапу e) прикладу 25 (1,9г) у ацетонітрилі (100мл) та суміш гріли при 40°С протягом 2 годин. Після завершення реакції ацетонітрил видаляли роторним випарюванням, одержавши потрібну сполуку (1,7г). МС (ESI) ВР 479 (+Н) (g) 3-хлор-2-флуор-бензолметантіол, Суміш 3-хлор-2-флуорбензилброміду (5,0г), тіосечовини (3,4г) у розчиннику етанол (200мл) гріли під зворотним холодильником протягом 16 годин. Суміш випарювали досуха та до залишку додавали розчин гідроксиду натрію (30г) у воді (300мл) та суміш гріли під зворотним холодильником протягом 1 години. Охолоджували до кімнатної температури та підкислювали концентрованою гідрохлоридною кислотою, продукт екстрагували у ефір, одержавши потрібну сполуку як масло (2,51г). ЯМР dН (CDCI 3) 7,32-21 (2Н, m), 7,04 (1Н, t), 3,75 (2Н, d), 1,90 (1Н, t). (h) 1,1-диметилетиловий естер [(2R)-2-[[2-аміно-5-[[(3-хлор-2-флуорфеніл)-метил]тіо]тіазоло[4,5d]піримідин-7-іл]аміно]пропіл]карбамової кислоти До суміші продукту з етапу f) прикладу 25 (1,2г), продукту з етапу g) прикладу 25 (1,6г) у змішаному розчиннику етанол (30мл) та диметилсульфоксид (5мл) додавали борогідрид натрію (100мг) та суміш гріли при 50°С протягом 2 годин. Етанол видаляли роторним випарюванням та сирий продукт екстрагували етилацетатом та промивали водою. Потрібну сполуку отримали очисткою (SiO2, 1:1 дихлорметан :етилацетат як елюент), одержавши (1,95г). МС (ESI) ВР 499 (+Н) (і) 1,1-диметилетиловий естер [(2R)-2-[[2-бром-5-[[(3-хлор-2-флуорфеніл)метил]-тіо]тіазоло[4,5d]піримідин-7-іл]аміно]пропіл]карбамової кислоти Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу h) прикладу 25. МС (АРСІ) 562 (М+Н+, 100%). (j) 1,1-диметилетиловий естер [(2R)-2-[[5-[[(3-хлор-2-флуорфеніл)метил]тіо]-2-метокситіазоло[4,5d]піримідин-7-іл]аміно]пропіл]карбамової кислоти Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу і) прикладу 25. МС (АРСІ) 514 (М+Н+, 100%). (k) 7-[[(1R)-2-аміно-1-метилетил]аміно]-5-[[(3-хлор-2-флуорфеніл)метил]тіо]-тіазоло[4,5-d]піримідин-2-(3Н)он Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу j) прикладу 25. Т.пл. 241-3°C МС (АРСІ) 400 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 7,56 (1Н, m), 7,49 (1Н, m), 7,17 (1Н, m), 7,05 (1Н, bs), 4,44 (1Н, m), 4,39 (2Н, ab), 2,92 (2Н, d), 1,13 (3Н, d). ПРИКЛАД 26 (2S)-2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2,3-дигідро-2-оксотіазоло[4,5-d]піримідин-7-іл]аміно]-3гідроксипропанамід (a) (2S)-2-[[2-аміно-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-3 гідроксипропанамід Потрібну сполуку виготовляли способом з етапу а) прикладу 2, використовуючи продукт з етапу b) прикладу 4 (2г, 6ммоль), 1-серинамід (0,66г, 6ммоль), N-метилпіролідинон (80мл), та діізопропілетиламін (2мл), одержавши потрібну сполуку (1,36г) Т.пл. 145-151°C МС (АРСІ) 413 (М+Н+), 100%). ЯМР dΗ (d6-диметилсульфоксид) 8,10 (2Н, brs), 7,40-7,07 (6Н, m), 4,57 (1Н, q), 4,43 (1H,d), 4,36(1 Η, d),3,71(2H,d). (b) (2S)-2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2,3-дигідро-2-оксотіазоло[4,5-d]-піримідин-7-іл]аміно]-3гідроксипропанамід Виготовлено послідовним використанням способів з етапів e), f), та g) прикладу 1, використовуючи продукт з етапу (а) прикладу 26. Сполуки, утворені протягом розділення, не були очищеними чи охарактеризованими. МС (АРСІ) 414 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,47 (1Н, Чи), 7,47 (1Н, br), 7,42 (1Н, s), 7,34 (2Н, m), 7,13 (1Н, 15m), 7,09 (1Н, s), 4,90 (1Н, t), 4,58 (1Н, m), 4,39 (2Н, m), 3,70 (2Н, m). ПРИКЛАД 27 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(2-тієнілметил)тіо]тіазоло(4,5-d]-піримідин-2(3Н)-он а) 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(2-тієнілметил)тіо]тіазоло[4,5-d]-піримідин-2(3Н)-он Потрібну сполуку виготовляли способом, описаним у прикладі 16 з етапу b) з продукту з етапу e) прикладу 15 (0,300г, 0,79ммоль) та 2-тіофенметантіолу (0,32мл, 3,9ммоль). Продукт отримали з низьким виходом 3% як білий ліофілат (0,010г). МС (АРСІ) 355 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,50 (1Н, be), 7,36 (1Н, m), 7,16 (1Н, bs), 7,07 (1Н, m), 6,92 (1Н, m), 4,72 (1Н, bs), 4,55 (2Н, d), 4,26 (1Н, m), 3,44 (2Н, m), 1,12 (3Н, d). ПРИКЛАД 28 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5[[[3-метил-4-(метилсульфоніл)феніл]метил]тіо]тіазоло[4,5d]піримідин-2(3Н)-он. a) 3-метил-4-(метилтіо)бензальдегід Хлорид стануму (IV) (13,6мл, 0,1166моль) додавали до охолодженого на бані лід-вода розчину 1-метил-2(метилтіо)бензолу (10г, 0,0733моль) у безводному дихлорметані (200мл) під азотом та перемішували протягом ще 2 годин при 0°С. Уводили a,a-дихлорметилметиловий етер (6,56мл, 0,073моль) та реакційну суміші перемішували протягом 1 години при температурі нижче 10°С перед припиненням охолодження. Після встановлення кімнатної температури реакційну суміші виливали у воду з льодом (400мл), перемішували та далі екстрагували дихлорметаном (´3). Поєднані органічні шари сушили безводним сульфатом магнію, фільтрували, концентрували на силікагелі та очищали імпульсною хроматографією, елююючи діетиловим етером/ізогексаном (10:1), одержавши потрібну сполуку як коричневе масло (6,54г) з виходом 54%. ГХ-МС 166 (М+, 100%). ЯМР dΗ (CDCI 3) 9,91 (1Н, s), 7,68 (1Н, m), 7,62 (1Н, s), 7,24 (1Н, t), 2,54 (3Н, s), 2,36 (3H,s). b) 3-метил-4-(метилтіо)бензолметанол Борогідрид натрію (1-40г, 0,037моль) додавали до охолодженого на бані лід-вода розчину продукту з етапу а) прикладу 28 (6,16г, 0,037моль) у етанолі (50мл). Через 1 годину, реакційну суміші нейтралізували обережним додаванням водної гідрохлоридної кислоти (2 молярна) та концентрували у вакуумі для видалення органічного розчиннику. Остаточний водний розчин далі екстрагували етилацетатом (´3). Поєднані органічні шари сушили безводним сульфатом магнію, фільтрували, та концентрували у вакуумі, одержавши потрібну сполуку як коричневе масло (6г) з кількісним виходом. ГХ-МС 168 (М+,100%). ЯМР dΗ (CDCI 3) 7,18 (3Н, m), 4,62 (2Н, bs), 2,46 (3Н, s), 2,33 (3Н, s). c) 3-метил-4-(метилсульфоніл)бензолметанол 3-хлорпероксибензойну кислоту (57-86%, 20,4г) перемішували у дихлорметані (150мл), сушили безводним сульфатом магнію та фільтрували. Фільтрат додавали краплями протягом 1 години до охолодженого на бані лід-вода перемішуваного розчину продукту з етапу b) прикладу 28 (5,67г, 0,034моль) у дихлорметані (50мл). Реакційну суміші фільтрували та фільтрат промивали водним розчином гідрокарбонату натрію, а потім водним розчином дитіоніту натрію (10г Na2O4S2 у 150мл води). Органічний шар сушили безводним сульфатом магнію, фільтрували, та концентрували у вакуумі перед очисткою імпульсною хроматографією, елююючи дихлорметаном/метанолом (100:2). Потрібну сполуку отримали як жовте масло (5,52г) з виходом 82%. МС (АРСІ) 201,1 (М+Н+, 94,3%). ЯМР dΗ (CDCI 3) 7,87 (1Н, d), 7,38 (2Н, m), 5,40 (1Н, q), 4,56 (2Н, d), 3,18 (3Н, s), 2,61 (3Н, s). d) 3-метил-4-(метилсульфоніл)бензолметантіолацетат Діетилазодикарбоксилат (4,33мл, 0,028моль) додавали до охолодженого на бані лід-вода розчину трифенілфосфіну (7,20г, 0,028моль) у тетрагідрофурані (40мл). В утворену суспензію додавали розчин продукту з етапу с) прикладу 28 (5,5г, 0,028моль) у тетрагідрофурані (20мл). Після розчинення осаду, тіолоцтову кислоту додавали до розчину реакційної суміші та видаляли охолодження. Через 16 годин витримки при кімнатній температурі реакційну суміш концентрували на силікагелі та очищали імпульсною хроматографією, елююючи ізогексаном/етилацетатом (2:1). Потрібну сполуку отримали як рожеву тверду речовину (2,46г) з виходом 35%. ЯМР dΗ (d6-диметилсульфоксид) 7,84 (1Н, d), 7,36 (2Н, m), 4,16 (2Н, s), 3,19 (3Н, s), 2,61 (3Н, s), 2,37 (3Н, s). e) біс[[3-метил-4-(метилсульфоніл)феніл]метил]дисульфід Суміш продукту з етапу d) прикладу 28 (1,98г, 7,66ммоль) та 7 молярного метанольного аміаку (30мл) перемішували протягом 24 годин. Продукт осаджували розчину як білу тверду речовину та виділяли фільтруванням та сушили у вакуумі. Фільтрат подібно обробляли 7 молярним аміаком у метанолі та одержали другу порцію білого твердого продукту. Загалом, потрібну сполуку отримали з виходом 32% (0,534г). МС (АРСІ) 451 (M+NH4+, 98,9%). ЯМР dΗ (d6-диметилсульфоксид) 7,88 (2Н, s), 7,38-7,34 (4Н, m), 3,88 (4Н, s), 3,20 (6Н, s), 2,64 (6Н, s). f) 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[[[3-метил-4-(метилсульфоніл)-феніл]метил]тіо]тіазоло[4,5d]піримідин-2(3Н)-он Потрібну сполуку виготовляли способом з етапу b) прикладу 16, використовуючи продукт з етапу e) прикладу 15 (0,20г, 0,53ммоль) та продукт з етапу e) прикладу 28 (0,34г, 0,79ммоль), одержавши 11% продукту як білий ліофілат (0,025г). МС (АРСІ) 441 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,40 (1Н, s), 7,81 (1Н, d), 7,52 (2Н, m), 7,33 (1Н, d), 4,74 (1Н, t), 4,35 (2Н, s), 4,19 (1Н, m), 3,41 (1Н, m), 3,34-3,28 (1Н, m), 3,18 (3Н, s), 2,61 (3Н, s), 1,08 (3H,d). ПРИКЛАД 29 5-[[[3-хлор-4-(трифлуорметокси)феніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5d]піримідин-2(3Н)-он a) 3-хлор-4-(трифлуорметокси)бензолметантіол До розчину 3-хлор-4-(трифлуорметокси)бензилброміду (5г) у етанолі (100мл) додавали тіосечовину (5г) та суміш гріли під зворотним холодильником протягом 2 годин. Суміш випарювали досуха та залишок переносили у воду (100мл). До цього розчину додавали гранули гідроксиду натрію (3г) та суміш гріли під зворотним холодильником протягом 1 години. Суміші давали охолонути до кімнатної температури та підкислювали концентрованою гідрохлоридною кислотою, суміш екстрагували ефіром, сушили та випарювали, одержавши потрібну сполуку як білу воскоподібну тверду речовину (3,5г). ЯМР dН (CDCI 3) 7,35-7,09 (3Н, m), 3,58 (2Н, s). b) 5-[[[3-хлор-4-(трифлуорметокси)феніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5d]піримідин-2(3Н)-он Потрібну сполуку виготовляли способом, описаним у прикладі 16 з етапу b), використовуючи продукт з етапу e) прикладу 15 (0,40г, 1,05ммоль) та продукт з етапу а) прикладу 29 (0,71г, 1,5ммоль), одержавши 10% продукту як білий ліофілат (0,046г). МС (АРСІ) 467 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,42 (1Н, s), 7,75 (1Н, m), 7,52 (2Н, m), 7,43 (1Н,d), 4,72 (1Н, t), 10 4,34 (2Н, d), 4,18 (1Н, квінтет), 3,46-3,27 (2Н, m), 1,07 (3Н, d). ПРИКЛАД 30 5-[[[2-флуор-3-(трифлуорметил)феніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5d]піримідин-2(3Н)-он a) 2-флуор-3-(трифлуорметил)бензолметантіол Потрібну сполуку виготовляли з 2-флуор-(3-трифлуорметил)бензилброміду (10г), використовуючи спосіб з етапу а) прикладу 29. ЯМР dΗ (CDCI 3) 7,68-7,18 (3Н, m), 3,74 (2Н, s), 1,98 (1Н, s). b) 5-[[[2-флуор-3-(трифлуорметил)феніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5d]піримідин-2(3Н)-он Потрібну сполуку виготовляли способом, описаним у прикладі 16 з етапу b), використовуючи продукт з етапу e) прикладу 15 (0,47г, 1,23ммоль) та продукт з етапу а) прикладу 30 (0,775г, 3,7ммоль), одержавши 5% продукту як білий ліофілат (0,025г). МС (АРСІ) 435 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,42 (1Н, s), 7,92 (1Н, t), 7,68 (1Н, t), 7,35 (2Н, m), 4,71 (1Н, bs), 4,42 (2Н, m), 4,16 (1Н, квінтет), 3,40-3,30 (2Н, m), 1,07 (3Н, d). ПРИКЛАД 31 Моногідрохлорид 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[2-[(диметиламіно)етил]-аміно]тіазоло[4,5d]піримідин-2(3Н)-ону (a) 2-бром-7-хлор-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин Продукт з етапу (b) прикладу 4 (8,0г) суспендували у бромоформі (200мл), а потім додавали третбутилнітрит (8мл) та все це гріли при 60°С протягом 30 хвилин. Розчинники видаляли під зниженим тиском та залишок очищали хроматографією на колонці (діоксид силіцію, 1:1 дихлорметан/ізогексан), одержавши жовту тверду речовину (5,6г). МС (АРСІ) 409/411 (М+Н, 100%). (b) 7-хлор-5-[(2,3-дифлуорфенілметил)тіо]-2-метокситіазоло[4,5-d]піримідин Продукт з етапу а) (5,6г) прикладу 31 суспендували у метанолі (150мл) та додавали порошок гідроксиду калію (0,77г). Все це перемішували при кімнатній температурі протягом 2 годин. рН суміші доводили до 7 кількома краплями концентрованої гідрохлоридної кислоти перед її випарюванням досуха. Очищали хроматографією на колонці (діоксид силіцію, 3:2-1:1 ізогексан/дихлорметан), одержавши білу речовину (2,0г). МС (АРСІ) 360/362 (М+Н, 100%). (c) 7-хлор-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2(3Н)-он Продукт з етапу (b) прикладу 31 (2,0г) розчиняли у діоксані (150мл), а потім додавали концентровану гідрохлоридну кислоту (1мл) та воду (1мл) і все це гріли при 40°С протягом 67 годин. Суміш випарювали досуха та очищали хроматографією на колонці (діоксид силіцію, дихлорметан), одержавши білу речовину (1,4г). МС (АРСІ) 346/348 (М+Н, 100%). (d) Моногідрохлорид 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[2-[(диметиламіно)-етил]аміно]тіазоло[4,5 d]піримідин-2(3Н)-ону Продукт з етапу (с) прикладу 31 (1,4г) розчиняли у сухому тетрагідрофурані (5мл) та до розчину додавали Ν,Ν-диметилетилендіамін (0,25г) у балоні, який гріли при 80°С протягом 24 годин. Розчинники видаляли під зниженим тиском та залишок розподіляли між етилацетатом та розсолом. Поєднані органічні екстракти сушили сульфатом натрію та випарювали під зниженим тиском для наступної очистки залишку хроматографією на колонці (діоксид силіцію, 5:1 етилацетат/метанол), одержавши вільну основу як липку речовину (0,095г). Це перетворювали у моногідрохлорид суспендуванням твердої речовини у метанолі (10мл), а потім додаванням концентрованої гідрохлоридної кислоти (3 краплі) для забезпечення розчинення, а далі води (100мл) для сублімаційної сушки сполуки, одержавши коричневий порошок (0,080г). Т.пл. 263°С(розкл.) МС (АРСІ) 398 (М+Н, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,57 (1Н, s), 10,22 (1Н, s), 7,94 (1Н, t), 7,40 (1Н, m), 7,34 (1Н, m), 7,16 (1Н, m), 4,43 (2Н, s), 3,78 (2Н, s), 3,21 (2Н, m), 2,78 (6Н, d) ПРИКЛАД 32 5-[[(2-флуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он (a) 2-[(2-аміно-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно)-(2R)-1-пропанол Продукт з етапу с) прикладу 1 (25,0г), D-аланінол (12,3г) та діізопропілетиламін (26,0г) розбавляли у Nметилпіролідиноні (250мл) та перемішували при 100°С протягом 24 годин перед охолодженням та виливали реакційну суміші у воду (2,5л). Осад фільтрували та сушили у вакуумі перед його попередньою абсорбцією на силікагелі. Хроматографія, використовуючи ЕtOАс 4% МеОН/ЕtOАс як елюент, дала потрібний продукт як жовту тверду речовину (9,0г. 32%). МС (АРСІ) 347 (М+Н, 100%). (b) 2-[(2-аміно-5-меркаптотіазоло[4,-d]піримідин-7-іл)аміно]-(2R)-1-пропанол Натрій металевий додавали порціями до розчину продукту з етапу а) прикладу 32 (5,0г) у аміаку (150мл) до стійкого блакитного кольору. Амонію хлорид далі додавали та розчиннику давали випаритися. Залишок розчиняли у воді (200мл) та фільтрували перед нейтралізацією 2М розчином HCL. Сірий осад фільтрували, промивали водою (200мл) та сушили у вакуумі протягом 48 годин, одержавши потрібну сполуку як коричневу речовину (3,0г). МС (АРСІ) 258 (М+Н, 100%). (c) 2-[(2-аміно-5-[[(2-флуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол 2-флуорбензилбромід (0,369г) додавали порціями до розчину продукту з етапу b) прикладу 32 (0,5г) та діізопропілетиламіну (0,26г) у диметилсульфоксиді/N-метилпіролідиноні (4мл/0,5мл) при 50°С та перемішування продовжували протягом 1 години. Суміш розподіляли між водою (200мл) та ЕtOАс (120мл). Органічну фазу збирали та промивали ще водою (200мл), сушили сульфатом магнію та концентрували на силікагелі. Потрібну сполуку очищали імпульсною хроматографією, використовуючи дихлорметан, а потім ЕtOАс як елюенти, одержавши білу речовину (245мг, 35%). МС (АРСІ) 366 (М+Н, 100%) (d) 2-[[2-бром-5-[[(2-флуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Ізоамілнітрит (0,3мл) додавали до суспензії продукту з етапу с) прикладу 32 (0,23г) у бромоформі (15мл) та ацетонітрилу (15мл) при 50°С. Перемішування продовжували протягом 30 хвилин перед концентруванням приблизно до 3мл. Залишок очищали хроматографією на колонці, використовуючи 20% ЕtOАс/дихлорметан як елюент, одержавши потрібну сполуку як жовту тверду речовину (102мг, 38%). МС (АРСІ) 429 (М+Н, 100 %). (e) 2-[[5-[[(2-флуорфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Гідроксид калію (27мг) додавали до розчину продукту з етапу d) прикладу 32 (0,1г) у МеОН (10мл). Суміш перемішували протягом 24 годин перед нейтралізацією до рН7 2М розчином НСІ. Летючі речовини видаляли у вакуумі та продукт використовували безпосередньо у наступному етапі. МС (АРСІ) 381 (М+Н, 100 %). (f) 5-[[(2-флуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло-[4,5d]піримідин-2(3Н)-он Продукт з етапу e) прикладу 32 розчиняли у 1,4-діоксані (50мл), воді (1мл) та концентрованому розчині НСІ (0,5мл) та перемішували протягом 20 годин при 40°С. Летючі речовини видаляли під зниженим тиском та сирий продукт очищали препаративною ВЕРХ, отримавши потрібну сполуку як білу тверду речовину (21мг). МС (АРСІ) 367 (М+Н, 100 %) ЯМР dΗ (d6-диметилсульфоксид) 12,40 (1Н, s), 8,14-7,11 (5Н, m), 4,72 (1Н, t), 4,35 (2Н, m), 4,22 (1 Н, m), 3,47-3,29 (2Н, m), 1,10 (3Н, d) ПРИКЛАД 33 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[[(2-метоксифеніл)метил]тіо]тіазоло-[4,5-d]піримідин-2(3H)-он (а) 2-[[2-аміно-5-[[(2-метоксифеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу с) прикладу 32, використовуючи продукт з етапу b) прикладу 32. МС (АРСІ) 378 (М+Н+, 100%). (b) 2-[(2-бром-5-[[(2-метоксифеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу d) прикладу 32, використовуючи продукт з етапу а) прикладу 33. МС (АРСІ) 441 (М+Н+, 100%). (c) 2-[[2-метокси-5-[[(2-метоксифеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу e) прикладу 32, використовуючи продукт з етапу b) прикладу 33. МС (АРСІ) 393 (М+Н+, 100%). (d) 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[[(2-метоксифеніл)метил]тіо]тіазоло-[4,5-d]піримідин-2(3Н)-он Виготовлено способом з етапу f) прикладу 32, використовуючи продукт з етапу с) прикладу 33. МС (АРСІ) 379 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 7,40 (1Н, dd), 7,22 (1Н, dt), 6,97 (1Н, d), 6,84 (1Н, dt), 6,00 (1Н, d), 4,25 (2Н, m), 4,15 (1Н, m), 3,83 (3Н, s), 3,48-3,31 (2Н, m), 1,10 (3Н, d). ПРИКЛАД 34 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(2-феноксіетил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-он (а) 2-[[2-аміно-5-[(2-феноксіетил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу с) прикладу 32, використовуючи продукт з етапу b) прикладу 32. МС (АРСІ) 378 (М+Н+, 100%). (b) 2-[(2-бром-5-[[(2-феноксіетил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу d) прикладу 32, використовуючи продукт з етапу а) прикладу 34. МС (АРСІ) 441 (М+Н+, 100%). (c) 2-[[2-метокси-5-[(2-феноксіетил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу e) прикладу 32, використовуючи продукт з етапу b) прикладу 34. МС (АРСІ) 393 (М+Н+, 100%). (d) 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(2-феноксіетил)тіо]тіазоло[4,5-d]-піримідин-2(3Н)-он Виготовлено способом з етапу f) прикладу 32, використовуючи продукт з етапу с) прикладу 34. МС (АРСІ) 379 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 12,37 (1Н, s), 7,30-7,26 (3Н, m), 6,96-6,91 (3Н, m), 4,71 (1Н, t), 15 4,2,34,14 (3Н, m), 3,46-3,28 (4Н, m), 1,08 (3Н, d) ПРИКЛАД 35 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[[(3-метилфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2(3Н)-он (а) 2-[[2-аміно-5-[[(3-метилфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу с) прикладу 32, використовуючи продукт з етапу b) прикладу 32. МС (АРСІ) 362 (М+Н+, 100%). (b) 2-[[2-бром-5-[[(3-метилфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу d) прикладу 32, використовуючи продукт з етапу а) прикладу 35. МС (АРСІ) 425 (М+Н+, 100%). (с) 2-[[2-метокси-5-[[(3-метилфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу e) прикладу 32, використовуючи продукт з етапу b) прикладу 35. МС (АРСІ) 377 (М+Н+, 100%). (d) 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[[(3-метилфеніл)метил]тіо]тіазоло[4,5-d]піримідин-2(3H)-он Виготовлено способом з етапу f) прикладу 32, використовуючи продукт з етапу с) прикладу 35. МС (АРСІ) 363 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 12,37 (1Н, s), 7,2,3-7,16 (4Н, m), 7,04 (1Н, d), 4,73 (1Н, t), 4,28 (2Н, m), 4,24 (1Н, m), 3,48-3,30 (2Н, m), 2,28 (3Н, s), 1,11 (3Н, d). ПРИКЛАД 36 5-[[(2-флуор-3-метилфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]-тіазоло[4,5-d]піримідин-2(3Н)он (a) 2-[[2-аміно-5-[[(2-флуор-3-метилфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]-аміно]-(2R)-1-пропанол Виготовлено способом з етапу с) прикладу 32, використовуючи продукт з етапу b) прикладу 32. МС (АРСІ) 380 (М+Н+, 100%). (b) 2-[[2-бром-5-[[(2-флуор-3-метилфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]-аміно]-(2R)-1-пропанол Виготовлено способом з етапу d) прикладу 32, використовуючи продукт з етапу а) прикладу 36. МС (АРСІ) 443 (М+Н+, 100%). (с) 2-[[5-[[(2-флуор-3-метилфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу e) прикладу 32, використовуючи продукт з етапу b) прикладу 36. МС (АРСІ) 395 (М+Н+, 100%). (d) 5-[[(2-флуор-3-метилфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метиле-тил]аміно]тіазоло[4,5-d]піримідин2(3Н)-он Виготовлено способом з етапу f) прикладу 32, використовуючи продукт з етапу с) прикладу 36. МС (АРСІ) 381 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,39 (1Н, s), 7,37-7,00 (4Н, m), 4,72 (1Н, t), 4,33 (2Н, m), 4,22 (1Н, m), 3,47-3,30 (2Н, m). 2,23 (3Н, s), 1,11 (3Н, d) ПРИКЛАД 37 5-[[(3-хлорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он (а)2-[[2-аміно-5-[[(3-хлорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу с) прикладу 32, використовуючи продукт з етапу b) прикладу 32. МС (АРСІ) 382 (М+Н+, 100%). (b) 2-[[2-бром-5-[[(3-хлорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу d) прикладу 32, використовуючи продукт з етапу а) прикладу 37. МС (АРСІ) 445 (М+Н+, 100%). (c) 2-[(5-[[(3-хлорфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу e) прикладу 32, використовуючи продукт з етапу b) прикладу 37. S (АРСІ) 397 (М+Н+, 100%). (d) 5-[[(3-хлорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он Виготовлено способом з етапу f) прикладу 32, використовуючи продукт з етапу с) прикладу 37. МС (АРСІ) 383 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,40 (1Н, s), 7,49 (1Н, d), 7,43-7,30 (4Н, m), 4,72 (1Н, t), 4,32 15 (2Н, m), 4,21 (1Н, m), 3,48-3,26 (2Н, m), 1,09 (3Н, d). ПРИКЛАД 38 5-[[(3-бромфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]-піримідин-2(3Н)-он (а) 2-[[2-аміно-5-[[(3-бромфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу с) прикладу 32, використовуючи продукт з етапу b) прикладу 32. МС (АРСІ) 426 (М+Н+, 100%). (b) 2-[[2-бром-5-[[(3-бромфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу d) прикладу 32, використовуючи продукт з етапу а) прикладу 38. МС (АРСІ) 491 (М+Н+, 100%). (c) 2-[[5-[[(3-бромфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу e) прикладу 32, використовуючи продукт з етапу b) прикладу 38. МС (АРСІ) 443 (М+Н+, 100%). (d) 5-[[(3-бромфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он Виготовлено способом з етапу f) прикладу 32, використовуючи продукт з етапу с) прикладу 38. МС (АРСІ) 427 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,40 (1Н, s), 7,63 (1Н, t), 7,46-7,24 (4Н, m), 4,72 (1Н, t), 4,31 (2Н, m), 4,21 (1Н, m), 3,48-3,26 (2Н, m), 1,10 (3Н, d) ПРИКЛАД 39 5-[[[4-(дифлуорметокси)феніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло [4,5-d]піримідин2(3Н)-он (a) 2-[[2-аміно-5-[[[4-(дифлуорметокси)феніл]метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу с) прикладу 32, використовуючи продукт з етапу b) прикладу 32. МС (АРСІ) 414 (М+Н+, 100%). (b) 2-[[2-бром-5-[[[4-(дифлуорметокси)феніл]метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу d) прикладу 32, використовуючи продукт з етапу а) прикладу 39. МС (АРСІ) 477 (М+Н+, 100%). (c) 2-[[5-[[[4-(дифлуорметокси)феніл]метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1пропанол Виготовлено способом з етапу у) прикладу 32, використовуючи продукт з етапу b) прикладу 39. МС (АРСІ) 429 (М+Н+, 100%). (d) 5-[[[4-(дифлуорметокси)феніл]метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин2(3Н)-он Виготовлено способом з етапу f) прикладу 32, використовуючи продукт з етапу с) прикладу 39. МС (АРСІ) 415 (М+Н+, 100%). ЯМР dН (d6-диметилсульфоксид) 12,38 (1Н, s), 7,48 (2Н, dt), 7,26 (1Н, d), 7,19 (1Η, t), 7,11 (2Н, 15 dd), 4,73 (1Н, t), 4,31 (2Н, m), 4,21 (1Н, m), 3,47-3,30 (2Н, m), 1,10 (3Н, d) ПРИКЛАД 40 (+/-)-5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-гідрокси-1-(метоксиметилетил]аміно]-тіазоло[4,5-d]піримідин2(3Н)-он (a) Гідрохлорид (+/-)-2-аміно-3-метокси-1-пропанолу До суспензії DL-3-метокси-аланіну (1,0г) у сухому ТГФ (100мл) додавали комплекс боран-метилсульфід (10мл) та суміш гріли під зворотним холодильником протягом 16 годин. Суміш далі гасили метанолом під зворотним холодильником, випарювали досуха та залишок переносили у метанольний гідрогенхлорид (100мл) та гріли під зворотним холодильником протягом ще 2 годин, випарювали досуха, одержавши потрібну сполуку як безбарвну смолу (1,0г). ЯМР dН (D2O) 3,40 (3Н, s), 3,53-3,74 (4Н, m), 3,81 (1Н, m) (b) (+/-)-2-[[2-аміно-5-[І(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл] аміно]-3-метокси-1пропанол, Виготовлено способом з етапу а) прикладу 12, використовуючи продукт з етапу b) прикладу 4 та продукт з етапу а) прикладу 40. МС (АРСІ) 414 (М+Н+, 100%). (c) (+/-)-2-[[2-хлор-5-[[(2,3-дифлуорфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]-аміно]-3-метокси-1пропанол, До розчину продукту з етапу b) прикладу 40 (1,0г) у суміші концентрованої гідрохлоридної кислоти (40мл) та води (32мл), що охолоджено у льодяній воді, додавали розчин нітриту натрію (0,4г) у воді (5мл) і перемішували при цій температурі протягом 2 годин. Суміш далі екстрагували етилацетатом, сушили та випарювали, одержавши потрібну сполуку (0,6г). МС (АРСІ) 434 (М+ІТ, 100%). (d) (+/-)-2-[[5-[[(2,3-дифлуорфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7-іл]аміно]-3-метокси-1пропанол, Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу с) прикладу 40. МС (АРСІ) 429 (М+Н+, 100%). (e) (+/-)-5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-гідрокси-1-(метоксиметил)етил]-аміно]тіазоло[4,5d]піримідин-2(3Н)-он Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу d) прикладу 40. МС (АРСІ) 415 (М+Н+, 100%). ПРИКЛАД 41 7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]-піримідин-2(3Н)-он (a) 2-[[2-аміно-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1,3-пропандіол Виготовлено способом з етапу а) прикладу 12, використовуючи продукт з етапу с) прикладу 1 та 2-аміно1,3-пропандіол. МС (АРСІ) 364 (М+Н+,100%). ЯМР dН (d6-диметилсульфоксид) 7,42-7,38 (1Н, m), 7,28 (1Н, t), 7,22 (1Н, t), 5,30 (1Н, d), 4,63 (1Н, bs), 4,28 (2Н, s),4,03 (1Н, m),3,54-3,40 (4Н, m). (b) 2-[(2-хлор-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно)-1,3-пропандіол, Виготовлено способом з етапу с) прикладу 40 та продукту з етапу а) прикладу 41 МС (АРСІ) 384 (М+Н+, 100%). (с) 2-[[2-ацетокси-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1,3-пропандіол Виготовлено способом з етапу f) прикладу 1 та продукту з етапу b) прикладу 41. МС (АРСІ) 379 (М+Н+, 100%). (d) 7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-он Виготовлено способом з етапу g) прикладу 1 та продукту з етапу с) прикладу 41. МС (АРСІ) 365 (М+Н+, 100%). ПРИКЛАД 42 5-[[(2-бромфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3H)-он (a) 2-[[2-аміно-5-[[(2-бромфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу с) прикладу 32, використовуючи продукт з етапу b) прикладу 32. МС (АРСІ) 428 (М+Н+, 100%). (b) 2-[[2-бром-5-[[(2-бромфеніл)метил]тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу e) прикладу 1, використовуючи продукт з етапу а) прикладу 42. МС (АРСІ) 491 (М+Н+, 100%). (c) 2-[[5-[[(2-бромфеніл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7-іл]аміно]-(2R)-1-пропанол Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 42. МС (АРСІ) 443 (М+Н+, 100%). (d) 5-[[(2-бромфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазоло[4,5-d]піримідин-2(3Н)-он Виготовлено способом з етапу д) прикладу 1, використовуючи продукт з етапу с) прикладу 42. МС (АРСІ) 427 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,41 (1Н, s), 7,65-7,14 (5Н, m), 4,72 (1Н, t), 4,42 (2Н, s), 4,21 (1Н, m), 3,47-3,30 (2Н, m), 1,10 (ЗН, d) ПРИКЛАД 43 Сіль 5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]тіазо-ло[4,5-d]піримідин-2(3Н)ону з натрієм Продукт з етапу d) прикладу 5 суспендували у воді та до цієї суспензії додавали 1 еквівалент 0,1Η розчину гідроксиду натрію, а потім додавали невелику аліквоту тетрагідрофурану для полегшення розчинення. Утворений розчин далі ліофізували, одержавши потрібну сполуку як безбарвну тверду речовину. Т.пл. 218-220°С МС (АРСІ) 385 (М+Н+, 100%). ЯМР dΗ (d6-ДМСО) 7,39-7,09 (3Н, m), 5,60-(1Н, d), 4,65 (1Н, m), 4,34 (2Н, q), 4,09 (1Н, m), 3,44-3,27 (2H,m),1,06 (3Н, d). ПРИКЛАД 44 Сіль 5-[(3-хлор-2-флуорфеніл)метил]тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]-тіазоло[4,5-d]піримідин2(3Н)-ону з натрієм Виготовлено як у прикладі 43, використовуючи продукт з етапу b) прикладу 17. МС (АРСІ) 401 (М+Н+, 100%). ПРИКЛАД 45 Сіль (+/-)-5-[[(2,3-дифлуорфеніл)метил]тіо]-7-[[2-гідрокси-1-(метоксиметил)етил]-аміно]тіазоло[4,5d]піримідин-2(3Н)-ону з натрієм Виготовлено способом з прикладу 43, використовуючи продукт з етапу e) прикладу 40. Т.пл. >250°С МС (АРСІ) 415 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 7,39-7,04 (3Н, m), 5,51 (1Н, d), 4,68 (1Н, t), 4,34 (2Н, q), 4,22 (1Η, m), 3,513,35 (4Н, m), 3,32 (3Н, s). ПРИКЛАД 46 Сіль 7-[[2-гідрокси-1-(гідроксиметил)етил]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]піримідин-2(3Н)-ону з натрієм Виготовлено способом з прикладу 43, використовуючи продукт з етапу d) прикладу 41. МР 231-2°С МС (АРСІ) 365 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 7,41-7,18 (5Н, m), 5,30 (1Н, d), 4,63 (2Н, s), 4,28 (2Н, s), 4,06 (1Н, m), 3,50 (4Н, m). ПРИКЛАД 47 Сіль 7-[[(1R)-2-гідрокси-1-метилетил]аміно]-5-[(фенілметил)тіо]тіазоло[4,5-d]-піримідин-2(3Н)-ону з натрієм Виготовлено способом з прикладу 43, використовуючи продукт з етапу d) прикладу 3. Т.пл. (всихає 110) плавиться 221 -225°С МС (АРСІ) 349 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 7,41-7,18 (5Н, m), 5,58 (1Н, d), 4,65 (1Н, t), 4,28 (2Н, q), 4,11 (1Н, m), 3,493,31 (2Н, m), 1,08 (3Н, d). ПРИКЛАД 48 5-[(5-хлор-1,2,3-тіадіазол-4-іл)тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]-тіазоло[4,5-d]піримідин-2(3H)-он, (а) (2R)-2-[[2-аміно-5-[(5-хлор-1,2,3-тіадіазол-4-іл)тіо]тіазоло[4,5-d]піримідин-7-іл]аміно]-1-пропанол Виготовлено способом з етапу с) прикладу 32, використовуючи продукт з етапу b) прикладу 32 та 5-хлор4-(хлорметил)-1,2,3-тіадіазол. МС (АРСІ) 390 (М+Н+, 100%). (b) (2R)-2-[[2-хлор-5-[[(5-хлор-1,2,3-тіадіазол-4-іл)метил)тіо]тіазоло(4,5-d]піримідин-7-іл]аміно]-1-пропанол Виготовлено способом з етапу с) прикладу 40, використовуючи продукт з етапу а) прикладу 48 МС (АРСІ) 409 (М+Н+, 100%). (с) (2R)-2-[[5-[[(5-хлор-1,2,3-тіадіазол-4-іл)метил]тіо]-2-метокситіазоло[4,5-d]піримідин-7-іл]аміно]-1пропанол Виготовлено способом з етапу f) прикладу 1, використовуючи продукт з етапу b) прикладу 48. МС (АРСІ) 405 (М+Н+, 100%). (d) 5-[(5-хлор-1,2,3-тіадіазол-4-іл)тіо]-7-[[(1R)-2-гідрокси-1-метилетил]аміно]-тіазоло[4,5-d]піримідин-2(3Н)он, Виготовлено способом з етапу g) прикладу 1, використовуючи продукт з етапу с) прикладу 48. МС (АРСІ) 391 (М+Н+, 100%). ЯМР dΗ (d6-диметилсульфоксид) 12,39 (1Н, s), 7,39 (1Н, d), 4,76 (2Н, АВ), 4,70 (1Н, t), 4,24 (1Н, m), 3,483,30 (2Н, m), 1,11 (3Н, d) Фармакологічні результати Аналіз зв'язування з лігандами [125І]ІL-8 (людини, рекомбінантний) отримали від Amersham, U.K. зі специфічною активністю 2000Кі/ммоль. Усі інші хімікати були аналітичної якості. Високі рівні hrCXCR2 було експресовано у клітинах НЕК 293 (клітини нирок ембріона людини 293 ЕСАСС №85120602) (Lee et al. 0992; J.Biol. Chem. 267 рр.16283-16291). кДНК hrCXCR2 ампліфікували та клонували з нейтрофільної мРНК людини. ДНК клонували у PCRScript (Stratagene) та клони ідентифікували, використовуючи ДНК. Кодувальні послідовності субклонували у евкаріотний експресійний вектор RcCMV (Invitrogen). Плазмідну ДНК виготовляли, використовуючи Quiagen Megaprep 2500 та трансфектували у клітини НЕК 293, використовуючи реагент Lipofectamine (Gibco BRL). Клітини найкраще експресуючого клону збирали у буферований фосфатом сольовий розчин, що містить 0,2% (за масою/об'ємом) (EDTA) та центрифугували (200g, 5 хвилин). Гранули клітин ресуспендували у льодяному гомогенізаційному буфері [10мМ ГЕПЕС (рН7,4), 1мМ дитіотреїтолу, 1мМ EDTA та панель інгібіторів протеази (1мМ фенілметилсульфонілфлуорид, 2мкг/мл інгібітору трипсину сої, 3мМ бензамідину, 0,5мкг/мл лейпептину та 100мкг/мл бацитрацину)] та клітини залишали рости протягом 30 хвилин. Виготовлення клітин припиняли, використовуючи ручний гомогенізатор зі ступки/PTFE пестику та мембрани клітин збирали центрифугуванням (45 хвилин, 100000g, 4°С). Мембранний препарат зберігали при -70°С у гомогенізаційному буфері з доданим розчином солі Тироде (137мМ NaCI, 2,7мМ KСІ, 0,4мМ NaH2PO4, 0,1% (за масою/об'ємом) желатину та 10% (за об'ємом) гліцерину. Усі дослідження проводили у 96-коміркових фільтрувальних планшетах MultiScreen 0,45мкм (Millipore, U.K.). Кожне дослідження включало приблизно 50пМ [125l]IL-8 та мембрани (еквівалент приблизно 200000 клітин) у буфері для дослідження [розчин солі Тироде з доданими 10мМ ГЕПЕС (рН7,4), 1,8мМ СаСІ 2, 1мМ MgСІ 2 0,125мг/мл бацитрацину та 0,1% (за масою/об'ємом) до досягнення кінцевої концентрації диметилсульфоксиду 1% (за об'ємом). Дослідження ініціювали додаванням мембран та через 1,5 години при кімнатній температурі мембрани збирали фільтруванням, використовуючи вакуумний колектор Millipore MultiScreen та промивали двічі буфером для дослідження (без бацитрацину). Нижній планшет видаляли від планшетного набору MultiScreen, фільтри сушили при кімнатній температурі, вибивали та лічили на лічильнику Cobra. Сполуки формули (І) згідно з прикладами, як виявлено, мають величину ІK50 менше 10мкМ. Дослідження інтрацелюлярної мобілізації кальцію Нейтрофіли людини виготовляли з обробленої EDTA периферійної крові, як раніше описано (Baly et al. (1997) Methods in Enzymology, 287, рр.70-72), у накопичувальному буфері [розчин солі Тироде (137мМ NaCI, 2,7мМ KСІ, 0,4мМ NaH2PO4, доповнений 5,7мМ глюкозою та 10мМ ГЕПЕС (рН7,4)]. Хемокін GR-Oa (людини, рекомбінантний) одержали від R&D Systems (Abingdon, U.K.). Усі інші хімікати були аналітичної якості. Зміни інтрацелюлярного вільного кальцію вимірювали флуорометрично завантаженням нейтрофілів чутливим до кальцію флуоресцентним барвником, fluo-3, як описано раніше [Merritt et al. (1990) Biochem. J., 11 269, pp.513-519]. Клітини завантажували протягом 1 години при 37°С у завантажувальному буфері (накопичувальний буфер з 0,1% (за масою/об'ємом) желатину), що містить 5мкМ естеру fluo-3 AM, промивали завантажувальним буфером та ресуспендували у розчині солі Тироде, доповненому 5,7мМ глюкози, 0,1%(за масою/об'ємом) альбуміну коров'ячої сироватки (BSA), 1,8мМ СаСІ 2 та 1мМ MgСІ2. Клітини піпетували у 96-коміркових мікропланшетах з чорними стінками, прозорим дном, (Costar, Boston, U.S.A.) та центрифугували (200g, 5 хвилин, кімнатна температура). Сполуку формули (І) згідно з прикладами попередньо розчиняли у диметилсульфоксиді та додавали до кінцевої концентрації диметилсульфоксиду 0,1% (за об'ємом). Дослідження ініціювали додаванням концентрації GROa A50 та тимчасове зростання флуоресценції fluo-3 (lEx=490нм та l Em=520нм) відстежували, використовуючи флуориметр FLIPR (Fluorometric Imaging Plate Reader, Molecular Devices, Sunnyvale, U.S.A.). Сполуки формули (І) згідно з прикладами тестували як антагоністи рецепторів CXCR2 у нейтрофілах людини.
ДивитисяДодаткова інформація
Назва патенту англійськоюThiazolo[4,5-d]pyrimidine derivatives, a method for the preparation thereof (variants), intermediary compounds, pharmaceutical composition based thereon and a method for the preparation of such composition
Автори англійськоюBonnert Roger Victor
Назва патенту російськоюПоизводные тиазоло[4,5-d]пиримидина, способ их получения (варианты), промежуточные соединения, фармацевтическая композиция на их основе и способ изготовления такой композиции
Автори російськоюБоннерт Роджер Виктор
МПК / Мітки
МПК: A61P 9/10, A61P 17/06, C07D 513/04, A61P 19/02, A61K 31/519, A61P 37/08, A61P 11/06, A61P 29/00
Мітки: композиції, тіазоло[4,5-d]піримідину, фармацевтична, основі, такої, похідні, варіанти, проміжні, сполуки, композиція, виготовлення, одержання, спосіб
Код посилання
<a href="https://ua.patents.su/21-73521-pokhidni-tiazolo45-dpirimidinu-sposib-kh-oderzhannya-varianti-promizhni-spoluki-farmacevtichna-kompoziciya-na-kh-osnovi-ta-sposib-vigotovlennya-tako-kompozici.html" target="_blank" rel="follow" title="База патентів України">Похідні тіазоло[4,5-d]піримідину, спосіб їх одержання (варіанти), проміжні сполуки, фармацевтична композиція на їх основі та спосіб виготовлення такої композиції</a>
Попередній патент: Кожух самоспікного електрода
Наступний патент: Спосіб прогнозування тромботичних ускладнень при розвитку патологій внутрішньосудинного згортання крові
Випадковий патент: Спосіб оцінки функціонального стану печінки в експерименті