Піримідинові та піридинові сполуки та їх застосування
Формула / Реферат
1. Сполука формули (I)
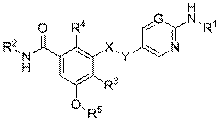 (I)
(I)
або її фармацевтично прийнятна сіль,
де
X являє собою СН2, Y вибраний з CH2, O або S(O)2; або X та Y разом зі зв'язком між ними утворюють -CH=CH- або -C≡C-;
G являє собою N або CH;
R1 являє собою арил або гетероарил, кожний з яких необов'язково заміщений одним або декількома замісниками, незалежно вибраними з галогену, -NR6R7, -OR8, -S(O)nR9, -(CH2)r-C(O)R10, -CN, -C(O)NR6R7, -NR6C(O)R10, -NR6S(O)nR9, -NR6S(O)nNR11R12, -NR6C(O)OR8, -NR6C(O)NR11R12, -NO2, -S(O)nNR6R7, оксо, необов'язково заміщеного алкілу, -(CH2)p-необов'язково заміщеного циклоалкілу, -(CH2)m-необов'язково заміщеного гетероциклілу, -(CH2)q-необов'язково заміщеного гетероарилу, необов'язково заміщеного алкенілу та необов'язково заміщеного алкінілу;
R2 незалежно вибраний з необов'язково заміщеного C1-C6алкілу, необов'язково заміщеного C1-C6алкокси або необов'язково заміщеного C3-C8циклоалкілу;
R3, R4 незалежно вибрані з водню, галогену, -CN або необов'язково заміщеного C1-C6алкілу,
R5 являє собою C1-C6алкіл,
або R3 та R5 разом з атомом О, до якого приєднаний R5, та зі зв'язком між ними утворюють 5- або 6-членне оксивмісне гетероциклічне кільце;
n дорівнює 1 або 2;
m, p, q та r незалежно вибрані з 0, 1, 2, 3, 4, 5, 6;
R6, R7, R8, R9, R10, R11 та R12 незалежно вибрані з водню, алкілу, циклоалкілу, арилу, гетероарилу, гетероциклілу, кожний з яких, за виключенням водню, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з галогену, гідроксилу, меркапто, оксо, алкілу, циклоалкілу, гетероциклілу, необов'язково заміщеного аміно та необов'язково заміщеного аміду,
де кожна вищезазначена необов'язково заміщена група, для якої замісник(и) спеціально не зазначений(і), може бути незаміщеною або незалежно заміщеною одним або декількома, наприклад одним, двома або трьома, замісниками, незалежно вибраними з C1-C6алкілу, C2-C6алкенілу, C2-C6алкінілу, циклоалкілу, арилу, гетероциклілу, гетероарилу, арил-C1-C6алкіл-, гетероарил-C1-C6алкіл-, C1-C6галогеналкіл-, -OC1-C6алкілу, -OC2-C6алкенілу, -OC1-C6алкілфенілу, -C1-C6алкіл-OH, -C1-C6алкіл-SH, -C1-C6алкіл-O-C1-C6алкілу, -OC1-C6галогеналкілу, галогену, -OH, меркапто, -NH2, -C1-C6алкіл-NH2, -N(C1-C6алкіл)2, -NH(C1-C6алкіл), -N(C1-C6алкіл)(C1-C6алкілфеніл), -NH(C1-C6алкілфеніл), ціано, нітро, оксо, -C(O)-OH, -C(O)OC1-C6алкілу, -CON(C1-C6алкіл)2, -CONH(C1-C6алкіл), -CONH2, -NHC(O)(C1-C6алкіл), -NHC(O)(феніл), -N(C1-C6алкіл)C(O)(C1-C6алкіл), -N(C1-C6алкіл)C(O)(феніл), -C(O)C1-C6алкілу, -C(O)C1-C6алкілфенілу, -C(O)C1-C6галогеналкілу, -OC(O)C1-C6алкілу, -S(O)2-C1-C6алкілу, -S(O)-C1-C6алкілу, -S(O)2-фенілу, -S(O)2-C1-C6галогеналкілу, -S(O)2NH2, -S(O)2NH(C1-C6алкіл), -S(O)2NH(феніл), -NHS(O)2(C1-C6алкіл), -NHS(O)2(феніл) та -NHS(O)2(C1-C6галогеналкіл).
2. Сполука формули (I) за п. 1, де кожна необов'язково заміщена група, для якої замісник(и) спеціально не зазначений(і), може бути незаміщеною або незалежно заміщеною одним або декількома замісниками, незалежно вибраними з гідроксилу, меркапто, галогену, C1-C6алкілу, C2-C6алкенілу, C2-C6алкінілу, -OC1-C6алкілу, -NH2, -N(C1-C6алкіл)2, -NH(C1-C6алкіл), ціано, нітро, оксо, -S(O)2-C1-C6алкілу, -S(O)-C1-C6алкілу, -S(O)2-C1-C6галогеналкілу, -C(O)-OH, -C1-C6алкіл-OH, -C1-C6алкіл-SH, гетероциклілу, або її фармацевтично прийнятна сіль.
3. Сполука формули (I) за п. 1 або п. 2, де R1 являє собою арил або гетероарил, кожний з яких необов'язково заміщений одним або декількома замісниками, незалежно вибраними з
(1) галогену;
(2) оксо;
(3) необов'язково заміщеного алкілу;
(4) -(CH2)m-необов'язково заміщеного гетероциклілу;
(5) -(CH2)p-необов'язково заміщеного циклоалкілу;
(6) -(CH2)q-необов'язково заміщеного гетероарилу;
(7) -S(O)nR9;
(8) -(CH2)r-C(O)R10;
(9) необов'язково заміщеного алкенілу;
(10) необов'язково заміщеного алкінілу;
(11) -OR8;
де n дорівнює 1 або 2; m, p, q та r незалежно вибрані з 0, 1, 2, 3, 4, 5, 6; R8, R9 та R10 незалежно вибрані з водню, алкілу, гетероциклілу, кожен з яких, за виключенням водню, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з алкілу, оксо, гетероциклілу;
де "необов'язково заміщений алкіл", "необов'язково заміщений гетероцикліл", "необов'язково заміщений циклоалкіл", "необов'язково заміщений гетероарил", "необов'язково заміщений алкеніл" та "необов'язково заміщений алкініл” у вищезазначеному R1 може бути незаміщеним або незалежно заміщеним одним або декількома замісниками, незалежно вибраними з гідроксилу, меркапто, галогену, C1-C6алкілу, C2-C6алкенілу, C2-C6алкінілу, -OC1-C6алкілу, -NH2, -N(C1-C6алкіл)2, -NH(C1-C6алкіл), ціано, нітро, оксо, -S(O)2-C1-C6алкілу, -S(O)-C1-C6алкілу, -S(O)2-C1-C6галогеналкілу, -C(O)-OH, -C1-C6алкіл-OH, -C1-C6алкіл-SH, гетероциклілу,
або її фармацевтично прийнятна сіль.
4. Сполука формули (I) за п. 3, де R1 являє собою арил або гетероарил, кожний з яких необов'язково заміщений одним або декількома замісниками, незалежно вибраними з
(1) галогену;
(2) оксо;
(3) алкілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з гідроксилу, меркапто, галогену, -OC1-C6алкілу, -NH2, -N(C1-C6алкіл)2, -NH(C1-C6алкіл), ціано, нітро, -S(O)2-C1-C6алкілу, -S(O)-C1-C6алкілу, C(O)-OH;
(4) -(CH2)m-гетероциклілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C1-C6алкілу, -C1-C6алкіл-OH, -C1-C6алкіл-SH та оксо, де m дорівнює 0, 1, 2, 3, 4, 5 або 6;
(5) -(CH2)p-незаміщеного циклоалкілу, де p дорівнює 0, 1, 2, 3, 4, 5 або 6;
(6) -(CH2)q-гетероарилу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C1-C6алкілу, де q дорівнює 0, 1, 2, 3, 4, 5 або 6;
(7) -S(O)nR9, де R9 являє собою C1-C6алкіл та n дорівнює 1 або 2;
(8) -(CH2)r-C(O)R10, де R10 являє собою гетероцикліл, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з C1-C6алкілу та оксо, та r дорівнює 0, 1, 2, 3, 4, 5 або 6;
(9) незаміщеного C2-C6алкенілу;
(10) незаміщеного C2-C6алкінілу;
(11) -OR8, де R8 вибраний з водню, алкілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з гетероциклілу,
або її фармацевтично прийнятна сіль.
5. Сполука формули (I) за п. 1, де R1 являє собою арил або гетероарил, кожний з яких необов'язково заміщений одним або декількома замісниками, незалежно вибраними з
(1) галогену;
(2) -NR6R7, де R6 та R7 незалежно вибрані з водню та C1-C6алкілу, необов'язково заміщеного аміно, який необов'язково заміщений C1-C6алкілом;
(3) -OR8, де R8 вибраний з водню таC1-C6алкілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з гетероциклілу, необов'язково заміщеного -OH або меркапто, та аміно, необов'язково заміщеного C1-C6алкілом,
(4) -S(O)nR9, де R9 являє собою C1-C6алкіл та n дорівнює 1 або 2;
(5) -(CH2)r-C(O)R10, де R10 являє собою C1-C6алкіл або гетероцикліл, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з C1-C6алкілу та оксо, та r дорівнює 0, 1, 2, 3, 4, 5 або 6;
(6) -CN;
(7) -C(O)NR6R7, де R6 та R7 незалежно вибрані з водню та C1-C6алкілу, необов'язково заміщеного аміно, який необов'язково заміщений C1-C6алкілом;
(8) -NR6C(O)R10, де R6 являє собою H та R10 являє собою C1-C6алкіл;
(9) оксо;
(10) алкілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з гідроксилу, меркапто, галогену, -OC1-C6алкілу, -NH2, -N(C1-C6алкіл)2, -NH(C1-C6алкіл), ціано, нітро, -S(O)2-C1-C6алкілу, -S(O)-C1-C6алкілу, -C(O)-OH;
(11) -(CH2)p-незаміщеного циклоалкілу, де p дорівнює 0, 1, 2, 3, 4, 5 або 6;
(12) -(CH2)m-гетероциклілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C1-C6алкілу, C3-C8циклоалкілу, -C1-C6алкіл-OH, -C1-C6алкіл-SH, -C1-C6алкіл-O-C1-C6алкілу, -NH2, -N(C1-C6алкіл)2, -NH(C1-C6алкіл), оксо, -C(O)C1-C6алкілу, де m дорівнює 0, 1, 2, 3, 4, 5 або 6;
(13) -(CH2)q-гетероарилу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C1-C6алкілу, де q дорівнює 0, 1, 2, 3, 4, 5 або 6;
(14) незаміщеного C2-C6алкенілу;
(15) незаміщеного C2-C6алкінілу;
або її фармацевтично прийнятна сіль.
6. Сполука формули (I) за п. 4 або п. 5, де R1 являє собою радикал кільця або кільцевої системи, вибраних з
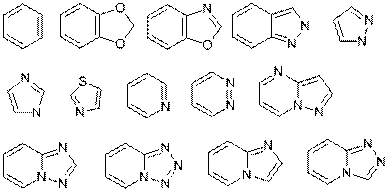
 ,
,
кожний з яких необов'язково заміщений, як зазначено у п. 4 або п. 5,
або її фармацевтично прийнятна сіль.
7. Сполука формули (I) за п. 4 або п. 5, де R1 вибраний з
 ,
,
кожний з яких необов'язково заміщений, як зазначено у п. 4 або п. 5,
або її фармацевтично прийнятна сіль.
8. Сполука формули (I) за п. 1, де R8 являє собою водень або C1-C6алкіл, необов'язково заміщений гетероциклілом, або її фармацевтично прийнятна сіль.
9. Сполука формули (I) за п. 1, де R10 являє собою гетероцикліл, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з C1-C6алкілу та оксо, або її фармацевтично прийнятна сіль.
10. Сполука формули (I) за п. 1, де R1 являє собою арил, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з (1) галогену; (2) алкілу, необов'язково заміщеного за допомогою -C(O)-OH; (3) -(CH2)m-гетероциклілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C1-C6алкілу, -C1-C6алкіл-OH, -C1-C6алкіл-SH та оксо, де m дорівнює 0, 1, 2, 3, 4, 5 або 6; (4) -(CH2)q-гетероарилу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C1-C6алкілу, де q дорівнює 0; (5) -(CH2)r-C(O)R10, де R10 являє собою гетероцикліл, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з C1-C6алкілу та оксо, та r дорівнює 0; (6) незаміщеного C2-C6алкенілу; (7) незаміщеного C2-C6алкінілу; (8) -OR8, де R8 вибраний з водню, алкілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з гетероциклілу,
або її фармацевтично прийнятна сіль.
11. Сполука формули (I) за будь-яким з пп. 1-10, де R1 являє собою феніл, заміщений піперазинілом, при цьому піперазиніл необов'язково заміщений одним або декількома C1-C6алкілами або C3-C8циклоалкілами, переважно C1-C6алкілами, більш переважно R1 являє собою феніл, заміщений піперазинілом, який необов'язково заміщений одним або декількома метилами або етилами, або її фармацевтично прийнятна сіль.
12. Сполука формули (I) за п. 11, де R1 являє собою феніл, заміщений піперазинілом, при цьому піперазиніл необов'язково заміщений одним або декількома C1-C6алкілами, переважно R1 являє собою феніл, заміщений піперазинілом, який необов'язково заміщений одним або декількома метилами або етилами, або її фармацевтично прийнятна сіль.
13. Сполука формули (I) за п. 1, де R1 являє собою піразоліл, який необов'язково заміщений одним або декількома замісниками, вибраними з
(1) алкілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з гідроксилу, меркапто, галогену, -OC1-C6алкілу, -NH2, -N(C1-C6алкіл)2, -NH(C1-C6алкіл), -S(O)2-C1-C6алкілу, -S(O)-C1-C6алкілу;
(2) -(CH2)m-гетероциклілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C1-C6алкілу, де m дорівнює 0, 1, 2, 3, 4, 5 або 6;
(3) -(CH2)p-незаміщеного циклоалкілу, де p дорівнює 0, 1, 2, 3, 4, 5 або 6;
(4) -(CH2)q-гетероарилу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C1-C6алкілу, де q дорівнює 0, 1, 2, 3, 4, 5 або 6;
(5) -S(O)nR9, де R9 являє собою C1-C6алкіл та n дорівнює 1 або 2;
(6) -(CH2)r-C(O)R10, де R10 являє собою гетероцикліл, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з C1-C6алкілу та оксо, та r дорівнює 0, 1, 2, 3, 4, 5 або 6,
або її фармацевтично прийнятна сіль.
14. Сполука формули (I) за будь-яким з пп. 1-13, де R2 вибраний з C1-C6алкілу, C1-C6алкокси, необов'язково заміщеного гідроксилом, або C3-C8циклоалкілу, або її фармацевтично прийнятна сіль.
15. Сполука формули (I) за п. 14, де R2 являє собою метил, етил, метокси, етокси, заміщений гідроксилом, ізопропокси або циклопропіл, або її фармацевтично прийнятна сіль.
16. Сполука формули (I) за будь-яким з пп. 1-13, де R3, R4 незалежно вибрані з водню, галогену, -CN або незаміщеного C1-C6алкілу, R5 являє собою C1-C6алкіл, або R3 та R5 разом з атомом О, до якого приєднаний R5, та зі зв'язком між ними утворюють 5- або 6-членне оксивмісне гетероциклічне кільце, або її фармацевтично прийнятна сіль.
17. Сполука формули (I) за будь-яким з пп. 1-13, де R4 являє собою водень, та R3 і R5 разом з атомом О, до якого приєднується R5, та зі зв'язком між ними утворюють фуран або дигідрофуранове кільце, або її фармацевтично прийнятна сіль.
18. Сполука формули (I) за п. 1, де зазначена сполука вибрана зі сполук 1-309:
Сполука №
Структура
1
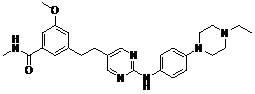
2
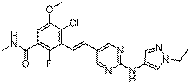
3
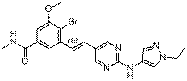
4
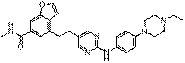
5
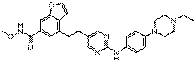
6
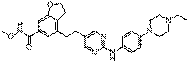
7
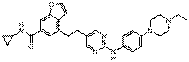
8
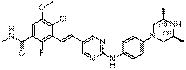
9
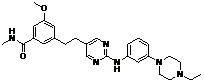
10
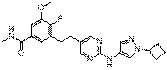
11
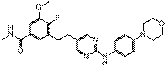
12
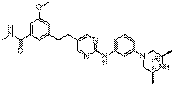
13
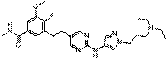
14
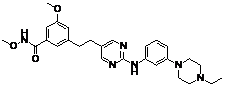
15
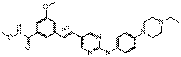
16
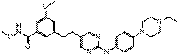
17
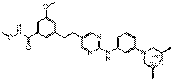
18
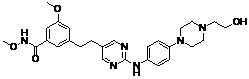
19
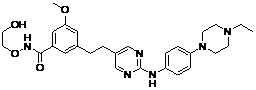
20

21
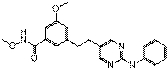
22
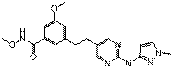
23
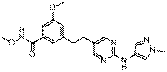
24
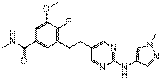
25
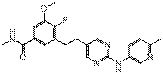
26
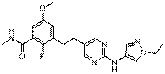
27
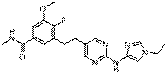
28
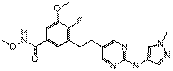
29
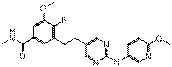
30
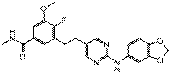
31
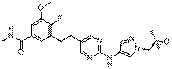
32
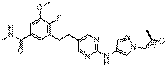
33
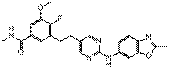
34
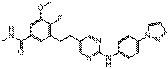
35
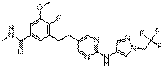
36
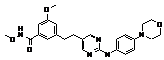
37

38
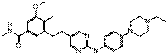
39
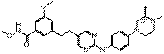
40
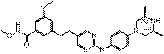
41
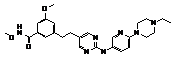
42
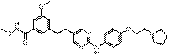
43
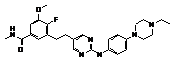
44
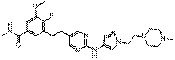
45
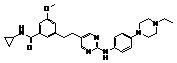
46
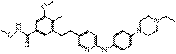
47
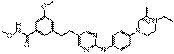
48
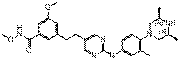
49
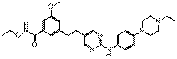
50
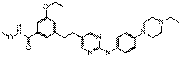
51
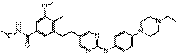
52
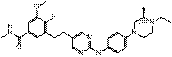
53
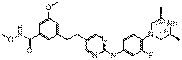
54
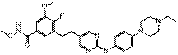
55
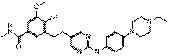
56
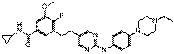
57
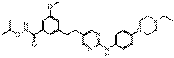
58
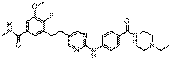
59
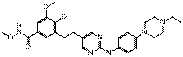
60
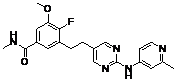
61
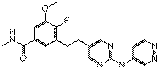
62
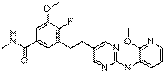
63
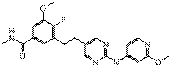
64
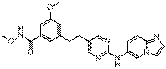
65
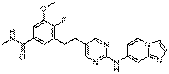
66
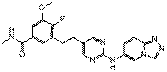
67
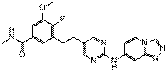
68
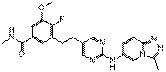
69
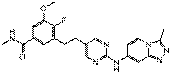
70
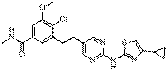
71
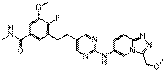
72
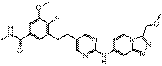
73
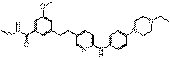
74
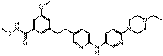
75
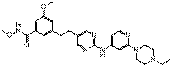
76
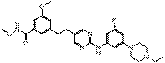
77
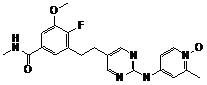
78
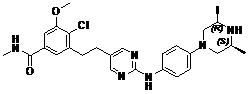
79
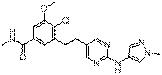
80
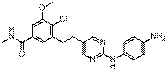
81
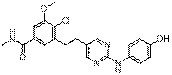
82
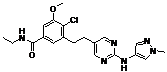
83
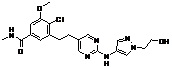
84
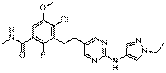
85
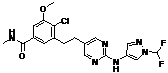
86
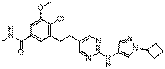
87
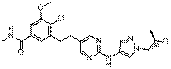
88
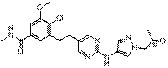
89
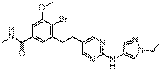
90
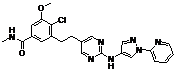
91
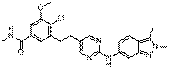
92
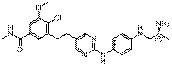
93
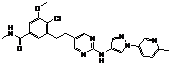
94
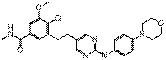
95
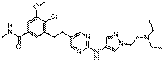
96
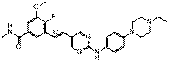
97
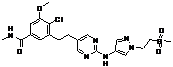
98
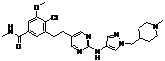
99
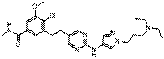
100
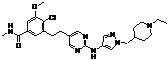
101
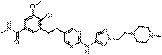
102
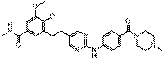
103
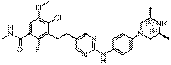
104
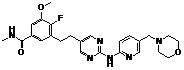
105
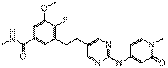
106
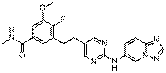
107
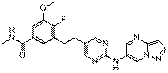
108
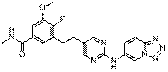
109
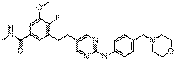
110
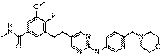
111
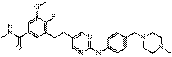
112
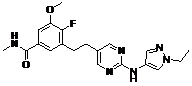
113
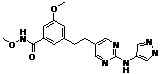
114
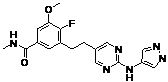
115
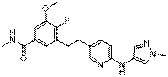
116
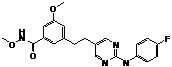
117

118
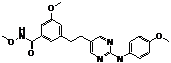
119
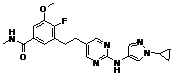
120
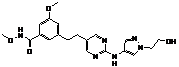
121
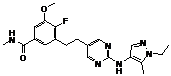
122
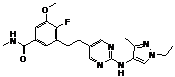
123
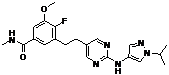
124
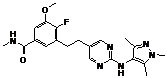
125

126
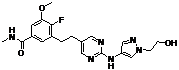
127
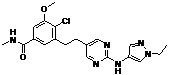
128
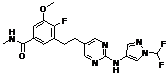
129

130
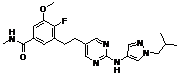
131
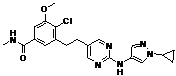
132
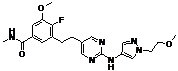
133
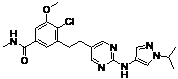
134
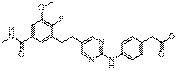
135

136
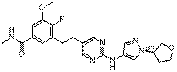
137
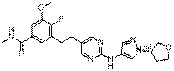
138

139
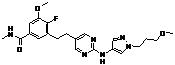
140

141
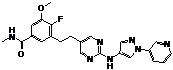
142
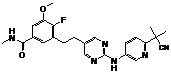
143

144
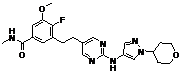
145
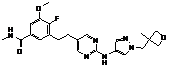
146
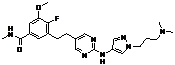
147
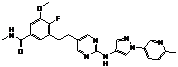
148
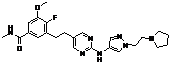
149
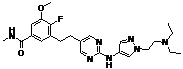
150
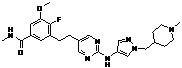
151

152
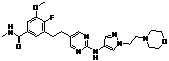
153
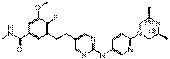
154
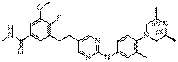
155
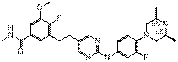
156
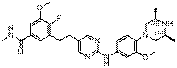
157
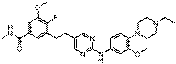
158
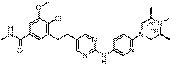
159
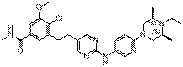
160
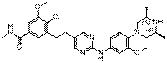
161
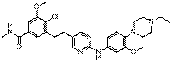
162

163

164
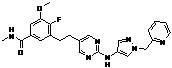
165
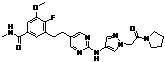
166
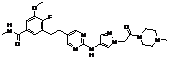
167

168
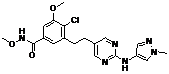
169
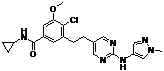
170
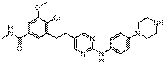
171
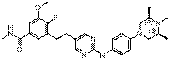
172
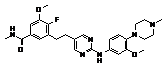
173
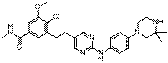
174
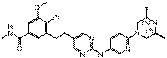
175
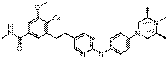
176
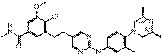
177
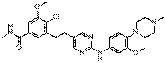
178
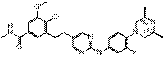
179
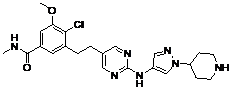
180

181
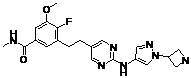
182
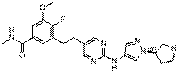
183
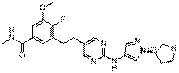
184
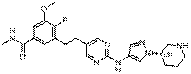
185
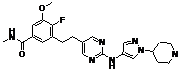
186
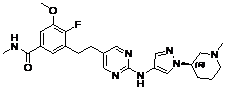
187
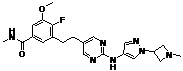
188
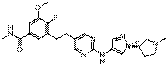
189
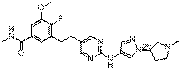
190
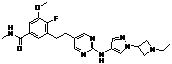
191
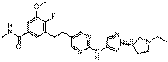
192
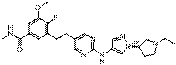
193
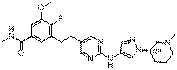
194
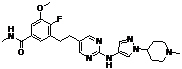
195
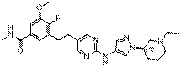
196
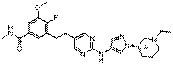
197

198
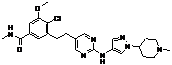
199

200
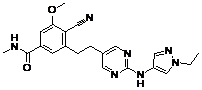
201
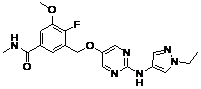
202
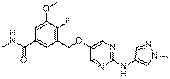
203
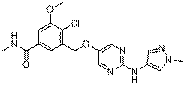
204
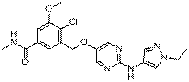
205
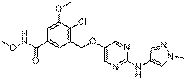
206
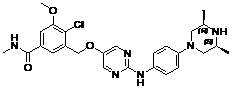
207
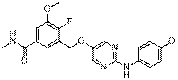
208
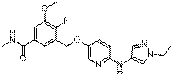
209
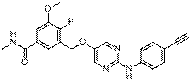
210
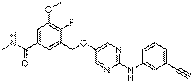
211
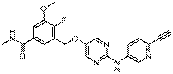
212
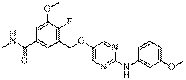
213
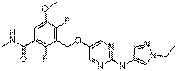
214
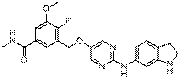
215
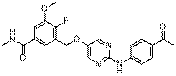
216
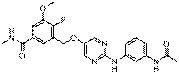
217
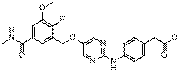
218
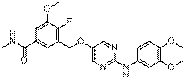
219
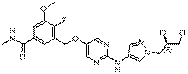
220
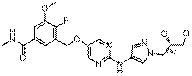
221
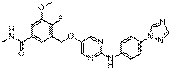
222
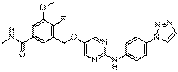
223
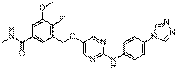
224
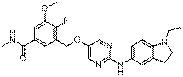
225
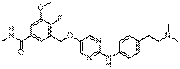
226
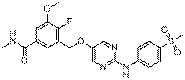
227
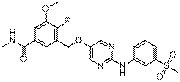
228
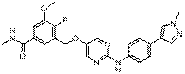
230
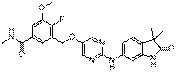
231
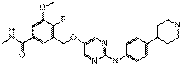
232
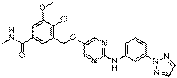
233
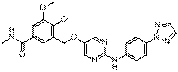
234
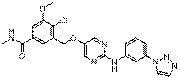
235
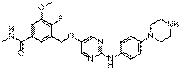
236
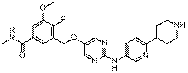
237
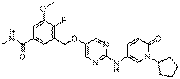
238
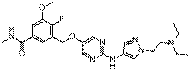
239
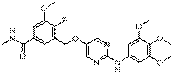
240
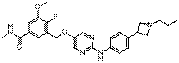
241
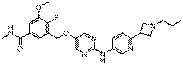
242
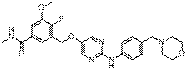
243
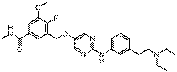
244
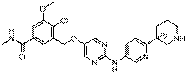
245
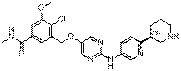
246
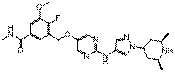
247
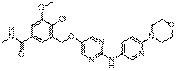
248
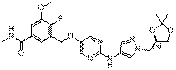
249
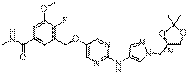
250
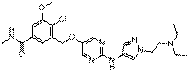
251
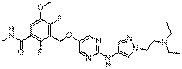
252
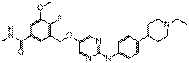
253
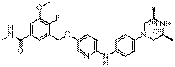
254
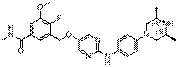
255
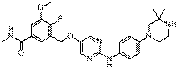
256
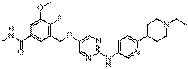
257
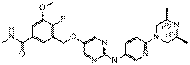
258
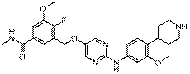
259
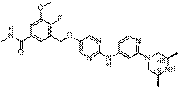
260
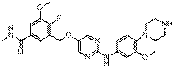
261
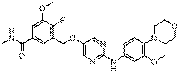
262
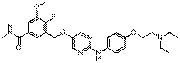
263
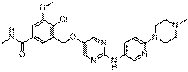
264
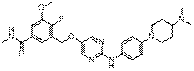
265
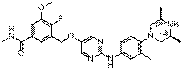
266
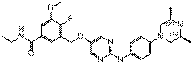
267
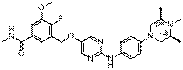
268
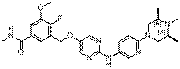
269
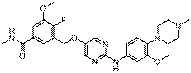
270
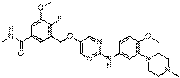
271
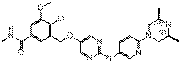
272
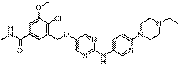
273
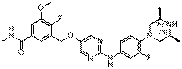
274
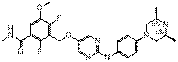
275
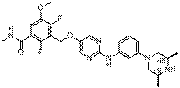
276
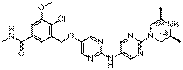
277
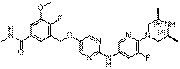
278
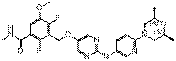
279
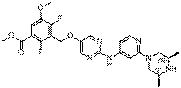
280
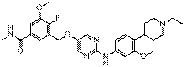
281
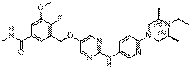
282
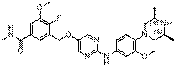
283
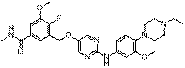
284
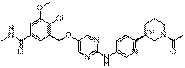
285
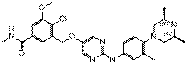
286
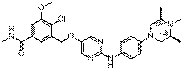
287
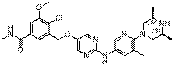
288
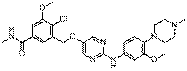
289
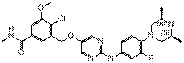
290
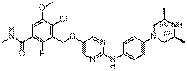
291
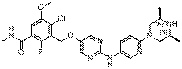
292
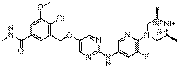
293
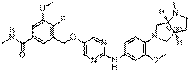
294
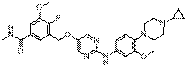
295
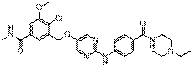
296
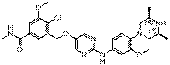
297
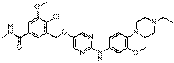
298
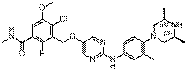
299
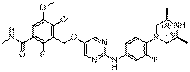
301
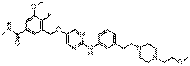
302
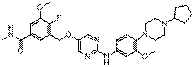
303
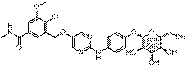
304
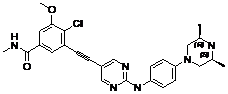
305
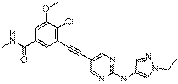
306
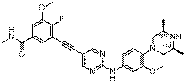
307
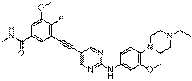
308
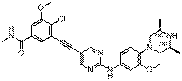
309
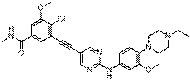
або її фармацевтично прийнятна сіль.
19. Сполука формули (I) за будь-яким з пп. 1-18 та/або її фармацевтично прийнятна сіль як медикамент.
20. Фармацевтична композиція, яка містить щонайменше одну сполуку формули (I) за будь-яким з пп. 1-18 та/або щонайменше одну її фармацевтично прийнятну сіль та необов'язково щонайменше один фармацевтично прийнятний носій.
21. Спосіб in vivo або in vitro інгібування активності FGFR, асоційованої з захворюванням, яке реагує на інгібування FGFR, що передбачає введення FGFR у контакт з ефективною кількістю щонайменше однієї сполуки формули (I) за будь-яким з пп. 1-18 та/або щонайменше однієї її фармацевтично прийнятної солі.
22. Спосіб лікування захворювання, яке реагує на інгібування FGFR, що передбачає введення суб'єкту, який потребує цього, ефективної кількості для лікування зазначеного захворювання щонайменше однієї сполуки формули (I) за будь-яким з пп. 1-18 та/або щонайменше однієї її фармацевтично прийнятної солі.
23. Спосіб за п. 22, де захворювання, яке реагує на інгібування FGFR, являє собою рак, наприклад рак легені, рак шлунка, рак печінки, рак молочної залози, рак яєчника, ендометріальну карциному або карциному сечового міхура.
24. Застосування щонайменше однієї сполуки формули (I) за будь-яким з пп. 1-18 та/або щонайменше однієї її фармацевтично прийнятної солі у виготовленні медикаменту для лікування захворювання, яке реагує на інгібування FGFR.
25. Застосування за п. 24, де захворювання, яке реагує на інгібування FGFR, являє собою рак, наприклад рак легені, рак шлунка, рак печінки, рак молочної залози, рак яєчника, ендометріальну карциному або карциному сечового міхура.
Текст
Реферат: Даний винахід стосується нових піримідинових та піридинових сполук формули (І) або їх фармацевтично прийнятних солей O R R 2 X N H R O H N G 4 R Y R 1 N 3 5 , (I) 1 2 3 4 5 де R , R , R , R , R , X, Y та G визначені в описі, фармацевтичних композицій, що їх містять, способу їх отримання та їх застосування у терапії захворювання, яке реагує на інгібування FGFR, наприклад раку. UA 113470 C2 (12) UA 113470 C2 UA 113470 C2 5 10 15 20 25 30 35 40 45 50 Галузь даного винаходу Даний винахід відноситься до нових піримідинових та піридинових сполук, фармацевтичних композицій, що містять їх, способу їх отримання та їх застосування в терапії. Передумови винаходу Фактор росту фібробластів (FGF) визначено важливим медіатором у багатьох фізіологічних процесах. Родина рецепторів фактора росту фібробластів рецепторних тирозинкіназ включає чотири представника (FGFR1, FGFR2, FGFR3 та FGFR4). Фактори росту фібробластів (FGF) та їх рецептори (FGFR) відіграють важливі ролі у клітинній проліферації, клітинному диференціюванні, міграції клітин, виживанні клітин, синтезі білка та ангіогенезі. Є багато даних, що безпосередньо зв'язують передачу сигналу FGF з раком. Порушення регуляції передачі сигналу FGFR було залучено до ряду ракових захворювань, у тому числі сквамозного недрібноклітинного раку легені (NSCLC), дрібноклітинного раку легені (SCLC), карциноми шлунку, печінки, молочної залози, яєчника, ендометрія та сечового міхура, наприклад, було виявлено, що FGFR1 ампліфікується в 22 % випадків сквамозного NSCLC, ампліфікації FGFR2 були зареєстровані у майже 10 % випадків раку шлунка, та мутація FGFR3 була виявлена у приблизно 50-60 % випадків нем'язової інвазії та у 17 % випадків раку сечового міхура високого ступеню, що викликає значний інтерес до FGFR як мішеней для терапевтичного втручання. Таким чином, потрібні нові сполуки та способи модуляції генів FGFR та лікування проліфераційних порушень, у тому числі раку. Даний винахід спрямований на ці потреби. Короткий опис винаходу Даний винахід відноситься до сполуки формули (I): (I), та/або її проліків, енантіомерів, діастереомерів, таутомерів або їх сумішей у будь-якому співвідношенні, або до її фармацевтично прийнятної солі; де X являє собою СН2, Y вибраний з CH2, O або S(O)2; або X та Y разом зі зв'язком між ними утворюють -CH=CH- або -C≡C-; G являє собою N або CH; 1 R являє собою арил або гетероарил, який необов'язково заміщений одним або декількома 6 7 8 9 10 замісниками, незалежно вибраними з галогену, -NR R , -OR , -S(O)nR , -(CH2)r-C(O)R , -CN, 6 7 6 10 6 9 6 11 12 6 8 6 11 12 C(O)NR R , -NR C(O)R , -NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , -NR C(O)NR R , -NO2, 6 7 -S(O)nNR R , оксо, необов'язково заміщеного алкілу, -(CH2)p-необов'язково заміщеного циклоалкілу, -(CH2)m-необов'язково заміщеного гетероциклілу, -(CH2)q-необов'язково заміщеного гетероарилу, необов'язково заміщеного алкенілу та необов'язково заміщеного алкінілу; 2 R незалежно вибраний з необов'язково заміщеного C1-C6алкілу, необов'язково заміщеного C1-C6алкоксі або необов'язково заміщеного C3-C8циклоалкілу; 3 4 R , R незалежно вибрані з водню, галогену, -CN або необов'язково заміщеного C1-C6алкілу, 5 R являє собою C1-C6алкіл, 3 5 5 або R та R разом з атомом О, до якого приєднаний R , та зі зв'язком між ними утворюють 5- або 6-членне окси-вмісне гетероциклічне кільце; n дорівнює 1 або 2; m, p, q та r незалежно вибрані з 0, 1, 2, 3, 4, 5, 6; 6 7 8 9 10 11 12 R , R , R , R , R , R та R незалежно вибрані з водню, алкілу, циклоалкілу, арилу, гетероарилу, гетероциклілу, кожен з яких, за виключенням водню, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з галогену, гідроксилу, меркапто, оксо, алкілу, циклоалкілу, гетероциклілу, необов'язково заміщеного аміно та необов'язково заміщеного аміду, де кожна вищезазначена необов'язково заміщена група, для якої замісник(и) спеціально не зазначений(і), може бути незаміщеною або незалежно заміщеною одним або декількома, наприклад, одним, двома або трьома, замісниками, незалежно вибраними з C1-C6алкілу, C2C6алкенілу, C2-C6алкінілу, циклоалкілу, арилу, гетероциклілу, гетероарилу, арил-C1-C6алкіл-, гетероарилC1-C6алкіл-, C1-C6галогеналкіл-, -OC1-C6алкілу, -OC2-C6алкенілу, OC1-C6алкілфенілу, -C1-C6алкіл-OH, -C1-C6алкіл-SH, -C1-C6алкіл-O-C1-C6алкілу, -OC1-C6галогеналкілу, галогену, -OH, 1 UA 113470 C2 5 10 15 20 25 30 35 40 45 50 55 60 меркапто, -NH2, -C1-C6алкіл-NH2, -N(C1-C6алкіл)2, -NH(C1-C6алкіл), -N(C1-C6алкіл)(C1C6алкілфеніл), -NH(C1-C6алкілфеніл), ціано, нітро, оксо, -C(O)-OH, -C(O)OC1-C6алкілу, -CON(C1C6алкіл)2, -CONH(C1-C6алкіл), -CONH2,NHC(O)(C1-C6алкіл), -NHC(O)(феніл), -N(C1C6алкіл)C(O)(C1-C6алкіл), -N(C1-C6алкіл)C(O)(феніл), -C(O)C1-C6алкілу, -C(O)C1-C6алкілфенілу, C(O)C1-C6галогеналкілу, -OC(O)C1-C6алкілу, -S(O)2-C1-C6алкілу, -S(O)-C1-C6алкілу, -S(O)2фенілу, -S(O)2-C1-C6галогеналкілу, -S(O)2NH2, -S(O)2NH(C1-C6алкіл), -S(O)2NH(феніл), NHS(O)2(C1-C6алкіл), -NHS(O)2(феніл) та -NHS(O)2(C1-C6галогеналкіл), в яких кожен з фенілу, арилу, гетероциклілу та гетероарилу необов'язково заміщений одним або декількома замісниками, вибраними з галогену, циклоалкілу, гетероциклілу, C1-C4алкілу, C1-C6галогеналкіл, -OC1-C6алкілу, C1-C6алкіл-OH, -C1-C6алкіл-O-C1-C6алкілу, -OC1-C6галогеналкілу, ціано, нітро, NH2, -C(O)-OH, -C(O)OC1-C6алкілу, -CON(C1-C6алкіл)2, -CONH(C1-C6алкіл), -CONH2, -NHC(O)(C1C6алкіл), -NH(C1-C6алкіл)C(O)(C1-C6алкіл), -SO2(C1-C6алкіл), -SO2(феніл), -SO2(C1C6галогеналкіл), -SO2NH2, -SO2NH(C1-C6алкіл), -SO2NH(феніл), -NHSO2(C1-C6алкіл), NHSO2(феніл) та -NHSO2(C1-C6галогеналкіл). Також запропоновано фармацевтичну композицію, що містить щонайменше одну сполуку формули (I) та/або щонайменше одну її фармацевтично прийнятну сіль, описану у даному документі, та необов'язково щонайменше один фармацевтично прийнятний носій. Також запропоновано спосіб in vivo або in vitro інгібування активності FGFR, що передбачає введення FGFR у контакт з ефективною кількістю щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаної у даному документі. Також запропоновано спосіб лікування захворювання, яке реагує на інгібування FGFR, що передбачає введення суб'єкту, який потребує цього, кількості, ефективної для лікування зазначеної хвороби, щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаної у даному документі. Також запропоновано застосування щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаної у даному документі, для лікування захворювання, що реагує на інгібування FGFR. Також запропоновано застосування щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаної у даному документі, у виготовленні медикаменту для лікування захворювання, що реагує на інгібування FGFR. Детальний опис винаходу Визначення Використані у даній заявці наступні слова, фрази та символи, як правило, передбачають значення, що наведено нижче, за виключенням тих випадків, коли у контексті, в якому вони застосовуються, вказується інше. Тире (“-”), яке розташоване не між двома буквами або символами, використовується для зазначення точки приєднання замісника. Наприклад, -C(O)NH2 приєднується через атом вуглецю. Термін "алкіл", як застосовується у даному документі, відноситься до прямого або розгалуженого насиченого вуглеводневого радикала, що містить 1-18, переважно 1-12, більш переважно 1-6, ще більш переважно 1-4, особливо 1-3 атомів вуглецю. Приклади алкільних груп включають без обмеження метил, етил, н-пропіл, ізо-пропіл, н-бутил, ізо-бутил, втор-бутил та трет-бутил. Термін "алкоксі", як застосовується у даному документі, відноситься до групи –O-алкіл, де алкіл визначений вище. Приклади алкоксигруп включають без обмеження метоксі, етоксі, нпропілоксі, ізо-пропілоксі, н-бутилоксі, ізо-бутилоксі, трет-бутилоксі, пентилоксі, гексилоксі, у тому числі їх ізомери. Термін "алкеніл", як застосовується у даному документі, відноситься до прямого або розгалуженого вуглеводневого радикала, що містить один або декілька подвійних зв'язків C=C та 2-10, переважно 2-6, більш переважно 2-4 атомів вуглецю. Приклади алкенільних груп включають без обмеження вініл, 2-пропеніл та 2-бутеніл. Термін "алкініл", як застосовується у даному документі, відноситься до прямого або розгалуженого вуглеводневого радикала, що містить один або декілька потрійних зв'язків C≡C та 2-10, переважно 2-6, більш переважно 2-4 атомів вуглецю. Приклади алкінільних груп включають без обмеження етиніл, 2-пропініл та 2-бутиніл. Термін "циклоалкіл", як застосовується у даному документі, відноситься до насиченого та частково ненасиченого циклічного вуглеводневого радикала з 3-12, переважно 3-8, більш переважно 3-6 атомами вуглецю. Приклади циклоалкільних груп включають без обмеження циклопропіл, циклобутил, циклопентил, циклопентеніл, циклогексил, циклогексеніл, циклогептил та циклооктил. Кільце циклоалкільної групи може бути насиченим або мати один або декілька, 2 UA 113470 C2 5 10 15 20 25 30 35 40 45 50 55 60 наприклад, один або два подвійних зв'язки (тобто бути частково ненасиченим), але не повністю спряженим, і не арилом, визначеним у даному документі. Термін "арил", як застосовується у даному документі, відноситься до 5- та 6-членного моноциклічного карбоциклічного ароматичного вуглеводневого радикала та 8-12-членного біциклічного карбоциклічного вуглеводневого радикала, де щонайменше одне кільце є ароматичним, наприклад, феніл, нафталеніл, 1,2,3,4-тетрагідронафталеніл, інденіл, інданіл, азуленіл. Термін "галоген", як застосовується у даному документі, включає фтор, хлор, бром та йод, а термін "галогеновий", як застосовується у даному документі, включає фторний, хлорний, бромний та йодний. Термін "гетероарил", як застосовується у даному документі, відноситься до 5-6-членного моноциклічного ароматичного вуглеводневого радикала, що містить один або декілька, наприклад, від 1 до 4, або, в деяких варіантах здійснення, від 1 до 3, в деяких варіантах здійснення, 1 або 2 гетероатома, незалежно вибраних з N, O та S, при цьому решта атомів кільця являють собою вуглець; та 8-12-членного біциклічного вуглеводневого радикала, що містить один або декілька, наприклад, від 1 до 4, або, в деяких варіантах здійснення, від 1 до 3, в деяких варіантах здійснення, 1 або 2 гетероатома, незалежно вибраних з N, O та S, при цьому решта атомів кільця являють собою вуглець, де щонайменше одне з кілець є ароматичним. Наприклад, біциклічний гетероарил включає 5-7-членне гетероциклічне ароматичне кільце, конденсоване з 5-7-членним циклоалкільним кільцем. Якщо загальне число атомів S і O у гетероарильній групі перевищує 1, то такі гетероатоми розташовані не поруч один з одним. У деяких варіантах здійснення загальне число атомів S і O у гетероарильній групі становить не більше 2. У деяких варіантах здійснення загальне число атомів S і O у гетероарильній групі становить не більше 1. Гетероарильна група також включає таку, де гетероатом N зустрічається у вигляді N-оксиду, такого як піридиніл-N-оксиди. Приклади гетероарильної групи включають без обмеження піридил, піридил-N-оксид, такий як пірид-2-іл, пірид-3-іл, пірид-4-іл або їх N-оксид; піразиніл, такий як піразин-2-іл, піразин-3-іл; піримідиніл, такий як піримідин-2-іл, піримідин-4-іл; піразоліл, такий як піразол-1-іл, піразол-3-іл, піразол-4-іл, піразол-5-іл; імідазоліл, імідазол-2-іл, імідазолін-4-іл; оксазоліл; ізоксазоліл; тіазоліл; ізотіазоліл; тіадіазоліл; тетразоліл; триазоліл, такий як 1H-1,2,4-триазоліл, 4H-1,2,4триазоліл, 1H-1,2,3-триазоліл, 2H-1,2,3-триазоліл; тієніл; фурил; піраніл; піроліл; піридазиніл; безодіоксоліл, такий як бензо[d][1,3]діоксоліл; бензоксазоліл, такий як бензо[d]оксазоліл; імідазопіридиніл, такий як імідазо[1,2-a]піридиніл; триазолoпіридиніл, такий як [1,2,4]триазолo[4,3-a]піридиніл та [1,2,4]триазолo[1,5-a]піридиніл; індазоліл, 2H-індазоліл; піразолoпіримідиніл, такий як піразолo[1,5-a]піримідиніл; тетразолопіридиніл, такий як тетразоло[1,5-a]піридиніл; бензотієніл; бензофурил; бензоімідазолініл; індоліл; індолініл; хинолініл, ізохінолініл, 1,2,3,4-тетрагідрохінолініл та 5,6,7,8-тетрагідроізохінолініл. Термін "гетероцикліл", як застосовується у даному документі, відноситься до 3-14-членного, переважно 4-12-членного моноциклічного, біциклічного або трициклічного насиченого або частково ненасиченого вуглеводневого радикала, що містить щонайменше 2 атоми вуглецю та 1, 2 або 3 гетероатоми, незалежно вибраних з кисню, сірки та азоту. Більш переважно "гетероцикліл" відноситься до 4-8-членної, особливо 4-, 5- або 6-членної моноциклічної гетероциклільної групи, що містить 1 або 2 гетероатоми, незалежно вибраних з N, O та S. "Гетероцикліл" також відноситься до аліфатичного спіроциклічного кільця, що містить один або декілька гетероатомів, незалежно вибраних з N, O та S. Кільця можуть бути насиченими або мати один або декілька подвійних зв'язків (тобто частково ненасиченими). Точкою приєднання може бути вуглець або гетероатом у гетероциклічній групі. Однак, жодне з кілець в гетероциклільній групі не є ароматичним, таким чином, гетероциклільна група не є гетероарильною, як зазначено у даному документі. Гетероциклільна група також включає такі, де гетероатом N або S зустрічається у складі її оксиду. Приклади гетероциклілу включають без обмеження оксетаніл, такий як оксетан-2-іл або оксетан-3-іл; азетидиніл, такий як азетидин-2-іл або азетидин-3-іл; піролідиніл, такий як піролідин-1-іл, піролідин-2-іл, піролідин-3-іл; тетрагідрофураніл, такий як тетрагідрофуран-2-іл, тетрагідрофуран-3-іл; тетрагідропіраніл, такий як тетрагідропіран-2-іл, тетрагідропіран-3-іл, тетрагідропіран-4-іл; діоксоланіл, такий як 1,3-діоксоланіл; діоксаніл, такий як 1,4-діоксаніл, 1,3-діоксаніл; морфолініл, морфолініл-N-оксид, такий як морфолін-2-іл, морфолін-3-іл, морфолін-4-іл (морфоліно) (пронумерований, де кисню призначено пріоритет 1); тіоморфолініл, 1-оксо-тіоморфолін-4-іл, 1,1-діоксо-тіоморфолін-4-іл; імідазолініл, такий як імідазолідин-2-іл, імідазолідин-4-іл; піразолідиніл, такий як піразолідин-2іл, піразолідин-3-іл; піперидиніл або піперидиніл-N-оксид, такий як піперидин-1-іл та піперидин 3 UA 113470 C2 5 10 15 20 25 30 35 40 45 50 55 60 2-іл, піперидин-3-іл, піперидин-4-іл або його N-оксид; та піперазиніл, такий як піперазин-1-іл, піперазин-2-іл, піперазин-3-іл; октагідропіроло[3,4-b]піроліл. Термін "5- або 6-членне окси-вмісне гетероциклічне кільце", як застосовується у даному документі, відноситься до 5- або 6-членного ненасиченого кільця, що необов'язково містить один або два гетероатоми, незалежно вибрані з N, O або S, на додаток до кисневого 5 гетероатома, що зв'язує фенільне кільце та групу R у формулі (I) з іншими кільцевими атомами, що є атомами вуглецю. "5- або 6-членне окси-вмісне гетероциклічне кільце" переважно являє собою фуран, дигідрофуран, піран або дигідропіран. "Гідроксил" відноситься до радикала –OH. "Нітро" відноситься до радикала –NO2. "Меркапто" відноситься до радикала –SH. "Ціано" відноситься до радикала –CN. "Оксо" відноситься до радикала =O. "Карбоксил" відноситься до радикала –C(O)-OH. Термін "необов'язковий" або "необов'язково" означає, що подія або факт, описані далі, можуть відбуватися або можуть не відбуватися, і що опис включає випадки, коли відбувається подія або факт, і випадки, коли це не відбувається Наприклад, "необов'язково заміщений алкіл" охоплює як "незаміщений алкіл", так і "заміщений алкіл", визначені в даному документі. Передбачається, що фахівцям у даній галузі буде зрозуміло стосовно будь-якої групи, яка містить один або декілька замісників, що такі групи не включають будь-яке заміщення або патерни заміщення, які є стерично неможливими, хімічно некоректними, синтетично нездійсненними та/або нестабільними за своєю природою. Термін "заміщений", як застосовується у даному документі, означає, що один або декілька атомів водню на певних атомі або групі заміщені одним або декількома, вибраними із зазначеної групи замісників, за умов, що не перевищена нормальна валентність певного атома. Якщо замісником є оксо (тобто =O), то на окремому атомі заміщаються 2 водня. Комбінації замісників та/або змінних є припустимими, тільки якщо такі комбінації дають хімічно коректні та стабільні сполуки. Хімічно коректна та стабільна структура означає сполуку, яка достатньо стійка, щоб витримати виділення з реакційної суміші та подальше складання як засобу, який має щонайменше практичну застосовність. Якщо не вказано інше, замісників називають в основній структурі. Наприклад, має бути зрозумілим, що якщо у ролі можливого замісника згадується (циклоалкіл)алкіл, то точка приєднання цього замісника до основної структури розташована на алкільній частині. Термін "заміщений одним або декількома замісниками", як застосовується у даному документі, означає, що один або декілька атомів водню на певному атомі або групі незалежно заміщені одним або декількома, вибраними з зазначеної групи замісників. В деяких варіантах здійснення "заміщений одним або декількома замісниками" означає, що зазначений атом або група заміщені двома замісниками, незалежно вибраними із зазначеної групи замісників. В деяких варіантах здійснення "заміщений одним або декількома замісниками" означає, що зазначений атом або група заміщені трьома замісниками, незалежно вибраними із зазначеної групи замісників. В деяких варіантах здійснення "заміщений одним або декількома замісниками" означає, що зазначений атом або група заміщені чотирма замісниками, незалежно вибраними із зазначеної групи замісників. Фахівцям в даній галузі буде зрозуміло, що деякі зі сполук формули (I) можуть містити один або декілька хіральних центрів та, таким чином, існувати у двох або більше стереоізомерних формах. Рацемати цих ізомерів, окремі ізомери та суміші, збагачені одним енатіомером, а також діастереомери, якщо існують два хіральних центри, та суміші, частково збагачені конкретними діастереомерами, підпадають під об'єм даного винаходу. Крім того, фахівцям в даній галузі буде зрозуміло, що даний винахід передбачає усі їх окремі стереоізомери (наприклад, енантіомери), рацемічні суміші або частково розділені суміші сполук формули (I) та, якщо необхідно, окремі таутомерні форми. Можна застосовувати рацемати як такі або можна розділяти на їх окремі ізомери. Розділення може дати стереохімічно чисті сполуки або суміші, збагачені на один або декілька ізомерів. Способи відділення ізомерів добре відомі (cf. Allinger N. L. та Eliel E. L. in "Topics in стереоchemistry", Vol. 6, Wiley Interscience, 1971) та передбачають фізичні способи, такі як хроматографія із застосуванням хірального адсорбенту. Окремі ізомери можуть бути отримані у хіральній формі з хіральних попередників. Як альтернатива, окремі ізомери можуть бути відділені хімічно з суміші шляхом утворення діастереомерних солей хіральної кислоти, наприклад, окремі енантіомери 10-камфорсульфокислоти, камфорної кислоти, альфабромкамфорної кислоти, винної кислоти, діацетилвинної кислоти, яблучної кислоти, піролідон-5 4 UA 113470 C2 5 10 15 20 25 30 35 40 45 50 55 60 карбонової кислоти та подібні, фракційної кристалізації солей, а потім вилучення однієї або обох розділених основ, при необов'язковому повторенні процесу з отриманням таким чином однієї або обох практично вільних одна від іншої; тобто у формі з оптичною чистотою >95 %. Як альтернатива, рацемати можуть бути ковалентно зв'язані з хіральною сполукою (допоміжною сполукою) з утворенням діастереомерів, які можуть бути відділенні хроматографією або фракційною кристалізацією, після чого хіральну допоміжну сполуку хімічно видаляють з отриманням чистих енантіомерів. "Фармацевтично прийнятна сіль" включає без обмеження солі приєднання кислот, утворені сполукою формули (I) з неорганічною кислотою, такі як гідрохлорид, гідробромід, карбонат, бікарбонат, фосфат, сульфат, сульфіт, нітрат тощо; а також з органічною кислотою, такі як форміат, ацетат, малат, малеат, фумарат, тартрат, сукцинат, цитрат, лаклат, метансульфонат, п-толуолсульфонат, 2-гідроксіетилсульфонат, бензоат, саліцилат, стеарат та солі алкандикарбонової кислоти формули HOOC-(CH2)n-COOH, де n дорівнює 0-4, тощо. Також "фармацевтично прийнятна сіль" включає солі приєднання основ, утворені сполукою формули (I), що несе кислотний фрагмент, з фармацевтично прийнятними катіонами, наприклад, натрію, калію, кальцію, алюмінію, літію та амонію. Крім того, якщо сполуку, описану в даному документі, одержують у вигляді солі приєдання кислот, вільну основу можна одержувати підлужуванням розчину солі приєдання кислот. Навпаки, якщо продукт є вільною основою, сіль приєднання кислот, зокрема фармацевтично прийнятну сіль приєднання кислот, можна одержувати шляхом розчинення вільної основи в прийнятному розчиннику та обробки розчину кислотою згідно з традиційними процедурами одержання солей приєднання кислот з основних сполук. Фахівці в даній галузі встановлять різні методики синтезу, які можуть бути застосовані без зайвого експерименту для одержання нетоксичних фармацевтично прийнятних солей приєднання кислот. Термін "сольвати" означає форми приєднання сольвентів, що містять або стехіометричні, або нестехіометричні кількості сольвенту. Деякі сполуки мають тенденцію зберігати фіксоване молярне співвідношення сольвентних молекул у твердому стані з утворенням таким чином сольвату. Якщо сольвентом є вода, то утворений сольват являє собою гідрат, якщо сольвентом є спирт, то утворений сольват являє собою алкоголят. Гідрати утворюються шляхом комбінації однієї або декілька молекул води з однією з речовин, в яких вода зберігає свій молекулярний стан як H2O, при цьому така комбінація здатна утворювати один або декілька гідратів, наприклад, гемігідрати, моногідрат та дігідрат. "Проліки" являють собою сполуку, яка перетворюється на терапевтично активну сполуку після введення, та термін треба інтерпретувати в даному документі в широкому сенсі, як це зазвичай розуміється у рівні техніки. Без обмеження об'єму даного винаходу перетворення може відбуватися шляхом гідролізу естерної групи або певної іншої біологічно лабільної групи. В цілому, але не обов'язково, проліки є неактивними або менш активними, ніж терапевтично активна сполука, на яку вони перетворюються. Наприклад, естер може бути отриманий з карбонової кислоти C1 (тобто кінцевої карбонової кислоти природного простагландину) або естер може бути отриманий з карбоновокислотної функціональної групи на іншій частині молекулі, наприклад, на фенільному кільці. Без обмеження, естером може бути алкільний естер, арильний естер або гетероарильний естер. Як застосовується у даному документі, терміни "група", "радикал" або "фрагмент" є синонімами та включають функціональні групи або фрагменти молекул, що можуть приєднуватися до інших фрагментів молекул. Терміни "процес лікування", "лікувати" або "лікування" хвороби або порушення відносяться до введення однієї або декількох фармацевтичних речовин, зокрема щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаної у даному документі, суб'єкту, що страждає на хворобу або порушення, або має симптом хвороби або порушення, або схильний до хвороби або порушення, з метою виліковування, підліковування, полегшення, ослаблення, зміни, лікування, усунення, досягнення позитивної динаміки або впливу щодо хвороби або порушення, симптомів хвороби або порушення, або схильності до хвороби або порушення. У деяких варіантах здійснення захворюванням або порушенням є рак. Терміни "процес лікування", "приведення у контакт" та "приведення до реакції" по відношенню до хімічної реакції означають додавання або змішування двох або більше реагентів при відповідних умовах з отриманням зазначеного та/або бажаного продукту. Слід розуміти, що реакція, яка дає зазначений та/або бажаний продукт необов'язково може бути безпосередньо результатом комбінації двох реагентів, які додавали спочатку, тобто, може бути одна або декілька проміжних сполук, які утворюються у суміші, що в кінцевому рахунку веде до утворення 5 UA 113470 C2 5 10 15 20 25 30 35 40 45 50 55 зазначеного та/або бажаного продукту. Термін "ефективна кількість", як застосовується у даному документі, відноситься до кількості щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаної у даному документі, ефективної для "лікування", як визначено вище, хвороби або порушення у суб'єкта, який реагує на інгібування FGFR. Ефективна кількість може викликати будь-яку зі змін, яку можна спостерігати або вимірювати у суб'єкта, як описано вище у визначенні вищезазначених термінів "процес лікування", "лікувати" або "лікування". Наприклад, у випадку раку ефективна кількість може зменшувати число ракових або пухлинних клітин; зменшувати розмір пухлини; інгібувати або зупиняти інфільтрацію пухлинних клітин у периферичні органи, у тому числі, наприклад, поширення пухлини в м'яку тканину та кістку; інгібувати та зупиняти метастазування пухлини; інгібувати та зупиняти ріст пухлини; послабляти певною мірою один або декілька симптомів, асоційованих з раком, зменшувати захворюваність і смертність; покращувати якість життя або характеризуватися комбінацією таких ефектів. Ефективна кількість може бути кількістю, достатньою для зменшення симптомів захворювання, що реагує на інгібування FGFR. Термін "ефективна кількість" також може стосуватися кількості щонайменше однієї сполуки формули (I) та/або щонайменше однієї фармацевтично прийнятної солі, описаних у даному документі, ефективної для інгібування активності FGFR у суб'єкта, який реагує на інгібування FGFR. Термін "інгібування" або "процес інгібування" означає зниження вихідної активності біологічної активності або процесу. "Інгібування FGFR" відноситься до зниження активності FGFR як прямого або опосередкованого реагування на присутність щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаної у даному документі, відносно активності FGFR за відсутності щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі. Зниження активності може бути викликане прямою взаємодією щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаної у даному документі, з FGFR, або викликане взаємодією щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаної у даному документі, з одним або декількома іншими факторами, які у свою чергу впливають на активність FGFR. Наприклад, присутність щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаних у даному документі, може знижувати активність FGFR шляхом прямого зв'язування з FGFR, шляхом забезпечення (безпосередньо або опосередковано) іншого фактора для зниження активності FGFR або шляхом (прямо або опосередковано) зниження кількості FGFR, присутнього в клітині або організмі. Термін "суб'єкт" як застосовується у даному документі означає ссавців та відмінних від ссавців тварин. Ссавці передбачають будь-якого представника класу ссавців, у тому числі без обмеження людей; відмінних від людей приматів, таких як шимпанзе та інші людиноподібні мавпи і види мавп; сільськогосподарських тварин, таких як велика рогата худоба, коні, вівці, кози та свині; домашніх тварин, таких як кролі, собаки та кішки; лабораторних тварин, у тому числі гризунів, таких як щури, миші та морські свинки; та подібних. Приклади відмінних від ссавців тварин включають без обмеження птицю та подібних. Термін "суб'єкт" не визначає конкретні вік або стать. Термін "фармацевтично прийнятний" означає, що речовина, яка супроводжує цей термін, застосовна в отриманні фармацевтичної композиції та зазвичай є безпечною, нетоксичною, та не є ні біологічно, ні іншим чином небажаною, особливо для фармацевтичного застосування людиною. Термін "приблизно", що застосовується в даному документі, означає близько, біля, наближено або зразково. Якщо термін "приблизно" застосовується разом з числовим діапазоном, він модифікує цей діапазон шляхом розширення межі вище та нижче зазначених числових значень. В цілому, термін "приблизно" застосовується в даному документі для модифікації числового значення вище та нижче встановленого значення за допомогою дисперсії 20 %. Технічні та наукові терміни, застосовні в даному винаході та не визначені спеціально, мають значення, загальновідомі фахівцям в даній галузі, до якої належить даний винахід. Варіанти здійснення даного винаходу Згідно з одним аспектом даний винахід забезпечує сполуку формули (I): 6 UA 113470 C2 5 10 15 20 25 30 35 40 45 50 (I), та/або її проліки, енантіомери, діастереомери, таутомери або їх суміші у будь-якому співвідношенні, або її фармацевтично прийнятну сіль; де X являє собою СН2, Y вибраний з CH2, O або S(O)2; або X та Y разом зі зв'язком між ними утворюють -CH=CH- або -C≡C-; G являє собою N або CH; 1 R являє собою арил або гетероарил, кожний з яких необов'язково заміщений одним або 6 7 8 9 декількома замісниками, незалежно вибраними з галогену, -NR R , -OR , -S(O)nR , -(CH2)r10 6 7 6 10 6 9 6 11 12 6 8 C(O)R , -CN, -C(O)NR R , -NR C(O)R , -NR S(O)nR , -NR S(O)nNR R , -NR C(O)OR , 6 11 12 6 7 NR C(O)NR R , -NO2, -S(O)nNR R , оксо, необов'язково заміщеного алкілу, -(CH2)pнеобов'язково заміщеного циклоалкілу, -(CH2)m-необов'язково заміщеного гетероциклілу, (CH2)q-необов'язково заміщеного гетероарилу, необов'язково заміщеного алкенілу та необов'язково заміщеного алкінілу; 2 R незалежно вибраний з необов'язково заміщеного C1-C6алкілу, необов'язково заміщеного C1-C6алкоксі або необов'язково заміщеного C3-C8циклоалкілу; 3 4 R , R незалежно вибрані з водню, галогену, -CN або необов'язково заміщеного C1-C6алкілу, 5 R являє собою C1-C6алкіл, 3 5 5 або R та R разом з атомом О, до якого приєднаний R , та зі зв'язком між ними утворюють 5- або 6-членне окси-вмісне гетероциклічне кільце; n дорівнює 1 або 2; m, p, q та r незалежно вибрані з 0, 1, 2, 3, 4, 5, 6; 6 7 8 9 10 11 12 R , R , R , R , R , R та R незалежно вибрані з водню, алкілу, циклоалкілу, арилу, гетероарилу, гетероциклілу, кожен з яких, за виключенням водню, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з галогену, гідроксилу, меркапто, оксо, алкілу, циклоалкілу, гетероциклілу, необов'язково заміщеного аміно та необов'язково заміщеного аміду, де кожна вищезазначена необов'язково заміщена група, для якої замісник(и) спеціально не зазначений(і), може бути незаміщеною або незалежно заміщеною одним або декількома, наприклад, одним, двома або трьома, замісниками, незалежно вибраними з C1-C6алкілу, C2C6алкенілу, C2-C6алкінілу, циклоалкілу, арилу, гетероциклілу, гетероарилу, арил-C1-C6алкіл-, гетероарилC1-C6алкіл-, C1-C6галогеналкіл-, -OC1-C6алкілу, -OC2-C6алкенілу, -OC1-C6алкілфенілу, -C1-C6алкіл-OH, -C1-C6алкіл-SH, -C1-C6алкіл-O-C1-C6алкілу, -OC1-C6галогеналкілу, галогену, -OH, меркапто, -NH2, -C1-C6алкіл-NH2, -N(C1-C6алкіл)2, -NH(C1-C6алкіл), -N(C1-C6алкіл)(C1C6алкілфеніл), -NH(C1-C6алкілфеніл), ціано, нітро, оксо, -C(O)-OH, -C(O)OC1-C6алкілу, -CON(C1C6алкіл)2, -CONH(C1-C6алкіл), -CONH2, -NHC(O)(C1-C6алкіл), -NHC(O)(феніл), -N(C1C6алкіл)C(O)(C1-C6алкіл), -N(C1-C6алкіл)C(O)(феніл), -C(O)C1-C6алкілу, -C(O)C1-C6алкілфенілу, C(O)C1-C6галогеналкілу, -OC(O)C1-C6алкілу, -S(O)2-C1-C6алкілу, -S(O)-C1-C6алкілу, -S(O)2фенілу, -S(O)2-C1-C6галогеналкілу, -S(O)2NH2, -S(O)2NH(C1-C6алкілу), -S(O)2NH(феніл), NHS(O)2(C1-C6алкіл), -NHS(O)2(феніл) та -NHS(O)2(C1-C6галогеналкіл). Згідно з варіантом здійснення сполуки формули (I) кожна вищезазначена необов'язково заміщена група може бути незаміщеною або незалежно заміщеною одним або декількома замісниками, незалежно вибраними гідроксилу, меркапто, галогену, C1-C6алкілу, C2-C6алкенілу, C2-C6алкінілу, -OC1-C6алкілу, -NH2, N(C1-C6алкіл)2, -NH(C1-C6алкіл), ціано, нітро, оксо, -S(O)2-C1C6алкілу, -S(O)-C1-C6алкілу, -S(O)2-C1-C6галогеналкілу, -C(O)-OH, -C1-C6алкіл-OH, -C1-C6алкілSH, гетероциклілу. 1 Згідно з варіантом здійснення сполуки формули (I) R являє собою арил або гетероарил, кожний з яких необов'язково заміщений одним або декількома замісниками, незалежно вибраними з галогену, оксо, необов'язково заміщеного алкілу, -(CH2)m-необов'язково заміщеного гетероциклілу, -(CH2)p-необов'язково заміщеного циклоалкілу, -(CH2)q-необов'язково заміщеного 9 10 гетероарилу, -S(O)nR , -(CH2)r-C(O)R , необов'язково заміщеного алкенілу, необов'язково 8 заміщеного алкінілу, -OR , де n дорівнює 1 або 2; m, p, q та r незалежно вибрані з 0, 1, 2, 3, 4, 5, 8 9 10 6; R , R та R незалежно вибрані з водню, алкілу, гетероциклілу, кожен з яких, за виключенням 7 UA 113470 C2 5 10 15 20 25 30 35 40 45 50 55 водню, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з алкілу, оксо, гетероциклілу; де "необов'язково заміщений алкіл", "необов'язково заміщений гетероцикліл", "необов'язково заміщений циклоалкіл", "необов'язково заміщений гетероарил", "необов'язково 1 заміщений алкеніл" та "необов'язково заміщений алкініл" в вищезазначеному R можуть бути незаміщеними або незалежно заміщеними одним або декількома замісниками, незалежно вибраними з гідроксилу, меркапто, галогену, C1-C6алкілу, C2-C6алкенілу, C2-C6алкінілу, -OC1C6алкілу, -NH2, -N(C1-C6алкіл)2, -NH(C1-C6алкіл), ціано, нітро, оксо, -S(O)2-C1-C6алкілу, -S(O)-C1C6алкілу, -S(O)2-C1-C6галогеналкілу, -C(O)-OH, -C1-C6алкіл-OH, -C1-C6алкіл-SH, гетероциклілу. 1 Згідно з варіантом здійснення сполуки формули (I) R являє собою арил або гетероарил, кожний з яких необов'язково заміщений одним або декількома замісниками, незалежно вибраними з (1) галогену; (2) оксо; (3) алкілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з гідроксилу, меркапто, галогену, -OC1-C6алкілу, -NH2, N(C1-C6алкіл)2, -NH(C1-C6алкіл), ціано, нітро, -S(O)2-C1-C6алкілу, -S(O)-C1-C6алкілу, -C(O)-OH; (4) -(CH2)m-гетероциклілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C1-C6алкілу, -C1-C6алкіл-OH, -C1-C6алкіл-SH та оксо, де m дорівнює 0, 1, 2, 3, 4, 5 або 6; (5) -(CH2)p-незаміщеного циклоалкілу, де p дорівнює 0, 1, 2, 3, 4, 5 або 6; (6) -(CH2)qгетероарилу, необов'язково заміщеного одним або декількома замісниками, незалежно 9 9 вибраними з C1-C6алкілу, де q дорівнює 0, 1, 2, 3, 4, 5 або 6; (7) -S(O)nR , де R являє собою C110 10 C6алкіл, та n дорівнює 1 або 2; (8) -(CH2)r-C(O)R , де R являє собою гетероцикліл, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з C1C6алкілу та оксо, де r дорівнює 0, 1, 2, 3, 4, 5 або 6; (9) незаміщеного C2-C6алкенілу; (10) 8 8 незаміщеного C2-C6алкінілу; (11) -OR , де R вибраний з водню, алкілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з гетероциклілу. 1 Згідно з варіантом здійснення сполуки формули (I) R являє собою арил або гетероарил, кожний з яких необов'язково заміщений одним або декількома замісниками, незалежно вибраними з (1) галогену; 6 7 6 7 (2) –NR R , де R та R незалежно вибрані з водню та C1-C6алкілу, необов'язково заміщеного аміно, який необов'язково заміщений C1-C6алкілом; 8 8 (3) -OR , де R вибраний з водню та C1-C6алкілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з гетероциклілу, необов'язково заміщеного –OH або меркапто, та аміно, необов'язково заміщеного C1-C6алкілом, 9 9 (4) -S(O)nR , де R являє собою C1-C6алкіл, та n дорівнює 1 або 2; 10 10 (5) -(CH2)r-C(O)R , де R являє собою C1-C6алкіл або гетероцикліл, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з C1-C6алкілу та оксо, де r дорівнює 0, 1, 2, 3, 4, 5 або 6; (6) –CN; 6 7 6 7 (7) -C(O)NR R , де R та R незалежно вибрані з водню та C1-C6алкілу, необов'язково заміщеного аміно, який необов'язково заміщений C1-C6алкілом; 6 10 6 10 (8) –NR C(O)R , де R являє собою H, та R являє собою C1-C6алкіл; (9) оксо; (10) алкілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з гідроксилу, меркапто, галогену, -OC1-C6алкілу, -NH2, -N(C1-C6алкіл)2, -NH(C1C6алкіл), ціано, нітро, -S(O)2-C1-C6алкілу, -S(O)-C1-C6алкілу, -C(O)-OH; (11) -(CH2)p-незаміщеного циклоалкілу, де p дорівнює 0, 1, 2, 3, 4, 5 або 6; (12) -(CH2)m-гетероциклілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C1-C6алкілу, C3-C8циклоалкілу, -C1-C6алкіл-OH, -C1-C6алкіл-SH, -C1C6алкіл-O-C1-C6алкілу, -NH2, -N(C1-C6алкіл)2, -NH(C1-C6алкіл), оксо, -C(O)C1-C6алкілу, де m дорівнює 0, 1, 2, 3, 4, 5 або 6; (13) -(CH2)q-гетероарилу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C1-C6алкілу, де q дорівнює 0, 1, 2, 3, 4, 5 або 6; (14) незаміщеного C2-C6алкенілу; (15) незаміщеного C2-C6алкінілу. 1 Згідно з будь-якими з попередніх варіантів здійснення, R являє собою радикал кільця або кільцевої системи, вибраних з 8 UA 113470 C2 N H , кожний з яких необов'язково заміщений, як визначено вище. 1 Відповідно до будь-яких з попередніх варіантів здійснення, R вибраний з 5 N H , 10 15 20 кожний з яких необов'язково заміщений, як визначено вище. 8 Згідно з варіантом здійснення сполуки формули (I) R являє собою атом водню або C1C6алкіл, необов'язково заміщений гетероциклілом. 10 Згідно з варіантом здійснення сполуки формули (I) R являє собою гетероцикліл, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з C1C6алкілу та оксо. 1 Згідно з варіантом здійснення сполуки формули (I) R являє собою феніл, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з (1) галогену; (2) алкілу, необов'язково заміщеного за допомогою -C(O)-OH; (3) -(CH2)m-гетероциклілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C 1-C6алкілу, -C1C6алкіл-OH, -C1-C6алкіл-SH та оксо, де m дорівнює 0, 1, 2, 3, 4, 5 або 6; (4) -(CH2)q-гетероарилу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C 110 10 C6алкілу, де q дорівнює 0; (5) -(CH2)r-C(O)R , де R являє собою гетероцикліл, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з C 1-C6алкілу та оксо, де r 8 8 дорівнює 0; (6) незаміщеного C2-C6алкенілу; (7) незаміщеного C2-C6алкінілу; (8) -OR , де R вибраний з водню, алкілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з гетероциклілу. 1 Згідно з варіантом здійснення сполуки формули (I) R являє собою феніл, заміщений 9 UA 113470 C2 5 10 15 20 25 30 35 40 45 50 55 60 піперазинілом, при цьому піперазиніл необов'язково заміщений одним або декількома C 11 C6алкілами або C3-C8циклоалкілами, переважно C1-C6алкілом, більш переважно R являє собою феніл, заміщений піперазинілом, який необов'язково заміщений одним або декількома 1 метилами або етилами. Згідно з конкретним варіантом здійснення R являє собою феніл, заміщений піперазинілом, при цьому піперазиніл необов'язково заміщений одним або 1 декількома C1-C6алкілами. Згідно з більш конкретним варіантом здійснення R являє собою феніл, заміщений піперазинілом, який необов'язково заміщений одним або декількома метилами або етилами. 1 Згідно з варіантом здійснення сполуки формули (I) R являє собою піразоліл, який необов'язково заміщений одним або декількома замісниками, вибраними з (1) алкілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з гідроксилу, меркапто, галогену, -OC1-C6алкілу, -NH2, -N(C1-C6алкіл)2, -NH(C1-C6алкіл), -S(O)2-C1C6алкілу, -S(O)-C1-C6алкілу; (2) -(CH2)m-гетероциклілу, необов'язково заміщеного одним або декількома замісниками, незалежно вибраними з C1-C6алкілу, де m дорівнює 0, 1, 2, 3, 4, 5 або 6; (3) -(CH2)p-незаміщеного циклоалкілу, де p дорівнює 0, 1, 2, 3, 4, 5 або 6; (4) -(CH2)qгетероарилу, необов'язково заміщеного одним або декількома замісниками, незалежно 9 9 вибраними з C1-C6алкілу, де q дорівнює 0, 1, 2, 3, 4, 5 або 6; (5) -S(O)nR , де R являє собою C110 10 C6алкіл, та n дорівнює 1 або 2; (6) -(CH2)r-C(O)R , де R являє собою гетероцикліл, необов'язково заміщений одним або декількома замісниками, незалежно вибраними з C 1C6алкілу та оксо, де r дорівнює 0, 1, 2, 3, 4, 5 або 6. 2 Згідно з будь-яким з попередніх варіантів здійснення R вибраний з C1-C6алкілу, C1C6алкоксі, необов'язково заміщеного гідроксилом, або C 3-C8циклоалкілу (переважно C32 C6циклоалкілу). Згідно з конкретним варіантом здійснення R являє собою метил, етил, метоксі, етоксі, заміщений гідроксилом, ізопропоксі або циклопропіл. Згідно з конкретним варіантом 2 здійснення R являє собою метил. 3 4 Згідно з будь-яким з попередніх варіантів здійснення R , R незалежно вибрані з водню, 5 галогену, -CN або незаміщеного C1-C6алкілу (переважно незаміщеного C1-C3алкілу), R являє 3 5 собою C1-C6алкіл, переважно C1-C3алкіл, або R та R разом з атомом О, до якого приєднаний 5 R , та зі зв'язком між ними, утворюють 5- або 6-членне окси-вмісне гетероциклічне кільце. Згідно 3 4 з конкретним варіантом здійснення R являє собою водень, F, Cl, Br, –CN, метил, R являє 5 собою водень або F, R являє собою метил або етил. Згідно з іншим конкретним варіантом 4 3 5 5 здійснення R являє собою водень, та R та R разом з атомом О, до якого приєданий R , та зі зв'язком між ними утворюють фуранове або дигідрофуранове кільце. Згідно з конкретним варіантом здійснення сполука формули (I) вибрана зі сполук 1-309, отриманих у прикладах. У іншому аспекті даний винахід відноситься до фармацевтичної композиції, що містить щонайменше одну сполуку формули (I) та/або щонайменше одну її фармацевтично прийнятної сіль, описану у даному документі, та необов'язково щонайменше один фармацевтично прийнятний носій. У іншому аспекті даний винахід відноситься до способу in vivo або in vitro інгібування активності FGFR, що передбачає введення FGFR у контакт з ефективною кількістю щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаної у даному документі. У іншому аспекті даний винахід відноситься до способу лікування захворювання, яке реагує на інгібування FGFR, що передбачає введення суб'єкту, який потребує цього, ефективної кількості для лікування зазначеної хвороби щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаної у даному документі. У іншому аспекті даний винахід відноситься до застосування щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаної у даному документі, для лікування захворювання, яке реагує на інгібування FGFR. У іншому аспекті даний винахід відноситься до застосування щонайменше однієї сполуки формули (I) та/або щонайменше однієї її фармацевтично прийнятної солі, описаної у даному документі, у виготовленні медикаменту для лікування захворювання, що реагує на інгібування FGFR. Згідно з деякими варіантами здійснення зазначеною хворобою, яка реагує на інгібування FGFR, є рак, наприклад, рак легені, рак шлунку, рак печінки, рак молочної залози, рак яєчника, ендометріальна карцинома або карцинома сечового міхура. Сполука формули (I), описана в даному документі, та/або її фармацевтично прийнятна сіль може бути синтезована з комерційно доступних вихідних матеріалів за допомогою способів, добре відомих в даній галузі, разом з розкриттям даної патентної заявки. Наступні схеми 10 UA 113470 C2 ілюструють способи одержання деяких сполук, розкритих у даному документі. Схема I 5 10 15 Як показано на схемі I, сполуки формули (I) можуть бути отримані відновленням сполук формули (V). Відновлення можна здійснювати з воднем за присутності каталізатора, такого як паладій або платина тощо, або здійснювати з іншими відновлювачами, такими як 4метилбензолсульфоногідразид тощо. Сполуки формули (V) можуть бути отримані зі сполук формули (IV) шляхом амінолізної реакції без іншого реагенту або з іншим реагентом, таким як триметилалюміній. Згідно з іншими варіантами здійснення сполуки формули (I) можуть бути отримані зі сполук формули (III), які можуть бути отримані шляхом відновлення сполук формули (IV), способу з реакцією гідролізу, а потім з реакцією приєднання або іншими придатними 1 2 3 способами, які можуть бути відомими фахівцю в даній галузі. І R , R , і R зазначені у даному документі вище. Схема II 20 25 Як показано на схемі II, сполуки формули (VIII) можуть бути отримані зі сполук формули (VI) 1 2 3 за умов, описаних на схемі I. І R , R , R , і Y зазначені у даному документі вище. Одержані таким чином сполуки далі можуть бути модифіковані за їхніми периферичними положеннями з одержанням бажаних сполук. Синтетичні хімічні перетворення описані, наприклад, у R. Larock, Comprehensive Organic Transformations, VCH Publishers (1989); T.W. Greene and P.G.M. Wuts, 11 UA 113470 C2 rd 5 10 15 20 25 30 35 40 45 50 55 60 Protective Groups in Organic Synthesis, 3 Ed., John Wiley and Sons (1999); L. Fieser and M. Fieser, Fieser and Fieser's Reagents for Organic Synthesis, John Wiley and Sons (1994); та L. Paquette, ed., Encyclopedia of Reagents for Organic Synthesis, John Wiley and Sons (1995) та наступні їх видання. Перед застосуванням сполука формули (I) та/або її фармацевтично прийнятна сіль, описані в даному документі, можуть бути очищені за допомогою колонкової хроматографії, високоефективної рідинної хроматографії, кристалізації або іншими придатними способами. Фармацевтичні композиції та застосовність Композиція, що містить щонайменше одну сполуку формули (I) та/або щонайменше одну її фармацевтично прийнятну сіль, описані в даному документі, може бути введена різними відомими шляхами, такими як пероральний, парентеральний, за допомогою інгаляційного розпилення або через імплантований резервуар. Термін "парентеральний", як використовується у даному документі, включає техніки підшкірної, внутрішньошкірної, внутрішньовенної, внутрішньом'язової, внутрішньосуглобової, внутрішньоартеріальної, внутрішньосиновіальної, інтрастернальної, інтратекальної, внутрішньовогнищевої та внутрішньочерепної ін'єкції або інфузії. Пероральна композиція може являти собою будь-яку лікарську форму, прийнятну для перорального введення, включаючи без обмеження таблетки, капсули, емульсії та водні суспензії, дисперсії та розчини. Традиційно застосовувані носії для таблеток включають лактозу та кукурудзяний крохмаль. Як правило, у таблетки також додають змащувальні засоби, такі як стеарат магнію. Для перорального введення у формі капсул придатні розріджувачі включають лактозу та сухий кукурудзяний крохмаль. Якщо водні суспензії або емульсії вводяться перорально, то активний інгредієнт може бути суспендованим або розчиненим у масляній фазі, поєднаній з емульгувальними або суспендувальними засобами. За необхідності можуть бути додані певні підсолоджувачі, ароматизатори або барвники. Стерильна композиція для ін'єкції (наприклад, водна суспензія або масляна суспензія) може бути складена згідно з техніками, відомими у даній галузі, з використанням прийнятних диспергувальних або змочувальних засобів (таких як, наприклад, Tween 80) і суспендувальних засобів. Стерильна проміжна сполука для ін'єкції також може являти собою стерильний розчин або суспензію для ін'єкції в нетоксичному розріджувачі або розчиннику, прийнятних для парентерального введення, наприклад, у вигляді розчину в 1,3-бутандіолі. З числа фармацевтично прийнятних середовищ та розчинників можна застосовувати маніт, воду, розчин Рінгера та ізотонічний розчин хлориду натрію. Крім того, стерильні нелеткі масла традиційно використовуються як розчинник або суспендувальне середовище (наприклад, синтетичні моно- або дигліцериди). Жирні кислоти, такі як олеїнова кислота та її гліцеридні похідні, застосовні у проміжних сполуках ін'єкційних препаратів, так само як і природні фармацевтично прийнятні олії, такі як оливкова олія або рицинова олія, особливо в їх поліоксиетильованих формах. Дані масляні розчини або суспензії також можуть містити довголанцюговий спиртовий розріджувач або дисперсант, або карбоксиметилцелюлозу, або подібні засоби для диспергування. Інгаляційна композиція може бути отримана згідно з техніками, добре відомими в галузі одержання фармацевтичних препаратів, і може бути отримана у вигляді розчинів у фізіологічному розчині з використанням бензилового спирту або інших прийнятних консервантів, стимуляторів абсорбції для посилення біодоступності, фторвуглеців та/або інших засобів, що розчиняють, або диспергувальних засобів, відомих у даній галузі техніки. Композиція для місцевого застосування може бути складена у формі масла, крему, лосьйону, мазі тощо. Придатні носії для композиції включають рослинні або мінеральні масла, медичний вазелін (білий м'який парафін), жири або масла з розгалуженим ланцюгом, тваринні жири та високомолекулярні спирти (більше C12). У деяких варіантах здійснення фармацевтично прийнятним носієм є носій, у якому розчиняється активний інгредієнт. Також можуть бути включені емульгатори, стабілізатори, зволожувальні засоби та антиоксиданти, а також засоби, що надають колір або аромат, за необхідності. Крім того, у таких складах для місцевого застосування можуть бути використані підсилювачі черезешкірної проникності. Приклади таких підсилювачів можна знайти у патентах США №№ 3989816 та 4444762. Креми можуть бути складені із суміші мінерального масла, самоемульгувального бджолиного воску та води, у яку підмішана суміш активного інгредієнта, розчиненого в невеликій кількості олії, такої як мигдальна олія. Приклад такого крему включає за вагою приблизно 40 частин води, приблизно 20 частин бджолиного воску, приблизно 40 частин мінерального масла та приблизно 1 частину мигдальної олії. Мазі можуть бути складені шляхом змішування розчину 12 UA 113470 C2 5 10 15 20 25 30 35 40 45 50 55 60 активного інгредієнта в рослинній олії, такій як мигдальна олія, з теплим м'яким парафіном і забезпечення охолодження суміші. Прикладом такої мазі є мазь, яка включає приблизно 30 % за вагою мигдальної олії і приблизно 70 % за вагою білого м'якого парафіну. Фармацевтично прийнятний носій стосується носія, який є сумісним з активними інгредієнтами композиції (а у деяких варіантах здійснення, здатним стабілізувати активні інгредієнти) і нешкідливим для суб'єкта, який підлягає лікуванню. Наприклад, солюбілізувальні засоби, такі як циклодекстрини (які утворюють специфічні, більш розчинні комплекси зі сполукою формули (I) та/або її фармацевтично прийнятною сіллю, описаною в даному документі), можуть застосовуватися як фармацевтичні допоміжні засоби для доставки активних інгредієнтів. Приклади інших носіїв включають колоїдний діоксид кремнію, стеарат магнію, целюлозу, лаурилсульфат натрію та барвники, такі як D&C Yellow № 10. Прийнятні in vitro аналізи можуть використовуватися для попередньої оцінки ефективності сполуки формули (I) та/або її фармацевтично прийнятної солі, описаної в даному документі, щодо інгібування активності FGFR кінази. Сполуку формули (I) та/або її фармацевтично прийнятну сіль, описані в даному документі, можна додатково перевірити щодо ефективності лікування запального захворювання за допомогою in vivo аналізів. Наприклад, сполуку формули (I) та/або її фармацевтично прийнятну сіль, описані в даному документі, можна ввести тварині (наприклад, мишачій моделі), що страждає запальним захворюванням, та оцінити їх терапевтичні ефекти. На підставі результатів також може бути визначений належний діапазон доз та метод введення для тварин, таких як людина. Сполуку формули (I) та/або її фармацевтично прийнятну сіль, описані в даному документі, можна використовувати для досягнення сприятливого терапевтичного або профілактичного ефекту, наприклад у суб'єктів, хворих на рак. Як застосовується у даному документі, термін "рак" відноситься до клітинного порушення, що характеризується неконтрольованою або дисрегульованою клітинною проліферацією, зниженим клітинним диференціюванням, неприпустимою здатністю уражати оточувальну тканину та/або здатністю заново проростати на ектопічні ділянки. Термін "рак" передбачає без обмеження солідні пухлини та гемобластози. Термін "рак" охоплює хвороби шкіри, тканин, органів, кісток, хрящів, крові та судин. Термін "рак", крім того, охоплює первинний та метастатичний типи раку. Необмежувальні приклади солідних пухлин включають рак підшлункової залози; рак сечового міхура; колоректальний рак; рак молочної залози, у тому числі метастатичний рак молочної залози; рак простати, у тому числі андроген-залежний та андроген-незалежний рак простати; рак нирки, у тому числі, наприклад, метастатична нирковоклітинна карцинома; гепатоклітинний рак; рак легені, у тому числі, наприклад, недрібноклітинний рак легені (NSCLC), бронхіолоальвеолярна карцинома (BAC) та аденокарцинома легені; рак яєчника, у тому числі, наприклад, прогресуючий епітеліальний або первинний перитонеальний рак; цервікальний рак; шлунково-кишковий рак; рак стравоходу; рак голови та шиї, у тому числі, наприклад, сквамозноклітинна карцинома голови та шиї; рак шкіри, у тому числі, наприклад, злоякісна меланома; нейроендокринний рак, у тому числі метастатичні нейроендокринні пухлини; пухни мозку, у тому числі, наприклад, гліома, анапластична олігодендрогліома, мультиформна гліобластома дорослих та анапластична астроцитома дорослих; рак кістки; саркома м'яких тканин та тиреокарцинома. Необмежувальні приклади гематологічних злоякісних захворювань включають гострий мієлоїдний лейкоз (AML); хронічний мієлогенний лейкоз (CML), у тому числі прискорений CML та CML у бластній фазі (CML-BP); гострий лімфобластний лейкоз (ALL); хронічний лімфоцитарний лейкоз (CLL); хворобу Ходжкіна (HD); неходжкінську лімфому (NHL), у тому числі фолікулярну лімфому та лімфому мантильних клітин; B-клітинну лімфому; T-клітинну лімфому; множинну мієлому (MM); макроглобулінемію Вальденстрема; мієлодиспластичні синдроми (MDS), у тому числі рефракторну анемію (RA), рефракторну анемію з кільцеподібними сидеробластами (RARS), (рефракторну анемію з надлишком бластів (RAEB) та RAEB в трансформації (RAEB-T) та мієлопроліферативні синдроми. У деяких варіантах здійснення приклади раку, що належить лікуванню, включають без обмеження рак легені (такий як сквамозний недрібноклітинний рак легені (NSCLC), дрібноклітинний рак легені (SCLC)), рак шлунка, рак печінки, рак молочної залози, рак яєчника, ендометріальну карциному та карциноми сечового міхура. У деяких варіантах здійснення сполуку формули (I) та/або її фармацевтично прийнятну сіль, описані в даному документі, вводять у комбінації з іншим терапевтичним засобом. У деяких варіантах здійснення іншим терапевтичним засобом є засіб, який зазвичай вводять пацієнтам із захворюванням або станом, який лікують. Cполуку формули (I) та/або її фармацевтично прийнятну сіль, описані в даному документі, можна вводити з іншим терапевтичним засобом в 13 UA 113470 C2 5 10 15 20 25 30 35 40 45 одній лікарській формі або у вигляді окремої лікарської форми. При введенні у вигляді окремої лікарської форми інший терапевтичний засіб можна вводити перед, одночасно або після введення сполуки формули (I) та/або її фармацевтично прийнятної солі, описаних у даному документі. У деяких варіантах здійснення сполуку формули (I) та/або її фармацевтично прийнятну сіль, описані в даному документі, вводять у комбінації з протинеопластичним засобом. Як застосовується у даному документі, термін "протипухлинний засіб" відноситься до будь-якого засобу, що вводять суб'єкту, що страждає на рак, з метою лікування раку. Необмежувальні приклади протипухлинних засобів включають радіотерапію; імунотерапію; хіміотерапевтичні засоби, що пошкоджують ДНК, та хіміотерапевтичні засоби, що порушують розмноження клітин. Необмежувальні приклади хіміотерапевтичні засоби, що пошкоджують ДНК, включають інгібітори топоізомерази I (наприклад, іринотекан, топотекан, камптотецин і його аналоги або метаболіти та доксорубіцин); інгібітори топоізомерази II (наприклад, етопозид, теніпозид та даунорубіцин); алкілувальні засоби (наприклад, мелфалан, хлорамбуцил, бусульфан, тіотепа, іфосфамід, кармустин, ломустин, семустин, стрептозоцин, декарбазин, метотрексат, мітомуцин C та циклофосфамід); інтеркалятори ДНК (наприклад, цисплатин, оксаліплатин та карбоплатин); інтеркалятори ДНК та генератори вільних радикалів, такі як блеоміцин; та нуклеозидні міметики (наприклад, 5-фторурацил, капецитибін, гемцитабін, флударабін, цитарабін, меркаптопурин, тіогуанін, пентостатин та гідроксисечовина). Хіміотерапевтичні засоби, що порушують розмноження клітин, включають паклітаксел, доцетаксел та родинні аналоги; вінкристин, вінбластин та родинні аналоги; талідомід та родинні аналоги (наприклад, CC-5013 та CC-4047); інгібітори протеїнтирозинкінази (наприклад, іматиніб мезилат та гефітиніб); інгібітори протеасоми (наприклад, бортезоміб); інгібітори NF-каппа B, у тому числі інгібітори I каппа B кінази; антитіла, які зв'язуються з білками, що надекспресуються при різновидах раку та тим самим негативно регулюють розмноження клітин (наприклад, трастузумаб, ритуксимаб, цетуксимаб та бевацизумаб); та інші інгібітори білків або ферментів, які, як відомо, позитивно регулюються, надекспресуються або активуються при різновидах раку, інгібування яких негативно регулює розмноження клітин. Приклади Нижченаведені приклади призначені виключно для ілюстрації та не повинні розглядатися як будь-яким чином обмежувальні. Були докладені зусилля для забезпечення точності щодо застосовуваних чисел (наприклад, кількостей, температури тощо), але повинні враховуватися деякі експериментальні помилки та відхилення. Якщо не зазначене інше, частини є частинами за вагою, температура наведена у градусах Цельсію, а тиск є атмосферним або близьким до 1 такого. Усі дані MS були перевірені за допомогою Agilent 6120 та/або Agilent 1100. H-ЯМР спектри реєстрували на приладі, що працює при 400 МГц. ЯМР спектри зрізків в розчинах CDCl 3 (зареєстровані у ppm) отримували із застосуванням хлороформу як еталонного стандарту (7,26 ppm) або тетраметилсилану як внутрішнього стандарту (0,00 ppm) за необхідності. При потребі використовували інші розчинники для ЯМР. Якщо реєструються пікові множинності, застосовуються наступні абревіатури: s (сінглет), d (дуплет), t (триплет), m (мультиплет), q (квартет), br (розширений), dd (дуплет дуплетів), dt (дуплет триплетів). Константи зв'язку, якщо приводяться, виражаються у герцах (Гц). Усі реагенти, за винятком проміжних сполук, застосовані у даному винаході, є комерційно доступними. Усі назви сполук, за винятком реагентів, складені за допомогою Chemdraw. Крім того, для зручності та для чіткого зрозуміння фахівцями даної галузі, не усі атоми водню були спеціально зазначені як такі, що зв'язуються з кожним атомом вуглецю та/або азоту. Наприклад, сполука 16 позначається формулою у нижченаведеному прикладі 3, де не був вказаний один атом водню, що зв'язується з атомом азоту між піримідиновим кільцем та фенільним кільцем. Відповідно, ця формула представляє ту O O N H N N O 50 N N N H саму сполуку, що й формула . У наступних прикладах застосовуються нижченаведені абревіатури 14 UA 113470 C2 5 10 15 20 25 AIBN a, a'-азо-ізобутироннітрил CCl4 перхлорметан DCM дихлорметан DEAD діетилазодикарбоксилат DIPEA N, N-діізопропілетиламін DMF N, N-диметилформамід EA етилацетат год. година(и) HATU O-(7-азабензотриазол-1-іл)-N, N,N',N'-тетра-метилуронію гексафторфосфат ISCO комбінована флеш-хроматографія KHMDS калію біс(триметилсиліл)амід мл мілілітр(и) хв. хвилина(и) MeOH метанол NBS N-бромсукцинімід NIS N-йодсукцинімід PE петролейний етер Pd(dppf)Cl2·CH2Cl2 1,1'-біс(дифенілфосфіно)фероцен-паладію(II) дихлорид дихлорметановий комплекс Pd(PPh3)4 тетракіс(трифенілфосфін)паладій(0) PdCl2(PPh3)2 біс(трифенілфосфін)паладій(II)дихлорид PPh3 трифенілфосфін PTLC препаративна тонкошарова хроматографія THF тетрагідрофуран TFA трифтороцтова кислота ксантофос 4,5-біс(дифенілфосфіно)-9,9-диметилксантен Проміжна сполука 1 Водн. NaOH Метил-3-бром-4-фтор-5-метоксибензоат 30 35 40 45 50 (A) 3-Бром-4-фтор-5-йодбензойна кислота До суміші 3-бром-4-фторбензойної кислоти (45 г, 0,21 моля) у H2SO4 (96 %, 150 мл) порціями додавали NIS (50 г, 0,22 моля) при 0 °C за 30 хв. Суміш перемішували при кімнатній температурі протягом 2 годин. Потім суміш розбавляли льодяною водою, фільтрували. Відфільтрований матеріал промивали льодяною водою, сушили з отриманням названої сполуки у вигляді жовтої твердої речовини (60 г, 84,7 % вихід). MS (маса/заряд): 342,7, 344,7 (M-H) . (B) 3-Бром-4-фтор-5-гідроксибензойна кислота Суміш 3-бром-4-фтор-5-йодбензойної кислоти (60 г, 0,17 моля), Cu2O (3,0 г, 0,021 моля) та NaOH (35 г, 0,88 моля) у воді (600 мл) нагрівали при 100 °C протягом 16 годин. Потім реакційну суміш охолоджували при кімнатній температурі та фільтрували. Фільтрат підкислювали водн. HCl (5 N) та екстрагували за допомогою EA. Органічний шар відділяли, концентрували та сушили з отриманням названої сполуки у вигляді жовтої твердої речовини (35 г, 85,6 % вихід). (C) Метил-3-бром-4-фтор-5-метоксибензоат До суміші 3-бром-4-фтор-5-гідроксибензойної кислоти (35 г, 0,15 моля) та K2CO3 (45 г, 0,32 моля) у DMF (150 мл) додавали йодметан (45 г, 0,32 моля) при кімнатній температурі. Суміш перемішували при 80 °C протягом 4 годин. Потім суміш розбавляли водою, екстрагували за допомогою EA. Органічний шар відділяли та концентрували, а потім залишок очищали хроматографією на сілікагелі (PE/EA) з отриманням названої сполуки у вигляді білої твердої + речовини (15 г, 38,3 % вихід). MS (маса/заряд): 263,2, 265,2 (M+H) . Наступні проміжні сполуки отримували за процедурами з проміжною сполукою 1 із застосуванням відповідних проміжних сполук та реагентів при відповідних умовах, що будуть відомі фахівцю в даній галузі. 55 15 UA 113470 C2 Проміжна сполука Структура MS (маса/заряд) (M+H) 2 199,1 3 215,0 4 245,0/247,0 5 259,0/261,0 6 262,8/264,8 7 278,9/280,9 8 + 297,0/299,0 Проміжна сполука 9 Метил-4-бром-3-йод-5-метоксибензоат Водн. NaOH 5 10 (A) 4-Бром-3,5-дийодбензойна кислота До суміші 4-бромбензойної кислоти (2,7 г, 13 ммолей) у H 2SO4 (96 %, 50 мл) порціями додавали NIS (7,5 г, 33 ммоля) при 0 °C за 15 хвилин та утворену суміш перемішували при кімнатній температурі протягом 2 годин. Потім суміш розбавляли льодяною водою, потім водним розчином Na2SO3. Потім суміш фільтрували. Відфільтрований матеріал промивали льодяною водою, сушили з отриманням названої сполуки у вигляді світло-рожевої твердої 16 UA 113470 C2 5 10 15 20 25 30 35 40 речовини (5,8г, 95,4 % вихід). MS (маса/заряд): 450,5, 452,5 (M-H) . (B) 4-Бром-3-гідрокси-5-йодбензойна кислота Суміш 4-бром-3,5-дийодбензойної кислоти (3,0 г, 6,6 ммоля), Cu2O (0,10 г, 0,70 ммоля) та NaOH (1,4 г; 35 ммоля) у воді (30 мл) нагрівали при 80 °C протягом 3 годин. Потім реакційну суміш розбавляли водою, підкисляли за допомогою водн. HCl (10 N), потім фільтрували. Відфільтрований матеріал промивали льодяною водою та сушили з отриманням названої сполуки у вигляді жовтої твердої речовини (1,8 г, 79,2 % вихід). MS (маса/заряд): 340,6, 342,6 (M-H) . (C) Метил-4-бром-3-йод-5-метоксибензоат До суміші 4-бром-3-гідрокси-5-йодбензойної кислоти (1,8 г, 5,3 ммоля) та K 2CO3 (1,8 г, 13 ммолей) у DMF (30 мл) додавали йодметан (1,7 г, 12 ммолей) при кімнатній температурі, а потім суміш перемішували при 80 °C протягом 4 годин. Потім суміш розбавляли водою, екстрагували за допомогою EA. Органічний шар відділяли та концентрували з отриманням названої сполуки у + вигляді сірої твердої речовини (1,9 г, 97,6 % вихід). MS (маса/заряд): 370,7, 372,7 (M+H) . Проміжна сполука 10 3-Бром-N, 5-диметоксибензамід (A) 3-Бром-5-йод-N-метоксибензамід До розчину 3-бром-5-йодбензойної кислоти (5,0 г, 15 ммолей) та метоксиламіну гідрохлориду (1,3 г, 16 ммоль) у DCM (70 мл) додавали HATU (7,0 г, 18 ммолей) та DIPEA (4,0 г, 31 ммоль). Отриману суміш перемішували при кімнатній температурі протягом 16 годин, розбавляли водою та екстрагували за допомогою DCM. Об'єднані органічні шари концентрували, а залишок очищали хроматографією на сілікагелі (DCM/MeOH) з отриманням названої сполуки у вигляді білої твердої речовини (4,2 г, 77,1 % вихід). MS (маса/заряд): 356,2, + 358,2 (M+H) . (B) 3-Бром-N, 5-диметоксибензамід Суміш 3-бром-5-йод-N-метоксибензаміду (3,6 г, 10 ммоля), CuI (0,20 г, 1,1 ммоля), 1,10фенантроліну (0,38 г, 2,1 ммоля) та Cs2CO3 (4,6 г, 14 ммолей) у MeOH (20 мл) нагрівали при 100 °C протягом 1 години у мікрохвилях. Потім суміш фільтрували та відфільтрований матеріал промивали за допомогою MeOH (20 мл). Фільтрат концентрували та залишок очищали хроматографією на сілікагелі (PE/EA) з отриманням названої сполуки у вигляді твердої + речовини кавового кольору (1,1 г, 41,8 % вихід). MS (маса/заряд): 262,0, 260,0 (M+H) . Проміжна сполука 11 Метил-2,4-дифтор-5-метокси-3-метилбензоат (A) Метил-2,4-дифтор-5-метокси-3-метилбензоат До розчину метил-4-фтор-3-метокси-5-метилбензоат (5,0 г, 25,23 ммоля) та 1-(хлорметил)-4фтор-1,4-діазабіцикло[2.2.2]октан-1,4-діій тетрафторборату (9,8 г, 27,66 ммоля) в ацетонітрилі (150 мл) додавали оцтову кислоту (30 мл) та отриману суміш перемішували при 70 °C протягом 18 годин в атмосфері азоту. Леткі речовини видаляли при зниженому тиску та залишок очищали колонковою хроматографією на сілікагелі (елюювали з EA у PE 0~100 %) з отриманням названої + сполуки у вигляді білої твердої речовини (1,50 г, 27,5 % вихід). MS (маса/заряд): 217,0 (M+H) . Проміжна сполука 12 Метил-3-(бромметил)-4-хлор-5-метоксибензоат 17 UA 113470 C2 5 10 (A) Метил-3-(бромметил)-4-хлор-5-метоксибензоат До розчину метил-4-хлор-3-метокси-5-метилбензоату (2,00 г, 9,32 ммоля) в CCl4 (40 мл) додавали NBS (1,99 г, 11,18 ммоля) та AIBN (153 мг, 0,93 ммоля). Потім суміш перемішували при 70 °C протягом ночі. Після охолодження при кімнатній температурі суміш розподіляли між DCM та водою. Водний шар екстрагували за допомогою DCM. Об'єднані органічні шари промивали водою та сольовим розчином, сушили над безводним натрію сульфатом та концентрували. Залишок суспендували в PE (5 мл) та перемішували протягом 1 години при кімнатній температурі. Після фільтрації відфільтрований матеріал промивали з PE (2*2 мл), сушили при зниженому тиску при 60 °C протягом 1 години з отриманням жовтої твердої + речовини (2,66 г, 97,3 % вихід). MS (маса/заряд): 293,0/295,0 (M+H) . Наступну проміжну сполуку отримували за процедурами з проміжною сполукою 12 із застосуванням відповідних проміжних сполук та реагентів при відповідних умовах, які відомі фахівцю в даній галузі. 15 Проміжна сполука Структура MS (маса/заряд) (M+H) 13 277,0/279,0 14 + 295,3/297,3 Проміжна сполука 15 1-Етил-1H-піразол-4-амін 20 25 30 (A) 1-Етил-1H-піразол-4-амін До розчину 4-нітро-1H-піразолу (500 мг, 4,42 ммоля) у безводному THF (20 мл) порціями додавали NaH (60 % дисперсія у мінеральному маслі, 353 мг, 8,84 ммоля) при 0 °C. Отриману суміш перемішували при 0 °C протягом 10 хвилин. Потім краплями додавали 1-брометан (723 мг, 6,64 ммоля) у безводному THF (2 мл) при 0 °C. Суміш перемішували при температурі середовища протягом 16 годин. Потім реакцію гасили за допомогою H 2O (20 мл) та видаляли леткі речовини при зниженому тиску. Отриманий водний шар екстрагували за допомогою EA (2*30 мл). Об'єднані екстракти концентрували при зниженому тиску. Залишок розчиняли в MeOH (30 мл), а потім додавали Pd/C (10 %, 100 мг). Суміш перемішували при температурі середовища в атмосфері водню протягом 16 годин. Каталізатор відфільтровували. Фільтрат концентрували та залишок очищали за допомогою ISCO (елюювали з MeOH в H 2O 0~100 %) з отриманням названої сполуки у вигляді коричневого масла (260 мг, 52,9 % вихід, 2 стадії). MS + (маса/заряд): 112,1 (M+H) . Проміжна сполука 16 (R)-Трет-бутил-3-(4-аміно-1H-піразол-1-іл)піперидин-1-карбоксилат 18 UA 113470 C2 5 10 15 (A) (R)-Трет-бутил-3-(4-нітро-1H-піразол-1-іл)піперидин-1-карбоксилат До розчину 4-нітро-1H-піразолу (1, 2,0 г, 17,7 ммоля), (S)-трет-бутил-3-гідроксипіперидин-1карбоксилату (4,2 г, 21,2 ммоля) та PPh3 (6,9 г, 26,6 ммоля) у THF (35 мл) краплями додавали DEAD (4,6 г, 26,6 ммоля) з охолодженням у бані з льодяною водою. Після додавання суміш перемішували при кімнатній температурі ще 12 годин. Отриману суміш концентрували in vacuo. Залишок очищали хроматографією на сілікагелі (елюювали з EA в PE 0–60 %) з отриманням + жовтого масла (2,5 г, 47,7 % вихід). MS (маса/заряд): 197,0 (M+H-100) . (B) (R)-Трет-бутил-3-(4-аміно-1H-піразол-1-іл)піперидин-1-карбоксилат Суміш (R)-трет-бутил-3-(4-нітро-1H-піразол-1-іл)піперидин-1-карбоксилату (1,0 г, 3,37 ммоля) та Pd/C (5 %, 200 мг) у MeOH (20 мл) перемішували при 1 атм. H2 при кімнатній температурі протягом 12 годин. Отриману суміш фільтрували та фільтрат концентрували in vacuo з + отриманням коричневого масла (920 мг, кількісний вихід). MS (маса/заряд): 267,0 (M+H) . Наступні проміжні сполуки отримували за процедурами з проміжною сполукою 16 із застосуванням відповідних проміжних сполук та реагентів при відповідних умовах, що будуть відомі фахівцю в даній галузі. Проміжна сполука Структура MS (маса/заряд) (M+H) 17 140,0 18 154,0 19 154,1 20 168,0 21 182,9(M+H-56) 22 153,0(M+H-100) + 23 153,1(M+H-100) + 24 167,0(M+H-100) + 25 267,1 19 + + UA 113470 C2 Проміжна сполука 26 (R)-1-(4-Аміно-1H-піразол-1-іл)пропан-2-ол 5 10 15 20 (A) (R)-1-(4-Нітро-1H-піразол-1-іл)пропан-2-ол До розчину 4-нітро-1H-піразолу (500 мг, 4,42 ммоля) у DMF (5 мл) додавали (R)-2метилоксиран (282 мг, 4,86 ммоля) та K2CO3 (1,2 г, 8,84 ммоля). Отриману суміш перемішували при 60 °C у закритій пробірці протягом 16 годин. Реакційну суміш розподіляли між H 2O (30 мл) та EA (30 мл). Органічний шар концентрували та очищали за допомогою ISCO (PE/ EA) з отриманням названої сполуки у вигляді безкольорового масла (360 мг, 47,6 % вихід). MS + (маса/заряд): 171,9 (M+H) . (B) (R)-1-(4-Аміно-1H-піразол-1-іл)пропан-2-ол До розчину (R)-1-(4-нітро-1H-піразол-1-іл)пропан-2-олу (140 мг, 0,82 ммоля) у MeOH (30 мл) додавали Pd/C (10 %, 50 мг). Суміш перемішували при температурі середовища в атмосфері водню протягом 16 годин. Каталізатор відфільтровували та фільтрат концентрували з отриманням названої сполуки у вигляді коричневого масла (115 мг, 0,82 ммоля, кількісний + вихід). MS (маса/заряд): 142,1 (M+H) . Наступну проміжну сполуку отримували за процедурами з проміжною сполукою 26 із застосуванням відповідних проміжних сполук та реагентів при відповідних умовах, які відомі фахівцю в даній галузі. Проміжна сполука Структура 27 MS (маса/заряд) (M+H) + 142,0 Проміжна сполука 28 3-(4-Етилпіперазин-1-іл)анілін 25 30 35 40 (A) 1-Етил-4-(3-нітрофеніл)піперазин Суміш 1-етилпіперазину (3,23 г, 0,0283 моля) та 1-фтор-3-нітробензолу (2,0 г, 0,0142 моля) нагрівали із зворотним холодильником протягом 2 днів. Отриману суміш охолоджували та концентрували in vacuo. Залишок вливали у воду (50 мл), екстрагували за допомогою EA (2*50 мл). Об'єднані екстракти промивали сольовим розчином, концентрували in vacuo. Залишок очищали за допомогою ISCO (елюювали з EA у PE 0-70 %) з отриманням жовтої твердої + речовини (1,80 г, 54,0 % вихід). MS (маса/заряд): 236,1 (M+H) . (B) 3-(4-Етилпіперазин-1-іл)анілін Суміш 1-етил-4-(3-нітрофеніл)піперазину (1,8 г, 0,00765 моля) та Rany-Ni (1,0 г) у MeOH (20 мл) перемішували в 1 атм. H2 при кімнатній температурі протягом 6 годин. Отриману суміш фільтрували та фільтрат концентрували in vacuo з отриманням сірої завісі (1,5 г, 95,5 % вихід). + MS (маса/заряд): 206,2 (M+H) . Наступні проміжні сполуки отримували за процедурами з проміжною сполукою 28 із застосуванням відповідних проміжних сполук та реагентів при відповідних умовах, що будуть відомі фахівцю в даній галузі. Проміжна сполука Структура 29 MS (маса/заряд) (M+H) 178,1 20 + UA 113470 C2 Проміжна сполука Структура MS (маса/заряд) (M+H)+ 30 206,1 Проміжна сполука 31 5-Бром-N-(4-((3R, 5S)-3,5-диметилпіперазин-1-іл)феніл)піримідин-2-амін 5 10 15 (A) 5-Бром-N-(4-((3R, 5S)-3,5-диметилпіперазин-1-іл)феніл)піримідин-2-амін Суміш 5-бром-2-хлорпіримідину (392 мг, 2,03 ммоля), 4-((3R, 5S)-3,5-диметилпіперазин-1іл)аніліну (416 мг, 1,968 ммоля) та TFA (0,5 мл, 6,09 ммоля) у пропан-2-олі (5 мл) перемішували при 150 °C протягом 80 хвилин у мікрохвилях. Отриману суміш концентрували, підвищували основність за допомогою аміачної води, очищали за допомогою ISCO (DCM/MeOH) з отриманням названої сполуки у вигляді жовтої твердої речовини (550 мг, 74,9 % вихід). MS + (маса/заряд): 362,0(M+H) . Наступні проміжні сполуки отримували за процедурами з проміжною сполукою 31 із застосуванням відповідних проміжних сполук та реагентів при відповідних умовах, що будуть відомі фахівцю в даній галузі. Проміжна сполука Структура MS (маса/заряд) (M+H) 32 206,1 33 267,9/269,9 34 361,1/363,1 35 362,1/364,1 36 362,1/364,1 Проміжна сполука 37 4-((6-Бромпіридин-3-іл)метил)морфолін 20 (A) 4-((6-Бромпіридин-3-іл)метил)морфолін 21 + UA 113470 C2 5 10 15 До розчину 6-бромнікотинальдегіду (1,0 г, 5,4 ммоля) та морфоліну (0,50 г, 5,7 ммоля) у 1,2дихлоретані (30 мл) додавали натрію триацетоксиборгідрид (1,8 г, 8,5 ммоля) та отриману суміш перемішували при кімнатній температурі протягом 2 годин. Суміш концентрували та очищали за допомогою ISCO (елюювали з MeOH у H 2O 0~100 %) з отриманням названої сполуки у вигляді жовтої твердої речовини (0,80 г, 57,9 % вихід). MS (маса/заряд): 256,9/258,9 + (M+H) . Проміжна сполука 38 1-(4-Амінофеніл)піридин-2(1H)-он (A) 1-(4-Амінофеніл)піридин-2(1H)-он Суміш піридин-2-олу (2,00 г, 21,0 ммоля), 4-йоданіліну (4,61 г, 21,0 ммоля), 8-хінолінолу (0,61 г, 4,2 ммоля), CuI (0,80 г, 4,2 ммоля) та Cs2CO3 (10,26 г, 31,5 ммоля) у DMSO (50 мл) перемішували при 120 °C протягом ночі. Після фільтрації фільтрат розподіляли між EA та водою та водний шар додатково екстрагували за допомогою EA. Об'єднані органічні шари промивали водою та сольовим розчином, сушили над безводним натрію сульфатом та концентрували з отриманням названої сполуки у вигляді зеленої твердої речовини (1,56 г, + 39,8 % вихід). MS (маса/заряд): 186,9 (M+H) . Проміжна сполука 39 (E)-Метил-4-хлор-3-метокси-5-(2-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)вініл)бензоат 20 25 30 (A) (E)-Метил-4-хлор-3-метокси-5-(2-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2іл)вініл)бензоат Суміш метил-3-бром-4-хлор-5-метоксибензоату (24 г, 86 ммолей), 4,4,5,5-тетраметил-2вініл-1,3,2-діоксаборолану (26,5 г, 172 ммоля), Pd(PPh3)4 (6 г, 5,16 ммоля) та DIPEA (27,7 г, 215 ммолей) у анізолі (450 мл) перемішували при 140 °C в атмосфері азоту протягом 16 годин. Леткі речовини видаляли при зниженому тиску та залишок очищали хроматографією на сілікагелі (елюювали з PE/ EA=10:1). Неочищений продукт після очищення знову промивали за допомогою PE з отриманням названої сполуки у вигляді жовтої твердої речовини (14,5 г, 47,9 % + вихід). MS (маса/заряд): 353,1 (M+H) . Наступні проміжні сполуки отримували за процедурами з проміжною сполукою 39 із застосуванням відповідних проміжних сполук та реагентів при відповідних умовах, що будуть відомі фахівцю в даній галузі. Проміжна сполука Структура MS (маса/заряд) (M+H) 40 319,2 41 333,2 22 + UA 113470 C2 Проміжна сполука Структура MS (маса/заряд) (M+H) 42 334,5 43 337,0 44 337,4 45 347,2 46 342,1 47 + 436,3 Проміжна сполука 48 (E)-Метил-4-хлор-3-(2-(2-хлорпіримідин-5-іл)вініл)-5-метоксибензоат 5 10 (A) (E)-Метил-4-хлор-3-(2-(2-хлорпіримідин-5-іл)вініл)-5-метоксибензоат Суміш (E)-метил-4-хлор-3-метокси-5-(2-(4,4,5,5-тетраметил-1,3,2 -діоксаборолан-2іл)вініл)бензоату (8,0 г, 23 ммоля), 5-бром-2-хлорпіримідину (5,5 г, 28 ммолей), K 2CO3 (7,8 г, 56 ммолей) та Pd(dppf)Cl2·CH2Cl2 (0,80 г, 1,1 ммоля) у діоксані (100 мл) та воді (20 мл) нагрівали при 80 °C протягом 30 хв. Потім суміш концентрували та залишок розподіляли між водою (400 мл) та DCM (300 мл). Водний шар екстрагували за допомогою DCM (2*150 мл). Об'єднані органічні шари концентрували. Потім залишок диспергували у етанолі (50 мл) та фільтрували. 23 UA 113470 C2 5 Відфільтрований матеріал промивали за допомогою етанолу (3*20 мл), а потім сушили з отриманням названої сполуки у вигляді жовтої твердої речовини (5,5 г, 71,5 % вихід). MS + (маса/заряд): 338,9 (M+H) . Наступні проміжні сполуки отримували за процедурами з проміжною сполукою 48 із застосуванням відповідних проміжних сполук та реагентів при відповідних умовах, що будуть відомі фахівцю в даній галузі. Проміжна сполука Структура MS (маса/заряд) (M+H) 49 50 305,0 51 323,0 52 348,0/350,0 53 10 304,0 365,8/367,8 Приклад 1. Синтез сполук 1-8 Сполука 1 3-(2-(2-((4-(4-Етилпіперазин-1-іл)феніл)аміно)піримідин-5-іл)етил)-5-метокси-Nметилбензамід 24 + UA 113470 C2 5 10 15 20 25 30 (A) (E)-Метил-3-(2-(2-(4-(4-етилпіперазин-1-іл)феніламіно)піримідин-5-іл)вініл)-5метоксибензоат Суміш (E)-N-(4-(4-етилпіперазин-1-іл)феніл)-5-(2-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2іл)вініл)піримідин-2-аміну (170 мг, 0,39 ммоля), метил-3-бром-5-метоксибензоату (96 мг, 0,39 ммоля), Pd(dppf)Cl2·CH2Cl2 (16 мг, 0,020 ммоля) та Na2CO3 (103 мг, 0,975 ммоля) у 1,4-діоксані (4 мл) та воді (1 мл) перемішували при 120 °C протягом 30 хв. у мікрохвилях. Отриману суміш розподіляли між 2 N HCl (20 мл) та EA (30 мл). Потім підвищували основність водного шару за допомогою 2 N NaOH до pH=8 та екстрагували за допомогою EA (2*30 мл). Об'єднані екстракти концентрували з отриманням названої сполуки у вигляді оранжевої твердої речовини (100 мг, + 54,1 % вихід). MS (маса/заряд): 474,0 (M+H) . (B) (E)-3-(2-(2-(4-(4-Етилпіперазин-1-іл)феніламіно)піримідин-5-іл)вініл)-5-метокси-Nметилбензамід Суміш (E)-метил-3-(2-(2-(4-(4-етилпіперазин-1-іл)феніламіно)піримідин-5-іл)вініл)-5метоксибензоату (100 мг, 0,211 ммоля) та метиламіну (5 мл, 35 % розчин в етанолі) перемішували при 120 °C протягом 50 хв. у мікрохвилях. Отриману суміш розподіляли між водою (20 мл) та EA (20 мл). Водний шар екстрагували за допомогою EA (2*20 мл). Об'єднаний органічний шар концентрували з отриманням названої сполуки у вигляді жовтої твердої + речовини (60 мг, 60,1 % вихід). MS (маса/заряд): 472,9(M+H) . (C) 3-(2-(2-(4-(4-Етилпіперазин-1-іл)феніламіно)піримідин-5-іл)етил)-5-метокси-Nметилбензамід До суміші (E)-3-(2-(2-(4-(4-етилпіперазин-1-іл)феніламіно)піримідин-5-іл)вініл)-5-метокси-Nметилбензаміду (60 мг, 0,127 ммоля) у MeOH (20 мл) додавали Pd/C(10 %, 20 мг). Отриману суміш перемішували при температурі середовища в атмосфері водню протягом ночі. Отриману суміш фільтрували крізь целіт, фільтрат концентрували, очищали за допомогою PTLC (DCM/MeOH=15:1) з отриманням названої сполуки у вигляді жовтої твердої речовини (19 мг, + 1 31,5 % вихід). MS (маса/заряд): 474,9(M+H) . H ЯМР (400 МГц, CD3OD) δ 8,11 (s, 2H), 7,44 (d, J=9,0 Гц, 2H), 7,21 (s, 1H), 7,19 (s, 1H), 6,95 (d, J=9,0 Гц, 2H), 6,88 (s, 1H), 3,79 (s, 3H), 3,18–3,12 (m, 4H), 2,94 (t, J=7,4 Гц, 2H), 2,92 (s, 3H), 2,82 (t, J=7,4 Гц, 2H), 2,67–2,62 (m, 4H), 2,49 (q, J=7,2 Гц, 2H), 1,14 (t, J=7,2 Гц, 3H). Наступні сполуки одержували згідно з процедурами для сполуки 1 із застосуванням відповідних проміжних сполук та реагентів при відповідних умовах, що будуть відомі фахівцю в даній галузі. 35 Сполука Структура LC-MS (маса/ заряд) + (M+H) 1 H ЯМР 1 2 431,2 25 H ЯМР (400 МГц, CDCl3) δ 8,58 (s, 2H), 7,91 (s, 1H), 7,58 (d, J=6,6 Гц, 1H), 7,53 (s, 1H), 7,12 (s, 2H), 6,96 (s, 1H), 6,78 (d, J=9,3 Гц, 1H), 4,18 (q, J=7,3 Гц, 2H), 3,96 (s, 3H), 3,06 (d, J=4,8 Гц, 3H), 1,52 (t, J=7,4 Гц, 3H). UA 113470 C2 Сполука Структура LC-MS (маса/ заряд) + (M+H) 1 H ЯМР 1 3 4 5 6 7 8 5 H ЯМР (400 МГц, CD3OD) δ 8,59 (s, 2H), 7,94 (s, 1H), 7,71 (d, J=1,8 Гц, 1H), 7,57 (s, 1H), 7,44 (d, J=16,3 Гц, 1H), 7,32 (d, J=1,6 457,1/459,1 Гц, 1H), 7,00 (d, J=16,3 Гц, 1H), 4,17 (q, J=7,3 Гц, 2H), 3,98 (s, 3H), 2,99 (s, 3H), 1,51 (t, J=7,3 Гц, 3H). 1 H ЯМР (400 МГц, CD3OD) δ 8,06 (s, 2H), 7,85–7,82 (m, 2H), 7,55–7,52 (m, 1H), 7,46 (d, J=9,0 Гц, 2H), 6,97 (d, J=9,0 Гц, 2H), 485,2 6,91–6,89 (m, 1H), 3,40–3,32 (m, 4H), 3,27– 3,23 (m, 4H), 3,19 (t, J=7,6 Гц, 2H), 3,07 (q, J=7,6 Гц, 2H), 2,95–2,90 (m, 5H), 1,33 (t, J=7,6 Гц, 3H). 1 H ЯМР (400 МГц, CD3OD) δ 8,05 (s, 2H), 7,86 (s, 1H), 7,78 (s, 1H), 7,50–7,39 (m, 3H), 6,98–6,88 (m, 3H), 3,80 (s, 3H), 3,21– 501,2 3,08 (m, 6H), 2,90 (t, J=7,2 Гц, 2H), 272– 2,61 (m, 4H), 2,51 (q, J=7,1 Гц, 2H), 1,14 (t, J=7,1 Гц, 3H). 1 H ЯМР (400 МГц, CD3OD) δ 8,00 (s, 2H), 7,35 (d, J=9,0 Гц, 2H), 7,00 (d, J=2,4 Гц, 1H), 6,89–6,84 (m, 3H), 4,42 (t, J=8,7 Гц, 503,1 2H), 3,68 (s, 3H), 3,08–3,06 (m, 4H), 2,96 (t, J=8,7 Гц, 2H), 2,79–2,69 (m, 4H), 2,59–2,56 (m, 4H), 2,42 (q, J=7,2 Гц, 2H), 1,06 (t, J=7,2 Гц, 3H). 1 H ЯМР (400 МГц, CD3OD) δ 8,05 (s, 2H), 7,85–7,83 (m, 2H), 7,53–7,50 (m, 1H), 7,42 (d, J=7,2 Гц, 2H), 6,94 (d, J=7,2 Гц, 2H), 6,91–6,89 (m, 1H), 3,18–3,14 (m, 6H), 2,90 511,2 (t, J=7,5 Гц, 2H), 2,88–2,83 (m, 1H), 2,66– 2,64 (m, 4H), 2,50 (q, J=7,2 Гц, 2H), 1,14 (t, J=7,2 Гц, 3H), 0,81–0,78 (m, 2H), 0,65–0,63 (m, 2H). 1 H ЯМР (400 МГц, CDCl3) δ 8,56 (s, 2H), 7,57 (d, J=6,5 Гц, 1H), 7,47 (d, J=8,8 Гц, 2H), 7,13 (s, 1H), 7,11 (s, 2H), 6,94 (d, 525,3 J=8,8 Гц, 2H), 6,78 (d, J=7,8 Гц, 1H), 3,96 (s, 3H), 3,51–3,44 (m, 2H), 3,12–3,07 (m, 2H), 3,06 (d, J=4,7 Гц, 3H), 2,31 (t, J=11,0 Гц, 2H), 1,16 (d, J=6,3 Гц, 6H). Приклад 2. Синтез сполук 9-13 Сполука 9 3-(2-(2-((3-(4-Етилпіперазин-1-іл)феніл)аміно)піримідин-5-іл)етил)-5-метокси-Nметилбензамід 26 UA 113470 C2 5 10 15 20 25 30 (A) (E)-Метил-3-(2-(2-((3-(4-етилпіперазин-1-іл)феніл)аміно)піримідин-5-іл)вініл)-5метоксибензоат Суміш 5-бром-N-(3-(4-етилпіперазин-1-іл)феніл)піримідин-2-аміну (113 мг, 0,31 ммоля), (E)метил-3-метокси-4-(2-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)вініл)бензоату (100 мг, 0,31 . ммоля), K2CO3 (87 мг, 0,63 ммоля), Pd(dffp)2Cl2 CH2Cl2 (20 мг, 0,022 ммоля) та води (1 мл) у діоксані (5 мл) нагрівали при 100 °C протягом 1 години у мікрохвилях. Отриману суміш охолоджували та концентрували in vacuo. Залишок розчиняли у DCM (10 мл) та промивали водою та сольовим розчином. Органічний шар концентрували, очищали за допомогою ISCO (елюювали з MeOH у DCM 0-10 %) з отриманням жовтої твердої речовини (70 мг, 47,4 % вихід). + MS (маса/заряд): 462,2 (M+H) . (B) (E)-3-(2-(2-((3-(4-Етилпіперазин-1-іл)феніл)аміно)піримідин-5-іл)вініл)-5-метокси-Nметилбензамід Суміш (E)-метил-3-(2-(2-((3-(4-етилпіперазин-1-іл)феніл)аміно)піримідин-5-іл)вініл)-5метоксибензоату (70 мг, 0,15 ммоля) у метиламіні (5 мл, 35 % розчин в етанолі) нагрівали при 120 °C протягом 30 хв. у мікрохвилях. Отриману суміш охолоджували та концентрували in vacuo + з отриманням жовтої твердої речовини (70 мг, кількісний вихід). MS (маса/заряд): 473,2 (M+H) . (C) 3-(2-(2-((3-(4-Етилпіперазин-1-іл)феніл)аміно)піримідин-5-іл)етил)-5-метокси-Nметилбензамід Суміш (E)-3-(2-(2-((3-(4-етилпіперазин-1-іл)феніл)аміно)піримідин-5-іл)вініл)-5-метокси-Nметилбензаміду (70 мг, 0,15 ммоля) та Pd/C (5 %, 25 мг) у MeOH (15 мл) перемішували в 1 атм. H2 при 40 °C протягом 12 годин. Отриману суміш фільтрували та фільтрат концентрували in vacuo. Залишок очищали за допомогою PTLC (DCM/MeOH=10:1) з отриманням названої + сполуки у вигляді білої твердої речовини (23,0 мг, 32,8 % вихід). MS (маса/заряд): 475,2 (M+H) . 1 H ЯМР (400 МГц, CD3OD) δ 8,18 (s, 2H), 7,37 (s, 1H), 7,24-7,21 (m, 2H), 7,18-7,11 (m, 2H), 6,89 (s, 1H), 6,65 (d, J=8,1 Гц) 3,83 (s, 3H), 3,31-3,26 (m, 4H), 2,95-2,82 (m, 1H), 2,75-2,67 (m, 2H), 1,23 (t, J=7,2 Гц, 3H). Наступні сполуки одержували згідно з процедурами для сполуки 9 із застосуванням відповідних проміжних сполук та реагентів при відповідних умовах, що будуть відомі фахівцю в даній галузі. Сполу-ка Структура LC-MS (маса/ заряд) + (M+H) 1 H ЯМР 1 10 425,0 27 H ЯМР (400 МГц, CDCl3) δ 8,15 (s, 2H), 7,91 (s, 1H), 7,44 (s, 1H), 7,32 (d, J=6,0 Гц, 1H), 7,21 (s, 1H), 7,00 (d, J=4,3 Гц, 1H), 4,77–4,69 (m, 1H), 3,90 (s, 3H), 2,97 (d, J=4,6 Гц, 3H), 2,91 (t, J=7,4 Гц, 2H), 2,79 (t, J=7,3 Гц, 2H), 2,62–2,41 (m, 4H), 1,92–1,83 (m, 2H). UA 113470 C2 Сполу-ка Структура LC-MS (маса/ заряд) + (M+H) 1 H ЯМР 1 11 465,9 12 475,1 13 483,9 H ЯМР (400 МГц, DMSO-d6) δ 9,20 (s, 1H), 8,38 (d, J=4,6 Гц, 1H), 8,20 (s, 2H), 7,53 (d, J=9,1 Гц, 2H), 7,42 (d, J=7,8 Гц, 1H), 7,37 (d, J=4,3 Гц, 1H), 6,85 (d, J=9,1 Гц, 2H), 3,83 (s, 3H), 3,75–3,67 (m, 4H), 3,03–2,96 (m, 4H), 2,88 (t, J=7,3 Гц, 2H), 2,76–2,72 (m, 5H). 1 H ЯМР (400 МГц, CD3OD) δ 8,17 (s, 2H), 7,29 (s, 1H), 7,22 (s, 1H), 7,20 (s, 1H), 7,15– 7,08 (m, 2H), 6,88 (s, 1H), 6,62 (d, J=7,7 Гц, 1H), 3,79 (s, 3H), 3,56–3,50 (m, 2H), 3,02– 2,96 (m, 2H), 2,93–2,90 (m, 2H), 2,89 (s, 3H), 2,87–2,82 (m, 2H), 2,27 (t, J=11,2 Гц, 2H), 1,14 (d, J=6,4 Гц, 6H). 1 H ЯМР (400 МГц, CD3OD) δ 8,14 (s, 2H), 7,95 (s, 1H), 7,53 (s, 1H), 7,41 (dd, J=7,8 Гц, 2,1 Гц, 1H), 7,27 (dd, J=6,0 Гц, 2,1 Гц, 1H), 4,15–4,09 (m, 2H), 3,88 (s, 3H), 2,94 (t, J=7,6 Гц, 2H), 2,89 (s, 3H), 2,81 (t, J=7,6 Гц, 2H), 2,55 (q, J=7,2 Гц, 4H), 2,50–2,43 (m, 2H), 2,02–1,99 (m, 2H), 1,01 (t, J=7,2 Гц, 6H). Приклад 3. Синтез сполук 14-17 Сполука 14 3-(2-(2-((3-(4-Етилпіперазин-1-іл)феніл)аміно)піримідин-5-іл)етил)-N, 5-диметоксибензамід 5 10 15 20 (A) (E)-3-(2-(2-((3-(4-Етилпіперазин-1-іл)феніл)аміно)піримідин-5-іл)вініл)-N, 5диметоксибензамід Суміш (E)-N, 3-диметокси-5-(2-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)вініл)бензаміду (0,10 г, 0,30 ммоля), 5-бром-N-(3-(4-етилпіперазин-1-іл)феніл)піримідин-2-аміну (0,11 г, 0,30 . ммоля), Na2CO3 (0,07 г, 0,66 ммоля) та Pd(dffp)2Cl2 CH2Cl2 (0,025 г, 0,034 ммоля) у діоксані (5 мл) та воді (1 мл) нагрівали при 100 °C протягом 30 хв. у мікрохвилях. Потім суміш фільтрували та фільтрат очищали за допомогою ISCO (елюювали з MeOH у H2O 0~100 %) з отриманням безпосередньо названої сполуки у вигляді жовтої твердої речовини (0,036 г, 24,6 % вихід). MS + (маса/заряд): 489,7 (M+H) . (B) 3-(2-(2-((3-(4-Етилпіперазин-1-іл)феніл)аміно)піримідин-5-іл)етил)-N, 5диметоксибензамід Розчин (E)-3-(2-(2-((3-(4-етилпіперазин-1-іл)феніл)аміно)піримідин-5-іл)вініл)-N, 5диметоксибензаміду (0,036 г, 0,078 ммоля) у MeOH (15 мл) додавали Pd/C (10 %, 0,04 г) та суміш перемішували при 35 °C протягом 40 годин в атмосфері водню. Суміш фільтрували та фільтрат концентрували. Залишок очищали за допомогою PTLC (DCM/MeOH) з отриманням названої сполуки у вигляді жовтої твердої речовини (0,020 г, 55,3 % вихід). MS (маса/заряд): 28
ДивитисяДодаткова інформація
Назва патенту англійськоюNovel pyrimidine and pyridine compounds and their usage
Автори англійськоюSu, Wei-Guo, Zhang, Weihan, Li, Jinshui
Автори російськоюСу Вэй-Го, Чжан Вэйхань, Ли Цзиньхуэй
МПК / Мітки
МПК: A61K 31/44, C07D 213/04, A61K 31/505, C07D 239/24
Мітки: сполуки, піримідинові, піридинові, застосування
Код посилання
<a href="https://ua.patents.su/120-113470-pirimidinovi-ta-piridinovi-spoluki-ta-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Піримідинові та піридинові сполуки та їх застосування</a>
Попередній патент: Спосіб очищення води від сполук бору
Наступний патент: Спосіб детекції аденозин-5′-трифосфату у водних розчинах
Випадковий патент: Циркуляційно-інгібіторний клапан












