Піридинові похідні як інгібітори реаранжованої у процесі трансфекції (ret) кінази
Номер патенту: 115264
Опубліковано: 10.10.2017
Автори: Раха Каушик, Йанг Хайінг, Гуан Емі Гуйпінг, Ю Хайю, Ейдем Хіларі Шенк, Чунг Муі, Гонг Цзен, Ву Ченгд, Демартіно Майкл П., Цзанг Цзилю
Формула / Реферат
1. Сполука відповідно до формули (І):
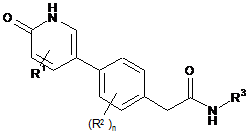 , (I)
, (I)
де:
R1 являє собою водень, галоген, (С1-С6)алкіл, галоген(С1-С6)алкіл, (С3-С6)циклоалкіл, гідроксил, (С1-С6)алкокси, галоген(С1-С6)алкокси, (С3-С6)циклоалкокси, аміно, ((С1-С6)алкіл)аміно- або ((С1-С6)алкіл)((С1-С6)алкіл)аміно-;
кожен R2 незалежно вибраний з групи, що включає галоген, (С1-С6)алкіл, галоген(С1-С6)алкіл, (С3-С6)циклоалкіл, ціано, гідроксил, (С1-С6)алкокси, галоген(С1-С6)алкокси, (С3-С6)циклоалкокси, аміно, ((С1-С6)алкіл)аміно- і ((С1-С6)алкіл)((С1-С6)алкіл)аміно-;
R3 являє собою феніл або 5- або 6-членний гетероарил, кожен з яких необов'язково заміщений одним-трьома замісниками, незалежно вибраними з галогену, (С1-С6)алкілу, галоген(С1-С6)алкілу, (С3-С6)циклоалкілу, ціано, 5- або 6-членного гетероарилу, -OR4 і -CONR5R6; де вказаний (С1-С6)алкіл необов'язково заміщений ціано, гідроксилом, (С1-С4)алкокси, галоген(С1-С4)алкокси або -NR5R6; і де вказаний 5- або 6-членний гетероарильний замісник необов'язково заміщений галогеном, (С1-С4)алкілом або галоген(С1-С4)алкілом;
R4 являє собою водень, (С1-С4)алкіл, галоген(С1-С6)алкіл, (С3-С6)циклоалкіл або 4-6-членний гетероциклоалкіл; де вказаний (С1-С4)алкіл необов'язково заміщений ціано, гідроксилом, (С1-С4)алкокси, галоген(С1-С4)алкокси або -NR5R6; і де вказаний (С3-С6)циклоалкіл необов'язково заміщений одним або двома замісниками, незалежно вибраними з (С1-С4)алкілу, галоген(С1-С4)алкілу, гідроксилу, гідроксі(С1-С4)алкілу, (С1-С4)алкокси та галоген(С1-С4)алкокси; і де вказаний 4-6-членний гетероциклоалкіл необов'язково заміщений одним або двома замісниками, незалежно вибраними з (С1-С4)алкілу і галоген(С1-С4)алкілу;
R5 і R6, кожен незалежно, вибрані з групи, що включає водень, (С1-С4)алкіл і галоген(С1-С4)алкіл;
або R5 і R6, узяті разом з азотом, до якого вони приєднані, являють собою 5- або 6-членне насичене кільце, що необов'язково містить додатковий гетероатом, вибраний з кисню, азоту та сірки, де вказане кільце необов'язково заміщене галогеном, (С1-С4)алкілом або галоген(С1-С4)алкілом; та
n має значення 0, 1 або 2;
або її фармацевтично прийнятна сіль.
2. Сполука або фармацевтично прийнятна сіль за п. 1, представлена формулою (II):
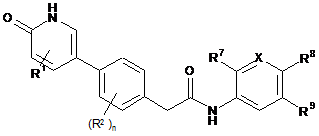 , (II)
, (II)
де:
X являє собою N або CR10;
R1 являє собою водень, галоген, (С1-С6)алкіл, галоген(С1-С6)алкіл, (С3-С6)циклоалкіл, гідроксил, (С1-С6)алкокси, галоген(С1-С6)алкокси, (С3-С6)циклоалкокси, аміно, ((С1-С6)алкіл)аміно- або ((С1-С6)алкіл)((С1-С6)алкіл)аміно-;
кожен R2 незалежно вибраний з групи, що включає галоген, (С1-С6)алкіл, галоген(С1-С6)алкіл, (С3-С6)циклоалкіл, ціано, гідроксил, (С1-С6)алкокси, галоген(С1-С6)алкокси, (С3-С6)циклоалкокси, аміно, ((С1-С6)алкіл)аміно- та ((С1-С6)алкіл)((С1-С6)алкіл)аміно-;
R4 являє собою водень, (С1-С6)алкіл, галоген(С1-С6)алкіл, (С3-С6)циклоалкіл або 4-6-членний гетероциклоалкіл; де вказаний (С1-С6)алкіл необов'язково заміщений ціано, гідроксилом, (С1-С4)алкокси, галоген(С1-С4)алкокси або -NR5R6; і де вказаний (С3-С6)циклоалкіл необов'язково заміщений одним або двома замісниками, незалежно вибраними з (С1-С4)алкілу, галоген(С1-С4)алкілу, гідроксилу, гідроксі(С1-С4)алкілу, (С1-С4)алкокси і галоген(С1-С4)алкокси; і де вказаний 4-6-членний гетероциклоалкіл необов'язково заміщений одним або двома замісниками, незалежно вибраними з (С1-С4)алкілу та галоген(С1-С4)алкілу;
R5 і R6, кожен незалежно, вибрані з групи, що включає водень, (С1-С4)алкіл і галоген(С1-С4)алкіл;
або R5 і R6, узяті разом з азотом, до якого вони приєднані, являють собою 5- або 6-членне насичене кільце, що необов'язково містить додатковий гетероатом, вибраний з кисню, азоту та сірки, де вказане кільце необов'язково заміщене галогеном, (С1-С4)алкілом або галоген(С1-С4)алкілом;
R7 являє собою водень, галоген або (С1-С4)алкокси;
R8 являє собою водень, галоген, (С1-С6)алкіл, галоген(С1-С6)алкіл, (С3-С6)циклоалкіл, ціано, 5- або 6-членний гетероарил, -OR4 або -CONR5R6; де вказаний (С1-С6)алкіл необов'язково заміщений ціано, гідроксилом, (С1-С4)алкокси, галоген(С1-С4)алкокси або -NR5R6; і де вказаний 5- або 6-членний гетероарил необов'язково заміщений галогеном, (С1-С4)алкілом або галоген(С1-С4)алкілом;
R9 являє собою водень, галоген або галоген(С1-С4)алкіл;
R10 являє собою водень, галоген, галоген(С1-С4)алкіл або 5- або 6-членний гетероарил, де вказаний 5- або 6-членний гетероарил необов'язково заміщений галогеном, (С1-С4)алкілом або галоген(С1-С4)алкілом; і
n має значення 0, 1 або 2;
за умови, що, коли X являє собою CR10, щонайменше один з R7, R8, R9 і R10 являє собою водень.
3. Сполука або фармацевтично прийнятна сіль за п. 2, де R7 являє собою водень або фтор.
4. Сполука або фармацевтично прийнятна сіль за п. 2 або 3, де R8 являє собою водень, фтор, хлор, (С1-С6)алкіл, галоген(С1-С4)алкіл, ціано, (С1-С4)алкокси, гідроксі(С2-С4)алкокси-, (С1-С4)алкоксі(С2-С4)алкокси-, аміно(С1-С4)алкокси-, ((С1-С4)алкіл)аміно(С2-С4)алкокси-, ((С1-С4)алкіл)((С1-С4)алкіл)аміно(С2-С4)алкокси- або -CONH2; де вказаний (С1-С6)алкіл необов'язково заміщений ціано, гідроксилом, (С1-С4)алкокси, аміно, ((С1-С4)алкіл)аміно- або ((С1-С4)алкіл)((С1-С4)алкіл)аміно-.
5. Сполука або фармацевтично прийнятна сіль за п. 4, де R8 являє собою водень або (С1-С6)алкіл; де вказаний (С1-С6)алкіл необов'язково заміщений ціано, гідроксилом, (С1-С4)алкокси, аміно, ((С1-С4)алкіл)аміно- або ((С1-С4)алкіл)((С1-С4)алкіл)аміно-.
6. Сполука або фармацевтично прийнятна сіль за будь-яким з пп. 2-5, де R9 являє собою галоген(С1-С4)алкіл.
7. Сполука або фармацевтично прийнятна сіль за п. 6, де R9 являє собою трифторметил.
8. Сполука або фармацевтично прийнятна сіль за будь-яким з пп. 2-7, де X являє собою СН.
9. Сполука або фармацевтично прийнятна сіль за будь-яким з пп. 2-7, де X являє собою N.
10. Сполука або фармацевтично прийнятна сіль за будь-яким з пп. 1-9, де R1 являє собою (С1-С4)алкокси.
11. Сполука або фармацевтично прийнятна сіль за п. 10, де R1 являє собою етокси.
12. Сполука або фармацевтично прийнятна сіль за будь-яким з пп. 1-11, де n має значення 1 або 2, і кожен R2 незалежно являє собою галоген.
13. Сполука або фармацевтично прийнятна сіль за п. 12, де кожен R2 являє собою фтор.
14. Сполука за п. 1, яка являє собою:
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(6-(2-гідроксипропан-2-іл)-5-(трифторметил)піридин-3-іл)ацетамід;
N-(6-етокси-5-(трифторметил)піридин-3-іл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(4-(3-гідрокси-2,2-диметилпропіл)-3-(трифторметил)феніл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2,3-дифторфеніл)-N-(4-(2-гідроксіетокси)-3-(трифторметил)феніл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(4-(3-гідрокси-2,2-диметилпропіл)-3-(трифторметил)феніл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-3-фторфеніл)-N-(4-(3-гідрокси-2,2-диметилпропіл)-3-(трифторметил)феніл)ацетамід;
N-(4-ціано-3-(трифторметил)феніл)-2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-3-фторфеніл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2,6-дифторфеніл)-N-(4-(2-гідроксіетокси)-3-(трифторметил)феніл)ацетамід;
N-(4-ціано-3-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
N-(6-(2-(диметиламіно)етокси)-5-(трифторметил)піридин-3-іл)-2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(4-метил-1Н-імідазол-1-іл)-5-(трифторметил)феніл)ацетамід;
N-(6-(2-ціанопропан-2-іл)-5-(трифторметил)піридин-3-іл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(4-(2-гідроксіетокси)-3-(трифторметил)феніл)ацетамід;
N-(6-(ціанометил)-5-(трифторметил)піридин-3-іл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
N-(6-(1-ціаноетил)-5-(трифторметил)піридин-3-іл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
N-(4-хлор-3-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропiридин-3-іл)-2-фторфеніл)ацетамід;
N-(4-((диметиламіно)метил)-3-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
N-(3,4-дихлорфеніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(5-(1,1,1-трифтор-2-метилпропан-2-іл)ізоксазол-3-іл)ацетамід;
2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(4-(2-гідроксіетокси)-3-(трифторметил)феніл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(4-((4-етилпіперазин-1-іл)метил)-3-(трифторметил)феніл)ацетамід;
N-(2,5-дифторфеніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
4-(2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамідо)-2-(трифторметил)бензамід;
N-(2,4-дифтор-5-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
N-(3,5-біс(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід або
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(2-фтор-5-(трифторметил)феніл)ацетамід;
2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(1,1,1-трифтор-2-метилпропан-2-іл)ізоксазол-5-іл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(1,1,1-трифтор-2-метилпропан-2-іл)ізоксазол-5-іл)ацетамід;
2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(5-метил-1,3,4-оксадіазол-2-іл)-5-(трифторметил)феніл)ацетамід;
2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(5-(1,1,1-трифтор-2-метилпропан-2-іл)ізоксазол-3-іл)ацетамід;
2-(4-(4-етоксі-6-оксо-1,б-дигідропіридин-3-іл)-2-фторфеніл)-N-(6-(1-гідроксі-2-метилпропан-2-іл)-5-(трифторметил)піридин-3-іл)ацетамід;
2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-3-фторфеніл)-N-(4-(3-гідрокси-2,2-диметилпропіл)-3-(трифторметил)феніл)ацетамід;
2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(трифторметил)феніл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(4-метил-1Н-піразол-1-іл)-5-(трифторметил)феніл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(3-метил-1Н-піразол-1-іл)-5-(трифторметил)феніл)ацетамід;
N-(3-(1Н-піразол-4-іл)-5-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(6-(1,1,1-трифтор-2-метилпропан-2-іл)піридин-3-іл)ацетамід;
N-(4-ціано-3-(трифторметил)феніл)-2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(2-морфоліноетокси)-5-(трифторметил)феніл)ацетамід;
2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(1,1,1-трифтор-2-метилпропан-2-іл)ізоксазол-5-іл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(1-метил-3-(1,1,1-трифтор-2-метилпропан-2-іл)-1Н-піразол-5-іл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(1,1,1-трифтор-2-метилпропан-2-іл)-1Н-піразол-5-іл)ацетамід;
N-(4-(2,2-дифтор-3-гідроксипропіл)-3-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
N-(3-(2Н-тетразол-5-іл)-5-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(1-метил-1Н-піразол-4-іл)-5-(трифторметил)феніл)ацетамід або
N-(3-(2-(диметиламіно)етокси)-5-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід;
або її фармацевтично прийнятна сіль.
15. Сполука за п. 1, яка відповідає формулі
 ,
,
або її фармацевтично прийнятна сіль.
16. Сполука за п. 15, де сполука являє собою вільну основу.
17. Фармацевтична композиція, що включає сполуку або фармацевтично прийнятну сіль за будь-яким одним з пп. 1-16 і фармацевтично прийнятний ексципієнт.
Текст
Реферат: Даний винахід стосується нових сполук, які є інгібіторами реаранжованої у процесі трансфекції (RET) кінази, фармацевтичних композицій, що їх містять, способів їх отримання та їх застосування в терапії, окремо або в комбінації, для нормалізації чутливості, рухливості та/або секреції шлунково-кишкового тракту та/або розладів або захворювань черевної порожнини та/або лікування захворювань, пов'язаних з дисфункцією RET, або де модуляція RET активності може мати терапевтичний ефект, включаючи, але не обмежуючись цим, всі класифікації UA 115264 C2 (12) UA 115264 C2 синдрому подразненої товстої кишки (IBS), включаючи тип дефекації з переважанням діареї, з переважанням запору або переміжний тип, функціональне здуття живота, функціональний запор, функціональну діарею, невизначений функціональний розлад кишечнику, функціональний абдомінальний больовий синдром, хронічний ідіопатичний запор, функціональні розлади стравоходу, функціональні гастродуоденальні розлади, функціональний аноректальний біль, запальне захворювання кишечнику, проліферативні захворювання, як-от недрібноклітинний рак легені, гепатоцелюлярна карцинома, рак прямої кишки, медулярний рак щитовидної залози, фолікулярний рак щитовидної залози, анапластичний рак щитовидної залози, папілярний рак щитовидної залози, пухлини головного мозку, рак черевної порожнини, солідні пухлини, інші види раку легенів, рак голови та шиї, гліоми, нейробластоми, синдром Фон Гіппеля-Ліндау та злоякісні пухлини нирок, рак молочної залози, рак фаллопієвих труб, рак яєчників, перехідноклітинний рак, рак передміхурової залози, рак стравоходу і гастроезофагеального переходу, рак жовчних проток, аденокарцинома та будь-яке злоякісне новоутворення з підвищеною активністю RET-кінази. UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 ГАЛУЗЬ, ДО ЯКОЇ НАЛЕЖИТЬ ВИНАХІД Даний винахід відноситься до нових сполук, які є інгібіторами реаранжованої у процесі трансфекції (RET) кінази, до фармацевтичних композицій, що їх містять, до способів їх отримання та до їх застосування в терапії, окремо або в комбінації, для нормалізації чутливості, рухливості та/або секреції шлунково-кишкового тракту та/або абдомінальних розладів або захворювань та/або лікування захворювань, пов'язаних з дисфункцією RET, або де модуляція RET активності може мати терапевтичний ефект, включаючи, але не обмежуючись цим, всі класифікації синдрому подразненої товстої кишки (IBS), включаючи тип дефекації з переважанням діареї, з переважанням запору або переміжний тип, функціональне здуття живота, функціональний запор, функціональну діарею, невизначений функціональний розлад кишечнику, функціональний абдомінальний больовий синдром, хронічний ідіопатичний запор, функціональні розлади стравоходу, функціональні гастродуоденальні розлади, функціональні аноректальні болі, запальне захворювання кишечнику, проліферативні захворювання, як-от недрібноклітинний рак легені, гепатоцелюлярна карцинома, рак прямої кишки, медулярний рак щитовидної залози, фолікулярний рак щитовидної залози, анапластичний рак щитовидної залози, папілярний рак щитовидної залози, пухлини головного мозку, рак черевної порожнини, солідні пухлини, інші види раку легенів, рак голови та шиї, гліоми, нейробластоми, синдром Фон Гіппеля-Ліндау та злоякісні пухлини нирок, рак молочної залози, рак фаллопієвих труб, рак яєчників, перехідно-клітинний рак, рак передміхурової залози, рак стравоходу і гастроезофагеального переходу, рак жовчних проток та аденокарцинома і будь-яке злоякісне новоутворення з підвищеною активністю RET кінази. ПЕРЕДУМОВИ СТВОРЕННЯ ВИНАХОДУ Синдром подразненої товстої кишки (IBS) є поширеним захворюванням, на яке страждають 10-20 % людей у розвинених країнах, і характеризується порушенням функцій роботи кишечнику, здуттям живота та вісцеральною гіперчутливістю (Camilleri, M., N. Engl. J. Med., 2012, 367:1626-1635). Тоді як етіологія IBS невідома, передбачають, що він є результатом або порушення між головним мозком і шлунково-кишковим трактом, порушення мікрофлори кишечнику або підвищеним запаленням. Зміни в шлунково-кишковому тракті, що з'являються в результаті, впливають на нормальний транзит кишечнику, що призводить або до діареї, або до запору. Крім того, у більшості хворих IBS сенсибілізація периферичної нервової системи призводить в результаті до вісцеральної гіперчутливості або алодинії (Keszthelyi, D., Eur. J. Pain, 2012, 16:1444-1454). Хоча IBS безпосередньо не змінює очікувану тривалість життя, він значно впливає на якість життя пацієнта. Більш того, великі фінансові витрати пов'язані з наданням медичних послуг у зв'язку з IBS, і має місце зниження продуктивності праці унаслідок відсутності співробітника (Nellesen, D., et al., J. Manag. Care Pharm., 2013, 19:755-764). Одним з найбільш важливих симптомів, які значно впливають на якість життя пацієнта з IBS, є вісцеральний біль (Spiegel, B., et al., Am. J. Gastroenterol., 2008, 103:2536-2543). Молекулярні стратегії, які інгібують пов'язаний з IBS вісцеральний біль, зможуть значно впливати на якість життя пацієнта з IBS і понизити пов'язані з цим витрати. Реаранжований у процесі трансфекції (RET) являє собою тирозинову кіназу рецептора нейронального чинника зростання, яка активується при зв'язуванні одного з чотирьох нейротрофічних чинників нейротрофічного чинника гліальних клітин (GDNF), нейротурину, артеміну і персефіну в комбінації з ко-рецептором сімейства GDNF рецепторів альфа-1, 2, 3 і 4, відповідно (Plaza-Menacho, I., et al., Trends Genet., 2006, 22:627-636). RET, як відомо, грає важливу роль у розвитку і виживанні аферентних ноцицепторів у шкірі та кишечнику. Миші з RET кіназним "нокаутом" не мають кишкових нейронів і мають інші аномалії нервової системи, що дають підставу припускати, що в процесі розвитку необхідний функціональний RET кіназний білковий продукт (Taraviras, S. et al., Development, 1999, 126:2785-2797). Більш того, популяційні дослідження пацієнтів з хворобою Гіршпрунга, що характеризується непрохідністю товстої кишки через відсутність нормального розслаблення товстої кишки, мають високу частку як сімейних, так і спорадичних RET мутацій з втратою функції (Butler Tjaden N., et al., Transl. Res., 2013, 162:1-15). Аналогічним чином, аберантна RET кіназна активність пов'язана з множинною ендокринною неоплазією (MEN 2A і 2B), сімейною медулярною карциномою щитовидної залози (FMTC), папілярним раком щитовидної залози (РТС) і хворобою Гіршпрунга (HSCR) (Borello, M., et al., Expert Opin. Ther. Targets, 2013, 17:403-419). MEN 2A являє собою раковий синдром унаслідок мутації у позаклітинному цистеїн-збагаченому домені RET, що призводить до димеризації через дисульфідний зв'язок, що викликає конститутивну активацію активності тирозинкінази (Wells Jr, S., et al., J. Clin. Endocrinol. Metab., 2013, 98:3149-3164). В індивідуумів з такою мутацією може 1 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 розвинутися медулярний рак щитовидної залози (МТС), гіперплазія паращитовидної залози та феохромоцитома. MEN 2B викликається мутацією Met918Thr в RET, яка змінює специфічність тирозинкінази. MEN 2B аналогічний MEN 2A, але з відсутністю паратиреоїдної гіперплазії, і також призводить до розвитку багаточисельних гангліїв слизистої оболонки губ, язика і кишкового тракту. Хромосомні перебудови, що сполучають промотор і NH2-термінальні домени або незв'язаний ген(и) з COOH-кінцем RET кінази, що призводять у результаті до конститутивно активованих химерних форм рецептора (RET/PTC), як вважають, є подіями, що ініціюють пухлину, в РТС (Viglietto, G. et al., Oncogene, 1995, 11:1207-1210). РТС охоплюють близько 80 % всіх карцином щитовидної залози. Ці дані вказують, що інгібування RET може бути вигідною терапевтичною стратегією для лікування болю, пов'язаного з IBS та іншими шлунковокишковими розладами, і для лікування ракових захворювань з конститутивною RET кіназною активністю. КОРОТКИЙ ВИКЛАД ВИНАХОДУ Даний винахід відноситься до сполук формули (I): де: 1 R являє собою водень, галоген, (C1-C6)алкіл, галоген(C1-C6)алкіл, (C3-C6) циклоалкіл, гідроксил, (C1-C6)алкоксі, галоген(C1-C6)алкоксі, (C3-C6)циклоалкоксі, аміно, ((C1-C6)алкіл)аміноабо ((C1-C6)алкіл)((C1-C6)алкіл)аміно-; 2 кожен R незалежно вибраний з групи, що включає галоген, (C 1-C6)алкіл, галоген(C1C6)алкіл, (C3-C6)циклоалкіл, ціано, гідроксил, (C1-C6)алкоксі, галоген(C1-C6)алкоксі, (C3C6)циклоалкоксі, аміно, ((C1-C6)алкіл)аміно- і ((C1-C6)алкіл)((C1-C6) алкіл)аміно-; 3 R являє собою феніл або 5- або 6-членний гетероарил, кожен з яких необов'язково заміщений одним-трьома замісниками, незалежно вибраними з групи, що включає галоген, (C 14 C6)алкіл, галоген(C1-C6)алкіл, (C3-C6)циклоалкіл, ціано, 5- або 6-членний гетероарил, -OR і 5 6 CONR R ; де вказаний (C1-C6)алкіл необов'язково заміщений групами ціано, гідроксил, (C15 6 C4)алкоксі, галоген(C1-C4) алкоксі або -NR R ; і де вказаний 5- або 6-членний гетероарильний замісник необов'язково заміщений галогеном, (C 1-C4)алкілом або галоген(C1-C4)алкілом; 4 R являє собою водень, (C1-C6)алкіл, галоген(C1-C6)алкіл, (C3-C6)циклоалкіл або 4-6-членний гетероциклоалкіл; де вказаний (C1-C6)алкіл необов'язково заміщений ціано, гідроксилом, (C 15 6 C4)алкоксі, галоген(C1-C4)алкоксі або -NR R ; і де вказаний (C3-C6)циклоалкіл необов'язково заміщений одним або двома замісниками, незалежно вибраними з групи, що включає (C1C4)алкіл, галоген(C1-C4)алкіл, гідроксил, гідроксі(C1-C4)алкіл, (C1-C4)алкоксі і галоген(C1C4)алкоксі; і де вказаний 4-6-членний гетероциклоалкіл необов'язково заміщений одним або двома замісниками, незалежно вибраними з (C1-C4)алкілу і галоген(C1-C4)алкілу; 5 6 R і R , кожен незалежно, вибрані з групи, що включає водень, (C 1-C4)алкіл і галоген(C1C4)алкіл; 5 6 або R і R , узяті разом з азотом, до якого вони приєднані, являють собою 5- або 6-членне насичене кільце, що необов'язково містить додатковий гетероатом, вибраний з кисню, азоту і сірки, де вказане кільце необов'язково заміщене галогеном, (C 1-C4)алкілом або галоген(C1C4)алкілом; та n має значення 0, 1 або 2; або їх фармацевтично прийнятних солей. Даний винахід також відноситься до фармацевтичної композиції, що містить сполуку формули (I) і фармацевтично прийнятний ексципієнт. Даний винахід також відноситься до способу лікування синдрому подразненої товстої кишки, що включає введення людині, що потребує цього, ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. Даний винахід також відноситься до способу лікування раку, що включає введення людині, що потребує цього, ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. 2 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 Даний винахід також відноситься до сполук формули (I) для застосування в терапії. Даний винахід також відноситься до застосування сполуки формули (I) або її фармацевтично прийнятної солі для лікування синдрому подразненої товстої кишки. Даний винахід також відноситься до застосування сполуки формули (I) або її фармацевтично прийнятної солі для лікування раку. Даний винахід також відноситься до застосування сполуки формули (I) або її фармацевтично прийнятної солі при отриманні лікарського засобу для лікування захворювань, опосередкованих RET. Даний винахід також відноситься до застосування сполуки формули (I) або її фармацевтично прийнятної солі для отримання лікарського засобу для лікування синдрому подразненої товстої кишки. Даний винахід також відноситься до застосування сполуки формули (I) або її фармацевтично прийнятної солі для отримання лікарського засобу для лікування раку. ДЕТАЛЬНИЙ ОПИС ВИНАХОДУ Даний винахід відноситься до сполук формули (I) або їх фармацевтично прийнятних солей, як визначено раніше. Даний винахід також відноситься до сполук формули (II): де: 10 X являє собою N або CR ; 1 R являє собою водень, галоген, (C1-C6)алкіл, галоген(C1-C6)алкіл, (C3-C6) циклоалкіл, гідроксил, (C1-C6)алкоксі, галоген(C1-C6)алкоксі, (C3-C6)циклоалкоксі, аміно, ((C1-C6)алкіл)аміноабо ((C1-C6)алкіл)((C1-C6)алкіл)аміно-; 2 кожен R незалежно вибраний з групи, що включає галоген, (C 1-C6)алкіл, галоген(C1C6)алкіл, (C3-C6)циклоалкіл, ціано, гідроксил, (C1-C6)алкоксі, галоген(C1-C6)алкоксі, (C3C6)циклоалкоксі, аміно, ((C1-C6)алкіл)аміно- і ((C1-C6)алкіл)((C1-C6)алкіл)аміно-; 4 R являє собою водень, (C1-C6)алкіл, галоген(C1-C6)алкіл, (C3-C6)циклоалкіл або 4-6-членний гетероциклоалкіл; де вказаний (C1-C6)алкіл необов'язково заміщений ціано, гідроксилом, (C 15 6 C4)алкоксі, галоген(C1-C4)алкоксі або -NR R ; і де вказаний (C3-C6)циклоалкіл необов'язково заміщений одним або двома замісниками, незалежно вибраними з групи, що включає (C 1C4)алкіл, галоген(C1-C4)алкіл, гідроксил, гідроксі(C1-C4)алкіл, (C1-C4)алкоксі і галоген(C1C4)алкоксі; і де вказаний 4-6-членний гетероциклоалкіл необов'язково заміщений одним або двома замісниками, незалежно вибраними з групи, що включає (C 1-C4)алкіл і галоген(C1C4)алкіл; 5 6 R і R , кожен незалежно, вибрані з групи, що включає водень, (C 1-C4)алкіл і галоген(C1C4)алкіл; 5 6 або R і R , узяті разом з азотом, до якого вони приєднані, являють собою 5- або 6-членне насичене кільце, що необов'язково містить додатковий гетероатом, вибраний з кисню, азоту і сірки, де вказане кільце необов'язково заміщене галогеном, (C1-C4)алкілом або галоген(C1C4)алкілом; 7 R являє собою водень, галоген або (C1-C4)алкоксі; 8 R являє собою водень, галоген, (C1-C6)алкіл, галоген(C1-C6)алкіл, (C3-C6) циклоалкіл, ціано, 4 5 6 5- або 6-членний гетероарил, -OR або -CONR R ; де вказаний (C1-C6)алкіл необов'язково 5 6 заміщений ціано, гідроксилом, (C 1-C4)алкоксі, галоген(C1-C4)алкоксі або -NR R ; і де вказаний 5або 6-членний гетероарил необов'язково заміщений галогеном, (C1-C4)алкілом або галоген(C1C4)алкілом; 9 R являє собою водень, галоген або галоген(C1-C4)алкіл; 10 R являє собою водень, галоген, галоген(C1-C4)алкіл або 5- або 6-членний гетероарил, де вказаний 5- або 6-членний гетероарил необов'язково заміщений галогеном, (C 1-C4)алкілом або галоген(C1-C4)алкілом; і n має значення 0, 1 або 2; 3 UA 115264 C2 10 5 10 15 20 25 30 35 40 45 50 55 60 7 8 9 10 за умови, що коли X являє собою CR , щонайменше один з R , R , R і R являє собою водень; або їх фармацевтично прийнятних солей. У іншому варіанті здійснення, даний винахід відноситься до сполук формули (I) або (II), де 1 R являє собою фтор, хлор, (C1-C4)алкіл, гідроксил, (C1-C4)алкоксі, галоген(C1-C4)алкоксі, (C3C6)циклоалкоксі, аміно, ((C1-C6)алкіл)аміно- або ((C1-C6)алкіл)((C1-C6)алкіл)аміно-. В іншому 1 варіанті здійснення, даний винахід відноситься до сполук формули (I) або (II), де R являє собою (C1-C4)алкоксі. У конкретному варіанті здійснення, даний винахід відноситься до сполук 1 формули (I) або (II), де R являє собою етоксі. У іншому варіанті здійснення, даний винахід відноситься до сполук формули (I) або (II), де n 2 має значення 1 або 2, і кожен R незалежно являє собою галоген. В іншому варіанті здійснення, 2 даний винахід відноситься до сполук формули (I) або (II), де n має значення 1 або 2, і кожен R являє собою фтор. 3 У іншому варіанті здійснення, даний винахід відноситься до сполук формули (I), де R являє собою феніл, який необов'язково заміщений одним-трьома замісниками, незалежно вибраними з групи, що включає галоген, (C1-C6)алкіл, галоген(C1-C6)алкіл, (C3-C6)циклоалкіл, ціано, 5- або 4 5 6 6-членний гетероарил, -OR і -CONR R ; де вказаний (C1-C6)алкіл необов'язково заміщений 5 6 групами ціано, гідроксил, (C1-C4)алкоксі, галоген(C1-C4)алкоксі або -NR R ; і де вказаний 5- або 6-членний гетероарил необов'язково заміщений галогеном, (C 1-C4)алкілом або галоген(C1C4)алкілом. В іншому варіанті здійснення, даний винахід відноситься до сполук формули (I), де 3 R являє собою феніл, який необов'язково заміщений одним-трьома замісниками, незалежно вибраними з групи, що включає фтор, хлор, (C1-C6)алкіл, галоген(C1-C4)алкіл, ціано, (C1C4)алкоксі, гідроксі(C2-C4) алкоксі-, (C1-C4)алкоксі(C2-C4)алкоксі-, аміно(C2-C4)алкоксі-, ((C1C4)алкіл)аміно(C2-C4)алкоксі-, ((C1-C4)алкіл)((C1-C4)алкіл)аміно(C2-C4)алкоксі- і -CONH2; де вказаний (C1-C6)алкіл необов'язково заміщений ціано, гідроксилом, (C 1-C4)алкоксі, аміно, ((C1C4)алкіл)аміно- або ((C1-C4)алкіл)((C1-C4)алкіл)аміно-. В іншому варіанті здійснення, даний 3 винахід відноситься до сполук формули (I), де R являє собою феніл, який необов'язково заміщений одним або двома замісниками, незалежно вибраними з (C 1-C4)алкілу і галоген(C1C4)алкілу; де вказаний (C1-C4)алкіл необов'язково заміщений ціано або гідроксилом. 3 У іншому варіанті здійснення, даний винахід відноситься до сполук формули (I), де R являє собою фураніл, тієніл, піроліл, імідазоліл, піразоліл, триазоліл, тетразоліл, оксазоліл, тіазоліл, ізоксазоліл, ізотіазоліл, оксадіазоліл, тіадіазоліл, піридиніл, піридизаніл, піразиніл, піримідиніл або триазиніл, кожен з яких необов'язково заміщений одним-трьома замісниками, незалежно вибраними з групи, що включає галоген, (C1-C6)алкіл, галоген(C1-C6)алкіл, (C3-C6)циклоалкіл, 4 5 6 ціано, 5- або 6-членний гетероарил, -OR і -CONR R ; де вказаний (C1-C6)алкіл необов'язково 5 6 заміщений ціано, гідроксилом, (C 1-C4)алкоксі, галоген(C1-C4)алкоксі або -NR R ; і де вказаний 5або 6-членний гетероарил необов'язково заміщений галогеном, (C1-C4)алкілом або галоген(C1C4)алкілом. В іншому варіанті здійснення, даний винахід відноситься до сполук формули (I), де 3 R являє собою фураніл, тієніл, піроліл, імідазоліл, піразоліл, триазоліл, тетразоліл, оксазоліл, тіазоліл, ізоксазоліл, ізотіазоліл, оксадіазоліл, тіадіазоліл, піридиніл, піридизаніл, піразиніл, піримідиніл або триазиніл, кожен з яких необов'язково заміщений одним-трьома замісниками, незалежно вибраними з групи, що включає фтор, хлор, (C1-C6)алкіл, галоген(C1-C4)алкіл, ціано, (C1-C4)алкоксі, гідроксі(C2-C4)алкоксі-, (C1-C4) алкоксі(C2-C4)алкоксі-, аміно(C2-C4)алкоксі-, ((C1C4)алкіл)аміно(C2-C4)алкоксі-, ((C1-C4)алкіл)((C1-C4)алкіл)аміно(C2-C4)алкоксі- і -CONH2; де вказаний (C1-C6)алкіл необов'язково заміщений ціано, гідроксилом, (C1-C4)алкоксі, аміно, ((C1C4)алкіл) аміно- або ((C1-C4)алкіл)((C1-C4)алкіл)аміно-. 3 У іншому варіанті здійснення, даний винахід відноситься до сполук формули (I), де R являє собою піридиніл, який необов'язково заміщений одним-трьома замісниками, незалежно вибраними з групи, що включає фтор, хлор, (C1-C6)алкіл, галоген(C1-C4)алкіл, ціано, (C1C4)алкоксі, гідроксі(C2-C4)алкоксі-, (C1-C4) алкоксі(C2-C4)алкоксі-, аміно(C2-C4)алкоксі-, ((C1C4)алкіл)аміно(C2-C4)алкоксі-, ((C1-C4)алкіл)((C1-C4)алкіл)аміно(C2-C4)алкоксі- і -CONH2; де вказаний (C1-C6)алкіл необов'язково заміщений ціано, гідроксилом, (C 1-C4)алкоксі, аміно, ((C1C4)алкіл) аміно- або ((C1-C4)алкіл)((C1-C4)алкіл)аміно-. В іншому варіанті здійснення, даний 3 винахід відноситься до сполук формули (I), де R являє собою піридиніл, який необов'язково заміщений одним або двома замісниками, незалежно вибраними з групи, що включає (C 1C4)алкіл і галоген(C1-C4)алкіл; де вказаний (C1-C4)алкіл необов'язково заміщений ціано або гідроксилом. 3 У іншому варіанті здійснення, даний винахід відноситься до сполук формули (I), де R являє собою фураніл, тієніл, піроліл, імідазоліл, піразоліл, триазоліл, тетразоліл, оксазоліл, тіазоліл, ізоксазоліл, ізотіазоліл, оксадіазоліл, тіадіазоліл, піридиніл, піридизаніл, піразиніл, піримідиніл 4 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 або триазиніл, кожен з яких необов'язково заміщений (C1-C4)алкілом або галоген(C1-C4)алкілом. 3 В іншому варіанті здійснення, даний винахід відноситься до сполук формули (I), де R являє собою ізоксазоліл, який необов'язково заміщений (C1-C4)алкілом або галоген(C1-C4)алкілом. 7 У іншому варіанті здійснення, даний винахід відноситься до сполук формули (II), де R являє собою водень або галоген. У конкретному варіанті здійснення, даний винахід відноситься до 7 сполук формули (II), де R являє собою водень або фтор. У конкретнішому варіанті здійснення, 7 даний винахід відноситься до сполук формули (II), де R являє собою водень. 8 У іншому варіанті здійснення, даний винахід відноситься до сполук формули (II), де R являє собою водень, фтор, хлор, (C1-C6)алкіл, галоген(C1-C4)алкіл, ціано, (C1-C4)алкоксі, гідроксі(C2C4)алкоксі-, (C1-C4)алкоксі(C2-C4)алкоксі-, аміно(C2-C4) алкоксі-, ((C1-C4)алкіл)аміно(C2-C4)алкоксі, ((C1-C4)алкіл)((C1-C4)алкіл)аміно(C2-C4) алкоксі- або -CONH2; де вказаний (C1-C6)алкіл необов'язково заміщений ціано, гідроксилом, (C1-C4)алкоксі, аміно, ((C1-C4)алкіл)аміно- або ((C1C4)алкіл)((C1-C4) алкіл)аміно-. В іншому варіанті здійснення, даний винахід відноситься до 8 сполук формули (II), де R являє собою водень або (C1-C6)алкіл; де вказаний (C1-C6)алкіл необов'язково заміщений ціано, гідроксилом, (C1-C4)алкоксі, аміно, ((C1-C4)алкіл) аміно- або ((C1C4)алкіл)((C1-C4)алкіл)аміно-. В іншому варіанті здійснення, даний винахід відноситься до сполук 8 формули (II), де R являє собою (C1-C4)алкіл, який необов'язково заміщений ціано, гідроксилом, (C1-C4)алкоксі, аміно, ((C1-C4)алкіл) аміно- або ((C1-C4)алкіл)((C1-C4)алкіл)аміно-. 9 У іншому варіанті здійснення, даний винахід відноситься до сполук формули (II), де R являє собою галоген(C1-C4)алкіл. У конкретному варіанті здійснення, даний винахід відноситься до 9 сполук формули (II), де R являє собою трифторметил. У іншому варіанті здійснення, даний винахід відноситься до сполук формули (II), де X являє 10 10 собою CR , і R являє собою водень, галоген, галоген(C1-C4) алкіл, фураніл, тієніл, піроліл, імідазоліл, піразоліл, триазоліл, тетразоліл, оксазоліл, тіазоліл, ізоксазоліл, ізотіазоліл, оксадіазоліл, тіадіазоліл, піридиніл, піридизаніл, піразиніл, піримідиніл або триазиніл, де вказаний фураніл, тієніл, піроліл, імідазоліл, піразоліл, триазоліл, тетразоліл, оксазоліл, тіазоліл, ізоксазоліл, ізотіазоліл, оксадіазоліл, тіадіазоліл, піридиніл, піридизаніл, піразиніл, піримідиніл або триазиніл необов'язково заміщений галогеном, (C1-C4)алкілом або галоген(C1C4)алкілом. В іншому варіанті здійснення, даний винахід відноситься до сполук формули (II), де 10 10 X являє собою CR , і R являє собою водень, фтор, хлор або трифторметил. У конкретному варіанті здійснення, даний винахід відноситься до сполук формули (II), де X являє собою CH. В іншому конкретному варіанті здійснення, даний винахід відноситься до сполук формули (II), де X являє собою N. У конкретнішому варіанті здійснення, даний винахід відноситься до сполук формули (II) або їх фармацевтично прийнятних солей, де: X являє собою CH; 1 R являє собою (C1-C4)алкоксі; 2 кожен R незалежно являє собою галоген; 7 R являє собою водень або галоген; 8 R являє собою водень, фтор, хлор, (C1-C6)алкіл, галоген(C1-C4)алкіл, ціано, (C1-C4)алкоксі, гідроксі(C2-C4)алкоксі-, (C1-C4)алкоксі(C2-C4)алкоксі-, аміно(C2-C4) алкоксі-, ((C1C4)алкіл)аміно(C2-C4)алкоксі-, ((C1-C4)алкіл)((C1-C4)алкіл)аміно(C2-C4) алкоксі- або -CONH2; де вказаний (C1-C6)алкіл необов'язково заміщений ціано, гідроксилом, (C 1-C4)алкоксі, аміно, ((C1C4)алкіл)аміно- або ((C1-C4)алкіл)((C1-C4) алкіл)аміно-; 9 R являє собою галоген(C1-C4)алкіл; та n має значення 1 або 2. У конкретнішому варіанті здійснення, даний винахід відноситься до сполук формули (II) або їх фармацевтично прийнятних солей, де: X являє собою N; 1 R являє собою (C1-C4)алкоксі; 2 кожен R незалежно являє собою галоген; 7 R являє собою водень або галоген; 8 R являє собою водень, фтор, хлор, (C1-C6)алкіл, галоген(C1-C4)алкіл, ціано, (C1-C4)алкоксі, гідроксі(C2-C4)алкоксі-, (C1-C4)алкоксі(C2-C4)алкоксі-, аміно(C2-C4) алкоксі-, ((C1C4)алкіл)аміно(C2-C4)алкоксі-, ((C1-C4)алкіл)((C1-C4)алкіл)аміно(C2-C4) алкоксі- або -CONH2; де вказаний (C1-C6)алкіл необов'язково заміщений ціано, гідроксилом, (C 1-C4)алкоксі, аміно, ((C1C4)алкіл)аміно- або ((C1-C4)алкіл)((C1-C4) алкіл)аміно-; 9 R являє собою галоген(C1-C4)алкіл; та n має значення 1 або 2. Даний винахід також відноситься до сполук, які проілюстровані в Експериментальному 5 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 розділі. Конкретні сполуки за даним винаходом включають: 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(6-(2-гідроксипропан-2-іл)-5(трифторметил)піридин-3-іл)ацетамід; N-(6-етоксі-5-(трифторметил)піридин-3-іл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2фторфеніл)ацетамід; 2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(4-(3-гідроксі-2,2диметилпропіл)-3-(трифторметил)феніл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2,3-дифторфеніл)-N-(4-(2-гідроксіетоксі)-3(трифторметил)феніл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(4-(3-гідроксі-2,2диметилпропіл)-3-(трифторметил)феніл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-3-фторфеніл)-N-(4-(3-гідроксі-2,2диметилпропіл)-3-(трифторметил)феніл)ацетамід; N-(4-ціано-3-(трифторметил)феніл)-2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-3фторфеніл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2,6-дифторфеніл)-N-(4-(2-гідроксіетоксі)-3(трифторметил)феніл)ацетамід; N-(4-ціано-3-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2фторфеніл)ацетамід; N-(6-(2-(диметиламіно)етоксі)-5-(трифторметил)піридин-3-іл)-2-(4-(4-етоксі-6-оксо-1,6дигідропіридин-3-іл)-2-фторфеніл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(4-метил-1H-імідазол-1-іл)-5(трифторметил)феніл)ацетамід; N-(6-(2-ціанопропан-2-іл)-5-(трифторметил)піридин-3-іл)-2-(4-(5-етоксі-6-оксо-1,6дигідропіридин-3-іл)-2-фторфеніл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(4-(2-гідроксіетоксі)-3(трифторметил)феніл)ацетамід; N-(6-(ціанометил)-5-(трифторметил)піридин-3-іл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3іл)-2-фторфеніл)ацетамід; N-(6-(1-ціаноетил)-5-(трифторметил)піридин-3-іл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3іл)-2-фторфеніл)ацетамід; N-(4-хлор-3-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2фторфеніл)ацетамід; N-(4-((диметиламіно)метил)-3-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6дигідропіридин-3-іл)-2-фторфеніл)ацетамід; N-(3,4-дихлорфеніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(5-(1,1,1-трифтор-2метилпропан-2-іл)ізоксазол-3-іл)ацетамід; 2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(4-(2-гідроксіетоксі)-3(трифторметил)феніл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(4-((4-етилпіперазин-1іл)метил)-3-(трифторметил)феніл)ацетамід; N-(2,5-дифторфеніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамід; 4-(2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)ацетамідо)-2(трифторметил)бензамід; N-(2,4-дифтор-5-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2фторфеніл)ацетамід; N-(3,5-біс(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2фторфеніл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(2-фтор-5(трифторметил)феніл)ацетамід; 2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(1,1,1-трифтор-2метилпропан-2-іл)ізоксазол-5-іл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(1,1,1-трифтор-2метилпропан-2-іл)ізоксазол-5-іл)ацетамід; 2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(5-метил-1,3,4-оксадіазол-2іл)-5-(трифторметил)феніл)ацетамід; 2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(5-(1,1,1-трифтор-2метилпропан-2-іл)ізоксазол-3-іл)ацетамід; 6 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(6-(1-гідроксі-2-метилпропан-2іл)-5-(трифторметил)піридин-3-іл)ацетамід; 2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-3-фторфеніл)-N-(4-(3-гідроксі-2,2диметилпропіл)-3-(трифторметил)феніл)ацетамід; 2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3(трифторметил)феніл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(4-метил-1H-піразол-1-іл)-5(трифторметил)феніл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(3-метил-1H-піразол-1-іл)-5(трифторметил)феніл)ацетамід; N-(3-(1H-піразол-4-іл)-5-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)2-фторфеніл)ацетамід; 2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(6-(1,1,1-трифтор-2метилпропан-2-іл)піридин-3-іл)ацетамід; N-(4-ціано-3-(трифторметил)феніл)-2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2фторфеніл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(2-морфоліноетоксі)-5(трифторметил)феніл)ацетамід; 2-(4-(4-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(1,1,1-трифтор-2метилпропан-2-іл)ізоксазол-5-іл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(1-метил-3-(1,1,1-трифтор-2метилпропан-2-іл)-1H-піразол-5-іл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(1,1,1-трифтор-2метилпропан-2-іл)-1H-піразол-5-іл)ацетамід; N-(4-(2,2-дифтор-3-гідроксипропіл)-3-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6дигідропіридин-3-іл)-2-фторфеніл)ацетамід; N-(3-(2H-тетразол-5-іл)-5-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3іл)-2-фторфеніл)ацетамід; 2-(4-(5-етоксі-6-оксо-1,6-дигідропіридин-3-іл)-2-фторфеніл)-N-(3-(1-метил-1H-піразол-4-іл)-5(трифторметил)феніл)ацетамід; і N-(3-(2-(диметиламіно)етоксі)-5-(трифторметил)феніл)-2-(4-(5-етоксі-6-оксо-1,6дигідропіридин-3-іл)-2-фторфеніл)ацетамід; або їх фармацевтично прийнятні солі. Середньому фахівцеві в даній галузі буде зрозуміло, що сполуки за даним винаходом можуть мати альтернативні назви, коли використовують іншу програму привласнення назв. Даний винахід також відноситься до сполук формули (I) або (II) або будь-яких з ілюстративних сполук або їх фармацевтично прийнятних солей для застосування в терапії. Зокрема, для застосування в лікуванні захворювань, опосередкованих RET: синдром подразненої товстої кишки (IBS) включаючи тип дефекації з переважанням діареї, з переважанням запору або переміжний тип, функціональне здуття живота, функціональний запор, функціональна діарея, невизначений функціональний розлад кишечнику, функціональний абдомінальний больовий синдром, хронічний ідіопатичний запор, функціональні розлади стравоходу, функціональні гастродуоденальні розлади, функціональний аноректальний біль, запальне захворювання кишечнику, проліферативне захворювання, як-от недрібноклітинний рак легені, гепатоцелюлярна карцинома, рак прямої кишки, медулярний рак щитовидної залози, фолікулярний рак щитовидної залози, анапластичний рак щитовидної залози, папілярний рак щитовидної залози, пухлини головного мозку, рак черевної порожнини, солідні пухлини, інші види раку легенів, рак голови та шиї, гліоми, нейробластоми, синдром Фон Гіппеля-Ліндау і злоякісні пухлини нирок, рак молочної залози, рак фаллопієвих труб, рак яєчників, перехідно-клітинний рак, рак передміхурової залози, рак стравоходу та гастроезофагеального переходу, рак жовчних проток та аденокарцинома. Зокрема, даний винахід відноситься до сполук формули (I) або (II) або будь-яких з ілюстративних сполук або їх фармацевтично прийнятних солей для застосування в лікуванні синдрому подразненої товстої кишки (IBS), включаючи тип дефекації з переважанням діареї, з переважанням запору або переміжний тип, функціонального здуття живота, функціонального запору, функціональної діареї, невизначеного функціонального розладу кишечнику, функціонального абдомінального больового синдрому, хронічного ідіопатичного запору, функціональних розладів стравоходу, функціональних гастродуоденальних розладів, функціонального аноректального болю, запального захворювання кишечнику, недрібноклітинного раку легені, гепатоцелюлярної карциноми, колоректального раку, медулярного раку щитовидної залози, фолікулярного раку 7 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 щитовидної залози, анапластичного раку щитовидної залози, папілярного раку щитовидної залози, пухлини головного мозку, раку черевної порожнини, солідних пухлин, інших видів раку легенів, раку голови та шиї, гліоми, нейробластоми, синдрому Фон Гіппеля-Ліндау і злоякісних пухлин нирок, раку молочної залози, раку фаллопієвих труб, раку яєчників, перехідно-клітинного раку, раку передміхурової залози, раку стравоходу та гастроезофагеального переходу, раку жовчних проток та аденокарциноми. Даний винахід також відноситься до сполук формули (I) або (II) або будь-яких з ілюстративних сполук або їх фармацевтично прийнятних солей для застосування як лікарський засіб. В іншому варіанті здійснення, винахід відноситься до застосування сполук за даним винаходом для отримання лікарського засобу для лікування захворювань, опосередкованих RET. Даний винахід також відноситься до сполук формули (I) або (II) або будь-яких з ілюстративних сполук або їх фармацевтично прийнятних солей для отримання лікарського засобу для лікування синдрому подразненої товстої кишки. Даний винахід також відноситься до сполук формули (I) або (II) або будь-яких з ілюстративних сполук або їх фармацевтично прийнятних солей для отримання лікарського засобу для лікування раку. Даний винахід також відноситься до застосування сполук формули (I) або (II) або будь-яких ілюстративних сполук у терапії. Винахід також включає застосування сполук за даним винаходом як активний терапевтичний засіб, зокрема для лікування захворювань, опосередкованих RET. Даний винахід також відноситься до застосування сполук формули (I) або (II) або будь-яких ілюстративних сполук для лікування синдрому подразненої товстої кишки. Даний винахід також відноситься до застосування сполук формули (I) або (II) або будь-яких ілюстративних сполук для лікування раку. З урахуванням їх потенційного застосування в медицині, солі сполук формули (I) переважно є фармацевтично прийнятними. Відповідні фармацевтично прийнятні солі включають солі, описані в Berge, Bighley and Monkhouse, J. Pharm. Sci. (1977) 66, pp 1-19. Солі, охоплені терміном "фармацевтично прийнятні солі", відносяться до не-токсичних солей сполук за даним винаходом. Солі розкриваних сполук, що містять основний амін або іншу основну функціональну групу, можна отримати будь-яким відповідним способом, відомим у даній галузі, включаючи обробку вільної основи неорганічною кислотою, як-от хлористоводнева кислота, бромистоводнева кислота, сірчана кислота, азотна кислота, фосфорна кислота і подібні, або органічною кислотою, як-от оцтова кислота, трифтороцтова кислота, малеїнова кислота, бурштинова кислота, мигдалева кислота, фумарова кислота, малонова кислота, піровиноградна кислота, щавлева кислота, гліколева кислота, саліцилова кислота, піраносидильна кислота, якот глюкуронова кислота або галактуронова кислота, альфа-оксикислота, як-от лимонна кислота або винна кислота, амінокислоти, як-от аспарагінова кислота або глутамінова кислота, ароматична кислота, як-от бензойна кислота або корична кислота, сульфонова кислота, як-от пара-толуолсульфонова кислота, метансульфонова кислота, етансульфонова кислота, або подібні. Приклади фармацевтично прийнятних солей включають сульфати, піросульфати, бісульфат, сульфіти, бісульфіти, фосфати, хлориди, броміди, йодиди, ацетати, пропіонати, деканоати, каприлати, акрилати, формати, ізобутирати, капроати, гептаноати, пропіолати, оксалати, малонати, сукцинати, суберати, себакати, фумарати, малеати, бутин1,4діоати, гексин-1,6-діоати, бензоати, хлорбензоати, метилбензоати, динітробензоати, гідроксибензоати, метоксибензоати, фталати, фенілацетати, фенілпропіонати, фенілбутирати, цитрати, лактати γгідроксибутирати, гліколяти, тартрати, манделати і сульфонати, як-от ксилолсульфонати, метансульфонати, пропансульфонати, нафталін1сульфонати і нафталін2сульфонати. Солі розкриваних сполук, що містять карбонову кислоту або іншу кислотну функціональну групу, можна отримати шляхом взаємодії з відповідною основою. Таку фармацевтично прийнятну сіль можна отримати з основою, яка дає фармацевтично прийнятний катіон, яка включає солі лужного металу (зокрема, натрію і калію), солі лужно-земельного металу (зокрема, кальцію і магнію), солі алюмінію і солі амонію, а також солі, отримані з фізіологічно прийнятних органічних основ, як-от триметиламін, триетиламін, морфолін, піридин, піперидин, піколін, дициклогексиламін, N, N’-дибензилетилендіамін, 2-гідроксіетиламін, біс-(2-гідроксіетил)амін, три-(2-гідроксіетил)амін, прокаїн, дибензилпіперидин, дегідроабіетиламін, N, N’бісдегідроабіетиламін, глюкамін, N-метилглюкамін, колідин, холін, хінін, хінолін і основна амінокислота, як-от лізин та аргінін. Інші солі, які не є фармацевтично прийнятними, можуть бути корисними в отриманні сполук за даним винаходом, і їх слід розглядати як утворюючі ще один аспект даного винаходу. Ці солі, як-от трифторацетат, хоча і не є самі по собі фармацевтично прийнятними, можуть бути корисними в отриманні солей, корисних як проміжні сполуки при отриманні сполук за даним винаходом та їх фармацевтично прийнятних солей. 8 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 Якщо сполука за даним винаходом, що містить основний амін або іншу основну функціональну групу, виділяють у вигляді солі, то відповідну форму вільної основи цієї сполуки можна отримати будь-яким відповідним способом, відомим у даній галузі, включаючи обробку солі неорганічною або органічною основою, переважно неорганічною або органічною основою, що має вищі значення pKa, ніж форма вільної основи сполуки. Аналогічно, якщо сполуку за даним винаходом, що містить карбонову кислоту або іншу кислотну функціональну групу, виділяють у вигляді солі, відповідну форму вільної кислоти цієї сполуки можна отримати будьяким відповідним способом, відомим у даній галузі, включаючи обробку солі неорганічною або органічною кислотою, переважно неорганічною або органічною кислотою, що має нижче значення pKa, ніж форма вільної кислоти сполуки. У даний заявці, термін "сполука формули (I)” відноситься до однієї або декількох сполук формули (I). Сполука формули (I) може існувати в твердій або рідкій формі. У твердому стані, вона може існувати в кристалічній або некристалічній формі або у вигляді їх суміші. Фахівцям у даній галузі буде очевидно, що фармацевтично прийнятні сольвати можуть бути утворені для кристалічних або не-кристалічних сполук. У кристалічних сольватах молекули розчинника вбудовані в кристалічну решітку в процесі кристалізації. Сольвати можуть включати не-водні розчинники, як-от, але не обмежуючись цим, етанол, ізопропанол, DMSO, оцтова кислота, етаноламін або етилацетат, або вони можуть включати воду як розчинник, яка може бути вбудована в кристалічну решітку. Сольвати, в яких вода являє собою розчинник, вбудований у кристалічну решітку, зазвичай називають "гідратами". Гідрати включають стехіометричні гідрати, а також композиції, що містять різні кількості води. Винахід включає всі такі сольвати. Фахівцям у даній галузі також буде очевидно, що деякі сполуки за даним винаходом, які існують у кристалічній формі, включаючи їх різні сольвати, можуть проявляти поліморфізм (тобто, здатність проявлятися в різних кристалічних структурах). Ці різні кристалічні форми зазвичай відомі як "поліморфи". Винахід включає всі такі поліморфи. Поліморфи мають однаковий хімічний склад, але відрізняються упаковкою, геометричним розташуванням та іншими описовими характеристиками кристалічного твердого стану. З цієї причини поліморфи, можуть мати різні фізичні властивості, як-от форма, щільність, твердість, деформативність, стійкість і властивості розчинення. Поліморфи зазвичай показують різні температури плавлення, ІЧ-спектри і порошкові рентгенограми, які можуть бути використані для ідентифікації. Фахівцям у даній галузі буде очевидно, що різні поліморфи можна отримати, наприклад, змінюючи або регулюючи умови реакції або реагенти, використовувані при отриманні сполуки. Наприклад, зміни температури, тиску або розчинника можуть дати в результаті поліморфи. Окрім цього, один поліморф може самовільно перетворитися в інший поліморф за певних умов. Сполука формули (I) або (II) або її солі можуть існувати в стереоізомерних формах (наприклад, вона містить один або декілька асиметричних атомів вуглецю). Окремі стереоізомери (енантіомери і діастереомери) і суміші цих сполук включені в обсяг даного винаходу. Обсяг даного винаходу включає суміші стереоізомерів, а також очищені енантіомери або енантіомерно/діастереомерно збагачені суміші. Аналогічно, повинно бути зрозуміло, що сполука або сіль формули (I) або (II) може існувати в таутомерних формах, відмінних від представлених у формулі, і які також включені в обсяг даного винаходу. Наприклад, тоді як сполуки формули (I) і (II) представлені як такі, що містять групу піридин-2-он, відповідний 2-гідроксипіридиновий таутомер також включений в обсяг даного винаходу. Повинно бути зрозуміло, що даний винахід включає всі комбінації і підмножини конкретних груп, визначених раніше в даній заявці. Для фахівця в даній галузі буде очевидним, що деякі захищені похідні сполук формули (I) або (II), які можна отримати до або після кінцевої стадії видалення захисту, можуть не мати фармакологічну активність як таку, але можуть, у деяких випадках, використовуватися для перорального або парентерального введення і потім метаболізуватися в організмі з утворенням сполук за даним винаходом, які є фармакологічно активними. Тому такі похідні можуть бути описані як "проліки". Крім того, деякі сполуки за даним винаходом можуть діяти як проліки інших сполук за даним винаходом. Всі захищені похідні і проліки сполук за даним винаходом включені в обсяг даного винаходу. Приклади відповідних проліків для сполук за даним винаходом описані в Drugs of Today, Volume 19, Number 9, 1983, pp 499-538 і в Topics in Chemistry, Chapter 31, pp 306-316 і в "Design of Prodrugs" by H. Bundgaard, Elsevier, 1985, Chapter 1. Для фахівця в даній галузі також є очевидним, що деякі групи, відомі фахівцям у даній галузі як "про-групи", наприклад, як описано в H. Bundgaard в "Design of Prodrugs", можна розташовувати на відповідних функціональних групах, коли такі функціональні групи присутні в сполуках за даним винаходом. Переважні "про 9 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 групи" для сполук за даним винаходом включають: складний ефір, карбонатний ефір, напівефір, фосфатний ефір, нітроефір, сульфатний ефір, сульфоксид, амід, карбамат, азо-, фосфамід, глікозид, простий ефір, ацетальні і кетальні похідні сполук формули (I) або (II). Введення сполуки за даним винаходом у вигляді проліків може дати можливість фахівцям у даній галузі здійснити одне або більш з наступного: (a) модифікувати початок дії сполуки in vivo; (b) модифікувати тривалість дії сполуки in vivo; (c) модифікувати транспорт або дистрибуцію сполуки in vivo; (d) модифікувати розчинність сполуки in vivo; і (e) здолати побічний ефект або інші труднощі, пов'язані зі сполукою. Даний винахід також включає ізотопно-мічені сполуки, які ідентичні тим, які перелічені у формулі (I) і далі, за винятком того, що один або декілька атомів заміщені атомом, що має атомну масу або масове число відмінні від атомної маси або масового числа, такі, що зазвичай зустрічаються в природі. Приклади ізотопів, які можуть бути включені в сполуки за даним винаходом та їх фармацевтично прийнятні солі, включають ізотопи водню, вуглецю, азоту, 2 3 11 13 14 15 17 18 31 32 35 кисню, фосфору, сірки, фтору, йоду і хлору, такі як H, H, C, C, C, N, O, O, P, P, S, 18 36 123 125 F, Cl, I та I. Сполуки за даним винаходом і фармацевтично прийнятні солі вказаних сполук, які містять вказані вище ізотопи та/або інші ізотопи інших атомів, включені в обсяг даного винаходу. Ізотопно-мічені сполуки за даним винаходом, наприклад, ті, в які включені радіоактивні ізотопи, 3 14 як-от H або C, є корисними в аналізах розподілу лікарського засобу та/або тканин субстрату. 3 14 Ізотопи тритію, тобто H і вуглецю-14, тобто C, є особливо переважними, завдяки легкості їх 11 18 отримання і виявлюваності. Ізотопи C і F є особливо корисними в ПЕТ (позитронно-емісійна 125 томографія), і I ізотопи є особливо корисними в ОФЕКТ (одинфотонна емісійна комп'ютерна томографія), всі вони є корисними в томографії головного мозку. Окрім цього, заміщення більш 2 важкими ізотопами, такими як дейтерій, тобто H, може дати певні терапевтичні переваги в результаті більшої метаболічної стабільності, наприклад, збільшений період напіврозпаду in vivo або зниження вимог дозування і, отже, можуть бути переважними в деяких обставинах. Ізотопно-мічені сполуки формули (I) і наступні за даним винаходом, як правило, можуть бути отримані шляхом здійснення процедур, розкритих нижче на схемах та/або в Прикладах, з використанням легко доступного ізотопно-міченого реагенту замість не міченого ізотопом реагенту. ВИЗНАЧЕННЯ Терміни використовуються в їх загальноприйнятих значеннях. Наступні визначення призначені для роз'яснення, але не обмеження, визначуваних термінів. У даній заявці, термін "алкіл" являє собою насичену, з прямим ланцюгом або розгалужену вуглеводневу групу. Термін "(C1-C6)алкіл" відноситься до алкільної групи, що містить від 1 до 6 атомів вуглецю. Ілюстративні алкіли включають, але не обмежуються цим, метил, етил, нпропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, пентил і гексил. Коли термін "алкіл" використовують у комбінації з іншими групами замісників, як-от "галоген(C1-C4)алкіл" або "гідроксі(C1-C4)алкіл", термін "алкіл" призначений для обхвату дивалентного вуглеводневого радикала з прямим або розгалуженим ланцюгом, де точка приєднання проходить через алкільну групу. Термін "галоген(C1-C4)алкіл" призначений для позначення радикала, що містить один або декілька атомів галогену, які можуть бути однаковими або різними, на одному або декількох атомах вуглецю алкільної групи, що містить від 1 до 4 атомів вуглецю, який являє собою вуглецевий радикал з прямим або розгалуженим ланцюгом. Приклади груп "галоген(C 1-C4)алкіл", корисних у даному винаході, включають, але не обмежуються цим, -CF3 (трифторметил), -CCl3 (трихлорметил), 1,1-дифторетил, 2,2,2трифторетил та гексафторизопропіл. Приклади груп "гідроксі(C 1-C4)алкіл", корисних у даному винаході, включають, але не обмежуються цим, гідроксиметил, гідроксіетил і гідроксіізопропіл. "Алкоксі" відноситься до групи, що містить алкільний радикал, визначений вище, приєднаній через кисневий зв'язувальний атом. Термін “(C1-C4)алкоксі" відноситься до вуглеводневого радикала з прямим або розгалуженим ланцюгом, що містить, щонайменше 1 і до 4 атомів вуглецю, приєднаного через кисневий зв'язувальний атом. Типові “(C 1-C4)алкоксі" групи, корисні в даному винаході, включають, але не обмежуються цим, метоксі, етоксі, н-пропоксі, ізопропоксі, н-бутоксі, втор-бутоксі, ізобутоксі та трет-бутоксі. Коли термін "алкоксі" використовують у комбінації з іншими групами замісників, такими як "галоген(C1-C6)алкоксі", "гідроксі(C2-C4)алкоксі" або “(C1-C4) алкоксі(C2-C4)алкоксі", термін "алкоксі" призначений для позначення дивалентного вуглеводневого радикала з прямим або розгалуженим ланцюгом, де точка приєднання проходить через алкільну групу через кисневий зв'язувальний атом. Термін "галоген(C1-C6)алкоксі" відноситься до вуглеводневого радикала з прямим або розгалуженим ланцюгом, що містить, щонайменше, 1 і до 6 атомів вуглецю з одним 10 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 або декількома атомами галогену, які можуть бути однаковими або різними, зв'язаних з одним або декількома атомами вуглецю, де радикал приєднаний через кисневий зв'язувальний атом. Типові "галоген(C1-C6)алкоксі" групи, корисні в даному винаході, включають, але не обмежуються цим, -OCHF2 (дифторметоксі), -OCF3 (трифторметоксі) і -OCH(CF3)2 (гексафторізопропоксі). Приклади груп "гідроксі(C 2C4)алкоксі", корисних у даному винаході, включають, але не обмежуються цим, 2-гідроксіетоксі і 2-гідроксіізопропоксі. Приклади груп “(C1-C4) алкоксі(C2-C4)алкоксі", корисних у даному винаході, включають, але не обмежуються цим, 2-метоксіетоксі, 2-етоксіетоксі, 2-ізопропоксіетоксі, 2метоксіізопропоксі і 2-етоксіізопропоксі. Як використовується в даній заявці, термін "циклоалкіл" відноситься до не-ароматичного насиченого циклічного вуглеводневого кільця, що містить певну кількість атомів вуглецю. Термін “(C3-C6)циклоалкіл" відноситься до не-ароматичного циклічного вуглеводневого кільця, що містить від трьох до шести кільцевих атомів вуглецю. Типові “(C 3-C6)циклоалкіл" групи, корисні в даному винаході, включають циклопропіл, циклобутил, циклопентил та циклогексил. Як використовується в даній заявці, термін "циклоалкілоксі-” відноситься до групи, що містить циклоалкільний радикал, визначений вище, приєднаний через кисневий зв'язувальний атом. Типові “(C3-C8)циклоалкілоксі-” групи, корисні в даному винаході, включають циклопропілоксі, циклобутилоксі, циклопентилоксі, циклогексилоксі, циклогептилоксі і циклооктилоксі. Як використовується в даній заявці, "4-6-членний гетероциклоалкіл" являє собою групу або фрагмент, що включає не-ароматичний моновалентний моноциклічний радикал, який є насиченим або частково ненасиченим, таким, що містить 4, 5 або 6 кільцевих атомів, який включає один або два гетероатоми, вибраних незалежно з кисню, сірки й азоту. Ілюстративні приклади 4-6-членних гетероциклоалкільних груп, корисних у даному винаході, включають, але не обмежуються цим азетидиніл, оксетаніл, піролідиніл, піразолідиніл, піразолініл, імідазолідиніл, імідазолініл, оксазолініл, тіазолініл, тетрагідрофураніл, дигідрофураніл, 1,3діоксоланіл, піперидиніл, піперазиніл, морфолініл, тіоморфолініл, тетрагідропіраніл, дигідропіраніл, 1,3-діоксаніл, 1,4-діоксаніл, 1,3-оксатіоланіл, 1,3-оксатіаніл, 1,3-дитіаніл, 1,4оксатіоланіл, 1,4-оксатіаніл і 1,4-дитіаніл. Як використовується в даній заявці, "5- або 6-членний гетероарил" являє собою групу або фрагмент, що включає ароматичний моновалентний моноциклічний радикал, що містить 5 або 6 кільцевих атомів, включаючи, щонайменше, один вуглецевий атом і 1-4 гетероатоми, незалежно вибраних з азоту, кисню та сірки. Окремі 5-членні гетероарильні групи, містять один кільцевий гетероатом азоту, кисню або сірки і необов'язково містять 1, 2 або 3 додаткових кільцевих атоми азоту. Окремі 6-членні гетероарильні групи містять 1, 2 або 3 кільцевих гетероатоми азоту. Ілюстративні приклади 5- або 6-членних гетероарильних груп, корисних у даному винаході, включають, але не обмежуються цим фураніл, тієніл, піроліл, імідазоліл, піразоліл, триазоліл, тетразоліл, оксазоліл, тіазоліл, ізоксазоліл, ізотіазоліл, оксадіазоліл, тіадіазоліл, піридиніл, піридизаніл, піразиніл, піримідиніл і триазиніл. Терміни "галоген" і "гало" являють собою хлор, фтор, бром або йод замісники. "Гідроксі" або "гідроксил" призначений для позначення радикала -OH. Як використовується в даній заявці, термін "ціано" відноситься до групи -CN. Як використовується в даній заявці, термін "необов'язково заміщений" вказує, що група, така як алкіл, циклоалкіл, феніл або гетероарил, може бути незаміщеною або група може бути заміщена одним або декількома замісником(замісниками), як визначено. У разі, коли групи можуть бути вибрані з ряду альтернативних груп, вибрані групи можуть бути однаковими або відмінними один від одного. Термін "незалежно" означає, що коли більш ніж один замісник вибраний з ряду можливих замісників, ці замісники можуть бути однаковими або відмінними один від одного. Альтернативні визначення для різних груп і груп замісників формули (I) або (II), представлені в описі винаходу, призначені для конкретного опису кожного з видів сполук, розкриваних у даній заявці, індивідуально, а також груп одного або декількох видів сполук. Обсяг даного винаходу включає будь-яку комбінацію цих визначень груп і груп замісників. "Фармацевтично прийнятний" відноситься до таких сполук, речовин, композицій і лікарських форм, які є, згідно зваженій медичній оцінці, відповідними для використання у контакті з тканинами людини і тварин без зайвої токсичності, подразнення або інших проблем або ускладнень, сумірно з розумним співвідношенням користь/ризик. У даній заявці, термін "фармацевтично прийнятні солі" відноситься до солей, які зберігають бажану біологічну активність сполуки за даним винаходом і проявляють мінімальні небажані токсикологічні ефекти. Ці фармацевтично прийнятні солі можна отримати in situ в процесі 11 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 кінцевого виділення або очищення сполуки або шляхом окремої взаємодії очищеної сполуки у формі її вільної кислоти або формі вільної основи з відповідною основою або кислотою, відповідно. ФАРМАЦЕВТИЧНІ КОМПОЗИЦІЇ Винахід також забезпечує фармацевтичну композицію (також називану фармацевтичний склад), що містить сполуку формули (I) або (II) або її фармацевтично прийнятну сіль і один або декілька ексципієнтів (також називаних у фармацевтиці носіями та/або розчинниками). Ексципієнти є фармацевтично прийнятними в сенсі сумісності з іншими інгредієнтами композиції і не шкідливими для їх реципієнта (тобто, пацієнта). Відповідні фармацевтично прийнятні ексципієнти включають наступні типи ексципієнтів: розчинники, наповнювачі, сполучні, розпушувачі, мастильні речовини, гліданти, гранулюючі речовини, агенти покриття, змочуючі речовини, розчинники, со-розчинники, суспендуючі речовини, емульгатори, підсолоджувачі, ароматизатори, смакові маскувальні агенти, барвники, речовини, що запобігають злежуванню, зволожувачі, хелатотвірні агенти, пластифікатори, речовини, що підвищують в'язкість, антиоксиданти, консерванти, стабілізатори, поверхневоактивні речовини і буферні речовини. Фахівцям у даній галузі буде очевидно, що деякі фармацевтично прийнятні ексципієнти можуть виконувати більш ніж одну функцію і можуть виконувати альтернативні функції залежно від того, яка кількість ексципієнта присутня в композиції і які інші інгредієнти присутні в композиції. Кваліфіковані фахівці мають знання і навики в даній галузі, що дозволяють їм вибрати відповідні фармацевтично прийнятні ексципієнти у відповідних кількостях для використання у винаході. Окрім цього, існує ряд ресурсів, які доступні фахівцям у даній галузі, які описують фармацевтично прийнятні ексципієнти і можуть бути корисними у виборі відповідних фармацевтично прийнятних ексципієнтів. Приклади включають Remington's Pharmaceutical Sciences (Mack Publishing Company), The Handbook of Pharmaceutical Additives (Gower Publishing Limited) і The Handbook of Pharmaceutical Excipients (the American Pharmaceutical Association and the Pharmaceutical Press). Фармацевтичні композиції за даним винаходом отримують з використанням технологій і способів, відомих фахівцям у даній галузі. Деякі із способів, зазвичай використовуваних у даній галузі, описані в Remington's Pharmaceutical Sciences (Mack Publishing Company). Відповідно до іншого аспекту даного винаходу, забезпечується спосіб отримання фармацевтичної композиції, що включає змішування (або домішування) сполуки формули (I) або (II) або її фармацевтично прийнятної солі, з щонайменше одним ексципієнтом. Фармацевтичні композиції можуть бути в стандартній лікарській формі, що містить заздалегідь певну кількість активного інгредієнта на стандартну дозу. Така одиниця може містити терапевтично ефективну дозу сполуки формули (I) або (II) або її фармацевтично прийнятної солі або частину терапевтично ефективної дози, таку, що декілька стандартних лікарських форм можна вводити в заданий час для досягнення бажаної терапевтично ефективної дози. Переважні стандартні лікарські форми являють собою композиції, що містять добову дозу або частину дози, як вказано вище, або відповідну частину дози, активного інгредієнта. Крім того, такі фармацевтичні композиції можна отримати будь-яким із способів, добре відомих у галузі фармацевтики. Фармацевтичні композиції можуть бути адаптовані для введення будь-яким відповідним шляхом, наприклад, пероральним (включаючи трансбукальний або сублінгвальний), ректальним, назальним, місцевим (включаючи букальний, під'язиковий або трансдермальний), вагінальним або парентеральним (включаючи підшкірний, внутрішньом'язовий, внутрішньовенний або внутрішньошкірний) шляхом. Такі композиції можна отримати будь-яким способом, відомим у даній галузі фармації, наприклад, шляхом приведення активного інгредієнта в асоціацію з ексципієнтом(ексципієнтами). Коли вони адаптовані для перорального введення, фармацевтичні композиції можуть бути представлені в дискретних одиницях, як-от таблетки або капсули, порошки або гранули, розчини або суспензії у водних або не-водних рідинах, їстівні пінки і збиті пінки, рідкі емульсії масло-у-воді або рідкі емульсії вода-у-маслі. Сполука або її сіль за даним винаходом або фармацевтична композиція за даним винаходом можуть бути включені в цукерки, пастили та/або композиції для розсмоктування для введення у вигляді "швидкорозчинного" лікарського засобу. Наприклад, для перорального введення у формі таблетки або капсули, активний компонент лікарського засобу може бути об'єднаний з пероральним, не-токсичним фармацевтично прийнятним інертним носієм, як-от етанол, гліцерин, вода і подібні. Порошки або гранули отримують шляхом подрібнення сполуки до відповідного дрібного розміру і змішування з 12 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 аналогічно подрібненим фармацевтичним носієм, як-от харчовий вуглевод, як, наприклад, крохмаль або маніт. Також можуть бути присутніми ароматизатори, консерванти, диспергуючі і барвники. Капсули отримують шляхом приготування порошкової суміші, як описано вище, і заповнення отриманою сумішшю желатинових або не-желатинових оболонок. Гліданти і мастильні речовини, як-от колоїдний діоксид кремнію, тальк, стеарат магнію, стеарат кальцію, твердий поліетиленгліколь, можуть бути додані в порошкову суміш перед процедурою заповнення. Дезинтегруюча або солюбілізуюча речовина, така як агар-агар, карбонат кальцію або карбонат натрію, також може бути додана для поліпшення доступності лікарського засобу при проковтуванні капсули. Більш того, при бажанні або необхідності, відповідні сполучні речовини, мастильні речовини, розпушувачі і барвники також можуть бути введені в суміш. Відповідні сполучні речовини включають крохмаль, желатин, натуральні цукри, як-от глюкоза або бета-лактоза, цукристі речовини з кукурудзи, природні і синтетичні камеді, як-от аравійська камедь, трагакант, альгінат натрію, карбоксиметилцелюлоза, поліетиленгліколь, віск і подібні. Мастильні речовини, використовувані в цих лікарських формах, включають олеат натрію, стеарат натрію, стеарат магнію, бензоат натрію, ацетат натрію, хлорид натрію і подібні. Розпушувачі включають, без обмеження, крохмаль, метилцелюлозу, агар, бентоніт, ксантанову камедь і подібні речовини. Таблетки сформульовані, наприклад, шляхом отримання порошкової суміші, гранулювання або компактування, додавання мастильної речовини і розпушувача і пресовання в таблетки. Порошкову суміш отримують шляхом змішування сполуки, подрібненої відповідним чином, з розчинником або основою, як описано вище, і необов'язково, зі сполучною речовиною, як-от карбоксиметилцелюлоза й альгінат, желатин або полівінілпіролідон, розчином речовини, що уповільнює розчинення, як-от парафін, прискорювачем ресорбції, як-от четвертинна сіль, та/або агентом абсорбції, як-от бентоніт, каолін або дикальцій фосфат. Порошкову суміш можна гранулювати шляхом змочування сполучної речовини, як-от сироп, крохмальна паста, клейка аравійська камедь або розчини целюлозних або полімерних матеріалів, і продавлювання через сито. Як альтернатива гранулюванню, порошкову суміш можна пропускати через машину для таблетування, внаслідок чого утворюється незавершена компактна форма, що розбивається на гранули. Гранули можуть бути змащені для запобігання прилипанню до штампу для таблетування шляхом додавання стеаринової кислоти, стеаратної солі, тальку або мінерального масла. Змащену суміш потім пресують в таблетки. Сполуку або сіль за даним винаходом також можна об'єднати з текучим інертним носієм і пресувати в таблетки безпосередньо, минаючи стадії дроблення або компактування. Можуть бути забезпечені чисте непрозоре захисне покриття, що складається з ущільнювального покриття з шелаку, покриття з цукру або полімерного матеріалу і полірувальне покриття з воску. До цих покриттів можна додати барвники, аби відрізняти різні дозування. Рідини для перорального введення, як-от розчини, сиропи та еліксири, можна отримати в стандартній лікарській формі так, щоб задана кількість містила заздалегідь певну кількість активного інгредієнта. Сиропи можна отримати шляхом розчинення сполуки або її солі за даним винаходом у відповідному образом ароматизованому водному розчині, тоді як еліксири отримують з використанням не-токсичного спиртного розчинника. Суспензії можуть бути сформульовані шляхом диспергування сполуки або солі за даним винаходом в не-токсичному розчиннику. Солюбілізатори та емульгатори, як-от етоксильовані ізостеарилові спирти та ефіри поліоксіетилену і сорбіту, консерванти, смакові добавки, як-от масло перцевої м'яти, натуральні підсолоджувачі, сахарин або інші штучні підсолоджувачі і подібні, також можна додати. При необхідності, композиції лікарських форм для перорального введення можуть бути мікроінкапсульованими. Композиція також може бути отримана для пролонгованого або сповільненого вивільнення, наприклад, шляхом нанесення покриття або поміщення подрібненої речовини в полімери, віск або т.п. Як використовується в даній заявці, для доставки фармацевтичної композиції переважними є таблетки та капсули. Як використовується в даній заявці, термін "лікування" відноситься до полегшення певного стану, усунення або розслаблення одного або декількох симптомів стану, уповільнення або припинення розвитку стану і запобігання або відстрочення повторного виникнення стану у пацієнта або суб'єкта, що раніше хворів або має такий діагноз. Даний винахід забезпечує спосіб лікування ссавця, зокрема, людини, що страждає від синдрому подразненої товстої кишки (IBS), включаючи тип дефекації з переважанням діареї, з переважанням запору або переміжний тип, функціонального здуття живота, функціонального запору, функціональної діареї, невизначеного функціонального розладу кишечнику, 13 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 функціонального абдомінального больового синдрому, хронічного ідіопатичного запору, функціонального розладу стравоходу, функціональних гастродуоденальних розладів, функціонального аноректального болю, запального захворювання кишечнику, проліферативних захворювань, як-от недрібноклітинний рак легені, гепатоцелюлярна карцинома, рак прямої кишки, медулярний рак щитовидної залози, фолікулярний рак щитовидної залози, анапластичний рак щитовидної залози, папілярний рак щитовидної залози, пухлини головного мозку, рак черевної порожнини, солідні пухлини, інші види раку легенів, рак голови та шиї, гліоми, нейробластоми, синдром Фон Гіппеля-Ліндау і злоякісні пухлини нирок, рак молочної залози, рак фаллопієвих труб, рак яєчників, перехідно-клітинний рак, рак передміхурової залози, рак стравоходу і гастроезофагеального переходу, рак жовчних проток та аденокарцинома або їх комбінації. Таке лікування включає стадію введення терапевтично ефективної кількості сполуки формули (I) або (II) або її фармацевтично прийнятної солі вказаному ссавцеві, зокрема, людині. Лікування також може включати стадію введення терапевтично ефективної кількості фармацевтичної композиції, що містить сполуку формули (I) або (II) або її фармацевтично прийнятну сіль, вказаному ссавцеві, зокрема, людині. Як використовується в даній заявці, термін "ефективна кількість" означає, кількість лікарського засобу або фармацевтичного засобу, яка викликатиме біологічну або медичну відповідь тканини, системи, тварини або людини, до якої прагнуть, наприклад, дослідник або клініцист. Термін "терапевтично ефективна кількість" означає будь-яку кількість, яка, в порівнянні з відповідним суб'єктом, який не отримав такої кількості, приводить до підвищення якості лікування, зцілення, запобігання або полегшення захворювання, розладу або побічних ефектів або зниження швидкості розвитку захворювання або розладу. Термін також охоплює своїм об'ємом кількості, ефективні для посилення нормальної фізіологічної функції. Для застосування в терапії, терапевтично ефективні кількості сполуки формули (I) або (II), а також їх солей, можна вводити у вигляді хімічної сполуки як такої. Окрім цього, активний інгредієнт може бути представлений у вигляді фармацевтичної композиції. Хоча цілком можливо, що для застосування в терапії, терапевтично ефективну кількість сполуки формули (I) або (II) або її фармацевтично прийнятної солі, можна вводити у вигляді хімічної сполуки як такої, вона зазвичай представлена як активний інгредієнт фармацевтичної композиції або складу. Точна терапевтично ефективна кількість сполуки або її солі за даним винаходом залежатиме від ряду чинників, включаючи, але не обмежуючись цим, вік і масу тіла суб'єкта (пацієнта), що лікується, конкретне захворювання, що потребує лікування, і його тяжкість, природу фармацевтичного складу/композиції і спосіб введення, і, кінець кінцем, визначатиметься по розсуду лікаря або ветеринара. Зазвичай сполука формули (I) або (II) або її фармацевтично прийнятна сіль будуть надані для лікування в діапазоні від близько 0,1 до 100 мг/кг маси тіла реципієнта (пацієнта, ссавця) на добу і, типовіше, в діапазоні від 0,1 до 10 мг/кг маси тіла на добу. Допустиме добове дозування може складати від близько 0,1 до близько 1000 мг/доба, і переважно від близько 1 до близько 100 мг/доба. Ця кількість може бути представлена у вигляді разової дози на добу або у вигляді декількох (як, наприклад, дві, три, чотири, п'ять або більше) суб-доз на добу, так, аби загальна добова доза залишалася такою самою. Ефективну кількість солі сполуки можна визначити як пропорцію ефективної кількості сполуки формули (I) або (II) у чистому вигляді. Аналогічні дозування мають бути відповідними для лікування інших станів, указаних в даній заявці для лікування. Загалом, визначення відповідного дозування може легко здійснити фахівець у галузі медицини або фармацевтики. Сполуки за даним винаходом можна використовувати окремо або в комбінації з одним або декількома іншими терапевтичними засобами. Отже, даний винахід забезпечує комбінацію, що містить сполуку формули (I) або її фармацевтично прийнятну сіль і один або декілька інших терапевтичних засобів. Такі комбінації можуть бути представлені окремо (де кожна активна речовина в окремій композиції), або активні речовини можуть бути представлені в об'єднаній композиції. Сполуки за даним винаходом можна об'єднувати або вводити спільно з іншим терапевтичним засобом, зокрема, засобами, які можуть підвищувати активність або час розподілу сполук. Комбіновані терапії відповідно до винаходу включають введення, щонайменше, однієї сполуки за даним винаходом і використання, щонайменше, одного іншого способу лікування. В одному варіанті здійснення винаходу, комбіновані терапії відповідно до винаходу включають введення щонайменше однієї сполуки за даним винаходом і хірургічне лікування. В одному варіанті здійснення винаходу, комбіновані терапії відповідно до винаходу включають введення щонайменше однієї сполуки за даним винаходом і променеву терапію. В одному варіанті здійснення винаходу, комбіновані терапії відповідно до винаходу включають 14 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 введення щонайменше однієї сполуки за даним винаходом і щонайменше одного засобу підтримуючої терапії (наприклад, щонайменше, одного протиблювотного засобу). В одному варіанті здійснення винаходу, комбіновані терапії відповідно до даного винаходу включають введення, щонайменше, однієї сполуки за даним винаходом і щонайменше одного іншого хіміотерапевтичного агента. В одному конкретному варіанті здійснення, винахід включає введення щонайменше однієї сполуки за даним винаходом і щонайменше одного протипухлинного засобу. Ще в одному варіанті здійснення, винахід включає терапевтичний режим, де RET інгібітори за даним розкриттям є неактивними і самі по собі неактивними або в значній мірі неактивними, але при об'єднанні з іншою терапією, яка може або не може бути активною як автономна терапія, комбінація забезпечує корисний терапевтичний результат. Термін "спільне введення" і його похідні в даній заявці відноситься або до одночасного введення, або до будь-якого способу роздільного послідовного введення інгібуючої RET сполуки, як описано в даній заявці, і додаткового активного інгредієнта або інгредієнтів, особливо тих, які, як відомо, є корисними в лікуванні раку, включаючи хіміотерапію та променеву терапію. Термін додатковий активний інгредієнт або інгредієнти, як використовується в даній заявці, включає будь-яку сполуку або терапевтичний засіб, відомий або який демонструє переважні властивості при введенні пацієнтові, що потребує лікування ракового захворювання. Переважно, коли введення не є одночасним, сполуки вводять одна за одною за короткий проміжок часу. Крім того, це не має значення, якщо сполуки вводять в одній і тій самій лікарській формі, наприклад, одну сполуку можна вводити місцево, а іншу сполуку можна вводити перорально. Зазвичай, будь-який протипухлинний засіб, який має активність проти сприйнятливої пухлини, що лікується, можна вводити спільно для лікування конкретних видів ракових захворювань за даним винаходом. Приклади таких засобів можна знайти в Cancer Principles and Practice of Oncology by V.T. Devita and S. Hellman (editors), 6th edition (February 15, 2001), Lippincott Williams & Wilkins Publishers. Середній фахівець у даній галузі зможе визначити, які комбінації засобів можуть бути корисними, на основі конкретних характеристик лікарських засобів і ракового захворювання, що лікується. Звичайні протипухлинні засоби, корисні в даному винаході, включають, але не обмежуються цим, засоби, що впливають на мікротрубочки, як-от дитерпеноїди й алкалоїди барвінку; платинові координаційні комплекси; алкілувальні засоби, як-от азотисті іприти, оксазафосфорини, алкілсульфонати, нітрозосечовини і триазини; антибіотичні засоби, як-от антрацикліни, актиноміцини і блеоміцини; інгібітори топоізомерази II, як-от епідофілотоксини; антиметаболіти, як-от пуринові і піримідинові аналоги і анти-фолатні сполуки; інгібітори топоізомерази I, як-от камптотецини; гормони і гормональні аналоги; інгібітори ДНК метилтрансферази, як-от азацитидин і децитабін; інгібітори шляху сигнальної трансдукції; інгібітори не-рецепторної тирозинкінази, зв'язаної з ангіогенезом; імунотерапевтичні засоби; проапоптотичні засоби; та інгібітори сигналу клітинного циклу. Звичайний будь-який хіміотерапевтичний засіб, який має активність проти сприйнятливої пухлини, що лікується, можна використовувати в комбінації зі сполукою за даним винаходом, за умови, що цей засіб клінічно сумісний з терапією, що використовує сполуку за даним винаходом. Типові протипухлинні засоби, корисні в даному винаході, включають, але не обмежуються цим: алкілувальні засоби, анти-метаболіти, протипухлинні антибіотики, антимітотичні засоби, нуклеозидні аналоги, інгібітори топоізомерази I і II, гормони і гормональні аналоги; ретиноїди, інгібітори гістондеацетилази; інгібітори шляху сигнальної трансдукції, включаючи інгібітори клітинного зростання або функції чинників зростання, інгібітори ангіогенезу і інгібітори серинової/треонінової або іншої кінази; інгібітори циклінзалежної кінази; антисмислові терапії і імунотерапевтичні засоби, включаючи моноклональні антитіла, вакцини або інші біологічні засоби. Нуклеозидні аналоги являють собою такі сполуки, які перетворюються в деоксинуклеотидтрифосфати і вбудовуються в ДНК, що реплікується, замість цитозину. ДНК метилтрансферази стають ковалентно зв'язаними з модифікованими основами, що приводить до неактивного ферменту і зниженого ДНК метилування. Приклади нуклеозидних аналогів включають азацитидин і децитабін, які використовують для лікування мієлодиспластичного розладу. Інгібітори гістондеацетилази (HDAC) включають вориностат, для лікування шкірної Тклітинної лімфоми. HDAC модифікують хроматин через деацетилювання гістонів. Окрім цього, вони мають всілякі субстрати, включаючи багаточисельні чинники транскрипції і сигнальні молекули. Інші інгібітори HDAC знаходяться у стадії розробки. Інгібітори шляху сигнальної трансдукції являють собою такі інгібітори, які блокують або інгібують хімічний процес, який викликає внутрішньоклітинні зміни. У даній заявці ця зміна являє собою клітинну проліферацію або диференціацію або виживання. Інгібітори шляху сигнальної 15 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 трансдукції, корисні в даному винаході, включають, але не обмежуються цим, інгібітори рецепторних тирозинкіназ, не-рецепторних тирозинкіназ, блокаторів SH2/SH3 домену, серинових/треонінових кіназ, фосфатидилінозитол-3-OH кіназ, передачі сигналу міоінозиту і Ras онкогенів. Інгібітори шляху сигнальної трансдукції можна використовувати в комбінації зі сполукою за даним винаходом в композиціях і способах, описаних вище. Інгібітори зв'язаних з ангіогенезом рецепторних кіназ також можуть знайти застосування в даному винаході. Інгібітори ангіогенезу, зв'язаного з VEGFR і TIE-2, обговорювалися вище у зв'язку з інгібіторами сигнальної трансдукції (обидва являють собою рецепторні тирозинкінази). Інші інгібітори можна використовувати в комбінації зі сполукою за даним винаходом. Наприклад, анти-VEGF антитіла, які не розпізнають VEGFR (рецепторна тирозинкіназа), але зв'язуються з лігандом; малі молекули-інгібітори інтегрину (альфаv бета3), які інгібують ангіогенез; ендостатин і ангіостатин (не-РТК) також можуть виявитися корисними в комбінації зі сполукою за даним ® винаходом. Один приклад VEGFR антитіла являє собою бевацизумаб (AVASTIN ). Деякі інгібітори рецепторів чинника зростання знаходяться в стадії розробки і включають антагоністи лігандів, антитіла, інгібітори тирозинкінази, анти-смислові олігонуклеотиди та аптамери. Будь-які з цих інгібіторів рецепторів чинників зростання можна використовувати в комбінації зі сполукою за даним винаходом в будь-якій з композицій і способів/застосувань, ® описаних у даній заявці. Трастузумаб (Herceptin ) являє собою приклад інгібітора функції чинника зростання на основі анти-erbB2 антитіла. Один приклад інгібітора функції чинника TM зростання на основі анти-erbB1 антитіла являє собою цетуксимаб (ERBITUX , C225). ® Бевацизумаб (Avastin ) являє собою приклад моноклонального антитіла, направленого проти VEGFR. Приклади малих молекул-інгібіторів рецепторів епідермального чинника зростання ® ® включають, але не обмежуються цим, лапатиніб (Tykerb ) і ерлотиніб (TARCEVA ). Іматиніб ® мезилат (GLEEVEC ) являє собою приклад PDGFR інгібітора. Приклади VEGFR інгібіторів ® включають пазопаніб (Votrient ), ZD6474, AZD2171, PTK787, сунітиніб та сорафеніб. Засоби, що впливають на мікротрубочки або антимітотичні засоби являють собою фазоспецифічні засоби, активні проти мікротрубочок пухлинних клітин у фазі M або мітозу клітинного циклу. Приклади засобів, що діють на мікротрубочки, включають, але не обмежуються цим, дитерпеноїди та алкалоїди барвінку. Дитерпеноїди, які отримують з природних джерел, являють собою фазоспецифічні протиракові засоби, які впливають на G2/M фази клітинного циклу. Вважають, що дитерпеноїди стабілізують β-тубулінову субодиницю мікротрубочок, за допомогою зв'язування з цим білком. Виявилось, що розборка білка потім інгібується з зупинкою мітозу і подальшою клітинною загибеллю. Приклади дитерпеноїдів включають, але не обмежуються цим, паклітаксел і його аналог доцетаксел. Паклітаксел, 5β,20-епоксі-1,2α,4,7β,10β,13α-гекса-гідрокситакс-11-ен-9-он 4,10-діацетат 2бензоат 13-ефір з (2R, 3S)-N-бензоїл-3-фенілізосерином; являє собою природний дитерпеновий продукт, виділений з Тихоокеанського тисового дерева Taxus brevifolia, і є комерційно доступним як розчин для ін'єкцій TAXOL. Він є членом таксанового сімейства терпенів. Вперше він був виділений в 1971 році Wani et al. J. Am. Chem, Soc., 93:2325 (1971), який охарактеризував його структуру за допомогою хімічних методів і методами рентгенівської кристалографії. Один з механізмів його активності відноситься до здатності паклітакселу зв'язувати тубулін, тим самим пригнічуючи зростання ракових клітин. Schiff et al., Proc. Natl, Acad, Sci. USA, 77:1561-1565 (1980); Schiff et al., Nature, 277:665-667 (1979); Kumar, J. Biol, Chem, 256: 10435-10441 (1981). Для огляду синтезу і протипухлинної активності деяких похідних паклітакселу см.: D. G. I. Kingston et al., Studies in Organic Chemistry vol. 26, entitled "New trends in Natural Products Chemistry 1986", Attaur-Rahman, P.W. Le Quesne, Eds. (Elsevier, Amsterdam, 1986) pp 219-235. Паклітаксел був схвалений для клінічного застосування для лікування рефрактерного раку яєчників у США (Markman et al., Yale Journal of Biology і Medicine, 64:583, 1991; McGuire et al., Ann. Int. Med., 111:273,1989) і для лікування раку молочної залози (Holmes et al., J. Nat. Cancer Inst., 83:1797,1991.). Він є потенційним кандидатом для лікування новоутворень шкіри (Einzig et. al., Proc. Am. Soc. Clin. Oncol., 20:46) і карцином голови та шиї (Forastire et. al., Sem. Oncol., 20:56, 1990). Сполука також демонструє потенціал для лікування полікистозу нирок (Woo et. al., Nature, 368:750. 1994), раку легенів та малярії. Лікування пацієнтів за допомогою паклітакселу приводить до придушення кісткового мозку (безліч клітинних ліній, Ignoff, R.J. et. al, Cancer Chemotherapy Pocket Guide, 1998), пов'язаного з тривалим введенням концентрацій вище порогового значення (50нМ) (Kearns, C.M. et. al., Seminars in Oncology, 3(6) p, 16-23, 1995). Доцетаксел (2R, 3S)-N-карбоксі-3-фенілізосерин N-трет-бутиловий ефір, 13-ефір з 5β-20епоксі-1,2α,4,7β,10β,13α-гексагідрокситакс-11-ен-9-он 4-ацетат 2-бензоатом, тригідратом; є 16 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 комерційно доступним у вигляді розчину для ін'єкцій як TAXOTERE . Доцетаксел показаний для лікування раку молочної залози. Доцетаксел являє собою напівсинтетичну похідну паклітакселу, див. вище, отриману з використанням природного попередника, 10-деацетил-бакатину III, екстрагованого з голок Європейського Тисового дерева. Дозо-обмежувальною токсичністю доцетакселу, є нейтропенія. Алкалоїди барвінку являють собою фазоспецефічні протипухлинні засоби, отримані з рослини барвінку. Алкалоїди барвінку діють в M фазі (мітоз) клітинного циклу шляхом специфічного зв'язування з тубуліном. Отже, зв'язана молекула тубуліну не може полімеризуватися в мікротрубочки. Як вважають, мітоз пригнічується в метафазі з подальшою загибеллю клітин. Приклади алкалоїдів барвінку включають, але не обмежуються цим, вінбластин, вінкристин і вінорелбін. Вінбластин, вінкалейкобластинсульфат, є комерційно доступним у вигляді VELBAN як розчин для ін'єкцій. Хоча він має можливе показання як допоміжна терапія різних солідних пухлин, він перш за все показаний для лікування тестикулярного раку і різних лімфом, включаючи хворобу Ходжкіна; і лімфоцитарних і гістіоцитарних лімфом. Мієлосупресія є дозообмежувальним побічним ефектом вінбластину. Вінкристин, вінкалейкобластин, 22-оксо-, сульфат, є комерційно доступним у вигляді ONCOVIN як розчин для ін'єкцій. Вінкристин показаний для лікування гострих лейкозів і також знайшов застосування в лікуванні хвороби Ходжкіна і неходжкінських злоякісних лімфом. Алопеція та неврологічні ефекти є найбільш поширеними побічними ефектами вінкристину, та у меншій мірі виникають ефекти мієлосупресії і шлунково-кишкового мукозита. Вінорелбін, 3",4’-дидегідро-4’-деоксі-C’-норвінкалейкобластин [R-(R*,R*)-2,3дигідроксибутандіоат (1:2)(сіль)], комерційно доступний як розчин для ін'єкцій вінорелбінтартрату (NAVELBINE), являє собою напівсинтетичний алкалоїд барвінку. Вінорелбін показаний як самостійний засіб або в комбінації з іншим хімотерапевтичним засобом, як-от цисплатин, для лікування різних солідних пухлин, особливо недрібноклітинного раку легенів, поширеного раку молочної залози та гормонорезистентного раку передміхурової залози. Мієлосупресія є найбільш поширеним дозообмежувальним побічним ефектом вінорелбіну. Платинові координаційні комплекси являють собою не-фазоспецефічні протиракові засоби, які є інтерактивними з ДНК. Платинові комплекси проникають в пухлинні клітини, проходять гідратацію й утворюють внутрішньо- і міжланцюжкові поперечні зшивання з ДНК, викликаючи несприятливі біологічні дії на пухлину. Приклади платинових координаційних комплексів включають, але не обмежуються цим, цисплатин і карбоплатин. Цисплатин, цис-діаміндихлорплатину, є комерційно доступним у вигляді PLATINOL як розчин для ін'єкцій. Цисплатин перш за все показаний для лікування метастатичного тестикулярного раку і раку яєчників і пізньої стадії раку сечового міхура. Основними дозообмежувальними побічними ефектами цисплатин є нефротоксичність, яку можна контролювати гідратацією, і діурез та ототоксичність. Карбоплатин, платина, діамін [1,1-циклобутан-дикарбоксилат(2-)-O, O"], є комерційно доступним у вигляді PARAPLATIN як розчин для ін'єкцій. Карбоплатин перш за все показаний як основне й допоміжне лікування пізньої стадії карциноми яєчників. Придушення кісткового мозку є дозоообмежувальною токсичністю карбоплатину. Алкілувальні засоби є не-фазоспецифічними протираковими засобами та сильними електрофілами. Зазвичай алкілувальні засоби утворюють ковалентні зв'язки, шляхом алкілування, з ДНК через нуклеофільні групи ДНК молекули, як-от фосфатна, аміно, сульфгідрильна, гідроксильна, карбоксильна та імідазольна група. Таке алкілування порушує функцію нуклеїнової кислоти, приводячи до клітинної загибелі. Приклади алкілувальних засобів включають, але не обмежуються цим, азотисті іприти, як-от циклофосфамід, мелфалан і хлорамбуцил; алкілсульфонати, як-от бусульфан; нітрозосечовини, як-от кармустин; і триазини, такі як дакарбазин. Циклофосфамід, 2-[біс(2-хлоретил)аміно]тетрагідро-2H-1,3,2-оксазафосфорин 2-оксид моногідрат, є комерційно доступним у вигляді розчину для ін'єкцій або таблеток як CYTОКСАN . Циклофосфамід показаний як окремий засіб або в комбінації з іншими хіміотерапевтичними засобами для лікування злоякісних лімфом, множинної мієломи та лейкозів. Алопеція, нудота, блювота та лейкопенія є найбільш типовими дозообмежувальними побічними ефектами циклофосфаміду. Мелфалан, 4-[біс(2-хлоретил)аміно]-L-фенілаланін, є комерційно доступним у вигляді розчину для ін'єкцій або таблеток як ALKERAN. Мелфалан показаний для паліативного лікування множинної мієломи та неоперабельної епітеліальної карциноми яєчника. Придушення 17 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 кісткового мозку є найбільш поширеним дозообмежувальним побічним ефектом мелфалану. Хлорамбуцил, 4-[біс(2-хлоретил)аміно]бензолбутанова кислота, є комерційно доступним у вигляді LEUKERAN таблеток. Хлорамбуцил показаний для паліативного лікування хронічного лімфолейкозу та злоякісних лімфом, як-от лімфосаркома, гігантофолікулярна лімфома та хвороба Ходжкіна. Придушення кісткового мозку є найбільш поширеним дозообмежувальним побічним ефектом хлорамбуцилу. Бусульфан, 1,4-бутандіол диметансульфонат, є комерційно доступним у вигляді MYLERAN таблеток. Бусульфан показаний для паліативного лікування хронічного мієлогенного лейкозу. Придушення кісткового мозку є найбільш поширеним дозообмежувальним побічним ефектом бусульфану. Кармустин, 1,3-[біс(2-хлоретил)-1-нітрозосечовина, є комерційно доступним у вигляді окремих флаконів ліофілізованої речовини як BіCNU. Кармустин показаний для паліативного лікування як окремий засіб або в комбінації з іншими засобами для лікування пухлин головного мозку, множинної мієломи, хвороби Ходжкіна та не-ходжкінських лімфом. Сповільнена мієлосупресія є найбільш поширеним дозообмежувальним побічним ефектом кармустину. Дакарбазин, 5-(3,3-диметил-1-триазено)-імідазол-4-карбоксамід, є комерційно доступним у вигляді окремих флаконів речовини як DTIC-Dome. Дакарбазин показаний для лікування метастатичної злоякісної меланоми та в комбінації з іншими засобами для допоміжного лікування хвороби Ходжкіна. Нудота, блювота й анорексія є найбільш типовими дозообмежувальними побічними ефектами дакарбазину. Протипухлинні антибіотики являють собою не-фазоспецефічні засоби, які зв'язуються або інтеркалують з ДНК. Звичайна така дія приводить до стабільних ДНК комплексів або розриву ланцюга, що порушує звичайну функцію нуклеїнових кислот, приводячи до клітинної загибелі. Приклади протипухлинних антибіотиків включають, але не обмежуються цим, актиноміцини, якот дактиноміцин, антроцикліни, як-от даунорубіцин і доксорубіцин; і блеоміцини. Дактиноміцин, також відомий як Актиноміцин D, є комерційно доступним у формі для ін'єкцій як COSMEGEN. Дактиноміцин показаний для лікування пухлини Вільма і рабдоміосаркоми. Нудота, блювота й анорексія є найбільш типовими дозообмежувальними побічними ефектами дактиноміцину. Даунорубіцин (8S-цис-)-8-ацетил-10-[(3-аміно-2,3,6-тридезоксі-α-L-ліксо-гексопіранoзил)оксі]-7,8,9,10-тетрагідро-6,8,11-тригідроксі-1-метоксі-5,12 нафтацендіон гідрохлорид, є комерційно доступним у вигляді ліпосомної форми для ін'єкцій як DAUNOXOME або як препарат для ін'єкцій CERUBIDINE. Даунорубіцин показаний для индукції ремісії для лікування гострого не-лімфоцитарного лейкозу та пізньої стадії ВІЛ-асоційованої саркоми Капоші. Мієлосупресія є найбільш поширеним дозообмежувальним побічним ефектом даунорубіцину. Доксорубіцин (8S, 10S)-10-[(3-аміно-2,3,6-тридезоксі-α-L-ліксо-гексопіранoзил)оксі]-8гліколоіл, 7,8,9,10-тетрагідро-6,8,11-тригідроксі-1-метоксі-5,12 нафтацендіон гідрохлорид, є комерційно доступним у вигляді форми для ін'єкцій як RUBEX або ADRIAMYCIN RDF. Доксорубіцин перш за все показаний для лікування гострого лімфобластного лейкозу та гострого мієлобластного лейкозу, але він також є корисним компонентом для лікування деяких солідних пухлин і лімфом. Мієлосупресія є найбільш поширеним дозообмежувальним побічним ефектом доксорубіцину. Блеоміцин, суміш цитотоксичних глікопептидних антибіотиків, виділених з штаму Streptomyces verticillus, є комерційно доступним у вигляді BLENOXANE . Блеоміцин показаний як паліативне лікування, як окремий засіб або в комбінації з іншими засобами, сквамозноклітинної карциноми, лімфом і тестикулярних карцином. Легенева і шкірна токсичність є найбільш типовими дозообмежувальними побічними ефектами блеоміцину. Інгібітори топоізомерази II включають, але не обмежуються цим, епідофілотоксини. Епідофілотоксини являють собою фазоспецефічні протипухлинні засоби, виділені з мандрагори. Епідофілотоксини зазвичай впливають на клітини в S і G2 фазах клітинного циклу шляхом утворення трьохчасткового комплексу з топоізомеразою II і ДНК, викликаючи розриви ланцюга ДНК. Розриви ланцюга акумулюються і далі слідує клітинна загибель. Приклади епідофілотоксинів включають, але не обмежуються цим, етопозид та теніпозид. Етопозид, 4’-деметил-епідофілотоксин 9[4,6-0-(R)-етиліден-β-D-глюкoпіранозид], є комерційно доступним у вигляді розчину для ін'єкцій або капсул як VеPESID і широко відомий як VP-16. Етопозид показаний як окремий засіб або в комбінації з іншими хіміотерапевтичними засобами для лікування тестикулярного раку і недрібноклітинного раку легені. Мієлосупресія є найбільш типовим побічним ефектом етопозиду. Випадки лейкопенії зазвичай тяжчі, ніж тромбоцитопенія. Теніпозид, 4’-деметил-епідофілотоксин 9[4,6-0-(R)-теніліден-β-D-глюкoпіранозид], є 18 UA 115264 C2 5 10 15 20 25 30 35 40 45 50 55 60 комерційно доступним у вигляді розчину для ін'єкцій як VUMON і широко відомий як VM-26. Теніпозид показаний як окремий засіб або в комбінації з іншими хіміотерапевтичними засобами для лікування гострого лейкозу у дітей. Мієлосупресія є найбільш поширеним дозообмежувальним побічним ефектом теніпозиду. Теніпозид може викликати як лейкопенію, так і тромбоцитопенію. Антиметаболічні протипухлинні засоби являють собою фазоспецефічні протипухлинні засоби, які діють в S фазі (синтез ДНК) клітинного циклу шляхом інгібування синтезу ДНК або шляхом інгібування синтезу пуринових або піримідинових основ і, таким чином, обмежують синтез ДНК. Отже, S фаза далі не розвивається і далі слідує клітинна загибель. Приклади антиметаболічних протипухлинних засобів включають, але не обмежуються цим, фторурацил, метотрексат, цитарабін, меркаптопурин, тіогуанін і гемцитабін. 5-Фторурацил, 5-фтор-2,4-(1H, 3H)піримідиндіон, є комерційно доступним як фторурацил. Введення 5-фторурацилу приводить до інгібування синтезу тимідилату і також включення як в РНК, так і в ДНК. Результатом зазвичай є клітинна загибель. 5-Фторурацил показаний як окремий засіб або в комбінації з іншими хіміотерапевтичними засобами для лікування карцином молочної залози, товстої кишки, прямої кишки, шлунку та підшлункової залози. Мієлосупресія і мукозит є дозообмежувальними побічними ефектами 5-фторурацилу. Інші фторпіримідинові аналоги включають 5-фтор деоксіуридин (флоксиридин) і 5-фтордеоксіуридин монофосфат. Цитарабін, 4-аміно-1-β-D-арабінофуранозил-2 (1H)-піримідинон, є комерційно доступним як CYTOSAR-U і широко відомий як Ara-C. Вважають, що цитарабін проявляє клітинну фазоспецефічність у S-фазі шляхом інгібування подовження ланцюга ДНК шляхом кінцевого включення цитарабіну зростаючий ланцюг ДНК. Цитарабін показаний як окремий засіб або в комбінації з іншими хіміотерапевтичними засобами для лікування гострого лейкозу. Інші цитидинові аналоги включають 5-азацитидин і 2",2’-дифтордеоксицитидин (гемцитабін). Цитарабін індукує лейкопенію, тромбоцитопенію та мукозит. Меркаптопурин, 1,7-дигідро-6H-пурин-6-тіон моногідрат, є комерційно доступним як PURINETHOL. Меркаптопурин демонструє клітинну фазоспецефічність у S-фазі шляхом інгібування синтезу ДНК за допомогою ще не встановленого механізму. Меркаптопурин показаний як окремий засіб або в комбінації з іншими хіміотерапевтичними засобами для лікування гострого лейкозу. Мієлосупресія та шлунково-кишковий мукозит є очікуваними побічними ефектами меркаптопурину при високих дозах. Корисним меркаптопуриновим аналогом є азатіоприн. Тіогуанін, 2-аміно-1,7-дигідро-6H-пурин-6-тіон, є комерційно доступним як TABLOID . Тіогуанін демонструє клітинну фазоспецефічність у S-фазі шляхом інгібування синтез ДНК за допомогою ще не встановленого механізму. Тіогуанін показаний як окремий засіб або в комбінації з іншими хіміотерапевтичними засобами для лікування гострого лейкозу. Мієлосупресія, включаючи лейкопенію, тромбоцитопенію й анемію, є найбільш поширеним дозообмежувальним побічним ефектом введення тіогуаніну. Проте виникають шлунковокишкові побічні ефекти, і вони можуть бути дозообмежувальними. Інші пуринові аналоги включають пентостатин, еритрогідроксиноніладенін, флударабін фосфат і кладрибін. Гемцитабін, 2’-деоксі-2", 2’-дифторцитидин моногідрохлорид (β-ізомер), є комерційно доступним як GEMZAR. Гемцитабін демонструє клітинну фазоспецефічність у S-фазі і шляхом блокування проходження клітин через G1/S межу. Гемцитабін показаний в комбінації із цисплатином для лікування недрібноклітинного раку легені, що локально розвивається, і окремо для лікування раку підшлункової залози, що локально розвивається. Мієлосупресія, включаючи лейкопенію, тромбоцитопенію й анемію, є найбільш поширеним дозообмежувальним побічним ефектом введення гемцитабіну. Метотрексат, N-[4[[(2,4-діаміно-6-птеридиніл)метил]метиламіно]бензоїл]-L-глутамінова кислота, є комерційно доступним у вигляді метотрексат натрію. Метотрексат демонструє клітиннофазові ефекти конкретно в S-фазі шляхом інгібування синтезу, репарації та/або реплікації ДНК через інгібування редуктази дигідрофолієвої кислоти, яка необхідна для синтезу пуринових нуклеотидів і тимідилату. Метотрексат показаний як окремий засіб або в комбінації з іншими хіміотерапевтичними засобами для лікування хоріокарциноми, менінгеального лейкозу, не-ходжкінської лімфоми і карцином молочної залози, голови, шиї, яєчника та сечового міхура. Мієлосупресія (лейкопенія, тромбоцитопенія й анемія) і мукозит є очікуваним побічним ефектом введення метотрексату. Камптотецини, включаючи, камптотецин і похідні камптотецину є доступними або знаходяться на стадії розробки як інгібітори Топоізомерази I. Вважають, що цитотоксична активність камптотецинів пов'язана з їх активністю інгібування Топоізомерази I. Приклади камптотецинів включають, але не обмежуються цим іринотекан, топотекан і різні оптичні форми 19 UA 115264 C2 5 10 15 20 25 30 35 40 45 7-(4-метилпіперазинo-метилен)-10,11-етилендіоксі-20-камптотецину, описані нижче. Іринотекан HCl, (4S)-4,11-діетил-4-гідроксі-9-[(4-піперидинопіперидино) карбонілоксі]-1Hпіранo[3",4",6,7]індолізино[1,2-b]хінолін-3,14(4H, 12H)-діон гідрохлорид, є комерційно доступним у вигляді розчину для ін'єкцій CAMPTOSAR . Іринотекан являє собою похідну камптотецину, яка зв'язується, разом з його активним метаболітом SN-38, з комплексом топоізомераза I - ДНК. Вважається, що цитотоксичність виникає в результаті невідновних розривів подвійного ланцюга, що викликаються взаємодією топоізомераза I: ДНК: іринотекан або SN-38 трьохчасткового комплексу з реплікаційними ферментами. Іринотекан показаний для лікування метастатичного раку товстої кишки або прямої кишки. Дозообмежувальними побічними ефектами іринотекану HCl є мієлосупресія, включаючи нейтропенію, і шлунково-кишкові ефекти, включаючи діарею. Топотекан HCl (S)-10-[(диметиламіно)метил]-4-етил-4,9-дигідроксі-1Hпіранo[3",4",6,7]індолізино[1,2-b]хінолін-3,14-(4H, 12H)-діон моногідрохлорид, є комерційно доступним у вигляді розчину для ін'єкцій HYCAMTIN. Топотекан являє собою похідну камптотецину, яка зв'язується з комплексом топоізомераза I - ДНК і запобігає ре-лігуванню окремих розривів ланцюга, викликаних Топоізомеразою I відповідь на деформацію кручення ДНК молекули. Топотекан показаний для допоміжного лікування метастатичної карциноми яєчника і дрібноклітинного раку легені. Дозообмежувальним побічним ефектом топотекану HCl є мієлосупресія, головним чином нейтропенія. ОТРИМАННЯ СПОЛУК Загальні схеми синтезу Сполуки за даним винаходом можна отримати різними способами, включаючи добре відомі стандартні способи синтезу. Далі представлені ілюстративні загальні способи синтезу і потім отримання конкретних сполук за даним винаходом у робочих прикладах. Фахівцям у даній галузі буде зрозуміло, що якщо описаний в даній заявці замісник не сумісний з описаними в даній заявці способами синтезу, замісник може бути захищений відповідною захисною групою, яка є стабільною в умовах реакції. Захисну групу можна видалити в будь-який момент у послідовності реакцій, аби забезпечити необхідну проміжну або кінцеву сполуку. У всіх описаних далі схемах захисні групи для чутливих або реакційно-здатних груп застосовують у міру необхідності відповідно до загальних принципів хімічного синтезу. Маніпуляції із захисними групами здійснюють відповідно до стандартних методів органічного синтезу (T.W. Green and P.G.M. Wuts, (1991) Protecting Groups in Organic Synthesis, John Wiley & Sons, включений за допомогою посилання відносно захисних груп). Ці групи видаляють на відповідній стадії синтезу сполук з використанням способів, які є очевидними для фахівця в даній галузі техніки. Вибір способів, а також умов реакції і порядок їх виконання мають бути сумісні з отриманням сполук за даним винаходом. Синтез сполук загальної формули (I) і їх фармацевтично прийнятних похідних і солей можуть здійснити, як описано нижче в схемах 1-5, фахівці в даній галузі. У наступному описі групи є такими, як визначено вище для сполук формули (I), якщо не вказане інше. Вихідні речовини є комерційно доступними або отримані з комерційно доступних вихідних речовин з використанням способів, відомих фахівцям у даній галузі. Сполуки формули (I) можна отримати, як проілюстровано на схемі 1. Відповідним чином заміщена кислота A може вступати у взаємодію з первинним аміном в умовах утворення амідного зв'язку, як-от HOBt, EDC і Et3N в DMF, з утворенням арилбромідної проміжної сполуки B. Проміжну сполуку B можна піддати взаємодії з проміжним боронатним ефіром C в умовах зв'язування з паладієм, як-от з PdCl2(dppf) і Cs2CO3, з отриманням проміжної сполуки D. Видалення захисної парметоксибензильної (PMB) або бензильної (Bn) групи можна здійснити в присутності паладію на вуглеці в атмосфері Н2 з отриманням сполук формули (I). 20 UA 115264 C2 Схема 1 5 10 15 20 Проміжну сполуку D також можна отримати, як проілюстровано на схемі 2. Арилбромід B може бути перетворений у боронатний ефір у відповідних умовах, як-от з PdCl2(dppf) і KOAc в 1,4-діоксані, з отриманням проміжного боронатного ефіру E. Відповідним чином заміщений 3бромпіридин потім можна піддати взаємодії з проміжною сполукою E в умовах зв'язування з паладієм, як-от з PdCl2(dppf) і Cs2CO3, з отриманням проміжної сполуки D. В умовах, аналогічних тим, які описані на схемі 1, можна далі перетворити проміжну сполуку D у сполуки формули (I). Схема 2 Проміжну сполуку D також можна отримати, як проілюстровано на схемі 3. Арилбромід F може бути перетворений у боронатний ефір у відповідних умовах, як-от PdCl2(dppf) і KOAc в 1,4діоксані, з отриманням проміжного боронатного ефіру G. Проміжний метиловий ефір G може бути перетворений у проміжний первинний амід H у лужних умовах з використанням аміаку. Відповідним чином заміщений 3-бромпіридин потім можна піддати взаємодії з проміжною сполукою H в умовах зв'язування з паладієм, як-от з PdCl2(dppf) і Cs2CO3, з отриманням проміжної сполуки I. Проміжна сполука I далі може бути перетворена в проміжну сполуку D шляхом зв'язування з відповідним чином заміщеним арилбромідом у відповідних умовах, наприклад, з використанням Pd2(dba)3, Xantphos і Cs2CO3 в 1,4-діоксані. В умовах, аналогічних тим, які описані на схемі 1, можна далі перетворити проміжну сполуку D у сполуки формули (I). 21 UA 115264 C2 Схема 3 5 10 15 Проміжну сполуку I також можна отримати, як проілюстровано на схемі 4. Арилбромідну проміжну сполуку J можна піддати взаємодії з заміщеним піридинборонатним ефіром в умовах зв'язування з паладієм, як-от з PdCl2(dppf) і Cs2CO3, з отриманням проміжної сполуки I. Проміжна сполука I далі може бути перетворена в сполуки формули (I), як продемонстровано на Схемах 3 і 1. Схема 4 Сполуку формули (I) також можна отримати, як проілюстровано на схемі 5. Відповідним чином заміщену кислоту A можна піддати взаємодії з відповідним чином заміщеним піридин-3ілборонатним ефіром в умовах зв'язування з паладієм, як-от з PdCl2(dppf) і Cs2CO3, з отриманням проміжної сполуки K. Видалення захисної параметоксибензильної (PMB) або бензильної (Bn) групи проміжної сполуки K у присутності паладію на вуглеці в атмосфері H 2 дає в результаті проміжну сполуку L. Кислотну проміжну сполуку L потім можна піддати взаємодії з відповідним чином заміщеним первинним аміном в умовах утворення амідного зв'язку, як-от HOBt, EDC і Et3N в DMF, з отриманням сполуки формули (I). 22 UA 115264 C2 Схема 5 5 10 15 20 ЕКСПЕРИМЕНТАЛЬНА ЧАСТИНА Наступні приклади ілюструють даний винахід. Дані приклади призначені не для обмеження обсягу даного винаходу, а швидше як керівництво для фахівців у даній галузі для отримання і використання сполук, композицій і способів даного винаходу. Тоді як описані окремі варіанти здійснення даного винаходу, фахівцям у даній галузі повинно бути зрозуміло, що можливі різні зміни і модифікації без відступу від суті та обсягу даного винаходу. Якщо не вказане інше, реагенти є комерційно доступними або отримані у відповідності з процедурами, описаними в літературі. Символи й умовні позначення, використовувані в описах процесів, схем і прикладів, аналогічні тим, які використовують у сучасній науковій літературі, наприклад, у журналі американського хімічного суспільства або журналі біологічної хімії. У прикладах: Хімічні зсуви виражені в мільйонних долях (млн.д.). Константи взаємодії (J) представлені в герцах (Hz). Картини розщеплювання описують уявні мультиплетності і позначаються як с (синглет), д (дуплет), т (триплет), кв. (квартет), пд (подвійний дуплет), пт (подвійний триплет), пкв. (подвійний квартет), м (мультиплет), шир (широкий). Колонкову флеш-хроматографію здійснювали на силікагелі. Для найменування використовували програми ACDLABs 11.0 Namebatch, ACD IUPAC або ® ChemDraw . Абревіатури BH3•DMS комплекс боран-диметилсульфід Boc2O ди-трет-бутилдикарбонат CDCl3 хлороформ-d CD3OD метанол-d4 CHCl3 хлороформ Cs2CO3 карбонат цезію DCE дихлоретан DCM дихлорметан DIBAL-H діізобутилалюміній гідрид DIEA діізопропілетиламін DMF N, N-диметилформамід DMSO диметилсульфоксид EA етилацетат EDC N-(3-диметиламінопропіл)-N'-етилкарбонат ЕР-РХМС електророзпилення - рідинна хроматографія-мас-спектрометрія Et3N триетиламін ЕtOH етанол г грам(и) год. година(и) H2 газоподібний водень HATU O-(7-азабензoтриазол-1-іл)-N, N,N',N'-тетраметилуроній гексафторфосфат 23 UA 115264 C2 HCl H2O HOBt HPLC H2SO4 in vacuo K2CO3 KCN KOAc KOH LAH LCMS LiOH•H2O m-CPBA MеCN MеI MеOH мг MgSO4 хв мл ммоль N2 NaBH4 NаCN Na2CO3 NаH NaHCO3 NаOH Na2SO4 Na2S2O3 NBS n-BuLi NH4Cl NH4OH NIS НМR PBr3 Pd/C PdCl2(dppf) Pd2(dba)3 PE PMB POCl3 rt SOCl2 TBME TBS TBSCl TFA THF TLC ® T3P Xantphos хлористоводнева кислота вода гідроксибензoтриазол високоефективна рідинна хроматографія сірчана кислота під вакуумом карбонат калію ціанид калію ацетат калію гідроксид калію літійалюмінійгідрид рідинна хроматографія - мас-спектрометрія гідроксид літію гідрат мета-хлорпероксибензойна кислота ацетонітрил метилйодид метанол міліграм(и) сульфат магнію хвилина(хвилини) мілілітр(мілілітри) мілімоль(мілімолі) газоподібний азот боргідрид натрію ціанід натрію карбонат натрію гідрид натрію бікарбонат натрію гідроксид натрію сульфат натрію тіосульфат натрію N-бромсукцинімід Н-бутиллітій хлорид амонію гідроксид амонію N-йодсукцинімід ядерний магнітний резонанс трибромід фосфору паладій на вуглеці 1,1'-біс(дифенілфосфіно)фероцен]дихлорпаладій(II) трис(дибензиліденацетон)дипаладій(0) петролейний ефір пара-метоксибензил оксихлорид фосфору кімнатна температура тіонілхлорид трет-бутилметиловий ефір трет-бутилдиметилсиліл трет-бутилдиметилсилілхлорид трифтороцтова кислота тетрагідрофуран тонкошарова хроматографія пропілфосфоновий ангідрид 4,5-біс(дифенілфосфіно)-9,9-диметилксантен Отримання проміжних сполук Проміжна сполука 1: 3-Етоксі-2-((4-метоксибензил)оксі)-5-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)піридин 24 UA 115264 C2 Стадія 1: 3-Бром-5-етоксипіридин 5 10 15 20 25 30 35 Розчин 5-бромпіридин-3-олу (70 г, 402 ммоль), K2CO3 (111 г, 805 ммоль) і йодетану (69,0 г, 443 ммоль) в DMF (700 мл) перемішували протягом 16 годин при 25 °C. Потім суміш концентрували з отриманням залишку, який екстрагували за допомогою DCM (2200 мл), сушили над Na2SO4, фільтрували та концентрували, з отриманням 3-бром-5-етоксипіридину (53 1 г, 218 ммоль, 54,2 % вихід): H ЯМР (400МГц, CD3OD) δ 8,19-8,17 (м, 2H), 7,60-7,59 (м, 1H), 4,134,07 (м, 2H), 1,40 (т, J=7,0 Гц, 3H); ЕР-РХМС m/z 202 (M+H). Стадія 2: 3-Бром-5-етоксипіридин 1-оксид До розчину 3-бром-5-етоксипіридину (53 г, 262 ммоль) в DCM (200 мл) при 0 °C повільно додавали m-CPBA (67,9 г, 393 ммоль) протягом 30 хвилин. Потім отриманий розчин перемішували протягом 15 годин, суміш промивали розчином NaS 2O3 та екстрагували за допомогою DCM (2 300 мл), сушили над Na2SO4, фільтрували та органічну фазу концентрували з отриманням 1-оксиду 3-бром-5-етоксипіридину (40 г, 165 ммоль, 62,9 % вихід): 1 H ЯМР (400 МГц, CD3OD) δ 8,19-8,18 (м, 1H), 8,08-8,07 (м, 1H), 7,50-7,49 (м, 1H), 4,17-4,15 (д, J=8,8 Гц, 2H), 1,43 (т, J=7,0 Гц, 3H); ЕР-РХМС m/z 217 (M+H). Стадія 3: 5-Бром-2-хлор-3-етоксипіридин До розчину 1-оксиду 3-бром-5-етоксипіридину (40 г, 183 ммоль) в DCM (200 мл) при 0 °C повільно додавали POCl3 (159 мл, 1701 ммоль) протягом 30 хвилин. Потім отриманий розчин нагрівали до 45 °C протягом 15 годин. Суміш концентрували та екстрагували за допомогою DCM (2200 мл), сушили над Na2SO4, фільтрували та концентрували з отриманням 5-бром-21 хлор-3-етоксипіридину (30 г, 60,9 ммоль, 33,2 % вихід): H ЯМР (400 МГц, CD3OD) δ 8,00-7,99 (д, J=2,0 Гц, 1H), 7,65-7,64 (д, J=2,0 Гц, 1H), 4,17-4,12 (м, 2H), 1,44 (т, J=7,0 Гц, 2H); ЕР-РХМС m/z 235 (M+H). Стадія 4: 5-бром-3-етоксі-2-((4-метоксибензил)оксі)піридин До суміші (4-метоксифеніл)метанолу (16,71 г, 121 ммоль) в DMF (200 мл) додавали NаH (3,96 г, 165 ммоль) при 0 °C. Потім суміш перемішували протягом 30 хвилин, у вказану вище суміш додавали 5-бром-2-хлор-3-етоксипіридин (26 г, 110 ммоль); суміш перемішували протягом 12 годин при 80-90 °C. Суміш гасили за допомогою H 2O (20 мл), екстрагували за допомогою DCM (2200 мл), сушили над Na2SO4, фільтрували та концентрували з отриманням залишку, який очищали за допомогою колонкової хроматографії (10 % EA/90 % PE, колонка з силікагелім 360 г). Всі фракції, що містять продукт, як було виявлено за допомогою ТСХ (EA/PE=5:1, Rf=0,5), об'єднували та концентрували з отриманням 5-бром-3-етоксі-2-((4метоксибензил)оксі)піридину (36 г, 74,5 ммоль, 67,8 % вихід) у вигляді білої твердої речовини: 1 H ЯМР (400 МГц, CD3OD) δ 7,71 (д, J=2,0 Гц, 1H), 7,36-7,31 (м, 3H), 6,89-6,87 (м, 2H), 5,27 (с, 25 UA 115264 C2 2H), 4,05-4,00 (м, 2H) 3,77 (с, 3H), 2,37 (д, J=7,0 Гц, 3H); ЕР-РХМС m/z 338 (M+H). Стадія 5: 3-етоксі-2-((4-метоксибензил)оксі)-5-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2іл)піридин 5 10 15 До розчину 5-бром-3-етоксі-2-((4-метоксибензил)оксі)піридину (10 г, 29,6ммоль), 4,4,4',4',5,5,5',5'-октаметил-2,2'-бі(1,3,2-діоксаборолан) (8,26 г, 32,5 ммоль) і KOAc (7,25 г, 73,9 ммоль) в 1,4-діоксані (250 мл), перемішуваному в атмосфері азоту при 20 °C, додавали PdCl2(dppf) (1,082 г, 1,478 ммоль) однією порцією. Реакційну суміш перемішували при 100 °C протягом 3 годин. Суміш фільтрували і фільтрат концентрували у вакуумі з отриманням неочищеного продукту. Неочищену речовину очищали за допомогою колонкової хроматографії на силікагелі (PE/EA=10:1). Всі фракції, що містять продукт, як було виявлено за допомогою ТСХ (PE/EA=10:1, Rf=0,6), об'єднували та концентрували з отриманням 3-етоксі-2-((4метоксибензил)оксі)-5-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)піридину (9,2 г, 23,88 ммоль, 1 81,0 % вихід) у вигляді білої твердої речовини: H ЯМР (400 МГц, CDCl3) δ 8,10 (с, 1H), 7,42 (д, J=8,8 Гц, 2H), 7,33 (с, 1H), 6,88-6,85 (м, 2H), 5,45 (с, 2H), 4,11-4,06 (м, 2H), 3,78 (с, 3H), 1,43 (т, J=7,0 Гц, 3H), 1,33 (с, 12H); ЕР-РХМС m/z 386,0 (M+H). Проміжна сполука 2: 4-(2-(Бензилоксі)етоксі)-3-(трифторметил)анілін Стадія 1: 1-(2-(Бензилоксі)етоксі)-4-нітро-2-(трифторметил)бензол 20 25 30 35 40 До суміші 1-фтор-4-нітро-2-(трифторметил)бензолу (5 г, 23,91 ммоль) в DMF (50 мл) додавали K2CO3 (6,61 г, 47,8 ммоль) і 2-(бензилоксі)етанолу (4,00 г, 26,3ммоль) при кімнатній температурі. Суміш перемішували при 110 °C протягом 12 годин. РХМС і ТСХ (PE/EA=5:1, Rf=0,4) показували завершення реакції. Суміш фільтрували і фільтрат концентрували з отриманням неочищеного продукту, який очищали за допомогою колонкової хроматографії на силікагелі з отриманням 1-(2-(бензилоксі)етоксі)-4-нітро-2-(трифторметил)бензолу (7,1 г, 18,18 1 ммоль, 76,0 % вихід): H ЯМР (400 МГц, CDCl3) 8,49 (д, J=2,4 Гц, 1H), 8,38 (д, J=9,2 Гц, 1H), 7,547,28 (м, 5H), 7,13 (д, J=8,4 Гц, 1H), 4,56 (с, 2H), 4,36 (т, J=4,8 Гц, 2H), 3,89 (т, J=3,6 Гц, 2H); ЕРРХМС m/z 342(M+H). Стадія 2: 4-(2-(Бензилоксі)етоксі)-3-(трифторметил)анілін До суміші 1-(2-(бензилоксі)етоксі)-4-нітро-2-(трифторметил)бензолу (8,1 г, 23,73 ммоль) в MеOH (100 мл) додавали цинк (15,52 г, 237 ммоль) і NH 4Cl (12,70 г, 237 ммоль). Суміш перемішували при 20 °C протягом 3 годин. РХМС аналіз показав завершення реакції. Суміш фільтрували і фільтрат концентрували з отриманням неочищеного продукту, який очищали за допомогою колонкової хроматографії на силікагелі (PE/EA=5:1, R f=0,4), з отриманням 4-(21 (бензилоксі) етоксі)-3-(трифторметил)аніліну (5,1 г, 14,40 ммоль, 60,7 % вихід). H ЯМР (400МГц, CDCl3) 7,35-7,24 (м, 5H), 6,81 (т, J=8,4 Гц, 2H), 6,78 (д, J=2,8 Гц, 1H), 4,63 (с, 2H), 4,13 (т, J=4,8 Гц, 2H), 3,83 (т, J=3,6 Гц, 2H); ЕР-РХМС m/z 312(M+H). Проміжна сполука 3: 4-(3-((трет-Бутилдиметилсиліл)оксі)-2,2-диметилпропіл)-3(трифторметил)анілін 26 UA 115264 C2 Стадія 1: Етил 2, 2-диметил-3-(2-(трифторметил)феніл)пропаноат 5 10 15 20 25 30 35 40 До суміші діізопропіламіну (8,00 мл, 57,1 ммоль) в THF (300 мл), охолодженої до 0 °C, додавали n-BuLi (24,60 мл, 61,5 ммоль) по краплях.Суміш перемішували при 0 °C протягом 1 години. Потім до суміші, охолодженої до -30 °C, додавали розчин етилізобутирату (6,12 г, 52,7 ммоль) в THF (2 мл). Суміш перемішували при -30 °C протягом 1 години. До суміші додавали розчин 1-(бромметил)-2-(трифторметил)бензолу (10,5 г, 43,9 ммоль) в THF (5 мл) при -30 °C. Суміш перемішували при -30 °C протягом 3 годин і потім перемішували при 25 °C протягом 12 годин. Суміш гасили водним розчином NH4Cl та екстрагували за допомогою EA. Органічний шар промивали насиченим сольовим розчином, сушили над MgSO 4, фільтрували та концентрували. Неочищену речовину очищали за допомогою колонкової хроматографії на силікагелі (PE/EA=200:1). Всі фракції, що містять продукт, як було виявлено за допомогою ТСХ (PE/EA=10:1, Rf=0,6), об'єднували та концентрували з отриманням етил 2,2-диметил-3-(2(трифторметил)феніл)пропаноату (10 г, 35,3 ммоль, 80,0 % вихід) у вигляді твердої жовтої 1 речовини: H ЯМР (400 МГц, CDCl3) δ: 7,62 (д, J=8,0 Гц, 1H), 7,41 (т, J=7,6 Гц, 1H), 7,29 (т, J=7,6 Гц, 1H), 7,22 (д, J=8,0 Гц, 1H), 4,17 (кв, J=7,2 Гц, 2H), 3,14 (с, 3H), 1,25 (т, J=7,2 Гц, 3H), 1,18 (с, 6H); ЕР-РХМС m/z 275 (M+H). Стадія 2: Етил 2,2-диметил-3-(4-нітро-2-(трифторметил)феніл)пропаноат До розчину етил 2,2-диметил-3-(2-(трифторметил)феніл)пропаноату (10 г, 36,5 ммоль) в H2SO4 (5 мл, 94 ммоль), охолодженому до 0 °C, порціями додавали калій нітропероксокислоту (4,05 г, 40,1 ммоль). Суміш перемішували при 0 °C протягом 30 хвилин. Суміш виливали у воду з льодом та екстрагували за допомогою DCM. Органічний шар промивали насиченим сольовим розчином, сушили над Na2SO4, фільтрували та концентрували з отриманням етил 2,2-диметил3-(4-нітро-2-(трифторметил)феніл)пропаноату (8,5 г, 24,54 ммоль, 67,3 % вихід) у вигляді 1 твердої жовтої речовини: H ЯМР (400 МГц, CDCl3) δ: 8,59 (д, J=2,4 Гц, 1H), 8,47 (пд, J=2,4, 8,8 Гц, 1H), 7,82 (д, J=8,4 Гц, 1H), 5,97-5,83 (м, 2H); ЕР-РХМС m/z 320 (M+H). Стадія 3: Етил 3-(4-аміно-2-(трифторметил)феніл)-2,2-диметилпропаноат Реакційну суміш етил 2,2-диметил-3-(4-нітро-2-(трифторметил)феніл) пропаноату (8,5 г, 26,6 ммоль) і Pd/C (0,283 г, 2,66 ммоль) в MеOH (50 мл) гідрували з використанням H-куба 2 (параметри: 50 °C, 3,515 кг/см , 24 години). Суміш фільтрували та фільтрат концентрували. Неочищену речовину очищали за допомогою колонкової хроматографії на силікагелі (PE/EA=10:1). Всі фракції, що містять продукт, як було виявлено за допомогою ТСХ (PE/EA=5:1, Rf=0,4), об'єднували та концентрували з отриманням етил 3-(4-аміно-2-(трифторметил) феніл)2,2-диметилпропаноату (7 г, 22,42 ммоль, 84,0 % вихід) у вигляді не зовсім білої твердої 1 речовини: H ЯМР (400 МГц, CDCl3) δ: 6,98 (д, J=8,4 Гц, 1H), 6,91 (д, J=2,4 Гц, 1H), 6,71 (пд, J=2,4, 8,4 Гц, 1H), 4,15 (кв, J=6,8 Гц, 2H), 3,00 (с, 2H), 1,25 (т, J=7,2 Гц, 3H), 1,14 (с, 6H); ЕРРХМС m/z 290 (M+H). Стадія 4: 3-(4-Аміно-2-(трифторметил)феніл)-2,2-диметилпропан-1-ол 27 UA 115264 C2 5 10 15 20 До суміші етил 3-(4-аміно-2-(трифторметил)феніл)-2,2-диметилпропаноату (2 г, 6,91 ммоль) у THF (200 мл) порціями додавали LAH (0,525 г, 13,83 ммоль). Суміш перемішували при 25 °C протягом 10 годин. Суміш гасили 15 % водним розчином NаOH (10 мл). Суміш сушили над Na2SO4. Суміш фільтрували та фільтрат концентрували. Залишок очищали за допомогою колонкової хроматографії на силікагелі (PE/EA=8:1). Всі фракції, що містять продукт, як було виявлено за допомогою ТСХ (PE/EA=2:1, Rf=0,35), об'єднували та концентрували з отриманням 3-(4-аміно-2-(трифторметил)феніл)-2,2-диметилпропан-1-олу (1,1 г, 4,45 ммоль, 64,4 % вихід) у 1 вигляді ясно-жовтого масла: H ЯМР (400 МГц, MeOD) δ: 7,17 (д, J=8,4 Гц, 1H), 6,98 (д, J=2,4 Гц, 1H), 6,84 (пд, J=2,4, 8,0 Гц, 1H), 3,31 (с, 2H), 2,67 (д, J=1,2 Гц, 2H), 0,84 (с, 6H); ЕР-РХМС m/z 248 (M+H). Стадія 5: 4-(3-((трет-Бутилдиметилсиліл)оксі)-2,2-диметилпропіл)-3-(трифторметил)анілін До суміші 3-(4-аміно-2-(трифторметил)феніл)-2,2-диметилпропан-1-олу (300 мг, 1,213 ммоль) у DCM (150 мл) додавали імідазол (124 мг, 1,820 ммоль) і TBSCl (219 мг, 1,456 ммоль). Потім суміш перемішували при 25 °C протягом 5 годин. Суміш фільтрували та фільтрат концентрували. Неочищену речовину очищали за допомогою препаративної ТСХ (PE/EA=2:1, Rf=0,5) з отриманням 4-(3-((трет-бутилдиметилсиліл)оксі)-2,2-диметилпропіл)-31 (трифторметил)аніліну (350 мг, 0,930 ммоль, 77,0 % вихід) у вигляді твердої жовтої речовини: H ЯМР (400 МГц, CD3Cl) δ: 7,14 (д, J=8,4 Гц, 1H), 6,86 (д, J=2,8 Гц, 1H), 6,70 (пд, J=2,8, 8,4 Гц, 1H), 3,20 (с, 2H), 2,62 (д, J=1,2 Гц, 2H), 0,87 (с, 9H), 0,73 (с, 6H), 0,00 (с, 6H); ЕР-РХМС m/z 362 (M+H). Проміжна сполука 4: 2-(4-Бром-2-фторфеніл)оцтова кислота Стадія 1: 2-(4-Бром-2-фторфеніл)ацетонітрил 25 30 35 40 Суспензію NаCN (2,085 г, 42,5 ммоль) в DMF (20 мл) додавали до розчину 4-бром-1(бромметил)-2-фторбензолу (5,7 г, 21,27 ммоль) у DMF (20 мл). Суміш перемішували при 26 °C протягом 10 годин. Потім розчин концентрували та розподіляли між EA і насиченим розчином NaHCO3. Об'єднаний органічний екстракт промивали насиченим сольовим розчином, сушили над MgSO4, фільтрували та концентрували. Отриманий 2-(4-бром-2-фторфеніл)ацетонітрил (4,01 г, 18,74 ммоль, 88,0 % вихід) використовували на наступній стадії без додаткового 1 очищення. ТСХ (PE/EA=1/1, Rf 0,5): H ЯМР (400 МГц, CDCl3) δ 7,24-7,37 (м, 3H), 3,70 (с, 2H). Стадія 2: 2-(4-Бром-2-фторфеніл)оцтова кислота NаOH (56,2 мл, 112 ммоль) додавали до розчину 2-(4-бром-2-фторфеніл) ацетонітрилу (4,01 г, 18,74 ммоль) в MеOH (30 мл). Суміш перемішували при 100 °C протягом 12 годин. Суміш охолоджували до кімнатної температури. Потім розчин концентрували та розподіляли між EA і насиченим розчином NaHCO3. Об'єднаний органічний екстракт промивали насиченим сольовим розчином, сушили над MgSO4, фільтрували та концентрували. Отриману 2-(4-бром-2фторфеніл)оцтову кислоту (4,13 г, 17,72 ммоль, 95,0 % вихід) використовували на наступній 1 стадії без додаткового очищення. ТСХ (PE/EA=1/1, R f=0,4): H ЯМР (400 МГц, CDCl3) δ 7,22-7,31 (м, 2H), 7,13 (т, J=8,05 Гц, 1H), 3,67 (с, 2H); ЕР-РХМС m/z 232,9 (M+H). 28
ДивитисяДодаткова інформація
Назва патенту англійськоюPyridine derivatives as rearranged during transfection (ret) kinase inhibitors
Автори англійськоюEidam, Hilary Schenck, Demartino, Michael P., Gong, Zhen, Guan, Amy Huiping, Raha, Kaushik, Wu, Chengde, Yang, Haiying, Yu, Haiyu, Zhang, Zhiliu, Cheung, Mui
Автори російськоюЭйдем Хилари Шэнк, Дэмартино Майкл П., Гонг Цзен, Гуан Эми Гуйпинг, Раха Каушик, Ву Чэнгд, Йанг Хайинг, Ю Хайю, Цзанг Цзилю, Чунг Муи
МПК / Мітки
МПК: C07D 213/69, C07D 413/12, C07D 401/12, A61K 31/4412
Мітки: процесі, інгібітори, реаранжованої, піридинові, ret, похідні, трансфекції, кінази
Код посилання
<a href="https://ua.patents.su/120-115264-piridinovi-pokhidni-yak-ingibitori-rearanzhovano-u-procesi-transfekci-ret-kinazi.html" target="_blank" rel="follow" title="База патентів України">Піридинові похідні як інгібітори реаранжованої у процесі трансфекції (ret) кінази</a>
Попередній патент: Підвіска автомобіля
Наступний патент: Абразивний дріт для різання, спосіб його виготовлення і його застосування
Випадковий патент: Спосіб лікування рубцевих згинальних контрактур пальців кисті












