Фармацевтична композиція, що містить похідні естра-1,3,5(10)-трієну
Номер патенту: 48143
Опубліковано: 15.08.2002
Автори: ЕЛЬГЕР Вальтер, Реддерзен Гудрун, Шнайдер Біргітт, Сіманн Ханс-Йоахім, Шварц Сігфрід
Формула / Реферат
1. Фармацевтическая композиция в виде таблеток, таблеток с регулируемым высвобождением, пастилок, пилюль, капсул, таблеток с пленочным покрытием и таблеток с пленочным покрытием с регулируемым высвобождением, предназначенная для гормональной контрацепции, заместительной терапии гормона менопаузы и для лечения гинекологических и андрологических заболеваний, таких, как карциномы молочной железы и предстательной железы, содержащая в качестве активного ингредиента производные эстра-1,3,5(10)-триена, несущие в их С3-положении группу общей формулы
R-SО2-О-,
где
R обозначает группу R1R2N, в которой
R1 и R2 не зависят друг от друга и обозначают атом водорода, С1-С5 алкильный радикал или вместе с атомом азота обозначают полиметилениминогруппу, содержащую 4-6 атомов углерода, или морфолиногруппу, за исключением следующих соединений:
17-гидроксиэстра-1,3,5(10)-триен-3-ил-N, N-ди С1-С5 алкиламидосульфонат,
17-гидроксиэстра-1,3,5(10)-триен-3-ил-пирролидинсульфонат,
17-гидроксиэстра-1,3,5(10)-триен-3-ил-морфолинсульфонат,
17-оксоэстра-1,3,5(10)-триен-3-ил-N, N-диметиламидосульфонат,
17-оксоэстра-1,3,5(10)-триен-3-ил-N, N-диэтиламидосульфонат,
17-оксоэстра-1,3,5(10)-триен-3-ил-пирролидинсульфонат,
17-оксоэстра-1,3,5(10)-триен-3-ил-морфолинсульфонат,
17-гидрокси-19-нор-17-прегна-1,3,5(10)-триен-20-ин-3-ил-N, N-диметиламидосульфонат,
17-гидрокси-19-нор-17-прегна-1,3,5(10)-триен-20-ин-3-ил-N, N-диэтиламидосульфонат,
17-гидрокси-19-нор-17-прегна-1,3,5(10)-триен-20-ин-3-илпирролидинсульфонат,
17-гидрокси-19-нор-17-прегна-1,3,5(10)-триен-20-ин-3-илморфолинсульфонат.
2. Фармацевтическая композиция по п. 1, содержащая активный ингредиент общей формулы (I)
где
R обозначает группу R1R2N, в которой R1 и R2 не зависят друг от друга и обозначают атом водорода, С1-С5 алкильный радикал или вместе с атомом азота обозначают полиметилениминогруппу, содержащую 4-6 атомов углерода, или морфолиногруппу,
R3 обозначает атом водорода, гидроксильную группу или алкоксигруппу, содержащую 1-5 атомов углерода,
R4 обозначает атом водорода или C1-С5 алкильный радикал,
R5 обозначает атом водорода, гидроксильную группу, этерифицированную гидроксильную группу, галоидалкил- или алкоксигруппу, содержащую 1-5 атомов углерода,
R6 и R7 обозначают атомы водорода или вместе образуют метиленовую группу,
R8, R9 и R10 не зависят друг от друга и обозначают атом водорода или гидроксильную группу,
причем кольцо В необязательно содержит одну или две двойные связи, или необязательно
R9 обозначает алкинильный радикал, содержащий до 5 атомов углерода, или
R9 и R10 вместе обозначают атом кислорода, или
R6 и R9 обозначают виниленовую или этиленовую группу.
3. Фармацевтическая композиция по п. 1 или 2, содержащая
17-гидроксиэстра-1,3,5(10)-триен-3-илсульфамат,
17-гидроксиэстра-1,3,5(10)-триен-3-ил-N, N-диэтилсульфамат,
17-гидроксиэстра-1,3,5(10)-триен-3-ил-N, N-диметилсульфамат,
17-гидроксиэстра-1,3,5(10),7-тетраен-3-ил-N, N-диэтилсульфамат,
17-гидроксиэстра-1,3,5(10),6,8-пентаен-3-ил-N, N-диметилсульфамат,
17-оксоэстра-1,3,5(10)-триен-3-илсульфамат,
17-оксоэстра-1,3,5(10)-триен-3-ил-N, N-диметилсульфамат,
17-оксоэстра-1,3,5(10)-триен-3-ил-N, N-диэтилсульфамат,
16, 17-дигидроксиэстра-1,3,5(10)-триен-3-илсульфамат,
16, 17-дигидроксиэстра-1,3,5(10)-триен-3-ил-N, N-диметилсульфамат,
16, 17-дигидроксиэстра-1,3,5(10)-триен-3-ил-N, N-диэтилсульфамат,
2,17-дигидроксиэстра-1,3,5(10)-триен-3-ил-N, N-диметилсульфамат,
2-метокси-17-гидроксиэстра-1,3,5(10)-триен-3-ил-N, N-диэтилсульфамат,
17-гидрокси-19-нор-17-прегна-1,3,5(10)-триен-20-ин-3-илсульфамат,
17-гидрокси-19-нор-17-прегна-1,3,5(10)-триен-20-ин-3-ил-N-метилсульфамат,
17-гидрокси-19-нор-17-прегна-1,3,5(10)-триен-20-ин-3-ил-N, N-диметилсульфамат,
17-гидрокси-19-нор-17-прегна-1,3,5(10)-триен-20-ин-3-ил-N, N-диэтилсульфамат,
17-гидрокси-19-нор-17-прегна-1,3,5(10)-триен-20-ин-3-илпирролидинсульфонат,
17-гидрокси-14, 15-метиленэстра-1,3,5(10)-триен-3-ил-N, N-диметилсульфамат,
17-гидрокси-14, 15-метиленэстра-1,3,5(10)-триен-3-ил-N, N-диэтилсульфамат,
17-гидрокси-14, 15-метиленэстра-1,3,5(10)-триен-3-илпирролидинсульфонат,
17-гидрокси-14, 15-метиленэстра-1,3,5(10)-триен-3-илморфолинсульфонат,
17-гидрокси-14, 15-метиленэстра-1,3,5(10)-триен-3-ил-N-метилсульфамат,
17-гидрокси-14, 15-метиленэстра-1,3,5(10)-триен-3-илсульфамат,
17-гидрокси-14, 15-метиленэстра-1,3,5(10),7-тетраен-3-ил-N, N-диметилсульфамат,
17-гидрокси-14, 15-метиленэстра-1,3,5(10),6,8-пентаен-3-ил-N, N-диэтилсульфамат,
17-гидрокси-14, 15-метиленэстра-1,3,5(10),8-тетраен-3-ил-N, N-диметилсульфамат,
11-хлорметил-17-гидроксиэстра-1,3,5(10)-триен-3-ил-N, N-диметилсульфамат,
17-гидрокси-14, 17-виниленэстра-1,3,5(10)-триен-3-ил-N, N-диэтилсульфамат,
14, 17-этилен-17-гидроксиэстра-1,3,5(10)-триен-3-илпирролидинсульфонат,
16, 17-дигидрокси-14, 17-этиленэстра-1,3,5(10)-триен-3-ил-N, N-диэтилсульфамат,
17-гидрокси-7-метилэстра-1,3,5(10)-триен-3,11-диил-3-N, N-диметилсульфамат-11-нитрат или
17-гидрокси-11-метокси-19-нор-17-прегна-1,3,5(10)-триен-20-ин-3-ил-N, N-диметилсульфамат.
Текст
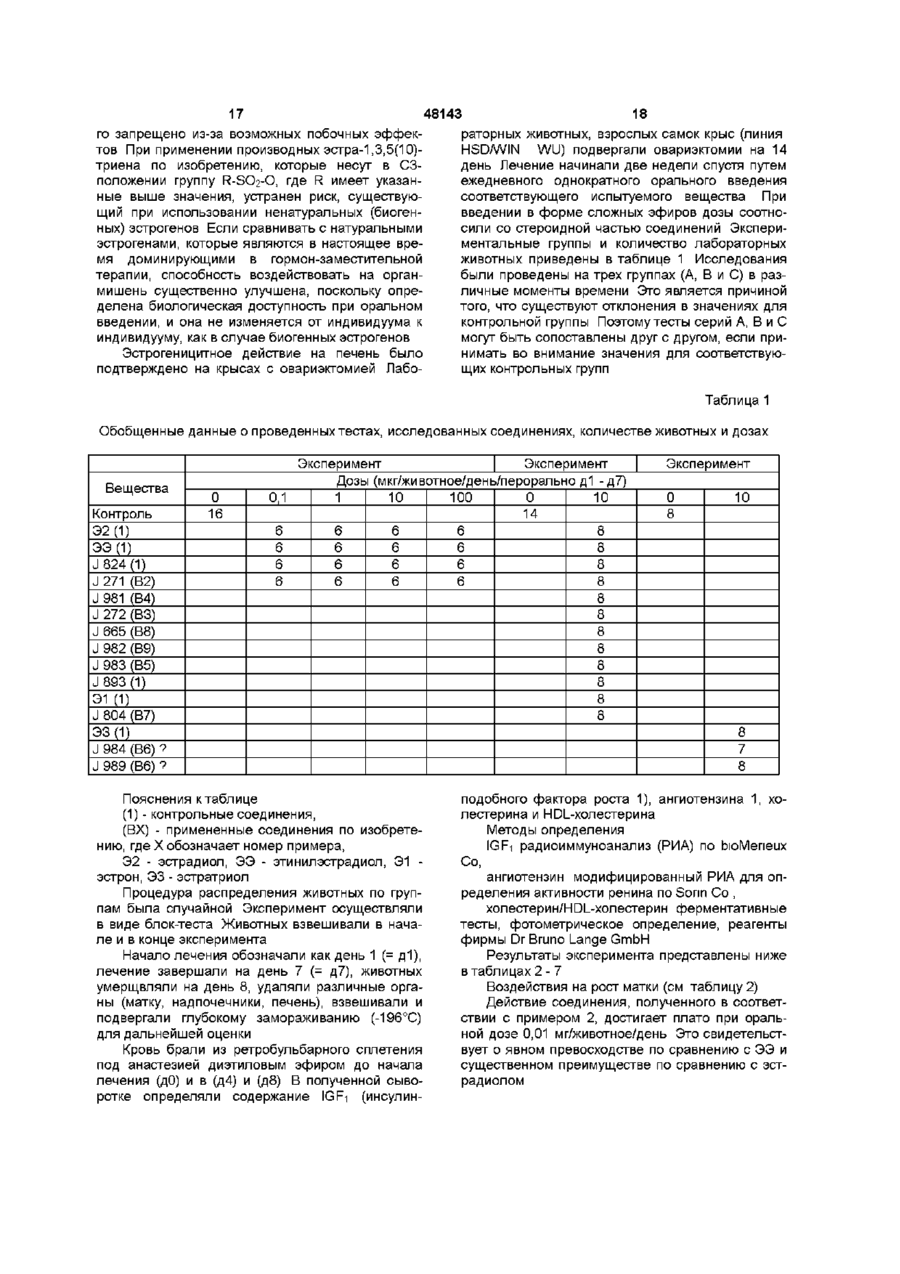
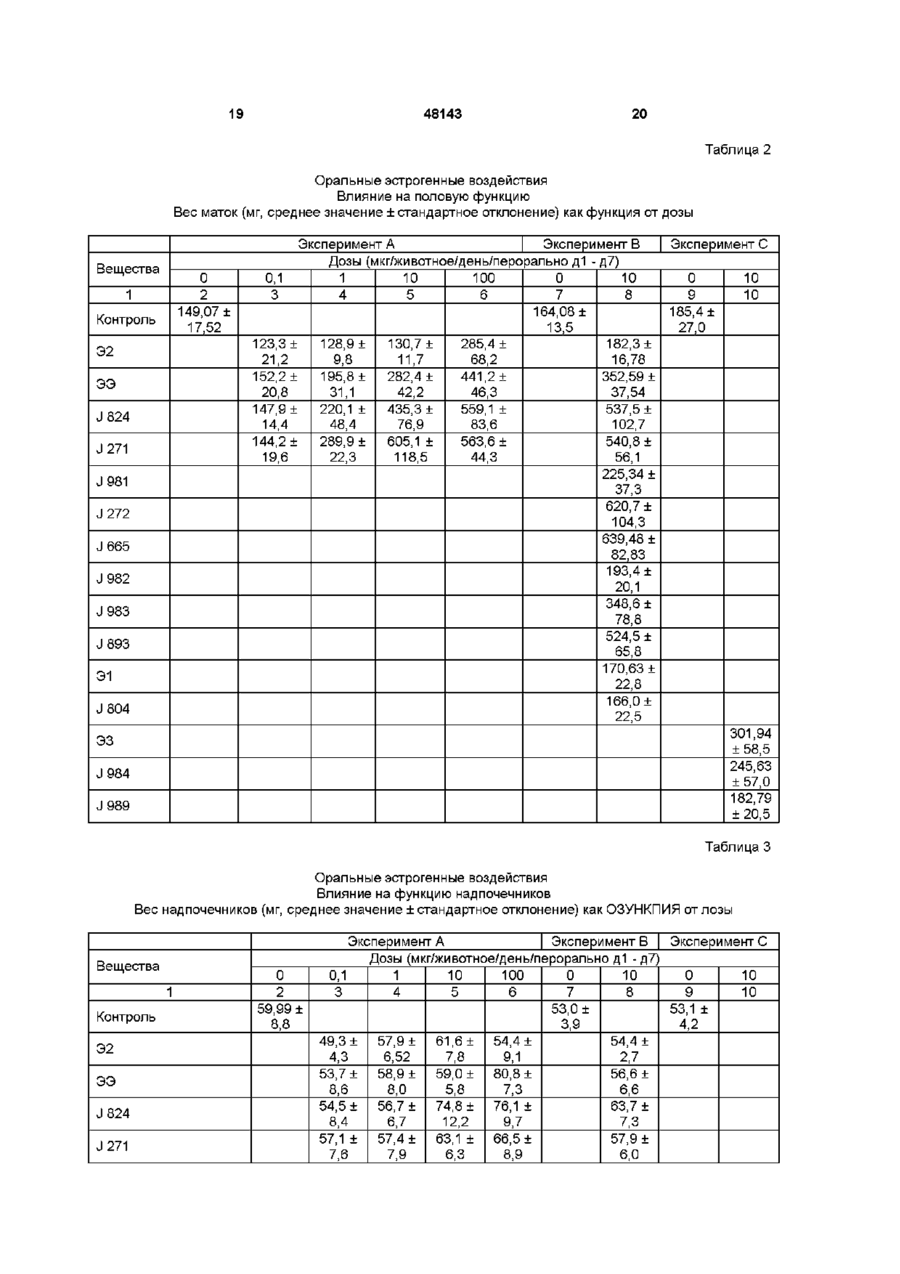
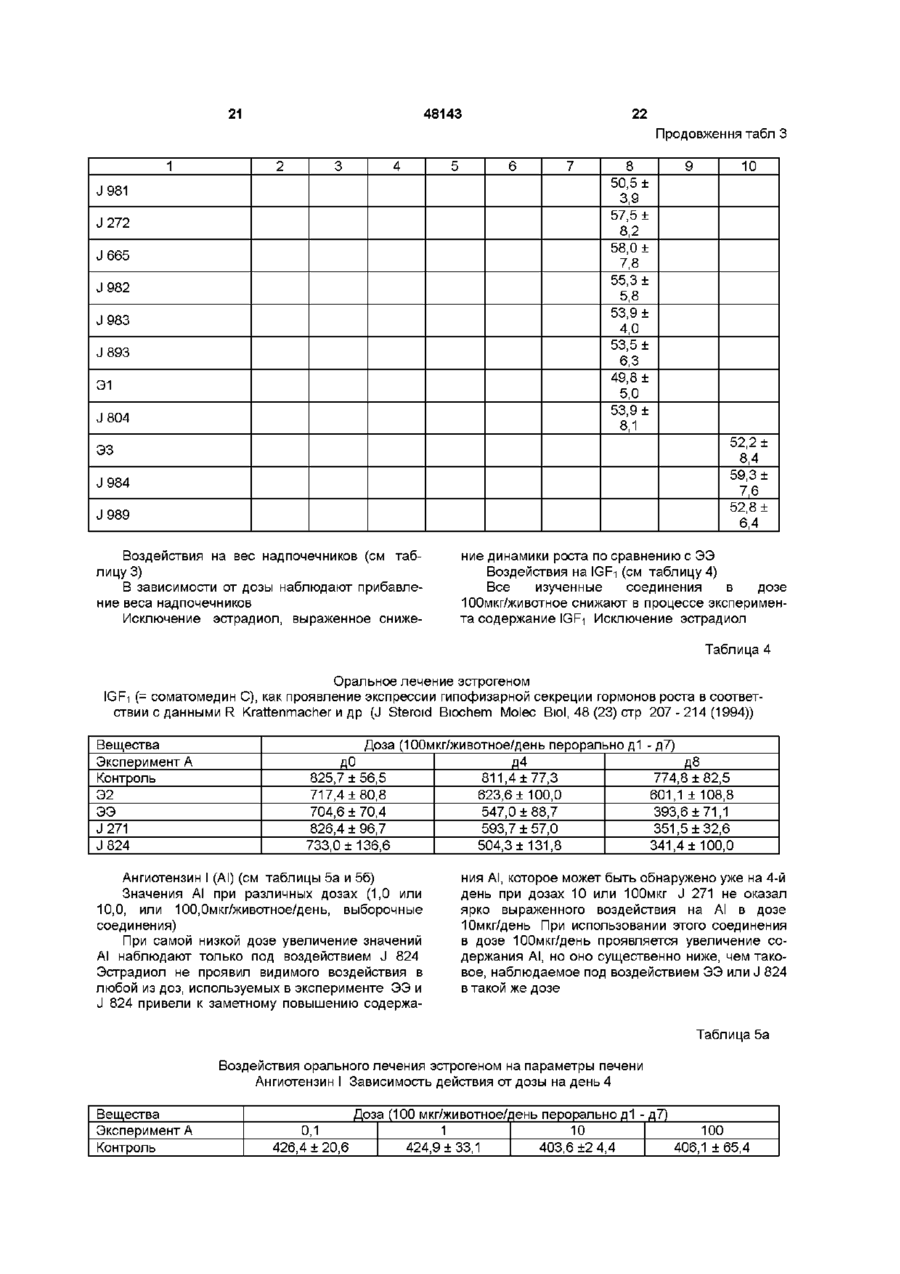
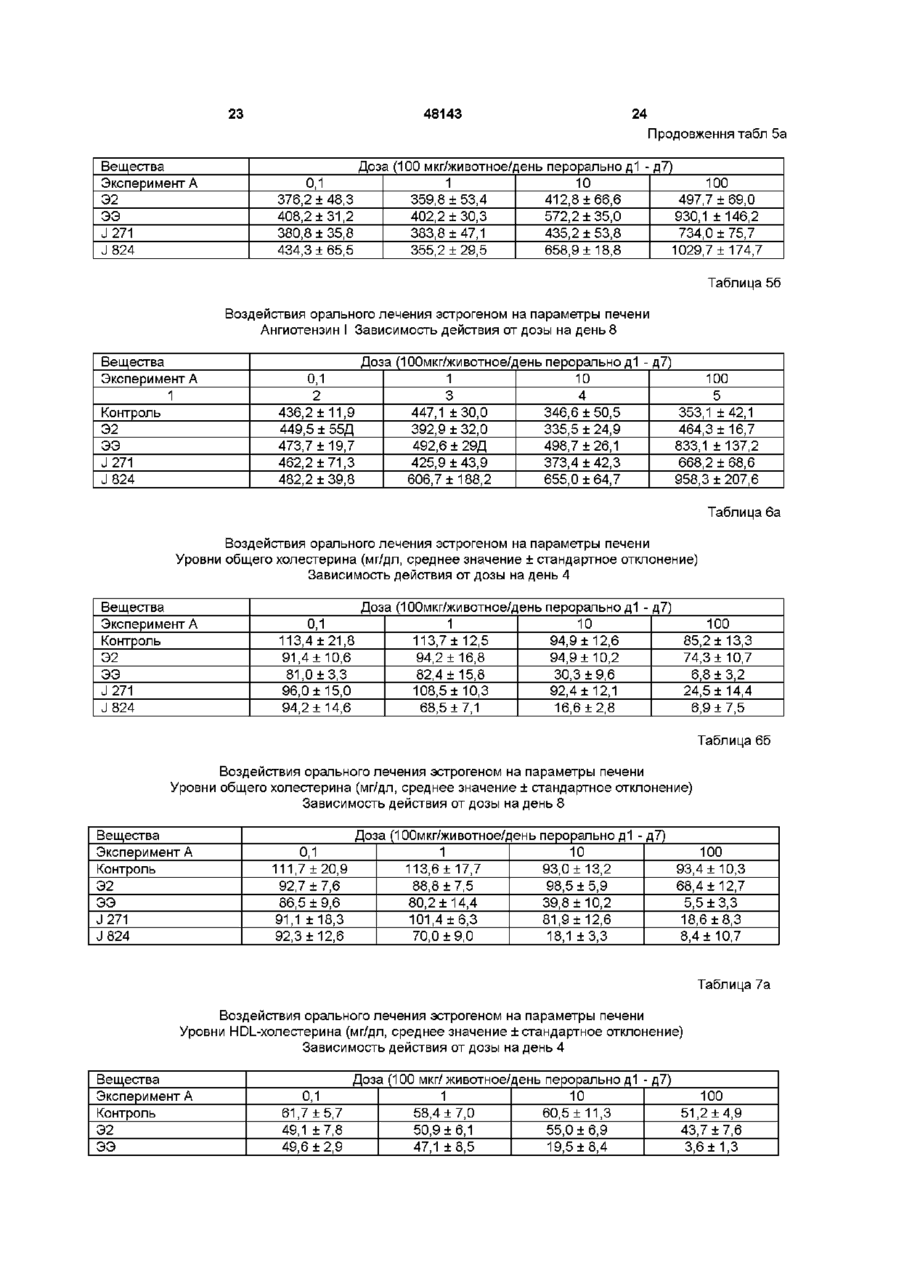
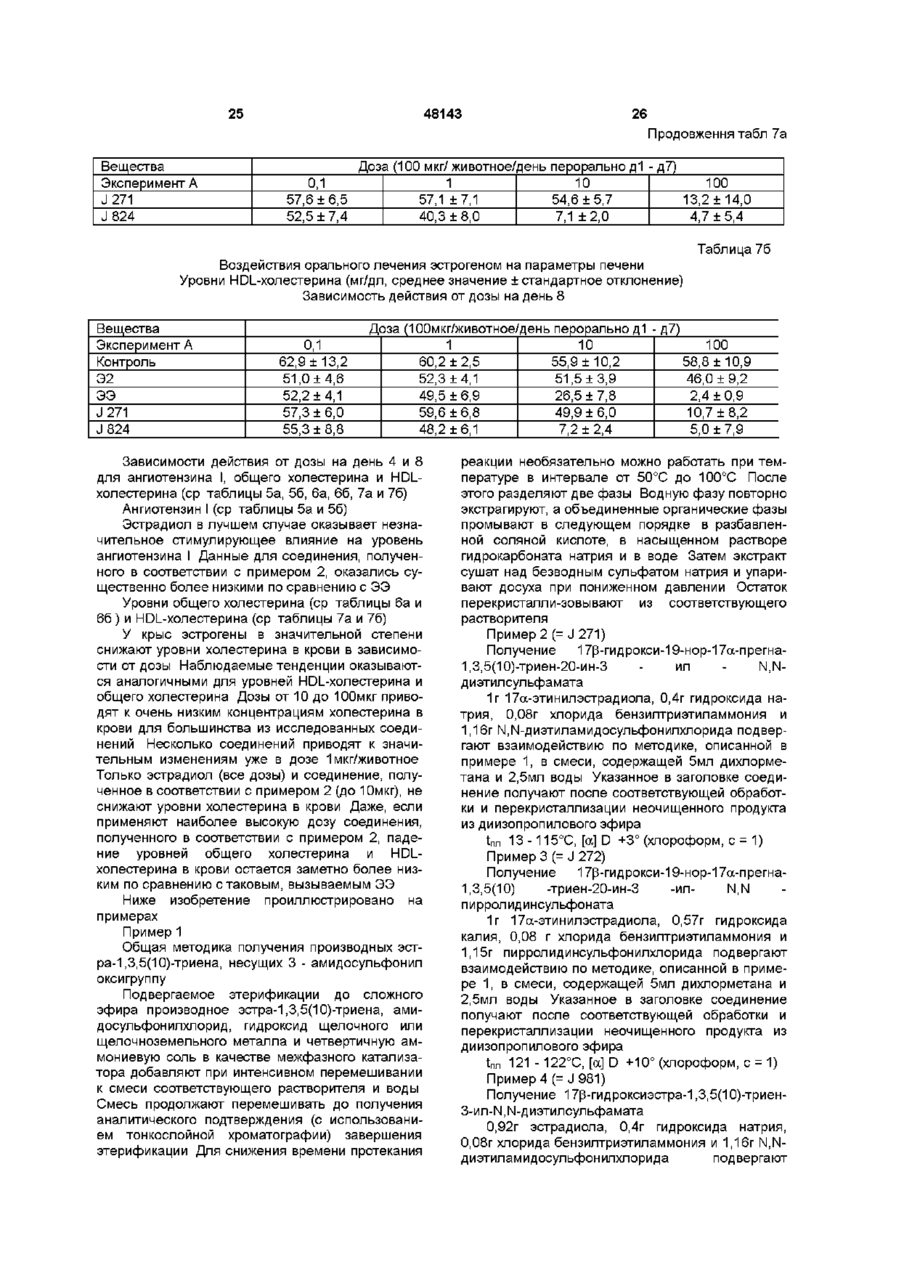
1 Фармацевтическая композиция в виде таблеток, таблеток с регулируемым высвобождением, пастилок, пилюль, капсул, таблеток с пленочным покрытием и таблеток с пленочным покрытием с регулируемым высвобождением, предназначенная для гормональной контрацепции, заместительной терапии гормона менопаузы и для лечения гинекологических и андрологических заболеваний, таких, как карциномы молочной железы и предстательной железы, содержащая в качестве активного ингредиента производные эстра-1,3,5(10)-триена, несущие в их СЗ-положении группу общей формулы R-SO2-O-, ГДЄ 1 2 R обозначает группу R R N, в которой 1 2 R и R не зависят друг от друга и обозначают атом водорода, С1-С5 алкильный радикал или вместе с атомом азота обозначают полиметилениминогруппу, содержащую 4-6 атомов углерода, или морфолиногруппу, за исключением следующих соединений 17 р -гидроксиэстра-1,3,5(10)-триен-3-ил-І\І, N-ди С1-С5 алкиламидосульфонат, 17 р -гидроксиэстра-1,3,5(10)-триен-3-илпирролидинсульфонат, 17 р -гидроксиэстра-1,3,5(10)-триен-3-илморфолинсульфонат, 17-оксоэстра-1,3,5(10)-триен-3-ил-Ы, Nдиметиламидосульфонат, 17 р -оксоэстра-1,3,5(10)-триен-3-ил-Ы, Nдиэтиламидосульфонат, 17-оксоэстра-1,3,5(10)-триен-3-илпирролидинсульфонат, 17-оксоэстра-1,3,5(10)-триен-3-илморфолинсульфонат, 17 р -гидрокси-19-нор-17 а -прегна-1,3,5(10)-триен20-ин-3-ил-І\І, N-диметиламидосульфонат, 17 р -гидрокси-19-нор-17 а -прегна-1,3,5(10)-триен20-ин-3-ил-І\І, N-диэтиламидосульфонат, 17 р -гидрокси-19-нор-17 а -прегна-1,3,5(10)-триен20-ин-З-ил пиррол ид инсульфонат, 17 р -гидрокси-19-нор-17 а -прегна-1,3,5(10)-триен20-ин-З-илморфол инсульфонат 2 Фармацевтическая композиция по п 1, содержащая активный ингредиент общей формулы (I) R q ГО где R обозначает группу R 1 R 2 N, в которой R 1 и R 2 не зависят друг от друга и обозначают атом водорода, С1-С5 алкильный радикал или вместе с атомом азота обозначают полиметилениминогруппу, содержащую 4-6 атомов углерода, или морфолиногруппу, R обозначает атом водорода, гидроксильную группу или алкоксигруппу, содержащую 1-5 атомов углерода, R4 обозначает атом водорода или С1-С5 алкильный радикал, R 5 обозначает атом водорода, гидроксильную группу, этерифицированную гидроксильную группу, галоидалкил- или алкоксигруппу, содержащую 1-5 атомов углерода, R 6 и R 7 обозначают атомы водорода или вместе образуют метиленовую группу, R8, R 9 и R 10 не зависят друг от друга и обозначают 00 48143 4 20-ин-3-ил-І\І, N-диметилсульфамат, атом водорода или гидроксильную группу, 17 р -гидрокси-19-нор-17 а -прегна-1,3,5(10)-триенпричем кольцо В необязательно содержит одну или две двойные связи, или необязательно 20-HH-3-nn-N, N-диэтилсульфамат, R9 обозначает алкинильный радикал, содержащий 17 р -гидрокси-19-нор-17 а -прегна-1,3,5(10)-триендо 5 атомов углерода, или 20-ин-З-ил пиррол ид инсульфонат, 9 10 R и R вместе обозначают атом кислорода, или 17 р -гидрокси-14а, 15а -метиленэстра-1,3,5(10)R6 и R9 обозначают виниленовую или этиленовую триен-З-ил-N, N-диметилсульфамат, группу 17 р -гидрокси-14а, 15а -метиленэстра-1,3,5(10)3 Фармацевтическая композиция по п 1 или 2, триен-З-ил-N, N-диэтилсульфамат, содержащая 17 р -гидрокси-14а, 15а -метиленэстра-1,3,5(10)17 р -гидроксиэстра-1,3,5(10)-триен-3триен-3-ил пиррол ид инсульфонат, илсульфамат, 17 р -гидрокси-14а, 15а -метиленэстра-1,3,5(10)17 р -гидроксиэстра-1,3,5(10)-триен-3-ил-Ы, Nтриен-3-илморфол инсульфонат, диэтилсульфамат, 17 р -гидрокси-14а, 15а -метиленэстра-1,3,5(10)17 р -гидроксиэстра-1,3,5(10)-триен-3-ил-Ы, Nтриен-З-ил-^метилсульфамат, диметилсульфамат, 17 р -гидрокси-14а, 15а -метиленэстра-1,3,5(10)17 р -гидроксиэстра-1,3,5(10),7-тетраен-3-ил-І\І, Nтриен-3-илсульфамат, диэтилсульфамат, 17 р -гидрокси-14а, 15а -метиленэстра17 р -гидроксиэстра-1,3,5(10),6,8-пентаен-3-ил-І\І, 1,3,5(10),7-тетраен-3-ил-^ N-диметилсульфамат, N-диметилсульфамат, 17-оксоэстра-1,3,5(10)-триен-3-илсульфамат, 17 р -гидрокси-14а, 15а -метиленэстра17-оксоэстра-1,3,5(10)-триен-3-ил-Ы, N1,3,5(10),6,8-пентаен-3-ил-^ N-диэтилсульфамат, диметилсульфамат, 17 р -гидрокси-14а, 15а -метиленэстра17-оксоэстра-1,3,5(10)-триен-3-ил-Ы, N1,3,5(10),8-тетраен-3-ил-^ N-диметилсульфамат, диэтилсульфамат, 11 р -хлорметил-17 р -гидроксиэстра-1,3,5(10)16а, 17 р -дигидроксиэстра-1,3,5(10)-триен-3триен-З-ил-N, N-диметилсульфамат, илсульфамат, 17р-гидрокси-14а , 17а -виниленэстра-1,3,5(10)1 6 а , 17 р -дигидроксиэстра-1,3,5(10)-триен-3-илтриен-З-ил-N, N-диэтилсульфамат, N, N-диметилсульфамат, 14а, 17а -этилен-17 р -гидроксиэстра-1,3,5(10)1 6 а , 17 р -дигидроксиэстра-1,3,5(10)-триен-3-илтриен-3-ил пиррол ид инсульфонат, N, N-диэтилсульфамат, 1 6 а , 17 р -дигидрокси-14а, 17а -этиленэстра2,17 р -дигидроксиэстра-1,3,5(10)-триен-3-ил-Ы, N1,3,5(10)-триен-3-ил-^ N-диэтилсульфамат, диметилсульфамат, 17 р -гидрокси-7 а -метилэстра-1,3,5(10)-триен2-метокси-17 р -гидроксиэстра-1,3,5(10)-триен-33,11 р-диил-3-N, N-диметилсульфамат-И-нитрат ил-N, N-диэтилсульфамат, или 17 р -гидрокси-19-нор-17 а -прегна-1,3,5(10)-триен17 р -гидрокси-11 р -метокси-19-нор-17 а -прегна20-ин-З-илсульфамат, 1,3,5(10)-триен-20-ин-3-ил-^ N17 р -гидрокси-19-нор-17 а -прегна-1,3,5(10)-триендиметилсульфамат 20-ин-3-ил-М-метилсульфамат, 17 р -гидрокси-19-нор-17 а -прегна-1,3,5(10)-триен Настоящее изобретение относится к фармацевтическим композициям, содержащим в качестве активных ингредиентов производные эстра1,3,5(10) -триена, несущие группу R-SO2-O в СЗположении Эстрогены играют основную роль в гормональной контрацепции, в заместительной терапии менопаузального гормона (HRT) и при лечении гинекологических (например, карциномы молочной железы) и гидрологических (например, карциномы предстательной железы) заболеваниях Для HRT и контрацепции эстрогены в основном применяют вместе с гестагеном, например, леворногестрелом, дезогестрелом, гестоденом, дроспирореноном, норэфистероном, ципротеронацетатом, хлормадинонацетатом, диеногестом При использовании для контрацепции эстрогены нужны для безопасного подавления созрева ния фолликулов и овуляции, однако, кроме того, они замещают подавленную в значительной степени эндогенную секрецию яичниками эстрадиола Это замещение важно для поддержания искусственного менструального цикла и других половых функций, что не может быть осуществлено в достаточной степени даже при использовании гестагена Более того, эндогенные эстрогены выгоняют важные функции в центральной нервной системе и в процессах метаболизма женского организма Нормальные уровни эстрогена играют значительную роль для здоровья индивидуумов (L Zichella, Clinical Management of the Menopausal Woman, Int J of Fertil and Menop Studies, 38, Suppl 1 (1993), стр 1 5 - 2 2 ) Эстрогены противодействуют развитию сердечно-сосудистых заболеваний с помощью различных механизмов, в 48143 частности создавая предпочтительные режимы липопротеинов в крови (G Samsioe, Hormone Replacement and Cardiovascular Disease, Int J of Fertil and Menop Studies, 38, Suppl 1 (1993), стр 23 29), ингибируя отложения липидов в стенке сосудов (В Clarkson, Experimental Effects of Progesterone versus Progestins on Arterial Wall, Gynecol Endocrmol, 6, Suppl 1 (1992), стр 15), оказывая благоприятное воздействие на сосудистый тонус, снижая тем самым кровяное давление (R A Lobo, Estrogen and Cardiovascular Disease, Ann New York Acad Sciences, 592 (1990), стр 286 - 294), снижая сопротивление кровотоку в важных участках сосудов и уменьшая сократительные стимулы к мышцам сосудов (С Jiang и др , Acute effect of ПВ-estradiol on rabbit coronary artery contractile responses to endothehn-1, Am J PhysioL, 263 (1992), H271 - H275) Внутренние стенки сосудов под воздействием эстрогенов высвобождают факторы (простациклин), которые противодействуют развитию тромбов в крови Эстрогены необходимы для защиты костной структуры у женщин Их недостаток может быть причиной деструкции кости (остеопороз) (С Cnstiansen, Prevention and Treatment of Osteoporosis with Hormone Replacement Therapy, Int J of Fertil and Menop Studies, 38, Suppl 1 (1993), стр 45 54) Эти последние воздействия эстрогенов на центральную нервную систему и метаболизм являются основным аспектом HRT Однако, несмотря на все положительные аспекты эстрогенной терапии, также существуют нерешенные проблемы, которые ограничивают терапевтическое использование эстрогенов или вызывают нежелательные явления Натуральные эстрогены (эстрадиол, эстрон, эстронсульфат, сложные эфиры эстрадиола, эстриол) только в очень незначительной степени становятся биологически доступными при введении оральным путем (К В Lokmd и др,, Oral bioavailability of ITB-estradiol and various ester prodrugs in the rat, Int J Pharmaceutics, 76 (1991), стр 177-182) Эта степень биологической доступности может так сильно изменяться от индивидуума к индивидууму, что не могут быть даны общие рекомендации по дозированию Эти фармакокинетические факторы привели к негативной оценке натуральных эстрогенов как средств контрацепции (W Kuhnz и др , Pharmacokmetics of Estradiol, Free and Total Estrone, in Young Women Following Single Intravenous and Oral Administration of 17 B-Estradiol, Arzneimittel-Forschung/Drug Res, 43 (II), 9, (1993), стр 966-973) Другой проблемой является быстрое удаление веществ из крови Замещение эстрогена при HRT часто следует регулировать индивидуально Поэтому разработка пролекарства эстрадиола, направленная на улучшение биологической доступности, не имела успеха (К В Lokmd и др , см выше) Синтетические эстрогены также обладают существенными недостатками Наиболее важным измененным синтетическим путем эстрогенным стероидом является этинилэстрадиол (ЭЭ) Этот эстроген является основным при контрацепции оральным путем В отличие от ЭЭ местранол применяют в небольшом количестве случаев, он представляет собой "пролекарство", которое в организме в результате метаболизма превращается в ЭЭ (J W Goldzieher, Selected aspects of the pharmacokmetics and metabolism of ethmyl estrogens and their clinical implications, Am L Obstet GynecoL, 163 (1990), стр 318 - 322) ЭЭ при введении людям оральным путем обладает существенно более хорошей биологической доступностью, чем указанные выше натуральные эстрогены, однако его биологическая доступность при оральном введении в значительной степени изменяется от индивидуума к индивидууму Goldzieher отметил негативное с фармакодинамической точки зрения значение изменения площади под кривой (AUC) зависимости времени полужизни и времени, при котором достигаются максимальные концентрации в крови Наибольшее значение AUC, обнаруженное в этом исследовании при измерении от 0 до 24 часов после введения, составляло 2121 пг х ч/мл Наименьшее значение AUC составляло 284 пг х ч/мл Аналогичное 6- или 7-кратное изменение значения AUC описано у Humpel и др (Humpel и др , Comparison of Serum Ethmyl Estradiol, Sex-Hormone-Binding Globulin, Corticoid-Bmding Globulin and Cortisol Levels in Women Using Two Low-Dose Combined Oral Contraceptives, Horm Res , 33 (1990), стр 35 - 39) После резорбции из полости кишечника введенные оральным путем активные ингредиенты проникают в организм через печень Этот факт является особенно важным для эстрогенных агентов, поскольку печень представляет собой органмишень для эстрогенов, оральное поглощение эстрогенов вызывает сильные эстрогенные воздействия на печень Секреторная активность, которая контролируется эстрогенами в печени человека, включает синтез транспортных протеинов, кортикостероидсвязывающего глобулина (CBG), глобулина, связывающего половой гормон (SHBG), тироксинсвязывающего глобулина (TBG), ангиотензиногена, нескольких факторов, важных для физиологии свертывания крови, и липопротеинов Если натуральные эстрогены вводят в женский организм, минуя прохождение через печень (например, путем трансдермального введения), указанные выше функции печени фактически остаются неизмененными (U Larsson-Cohn и др , Some biochemical consequences of postmenopausal hormone replacement treatment, в The Controversial Climacteric, ред Р A van Keep и др , MTP Press Ltd (1982)) Терапевтически эквивалентные дозы натуральных эстрогенов при введении оральным путем приводят к выраженным изменениям параметров деятельности печени увеличению SHBG, CBG, ангиотензиногена, HDL (липопротеина высокой плотности) (J С Stevenson и др , Oral Versus Transdermal Hormone Replacement Therapy, Int J of Fertil and Menop Studies, 38, Suppl 1 (1993), стр ЗО - 35) Эти воздействия эстрогена на печень являются более выраженными, если вместо натуральных эстрогенов используют композиции, содержащие эквинэстроген (так называемые конъюгированные эстрогены) (С A Mashchak и др, Comparison of pharmacodynamic properties of various estrogen 48143 formulations, Am J Obstet Gynecol , 144 (1982), стр 511 - 5 1 8 ) Этинилэстрадиол и диэтилстилбестрол (ДЭС) обладают даже более высокой эстрогеницитностью в отношении печени В отношении антигонадотрофных свойств ЭЭ оказывает приблизительно в 8 - 10 раз более сильное эстрогенное действие на печень, чем введенные оральным путем натуральные эстрогены Это является очень нежелательным различием свойств (В von Schoultz и др , Estrogen Therapy and Liver Function - Metabolic Effects of Oral and Parenteral Administration, The Prostate, 14, (1989), стр 389 - 395) Следующие данные показывают, что нежелательных гепатических реакций на эстроген нельзя избежать за счет снижения доз ЭЭ в контрацептивах Подтверждено, что уменьшение содержания ЭЭ с 30 мкг до 20мкг в каждом случае в сочетании со 150мкг одного и того же гестагена не снижает существенно увеличенный уровень ангиотензина спустя три месяца и приводит только к незначительному снижению этих показателей спустя 6 месяцев (A Basdevant и др , Hemostatic and metabolic effects of lowering the ethmyl estradiol dose from 30 meg to 20 meg in oral contraceptives containing desogestrel, Contraception, 48 (1993), стр 193 204) Известным осложнением, которое может наблюдаться после введения высоких доз эстрогена мужчинам, страдающим карциномой предстательной железы, является смертельная тромбоэмболия (В von Schoultz и др , см выше) Способность ЭЭ вызывать побочные воздействия на печень, хотя и в более слабой форме, определяет стратегию оральной гормональной контрацепции Принимая во внимание, с одной стороны, требуемые контрацептивные воздействия и поддержание менструального процесса, а с другой стороны, необходимость учитывать существенные потенциальные побочные воздействия, задача регулирования уровней ЭЭ в крови может быть сравнена с хождением по канату Вполне вероятно, что большой процент женщин не может применять оральные контрацептивы либо из-за нарушений менструальных кровотечений, либо из-за обусловленных эстрогеном побочных воздействий, превышающих порог толерантности Гормональные контрацептивы существенно увеличивают риск заболевания и смерти от определенных сердечно-сосудистых болезней (V Wynn, Oral contraceptives and coronary disease, J Reprod Med , 36 Suppl 3, (1991), стр 219 - 225) Поскольку такие риски зависят от возраста (J I Mann, Oral contraceptives and myocardial infarction in young women, Pharmacol steroid Contracept Drugs, ред-ры S Garrattim и Н W Berendes, Raven Press, New York, (1977), стр 289 - 296), некоторые авторитеты в области медицины предостерегали женщин старше 35 лет от приема гормональных контрацептивов Курящие женщины старше 35 лет и применяющие гормональные контрацептивы, подвергают себя сильному риску возникновения сердечно-сосудистых заболеваний (F A Leidenberger, Khmsche Endokrmologie fur Frauenarzte, стр 382-383, J I Mann, см выше) Риск смертельных сердечно-сосудистых заболеваний возрастает в 5 8 - 6 раз у женщин, использующих оральные контрацептивы по сравнению с контрольными группами (F A Leidenberger, см выше) Эти данные доказывают, что большие группы фертильных женщин совсем не могут применять оральные контрацептивы или могут применять их, только подвергая себя неоправданно большому риску В соответствии с уровнем данной области техники эта проблема связана с эстрогенным компонентом гормональных контрацептивов и не связана с гестагенным компонентом (Skouby и др , J Obstet Gynekol , (1990), 1535 - 1537) На "согласительном совещании" было сделано заключение, что риск смертельных инфарктов миокарда не зависит от продолжительности введения Это открытие доказывает, что образование тромбов, вызывающих смерть, происходит не в сердце вследствие дефектов стенки артерии (атеросклероз), а в печени вследствие острых воздействий на гемостатические функции (R A Lobo, см выше) Следовательно, снижение эстрогенных воздействий на печень представляет собой, как полагают, перспективный путь исключения рисков, связанных с гормональной контрацепцией, и устранения указанных ограничений по применению Описанные для ЭЭ риски в значительной степени исключены в случае натуральных эстрогенов, т е эстрогенов, имеющих более низкую печеночную эстрогеницитность по сравнению с ЭЭ (R A Lobo, см выше) HRT, основанная на использовании натуральных гормонов, требует индивидуального подбора доз с использованием современных методов Такое лечение включает целый ряд неподдающихся учету факторов, существует выраженный риск как пере-, так и недостаточной дозировки Следовательно, задачей, положенной в основу настоящего изобретения, является создание фармацевтических композиций, не оказывающих описанных выше нежелательных и побочных эффектов Эта задача решается в соответствии с изобретением путем создания фармацевтических композиций, содержащих в качестве активных ингредиентов производные эстра-1,3,5(10)-триена, несущие в их СЗ-положении группу общей формулы R - SO 2 -OГДЄ 12 R обозначает группу R R N, в которой R 1 и R 2 не зависят друг от друга и обозначают атом водорода, С 1 -С5алкильный радикал или вместе с атомом азота обозначают полиметилениминогруппу, содержащую 4 - 6 атомов углерода, или морфолиногруппу Производные эстра-1,3,5(10)-триена, входящие в состав фармацевтических композиций по изобретению и несущие в СЗ-положении R-SO2-Oгруппу, где R имеет указанные выше значения, кроме того, могут необязательно содержать двойные связи между 6 и 7 , 7 и 8 , 8 и 9 , 9 и 1 1 , 8 и 1 4 , 14 и 15 и/или 15 и 16 атомами углерода Производные эстра-1,3,5(10)-триена, входящие в состав фармацевтических композиций по изобретению и несущие в СЗ-положении R-SO2-Oгруппу, где R имеет указанные выше значения, 48143 могут необязательно нести оксогруппы у 6, 7, 11, 15, 16 и/или 17 атома углерода Производные эстра-1,3,5(10)-триена, входящие в состав фармацевтических композиций по изобретению и несущие в СЗ-положении R-SO2-Oгруппу, где R имеет указанные выше значения, могут нести дополнительные гидроксильные группы, необязательно этерифицированные в сложный или простой эфир, у 6, 7, 9, 11, 14, 16 и/или 17 атома углерода Гидроксильные группы этерифицируют, используя обычные производные физиологически приемлемых неорганических и органических кислот, например, фосфорной кислоты, серной кислоты, щавелевой кислоты, малеиновой кислоты, фумаровой кислоты, молочной кислоты, винной кислоты, яблочной кислоты, лимонной кислоты, салициловой кислоты, валериановой кислоты, адипиновой кислоты и бензойной кислоты Другие кислоты, которые могут применяться, описаны, например, в Fortschritte der Arzneimittelforschung, т 10, стр 224 - 225, Birkhauser Verlag, Basel и Stuttgart, 1966, и-в Journal of Pharmaceutical Sciences, T 66, стр 1-5(1977) Гидроксильные группы этерифицируют до простого эфира, используя обычные производные алифатических спиртов, содержащие до 6 атомов углерода Производные эстра-1,3,5(10)-триена, входящие в состав фармацевтических композиций по изобретению и несущие в СЗ-положении R-SO2-Oгруппу, где R имеет указанные выше значения, могут у 6, 7, И, 14, 15, 16 и/или 17 атома углерода необязательно нести дополнительные алкильные группы, алкилиденовые группы, алкенильные группы и алкинильные группы, содержащие до 5 атомов углерода, причем эти группы необязательно сами могут нести аналогичные группы или галоген Производные эстра-1,3,5(10)-триена, входящие в состав фармацевтических композиций по изобретению и несущие в СЗ-положении R-SO2-Oгруппу, где R имеет указанные выше значения, могут необязательно нести между 14 и 15 или 14 и 17 атомами углерода дополнительные группы алкилена или алкенилена, содержащие до 3 атомов углерода Среди производных 3-сульфаматэстра1,3,5(10)-триена, входящих в состав фармацевтических композиций по изобретению и несущих в СЗ-положении R-SO2-O-rpynny, где R имеет указанные выше значения, можно отметить, например, 17р-гилроксиэстра-1,3,5(10)-триен-3илсульфамат, 17р-гидроксиэстра-1,3,5(10)-триен-3-ил-Ы, Nдиэтилсульфамат, 17р-гидроксиэстра-1,3,5(10)-триен-3-ил-Ы, Nдиметилсульфамат, 17р-гидроксиэстра-1,3,5(10),7-тетраен-3-илN.N-диэтилсульфамат, 17р-гадроксиэстра-1,3,5(10),6,8-пентаен-3-илN.N-диметилсульфамат, 17-оксоэстра-1,3,5(10)-триен-3-илсульфамат, 17-оксоэстра-1,3,5(10)-триен-3-ил-Ы, Nдиметилсульфамат, 17-оксоэстра-1,3,5(10)-триен-3-ил-Ы, Nдиэтилсульфамат, 10 16а,17р-дигидроксиэстра-1,3,5(10)-триен-3илсульфамат, 16а,17р-дигидроксиэстра-1,3,5(10)-триен-3-илN.N-диметилсульфамат, 16а,17р-дигидроксиэстра-1,3,5(10)-триен-3-илN.N-диэтилсульфа-мат, 2,17р-дигидроксиэстра-1,3,5(10)-триен-3-илN.N-диметилсульфамат, 2-метокси-17р-гидроксиэстра-1,3,5(10)-триен3-ил-г\1,1\1-диэтилсульфамат, 17р-гидрокси-19-нор-17а-прегна-1,3,5(10) триен-20-ин-З-илсульфамат, 17р-гидрокси-19-нор-17а-прегаа-1,3,5(10)триен-20-ин-3-ил-І\І-метилсульфамат, 17р-гидрокси-19-нор-17а-прегна-1,3,5(10)триен-20-ин-3-ил-г\І,І\І-диметилсул ьфамат, 17р-гидрокси-19-нор-17а-прегаа-1,3,5(10)триен-20-ин-3-ил-г\1,1\1-диэтилсул ьфамат, 17р-гидрокси-19-нор-17а-прегаа-1,3,5(10)триен-20-ин-З-ил пиррол ид инсульфонат, 17р-гидрокси-14а, 15а-метиленэстра-1,3,5(10)триен-3-ил-г\І,І\І-диметилсул ьфамат, 17р-гадрокси-14а, 15а-метршенэстра-1,3,5(10)триен-3-ил-г\1,1\1-диэтилсул ьфамат, 17р-гадрокси-14а, 15а-метиленэстра-1,3,5(10)триен-3-ил пиррол ид инсульфонат, 17р-гидрокси-14а, 15а-метиленэстра-1,3,5(10)триен-3-илморфол инсульфонат, 17р-гидрокси-14а, 15а-метиленэстра-1,3,5(10)триен-З-ил-Ы-метилсул ьфамат, 17р-гидрокси-14а, 15а-метиленэстра-1,3,5(10)триен-3-илсул ьфамат, 17р-гидрокси-14а, 15а - метил енэстра1,3,5(10), 7-тетраен-3-ил-І\І,І\І -д и мети л сул ьфамат, 17р-гад рокси-14а, 15а-метиленэстра1,3,5(10),6,8-пентаен-3-ил-г\1,1\1 - диэтилсульфамат, 17р-гидрокси-14а, 15а-метиленэстра1,3,5(10),8-тетраен-3-ил-г\1,1\1 -д и мети л сул ьфамат, 11 р-хлорметил-17р-гидроксиэстра-1,3,5(10) триен-3-ил-г\І,І\І-диметилсул ьфамат, 17р-гидрокси-14а, 17а-виниленэстра-1,3,5(10)триен-3-ил-г\1,1\1-диэтилсул ьфамат, 14а, 17а-этилен-17р-гидроксиэстра-1,3,5(10)триен-3-ил пиррол ид инсульфонат, 16а, 17р-дигидрокси-14а, 17а -этиленэстра1,3,5(10) -триен-З-ил-N.N -диэтилсульфамат, 17р-гидрокси-7а-метилэстра-1,3,5(10)-триен3,11р-диил-3-г\1,г\1-диметилсульфамат-11 -нитрат и 17р-гидрокси-11 р-метокси-19-нор-17а-прегаа1,3,5(10)-триен-20-ин-3-ил-ІЧ Nд и мети л сул ьфамат Предпочтительные фармацевтические композиции по изобретению содержат производные эстра-1, 3,5(10)-триена общей формулы I где 12 11 48143 1 2 R обозначает группу R R N, в которой амидосульфонилхлоридом, этерифицируя тем 1 2 самым группу 3-ОН производного эстра-1,3,5(10)R и R не зависят друг от друга и обозначают триена атом водорода, СгСбалкильный радикал или вмеРеакцию осуществляют обычным способом с сте с атомом азота обозначают полиметиленимииспользованием двухфазной системы в присутстногруппу, содержащую 4 - 6 атомов углерода, или 3 вии четвертичной аммониевой соли в качестве морфолиногруппу, R обозначает атом водорода, межфазного катализатора Температуры реакций гидроксильную группу или алкоксигруппу, содернаходятся в диапазоне от комнатной температуры жащую 1 - 5 атомов углерода, 4 до 100°С Применяемые растворители представR обозначает атом водорода или d ляют собой стандартные двухфазные системы, Сбалкильный радикал, 5 такие, как хлороформ-вода, дихлорметан-вода, R обозначает атом водорода, гидроксильную толуол-вода и т д группу, этерифицированную гидроксильную групНекоторые соединения, входящие в композипу, галоидалкил- или алкоксигруппу, содержащую ции по изобретению, являются известными 1 - 5 атомов углерода, 6 7 Так, в заявке WO 93/05064 описано применеR и R обозначают атомы водорода или вмение эстрон-3-сульфаматов в качестве ингибиторов сте образуют метиленовую группу, 8 10 стероидных сульфатаз R , R и R не зависят друг от друга и обознаВ патенте ГДР DD 207447 описано применечают атом водорода или гидроксильную группу, ние N.N-диалкилсульфаматных производных этипричем кольцо В необязательно содержит одну нилэстрадиола в качестве агента для борьбы с или две двойные связи, или необязательно 9 грызунами R обозначает алкинильный радикал, содерКроме того, в выложенных заявках на патент жащий до 5 атомов углерода, или Германии DE-OS 2426779, DE-OS 2426778 и в DER9 и R10 вместе обозначают атом кислорода, OS 2426777 описаны 3-сульфаматные производили ные эстратриенов, несущие дополнительную гидR6 и R9 обозначают виниленовую или этилероксильную группу в положении 1 новую группу Кроме того, в патентах ГДР DD 77709 и в DD Особенно предпочтительными являются фар114806 описано получение активных ингредиенмацевтические композиции по изобретению, сотов, входящих в состав фармацевтических комподержащие производные эстра-1,3,5(10)-триена зиций по изобретению общей формулы 1, где R5 и R6 обозначают гидроОднако, до настоящего времени неизвестны ксильные группы фармацевтические композиции, которые содержат Кроме того, особенно предпочтительными явв качестве активных ингредиентов 3-сульфаматы ляются фармацевтические композиции по изобрепроизводных эстра-1,3,5(10)-триена и которые тению, содержащие производные эстра-1,3,5(10)могут применяться для контрацепции, HRT и летриена обшей формулы 1, и в которых R3 и R4 чения карциномы вместе обозначают метиленовую группу Другим предметом настоящего изобретения Наиболее предпочтительными являются является применение производных эстрафармацевтические композиции, содержащие 1,3,5(10)-триена, несущих в их СЗ-положении 17р-гадрокси-19-нор-17а-прегаа-1,3,5(10)группу общей формулы триен-20-ин-3-ил-г\1,г\1-диэтилсульфамат, R-SO2-O17р-гидрокси-19-нор-17а-прегна-1,3,5(10)ГДЄ триен-20-ин-З-ил пиррол ид инсульфонат, 12 17р-гидроксиэстра-1,3,5(10)-триен-3-ил-Ы, NR обозначает группу R R N, в которой диэтилсульфамат, R1 и R2 не зависят друг от друга и обозначают 17р-гидрокси-14а, 15а-метиленэстра-1,3,5(10)атом водорода, СгСбалкильный радикал или вметриен-3-ил-1\1,г\1-диэтилсульфамат, сте с атомом азота обозначают полиметиленими16а,17р-дигидроксиэстра-1,3,5(10)-триен-3-илногруппу, содержащую 4 - 6 атомов углерода, или морфолиногруппу, для получения лекарств, предN.N-диметилсульфамат, назначенных для гормональной контрацепции, эстра-1,3,5(10)-триен-17-он-3-ил-г\І,І\Ізаместительной терапии климактерического гордиэтилсульфамат, мона и лечения гинекологических и андрологиче17р-гадрокси-19-нор-17а-прегаа-1,3,5(10)ских заболеваний, таких, как карциномы молочной триен-20-ин-3-ил-г\І,І\І-диметилсульфамат, железы и предстательной железы 17р-гадрокси-14а, 15а-метиленэстра-1,3,5(10)Предпочтительными для получения лекарств, триен-3-ил-г\І,І\І-диметилсульфамат и предназначенных для гормональной контрацеп16а,17р-дигидроксиэстра-1,3,5(10)-триен-3-илции, заместительной терапии климактерического N.N-диэтилсульфамат гормона и лечения гинекологических и андрологиПроизводные эстра-1,3,5(10)-триена, входяческих заболеваний, таких, как карциномы молочщие в состав фармацевтических композиций по ной железы и предстательной железы, являются изобретению, получают с помощью хорошо изпроизводные эстра-1,3,5(10)-триена общей форвестного способа путем взаимодействия произмулы I водного эстра-1,3,5(10)-триена с соответствующим образом замещенным 48143 V ГДЄ (1} 12 R обозначает группу R R N, в которой 1 2 R и R не зависят друг от друга и обозначают атом водорода, СгСбалкильный радикал или вместе с атомом азота обозначают полиметилениминогруппу, содержащую 4 - 6 атомов углерода, или 3 морфолиногруппу, R обозначает атом водорода, гидроксильную группу или алкоксигруппу, содержащую 1 - 5 атомов углерода, R4 обозначает атом водорода или d Сбалкильный радикал, R5 обозначает атом водорода, гидроксильную группу, этерифицированную гидроксильную группу, галоидалкил- или алкоксигруппу, содержащую 1 - 5 атомов углерода, R6 и R7 обозначают атомы водорода или вместе образуют метиленовую группу, R8, R и R10 не зависят друг от друга и обозначают атом водорода или гидроксильную группу, причем кольцо В необязательно содержит одну или две двойные связи, или необязательно R9 обозначает алкинильный радикал, содержащий до 5 атомов углерода, или R9 и R10 вместе обозначают атом кислорода, или R6 и R9 обозначают виниленовую или этиленовую группу Например, соединения 17р-гидроксиэстра-1,3,5(10)-триен-3илсульфамат, 17р-гадроксиэстра-1,3,5 (10)-триен-3-ил-г\1,г\1диэтилсульфамат, 17р-гидроксиэстра-1,3,5 (10) -триен-3 -ил-N.Nдиметилсульфамат, 17р-гадроксиэстра-1,3,5(10),7-тетраен-3-илN.N-диэтилсульфамат, 17р-гидроксиэстра-1,3,5(10), 6,8-пентаен-З-илN.N-диметилсульфамат, 17-оксоэстра-1,3,5(10) - триен-3-илсульфамат, 17-оксоэстра-1,3,5 (10) -триен-З-ил-N.Nдиметилсульфамат, 17-оксоэстра-1,3,5(10)-триен-3-ил-Ы, Nдиэтилсульфамат, 16а,17р-дигидроксиэстра-1,3,5(10)-триен-3илсульфамат, 16а, 17р-дигидроксиэстра-1,3,5(10) -триен-3ил-г\І,І\І-диметилсульфамат, 16а, 17р-дигидроксиэстра-1,3,5(10)-триен-3ил-г\1,1\1-диэтилсульфамат, 2,17р-дигидроксиэстра-1,3,5(10)-триен-3-илN.N-диметилсульфамат, 2-метокси-17р-гидроксиэстра-1,3,5 (Ю)-триен3 -ил-г\1,1\1-диэтилсульфамат, 17р-гидрокси-19-нор-17а-прегна-1,3,5(10)триен-20-ин-З-илсульфамат, 17р-гадрокси-19-нор-17а-прегаа-1,3,5(10)триен-20-ин-3-ил-І\І-метилсульфамат, 14 17р-гидрокси-19-нор-17а-прегна-1,3,5(10)триен-20-ин-3-ил-г\І,І\І-диметилсульфамат, 17р-гидрокси-19-нор-17а-прегна-1,3,5(10) триен-20-ин-3-ил-1\1,г\1-диэтилсульфамат, 17р-шдрокси-19-нор-17а-прегна-1,3,5(10)триен-20-ин-З-ил пиррол ид инсульфонат, 17р-гидрокси-14а, 15а-метиленэстра-1,3,5(10)триен-3-ил-г\І,І\І-диметилсульфамат, 17р-гидрокси-14а, 15а-метиленэстра-1,3,5(10)триен-3-ил-1\1,г\1-диэтилсульфамат, 17р-гидрокси-14а, 15аметил енэстра1,3,5(10) -триен-3-илпирролидинсульфонат, 17р-гидрокси-14а, 15а-метиленэстра-1,3,5(10)триен-3-илморфол инсульфонат, 17р-гидрокси-14а, 15а-метиленэстра-1,3,5(10)триен-З-ил-Ы-метилсульфамат, 17р-гидрокси-14а, 15а-метиленэстра-1,3,5(10)триен-3-илсульфамат, 17р-гидрокси-14а, 15а-метиленэстра1,3 5(10),7-тетраен-3-ил-1\1,М -диметилсульфамат, 17р-гидрокси-14а, 15а-метиленэстра1,3,5(10),6,8-пентаен-3-ил-1\1,М - диэтилсульфамат, 17р-гидрокси-14а, 15а-метиленэстра1,3 5(10),8-тетраен-3-ил-1\1,М -диметилсульфамат, 11 р-хлорметил-17р-гидроксиэстра-1,3,5(10)триен-3-ил-г\І,І\І-диметилсульфамат, 17р-гидрокси-14а, 17а-виниленэстра-1,3,5(10)триен-3-ил-1\1,г\1-диэтилсульфамат, 14а, 17а-этилен-17р-гидроксиэстра-1,3,5(10)триен-3-ил пиррол ид инсульфонат, 16а, 17р-д игадрокси-14а, 17а-этиленэстра1,3,5(10)-триен-3-ил-г\1,г\1-диэтилсульфамат, 17р-гидрокси-7а-метилэстра-1,3,5(10)-триен3,11р-диил-3-М,М-диметилсульфамат-11-нитрат и 17р-гидрокси-11 р-метокси-19-нор-17а-прегна1,3,5(10)-триен-20-ин-3-ил-М,М-диметилсульфамат применяют для получения лекарств, предназначенных для гормональной контрацепции, заместительной терапии климактерического гормона и лечения гинекологических и андрологических заболеваний, таких, как карциномы молочной железы и предстательной железы Фармацевтические композиции по изобретению дополнительно содержат один или несколько из указанных выше гестагенов, таких, как леворногестрел, дезогестрел, гестоден, дроспироренон, норэфистерон, ципротеронацетат, хлормадинонацетат, диеногест Кроме того, фармацевтические препараты по изобретению могут быть представлены в виде многоступенчатых или сложных композиций Сложная композиция по изобретению может быть составлена, например, из первой ступени, содержащей комбинацию нескольких компонентов, т е натурального эстрогена, синтетического эстрогена, прогестина и/или производного эстра1,3,5(10)-триена, которое несет в СЗ-положении группу R-SO2-O, где R имеет указанные выше значения, и необязательно одной или нескольких дополнительных ступеней, содержащих либо фармацевтически безопасное плацебо, либо натуральный или синтетический прогестин, либо биогенный или синтетический эстроген, либо производное эстра-1,3,5(10)-триена, которое несет в СЗ-положении группу R-SO2-O, где R имеет ука 16 15 48143 занные выше значения, либо комбинацию невеществами, такими, как крахмал или желатин, скольких компонентов, т е биогенного эстрогена, замасливателями, такими, как стеарат магния или синтетического эстрогена, гестагена, производнотальк и/или материалами, с помощью которых го эстра-1,3,5(10)-триена, которое несет в СЗполучают эффект депо, такими, как карбоксилпоположении группу R-SO2-O, где R имеет указанлиметилен, карбоксиметил целлюлоза, ацетатные выше значения, либо комбинацию синтетичефталат целлюлозы или поливинилацетат Таблетских эстрогенов или производного эстра-1,3,5(10)ки могут состоять из нескольких слоев триена, которое несет в СЗ-положении группу RПастилки могут быть получены соответственSO2-O, где R имеет указанные выше значения, и но путем покрытия сердцевины, изготовленной по гестагена аналогии с производством таблетки, с использованием агентов, обычно применяемых для покрыБиогенный эстроген включает, например, интия пастилки, например, поливинил пиррол идона гредиент, представляющий собой эстрадиол, эсили шеллака, гуммиарабика, талька, диоксида трон, эстран, эстриольную группу и другие биогентитана или сахара Покрытие постилки может такные эстрогены, или по крайней мере соединение, же состоять из нескольких слоев, в которых могут от которого вскоре после проникновения отщепбыть использованы адъюванты, указанные выше в ляется один из указанных выше эстрогенных инабзаце о таблетках гредиентов Синтетический эстроген включает в соответКапсулы, содержащие активные ингредиенты, ствии с изобретением по крайней мере один инмогут быть получены, например, путем смешения гредиент, представляющий собой этинилэстрадиактивного вещества с инертным субстратом, таол, местранольную группу и другие синтетические ким, как лактоза или сорбит, и инкапсулирования эстрогены, или по крайней мере одно соединение, такой смеси в желатиновые капсулы от которого вскоре после проникновения отщепПоскольку обычные, применяемые в медициляется один из указанных выше эстрогенных инне, производные эстрогена обладают серьезными гредиентов недостатками, следовательно, существует настоятельная необходимость в соответствующих Гестаген включает в соответствии с изобретефармацевтических препаратах, которые лишены нием по крайней мере один ингредиент, предуказанных недостатков ставляющий собой леворногестрел, дезогестрел, диеногест, прогестерон, н о рэфистерон ацетат, Несмотря на тот факт, что некоторые активхлормадинонацетат, ципротеронацетат и другие ные ингредиенты, входящие в фармацевтические натуральные и/или синтетические гестагены, или композиции по изобретению, уже были известны в по крайней мере одно соединение, которое вскоре течение некоторого времени и были подробно после проникновения отщепляет один из указанизучены фармакологами, их предпочтительные ных выше гестагенных ингредиентов свойства в отношении функций печени ранее не были описаны Другим предметом настоящего изобретения являются фармацевтические композиции, которые Неожиданно было установлено, что активные могут применяться для гормональной контрацепагенты, применяемые в соответствии с изобретеции, заместительной терапии климактерического нием, действуют лучше, чем ЭЭ, сточки зрения их гормона и лечения гинекологических и гидрологиэстрогенной эффективности, проявляя при этом ческих заболеваний, таких, как карциномы молочмаксимальные эстрогенные действия в отношении ной железы и предстательной железы матки, и не оказывают более сильного эстрогенного действия на печень по сравнению с натуральЕще одним предметом настоящего изобретеным эстрогенном эстрад иолом Это сочетание ния являются фармацевтические композиции в терапевтических свойств является очевидным виде таблеток, таблеток с регулируемым высвопреимуществом активных агентов по изобретению бождением, пастилок, пилюль, капсул, таблеток с по сравнению с натуральными или синтетическипленочным покрытием и таблеток с пленочным ми эстрогенами покрытием с регулируемым высвобождением Лекарства по изобретению получают известКонтрацептивы по изобретению, содержащие ным способом, используя твердые или жидкие производные эстра-1,3,5(10)-триена, которые несубстраты или растворители и обычные адъювансут в СЗ-положении группу R-SO2-O, где R имеет ты, применяемые для приготовления фармацевуказанные выше значения, требуют разработки тических препаратов, с соответствующей дозировполностью нового подхода к определению ограникой в зависимости от предполагаемого способа чений при гормональной контрацепции, поскольку введения Предпочтительными композициями явони оказывают небольшое или не оказывают соляются такие формы, которые пригодны для всем воздействия на гемостатическую систему орального введения, например, таблетки, таблетКонтрацептивы по изобретению, содержащие ки с пленочным покрытием, пастилки, капсулы, производные эстра-1,3,5(10)-триена, которые непилюли, порошки, растворы, суспензии или форсут в СЗ-положении группу R-SO2-O, где R имеет мы в виде депо указанные выше значения, могут назначаться в таких высоких дозах вследствие очень сильно Таблетки могут быть получены, например, пусниженных по сравнению с контролем эстрогентем смешения активного вещества с известными ных воздействий на менструальный цикл, что такадъювантами, например, с инертными разбавитеже является преимуществом по сравнению с тралями, такими, как декстроза, сахар, сорбит, мандиционными производными ЭЭ нит, поливинилпирролидон, с агентами, способствующими дезинтеграции, такими, как кукурузный Применение этинилэстрадиола (ЭЭ) в гормонкрахмал или альгиновая кислота, связующими заместительной терапии в настоящее время стро 17 48143 го запрещено из-за возможных побочных эффектов При применении производных эстра-1,3,5(10)триена по изобретению, которые несут в СЗположении группу R-SO2-O, где R имеет указанные выше значения, устранен риск, существующий при использовании ненатуральных (биогенных) эстрогенов Если сравнивать с натуральными эстрогенами, которые являются в настоящее время доминирующими в гормон-заместительной терапии, способность воздействовать на органмишень существенно улучшена, поскольку определена биологическая доступность при оральном введении, и она не изменяется от индивидуума к индивидууму, как в случае биогенных эстрогенов Эстрогеницитное действие на печень было подтверждено на крысах с овариэктомией Лабо 18 раторных животных, взрослых самок крыс (линия HSD/WIN WU) подвергали овариэктомии на 14 день Лечение начинали две недели спустя путем ежедневного однократного орального введения соответствующего испытуемого вещества При введении в форме сложных эфиров дозы соотносили со стероидной частью соединений Экспериментальные группы и количество лабораторных животных приведены в таблице 1 Исследования были проведены на трех группах (А, В и С) в различные моменты времени Это является причиной того, что существуют отклонения в значениях для контрольной группы Поэтому тесты серий А, В и С могут быть сопоставлены друг с другом, если принимать во внимание значения для соответствующих контрольных групп Таблица 1 Обобщенные данные о проведенных тестах, исследованных соединениях, количестве животных и дозах Вещества Контроль Э2(1) ЭЭ(1) J 824 (1) J 271 (В2) J 981 (В4) J 272 (ВЗ) J 665 (В8) J 982 (В9) J 983 (В5) J 893 (1) Э1 (1) J 804 (В7) Э3(1) J 984 (В6) ? J 989 (В6) ? 0 16 Эксперимент Эксперимент Дозы (мкг/животное/день/перорально д1 - д7) 0,1 1 10 100 0 10 14 6 6 6 6 8 6 6 6 6 8 6 6 6 6 8 6 6 6 6 8 8 8 8 8 8 8 8 8 Пояснения к таблице (1) - контрольные соединения, (ВХ) - примененные соединения по изобретению, где X обозначает номер примера, Э2 - эстрадиол, ЭЭ - этинилэстрадиол, Э1 эстрон, ЭЗ - эстратриол Процедура распределения животных по группам была случайной Эксперимент осуществляли в виде блок-теста Животных взвешивали в начале и в конце эксперимента Начало лечения обозначали как день 1 (= д1), лечение завершали на день 7 (= д7), животных умерщвляли на день 8, удаляли различные органы (матку, надпочечники, печень), взвешивали и подвергали глубокому замораживанию (-196°С) для дальнейшей оценки Кровь брали из ретробульбарного сплетения под анастезией диэтиловым эфиром до начала лечения (дО) и в (д4) и (д8) В полученной сыворотке определяли содержание IGFi (инсулин Эксперимент 0 8 10 8 7 8 подобного фактора роста 1), ангиотензина 1, холестерина и HDL-холестерина Методы определения IGFi радиоиммуноанализ (РИА) по ЬюМепеих Со, ангиотензин модифицированный РИА для определения активности ренина по Sorin Co , хол естери H/HDL-ХОЛ естери н ферментативные тесты, фотометрическое определение, реагенты фирмы Dr Bruno Lange GmbH Результаты эксперимента представлены ниже в таблицах 2 - 7 Воздействия на рост матки (см таблицу 2) Действие соединения, полученного в соответствии с примером 2, достигает плато при оральной дозе 0,01 мг/животное/день Это свидетельствует о явном превосходстве по сравнению с ЭЭ и существенном преимуществе по сравнению с эстрадиолом 19 48143 20 Таблица 2 Оральные эстрогенные воздействия Влияние на половую функцию Вес маток (мг, среднее значение ± стандартное отклонение) как функция от дозы Вещества 0 2 149,07 ± 17,52 1 Контроль Э2 ЭЭ J824 J271 J981 J272 J665 J982 J983 J893 Э1 J804 Эксперимент А Эксперимент В Дозы (мкг/животное/день/перорально д1 - д7) 0,1 1 10 100 0 10 3 4 5 6 7 8 164,08 ± 13,5 123,3 ± 128,9 ± 130,7 ± 285,4 ± 182,3 ± 21,2 9,8 11,7 68,2 16,78 152,2 ± 195,8 ± 282,4 ± 441,2 ± 352,59 ± 20,8 31,1 42,2 46,3 37,54 147,9 ± 220,1 ± 435,3 ± 559,1 ± 537,5 ± 14,4 48,4 76,9 83,6 102,7 144,2 ± 289,9 ± 605,1 ± 563,6 ± 540,8 ± 19,6 22,3 118,5 44,3 56,1 225,34 ± 37,3 620,7 ± 104,3 639,48 ± 82,83 193,4 ± 20,1 348,6 ± 78,8 524,5 ± 65,8 170,63 ± 22,8 166,0 ± 22,5 Эксперимент С 0 9 185,4 ± 27,0 10 10 301,94 ±58,5 245,63 ±57,0 182,79 ±20,5 ЭЗ J984 J989 Таблица 3 Оральные эстрогенные воздействия Влияние на функцию надпочечников Вес надпочечников (мг, среднее значение ± стандартное отклонение) как ОЗУНКПИЯ от лозы Вещества 1 Контроль Э2 ЭЭ J824 J271 0 2 59,99 ± 8,8 Эксперимент А Эксперимент В Эксперимент С Дозы (мкг/животное/день/перорально д1 - д7) 0,1 1 10 100 0 10 0 10 3 4 5 6 7 8 9 10 53,0 ± 53,1 ± 3,9 4,2 49,3 ± 57,9 ± 61,6 ± 54,4 ± 54,4 ± 4,3 6,52 7,8 9,1 2,7 53,7 ± 58,9 ± 59,0 ± 80,8 ± 56,6 ± 8,6 8,0 5,8 7,3 6,6 54,5 ± 56,7 ± 74,8 ± 76,1 ± 63,7 ± 8,4 6,7 12,2 9,7 7,3 57,1 ± 57,4 ± 63,1 ± 66,5 ± 57,9 ± 7,6 7,9 6,3 8,9 6,0 21 22 48143 Продовження табл З 1 2 3 4 5 6 J981 J272 J665 J982 J983 J893 Э1 J804 7 8 50,5 ± 3,9 57,5 ± 8,2 58,0 ± 7,8 55,3 ± 5,8 53,9 ± 4,0 53,5 ± 6,3 49,8 ± 5,0 53,9 ± 8,1 9 10 52,2 ± 8,4 59,3 ± 7,6 52,8 ± 6,4 ЭЗ J984 J989 Воздействия на вес надпочечников (см таблицу 3) В зависимости от дозы наблюдают прибавление веса надпочечников Исключение эстрад иол, выраженное сниже ние динамики роста по сравнению с ЭЭ Воздействия на IGFi (см таблицу 4) Все изученные соединения в дозе ЮОмкг/животное снижают в процессе эксперимента содержание IGFi Исключение эстрадиол Таблица 4 Оральное лечение эстрогеном GFi (= соматомедин С), как проявление экспрессии гипофизарнои секреции гормонов роста в соответствии с данными R Krattenmacher и др (J Steroid Biochem Molec Biol, 48 (23) стр 207-214(1994)) Вещества Эксперимент А Контроль Э2 ЭЭ J271 J824 Доза (ЮОмкг/животное/день перорально д1 -Д7) до 825,7 ± 56,5 717,4 ±80,8 704,6 ± 70,4 826,4 ± 96,7 733,0 ±136,6 Ангиотензин І (АІ) (смтаблицы 5а и 56) Значения АІ при различных дозах (1,0 или 10,0, или 100,0мкг/животное/день, выборочные соединения) При самой низкой дозе увеличение значений АІ наблюдают только под воздействием J 824 Эстрадиол не проявил видимого воздействия в любой из доз, используемых в эксперименте ЭЭ и J 824 привели к заметному повышению содержа Д4 811,4 ± 7 7 , 3 623,6 ± 1 0 0 , 0 547,0 ± 88,7 593,7 ± 57,0 504,3 ± 1 3 1 , 8 Д8 774,8 ± 82,5 601,1 ± 1 0 8 , 8 393,6 ± 7 1 , 1 351,5 ± 3 2 , 6 341,4 ± 1 0 0 , 0 ния AI, которое может быть обнаружено уже на 4-й день при дозах 10 или ЮОмкг J 271 не оказал ярко выраженного воздействия на АІ в дозе Юмкг/день При использовании этого соединения в дозе ЮОмкг/день проявляется увеличение содержания AI, но оно существенно ниже, чем таковое, наблюдаемое под воздействием ЭЭ или J 824 в такой же дозе Таблица 5а Воздействия орального лечения эстрогеном на параметры печени Ангиотензин I Зависимость действия от дозы на день 4 Вещества Эксперимент А Контроль 0,1 426,4 ± 20,6 Доза (100 мкг/животное/день перорально д1 - д7) 1 10 100 424,9 ±33,1 403,6 ±2 4,4 406,1 ±65,4 23 48143 24 Продовження табл 5а Вещества Эксперимент А Э2 ЭЭ J271 J824 376 408 380 434 0,1 2 ± 48,3 2 ±31,2 8 ± 35,8 3 ± 65,5 Доза (100 мкг/животное/день перорально д1 - Д7) 1 10 100 359,8 ± 53,4 412,8 ±66,6 497 7 ± 69,0 402,2 ± 30,3 572,2 ± 35,0 930, 1 ± 1 4 6 , 2 383,8 ±47,1 435,2 ± 53,8 734 0 ± 75,7 355,2 ± 29,5 658,9 ±18,8 1029 7 ± 1 7 4 , 7 Таблица 56 Воздействия орального лечения эстрогеном на параметры печени Ангиотензин I Зависимость действия от дозы на день 8 Вещества Эксперимент А 1 Контроль Э2 ЭЭ J271 J824 0,1 2 436,2 ±11,9 449,5 ± 55Д 473,7 ±19,7 462,2 ±71,3 482,2 ± 39,8 Доза (ЮОмкг/животное/день перорально д1 - Д7) 1 10 100 3 4 5 447,1 ±30,0 346,6 ± 50,5 353,1 ± 4 2 , 1 392,9 ± 32,0 335,5 ± 24,9 464,3 ± 1 6 , 7 492,6 ± 29Д 498,7 ±26,1 833,1 ± 1 3 7 , 2 425,9 ± 43,9 373,4 ± 42,3 668,2 ± 68,6 606,7 ±188,2 655,0 ± 64,7 958,3 ± 207,6 Таблица 6а Воздействия орального лечения эстрогеном на параметры печени Уровни общего холестерина (мг/дл, среднее значение ± стандартное отклонение) Зависимость действия от дозы на день 4 Вещества Эксперимент А Контроль Э2 ЭЭ J271 J824 0,1 113,4 ± 21,8 91,4 ±10,6 81,0 ±3,3 96,0 ±15,0 94,2 ±14,6 Доза (ЮОмкг/животное/день 1 113,7 ± 12,5 94,2 ±16,8 82,4 ±15,8 108,5 ±10,3 68,5 ±7,1 перорально д1 - Д7) 10 100 94,9 ±12,6 85,2 ± 1 3 , 3 94,9 ±10,2 74,3 ± 1 0 , 7 30,3 ±9,6 6,8 ± 3 , 2 92,4 ±12,1 24,5 ± 1 4 , 4 16,6 ±2,8 6,9 ± 7 , 5 Таблица 66 Воздействия орального лечения эстрогеном на параметры печени Уровни общего холестерина (мг/дл, среднее значение ± стандартное отклонение) Зависимость действия от дозы на день 8 Вещества Эксперимент А Контроль Э2 ЭЭ J271 J824 0,1 111 7 ± 20,9 92 7 ±7,6 86 5 ±9,6 91, 1 ±18,3 92, 3±12,6 Доза (ЮОмкг/животное/день 1 113,6 ± 17,7 88,8 ±7,5 80,2 ±14,4 101,4 ±6,3 70,0 ±9,0 перорально д1 - Д7) 10 100 93,0 ±13,2 93,4 ± 1 0 , 3 98,5 ±5,9 68,4 ± 1 2 , 7 39,8 ±10,2 5,5 ± 3 , 3 81,9 ±12,6 18,6 ± 8 , 3 18,1 ±3,3 8,4 ± 1 0 , 7 Таблица 7а Воздействия орального лечения эстрогеном на параметры печени Уровни HDL-холестерина (мг/дл, среднее значение ± стандартное отклонение) Зависимость действия от дозы на день 4 Вещества Эксперимент А Контроль Э2 ЭЭ 0,1 61,7 ±5,7 49,1 ±7,8 49,6 ±2,9 Доза (100 мкг/животное/день перорально д1 - д7) 1 10 100 58,4 ±7,0 60,5 ±11,3 51,2 ±4,9 50,9 ±6,1 55,0 ±6,9 43,7 ±7,6 47,1 ±8,5 19,5 ±8,4 3,6 ±1,3 25 48143 26 Продовження табл 7а Вещества Эксперимент А J271 J824 0,1 57,6 ±6,5 52,5 ±7,4 Доза (100 мкг/животное/день перорально д1 - д7) 1 10 100 57,1 ±7,1 54,6 ±5,7 13,2 ±14,0 40,3 ±8,0 7,1 ±2,0 4,7 ±5,4 Таблица 76 Воздействия орального лечения эстрогеном на параметры печени Уровни HDL-холестерина (мг/дл, среднее значение ± стандартное отклонение) Зависимость действия от дозы на день 8 Вещества Эксперимент А Контроль Э2 ЭЭ J271 J824 0,1 62,9 ±13,2 51,0 ±4,6 52,2 ±4,1 57,3 ±6,0 55,3 ±8,8 Доза (ЮОмкг/животное/день перорально д1 Д7) 1 10 100 60,2 ±2,5 55,9 ±10,2 58,8 ± 1 0 , 9 52,3 ±4,1 51,5 ±3,9 46,0 ± 9 , 2 49,5 ±6,9 26,5 ±7,8 2,4 ± 0 , 9 59,6 ±6,8 49,9 ±6,0 10,7 ± 8 , 2 48,2 ±6,1 7,2 ±2,4 5,0 ± 7 , 9 Зависимости действия от дозы на день 4 и 8 для ангиотензина I, общего холестерина и HDLхолестерина (ср таблицы 5а, 56, 6а, 66, 7а и 76) Ангиотензин I (ср таблицы 5а и 56) Эстрадиол в лучшем случае оказывает незначительное стимулирующее влияние на уровень ангиотензина I Данные для соединения, полученного в соответствии с примером 2, оказались существенно более низкими по сравнению с ЭЭ Уровни общего холестерина (ср таблицы 6а и 66) и HDL-холестерина (ср таблицы 7а и 76) У крыс эстрогены в значительной степени снижают уровни холестерина в крови в зависимости от дозы Наблюдаемые тенденции оказываются аналогичными для уровней HDL-холестерина и общего холестерина Дозы от 10 до ЮОмкг приводят к очень низким концентрациям холестерина в крови для большинства из исследованных соединений Несколько соединений приводят к значительным изменениям уже в дозе 1мкг/животное Только эстрадиол (все дозы) и соединение, полученное в соответствии с примером 2 (до Юмкг), не снижают уровни холестерина в крови Даже, если применяют наиболее высокую дозу соединения, полученного в соответствии с примером 2, падение уровней общего холестерина и HDLхолестерина в крови остается заметно более низким по сравнению с таковым, вызываемым ЭЭ Ниже изобретение проиллюстрировано на примерах Пример 1 Общая методика получения производных эстра-1,3,5(10)-триена, несущих 3 - амидосульфонил оксигруппу Подвергаемое этерификации до сложного эфира производное эстра-1,3,5(10)-триена, амидосульфонилхлорид, гидроксид щелочного или щелочноземельного металла и четвертичную аммониевую соль в качестве межфазного катализатора добавляют при интенсивном перемешивании к смеси соответствующего растворителя и воды Смесь продолжают перемешивать до получения аналитического подтверждения (с использованием тонкослойной хроматографии) завершения этерификации Для снижения времени протекания реакции необязательно можно работать при температуре в интервале от 50°С до 100°С После этого разделяют две фазы Водную фазу повторно экстрагируют, а объединенные органические фазы промывают в следующем порядке в разбавленной соляной кислоте, в насыщенном растворе гидрокарбоната натрия и в воде Затем экстракт сушат над безводным сульфатом натрия и упаривают досуха при пониженном давлении Остаток перекристалл и-зовывают из соответствующего растворителя Пример 2 (= J 271) Получение 17р-гидрокси-19-нор-17а-прегна1,3,5(10)-триен-20-ин-3 ил N,Nдиэтилсульфамата 1г 17а-этинилэстрадиола, 0,4г гидроксида натрия, 0,08г хлорида бензилтриэтиламмония и 1,16г 1\1,г\1-диэтиламидосульфонилхлорида подвергают взаимодействию по методике, описанной в примере 1, в смеси, содержащей 5мл дихлорметана и 2,5мл воды Указанное в заголовке соединение получают после соответствующей обработки и перекристаллизации неочищенного продукта из диизопропилового эфира t m 13-115°С, [a] D +3° (хлороформ, с = 1) Пример 3 (= J 272) Получение 17р-гидрокси-19-нор-17а-прегна1,3,5(10) -триен-20-ин-З -илN,N пиррол ид инсульфоната 1г 17а-этинилэстрадиола, 0,57г гидроксида калия, 0,08 г хлорида бензилтриэтиламмония и 1,15г пиррол ид инсульфонилхлорида подвергают взаимодействию по методике, описанной в примере 1, в смеси, содержащей 5мл дихлорметана и 2,5мл воды Указанное в заголовке соединение получают после соответствующей обработки и перекристаллизации неочищенного продукта из диизопропилового эфира t m 121 - 122°С, [a] D +10° (хлороформ, с = 1) Пример 4 (= J 981) Получение 17р-гидроксиэстра-1,3,5(10)-триен3-ил-г\1,1\1-диэтилсульфамата 0,92г эстрад иола, 0,4г гидроксида натрия, 0,08г хлорида бензилтриэтиламмония и 1,16rN,Nдиэтиламидосульфонилхлорида подвергают 27 48143 взаимодействию по методике, описанной в примере 1, в смеси, содержащей 5мл дихлорметана и 2,5мл воды Указанное в заголовке соединение получают посте соответствующей обработки и перекристаллизации неочищенного продукта из метанола t m 175 - 176°С, [a] D +57° (хлороформ, с = 1) Пример 5 (= J 983) Получение 17р-гидрокси-14а, 15аметиленэстра-1,3,5(10) -триен-3-ил - N,N - диэтилсульфамата 2г 14а, 15а-метиленэстра-1,3,5(10)-триен3,17р-диола суспендируют с 30мл толуола, 4мл воды, 0,32г хлорида бензилтриэтиламмо-ния, 2,94г N,Nдиэтиламидосульфонилхлорида и 2,1мл 40%-ного водного раствора гидроксида натрия и нагревают при перемешивании в течение двух часов до внутренней температуры 80°С После того, как смеси дают охладиться до комнатной температуры, ее подвергают соответствующей обработке, как описано в примере 1 Полученный неочищенный продукт хроматографируют на силикагеле (размер частиц от 0,063 до 0,2мм) Указанное в заголовке соединение получают после элюирования с использованием хлороформ а/этил ацетата и перекристаллизации из метанола t m 68 - 73°С, [a] D +98° (хлороформ, с = 1) Пример 6 (= J 989) Получение 16а,17р-дигидроксиэстра-1,3,5(10) -триен-3-ил-г\І,І\І-диметилсульфамата При перемешивании объединяют 120мл воды, 1,58г хлорида бензилтриэтиламмония, 7,44мл N.N-диметиламидосульфонилхлорида и 4мл 40%ного водного раствора гидроксида натрия с раствором из 2г эстриола в 800мл толуола при температуре 80°С Эту смесь нагревают до 80°С В течение этого времени значение рН реакционного раствора поддерживают на уровне 10, добавляя 40%-ный водный раствор гидроксида натрия Смеси дают охладиться до комнатной температуры, когда исходные соединения полностью прореагируют, и подвергают соответствующей обработке, как описано в примере 1 Полученный остаток перекристалл изовывают из ацетона/нгексана и получают указанное в заголовке соединение t m 180-181 °С, [a] D +48° (хлороформ, с = 1) Пример 7 (= J 804) Получение эстра-1,3,5(10)-триен-17-он-З-илN.N-диэтилсульфамата 0,91г эстрона, 1,73г гидроксида бария, 0,089г хлорида циклогек-силтриэтиламмония и 1,16г N,N 28 диэтиламидосульфонилхлорида подвергают взаимодействию по методике, описанной в примере 1, в смеси, содержащей 5мл четвертичного амилового спирта и 2,5мл воды Указанное в заголовке соединение получают после соответствующей обработки и перекристаллизации неочищенного продукта из метанола t m 176 - 180°С, [a] D +109° (хлороформ, с =1) Пример 8 (= J 665) Получение 17р-гидрокси-19-нор-17а-прегна1,3,5(10)-триен-20-ин-3 - ил - N,N - диметилсульфамата 1 г 17а-этинилэстрадиола, 2,4 г гидроксида натрия, 0,24 г хлорида триэтилбензиламмония и 3,6 мл г\І,І\І-диметиламидосульфонилхлорида подвергают взаимодействию по методике, описанной в примере 1, в смеси, содержащей 30мл дихлорметана и 6,6мл воды Указанное в заголовке соединение получают после соответствующей обработки, хроматографической очистки и перекристаллизации реакционного продукта из ацетона/н-гексана t m 157 - 160°С, [a] D +4° (хлороформ, с = 1) Пример 9 (= J 982) Получение 17р-гидрокси-14а, 15аметиленэстра-1,3,5(10) -триен-3-ил - N,N диметилсульфамата 1г 14а, 15а-метиленэстра-1,3,5(10)-триен3,17р-диола, 2,4г гидроксида натрия, 0,24г хлорида триэтилбензиламмония и 3,6мл N,Nдиметиламидосульфонилхлорида подвергают взаимодействию по методике, описанной в примере 1, в смеси, содержащей 30 мл дихлорметана и 6,6мл воды Указанное в заголовке соединение получают после соответствующей обработки, хроматографической очистки и перекристаллизации реакционного продукта из ацетона t m 193 - 196°С, [a] D +108° (хлороформ, с = 1) Пример 10 (= J 984) Получение 16а,17р-дигидроксиэстра-1,3,5(10) -триен-3-ил-г\1,1\1-диэтилсульфамата 2г эстриола, 5,2г гидроксида натрия, 1,72г хлорида триэтилбензиламмония и 9,75мл N,Nдиэтиламидосульфонилхлорида подвергают взаимодействию по методике, описанной в примере 1, в смеси, содержащей 800мл толуола и 128мл воды Указанное в заголовке соединение получают после соответствующей повторной перерабтки, хроматографической очистки и перекристаллизации из ацетона t m 121 - 124°С, [a] D +44° (хлороформ, с = 1) ДП «Український інститут промислової власності» (Укрпатент) вул Сім'ї Хохлових, 15, м Київ, 04119, Україна ( 0 4 4 ) 4 5 6 - 2 0 - 90 ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)216-32-71
ДивитисяДодаткова інформація
Назва патенту англійськоюPharmaceutical composition containing estra-l,3,5(10)-triene derivatives
Автори англійськоюElger Walter, Schneider Birgitt
Назва патенту російськоюФармацевтическая композиция, содержащая производные эстра-1,3,5(10)-триена
Автори російськоюЭльгер Вальтер, Шнайдер Биргитт
МПК / Мітки
МПК: A61K 31/56, A61K 31/565, C07J 43/00, C07J 41/00, C07J 53/00, A61K 31/58
Мітки: похідні, фармацевтична, містить, композиція, естра-1,3,5(10)-трієну
Код посилання
<a href="https://ua.patents.su/14-48143-farmacevtichna-kompoziciya-shho-mistit-pokhidni-estra-13510-triehnu.html" target="_blank" rel="follow" title="База патентів України">Фармацевтична композиція, що містить похідні естра-1,3,5(10)-трієну</a>
Попередній патент: Селектор довжин хвиль випромінювання
Наступний патент: Установка, яка використовує тиснення транспорту, що рухається, для отримання енергії