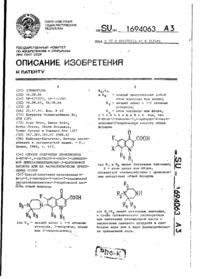
Спосіб одержання гуанідінотіазольних сполучень
Номер патенту: 5926
Опубліковано: 29.12.1994
Автори: Ясуо Ісомура, Сініті Цукамото, Масаакі Такеда, Ісао Янагісава, Норікі Іто, Йосіо Ісії, Ясуфумі Хірата
Формула / Реферат
1. Способ получения гуанидино-тиазольных соединений общей формулы 1
где R - атом водорода или низший алкил; Y - атом серы или метилен; m и n - целое число от 1 до 3;
или -СОNHR4,
R1 - атом водорода, нитрил, карбомоил, уреидная группа, гидроксил, низший алкоксил, низший ацил, ациламин, арилсульфамоил, аралкил, карбоксиметил или группа формулы - SO2R3;
R3 - низший алкил, галоидамзещенный низший алкил, незамещенный или замещенный арил, аминогруппа, моно- или ди-(низший алкил) амино-гулла или аралкиламиногруппа;
R2 - атом водорода, низший алкил, низший алкенил, низкий алкинил нитрил или низший ацил;
R4 - атом водорода, низший алкил, гидроксил или сульфамоил, отличающийся тем, что соединение общей формулы II
где R5 - низший алкил; Х - атом кислорода, группа NR1; или NR2, R, R1, R2, у, m и n имеют указанные значения, подвергают взаимодействию с амином формулы
соответственно где R1, R2, и R4 имеют указанные значения.
2. Способ по п. 1, отличающийся тем, что при использовании соединения общей формулы II, где Х означает N-R1, его подвергают взаимодействию с амином формулы R2-NН2, где R1 и R2 имеют указанные значения.
3. Способ по п. 1, отличающийся тем, что при использовании общей формулы II, где Х означает N-R2, его подвергают взаимодействию с амином формулы R1-NН2, где R1 и R2 имеют указанные значения.
4. Способ по п. 1, отличающийся тем, что при использовании соединения общей формулы II, где Х означает кислород, его подвергают взаимодействию с амином формулы R4-NН2, где R4 имеет указанные значения.
5. Способ по п. 1, отличающийся тем, что процесс ведут в среде безводного органического растворителя.
6. Способ по п. 1, отличающийся тем, что процесс ведут при комнатной температуре или при нагревании.
7. Способ по п. 1, отличающийся тем, что процесс ведут в нейтральных или основных условиях.
Приоритет по признакам:
06.03.79. при R - атом водорода, низший алкил; m и n - целое число от 1 до 3;
Y - атом серы;
где R1 - атом водорода, нитрил, карбомоил, ациламин, аралкил, карбоксиметил; R2 - атом водорода, низший алкил, низший алкенил, низший алкинил; Х - группа NR1 или NR2, где R1 и R2 имеют указанные значения.
23.06.79 при А - группа
R1 - гидроксил, низший алкоксил;
R1 - нитрил;
02.08.79. при А - группа
R1 - арилсульфамоил, группа -SO2R3; где R1 - низший алкил, галоидзамещенный низший алкил, незамещенный или замещенный арил, аминогруппа, моно- или ди-(низший алкил) аминогруппа, ариламиногруппа или аралкил-аминогруппа.
05.03.80 при А - группа СONНR4;
где R4 - атом водорода, низший алкил, гидроксил или сульфамоил;
R1 - уреидная группа;
Х - атом кислорода.
Текст
Союз Советских Социалистических Республик Р Т^ ПГ Г * ї ї ~ К ПАТЕНТУ (61) Дополнительный к патенту (22) Заявлено O5JD3.8O (23) Приоритет 25745/79 (31) 79508/79 98906/79 Опубликовано 23.10.8ЗчБюллетень № 39 Государственный комитет СССР по делам изобретений и открытий Кл. 3 (21) 2891152/23-04 06.03.79 (32) 2 3 . 0 6 . 7 9 ' 02.08.79 (33) Япония Дата опубликования описания 23.10,81 С 07 D 277/38 // А 61 К 31/425 (53)УДК 547.789. 1.07(083.8) Иностранцы Ясуфуми Хирата, Исао Янагисава, Есио Исии. Синити Цукамото, Норикн Ито, Ясуо Исомура и Масааки Такеда (Япония) (72) Авторы изобретения Иностранная фирма "Яманоути Фармасыотикал Ко, ЛТД" (Япония) (7!) Заявитель (54) СПОСОБ ПОЛУЧЕНИЯ ГУАНИДИНОТИАЗОЛЬНЫХ СОЕДИНЕНИЙ 1 Изобретение относится к способу получения новых производных гуанидинотназальных соединений общей формулы (О с= 5 где R - атом водорода или низший алкил; Y - атом серы или метилен; т и п - целое число от 1 до 3; А - группа формулы _ / ^ N—й* _ нил, нитрил или низший ацил; Кд.- атом водорода, низший алкил, грідроксил или сульфамоил, которые обладают антигистаминной а к ц тивностью и могут найти применение в медицине. Известен способ получения производных гуанидина форг^улы заключающийся в том, что соединение формулы ц г ИЛИ' т • атом водорода, нитрил, карба- \$ моил, уреидная группа, гидроксил, низший алкоксил, низший ацил, ацилами н, арил сул ьфамоил, аралкил, карбоксиметил или группа формулы - ^ 20 подвергают взаимодействию с соеди нением формулы в среде ацетонитрила в течение 24 ч низший алкил, галоидзамещенпри температуре кипения реакционной ный низший алкил, незамещенсеми [1] . ный или замещенный арил,аминогруппа, моно- или д и - ( н и з - 25 Цель изобретения - способ полуший алкил) аминогруппа, арилчения новых производных гуанидинотиааминогруппа или аралкиламиноэ о л а , расширяющих арсенал средств группа); воздействия на живой организм. атом водорода, низший алкил, Поставленная цель д о с т и г а е т с я низший алкенил, низший алки- 30 спосд^сщ^олучения соединений общей 876056 формулы 1 основанном на известной реакции взаимодействия сложных эфиров с аминами с образованием амид о в , который заключается в том, что соединение общей ФОРМУЛЫ ft-ММ. где Rg - низший алкил; X - атом кислорода, группа N-R 4 или N-R^; подвергают взаимодействию с амином формулы R^-NH^; R^-МН^или R^-NH^. При этом способ осуществляют в среде безводного органического р а с т ворителя. Кроме т о г о , процесс ведут при комнатной температуре или при н а г р е в а нии, в нейтральных или основных условиях. Соединения общей формулы 1 я в л я ются ингибиторами секреции желудочной ки слоты, индуцируемой гистамином, доказательством чего могут служить следующие медико-биологические тесты. 1. Секреция желудочной кислоты у анестезированных собак. Нечистокровных собак (дворняжек), весящих 8-15 кг, не кормят в т е ч е ние 24 ч и анестезируют внутривенным введением 30 мг/кг пентобарбитала. После лигатуры пилоруса и пищевода через вентральную стенку желудка анестезированным собакам вводят канюлю из нержавеющей с т а л и . Желудочный сок собирают из желудочной канюли посредством естественного дренирования самотеком каждые 15 мин. Т е с т и руемые соединения вводят собакам внутривенно после т о г о , как желудочная секреция, индуцированная н е п р е рывным внутривенным вливанием г и с т а мина (60 м к г / к г - ч ) , достигает у с т о й чивого уровня. Кислотность желудочного сока измеряют титрованием 0,05 N раствором NaOH при использовании автоматического титратора.Выражаемую в процентах степень ингибирования каждой дозы тестируемого л е карственного с р е д с т в а , вычисляют из разницы между количеством кислоты, выделяющейся перед введением л е к а р с т в а , и минимальным количеством с е к ретируемой кислоты, которое дости 10 15 20 25 30 35 40 гается обычно спустя 45 мин после введения л е к а р с т в а . Дозу, вызывающую 50%-ное ингибирование выделения ки слоты, у э н ают и з кри вой, отр ажающей зависимость между вводимой дозой лекарственного средства и достигаемой степенью ингибирования,причем указанную степень ингибирования откладывают на графике в полулогарифмической шкале против соответствующей дозы. Полученные данные приведены в графе А т а б л . 1 . II . Секреция желудочной кислоты у крыс с перевязанным пилорусом. Самцов крыс W i s t a r r a t s , весящих около 200 г , не кормят в т е ч е н и е 24 ч , но разрешают свободный д о с т у п к в о д е , при содержании до проведения экспериментов в индивидуальных к л е т к а х . ГІилорическую ч а с т ь желудка п е ревязывают под эфирным наркозом по методу Шея и д р . Тестируемые с о е д и нения вводят крысам в н у т р и д у о д е н а л ь но немедленно после п е ре в я з к и пилор у с а . Подопытных животных умерщвляют с п у с т я 4 ч после в в е д е н и я л е к а р с т в е н н о г о с р е д с т в а и собирают с о д е р жимое их желудков. Кислотность с о б ранного желудочного с о к а измеряют титрованием 0 , 0 5 N р а с т в о р о м г и д р о окиси натрия при использовании а в т о м а т и ч е с к о г о т и т р а т о р а . Степень ингибнрования желудочной секреции в р е з у л ь т а т е введения каждой испытуемой дозы тестируемых л е к а р с т в е н н ы х с р е д с т в вычисляют по р а з н и ц е в к о л и ч е с т в е выделившейся желудочной кислоты у крыс контрольной группы и крыс э к с п е р и м е н тальных г р у п п , которым вводили т е с т и руемые л е к а р с т в а . Величины ЕД^ 0 о п р е деляют по м е т о д у , аналогичному о п и санному. Полученные р е з у л ь т а т ы п р е д ставлены в графе В т а б л . 1 . III . Острая т о к с и ч н о с т ь на мышах. Тестируемые л е к а р с т в а в в о д я т внутривенно самцам мышей линии ICP,.имеющим вес около 35 г, в д о з е 0 , 1 мл/ /10 мг/10 с и животных оставляют под наблюдением на 7 д н е й . Величины ЛДе 0 определяют по методу " в в е р х и в н и з " при использовании 10 подопытных животных. Полученные р е з у л ь т а т ы п р е д ставлены в графе С т а б л . 1 . 50 В т а б л и ц е п о к а з а н а фармакологическая активность блокаторов гистаминовых ^ - р е ц е п т о р о в . 876056 Нт-блокирующая активность Соединение в А ЕД5о, мкг/кг мкг/кг N-сульфамоил-З- [(2-гуанидинотиазол-4-ил) метилті-ioj пропионамидин N-метансульфонил-З- [(2-гуанидннотиазол-4-ил )метилтио^проционамидина малеат N - к ар б амои л - 3 -[(2 - гу анилинотиазол-4-ил]метил -тио]пропионамидина дигидрохлорид N-циано- [(2-гуанидинотиазол-4~ил)метилтио] пропи о намидин 8, 7+0,5 ЛД50, мкг/кг 0,87 ( 0 , 3 8 - 1 , 9 7 ) 244,4 19,1+2,6 8,9 Н 5 , 0 1 ; N 19,99. П р и м е р 3. К 1,9 г э т н л - j - [(2-гуанидинотиазол-4-ил)метилтио] пропионимидата прибавляют 10 мл э т а нольного р а с т в о р а , 0,28 г цианамида и смесь оставляют на ночь при комнатной температуре. Затем растворитель отгоняют из реакционной смеси при пониженном остаточном давлении и полученный остаток очищают колоночной хроматографией на силикагеле при и с пользовании смеси растворителей хлороформ : метанол в качестве элюата. В итоге получают 1,35 г целевого N-циано- К2-гуанидинотиазол-4-ил)метилтио] пропионамидина с температурой плавления 102,5~104°С. Элементный анализ для Cg Н^Н T S ? : Найдено, %: с 3 7 , 8 4 ; Н 4 , 5 0 ; N 34,26, Вычислено, '• С 3 8 , 1 5 ; Н 4 , 6 2 : N 34,60. П р и м е ,р 4. Аналогично примеру 3 получают М-(2-пропинил)-3- [(2-гуанидинотиазол-4-ил)метилтиоТ.-пропиоиамидин. Для проведения реакции используют L 30 35 40 45 50 55 Ь n H.NCH^CSCH. . Масс-спектр т/е 296 (М + ). Спектр ядерного магнитного р е з о нанса,снятый в смеси деитерированного диметилсульфоксида (ДМСО-cU) и дейтерированного метанола (СД^ОД), 0^:2,30 м . д . (2Н,триплеті S C H C H v 2,70 м,Д(2 Н»Триплет Г., сД * ' J 65 I , О 5 М.Д (1Н,триплет, СНдС ЕСН) ; 10 876056 4,60 3,70 М.Д.С2Н, с и н г л е т , м . д . (2Н, д у б л е т , 6,4 8 м.д. -CH^S ) ; CH ПН, синглет, ^ \ S И ). П р и м е р 5. Аналогично примеру 3 получают N-бенэпл-З- [(2-гуанидинотиаэол-4-ил)метилтио]пропионамидин. При проведении реакции используют Масс-спектр т/е 241 (m-NH^CH^CfeH Спектр ядерного магнитного резо-' нанса, снятый в ДМСО-Д^; о*: 2, 38 м . д . (2Н, триплет") $ с н с н j . 2 Г 7 5 м . д . (2Н, т р и п л е т ] 1 ^ 4,17 м.д. м.д. 15 (2Н, синглет 3,60 шивании сухоП газообразный хлористый водород в течение 1,5 ч . Затем р е а к ционную смесь концентрируют при пониженном остаточном давлении, к остатку добавляют 10 мл этанола и смесь снова упаривают при пониженном давлении. 5 Полученный остаток растворяют в небольшом количестве этанола. К р а с г в о ру добавляют диэтиловый эфир и смесь оставляют на ночь. Выпавший в этик условиях кристаллический осадок отделяют фильтрованием и в итоге получают 0г55 г целевого днгидрохлорида N-карбамоил-3- [(2-гуанидииотиазол-4-ил) метилтио]пропионамидпна с температурой планпения 171-173 С. (2Н, синглет, 20 Элементный анализ для Cg H17N у 5 QOC L : Найдено, %: С 2 8 , 7 3 ; Н 4 , 6 4 , N 25,78. Вычислено, %: С 2 8 , 8 8 ; Н 4 , 5 8 ; N 26,19. П р и м е р 10. В 30 мл :>глнола растворяют 6,4 г метил-3-(2-ме-іилгуанидшюгиазол-4-илмєтшітио)протіоннміг6 , 4 5 м . д . (1Н, с и н г л е т , д а т а . К раствору прибавляют 0,9 г цианамида и реакционную смесь п е р е мешивают при комнатной температуре 7 , 3 0 м . д . (5Н Г с и н г л е т 25 в течение 2 ч, после чего р а с т в о р и тель отгоняют при пониженном д а в л е нии . Полученный поспе упаривания р е Н Н акционного раствора остаток очищают П р и м е р 6. Гидрохлорид 3 - [ ( 2 колоночной хроматографией, исполь-гуанидинотиазол-4-ил)метилтио]про30 зуя систему хлороформ-метанол в к а пионамидин с температурой плавления честве элюента. После перекристалли109-112°С. Для проведения реакции зации полученного продукта из этанола используют NH4.CI . получают 2,0 г целевого N-циаЕЮ-ЗЭлементный анализ для CH 5 S^Cl • 3.N 1 -(2-метил-гуанидинотиазол-4-илметилНайдено, %: С 3 2 , 3 3 , Н 5 , 0 1 , тио)пропионамидчна, показавшего тем3S пературу плавления 144-145°СN 28,28, Вычислено, %: С 3 2 , 5 9 , И 5 , 1 3 , N 28,51. Элементный анализ для С{0И,5Н7$' : ' " П р и м е р 7. N-Бензоил-З- [(2Найдено, %• С 4 0 , 1 3 , и ' 5 г 0 0 ; -гуанидинотиазол-4-ил)метилтио проN 32,68. пионамидгидразон с температурой 40 Вычислено, % С 4 0 , 3 9 ; II 3,08? • плавления ЮЗ-Юб^С. Для проведения N 32,97. этой реакции используют H^N - ІЇНСОП р и м е р 1 1 . в смеси 20 мл э т а н о л а , 30 мл хлороформа и 10 мп метанола растворяют, 1,0 г N-циано45 -3-(2-метилгуанидинотиазол-4-илмєіилЭлементный а н а л и з для CirH^NyOSj : тио)пропионамидпна. Раствор охлаждаН а й д е н о , %: С 4 7 , 4 3 , Н 5 , 0 0 , ют на ледяной бане до 0-5°С и в т е N 25,72. чение 1 у пропускают через него ток В ы ч и с л е н о , %: С 4 7 , 7 3 , Н 5 , 0 1 , сухого хлористого водорода, после N 25,97. 50 чего растворители ОТГОНЯІСТ при пониП р и м е р 8 . Ы-Ацетил-3- [ ( 2 женном остаточном давлении. Затем -гуанидинотиазол-4-ил)метилтио]прополученный остаток перекристаллипионамидгидразон с температурой зовывают из этанола и получают в итоп л а в л е н и я 1 6 3 - 1 6 6 ° с . Для п р о в е д е н и я г е 1/2 г целевого дигшдрохлорида Нреакции используют H -карбамоил-3-(2-метилгуаіш динотиа55 зол-4-илметилтио)пропионамидина, имеЭлементный а н а л и з д л я С , , Н . 7 ( ? 0S« ющего температуру плавления 180Найдено, ї : С 3 7 , 8 6 ; Н 5 , 6 2 ; N 30^73. 182°С. Вычислено, %: С 3 8 , 0 8 , Н 5 , 4 3 , N 31,09. Элементный анализ для C^H^hUOS,. С 1 х П р и м е р 9 . В с м е с и 15 мл э т а л і /z нли : нола и 10 мл хлороформа р а с т в о р я ю т Найдено, %: С 30,52; Н 5 , 0 6 ; 0,5 г N-циано-З- [(2-гуанидинотиазолN 24,41. |-4-ил)метилгиоТ, п р о п и о н а м и д и н а . р а с т Вычислено, %: С 30,29; Н 5,07; 'вор охлаждают с помощью б а н и , н а п о л N 24,08. ненной л е д я н о й в о д о й , и пропускают П р и м е р 12. В 49 мл метанола ч е р е з н е г о при охлаждении и п е р е м е 65 растворяют 2,0 г метип-3-(2-гунидино* 11 тиаэол-4-илметилтио) пропионимидата и 1,21 г бензолсульфонплгидразина.Раствор перемешивают при комнатной температуре в течение 24 ч , лосле чего упаривают в вакууме с целью отгонки растворителя. Полученный остаток очищают колоночной хроматографией, используя систему растворителей хлороформ-метанол в качестве элюента. В итоге получают 1,2 г целевого N-бензолсульфонил-3-(2-гуанидинотиазол-4-илметилтио) пропиои амид гидр аз о-на, имеющего температуру плавления 159,5-161°С. Элементный'"анализ для C^H^O^S^ : Найдено, %: С 40,30; Н 4,54; N 23,46. Вычислено, %: С 40,66; Н 4 , 6 3 ; N 23,71. П р и м е р 13. В 20 мл метанола суспенцируют 2 г метил-3-(2-гуаиидииотиаэол-4-илметилтио)пропионимидата и к этой суспензии прибавляют при перемешивании раствор 0,5 г глицина в 5 мл воды. После перемешивания р е акционной смеси в течение 2 ч при комнатной температуре растворитель отгоняют в вакууме. Полученный остаток перекристаллизовывают из смеси воды и ацетона. В итоге получают 1,0 г целевого 3-(2-гуанидинотиаэол- 4-илметилти.о) пропионамидиноглицин а, имеющего температуру плавления 140141 С (с разложением). Элементный анапиз дпя CJ-LN.O.So* *2 1/4 Н20 : Найдено, %: С 3 3 , 8 2 } Н 5,43; U 23,65 . Вычислено, %: С 33,65; Н 5,79; N 23,55. 12 876056 ); 8,10 м.д. (4Н, бисинглет Н ) . Масс-спектр m/є 276 (М + +1). П р и м е р 2 0 . В смеси 30 мл этанола и 30 мл воды растворяют 5,0 г метил 3-(2-гуакидинотиазол-4-илметилтио}-пропионимидата, полученный р а с т 20 вор выдерживают при 40°С в течение 20 ч , после чего растворитель отгоняют в вакууме. Образовавшийся о с т а ток очищают методом колоночной хроматографии при использовании в кахлороформмега25 честве эпюента смеси нол и выделенное из элюата вещество перекристаллизовывают из метанола. 3 итоге получают 3,2 г целевого 3-(2-гуанидинотиазол-4-илметилтио)про3D пионамида, имеющего температуру плавления 193-194°С (с разложением). 35 40 45 50 55 60 65 Элементный анализ для CglH^N^OSn: Найдено, %: С 3 6 , 9 7 ; Н 5 , 0 6 ; N 26,84. Вычислено, %: С 37,05; Н 5 , 0 5 ; N 27,00. П р и м е р 2 1 . В 50 мл IN р а с т вора соляной кислоты растворяют 2,5 г N-сульфамоил-З-(2-гуанидинотиазол-4-илметилтио)пропионамидина и полученный р а с т в о р перемешивают при 40 С в течение 2 ч . Образовавшийся кристаллический осадок отфильтровывают и перекристаллиэовывают из смеси метанола и э т и л а ц е т а т а . в итоге получают 1,65 г целевого гидрохлорида 3-(2-гуанидинотиазол-4-илметилтио) пропионилсулъфамида, имеющего температуру плавления 266-167°С. Элементный анализ для C Hj ^ g СЬН-0 g fN O S Найдено, Ї : С 2 4 , 7 8 ; Н 4 , 2 3 ; N 21,61. Вычислено, %: С 2 4 , 4 6 ; Н 4 , 3 6 ; N 21,39. П р и м е р 22. В 20 мл метанола растворяют 4,09 г метил-3- [(2-гуанидинотиаэол-4-ил)метилтио] лропионимидат а . Раствор нагревают до кипения и, продолжая кипячение с обратным холодильником, прибавляют к нему 15 мл р а с т в о р а 2,88 г сульфамила в метаноле После кипячения реакционного р а с т в о ра с обратным холодильником в т е ч е ние примерно 3 ч растворитель отгоняют при пониженном давлении и полученный о с т а т о к очищают колоночной хроматографией на силикагеле при использовании смеси хлороформметанол (с 15 876056 16 зоп-4-ил)метилтиоД пропионимидата и _*радиентом от 21:1 до 1:1) в качестве элгоента. Из элюата выделяют 3,26 г 590 мг бензолсульфонамида. Полученцелевого N-сульфамоип-З- [(2-гуачидиную смесь оставляют при комнатной нотиаэол-4-ил)метилтио]пропионамидина температуре на 24 ч . После этого ( с температурой плавпения 163-164 °С. растворитель отгоняют при пониженном Элементный анализ для Сэ HyN T 0^S^: давлении и полученное в остатке в е щество очищают колоночной хроматоНайдено, % С 2 8 , 3 7 , Н 4 48; графией на силикагеле при использоваN 28,97. Вычислено, нии в качестве элюента смеси хлороС 28,48; Н 4,43> N 29,06. форм-метанол ( 2 0 : 1 - ^ 1 0 : 1 ) . В итоге Спектр ядерного магнитного р е з о получают 855 мг целевого N-бензолнанса в ДМСО-dg еЛ 2,50 м . д . (2Н,мульти- 10 сульфонил-3- Г(2-гуанидинотиазол-4плет ^ S C H ^ C ^ - ) ; 2,65 м . д , (2Н, мулъ-ил)метилтио} пропионамида в виде типлет, - S C H J C H J - ) ; 3,60 М.Д. (2Н, аморфного вещества. Спектр ядерного магнитного р е з о 6,45 м.д. (1Н, сингсинглет нанса, снятый в дейтирированном диме5 15 тилсульфоксиде (ДМСО-с16) сл^2,60 м . д . (4Н, мультиплет, - SCH1CH1C^ ) ; лет Масс-спектр по методу с удвоением 3,55 м . д . (2Н, синглет, частоты m/e 338. П р и м е р 23. В 10,2 мл метанола растворяют 1,27 г м е т и л - 3 - [ ( 2 - г у а 6,40 м . д . (1Н, синглет, нидииотиазол-4-ил)метилтио]пропионими-1 дата и 0,86 г метансульфонамида. Полу ченный реакционный раствор выдерживают при комнатной температуре в т е • 7,50 м . д . (ЗН, чение 48 ч , после чего упаривают в 25 вакууме с целью отгонки растворителя. Вещество, полученное в о с т а т к е , очи К щают колоночной хроматографией на силикагеле при использовании смеси 7,80 м . д . (2НГ мультиплет хлороформ-метанол ( 2 0 : 1 - * 10:1) в к а - 3D чество элюеита. Иэ элюата выделяют 1,4 4 г желаемого N-мегансулъфонил- 3 - [(2-гуаиидинотиазол-4-ил)метилтио і ] Масс-спектр по методу Д m/e 398. пропионамидина в виде аморфного про- ( П р и м е р 2 5 . В 10 мл метанола дукта. растворяют 1 г метил-3- [(2-гуанидино35 тиазол-4-ил)метилтио]пропионимидата Спектр ядерного магнитного р е з о и 0,38 г метансульфонамида и раствор нанса, снятый в СД^ОД Ф-\ 2,58 м . д . оставляют для протекания реакции при (2Н, дублет, -SCH^CH^-) ; 2,76 м.д. комнатной температуре на 4 8 г. После (2Н, дублет, - SCH a CH a -j; 2,91 м . д . этого растворитель отгоняют при пони(ЗН, синглет, -СН а ); 3,67 м . д . (2Н, 40 женном давлении, вещество, полученное в о с т а т к е , растворяют в 3 мл этанола (1Н, М.Д. синглет и раствор оставляют охлаждаться в холодильнике, в результате чего из него выпадает белый кристаллический синглет 45 осадок. Выпавшие кристаллы отделяют г фильтрованием, сушат и получают в Масс-спектр по методу ЄI m/e 336. итоге 0, 7 г целевого N-метансульфонилПолученный таким образом N-метан- 3 - [12-гуанидинотиаэол-4-ил) метилтио] сульфонил-3- Г( 2-гуанидинотиазол-4-ил) пропионамидина с температурой плавметилтио]пропионамидип растворяют в ления 117-118°С. ацетоне и к этому раствору прибав50 Спектр ядерного магнитного р е з о ляют по каплям ацетоновый раствор нанса, снятый в дейтерированном ме0,5 г малеиновой кислоты, что привотаноле - СД^ОД , 0х- : 2,60 м . д . (2Н, дит к образованию кристаллического мультиплет, -ЭСН^СН^С); 2,80 м . д . осадка. Выпавшие кристаллы отфильт(2Н, мультиплет, - S С Н 2С Н оС ^ _ ^ ); ровывают и в итоге получают целевой 55 2,92 м . д . (ЗН, синглет, S ) мал^ат N-метансульфонил-З- [{2-гу анидинАтиаэол-4-ил)метилтио]пропионами3,66 м . д . (2И, с и н г л е т , дииа с температурой плавления 195); 197°С. Элементный анализ для CJJIVJN ^O^Sj : 6,50 м . д . (1Н, с и н г л е т , Найдено, %: С 34,64; II 4 , 4 9 ; N 18,13. П р и м е р 26, В Ю «ш этанола Вычислено, %: С 3 4 , 5 1 ; Н 4 , 4 5 ; растворяют 1 г метил-3- [(2-гуанидиноN 18.57. тиазол-4-ил)метилтио]пропионимидата П р и м е р 24 .В 8 мл метанола р а с т воряют 800 мг метнл-3-[(2-гуанидинотиа- 65 и 0,69 г п-аминобензолсульфонамида 17 876056 18 THOJ пропискамидин и мал ей нов о кислую и полученный раствор остаяляют на соль Н-бєі-пилсульфамил-З- [(2-гуани48 ч при комнатной температуре. После динотиазол-4-ил} метилTHOJ пропионэ т о г о растворитель отгоняют при пониженном давлении и полученный о с т а т о к ами дин а с температурой плавления очищают колоночной хроматографией 160-162^0. на силикателе при использовании в к а Для проведения реакции используют ч е с т в е элюента смеси хлороформ-метанал (с градиентом от 20:1 до 1 0 : 1 ) . В итоге получают 1,2 г целевого Н-(гт -аминобензолсульфонил)-3- Г(2-гуани~ Спектр ядерного магнитного р е з о диногиаэол-4-ил)-метилтио]пропиочамин а н с а , снятый в ДМСО-dft , о* : 2 , 5 0 м . д . дина в виде аморфного твердого в е 10 (2Н, м у л ь т и п л е т , -SCM^CH/jC^ ); щества. 2 , 6 4 м . д . (2Н, м у л ь т и п л е т -5СНдСНjC^ ) ; Спектр ядерного магнитного р е з о )ї 3,60 м . д . (2Н, сииглет, 2,50 м . д . нанса, снятый в ДМСО-dt, (2Н, мультиплет, -SCHjCH г ); ) ; 15 4,02 м . д . (2Н, дублет,- СНа 2,64 м . д . ( 2 Н , м у л ь т и п л е т , } А, 3,56 м.д.(2Н, синглет, '5,68 м . д . (2Н, с и н г л е т , ^ 6,46 м . д . \_ (1Н, синглет , _ / 20 6,40 м . д . ( 1 Н , синглет,/ 6,02 м.д. (4Нг сингле г,ц „ 7,18 м.д. (IH, квадруплет,! 6,54 м . д . (2Н, д у б л е т , - ^ 25 7,50 и 3,30 м.д. (2Н, синглет, 6,80 м.д. (4Н, синглет, 30 7,44 м.д. (2Н, дублет—(/ V _ 7,74/8,38 м.д. (2Н, синглет- С^ П р и м е р 27. Аналогично примеру 26 получают N-сульфамоил-З- [(2-N-метилгуанидинотиазол-4-ил)метил40 тио]пропионамидин. Для проведении реакции используют H^NSO^NH,. Температура плавления образца, перекристаллизованного из меганола 163-164 С С. Элементный анализ для СдН^М^О^З^: Найдено, %: С 30,47, Н 4 , 8 4 , N 27,80. Вычислено, %: С 30,76, Н 4 , 8 8 ; N 27,90. П р и м е р 2 8 . Аналогично примеру 26 получают М-сульфамоил-4-ил- [(2-гуанидинотиазол-4-ил)метилтио] бутирамидин. Для проведения реакции используют H^NSO^NHi. г Температура плавления продукта, перекристаллизованного из этилового спирта,1В9-161°С. Элементный анализ для CgH J 7 N T S 3 0 o : Найдено, %: С 3 0 , 3 9 ; Н 4 , 8 6 ; N 27,01. 60 Вычислено, %: С 30,76; Н 4 , 8 8 , N 27,90. П р и м е р 29. Аналогично примеру 23 получают N-бензилсульфамил3- [(2-гуанидинотиазол-4-ил)меіил65 N N Элементный анализ для ttf_ Н а й д е н о , %: С 4 1 , 7 9 ; Н 4 , 6 4 ; 17,90. В ы ч и с л е н о , %: С 4 1 , 9 8 ; Н 4 , 6 4 ; 18,04. П р и м е р 30. Аналогично примеру 23 получают N-диметилсульфамил-З- [(2-гуанидинотиазол-4-ил )могилтио] пропионамидин. Температура плавлення малеиновокислой соли 183-19Є С. Для проведения реакции используют Спектр ядерного магнитного резонанса, снятый в ДМСО-d^ , сЛ- : 2,59 м.д. (6Н, дублет, - N . ) ; 2 , 5 - 2 , 8 м.д. (4 8, 3,64 м.д. 6,84 м.д. (4Н, мультиплет, (2Н, синглет, / s синглет—4 -инглет х ; ^ c = N - 7,70 и 8,36 (2Н, синглет -С"" м.д. ). Элементный анализ для C /4 H^ N 7°6 S 3 : Найдено, Ьг С 34,82; Н 4 , 7 6 ; N 19,96. Вычислено, %: С 34,92, Н 4 , 8 1 ; N 20,30. П р и м е р 3 1 . Аналогично примеру 2 3 получают дималеат N-трифторметансульфонил-3- Г(2~гуанидинотриазол-4-ил)-метилтио]пропионамидина. 876056 19 Для проведения реакции используют т Температура плавления продукта, п е р е к р и с т а л л и з о в а н н о г о из м е т и л э т и л к е т о н а , 168-170°С. Элементный анализ для C^V^O^S^ : Найдено, %: С 3 2 , 7 0 ; Н 3,46; " N 14,00. Вычислено, %: С 3 2 , 8 0 ; И 3,40, N 13,50. П р и м е р 32 . Аналогично примеру 2 3 получают N-метилсульфамил-З- [(2-гуанидинотиазол-4-ил)метилтио] пропионамидин и е г о малеиновокислую с о л ь , имеющую температуру плавления 181-184°С. Для проведения реакции используют НQ^NS0-2_NHСН^Спектр я д е р н о г о магнитного р е з о н а н с а , снятый в ДМСО-с!^,
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for producing guanidine-thiasol substances
Автори англійськоюIsao Yanagisava
Назва патенту російськоюСпособ получения гуанидино-тиазольных соединений
Автори російськоюИсао Янагисава
МПК / Мітки
МПК: A61K 31/425, C07D 277/38
Мітки: спосіб, гуанідінотіазольних, сполучень, одержання
Код посилання
<a href="https://ua.patents.su/14-5926-sposib-oderzhannya-guanidinotiazolnikh-spoluchen.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання гуанідінотіазольних сполучень</a>
Попередній патент: Спосіб одержання 1,1-діоксіда пеніціланової кислоти або її ефіру
Наступний патент: Об’ємний залізобетонний елемент даху будівлі з горищем
Випадковий патент: Спосіб прогнозування ризику проведення повторних некректомій у хворих з пролежнями м'яких тканин