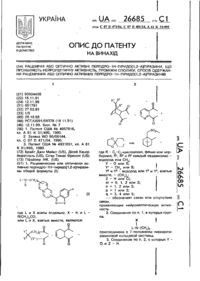
Спосіб одержання оптично-активних амінів та оптично-активний амід
Формула / Реферат
(21)2002065187
(57)
1. Спосіб одержання оптично-активних амінів загальної формули І
, (I)
де
R1 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з
1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил,
R2 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил,
R3 водень, гідрокси-, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, Х= кисень або NH, який відрізняється тим, що включає наступні стадії:
а) взаємодію сполук загальної формули II
, (II)
де
R1 заміщений або незаміщений, розгалужений або нерозгалужений
алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або
гетарил, зі сполуками формули
R2-XH, (III)
де
R2 заміщений або незаміщений, розгалужений або нерозгалужений
алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або
гетарил,
в присутності основи з одержанням сполук загальної формули IV
, (IV)
де
R1 заміщений або незаміщений, розгалужений або нерозгалужений
алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або
гетарил,
R2 заміщений або незаміщений, розгалужений або нерозгалужений
алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або
гетарил, Х= кисень або NH,
б) взаємодію реакційного розчину сполук загальної формули IV зі сполуками загальної формули
NH2R3, (V)
де
R3 водень, гідрокси-, заміщений або незаміщений, розгалужений або
нерозгалужений алкіл з 1-10 атомами вуглецю, з одержанням сполук загальної формули VI
, (VI)
де
R1 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил,
R2 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил,
R3 водень, гідрокси-, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, Х= кисень або NH,
в) гідрування сполук загальної формули VI з одержанням сполук загальної формули VII
, (VII)
де
R1 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил,
R2 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил,
R3 водень, гідрокси-, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, Х= кисень або NH,
в присутності каталізатора гідрування,
г) розщеплення рацематів сполук загальної формули VII з одержанням сполук загальної формули І оптично активною карбоновою кислотою або естерами загальної формули VIII
, (VIII)
де
R4 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю,
R5 водень, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю,
R6 водень, заміщений або незаміщений, розгалужений або
нерозгалужений алкіл з 1-10 атомами вуглецю або заміщений або
незаміщений феніл, n= 0 або 1,
в присутності ліпази або естерази.
2. Спосіб за п. 1, який відрізняється тим, що для розщеплення рацематів як оптично активну карбонову кислоту застосовують карбонову кислоту, вибрану з групи, що включає винну кислоту, дибензоїлвинну кислоту, мигдальну кислоту, камфорну кислоту, камфорсульфонову кислоту, п-гідрокси-мигдальну кислоту, п-СІ-мигдальну кислоту, феноксипропіонову кислоту, п-гідрокси-фенокси-пропіонову кислоту або молочну кислоту.
3. Спосіб за п. 1, який відрізняється тим, що при ферментативно-каталізованому розщепленні рацематів за допомогою естеру на стадії 1 (г) одержують суміш з оптично-активного, заміщеного гетероатомом, аміну загальної формули І, де радикали X, R1, R2 і R3 мають вказані нижче значення, і оптично активного, заміщеного гетероатомом, аміду загальної формули IX
, (IX)
де
R1 (С1-С6)-алкіл,
R2 феніл-(С1-С6)-алкіл,
R3 водень,
R5 водень,
R6 (С1-С6)-алкіл,
Х= кисень або NH,
n=0,
яку відокремлюють і розділяють.
4. Спосіб за п. 3, який відрізняється тим, що амід розщеплюють і одержують вільний амін, що утворився при розщепленні.
5. Спосіб за п. 3, який відрізняється тим, що отриманий амід рацемізують за умов розщеплення і повертають на стадію (г) способу за п. 1.
6. Спосіб за п. 4, який відрізняється тим, що отриманий амін рацемізують і повертають на стадію (г) способу за п. 1.
7. Спосіб за п. 1, який відрізняється тим, що стадію (а) проводять в присутності інертного при умовах реакції, апротонного розчинника.
8. Спосіб за п.1, який відрізняється тим, що основу на стадії (а) застосовують в діапазоні 0,001-10 мол. % в перерахунку на кількість сполуки формули III, що застосовують.
9. Спосіб за п. 8, який відрізняється тим, що на стадії (а) як основу застосовують алкоголяти лужного або лужноземельного металу або сильні основні аміни.
10. Спосіб за п. 1, який відрізняється тим, що отриманий на стадії (а) реакційний розчин нейтралізують перед взаємодією зі сполукою загальної формули (V).
11. Спосіб за п. 1, який відрізняється тим, що сполуки формул IV, VI або VII після стадій (а) до (в) виділяють перед початком наступної стадії.
12. Спосіб за п. 1, який відрізняється тим, що як сполуку загальної формули NH2R3 застосовують гідроксиламін.
13. Спосіб за п. 11, який відрізняється тим, що стадію (б) проводять в присутності інертного при умовах реакції, протонного розчинника.
14. Спосіб за п. 1, який відрізняється тим, що на стадії (в) застосовують каталізатори гідрування на базі Nі, Co, Pt, Pd, Ru або Rh.
15. Спосіб за п. 13, який відрізняється тим, що як каталізатор гідрування застосовують нікель Ренея.
16. Спосіб за п. 12 або 13, який відрізняється тим, що гідрування проводять в розчиннику.
17. Спосіб за будь-яким з пп. 13 - 15, який відрізняється тим, що гідрування проводять при тиску від нормального до 300 бар.
18. Спосіб одержання сполук загальної формули VII
, (VII)
який відрізняється тим, що включає наступні стадії:
а) взаємодію сполук загальної формули II
(II)
зі сполуками формули R2XH (III) в присутності основи з одержанням сполук загальної формули IV
, (IV)
б) взаємодію реакційного розчину сполук загальної формули IV зі сполукою загальної формули NH2R3 (V) з одержанням сполук загальної формули VI
, (VI)
в) гідрування сполуки загальної формули VI з одержанням сполук загальної формули VII в присутності каталізатора гідрування, причому замісники в формулах II, III, IV, V, VI і VII мають наведені в п. 1 значення.
19. Спосіб за п. 18, який відрізняється тим, що стадію (а) проводять в присутності інертного, за умов реакції, апротонного розчинника.
20. Спосіб за п.18, який відрізняється тим, що основу на стадії (а) застосовують в діапазоні 0,001-10 мол.% в перерахуванні на кількість сполуки формули III, що застосовують.
21. Спосіб за п. 20, який відрізняється тим, що на стадії (а) як основу застосовують алкоголяти лужного або лужноземельного металу або сильні основні аміни.
22. Спосіб за п. 18, який відрізняється тим, що отриманий на стадії (а) реакційний розчин нейтралізують перед взаємодією зі сполукою загальної формули (V).
23. Спосіб за п. 18, який відрізняється тим, що сполуки формул IV, VI або VII після стадій (а) до (в) виділяють перед початком наступної стадії.
24. Спосіб за п. 18, який відрізняється тим, що як сполуку загальної формули NH2R3 застосовують гідроксиламін.
25. Спосіб за п. 23, який відрізняється тим, що стадію (б) проводять в присутності інертного, за умов реакції, протонного розчинника.
26. Спосіб за п. 18, який відрізняється тим, що на стадії (в) застосовують каталізатори гідрування на базі Nі, Co, Pt, Pd, Ru або Rh.
27. Спосіб за п. 25 який відрізняється тим, що як каталізатор гідрування застосовують нікель Ренея.
28. Спосіб за п. 24 або 25, який відрізняється тим, що гідрування проводять в розчиннику.
29. Спосіб за будь-яким з пп. 25 - 27, який відрізняється тим, що гідрування проводять при тиску від нормального до 300 бар.
30. Сполуки формули IX
, (IX)
де
R1 (С1-С6)-алкіл,
R2 феніл-(С1-С6)-алкіл,
R3 водень,
R5 водень,
R6 (С1-С6)-алкіл,
Х= кисень або NH,
n=0.
Текст
УКРАЇНА (19) UA (11) 77651 (13) C2 (51) МПК (2006) C12P 41/00 C07B 55/00 C07B 57/00 C07C 209/58 (2006.01) C07C 209/86 (2006.01) C07C 213/00 C07C 215/00 C07C 217/10 (2006.01) C07C 235/08 (2006.01) МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ ДЕРЖАВНИЙ Д ЕПАРТАМЕНТ ІНТЕЛ ЕКТУАЛЬНОЇ ВЛАСНОСТІ ОПИС ДО ПАТЕНТУ НА ВИНАХІД (54) СПОСІБ ОДЕРЖАННЯ ОПТИЧНО-АКТИВНИХ АМІНІВ ТА ОПТИЧНО-АКТИВНИЙ АМІД де R1 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил, R2 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил, R3 водень, гідрокси-, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, Х= кисень або NH, який відрізняється тим, що включає наступні стадії: а) взаємодію сполук загальної формули II O O NHR3 R2 X * R2 (I) R1 * = оптично активний , де X R1 (IV) , (11) UA , де R1 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил, зі сполуками формули R2-XH, (III) де R2 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил, в присутності основи з одержанням сполук загальної формули IV 77651 (II) R1 (19) (21) 2002065187 (22) 13.11.2000 (24) 15.01.2007 (86) PCT/EP00/11191, 13.11.2000 (31) 199 56 786.7 (32) 25.11.1999 (33) DE (46) 15.01.2007, Бюл. №1, 2007р. (72) Дітріх Клаус , DE, Зігель Вольфганг , DE (73) БАСФ АКЦІЕНГЕЗЕЛЬШАФТ, DE (56) WO, 9728271, A1, 07.08.1997 WO, 9623894, A1, 08.08.1996 DE, 247144, C, 24.05.1912 DE, 723498, C, 18.08.1942 Andres C. et al. Tetrahedron letters, NL, Elsevier science publishers, Amsterdam, Bd.33, Nr.20, 12.05.1992, seiten 2895-2898 Besse P. et al./Tetrahedron:Assymetry 10 (1999), 2213-2224 Arlene Correa et al, Synth.commun., Bd.21, Nr.1, 1991, seiten 1-9 Gebhard R.R. et al, Hel.Chim.Acta, Bd.38, 1955, seite 915 Bongini A. et al, J.Org.Chemie, Bd.51, Nr.25, 1986, seiten 4905-4910 Emerson W.S. et al, J.Org.Chemie, Bd.14, 1949, Seite 702 Schneider O., Chem.Abstract, vol.41, no.19, 10.10.1947, seite 6199 Chovart Robert J. et al, J.Med.Chemie, Bd.42, Nr.5, 1999, seiten 833-848 (57) 1. Спосіб одержання оптично-активних амінів загальної формули І C2 2 (13) 1 3 77651 R1 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил, R2 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил, Х= кисень або NH, б) взаємодію реакційного розчину сполук загальної формули IV зі сполуками загальної формули NH2R3, (V) де R3 водень, гідрокси-, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, з одержанням сполук загальної формули VI R3 N R2 X (VI) R1 , де 1 R заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил, R2 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил, R3 водень, гідрокси-, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, Х= кисень або NH, в) гідрування сполук загальної формули VI з одержанням сполук загальної формули VII NHR3 R2 (VII) X R1 , де R1 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил, R2 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, арилалкіл, арил, гетарилалкіл або гетарил, R3 водень, гідрокси-, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, Х= кисень або NH, в присутності каталізатора гідрування, г) розщеплення рацематів сполук загальної формули VII з одержанням сполук загальної формули І оптично активною карбоновою кислотою або естерами загальної формули VIII O R4O O (CH2) n R6 (VIII) R5 , де R4 заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, R5 водень, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, 4 R6 водень, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю або заміщений або незаміщений феніл, n=0 або 1, в присутності ліпази або естерази. 2. Спосіб за п.1, який відрізняється тим, що для розщеплення рацематів як оптично активну карбонову кислоту застосовують карбонову кислоту, вибрану з групи, що включає винну кислоту, дибензоїлвинну кислоту, мигдальну кислоту, камфорну кислоту, камфорсульфонову кислоту, п-гідроксимигдальну кислоту, п-СІ-мигдальну кислоту, феноксипропіонову кислоту, п-гідрокси-феноксипропіонову кислоту або молочну кислоту. 3. Спосіб за п.1, який відрізняється тим, що при ферментативно-каталізованому розщепленні рацематів за допомогою естеру на стадії 1 (г) одержують суміш з оптично-активного, заміщеного гетероатомом, аміну загальної формули І, де радикали X, R1, R2 і R3 мають вказані нижче значення, і оптично активного, заміщеного гетероатомом, аміду загальної формули IX (IX) , де R1 (С1-С6)-алкіл, R2 феніл-(С1-С6)-алкіл, R3 водень, R5 водень, R6 (С1-С6)-алкіл, Х= кисень або NH, n=0, яку відокремлюють і розділяють. 4. Спосіб за п.3, який відрізняється тим, що амід розщеплюють і одержують вільний амін, що утворився при розщепленні. 5. Спосіб за п.3, який відрізняється тим, що отриманий амід рацемізують за умов розщеплення і повертають на стадію (г) способу за п.1. 6. Спосіб за п.4, який відрізняється тим, що отриманий амін рацемізують і повертають на стадію (г) способу за п.1. 7. Спосіб за п.1, який відрізняється тим, що стадію (а) проводять в присутності інертного при умовах реакції, апротонного розчинника. 8. Спосіб за п.1, який відрізняється тим, що основу на стадії (а) застосовують в діапазоні 0,00110мол.% в перерахунку на кількість сполуки формули III, що застосовують. 9. Спосіб за п.8, який відрізняється тим, що на стадії (а) як основу застосовують алкоголяти лужного або лужноземельного металу або сильні основні аміни. 10. Спосіб за п.1, який відрізняється тим, що отриманий на стадії (а) реакційний розчин нейтралізують перед взаємодією зі сполукою загальної формули (V). 5 77651 11. Спосіб за п.1, який відрізняється тим, що сполуки формул IV, VI або VII після стадій (а) до (в) виділяють перед початком наступної стадії. 12. Спосіб за п.1, який відрізняється тим, що як сполуку загальної формули NH2R3 застосовують гідроксиламін. 13. Спосіб за п.11, який відрізняється тим, що стадію (б) проводять в присутності інертного при умовах реакції, протонного розчинника. 14. Спосіб за п.1, який відрізняється тим, що на стадії (в) застосовують каталізатори гідрування на базі Nі, Co, Pt, Pd, Ru або Rh. 15. Спосіб за п.13, який відрізняється тим, що як каталізатор гідрування застосовують нікель Ренея. 16. Спосіб за п.12 або 13, який відрізняється тим, що гідр ування проводять в розчиннику. 17. Спосіб за будь-яким з пп.13-15, який відрізняється тим, що гідр ування проводять при тиску від нормального до 300 бар. 18. Спосіб одержання сполук загальної формули VII NHR3 R2 (VII) X R 1 , який відрізняється тим, що включає наступні стадії: а) взаємодію сполук загальної формули II O R1 , (II) зі сполуками формули R2XH (III) в присутності основи з одержанням сполук загальної формули IV O (IV) R2 X R1 , 19. Спосіб за п.18, який відрізняється тим, що стадію (а) проводять в присутності інертного, за умов реакції, апротонного розчинника. 20. Спосіб за п.18, який відрізняється тим, що основу на стадії (а) застосовують в діапазоні 0,001-10мол.% в перерахуванні на кількість сполуки формули III, що застосовують. 21. Спосіб за п. 20, який відрізняється тим, що на стадії (а) як основу застосовують алкоголяти лужного або лужноземельного металу або сильні основні аміни. 22. Спосіб за п.18, який відрізняється тим, що отриманий на стадії (а) реакційний розчин нейтралізують перед взаємодією зі сполукою загальної формули (V). 23. Спосіб за п.18, який відрізняється тим, що сполуки формул IV, VI або VII після стадій (а) до (в) виділяють перед початком наступної стадії. 24. Спосіб за п.18, який відрізняється тим, що як сполуку загальної формули NH2R3 застосовують гідроксиламін. 25. Спосіб за п.23, який відрізняється тим, що стадію (б) проводять в присутності інертного, за умов реакції, протонного розчинника. 26. Спосіб за п.18, який відрізняється тим, що на стадії (в) застосовують каталізатори гідрування на базі Nі, Co, Pt, Pd, Ru або Rh. 27. Спосіб за п.25 який відрізняється тим, що як каталізатор гідрування застосовують нікель Ренея. 28. Спосіб за п.24 або 25, який відрізняється тим, що гідр ування проводять в розчиннику. 29. Спосіб за будь-яким з пп.25-27, який відрізняється тим, що гідр ування проводять при тиску від нормального до 300бар. 30. Сполуки формули IX (IX) б) взаємодію реакційного розчину сполук загальної формули IV зі сполукою загальної формули NH2R3 (V) з одержанням сполук загальної формули VI N R2 X R3 (VI) R1 , в) гідрування сполуки загальної формули VI з одержанням сполук загальної формули VII в присутності каталізатора гідрування, причому замісники в формулах II, III, IV, V, VI і VII мають наведені в п. 1 значення. Винахід стосується способу одержання оптично активних амінів. Далі винахід стосується способу одержання рацемічних амінів, розщеплення рацематів яких може бути здійснене оптично активними карбоновими кислотами або ферментами. Винахід стосується також і рацемічних і оптично активних амінів, а також оптично активних амідів. Розщеплення рацематів амінів за допомогою реакції взаємодії зі складними ефірами, що каталізується ферментами, так само відомо, як і класич 6 , де R1 (С1-С6)-алкіл, R2 феніл-(С1-С6)-алкіл, R3 водень, R5 водень, R6 (С1-С6)-алкіл, Х= кисень або NH, n=0. не хімічне розщеплення рацематів за допомогою утворення діастереомерних солей оптично активними карбоновими кислотами [March J. Ad vanced Organic Chemistry, Reactions, Mechanisms and Structure. 4 th Ed. - John Wiley & Sons, Inc., 1992]. Так, наприклад, [Kitaguchi et al. // J. Amer. Chem. Soc. – 1989. – 111. – P. 3094-3095] описують розщеплення рацематів амінів трифторетилбутиратом при каталізі субтилізином. Енантіоселективність цієї реакції, однак, сильно залежить від 7 77651 розчинника. Навіть при самому придатному з описаних розчинників (3-метил-3-пентанолі) досягається тільки середня селективність. В міжнародній заявці [WO, 91/19002] описується спосіб хірального збагачення асиметричних первинних амінів, при якому аміни піддають реакції взаємодії з етилацетатом або етилбутиратом при каталізі субтилізином. Отримані при цьому надлишки енантіомерів є, однак, незадовільними, крім того потрібно тривалий час реакції від однієї до декількох тижнів. Енантіоселективне ацилювання 2-аміно-бутан-1-олу етиленацетатом при каталізі ліпазою підшлункової залози свині (PPL) описують у [Gotor et al. // J. Chem. Soc. Chem. Commun. – 1988. – P. 957-958]. При цьому складний ефір (етилацетат), що застосовується, використовується як розчинник. При застосуванні інших розчинників, відповідно, інших ферментів не одержують задовільних результатів. Енантіоселективний синтез амідів з рацемічних первинних амінів за допомогою реакції взаємодії 2-хлорпропіонату при каталізі субтилізином у гексані або Candida cylindracea в 3-метил-3пентанолі описується у [Brieva et al. // J. Chem. Soc. Chem. Commun. – 1990. – P. 1386-1387]. Каталізований ліпазою синтез оптично активних амідів з рацемічних, заміщених α-галогеном складних етилових ефірів пропіонової кислоти і первинних амінів описують у [Quiros et al. Tetrahedron: Asymmetry // 1993. – 4. – P. 1105-1112]. Енантіоселективність, що досягається при цій реакції взаємодії не є задовільною. Енантіоселективне ацилювання вторинних амінів, що каталізується ліпазою, описують у [Asensio et al. // Tetrahedron Letters. – 1991. – 32. – P. 4197-4198]. Ця реакція відбувається, однак, тільки при аміні енантіоселективно і тільки з середнім успіхом. Інші аміни взагалі не виявляють енантіоселективності. В патенті [US, 5057607] описується Nацилювання 3-амідо-азет-діонових сполук за допомогою G-амідази пеніциліну. G-амідаза пеніциліну має, однак, тільки дуже обмежений субстратний спектр, так що вона може застосовуватися тільки для одержання β-лактаму. В заявці [WO, 95/08636] описується спосіб розщеплення рацематів первинних і вторинних амінів за допомогою каталізованого ферментом ацилювання. Іншими джерелами, що описують спосіб каталізованого ферментом розщеплення рацематів амінів, є, наприклад, [WO, 96/23894; WO, 97/20946; WO, 97/2871; WO, 97/46698; WO, 98/03465]. У приведених публікаціях описані різні способи розщеплення рацематів амінів. Як продукт розщеплення рацематів поряд з цільовим продуктом також утворюється 50% небажаного енантіомера. Для промислового застосування цих способів важливим є те, що ці небажані енантіомери можуть бути рацемізовані і можуть повертатися в процес розщеплення рацематів, або ж що цей спочатку небажаний енантіомер є також тим, що застосовується для хімічного синтезу продуктом і разом з цим цінним продуктом. При ферментативному розщепленні рацематів один з енантіомерів є 8 присутній в формі аміду. Якщо цей амід є цінним продуктом, то він повинний розщеплюватися зі збереженням стереоцентра. Подібний спосіб розщеплення оптично активних амідів зі збереженням стереоцентра описується в патенті [US, 5905167]. Суттєвою проблемою для технічного розщеплення рацематів оптично активних, функціоналізованих амінів, таких, як аміноспирти, дотепер існує наявність рацемічного аміноспирту, що застосовується як вихідний продукт для розщеплення рацематів. Для забезпечення економічності способу потрібна розробка простого, надійного і недорогого синтезу з одержанням рацемічного функціоналізованого аміну. Авторами [Murata et al. // J. Chem. Soc. Jpn, Ind. Chem. Sect. – 1953. – 56. – P. 628; // Chem. Abstr. – 1955. – 49. - 7517g) пропонується спосіб одержання 1-бензилокси-3-бутанону з 3бутен-2-ону з застосуванням 3 еквівалентів бензилспирту і 0,04 мол. % Na-метаноляту. Недоліком при цьому методі є те, що надлишковий бензиловий спирт повинний відокремлюватися на іншій стадії способу. Крім того, при здійсненні способу часто має місце зворотне розщеплення продукту в вихідні матеріалу, тобто немає необхідної для технічного застосування способу надійності. Відомі до сьогоднішнього часу способи для розщеплення рацематів і одержання рацемічних, функціоналізованих амінів мають той недолік, що вони не мають необхідної для технічного використання простоти і надійності процесу і разом з цим можуть здійснюватися тільки при дуже спеціальних умовах. Крім того, вони вимагають значних кількостей вихідних матеріалів для синтезу рацемічного вихідного продукту, так що заснований на них спосіб не є економічним. Тому, задачею винаходу є розробка способу синтезу рацемічних амінів, таких, як аміноспиртів, а також заснованого на цьому способу розщеплення рацематів рацемічних, амінів, що забезпечує високу надійність процесу при високій енантіоселективності при розщепленні рацематів і який може застосовуватися в широкому діапазоні умов реакції і при цьому може здійснюватися з малими кількостями вихідного продукту і каталізатора, так що витрати на загальний спосіб можуть бути знижені. Ця задача вирішується способом одержання сполук загальної формули І І який відрізняється тим, що він включає наступні стадії: а) взаємодію сполук загальної формули II ІI з сполуками формули III R2 - XH ІII в присутності основи з одержанням сполук загальної формули IV 9 77651 ІV б) взаємодію реакційного розчину сполук загальної формули IV зі сполуками загальної формули V NH2R3 V з одержанням сполук загальної формули VI VI в) гідрування сполук загальної формули VI з одержанням сполук загальної формули VII VII в присутності каталізатора гідрування, г) розщеплення рацематів сполук загальної формули VII з одержанням сполук загальної формули І оптично активною карбоновою кислотою або складними ефірами загальної формули VIII VIII в присутності ліпази або естерази, причому замісники в формулах І, II, III, IV, V, VI, VII і VIII мають наступне значення: R1 - заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, алкеніл з 2-10 атомами вуглецю, алкініл з 210 атомами вуглецю, арилалкіл-, арил-, гетарилалкіл- або гетарил; R2 - заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, алкеніл з 3-10 атомами вуглецю, алкініл з 310 атомами вуглецю, арилалкіл-, арил-, гетарилалкіл- або гетарил; R3 - водень, гідрокси-, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, алкеніл з 3-10 атомами вуглецю або алкініл з 3-10 атомами вуглецю; R4 - заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю; R5 - водень, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю; R6 - водень, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю або заміщений або незаміщений феніл; Х - кисень або азот, переважно кисень; n - дорівнює 0 або 1. R1 означає в сполуках формул І, II, IV, VI, VII і IX заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-Ю атомами вуглецю, 10 алкеніл з 2-10 атомами вуглецю, алкініл з 2-10 атомами вуглецю, арилалкіл-, арил-, гетарилалкілабо гетарил-. Кращими залишками R1 є заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю або арил. Як алкільні залишки слід навести заміщені або незаміщені, розгалужені або нерозгалужені алкільні ланцюги з 1-10 атомами вуглецю, як наприклад, метил, етил, н-пропіл, 1-метилетил, н-бутил, 1-метилпропіл-, 2-метилпропіл, 1,1-диметилетил, н-пентил, 1-метилбутил, 2-метилбутил, 3метилбутил, 2,2-диметилпропіл, 1-етилпропіл, нгексил, 1,1-диметилпропіл, 1,2-диметилпропіл, 1метилпентил, 2-метилпентил, 3-метилпентил, 4метилпентил, 1,1-диметилбутил, 1,2диметилбутил, 1,3-диметилбутил, 2,2диметилбутил, 2,3-диметилбутил, 3,3диметилбутил, 1-етилбутил, 2-етилбутил, 1,1,2триметилпропіл, 1,2,2-триметилпропіл, 1-етил-1метилпропіл, 1-етил-2-метилпропіл, н-гептил, ноктил, н-ноніл або н-децил. Кращими залишками є метил, етил або пропіл. Як алкенільні залишки слід навести розгалужені або нерозгалужені алкенільні ланцюги з 2-10 атомами вуглецю, як наприклад, етеніл, пропеніл, 1-бутеніл, 2-бутеніл, 3-бутеніл, 2-метилпропеніл, 1-пентеніл, 2-пентеніл, 3-пентеніл, 4-пентеніл, 1метил-1-бутеніл, 2-метил-1-бутеніл, 3-метил-1 бутеніл, 1-метил-2-бутеніл, 2-метил-2-бутент, 3метил-2-бутеніл, 1-метил-3-бутеніл, 2-метил-3бутеніл, 3-метил-3-бутеніл, 1,1-диметил-2пропеніл, 1,2-диметил-1-пропеніл, 1,2-диметил-2пропеніл, 1-етил-1-пропеніл, 1-етил-2-пропеніл, 1гексеніл, 2-гексеніл, 3-гексеніл, 4-гексеніл, 5гексеніл, 1-метил-1-пентеніл, 2-метил-і-пентеніл, 3-метил-1-пентеніл, 4-метил-1-пентеніл, 1-метил2-пентеніл, 2-метил-2-пентеніл, 3-метил-2пентеніл, 4-метил-2-пентеніл, 1-метил-3-пентеніл, 2-метил-3-пентеніл, 3-метил-3-пентеніл, 4-метил3-пентеніл, 1-метил-4-пентеніл, 2-метил-4пентеніл, 3-метил-4-пентеніл, 4-метил-4-пентеніл, 1,1-диметил-2-бутеніл, 1,1-диметил-3-бутеніл, 1,2диметил-1-бутеніл, 1,2-диметил-2-бутеніл, 1,2диметил-3-бутеніл, 1,3-диметил-1-бутеніл, 1,3диметил-2-бутеніл, 1,3-диметил-3-бутеніл, 2,2диметил-3-бутеніл, 2,3-диметил-1-бутеніл, 2,3диметил-2-бутеніл, 2,3-диметил-3-бутеніл, 3,3диметил-1-бутеніл, 3,3-диметил-2-бутеніл, 1-етилі-бутеніл, 1-етил-2-бутеніл, 1-етил-3-бутеніл, 2етил-1-бутеніл, 2-етил-2-бутеніл, 2-етил-3-бутеніл, 1,1,2-триметил-2-пропеніл, 1-етил-1-метил-2пропеніл, 1-етил-2-метил-1-пропеніл, 1-етил-2метил-2-пропеніл, 1-гептеніл, 2-гептеніл, 3гептеніл, 4-гептеніл, 5-гептеніл, 6-гептеніл, 1октеніл, 2-октеніл, 3-октеніл, 4-октеніл, 5-октеніл, 6-октеніл, 7-октеніл, ноненіл або декеніл. Як алкінільні залишки слід навести розгалужені або нерозгалужені алкінільні ланцюги з 2-10 атомами вуглецю, як наприклад, етиніл, проп-1-ін1-іл, проп-2-ін-1-іл, н-бут-1-ин-1-іл, н-бут-1-ин-3-іл, н-бут-1-ил-4-іл, н-бут-2-ил-1-іл, н-пент-1-ил-1-іл, нпент-1-ил-3-іл, н-пент-1-ил-4-іл, н-пент-1-ил-5-іл, нпент-2-ин-1-іл, н-пент-2-ин-4-іл, н-пент-2-ил-5-іл, 3метил-бут-1-ин-3-іл, 3-метил-бут-1-ин-4-іл, н-гекс1-ин-1-іл, н-гекс-1-ин-3-іл, н-гекс-1-ин-4-іл, н-гекс-1 11 77651 ин-5-іл, н-гекс-1-ин-6-іл, н-гекс-2-ин-1-іл, н-гекс-2ин-4-іл, н-гекс-2-ин-5-іл, н-гекс-2-ин-6-іл, н-гекс-3ин-1-іл, н-гекс-3-ин-2-іл, 3-метил-пент-1-ин-1-іл, 3метил-пент-1-ин-3-іл, 3-метил-пент-1-ин-4-іл, 3метил-пент-1-ин-5-іл, 4-метил-пент-1-ин-1-іл, 4метил-пент-2-ин-4-іл або 4-метил-пент-2-ин-5-іл. Переважно багатократні зв'язки алкенільних або алкінільних залишків не повинні бути присутніми в α-положенні відносно карбонілвуглецю, тому що внаслідок цього має місце негативний вплив на селективність реакції (стадія способу (а)) і, в разі необхідності, потрібно очищення реактора. Електрони, що зміщують, і/або об'ємні залишки, такі, як трет.-бутил, можуть позитивно впливати на селективність. Як замісники вищенаведених залишків R1 придатні, крім кетонів або альдегідів, у принципі всі замісники, наприклад, один або декілька таких замісників, як галоген, такий, як фтор, аміно, гідрокси, алкіл, циклоалкіл, арил, алкілокси, бензилокси, феніл або бензил. Як арилалкільні залишки слід навести розгалужені або нерозгалужені феніл-(С1-С5-алкіл)залишки або нафтил-(С1-С5-алкіл)-залишки, такі, як фенілметил, фенілетил, фенілпропіл, феніл-1метилетил, фенілбутил, феніл-1-метилпропіл, феніл-2-метилпропіл, феніл-1,1-диметилетил, фенілпентил, феніл-1-метилбутил, феніл-2-метилбутил, феніл-3-метилбутил, феніл-2,2-диметилпропіл, феніл-1-етилпропіл, нафтилметил, нафтилетил, нафтилпропіл, нафтил-1-метилетил, нафтилбутил, нафтил-1-метилпропіл, нафтил-2-метилпропіл, нафтил-1,1-диметилетил, нафтилпентил, нафтил1-метилбутил, нафтил-2-метилбутил, нафтил-3метилбутил, нафтил-2,2-диметилпропіл, або нафтил-1-етилпропіл, а також їх ізомерні або стереомерні форми. Кращими залишками є нерозгалужені або розгалужені феніл- (С1-С5-алкіл)-залишки, такі, як фенілметил, фенілетил або фенілпропіл. Як арильні залишки слід навести, наприклад, феніл, метоксифеніл або нафтил, або ароматичні кільця або кільцеві системи, що мають від 6 до 18 атомів вуглецю в кільцевій системі, а також до 24 інших атомів вуглецю, що можуть утворювати інші неароматичні кільця або кільцеві системи, що мають від 3 до 8 атомів вуглецю в кільці, що в разі необхідності можуть бути заміщені одним або декількома такими залишками, як галоген, наприклад, фтор, аміно, гідрокси, алкіл, алкілокси або іншими залишками. Кращий при цьому необов'язково заміщений феніл, метоксифеніл або нафтил. Як гетарил(алкільні) залишки слід назвати, наприклад, такі гетарилалкільні залишки, що містять один або декілька атомів азоту, сірки і/або кисню в кільці або кільцевій системі і зв'язані з розгалуженим або нерозгалуженим С 1-С5-алкіленовим ланцюгом, таким, як метилен, етилен, н-пропілен, 1метилетилен, н-бутилен, 1-метилпропілен, 2метилпро-пілен, 1,1-диметилетилен, н-пентилен, 1-метилбутилен, 2-метилбутилєн, 3-метилбутилен, 2,2-диметилпропілен або 1-етилпропілен. Як гетарильні залишки слід навести прості або конденсовані ароматичні кільцеві системи з одним або декількома гетероароматичними від 3- до 7членними кільцями, що можуть містити один або 12 декілька гетероатомів, таких, як Ν, Ο або S і необов'язково можуть бути заміщені одним або декількома залишками, такими, як галоген, такий, як фтор, аміно, гідрокси, тіо, алкіл, алкілокси або інші ароматичні або інші насичені або ненасичені неароматичні кільця або кільцеві системи. R2 означає в сполуках формул І, III, IV, VI, VII і IX заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10атомами вуглецю, алкеніл з 2-10 атомами вуглецю, алкініл з 2-10 атомами вуглецю, арилалкіл-, арил-, гетарилалкілабо гетарил-. Кращими залишками для R1 є заміщений або незаміщений, розгалужений або нерозгалуженийалкіл з 1-10 атомами вуглецю або арилалкіл. Як алкільні залишки слід навести заміщені або незаміщені, розгалужені або нерозгалужені С 1-С10алкільні ланцюги, як наприклад метил, етил, нпропіл, 1-метилетил, н-бутил, 1-метилпропіл-, 2метилпропіл, 1,1-диметилетил, н-пентил, 1метилбутил, 2-метилбутил, 3-метилбутил, 2,2диметилпропіл, 1-етилпропіл, н-гексил, 1,1диметилпропіл, 1,2-диметилпропіл, 1метилпентил, 2-метилпентил, 3-метилпентил, 4метилпентил, 1,1-диметилбутил, 1,2диметилбутил, 1,3-диметилбутил, 2,2диметилбутил, 2,3-диметилбутил, 3,3диметилбутил, 1-етилбутил, 2-етилбутил, 1,1,2триметилпропіл, 1,2,2-триметилпропіл, 1-етил-1метилпропіл, 1-етил-2-метилпропіл, н-гептил, ноктил, н-ноніл або н-децил. Кращими залишками є метил, етил або пропіл. Як алкенільні залишки слід навести розгалужені або нерозгалужені С 1-С10-алкенільні ланцюги, як наприклад, 2-пропеніл, 2-бутеніл, 3-бутеніл, 2метилпропеніл, 2-пентеніл, 3-пентеніл, 4-пентеніл, 1-метил-2-бутеніл, 2-метил-2-бутеніл, 3-метил-2бутеніл, 1-метил-3-бутеніл, 2-метил-3-бутеніл, 3мехил-3-бутеніл, 1,1-диметил-2-пропеніл, 1,2диметил-2-пропеніл, 1-етил-2-пропеніл, 2-гексеніл, 3-гексеніл, 4-гексеніл, 5-гексеніл, 1-метил-2пентеніл, 2-метил-2-пентеніл, 3-метил-2-пентеніл, 4-метил-2-пентеніл, 1-метил-3-пентеніл, 2-метил3-пентеніл, 3-метил-3-пентеніл, 4-метил-3пентеніл, 1-метил-4-пентеніл, 2-метил-4-пентеніл, 3-метил-4-пентеніл, 4-метил-4-пентеніл, 1,1диметил-2-бутеніл, 1,1-диметил-3-бутеніл, 1,2диметил-2-бутеніл, 1,2-диметил-3-бутеніл, 1,3диметил-2-бутеніл, 1,3-диметил-3-бутеніл, 2,2диметил-3-бутеніл, 2,3-диметил-2-бутеніл, 2,3диметил-3-бутеніл, 3,3-диметил-2-бутеніл, 1-етил2-бутеніл, 1-етил-3-бутеніл, 2-етил-2-бутеніл, 2етил-3-бутеніл, 1,1,2-триметил-2-пропеніл, 1-етил1-метил-2-пропеніл, 1-етил-2-метил-2-про-пенил, 2-гептеніл, 3-гептеніл, 4-гептеніл, 5-гептеніл, 6гептеніл, 2-октеніл, 3-октеніл, 4-октеніл, 5-октеніл, 6-октеніл, 7-октеніл, ноненіл або декеніл. Кращими залишками є 2-пропеніл або 2-бутеніл. Як алкінільні залишки слід назвати розгалужені або нерозгалужені С 3-С10-алкінільні ланцюги, як наприклад, проп-2-ін-1-іл, н-бут-1-ин-3-іл, н-бут-1ин-4-іл, н-пент-1-ин-3-іл, н-пент-1-ин-4-іл, н-пент-1ин-5-іл, н-пент-2-ин-1-іл, н-пент-2-ин-4-іл, н-пент-2ин-5-іл, 3-метил-бут-1-ин-3-іл, 3-метил-бут-1-ин-4іл, н-гекс-1-ин-3-іл, н-гекс-1-ин-4-іл, н-гекс-1-ин-5 13 77651 іл, н-гекс-1-ин-6-іл, н-гекс-2-ин-1-іл, н-гекс-2-ин-4іл, н-гекс-2-ин-5-іл, н-гекс-2-ин-6-іл, н-гекс-3-ин-1іл, н-гекс-3-ин-2-іл, 3-метил-пент-1-ин-3-іл, 3метил-пент-1-ин-4-іл, 3-метил-пент-1-ин-5-іл, 4метил-пент-2-ин-4-іл або 4-метил-пент-2-ин-5-іл. Кращим залишком є проп-2-ін-1-іл. Як замісники вищенаведених залишків для R2 принципово придатні всі можливі замісники, наприклад, один або декілька таких замісників, як галоген, наприклад, фтор, аміно, гідрокси, алкіл, циклоалкіл, арил, алкілокси, бензилокси, феніл або бензил. Як арилалкільні залишки придатний феніл(апкіл з 1-5 атомами вуглецю)- або нафтил-(алкіл з 1-5 атомами вуглецю)-залишки з розгалуженими або нерозгалуженими ланцюгами, наприклад, фенілметил, фенілетил, фенілпропіл, феніл-1метилетил, фенілбутил, феніл-1-метилпропіл, феніл-2-метилпропіл, феніл-1,1-диметилетил, фенілпентил, феніл-1-метилбутил, феніл-2-метилбутил, феніл-3-метилбутил, феніл-2,2-диметилпропіл, феніл-1-етилпропіл, нафтилметил, нафтилетил, нафтилпропіл, нафтил-1-метилетил, нафтилбутил, нафтил-1-метилпропіл, нафтил-2-метилпропіл, нафтил-1,1-диметилетил, нафтилпентил, нафтил1-метилбутил, нафтил-2-метилбутил, нафтил-3метилбутил, нафтил-2,2-диметилпропіл, або нафтил-1-етилпропіл, а також їх ізомерні або стереоізомерні форми. Кращими залишками є фенілметил-, фенілетил- або нафтилметил. Як арильні залишки слід назвати, наприклад, феніл, метоксифеніл або нафтил, або ароматичні кільця або кільцеві системи, що мають від б до 18 атомів вуглецю в кільцевій системі, а також до 24 інших атомів вуглецю, що можуть утворювати інші неароматичні кільця або кільцеві системи, що мають від 3 до 8 атомів вуглецю в кільці, що необов'язково можуть бути заміщені одним або декількома залишками, такими, як галоген, наприклад, фтор, аміно, гідрокси, алкіл, алкілокси або інші залишки. Кращі при цьому необов'язково заміщені феніл, метоксифеніл або нафтил. Як гетарил(алкіл)-залишки придатні, наприклад, гетарилалкільні залишки, що містять один або декілька атомів азоту, сірки і/або кисню в кільці або в кільцевій системі і зв'язані з одним або декількома розгалуженими або нерозгалуженими С1-С5-алкіленовими ланцюгами, наприклад, такими, як метилен, етилен, н-пропілен, 1метилетилен, н-бутилен, 1-метилпропілен, 2метилпропілен, 1,1-диметилетилен, н-пентилен, 1метилбутилен, 2-метилбутилен, 3-метилбутилен, 2,2-диметилпропілен або 1-етилпропілен. Як гетарильні залишки слід навести прості або конденсовані ароматичні кільцеві системи з одним або декількома гетероароматичними від 3- до 7членними кільцями, що можуть містити один або декілька гетероатомів, таких, як Ν, Ο або S, і які необов'язково можуть бути заміщені одним або декількома залишками, такими, як галоген, наприклад, фтор, аміно, гідрокси, тіо, алкіл, алкілокси або іншими ароматичними або іншими насиченими або ненасиченими неароматичними кільцями або кільцевими системами. 14 R3 означає в сполуках формул І, V, VI, VII і IX водень, гідрокси-, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю, алкеніл з 3-10 атомами вуглецю або алкініл з 3-10 атомами вуглецю. Кращими залишками є водень або гідроксил. Як алкільні залишки слід навести заміщені або незаміщені, розгалужені або нерозгалужені С 1-С10алкільні ланцюги, наприклад, метил, етил, нпропіл, 1-метилетил, н-бутил, 1-метилпропіл-, 2метилпропіл, 1,1-диметилетил, н-пентил, 1метилбутил, 2-метилбутил, 3-метилбутил, 2,2диметил пропіл, 1-етилпропіл, н-гексил, 1,1диметилпропіл, 1,2-диметилпропіл, 1метилпентил, 2-метилпентил, 3-метилпентил, 4метилпентил, 1,1-диметилбутил, 1,2диметилбутил, 1,3-диметилбутил, 2,2диметилбутил, 2,3-диметилбутил, 3,3диметилбутил, 1-етилбутил, 2-етилбутил, 1,1,2триметилпропіл, 1,2,2-триметилпропіл, 1-етил-1метилпропіл, 1-етил-2-метилпропіл, н-гептил, ноктил, н-ноніл або н-децил. Кращими залишками є метил, етил або пропіл. Як алкенільні залишки слід навести розгалужені або нерозгалужені С 3-С10-алкенільні ланцюги, наприклад, пропеніл, 2-бутеніл, 3-бутеніл, 2метилпропеніл, 2-пентеніл, 3-пентеніл, 4-пентеніл, 1-метил-2-бутеніл, 2-метил-2-бутеніл, 3-метил-2бутеніл, 1-метил-3-бутеніл, 2-метил-3-бутеніл, 3метил-3-бутеніл, 1,1-диметил-2-пропеніл, 1,2диметил-2-пропеніл, 1-етил-2-пропеніл, 2-гексеніл, 3-гексеніл, 4-гексеніл, 5-гексеніл, 1-метил-2пентеніл, 2-метил-2-пентеніл, 3-метил-2-пентеніл, 4-метил-2-пентеніл, 1-метил-3-пентеніл, 2-метил3-пентеніл, 3-метил-3-пентеніл, 4-метил-3пентеніл, 1-метил-4-пентеніл, 2-метил-4-пентеніл, 3-метил-4-пентеніл, 4-метил-4-пентеніл, 1,1диметил-2-бутеніл, 1,1-диметил-3-бутеніл, 1,2диметил-2-бутеніл, 1,2-диметил-3-бутеніл, 1,3диметил-2-бутеніл, 1,3-диметил-3-бутеніл, 2,2диметил-3-бутеніл, 2,3-диметил-2-бутеніл, 2,3диметил-3-бутеніл, 3,3-диметил-2-бутеніл, 1-етил2-бутеніл, 1-етил-3-бутеніл, 2-етил-2-бутеніл, 2етил-3-буте-ніл, 1,1,2-триметил-2-пропеніл, 1етил-1-метил-2-пропеніл, 1-етил-2-метил-2пропеніл, 2-гептеніл, 3-гептеніл, 4-гептеніл, 5гептеніл, 6-гептеніл, 2-октеніл, 3-октеніл, 4-октеніл, 5-октеніл, 6-октеніл, 7-октеніл, ноненіл або декеніл. Як алкінільні залишки придатні розгалужені або нерозгалужені С 3-С10-алкінільні ланцюги, як наприклад, проп-2-ін-1-іл, н-бут-1-ин-З-іл, н-бут-1ин-4-іл, н-бут-2-ин-1-іл, н-пент-1-ин-3-іл, н-пент-1ин-4-іл, н-пент-1-ин-5-іл, н-пент-2-ин-1-іл, н-пент-2ин-4-іл, н-пент-2-ин-5-іл, 3-метил-бут-1-ин-3-іл, 3метил-бут-1-ин-4-іл, н-гекс-1-ин-3-іл, н-гекс-1-ин-4іл, н-гекс-1-ин-5-іл, н-гекс-1-ин-6-іл, н-гекс-2-ин-1іл, н-гекс-2-ин-4-іл, н-гекс-2-ин-5-іл, н-гекс-2-ин-6іл, н-гекс-3-ин-1-іл, н-гекс-3-ин-2-іл, 3-метил-пент1-ин-3-іл, 3-метил-пент-1-ин-4-іл, 3-метил-пент-1ин-5-іл, 4-метил-пент-2-ин-4-іл або 4-метил-пент-2ин-5-іл. Як замісники вищенаведених залишків R3 у принципі придатні всі замісники, наприклад, один або декілька таких замісників, як галоген, напри 15 77651 клад, фтор, аміно, гідрокси, алкіл, циклоалкіл, арил, алкілокси, бензилокси, феніл або бензил. R4 означає в сполуках формул VIII заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю. Як алкільні залишки слід навести заміщені або незаміщені, розгалужені або нерозгалужені С 1-С10алкільні ланцюги, як наприклад, метил, етил, нпропіл, 1-метилетил, н-бутил, 1-метилпропіл-, 2метилпропіл, 1,1-диметилетил, н-пентил, 1метилбутил, 2-метилбутил, 3-метил бутил, 2,2диметилпропіл, 1-етилпропіл, н-гексил, 1,1диметил пропіл, 1,2-диметилпропіл, 1метилпентил, 2-метилпентил, 3-метилпентил, 4метилпентил, 1,1-диметилбутил, 1,2диметилбутил, 1,3-диметилбутил, 2,2диметилбутил, 2,3-диметилбутил, 3,3диметилбутил, 1-етилбутил, 2-етилбутил, 1,1,2триметилпропіл, 1,2,2-триметилпропіл, 1-етил-1метилпропіл, 1-етил-2-метилпропіл, н-гептил, ноктил, н-ноніл або н-децил. Перевага віддається при цьому таким залишкам, як метил, етил, 1метилетил, пропіл, бутил або пентил. Як замісники наведених залишків для R4 в принципі придатні всі замісники, наприклад, один або декілька таких замісників, як галоген, наприклад, фтор, хлор або бром, ціано, нітро, аміно, гідрокси, алкіл, циклоалкіл, арил, алкілокси, бензилокси, феніл або бензил. Кращими замісниками є при цьому галоген, наприклад, хлор або бром, ціано, бензилокси, алкіл з 1-4 атомами вуглецю або гідрокси. R5 означає в сполуках формул VIII або IX водень, заміщенийабо незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю. Як алкільні залишки слід навести заміщені або незаміщені, розгалужені або нерозгапужені С 1-С10алкільні ланцюги, наприклад, такі, як метил, етил, н-пропіл, 1-метилетил, н-бутил, 1-метилпропіл-, 2метилпропіл, 1,1-диметилетил, н-пентил, 1метилбутил, 2-метилбутил, 3-метилбутил, 2,2диметилпропіл, 1-етилпропіл, н-гексил, 1,1диметилпропіл, 1,2-диметилпропіл, 1метилпентил, 2-метилпентил, 3-метилпентил, 4метилпентил, 1,1-диметилбутил, 1,2диметилбутил, 1,3-диметилбутил, 2,2диметилбутил, 2,3-диметилбутил, 3,3диметилбутил, 1-етилбутил, 2-етилбутил, 1,1,2триметилпропіл, 1,2,2-триметилпропіл, 1-етил-1метилпропіл, 1-етил-2-метилпропіл, н-гептил, ноктил, н-ноніл або н-децил. Кращими залишками є водень, метил, етил або пропіл. Як замісники вищенаведених залишків для R5 придатні в принципі всі замісники, наприклад, один або декілька таких замісників, як галоген, наприклад, фтор, хлор або бром, ціано, нітро, аміно, гідрокси, алкіл, циклоалкіл, арил, алкілокси, бензилокси, феніл або бензил. R6 означає в сполуках формул VIII і IX водень, заміщений або незаміщений, розгалужений або нерозгалужений алкіл з 1-10 атомами вуглецю або заміщений або незаміщений феніл. 16 Як алкільні залишки придатні при цьому заміщені або незаміщені, розгалужені або нерозгалужені С1-С10-алкільні ланцюги, наприклад такі, як метил, етил, н-пропіл, 1-метилетил, н-бутил, 1метилпропіл-, 2-метилпропіл, 1,1-диметилетил, нпентил, 1-метилбутил, 2-метилбутил, 3метилбутил, 2,2-диметилпропіл, 1-етилпропіл, нгексил, 1,1-диметилпропіл, 1,2-диметилпропіл, 1метилпентил, 2-метилпентил, 3-метилпентил, 4метилпентил, 1,1-диметилбутил, 1,2диметилбутил, 1,3-диметилбутил, 2,2диметилбутил, 2,3-диметилбутил, 3,3диметилбутил, 1-етилбутил, 2-етилбутил, 1,1,2триметилпропіл, 1,2,2-триметилпропіл, 1-етил-1метилпропіл, 1-етил-2-метилпропіл, н-гептил, ноктил, н-ноніл або н-децил. Кращими залишками є метил, етил або пропіл. Як замісники вищенаведених залишків для R6 придатні в принципі всі замісники, наприклад, один або декілька таких замісників, як галоген, наприклад, фтор, хлор або бром, ціано, нітро, аміно, гідрокси, алкіл, циклоалкіл, арил, алкілокси, бензилокси, феніл або бензил. Далі винахід стосується способу одержання сполук загальної формули VII VII який відрізняється тим, що він включає наступні стадії: а) взаємодію сполук загальної формули II ІI з сполуками формули III R2 - XH ІII в присутності основи з одержанням сполук загальної формули IV ІV б) взаємодію реакційної суміші сполук формули IV зі сполукою загальної формули V NH2R3 V з одержанням сполук загальної формули VI VI в) гідрування сполуки загальної формули VI з одержанням сполук загальної формули VII в присутності каталізатора гідрування, причому замісники в формулах II, III, IV, V, VI і VII мають значення, наведені в п. 1 формули винаходу. Схема І показує спосіб за винаходом для кращої наочності як приклад здійснення. 17 77651 Стадії (а) до (г) відповідають способу одержання функціоналізованих оптично активних амінів, наприклад, оптично активних аміноспиртів або оптично активних діамінів. Стадії способу (а) до (в) відповідають способу одержання функціоналізованих, рацемічних амінів, що після цього можуть піддаватися реакції розщеплення рацематів. На схемі І це розщеплення рацематів показане на прикладі ферментативного розщеплення рацематів. Воно може здійснюватися також і іншими способами розщеплення рацематів, як наприклад, класичним розщепленням рацематів діастереомерними солями або хроматографічними способами. Показані на схемі І замісники мають вищенаведене значення. Схема показує, крім того, оптимальну можливість нейтралізації отриманого на стадії (а) реакційного розчину перед взаємодією зі сполуками загальної формули NH2R3 (V). Якщо сполуки загальної формули R2-XH (III) застосовують з великим надлишком у перерахуванні на реагент (II), то нейтралізація реакційного розчину потрібна перед наступною реакцією взаємодії, тому що інакше при об'єднанні надлишкової сполуки R2-XH може виникати небажане зворотне розщеплення продукту реакції. Це призводить до втрат виходу цільового продукту і вимагає очищення продукту. При застосуванні кращих для винаходу кількостей сполуки (III) від 0,5 до 2,5 еквівалентів, переважно від 0,5 до 2,0; особливо переважно від 0,7 до 1,5; і 18 зокрема від 0,9 до 1,1 еквівалентів у перерахуванні на реагент (II) не потрібно об'єднання і нейтралізації реакційного розчину перед стадією (б). Вона, однак, може переважно здійснюватися в залежності від вихідного продукту, щоб підвищити надійність способу. Для нейтралізації можуть застосовуватися всі можливі мінеральні кислоти, такі, як НСІ, H2SO4 або Н3РО4 або органічні кислоти, як наприклад, низькі аліфатичні карбонові кислоти, такі, як мурашина кислота. Переважно застосовують ортофосфорну кислоту. Як основа для способу за винаходом на стадії (а) придатні в принципі всі основи, що можуть каталізувати приєднання сполуки (III), по Міхаелю, до сполуки (II), такі, як NaOH, КОН, третинні аміни або алкоголяти лужних і лужноземельних металів. Як кращі основи слід навести, наприклад, такі алкоголяти лужних і лужноземельних металів, як метанолят натрію, етанолят натрію, бутанолят натрію, трет.-бутанолят натрію, трет.-бутанолят калію або сильні основні аміни, такі, як діазабіциклоундецен. Основу як каталізатор застосовують в концентрації від 0,001 до 10мол.%, переважно, від 0,01 до 5мол.%, особливо переважно від 0,3 до 0,5мол.% у перерахуванні на сполуку (III), що застосовується. Стадія (а) способу може проводитися в присутності інертного за умов реакції, апротонного розчинника. Прикладами такого розчинника є вуглеводні, такі, як гексан, циклогексан, бензол або толуол або прості ефіри, наприклад, метилтрет.бутиловий ефір, діетиловий спирт, дибутиловий ефір або тетрагідрофуран. Переважно реакцію проводять в відсутності розчинника. Реакцію [стадію (а) способу] проводять переважно при температурі від -30 до +50°С, переважно від -5 до +10°С. Кращими сполуками загальної формули (V) є аміак, первинні і вторинні аліфатичні аміни і гідроксиламін. Переважно стадія (б) способу за винаходом проводиться з гідроксиламіном, що застосовується як водяний розчин або як водяний розчин своєї солі, як наприклад, гідроксиламін гідрохлорид, гідроксиламін-сульфат. У разі необхідності як і інші сполуки формули (V) в присутності основи, такої, як натрієвий луг або ацетат натрію. Переважно застосовують водяний розчин вільного гідроксиламіну. Реакцію можна здійснювати в інертному, протонному розчиннику, такому, як вода або спирт, такий, як метанол, етанол, пропанол, бутанол або ізо-бутанол. Переважно реакцію проводять в воді. Реакцію [стадію (б)] проводять переважно при температурі від 0 до +100°С, переважно від 20 до 40°С. Гідрування за способом за винаходом [стадію (в) способу] можна проводити зі звичайними каталізаторами гідрування, наприклад, на базі Ni, Co, Hg, Pt, Pd, Ru або Rh. Звичайний каталізатор такий, що застосовується для гомогенного, являє собою, наприклад, каталізатор Вілкінсона. Гідрування може здійснюватися в гетерогенному або гомогенному каталізі. З економічних міркувань і внаслідок гарної доступності як каталізатора від 19 77651 дають перевагу каталізатору нікелю Ренея. Пдрування проводять переважно в інертному до умов реакції розчиннику. Подібні розчинники являють собою, наприклад, вуглеводні, такі, як гексан, циклогексан, бензол або толуол, прості ефіри, наприклад, метилтрет.-бутиловий ефір, діетиловий спирт, дибутиловий ефір або тетрагідрофуран. Або ж спирти, такі, як метанол, етанол, пропанол, бутанол або ізо-бутанол. Переважно застосовують як розчинник тетрагідрофуран або метанол. Реакцію [стадію (в) способу] проводять переважно при температурі від 0 до +150°С, переважно, від 50 до 100°С. Гідрування звичайне здійснюють при тиску в діапазоні від нормального тиску до 300х105Па. Переважно реакцію проводять при тиску (50-150)х105Па. Розщеплення рацематів може здійснюватися як описано вище ферментативним розщепленням рацематів або класичним хімічним розщепленням, також можна застосовувати і хроматографічні способи. Кращим є при цьому розщеплення рацематів за допомогою ферментів або діадтереомерних солей, зокрема, перевага віддається ферментативному розщепленню рацематів. Для відділення діастереомерними солями придатні в принципі всі оптично активні карбонові солі. Кращими оптично активними карбоновими солями є винна кислота, ди-бензоїлвинна кислота, мигдальна кислота, камфорна кислота, камфорсульфонова кислота, п-гідрокси-мигдальна кислота, п-СІ-мигдальна кислота, феноксипропіонова кислота, п-гідрокси-фенокси-пропіонова кислота або молочна кислота. Кращою для розщеплення рацематів є мигдальна кислота. Утворення солі може здійснюватися в інертному розчиннику, такому, як наприклад, вуглеводень, такий, як гексан, циклогексан, бензол або толуол; або в простому ефірі, такому, як метилтрет.-бутиловий ефір, діетиловий спирт, дибутиловий ефір або тетрагідрофуран, або в спирті, наприклад такому, як метанол, етанол, пропанол, ізо-пропанол, бутанол або ізобутанол. Для перекристалізації використовують доцільним чином спирт, наприклад, метанол, етанол, пропанол, ізо-пропанол, бутанол або ізобутанол. Переважно застосовують ізо-пропанол. Для поліпшення кристалізації розчин може охолоджуватися. В тому випадку, якщо сіль, що утворилася, випадає, нагріванням вона повертається в розчин і повільно при охолодженні знову викристалізовується. В тому випадку, якщо потрібно, кристалізацію можна проводити декілька разів. Розщеплення рацематів функціоналізованих амінів може проводитися за допомогою ферментів, таких, як естераза або ліпаза. Як ліпази і естерази для способу за винаходом придатні в принципі всі естерази і ліпази, що одержуються з рослин, тварин або мікроорганізмів. Перевагу дає застосування мікробіологічних ліпаз, які можна виділяти, наприклад, з еукаріотних організмів, таких, як гриби або дріжджі або прокаріотних організмів, таких, як бактерії. Особливо добре придатні бактеріальні ліпази з Bacillus або Pseudomonas, наприклад, Amano P або ліпаза з Pseudomonas spec. DSM 8246 або ліпази з грибів, таких, як Aspergillus або з дріжджів, таких, як 20 Candida або Yerrowia. іншими придатними ліпазами є ферменти, що поставляються фірмою Novo Nordisk, зокрема ліпази SP 523, SP 524, SP 525, SP 526 і Novozym ® 435, що одержуються з дріжджів, наприклад, з Candida antarctica. Іншими прикладами можуть бути ліпази Chirazyme L1, L2, L3, L4, L5, L6, L7 і L8, що поставляються фірмою Roche Molecular Biochemicals Roche Diagnostic, GmbH, Penzberg. Ліпази можуть застосовуватися в нативній або імобілізованій формі. Імобілізовані ліпази можуть бути мікрокапсульовані, емульговані передполімеризатами і полімеризовані, зшиті біфункціональними речовинами (олігомерами, альдегідами і т.п.) або зв'язані з органічними або неорганічними матеріалами носіями, наприклад, такими, як целіт, леватит, цеоліт, полісахариди, поліаміди або полістирольні смоли. Особливо кращі ліпази Novozym ® 435 і Chirazyme L2. Реакція з естеразами або ліпазами проводиться взагалі при атмосферному тиску. В разі необхідності, під інертним газом, наприклад, азотом або аргоном. Вона може здійснюватися також і при підвищеному тиску. Температура при взаємодії рацемічних амінів формули VII з придатними для розщеплення рацематів складними ефірами, що в альфаположенні до карбонілвуглецю мають атом кисню, спеціально з складними ефірами загальної формули VIII VIІІ звичайно складає від 0 до 90°С, переважно, від 10 до 60°С, особливо переважно, від 20 до 50°С. Замісники кращих складних ефірів формули VIII мають вищенаведене значення. Взаємодію складного ефіру з рацемічним, функціоналізованим аміном, тобто з відповідним аміноспиртом або діаміном при ферментативному каталізі проводять звичайно при кімнатній температурі. Час реакції складає в залежності від вихідної речовини від 1 до 48год. Вторинні аміноспирти, відповідно, діаміни, як правило, вимагають більш тривалого часу .реакції, ніж первинні аміни і діаміни. Менша реакційна здатність вторинних амінів може компенсуватися більш високою кількістю каталізатора в порівнянні з первинними амінами. На моль рацемічного аміну застосовують переважно від 0,5 до 2,0моль, переважно від 0,5 до 1,0моля складного ефіру. Необхідна кількість ферменту залежить від активності препаративної форми ферменту і від реакційної здатності аміну і може легко визначатися за допомогою попередніх досліджень. Як правило, застосовують від 0,1 до 10мас.%, переважно, від 1 до 5мас.% (мобілізованої препаративної форми ферменту (в перерахуванні на рацемічний амін). Novozym ® 435 має активність приблизно 7000-10000(PL U)/г, де (PL U) пропіллауратні одиниці (одиниці в перерахуванні на пропіллаурат як субстрат). Кількість ферменту, що подається залежить від виду ферменту і від активності препаративної форми ферменту. Оптимальна для реакції кіль 21 77651 кість ферменту може легко визначатися простими попередніми дослідженнями. Хід реакції можна легко прослідкувати звичайними методами, наприклад, хроматографією або рідинною хроматографією високого тиску. Якщо бажаний вихід, як правило 50%, досягнутий, реакцію закінчують переважно видаленням каталізатора, наприклад, відфільтровуванням ферменту. Реакцію можна зупиняти також і за допомогою добавки речовин, що руйнують фермент, таких, як кислоти або луги або за допомогою нагрівання. При безперервному режимі реакцію взаємодії можна регулювати через навантаження ферменту, тобто кількості аміну, що в одиницю часу прокачують через реактор ферменту. Спосіб може проводитися переважно безперервно, однак, він може проводитися періодично або напівбезперервно. Розщеплення рацематів, каталізоване ферментом, може здійснюватися як у протонному або апротонному розчиннику, так і без розчинника. Придатними розчинниками можуть бути, наприклад, вугле водні, такі, як гексан, циклогексан або толуол, простий ефір, наприклад, діетиловий спирт, діоксан, метилтрет.-бутиловий ефір, трет.амілметиловий ефір або тетрагідрофуран, нітрили, такі, як ацетонітрил, бутиронітрил, спирти, такі, як трет.-бутанол, 3-метил-3-пентанол, і галогеновані вугле водні, наприклад, метиленхлорид. Реакція проходить особливо добре тоді, коли розчинник і вихідні речовини є по можливості безводними. Перевагою для розщеплення рацематів є те, що розчинники і вихідні речовини амін і складний ефір осушені. Це може здійснюватися відомим фахівцю в даній області методом, наприклад, азеотропним сушінням або сушінням такими засобами, що осушують, як сульфат натрію, сульфат магнію, гідроокис калію, фосфорпентоксид, молекулярне сито, силікагель або окис алюмінію. Наприкінці каталізованого ферментом розщеплення рацематів є в наявності суміш з ацильованого енантіомера аміну загальної формули IX ІХ неперетвореного енантіомера аміну, що вивільнився при ацилюванні з складного ефіру спирту і можливо застосованого в надлишку складного ефіру. Для поділу цієї суміші придатні особливо дистилятивні й екстрактивні способи. Так наприклад, низькокиплячі аміни можуть безпосередньо відганятися з реакційної суміші. Амід може бути потім відділений від спирту і, в разі необхідності, від складного ефіру відгонкою або екстракцією і потім може гідрапізуватися звичайним чином, наприклад, кип'ятінням з натрієвим і калієвим лугом з рацемізацією або ж без рацемізації [US, 5905167]. Патент [US, 5905167] описує в стовпцях 2 до 5 і в прикладі 2 спосіб розщеплення амідів з одержанням стереоцентрів. Утворений при гідролізі другий енантіомер аміну може відокремлюватися від на 22 явної в формі солі карбонової кислоти дистиляцією або екстракцією. Це відбувається переважно екстракцією, причому як агент екстракції застосовується простий ефір, наприклад, діетиловий спирт, метил-трет.-бутиловий ефір і дибутиловий ефір, галогеновані вуглеводні, наприклад, дихлорметан або трихлоретилен або вуглеводні, наприклад, пентан, гексан, циклогексан, бензол, толуол і ксилол. Кращою формою проведення виділення аміну є перегонка з водяною парою. Особливо придатна форма виконання винаходу полягає в тому, що розщеплення проводять при такій високій температурі, що отриманий продукт реакції (амін) переганяється з водяною парою і відразу віддаляється з реакційної суміші, в той час як кислота, що при лужних умовах дисоційована, залишається в реакційній суміші. Таким чином можуть перероблятися аміни в способах за винаходом. Отриманий вільний амін може застосовуватися як цінний продукт для подальшого синтезу або ж після рацемізації може повертатися в процес на стадію (г). Також і безпосередньо розщеплений при рацемізації амід може повертатися на цю стадію процесу. Таким чином, теоретично весь рацемат може переводитися в бажаний енантіомер. Така рацемізація може здійснюватися під такими ж умовами, при яких одержують аміни або кетони, ("відбудовне амінування"). Утворена при гідролізі кислота може регенуватися після підкислення розчину гідролізу переважно екстракцією і відповідно до звичайних способів етерифіцикації і рекуперації. Переважно способи за винаходом придатні для одержання рацемічних аміноспиртів загальної формули Іс, Іc а також до їх розщеплення рацематів за допомогою енантіоселективного ацилування, причому замісники мають вищенаведене значення. Далі винахід стосується сполук формул І, VII і IX: І VII ІХ в яких замісники мають вищенаведені значення. Кращі сполуки формул І, VII і IX являють собою наступні сполуки: 23 Способи за винаходом не тільки придатні як способи одержання оптично активних первинних і вторинних функціоналізованих амінів, таких, як аміноспирти або діаміни, але і можуть бути компонентами складного хімічного або багатостадійного синтезу, наприклад, при одержанні лікарських діючих речовин або засобів захисту рослин. Наступні приклади служать для пояснення винаходу. Приклади Приклад 1. Стадії способу (а) і (б) Синтез 1-бензилокси-З-бутаноноксиму (схема III) 648г (6,0моль) бензилового спирту змішують при 0°С з 2,6г (24ммоль) трет.-бутаноляту калію і перемішують протягом 30хв. Протягом 30хв. додають краплями 441г (6,3моль) свіжедистильованого метил-вінілкетону. Охолодженням температуру утримують при 0-10°С. Після закінчення подачі реакційну суміш перемішують ще протягом 1,0год. при 10°С. Після цього додають краплями 2,8г (24ммоль) ортофосфорної кислоти (в якості 77651 24 85% водяного розчину). Суміш нагрівають до кімнатної температури (~23°С).За даними спектроскопії 1Н-ЯМР при реакції одержують 1-бензилокси-3-бутанон 1 Н-ЯМР: d=2,05 (s; 3Н), 2,60 (t, J=7,0Hz; 2H), 3,65 (t, J=7,0Hz; 2H), 4,45 (s, 2H), 7,25 (m, 5H). До сирого 1-бензилокси-3-бутанону додають краплями при сильному перемішуванні 471г 51,7% водяного розчину (7,37моль) гідроксиламіну таким чином, що температура реакції залишається приблизно при 35°С. Після цього реакційну суміш перемішують ще 15год. На др угий день відокремлюють верхню водяну фазу, нижню органічну фазу завантажують в 500мл толуолу і нагрівають в водовіддільнику доти, поки більше не утвориться води. Розчинник і летучі компоненти відганяють при 0,5мм (температура ванни: 100°С), як залишок залишається 1100г (95%) 1-бензилокси-3бутаноноксиму в якості E/Z-суміші. Головний ізомер (приблизно 65%): 1 Н-ЯМР: d=1,90 (s; 3Н), 2,50 (t, J=7,0Hz; 2H), 3,65 (t, J=7,0Hz; 2H), 4,50 (s, 2H), 7,30 (m, 5H), 9,30 (s, шир., 1Н). Ізомер малої кількості (близько 35%): 1 Н-ЯМР: d=1,95 (s; 3Н), 2,75 (t, J=7,0Hz; 2H), 3,65 (t, J=7,0 Hz; 2H), 4,50 (s, 2H), 7,30 (m, 5H), 9,30(s, шир., 1Н). Приклад 2. Гідрування з одержанням 1бензилокси-З-амінобутану (рацемічного ВОВА) [стадія способу (с), схема IV] В автоклав подають 100г нікелю Ренея в 300мл тетрагідрофурану і змішують з розчином 850г (4,4моль) 1-бензилокси-3-бутанооксиму в 2,5л тетрагідрофурану. В автоклаві встановлюють тиск водню в 100х105Па і при перемішуванні нагрівають до 80°С. При цьому починається екзотермічна реакція, за допомогою наступного дозування водневого газу тиск утримують постійним. Після закінчення поглинання водню тиск підвищують до 150х105Па і перемішують ще протягом 4год. Після цього реакційну суміш охолоджують, мішалку виключають і декантують каталізатор. Злегка мутний реакційний розчин фільтрують над силікагелем і прозорим фільтратом звільняють від розчинника в ротаційному випарнику. Важколетучий залишок фракціонують в вакуумі масляного насоса і дистилюють. При 1,3мм (85-87°С) продукт переходить в рацемічний R- і S-1-бензилокси-3-амінобутан (ВОВА) у вигляді прозорої рідини. Вихід складає 646г (83%) 1 Н-ЯМР: d=1,05 (d, J=7H z; 3H), 1,35 (s, шир; 2H), 1,65 (mс; 2H), 3,10 (mс; 1H), 3,55 (mс; 2H), 4,50 (s, 2H), 7,30 (m, 5H). Приклад 3. Розщеплення рацематів [стадія способу (г)] А. Енантіомерна аналітика R- і S-1бензилокси-3-амінобутану (ВОВА): Дериватизація (схема V): 0,5г аміну розчиняють в 25мл діетилового спирту. Розчин охолоджують до 0°С і за один раз 25 77651 додають 0,2мл бензоїлхлориду. Реакційну суміш перемішують при кімнатній температурі протягом 30 хвилин і потім змішують з 10мл води. Водяну фазу відокремлюють і верхню органічну фазу промивають послідовно щораз за допомогою 10мл 10% соляної кислоти, водою і насиченим розчином гідрокарбонату натрію. Реакційну суміш сушать над сульфатом натрію. Потім беруть 1мл розчину, розбавляють за допомогою 5мл н-гексану й аналізують рідинною хроматографією високого тиску. Схема V: Дериватизація Колона: Температура: Детектор: Кількість, що впорскується: Розчинник: Плинність: 26 Відповідно до аналізу ЖХВД S-1-бензилокси3-амінобутан (S-BOBA) мав значення ізомерів у 50,5%. Після цього сіль, що випала, ще раз перекристапізовують з 100мл ізопропанолу. На закінчення амін вивільняють з солі, що утворилася, за допомогою обробки за допомогою 10мл 50% натрієвого лугу, екстрагують за допомогою 50мл простого ефіру й екстракт концентрують. Одержують 2,2г (34%) S-1-бензилокси-3-амінобутану (SBOBA). Відповідно до аналізу ЖХВД чистота енантіомерів складає 90% ізомерів. Приклад 5. Розщеплення рацематів за допомогою каталізованого ферментом розщеплення рацематів Chiralcel OD Daicel Chemical Industries, Ltd. Кімнатна Абсорбція при 214нм 20мкл н-гексан/ізопропанол/етанол (300:50:0,8 об./об./об.) 1,3мл/хв. (при прибл. 40кг/см 2) Приклад 4. Розщеплення рацематів за допомогою кристалізації До розчину з 12,8г (71,5ммоль) рацемічного Rі S-1-бензилокси-3-амінобутану (ВОВА) в 70мл ізопропанолу додають краплями розчин з 2,15г (35,6ммоль) оцтової кислоти і 5,4г (35,6ммоль) Dмигдальної кислоти в 50мл ізопропанолу. Осад, що випав, нагріванням знову повертають в розчин і потім залишають на викристалізовування. З проби відсмоктаної солі вивільняють зв'язаний амін за допомогою обробки натрієвим лугом. 1500г (8,43моль) рацемічного R- і S-1бензилокси-3-амінобутану (рац. ВОВА) охолоджують до 0°С і змішують з 523г (3,96моль) складного ізопропілового ефіру метоксиоцтової кислоти. До реакційної суміші додають 75г Novozym 435® і при перемішуванні при кімнатній температурі (~23°С) нагрівають. Через 15год. відфільтровують каталізатор і промивають за допомогою 1л толуолу. Фільтрат звільняють в вакуумі від летучих компонентів і після цього реакційну суміш дистилюють в тонкошаровому випарнику (1,0х102Па, 180°С). Як дистилят у верхній частині колони присутній S-1бензилокси-3-амінобутан при (95-98°С), як важкокиплячий продукт в нижній частині колони присутній R-1-бензилокси-3-амінобутанамід. Одержують 802,5г (53%) S-1-бензилокси-3амінобутану (S-BOBA), що відповідно до аналізу ЖХВД має оптичну чистоту в 90% ізомерів. У нижній частині колони присутні 964г (45,5%) R-1-бензилокси-3-амінобутанамід (R-ВОВамід) (оптична чистота 98% ізомерів). R-ВОВамід, 1Н-ЯМР: d=1,20 (d, J=7Hz; 3Н), 1,65-1,95 (mс; 2Н), 3,15 (s; 3Н), 3,50-3,70 (mс; 2Н), 3,75 і 3,85 (АВ-система, JAB=10,5Hz; 2Н), 4,20 (mс; 1Н), 4,50 (s, 2Н), 6,90 (s, шир.; 1Н), 7,10-7,40 (m; 5Н). Приклад 6. Розщеплення R-BOBаміду 27 77651 Суміш з 918г (3,66моль) R-ВОВаміду і 900г триетаноламіну змішують при 120°С з 800г (10моль) 50% натрієвого лугу і перемішують протягом 3год. при цій температурі. Після охолодження реакційну суміш розбавляють за допомогою Комп’ютерна в ерстка В. Сердюк 28 1,5л води і три рази екстрагують щораз за допомогою 1л діетилового спирту. Зібрані екстракти промивають послідовно 1л води і 100мл насиченого розчину хлористого натрію, суша ть над сульфатом натрію і потім концентрують. Як залишок залишається 625г (95%) R-BOBA у вигляді злегка жовтого масла. Оптична чистота згідно ЖХВД складає 97% ізомерів. Підписне Тираж 26 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for producing optically active amines and optically active amide
Назва патенту російськоюСпособ получения оптически-активных аминов и оптически-активный амид
МПК / Мітки
МПК: C07C 209/86, C07C 235/08, C07C 215/00, C07B 57/00, C12P 41/00, C07C 209/58, C07C 213/00, C07C 217/10, C07B 55/00
Мітки: оптично-активний, одержання, спосіб, амід, оптично-активних, амінів
Код посилання
<a href="https://ua.patents.su/14-77651-sposib-oderzhannya-optichno-aktivnikh-aminiv-ta-optichno-aktivnijj-amid.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання оптично-активних амінів та оптично-активний амід</a>
Попередній патент: Комбінація інгібітора зворотного захоплення серотоніну та дерамциклану
Наступний патент: Підшипник кочення миколи загути (варіанти)
Випадковий патент: Плуг з вібраційною підвіскою