Спосіб отримання (3r,3as,6ar)-гексагідрофуро[2,3-b]фуран-3-іл(1s,2r)-3-[[(4-амінофеніл)сульфоніл](ізобутил)аміно]-1-бензил-2-гідроксипропілкарбамату
Номер патенту: 85567
Опубліковано: 10.02.2009
Автори: Зінсер Хартмут Бургхард, Ебєрт Біргіт М., Вігерінк Піт Том Берт Пауль, Гойваертс Ніколаас Марта Фелікс
Формула / Реферат
1. Спосіб отримання сполуки формули (6)
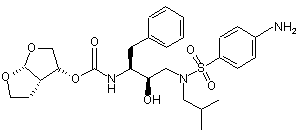 , (6)
, (6)
її солей приєднання, поліморфних і/або псевдополіморфних форм, який відрізняється тим,
що включає
(і) введення ізобутиламіногрупи в сполуку формули (1)
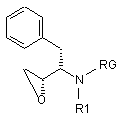 , (1)
, (1)
де
RG представляє амінозахисну групу;
R1 являє собою водень або С1-6-алкіл;
(іі) введення п-нітрофенілсульфонільної групи в сполуку, одержану на стадії (і);
(ііі) відновлення нітрогрупи сполуки, одержаної на стадії (іі);
(iv) видалення захисної групи зі сполуки, одержаної на стадії (ііі); і
(v) здійснення реакції сполучення сполуки, одержаної на стадії (iv), з (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3-ільним похідним.
2. Спосіб отримання сполуки формули (6) за п. 1, який відрізняється тим, що зазначений спосіб включає стадії:
введення ізобутиламіногрупи в сполуку формули (I¢)
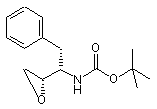 (I¢)
(I¢)
з утворенням сполуки формули (2¢)
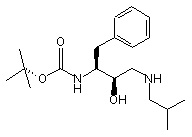 , (2')
, (2')
введення п-нітрофенілсульфонільної групи в сполуку формули (2¢) з утворенням сполуки формули (3¢)
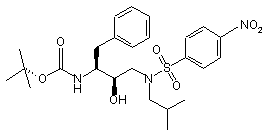 , (3')
, (3')
відновлення нітрогрупи сполуки формули (3¢) з утворенням сполуки формули (4¢)
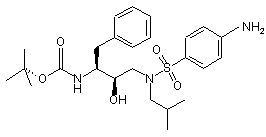 , (4')
, (4')
видалення захисної групи зі сполуки формули (4¢) з утворенням сполуки формули (5)
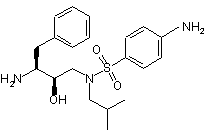 , (5)
, (5)
сполучення сполуки формули (5) з (3R,3aS,6aR)-гeкcaгiдpoфypo[2,3-b]фуран-3-ільним похідним з утворенням сполуки формули (6).
3. Спосіб за будь-яким з пп. 1, 2, де стадію (і) здійснюють у толуолі.
4. Спосіб за будь-яким з пп. 1-3, де стадію (іі) здійснюють у толуолі, етилацетаті, метиленхлориді, дихлорметані або тетрагідрофурані.
5. Спосіб за будь-яким з пп. 1-4, де стадію (ііі) здійснюють у присутності до 10 мол. % первинного або вторинного аміну, переважно етаноламіну, з паладієм-на-вугіллі в атмосфері водню.
6. Спосіб за будь-яким з пп. 1-5, де стадію (iv) здійснюють у кислому або лужному середовищі.
7. Спосіб за будь-яким з пп. 1-6, де сполуку формули (5) кристалізують, розчиняючи її в суміші розчинників, доводячи рН до величини більше 9 і підтримуючи концентрацію сполуки формули (5) у розчині на рівні від 4 % до 15 % (мас./мас.).
8. Спосіб за будь-яким з пп. 1-7, де сполуку формули (5) кристалізують при температурі від 0 °С до 10 °С.
9. Спосіб за будь-яким з пп. 7-8, де під час кристалізації додають зародкові кристали сполуки формули (5).
10. Спосіб за будь-яким із пп. 7-9, де суміш розчинників містить один або кілька розчинників, що змішуються з водою, і воду.
11. Спосіб за будь-яким з пп. 7-9, де суміш розчинників містить один або кілька розчинників, що не змішуються з водою, і воду.
12. Спосіб за п. 10, де суміш розчинників являє собою метанол, ізопропанол і воду у співвідношенні 1:6,5:8, відповідно.
13. Спосіб за будь-яким з пп. 1-12, де (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3-ол або його попередник перед сполученням зі сполукою формули (5) уводять у взаємодію з біс(4-нітрофеніл)карбонатом.
14. Спосіб за будь-яким з пп. 1-12, де (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3-ол або його попередник перед сполученням зі сполукою формули (5) уводять у взаємодію з дисукцинімідилкарбонатом.
15. Спосіб за пп. 13 або 14, де взаємодію (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3-олу або його попередника з похідним карбонової кислоти активують (аміном) основою, переважно триетиламіном або піридином.
16. Застосування сполуки формули (5), її солей приєднання, поліморфних і/або псевдополіморфних форм для одержання сполуки формули (6).
17. Застосування сполуки формули (5) за п. 16, де сполука формули (5) знаходиться у формі вільної основи.
18. Застосування сполуки за будь-яким з пп. 1-17 як проміжної сполуки для одержання сполуки формули (6).
Текст
1. Спосіб отримання сполуки формули (6) 3 85567 O O NH N H OH , (2') введення п-нітрофенілсульфонільної групи в сполуку формули (2¢) з утворенням сполуки формули (3¢) NO2 O O O N N H S O OH , (3') відновлення нітрогрупи сполуки формули (3¢) з утворенням сполуки формули (4¢) NH2 O O O N N H S O OH , (4') видалення захисної групи зі сполуки формули (4¢) з утворенням сполуки формули (5) NH2 O N H 2N S O OH , (5) сполучення сполуки формули (5) з (3R,3aS,6aR)-гeкcaгiдpoфypo[2,3-b]фуран-3-ільним похідним з утворенням сполуки формули (6). 3. Спосіб за будь-яким з пп. 1, 2, де стадію (і) здійснюють у толуолі. 4. Спосіб за будь-яким з пп. 1-3, де стадію Даний винахід відноситься до способу одержання (3R,3aS,6aR)-гексагідрофуро[2, 3-b]фуран3-іл(1S,2R)-3-[[(4амінофеніл)сульфоніл](ізобутил)аміно]-1-бензил-2гідроксипропілкарбамату, а також проміжних сполук для застосування у зазначеному способі. Зок 4 (іі) здійснюють у толуолі, етилацетаті, метиленхлориді, дихлорметані або тетрагідрофурані. 5. Спосіб за будь-яким з пп. 1-4, де стадію (ііі) здійснюють у присутності до 10 мол. % первинного або вторинного аміну, переважно етаноламіну, з паладієм-на-вугіллі в атмосфері водню. 6. Спосіб за будь-яким з пп. 1-5, де стадію (iv) здійснюють у кислому або лужному середовищі. 7. Спосіб за будь-яким з пп. 1-6, де сполуку формули (5) кристалізують, розчиняючи її в суміші розчинників, доводячи рН до величини більше 9 і підтримуючи концентрацію сполуки формули (5) у розчині на рівні від 4 % до 15 % (мас./мас.). 8. Спосіб за будь-яким з пп. 1-7, де сполуку формули (5) кристалізують при температурі від 0 °С до 10 °С. 9. Спосіб за будь-яким з пп. 7-8, де під час кристалізації додають зародкові кристали сполуки формули (5). 10. Спосіб за будь-яким із пп. 7-9, де суміш розчинників містить один або кілька розчинників, що змішуються з водою, і воду. 11. Спосіб за будь-яким з пп. 7-9, де суміш розчинників містить один або кілька розчинників, що не змішуються з водою, і воду. 12. Спосіб за п. 10, де суміш розчинників являє собою метанол, ізопропанол і воду у співвідношенні 1:6,5:8, відповідно. 13. Спосіб за будь-яким з пп. 1-12, де (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3-ол або його попередник перед сполученням зі сполукою формули (5) уводять у взаємодію з біс(4нітрофеніл)карбонатом. 14. Спосіб за будь-яким з пп. 1-12, де (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3-ол або його попередник перед сполученням зі сполукою формули (5) уводять у взаємодію з дисукцинімідилкарбонатом. 15. Спосіб за пп. 13 або 14, де взаємодію (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3-олу або його попередника з похідним карбонової кислоти активують (аміном) основою, переважно триетиламіном або піридином. 16. Застосування сполуки формули (5), її солей приєднання, поліморфних і/або псевдополіморфних форм для одержання сполуки формули (6). 17. Застосування сполуки формули (5) за п. 16, де сполука формули (5) знаходиться у формі вільної основи. 18. Застосування сполуки за будь-яким з пп. 1-17 як проміжної сполуки для одержання сполуки формули (6). рема, винахід відноситься до способів одержання (3R,3aS,6aR)-гексагідрофуро[2, 3-b]фypaн-3іл(1S,2R)-3-[[(4амінофеніл)сульфоніл](ізобутил)аміно]-1-бензил-2гідроксипропілкарбамату, які здійснюють із застосуванням проміжної сполуки 4-aмiнo-N-[(2R,3S)-3 5 85567 aмiнo-2-гiдpoкcи-4-фeнiлбyтил]-Niзoбyтилбeнзoлcyльфoнaмiдy, які можна застосовувати в промисловому масштабі. Вірус, що викликає синдром набутого імунодефіциту (СНІД), відомий під різними назвами, у тому числі, як Т-лімфоцитарний вірус III (HTLV-III) або лімфаденопатії-асоційований вірус (LAV) або вірус СНІДУ (ARV) або вірус імунодефіциту людини (ВІЛ). Дотепер ідентифіковані два різних сімейства, тобто, ВІЛ-1 і ВІЛ-2. Далі в описі абревіатура ВІЛ буде використовуватися для загального позначення таких вірусів. Одним з визначальних етапів у життєвому циклі ретровірусів є процессинг білків-попередників ретровірусною протеазою. Наприклад, під час циклу реплікації вірусу ВІЛ продукти транскрипції генів gag і gag-pol транслюються як білки, які потім процесуються кодованою вірусом протеазою з утворенням ферментів і структурних білків серцевини вірусу. Найчастіше білкипопередники gag процесуються в корові білки, а білки-попередники рol процесуються у вірусні ферменти, наприклад, зворотну транскриптазу та ретровірусну протеазу. Правильний процесинг білків-попередників ретровірусною протеазою необхідний для складання інфекційних віріонів, що, таким чином, робить ретровірусну протеазу привабливою мішенню для противірусної терапії. Зокрема, ВІЛ протеаза є привабливою мішенню для лікування ВІЛ. На ринку та у розробці є кілька інгібіторів протеаз. Гідроксиетиламіносульфонамідні інгібітори протеази ВІЛ, наприклад, 4амінобензолгідроксиетиламіносульфонаміди, описані як такі, що мають сприятливі фармакологічні і фармакокінетичні властивості проти вірусу ВІЛ дикого типу та мутантів. Типовим представником 4-амінобензолгідроксиетиламіносульфонамідного класу інгібіторів протеаз є ампренавір. Спосіб синтезу ампренавіру описаний в WO 99/48885 (Glaxo Group Ltd.). 4амінобензолгідроксиетиламіносульфонаміди також можна одержати відповідно до методик, описаних в ЕР 715618, WO 99/67417, US 6248775 і в Bioorganic and Chemistry Letters, Vol.8, pp.687-690, "Potent HIV protease inhibitors incorporating highaffinity P 2-ligands and (R)-(hydroxyeth ylamino) sulfonamide isostere", і всі зазначені роботи включені в даний опис як посилання. Зокрема, опис (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3іл(1S,2R)-3-[[(4амінофеніл)сульфоніл](ізобутил)аміно]-1-бензил-2гідроксипропілкарбамату, названого в даному описі сполукою (6), і способи його одержання можна знайти в WO 99/67417 (USA, The Secretary, Dpt. of Health and Human Services) і в РСТ/ЕР 03/50176 (Tibotec N.V.). WO 03/057665 (Ajinomoto K.K.) відноситься до способу одержання кристалів бензолсульфонамідних похідних. Зокрема, описується кристалізація (2R,3S)-N-(3-аміно-2-гідрокси-4-фенілбутил)-Nізобутил-4-амінобензолсульфонаміду, що є проміжною сполукою, що представляє інтерес для одержання (ЗR,3аS,6аR)-гексагідрофуро[2, 3-b]фуран3-іл(1S,2R)-3-[[(4амінофеніл)сульфоніл](ізобутил)аміно]-1-бензил-2 6 гідроксипропілкарбамату. Зазначену проміжну сполуку одержують, як розкривається, починаючи з (2S,3S)-3-бензилоксикарбоніламіно-1,2-епоксі-4фенілбутан у, у взаємодію з яким уводять ізобутиламін, з наступним сполученням з пнітробензолсульфонілхлоридом з утворенням (2R,3S)-N-(3-бензил оксикарбоніламіно-2-гідрокси4-фенілбутил)-N-ізобутил-4нітробензолсульфонаміду, який відновлюють із одночасним видаленням захисної групи, і одержують проміжну сполуку, що цікавить. Зокрема, у способі в якості амінозахисної групи для корової молекули використовують бензилоксикарбоніл (Cbz або Z). Відзначається, що одночасне відновлення нітрогрупи і видалення захисної групи Cbz з (2R,3S)-N-(3-бензилоксикарбоніламіно-2-гідрокси4-фенілбутил)-ізобутил-4нітробензолсульфонаміду приводить до сильно екзотермічної реакції. Екзотермічних реакцій, по можливості, варто уникати або зводити їх до мінімуму, тому що в цьому випадку сутужніше регулювати температур у реакцій, тобто, якщо температура реакції буде занадто низкою, швидкість реакції мала, і потрібен тривалий час; якщо температура реакції буде занадто високою, швидкість реакції є занадто високою, і відбувається недостатнє перемішування, що сприяє нерівномірному протіканню реакції, швидкому окиснюванню продуктів, що утворилися, або можуть відбуватися небажані побічні реакції, у результаті чого селективність по продукту знижується. З іншого боку, також відзначається, що каталітична реакція, що розкривається в WO 03/057665, не включає обробку в кислому середовищі. При відсутності обробки кислотою каталізатор, який використовували під час відновлення і видалення захисної групи Cbz, буде отруюватися сіркою п-нітробензолсульфонілхлориду. Отр уєний каталізатор неминуче приведе до появи побічних продуктів реакції, знижуючи селективність по продукту. Для того, щоб хімічний спосіб був прийнятний для промислового масштабу, він повинен дозволяти одержувати сполуки із прийнятним виходом і ступенем чистоти, причому в той же час бути легким і простим у здійсненні, а також ефективним по витратах. Такий новий спосіб, прийнятний у промисловому масштабі, знайдений для синтезу сполуки формули (6). Зокрема, даний винахід відноситься до зручного способу одержання сполуки формули (6) і проміжних сполук для його одержання, його солей приєднання, поліморфних і/або псевдополіморфних форм у промисловому масштабі. Конкретніше, даний винахід відноситься до прийнятного способу синтезу сполуки формули (6), що також має перевагу поліпшеної і ефективної по витратах кристалізації (2R,3S)-N-(3-аміно-2-гідрокси-4 7 85567 фенілбутил)-N-ізобутил-4амінобензолсульфонаміду із прийнятними ступенем чистоти й виходом. Навіть конкретніше, даний винахід стосується роздільного способу проведення реакцій відновлення і видалення захисної групи, що включає обробку кислотою і в результаті приводить до більш регульованого, селективного та ефективного по витратах способу. В одному втіленні даний винахід відноситься до вдосконаленого способу кристалізації з регулюванням рН і концентрації в певному інтервалі, у те час як в WO 03/057665 у зв'язку із кристалізацією згадується тільки нагрівання розчину в полярному розчиннику для того, щоб поліпшити вихід, або нагрівання розчину (30-80°С) для того, щоб розчинити кристали, що є присутніми у розчині в полярному розчиннику, щоб поліпшити очищення. Даний винахід також має перевагу застосування комерційно доступної вихідної речовини, такого як трет-бутиловий ефір 1-оксираніл-2фенілетилкарбамінової кислоти. Крім того, попередника сполуки формули (6), тобто, (2R,3S)-N-(3аміно-2-гідрокси-4-фенілбутил)-N-ізобутил-4амінобензолсульфонамід або сполуку формули (5), можна одержати процедурою в одному реакторі, що приводить до його ефективного використання та виключення стадій очищення проміжної сполуки. Також реагенти, які використовують в зазначеному способі, є безпечними і доступними у великій кількості. Крім того, кожну стадію зазначеного способу проводять у регульованих умовах, і одержують необхідну сполуку з оптимальним виходом. Також кожну стадію зазначеного способу проводять стереоселективно, що дозволяє синтезувати чисті стереоізомерні форми необхідних сполук. Інші задачі й переваги даного винаходу стануть очевидні з наступного далі докладного опису в сполученні із прикладеними прикладами. В ЕР 0754669 (Kaneka Corporation) описуються способи одержання альфа-галогенкетонів, альфагалогенгідринів і епоксидів; в ЕР 1029856 (Kaneka Corporation) розкривається спосіб одержання (2R,3S)-3-аміно-1, 2-оксирану; і ЕР 1067125, також Kaneka Corporation, відноситься до способу одержання трет-1,2-епоксі-3-аміно-4-фенілбутану. В ЕР 774453 (Ajinomoto Co., Inc.) описується спосіб одержання 3-аміно-2-оксо-1-галогенпропанових похідних. В WO 01/12599 (Samchully Pharm Co. Ltd.) описуються нові етилгідразинові похідні і способи їх одержання. В WO 01/46120 (Aerojet Fine Chemicals LLC) розкривається поліпшений спосіб одержання гідрохлориду 2S,3S-N-ізобутил-N-(2гідроксі-3-аміно-4-фенілбутил)-пнітробензолсульфонаміду й інших похідних 2гідрокси-1, 3-діамінів. В WO 96/28418 (G.D. Searle & Co., Inc.) розкриваються сульфонілалканоіламіногідроксиетиламіносульфонамідні інгібітори ретровірусних протеаз. В WO 94/04492 (G.D. Searle & Co., Inc.) розкриваються гідроксиетиламіносульфонаміди альфа- і бета-амінокислот, застосовувані як інгібітори ретровірусних протеаз. В WO 97/21685 (Abbott) розкривається одержання пептидних аналогів як інгібіторів ретровірусних протеаз. В WO 94/05639 (Vertex Pharmaceuticals) опису 8 ються сульфонамідні інгібітори аспартилпротеази ВІЛ-1. Даний винахід відноситься до способу одержання сполуки формули (6) її солей приєднання, поліморфних і/або псевдополіморфних форм, що включає (i) введення ізобутиламіногрупи в сполуку формули (1) де PG представляє амінозахисну гр упу; R1 являє собою водень або C1-6-алкіл; (іi) введення п-нітрофенілсульфонільної групи в сполуку, одержаної на стадії (i); (ііi) відновлення нітрогрупи сполуки, одержаної на стадії (іi); (iv) видалення захисної групи зі сполуки, одержаної на стадії (ііi); і (v) реакцію сполучення сполуки, одержаної на стадії (iv), з (3R,3аS,6аR)-гексагідрофуро[2,3b]фуран-3-ільним похідним з утворенням сполуки формули (6). В одному втіленні даний винахід відноситься до способу одержання сполуки формули (6), що відрізняється тим, що зазначений спосіб включає стадії введення ізобутиламіногрупи в сполуку формули (1’) з утворенням сполуки формули (2’) введення п-нітрофенілсульфонільної групи в сполуку формули (2’) з утворенням сполуки формули (3’) 9 відновлення нітрогрупи сполуки формули (3’) з утворенням сполуки формули (4’) видалення захисної групи зі сполуки формули (4’) з утворенням сполуки формули (5) сполучення сполуки формули (5) з (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3-ільним похідним з утворенням сполуки формули (6). Таким чином, даний винахід включає способи одержання сполуки формули (6), його солей приєднання, поліморфних і/або псевдополіморфних форм через проміжну сполуку формули (5) Переважно, сполуку формули (5) кристалізують як вільну основу. З іншого боку, сполук у формули (5) кристалізують у вигляді солей із сильними кислотами, такими як соляна кислота, бромводнева кислота, метансульфонова кислота, сірчана кислота, щавлева кислота, лимонна кислота й т.п.. Кристалізація сполуки формули (5) поліпшує ступінь його чистоти й вихід - обоє фактора сприятливі для одержання сполуки формули (6). З іншого боку, сполука формули (5) можна кристалізувати у вигляді його поліморфної й/або псевдополіморфної форми. Переважно, сполуку формули (6) кристалізують у вигляді псевдополіморфної форми, краще у вигляді алкоголяту, переважніше, у вигляді етаноляту. Сполука формули (1) Сполука формули (1) являє собою 85567 10 Де PG представляє амінозахисну гр упу; R1 являє собою водень або С 1-6-алкіл. Термін "амінозахисна група", який використовується у даному описі, відноситься до одного або декількох замісників, що видаляються селективно, в аміногрупі, якізвичайно використовують для блокування або захисту функціональної аміногрупи від небажаних побічних реакцій під час процедур синтезу, і включає всі звичайні амінозахисні групи. Прикладами амінозахисних груп є уре танові групи, що блокують, такі як трет-бутоксикарбоніл ("Вос"), 2-(4-біфеніл)пропіл(2)оксикарбоніл ("Уріс"), 2 фенілпропіл(2)оксикарбоніл ("Ріс"), 2-(4ксеніл)ізопроксикарбоніл, ізопропоксикарбоніл, 1,1- дифенілетил(1)оксикарбоніл, 1,1-дифенілпропіл(1)оксикарбоніл, 2-(3, 5-диметоксифеніл)пропіл(2)оксикарбоніл ("Ddz"), 2-(п-5-толуіл)пропіл(2)оксикарбоніл, 1метилциклопентанілоксикарбоніл, циклогексанілоксикарбоніл, 1-метилциклогексанілоксикарбоніл, 2метилциклогексанілоксикарбоніл, етоксикарбоніл, 2-(4-толуілсульфоніл)етоксикарбоніл, 2-(метилсульфоніл)етоксикарбоніл, 2(трифенілфосфино)етоксикарбоніл, 9-флуороенілметоксикарбоніл ("Fmoc"), 2-(триметилсиліл)етоксикарбоніл, алілоксикарбоніл, 1-(триметилсилілметил) проп-1енілоксикарбоніл, 5-бензизоксалілметоксикарбоніл, 4-ацетоксибензилоксикарбоніл, 2,2,2-трихлоретоксикарбоніл, триброметоксикарбоніл, 2-етиніл(2)пропоксикарбоніл, циклопропілметоксикарбоніл, ізоборнілоксикарбоніл, 1 -пипериділоксикарбоніл, бензилоксикарбоніл ("Z" або "Cbz"), 4-фенілбензилоксикарбоніл, 2-метилбензилоксикарбоніл, a-2,4,5,-тетраметилбензилоксикарбоніл ("Tmz"), 4-метоксибензилоксикарбоніл, 4-фторбензилоксикарбоніл, 4хлорбензилоксикарбоніл, 3-хлорбензилоксикарбоніл, 2-хлорбензилоксикарбоніл, дихлорбензилоксикарбоніл, 4-бромбензилоксикарбоніл, орто-бромбензилоксикарбоніл, 3-бромбензилоксикарбоніл, 4-нітробензилоксикарбоніл, 4-ціанобензилоксикарбоніл, 4-(децилокси)бензилоксикарбоніл, і т.п., бензоілметилсульфонільна група, дитіосукциноільна ("Dts") група, 2-(нітро)фенілсульфенільна група ("Nps"), дифенілфосфіноксидна група й подібні групи. Види використовуваних амінозахисних груп, як правило, не є визначальним чинником доти, поки дериватизована аміногрупа стійка в умовах наступних реакцій і може бути вилучена в підходящий момент без руйнування іншої частини сполуки. Іншими прикладами амінозахисних гр уп є фенілацетил, форміл ("For"), тритил (Trt), ацетил, трифторацетил (TFA), трихлорацетил, дихлорацетил, хлорацетил, бромацетил, йодацетил, бензоіл, трет-амілоксикарбоніл, трет-бутоксикарбоніл, 3,4диметоксибензилоксикарбоніл, 4-(фені 11 85567 лазо)бензилоксикарбоніл, 2-фурфурилоксикарбоніл, дифенілметоксикарбоніл, 1,1-диметилпропоксикарбоніл, фталіл або фталімидо, сукциніл, аланіл, лейцил і 8-хінолілоксикарбоніл, бензил, дифенілметил, 2-нітрофенілтіо, 2,4-динітрофенілтіо, метансульфоніл, пара-толуолсульфоніл, N,Nдиметиламінометилен, бензиліден, 2-гідроксибензиліден, 2-гідроксі-5-хлорбензиліден, 2-гідроксі-1нафтилметилен, З-гідроксі-4-піридилметилен, циклогексиліден, 2-етоксикарбонілциклогексиліден, 2етоксикарбонілциклопентиліден, 2-ацетилциклогексиліден, 3,3-диметил-5-оксициклогексиліден, дифенілфосфорил, дибензилфосфорил, 5-метилоксо-2Н-1,3 діоксол-4-ілметил, триметилсиліл, триетилсиліл, трифенілсиліл,2-(п-біфеніл)-1-метилетоксикарбоніл, диізопропілметоксикарбоніл, циклопентилоксикарбоніл, адамантилоксикарбоніл, трифенілметил, триметилсилан, фенілтіокарбоніл, пара-нітробензилкарбоніл. Іншими амінозахисними групами є 2,7-ди-третбутил[9-(10,10-діоксо-10,10,10,10-тетрагідротіоксантил)]метилоксикарбоніл; 2-триметилсилілетилоксикарбоніл; 2-фенілетилоксикарбоніл; 1,1-диметил-2,2-диброметилоксикарбоніл; 1-метил-1-(4біфеніл)етилоксикарбоніл; п-нітробензилоксикарбоніл; 2-(п-толуолсульфоніл)етилоксикарбоніл; мхлор-п-ацилоксибензилоксикарбоніл;5-бензилизоксазолилметилоксикарбоніл; п(дигідроксиборил)бензилоксикарбоніл; м-нітрофенілоксикарбоніл; о-нітробензилоксикарбоніл; 3,5-диметоксибензилоксикарбоніл; 3,4-диметокси6-нітробензилоксикарбоніл; N'-п-толуолсульфоніламінокарбоніл; трет-амілоксикарбоніл; п-децилоксибензилоксикарбоніл; 2,2-диметоксикарбонілвінілоксикарбоніл; ди(2-піридил)метилоксикарбоніл; 2-фуранілметилоксикарбоніл; дитіасукцинімід; 2, 5-диметилпирол; 5-дибензилсуберил і метансульфонамідна група. Кращою амінозахисною групою є Вос. Інші приклади амінозахисних груп добре відомі в те хніці органічного синтезу та пептидів і описані, наприклад, в T.W. Greene and P.G.M. Wuts, Protective Groups in Organic Synthesis, 2nd ed., John Wiley and Sons, New York, Chapter 7, 1991; M. Bodanzsky, Principles of Peptide Synthesis, 1 st and 2nd reviser ed., Springer-Verlag, New York, 1984 and 1993; Stewart and Young, Solid Phase Peptide Synthesis, 2nd ed., Pierce Chemical Co., Rockford, IL 1984; L. Fieser and M. Fieser, Fieser and Fieser's Reagents for Organic Synthesis, John Wiley and Sons (1994); L. Paquette, ed., Encyclopedia of Reagents for Organic Synthesis, John Wiley and Sons (1995). Придатні амінозахисні групи також наводяться в, наприклад, WO 98/07685. Термін "С1-6-алкіл"у відношенні до групи або частини групи позначає лінійні або розгалужені насичені вуглеводневі радикали з 1-6 атомами вуглецю, такі як метил, етил, ізопропіл, бутил, пентил, гексил, 2-метилбутил, 3-метилпентил і подібні. Переважно, сполука формули (1) являє собою сполуку формули (1’), наведеної нижче, де. PG являє собою трет-бутоксикарбоніл або "Вос", і R1 являє собою водень. Сполуки формули (1) і (1’) комерційно доступні і можуть бути отримані різни 12 ми способами, описаними в літературі, наприклад, так, як описано в WO 95/06030 (Searle & Co.), як описано в ЕР 0754669, ЕР 1029856 і ЕР 1067125, Kaneka Corporation, і так, як описано в ЕР 1081133 і ЕР 1215209, Ajinomoto KK. Сполука формули (2) Сполуку формули (1) піддають амінуванню по епоксидній групі і одержують сполуку формули (2). Термін "амінування", вжитий у даному описі, відноситься до процесу, у якому первинний амін, ізобутиламін, уводять в органічну молекулу формули (1). Амінування сполуки формули (1) можна здійснити декількома способами, описаними в літературі, наприклад, так, як описано в WO 95/06030, включеної в даний опис як посилання. У кращому втіленні сполуку формули (1’) уводять у взаємодію з ізобутиламіном, і одержують сполуку формули (2’). Амінування епоксидних сполук описується, наприклад, в March, Ad vanced Organic Chemistry, 368-69 (3rd Ed., 1985), і в McManus et al., 3 Synth. Comm. 177 (1973), включених у даний опис як посилання. Сполуки формули (2) і (2’) можна одержати придатним способом відповідно до методики, описаної в WO 97/18205. Агент амінування ізобутиламін може також виконувати функцію розчинника, і в такому випадку буде додаватися його надлишок. В інших втіленнях процес амінування здійснюють у присутності одного або декількох розчинників інших, ніж ізобутиламін. У кращому втіленні зазначені розчинники використовують при обробці сполук формули (2) і (2’). Придатні розчинники включають протонні, апротонні та біполярні апротонні органічні розчинники, такі як, наприклад, спирти, а саме метанол, етанол, ізопропанол, н-бутанол, трет-бутанол і т.п.; кетони, такі як ацетон; прості ефіри, такі як диетиловий ефір, тетрагідрофуран, діоксан і т.п.; складні ефіри, такі як етилацетат; аміни, такі як триетиламін; аміди, такі як N, N-диметилформамід або диметилацетамід; розчинники, що містять хлор, такі як дихлорметан, і інші розчинники, такі 13 85567 як толуол, диметилсульфоксид, ацетонітрил, і їх суміші. Кращим розчинником є толуол. Взаємодію звичайно можна проводити в широкому інтервалі температур, наприклад, від приблизно -20°С до приблизно 200°С, але переважно, хоча й не обов'язково, взаємодію проводять при температурі кипіння розчинника, тобто, між 40°С та 100°С, краще – між 60°С та 90°С. Придатні еквівалентні співвідношення між сполукою формули (1) і агентом амінування можуть коливатися від 1:1 до 1:99, відповідно. Переважно, співвідношення еквівалентів між сполукою формули (2) і агентом амінування становить від 1:5 до 1:20, ще краще співвідношення становить від 1:10 до 1:15. У втіленні винаходу реакцію амінування проводять у присутності приблизно 15 еквівалентів ізобутиламіну з використанням як розчинника толуолу та нагріванням при приблизно 79°С. Сполуки формули (3) Сполуку формули (3) одержують введенням сульфонільної групи п-нітробензол-SО2 у проміжну сполуку формули (2). Так, у кращому втіленні сполуку формули (3’) будуть одержувати сульфонілюванням сполуки формули (2’). Як такі, сполуки формули (2) і (2’) будуть взаємодіяти з агентом сульфонілювання з перетворенням у сполуку формули (3) і (3’). Термін "сульфонілювання", вжитий у даному описі, відноситься до процесу, у якому пнітробензолсульфонільну групу вводять в органічну молекулу формули (2) і (2’). Термін "сульфування", вжитий у даному описі, відноситься до процесу одержання агента сульфонілювання. Термін "агент сульфонілювання" відноситься до пнітробензолсульфонільних похідних, таким як пнітробензолсульфонільні галогенопохідні. Агенти сульфонілювання, і зокрема, пнітробензолсульфонільні галогенопохідні, можна одержати окиснюванням тіолів до сульфонілхлоридів з використанням хлору в присутності води в строго регульованих умовах. Крім того, можна перетворити сульфонові кислоти в суль фонілгалогеніди з використанням таких реагентів, як РСІ5, a також в ангідриди з використанням відповідних дегиратуючи х реагентів. Сульфонові кислоти, у свою чергу, можна одержати з використанням процедур, добре відомих у техніці. Також такі сульфонові кислоти доступні комерційно. Агенти сульфонілювання також можна одержати процедурами сульфування, описаними в роботах "Sulfonation and Related Reactions", E.E. Gilbert, 14 R.E. Krieger Publishing Co., Hungtington, N.Y. (1977); "Mechanistic Aspects of Aromatic Sulfonation and Desulfonation", H. Cerfontain, Interscience Publishers, NY (1968), і в US 6455738 "ProceS for sulfonation of an aromatic compound", які всі включені в даний опис як посилання. Обробку сполук формули (2) і (2’) агентом сульфонілювання можна здійснити в присутності розчинника при нагріванні приблизно від 25°С до 250°С, переважно, від 70°С до 100°С, і перемішуванні. Після сульфонілювання агент сульфонілювання, що залишився, або будь-які солі переважно, хоча необов'язково, видаляють із реакційної суміші. Видалення здійснюють повторюваними промиваннями водою, зміною рН, поділом органічної й водної фаз, ультрафільтрацією, зворотним осмосом, центрифугуванням і/або фільтрацією, або подібними способами. Сполуки формули (3) і (3’) одержують взаємодією сульфонілювального агента із проміжними сполуками формули (2) і (2’) у придатних розчинниках у лужному середовищі. Підходящими лужними середовищами є звичайні ненуклеофільні неорганічні або органічні основи і/або акцептори кислоти. Звичайні ненуклеофільні неорганічні або органічні основи включають, наприклад, гідриди, гідроксиди, аміди, алкоголяти, ацетати, карбонати або гідрокарбонати лужноземельних металів або гідриди лужних металів, такі як, наприклад, гідрид натрію, гідрид калію або гідрид кальцію, і аміди металів, такі як амід натрію, амід калію, диізопропіламід літію або гексаметилдисілазид калію, і алкани металів, такі як метилат натрію, етилат натрію, трет-бутилат калію, гідроксид натрію, гідроксид калію, гідроксид амонію, ацетат натрію, ацетат калію, ацетат кальцію, ацетат амонію, карбонат натрію, бікарбонат натрію, карбонат калію, бікарбонат калію, карбонат цезію, гідрокарбонат калію, гідрокарбонат натрію або карбонат амонію, а також органічні азотвмісні сполуки, такі як триалкіламіни, такі як, наприклад, триметиламін, триетиламін, трибутиламін, N,N-диметиланілін, N,Nдиметилбензиламін, N,N-диізопропілетиламін, піридин, 1,4-диазабіцикло[2.2.2]октан (DABCO), 1,5-диазабіцикло[4.3.0] нон-5-ен (DBN) або 1,8диазабіцикло[5.4.0]ундец-7-ен (DBU), або можна використовува ти надлишок підходящого піперидину. Переважно використовують триетиламін. Придатні розчинники зазначені вище при одержанні сполук формул (2) і (2’), причому кращі такі інертні розчинники, як, наприклад, толуол, етилацетат, метиленхлорид, дихлорметан і тетрагідрофуран. Звичайно співвідношення еквівалентів, розраховані для сполук формули (1) або (1’) і агента сульфонілювання, коливаються від 1:1 до 1:3, відповідно. Переважно, співвідношення еквівалентів сполук формули (1) або (1’) і агента сульфонілювання становить від 1:1 до 1:2, краще, коли співвідношення становить приблизно 1:1,15. Сполуки формули (4) Сполуки формули (4) і (4’) одержують взаємодією нітрогрупи проміжних сполук формули (3) і (3’), відповідно, з відновником, необов'язково, в атмосфері водню. 15 85567 Відновники, придатні для відновлення нітрогрупи, являють собою відновники, що містять метали, такі як комплекси бору, диборан, борогідрид натрію, борогідрид літію, борогідрид натрію-LiCl, алюмогідрид літію або диізобутилалюмогідрид; такі метали, як залізо, цинк, олово й т.п.; і утримуючі перехідні метали, такі як паладій-на-вугіллі, оксид платини, нікель Ренея, родій, рутеній і т.п.. Коли застосовують каталітичне відновлення, як джерело водню можна використовувати форміат амонію, дигідрофосфат натрію, гідразин. Придатні розчинники для відновлення нітрогрупи можна вибрати з води, спиртів, таких як метанол, етанол, ізопропанол, трет-бутиловий спирт, складних ефірів, таких як етилацетат, амідів, таких як диметилформамід, оцтової кислоти, дихлорметану, толуолу, ксилолу, бензолу, пентану, гексану, гептану, петролейного ефіру, 1,4-тіоксану, диетилового ефіру, диізопропілового ефіру, те трагідрофурану, 1,4-діоксану, 1,2-диметоксиетану, диметилсульфоксиду або їх сумішей. Взагалі, можна використовува ти будь-який розчинник, прийнятний для використання в процесі хімічного відновлення. Зазначену стадію відновлення можна здійснювати при температурах, від -78°С до 55°С, переважно, від -10°С до 50°С, причому кращі температури перебувають в інтервалі від 0°С до 50°С, краще від 5°С до 30°С. Час реакції може варіюватися від 30 хвилин до 2 діб, краще - від 1 години до 24 годин. Відповідно до кращого втілення стадію відновлення здійснюють із використанням паладію-навугіллі, суспендованого в метанолі. В іншому кращому втіленні можна використовувати додаткову кількість вугілля. Співвідношення еквівалентів сполук формули (3) або (3’) і водню коливаються від 1:1 до 1:10, відповідно. Краще, коли співвідношення еквівалентів сполук формули (3) або (3’) і водню становить від 1:1 до 1:5, краще, коли співвідношення становить приблизно 1:3. Сполуки формули (5) Сполуку формули (5) одержують видаленням захисної групи із проміжних сполук формули (4) і (4’) у звичайних умовах у кислому середовищі. З іншого боку, можна використовувати і лужне середовище. Видалення амінозахисної групи можна досягти в умовах, які не впливають на іншу частину молекули. Такі способи добре відомі в те хніці й включають гідроліз у кислому середовищі, гідрогеноліз і т.п., причому також використовують звичайно відомі кислоти в придатних розчинниках. Приклади кислот, які використовують при ви 16 даленні амінозахисної групи, включають такі неорганічні кислоти, як соляна кислота, азотна кислота, хлорводнева кислота, сірчана кислота й фосфорна кислота: такі органічні кислоти, як оцтова кислота, трифтороцтова кислота, метансульфонова кислота й п-толуолсульфоновая кислота: кислоти Льюїса, такі як трифторид бору; катіонообмінні смоли кислотного характеру, такі як Dowex 50W™. Із зазначених кислот кращими є неорганічні й органічні кислоти. Кращими є соляна кислота, сірчана кислота, фосфорна кислота трифтороцтова кислота, і найкращою є соляна кислота. Розчинник, який використовують під час видалення захисної групи із проміжних сполук формули (4) і (4’), не робить шкідливого впливу на реакцію й щонайменше, певною мірою розчиняє вихідні речовини. Придатними розчинниками є такі аліфатичні вуглеводні, як гексан, гептан і петролейний ефір; такі ароматичні вуглеводні, як бензол, толуол, ксилол і мезитилен; такі галогенвмісні вуглеводні, як метиленхлорид, хлороформ, чотирьохлористий вуглець і дихлоретан; такі прості ефіри, як диетиловий ефір, тетрагідрофуран, 1,4-діоксан і 1, 2-диметоксиетан; такі спирти, як метанол, етанол, пропанол, ізопропанол і бутанол; такі складні ефіри, як метилацетат, етилацетат, метилпропіонат і етилпропіонат; такі нітрили, як ацетонітрил; такі аміди, як N,N-диметилформамід і N,Nдиметилацетамід; такі сульфоксиди, як диметилсульфоксид, і їх суміші. Кращими є ароматичні вуглеводні, спирти й складні ефіри. Спирти й вода є кращими, а вода, ізопропанол, етанол і метанол є найкращими. Також кращими є суміші метанолу, води та ізопропанолу або етанолу та суміші етанолу і води. Температура реакції залежить від таких факторів, як природа вихідних речовин, розчинників і кислот. Однак, як правило, вона становить від -20°С до 150°С, і переважно, від 30°С до 100°С, навіть кращою є температура утворення флегми. Час реакції залежить від реагентів, температури та подібних факторів. Зазвичай він становить від 5 хвилин до 72 годин, і переважно, від 15 хвилин до 4 годин. Приклади реагентів і способів видалення з амінів амінозахисних груп можна також знайти в роботі Protective Groups in Organic Synthesis, Theodora W. Greene, New York, John Wiley and Sons, Inc., 1981, включеної в даний опис як посилання. Як відомо фахівцям у даній області техніки, вибір способу буде визначати реагенти й методики, використовувані при видаленні амінозахисної групи. Співвідношення еквівалентів сполук формули (3) або (3’) і кислоти в розчиннику можуть варіювати від 1:2 до 1:50, відповідно. Переважно, співвідношення еквівалентів сполук формули (3) або (3’) і кислоти становить від 1:2 до 1:8, краще, коли співвідношення становить приблизно 1:2. У кращому втіленні даного винаходу сполуку формули (5) кристалізують. Кристалізацію сполуки формули (5) проводять, розчиняючи сполуку формули (5) у суміші розчинників, установлюючи рН розчину й концентрацію сполуки формули (5). Можна додавати кристали сполуки формули (5). 17 85567 Суміш розчинників, яку використовують при кристалізації, може складатися з одного або декількох розчинників, що змішуються з водою, і води, або, система розчинників складається з одного або декількох розчинників, що не змішуються з водою, і води. Приклади розчинників, що змішуються з водою, включають такі спирти С 1-С4, як метанол, етанол, н-пропанол, ізопропанол, н-бутанол, ізобутанол; такі циклічні прості ефіри, як тетрагідрофуран або діоксан; такі аміди, як диметилформамід, диметилацетамід, N-метилпіролідон; диметилсульфоксид, ацетонітрил, суміш вищевказаних розчинників один з одним або з водою або воду. Прикладами розчинників, що не змішуються з водою, є такі вуглеводні, як пентан, гексан, циклогексан, метилциклогексан, гептан, толуол, ксилол; такі складні ефіри C4-C8, як метилформиат, етилформиат, метилацетат, етилацетат; такі прості ефіри С4-С8, як диетиловий ефір, третбутилметиловий ефір, ізопропіловий ефір; такі розчинники, що містять хлор, як метиленхлорид, дихлорметан, хлороформ, дихлоретан, хлорбензол; або їх подвійні або багатокомпонентні суміші. Коли використовують такі розчинники, що не змішуються з водою, сполуку формули (5) видаляють розділенням органічної та водної фаз. Регулювання концентрації сполуки формули (5) можна здійснювати додаванням води або інших придатних розчинників або випарюванням, відгоном розчинника або будь-якими іншими методами концентрування. У кращому способі кристалізації підтримують концентрацію сполуки формули (5) від 0,1% до 40% (мас/мас), переважно - від 1% до 30%, краще - від 2% до 20%, і ще краще - від 4% до 15%, мас/мас. Контроль або безпосередній (поточний) контроль концентрації сполуки формули (5) у розчині можна здійснювати будь-яким способом, відомим фа хівцям у даній області техніки, наприклад, хроматографією ВЕРХ, виміром щільності, титруванням і т.п.. Переважно, розчинник, що використовують при кристалізації сполуки формули (5), є тим же самим розчинником, що використовують при видаленні захисної групи із проміжної сполуки формули (4) або (4’). З іншого боку, якщо використовують кілька розчинників, один або кілька розчинників, використовуваних при кристалізації сполуки формули (5), є тими ж самими одним або декількома розчинниками, які використовують при видаленні захисної групи із проміжної сполуки формули (4) або (4’). Регулювання рН розчину, що містить сполуку формули (5), можна здійснювати додаванням основ, таких як гідроксид натрію, карбонат натрію, гідроксид калію, гідроксид літію, аміак, гідразин, гідроксид кальцію, метиламін, етиламін, анілін, етилендіамін, триетиламін, гідроксид тетраетиламонію, аміни С2-С18, гідроксид амонію С 4-С18, метоксид натрію, метоксид калію, органічної основи С1-С4, кожної з основ, перерахованих вище, і їх суміші. рН розчину, що містить сполуку формули (5), буде підтримуватися в лужній області, переважно, більше 7, краще, коли рН буде становити більше 8, а ще краще - більше 9. 18 В одному втіленні після додавання основи суспензію перемішують протягом 1-48 годин, переважно, 1-10 годин, а ще краще - протягом 1-5 годин. Робоча температура, яку використовують при осадженні сполуки формули (5), може варіюватися від -20°С до 50°С. Краще, коли робоча температура під час осадження становить від -15°С до 10°С, ще краще - від -10°С до 10°С, найкраще - близько 5°С. В іншому втіленні сполуку формули (5) збирають центрифугуванням і сушать у вакуумі при приблизно 65°С. Краща кристалічна сполука формули (5) перебуває у формі вільної основи. З іншого боку, іншими придатними сполуками є кристалічні сполуки формули (5) у формі солі, де сіль вибирають із числа гідрохлориду, гідроброміду, трифторацетату, фумарату, хлорацетату й метансульфонату та подібних солей. Проміжні сполуки формули (5) також є активними інгібіторами ретровірусних протеаз. (3R,3аS,6аR-Гексагідрофуро[2, 3-b]фуран-3-ільне похідне (3R,3аS,6аR)-Гексагідрофуро[2, 3b]фуран-3-ол і його попередники можна синтезувати так, як описано в WO 03/022853. (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3-ол і його попередники придатним способом активуються агентами сполучення з утворенням (3R,3аS,6аR)-гексагідрофуро[2, 3-b]фуран-3ільного похідного, котре може піддаватися карбамоілуванню сполукою формули (5). Активацію (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3-ола і його попередників проводять перед їх сполученням зі сполукою формули (5). Зазначена активація (3R,3аS,6аR)-гексагідрофуро[2, 3-b]фуран-3-олу і його попередників і їх сполучення зі сполукою формули (5) проводять в одному реакторі, тому що вилучення активованої проміжної сполуки не є обов'язковим, що є додатковою перевагою способу. Попередниками (3R,3аS,6аR)гексагідрофуро[2,3-b]фуран-3-олу є такі сполуки, у яких кисень функціональної спиртової групи захищений такими о-захисними групами, як третбутиле фірна група ("Вос"), ацетатні, бензильні групи, бензилефірні групи, алільні, такі силілзахисні групи, як трет-бутилдиметилсиліл (TBS), триметилсилілетоксиметил (SEM), такі алкоксиалкільні групи, як метоксиетоксиметил (MEM), метоксиметил (MOM), тетрагідропіраніл (ТНР), тетрагідропіраніл (ТНЕ), і подібними групами. Коли використовують попередники (3R,3аS,6аR)гексагідрофуро[2,3-b]фуран-3-олу, видалення захисної групи можна здійснити до сполучення або безпосередньо in situ. Видалити спиртозахисні групи можна в кислому або лужному середовищах, причому кращим є кисле середовище. Захисні групи добре відомі в техніці, див., наприклад, Greene T.W., Protective Groups in Organic Synthesis, John Wiley and Sons, Inc., New York, 1991. З іншого боку, (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3-ол і його попередники можна одержати через динамічне діастереоселективне розділення рецемічних сумішей гексагідрофуро[2,3-b]фуран-3-олу. У такому випадку рецемічну суміш піддають дії певних 19 85567 ферментів, таких як панкреатична ліпаза свині, панкреатин Candida cylindracca і т.п., у присутності придатних розчинників і реагентів, таких як оцтовий ангідрид і вінілацетат. Такий альтернативний спосіб дозволяє одержати in situ необхідний енантіомер (3R,3аS,6аR)-гексагідрофуро[2, 3-b]фуран3-ол, якому можна зручно активувати за способом в одному реакторі; непотрібний стереоізомер блокується або стає інертним. Прикладами агентів сполучення, використовуваних у реакціях карбамоілювання, є такі карбонати, як біс(4-нітрофеніл)карбонат, дисукцинімідилкарбонат (DSC), карбонілдиімидазол (CDI). Іншими агентами сполучення є такі хлорформіати, як пнітрофенілхлорформиат, такі фосгени, як фосген і трифосген. Зокрема, коли (3R,3аS,6аR)гексагідрофуро[2,3-b]фуран-3-ол обробляють дисукцинімидилкарбонатом, одержують 1([[(3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3ілокси]карбоніл]окси)-2,5-піролідиндіон. Зазначена сполука є кращим похідним (3R,3аS,6аR)гексагідрофуро[2,3-b]фуран-3-ілу. У випадку активації (3R,3aS,6aR)гексагідрофуро [2,3-b]фуран-3-олу і його попередників агентом сполучення рекомендується присутність спирту в концентраціях від 1% до 20% (мас/мас), переважно - у концентрації від 2% до 15% (мас/мас), ще краще – у концентрації від 4% до 10% (мас/мас). Взаємодію похідного (3R,3aS,6aR)гексагідрофуро[2, 3-b]фуран-3-ілу зі сполукою формули (5) здійснюють в присутності таких придатних розчинників, як тетрагідрофуран, диметилформамід, ацетонітрил, діоксан, дихлорметан або хлороформ, і, необов'язково, таких основ, як триетиламін, хоча також придатні сполучення розчинників і основ, розкритих в даному описі вище. Із числа розчинників кращими є апротонні, такі як тетрагідрофуран, ацетонітрил, диметилформамід, етилацетат і подібні. В одному втіленні під час сполучення похідного (3R,3аS,6аR)-гeкcaгiдpoфypo[2, 3-b]фуран-3-ілу зі сполукою формули (5) зазначене похідне є присутнім у концентрації від 1% до 15% (мас/мас), переважно - у концентрації від 5% до 12% (мас/мас), ще краще – у концентрації від 8% до 12% (мас/мас). Реакцію карбомоілювання здійснюють при температурі від -70°С до 40°С, переважно, від -10°С до 20°С. Сполука, отримана сполученням похідного (3R,3аS,6аR)-гeкcaгiдpoфypo[2,3-b]фуран-3-ілу зі сполукою формули (5), являє собою сполуку формули (6). Сполука формули (6) переважно, буде сольватуватись спиртами, такими як етанол, метанол, причому кращою формою сольвату є етанолят. Сольватація сполуки формули (6) описана в РСТ/ЕР 03/50176 (Tibotec N.V.) включеного в даний опис як посилання. 20 У кожному способі одержання, представленому ви ще, продукти реакції, наприклад, сполуки формули (3), (3’), (4), (4’), (5) і кінцевий продукт формули (6), можна виділити з реакційної суміші й, при необхідності, додатково очистити згідно з методиками, відомими у техніці, таким як, наприклад, екстракція, кристалізація, перегонка, розтирання в порошок і хроматографія. Для лікувального застосування солі сполук по винаходу являють собою солі, у яких протиіон є фармацевтично або фізіологічно прийнятним. Однак, солі з фармацевтично неприйнятними протиіонами також можуть знайти застосування, наприклад, при одержанні або очищенні фармацевтично прийнятної сполуки даного винаходу. Всі солі, чи є вони фармацевтично прийнятними чи ні, включені в об'єм даного винаходу. Фармацевтично прийнятні солі сполук винаходу, тобто, у формі продуктів, розчинних або здатних до диспергування у воді або олії, включають звичайні нетоксичні солі або солі четвертинного амонію, які утворяться, наприклад, з неорганічними або органічними кислотами або основами. Приклади таких солей приєднання кислот включають ацетати, адипати, альгінати, аспартати, бензоати, бензолсульфонати, бісульфати, бутирати, цитрати, камфорати, камфорсульфонати, циклопентанпропіонати, диглюконати, додецилсульфати, етансульфонати, фумарати, глюкогептаноати, гліцерофосфати, гемісульфати, гептаноати, гексаноати, гідрохлориди, гідроброміди, гідройодиди, 2-гідроксиетансульфонати, лактати, малеати, метансульфонати, 2нафталінсульфонати, нікотинати, оксалати, фосфати, памоати, пектинати, персульфати, 3фенілпропіонати, пікрати, пивалати, пропіонати, сукцинати, тартрати, тіоціанати, тозилати та ундеканоати. Приклади солей приєднання основ включають солі амонію, солі лужних металів, такі як натрієві й калієві солі, солі лужноземельних металів, такі як кальцієві й магнієві солі, солі з органічними основами, такі як солі дициклогексиламіну, солі метил-D-глюкаміну, і солі з амінокислотами, такими як аргінін, лізин і т.д.. Також основні азотвмісні групи можуть бути кватернізовани такими агентами, як нижчі алкілгалогеніди, такі як метил-, етил-, пропіл- і бутилхлорид, -бромід і -йодид, диалкілсульфати, подібні диметил-, диетил-, дибутил- і диамилсульфатам, галогеніди з довгим ланцюгом, такі як децил-, лаурил-, миристил- і стеарилхлорид, -бромід і -йодид, аралкілгалогеніди, такі як бензил- і фенілетилбромид, і іншими. Інші фармацевтично прийнятні солі включають етаноляти й сульфати солей сульфатів. Термін "поліморфна форма" відноситься до властивості сполук формули (5) і (6) існувати в аморфній формі, у поліморфній формі, у кристалі 21 85567 чній формі з різними структурами, що змінюються по твердості, формі й розмірам кристалів. Різні кристалічні форми можна виявити методами кристалографії або побічно, оцінюючи розходження у фізичних і/або хімічних властивостях, пов'язаних з певним поліморфом. Поліморфи мають розходження у фізичних властивостях, таких як розчинність, розчинення, стабільність у твердому стані, а також у поводженні при переробці в сипкості порошку й ущільнення під час таблетування. Терміни "псевдополімерна форма" або "сольвати" відносяться до агрегатів, що складають із молекул сполуки формули (6) і його солей із захопленими молекулами розчинниками або, що утворили з ними комплекс у співвідношенні моль/моль і з різним ступенем сольватації. Проміжні сполуки по винаходу також можуть існувати в таутомерних формах. Мається на увазі, що такі форми, хоча і не вказані явно в сполуках, описаних у даному описі, входять в об'єм даного винаходу. Чисті стереоізомерні форми сполук і проміжних сполук, що згадуються в даному описі, визначаються як ізомери, по суті, вільні від інших енантіомерних або діастереомерних форм тієї ж основної молекулярної структури зазначених сполук або проміжних сполук. Зокрема, термін "стереоізомерно чистий" відноситься до сполук або проміжних сполук зі стереоізомерним надлишком, щонайменше, 80% (тобто, що має мінімум 90% одного ізомеру й максимум 10% інших можливих ізомерів) і до стереоізомерного надлишку 100% (тобто, що має 100% одного ізомеру й ніяких інших ізомерів), особливо, сполукам або проміжним сполукам зі стереоізомерним надлишком від 90% до 100%, ще краще - зі стереоізомерним надлишком від 94% до 100%, і найкраще - зі стереоізомерним надлишком від 97% до 100%. Терміни "енантіомерно чистий" і "діастереомерно чистий" варто розуміти подібним чином, але у відношенні енантіомерного надлишку й, відповідно, діастереомерного надлишку в сумішах, що представляють інтерес. Чисті стереоізомерні форми сполук і проміжних сполук даного винаходу можна одержати, застосовуючи процедури, відомі в техніці. Наприклад, енантіомери можна відокремити друг від друга вибірковою кристалізацією їх діастереомерних солей з оптично активними кислотами або основами. їх прикладами є винна кислота, дибензоілвинна кислота, дитолуоілвинна кислота й камфорсульфонова кислота. З іншого боку, енантіомери можна розділити хроматографічними методами з використанням оптично активних нерухливих фаз. Зазначені чисті стереохімічні ізомерні форми також можна одержати з відповідних чистих стереохімічних ізомерних форм відповідних вихідних речовин, за умови, що реакція стереоспецифічна. Переважно, у випадку якщо потрібен певний стереоізомер, зазначену сполуку можна синтезувати стереоспецифічними способами. У зазначених способах будуть переважно використовуватися енантіомерно чисті вихідні речовини. Рацемати діастереомерів сполук і проміжних сполук даного винаходу можна розділити окремо звичайними способами. Найбільш вигідними фізич 22 ними способами поділу, є, наприклад, вибіркова кристалізація та хроматографія, наприклад, колонкова. Фахівцеві в даній області техніки зрозуміло, що сполуки й проміжних сполук даного винаходу містять, щонайменше, два асиметричних центри й, таким чином, можуть існувати в різних стереоізомерних формах. Такі асиметричні центри на фігурах, наведених нижче, зазначені зірочками (*). Абсолютна конфігурація кожного асиметричного центра, що може бути присутнім у сполуках і проміжних сполуках даного винаходу, може бути зазначена стереохімічними дескрипторами R і S, причому таке позначення R і S відповідає правилам, описаним в Pure Appl. Chem., 1976,45,11-30. Також мається на увазі, що даний винахід включає всі ізотопи, що зустрічаються в сполуках даного винаходу. Ізотопи включають атоми з однаковим атомним номером, але з різними масовими числами. Наприклад, як загальний приклад без обмеження, ізотопи водню включають тритій і дейтерій. Ізотопи вуглецю включають С-13 і С-14. Реагенти й розчинники, які використовують в описі, можна заміняти їх функціональними альтернативами або функціональними похідними, відомими фа хівцям у даній області техніки. Також такі умови реакцій, як час перемішування, очищення й температуру можна оптимізувати для реакції. Подібним чином, продукти реакції можна витягати із середовища й, при необхідності, додатково очищати відповідно до методик, взагалі відомим у техніці, таким як, наприклад, екстракція, кристалізація, розтирання в порошок і хроматографія. Ряд проміжних сполук і вихідних речовин, які використовують у вищеописаних способах одержання, є відомими сполуками, у той час як інші можна одержати відповідно до способів, відомим у техніці одержання зазначених або подібних сполук. Сполуки формули (5) і всі проміжні сполуки, що ведуть до утворення стереоізомерно чистих сполук, становлять особливий інтерес при одержанні 4-амінобензолсульфонамідів як інгібіторів ВІЛ протеази, як розкривається в WO 95/06030, WO 96/22287, WO 96/28418, WO 96/28463, WO 96/28464, WO 96/28465, WO 97/18205 і WO 02/092595, включених у даний опис як посилання, і зокрема, інгібітору ВІЛ протеази сполуки формули (6), як і будь-якої їх солі приєднання, поліморфні і/або псевдополіморфні форми. 23 85567 Таким чином, даний винахід також відноситься до інгібіторів протеази ВІЛ, таким як сполука формули (6), і будь-яким її солям приєднання, поліморфним і/або псевдополіморфним формам, одержаних з використанням будь-якої проміжної сполуки, описаної в даному описі, де і проміжні сполуки, і сполуку формули (6) одержують, як описано у даному винаході. Таким чином, даний винахід також відноситься до інгібіторів ВІЛ протеази, таких як сполука формули (6), і будь-яким їх солям приєднання, поліморфним і/або псевдополіморфним формам, отриманим з використанням сполуки (5) як проміжної сполуки, де як сполуку формули (5), так і сполуку формули (6) одержують так, як описано в даному винаході. Наведені далі приклади призначені для пояснення даного винаходу. Приклади приводяться як приклади винаходу і не повинні розглядатися як обмеження об'єму винаходу. ПРИКЛАДИ Приклад 1. Одержання трет-бутилового ефіру (1-бензил-2-гідрокси-3-ізобутиламінопропіл) карбамінової кислоти До 154,4кг ізобутиламіну додають третбутиловий ефір (1-оксираніл-2фенілетил)карбамінової кислоти (53,3кг), і потім розчин нагрівають зі зворотним холодильником. При зниженому тиску з реакційної суміші видаляють ізобутиламін і потім заміняють його толуолом. Приклад 2. Одержання трет-бутилового ефіру (1-бензил-2-гідрокси-3-[ізобутил(4нітробензолсульфоніл)аміно]пропіл) карбамінової кислоти До розчину, одержаного в прикладі 1, додають 26,7кг триетиламіна, і отриманий розчин нагрівають до 82-88°С. До розчину поступово додають розчин 4-нітробензолсульфонілхлориду (53кг) у толуолі й перемішують. Одержану реакційну суміш промивають водою. Промитий розчин трет-бутилового е фіру (1бензил-2-гідрокси-3-[ізобутил(4нітробензолсульфоніл)аміно]пропіл)карбамінової кислоти нагрівають, і потім додають толуол і нгептан. Отриманий розчин охолоджують і вносять зародки кристалів трет-бутилового ефір у (1бензил-2-гідрокси-3-[ізобутил(4нітробензолсульфоніл)аміно]пропіл)карбамінової кислоти. Після того, як спостерігають випадання кристалічної речовини в осад, розчин перемішують і потім поступово охолоджують до 20-30°С. Одержану кристалічну речовину відфільтровують і промивають змішаним розчинником, що складається з толуолу й н-гептану, і одержують вологі кристали трет-бутилового ефіру (1-бензил-2-гідрокси-3[ізобутил(4нітробензолсульфоніл)аміно]пропіл)карбамінової кислоти (вихід 87-91% відносно трет-бутилового ефіру (1-оксариніл-2-фенілетил)карбамінової кислоти). Приклад 3. Одержання трет-бутилового ефіру (1-бензил-2-гідрокси-3-[ізобутил(4амінобензолсульфоніл)аміно] пропіл)карбамінової кислоти Вологі кристали трет-бутилового ефір у (1 24 бензил-2-гідрокси-3-[ізобутил(4нітробензолсульфоніл)аміно] пропіл)карбамінової кислоти суспендують в етанолі (приблизно 950л) і потім гідрують у присутності 10 мас.% паладію на вугіллі при температурі приблизно 5-30°С. Паладій на вугіллі з реакційної суміші видаляють фільтрацією й потім фільтрат концентрують при зниженому тиску з одержанням розчину трет-бутилового ефіру (1-бензил-2-гідрокси-3-[ізобутил(4амінобензолсульфоніл)аміно]пропіл)карбамінової кислоти в етанолі. Приклад 4. Одержання 4-аміно-N-(2R,3S) (3аміно-2-гідрокси-4-фенілбутил)-Nізобутилбензолсульфонаміду Розчин трет-бутилового ефіру (1-бензил-2гідрокси-3-[ізобутил(4амінобензолсульфоніл)аміно]пропіл)карбамінової кислоти, отриманий у прикладі 3, кип'ятять зі зворотним холодильником, і потім додають концентровану соляну кислоту (35-37кг). Розчин перемішують. Потім отриманий розчин охолоджують до температури 40±3°С, і потім додають воду. рН розчину доводять до приблизно 9,5 водним розчином гідроксиду натрію, при цьому утворяться кристали 4-аміно-N-(3-аміно-2-гідрокси-4-фенілбутил)-Nізобутилбензолсульфонаміду. До одержаного розчину ще додають воду для доведення концентрації 4-аміно-N-(3-аміно-2-гідрокси-4-фенілбутил)-NІзобутилбензолсульфонаміду до 5, 5-5,8 мас. %, і потім отриманий розчин охолоджують до температури 6±4°С. Одержану кристалічну речовину відфільтровують і промивають змішаним розчинником, що складається з води та етанолу, і потім промивають водою. Одержану вологу кристалічну речовину сушать у вакуумі, і одержують продукт (2R,3S)-N-(3-аміно-2-гідрокси-4-фенілбутил)-Nізобутил-4-амінобензолсульфонамід. Вихід становить 75-85% відносно трет-бутилового ефіру (1бензил-2-гідрокси-3-[ізобутил( 4нітробензолсульфоніл)аміно]пропіл)карбамінової кислоти. Приклад 5. Одержання 4-аміно-N-((2R,3S)-3аміно-2-гідрокси-4-фенілбутил)-N(ізобутил)бензолсульфонаміду Суспендують у метанолі 50,00г третбутилового ефір у (1-бензил-2-гідрокси)-3[ізобутил(4нітробензолсульфоніл)аміно]пропіл)карбамінової кислоти, одержаної відповідно до методик, описаних в WO 99/48885, WO 01/12599 і WO 01/46120, 2 мол.% етаноламіну та паладій на активованому вугіллі, продувають інертним газом, і створюють вакуум. При температурі в реакторі 22-30°С подають приблизно 3,0 екв. водню при надлишковому тиску. Потім каталізатор видаляють фільтрацією. Безбарвний (до злегка жовтуватого) розчин обробляють 21,70г соляної кислоти, (37 мас. %), і суміш кип'ятять зі зворотним холодильником протягом 2 годин. По завершенні перетворення метанол видаляють перегонкою. Проводять осадження із суміші розчинників МеОН/вода/ІРА, 1:8:6,5. При температурі 0-7°3 додають порціями 30% розчин гідроксиду натрію доти, поки величина рН не стане р>12,5. Через 4-48 годин речовина, що випала в 25 85567 осад, білого кольору відфільтровують, промивають водою та ізопропанолом. Вологий продукт реакції сушать у вакуумі при 65°С. Спосіб дає 36,94г порошку від білого до жовтуватого кольору. Приклад 6. Одержання 4-аміно-N-((2R,3S)-3аміно-2-гідрокси-4-фенілбутил)-Nізобутил)бензолсульфонаміду Суспендують в етанолі 50,00г трет-бутилового ефіру (1-бензил-2-гідрокси-3-[ізобутил(4нітробензолсульфоніл)аміно]пропіл)карбамінової кислоти, одержаної відповідно до процедур, описаних в WO 99/48885, WO 01/12599 і WO 01/46120, і паладій на активованому вугіллі, продувають інертним газом, і створюють вакуум. При температурі в реакторі 22-30°С подають приблизно 3,0 екв. водню при надлишковому тиску. Потім каталізатор видаляють фільтрацією. Після відгону спирту в колбі залишається трет-бутиловий ефір (1-бензил2-гідрокси-3-[ізобутил(4амінобензолсульфоніл)аміно]пропіл)карбамінової кислоти у вигляді безбарвної піни з виходом 97%. Трет-бутиловий ефір (1-бензил-2-гідрокси-3[ізобутил(4амінобензолсульфоніл)аміно]пропіл)карбамінової кислоти розчиняють у метанолі, обробляють 21,70г соляної кислоти, (37 мас. %) і кип'ятять зі зворотним холодильником протягом 2 годин. Після завершення перетворення більшу частин у спирту видаляють відгоном. Солянокислу сіль 4-аміно-N((2R,3S)-3-аміно-2-гідрокси-4-фенілбутил)-Nізобутил)бензолсульфонаміду осаджують, видаляючи більшу частину спирту відгоном і додаючи дихлорметан до теплого (40°С) розчину. При перемішуванні й охолодженні до кімнатної температури солянокисла сіль відразу ж випадає в осад. Осадження 4-аміно-N-((2R,3S)-3-аміно-2-гідрокси4-фенілбутил)-N-ізобутил)бензолсульфонаміду проводять, розчиняючи хлороводневу сіль у суміші розчинників ЕtOН/вода, 1:1. При температурі 0-7°С додають порціями 30% розчин гідроксиду натрію доти, поки величина рН не досягне р>12,5. Через 4-48 годин речовину білого кольору, що випала в осад, відфільтровують, промивають водою й сушать у вакуумі. Спосіб дає 33,78г порошку від білого до жовтуватого кольору. Приклад 7. Одержання етаноляту (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3іл(1S,2R)-3-[[(4амінофеніл)сульфонал](ізобутил)аміно]-1-бензил2-гідроксипропілкарбамату До 120ммоль дисукцинімідилкарбонату (95%) в ацетонітрилі додають 100ммоль (3R,3аS,6аR)гексагідрофуро[2,3-b]фуран-3-олу в етилацетаті. Потім додають розчин 140ммоль триетиламіну в етилацетаті і перемішують. Суміш охолоджують і обробляють суспензією 92ммоль 4-аміно-N((2R,3S)-3-аміно-2-гідрокси-4-фенілбутил)-N(ізобутил)бензолсульфонаміду в е тилацетаті. Додають в етанолі 20ммоль метиламіну у вигляді 41% водяного розчину, і суміш гріють. Реакційну суміш двічі промивають 10% розчином Na2СО3 і водою. Розчинник випарюють, і додають етанол. Відганяють ще одну частину розчинника. Підтримують температуру приблизно 40-45°С, і ініціюють кристалізацію внесенням зародків кристалів. Після 26 перемішування суміш охолоджують, перемішують ще протягом 90хв, охолоджують і знову перемішують протягом 60хв. Речовину, що випала в осад, відфільтровують і промивають етанолом. Вологий продукт реакції сушать у вакуумі при 40°С. Суспендують і розчиняють в абсолютному етанолі 43,5г (3R,3аS,6аR)-гексагідрофуро[2,3b]фуран-3-іл(1S,2R)-3-[[(4амінофеніл)сульфоніл](ізобутил)аміно]-1-бензил-2гідроксипропілкарбамату. Прозорий розчин охолоджують, і вносять зародки кристалів. При охолодженні суміші відбувається кристалізація. Продовжують перемішування ще протягом 60хв, потім суміш охолоджують, перемішують, і відфільтровують продукт, що промивають холодним абсолютним етанолом. Вологий продукт сушать у вакуумі при 40°С. Вихід 42,1г = 71%. Приклад 8. Одержання етаноляту (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3іл(1S,2R)-3-[[(4амінофеніл)сульфоніл](ізобутил)аміно]-1-бензил-2гідроксипропілкарбамату До 105ммоль біс(4-нітрофеніл)карбонату в ацетонітрилі додають 100ммоль (3R,3аS,6аR)гексагідрофуро[2,3-b]фуран-3-олу в етилацетаті. Потім додають розчин 250ммоль триетиламіну в етилацетаті і перемішують. Суміш обробляють суспензією 95ммоль 4-аміно-N-((2R,3S)-3-аміно-2гідрокси-4-фенілбутил)-N(ізобутил)бензолсульфонаміду в е тилацетаті. Додають в етанолі 20ммоль метиламіну у вигляді 41% водяного розчину. Реакційну суміш три рази промивають 10% розчином К2СО3 і водою. Розчинник випарюють, і додають етанол. Відганяють ще одну частину розчинника. Підтримують температур у приблизно 40-45°С, і ініціюють кристалізацію запалом. Після перемішування суміш охолоджують, перемішують ще протягом 90хв, охолоджують і знову перемішують протягом 60хв. Речовину, що випала в осад, відфільтровують і промивають етанолом. Вологий продукт реакції сушать у вакуумі при 40°С. Суспендують і розчиняють в абсолютному етанолі 43,5г (3R,3аS,6аR)гексагідрофуро[2,3-b]фуран-3-іл(1S,2R)-3-[[(4амінофеніл)сульфоніл](ізобутил)аміно]-1-бензил-2гідроксипропілкарбамату. Прозорий розчин охолоджують, і вносять зародки кристалів. При охолодженні суміші відбувається кристалізація. Продовжують перемішування ще протягом 60хв, потім суміш охолоджують, перемішують, і відфільтровують продукт, що промивають холодним абсолютним етанолом. Вологий продукт сушать у вакуумі при 40°С Вихід 47,9г = 81%. Приклад 9. Одержання етаноляту (3R,3аS,6аR)-гексагідрофуро[2,3-b]фуран-3іл(1S,2R)-3- [[(4-амінофеніл)сульфоніл] (ізобутил)аміно]-1-бензил-2-гідроксипропілкарбамату До 110ммоль дисукцинимидилкарбонату (95%) в ацетонітрилі додають 100ммоль (3R,3aS,6aR)гексагідрофуро[2,3-b]фуран-3-олу в ацетонітрилі. Потім додають 300ммоль піридину й перемішують. Суміш охолоджують і обробляють суспензією 95ммоль 4-aмiнo-N-((2R,3S)-3-aмiнo-2-гiдpoкcи-4фeнiлбyтил)-N-(iзoбyтил)бeнзoлcyльфoнaмiдy в ацетонітрилі, і потім додають 100ммоль триетила 27 85567 міну. Потім додають 20ммоль метиламіну у вигляді 41% водяного розчину, і суміш гріють. Відганяють 80г розчинника, додають МТВЕ, і реакційну суміш промивають 10% розчином Na2CO3, сумішшю сульфату натрію й сарною кислоти і знову 10% розчином Na2CO3. Розчинник випарюють, і додають етанол. Відганяють ще одну частину розчинника. Підтримують температуру приблизно 4045°С, і ініціюють кристалізацію введенням зародків кристалів. Після перемішування суміш охолоджують, перемішують ще протягом 90хв, охолоджують і знову перемішують протягом 60хв. Речовину, що випала в осад, відфільтровують і промивають етанолом. Вологий продукт реакції сушать у вакуумі Комп’ютерна в ерстка А. Крулевський 28 при 40°С. Суспендують і розчиняють в абсолютному етанолі 43,5г (3R,3aS,6aR)гексагідрофуро[2,3-b]фypaн-3-іл(1S,2R)-3-[[(4амінофеніл)сульфоніл] (ізобутил)аміно]-1-бензил2-гідроксипропілкарбамату. Прозорий розчин охолоджують, і вносять зародки кристалів. При охолодженні суміші відбувається кристалізація. Продовжують перемішування ще протягом 60хв, потім суміш охолоджують, перемішують, і відфільтровують продукт, який промивають холодним абсолютним етанолом. Вологий продукт сушать у вакуумі при 40°С. Вихід 48,1г = 81%. Підписне Тираж 28 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of (3r,3as,6ar)-hexahydrofuro [2,3-b] furan-3-yl (1s,2r)-3-[[(4-aminophenyl) sulfonyl] (isobutyl) amino]-1-benzyl-2-hydroxypropylcarbamate
Автори англійськоюGoyvaerts Nicolaas Martha Felix, Wigerinck Piet Tom Bert Paul, Zinser Hartmut Burghard, Ebert Birgit M.
Назва патенту російськоюСпособ получения (3r,3as,6ar)-гексагидрофуро[2,3-b]фуран-3-ил(1s,2r)-3-[[(4-аминофенил)сульфонил](изобутил)амино]-1-бензил-2-гидроксипропилкарбамата
Автори російськоюГойваэртс Николаас Марта Феликс, Вигеринк Пит Том Берт Пауль, Зинсер Хартмут Бургхард, Эберт Биргит М.
МПК / Мітки
МПК: C07D 493/04
Мітки: 3r,3as,6ar)-гексагідрофуро[2,3-b]фуран-3-іл(1s,2r)-3-[[(4-амінофеніл)сульфоніл](ізобутил)аміно]-1-бензил-2-гідроксипропілкарбамату, спосіб, отримання
Код посилання
<a href="https://ua.patents.su/14-85567-sposib-otrimannya-3r3as6ar-geksagidrofuro23-bfuran-3-il1s2r-3-4-aminofenilsulfonilizobutilamino-1-benzil-2-gidroksipropilkarbamatu.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання (3r,3as,6ar)-гексагідрофуро[2,3-b]фуран-3-іл(1s,2r)-3-[[(4-амінофеніл)сульфоніл](ізобутил)аміно]-1-бензил-2-гідроксипропілкарбамату</a>
Попередній патент: Електрогідравлічний монітор
Наступний патент: Пристрій для виконання арифметичних операцій
Випадковий патент: 3,5-заміщені піперидини як інгібітори реніну












