Інгібітори 11-бета-гідроксистероїдної дегідрогенази типу 1
Номер патенту: 86813
Опубліковано: 25.05.2009
Автори: Хен Найанхе, Хенрікссон Мартін, Валлгарда Йєрк, Хоман Еверт, Кей Гуолін, Йоханссон Ларс, Фріззл Меттью Дж., Ст. Джін Девід, Ліу Куінгюян, Моніз Джордж А., Бартбергер Майкл Д., Фотсч Крістофер Х., Тіглі Крістофер, Беркот Ерік, Юан Честер Ченгуанг, Уільямс Мередіт, Хуанг Куі, Хангейт Рендалл У., Лі Айвен
Формула / Реферат
1. Сполука загальної формули (III):
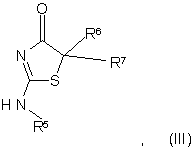
у якій:
R5 являє собою необов'язково заміщений феніл-(CR10aR10a)1-3-; та у якій R10a незалежно вибирають з групи, що включає Н, метил, фтор, або R10a та R10a можуть об'єднуватися разом з утворенням С3-С6-циклоалкільного кільця,
R6 вибирають з групи, що включає С1-8-алкіл, С1-8-алкокси, С3-10-циклоалкіл, гетероцикліл, С3-10-циклоалкіл-С1-8-алкіл, CN-С1-8-алкіл, арил, арил-С1-8-алкіл, гетероцикліл-С1-8-алкіл та галоалкіл;
R7 вибирають з групи, що включає -NR8R9, гало, С1-8-алкіл, -(CR8R9)n-OR8, -S-С1-С8-алкіл, С3-10-циклоалкіл, гетероцикліл, С3-10-циклоалкіл-С1-8-алкіл, ціано-С1-8-алкіл, арил, арил-С1-8-алкіл, гетероцикліл-С1-8-алкіл, гетероцикліл-С(О)-С1-8-алкіл, гетероцикліл-SО2-С1-8-алкіл, С1-8-галоалкіл, R8R9N-С1-8-aлкiл, НО-С1-8-алкіл, -С(О)-С3-С10-циклоалкіл, -С(О)-С1-С8-галоалкіл, -(CR8R9)n-Y-(CR8R9)n-гетероцикліл та -(CR8R9)n-Y-(CR8R9)n-C(O)-R8 (де n являє собою 0-5, Y являє собою NR10, О або S);
де будь-який арильний, алкільний, гетероциклільний або циклоалкільний залишок є необов'язково заміщеним за допомогою однієї або більше груп,таких як
-С1-С8-алкіл,
-гало,
-ОН,
-OR10,
-С1-С8-алкіл-SО2-,
-SО2-арил,
-C(O)-(CR8R9)n-карбамат,
-С(О)-О-С1-С8-алкіл,
-С(О)-С1-С8-алкіл,
-C(O)-(CR8R9)n-C(O)-NR8R9,
-C(O)-(CR8R9)n-NR8-C(O)-С1-С8-алкіл,
-C(O)-(CR8R9)n-NR8R9,
-С(О)-С3-С10-циклоалкіл,
-С(О)-арил,
-C(O)-(CR8R9)n-гетероцикліл,
-С1-С8-алкіл-OR8,
-С(О)-гало-С1-С8-алкіл або
-C(O)-(CR8R9)n-apил,
де будь-який арильний, алкільний, циклоалкільний або гетероциклільний залишок є необов'язково незалежно заміщеним за допомогою однієї або більше груп, таких як С1-C8-алкіл, арил, галоген, -NR10R10, С1-С8-галоалкіл, НО-С1-С8-алкіл, R8R9N-С1-С8-алкіл, С1-С8-aлкiл-ORl0, -OR10, (С3-С10)-циклоалкіл або С1-С8-алкілсульфоніл, -О-(CR8R9)n-гетероцикліл, -O-(CR8R9)n-C(O)-NR8R9, -O-(CR8R9)n-NR8R9, -Y-(CR8R9)n-NR8-C(O)-С1-С8-aлкіл, -Y-(CR8R9)n-гетероцикліл, -O-(CR8R9)n-NR8R9, -С1-С8-алкіл-SО2 або -O-(CR8R9)n-N-C(O)-гетероцикліл;
де R8 та R9 кожен незалежно вибирають з груп, таких як атом водню, С1-С8алкіл, С1-С8алкокси, -NR10R10, -S-(С1-С8)алкіл, арил та гетероцикліл;
будь-який алкіл, алкокси, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає гало, незаміщений С1-С8-алкіл, незаміщений С1-С8-алкокси, незаміщений С1-С8-тіоалкокси та незаміщений арил(С1-С4)алкіл; де R10 незалежно вибирають з групи, що включає водень, С1-С8-алкіл, арил-С1-С8-алкіл, С1-С8-алкокси, -S-(С1-С8)-алкіл, гетероцикліл та арил; будь-який алкіл, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає гало, незаміщений С1-С8-алкіл, незаміщений С1-С8-алкокси, незаміщений С1-С8-тіоалкокси та незаміщений арил(С1-С4)алкіл;
або R6 та R7 утворюють, разом з атомом вуглецю, до якого вони прикріплені, насичений, частково ненасичений або ненасичений С3-10-циклоалкіл або насичений, частково ненасичений або ненасичений С4-С14-гетероцикліл;
де циклоалкіл або гетероцикліл може бути необов'язково заміщений за допомогою однієї або більше груп, таких як С1-С8-алкіл, арил, С1-С8-галоалкіл, арил-С1-С8-алкіл, С3-С10-циклоалкіл, -OR8, =O, =NRS, =N-OR8, -NR8R9, -SR8, -гало, -OC(O)R8, -C(O)R8, -CO2R8, -CONR8R9, -OC(O)NR8R9, -NR9C(O)R8, -NR8C(O)NR8R9, -NR8SO2NR8R9, -NR8CO2R9, -NHC(NH2)=NH, -NR8C(NH2)=NH, -NHC(NH2)=NR8, -S(O)R8, -SO2R8, -SO2NR8R9, -NR8SO2R9, -CN та -NO2;
та її фармацевтично прийнятні солі, сольвати, гідрати, геометричні ізомери, таутомери, оптичні ізомери, N-оксиди та форми проліків, за умови, що: коли
R6=R7=мeтил, тоді R5 не являє собою феніл або 4-йодфеніл,
R6=R7=фeнiл, тоді R5 не являє собою феніл, та
R6 та R7 об'єднуються разом з утворенням циклопропільного кільця, тоді R5 не являє собою н-бутил, циклогексил, бензил, феніл або нафтил.
2.Сполука за п. 1, у якій R5 являє собою необов'язково заміщений феніл-(CR10aR10a)1-3-; та у якій R10a незалежно вибирають з групи, що включає Н, метил, фтор, або R10a та R10a можуть об'єднуватися разом з утворенням С3-С6-циклоалкільного кільця.
3. Сполука за п. 2, у якій R5 являє собою (необов'язково заміщений феніл)-(С(СН3)2)-, (необов'язково заміщений феніл)-(СНСН3) або бензил.
4. Сполука загальної формули (III):

у якій:
R5 вибирають з атома водню, С1-8-алкілу, С3-10-циклоалкілу, С3-10-циклоалкіл-С1-8-алкілу, арилу, арил-С1-8-алкілу, гетероциклілу, гетероцикліл-С1-8-алкілу та галоалкілу;
де будь-який арильний, циклоалкільний або гетероциклільний залишок є необов'язково незалежно заміщеним за допомогою однієї або більше груп, таких як С1-8-алкіл, арил, галоген, гало-С1-8-алкіл, HO-С1-8-алкіл, R8R9N-С1-8-алкіл, С1-8-алкіл-OR10, -OR10, (С3-С10)-циклоалкіл або С1-С8-алкілсульфоніл;
R6 вибирають з групи, що включає С1-8-алкіл, С3-10-циклоалкіл, насичений або частково ненасичений гетероцикліл, гетероарил та арил;
R7 вибирають з групи, що включає -NR8R9, гало, С1-8-алкіл, -(CR8R9)n-OR8 , -S- С1-С8-алкіл, С3-10-циклоалкіл, гетероцикліл, С3-10-циклоалкіл-С1-8-алкіл, ціано-С1-8-алкіл, арил, арил-С1-8-алкіл, гетероцикліл-С1-8-алкіл, гетероцикліл-С(О)-С1-8-алкіл, гетероцикліл-SО2-С1-8-алкіл, С1-8-галоалкіл, R8R9N-С1-8-aлкiл, НО-С1-8-алкіл, -С(О)-С3-С10-циклоалкіл, -С(О)-С1-8-галоалкіл, -(CR8R9)n-Y-(CR8R9)n-гетероцикліл та -(CR8R9)n-Y-(CR8R9)n-C(O)-R8 (де n являє собою 0-5, Y являє собою NR10, О або S);
де будь-який арильний, алкільний, гетероциклільний або циклоалкільний залишок є необов'язково заміщеним за допомогою однієї або більше груп, таких як
-С1-С8-алкіл,
-гало,
-ОН,
-OR10,
С1-С8-алкіл-SО2-,
-SО2-арил,
-C(O)-(CR8R9)n-карбамат,
-С(О)-О-С1-С8-алкіл,
-С(О)-С1-С8-алкіл,
-C(O)-(CR8R9)n-C(O)-NR8R9,
-C(O)-(CR8R9)n-NR8-C(O)-С1-С8-алкіл,
-C(O)-(CR8R9)n-NR8R9,
-С(О)-С3-С10-циклоалкіл,
-С(О)-арил,
-С(О)-(СR8R9)n-гетероцикліл,
-С1-С8алкіл-ОR8,
-С(О)-гало-С1-С8-алкіл або
-C(O)-(CR8R9)n-арил,
де будь-який арильний, алкільний, циклоалкільний або гетероциклільний залишок є необов'язково незалежно заміщеним за допомогою однієї або більше груп, таких як C1-С8-алкіл, арил, галоген, -NR10R10, С1-С8-галоалкіл, НО-С1-С8-алкіл, R8R9N-С1-С8-алкіл, С1-С8-алкіл-OR10, -OR10, (С3-С10)-циклоалкіл або С1-С8-алкілсульфоніл, -O-(CR8R9)n-гетероцикліл, -O-(CR8R9)n-C(O)-NR8R9, -O-(CR8R9)n-NR8R9, -Y-(CR8R9)n-NR8-C(O)-С1-С8-алкіл, -Y-(CR8R9)n-гетероцикліл, -O-(CR8R9)n-NR8R9, С1-С8-алкіл-SO2 або -O-(CR8R9)n-N-C(O)-гетероцикліл;
у якій R8 та R9 кожен незалежно вибирають з груп, таких як атом водню, С1-С8-алкіл, С1-С8-алкокси, -NR10R10, -S-(С1-С8)алкіл, арил та гетероцикліл; будь-який алкіл, алкокси, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає -гало, незаміщений С1-С8-алкіл, незаміщений С1-С8-алкокси, незаміщений С1-С8-тіоалкокси та незаміщений арил(С1-С4)алкіл; де R10 незалежно вибирають з групи, що включає водень, С1-С8-алкіл, арил-С1-С8алкіл, С1-С8алкокси, -S-(С1-С8)алкіл, гетероцикліл та арил;
будь-який алкіл, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає гало, незаміщений С1-С8алкіл, незаміщений С1-С8-алкокси, незаміщений С1-С8-тіоалкокси та незаміщений арил(С1-С4)алкіл; або R6 та R7 утворюють, разом з атомом вуглецю, до якого вони прикріплені, насичений, частково ненасичений або ненасичений С3-10-циклоалкіл або насичений, частково ненасичений або ненасичений С4-С14-гетероцикліл;
у якій циклоалкіл або гетероцикліл може бути необов'язково заміщений за допомогою однієї або більше груп, таких як С1-С8-алкіл, арил, С1-С8-галоалкіл, арил-С1-С8-алкіл, С3-С10-циклоалкіл, -OR8, =O, =NR8, =N-OR8, -NR8R9, -SR8, -гало, -OC(O)R8, -C(O)R8, -CO2R8, -CONR8R9, -OC(O)NR8R9, -NR9C(O)R8, -NR8C(O)NR8R9, -NR8SO2NR8R9, -NR8CO2R9, -NHC(NH2)=NH, -NR8C(NH2)=NH, -NHC(NH2)=NR8, -S(O)R8, -SO2R8, -SO2NR8R9, -NR8SO2R9, -CN та -NO2;
та її фармацевтично прийнятні солі, сольвати, гідрати, геометричні ізомери, таутомери, оптичні ізомери, N-оксиди та форми проліків, за умови, що: коли
R6=R7=мeтил, тоді R5 не являє собою феніл або 4-йодфеніл,
R6=R7=феніл, тоді R5 не являє собою феніл, та
R6 та R7 об'єднуються разом з утворенням циклопропільного кільця, тоді R5 не являє собою н-бутил, циклогексил, бензил, феніл або нафтил.
5. Сполука за п. 4, у якій R6 являє собою С1-С8-алкіл.
6. Сполука за п. 5, у якій R6 вибирають з групи, що включає метил, етил, н-пропіл або ізопропіл.
7. Сполука, вибрана з групи, що включає:
2-(біцикло[2.2.1]гепт-2-иламіно)-5-ізопропіл-1,3-тіазол-4(5Н)-он;
2-(біцикло[2.2.1]гепт-2-иламіно)-5-етил-1,3-тіазол-4(5Н)-он;
2-(біцикло[2.2.1]гепт-2-иламіно)-5-феніл-1,3-тіазол-4(5Н)-он;
2-(циклогексиламіно)-5-етил-1,3-тіазол-4(5Н)-он;
2-(біцикло[2.2.1]гепт-2-иламіно)-5,5-диметил-1,3-тіазол-4(5Н)-он;
5-ізопропіл-2-(трицикло[3.3.1.0~3,7~]нон-3-іламіно)-1,3-тіазол-4(5Н)-он;
6-(трицикло[3.3.1.0~3,7~]нон-3-іламіно)-5-тіа-7-азаспіро[3.4]окт-6-ен-8-он;
2-(трицикло[3.3.1.0~3,7~]нон-3-іламіно)-1,3-тіазол-4(5Н)-он;
6-(циклооктиламіно)-5-тіа-7-азаспіро[3.4]окт-6-ен-8-он;
6-(циклогептиламіно)-5-тіа-7-азаспіро[3.4]окт-6-ен-8-он;
6-(біцикло[2.2.1]гепт-2-иламіно)-5-тіа-7-азаспіро[3.4]окт-6-ен-8-он;
6-[(2,2,3,3-тетраметилциклопропіл)аміно]-5-тіа-7-азаспіро[3.4]окт-6-ен-8-он;
6-[(2-метилфеніл)аміно]-5-тіа-7-азаспіро[3.4]окт-6-ен-8-он;
2- [(циклогексилметил)аміно]-5,5-диметил-1,3-тіазол-4(5Н)-он;
2-[(2-фторфеніл)аміно]-5-ізопропіл-1,3-тіазол-4(5Н)-он;
2-[(циклогексилметил)аміно]-5-(2-гідроксифеніл)-1,3-тіазол-4(5Н)-он;
(5S)-2-(циклогептиламіно)-5-метил-1,3-тіазол-4(5Н)-он;
(5R)-2-(циклoгeптилaмiнo)-5-мeтил-l,3-тiaзoл-4(5H)-oн;
2-(циклогептиламіно)-5-етил-1,3-тіазол-4(5Н)-он;
2-(циклогептиламіно)-5-ізопропіл-1,3-тіазол-4(5Н)-он;
5-трет-бутил-2-(циклогептиламіно)-1,3-тіазол-4(5Н)-он;
2-(циклооктиламіно)-5-етил-1,3-тіазол-4(5Н)-он;
5-ізопропіл-2-[(2-ізопропілфеніл)аміно]-1,3-тіазол-4(5Н)-он;
5-етил-2-[(2-ізопропілфеніл)аміно]-1,3-тіазол-4(5Н)-он;
2-[(2-хлорфеніл)аміно]-5-етил-1,3-тіазол-4(5Н)-он;
5-етил-2-[(2-метилфеніл)аміно]-1,3-тіазол-4(5Н)-он;
5-ізопропіл-2-[(2,2,3,3-тетраметилциклопропіл)аміно]-1,3-тіазол-4(5Н)-он;
2-(біцикло[2.2.1]гепт-2-иламіно)-5-(4-гідроксибензил)-1,3-тіазол-4(5Н)-он;
5-[(циклогексилметил)аміно]-4-тіа-6-азаспіро[2.4]гепт-5-ен-7-он;
2-(циклогептиламіно)-5-(3,4-дигідроксибензил)-1,3-тіазол-4(5Н)-он;
2-(циклогептиламіно)-5-(1Н-імідазол-4-ілметил)-1,3-тіазол-4(5Н)-он;
2-(циклогептиламіно)-5-ізобутил-1,3-тіазол-4(5Н)-он;
2-(циклогептиламіно)-5-(1Н-індол-3-ілметил)-1,3-тіазол-4(5Н)-он;
2-(циклогептиламіно)-5-(4-гідроксибензил)-1,3-тіазол-4(5Н)-он;
(5R)-2-(циклогептиламіно)-5-(циклогексилметил)-1,3-тіазол-4(5Н)-он;
2-(циклооктиламіно)-5-(4-гідроксибензил)-1,3-тіазол-4(5Н)-он;
(5S)-2-(циклогептиламіно)-5-(циклогексилметил)-1,3-тіазол-4(5Н)-он;
[2-(циклогептиламіно)-4-оксо-4,5-дигідро-1,3-тіазол-5-іл]ацетонітрил;
2-(циклогептиламіно)-5-(піридин-3-ілметил)-1,3-тіазол-4(5Н)-он;
5-ізопропіл-2-[(2-метилфеніл)аміно]-1,3-тіазол-4(5Н)-он;
2-(циклооктиламіно)-5,5-диметил-1,3-тіазол-4(5Н)-он;
2-(циклооктиламіно)-5-ізопропіл-1,3-тіазол-4(5Н)-он;
2-(біцикло[2.2.1]гепт-2-иламіно)-1-тіа-3-азаспіро[4.5]дец-2-ен-4-он;
2-(трицикло[3.3.1.0~3,7~]нон-3-іламіно)-1-тіа-3-азаспіро[4.5]дец-2-ен-4-он;
2-(циклогептиламіно)-1-тіа-3-азаспіро[4.5]дец-2-ен-4-он;
2-(циклооктиламіно)-1-тіа-3-азаспіро[4.5]дец-2-ен-4-он;
2-{[1-(4-хлорфеніл)циклобутил]аміно}-5-ізопропіл-1,3-тіазол-4(5Н)-он;
6-{[1-(4-хлорфеніл)циклобутил]аміно}-5-тіа-7-азаспіро[3.4]окт-6-ен-8-он;
2-(циклогептиламіно)-5,5-діетил-1,3-тіазол-4(5Н)-он;
(5S)-5-ізопропіл-2-{[(2S)-2-фенілпропіл]аміно}-1,3-тіазол-4(5Н)-он;
(5R)-5-етил-2-{[(2S)-2-фенілпропіл]аміно}-1,3-тіазол-4(5Н)-он;
(5S)-5-етил-2-{[(2S)-2-фенілпропіл]аміно}-1,3-тіазол-4(5Н)-он;
(5R)-5-ізопропіл-2-{[(2R)-2-фенілпропіл]аміно}-1,3-тіазол-4(5Н)-он;
(5S)-5-ізопропіл-2-{[(2R)-2-фенілпропіл]аміно}-1,3-тіазол-4(5Н)-он;
(5R)-5-етил-2-{[(2R)-2-фенілпропіл]аміно}-1,3-тіазол-4(5Н)-он;
(5S)-5-етил-2-{[(2R)-2-фенілпропіл]аміно}-1,3-тіазол-4(5Н)-он;
2-аніліно-5-ізопропіл-1,3-тіазол-4(5Н)-он;
5-ізопропіл-2-[(2-морфолін-4-ілетил)аміно]-1,3-тіазол-4(5Н)-он;
2-(біцикло[2.2.1]гепт-2-иламіно)-1-тіа-3-азаспіро[4.4]нон-2-ен-4-он;
2-(циклогептиламіно)-1-тіа-3-азаспіро[4.4]нон-2-ен-4-он;
2-(циклооктиламіно)-1-тіа-3-азаспіро[4.4]нон-2-ен-4-он;
2-[(2,2,3,3-тетраметилциклопропіл)аміно]-1-тіа-3-азаспіро[4.4]нон-2-ен-4-он;
2-[(2-хлорбензил)аміно]-5-ізопропіл-1,3-оксазол-4(5Н)-он;
2-[(4-хлорбензил)аміно]-5-ізопропіл-1,3-оксазол-4(5Н)-он;
5-ізопропіл-2-[(2,2,6,6-тетраметилпіперидин-4-іл)аміно]-1,3-оксазол-4(5Н)-он;
5-ізопропіл-2-[(2-морфолін-4-ілетил)аміно]-1,3-оксазол-4(5Н)-он;
5-бензил-2-[(циклогексилметил)аміно]-1,3-оксазол-4(5Н)-он;
2-(циклогептиламіно)-5-ізопропіл-1,3-оксазол-4(5Н)-он;
2-(біцикло[2.2.1]гепт-2-иламіно)-5-ізопропіл-1,3-оксазол-4(5Н)-он;
2-(біцикло[2.2.1]гепт-2-иламіно)-5-ізобутил-1,3-оксазол-4(5Н)-он;
2-(циклогептиламіно)-5-ізобутил-1,3-оксазол-4(5Н)-он;
5-ізобутил-2-[(2-метилфеніл)аміно]-1,3-оксазол-4(5Н)-он, та
її фармацевтично прийнятні солі, сольвати, гідрати, геометричні ізомери, таутомери, оптичні ізомери, N-оксиди та форми проліків.
8. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-7 як активний інгредієнт у комбінації з фармацевтично прийнятним розріджувачем або носієм.
9. Фармацевтична композиція за п. 8, де композиція рецептована для пероральної доставки.
10. Фармацевтична композиція за п. 8, у якій пероральна доставка відбувається у формі таблетки.
11. Спосіб профілактики або лікування розладу, опосередкованого ферментом 11-β-гідроксистероїдної дегідрогенази типу 1, або досягнення імуномодуляції, що включає введення особі, що цього потребує, сполуки за будь-яким з пп. 1-7.
12. Спосіб за п. 11, у якому розлад вибирають з групи, що включає діабет, синдром X, ожиріння, глаукому, гіперліпідемію, гіперглікемію, гіперінсулінемію, гіпертензію, остеопороз, деменцію, депресію, вірусні хвороби та запальні хвороби.
13. Спосіб за п. 11 для лікування або профілактики медичного стану, що включає уповільнене або погіршене загоєння рани.
14. Спосіб за п. 13, у якому медичний стан, що включає уповільнене або погіршене загоєння рани, являє собою діабет.
15. Спосіб за п. 11, у якому медичний стан, що включає уповільнене або погіршене загоєння рани, спричинений лікуванням глюкокортикоїдами.
16. Спосіб за п. 11 для сприяння загоєнню рани при хронічних ранах, таких як діабетичні виразки, венозні виразки або пролежневі виразки.
17. Спосіб за п. 11, у якому імуномодуляцію вибирають з групи, що включає туберкульоз, лепру та псоріаз.
18.Спосіб інгібування ферменту 11-![]() -гідроксистероїдної дегідрогенази типу 1, який включає введення особі, якій необхідне таке лікування, ефективної кількості сполуки за будь-яким з пп. 1-7.
-гідроксистероїдної дегідрогенази типу 1, який включає введення особі, якій необхідне таке лікування, ефективної кількості сполуки за будь-яким з пп. 1-7.
19.Сполука, вибрана з групи, що включає:
2-[1-(4-фторфеніл)-етиламіно]-5-метил-5-(тетрагідропіран-4-ілметил)-тіазол-4-он;
(5S)-5-((1-ацетил-4-піперидиніл)метил)-2-((1S,4R)-біцикло[2.2.1]гепт-2-иламіно)-5-метил-1,3-тіазол-4(5Н)-он;
(5R)-2-((1S,4R)-біцикло[2.2.1]гепт-2-иламіно)-5-метил-5-(тетрагідро-2Н-піран-4-ілметил)-1,3-тіазол-4(5Н)-он;
(5S)-2-((1S,4R)-біцикло[2.2.1]гепт-2-иламіно)-5-метил-5-тетрагідро-2Н-піран-4-іл-1,3-тіазол-4(5Н)-он;
2-((1R,2R,4S)-біцикло[2.2.1]гепт-2-иламіно)-8-окса-1-тіа-3-азаспіро[4.5]дец-2-ен-4-он;
(5S)-2-((1S,4R)-біцикло[2.2.1]гепт-2-иламіно)-5-((1-(3-фуранілкарбоніл)-4-піперидиніл)метил)-5-метил-1,3-тіазол-4(5Н)-он;
2-(1-циклогексилетиламіно)-5-ізопропіл-5-метил-тіазол-4-он;
2-(5,5-дифторбіцикло[2.2.1]гепт-2-иламіно)-5-ізопропіл-5-метилтіазол-4-он;
2-(біцикло[2.2.1]гепт-2-иламіно)-5-ізопропіл-5-метилтіазол-4-он;
2-[1-(2-трифторметил-феніл)-етиламіно]-8-окса-1-тіа-3-азаспіро[4.5]дец-2-ен-4-он;
(5R)-2-((1S,2S,4R)-біцикло[2.2.1]гепт-2-иламіно)-5-метил-5-(трифторметил)-1,3-тіазол-4(5Н)-он;
2-(біцикло[2.2.1]гепт-2-иламіно)-5-(1-фтор-1-метилетил)-5-метилтіазол-4-он;
2-[1-(4-фторфеніл)-етиламіно]-5-метил-5-піридин-4-ілтіазол-4-он;
5-метил-5-піридин-4-іл-2-[1-(2-трифторметилфеніл)-етиламіно]-тіазол-4-он;
2-[1-(2-фторфеніл)-етиламіно]-5-метил-5-піридин-4-ілтіазол-4-он;
5-(1-фтор-1-метилетил)-2-[1-(2-фторфеніл)-етиламіно]-5-метилтіазол-4-он;
2-[1-(2-фторфеніл)-етиламіно]-5-метил-5-трифторметилтіазол-4-он;
5-(1,1-дифторетил)-2-[1-(4-фторфеніл)-етиламіно]-5-метилтіазол-4-он;
2-[1-(2-хлорфеніл)-етиламіно]-5-метил-5-трифторметилтіазол-4-он;
2-[1-(4-фторфеніл)-етиламіно]-5-мeтил-5-трифторметилтіазол-4-он;
2-[1-(2-хлорфеніл)-етиламіно]-5-метил-5-трифторметилтіазол-4-он;
2-[1-(4-фторфеніл)-етиламіно]-5-(2-метоксипіридин-4-іл)-5-метилтіазол-4-он;
5-(1,1-дифторетил)-2-[1-(4-фторфеніл)-етиламіно]-5-метилтіазол-4-он та
5-(1-фтор-1-метилетил)-2-[1-(4-фторфеніл)-етиламіно]-5-метилтіазол-4-он, та
її фармацевтично прийнятні солі, сольвати, гідрати, геометричні ізомери, таутомери, оптичні ізомери, N-оксиди та форми проліків.
20. Спосіб одержання сполуки за п. 1 або п. 4 та її фармацевтично прийнятних солей, сольватів, гідратів, геометричних ізомерів, таутомерів, оптичних ізомерів, N-оксидів та форм проліків, в якому здійснюють реакцію по схемі:
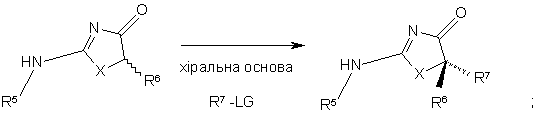
де:
X являє собою S або О; та
LG являє собою відхідну групу.
21. Спосіб за п. 20, у якому LG вибирають з групи, що включає галогенід, тозилат, мезилат та трифлат.
22. Спосіб за п. 20, у якому хіральна основа являє собою хіральну літієву основу.
Текст
1. Сполука загальної формули (III): O R6 N R7 S HN R5 , (III) у якій: R5 являє собою необов'язково заміщений феніл(CR10aR10a)1-3-; та у якій R10a незалежно вибирають з групи, що включає Н, метил, фтор, або R10a та R10a можуть об'єднуватися разом з утворенням С3-С6циклоалкільного кільця, R6 вибирають з групи, що включає С1-8-алкіл, С1-8алкокси, С3-10-циклоалкіл, гетероцикліл, С3-10циклоалкіл-С1-8-алкіл, CN-С1-8-алкіл, арил, арил-С1-8алкіл, гетероцикліл-С1-8-алкіл та галоалкіл; R7 вибирають з групи, що включає -NR8R9, гало, С1-8алкіл, -(CR8R9)n-OR8, -S-С1-С8-алкіл, С3-10циклоалкіл, гетероцикліл, С3-10-циклоалкіл-С1-8алкіл, ціано-С1-8-алкіл, арил, арил-С1-8-алкіл, гетероцикліл-С1-8-алкіл, гетероцикліл-С(О)-С1-8-алкіл, гетероцикліл-SО2-С1-8-алкіл, С1-8-галоалкіл, R8R9N-С1-8aлкiл, НО-С1-8-алкіл, -С(О)-С3-С10-циклоалкіл, -С(О)С1-С8-галоалкіл, -(CR8R9)n-Y-(CR8R9)n-гетероцикліл та -(CR8R9)n-Y-(CR8R9)n-C(O)-R8 (де n являє собою 0-5, Y являє собою NR10, О або S); 86813 4 де будь-який арильний, алкільний, гетероциклільний або циклоалкільний залишок є необов'язково заміщеним за допомогою однієї або більше груп,таких як -С1-С8-алкіл, -гало, -ОН, -OR10, -С1-С8-алкіл-SО2-, -SО2-арил, -C(O)-(CR8R9)n-карбамат, -С(О)-О-С1-С8-алкіл, -С(О)-С1-С8-алкіл, -C(O)-(CR8R9)n-C(O)-NR8R9, -C(O)-(CR8R9)n-NR8-C(O)-С1-С8-алкіл, -C(O)-(CR8R9)n-NR8R9, -С(О)-С3-С10-циклоалкіл, -С(О)-арил, -C(O)-(CR8R9)n-гетероцикліл, -С1-С8-алкіл-OR8, -С(О)-гало-С1-С8-алкіл або -C(O)-(CR8R9)n-apил, де будь-який арильний, алкільний, циклоалкільний або гетероциклільний залишок є необов'язково незалежно заміщеним за допомогою однієї або більше груп, таких як С1-C8-алкіл, арил, галоген, NR10R10, С1-С8-галоалкіл, НО-С1-С8-алкіл, R8R9N-С1С8-алкіл, С1-С8-aлкiл-ORl0, -OR10, (С3-С10)-циклоалкіл або С1-С8-алкілсульфоніл, -О-(CR8R9)n8 9 8 9 гетероцикліл, -O-(CR R )n-C(O)-NR R , -O-(CR8R9)nNR8R9, -Y-(CR8R9)n-NR8-C(O)-С1-С8-aлкіл, -Y-(CR8R9)nгетероцикліл, -O-(CR8R9)n-NR8R9, -С1-С8-алкіл-SО2 або O-(CR8R9)n-N-C(O)-гетероцикліл; де R8 та R9 кожен незалежно вибирають з груп, таких як атом водню, С1-С8алкіл, С1-С8алкокси, NR10R10, -S-(С1-С8)алкіл, арил та гетероцикліл; будь-який алкіл, алкокси, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає гало, незаміщений С1-С8-алкіл, незаміщений С1-С8-алкокси, незаміщений С1-С8тіоалкокси та незаміщений арил(С1-С4)алкіл; де R10 незалежно вибирають з групи, що включає водень, С1-С8-алкіл, арил-С1-С8-алкіл, С1-С8-алкокси, -S-(С1-С8)-алкіл, гетероцикліл та арил; будь-який алкіл, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає гало, незаміщений С1-С8-алкіл, незаміщений С1-С8-алкокси, незаміщений С1-С8-тіоалкокси та незаміщений арил(С1-С4)алкіл; або R6 та R7 утворюють, разом з атомом вуглецю, до якого вони прикріплені, насичений, частково ненасичений або ненасичений С3-10-циклоалкіл або насичений, частково ненасичений або ненасичений С4-С14-гетероцикліл; де циклоалкіл або гетероцикліл може бути необов'язково заміщений за допомогою однієї або більше груп, таких як С1-С8-алкіл, арил, С1-С8галоалкіл, арил-С1-С8-алкіл, С3-С10-циклоалкіл, -OR8, =O, =NRS, =N-OR8, -NR8R9, -SR8, -гало, -OC(O)R8, -C(O)R8, -CO2R8, -CONR8R9, -OC(O)NR8R9, NR9C(O)R8, -NR8C(O)NR8R9, -NR8SO2NR8R9, -NR8CO2R9, -NHC(NH2)=NH, -NR8C(NH2)=NH, -NHC(NH2)=NR8, S(O)R8, -SO2R8, -SO2NR8R9, -NR8SO2R9, -CN та -NO2; 5 та її фармацевтично прийнятні солі, сольвати, гідрати, геометричні ізомери, таутомери, оптичні ізомери, N-оксиди та форми проліків, за умови, що: коли R6=R7=мeтил, тоді R5 не являє собою феніл або 4йодфеніл, R6=R7=фeнiл, тоді R5 не являє собою феніл, та R6 та R7 об'єднуються разом з утворенням циклопропільного кільця, тоді R5 не являє собою н-бутил, циклогексил, бензил, феніл або нафтил. 2.Сполука за п.1, у якій R5 являє собою необов'язково заміщений феніл-(CR10aR10a)1-3-; та у якій R10a незалежно вибирають з групи, що включає Н, метил, фтор, або R10a та R10a можуть об'єднуватися разом з утворенням С3-С6-циклоалкільного кільця. 3. Сполука за п.2, у якій R5 являє собою (необов'язково заміщений феніл)-(С(СН3)2)-, (необов'язково заміщений феніл)-(СНСН3) або бензил. 4. Сполука загальної формули (III): O R6 N R7 S HN R5 , (III) у якій: R5 вибирають з атома водню, С1-8-алкілу, С3-10циклоалкілу, С3-10-циклоалкіл-С1-8-алкілу, арилу, арил-С1-8-алкілу, гетероциклілу, гетероцикліл-С1-8алкілу та галоалкілу; де будь-який арильний, циклоалкільний або гетероциклільний залишок є необов'язково незалежно заміщеним за допомогою однієї або більше груп, таких як С1-8-алкіл, арил, галоген, гало-С18 9 8-алкіл, HO-С1-8-алкіл, R R N-С1-8-алкіл, С1-8-алкіл10 10 OR , -OR , (С3-С10)-циклоалкіл або С1-С8алкілсульфоніл; R6 вибирають з групи, що включає С1-8-алкіл, С3-10циклоалкіл, насичений або частково ненасичений гетероцикліл, гетероарил та арил; R7 вибирають з групи, що включає -NR8R9, гало, С18 9 8 , -S- С1-С8-алкіл, С3-108-алкіл, -(CR R )n-OR циклоалкіл, гетероцикліл, С3-10-циклоалкіл-С1-8алкіл, ціано-С1-8-алкіл, арил, арил-С1-8-алкіл, гетероцикліл-С1-8-алкіл, гетероцикліл-С(О)-С1-8-алкіл, гетероцикліл-SО2-С1-8-алкіл, С1-8-галоалкіл, R8R9N-С18-aлкiл, НО-С1-8-алкіл, -С(О)-С3-С10-циклоалкіл, -С(О)С1-8-галоалкіл, -(CR8R9)n-Y-(CR8R9)n-гетероцикліл та (CR8R9)n-Y-(CR8R9)n-C(O)-R8 (де n являє собою 0-5, Y являє собою NR10, О або S); де будь-який арильний, алкільний, гетероциклільний або циклоалкільний залишок є необов'язково заміщеним за допомогою однієї або більше груп, таких як -С1-С8-алкіл, -гало, -ОН, -OR10, С1-С8-алкіл-SО2-, -SО2-арил, -C(O)-(CR8R9)n-карбамат, -С(О)-О-С1-С8-алкіл, -С(О)-С1-С8-алкіл, 86813 6 -C(O)-(CR8R9)n-C(O)-NR8R9, -C(O)-(CR8R9)n-NR8-C(O)-С1-С8-алкіл, -C(O)-(CR8R9)n-NR8R9, -С(О)-С3-С10-циклоалкіл, -С(О)-арил, -С(О)-(СR8R9)n-гетероцикліл, -С1-С8алкіл-ОR8, -С(О)-гало-С1-С8-алкіл або -C(O)-(CR8R9)n-арил, де будь-який арильний, алкільний, циклоалкільний або гетероциклільний залишок є необов'язково незалежно заміщеним за допомогою однієї або більше груп, таких як C1-С8-алкіл, арил, галоген, NR10R10, С1-С8-галоалкіл, НО-С1-С8-алкіл, R8R9N-С1С8-алкіл, С1-С8-алкіл-OR10, -OR10, (С3-С10)-циклоалкіл або С1-С8-алкілсульфоніл, -O-(CR8R9)n-гетероцикліл, -O-(CR8R9)n-C(O)-NR8R9, -O-(CR8R9)n-NR8R9, -Y(CR8R9) n-NR8-C(O)-С1-С8-алкіл, -Y-(CR8R9)n8 9 8 9 гетероцикліл, -O-(CR R )n-NR R , С1-С8-алкіл-SO2 або -O-(CR8R9)n-N-C(O)-гетероцикліл; у якій R8 та R9 кожен незалежно вибирають з груп, таких як атом водню, С1-С8-алкіл, С1-С8алкокси, -NR10R10, -S-(С1-С8)алкіл, арил та гетероцикліл; будь-який алкіл, алкокси, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає -гало, незаміщений С1-С8-алкіл, незаміщений С1-С8-алкокси, незаміщений С1-С8тіоалкокси та незаміщений арил(С1-С4)алкіл; де R10 незалежно вибирають з групи, що включає водень, С1-С8-алкіл, арил-С1-С8алкіл, С1-С8алкокси, -S-(С1С8)алкіл, гетероцикліл та арил; будь-який алкіл, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає гало, незаміщений С1-С8алкіл, незаміщений С1С8-алкокси, незаміщений С1-С8-тіоалкокси та незаміщений арил(С1-С4)алкіл; або R6 та R7 утворюють, разом з атомом вуглецю, до якого вони прикріплені, насичений, частково ненасичений або ненасичений С3-10-циклоалкіл або насичений, частково ненасичений або ненасичений С4-С14гетероцикліл; у якій циклоалкіл або гетероцикліл може бути необов'язково заміщений за допомогою однієї або більше груп, таких як С1-С8-алкіл, арил, С1-С8галоалкіл, арил-С1-С8-алкіл, С3-С10-циклоалкіл, OR8, =O, =NR8, =N-OR8, -NR8R9, -SR8, -гало, OC(O)R8, -C(O)R8, -CO2R8, -CONR8R9, OC(O)NR8R9, -NR9C(O)R8, -NR8C(O)NR8R9, NR8SO2NR8R9, -NR8CO2R9, -NHC(NH2)=NH, NR8C(NH2)=NH, -NHC(NH2)=NR8, -S(O)R8, -SO2R8, SO2NR8R9, -NR8SO2R9, -CN та -NO2; та її фармацевтично прийнятні солі, сольвати, гідрати, геометричні ізомери, таутомери, оптичні ізомери, N-оксиди та форми проліків, за умови, що: коли R6=R7=мeтил, тоді R5 не являє собою феніл або 4йодфеніл, R6=R7=феніл, тоді R5 не являє собою феніл, та R6 та R7 об'єднуються разом з утворенням циклопропільного кільця, тоді R5 не являє собою нбутил, циклогексил, бензил, феніл або нафтил. 5. Сполука за п.4, у якій R6 являє собою С1-С8-алкіл. 7 6. Сполука за п.5, у якій R6 вибирають з групи, що включає метил, етил, н-пропіл або ізопропіл. 7. Сполука, вибрана з групи, що включає: 2-(біцикло[2.2.1]гепт-2-иламіно)-5-ізопропіл-1,3тіазол-4(5Н)-он; 2-(біцикло[2.2.1]гепт-2-иламіно)-5-етил-1,3-тіазол4(5Н)-он; 2-(біцикло[2.2.1]гепт-2-иламіно)-5-феніл-1,3-тіазол4(5Н)-он; 2-(циклогексиламіно)-5-етил-1,3-тіазол-4(5Н)-он; 2-(біцикло[2.2.1]гепт-2-иламіно)-5,5-диметил-1,3тіазол-4(5Н)-он; 5-ізопропіл-2-(трицикло[3.3.1.0~3,7~]нон-3іламіно)-1,3-тіазол-4(5Н)-он; 6-(трицикло[3.3.1.0~3,7~]нон-3-іламіно)-5-тіа-7азаспіро[3.4]окт-6-ен-8-он; 2-(трицикло[3.3.1.0~3,7~]нон-3-іламіно)-1,3-тіазол4(5Н)-он; 6-(циклооктиламіно)-5-тіа-7-азаспіро[3.4]окт-6-ен-8он; 6-(циклогептиламіно)-5-тіа-7-азаспіро[3.4]окт-6-ен8-он; 6-(біцикло[2.2.1]гепт-2-иламіно)-5-тіа-7азаспіро[3.4]окт-6-ен-8-он; 6-[(2,2,3,3-тетраметилциклопропіл)аміно]-5-тіа-7азаспіро[3.4]окт-6-ен-8-он; 6-[(2-метилфеніл)аміно]-5-тіа-7-азаспіро[3.4]окт-6ен-8-он; 2- [(циклогексилметил)аміно]-5,5-диметил-1,3-тіазол4(5Н)-он; 2-[(2-фторфеніл)аміно]-5-ізопропіл-1,3-тіазол4(5Н)-он; 2-[(циклогексилметил)аміно]-5-(2-гідроксифеніл)1,3-тіазол-4(5Н)-он; (5S)-2-(циклогептиламіно)-5-метил-1,3-тіазол4(5Н)-он; (5R)-2-(циклoгeптилaмiнo)-5-мeтил-l,3-тiaзoл4(5H)-oн; 2-(циклогептиламіно)-5-етил-1,3-тіазол-4(5Н)-он; 2-(циклогептиламіно)-5-ізопропіл-1,3-тіазол-4(5Н)он; 5-трет-бутил-2-(циклогептиламіно)-1,3-тіазол-4(5Н)он; 2-(циклооктиламіно)-5-етил-1,3-тіазол-4(5Н)-он; 5-ізопропіл-2-[(2-ізопропілфеніл)аміно]-1,3-тіазол4(5Н)-он; 5-етил-2-[(2-ізопропілфеніл)аміно]-1,3-тіазол-4(5Н)он; 2-[(2-хлорфеніл)аміно]-5-етил-1,3-тіазол-4(5Н)-он; 5-етил-2-[(2-метилфеніл)аміно]-1,3-тіазол-4(5Н)-он; 5-ізопропіл-2-[(2,2,3,3тетраметилциклопропіл)аміно]-1,3-тіазол-4(5Н)-он; 2-(біцикло[2.2.1]гепт-2-иламіно)-5-(4гідроксибензил)-1,3-тіазол-4(5Н)-он; 5-[(циклогексилметил)аміно]-4-тіа-6азаспіро[2.4]гепт-5-ен-7-он; 2-(циклогептиламіно)-5-(3,4-дигідроксибензил)-1,3тіазол-4(5Н)-он; 2-(циклогептиламіно)-5-(1Н-імідазол-4-ілметил)1,3-тіазол-4(5Н)-он; 2-(циклогептиламіно)-5-ізобутил-1,3-тіазол-4(5Н)он; 2-(циклогептиламіно)-5-(1Н-індол-3-ілметил)-1,3тіазол-4(5Н)-он; 86813 8 2-(циклогептиламіно)-5-(4-гідроксибензил)-1,3тіазол-4(5Н)-он; (5R)-2-(циклогептиламіно)-5-(циклогексилметил)1,3-тіазол-4(5Н)-он; 2-(циклооктиламіно)-5-(4-гідроксибензил)-1,3тіазол-4(5Н)-он; (5S)-2-(циклогептиламіно)-5-(циклогексилметил)1,3-тіазол-4(5Н)-он; [2-(циклогептиламіно)-4-оксо-4,5-дигідро-1,3-тіазол5-іл]ацетонітрил; 2-(циклогептиламіно)-5-(піридин-3-ілметил)-1,3тіазол-4(5Н)-он; 5-ізопропіл-2-[(2-метилфеніл)аміно]-1,3-тіазол4(5Н)-он; 2-(циклооктиламіно)-5,5-диметил-1,3-тіазол-4(5Н)он; 2-(циклооктиламіно)-5-ізопропіл-1,3-тіазол-4(5Н)он; 2-(біцикло[2.2.1]гепт-2-иламіно)-1-тіа-3азаспіро[4.5]дец-2-ен-4-он; 2-(трицикло[3.3.1.0~3,7~]нон-3-іламіно)-1-тіа-3азаспіро[4.5]дец-2-ен-4-он; 2-(циклогептиламіно)-1-тіа-3-азаспіро[4.5]дец-2-ен4-он; 2-(циклооктиламіно)-1-тіа-3-азаспіро[4.5]дец-2-ен4-он; 2-{[1-(4-хлорфеніл)циклобутил]аміно}-5-ізопропіл1,3-тіазол-4(5Н)-он; 6-{[1-(4-хлорфеніл)циклобутил]аміно}-5-тіа-7азаспіро[3.4]окт-6-ен-8-он; 2-(циклогептиламіно)-5,5-діетил-1,3-тіазол-4(5Н)он; (5S)-5-ізопропіл-2-{[(2S)-2-фенілпропіл]аміно}-1,3тіазол-4(5Н)-он; (5R)-5-етил-2-{[(2S)-2-фенілпропіл]аміно}-1,3тіазол-4(5Н)-он; (5S)-5-етил-2-{[(2S)-2-фенілпропіл]аміно}-1,3-тіазол4(5Н)-он; (5R)-5-ізопропіл-2-{[(2R)-2-фенілпропіл]аміно}-1,3тіазол-4(5Н)-он; (5S)-5-ізопропіл-2-{[(2R)-2-фенілпропіл]аміно}-1,3тіазол-4(5Н)-он; (5R)-5-етил-2-{[(2R)-2-фенілпропіл]аміно}-1,3тіазол-4(5Н)-он; (5S)-5-етил-2-{[(2R)-2-фенілпропіл]аміно}-1,3тіазол-4(5Н)-он; 2-аніліно-5-ізопропіл-1,3-тіазол-4(5Н)-он; 5-ізопропіл-2-[(2-морфолін-4-ілетил)аміно]-1,3тіазол-4(5Н)-он; 2-(біцикло[2.2.1]гепт-2-иламіно)-1-тіа-3азаспіро[4.4]нон-2-ен-4-он; 2-(циклогептиламіно)-1-тіа-3-азаспіро[4.4]нон-2-ен4-он; 2-(циклооктиламіно)-1-тіа-3-азаспіро[4.4]нон-2-ен-4он; 2-[(2,2,3,3-тетраметилциклопропіл)аміно]-1-тіа-3азаспіро[4.4]нон-2-ен-4-он; 2-[(2-хлорбензил)аміно]-5-ізопропіл-1,3-оксазол4(5Н)-он; 2-[(4-хлорбензил)аміно]-5-ізопропіл-1,3-оксазол4(5Н)-он; 5-ізопропіл-2-[(2,2,6,6-тетраметилпіперидин-4іл)аміно]-1,3-оксазол-4(5Н)-он; 5-ізопропіл-2-[(2-морфолін-4-ілетил)аміно]-1,3оксазол-4(5Н)-он; 9 5-бензил-2-[(циклогексилметил)аміно]-1,3-оксазол4(5Н)-он; 2-(циклогептиламіно)-5-ізопропіл-1,3-оксазол4(5Н)-он; 2-(біцикло[2.2.1]гепт-2-иламіно)-5-ізопропіл-1,3оксазол-4(5Н)-он; 2-(біцикло[2.2.1]гепт-2-иламіно)-5-ізобутил-1,3оксазол-4(5Н)-он; 2-(циклогептиламіно)-5-ізобутил-1,3-оксазол-4(5Н)он; 5-ізобутил-2-[(2-метилфеніл)аміно]-1,3-оксазол4(5Н)-он, та її фармацевтично прийнятні солі, сольвати, гідрати, геометричні ізомери, таутомери, оптичні ізомери, N-оксиди та форми проліків. 8. Фармацевтична композиція, що містить сполуку за будь-яким з пп.1-7 як активний інгредієнт у комбінації з фармацевтично прийнятним розріджувачем або носієм. 9. Фармацевтична композиція за п.8, де композиція рецептована для пероральної доставки. 10. Фармацевтична композиція за п.8, у якій пероральна доставка відбувається у формі таблетки. 11. Спосіб профілактики або лікування розладу, опосередкованого ферментом 11-βгідроксистероїдної дегідрогенази типу 1, або досягнення імуномодуляції, що включає введення особі, що цього потребує, сполуки за будь-яким з пп.1-7. 12. Спосіб за п.11, у якому розлад вибирають з групи, що включає діабет, синдром X, ожиріння, глаукому, гіперліпідемію, гіперглікемію, гіперінсулінемію, гіпертензію, остеопороз, деменцію, депресію, вірусні хвороби та запальні хвороби. 13. Спосіб за п.11 для лікування або профілактики медичного стану, що включає уповільнене або погіршене загоєння рани. 14. Спосіб за п.13, у якому медичний стан, що включає уповільнене або погіршене загоєння рани, являє собою діабет. 15. Спосіб за п.11, у якому медичний стан, що включає уповільнене або погіршене загоєння рани, спричинений лікуванням глюкокортикоїдами. 16. Спосіб за п.11 для сприяння загоєнню рани при хронічних ранах, таких як діабетичні виразки, венозні виразки або пролежневі виразки. 17. Спосіб за п.11, у якому імуномодуляцію вибирають з групи, що включає туберкульоз, лепру та псоріаз. 18.Спосіб інгібування ферменту 11- b гідроксистероїдної дегідрогенази типу 1, який включає введення особі, якій необхідне таке лікування, ефективної кількості сполуки за будьяким з пп.1-7. 19.Сполука, вибрана з групи, що включає: 2-[1-(4-фторфеніл)-етиламіно]-5-метил-5(тетрагідропіран-4-ілметил)-тіазол-4-он; (5S)-5-((1-ацетил-4-піперидиніл)метил)-2-((1S,4R)біцикло[2.2.1]гепт-2-иламіно)-5-метил-1,3-тіазол4(5Н)-он; (5R)-2-((1S,4R)-біцикло[2.2.1]гепт-2-иламіно)-5метил-5-(тетрагідро-2Н-піран-4-ілметил)-1,3тіазол-4(5Н)-он; (5S)-2-((1S,4R)-біцикло[2.2.1]гепт-2-иламіно)-5метил-5-тетрагідро-2Н-піран-4-іл-1,3-тіазол-4(5Н)он; 86813 10 2-((1R,2R,4S)-біцикло[2.2.1]гепт-2-иламіно)-8-окса1-тіа-3-азаспіро[4.5]дец-2-ен-4-он; (5S)-2-((1S,4R)-біцикло[2.2.1]гепт-2-иламіно)-5-((1(3-фуранілкарбоніл)-4-піперидиніл)метил)-5метил-1,3-тіазол-4(5Н)-он; 2-(1-циклогексилетиламіно)-5-ізопропіл-5-метилтіазол-4-он; 2-(5,5-дифторбіцикло[2.2.1]гепт-2-иламіно)-5ізопропіл-5-метилтіазол-4-он; 2-(біцикло[2.2.1]гепт-2-иламіно)-5-ізопропіл-5метилтіазол-4-он; 2-[1-(2-трифторметил-феніл)-етиламіно]-8-окса-1тіа-3-азаспіро[4.5]дец-2-ен-4-он; (5R)-2-((1S,2S,4R)-біцикло[2.2.1]гепт-2-иламіно)-5метил-5-(трифторметил)-1,3-тіазол-4(5Н)-он; 2-(біцикло[2.2.1]гепт-2-иламіно)-5-(1-фтор-1метилетил)-5-метилтіазол-4-он; 2-[1-(4-фторфеніл)-етиламіно]-5-метил-5-піридин-4ілтіазол-4-он; 5-метил-5-піридин-4-іл-2-[1-(2-трифторметилфеніл)етиламіно]-тіазол-4-он; 2-[1-(2-фторфеніл)-етиламіно]-5-метил-5-піридин4-ілтіазол-4-он; 5-(1-фтор-1-метилетил)-2-[1-(2-фторфеніл)етиламіно]-5-метилтіазол-4-он; 2-[1-(2-фторфеніл)-етиламіно]-5-метил-5трифторметилтіазол-4-он; 5-(1,1-дифторетил)-2-[1-(4-фторфеніл)-етиламіно]-5метилтіазол-4-он; 2-[1-(2-хлорфеніл)-етиламіно]-5-метил-5трифторметилтіазол-4-он; 2-[1-(4-фторфеніл)-етиламіно]-5-мeтил-5трифторметилтіазол-4-он; 2-[1-(2-хлорфеніл)-етиламіно]-5-метил-5трифторметилтіазол-4-он; 2-[1-(4-фторфеніл)-етиламіно]-5-(2метоксипіридин-4-іл)-5-метилтіазол-4-он; 5-(1,1-дифторетил)-2-[1-(4-фторфеніл)-етиламіно]5-метилтіазол-4-он та 5-(1-фтор-1-метилетил)-2-[1-(4-фторфеніл)етиламіно]-5-метилтіазол-4-он, та її фармацевтично прийнятні солі, сольвати, гідрати, геометричні ізомери, таутомери, оптичні ізомери, N-оксиди та форми проліків. 20. Спосіб одержання сполуки за п.1 або п.4 та її фармацевтично прийнятних солей, сольватів, гідратів, геометричних ізомерів, таутомерів, оптичних ізомерів, N-оксидів та форм проліків, в якому здійснюють реакцію по схемі: O O N HN R5 X N R6 HN хіральна основа R7 -LG R5 X R7 R6 ; де: X являє собою S або О; та LG являє собою відхідну групу. 21. Спосіб за п.20, у якому LG вибирають з групи, що включає галогенід, тозилат, мезилат та трифлат. 22. Спосіб за п.20, у якому хіральна основа являє собою хіральну літієву основу. 11 Даний винахід відноситься до нових сполук, до фармацевтичних композицій, що містять ці сполуки, а також до застосування цих сполук у медицині та для одержання лікарського засобу, який діє на фермент 11-β-гідроксистероїдної дегідрогенази типу 1 людини (11βHSD1l). Гідроксистероїдні дегідрогенази (HSD) регулюють розміщення та активацію рецепторів стероїдних гормонів шляхом перетворення стероїдних гормонів у їх неактивні метаболіти. Як сучасний огляд [дивись Nobel та інші, Eur. J. Biochem. 2001, 268: 4113-4125]. Існують численні класи HSD. 11-бетагідроксистероідні дегідрогенази (11β-HSD1) каталізують взаємне перетворення активних глюкокортикоїдів (таких як кортизол та кортикостерон), та їх інертних форм (таких як кортизон та 11дегідрокортикостерон). Ізоформна 11-бетагідроксистероїдна дегідрогеназа типу 1 (11β-HSD1) експресується у печінці, жировій тканині, мозку, легенях та інших глюкокортикоїдних тканинах та являє собою потенційну ціль для терапії, спрямованої на численні розлади, що можуть бути полегшені шляхом зниження глюкокортикоїдної дії, такі як діабет, ожиріння та когнітивні дисфункції, пов'язані з віком. [Seckl, та інші, Endocrinology, 2001, 142: 1371-1376]. Різні ізоферменти 17-бета-гідроксистероїдних дегідрогеназ (17β-HSD) зв'язуються з андрогеновими рецепторами або естрогеновими рецепторами та каталізують взаємне перетворення різних статевих гормонів, включаючи естрадіол/естрон та тестостерон/андростендіон. До сьогодні, у людей ідентифіковано шість ізоферментів та вони експресуються у різних тканинах людини, включаючи ендометріальну тканину, тканину молочної залози, тканину кишечнику, та у яєчках. 17-бетаГідроксистероїдна дегідрогеназа типу 2 (17βHSD2) експресується у ендометрії людини та її активність, як описано, пов'язана з раком шийки матки. [Kitawaki та інші, J. Clin. Endocrin. Metab., 2000, 85: 1371-3292-3296]. 17-бетаГідроксистероїдна дегідрогеназа типу 3 (17βHSD3) експресується у яєчках та її модуляція може бути корисною для лікування андрогенпов'язаних розладів. Андрогени та естрогени є активними у їх 17βгідрокси конфігураціях, в той час як їх 17-кето похідні не прикріплюються до андрогенового та естрогенового рецепторів і є, таким чином, неактивними. Перетворення між активною та неактивною формами (естрадіол/естрон та тестостерон/андростендіон) статевих гормонів каталізується членами сімейства 11β-HSD. 11β-HSD1 каталізує утворення естрадіолу у тканині молочної залози, що є важливим для росту злоякісних пухлин молочної залози. [Labrie та інші, Моl. Cell. Endocrinol. 1991, 78: С113-С118]. Передбачають, що 17β-HSD4 грає подібну роль при раку кишечнику. [English та інші, J. Clin. Endocrinol. Metab. 1999, 84: 2080-2085]. 17β-HSD3 майже винятково екс 86813 12 пресується у яєчках та перетворює андростендіон у тестостерон. Недостатність цього ферменту у процесі розвитку плоду приводить до чоловічого псевдогермафродитизму. [Geissler та інші, Nat. Genet. 1994, 7: 34-39]. Як 17β-HSD3, так і різні 3αHSD1зоферменти залучаються у комплексні метаболічні шляхи, які ведуть до перемішування між неактивною та активною формами андрогенів. [Penning та інші, Biochem. J. 2000, 351: 67-77]. Таким чином, модуляція певних HSD може мати потенційно позитивні ефекти у лікуванні андроген-та естроген-пов'язаних розладів. 20-альфа-гідроксистероїдні дегідрогенази (20α-HSD) каталізують взаємне перетворення прогестинів (таке як між прогестероном та 20αгідрокси-прогестероном). Інші речовини для 20αHSD включають 17α-гідроксипрегненолон або 17αгідроксипрогестерон, приводять до 20α-ОН стероїдів. Були ідентифіковані декілька 20αHSD1зоформ та 20α-HSD експресуються у різних тканинах, включаючи плаценту, яєчники, яєчка та надниркові залози. [Peltoketo, та інші, J. Моl. Endocrinol. 1999, 23: 1-11]. 3-альфа-гідроксистероїдні дегідрогенази (3αHSD) каталізують взаємне перетворення андрогенів дигідротестостерону (DHT) та 5а-андростан3а,17р-діолу та взаємне перетворення андрогенів DHEA та андростендіону і, тому, грають важливу роль у андрогеновому метаболізмі. [Ge та інші, Biology of Reproduction 1999, 60: 855-860]. 1. Глюкокортикоїди, діабет та вироблення глюкози печінкою Впродовж більше ніж півстоліття відомо, що глюкокортикоїди відіграють головну роль у діабеті. Наприклад, видалення пітуітарної залози або надниркової залози у тварини, хворої на діабет, полегшує найбільш важкі симптоми діабету та знижує концентрацію глюкози у крові [Long, CD. та Leukins, F.D.W. (1936) J. Exp. Med. 63: 465-490; Houssay, B.A. (1942) Endocrinology 30: 884-892]. Також добре відомо, що глюкокортикоїди роблять можливим ефект глюкагону на печінку. Роль 11βHSD1 як важливого регулятора локального глюкокортикоїдного ефекту і, таким чином, вироблення глюкози печінкою добре досліджена [дивись, наприклад, Jamieson та інші (2000) J. Endocrinol. 165: 685-692]. Печінкова чутливість до інсуліну була покращена у здорових людейволонтерів, яких лікували неспецифічним 11βHSD1 інгібіторним карбеноксолоном [Walker, B.R. та інші (1995) J. Clin. Endocrinol. Metab. 80: 3155-3159]. Більше того, очікуваний механізм був доведений різними експериментами на мишах та щурах. Ці дослідження показали, що mRNA рівні та активності двох ключових ферментів у виробленні глюкози печінкою були знижені, а саме: обмежуючий швидкість фермент у глюконеогенезі, фосфоенолпіруват карбоксикіназа (РЕРСК), та глюкоза-6-фосфатаза (G6Pase) фермент, що каталізує останню загальну стадію глюконеогенезу та гликогенозу. Нарешті, рівні глюкози у крові та 13 вироблення глюкози печінкою були знижені у мишей, у яких 11βHSD1 ген вилучений. Дані цієї моделі також підтверджують, що інгібування 11βHSD1 не спричинить гіпоглікемію, як передбачали, так як базальні рівні РЕРСK та G6Pase регулюються незалежно від глюкокортикоїдів [Kotelevtsev, Υ. Та інші, (1997) Ргос. Natl. Acad. Sci. USA 94: 14924-14929]. У FR 2,384,498 розкриті сполуки, що мають сильний гіпоглікемічний ефект. Тому, лікування гіперглікемії за допомогою цих сполук може привести до гіпоглікемії. 2. Можливе зниження ожиріння та факторів серцево-судинного ризику, пов'язаного з ожирінням Ожиріння являє собою важливий фактор у синдромі X, а також у більшості (>80%) випадків діабету типу 2, та здається, сальниковий жир є особливо важливим. Абдомінальне ожиріння тісно пов'язане з непереносимістю глюкози, гіперінсулінемією, гіпертригліцеридемією, та іншими факторами так званого синдрому X (наприклад, підвищений кров'яний тиск, знижені рівні HDL та підвищені рівні VLDL) [Montague & O'Rahilly, Diabetes 49: 883-888, 2000]. Було показано, що інгібування 11βHSD1 ферменту у пре-адипоцитах (стромальні клітини) знижує швидкість диференціювання у адипоцити. Передбачають, що це приводить до зменшеного росту (можливо зниження) сальникового жирового депо, тобто зниження загального ожиріння [Bujalska, I.J., S. Kumar, та P.M. Stewart (1997) Lancet 349: 1210-1213]. Інгібування 11βHSD1 у зрілих адипоцитах, як очікується, буде зменшувати секрецію інгібітору активатору плазміногену 1 (РАІ-1) - незалежний серцево-судинний фактор ризику [Halleux, CM. та інші (1999) J. Clin. Endocrinol. Metab. 84: 40974105]. Більш того, існує чітка кореляція між глюкокортикоїдною "активністю" та серцево-судинним фактором ризику, яка передбачає, що зниження глюкокортикоїдних ефектів могло б мати позитивний ефект [Walker, B.R. та інші (1998) Hypertension 31. 891-895; Fraser, R. та інші (1999) Hypertension 33: 1364-1368]. Адреналектомія зменшує ефект голоду для збільшення як споживання їжі, так і гіпоталамічної нейропептидної Υ експресії. Це підтверджує роль глюкокортикоїдів у сприянні споживання їжі та передбачає, що інгібування 11βHSD1 у мозку могло б збільшити безпечність і, тому, знизити споживання їжі [Woods, S.C. та інші (1998) Science, 280: 1378-1383]. 3. Можливі позитивні ефекти на підшлункову залозу Інгібування 11βHSD1 у виділених мишиних βклітинах підшлункової залози покращує стимульовану глюкозою секрецію інсуліну [Davani, В. та інші (2000) J. Вiol. Chem. 2000 Nov 10; 275(45): 348414]. Раніше було відомо, що глюкокортикоїди знижують вивільнення інсуліну у підшлунковій залозі in vivo [Billaudel, В. та B.C.J. Sutter (1979) Horm. Metab. Res. 11: 555-560]. Таким чином, передбачають, що інгібування 11βHSD1 приводить до одержання інших позитивних ефектів для лікування діабету, окрім ефектів на печінку та жир. 86813 14 4. Можливі позитивні ефекти на пізнавальну функцію та деменцію Стрес та глюкокортикоїди впливають на когнітивну функцію [de Quervain, D.J.-F., В. Roozendaal, та J.L. McGaugh (1998) Nature 394: 787-790]. Фермент 11βHSD1 контролює рівень глюкокортикоїдної дії у мозку і, таким чином, вносить свій вклад у нейротоксичність [Rajan, V., C.R.W. Edwards, та J.R. Seckl, J. (1996) Neuroscience 16: 65-70; Seckl, J.R., Front. (2000) Neuroendocrinol. 18: 49-99]. Неопубліковані результати показують значне покращення пам'яті у щурів, яких обробляли за допомогою неспецифічного 11βHSD1 інгібітору (J. Seckl, персональне повідомлення). Базуючись на описаному вище та на відомих ефектах глюкокортикоїдів у мозку, також може бути припущено, що інгібування 11βHSD1 у мозку може призвести до зменшення стану неспокою [Tranche, F. та інші (1999) Nature Genetics 23: 99-103]. Таким чином, підсумовуючи, є припущення про те, що інгібування 11βHSD1 у мозку людини буде запобігати реактивації кортизону у кортизол та захищати від шкідливих глюкокортикоїд-опосередкованих ефектів на нейрональне виживання та інші аспектів нейрональноі функції, включаючи когнітивне ураження, депресію та підвищений апетит. 5. Можливе застосування імуно-модуляції, використовуючи інгібітори 11βHSD1 Загальне розуміння полягає в тому, що глюкокортикоїди пригнічують імунну систему. Але насправді, існує динамічна взаємодія між імунною системою та ΗΡΑ (гіпоталамно-гіпофізарнонаднирковою) віссю [Rook, G.A.W. (1999) Baillier's Clin. Endocrinol. Metab. 13: 576-581]. Баланс між клітино-опосередкованою відповіддю та гуморальними відповідями модулюється глюкокортикоїдами. Висока глюкокортикоїдна активність, така як у стані стресу, пов'язана з гуморальною відповіддю. Таким чином, інгібування ферменту 11βHSD1 запропоновано як засіб зміщення відповіді у бік клітино-базисної реакції. При певних хворобливих станах, включаючи туберкульоз, лепру (гансеніаз) та псоріаз, імунна реакція є звичайно зміщеною у бік гуморальної відповіді, коли фактично відповідна відповідь була б клітино-базисною. Тимчасове інгібування 11βΗβD1, локальне або системне, може бути використане для спрямування імунної системи на відповідну відповідь ([Mason, D. (1991) Immunology Today 12: 57-60; Rook та інші], дивись вище). Аналогічно, застосування 11βHSD1 інгібування, у цьому випадку тимчасове, спричинило б посилення імунної відповіді разом з імунізацією для забезпечення того, що, при необхідності, була б одержана клітино-базисна відповідь. 6. Зниження внутрішньоочного тиску Останні дані передбачають, що рівні глюкокортикоїдних цільових рецепторів та 11βHSD ферментів визначають схильність до глаукоми [Stokes, J. та інші (2000) Invest. Ophthalmol. 41: 1629-1638]. Крім того, інгібування 11βHSD1 нещодавно було представлене як новий підхід до зниження внутрішньоочного тиску [Walker Ε. А. та інші, poster P3698 at the Endocrine society meeting June 12-15, 1999, San Diego]. Внутрішнє приймання карбенок 15 солону, неспецифічного інгібітору 11βHSD1, як показали, приводить до зниження внутрішньоочного тиску на 20% у нормальних суб'єктів. У оці, експресія 11βHSD1 обмежується до базальних клітин ендотелію рогівки та непігментованого епітелію рогівки (місце вироблення води), до м'язу вій та до сфінктеру та м'язів розширення райдужної оболонки. На противагу, дистанційний ізофермент 11βHSD2 сильно експресується у непігментованому циліарному епітелію та ендотелію рогівки. Жоден з ферментів не був виявлений у трабекулярній сітчастій структурі, місце дренажу. Таким чином, передбачається, що 11βHSD1 грає роль у вироблення води, скоріше ніж дренажу, але наразі невідомо, чи це відбувається шляхом перешкоджання активації глюкокортикоїдного або мінералокортикоїдного рецептору, чи їх обох. 7. Знижений остеопороз Глюкокортикоїди грають важливу роль у розвиненні та функціонуванні скелету, але є шкідливими при надлишку. Глюкокортикоїд-викликана втрата кісткової маси відбувається, принаймні частково, через інгібування утворення кісток, що включає пригнічення проліферації остеобласту та колагенового синтезу [Kim, C.H., Cheng, S.L. та Kim, G.S. (1999) J. Endocrinol. 162: 371-379]. Негативний вплив на утворення кісткового вузлового потовщення міг би бути заблокований за допомогою неспецифічного інгібітору карбеноксолону, що передбачає важливу роль 11βHSD1 у глюкокортикоїдному ефекті [Bellows, C.G., Сіассіа, A. and Heersche, J.N.M. (1998) Bone 23: 119-125]. З інших даних припускають, що 11βHSD1 грає роль у забезпеченні достатньо високих рівнів активного глюкокортикоїду у остеокластах, і, таким чином, у збільшенні ресорбції кісток [Cooper, M.S. та інші (2000) Bone 27: 375-381]. Взяті разом, ці різні дані вказують на те, що інгібування 11βHSD1 може мати корисні ефекти проти остеопорозу за рахунок більше ніж одного механізму, які відбуваються паралельно 8. Зниження гіпертензії Жовчні кислоти інгібують 11βгідроксистероїдну дегідрогеназу типу 2. Це приводить до зміщення у загальному балансі у тілі на користь кортизолу відносно кортизону, як показано шляхом дослідження співвідношення сечових метаболітів [Quattropani, С, Vogt, В., Odermatt, Α., Dick, В., Frey, В.М., Frey. F J. (2001) J. Clin. Invest. Nov; 108 (9): 1299-305. "Reduced activity of 11betahydroxysteroid dehydrogenase in patients with cholestasis".]. Зниження активності 11βHSD1 у печінці за допомогою селективного інгібітору, як передбачають, обертає цей дисбаланс, та сильно протидіє симптомам, таким як гіпертензія, під час очікування хірургічного лікування видалення закупорки жовчних протоків. У [WO 99/65884] розкриті вуглець-заміщені амінотіазольні інгібітори циклін-залежних кіназ. Ці сполуки можуть бути, наприклад, використані для лікування раку, запалення та артриту. У [US 5,856,347] розкритий антибактеріальний препарат або бактерицидний засіб, що включає похідні 2амінотіазолу та/або їх сіль. Крім того, у [US 5,403,857] описані бензолсульфонамідні похідні, 86813 16 що мають 5-ліпоксигеназну інгібіторну активність. Додатково, тетрагідротіазоло[5,4-с]піридини розкриті у: [Analgesic tetrahydrothiazolo[5,4-c]pyridines. Fr. Addn. (1969), 18 pp, Addn. to Fr. 1498465. CODEN: FAXXA3; FR 94123 19690704 CAN 72:100685 AN 1970:100685 CAPLUS та 4,5,6,7Tetrahydrothiazolo[5,4-c]pyridines. Neth. Appl. (1967), 39 pp. CODEN: NAXXAN NL 6610324 19670124 CAN 68:49593, AN 1968: 49593 CAPLUS]. Однак, у жодному з описаних вище джерел не розкрито сполуки відповідно до даного винаходу, або їх застосування для лікування діабету, ожиріння, глаукоми, остеопорозу, когнітивних розладів, імунних розладів, депресії та гіпертензії. У [WO 98/16520] розкриті сполуки, що інгібують матриксні металопротеїнази (ММР) та TNF-α конвертуючий фермент (ТАСЕ). У [ЕР 0 749 964 А1 та US 5,962,490] описані сполуки, що мають антагоністичну активність до ендотелінового рецептору. У [WO 00/02851] розкриті сполуки, що пов'язані з порушеним cGMP балансом. Жодна з цих сполук не підпадає під формулу (І) відповідно до даного винаходу. Більш того, нічого не сказано про вплив на 11βHSD1. У [US 5 783 697] описані тіофенові похідні як інгібітори PGE2 та LTB4. Нічого не сказано про дію на 11βHSD1. У [ЕР 0 558 258, ЕР 0 569 193 та ЕР 1 069 114] розкриті ізоксазольні похідні як ендотелінові агоністи та антагоністи. Нічого не сказано про дію на 11βHSD1. 9. Загоєння рани Кортизол виконує широкий ряд метаболічних функцій та інших функцій. Велика кількість глюкокортикоїдних впливів продемонстрована на пацієнтах з тривалим підвищенням у плазмі глюкокортикоїдів, так званий "Синдром Кушинга (Cushing's syndrome)". Пацієнти з синдромом Кушинга мають тривале підвищення у плазмі глюкокортикоїдів та показують порушення переносимості глюкози, діабет типу 2, загальне ожиріння та остеопороз. Ці пацієнти також мають порушення у загоєнні ран та ламку шкіру [Ganong, W.F. Review of Medical Physiology. Eighteenth edition ed. Stamford, Connecticut: Appleton & Lange; 1997]. Як було показано, глюкокортикоїди підвищують ризик інфікування та затримують загоєння відкритих ран [Anstead, G.M. Steroids, retinoids, and wound healing. Adv Wound Care 1998; 11 (6): 27785]. Пацієнти, яких піддавали лікуванню глюкокортикоїдами, мають у 2-5 разів підвищений ризик ускладнень, при хірургічному лікуванні [Diethelm, A.G. Surgical management of complications of steroid therapy. Ann Surg 1977; 185(3): 251-63]. У [Європейській патентній заявці No.ЕР 0902288] описаний спосіб діагностики стану загоєння рани у пацієнта, що включає визначення рівнів кортизолу у рані. Автори роблять припущення, що підвищені рівні кортизолу у рідині рани, по відношенню до нормальних рівнів у плазмі у здорових пацієнтів, співвідносяться з великими ранами, що не загоюються [Hutchinson, T.C., Swaniker, H.P., Wound diagnosis by quantitating Cortisol in wound fluids. European patent application No.EP 0 902 288, опублікована 17.03.1999]. 17 У людей, 11β-HSD каталізує перетворення кортизолу у кортизон, та навпаки. Параленьна функція 11β-HSD у гризунів являє собою взаємне перетворення кортикостерону та 11дегідрокортикостерону [Frey, F.J., Escher, G., Frey, B.M. Pharmacology of 11 beta-hydroxysteroid dehydrogenase. Steroids 1994; 59(2): 74-9]. Два ізоферменти 11β-HSD, 11β-HSD1 та 11β-ΗSD2, охарактеризовані, та відрізняються один від одного функцією та розподіленням у тканинах [Albiston, A.L., Obeyesekere, V.R., Smith, R.E., Krozowski, Z.S. Cloning and tissue distribution of the human 11 betahydroxysteroid dehydrogenase type 2 enzyme. Моl Cell Endocrinol 1994;105(2): R11-7]. Подібно GR, 11β-HSD1 експресується у багатьох тканинах, таких як печінка, жирова тканина, кора наднирковика, гонади, легеня, гіпофіз, мозок, око тощо [Monder C, White PC. 11 beta-hydroxysteroid dehydrogenase. Vitam Horm 1993; 47: 187-271; Stewart, P.M., Krozowski, Z.S. 11 betaHydroxysteroid dehydrogenase. Vitam Horm 1999; 57: 249-324; Stokes, J., Noble, J., Brett, L., Phillips, C, Seckl, J.R., O'Brien, C, та інші Distribution of glucocorticoid and mineralocorticoid receptors and 11 beta-hydroxysteroid dehydrogenases in human and rat ocular tissues. Invest Ophthalmol Vis Sci 2000; 41(7): 1629-38]. Функція 11β-HSD1 полягає у точному налагодженні місцевої дії глюкокортикоїдів. Активність 11β-HSD була продемонстрована у шкірі людей та гризунів, у фібробластах людини та у тканині шкірних заглиблень щура [Hammami, M.M., Siiteri, P.K. Regulation of 11 betahydroxysteroid dehydrogenase activity in human skin fibroblasts: enzymatic modulation of glucocorticoid action. J Clin Endocrinol Metab 1991; 73(2): 326-34]; Cooper, M.S., Moore, J., Filer, Α., Buckley, C.D., Hewison, M., Stewart, P.M. 11 beta-hydroxysteroid dehydrogenase in human fibroblasts: expression and regulation depends on tissue of origin. ENDO 2003 Abstracts 2003; Teelucksingh, S., Mackie, A.D., Burt, D., Mclntyre, M.A., Brett, L., Edwards, C.R. Potentiation of hydrocortisone activity in skin by glycyrrhetinic acid. Lancet 1990; 335(8697): 1060-3; Slight, S.H., Chilakamarri, V.K., Nasr, S., Dhalla, A.K., Ramires, F.J., Sun, Y., та інші Inhibition of tissue repair by spironolactone: role of mineralocorticoids in fibrous tissue formation. Моl Cell Biochem 1998; 189 (1-2): 47-54). Загоєння рани включає послідовність подій, таких як запалення, проліферація фібробласту, секреція основних речовин, вироблення колагену, ангіогенез, зменшення рани та епітеліалізація. Воно може бути розділено на три фази: запальна, проліферативна та корекційна фази (розглянуто Anstead та співавторами, див. вище). У хворих після хірургічної операції, лікування глюкокортикоїдами підвищує ризик інфікування рани та затримку лікування відкритих ран. На тваринних моделях було показано, що примусовий стрес уповільнює загоєння рани шкіри та підвищує сприйнятливість до бактеріальної інфекції у процесі лікування рани. Ці ефекти були обернені шляхом лікування за допомогою антагоністу глюкокортикоїдного рецептору RU486 [Mercado, A.M., Quan, N., Padgett, D.A., Sheridan, J.F., Marucha, P.T. 86813 18 Restraint stress alters the expression of interleukin-1 and keratinocyte growth factor at the wound site: an in situ hybridization study. J Neuroimmunol 2002; 129(1-2): 74-83; Rojas, I.G., Padgett, D.A., Sheridan, J.F., Marucha, P.T. Stress-induced susceptibility to bacterial infection during cutaneous wound healing. Brain Behav Immun 2002; 16(1): 74-84]. Глюкокортикоїди забезпечують ці ефекти за рахунок пригнічення запалення, зниження міцності рани, інгібування контрактури рани та затриманої епітеліалізації (Anstead та інші, див. вище). Глюкокортикоїди впливають на загоєння рани шляхом впливу на вироблення або дію цитокінів та факторів росту, таких як IGF, TGF-β, EGF, KGF та PDGF [Beer, H.D., Fassler, R., Werner, S. Glucocorticoidregulated gene expression during cutaneous wound repair. Vitam Horm 2000; 59: 217-39; Hamon, G.A., Hunt, Т.К., Spencer, E.M. In vivo effects of systemic insulin-like growth factor-I alone and complexed with insulin-like growth factor binding protein-3 on corticosteroid suppressed wounds. Growth Regul 1993; 3(1): 53-6; Laato, M., Heino, J., Kahari, V.M., Niinikoski, J., Gerdin, B. Epidermal growth factor (EGF) prevents methylprednisolone-induced inhibition of wound healing. J Surg Res 1989; 47(4): 354-9; Pierce, G.F., Mustoe, T.A., Lingelbach, J., Masakowski, V.R., Gramates, P., Deuel, T.F. Transforming growth factor beta reverses the glucocorticoid-induced wound-healing deficit in rats: possible regulation in macrophages by plateletderived growth factor. Proc Natl Acad Sci U S A 1989; 86(7): 2229-33]. Також було показано, що глюкокортикоїди знижують синтез колагену у шкірі щура та миші in vivo та у фібробластах щура та людини [Oishi, Y., Fu, Z.W., Ohnuki, Y., Kato, Η., Noguchi, Т. Molecular basis of the alteration in skin collagen metabolism in response to in vivo dexamethasone treatment: effects on the synthesis of collagen type I and III, collagenase, and tissue inhibitors of metalloproteinases. Br J Dermatol 2002; 147(5): 85968]. У [WO 01/90090] розкриті тіазольні сполуки, які інгібують 11β-HSD1 людини, та можуть бути корисними для лікування розладів, таких як діабет, ожиріння, глаукома, остеопороз, когнітивні розлади та імунні розлади. Інші 11β-HSD1 інгібітори розкриті, наприклад, у [WO 01/90091; WO 01/90092; WO 01/90093; WO 01/90094; WO 03/043999; WO 03/044000; WO 03/044009; Патентній Заявці США No.2005/009821; WO 04/103980; WO 04/112784; WO 04/112781; WO 04/112785; WO 04/112783; WO 04/112782; WO 04/113310; WO 04/112779; та Шведській Патентній Заявці No.SE 0400227-5, поданій 4 лютого 2004]. Однак, застосування 11βHSD1 інгібіторів, відповідно до даного винаходу, для діабету, ожиріння, глаукоми, остеопорозу, когнітивних розладів, імунних розладів та загоєння рани раніше не було описано. Okawara та інші, не розкриваючи як інгібітори 11β-HSD1, описали одержання тіазол-5спіропропан-4(5Н)-онів, [див. J. Chem. Soc. Perkin Trans. I, 1733-1735 (1986)]. Сполуки відповідно до даного винаходу вирішують описані вище проблеми та являють собою новий клас розроблених сполук, які інгібують фер 19 мент 11-β-гідроксистероїдної дегідрогенази типу 1 людини (11β-HSD1), і можуть, таким чином, застосовуватись при лікуванні розладів, що мають відношення до 11β-HSD1 активності, таких як, не обмежуючись наведеними, діабет, ожиріння, глаукома, остеопороз, когнітивні розлади, імунні розлади, гіпертензія та загоєння рани. Одним з об'єктів даного винаходу є сполука загальної формули (І) в якій або (a) Z являє собою атом сірки, R1 являє собою атом водню, R2 вибирають з груп, таких як атом водню; С3-10-циклоалкіл, необов'язково незалежно заміщений за допомогою однієї або більше груп, таких як С1-8-алкіл та арил; С3-10-циклоалкіл-С1-8алкіл; арил; арил-С1-8-алкіл; гетероцикліл; гетероцикліл-С1-8-алкіл; де будь-який арильний або гетероциклільний залишок необов'язково незалежно заміщений за допомогою однієї або більше груп, таких як С1-8-алкіл та галоген; або R1 та R2 утворюють разом з атомом азоту, до якого вони прикріплені, моноциклічний гетероцикліл, необов'язково незалежно заміщений за допомогою однієї або більше груп, таких як арил-С1-8-алкіл, С1-8алкіл та галоген; R3 та R4 кожен незалежно вибирають з груп, таких як атом водню; С1-8-алкіл; С3-10циклоалкіл-С1-8-алкіл; ціано-С1-8-алкіл; арил; арилС1-8-алкіл; гетероцикліл-С1-8-алкіл; гетероарил-С1-8алкіл; або R3 та R4 утворюють разом з атомом вуглецю, до якого вони прикріплені, С3-10-циклоалкіл, де будь-який арильний залишок необов'язково незалежно заміщений за допомогою однієї або більше гідрокси груп; або (b) Z являє собою атом кисню, R1 являє собою атом водню, R2 вибирають з груп, таких як атом водню; С5-10-циклоалкіл, необов'язково незалежно заміщений за допомогою однієї або більше груп, таких як С1-8-алкіл та арил; С3-10-циклоалкіл-С1-8алкіл; арил, але не незаміщена фенільна група; арил-С1-8-алкіл; гетероцикліл; гетероцикліл-С3-8алкіл; де будь-який арильний або гетероциклільний залишок необов'язково незалежно заміщений за допомогою однієї або більше груп, таких як С1-8алкіл та галоген; R3 та R4 кожен незалежно вибирають з груп, таких як атом водню; С1-8-алкіл; С3-10циклоалкіл-С1-8-алкіл; ціано-С1-8-алкіл; арил, але не незаміщена фенільна група; арил-С1-8-алкіл; гетероцикліл-С1-8-алкіл; гетероарил-С1-8-алкіл; або R3 та R4 утворюють разом з атомом вуглецю, до якого вони прикріплені, С3-10-циклоалкіл, де будьякий арильний залишок необов'язково незалежно заміщений за допомогою однієї або більше гідрокси груп; та її фармацевтично прийнятні солі, сольвати, гідрати, геометричні ізомери, таутомери, оптичні ізомери, N-оксиди та форми проліків; за умови, що: коли R1 являє собою водень та 86813 20 Ζ являє собою сірку та R3=R4=метил, тоді R2 не являє собою феніл; Ζ являє собою сірку та R3=R4=метил, тоді R2 не являє собою 4-йодфеніл; Ζ являє собою сірку та R3=R4=метил, тоді R2 не являє собою феніл; Ζ являє собою атом сірки, R3=eтил та R4=H, тоді R2 не являє собою 3-метилфеніл; Ζ являє собою кисень та R3=H, тоді R4 не являє собою метил. Вважається за краще, коли: R1 та R2 кожен незалежно вибирають з групи, яка включає атом водню, циклогексил, циклогептил, циклооктил, 2,2,3,3-тетраметилциклопропіл, 1-(4-хлорфеніл)циклобутил, біцикло[2.2.1]гепт-2ил, трицикло[3.3.1.0~3,7~]нон-3-іл, циклогексилметил, феніл, 2-метилфеніл, 3-метилфеніл, 2ізопропілфеніл, 2-фторфеніл, 2-хлорфеніл, 2фенілпропіл, 2-хлорбензил, 4-хлорбензил, 4(2,2,6,6-тетраметил)піперидил, 2-морфолініл-4ілетил, або R1 та R2 утворюють разом з атомом азоту, до якого вони прикріплені, морфолініл, азокан або 4-бензилпіперидил; R3 та R4 кожен незалежно вибирають з груп, таких як атом водню, метил, етил, ізопропіл, ізобутил, трет-бутил, циклогексилметил, ціанометил, феніл, 2-гідроксифеніл, бензил, 2-гідроксибензил, 4-гідроксибензил, 3,4-дигідроксибензил, 1Німідазол-4-ілметил, індол-3-ілметил, 3піридилметил, або R3 та R4 утворюють разом з атомом вуглецю, до якого вони прикріплені, циклопропіл, циклобутил, циклопентил, циклогексил; за умови, що коли Ζ являє собою атом кисню, тоді жоден з R2, R3, та R4 не являє собою феніл. У кращому втіленні даного винаходу, коли Ζ являє собою сірку та обидва R та R4 являють собою метил або обидва R3 та R4 являють собою феніл, тоді R2 як арильну групу вибирають з груп, таких як 2-метилфеніл, 3-метилфеніл, 2ізопропілфеніл, 2-фторфеніл, та 2-хлорфеніл. Коли Ζ являє собою атом сірки, R3 являє собою етил та R4 являє собою атом водню, тоді R2 як арильну групу вибирають з груп, таких як 2-метилфеніл, 2ізопропілфеніл, 2-фторфеніл та 2-хлорфеніл. У кращому втіленні даного винаходу, коли Ζ являє собою атом кисню, кожен з R2, R3, та R4 як арильну групу вибирають з груп, таких як 2метилфеніл, 3-метилфеніл, 2-ізопропілфеніл, 2фторфеніл та 2-хлорфеніл. Коли Ζ являє собою кисень та R3 являє собою атом водню, тоді R як С1-8-алкільну групу вибирають з С2-8-алкільної групи. Кращі сполуки являють собою Приклади 138,40-66, 68 та 73-79. Іншим об'єктом даного винаходу є спосіб одержання сполуки, показаної вище, що включає принаймні одну з наступних стадій: a) введення у реакцію ізотіоціанату з амонієм з одержанням тіосечовини, b) введення у реакцію аміну з етоксикарбонілізотіоціанатом з одержанням тіосечовини, c) введення у реакцію тіосечовини з αбромкарбоновою кислотою з одержанням тіазолону, 21 86813 d) введення у реакцію тіосечовини з αбромкарбоновим естером з одержанням а тіазолону, е) введення у реакцію амінокислоти з одержанням α-бромкарбонової кислоти, f) введення у реакцію тіосечовини з 3-бром-2кумароном, g) введення у реакцію гуанідину з αгідроксискладним ефіром з одержанням первинного аміно-оксазолону, h) введення у реакцію первинного амінооксазолону та аміну з одержанням вторинного або третинного аміно-оксазолону, і) введення у реакцію тіосечовини та хлорангідриду α-бромкарбонової кислоти з одержанням тіазолону, та j) введення у реакцію карбонової кислоти з тіонілхлоридом та N-бромсукцинімідом з одержанням складного ефіру α-бромкарбонової кислоти. Додаткове втілення відноситься до сполуки загальної формули (II): (II) у якій: X являє собою S або О; R5 вибирають з атому водню, C1-C8 алкілу, С310-циклоалкілу, С3-10-циклоалкіл-С1-8-алкілу, арилу, арил-С1-8-алкілу, гетероциклілу, гетероцикліл-С1-8алкілу та галоалкілу; де будь-який арильний, циклоалкільний або гетероциклільний залишок є необов'язково незалежно заміщеним за допомогою однієї або більше груп, таких як С1-8-алкіл, арил, галоген, гало-С1-С8алкіл, HO-С1-С8-алкіл, R8R9N-С1-С8-алкіл, С1-С8алкіл-OR10, -OR10, (С3-С10)-циклоалкіл або С1-С8алкіл-сульфоніл; R6 вибирають з групи, що включає С1-8-алкіл, С1-8-алкокси, С3-10-циклоалкіл, гетероцикліл, С3-10циклоалкіл-С1-8-алкіл, CN-С1-8-алкіл, арил, арил-С18-алкіл, гетероцикліл-С1-8-алкіл та галоалкіл; R7 вибирають з групи, що включає -NR8R9, гало, С1-8-алкіл, -(CR8R9)n-OR8, -S-Ci-Cg-алкіл, С3-10циклоалкіл, гетероцикліл, С3-10-циклоалкіл-С1-8алкіл, ціано-С1-8-алкіл, арил, арил-С1-8-алкіл, гетероцикліл-С1-8-алкіл, гетероцикліл-С(О)-С1-8-алкіл, гетероцикліл-SО2-С1-8-алкіл, С1-8-галоалкіл, R8R9NС1-8-aлкiл, НО-С1-8-алкіл, -С(О)-С3-10-циклоалкіл, С(О)-С1-С8-галоалкіл, -(CR8R9)n-Y-(CR8R9)n8 9 гетероцикліл та -(CR R )n-Y-(CR8R9)n-C(O)-R8 (де n являє собою 0-5, Υ являє собою NR10, О або S); де будь-який арильний, алкільний, гетероциклільний або циклоалкільний залишок необов'язково заміщений за допомогою однієї або більше груп, таких як -С1-С8-алкіл, -гало, -ОН, -OR10, 22 С1-С8-алкіл-SО2-, -SО2-арил, -C(O)-(CR8R9)n-карбамат, -С(О)-О-С1-С8-алкіл, -С(О)-С1-С8-алкіл, -C(O)-(CR8R9)n-C(O)-NR8R9, -C(O)-(CR8R9)n-NR8-C(O)-С1-С8-алкіл -C(O)-(CR8R9)n-NR8R9, -С(О)-С3-С10-циклоалкіл, -С(О)-арил, -C(O)-(CR8R9)n-гетероцикліл, -С1-С8-алкіл-OR8, -С(О)-гало-С1-С8-алкіл або -C(O)-(CR8R9)n-apил, де будь-який арильний, алкільний, циклоалкільний або гетероциклільний залишок є необов'язково незалежно заміщеним за допомогою однієї або більше груп, таких як С1-8-алкіл, арил, галоген, -NR10R10, С1-С8-галоалкіл, НО-С1-С8-алкіл, R8R9NС1-С8-алкіл, С1-С8-aлкiл-OR10, -OR10, (С3-С10)циклоалкіл або С1-С8-алкіл-сульфоніл, -O(CR8R9)n-гетероцикліл, -O-(CR8R9)n-C(O)-NR8R9, O-(CR8R9)n-NR8R9, -Y-(CR8R9)n-NR8-C(O)-С1-С88 9 aлкiл, -Y-(CR R )n-гетероцикліл, -O-(CR8R9)n8 9 8 9 NR R , С1-С8-алкіл-SО2, або -O-(CR R )n-N-C(O)гeтepoциклiл; у якій R8 та R9 кожен незалежно вибирають з груп, таких як атом водню, С1-С8-алкіл, С1С8алкокси, -NR10R10, -S-(С1-С8)алкіл, арил та гетероцикліл; будь-який алкіл, алкокси, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає -гало, незаміщений С1-С8-алкіл, незаміщений С1-С8-алкокси, незаміщений С1-С8-тіоалкокси та незаміщений арил(С1-С4)алкіл; у якій R10 незалежно вибирають з групи, що включає водень, С1-С8-алкіл, арил-С1-С8-алкіл, С1С8-алкокси, -S-(С1-С8)алкіл, гетероцикліл та арил; будь-який алкіл, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає -гало, незаміщений С1-С8-алкіл, незаміщений С1-С8алкокси, незаміщений С1-С8-тіоалкокси та незаміщений арил(С1-С4)алкіл; або R6 та R7 утворюють, разом з атомом вуглецю, до якого вони прикріплені, насичений, частково ненасичений або ненасичений С3-10циклоалкіл або насичений, частково ненасичений або ненасичений С4-С14-гетероцикліл; де циклоалкіл або гетероцикліл може бути необов'язково заміщений за допомогою однієї або більше груп, таких як С1-С8-алкіл, арил, С1-С8галоалкіл, арил-С1-С3-алкіл, С3-С10-циклоалкіл. OR8, =O, =NR8, =N-OR8, -NR8R9, -SR8, -гало, OC(O)R8, -C(O)R8, -CO2R8, -CONR8R9, 8 9 9 8 8 OC(O)NR R , -NR C(O)R , -NR C(O)NR8R9, NR8SO2NR8R9, -NR8CO2R9, -NHC(NH2)=NH, NR8C(NH2)=NH, -NHC(NH2)=NR8, -S(O)R8, -SO2R8, SO2NR8R9, -NR8SO2R9, -CN та -NO2; та її фармацевтично прийнятних солей, сольватів, гідратів, геометричних ізомерів, таутомерів, оптичних ізомерів, N-оксидів та форм проліків, за умови, що: коли 23 86813 X являє собою S, R6=R7=мeтил, тоді R5 не являє собою феніл або 4-йодфеніл, X являє собою S, R6=R7=фeнiл, тоді R5 не являє собою феніл, та X являє собою S, R6 та R7 об'єднуються разом з утворенням циклопропільного кільця, тоді R5 не являє собою н-бутил, циклогексил, бензил, феніл або нафтил. У іншому втіленні винахід стосується сполуки загальної формули (III): (III) у якій: R5 вибирають з груп, таких як атом водню, С1С8-алкіл, С3-10-циклоалкіл, С3-10-циклоалкіл-С1-8алкіл, арил, арил-С1-8-алкіл, гетероцикліл, гетероцикліл-С1-8-алкіл та галоалкіл; де будь-який арильний, циклоалкільний або гетероциклільний залишок є необов'язково незалежно заміщеним за допомогою однієї або більше груп, таких як С1-8-алкіл, арил, галоген, гало-С1-С8алкіл, HO-С1-С8-алкіл, алкіл-С1-С8-алкіл, С1-С8алкіл-OR10, -OR10, (С3-С10)-циклоалкіл або С1-С8алкіл-сульфоніл; R6 вибирають з групи, що включає С1-8-алкіл. С1-8-алкокси, С3-10-циклоалкіл, гетероцикліл, С3-10циклоалкіл-С1-8-алкіл, CN-С1-8-алкіл, арил, арил-С18-алкіл, гетероцикліл-С1-8-алкіл та галоалкіл; R7 вибирають з групи, що включає -NR8R9, гало, С1-8-алкіл, -(CR8R9)n-OR8, -S-C1-C8-алкіл, С3-10циклоалкіл, гетероцикліл, С3-10-циклоалкіл-С1-8алкіл, ціано-С1-8-алкіл, арил, арил-С1-8-алкіл, гетероцикліл-С1-8-алкіл, гетероцикліл-С(О)-С1-8-алкіл, гетероцикліл-SО2-С1-8-алкіл, С1-8-галоалкіл, R8R9NС1-8-алкіл, НО-С1-8-алкіл, -С(О)-С3-С10-циклоалкіл, С(О)-С1-С8-галоалкіл, -(CR8R9)n-Y-(CR8R9)n8 9 гeтepoциклiл та -(CR R )n-Y-(CR8R9)n-C(O)-R8 (де n являє собою 0-5, Υ являє собою NR10, О або S); де будь-який арильний, алкільний, гетероциклільний або циклоалкільний залишок є необов'язково заміщеним за допомогою однієї або більше груп, таких як -С1-С8-алкіл, -гало, -ОН, -OR10, С1-С8-алкіл-SО2-, -SО2-арил, -C(O)-(CR8R9)n-карбамат, -С(О)-О-С1-С8-алкіл, -С(О)-С1-С8-алкіл, -C(O)-(CR8R9)n-C(O)-NR8R9, -C(O)-(CR8R9)n-NR8-C(O)-С1-С8-алкіл -C(O)-(CR8R9)n-NR8R9, -С(О)-С3-С10-циклоалкіл, -С(О)-арил, -C(O)-(CR8R9)n-гетероцикліл, 24 -С1-С8-алкіл-OR8, -С(О)-гало-С1-С8-алкіл або -C(O)-(CR8R9)n-арил, де будь-який арильний, алкільний, циклоалкільний або гетероциклільний залишок є необов'язково незалежно заміщеним за допомогою однієї або більше груп, таких як С1-8-алкіл, арил, галоген, -NR10R10, С1-С8-галоалкіл, НО-С1-С8-алкіл, R8R9NС1-С8-алкіл, С1-С8-алкіл-OR10, -OR10, (С3-С10)циклоалкіл або С1-С8-алкіл-сульфоніл, -O(CR8R9)n-гетероцикліл, -O-(CR8R9)n-C(O)-NR8R9, O-(CR8R9)n-NR8R9, -Y-(CR8R9)n-NR8-C(O)-С1-С88 9 алкіл, -Y-(CR R )n-гетероцикліл, -O-(CR8R9)nNR8R9, С1-С8-алкіл-SО2, або -O-(CR8R9)n-N-C(O)гетероцикліл; де R8 та R9 кожен незалежно вибирають з груп, таких як атом водню, С1-С8-алкіл, С1-С8алкокси, -NR10R10, -S-(С1-С8)алкіл, арил та гетероцикліл; будь-який алкіл, алкокси, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає -гало, незаміщений С1-С8-алкіл, незаміщений С1-С8-алкокси, незаміщений С1-С8-тіоалкокси та незаміщений арил(С1-С4)алкіл; де R10 незалежно вибирають з групи, що включає водень, С1-С8-алкіл, арил-С1-С8-алкіл, С1С8-алкокси, -S-(С1-С8)алкіл, гетероцикліл та арил; будь-який алкіл, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає -гало, незаміщений С1-С8-алкіл, незаміщений С1-С8алкокси, незаміщений С1-С8-тіоалкокси та незаміщений арил(С1-С4)алкіл; або R6 та R7 утворюють, разом з атомом вуглецю, до якого вони прикріплені, насичений, частково ненасичений або ненасичений С3-10циклоалкіл або насичений, частково ненасичений або ненасичений C4-C14-гетероцикліл; де циклоалкіл або гетероцикліл може бути необов'язково заміщений за допомогою однієї або більше груп, таких як С1-С8-алкіл, арил, С1-С8галоалкіл, арил-С1-С8-алкіл, С3-С10-циклоалкіл, OR8, =О, =NR8, =N-OR8, -NR8R9, -SR8, -гало, OC(O)R8, -C(O)R8, -CO2R8, -CONR8R9, 8 9 9 8 8 OC(O)NR R , -NR C(O)R , -NR C(O)NR8R9, NR8SO2NR8R9, -NR8CO2R9, -NHC(NH2)=NH, NR8C(NH2)=NH, -NHC(NH2)=NR8, -S(O)R8, -SO2R8, SO2NR8R9, -NR8SO2R9, -CN та -NО2; та її фармацевтично прийнятних солей, сольватів, гідратів, геометричних ізомерів, таутомерів, оптичних ізомерів, N-оксидів та форм проліків, за умови, що: коли R6=R7=мeтил, тоді R5 не являє собою феніл або 4-йодфеніл, R6=R7=феніл, тоді R5 не являє собою феніл, та R6 та R7 об'єднуються разом з утворенням циклопропільного кільця, тоді R не являє собою нбутил, циклогексил, бензил, феніл або нафтил. Інше втілення являє собою сполуку загальної формули (IV): 25 86813 (IV) у якій: R5 вибирають з груп, таких як атом водню, С1С8-алкіл, С3-10-циклоалкіл, С3-10-циклоалкіл-С1-8алкіл, арил, арил-С1-8-алкіл, гетероцикліл, гетероцикліл-С1-8-алкіл та галоалкіл; де будь-який арильний, циклоалкільний або гетероциклільний залишок є необов'язково незалежно заміщеним за допомогою однієї або більше груп, таких як С1-8-алкіл, арил, галоген, гало-С1-С8алкіл, HO-С1-С8-алкіл, R8R9N-С1-С8-алкіл, С1-С8алкіл-OR10, -OR10, (С3-С10)-циклоалкіл або С1-С8алкіл-сульфоніл; R6 вибирають з групи, що включає С1-8-алкіл, С1-8-алкокси, С3-10-циклоалкіл, гетероцикліл, С3-10циклоалкіл-С1-8-алкіл, CN-С1-8-алкіл, арил, арил-С18-алкіл, гетероцикліл-С1-8-алкіл та галоалкіл; R7 вибирають з групи, що включає –NR8R9, гало, С1-8-алкіл, -(CR8R9)n-OR8, -S-С1-С8-алкіл, С3-10циклоалкіл, гетероцикліл, С3-10-циклоалкіл-С1-8алкіл, ціано-С1-8-алкіл, арил, арил-С1-8-алкіл, гетероцикліл-С1-8-алкіл, гетероцикліл-С(О)-С1-8-алкіл, гетероцикліл-SО2-С1-8-алкіл, С1-8-галоалкіл, R8R9NС1-8-алкіл, НО-С1-8-алкіл, -С(О)-С3-С10-циклоалкіл, С(О)-С1-С8-галоалкіл, -(CR8R9)n-Y-(CR8R9)nгетероцикліл та -(CR8R9)n-Y-(CR8R9)n-C(O)-R8 (де n являє собою 0-5, Υ являє собою NR10, О або S); де будь-який арильний, алкільний, гетероциклільний або циклоалкільний залишок є необов'язково заміщеним за допомогою однієї або більше груп, таких як -С1-С8-алкіл, -гало, -ОН, -OR10, С1-С8-алкіл-SО2-, -SO2-арил, -C(O)-(CR8R9)n-Карбамат, -С(О)-О-С1-С8-алкіл, -С(О)-С1-С8-алкіл, -C(O)-(CR8R9)n-C(O)-NR8R9, -C(O)-(CR8R9)n-NR8-C(O)-С1-С8-алкіл -C(O)-(CR8R9)n-NR8R9, -С(О)-С3-С10-циклоалкіл, -С(О)-арил, -C(O)-(CR8R9)n-гетероцикліл, -С1-С8-алкіл-OR8, -С(О)-гало-С1-С8-алкіл або -C(O)-(CR8R9)n-apил, де будь-який арильний, алкільний, циклоалкільний або гетероциклільний залишок є необов'язково незалежно заміщеним за допомогою однієї або більше груп, таких як С1-8-алкіл, арил, галоген, -NR10R10, С1-8-галоалкіл, НО-С1-С8-алкіл, R8R9N-С1С8-алкіл, С1-С8-aлкiл-OR10, -OR10, (С3-С10)циклоалкіл або С1-С8-алкіл-сульфоніл, -О(CR8R9)n-гетероцикліл, -O-(CR8R9)n-C(O)-NR8R9, O-(CR8R9)n-NR8R9, -Y-(CR8R9)n-NR8-C(O)-С1-С88 9 алкіл, -Y-(CR R )n-гeтepoциклiл, -O-(CR8R9)n 26 NR8R9, С1-С8-алкіл-SО2, або -O-(CR8R9)n-N-C(O)гетероцикліл; у якій R8 та R9 кожен незалежно вибирають з груп, таких як атом водню, С1-С8-алкіл, С1-С8алкокси, -NR10R10, -S-(С1-С8)алкіл, арил та гетероцикліл; будь-який алкіл, алкокси, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає -гало, незаміщений С1-С8-алкіл, незаміщений С1-С8-алкокси, незаміщений С1-С8-тіоалкокси та незаміщений арил(С1-С4)алкіл; у якій R10 незалежно вибирають з групи, що включає водень, С1-С8-алкіл, арил-С1-С8-алкіл, С1С8-алкокси, -S-(С1-С8)алкіл, гетероцикліл та арил; будь-який алкіл, гетероцикліл або арил може бути заміщений за допомогою від одного до трьох замісників, вибраних з групи, що включає -гало, незаміщений С1-С8-алкіл, незаміщений С1-С8алкокси, незаміщений С1-С8-тіоалкокси та незаміщений арил(С1-С4)алкіл; або R6 та R7 утворюють, разом з атомом вуглецю, до якого вони прикріплені, насичений, частково ненасичений або ненасичений С3-10циклоалкіл або насичений, частково ненасичений або ненасичений C4-C14-гетероцикліл; де циклоалкіл або гетероцикліл може бути необов'язково заміщений за допомогою однієї або більше груп, таких як С1-С8-алкіл, арил, С1-С8галоалкіл, арил-С1-С8-алкіл, С3-С10-циклоалкіл, OR8, =O, =NR8, =N-OR8, -NR8R9, -SR8, -гало, OC(O)R8, -C(O)R8, -CO2R8, -CONR8R9, OC(O)NR8R9, -NR9C(O)R8, -NR8C(O)NR8R9, NR8SO2NR8R9, -NR8CO2R9, -NHC(NH2)=NH, NR8C(NH2)=NH, -NHC(NH2)=NR8, -S(O)R8, -SO2R8, SO2NR8R9, -NR8SO2R9, -CN та -NO2; та її фармацевтично прийнятні солі, сольвати, гідрати, геометричні ізомери, таутомери, оптичні ізомери, N-оксиди та форми проліків. Одне втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R5 вибирають з групи, що включає циклогексил, циклогептил, циклооктил, 2,2,3,3-тетраметилциклопропіл, 1-(4хлорфеніл)циклобутил, біцикло[2.2.1]гепт-2-ил, трицикло[3.3.1.0~3,7~]нон-3-іл, циклогексилметил, феніл, 2-метилфеніл, 3-метилфеніл, 2ізопропілфеніл, 2-фторфеніл, 2-хлорфеніл, 2фенілпропіл, 2-хлорбензил, 4-хлорбензил, 4(2,2,6,6-тетраметил)піперидил, 2-морфолініл-4ілетил та тетрагідропіран-4-іл-метил; та R6 та R7 кожен незалежно вибирають з групи, що включає метил, етил, ізопропіл, ізобутил, третбутил, циклогексилметил, ціанометил, феніл, 2гідроксифеніл, бензил, 2-гідроксибензил, 4гідроксибензил, 3,4-дигідроксибензил, 1Н-імідазол4-ілметил, індол-3-ілметил, 3-піридилметил; або R6 та R7 утворюють разом з атомом вуглецю, до якого вони прикріплені, циклопропіл, циклобутил, циклопентил, циклогексил. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 являє собою метил та R7 являє собою ізопропіл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R5 вибирають з групи, що включає необов'язково заміщений C1-C8 алкіл, 27 необов'язково заміщений С3-С10 циклоалкіл та необов'язково заміщений арил. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R5 являє собою С3-С8 алкіл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R5 являє собою необов'язково заміщений феніл-(CR10аR10а)1-3-; та у якій R10а незалежно вибирають з групи, що включає Н, метил, фтор, або R10а та R10а можуть об'єднуватися разом з утворенням С3-С6-циклоалкільного кільця. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R5 являє собою (необов'язково заміщений феніл)-(С(СН3)2)- (необов'язково заміщений феніл)-(СНСН3) або бензил. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R5 являє собою С3-С10 циклоалкіл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R5 вибирають з групи, що включає циклогексил, норборніл та адамантил. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R5 являє собою норборніл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R5 являє собою арил. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R5 вибирають з групи, що включає необов'язково заміщений феніл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 вибирають з групи, що включає C1-C8 алкіл, С3-С10 циклоалкіл, насичений або частково ненасичений гетероцикліл, гетероарил та арил. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 являє собою С1-С8 алкіл. Переважно, алкіл вибирають з групи, що включає метил, етил, н-пропіл та ізо-пропіл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 являє собою С3-С10 циклоалкіл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 вибирають з групи, що включає циклогексил, норборніл та адамантил. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 являє собою насичений або частково ненасичений 5 або 6-членний гетероцикліл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 вибирають з групи, що включає тетрагідрофурил, піперидиніл та тетрагідропіраніл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 являє собою 5 або 6 членне гетероарильне кільце. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 вибирають з групи, що включає піридил, фурил та піроліл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 являє собою С6-С10 арил. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 вибирають з групи, 86813 28 що включає необов'язково заміщений феніл та необов'язково заміщений бензил. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R7 вибирають з групи, що включає –NR8R9, C1-C8 алкокси, гетероцикліл та гетероцикліл- C1-C8-алкіл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R7 являє собою -NR8R9. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R8 являє собою метил, етил, ізопропіл або бутил. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R8 являє собою ізопропіл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R9 являє собою метил або Н. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R7 являє собою C1-C8 алкокси. Інше втілення відноситься до сполук Формули (І), (II), (НІ) або (IV), у якій: R7 являє собою метокси, етокси, пропокси або бутокси. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R7 являє собою нбутокси. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R7 являє собою насичений або частково ненасичений 5 або 6-членний гетероцикліл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R7 являє собою піролідиніл, морфолініл або піперидиніл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R7 являє собою піперидиніл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R7 являє собою гетероцикліл-C1-C8-алкіл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R7 являє собою гетероцикліл-С1-С3-алкіл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R7 являє собою необов'язково заміщений піперидин-4-іл-СН2-. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R7 являє собою R8піперидин-4-іл-СН2-. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 та R7 утворюють, разом з атомом вуглецю, до якого вони прикріплені, необов'язково ненасичений С3-10-циклоалкіл або необов'язково ненасичений С4-С14 гетероцикліл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 та R7 утворюють необов'язково ненасичений С3-С10 циклоалкіл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 та R7 утворюють шести-членне спіро кільце. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 та R7 утворюють п’яти-членне спіро кільце. 29 Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: R6 та R7 утворюють необов'язково ненасичений С4-С14 гетероцикліл. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: необов'язково ненасичений С4-С14 гетероцикліл являє собою шестичленне гетероциклічне спіро кільце. Інше втілення відноситься до сполук Формули (І), (II), (III) або (IV), у якій: С4-С14 гетероцикліл являє собою циклічне амідне спіро кільце. Одне втілення відноситься до сполуки, яку вибирають з групи, що включає: 2-(біцикло[2.2.1]гепт-2-иламіно)-5-ізопропіл1,3-тіазол-4(5Н)-он, 2-(біцикло[2.2.1]гепт-2-иламіно)-5-етил-1,3тіазол-4(5Н)-он, 2-(біцикло[2.2.1]гепт-2-иламіно)-5-феніл-1,3тіазол-4(5Н)-он, 2-(циклогексиламіно)-5-етил-1,3-тіазол-4(5Н)он, 2-(біцикло[2.2.1]гепт-2-иламіно)-5,5-диметил1,3-тіазол-4(5Н)-он, 5-Ізопропіл-2-(трицикло[3.3.1.0~3,7~]нон-3іламіно)-1,3-тіазол-4(5Н)-он, 6-(трицикло[3.3.1.0~3,7~]нон-3-іламіно)-5-тіа-7азаспіро[3.4]окт-6-ен-8-он, 2-(Трицикло[3.3.1.0~3,7~]нон-3-іламіно)-1,3тіазол-4(5Н)-он, 6-(Циклооктиламіно)-5-тіа-7-азаспіро[3.4]окт-6ен-8-он, 6-(Циклогептиламіно)-5-тіа-7-азаспіро[3.4]окт6-ен-8-он, 6-(Біцикло[2.2.1]гепт-2-иламіно)-5-тіа-7азаспіро[3.4]окт-6-ен-8-он, 6-[(2,2,3,3-Тетраметилциклопропіл)аміно]-5тіа-7-азаспіро[3.4]окт-6-ен-8-он, 6-[(2-Метилфеніл)аміно]-5-тіа-7азаспіро[3.4]окт-6-ен-8-он, 2-[(циклогексилметил)аміно]-5,5-диметил-1,3тіазол-4(5Н)-он, 2-[(2-фторфеніл)аміно]-5-ізопропіл-1,3-тіазол4(5Н)-он, 2-[(циклогексилметил)аміно]-5-(2гідроксифеніл)-1,3-тіазол-4(5Н)-он, (5S)-2-(циклогептиламіно)-5-метил-1,3-тіазол4(5Н)-он, (5R)-2-(циклогептиламіно)-5-метил-1,3-тіазол4(5Н)-он, 2-(циклогептиламіно)-5-етил-1,3-тіазол-4(5Н)он, 2-(циклогептиламіно)-5-ізопропіл-1,3-тіазол4(5Н)-он, 5-трет-бутил-2-(циклогептиламіно)-1,3-тіазол4(5Н)-он, 2-(циклооктиламіно)-5-етил-1,3-тіазол-4(5Н)он, 5-ізопропіл-2-[(2-ізопропілфеніл)аміно]-1,3тіазол-4(5Н)-он, 5-етил-2-[(2-ізопропілфеніл)аміно]-1,3-тіазол4(5Н)-он, 2-[(2-хлорфеніл)аміно]-5-етил-1,3-тіазол-4(5Н)он, 5-етил-2-[(2-метилфеніл)аміно]-1,3-тіазол4(5Н)-он, 86813 30 5-ізопропіл-2-[(2,2,3,3тетраметилциклопропіл)аміно]-1,3-тіазол-4(5Н)-он, 2-(біцикло[2.2.1]гепт-2-иламіно)-5-(4гідроксибензил)-1,3-тіазол-4(5Н)-он, 5-[(циклогексилметил)аміно]-4-тіа-6азаспіро[2.4]гепт-5-ен-7-он, 2-(циклогептиламіно)-5-(3,4дигідроксибензил)-1,3-тіазол-4(5Н)-он, 2-(циклогептиламіно)-5-(1Н-імідазол-4ілметил)-1,3-тіазол-4(5Н)-он, 2-(циклогептиламіно)-5-ізобутил-1,3-тіазол4(5Н)-он, 2-(циклогептиламіно)-5-(1Н-індол-3-ілметил)1,3-тіазол-4(5Н)-он, 2-(циклогептиламіно)-5-(4-гідроксибензил)-1,3тіазол-4(5Н)-он, (5R)-2-(циклогептиламіно)-5(циклогексилметил)-1,3-тіазол-4(5Н)-он, 2-(циклооктиламіно)-5-(4-гідроксибензил)-1,3тіазол-4(5Н)-он, (5S)-2-(циклогептиламіно)-5(циклогексилметил)-1,3-тіазол-4(5Н)-он, [2-(циклогептиламіно)-4-оксо-4,5-дигідро-1,3тіазол-5-іл]ацетонітрил, 2-(циклогептиламіно)-5-(піридин-3-ілметил)1,3-тіазол-4(5Н)-он, 5-Ізопропіл-2-[(2-метилфеніл)аміно]-1,3-тіазол4(5Н)-он, 2-(Циклооктиламіно)-5,5-диметил-1,3-тіазол4(5Н)-он, 2-(Циклооктиламіно)-5-ізопропіл-1,3-тіазол4(5Н)-он, 2-(Біцикло[2.2.1]гепт-2-иламіно)-1-тіа-3азаспіро[4.5]дец-2-ен-4-он, 2-(Трицикло[3.3.1.0~3,7~]нон-3-іламіно)-1-тіа3-азасшро[4.5]дец-2-ен-4-он, 2-(Циклогептиламіно)-1-тіа-3-азаспіро[4.5]дец2-ен-4-он, 2-(Циклооктиламіно)-1-тіа-3-азаспіро[4.5]дец2-ен-4-он, 2-{[1-(4-Хлорфеніл)циклобутил]аміно}-5ізопропіл-1,3-тіазол-4(5Н)-он, 6-{[1-(4-Хлорфеніл)циклобутил]аміно}-5-тіа-7азаспіро[3.4]окт-6-ен-8-он, 2-(циклогептиламіно)-5,5-діетил-1,3-тіазол4(5Н)-он, (5S)-5-ізопропіл-2-{[(2S)-2-фенілпропіл]аміно}1,3-тіазол-4(5Н)-он, (5R)-5-етил-2-{[(2S)-2-фенілпропіл]аміно}-1,3тіазол-4(5Н)-он, (5S)-5-етил-2-{[(2S)-2-фенілпропіл]аміно}-1,3тіазол-4(5Н)-он, (5R)-5-ізопропіл-2-{[(2R)-2-фенілпропіл]аміно}1,3-тіазол-4(5Н)-он, (5S)-5-ізопропіл-2-{[(2R)-2-фенілпропіл]аміно}1,3-тіазол-4(5Н)-он, (5R)-5-етил-2-{[(2R)-2-фенілпропіл]аміно}-1,3тіазол-4(5Н)-он, (5S)-5-етил-2-{[(2R)-2-фенілпропіл]аміно}-1,3тіазол-4(5Н)-он, 2-Аніліно-5-ізопропіл-1,3-тіазол-4(5Н)-он, 5-Ізопропіл-2-[(2-морфолін-4-ілетил)аміно]-1,3тіазол-4(5Н)-он, 2-(Біцикло[2.2.1]гепт-2-иламіно)-1-тіа-3азаспіро[4.4]нон-2-ен-4-он, 31 2-(Циклогептиламіно)-1-тіа-3-азаспіро[4.4]нон2-ен-4-он, 2-(Циклооктиламіно)-1-тіа-3-азаспіро[4.4]нон2-ен-4-он, 2-[(2,2,3,3-Тетраметилциклопропіл)аміно]-1тіа-3-азаспіро[4.4]нон-2-ен-4-он, 2-[(2-хлорбензил)аміно]-5-ізопропіл-1,3оксазол-4(5Н)-он, 2-[(4-хлорбензил)аміно]-5-ізопропіл-1,3оксазол-4(5Н)-он, 5-ізопропіл-2-[(2,2,6,6-тетраметилпіперидин-4іл)аміно]-1,3-оксазол-4(5Н)-он, 5-ізопропіл-2-[(2-морфолін-4-ілетил)аміно]-1,3оксазол-4(5Н)-он, 5-бензил-2-[(циклогексилметил)аміно]-1,3оксазол-4(5Н)-он, 2-(циклогептиламіно)-5-ізопропіл-1,3-оксазол4(5Н)-он, 2-(біцикло[2.2.1]гепт-2-иламіно)-5-ізопропіл1,3-оксазол-4(5Н)-он, 2-(біцикло[2.2.1]гепт-2-иламіно)-5-ізобутил-1,3оксазол-4(5Н)-он, 2-(циклогептиламіно)-5-ізобутил-1,3-оксазол4(5Н)-он, 5-ізобутил-2-[(2-метилфеніл)аміно]-1,3оксазол-4(5Н)-он, 2-(біцикло[2.2.1]гепт-2-иламіно)-5-ізопропіл-5метил-1,3-тіазол-4(5Н)-он, 5-етил-2-[(3-метилфеніл)аміно]-1,3-тіазол4(5Н)-он, 5-ізопропіл-2-морфолін-4-іл-1,3-оксазол-4(5Н)он, 2-(4-бензилпіперидин-1-іл)-5-ізопропіл-1,3оксазол-4(5Н)-он, 2-азокан-1-іл-5-ізопропіл-1,3-оксазол-4(5Н)-он, 2-[(циклогексилметил)аміно]-5-феніл-1,3оксазол-4(5Н)-он, та 2-(циклогептиламіно)-5-феніл-1,3-оксазол4(5Н)-он, та її фармацевтично прийнятних солей, сольватів, гідратів, геометричних ізомерів, таутомерів, оптичних ізомерів, N-оксидів та форм проліків. Одне втілення відноситься до фармацевтичної композиції, що включає сполуку відповідно до Формули (І), (II), (III), або (IV) у вигляді активного інгредієнту, у комбінації з фармацевтично прийнятним розріджувачем або носієм. У одному втіленні, фармацевтична композиція розроблена для пероральної доставки. У одному втіленні, форма пероральної доставки являє собою таблетку. Одне втілення відноситься до способу профілактики або лікування розладу, опосередкованого ферментом 11-β-гідроксистероїдної дегідрогенази типу 1, або досягненняімуно-модуляції, що включає застосування сполуки Формули (І), (II), (III), або (IV) до пацієнта. У одному втіленні, розлад вибирають з групи, що включає діабет, синдром X, ожиріння, глаукому, гіперліпідемію, гіперглікемію, гіперінсулінемія, гіпертензію, остеопороз, деменцію, депресію, вірусні хвороби та запальні хвороби. Інше втілення відноситься до лікування або профілактики медичного стану, що включає уповільнене або погіршене загоєння рани. 86813 32 Інше втілення відноситься до способів лікування, у яких медичний стан, що включає уповільнене або погіршене загоєння рани, являє собою діабет. Інше втілення відноситься до способів лікування, у яких медичний стан, що включає уповільнене або погіршене загоєння рани, спричинений лікуванням глюкокортикоїдами. Інше втілення відноситься до способів лікування для сприяння загоєнню ран при хронічних ранах, таких як діабетичні виразки, венозні виразки або пролежневі виразки. Інше втілення відноситься до способів лікування, у якому імуно-модуляцію вибирають з групи, що включає туберкульоз, лепру та псоріаз. Інше втілення відноситься до способу інгібування ферменту 11-β-гідроксистероїдної дегідрогенази типу 1, який включає застосування до пацієнта, якому необхідне таке лікування, ефективної кількості сполуки відповідно до Формули (І), (II), (III) або (IV). Одне втілення відноситься до сполуки, яку вибирають з таких як: 2-[1-(4-Фтор-феніл)етиламіно]-5-метил-5-(тетрагідро-піран-4-ілметил)тіазол-4-он; (5S)-5-((1-ацетил-4-піперидиніл)метил)-2((1S,4R)-біцикло[2.2.1]гепт-2-иламіно)-5-метил-1,3тіазол-4(5Н)-он; (5R)-2-((1S,4R)-біцикло[2.2.1]гепт-2-иламіно)-5метил-5-(тетрагідро-2Н-піран-4-ілметил)-1,3тіазол-4(5Н)-он; (5S)-2-((1S,4R)-біцикло[2.2.1]гепт-2-иламіно)-5метил-5-тетрагідро-2Н-піран-4-іл-1,3-тіазол-4(5Н)он; 2-((1R,2R,4S)-біцикло[2.2.1]гепт-2-иламіно)-8окса-1-тіа-3-азаспіро[4.5]дец-2-ен-4-он; (5S)-2-((1S,4R)-біцикло[2.2.1]гепт-2-иламіно)-5((1-(3-фуранілкарбоніл)-4-піперидиніл)метил)-5метил-1,3-тіазол-4(5Н)-он; 2-(1-Циклогексил-етиламіно)-5-ізопропіл-5метил-тіазол-4-он; 2-(5,5-Дифтор-біцикло[2.2.1]гепт-2-иламіно)-5ізопропіл-5-метил-тіазол-4-он; 2-[1-(2-Трифторметил-феніл)-етиламіно]-8окса-1-тіа-3-аза-спіро[4.5]дец-2-ен-4-он; (5R)-2-((1S,2S,4R)-біцикло[2.2.1]гепт-2иламіно)-5-метил-5-(трифторметил)-1,3-тіазол4(5Н)-он; 2-(Біцикло[2.2.1]гепт-2-иламіно)-5-(1-фтор-1метил-етил)-5-метил-тіазол-4-он; 2-[1-(4-Фтор-феніл)-етиламіно]-5-метил-5піридин-4-іл-тіазол-4-он; 5-Метил-5-піридин-4-іл-2-[1-(2-трифторметилфеніл)-етиламіно]-тіазол-4-он; 2-[1-(2-Фтор-феніл)-етиламіно]-5-метил-5піридин-4-іл-тіазол-4-он; 5-(1-Фтор-1-метил-етил)-2-[1-(2-фтор-феніл)етиламіно]-5-метил-тіазол-4-он; 2-[1-(2-Фтор-феніл)-етиламіно]-5-метил-5трифторметил-тіазол-4-он; 5-(1,1-Дифтор-етил)-2-[1-(4-фтор-феніл)етиламіно]-5-метил-тіазол-4-он; 2-[1-(2-Хлор-феніл)-етиламіно]-5-метил-5трифторметил-тіазол-4-он; 33 2-[1-(4-Фтор-феніл)-етиламіно]-5-метил-5трифторметил-тіазол-4-он; 2-[1-(2-Хлор-феніл)-етиламіно]-5-метил-5трифторметил-тіазол-4-он; 2-[1-(4-Фтор-феніл)-етиламіно]-5-(2-метоксипіридин-4-іл)-5-метил-тіазол-4-он; 5-(1,1-Дифтор-етил)-2-[1-(4-фтор-феніл)етиламіно]-5-метил-тіазол-4-он; та 5-(1-Фтор-1-метил-етил)-2-[1-(4-фтор-феніл)етиламіно]-5-метил-тіазол-4-он, та її фармацевтично прийнятних солей, сольватів, гідратів, геометричних ізомерів, таутомерів, оптичних ізомерів, N-оксидів та форм проліків. Іншим об'єктом даного винаходу є сполука відповідно до загальної формули (І) для застосування у терапії: у якій R1 та R2 кожен незалежно вибирають з груп, таких як атом водню; С3-10-циклоалкіл, необов'язково незалежно заміщений за допомогою однієї або більше груп, таких як С1-8-алкіл та арил; С3-10циклоалкіл-С1-8-алкіл; арил; арил-С1-8-алкіл; гетероцикліл; гетероцикліл-С1-8-алкіл; або R1 та R2 утворюють разом з атомом азоту, до якого вони прикріплені, гетероцикліл, необов'язково незалежно заміщений за допомогою однієї або більше груп, таких як арил-С1-8-алкіл, де будь-який арильний або гетероциклільний залишок необов'язково незалежно заміщений за допомогою однієї або більше груп, таких як С1-8-алкіл та галоген; R3 та R4 кожен незалежно вибирають з груп, таких як атом водню; С1-8-алкіл; С3-10-циклоалкілС1-8-алкіл; ціано-С1-8-алкіл; арил; арил-С1-8-алкіл; гетероцикліл-С1-8-алкіл; гетероарил-С1-8-алкіл; або R3 та R4 утворюють разом з атомом вуглецю, до якого вони прикріплені, С3-10-циклоалкіл, де будьякий арильний залишок необов'язково незалежно заміщений за допомогою однієї або більше гідрокси груп; Ζ являє собою сірку або кисень; та її фармацевтично прийнятні солі, сольвати, гідрати, геометричні ізомери, таутомери, оптичні ізомери, N-оксиди та форми проліків. У межах описаного вище втілення, вважається за краще, коли: R1 та R2 кожен незалежно вибирають з груп, таких як атом водню, циклогексил, циклогептил, циклооктил,2,2,3,3-тетраметилциклопропіл, 1-(4хлорфеніл)циклобутил, біцикло[2.2.1]гепт-2-ил, трицикло[3.3.1.0~3,7~]нон-3-іл, циклогексилметил, феніл, 2-метилфеніл, 3-метилфеніл, 2ізопропілфеніл, 2-фторфеніл, 2-хлорфеніл, 2фенілпропіл, 2-хлорбензил, 4-хлорбензил, 4(2,2,6,6-тетраметил)піперидил, 2-морфолініл-4ілетил, або R1 та R2 утворюють разом з атомом азоту, до якого вони прикріплені, морфолініл, азокан, або 4-бензилпіперидил; R3 та R4 кожен незалежно вибирають з груп, таких як атом водню, метил, етил, ізопропіл, ізобу 86813 34 тил, трет-бутил, циклогексилметил, ціанометил, феніл, 2-гідроксифеніл, бензил, 2-гідроксибензил, 4-гідроксибензил, 3,4-дигідроксибензил, 1Німідазол-4-ілметил, індол-3-ілметил, 3піридилметил, або R3 та R4 утворюють разом з атомом вуглецю, до якого вони прикріплені, циклопропіл, циклобутил, циклопентил, циклогексил. При використанні сполук Формули (І) у терапії (наприклад, Приклади 39, 67, та 69-72), вони можуть бути переважно використані у профілактиці або лікуванні розладу, опосередкованого ферментом 11-β-гідроксистероїдної дегідрогенази типу 1, або досягнення імуно-модуляції. У цьому втіленні, розлад може бути вибраний з таких як діабет, синдром X, ожиріння, глаукома, гіперліпідемія, гіперглікемія, гіперінсулінемія, гіпертензія, остеопороз, деменція, депресія, вірусні хвороби, та запальні хвороби. Також можливо, що лікування або профілактика медичного стану включає уповільнене або погіршене загоєння рани. Медичний стан, що включає уповільнене або погіршене загоєння рани, може бути пов'язаний з діабетом та може бути викликаний лікуванням глюкокортикоїдами. Сполуки Формули (І) для застосування у терапії можуть бути використані для сприяння загоєнню рани при хронічних ранах, таких як діабетичні виразки, венозні виразки або пролежневі виразки. Імуномодуляція може включати туберкульоз, лепру та псоріаз. Крім прикладів, наступні сполуки, відповідно до Формули (І), можуть бути ефективно використані у терапії: 5-етил-2-[(3-метилфеніл)аміно]-1,3-тіазол4(5Н)-он, 5-ізопропіл-2-морфолін-4-іл-1,3-оксазол-4(5Н)он, 2-(4-бензилпіперидин-1-іл)-5-ізопропіл-1,3оксазол-4(5Н)-он, 2-азокан-1-іл-5-ізопропіл-1,3-оксазол-4(5Н)-он, 2-[(циклогексилметил)аміно]-5-феніл-1,3оксазол-4(5Н)-он, 2-(циклогептиламіно)-5-феніл-1,3-оксазол4(5Н)-он. Інший об'єкт даного винаходу являє собою фармацевтичну композицію, що включає сполуку відповідно до Формули (І), для застосування у терапії як активний інгредієнт, у комбінації з фармацевтично прийнятним розріджувачем або носієм, особливо для застосування у профілактиці або лікуванні розладу, опосередкованого ферментом 11-β-гідроксистероїдної дегідрогенази типу 1, або досягнення імуно-модуляції. Фармацевтична композиція може включати другий активний інгредієнт. Другий активний інгредієнт може являти собою інгібітор 11-β-гідроксистероїдної дегідрогенази типу 1 або він може мати деяку іншу активність. Інший об'єкт даного винаходу являє собою спосіб профілактики або лікування розладу, опосередкованого ферментом 11-β-гідроксистероїдної дегідрогенази типу 1, або досягнення імуномодуляції, який включає застосування до пацієнта, якому необхідне таке лікування, ефективної кількості сполуки відповідно до Формули (І), (II), (III) та (IV). 35 Інший об'єкт даного винаходу являє собою спосіб інгібування ферменту 11-βгідроксистероїдної дегідрогенази типу 1, який включає застосування до пацієнта, якому необхідне таке лікування, ефективної кількості сполуки відповідно до Формули (І), (II), (III) та (IV). Інший об'єкт даного винаходу являє собою застосування сполуки відповідно до Формули (І), (II), (III) та (IV) для виробництва лікарського засобу для застосування у профілактиці або лікуванні розладу, опосередкованого ферментом 11-βгідроксистероїдної дегідрогенази типу 1, або досягнення імуно-модуляції. Приклади розладів, опосередкованих ферментом 11-β-гідроксистероїдної дегідрогенази типу 1, включають такі як: діабет, синдром X, ожиріння, глаукома, остеопороз, гіперліпідемія, гіперглікемія, гіперінсулінемія, гіпертензія, остеопороз, когнітивні розлади, деменція, депресія, імунні розлади, вірусні хвороби, загоєння рани та запальні хвороби. Переважно, медичний стан, що включає уповільнене або погіршене загоєння рани, являє собою діабет. Також переважно, коли медичний стан, що включає уповільнене або погіршене загоєння рани, спричинений лікуванням глюкокортикоїдами. Сполука відповідно до Формули (І), (II), (III) та (IV) може бути використана для сприяння загоєнню рани при хронічних ранах, таких як діабетичні виразки, венозні виразки або пролежневі виразки. Переважно, коли імуно-модуляцію вибирають з групи, що включає туберкульоз, лепру та псоріаз. Також, у об'єм даного винаходу попадає спосіб одержання сполуки формули (І). Спосіб включає процес, при якому беруть будь-яку проміжну сполуку, зображену у цьому описі, вводять у реакцію з одним або більше реагентами з утворенням сполуки Формули (І), (II), (III) та (IV), включаючи будьякі процеси, спеціально підкреслені у цьому описі. Застосування сполуки Формули (І), (II), (III) або (IV) для виробництва лікарського засобу для використання у профілактиці або лікуванні розладу, опосередкованого ферментом 11-βгідроксистероїдної дегідрогенази типу 1, або досягнення імуно-модуляції. У одному втіленні, розлад вибирають з групи, що включає діабет, синдром X, ожиріння, глаукому, гіперліпідемію, гіперглікемію, гіперінсулінемію, гіпертензію, остеопороз, деменцію, депресію, вірусні хвороби, та запальні хвороби. У іншому втіленні, медичний стан включає уповільнене або погіршене загоєння рани. У іншому втіленні, медичний стан, що включає уповільнене або погіршене загоєння рани, являє собою діабет. У іншому втіленні, медичний стан, що включає уповільнене або погіршене загоєння рани, спричинений лікуванням глюкокортикоїдами. У іншому втіленні, застосування проводять для сприяння загоєнню ран при хронічних ранах, таких як діабетичні виразки, венозні виразки або пролежневі виразки. У іншому втіленні, імуно-модуляцію вибирають з групи, що включає туберкульоз, лепру та псоріаз. Інші особливості та переваги даного винаходу стануть зрозумілі з детального опису та пунктів Формули винаходу. 86813 36 Сполуки у відповідності з даним винаходом можуть бути використані при деяких показаннях, які залучають фермент 11-β-гідроксистероїдної дегідрогенази типу 1. Таким чином, сполуки у відповідності з даним винаходом можуть бути використані проти деменції [дивись WO97/07789], остеопорозу [дивись Canalis, E. 1996, Mechanisms of glucocorticoid action in bone: implications to glucocorticoid-induced osteoporosis, Journal of Clinical Endocrinology and Metabolism, 81, 34413447] та можуть бути також використані для розладів у імунній системі [дивись Franchimont та інші, "Inhibition of Thl immune response by glucocorticoids: dexamethasone selectively inhibits IL-12-induced Stat 4 фосфорилагіоп in Τ lymphocytes", The journal of Immunology 2000, Feb 15, том 164 (4), стор.176874) і також у перерахованих вище показаннях. Різні терміни, використані, окремо та у комбінаціях, у описаному вище визначенні сполук, що мають Формулу (І), (II), (III) та (IV), будуть пояснені. Термін "арил" у даному описі включає ароматичні кільця (моноциклічні або біциклічні), що мають від 6 до 10 кільцевих атомів вуглецю, такі як феніл (Ph), нафтил, та інданіл (тобто 2,3дигідроінденіл), який необов'язково може бути заміщений за допомогою С1-6-алкілу. Приклади заміщених арильних груп включають бензил та 2метилфеніл. Термін "гетероарил" означає у даному описі моноциклічну, бі- або трициклічну ароматичну кільцеву систему (тільки одне кільце повинно бути ароматичним), що має від 5 до 14, переважно від 5 до 10 кільцевих атомів, наприклад, 5, 6, 7, 8, 9 або 10 кільцевих атомів (моно- або біциклічних), у якій один або більше з кільцевих атомів являють собою інший атом ніж вуглець, наприклад, такий як азот, сірка, кисень та селен, як частину кільцевої системи. Приклади таких гетероарильних кілець являють собою пірол, імідазол, тіофен, фуран, тіазол, ізотіазол, тіадіазол, оксазол, ізоксазол, оксадіазол, піридин, піразин, піримідин, піридазин, піразол, триазол, тетразол, хроман, ізохроман, хінолін, хіноксалін, ізохінолін, фталазин, циннолін, хіназоніл, індол, ізоіндол, бензотіофен, бензофуран, ізобензофуран, бензоксазол, 2,1,3бензоксадіазол, бензопіразол; бензотіазол, 2,1,3бензотіазол, 2,1,3-бензоселенадіазол, бензімідазол, індазол, бензодіоксан, індан, 1,5-нафтирідин, 1,8-нафтирідин, акридин, феназин та ксантен. Термін "гетероциклічний" та "гетероцикліл" у даному описі включає ненасичені, також як і частково та повністю насичені моно-, бі- та трициклічні кільця, що мають від 4 до 14, переважно від 4 до 10 кільцевих атомів, що включають один або більше гетероатомів (наприклад, таких як кисень, сірка або азот) як частину кільцевої системи, та всі інші кільцеві члени являють собою вуглець, такі як, наприклад, гетероарильні групи, зазначені вище, також як і відповідні частково насичені або повністю насичені гетероциклічні кільця. Приклади насичених гетероциклічних кілець включають азетидин, піролідин, піперидин, піперазин, морфолін, тіоморфолін, 1,4-оксазепан, азепан, фталімід, індолін, ізоіндолін, 1,2,3,4-тетрагідрохінолін, 1,2,3,4тетрагідроізохінолін, 3,4-дигідро-2H-1,4 37 бензоксазин, гексагідроазепін, 3,4-дигідро2(1Н)ізохінолін, 2,3-дигідро-1H-індол, 1,3-дигідро2Н-ізоіндол, азокан, 1-окса-4-азаспіро[4.5]дец-4ен, декагідроізохінолін, та 1,4-діазепан. Крім того, гетероцикліл або гетероциклічний залишок може бути необов'язково заміщеним за допомогою однієї або більше оксо груп. C1-8-алкіл у сполуці формули (І) відповідно до даної заявки може являти собою лінійну або розгалужену алкільну групу, що містить 1-8 атомів вуглецю. Приклади алкільних груп включають метил, етил, н-пропіл, ізопропіл, н-бутил, втор-бутил, трет-бутил, пентил, ізопентил, гексил, ізогексил, нгептил, та н-октил. Для частин інтервалу "C1-8алкіл" всі їх підгрупи передбачаються такими як С17-алкіл, С1-6-алкіл, С1-5-алкіл, С1-4-алкіл, С2-8-алкіл, С2-7-алкіл, С1-6-алкіл, С2-5-алкіл, С3-7-алкіл, С4-6алкіл, тощо. С1-8-алкокси група у сполуці формули (І) відповідно до даної заявки може являти собою лінійну або розгалужену алкокси групу, що містить 1-8 атомів вуглецю. Приклади алкокси груп включають метокси, етокси, пропокси, ізопропокси, бутокси, втор-бутокси, трет-бутокси, пентилокси, ізопентилокси, гексилокси, ізогексилокси, н-гептилокси, та н-октилокси. Для частин інтервалу "С1-6-алкокси" всі їх підгрупи передбачаються такими як С1-7алкокси, С1-6-алкокси, C1-5-алкокси, С1-4-алкокси, С2-8-алкокси, С2-7-алкокси, С2-6-алкокси, С2-5алкокси, С3-7-алкокси, С4-6-алкокси, тощо. С1-8-ацил у сполуці формули (І) відповідно до даної заявки може являти собою лінійну або розгалужену ацильну групу, що містить 1-8 атомів вуглецю. Приклади ацильних груп включають форміл, ацетил, пропіоніл, бутирил, ізобутирил, валерил, ізовалерил, н-гексаноїл, н-гептаноїл та ноктаноїл. Для частин інтервалу "С1-8-ацил" всі їх підгрупи передбачаються такими як С1-7-ацил, С1-6ацил, С1-5-ацил, С1-4-ацил, С2-8-ацил, С2-7-ацил, С26-ацил, С2-5-ацил, С3-7-ацил, С4-6-ацил, тощо. С2-8-алкеніл у сполуці формули (І) відповідно до даної заявки може являти собою лінійну або розгалужену алкенільну групу, що включає 2-8 атомів вуглецю. Приклади алкенільних груп включають вініл, 1-пропеніл, 2-пропеніл, ізопропеніл, 1бутеніл, 2-бутеніл, 1-пентеніл, 2-пентеніл, 1гексеніл, 2-гексеніл, 1-гептеніл, та 1-октеніл. Для частин інтервалу "С2-8-алкеніл" всі їх підгрупи передбачаються такими як С2-7-алкеніл, С2-6-алкеніл, С2-5-алкеніл, С2-4-алкеніл, С3-8-алкеніл, С3-7алкеніл, С3-6-алкеніл, С3-5-алкеніл, С4-7-алкеніл, С56-алкеніл, тощо. С3-10-циклоалкіл у сполуці формули (І) відповідно до даної заявки може являти собою необов'язково заміщену моноциклічну, біциклічну або трициклічну алкільну групу, що включає від 3 до 10 атомів вуглецю. Приклади циклоалкільних груп включають циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклононіл, циклодецил, біцикло[2.2.1]гепт-2-ил, трицикло[3.3.1.0~3,7~]нон-3-іл, (1R,2R,3R,5S)-2,6,6триметилбіцикло[3.1.1]гепт-3-ил, (1S,2S,3S,5R)2,6,6-триметилбіцикло[3.1.1]гепт-3-ил, 1адамантил, норадамантил, та 2,2,3,3тетраметилциклопропіл. для чаcтин інтервалу "С3 86813 38 10-циклоалкіл" всі їх підгрупи передбачаються такими як С3-9-циклоалкіл, С3-8-циклоалкіл, С3-7циклоалкіл, С3-6-циклоалкіл, С3-5-циклоалкіл, С4-10циклоалкіл, С5-10-циклоалкіл, С6-10-циклоалкіл, С710-циклоалкіл, С8-9-циклоалкіл, тощо. Крім того, циклоалкільний залишок може бути необов'язково заміщеним за допомогою однієї або більше оксо груп. С3-10-циклоалкеніл у сполуці формули (І) відповідно до даної заявки може являти собою необов'язково заміщену циклічну, біциклічну або трициклічну алкенільну групу, що включає від 3 до 10 атомів вуглецю. Приклади циклоалкенільних груп включають циклопропеніл, циклобутеніл, циклопентеніл, циклогексеніл, циклогептеніл, циклооктеніл, циклононеніл, циклодеценіл, та біцикло[2.2.1]гепт-5-ен-2-іл. Для частин інтервалу "С3-10циклоалкеніл" всі їх підгрупи передбачаються такими як С3-9-циклоалкеніл, С3-8-циклоалкеніл, С3-7циклоалкеніл, С3-6-циклоалкеніл, С3-5циклоалкеніл, С4-10-циклоалкеніл, С5-10циклоалкеніл, С3-10-циклоалкеніл, С7-10циклоалкеніл, C8-9-циклоалкеніл, тощо. Крім того, циклоалкенільний залишок може бути необов'язково заміщеним за допомогою однієї або більше оксо груп. Термін "галоген" або "гало" у даному описі включає фтор, хлор, бром та йод. Термін "сульфаніл" у даному описі означає тіо групу. Термін "-гетеро(С1-С8)алкіл" відноситься до залишку, у якому гетероатом, вибраний з необов'язково заміщеного азоту, сірки та кисню, являє собою точку прикріплення до ядра молекули та прикріплений до C1-C8 алкільного ланцюга. Термін "циклічне амідне спіро кільце" відноситься до сполук, у яких замісники у 5-положенні тіазолінонового або оксазолонового кільця об'єднуються разом з утворенням циклічного кільця, що має -NR10C(O)- у ньому. Приклад такого залишку показаний у прикладі нижче: Під виразом "моно- або ди-заміщений" у даному описі розуміють, що зазначені функціональні групи можуть бути заміщені за допомогою незалежно C1-8-ацилу, С2-8-алкенілу, C1-8-(цикло)алкілу, арилу, піридилметилу, або гетероциклічних кілець, наприклад, таких як азетидин, піролідин, піперидин, піперазин, морфолін та тіоморфолін, де гетероциклічні кільця необов'язково можуть бути заміщеними за допомогою C1-8-алкілу. Під виразом "необов'язково моно- або ди-заміщений'' у даному описі розуміють, що зазначені функціональні групи можуть бути також заміщені незалежно за допомогою водню. Коли два з зазначених вище термінів використовуються разом, розуміють, що остання група заміщена першою. Наприклад, С3-10-циклоалкіл-C18-алкіл означає C1-8-алкільну групу, яка заміщена за допомогою С3-10-циклоалкільної групи. Аналогі 39 чно, C1-8-галоалкіл означає C1-8-алкільну групу, яка заміщена за допомогою атому галогену. Метаболіти сполук Формули (І), (II), (III) та (IV) можуть приймати багато форм та даний винахід охоплює метаболіти сполук, також як і вихідну сполуку. Як використано у цьому описі, термін "проліки" означає похідну сполуки, яка може гідролізуватися, окислюватися або іншим чином взаємодіяти у біологічних умовах (in vitro або in vivo) з одержанням активної сполуки, особливо бензамідної похідної. Приклади проліків включають, але не обмежуються наведеними, похідні та метаболіти бензамідної похідної, які включають групи, що біогідролізуються, такі як біогідролізуємі аміди, біогідролізуємі складні ефіри, біогідролізуємі карбамати, біогідролізуємі карбонати, біогідролізуємі уреїди, та біогідролізуємі фосфатні аналоги (наприклад, монофосфатні, дифосфатні або трифосфатні). Переважно, проліки сполук з карбоксильними функціональними групами являють собою нижчі алкільні складні ефіри карбонової кислоти. Карбоксилатні складні ефіри легко одержують шляхом естерифікації будь-якого з залишків карбонової кислоти, що присутній у молекулі. Проліки зазвичай можуть бути одержані використовуючи добре відомі способи, такі як ті, що описані [Burger's Medicinal Chemistry and Drug Discovery 6-те вид. (Donald J. Abraham ред., 2001, Wiley) та Design and Application of Prodrugs (H. Bundgaard ред., 1985, Harwood Academic Publishers Gmfh]. "Таутомер" являє собою один з двох або більше структурних ізомерів, які існують у рівновазі та легко перетворюються з однієї ізомерної форми у іншу, у даному випадку, таутомери структур, показаних нижче, охоплюються даним винаходом. Як використано у цьому описі, "гідрат" являє собою форму сполуки Формули (І), (II), (III), або (IV), у якій молекули води приєднані у визначеному співвідношенні як невід'ємна частина кристалічної структури сполуки. Як використано у цьому описі, "сольват" являє собою форму сполуки Формули (І), (II), (III), або (IV), у якій молекули розчиннику приєднані у визначеному співвідношенні як невід'ємна частина кристалічної структури сполуки. В залежності від її структури, фраза "фармацевтично прийнятна сіль," як використано у цьому описі, відноситься до фармацевтично прийнятної солі органічної або неорганічної кислоти або основи бензамідної похідної. Типові фармацевтично прийнятні солі включають, наприклад, такі як солі лужних металів, солі лужноземельних металів, амонійні солі, водорозчинні та водо-нерозчинні солі, такі солі як ацетат, амсонат (4,4діаміностилбен-2,2-дисульфонат), бензолсульфонат, бензонат, бікарбонат, бісульфат, бітартрат, борат, бромід, бутират, кальцій, кальцію едетат, 86813 40 камсилат, карбонат, хлорид, цитрат, клавуларіат, дигідрохлорид, едетат, едісилат, естолат, езилат, фіунарат, глюцептат, глюконат, глутамат, гліколіларсанілат, гексафторфосфат, гексилрезорцинат, гідрабамін, гідробромід, гідрохлорид, гідроксинафтоат, йодид, ізотіонат, лактат, лактобіонат, лаурат, малат, малеат, манделат, мезилат, метилбромід, метилнітрат, метилсульфат, мукат, напсилат, нітрат, N-метилглюкамін амонійна сіль, 3-гідрокси-2нафтоат, олеат, оксалат, палмітат, памоат (1,1метен-біс-2-гідрокси-3-нафтоат, ейнбонат), пантотенат, фосфат/дифосфат, пікрат, полігалактуронат, пропіонат, п-толуолсульфонат, саліцилат, стеарат, субацетат, сукцинат, сульфат, сульфосалікулат, сурамат, таннат, тартрат, теоклат, тозилат, триетіодид та валерат. Більш того, фармацевтично прийнятна сіль може мати більше ніж один заряджений атом у її структурі. У цьому випадку фармацевтично прийнятна сіль може мати множинні контріони. Таким чином, фармацевтично прийнятна сіль може мати один або більше заряджених атомів та/або один або більше контріонів. Як використано у цьому описі, термін "геометричні ізомери" відноситься до сполук, що мають однакову молекулярну формулу, але атоми знаходяться у різних нееквівалентних положеннях одиндо одного. Як використано у цьому описі, термін "оптичні ізомери " відноситься до сполук з хіральними атомами, які мають здатність обертати площину поляризованого світла, R/S конфігурацію. Термін оптичний ізомер включає енантіомери та діастереомери, також як і сполуки, які можуть бути розрізнені одна від одної за допомогою позначень (D) та (L). Як використано у цьому описі: DCM означає дихлорметан, DEAD означає діетилазокарбоксилат, DMF означає диметилформамід, EDCI означає 1-(3-диметиламінопропіл)-3етилкарбодіімід гідрохлорид, Ефір означає діетиловий ефір, EtOAc означає етилацетат, HOBt означає 1-гідроксибензотриазол, HPLC означає високо ефективну рідинну хроматоргафію, LC означає рідинну хроматоргафію, MeCN означає ацетонітрил, DPPA означає дифенілфосфорилазид, RT означає кімнатну температуру, SM означає вихідний матеріал, TEA означає триетиламін, та THF означає тетрагідрофуран. Комбінації замісників та змінних, зображені у цьому винаході, являють собою тільки ті, що приводять до утворення стабільних сполук. Термін "стабільні", як використано у цьому описі, відноситься до сполук, які мають стабільність, достатню для виробництва, та які підтримують цілісність сполуки впродовж періоду часу, достатнього, щоб бути корисними для цілей, детально описаних у цьому описі (наприклад, терапевтичне застосування до пацієнта для лікування хвороби, 11-βHSD1 інгібування, 11-β-HSD1-опосередкованої хвороби). 41 Термін "форми проліків" у даному описі означає фармацевтично прийнятну похідну, таку як складний ефір або амід, при чому похідна біотрансформується у організмі з утворенням активного лікарського засобу [дивись Goodman та Gilman's, The Pharmacological basis of Therapeutics, 8-те вид., McGraw-Hill, Int. Ed. 1992, "Віоггашутворення Drugs, стор.13-15]. "Фармацевтично прийнятні" означає у даному описі, що сполука прийнятна для одержання фармацевтичної композиції, яка є в основному безпечною, нетоксичною та ні біологічно ні іншим чином небажаною та включає сполуку, корисну для ветеринарного застосування, а також для фармацевтичного застосування до людей. "Фармацевтично прийнятні солі" означають у даному описі солі, які є фармацевтично прийнятними, як визначено вище, та які мають бажану фармакологічну активність. Такі солі включають солі приєднання кислоти, утворені з органічною та неорганічною кислотами, такими як хлористий водень, бромистий водень, йодистий водень, сірчана кислота, фосфорна кислота, оцтова кислота, гліколева кислота, малеїнова кислота, малонова кислота, оксалінова кислота, метансульфонова кислота, трифтороцтова кислота, фумарова кислота, бурштинова кислота, винна кислота, лимонні кислота, бензойна кислота, аскорбінова кислота та подібні. Солі приєднання основи можуть бути утворені з органічними та неорганічними основами, такими як натрій, амоній, калій, кальцій, етаноламін, діетаноламін, N-метилглюкамін, холін та подібні. У даний винахід включені фармацевтично прийнятні солі або сполуки будь-яких формул даного опису. Фармацевтичні композиції у відповідності з даним винаходом включають фармацевтично прийнятний носій разом з принаймні однією зі сполук, що мають формулу (І), як представлено у цьому описі вище, розчиненою або диспергованою у ньому як активний, притимікробний інгредієнт. У кращому втіленні, терапевтична композиція є не імуногенною при застосуванні до пацієнта з терапевтичними цілями, поки ця ціль не спричинить імунної відповіді. Одержання фармакологічної композиції, що містить активні інгредієнти, розчинені або дисперговані у ній, є добре відомим у даній галузі техніки. Зазвичай такі композиції одержують у вигляді стерильних ін’єкційних форм або як рідкі розчини або суспензії, водні або неводні, однак, тверді форми, прийнятні для розчинення, або суспендування, у рідині безпосередньо перед застосуванням, також можуть бути одержані. Препарат також може бути емульгований. Активний інгредієнт може бути змішаний з наповнювачами, які є фармацевтично прийнятними та сумісними з активним інгредієнтом та у кількостях, придатних для застосування у терапевтичних способах, описаних у цьому описі. Прийнятні наповнювачі являють собою, наприклад, такі як вода, сольовий розчин, декстроза, гліцерин, етанол або подібні та їх комбінації. Крім того, при бажанні, композиція може містити незначні кількості допоміжних речовин, таких як зволожуючі або емуль 86813 42 гуючі агенти, рН буферні агенти та подібні, які збільшують ефективність активного інгредієнту. Допоміжні речовини також можуть бути у композиції. Фармацевтично прийнятні носії добре відомі у даній галузі техніки. Приклади рідких носіїв включають стерильні водні розчини, які не містять ніяких матеріалів крім активних інгредієнтів та води, або містять буфер, такий як фосфат натрію при фізіологічному значенні рН, фізіологічний сольовий розчин або обидва, такі як фосфатзабуферений сольовий розчин. Додатково, водні носії можуть містити більше ніж одну буферну сіль, також як і солі, такі як хлориди натрію та калію, декстроза, пропіленгліколь, поліетиленгліколь та інші розчинні речовини. Рідкі композиції також можуть містити рідкі фази крім та замість води. Приклади таких додаткових рідких фаз включають гліцерин, рослинні олії, такі як бавовняна олія, органічні складні ефіри, такі як етилолеат, та водо-масляні емульсії. Фармацевтична композиція відповідно до одного з кращих втілень даного винаходу, що включає сполуки формули (І), може включати фармацевтично прийнятні солі того компоненту у цьому описі як показано вище. Фармацевтично прийнятні солі включають солі приєднання кислоти (утворені з вільними аміно групами поліпептиду), які одержують з неорганічними кислотами, такими як, наприклад, соляна або фосфорна кислоти, або такими органічними кислотами як оцтова кислота, винна кислота, мигдальна кислота та подібні. Солі, утворені з вільними карбоксильними групами, також можуть бути одержані з неорганічних основ, таких як, наприклад, гідроксиди натрію, калію, амонію, кальцію або заліза, та таких органічних основ як ізопропіламін, триметиламін, 2етиламіноетанол, гістидин, прокаїн та подібні. Препарати відповідно до кращих втілень можуть застосовуватися перорально, місцево, внутрішньочеревинно, внутрісуглобно, внутрішньочерепно, внутрішньошкірно, внутрішньом'язово, внутріочно, інтратекально, внутрішньовенно, підшкірно. Інші шляхи відомі спеціалістам, кваліфікованим у даній галузі техніки. Композиції, що застосовують перорально, у відповідності з даним винаходом можуть бути у формі таблеток, капсул, порошків, гранул, пастилок, рідких або гелевих препаратів, таких як пероральні, місцеві або стерильні парентеральні розчини або суспензії. Таблетки та капсули для перорального застосування можуть бути у одиничній лікарській формі та можуть містити загальновикористовувані наповнювачі, такі як зв'язуючі агенти, наприклад, такі як сироп, гуміарабік, желатин, сорбіт, трагакант або полівініл-піролідон; наповнювачі, наприклад, такі як лактоза, цукор, кукурудзяний крохмаль, кальцію фосфат, кальцію гідрофосфат, натрію крохмаль гліколят, сорбіт або гліцин; любриканти для таблетування, наприклад, такі як стеарат магнію, тальк, поліетиленгліколь або діоксид кремнію (необов'язково колоїдний); дезінтегранти, наприклад, такі як картопляний крохмаль, або прийнятні зволожуючі агенти, такі як натрію лаурил-сульфат. Таблетки можуть бути 43 покриті відповідно до способів, добре відомих у звичайній фармацевтичній практиці. Пероральні рідкі препарати можуть бути у формі, наприклад, водної або масляної суспензій, розчинів, емульсій, сиропів або еліксирів або можуть бути у вигляді сухого продукту для відновлення водою або іншим прийнятним наповнювачем перед застосуванням. Такі рідкі препарати можуть містити загальновідомі добавки, такі як суспендуючі агенти, наприклад, такі як сорбіт, сироп, метилцелюлоза (необов'язково мікрокристалічна), глюкозний сироп, желатингідрогеновані харчові жири; емульгуючи агенти, наприклад, такі як лецитин, сорбітмоноолеат або гуміарабік, неводні наповнювачі (які можуть включати харчові олії), наприклад, такі як мигдальна олія, фракціонована кокосова олія, маслянисті складні ефіри, такі як гліцерин, пропіленгліколь, або етиловий спирт; консерванти, наприклад, такі як метил або пропіл п-гідроксибензоат або сорбінова кислота, та, при бажанні, загальновідомі ароматизатори або барвники. "Ефективна кількість" відноситься до кількості сполуки, яка дає терапевтичний ефект пацієнту, якого лікують. Терапевтичний ефект може бути об'єктивним (тобто вимірюваним за допомогою деякого тесту або маркеру) або суб'єктивним (тобто пацієнт дає ознаки або відчуває ефект). Фармацевтична композиція у відповідності з даним винаходом, може включати звичайно кількість принаймні 0,1 масовий відсоток сполуки, що має формулу (І), на масу загальної терапевтичної композиції. Масовий відсоток являє собою співвідношення за масою загальної композиції. Таким чином, наприклад, 0,1 масовий відсоток являє собою 0,1 грам сполуки, що має формулу (І), на 100 грам загальної композиції. Прийнятна добова пероральна доза для ссавця, переважно людини, може змінюватися в широких межах в залежності від стану пацієнта. Однак, прийнятною може бути доза сполуки, що має формулу (І), приблизно від 0,1 до 300мг/кг маси тіла. Композиції у відповідності з даним винаходом також можуть бути використані у ветеринарії і, таким чином, вони можуть включати ветеринарно прийнятний наповнювач або носій. Таким чином, сполуки та композиції можуть застосовуватися до тварин, наприклад, таких як коти, собаки, або коні, у способах лікування. Сполуки даного винаходу у міченій формі, наприклад, ізотопічно міченій, можуть бути використані як діагностичний агент. Даний винахід відноситься до способів одержання сполук будь-якої з формул у цьому описі, що включають введення у реакцію будь-якої однієї або більше сполук формул, схематично зображених у цьому описі, включаючи будь-які процеси, показані у цьому описі. Сполуки формули (І), представленої вище, можуть бути одержані за допомогою, або за аналогією, звичайних способів, та особливо відповідно до або за аналогією з наступними способами. Додатково, фармакологія invitro була досліджена використовуючи наступні реагенти та способи. Хімічні реактиви, використані у шляхах синтезу, показаних у цьому описі, можуть включати, 86813 44 наприклад, розчинники, реагенти, каталізатори, та реагенти для захисту групи та зняття захисту з групи. Способи, описані вище, також можуть додатково включати стадії, або перед або після стадій, описаних специфічно у цьому описі, для того, щоб додати або видалити прийнятні захисні групи для того, щоб зрештою провести синтез сполук. Крім того, різні стадії синтезу можуть бути виконані у альтернативній послідовності або порядку з одержанням бажаних сполук. Синтетичні хімічні трансформації та методології захищення груп (забезпечення захисту та зняття захисту), корисні у прийнятних сполуках, що синтезують, відомі у даній галузі техніки та включають, наприклад, ті, що описані у [R. Larock, Comprehensive Organic Transformations, VCH Publishers (1989); T.W. Greene та P.G.M. Wuts, Protective Groups in Organic Synthesis, 3те вид., John Wiley and Sons (1999); L. Fieser та Μ. Fieser, Fieser and Fieser's Reagents for Organic Synthesis, John Wiley and Sons (1994); та L. Paquette, ред., Encyclopedia of Reagents for Organic Synthesis, John Wiley and Sons (1995)] та їх наступні видання. Всі публікації, згадані у цьому описі, включені у даний опис шляхом посилання. Під виразом "що включає" розуміють "включаючи, але не обмежуючись наведеними." Таким чином, можуть бути присутні і інші не згадані речовини, добавки або носії. Далі винахід буде описаний посилаючись на наступні Приклади. Ці Приклади не слід розглядати як обмеження обсягу даного винаходу, а вони слугують тільки для ілюстрації. Приклади Біологічні приклади Сцинтиляційне дослідження подібності [1,2(n) - 3Н]-кортизон був придбаний у Amersham Pharmacia Biotech. Анти-кортизол моноклональне мишаче антитіло, клон 6D6.7 було одержане від Immunotech та гранули, покриті моноклональними анти-мишиними антитілами, Scintillation proximity assay (SPA) одержали від Amersham Pharmacia Biotech. NADPH, тетранатрієву сіль отримали від Calbiochem та глюкоза-6фосфат (G-6-P) був забезпечений від Sigma. Фермент 11-β-гідроксистероїдної дегідрогенази типу-1 (11-β-HSD1) людини був експресований у Pichia pastor is. 18-β-гліцирретинову кислоту (GA) одержали від Sigma. Серійні розведення сполук проводили на Tecan Genesis RSP 150. Сполуки для дослідження були розчинені у DMSO (1мм) та розбавлені у 50мМ Tris-НСl, рН7,2, що містить 1мМ EDTA. Мультиплікацію планшетів виконували на WallacQuadra. Кількість продукту [3Н]-кортизолу, прикріпленого до гранул, визначали у Packard, Top Count мікропланшетному рідинному сцинтиляційному лічильнику. Дослідження 11-β-HSD1 ферменту проводили на 96-лункових мікротитрових планшетах (Packard, Optiplate), що мають загальний об'єм лунки 220мкл та містять 30мМ Tris-HCl, рН7,2 з 1мМ EDTA, субстратну суміш мічену трітієм кортизон/NADPH (175нМ/181мкМ), G-6-P (1мм) та інгібітори у серійних розведеннях (від 9 до 0,15мкМ). Реакції ініціювали додаванням 11-β-HSD1 людини, або у вигляді 45 86813 Pichia pastor is клітинного гомогенату або як мікросоми, одержані з Pichia pastoris (кінцева кількість використаного ферменту змінювалась від 0,057 до 0,11мг/мл). Після змішування, планшети струшували впродовж 30-45 хвилин при кімнатній температурі. Реакції були припинені за допомогою 10мкл 1мМ GA стоп розчину. Далі додали моноклональне мишаче антитіло (10мкл 4мкМ), а потім 100мкл SPA гранул (суспендованих відповідно до інструкцій виробників). Відповідні контролі були забезпечені за рахунок не виключення 11-β-HSD1 для одержання значення неспецифічного зв'язування (NSB). Планшети накрили пластикового плівкою та інкубували на шейкері впродовж 30 хвилин, при кімнатній температурі, перед підрахунком. Кількість [3Н]-кортизолу, зв'язаного з гранулами, визначали у мікропланшетному рідинному сцинтиляційному лічильнику. Розрахунки значень Ki для інгібіторів проводили шляхом використання Activity Base. Значення Ki розраховують з ІС50, а значення Km розраховують, використовуючи рівняння ЧенгаПрушофа (Cheng Prushoff) (з оборотним інгібуванням, яке слідує з рівняння Міхаеліса-Ментена): Ki=IC50(1+[S]/Km ) [Cheng, Y.C.: Prushoff, W.H. Biochem. Pharmacol. 1973, 22, 3099-3108]. IC50 вимірюють експериментально у дослідженні, у якому зменшення обернення кортизону до кортизолу залежить від потенціалу інгібування кожної речовини. Значення Kі сполук даного винаходу для 11β-HSD1 ферменту зазвичай знаходиться у інтервалі від приблизно 10нМ до приблизно 10мкМ. Нижче представлені деякі приклади Kі у відповідності з даним винаходом. Приклад 10 14 48 Kі значення (нМ) 250 107 174 Клонування, експресування та очищення 11βHSD1 Експресування та очищення мишачого ферменту описане [J. Zhang, та іншими. Biochemistry, 44, 2005, стор.6948-57]. Експресування та очищення ферменту людини подібне до експресування та очищення мишачої послідовності. Ферментативне дослідження: ІС50 та Kі сполук визначають наступним способом: 1. Готують буфер дослідження, (рН7,2, 50мМ Tris-HCL, 1мМ EDTA) свіжий кожного тижня. 2. Готують наступні розчини: NADPH (Sigma, 200мкМ) 3 Н-Кортизон (Amersham Biosciences, 45 Сі/ммоль, 200нМ) Ферментний препарат (20нМ для людини, 10нМ для миші) Кортизольне антитіло (East Coast Biologicals, (1:50 розведення) Анти-мишачі SPA гранули (Amersham Biosciences, 15мг/мл) 18β-Гліцирретинова кислота ("GA")(Aldrich, 1мкМ). 46 Вихідний розчин сполуки (10мМ у DMSO), серійно розводять у буфері дослідження. Кожну сполуку тестують при шести різних концентраціях зазвичай (від 10мкМ до 0,1нМ). Всі розчини та розведення роблять у буфері дослідження. 3. Дослідження виконують використовуючи white/white, 96-лункові дослідні планшети (Corning) з загальним об'ємом 100мкл. 4. У кожну лунку 96-лункового планшету додають буфер дослідження (30мкл), сполуку (10мкл) NADPH (10мкл), та 3Н-кортизон (10мкл). 5. Реакцію ініціюють шляхом додавання 40мкл HSD-1 ферментного препарату до комірок. 6. Планшет накривають смужкою та інкубують на орбітальному шейкері впродовж 1 години при RT. 7. Через 1 годину, смужку видаляють та додають анти-кортизольне антитіло (10мкл), GA розчин (10мкл), та препарат SPA гранул (100мкл). 8. Планшет інкубують (30 хвилин) на орбітальному шейкері при RT. 9. Імпульси зчитують на TopCount NXT зчитувачі. 10. Спочатку будують криву залежності від дози, використовуючи Graphpad Prism програмне забезпечення, для одержання значень ІС50. Використовуючи значення ІС50 та відоме значення Km для субстрату та HSD1 ферменту, оцінка Kі може бути розрахована за рівнянням ЧенаПрушофа (Chen та Prusoff equation) {Kі ІС50/[1+(субстрат/Km)]}. = Крім зазначених вище прикладів, всі сполуки даного винаходу показали 11β-HSD1 ферментативну активність (IC50) У дослідженнях, що змінювалася у інтервалі від 10нМ до 10мкМ. Наступні сполуки показали активність у дослідженні ферментативної активності (Enzyme assay) з ІС50 значеннями менше ніж 20нМ: 2-((3-хлор-2-метилфеніл)аміно)-5-(1метилетил)-1,3-тіазол-4(5Н)-он; 5-метил-5-(піридин-4-іл)-2-(2(трифторметил)феніламіно)тіазол-4(5Н)-он; 2-((2-хлорфеніл)аміно)-5-метил-5-феніл-1,3тіазол-4(5Н)-он; (5S)-2-((2-хлорфеніл)аміно)-5-метил-5-феніл1,3-тіазол-4(5Н)-он; (5R)-2-((2-хлорфеніл)аміно)-5-метил-5-(1метилетил)-1,3-тіазол-4(5Н)-он; 2-((2-хлорфеніл)аміно)-5-метил-5-(1метилетил)-1,3-тіазол-4(5Н)-он; 2-((S)-1-циклогексилетиламіно)-5-ізопропіл-5метилтіазол-4(5Н)-он; (5S,7R)-2-(циклооктиламіно)-7-(метилокси)-1тіа-3-азаспіро[4.5]дец-2-ен-4-он; 2-((1S,2S,4R)-біцикло[2.2.1]гептан-2-іламіно)-5метил-5-((тетрагідро-2Н-піран-4-іл)метил)тіазол4(5Н)-он; 2-((5-фтор-2-метилфеніл)аміно)-5-(1-метил етил)-1,3-тіазол-4(5Н)-он; 2-(2-хлорфеніламіно)-5-метил-5-(тетрагідро2Н-піран-4-іл)тіазол-4(5Н)-он; 2-((R)-1-(4-фторфеніл)етиламіно)-5-ізопропіл5-метилтіазол-4(5Н)-он; 2-((2,5-дифторфеніл)аміно)-5-(1-метилетил)1,3-тіазол-4(5Н)-он; 47 86813 48 2-(циклогексилметиламіно)-5-метил-5-((S)тетрагідрофуран-3-іл)тіазол-4(5Н)-он; 5-метил-5-(1-метилетил)-2-((2(трифторметил)феніл)аміно)-1,3-тіазол-4(5Н)-он; 2-((1R,2R,4S)-біцикло[2.2.1]гептан-2-іламіно)-5метил-5-пропілтіазол-4(5Н)-он; 2-(о-толуїдино)-5-циклопентилтіазол-4(5Н)-он ; 2-((2-фторфеніл)аміно)-1-тіа-3азаспіро[4.4]нон-2-ен-4-он; 2-((3-фтортрицикло[3.3.1.1~3,7~]дец-1ил)аміно)-5-метил-5-(1-метилетил)-1,3-тіазол4(5Н)-он; (R)-5-ізопропіл-5-метил-2-((S)-1фенілетиламіно)тіазол-4(5Н)-он; 2-((2,6-дихлорфеніл)аміно)-5-(1-метилетил)1,3-тіазол-4(5Н)-он; 2-(циклогексилметиламіно)-5-((S)тетрагідрофуран-3-іл)тіазол-4(5Н)-он; 2-(біцикло[2.2.1]гепт-2-иламіно)-5-ізопропіл-5метил-1,3-тіазол-4(5Н)-он; 2-(2-хлорфеніламіно)-5-циклопентилтіазол4(5Н)-он; 2-(2-хлорфеніламіно)-5-циклогексилтіазол4(5Н)-он; 2-((2-хлорфеніл)аміно)-5-(1-метилетил)-1,3тіазол-4(5Н)-он ; 2-((S)-1-(4-фторфеніл)етиламіно)-5-метил-5(піридин-4-іл)тіазол-4(5Н)-он; 2-((S)-1-(2-фторфеніл)етиламіно)-5-метил-5(піридин-4-іл)тіазол-4(5Н)-он; 2-(2-фторфеніламіно)-5-((S)-тетрагідрофуран3-іл)тіазол-4(5Н)-он; 2-((1R,2R,4S)-біцикло[2.2.1]гептан-2-іламіно)-5метил-5-(2.2.2-трифторетил)тіазол-4(5Н)-он; 5-етил-5-метил-2-(трицикло[3.3.1.1~3,7~]дец1-иламіно)-1,3-тіазол-4(5 Н)-он; 2-(2-хлорфеніламіно)-5-метил-5-(піридин-4іл)тіазол-4(5Н)-он; 5-циклопентил-2-(2-фторфеніламіно)тіазол4(5Н)-он; 5-циклогексил-2-(2-фторфеніламіно)тіазол4(5Н)-он; 2-((R)-1-(2-фторфеніл)етиламіно)-5-ізопропіл5-метилтіазол-4(5Н)-он; (R)-2-((S)-1-(2-фторфеніл)етиламіно)-5ізопропіл-5-метилтіазол-4(5Н)-он; та 2-((2,4-дихлорфеніл)аміно)-5-(1-метилетил)1,3-тіазол-4(5Н)-он. Приклади синтезу Загальні схеми реакції Всі комерційні вихідні матеріали використовують без будь-якого очищення. Якщо відповідна α-бромкарбонова кислота або складний ефір не є комерційно доступними, речовини одержують відповідно до цього способу: 2-аміно-карбонову кислоту (1,0екв.) суспендують у 2,0Μ H2SO4 (4екв.), додають KВr (8екв.) та суміш охолоджують у льодяній бані. Повільно додають NaNO2 (1,3екв.), розчинений у воді. Реакційну суміш перемішують впродовж 4 годин у льодяній бані, перед тим як залишити досягати кімнатної температури. Реакційну суміш екстрагують за допомогою EtOAc. Органічну фазу сушать над MgSO4 перед концентруванням у вакуумі. Це приводить до одержання сирого продукту, який використовують на наступній стадії без додаткового очищення [J. Org. Chem. 2002, 67 (11), 35953600; Xinhua Qian; Bin Zheng; Brian Burke; Manohar T. Saindane та David R. Kronenthal]. Способи та матеріали 1 H ядерний магнітний резонанс (ЯМР) та 13С ЯМР проводять на Bruker PMR 500 спектрометрі при 500,1МГц та 125,1МГц, відповідно або на JEOL eclipse 270 спектрометрі при 270,0МГц та 67,5МГц, відповідно. Всі спектри записують використовуючи залишковий розчинник або тетраметилсилан (TMS) як внутрішній стандарт. ІЧ спектри записують на Perkin-Elmer Spectrum 1000 FT-IR спектрометрі. Електроспреєву мас-спектрометрію (MS) одержують використовуючи Agilent MSD масспектрометр. Точні визначення мас проводять на Micromass LCT dual probe. Елементні аналізи проводять на Vario El приладі або посилають у Mikro Kеmі у Uppsala. Аналітичну HPLC проводять на Agilent 1100 системі, оснащеній Системою А: АСЕ 3 (С8, 50´3,0мм) або Системою В: YMC ODS-AQ, (33´3,0мм), використовуючи систему елюентів: вода/0,1% TFA та CH3CN, 1мл/хвил., з градієнтом часу 3 хвилини. Препаративну HPLC проводять на Gilson системі, оснащеній Системою А: АСЕ 5 С8 колонка (50´20мм) градієнт часу 5 хвилин, Системою В: YMC ODS-AQ (150´30мм) градієнт часу 8,5 хвилин або Системою С: YMC ODS-AQ (50´20мм) градієнт часу 5 хвилин, використовуючи систему елюентів: вода/0,1% TFA та CH3CN. Препаративну флеш 49 хроматографію проводять на Merck силікагелі 60 (230-400 меш). Методологія синтезу Спосіб А або В використовують в залежності від того, чи використовують ізотіоціанат чи відповідний амін. Амін або ізотіоціанат замовляють або у Maybridge Ріс. або у Sigma-Aldrich Co. Спосіб А 1,0екв. відповідного ізотіоціанату перемішують у 2Μ амоніаку у етанолі (5екв.) впродовж 18 годин при RT. Випарювання у вакуумі приводить до одержання сирого продукту, який кристалізується при додаванні DCM. Кристали збирають на фільтрі та сушать на повітрі зодержанням тіосечовини. Спосіб В 1,0екв. аміну та етоксикарбонілізотіоціанату (1,0екв.) змішують у тестовій пробірці. Сильна екзотермічна реакція приводить до утворення білої пасти. її переносять у 5М розчин КОН та перемішують при 70°С впродовж 2 годин, у цей час LC аналіз показав повний гідроліз споміжної сполуки. Суміш охолоджують, розбавляють водою та екстрагують 3 рази хлороформом. Наступна препаративна LC привела до одержання бажаної тіосечовини. Спосіб С Тіосечовину (1,0екв.) та α-бромскладний ефір/α-бромкислоту (1,0екв.) розчиняють у ацетоні та нагрівають до 60°С у герметично закритій пробірці впродовж 15-72 годин. Розчинник видаляють, та продукт очищують шляхом кристалізації з МеОН / препаративної обернено-фазної HPLC. Спосіб СІ Тіосечовину (1,0екв.) та α-бромскладний ефір/α-бромкислоту (1,0екв.) змішують у воді та нагрівають у мікрохвильовій печі при 140°С впродовж 1 години. Водну фазу екстрагують двічі за допомогою DCM. Об'єднані органічні фази випарюють та одержаний сирий продукт очищують за допомогою препаративної обернено-фазної HPLC. Спосіб D Тіосечовину (1,0екв.) та α-бромскладний ефір (1,0екв.) розчиняють у 1,4-діоксані та нагрівають до 100°С у герметично закритій пробірці впродовж 1-11 днів. Розчинник видаляють, та осад очищують за допомогою препаративної обернено-фазної HPLC. Спосіб D1 Тіосечовину (1,0екв.) та α-бромскладний ефір (1,0екв.) розчиняють у THF та нагрівають до 70°С у герметично закритій пробірці впродовж 1 дня. Розчинник видаляють, та осад очищують за допомогою препаративної обернено-фазної HPLC. Спосіб D2 Тіосечовину (1,0екв.) та α-бромскладний ефір (1,0екв.) розчиняють у 2-пропанолі та нагрівають до 95°С у герметично закритій пробірці впродовж 3 днів. Розчинник видаляють, та осад очищують за допомогою препаративної обернено-фазної HPLC. Спосіб D3 Тіосечовину (1,0екв.) та α-бромскладний ефір/α-бромкислоту (1,0екв.) розчиняють у MeCN та нагрівають до 60°С у герметично закритій пробірці впродовж 2 днів. Розчинник видаляють, та 86813 50 осад очищують за допомогою препаративної обернено-фазної HPLC. Спосіб Ε Аміно-кислоту (1екв.) суспендують у 2,0Μ H2SO4, додають KВr (8екв.) та суміш охолоджують у льодяній бані. Повільно додають NaNO2 (1,3екв.), розчинений у воді. Реакційну суміш перемішують впродовж 4 годин, в той час як охолодження продовжується. Реакційну суміш потім екстрагують за допомогою EtOAc, промивають сольовим розчином та сольовим розчином, що містить Na2S2O3. Органічну фазу концентрують у вакуумі. Продукт використовують на наступній стадії без додаткового очищення. Спосіб F Тіосечовину (1екв.) та 3-бром-2-кумарон (1екв.) розчиняють у ацетоні та нагрівають до 60°С впродовж 3 годин. Додають воду. Збирають отриману тверду речовину. Перекристалізовують з суміші вода/MeCN. Збирають тверду речовину. Маточну рідину концентрують та отриману тверду речовину сушать у вакуумі з одержанням продукту. Спосіб G Карбонатну сіль гуанідину (1екв.) та альфагідрокси-складного ефіру (1екв.) розчиняють у EtOH та нагрівають до температури зрошення впродовж 2-10 годин. Суміш потім виливають у Н2О та залишають при 8°С впродовж 16 годин. Продукт збирають фільтруванням. Спосіб Η Аміно-оксазолон (1екв.) та амін (3екв.) додають до 4мл ЕtOН та поміщають у мікрохвильову піч при 130°С на 30 хвилин. Розчинник видаляють у вакуумі та продукти очищають за допомогою препаративної обернено-фазної HPLC. Спосіб І До охолодженого льодом розчину з 1екв. тіосечовини у DCM додають 3екв. 5% NaOH (водн.) та 2екв. дибромбутирил-хлориду, а потім невелику кількість бензилтриетиламоній хлориду. Реакційну суміш залишають для досягнення кімнатної температури та додають додаткові 5екв. 5% NaOH (водн.). DCM-шар відділяють та промивають двічі водою, сушать над MgSO4, фільтрують та концентрують. Продукт виділяють за допомогою препаративної обернено-фазної HPLC. Спосіб J Кислоту (1екв.) розчиняють у SOCl2 та нагрівають до 60°С впродовж 2 годин. NBS (2екв.), SOCl2 та 1 краплю НВr (водн.) додають при r.t. Реакційну суміш нагрівають до температури зрошення впродовж 75 хвилин. Розчинник видаляють у вакуумі, додають ССl4 та його відфільтровують. ССІ4 видаляють у вакуумі. Масло, що залишилося, розчиняють у ЕtOН та залишають на 16 годин при r.t. Розчинник потім видаляють у вакуумі. Це приводить до одержання продукту у вигляді αбромскладного ефіру. Приклади Способи A-J використовують для одержання сполук Прикладів 1-79, як описано нижче. Приклад 1 2-(біцикло[2.2.1]гепт-2-иламіно)-5ізопропіл-1,3-тіазол-4(5Н)-он 51 86813 52 Приклад 6 5-Ізопропіл-2(трицикло[3.3.1.0~3,7~]нон-3-іламіно)-1,3-тіазол4(5Н)-он Синтез проводять з N-біцикло[2.2.1]гепт-2илтіосечовини та етил 2-бромізовалерату відповідно до Способу С. 1 H ЯМР (400МГц, DMSO-d6) δ ppm 0,79 (m, 3Η), 0,97 (m, 3Η), 1,10 (m, 3Η), 1,45 (m, 4Η), 1,69 (m, 1Η), 2,22 (m, 2Η), 2,36 (m, 1Η), 3,74 (m, 1Η), 4,37 (m, 1Η), 9,56 (s, 1Η). MS (ESI+) для C13H20N2OS m/z 253 (M+H)+. Приклад 2 2-(біцикло[2.2.1]гепт-2-иламіно)-5етил-1,3-тіазол-4(5Н)-он Синтез проводять з N-біцикло[2.2.1]гепт-2илтіосечовини та етил 2-бромбутирату відповідно до Способу С 1 H ЯМР (400МГц, DMSO-d6) δ ppm 0,90 (m, 3Η), 1,03-1,23 (m, 3Η), 1,35-1,56 (m, 4Η), 1,65-1,84 (m, 2Η), 1,98 (m, 1Η), 2,24 (m, 2Η), 3,75 (m, 1Η), 4,22-4,40 (m, 1Η), 9,84 (s, 1Η). MS (ESI+) для C12H18N2OS m/z 239 (M+H)+. Приклад 3 2-(біцикло[2.2.1]гепт-2-иламіно)-5феніл-1,3-тіазол-4(5Н)-он Синтез проводять з N-біцикло[2.2.1]гепт-2илтіосечовини та метил-альфа-бромфенілацетату відповідно до Способу С. 1 H ЯМР (400МГц, DMSO-d6) δ ppm 1,05-1,24 (m, 3Η), 1,36-1,56 (m, 4Η), 1,66-1,80 (m, 1Η), 2,222,33 (m, 2Η), 3,78-3,90 (m, 1Η), 5,41 (s, 0,5Η), 5,43 (s, 0,5Η), 7,21-7,41 (m, 5Η), 9,39 (d, J=6,35Гц, 1Η). MS (ESI+) для C16H18N2OS m/z 287 (M+H)+. Приклад 4 2-(циклогексиламіно)-5-етил-1,3тіазол-4(5Н)-он Синтез проводять з н-циклогексилтіосечовини та етил 2-бромбутирату відповідно до Способу С. Одержують 201мг (75%). 1 H ЯМР (400МГц, DMSO-d6) δ ppm 0,91 (m, 3Η), 1,05-2,06 (m, 12Η), 3,76 (m, 1Η), 4,36 (m, 1Η), 10,11 (s, 1Η). MS (ESI+) для C11H18N2OS m/z 227 (M+H)+. Приклад 5 2-(біцикло[2.2.1]гепт-2-иламіно)-5,5диметил-1,3-тіазол-4(5Н)-он Синтез проводять з N-біцикло[2.2.1]гепт-2илтіосечовини та етил 2-бромізобутирату відповідно до Способу С. 1 H ЯМР (400МГц, DMSO-d6) δ ppm 1,05-1,21 (m, 3Η), 1,34-1,54 (m, 4Η), 1,48 (s, 2Η), 1,49 (s, 2Η), 1,50 (s, 1Η), 1,51 (s, 1Η), 1,67-1,74 (m, 1Η), 2,182,28 (m, 2Η), 3,20 (dd, J=7,69, 2,93Гц, 0,25Η), 3,733,82 (m, 0,75Η), 9,12 (d, J=6,59Гц, 1Η). MS (ESI+) для C12H18N2OS m/z 239 (M+H)+. Синтез проводять з Nтрицикло[3.3.1.0~3,7~]нон-3-ілтіосечовини та етил2-бром-3-метилбутаноату відповідно до Способу С. 1 H ЯМР (400МГц, DMSO-d6) δ 0,75 (d, J=6,6Гц, 3Η), 0,95 (d, J=6,8Гц, 3Н), 1,46-1,57 (m, 4Η), 1,882,10 (m, 6Η), 2,22-2,37 (m, 3Η), 2,43 (t, J=6,7Гц, 1Η), 4,23 (d, J=3,5Гц, 1Η), 9,29 (s, 1Η). MS (ESI+) для C15H22N2OS m/z 279 (М+Н)+. Приклад 7 6-(трицикло[3.3.1.0~3,7~]нон-3іламіно)-5-тіа-7-азаспіро[3.4]окт-6-ен-8-он Синтез проводять з Nтрицикло[3.3.1.0~3,7~]нон-3-ілтіосечовини та етил 1-бромциклобутанкарбоксилату відповідно до Способу D. 1 H ЯМР (400МГц, DMSO-d6) δ 1,45-1,57 (m, 4Η), 1,90-2,16 (m, 8Η), 2,22-2,27 (m, 2Η), 2,44-2,55 (m, 5Η, накладений з сигналом розчиннику), 9,24 (s, 1Η). MS (ESI+) для C5H20N2OS m/z 277 (М+Н)+. Приклад 8 2-(Трицикло[3.3.1.0~3,7~]нон-3іламіно)-1,3-тіазол-4(5Н)-он Синтез проводять з Nтрицикло[3.3.1.0~3,7~]нон-3-ілтіосечовини та етил бромацетату відповідно до Способу D1. 1 H ЯМР (400МГц, DMSO-d6) δ 1,45-1,61 (m, 4Η), 1,92-2,07 (m, 6Η), 2,23 (m, 1,7Η, головний ротамер), 2,82 (m, 0,3Η, мінорний ротамер), 2,45 (t, J=6,7Гц, 0,85Η, головний ротамер), 2,66 (t, J=6,8Гц, 0,15Η, мінорний ротамер), 3,83 (s, 1,7Η, головний ротамер), 4,09 (s, 0,3Η, мінорний ротамер), 9,38 (s, 1Η). MS (ESI+) для C12H16N2OS m/z 237 (M+H)+. Приклад 9 6-(Циклооктиламіно)-5-тіа-7азаспіро[3.4]окт-6-ен-8-он Синтез проводять з N-циклооктилтіосечовини та етил 1-бромциклобутан-карбоксилату відповідно до Способу D2. 1 H ЯМР (400МГц, DMSO-d6) δ 1,45-1,79 (m, 14Η), 1,86-2,00 (m, 1Η), 2,05-2,17 (m, 1Η), 2,41-2,53 (m, 4Η, накладений з сигналом розчиннику), 4,01 (m, 1Н), 9.09(d, J=7,5Гц, 1Н). 13 С ЯМР (100МГц, DMSO-d6) δ 16,31, 23,07, 24,97, 26,69, 30,88, 33,52, 54,69, 60,30, 175,09, 191,25, MS (ESI+) для C4H22N2OS m/z 267 (М+Н)+. Приклад 10 6-(Циклогептиламіно)-5-тіа-7азаспіро [3.4] окт-6-ен-8-он 53 Синтез проводять з N-циклогептилтіосечовини та етил 1-бромциклобутан-карбоксилату відповідно до Способу D. 1 H ЯМР (400МГц, DMSO-d6) δ 1,35-1,65 (m, 10Η), 1,83-1,97 (m, 3Η), 2,05-2,17 (m, 1Η), 2,41-2,53 (m, 4Η, накладений з сигналом розчиннику), 3,96 (m, 1Н), 9.09 (d, J=7,5Гц, 1Η). MS (ESI+) для C13H20N2OS m/z 253 (M+H)+. Приклад 11 6-(Біцикл о [2.2.1]гепт-2-иламіно)5-тіа-7-азаспіро [3.4]окт-6-ен-8-он Синтез проводять з N-біцикло[2.2.1]гепт-2илтіосечовини та етил 1-бромциклобутанкарбоксилату відповідно до Способу D. 1 H ЯМР (400МГц, DMSO-d6) δ 1,05-1,22 (m, 3Η), 1,33-1,49 (m, 4Η), 1,63-1,70 (m, 1Η), 1,86-2,00 (m, 1Η), 2,05-2,22 (m, 3Η), 2,42-2,53 (m, 4Η, накладений з сигналом розчиннику), 3,74 (m, 1Н), 8,98 (d, J=7,5Гц, 1Η). MS (ESI+) для C13H18N2OS m/z 251 (M+H)+. Приклад 12 6-[(2,2,3,3Тетраметилциклопропіл)аміно]-5-тіа-7азаспіро[3.4]окт-6-ен-8-он Синтез проводять з N-(2,2,3,3тетраметилциклопропіл)тіосечовини та етил 1бромциклобутанкарбоксилату відповідно до Способу D. 1 H ЯМР (400МГц, DMSO-d6) δ 0,92 (s, 3Η), 0,94 (s, 3Η), 1,06 (s, 3Η), 1,08 (s, 3Η), 1,88-2,00 (m, 1Η), 2,01 (s, 1Η), 2,06-2,17 (m, 1Η), 2,40-2,54 (m, 4Η, накладений з сигналом розчиннику), 8,78 (s br., 1Η). MS (ESI+) для C13H20N2OS m/z 253 (M+H)+. Приклад 13 6-[(2-Метилфеніл)аміно]-5-тіа-7азаспіро[3.4]окт-6-ен-8-он Синтез проводять з N-(2метилфеніл)тіосечовини та етил 1бромциклобутан-карбоксилату відповідно до Способу D. 1 H ЯМР (400МГц, DMSO-d6) δ 1,89 (m, 1Η), 2,04-2,13 (m, 1Η), 2,08 (s, 3Η), 2,39-2,48 (m, 2Η), 2,56-2,66 (m, 2Η), 6,81 (d, J=7,6Гц, 1Η), 7,03 (m, 1Η), 7,14 (m, 1Η), 7,20 (d, J=7,4Гц, 1Η), 11,67 (s br., 1Η). MS (ESI+) для C13H14N2OS m/z 247 (M+H)+. Приклад 14 2-[(циклогексилметил)аміно]-5,5диметил-1,3-тіазол-4(5Н)-он 86813 54 Синтез проводять з N(циклогексилметил)тіосечовини та етил 2бромізобутирату відповідно до Способу С 1 H ЯМР (270МГц, DMSO-d6) δ ppm 0,81-1,04 (m, 2Η), 1,03-1,32 (m, 3Η), 1,43-1,54 (m, 6Η), 1,551,78 (m, 6Η), 3,18-3,32 (m, 2Η), 9,28 (s, 1Η). MS (ESI+) для C12H20N2OS m/z 242 (М+Н)+. Приклад 15 2-[(2-фторфеніл)аміно]-5ізопропіл-1,3-тіазол-4(5Н)-он Синтез проводять з N-(2фторфеніл)тіосечовини та етил 2-бром-2метилбутирату відповідно до Способу С. 1 H ЯМР (270МГц, DMSO-d6) δ ppm 0,79-0,98 (m, 6Η), 2,29-2,44 (m, 1Η), 4,48 (d, J=3,59Гц, 1Η), 6,91-7,40 (m, 4Η). MS (ESI+) для C12H13FN2OS m/z 253 (M+H)+. Приклад 16 2-[(циклогексилметил)аміно]-5-(2гідроксифеніл)-1,3-тіазол-4(5Н)-он Синтез проводять з N(циклогексилметил)тіосечовини та 3-бром-2кумарону відповідно до Способу F. 1 H ЯМР (400МГц, ХЛОРОФОРМ-D) δ ppm 0,801,00 (m, 2H), 1,05-1,27 (m, 3Η), 1,55-1,81 (m, 6H), 3,24-3,34 (m, 2H), 5,42 (s, 1H), 6,73-6,81 (m, 2H), 7,02-7,14 (m, 2H), 9,19 (br.s, 1H, N-H), 9,81 (br.s, 1H, N-H). MS (ESI+) для C16H20N2O2S m/z 305 (M+H)+. Приклад 17 (5S)-2-(циклогептиламіно)-5метил-1,3-тіазол-4(5Н)-он Синтез проводять з N-циклогептилтіосечовини та (2S)-2-бромпропіонової кислоти відповідно до Способу С. 1 H ЯМР (400МГц, ХЛОРОФОРМ-D) δ ppm 1,351,70 (m, 12H), 1,45 (d, J=7,3Гц, 3Η), 1,72-2,00 (m, 1H), 3,90-4,03 (m, 1H). MS (ESI+) для C11H18N2OS m/z 227 (M+H)+. Приклад 18 (5R)-2-(циклогептиламіно)-5метил-1,3-тіазол-4(5Н)-он Синтез проводять з N-циклогептилтіосечовини та (2R)-2-бромпропіонової кислоти відповідно до Способу С. 1 H ЯМР (400МГц, ХЛОРОФОРМ-D) δ ppm 1,361,70 (m, 12H), 1,45 (d, J=7,5Гц, 3Η), 1,82-1,96 (m, 1H), 3,93-4,02 (m, 1H). MS (ESI+) для C11H18N2OS m/z 227 (M+H)+. 55 86813 56 Приклад 19 2-(циклогептиламіно)-5-етил-1,3тіазол-4(5Н)-он Синтез проводять з N-циклогептилтіосечовини та 2-броммасляної кислоти відповідно до Способу С 1 H ЯМР (270МГц, МЕТАНОЛ-d4) δ ppm 0,901,06 (m, 3Η), 1,40-2,17 (m, 14Η), 4,26 (dd, J=7,86, 4,02Гц, 1Η), 4,52-4,68 (m, 1Η). MS (ESI+) для C12H20N2OS m/z 241 (M+H)+. Приклад 20 2-(циклогептиламіно)-5-ізопропіл1,3-тіазол-4(5Н)-он Синтез проводять з N-(2ізопропілфеніл)тіосечовини та 2-бром-3метилмасляної кислоти відповідно до Способу С1. 1 H ЯМР (270МГц, DMSO-d6) δ ppm 0,87 (dd, J=8,78, 6,80Гц, 6H), 1,12-1,17 (m, 6H), 2,28-2,44 (m, 1H), 2,93-3,09 (m, 1H), 4,40 (d, J=3,46Гц, 1Η), 6,83 (dd, J=7,24, 1,79Гц, 1Η), 7,07-7,21 (m, 2Η), 7,267,36 (m, 1Η). MS (ESI+) для C15H20N2OS m/z 277 (M+H)+. Приклад 24 5-етил-2-[(2-ізопропілфеніл)аміно]1,3-тіазол-4(5Н)-он Синтез проводять з N-циклогептилтіосечовини та етил 2-бром-2-метилбутирату відповідно до Способу С 1 H ЯМР (270МГц, МЕТАНОЛ-d4) суміш трьох різних ротамерів-40%/30%/30% тільки основних; δ ppm 0,92-1,08 (m, 6Η), 1,43-2,16 (m, 12Η), 2,39-2,56 (m, 1Η), 3,98-4,20 (m, 1Η), 4,24-4,34 (m, 1Η). MS (ESI+) для C13H22N2OS m/z 255 (M+H)+. Приклад 21 5-трет-бутил-2(циклогептиламіно)-1,3-тіазол-4(5Н)-он Синтез проводять з N-(2ізопропілфеніл)тіосечовини та 2-бром-масляної кислоти відповідно до Способу С1. 1 H ЯМР (270МГц, DMSO-d6) δ ppm 0,88 (t, J=7,30Гц, 3Η), 1,14 (d, J=6,93Гц, 6Η), 1,63-2,06 (m, 2Η), 2,93-3,11 (m, 1Η), 4,32 (dd, J=7,36,4,27Гц, 1Η), 6,75-6,92 (m, 1Η), 7,06-7,21 (m, 2Η), 7,24-7,42 (m, 1Η). MS (ESI+) для C14H18N2OS m/z 263 (M+H)+. Приклад 25 2-[(2-хлорфеніл)аміно]-5-етил-1,3тгіазол-4(5Н)-он Синтез проводять з 2-аміно-3,3диметилбутанової кислоти та Nциклогептилтіосечовини відповідно до Способу Ε та С 1 H ЯМР (270МГц, МЕТАНОЛ-d4) δ ppm 0,830,94 (m, 4,5Η), 0,98-1,12 (m, 4,5Η), 1,47-1,97 (m, 11Η), 2,36-2,58 (m, 1Η), 4,03-4,18 (m, 1Η), 4,34-4,42 (m, 1Η). MS (ESI+) для C14H24N2OS m/z 269 (M+H)+. Приклад 22 2-(циклооктиламіно)-5-етил-1,3тіазол-4(5Н)-он Синтез проводять з N-(2хлорфеніл)тіосечовини та 2-бром-масляної кислоти відповідно до Способу С1. 1 H ЯМР (270МГц, МЕТАНОЛ-d4) δ ppm 1,011,23 (m, 3Η), 1,98-2,34 (m, 2Η), 4,58-4,72 (m, 1Η), 7,28-7,54 (m, 3Η), 7,54-7,68 (m, 1Η). MS (ESI+) для C11H11ClN2OS m/z 255 (M+H)+. Приклад 26 5-етил-2-[(2-метилфеніл)аміно]1,3-тіазол-4(5Н)-он Синтез проводять з N-циклооктил-тіосечовини та 2-бром-масляної кислоти відповідно до Способу С1. 1 H ЯМР (270МГц, МЕТАНОЛ-d4) δ ppm 0,891,03 (m, 3Η), 1,43-1,99 (m, 15Η), 1,98-2,16 (m, 1Η), 4,21-4,32 (m, 1Η), 4,55-4,66 (m, 1Η). MS (ESI+) для C13H22N2OS m/z 255 (M+H)+. Приклад 23 5-ізопропіл-2-[(2ізопропілфеніл)аміно]-1,3-тіазол-4(5Н)-он Синтез проводять з N-(2метилфеніл)тіосечовини та 2-бром-масляної кислоти відповідно до Способу С1. 1 H ЯМР (270МГц, МЕТАНОЛ-d4) δ ppm 1,071,18 (m, J=7,36, 7,36Гц, 3Η), 1,98-2,36 (m, 2Η), 2,11-2,13 (m, 3Η), 4,52-4,75 (m, 1Η), 7,12 (dd, J=20,54, 7,67Гц, 1Η), 7,22-7,46 (m, 3Η). MS (ESI+) для C12H14N2OS m/z 235 (M+H)+. Приклад 27 5-попропіл-2-[(2,2,3,3тетраметилциклопропіл)аміно]-1,3-тіазол-4(5Н)-он 57 86813 Синтез проводять з N-(2,2,3,3тетраметилциклопропіл)тіосечовини та етил-2бромізовалерату відповідно до Способу С. 1 H ЯМР (400МГц, CDCl3) δ ppm 0,99 (d, J=6,6Гц, 3Η), 1,08-1,16 (m, 9Η), 1,20 (d, J=3,4Гц, 6Η), 2,17 (s, 1Η). 2,59-2,72 (m, 1Η), 4,25 (d, J=3,9Гц, 1Η). MS (ES+) m/z 255 (M+H+). Приклад 28 2-(біцикло[2.2.1]гепт-2-иламіно)-5(4-гідроксибензил)-1,3-тіазол-4(5Н)-он Синтез проводять з (2S)-2-аміно-3-(4гідроксифеніл)пропіонової кислоти та Nбіцикло[2.2.1]гепт-2-илтіосечовини відповідно до Способу Ε та С. 1 H ЯМР (270МГц, DMSO-d6) δ 1,11 (d, J=9,65Гц, 3Η), 1,24-1,54 (m, 4Η), 1,56-1,76 (m, 1Η), 2,04-2,27 (m, 2Η), 2,61-2,84 (m, 1Η), 3,26 (dd, J=14,10, 3,96Гц, 1Η), 3,70 (s, 1Η), 4,42-4,52 (накладений з HDO піком) (m, 1Η), 6,57-6,72 (m, 2Η), 6,92-7,08 (m, 2Η), 9,07 (d, J=6,19Гц, 1Η). 1 H ЯМР (270МГц, МЕТАНОЛ-d4) δ 1,07-1,62 (m, 7Η), 1,67-1,88 (m, 1Η), 2,07-2,36 (m, 2Η), 2,92-3,11 (m, 1Η), 3,32-3,44 (частково накладений з MeOD піком) (m, 1Η), 3,64-3,76 (m, 1Η), 4,51-4,68 (m, 1Η), 6,62-6,76 (m, 2Η), 6,99-7,12 (m, 2Η). MS (ESI+) для C17H20N2O2S m/z 317 (M+H)+. Приклад 29 5-[(циклогексил метил)аміно]-4-тіа6-азаспіро[2,4]гепт-5-ен-7-он Синтез проводять з N(циклогексилметил)тіосечовини відповідно до Способу І. 1 H ЯМР (400МГц, ХЛОРОФОРМ-D) δ ppm 0,941,07 (m, 2Η), 1,10-1,36 (m, 3Η), 1,49-1,54 (m, 2Η), 1,66-1,86 (m, 8Η), 3,19 (d, J=6,59Гц, 2Η). MS m/z 239 (M+H)+. Приклад 30 2-(циклогептиламіно)-5-(3,4дигідроксибензил)-1,3-тіазол-4(5Н)-он Синтез проводять з (2S)-2-аміно-3-(3,4дигідроксифеніл)пропіонової кислоти та Nциклогептилтіосечовини відповідно до Способу Ε та С. 1 H ЯМР (500МГц, Розчинник) δ 1,43-1,57 (m, 6Η), 1,56-1,73 (m, 5Η), 1,84-2,01 (m, 2Η), 2,87 (dd, J=14,13, 9,42Гц, 1Η) (1Η прихований у піку MeOD), 3,97-4,06 (m, 1Η), 4,44-4,51 (m, 1Η), 6,52-6,57 (m, 1Η), 6,64-6,68 (m, 2Η). MS (ESI+) для C17H22N2O3S m/z 335 (М+Н)+. Приклад 31 2-(циклогептиламіно)-5-(1Німідазол-4-ілметил)-1,3-тіазол-4(5Н)-он Синтез проводять імідазол-4-іл)пропіонової з (2S)-2-аміно-3-(1Hкислоти та N 58 циклогептилтіосечовини відповідно до Способу Ε та С. 1 H ЯМР (270МГц, МЕТАНОЛ-d4) δ 1,43-2,06 (m, 12Η), 3,33-3,56 (m, 2Η), 3,93-4,08 (m, 1Η), 4,57-4,69 (m, 1Η), 7,27-7,42 (m, 1Η), 8,76-8,87 (m, 1Η). MS (ESI+) для C14H20N4OS m/z 293 (M+H)+. Приклад 32 2-(циклогептиламіно)-5-ізобутил1,3-тіазол-4(5Н)-он Синтез проводять з (2S)-2-аміно-4метилпентанової кислоти та Nциклогептилтіосечовини відповідно до Способу Ε та С. 1 H ЯМР (270МГц, МЕТАНОЛ-d4) δ 0,91-1,04 (m, 6Η), 1,43-1,86 (m, 12Η), 1,92-2,12 (m, 3Η), 3,95-4,11 (m, 1Η), 4,29-4,48 (m, 1Η). MS (ESI+) для C14H24N2OS m/z 269 (М+Н)+. Приклад 33 2-(циклогептиламіно)-5-(1H-індол3-ілметил)-1,3-тіазол-4(5Н)-он Синтез проводять з (2S)-2-аміно-3-(1H-індол-3іл)пропіонової кислоти та Nциклогептилтіосечовини відповідно до Способу Ε та С. 1 H ЯМР (270МГц, ХЛОРОФОРМ-D) δ 1,27-1,80 (m, 11Η), 1,84-1,99 (m, 1Η), 3,23-3,40 (m, 2Η), 3,76 (dd, J=15,09, 3,46Гц, 1Η), 4,65 (d, J=9,15, 3,96Гц, 1Η), 7,10-7,28 (m, 3Η), 7,40 (d, J=7,92Гц, 1Η), 7,59 (d, J=7,92Гц, 1Η), 8,26 (s, 1Η). MS (ESI+) для C19H23N3OS m/z 342 (М+Н)+. Приклад 34 2-(циклогептиламіно)-5-(4гідроксибензил)-1,3-тіазол-4(5Н)-он Синтез проводять з (2S)-2-аміно-3-(4гідроксифеніл)пропіонової кислоти та Nциклогептилтіосечовини відповідно до Способу Ε та С. 1 H ЯМР (270МГц, МЕТАНОЛ-d4) δ ppm 1,372,07 (m, 12Η), 2,91-3,11 (m, 1Η), 3,32-3,43 (m, 1Η), 3,86-4,02 (m, 1Η), 4,48-4,66 (m, 1Η), 6,60-6,76 (m, 2Η), 6,99-7,11 (m, 2Η). MS (ESI+) для C17H22N2O2S m/z 319 (М+Н)+. Приклад 35 (5R)-2-(циклогептиламіно)-5(циклогексилметил)-1,3-тіазол-4(5Н)-он Синтез проводять з (2S)-2-аміно-3циклогексилпропіонової кислоти та Nциклогептилтіосечовини відповідно до Способу Ε та С. 1 H ЯМР (270МГц,ХЛОРОФОРМ-D) δ ppm 0,851,90 (m, 22Η), 1,93-2,10 (m, 2Η), 2,14-2,30 (m, 1Η), 3,35-3,57 (m, 1Η), 4,23 (dd, J=11,32, 3,77Гц, 1Η). MS (ESI+) для C17H28N2OS m/z 309 (M+H)+. Приклад 36 2-(циклооктиламіно)-5-(4гідроксибензил)-1,3-тіазол-4(5Н)-он 59 Синтез проводять з (2S)-2-аміно-3-(4гідроксифеніл)пропіонової кислоти та Nциклооктилтіосечовини відповідно до Способу Ε та С. 1 H ЯМР (270МГц, ХЛОРОФОРМ-D) δ ppm 1,411,95 (m, 14Η), 3,07 (dd, J=14,47, 9,65Гц, 1Η), 3,433,59 (m, 2Η), 4,46 (dd, J=9,65, 3,96Гц, 1Η), 6,81 (d, J=8,41Гц, 2Η), 7,08 (d, J=8,41Гц, 2Η). MS (ESI+) для C18H24N2O2S m/z 333 (M+H)+. Приклад 37 (5S)-2-(циклогептиламіно)-5(циклогексилметил)-1,3-тіазол-4(5Н)-он Синтез проводять з (2R)-2-аміно-3циклогексилпропіонової кислоти та Nциклогептилтіосечовини відповідно до Способу Ε та С. 1 H ЯМР (270МГц, ХЛОРОФОРМ-D) δ ppm 0,871,86 (m, 22Η), 1,89-2,11 (m, 2Η), 2.11-2,30 (m, 1Η), 3,34-3,60 (m, 1Η), 4,23 (dd, J=11,32, 3,77Гц, 1Η), 8,81 (br.s, 1Η). MS (ESI+) для C17H28N2OS m/z 309 (M+H)+. Приклад 38 [2-(циклогептиламіно)-4-оксо-4,5дигідро-1,3-тіазол-5-іл] ацето-нітрил Синтез проводять з (2S)-2-аміно-3ціанопропіонової кислоти та Nциклогептилтіосечовини відповідно до Способу Ε та С. 1 H ЯМР (270МГц, ХЛОРОФОРМ-D) δ ppm 1,362,14 (m, 12Η), 2,85-3,11 (m, 1Η), 3,12-3,32 (m, 1Η), 3,43-3,58 (m, 1Η), 4,31-4,46 (m, 1Η). MS (ESI+) для C12H17N3OS m/z 252 (M+H)+. Приклад 39 5-етил-2-[(3-метилфеніл)аміно]1,3-тіазол-4(5Н)-он Комерційна сполука, SPECS. MS (ESI+) для C12H14N2OS m/z 235 (М+Н)+ HPLC 99%, RT=2,10хвил. (Система А, 10-97% MeCN впродовж 3хвил.). HPLC 99%, RT=1,58хвил. (Система В, 10-97% MeCN впродовж 3хвил.). Приклад 40 2-(циклогептиламіно)-5-(піридин-3ілметил)-1,3-тіазол-4(5Н)-он Синтез проводять з (2S)-2-аміно-3-піридин-3ілпропіонової кислоти та Nциклогептилтіосечовини відповідно до Способу Ε та С 1 H ЯМР (270МГц, ХЛОРОФОРМ-D) δ ppm 1,391,84 (m, 9Η), 1,88-2,06 (m, 2Η), 3,39-3,54 (m, 1Η), 3,64 (s, 2Η), 3,97 (s, 1Η), 4,75 (s, 1Η), 7,84-7,95 (m, 86813 60 1Η), 8,34 (d, J=7,67Гц, 1Η), 8,75 (d, J=5,07Гц, 1Η), 9,10 (s, 1Η). MS (ESI+) для C16H21N3OS m/z 304 (M+H)+. Приклад 41 5-Ізопропіл-2-[(2метилфеніл)аміно]-1,3-тіазол-4(5Н)-он Синтез проводять з N-(2метилфеніл)тіосечовини та етил 2-бром-3метилбутаноату відповідно до Способу С. 1 H ЯМР (400МГц, DMSO-d6) δ 0,84 (d, J=6,6Гц, 3Η), 0,88 (d, J=7,0Гц, 3Η), 2,10 (s, 3Η), 2,34 (m, 1Η), 4,32 (d, J=3,4Гц, 1Η), 6,83 (d, J=7,8Гц, 1Η), 7,03 (m, 1Η), 7,16 (m, 1Η), 7,21 (d, J=7,6Гц, 1Η). MS (ESI+) для C13H16N2OS m/z 249 (M+H)+. Приклад 42 2-(Циклооктиламіно)-5,5-диметил1,3-тіазол-4(5Н)-он Синтез проводять з етил-2-бром-2метилпропаноату та N-циклооктилтіосечовини відповідно до Способу С1. 1 H ЯМР (270МГц, DMSO-d6) δ ppm 1,46 (s, 3H), 1,47 (s, 3Η), 1,81-1,43 (m, 15H). MS (EI+) для C13H22N2OS m/z 255 (M+H)+. Приклад 43 2-(Циклооктиламіно)-5-ізопропіл1,3-тіазол-4(5Н)-он Синтез проводять з 2-бром-3-метилмасляної кислоти та N-циклооктил-тіосечовини відповідно до Способу С1. 1 H ЯМР (270МГц, МЕТАНОЛ-d4) Головний ізомер: δ ppm 0,85 (d, J=6,68Гц, 3Η), 1,01 (d, J=6,93Гц, 3Η), 1,44-1,91 (m, 14Η), 2,36-2,52 (m, 1Η), 3,98-4,12 (m, 1Η), 4,36 (d, J=3,71Гц, 1Η). MS (ΕΙ+) для C14H24N2OS m/z 269 (М+Н)+. Приклад 44 2-(Біцикло[2.2.1]гепт-2-иламіно)-1тіа-3-азаспіро[4.5]дец-2-ен-4-он Синтез проводять з N-біцикло[2.2.1]гепт-2илтіосечовини та метил 1бромциклогексанкарбоксилату відповідно до Способу D. 1 H ЯМР (400МГц, CDCI3) δ 1,12-2,44 (m, 21Η), 3,34 (m, 1Η). MS (ESI+) для C15H22N2OS m/z 279 (M+H)+. Приклад 45 2-(Трицикло[3.3.1.0~3,7~]нон-3іламіно)-1-тіа-3-азаспіро[4.5]дец-2-ен-4-он Синтез проводять з Nтрицикло[3.3.1.0~3,7~]нон-3-ілтіосечовини та метил 1-бромциклогексанкарбоксилату відповідно до Способу D. 1 H ЯМР (400МГц, CDCI3) δ 1,24-2,19 (m, 20 Η), 2,30 (m, 0,5Η, мінорний ротамер), 2,41 (m, 1,5Η, головний ротамер), 2,53 (m, 0,25Η, мінорний ротамер), 2,75 (m, 0,75Η, головний ротамер). MS (ESI+) для C17H24N2OS m/z 305 (М+Н)+. Приклад 46 2-(Циклогептиламіно)-1-тіа-3азаспіро [4.5]дец-2-ен-4-он
ДивитисяДодаткова інформація
Назва патенту англійськоюInhibitors of 11-beta-hydroxy steroid dehydrogenase type 1
Автори англійськоюHenriksson Martin, Homan Evert, Johansson Lars, Vallgarda Jerk, Williams Meredith, Bercot Eric, Fotsch Christopher H., Li Aiwen, Cai Guolin, Hungate Randall W., Yuan Chester Chenguang, Tegley Chirstopher, St. Jean David, Han Nianhe, Huang Qi, Liu Qingyian, Bartberger Michael D., Moniz George A., Frizzle Matthew J.
Назва патенту російськоюИнгибиторы бета-гидроксистероидной дегидрогеназы типа 1
Автори російськоюХенрикссон Мартин, Хоман Эверт, Йоханссон Ларс, Валлгарда Йерк, Уильямс Мередит, Беркот Эрик, Фотсч Кристофер Х., Ли Айвен, Кей Гуолин, Хангейт Рендалл У., Юан Честер Ченгуанг, Тигли Кристофер, Ст. Джин Девид, Хен Найанхе, Хуанг Куи, Лиу Куингюян, Бартбергер Майкл Д., Мониз Джордж А., Фриззл Меттью Дж.
МПК / Мітки
МПК: A61P 19/10, C07D 263/48, A61P 3/00, A61P 25/24, C07D 277/54, A61P 3/04, A61K 31/42, A61P 25/28, A61P 31/12, A61K 31/436, A61P 3/06, A61P 3/10, A61P 29/00
Мітки: інгібітори, 11-бета-гідроксистероїдної, типу, дегідрогенази
Код посилання
<a href="https://ua.patents.su/151-86813-ingibitori-11-beta-gidroksisterodno-degidrogenazi-tipu-1.html" target="_blank" rel="follow" title="База патентів України">Інгібітори 11-бета-гідроксистероїдної дегідрогенази типу 1</a>
Попередній патент: Спосіб прямого одержання електричної енергії з електрохімічної реакції та пристрій для його реалізації
Наступний патент: Ключ гайковий динамометричний
Випадковий патент: Спосіб фітотерапії залишкових явищ перенесених гострих гепатитів












