9-o-оксимові похідні еритроміцину а та фармацевтична композиція на їх основі
Номер патенту: 48958
Опубліковано: 16.09.2002
Автори: Сантанжело Франческо, Альбіні Енріко, Ботта Даніела, Романьяно Стефано, Скоппакассі Джованна, Пеллачіні Франко
Формула / Реферат
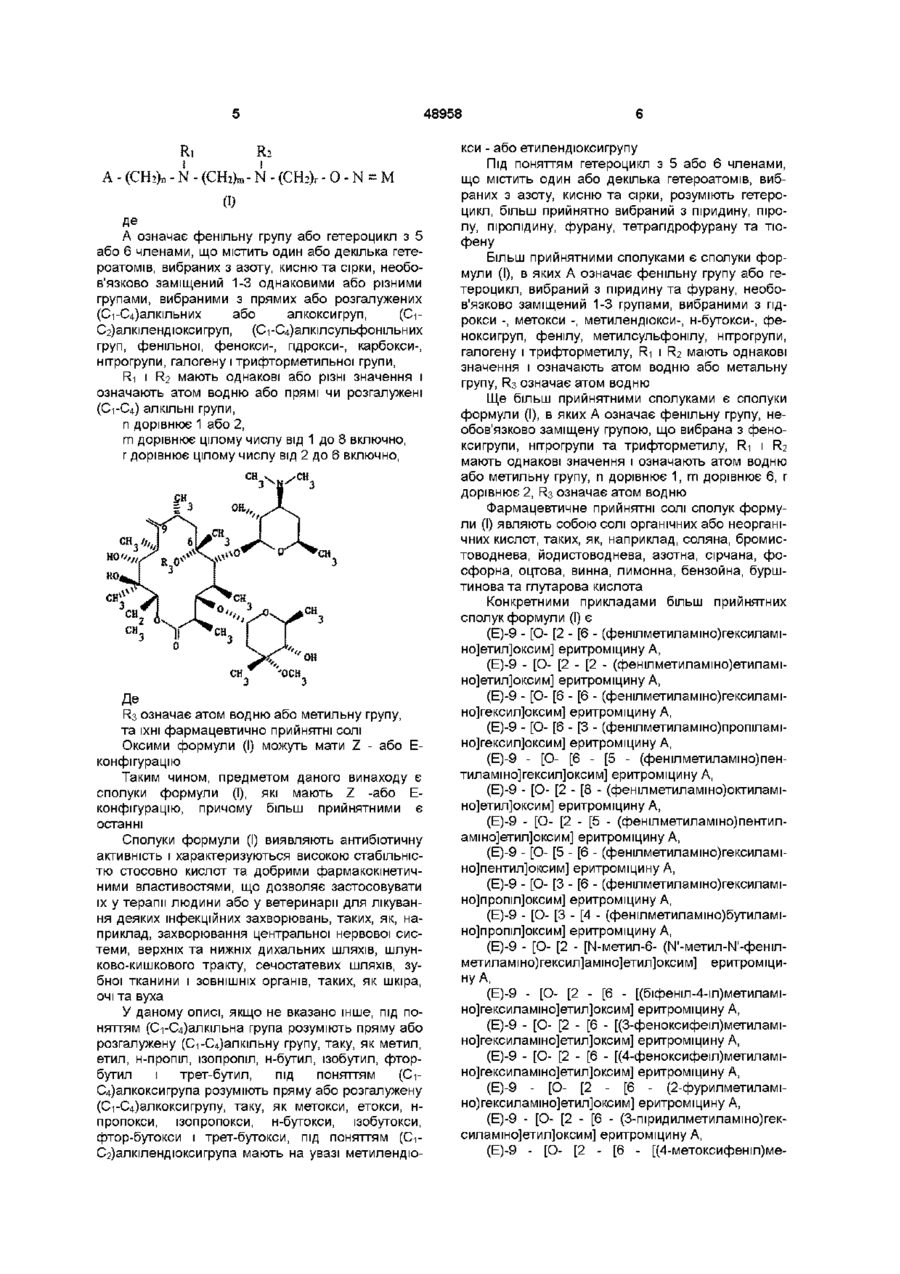
1. 9-О-оксимові похідні еритроміцину А формули
, (І)
де
А означає фенільну групу або гетероцикл з 5 чи 6 членами, що містить один або декілька гетероатомів, вибраних з азоту, кисню і сірки, необов'язково заміщений 1-3 однаковими або різними групами, вибраними з прямих або розгалужених (С1-С4)алкільних або алкоксигруп, (С1-С2)алкілендіоксигруп, (С1-С4)алкілсульфонільних груп, фенільної, фенокси -, гідрокси -, карбокси -, нітрогрупи, галогену і трифторметильної групи;
R1 і R2 мають однакові або різні значення і означають атом водню або пряму чи розгалужену (С1-С4)алкільну групу;
n дорівнює 1 або 2;
m дорівнює цілому числу від 1 до 8 включно;
r дорівнює цілому числу від 2 до 6 включно;
М означає групу формули
,
де
R3 означає атом водню або метильну групу;
та їх фармацевтично прийнятні солі.
2. Сполука за п. 1, яка відрізняється тим, що має Е-конфігурацію.
3. Сполука за п. 1, яка відрізняється тим, що А означає фенільну групу або гетероцикл, вибраний з піридину і фурану, необов'язково заміщений 1-3 групами, вибраними з гідрокси-, метокси-, метилендіокси-, н-бутокси-, фенокси-, фенільної, метилсульфонільної, нітрогрупи, галогену і трифторметильної групи;
R1 і R2 мають однакові або різні значення і означають атом водню або метильну групу;
R3 означає атом водню.
4. Сполука за п. 1, яка відрізняється тим, що А означає фенільну групу, необов'язково заміщену групою, вибраною з фенокси, нітро і трифторметилу;
R1 і R2 мають однакові значення і означають атом водню або метильну групу;
n дорівнює 1;
m дорівнює 6;
r дорівнює 2;
R3 означає атом водню.
5. Фармацевтична композиція, яка відрізняється тим, що містить терапевтично ефективну кількість однієї або декількох сполук формули (І) у суміші з фармацевтично прийнятним носієм.
Текст
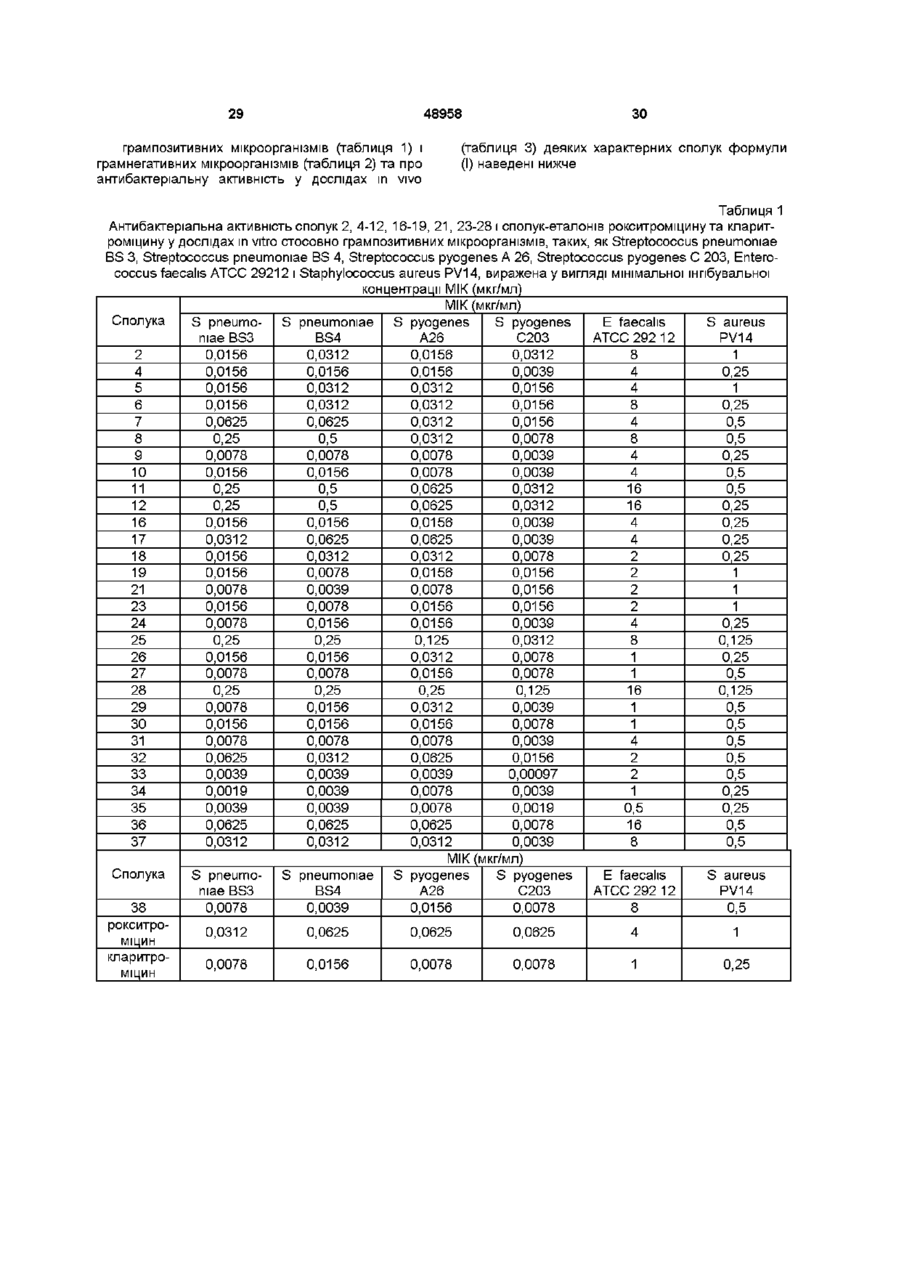
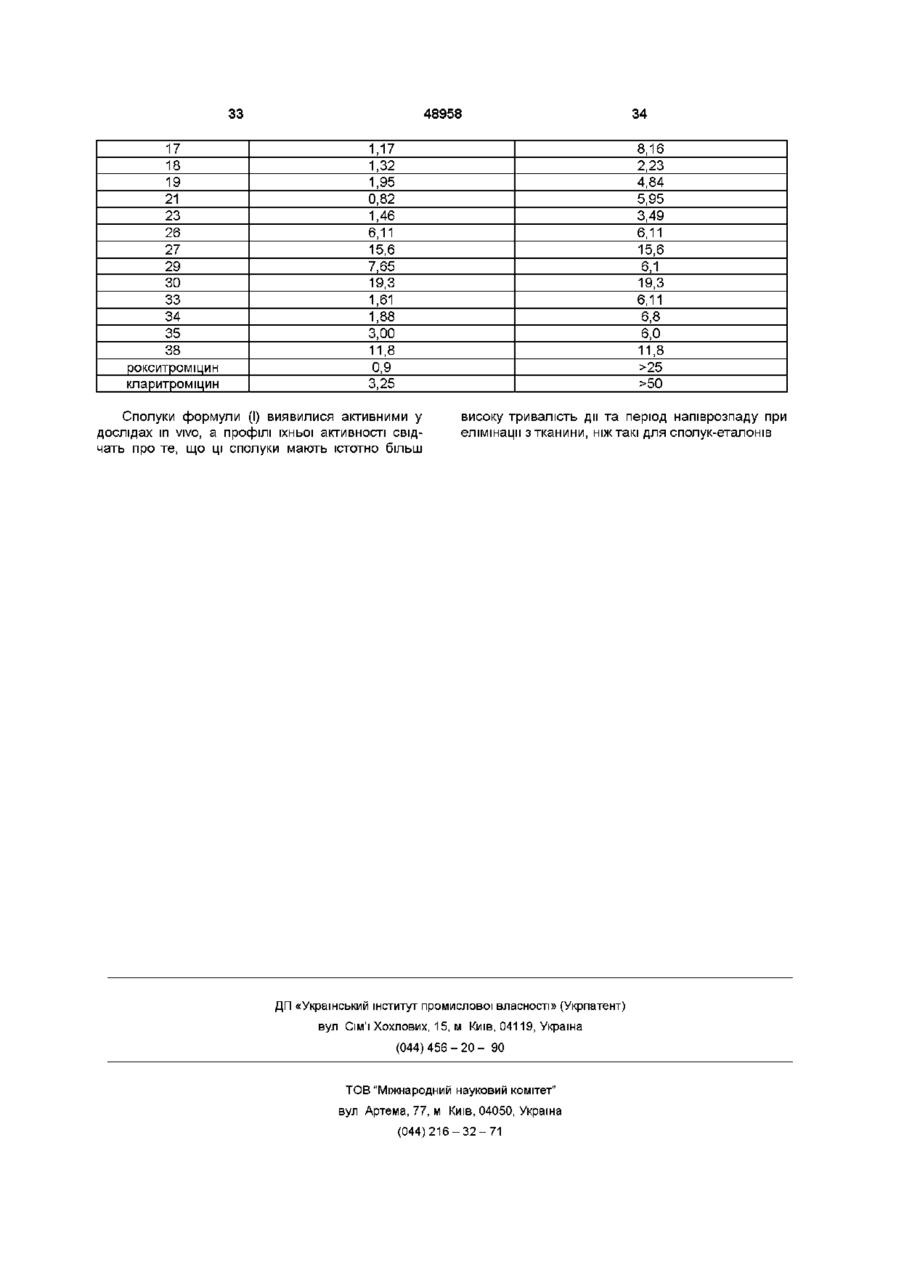
1 9-О-оксимові ПОХІДНІ еритроміцину А фор мули Де А означає фенільну групу або гетероцикл з 5 чи 6 членами, що містить один або декілька гетероатомів, вибраних з азоту, кисню і сірки, необов'язково заміщений 1-3 однаковими або різними групами, вибраними з прямих або розгалужених (Сі-С4)алкільних або алкоксигруп, ( d С2)алкілендюксигруп, (Сі-С4)алкілсульфонільних груп, фенільної, фенокси -, гідрокси -, карбокси -, нітрогрупи, галогену і трифторметильної групи, Ri і R2 мають однакові або різні значення і означають атом водню або пряму чи розгалужену ( d С4)алкільну групу, п дорівнює 1 або 2, m дорівнює цілому числу від 1 до 8 включно, г дорівнює цілому числу від 2 до 6 включно, М означає групу формули означає атом водню або метильну групу, та їх фармацевтично прийнятні солі 2 Сполука за п 1, яка відрізняється тим, що має Е-конфігурацію 3 Сполука за п 1, яка відрізняється тим, що А означає фенільну групу або гетероцикл, вибраний 3 піридину і фурану, необов'язково заміщений 1-3 групами, вибраними з гідрокси-, метокси-, метилендюкси-, н-бутокси-, фенокси-, фенільної, метилсульфонільної, нітрогрупи, галогену і трифторметильної групи, Ri і F 2 мають однакові або різні значення і озна? чають атом водню або метильну групу, F 3 означає атом водню ? 4 Сполука за п 1, яка відрізняється тим, що А означає фенільну групу, необов'язково заміщену групою, вибраною з фенокси, нітро і трифторметилу, Ri і R2 мають однакові значення і означають атом водню або метильну групу, п дорівнює 1, m дорівнює 6, г дорівнює 2, R3 означає атом водню 5 Фармацевтична композиція, яка відрізняється тим, що містить терапевтично ефективну КІЛЬКІСТЬ однієї або декількох сполук формули (І) у суміші з фармацевтично прийнятним носієм О 00 ю 00 48958 Даний винахід відноситься до похідних еритроміцину А, що мають антибіотичну аісгивність, придатних для лікування інфекційних захворювань, зокрема винахід відноситься до похідних 9[О-(амшоалкіл)оксиму] еритроміцину А, що має антибіотичну активність стосовно грампозитивних та грамнегативних мікроорганізмів Еритроміцин A [The Merck Index, XI вид , №3626] являє собою добре відомий макролід, що зустрічається в природних умовах, який має антибіотичну активність та наступну структуру СН. СН НО СН '-V0H О з оснз Окрім активності стосовно деяких мікроорганізмів, що не відносяться до бактерій, таких, як рикетсії та мікоплазми, еритроміцин А має антибактеріальну активність в основному стосовно грампозитивних мікроорганізмів, таких, як стрептококи, стафілококи і пневмококи, але він також виявляє ефективність стосовно деяких грамнегативних мікроорганізмів, таких, як, наприклад, Haemophilus mfluenzae, Neissena gonorrhoeae i Bordetella pertussis Окрім добре відомої активності стосовно вище зазначених прокаріотів за літературними даними, що нещодавно з'явилися, еритроміцин А та ІНШІ антибіотики з класу макролідів мають активність стосовно еукарютичних паразитів [Р A Lartey та ін , Advances in Pharmacology, 28, 307-343 (1994)] Стосовно еритроміцину А, так само як і стосовно інших антибактеріальних ЛІКІВ, у деяких штамів бактерій спостерігали явище СТІЙКОСТІ Зокрема це явище спостерігали при тривалому застосуванні еритроміцину А при лікуванні інфекцій, викликаних стафілококами [A Kucers і N McK Bennett, The use of antibiotics, A comprehensive Review with Clinical Emphasis, William Hememann Medical, IV вид , (1987)851-882] Зацікавленість антибіотиками з класу макролідів зумовлена можливістю їх застосування у КЛІНІЧНІЙ терапії та ветеринарії при лікуванні деяких інфекційних захворювань, таких, як, наприклад, інфекційні захворювання дихальних шляхів, шлунково-кишкового тракту, сечостатевих шляхів і ЗОВНІШНІХ органів, таких, як шкіра, очі і вуха Внаслідок своєї низької стабільності у кислому середовищі еритроміцин А необоротно перетворюється, наприклад, у шлунково-кишковому тракті при оральному уведенні, в похідну сполуку, позбавлену антибіотичної активності, що визначає пога ну біологічну доступність діючої речовини [Н А Kirst, Annual Reports in Medical Chemistry, 25,119128(1989)] Для подолання вище зазначених недоліків дослідження було спрямоване на сполуки, які, зберігаючи добрі антибіотичні властивості еритроміцину А, характеризувалися б більш високою стабільністю стосовно кислот та кращими фармакокшетичними властивостями, такими, як, наприклад, більш висока біологічна доступність при оральному уведенні, концентрація в крові, можливість проникати у тканини та період напіврозпаду Як приклад у даній галузі техніки можна навести карбамати та карбонати еритроміцину А або 9О-оксиму еритроміцину А, що описані в заявках на європейський патент 0216169 і 0284203 (обидві на ім'я Beecham Group PLC), а також сполуки, описані у європейській заявці 0033255 (фірма RousselUclaf) У європейській заявці 0033255 зокрема описані 9-О-оксимові ПОХІДНІ еритроміцину А формули R-A-O-N=Ery де Егу означає залишок еритроміцину А, в якому оксимова група (-N=Ery) заміщає карбонільну групу в положенні 9 (О=Егу), А означає пряму або розгалужену алкільну групу з 1-6 атомами вуглецю, R означає зокрема необов'язково заміщену алкоксигрупу з 1-6 атомами вуглецю або групу [N(Ri)R2], в якій Ri і R2 мають однакові або різні значення і означають атом водню або необов'язково заміщену алкільну групу з 1-6 атомами вуглецю Сполуки, описані в заявці на європейський патент 0033255, такі, як, наприклад, 9-[О-[(2метоксіетокси)метил]оксим] еритроміцину А, відомий під міжнародною незапатентованою назвою рокситроміцин [The Merck Index, XI вид , №8253], 9-[О-[(2-диметиламшо)етил]оксим] еритроміцину А та 9-[О-[(2-діетиламшо)етил]оксим] еритроміцину А, мають спектр активності in vitro, порівнянний з таким еритроміцину А, але мають більш високу стабільність стосовно кислот та кращі фармакокінетичні властивості Зазначені сполуки, отже, виявляють антибіотичну активність стосовно грампозитивних мікроорганізмів, таких, як стафілококи, стрептококи та стосовно деяких грамнегативних мікроорганізмів, таких, як, наприклад, Haemophilus mfluenzae і Haemophilus pertussis Згідно З даним винаходом були виявлені сполуки, що є 9-О-оксимовими похідними еритроміцину А, зокрема сполуки, які являють собою ПОХІДНІ 9-[О-(амшоалкіл)оксиму] еритроміцину А, що частково підпадають під обсяг, але не наведені як приклад у європейській заявці 0033255, які мають більш широкий спектр антибактеріальної активності стосовно грампозитивних мікроорганізмів, передусім стосовно грамнегативних мікроорганізмів, та поліпшені фармакокінетичні властивості, такі, як, наприклад, більша тривалість дії і більший період напіврозпаду при елімінації у тканинах порівняно зі сполуками, описаними у вищезазначеній європейській заявці Таким чином, предметом даного винаходу є сполуки формули 48958 Ri R2 A - (СШ)п - N - (СШ)т- N - (C3Hb)r - 0 - N - M fl) Де А означає фенільну групу або гетероцикл з 5 або 6 членами, що містить один або декілька гетероатомів, вибраних з азоту, кисню та сірки, необов'язково заміщений 1-3 однаковими або різними групами, вибраними з прямих або розгалужених (Сі-С4)алкільних або алкоксигруп, (dС2)алкілендюксигруп, (Сі-С4)алкілсульфонільних груп, фенільної, фенокси-, гідрокси-, карбокси-, нітрогрупи, галогену і трифторметильної групи, Ri і R2 мають однакові або різні значення і означають атом водню або прямі чи розгалужені (С1-С4) алкільні групи, п дорівнює 1 або 2, m дорівнює цілому числу від 1 до 8 включно, г дорівнює цілому числу від 2 до 6 включно, он означає атом водню або метильну групу, та їхні фармацевтично прийнятні солі Оксими формули (І) можуть мати Z - або Еконфігурацію Таким чином, предметом даного винаходу є сполуки формули (І), які мають Z -або Еконфігурацію, причому більш прийнятними є останні Сполуки формули (І) виявляють антибіотичну активність і характеризуються високою стабільністю стосовно кислот та добрими фармакокшетичними властивостями, що дозволяє застосовувати їх у терапії людини або у ветеринарії для лікування деяких інфекційних захворювань, таких, як, наприклад, захворювання центральної нервової системи, верхніх та нижніх дихальних шляхів, шлунково-кишкового тракту, сечостатевих шляхів, зубної тканини і ЗОВНІШНІХ органів, таких, як шкіра, очі та вуха У даному описі, якщо не вказано інше, під поняттям (Сі-С4)алкільна група розуміють пряму або розгалужену (Сі-С4)алкільну групу, таку, як метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, фторбутил і трет-бутил, під поняттям (dС4)алкоксигрупа розуміють пряму або розгалужену (Сі-С4)алкоксигрупу, таку, як метокси, етокси, нпропокси, ізопропокси, н-бутокси, ізобутокси, фтор-бутокси і трет-бутокси, під поняттям ( d С2)алкілендюксигрупа мають на увазі метилендю кси - або етилендюксигрупу Під ПОНЯТТЯМ гетероцикл з 5 або 6 членами, що містить один або декілька гетероатомів, вибраних з азоту, кисню та сірки, розуміють гетероцикл, більш прийнятно вибраний з піридину, піролу, піролідину, фурану, тетрапдрофурану та тюфену Більш прийнятними сполуками є сполуки формули (І), в яких А означає фенільну групу або гетероцикл, вибраний з піридину та фурану, необов'язково заміщений 1-3 групами, вибраними з гідрокси -, метокси -, метилендюкси-, н-бутокси-, феноксигруп, фенілу, метилсульфонілу, нітрогрупи, галогену і трифторметилу, Ri і R2 мають однакові значення і означають атом водню або метальну групу, R3 означає атом водню Ще більш прийнятними сполуками є сполуки формули (І), в яких А означає фенільну групу, необов'язково заміщену групою, що вибрана з феноксигрупи, нітрогрупи та трифторметилу, Ri і R2 мають однакові значення і означають атом водню або метильну групу, п дорівнює 1, m дорівнює 6, г дорівнює 2, R3 означає атом водню Фармацевтичне прийнятні солі сполук формули (І) являють собою солі органічних або неорганічних кислот, таких, як, наприклад, соляна, бромистоводнева, йодистоводнева, азотна, сірчана, фосфорна, оцтова, винна, лимонна, бензойна, бурштинова та глутарова кислота Конкретними прикладами більш прийнятних сполук формули (І) є (Е)-9 - [О- [2 - [6 - (фенілметиламшо)гексиламіно]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [2 - (фенілметиламшо)етиламіно]етил]оксим] еритроміцину А, (Е)-9 - [О- [6 - [6 - (фенілметиламшо)гексиламіно]гексил]оксим] еритроміцину А, (Е)-9 - [О- [6 - [3 - (фенілметиламшо)пропіламіно]гексил]оксим] еритроміцину А, (Е)-9 - [О- [6 - [5 - (фенілметиламшо)пентиламшо]гексил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [8 - (фенілметиламшо)октиламіно]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [5 - (фенілметиламшо)пентиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [5 - [6 - (фенілметиламшо)гексиламіно]пентил]оксим] еритроміцину А, (Е)-9 - [О- [3 - [6 - (фенілметиламшо)гексиламіно]пропіл]оксим] еритроміцину А, (Е)-9 - [О- [3 - [4 - (фенілметиламшо)бутиламіно]пропіл]оксим] еритроміцину А, (Е)-9 - [О- [2 - [N-метил-б- (N'-метил-М'-фенілметиламшо)гексил]амшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(біфеніл-4-іл)метиламіно]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(З-феноксифеіл)метиламіно]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(4-феноксифеіл)метиламіно]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - (2-фурилметиламіно)гексиламіно]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - (З-піридилметиламшо)гексиламіно]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(4-метоксифеніл)ме 8 48958 тиламіно]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(4-н-бутоксифеніл)метиламшо]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(3,4-метилендюксифеніл)метиламшо]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(4-метилсульфонілфеніл)мєтиламшо]гексиламіно]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(4-фторфеніл)метиламіно]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(2-трифторметилфеніл)метиламшо]гексиламіно]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(3-трифторметилфеніл)метиламшо]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(4-трифторметилфеніл)метиламшо]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(2-пдроксифеніл)метиламіно]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(З-пдроксифеніл)метиламшо]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(4-пдроксифеніл)метиламшо]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(3 З-дихлор-2-пдроксифеніл)мєтиламіно]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(2-нітрофеніл)метиламіно]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(З-нітрофеніл)метиламіно]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(4-нітрофеніл)метиламіно]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 -[О- [2 - [6 - [(4-пдрокси-З-нітрофеніл)метиламшо]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [6 - [(З-пдрокси-4-нітрофеніл)метиламшо]гексиламшо]етил]оксим] еритроміцину А, (Е)-9 - [О- [2 - [М-метил-6-[І\Г-метил-М'-(4-трифторметилфеніл)метиламшо] гексиламіно]етил]оксим] еритроміцину А Одержання сполук формули (І), що є предметом даного винаходу, може бути здійснене ВІДПОВІДНО до нижче описаного способу синтезу Спосіб включає, по-перше, реакцію конденсації між ВІДПОВІДНОЮ кислотою формули R. [ HN - {СШ>ы - СООН (II) де Ri та m мають вищевказані значення, з хлористим ацилом формули А - (СН2)ы - СОСІ (III) де А і п мають вищевказані значення Реакцію конденсації здійснюють ВІДПОВІДНО ДО стандартних методів в інертному розчиннику та за присутності основи, такої, як, наприклад, гідроксид лужного металу, з одержанням сполук формули Ri І А - (СШ)п-і - CON- (CH2)m-i - СООН (IV) де А, R-і, п і m мають вищевказані значення Одержані таким чином N-ациламшокислоти формули (IV) далі піддають конденсації ВІДПОВІДНО до стандартних методів з аміноефірами формули HN -(СН2)ы - C00R4 (V) де Ri і г мають вищевказані значення, a R4 означає метильну або етильну групу, з одержанням сполук формули Rs R2 ! І А -(СШ)п , - CON - (СЩт і - CON - (CHiJr-i - COOR4 (VI) де A,Ri,R2,R4,n,m і г мають вищевказані значення ВІДПОВІДНО ДО стандартних методів сполуки формули (VI) далі відновлюють, наприклад, за допомогою боропдриду натрію за присутності кислот, алюмопдриду ЛІТІЮ, диметилсульфідборану або шляхом каталітичного гідрування, до ВІДПОВІДНИХ аміноспиртів формули Ri ЇЬ І І А - № ) „ - CON - (CH2)m - CON - (СЩ Г - ОН (VII) де A,Ri,R2,n,m і г мають зазначені вище значення Аміноспирти формули (VII) потім перетворюють у ВІДПОВІДНІ сульфонільні ПОХІДНІ формули (VIII), наприклад, за допомогою метансульфонілхлориду або пара-толуолсульфоніл-хлориду, і далі конденсують з 9-О-оксимом еритроміцину А або з 9-О-оксимом 6-О-метил-еритроміцину А, причому обидві сполуки можуть бути подані формулою (IX), з одержанням сполук формули (І) Ri R2 І | (VID • A -(CHj), - N - 25 >50 Сполуки формули (І) виявилися активними у дослідах in vivo, а профілі їхньої активності свідчать про те, що ці сполуки мають істотно більш високу тривалість дії та період напіврозпаду при елімінації з тканини, ніж такі для сполук-еталонів ДП «Український інститут промислової власності» (Укрпатент) вул Сім'ї Хохлових, 15, м Київ, 04119, Україна ( 0 4 4 ) 4 5 6 - 2 0 - 90 ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)216-32-71
ДивитисяДодаткова інформація
Назва патенту англійською9-0-oxime derivatives of erythromycine and pharmaceutical composition thereof
Назва патенту російською9-o-оксимовые производные эритромицина а и фармацевтическая композиция на их основе
МПК / Мітки
МПК: C07H 17/08, A61K 31/70, A61P 31/04, A61P 33/02, A61K 31/7048, A61K 31/7042
Мітки: похідні, 9-o-оксимові, композиція, фармацевтична, основі, еритроміцину
Код посилання
<a href="https://ua.patents.su/17-48958-9-o-oksimovi-pokhidni-eritromicinu-a-ta-farmacevtichna-kompoziciya-na-kh-osnovi.html" target="_blank" rel="follow" title="База патентів України">9-o-оксимові похідні еритроміцину а та фармацевтична композиція на їх основі</a>