Екструдати з голчатими активними речовинами
Номер патенту: 105648
Опубліковано: 10.06.2014
Автори: Кляйнебудде Петер, Вітцлеб Ріке, Каніканті Венката-Рангарао, Хаманн Ханс-Юрген
Формула / Реферат
1. Екструдат, що містить принаймні одну фармацевтично активну речовину в формі голок, який відрізняються тим, що співвідношення між розміром частинок голчатої фармацевтично активної речовини та діаметром штрангу становить принаймні 1:25.
2. Екструдат за п. 1, у якого діаметр штрангу становить 0,5 мм або менше.
3. Екструдат за будь-яким із попередніх пунктів, який містить ліпідну основу як допоміжну речовину.
4. Екструдат за будь-яким із попередніх пунктів, який містить гліцериновий естер із С12-С24-жирними кислотами як ліпідну основу.
5. Екструдат за будь-яким із попередніх пунктів, який містить діестер гліцерину як ліпідну основу.
6. Екструдат за пунктом 5, який містить дибегенат гліцерину як ліпідну основу.
7. Екструдат за будь-яким із пунктів 1-4, який містить триестер гліцерину як ліпідну основу.
8. Екструдат за пунктом 7, який містить триміристат гліцерину, трипальмітат гліцерину або тристеарат гліцерину як ліпідну основу.
9. Екструдат за пунктом 8, який містить тристеарат гліцерину як ліпідну основу.
10. Екструдат за будь-яким із попередніх пунктів, який містить антистатик, зокрема поліетиленгліколь.
11. Екструдат за будь-яким із попередніх пунктів, одержаний шляхом екструзії при температурі нижче нижньої границі діапазону плавлення вміщеної в ньому основи.
Текст
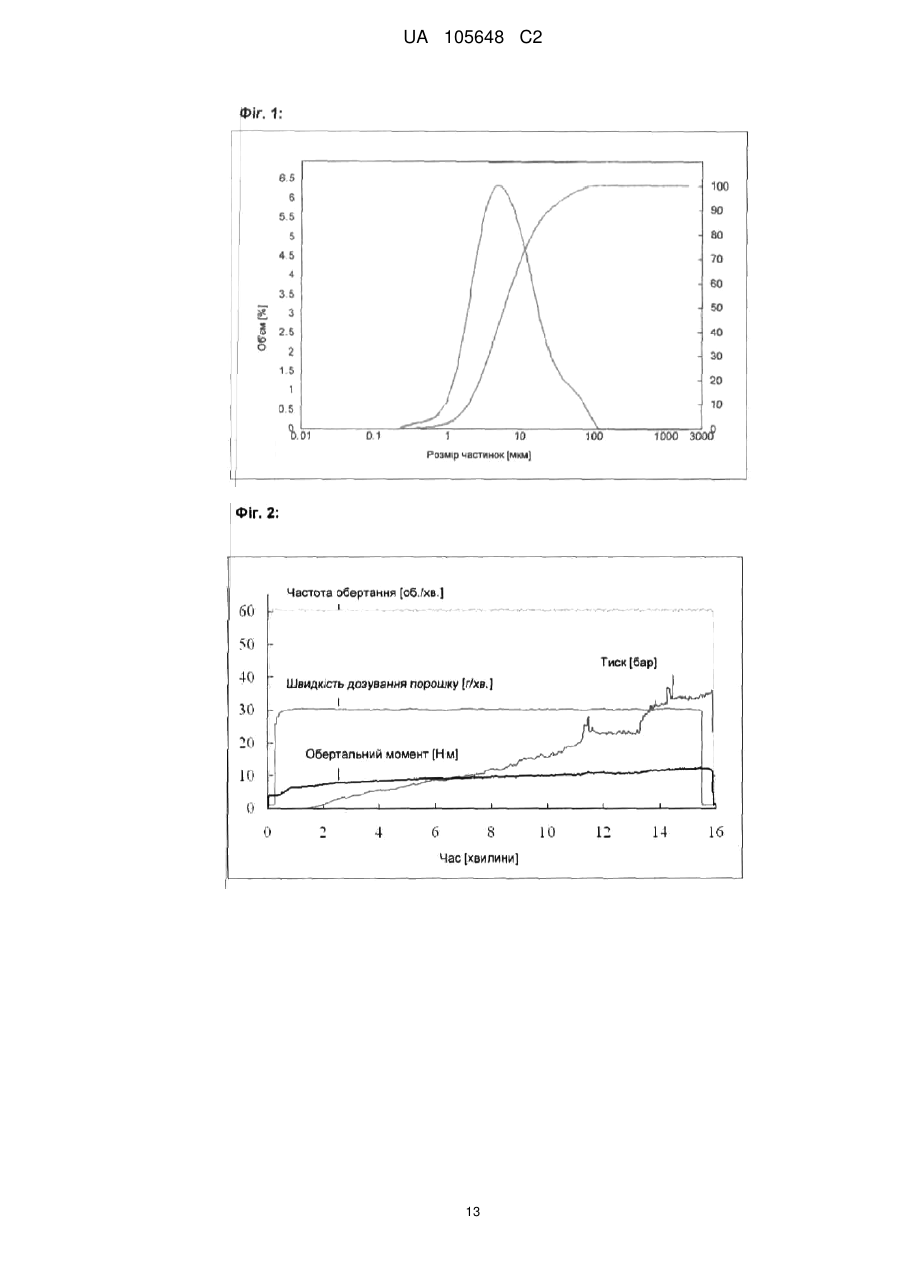
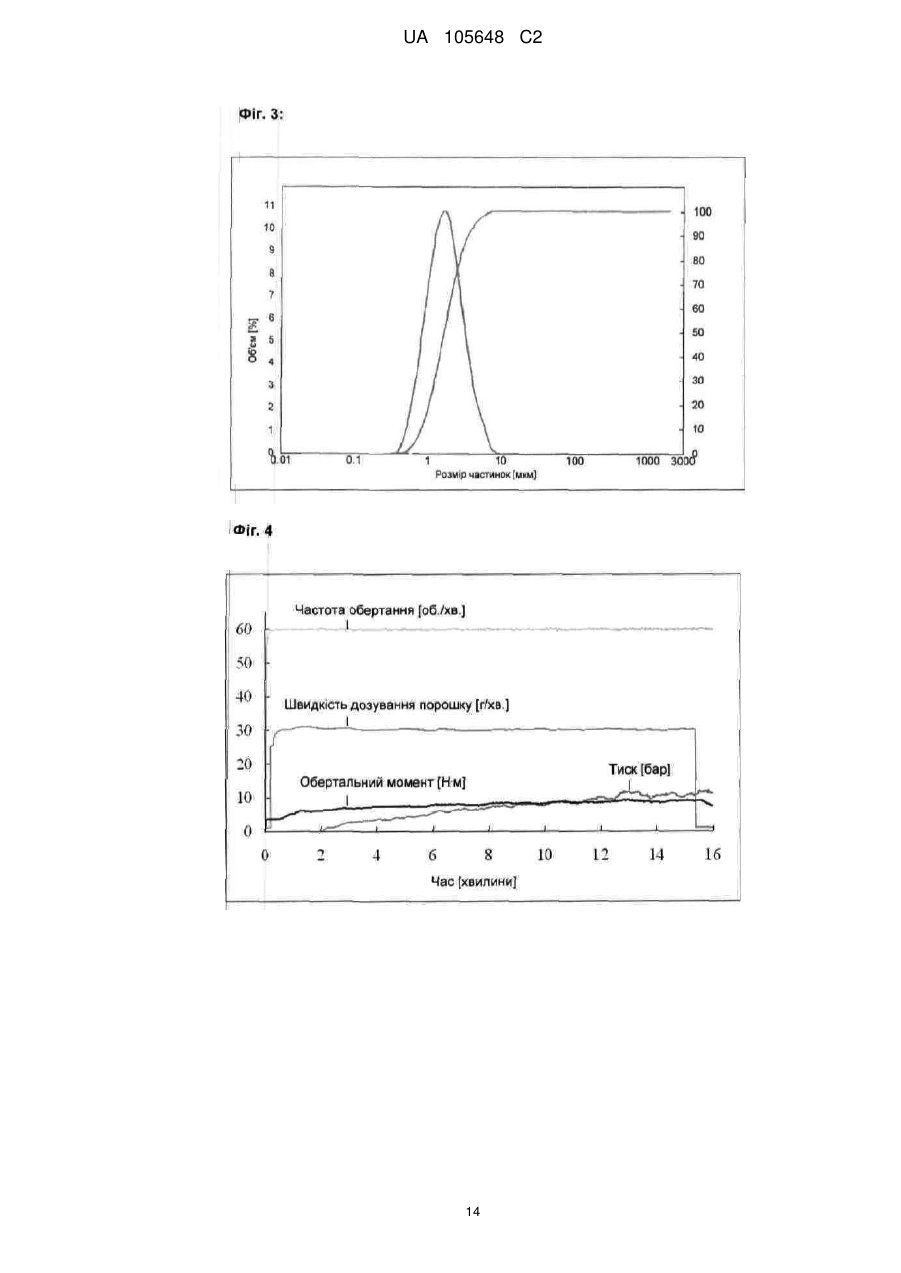
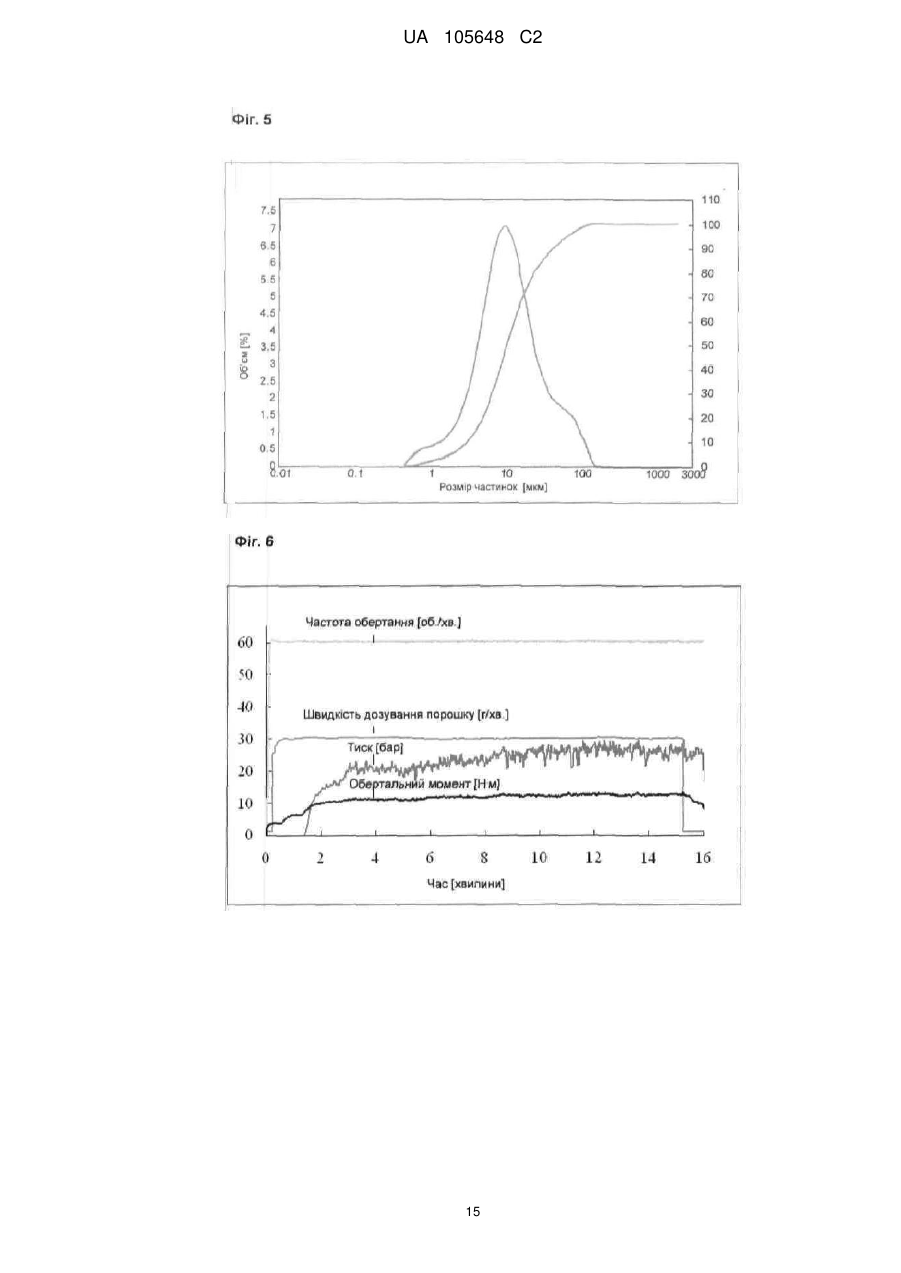
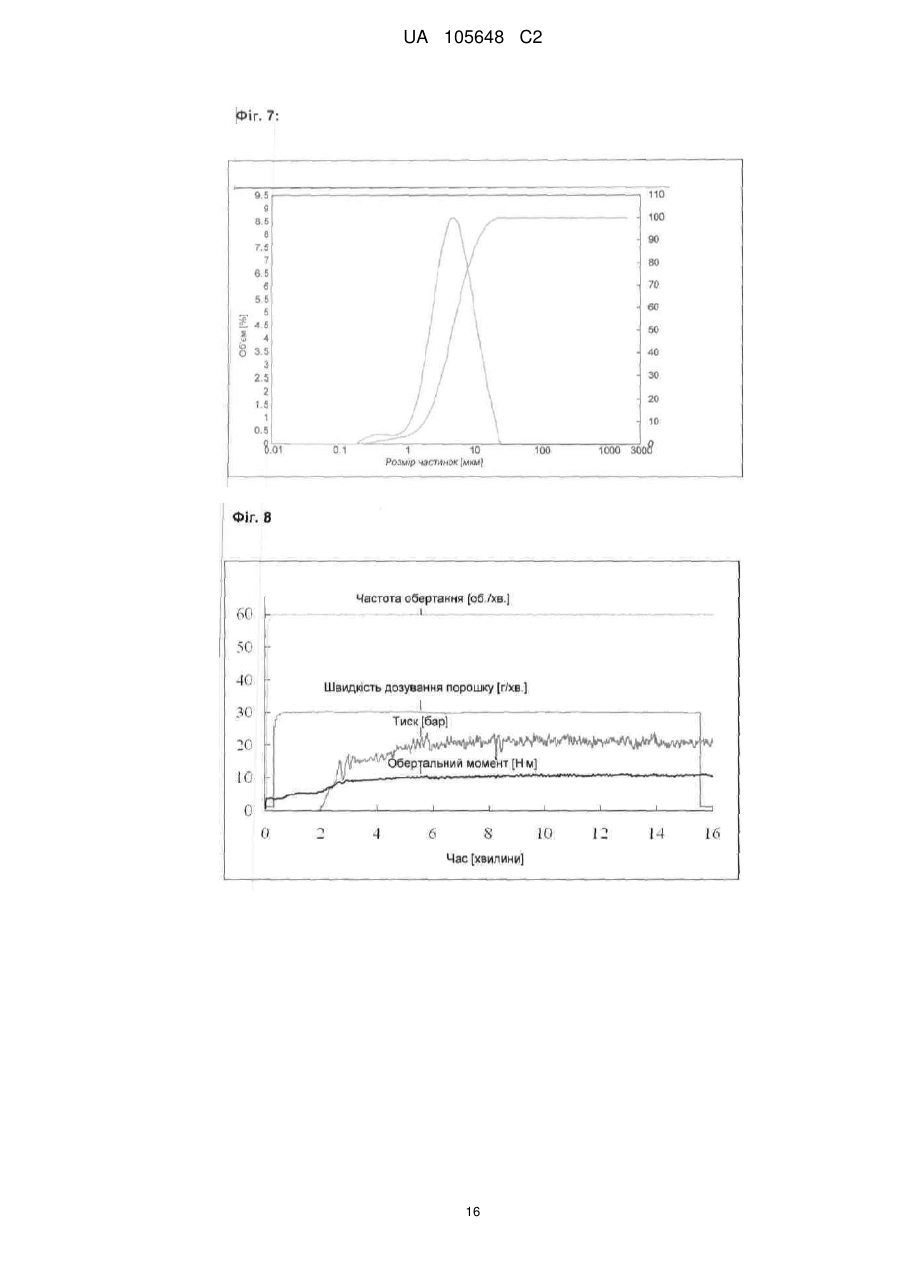
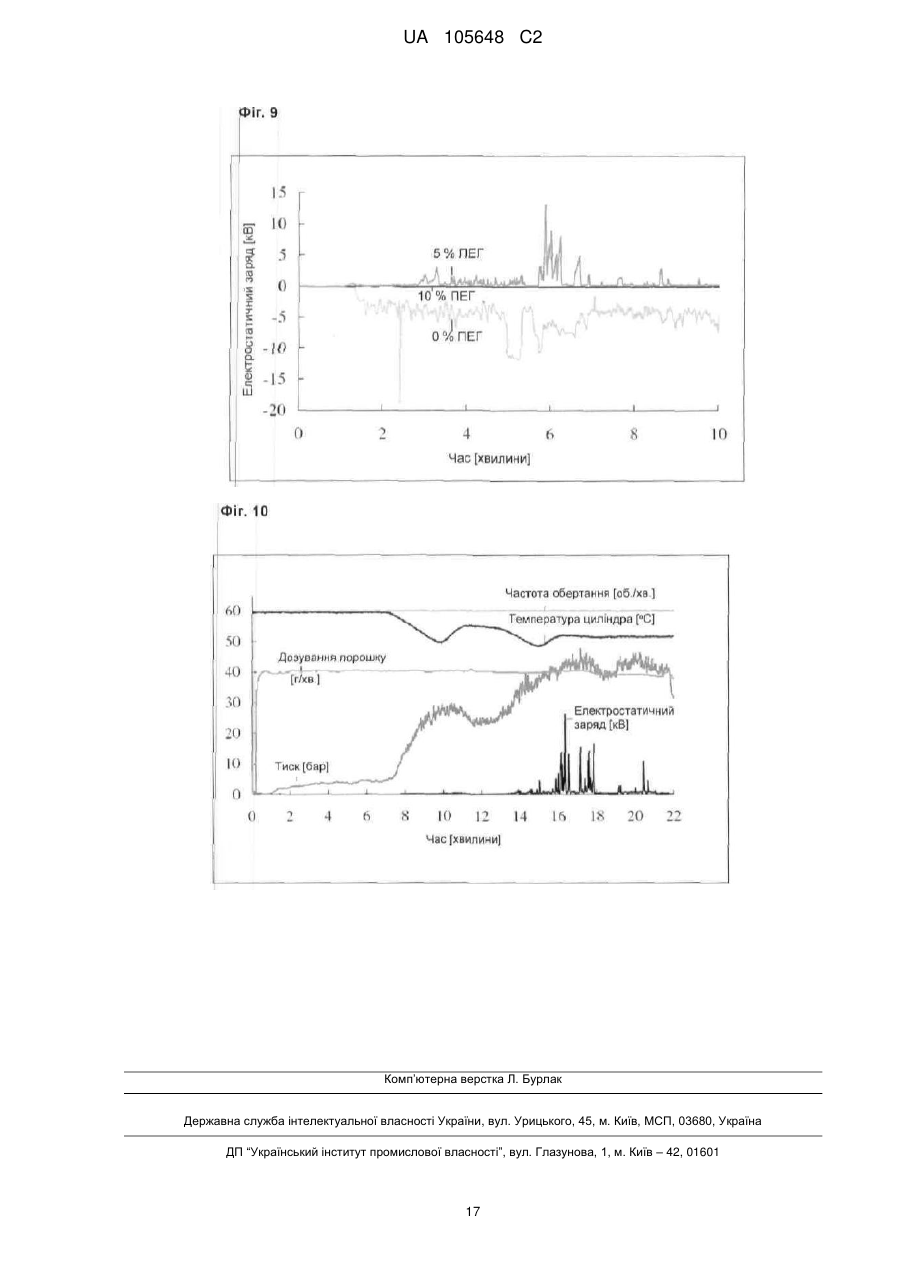
Реферат: Винахід стосується екструдатів, що містять принаймні одну фармацевтично активну речовину в формі голок, причому співвідношення між розміром частинок голчатої фармацевтично активної речовини та діаметром штрангу становить щонайменше 1:25, а також застосування цих екструдатів для одержання лікарських засобів. UA 105648 C2 (12) UA 105648 C2 UA 105648 C2 5 10 15 20 25 30 35 40 45 50 55 60 Винахід стосується екструдатів, що містять принаймні одну фармацевтично активну речовину в формі голок, причому співвідношення між розміром частинок голчатої фармацевтично активної речовини та діаметром штрангу становить щонайменше 1:15, а також застосування цих екструдатів для одержання лікарських препаратів. Маскування смаку гірких лікарських засобів має важливе значення для покращання комплаєнтності пацієнтів щодо лікарських засобів, не в останню чергу щодо педіатричних композицій, а також ветеринарних лікарських препаратів. Найпростішим способом маскування смаку є додавання ароматичних речовин, що може бути проблематичним, якщо необхідно приховати смак гірких речовин, а також речовин, що дуже добре розчиняються у воді (Bienz, 1996). Маскування смаку шляхом виготовлення гранулятів із активної речовини з гідрофобним носієм також описане в літературі (Kalbe та Hopkins, 1998). Інша можливість полягає у нанесенні покриття на лікарські форми. Для цього застосовують, наприклад, такі матеріали, як Євдрагіт Е (Eudragit E) (Cerea et al., 2004; Lovrecich et al., 1996; Ohta та Buckton, 2004; Petereit та Weisbrod, 1999), шелак (Pearnchob et al., 2003b; Pearnchob et al., 2003a) або похідні целюлози (Al-Omran et al., 2002; Li et al., 2002; Shirai et al., 1993). Недолік Євдрагіту Е полягає в тому, що маскування смаку ґрунтується на іонній взаємодії між катіонним допоміжним матеріалом та аніонними активними речовинами. Недоліком шелаку є те, що він є природним полімером, склад якого може варіювати. Навіть якщо не зважати на це, нанесення покриттів на лікарські форми є додатковою технологічною операцією, що потребує додаткової витрати коштів і часу. Крім цього, описані тверді дисперсії хінолон- або нафтиридонкарбонових кислот у нерозчинній шелаковій матриці (Cabrera, 2002). Іонообмінні смоли та комплекси включення також застосовують для маскування смаку. Можливість застосування іонообмінних смол обмежена внаслідок того, що лікарський засіб повинен мати іонні властивості (Chun та Choi, 2004; Lu et al., 1991; Prompruk et al., 2005). Комплекси включення можуть бути обтяжені лише невеликою кількістю лікарського препарату (Sohi et al., 2004). Ліпідні основи також можуть бути використані для маскування смаку. Описані монолітні лікарські форми на основі отвердженого жиру, які додатково містять лецитин і солодкі речовини (Suzuki et al., 2003; Suzuki et al., 2004). Їх недоліком є те, що ліпіди під час виготовлення мають бути повністю розплавлені, що може призвести до нестабільності фізичних характеристик. Окрім цього отверджений жир, дистеарат гліцеролу і стеаринову кислоту застосовують як ліпофільні зв'язувальні речовини у способі холодної екструзії, причому і в цьому випадку необхідним було використовувати Євдрагіт Е як покриття, щоб досягти маскування смаку (Breitkreutz et al., 2003). Екструзія жирів при температурі нижче їх температури плавлення для виготовлення лікарських форм також описана, проте не для маскування смаку (Reitz та Kleinebudde, 2007; Windbergs et al., 2008). Маскуючі смак композиції, що містять інгібітори гірази типу хінолону, одержували шляхом змішування активної речовини з вищими жирними кислотами та в разі необхідності іншими добавками, нагрівання, охолодження і наступного гранулювання чи подрібнення на порошок (Ahrens et al., 1998). Виготовляли також таблетки на основі восків (Adeyeye та Price, 1991; Adeyeye та Price, 1994; Zhou et al., 1996; Zhou et al., 1998). Дослідження показали, що швидкість вивільнення активних речовин залежить від температури плавлення використаного воску та його концентрації в таблетці. Чим вище були температура плавлення і вміст воску, тим повільніше відбувалося вивільнення. Іншу можливість маскування смаку описали Kim та Choi (2004), які виготовляли ядро з какао-масла або отвердженого жиру та активної речовини і наносили на нього покриття з альгінату натрію або карагеніну. Проте, жир при цьому повністю розплавляли, що негативно впливало на стабільність; крім цього, нанесення покриття було додатковою технологічною операцією. ® Описаний також Compritol 888 ATO як компонент, що утворює матрицю. Таблетки ® виготовляли з розплавленого Compritol , активної речовини та полісахаридного покриття (Mirghani et al., 2000). В іншому дослідженні матричні таблетки виготовляли шляхом пресування або із суміші порошків, або з подрібненої на порошок твердої дисперсії. Маскування смаку у таблетках із подрібненої на порошок твердої дисперсії було кращим; проте, для їх виготовлення ® Compritol доводилося повністю розплавляти (Li et al., 2006). Barthelemy використовував ® Compritol як покриття таблеток і гранул теофіліну. І в цьому випадку жир повністю розплавляли (Barthelemy et al., 1999). Застосування фосфоліпідів є іншою можливістю маскування гіркого смаку, але не інших смакових відтінків (Katsuragi et al., 1997; Takagi et al., 2001). Крім цього, додавання фосфоліпідів впливає на кристалічність ліпідів, що може призвести до нестабільності (Schubert, 2005). Маскування смаку порошків може бути досягнуте шляхом нашарування дрібних частинок 1 UA 105648 C2 5 10 15 20 25 30 35 40 45 50 55 60 допоміжної речовини на більші частинки активної речовини (Barra et al., 1999). Описані також корми для тварин, у які активні речовини були введені в процесі екструзії (Huber et al., 2003). Petereit et al. шляхом екструзії розплаву лужного лікарського препарату і метакрилового полімеру одержали екструдати із замаскованим смаком, які потім подрібнювали на гранулят чи порошок (Petereit et al., 2003), а також виготовляли здатну до швидкого розкладу лікарську форму шляхом змішування обох компонентів із середнє- чи довголанцюговою жирною кислотою в розплаві. Після отвердження продукт перемелювали і вводили у водорозчинну матрицю (Petereit et al., 2004). Досліджували лікарські засоби із контрольованим вивільненням, які містили активну речовину в ліпідній матриці з естеру бегенової кислоти і гідрофобного розріджувача (Nabil et al., 1998). Thombre описує композицію для декоративних тварин у формі мультичастинок із добавкою, маскуючою смак (Thombre, 2004). У аналогічній заявці "Екструдати із покращаним маскуванням смаку" (заявка на патент Німеччини № 102007026550.8, див. також паралельну PCT-заявку № PCT/EP2008/004218) описані придатні до фармацевтичного застосування екструдати з діаметром штрангу 0,5 мм і менше. Ці екструдати придатні для маскування смаку лікарських препаратів. Проте, при екструзії сумішей, що містять активні речовини у формі голок, виникають неочікувані проблеми: якщо кристали застосовуваних лікарських речовин мають голчату форму, здійснення стабільних і відтворюваних процесів одержання препаратів виявляється неможливим, навіть якщо довжина голок буде явно меншою, ніж діаметр штрангу. В принципі, труднощі при обробці голчатих лікарських речовин відомі з інших технологій одержання препаратів. Різні роботи свідчать про те, що властивості порошків і виготовлених із них таблеток залежать від форми частинок використаних матеріалів (Alderborn та Nyström, 1982; Wong та Pilpel, 1990). Наприклад, парацетамол, кристали якого мають голчатий габітус, дуже важко спресовувати в таблетки порівняно з речовинами з іншою формою кристалів, наслідком чого є розкришування таблеток і незадовільна плинність порошку (Wang & Zhang, 1995). Порошок ібупрофену, кристали якого мали голчату форму, також проявляв дуже низьку плинність, погані когезивні та адгезивні властивості, ущільнення і таблетування потребувало застосування великої кількості енергії, a одержані в результаті таблетки були механічно нестабільними. Шляхом агломерації або перекристалізації для одержання ізометричних форм кристалів параметри таблетування ібупрофену можуть бути помітно покращані (Jbilou et al., 1999; Rasenack та Müller, 2002). Проте, щодо процесу екструзії з технології обробки скла відомо, голчаті частинки розташовуються в напрямку екструзії. У цьому випадку бажано забезпечити їх вирівнювання для досягнення анізотропних властивостей виготовлюваного скла (Moisescu et al., 1999). Порівняно з ізометричними частинками в'язкість розм'якшеної скляної маси в процесі екструзії розплаву була явно вищою, якщо маса містила голчаті частинки (Yue et al., 1999). Фахівці могли б не очікувати проблем у тому випадку, якщо розмір частинок був би у кілька разів (наприклад у 5) менше діаметра штрангу, зокрема завдяки можливості припущення, що частинки сприятливо для екструзії розташовуватимуться паралельно. Проте, при екструзії сумішей, які містили голчаті активні речовини, неочікувано виникли проблеми; в рамках технологічного процесу вони, зокрема, полягали в скупченні матеріалу перед фільєрною пластиною, що призводило до блокування отворів фільєр і в результаті зростання тиску перед фільєрною пластиною екструдера. До того ж плинність порошкових сумішей була настільки низькою, що майже неможливо було підтримувати постійну швидкість дозування при високій технологічній швидкості. Для того щоб спосіб екструзії для голчатих активних речовин задовольняв наведеним вище вимогам, випробували різні варіанти: внесення змін у рецептуру, наприклад варіювання ліпідної основи, додавання інших допоміжних речовин або дослідження різних можливостей введення активних речовин не дали достатньо задовільних результатів. Окрім цього, можуть бути застосовані фільєрні пластини зі ступінчастим розширенням підвідного фільєрного каналу в напрямку технологічного процесу, що, проте, в даному випадку залежно від конкретних обставин може призводити до погіршання рівномірності технологічного процесу. Здійснення екструзії крізь фільєрні пластини з особливо гладкими поверхнями отворів також суттєво не поліпшило ситуацію. Як інші варіанти апаратурного оснащення можна застосовувати шнеки різних конфігурацій, що також не дозволяє покращити результати процесу. Можна також варіювати технологічні параметри: температуру, швидкість дозування та частоту обертів шнека. Температура екструзії може становити від значення на 20 °C нижче діапазону плавлення застосованого ліпіду до значень в межах діапазону плавлення. При надто низькій температурі фільєри негайно забиваються, і тиск дуже швидко зростає; при надто високій температурі ліпіди розплавляються повністю і виходять із фільєр у вигляді м'якої пасти. 2 UA 105648 C2 5 10 15 20 25 30 35 40 45 50 55 60 Проте, було виявлено, що при більших діаметрах фільєр може бути досягнуто певне покращання результатів. Оскільки жодна з інших змін не дозволяє вирішальним чином покращити технологічний процес, порошок активної речовини перемелюють (наприклад у повітряному струминному млині); в результаті перемелювання голчаті кристалічні структури подрібнюються. При достатньо малому розмірі частинок виготовлення екструдатів може бути безпроблемним. При достатньо тонко перемеленій активній речовині процес екструзії протікає, як правило, рівномірно і може бути відтворений під постійним тиском, навіть при вищому навантаженні лікарської речовини (наприклад 50 % або навіть до 80 %) та діаметрі фільєр, наприклад, 0,3 мм або навіть лише 0,2 мм. Тому винахід стосується: - Ескструдатів, що містять принаймні одну фармацевтично активну речовину в формі голок, які відрізняються тим, що співвідношення між розміром частинок голкоподібної фармацевтично активної речовини та діаметром штрангу становить щонайменше 1:15. - Застосування вищенаведених екструдатів для одержання лікарських засобів. Співвідношення між розміром частинок голчатої фармацевтично активної речовини та діаметром штрангу у звичайному випадку становить щонайменше 1:15, переважно щонайменше 1:20, особливо переважно щонайменше 1:25, цілком переважно 1:50, насамперед щонайменше 1:100. Розмір частинок у цьому контексті в разі сумнівів слід розуміти як визначене шляхом лазерної дифрактометрії значення d(0,9). В смислі винаходу значення d(0,9) означає віднесений до об'єму гранулометричний склад, при якому розмір (діаметр) 90 % всіх частинок є меншим або дорівнює цьому значенню (іноді для цього застосовують також значення (90) або d(v,90), причому останнє для пояснення, що йдеться про віднесений до об'єму гранулометричний склад). Відповідно слід розуміти значення (0,5), d(0,1) тощо. Наведені тут розміри частинок були визначені методом лазерної дифракційної спектрометрії за допомогою лазерного дифрактометра Mastersizer 2000 (блок диспергатора Hydro 2000G) виробництва компанії Malvern із оцінкою методом дифракції Франгофера, оскільки коефіцієнти заломлення частинок активної речовини не відомі. Для цього відповідну кількість пробного розчину, перемішуючи, піддавали попередньому диспергуванню із використанням 2-3 мл диспергуючого засобу (наприклад 0,1 %-ний водного розчину сульфосукцинату діоктилнатрію для празиквантелу або етанолу для месалазину). Потім дисперсію, перемішуючи (300 об./хв.) та перекачуючи насосом(900 об./хв.) подавали у блок диспергатора дифрактометра. За результатами оцінки із застосуванням відповідного програмного забезпечення одержали значення розміру частинок d(0,9) (чи d(0,5) тощо). Частинки активної речовини, які надто добре розчиняються у широко застосовуваних розчинниках (наприклад кофеїн), піддавали диспергуванню сухим способом за допомогою відповідного блока (наприклад Scirocco 2000 dry powder feeder) із застосуванням повітряного потоку під тиском повітря 0,5 бар. Діаметр штрангу відповідних винаходові екструдатів становить максимум 0,5 мм, особливо переважно максимум 0,3 мм. У звичайному випадку можуть бути застосовані екструдати, починаючи з діаметра 0,1 мм, переважно починаючи з 0,2 мм. У екструдатів, форма яких відрізняється від циліндричної, максимальна довжина кромки або довжина більшої осі еліпса становить максимум 0,5 мм, переважно максимум 0,3 мм. Екструдати містять придатну для екструзії основу із матеріалу, який піддається термопластичній деформації, або суміші кількох матеріалів, які піддаються термопластичній деформації, а також, у разі необхідності, інші фармацевтично прийнятні допоміжні та додаткові речовини. Основа складається із матеріалів, які піддаються термопластичній деформації, таких як полімери, наприклад поліакрилатів або похідних целюлоз, ліпідів, наприклад ацилгліцеридів, поверхнево-активних речовин, наприклад гліцеролмоностеарату або стеарату натрію, макроголів, наприклад поліетиленгліколю 6000, цукрів чи цукрових спиртів, наприклад манітолу або ксилітолу. Переважно застосовують ліпідну основу. Придатними до застосування як ліпідні основи є, наприклад, жирові основи, зокрема гліцероловий естер; переважно застосовують естери із C12-C24-жирними кислотами. Із гліцеринових естерів застосовують діестери гліцерину, такі як, наприклад, дибегенат гліцерину; триестери гліцерину, такі як, наприклад, трилаурат гліцерину, триміристат гліцерину, трипальміат гліцерину або тристеарат гліцерину, суміші моно, -ді- та –триестерів гліцерину, такі як, наприклад, пальмітостеарат гліцерину. Можуть бути застосовані також тригліцериди на основі кокосової олії, пальмової олії та/або пальмоядрова ® олія (такі як, наприклад, комерційно доступні за торговим найменуванням Witocan отверджені жири). Можуть бути застосовані також моно- або дигліцериди лимонної та/або молочної 3 UA 105648 C2 5 10 15 20 25 30 35 40 45 50 55 60 кислоти. Крім цього, можуть бути застосовані воски, насамперед такі, що містять від 30 до 60 атомів вуглецю, такі як цетилпальмітат. ® ® Такі ліпіди комерційно доступні, наприклад, за торговим найменуванням Precirol , Compritol ® та Dynasan . Особливо переважним прикладом із ряду діестерів гліцерину є дибегенат гліцерину (наприклад Compritol® 888 ATO, який містить в основному дибегенат гліцерину, а також моно- і трибегенат гліцерину). Особливо переважними прикладами із ряду триестерів гліцерину є триміристат гліцерину (наприклад Dynasan® 114), трипальмітат гліцерину (наприклад Dynasan® 116) та тристеарат гліцерину (наприклад Dynasan® 118). Переважно застосовують порошкоподібні жирові основи. Багато ліпідів є поліморфними та при змінах температури і тиску залежно від конкретних обставин можуть утворювати метастабільні форми. При зберіганні залежно від конкретних обставин може мати місце перетворення модифікацій і утворення стабільніших модифікацій. Згідно з описами в літературі [Reitz та Kleinebudde, 2007; Windbergs et al., 2008] триестери гліцерину (наприклад відомі як Dynasan®), зокрема триміристат гліцерину (Dynasan 114®) або трипальмітат гліцерину (наприклад Dynasan® 116), або тристеарат гліцерину (наприклад Dynasan® 118), є порівняно стійкими до таких змін і тому особливо придатні для застосування як ліпідні основи для лікарських засобів. Насамперед комерційно доступними речовинами, які застосовують як жирові основи, є суміші речовин, наприклад моно-, ді- та/або тригліцеридів. Порівняно з ними переважними є однокомпонентні жирові основи, які в основному складаються лише з одного компонента. Композиції, виготовлені із застосуванням цих допоміжних речовин, відрізняються високою стабільністю при зберіганні. Кількість застосовуваної основи (з матеріалів, які піддаються термопластичної деформації) залежить від кількості інших складових екструдатів. У звичайному випадку застосовують від 15 до 99 % [м/м], переважно від 20 до 99 % [м/м], особливо переважно від 25 до 80 % [м/м], цілком переважно від 30 до 70 % [м/м]. Нижня границя діапазону плавлення застосовуваних основ, насамперед ліпідних основ, як правило, дорівнює щонайменше 50 °C, переважно щонайменше 60 °C. Відповідні винаходові екструдати в разі необхідності можуть містити також одну чи кілька допоміжних та додаткових речовин. Такими речовинами є: засоби для регулювання плинності, переважно колоїдний діоксид кремнію у концентрації від 0,2 до 2 % [м/м]; лубриканти, переважно стеарат магнію або бегенат кальцію, у концентрації від 0,2 до 5 % [м/м]; поверхневоактивні речовини, переважно лецитин, у концентрації від 0,5 до 10 % [м/м]. Окрім цього, можуть бути застосовані також антиоксиданти; придатними до застосування є, наприклад, бутилгідроксіанізол (BHA) або бутилгідрокситолуол (BHT), які застосовують у звичайній кількості, як правило від 0,01 до 0,5 % [м/м], переважно від 0,05 до 0,2 % [м/м]. Процес вивільнення активної речовини можна регулювати, наприклад, шляхом додавання так званих пороутворювачів. Такими речовинами є, наприклад, цукри, особливо лактоза, поліоли, зокрема маніт, або поліетиленгліколі (ПЕГ), переважно від ПЕГ 1500 до ПЕГ 10000, особливо переважно від ПЕГ 1500 до ПЕГ 6000, наприклад ПЕГ 1500 (Macrogol 1500). Пороутворювачі застосовують у концентрації від 5 до 40 % [м/м], переважно в концентрації від 5 до 20 % [м/м]. Іншою можливістю впливу на вивільнення активної речовини є додавання допоміжних засобів для розпаду. До них належать так звані супердезінтегранти, такі як wie кросповідон, кроскармелоза натрію або зшитий карбоксиметилкрохмаль натрію. Супердезінтегранти застосовують у концентрації від 1 до 15 % [м/м], переважно в концентрації від 3 до 10 % [м/м]. В альтернативній формі виконання для цього можуть бути застосовані речовини, які розчиняються в кислотах та/або виділяють діоксид вуглецю, такі як карбонат магнію або карбонат кальцію. Речовини, які виділяють діоксид вуглецю, застосовують у концентрації від 5 % до 15 % [м/м], переважно в концентрації від 5 % до 10 % [м/м]. Окрім цього, відповідні винаходові екструдати можуть містити антистатики. Їх застосування рекомендоване насамперед у тому випадку, якщо електростатичні заряди негативно впливають на процес екструзії. Електростатичні заряди можуть призвести до забивання отворів фільєр, якому можна запобігти шляхом додавання антистатиків. Як антистатики застосовують переважно поліетиленгліколі (ПЕГ), насамперед застосовують поліетиленгліколі від ПЕГ 1500 до ПЕГ 6000. Для досягнення антистатичного ефекту ПЕГ слід застосовувати переважно у формі порошку і розплавляти в процесі екструзії. Тому при додаванні ПЕГ як антистатику температура плавлення ПЕГ має бути достатньо низькою, щоб в процесі екструзії розплавлявся ПЕГ, але не застосовувана жирова основа. Застосування не всіх основ супроводжується 4 UA 105648 C2 5 10 15 20 25 30 35 40 45 50 55 60 утворенням статичних зарядів. Цей ефект спостерігається насамперед у разі застосування триестерів гліцерину та жирних кислот, таких як, наприклад, триміристат гліцерину, трипальмітат гліцерину або тристеарат гліцерину. Тому при застосуванні таких основ рекомендується додавати до суміші для екструдування антистатик, щоб забезпечити безпроблемну екструзію. Антистатики застосовують у концентрації щонайменше 5 % [м/м], переважно щонайменше 10 % [м/м]. У звичайному випадку застосовують не менше 30 % [м/м]. Як фармацевтично активні речовини можуть бути застосовані активні речовини лікарських засобів, а саме такі, чий неприємний смак має бути прихований. Згідно з винаходом застосовують активні речовини, які перебувають у голчатій формі. Як правило, це голчаті кристали. Поняття "голки" чи "голчаті" у цьому контексті застосовують для частинок, довжина яких вочевидь перевищує їх діаметр, причому співвідношення між довжиною та діаметром становить щонайменше більше ніж 3:1, переважно більше ніж 5:1, особливо переважно більше ніж 10:1, цілком переважно більше ніж 20:1. Оскільки голки, як правило, не мають круглого перетину, у сумнівних випадках "діаметр" слід розуміти як найбільший розмір перпендикулярно довжині. У принципі, вибір голчатих активних речовин не дуже обмежений, оскільки немає потреби у розплавленні активної речовини. Завдяки спроможності екструдатів маскувати смак вони придатні переважно для застосування із активними речовинами, що мають неприємний, наприклад гіркий смак. Активні речовини можуть бути вибрані, наприклад, із таких груп: антибіотики, засоби проти паразитуючих простіших, антигельмінтні препарати, засоби для регулювання обміну речовин, протизапальні засоби. Самозрозуміло, поняття "активна речовина" охоплює також голчаті солі та сольвати. Конкретним прикладом активної речовини є месалазин. Месалазин є протизапальним лікарським засобом, який застосовують проти хронічних запальних кишкових захворювань. Він дуже важко розчиняється у воді, має температуру плавлення 280 °C і кристали голчатої форми. Іншим прикладом є кристалічний кофеїн. Переважним конкретним прикладом голчатої активної речовини є празиквантел, давно відомий антигельмінтний препарат, який ефективно діє проти стрічкових гельмінтів (цестодів) та шистозом. Він важко розчиняється у воді, має температуру плавлення 139 °C і кристали голчатої форми. У звичайному випадку застосовують перемелений у штифтовому млині матеріал із розміром частинок 25 мкм (виражений параметром d(0,9)), виряним шляхом лазерної дифрактометрії (фіг. 1). Шляхом уведення в ліпофільну матрицю можна – залежно від природи застосовуваної активної речовини – досягти затриманого вивільнення і, разом із цим, забезпечити ефект пролонгації. Кількість застосовуваної в екструдатах активної речовини залежить від інтенсивності дії та бажаного дозування. Було виявлено, що можуть бути також виготовляти еструдати з високою концентрацією активної речовини до 80 % [м/м], переважно до 70 % [м/м], особливо переважно до 60 % [м/м]. Стандартними діапазонами концентрації є, наприклад, від 1 до 80 % [м/м], переважно від 5 до 70 % [м/м], особливо переважно від 30 до 60 % [м/м]. Відповідні винаходу екструдати виготовляють шляхом змішування і наступного екструдування вихідних матеріалів (однієї чи кількох фармацевтично активних речовин, основи та, в разі необхідності, допоміжних і додаткових речовин). Екструзію здійснюють переважно при температурі, яка не призводить до повного розплавлення матеріалів, що піддаються термопластичному формуванню, а саме зазвичай при температурі від кімнатної, переважно від 40° C, до температури нижче діапазону температур плавлення матеріалів, які піддаються термопластичному формуванню. На практиці при цьому зазвичай орієнтуються на діапазон плавлення, наведений для відповідної основи. Як правило, температуру екструзії встановлюють не нижче ніж на 20 C, переважно на 15 C, особливо переважно на 10 C нижче нижньої границі діапазону плавлення основи, зокрема жирової основи. У звичайному випадку температуру екструзії встановлюють не вище нижчої границі діапазону плавлення основи, переважно на 1 C нижче, особливо переважно на 5 C нижче. Метою є запобігання одержанню м'якої пасти в результаті екструзії. Процес екструзії слід здійснювати, підтримуючи, наскільки це можливо, постійну температуру матеріалу. Для цього особливо придатними є шнекові екструдери з підігрівом, зокрема двошнекові екструдери. Екструдований штранг має переважно круглий переріз і зазначений вище діаметр. Екструдований штранг можна подрібнювати безпосередньо при екструзії ножем або, на окремій стадії процесу, шляхом щадного перемелювання в звичайному млині, наприклад у відцентровому млині. Розмір зерен одержаного продукту залежить від діаметру застосовуваної фільєри, причому довжина частинок подрібнених 5 UA 105648 C2 5 10 15 20 25 30 35 40 45 50 55 60 штрангів не перевищує потрійного діаметру штрангів. Типовий розмір зерен становить, наприклад, від 300 до 500 мкм або, при меншому діаметрі фільєри, також від 200 до 500 мкм. Згідно з переважною формою виконання винаходу перемелений продукт можна ще просіювати. В такий спосіб можна видалити частку дрібних фракцій. Наведене посилання на те, що екструдування здійснюють при температурі, нижчій ніж точка плавлення екструдатів, слід розуміти таким чином, що екструдати, як описано вище, екструдують при температурі, при якій застосовувана термопластична основа ще не повністю розплавляється. Часто інші складові, наприклад активні речовини, мають вищу точку плавлення. Такі екструдати придатні для приховування неприємного смаку окремих компонентів. Відповідні винаходу екструдати після щадного подрібнення в разі потреби можуть бути піддані переробці для одержання відповідних лікарських форм. Для подальшої переробки залежно від конкретних обставин іноді необхідно додавати інші додаткові речовини. Переважними згідно з винаходом лікарськими формами є таблетки, яким в разі необхідності можна надавати форму відповідно до передбаченого застосування. Іншими застосовуваними лікарськими формами є пасти, суспензії, пакетики-саше, капсули тощо. Відповідні винаходу екструдати чи лікарські засоби взагалі можна застосовувати для людей і тварин. Переважно їх застосовують в утриманні тварин і тваринництві для корисних, племінних, зоопаркових, лабораторних, піддослідних та декоративних домашніх тварин, і насамперед для ссавців. До корисних і племінних тварин належать ссавці, такі як велика рогата худоба, коні, вівці, свині, кози, верблюди, індійські водяні буйволи, осли, кролики, лані, північні олені, хутрові звірі, такі як норки, шиншили, бобри, а також птахи, такі як кури, гуси, індики, качки, голуби та страуси. Прикладами переважних корисних тварин є велика рогата худоба, вівці, свині та кури. До лабораторних і піддослідних тварин належать собаки, кішки, кролики та гризуни, такі як миші, щури, морські свинки та золотисті хом'яки. До домашніх і декоративних тварин належать собаки, кішки, коні, кролики, гризуни, такі як золотистий хом'як, морські свинки, миші, а також рептилії, амфібії та птахи для утримання в домашніх умовах і в зоопарку. Екструдати у звичайному випадку застосовують безпосередньо або в формі відповідних композицій (лікарських форм) ентерально, зокрема перорально. Ентеральне введення активних речовин здійснюють, наприклад, перорально в формі гранулятів, таблеток, капсул, паст, суспензій або кормів, до яких додані медикаменти. Можливістю перорального введення є так званий метод "посипання" (Topdressing), при цьому йдеться про порошок, гранулят або пасту, які наносять на корм і які тварина споживає разом із кормом. Придатними до застосування композиціями є: Тверді композиції, такі як, наприклад, грануляти, драже, таблетки, болюси та формовані вироби, які містять активну речовину. Для виготовлення твердих композицій подрібнені екструдати змішують з відповідними носіями, в разі потреби додаючи допоміжні речовини, і надають їм бажаної форми. Як носії можуть бути застосовані всі фізіологічно прийнятні тверді інертні речовини. Для цього використовують неорганічні та органічні речовини. Неорганічними речовинами є, наприклад, кухонна сіль, карбонати, такі як карбонат кальцію, гідрокарбонати, оксиди алюмінію, кремнієві кислоти, глиноземи, осаджений або колоїдний оксид кремнію, фосфати. Органічними речовинами є, наприклад, цукор, целюлоза, харчові продукти і корми, такі як сухе молоко, м'ясокісткове борошно, борошно із зерна злакових культур та зерновий шрот, крохмаль. Допоміжними речовинами є консерванти, антиоксиданти, барвники. Відповідні допоміжні речовини та їх кількість для застосування в принципі відомі фахівцям. Як консервант слід назвати, наприклад, сорбінову кислоту. Придатними до застосування антиоксидантами є, наприклад, бутилгідроксіанізол (BHA) або бутилгідрокситолуол (BHT). Як барвники застосовують придатні для фармацевтичних цілей органічні та неорганічні барвники чи пігменти, такі як, наприклад, оксид заліза. Іншими придатними до застосування допоміжними речовинами є лубриканти і речовини, які надають ковзкості (таблеткам), наприклад стеарат магнію, стеаринова кислота, тальк, бентоніти, речовини, які стимулюють розпад, такі як крохмаль або зшитий полівінілпіролідон, зв'язувальні речовини, такі як крохмаль, желатин або лінійний полівінілпіролідон, а також сухі зв'язувальні речовини, такі як мікрокристалічна целюлоза. Іншими застосовуваними допоміжними речовинами можуть бути рослинні жири, (наприклад 6 UA 105648 C2 5 10 15 20 25 30 35 40 45 50 55 60 оливкова олія, соєва олія, соняшникова олія) або жири тваринного походження, наприклад риб'ячий жир. Зазвичай їх застосовують у кількості від 0,5 до 20 % [м/м], переважно від 0,5 до 10 % [м/м], особливо переважно від 1 до 2 % [м/м]. Суспензії можуть бути введені перорально. Для їх виготовлення подрібнені екструдати суспендують у рідині-носії, в разі необхідності з додаванням інших допоміжних речовин, таких як змочувальні речовини, барвники, речовини, що стимулюють всмоктування, консерванти, антиоксиданти, фотостабілізатори. Як рідини-носії застосовують гомогенні розчинники або суміші розчинників, в яких не розчиняються відповідні екструдати. Відповідними прикладами є фізіологічно прийнятні розчинники, такі як вода, спирти, такі як етанол, бутанол, гліцерин, пропіленгліколь, поліетиленгліколі, а також суміші цих речовин. Як змочувальні речовини (диспергатори) можуть бути застосовані поверхнево-активні речовини. Прикладами таких речовин є: неіоногенні поверхнево-активні речовини, наприклад поліоксіетильована рицинова олія, поліоксіетильований моноолеат сорбітану, моностеарат сорбітану, моностеарат гліцерину, поліоксіетилстеарат, алкілфенолполігліколевий етер; амфолітичні поверхнево-активні речовини, такі як ди-Na-N-лаурил-ß-імінодипропіонат або лецитин; аніоноактивні поверхнево-активні речовини, такі як лаурилсульфат натрію, сульфати етерів жирних спиртів, моноетаноламінова сіль естеру ортофосфорної кислоти та монодіалкілполігліколевого етеру; катіоноактивні поверхнево-активні речовини, такі як хлорид цетилтриметиламонію. Іншими допоміжними речовинами є: речовини, які збільшують в'язкість та стабілізують суспензію, такі як карбоксиметилцелюлоза, метилцелюлоза та інші похідні целюлози та крохмалів, поліакрилати, альгінати, желатин, гуміарабік, полівінілпіролідон, полівініловий спирт, співполімери метилвінілового етеру і ангідриду малеїнової кислоти, поліетиленгліколі, воски, колоїдні кремнієві кислоти або суміші зазначених речовин. Напівтверді композиції можуть бути введені перорально. Вони відрізняються від описаних вище суспензій та емульсій лише вищою в'язкістю. Активні речовини можуть бути застосовані також у поєднанні з синергістами або іншими активними речовинами. Приклади Якщо не зазначено інше, наведені у відсотках дані є масовими відсотками відносно загальної маси готової суміші. Порівняльний приклад І: Екструдат, вміщуючий празиквантел: Порошкову суміш, яка складалася з активної речовини празиквантел (50 % [м/м]), розмір ® частинок d(0,9) = 25 мкм, див. фіг. 1), та допоміжні речовини компритол (Compritol 888 ATO) (49 % [м/м]), жирову основу, основним компонентом якої був дибегенат гліцерину (він містив також монота триестери, а також невелику кількість естерів із ® C16-C20-жирними кислотами), та аеросил (Aerosil 200) (1 % [м/м]), пірогенний колоїдний діоксид кремнію (називаний також високодисперсним діоксидом кремнію), який сприяє покращанню плинності порошкової маси, перед екструзією перемішували в лабораторному змішувачі при кімнатній температурі (15 хв., 40 об./хв.) і закладали в гравіметричний дозатор екструдера. Для екструзії розплаву застосовували синхронний двошнековий екструдер з прес-формою для круглих тонких заготовок і тупими шнековими насадками. У процесі екструзії суміші наведеного складу відбулося забивання численних фільєр (застосовували фільєрну пластину з 67 фільєрами, кожна діаметром 0,3 мм), внаслідок чого тиск безперервно зростав при незмінній частоті обертання і швидкості дозування (фіг. 2). Внаслідок зростання тиску за фільєрною пластиною в процесі із застосуванням неперемеленого празиквантелу значно зросла швидкість екструдатів на виході з незабитих фільєр. Приклад ІІ: Екструдат, вміщуючий тонко перемелений празиквантел Дослід із порівняльного прикладу повторювали із застосуванням празиквантелу, якій був двічі перемелений у струминному млині (d(0,5) = 1,7 мкм, d(0,9) = 3,6 мкм, див. фіг. 3). Процес екструзії у разі застосування перемеленого празиквантелу при завантаженні лікарським препаратом 50 % і діаметрі фільєр 0,3 мм був рівномірним і відтворюваним під постійним тиском. Згідно з характеристикою процесу, наведеною на фіг. 4, приблизно через 12 хвилин тиск стабілізувався на постійному рівні, причому явно був приблизно на 10 бар нижче, ніж у процесі із застосуванням неперемеленого празиквантелу (фіг. 2), в якому тиск через 15 хвилин від початку технологічного процесу зріс до значення близько 40 бар. Швидкість екструзії 7 UA 105648 C2 5 10 15 20 25 30 35 40 45 50 55 60 крізь усі фільєри була рівномірною. При порівнянні екструдатів, одержаних у Порівняльному прикладі І та в цьому Прикладі ІІ, було виявлено розбіжності: внаслідок сильного тертя ліпід сильніше притискався до поверхні екструдатів, що дуже добре було видно крізь растровий електронний мікроскоп; поверхня екструдатів була гладкою та рівною. На відміну від цього поверхня екструдатів із застосуванням перемеленого празиквантелу була нерівною, частинки празиквантелу були розташовані безпосередньо під поверхнею, і їх поверхня відрізнялася наявністю тонкого шару ліпідів. Порівняльний приклад ІІІ: екструдат, вміщуючий неперемелений месалазин Екструдати, вміщуючі неперемелений месалазин (d(0,5) = 10,7 мкм, d(0,9) = 44,0 мкм, див. фіг. 5), одержували аналогічно Порівняльному прикладу І. Порошкову суміш із 50 % [м/м] ® неперемеленого месалазину / 49 % [м/м] компритолу (Compritol ) / 1 % [м/м] високодисперсного ® діоксиду кремнію (Aerosil ) екструдували крізь фільєрну пластину з діаметром фільєр 0,3 мм. У технологічному процесі виникали аналогічні проблеми, що й у Порівняльному прикладі I. Згідно з характеристикою процесу (фіг. 6) через 10 хвилин тиск стабілізувався на значенні близько 25 бар, але ще коливався досить значно. У цьому досліді також спостерігали часткове забивання фільєр, яке, проте, відбувалося не так швидко і не в такому великому масштабі, ніж при застосуванні празиквантелу. Порівняльний приклад ІV: екструдат, вміщуючий перемелений месалазин Шляхом дворазового перемелювання у струминному млині одержали месалазин з меншим розміром частинок: d(0,5) = 4,9 мкм, d(0,9) = 11,9 мкм, див. фіг. 7. Після перемелювання частинки мали явно змінену форму. Завдяки застосуванню цього перемеленого месалазину у процесі екструзії аналогічно Порівняльному прикладі III вдалося вирішальним чином поліпшити технологічний процес. На фіг. 8 видно, що тиск вже через 5 хвилин стабілізувався на постійному рівні 20 бар, швидкість екструзії крізь усі фільєри була рівномірною. Отже, шляхом застосування перемеленого месалазину вдалося запобігти забиванню фільєр і таким чином покращити процес екструзії. При порівнянні екструдатів виявилося, що голчаті кристали месалазину із Порівняльного прикладу в процесі екструзії були зруйновані, в той час як перемелений на порошок месалазин із цього прикладу після екструзії ще зберігав початкову форму і розмір частинок, що добре було видно крізь оптичний мікроскоп за допомогою підігріваного носія об'єкта. Навпаки, голчаті кристали празиквантелу в процесі екструзії не були зруйновані і в екструдаті також ще мали початкову форму та розмір. На підставі описаних вище результатів фахівець міг би очікувати, що великі голчаті кристали месалазину при екструзії спричинять більші проблеми, ніж дрібніші голки празіквантелу. Проте, забивання фільєр та зумовлене цим швидке зростання тиску при застосуванні месалазину було не таким інтенсивним, як при застосуванні празиквантелу, оскільки переважна частина великих голок месалазину була подрібнена вже під час процесу під дією зрізувальних зусиль шнеків екструдера. Порівняльний приклад V: екструдат, не вміщуючий антистатика Аналогічно Прикладу ІІ одержували екструдати, вміщуючі перемелений празиквантел. Використовували порошкову суміш із 50 % [м/м] перемеленого празиквантелу / 49 % [м/м] ® ® динасану (Dynasan 116 ) / 1 % [м/м] високодисперсного діоксиду кремнію (Aerosil ), Dynasan ® 116 є жировою основою, яка на 98 % складається з трипальмітату гліцерину. Еструзію здійснювали крізь фільєрну пластину з фільєрами діаметром 0,3 мм. У процесі екструзії суміші цього складу відбувалося постійне збільшення статичного електричного заряду, утворюваного на екструдатах унаслідок тертя ліпофільної маси об внутрішню поверхню фільєр, так що вже через кілька хвилин екструдат починав сильно притягатися самим екструдером під дією електростатичного заряду і прилипав до екструзійної головки. Під дією цього заряду відбувалося також забивання деяких фільєр і зростав тиск за фільєрною пластиною, незважаючи на те, що застосовували перемелений празиквантел. Запис утворюваних зарядів можна було безперервно здійснювати за допомогою електростатичного датчика IZD 10-510 виробництва компанії SMC, який під час процесу був поміщений безпосередньо перед фільєрною пластиною. В процесі екструзії згідно з цим Порівняльним прикладом електростатичний заряд вже через неповних 2 хвилини вже досягав значення -5 кВ (фіг. 9). Порівняльний приклад VI: екструдат, вміщуючий антистатик Аналогічно Порівняльному прикладу V одержували екструдати із додаванням 5 та 10 % ПЕГ 1500 як антистатика. Використовували порошкову суміш із 50 % [м/м] перемеленого ® ® празиквантелу / 44 % [м/м] Dynasan 116 / 5 % [м/м] ПЕГ 1500 / 1 % [м/м] Aerosil , чи із 50 % ® [м/м] перемеленого празиквантелу / 39 % [м/м] Dynasan 116 / 10 % [м/м] ПЕГ 1500 / 1 % [м/м] 8 UA 105648 C2 ® 5 10 15 20 25 30 35 40 45 50 55 60 високодисперсного діоксиду кремнію (Aerosil ). Температура циліндра становила 60 C, що забезпечувало розплавлення ПЕГ 1500 в процесі екструзії. У процесі екструзії із застосуванням 5 % ПЕГ знову спостерігали забивання деяких фільєр, через 3 хвилини технологічного часу виміряне значення електростатичного заряду перед фільєрною пластиною досягло 1-2 кВ. На відміну від цього процес екструзії із застосуванням 10 % ПЕГ був рівномірним і відновлюваним, без забивання фільєр та без утворення електростатичного заряду, який можна зафіксувати вимірювальними пристроями (фіг. 9). Шляхом додавання 10 % ПЕГ як антистатика можна запобігти утворенню електростатичного заряду на екструдаті, вміщуючому високочисті тирестери гліцерину,і в такий спосіб помітно покращити технологічний процес. Порівняльний приклад VII: екструдат, вміщуючий нерозплавлений антистатик Аналогічно Прикладу VІ одержували екструдати із додаванням 10 % ПЕГ 6000 як антистатика. Використовували суміш із 50 % [м/м] перемеленого празиквантелу / 39 % [м/м] ® ® Dynasan 116 / 10 % [м/м] ПЕГ 6000 / 1 % [м/м] високодисперсного діоксиду кремнію (Aerosil ). Температуру циліндра спочатку встановили на 60 C, потім протягом 8 хвилин зменшили до 55 C і насамкінець охолодили до 52 C. Діапазон плавлення ПЕГ 6000 становив 55-60 C, тому ПЕГ після зниження температури циліндра вже не перебував у розплавленому стані. Процес протікав спочатку, аналогічно Прикладу VI із застосуванням 10 % ПЕГ 1500, рівномірно і без утворення електростатичного заряду, всі фільєри були вільні (фіг. 10). Після зниження температури екструдати виявилися електростатично зарядженими, деякі фільєри були забиті, внаслідок чого зріс тиск за фільєрною пластиною. Вдалося підтвердити, що ПЕГ в процесі екструзії мав перебувати в розплавленому стані, щоб проявити свою антистатичну дію. Порівняльний приклад VIII: екструдат, вміщуючий неперемелений кофеїн Одержували екструдати, які містили неперемелений кофеїн, аналогічно Порівняльному прикладу I. Використовували порошкову суміш із 50 % [м/м] неперемеленого кофеїну (розмір ® частинок d(0,9) = 1170 мкм) / 49 % [м/м] Compritol / 1 % [м/м] високодисперсного діоксиду ® кремнію (Aerosil ); екструзію здійснювали крізь фільєрну пластину з діаметром фільєр 0,3 мм. У технологічному процесі виникали проблеми, аналогічні описаним у Порівняльному прикладі I. Вже через 8 хвилин від початку процесу екструзії тиск внаслідок повного забивання фільєр збільшився настільки, що процес довелося перервати. Порівняльний приклад IX: екструдат, вміщуючий перемелений кофеїн Шляхом дворазового перемелювання у струминному млині одержали кофеїн з меншим розміром частинок. Використання цього перемеленого кофеїну в процесі екструзії аналогічно Прикладу ІІ дозволило вирішальним чином покращити технологічний процес. В процесі екструзії тиск вже через 3 хвилини стабілізувався на постійному рівні 5 бар; швидкість екструзії крізь усі фільєри була рівномірною. Отже, шляхом додавання перемеленого кофеїну можна було запобігти забиванню фільєр та помітно покращити процес екструзії. Аналогічно попереднім прикладам були одержані наведені далі екструдати: Приклад X 70 % [м/м] празиквантелу (перемеленого, d(0,9) = 5,7 мкм) 17 % [м/м] тристеарату гліцерину (Dynasan® 118) 12 % [м/м] ПЕГ 6000 ® 1 % [м/м] високодисперсного діоксиду кремнію (Aerosil ) Діаметр фільєр: 0,3 мм (100 % вільних фільєр в процесі екструзіїї), швидкість шнека: 60 об./хв., температура екструзії: 67 °C. Приклад ХІ 50 % [м/м] празиквантелу (перемеленого, d(0,9) = 5,7 мкм) 29 % [м/м] тристеарату гліцерину (Dynasan® 118) 20 % [м/м] ПЕГ 6000 ® 1 % [м/м] високодисперсного діоксиду кремнію (Aerosil ) Діаметр фільєр: 0,2 мм (180 фільєр, 100 % вільних фільєр в процесі екструзіїї), швидкість шнека: 60 об./хв., температура екструзії: 67 °C. Приклад ХII 50 % [м/м] празиквантелу (перемеленого, d(0,9) = 5,7 мкм) 29 % [м/м] тристеарату гліцерину(Dynasan® 118) 20 % [м/м] ПЕГ 6000 ® 1 % [м/м] високодисперсного діоксиду кремнію (Aerosil ) Діаметр фільєр: 0,3 мм (100 % вільних фільєр в процесі екструзіїї), швидкість шнека: 60 9 UA 105648 C2 5 10 15 20 25 30 35 40 45 50 55 60 об./хв., температура екструзії: 67 °C. Приклад ХIIІ 50 % [м/м] празиквантелу (перемеленого, d(0,9) = 5,7 мкм) 49 % [м/м] тристеарату гліцерину(Dynasan® 118) ® 1 % [м/м] високодисперсного діоксиду кремнію (Aerosil ) Діаметр фільєр: 0,3 мм (3 % вільних фільєр в процесі екструзіїї), швидкість шнека: 60 об./хв., температура екструзії: 67 °C. Біологічний приклад: тест на прийнятність на кішках Сорок кішок розділили на 4 групи по 10 тварин у кожній. Тестували по одному екструдату з Прикладів X - XIII на одну групу з 10 кішок таким чином: Екструдатом в кількості, яка відповідала дозі 5 мг празиквантелу на кілограм маси тіла, посипали (Topdressing) сухий корм для кішок і давали кішкам у звичайні часи годування. Всі кішки з'їдали весь корм. Це оцінювали як підтвердження прийнятності 100 %. Після тижневої перерви тест повторювали, при чому, проте, застосовували консервований корм (вологий) для кішок. Одержали такий самий результат, що і в тесті із застосуванням сухого корму, який оцінили як прийнятність 100 %. На фігурах зображено: Фіг. 1: Гранулометричний склад неперемеленого празикванталу, d(0,5) = 6,2 мкм, d(0,9) = 25,1 мкм, виміряний шляхом лазерної дифрактометрії після мокрого диспергування (пристрій Mastersizer 2000 Ver. 5.54, виробник – компанія Malvern Instruments, Молверн, Великобританія). Фіг. 2: Хід процесу екструзії при застосуванні суміші із 50 % неперемеленого празиквантелу / ® ® 49 % Compritol / 1 % високодисперсного діоксиду кремнію (Aerosil ), фільєрна пластина із діаметром фільєр 0,3 мм. Фіг. 3: Гранулометричний склад двічі перемеленого празикванталу, d(0,5) = 1,7 мкм, d(0,9) = 3,6 мкм, виміряний шляхом лазерної дифрактометрії після мокрого диспергування (пристрій Mastersizer 2000 Ver. 5.54, виробник – компанія Malvern Instruments, Молверн, Великобританія). Фіг. 4: Хід процесу екструзії при застосуванні суміші із 50 % перемеленого прази-квантелу / ® ® 49 % Compritol / 1 % високодисперсного діоксиду кремнію (Aerosil ), фільєрна пластина із діаметром фільєр 0,3 мм. Фіг. 5: Гранулометричний склад неперемеленого месалазину, d(0,5) = 10,7 мкм, d(0,9) = 44,0 мкм, виміряний шляхом лазерної дифрактометрії після мокрого диспергування (пристрій Mastersizer 2000 Ver. 5.54, виробник – компанія Malvern Instruments, Молверн, Великобританія). Фіг. 6: Хід процесу екструзії при застосуванні суміші із 50 % неперемеленого месала-зину / ® ® 49 % Compritol / 1 % високодисперсного діоксиду кремнію (Aerosil ), фільєрна пластина із діаметром фільєр 0,3 мм. Фіг. 7: Гранулометричний склад двічі перемеленого месалазину, d(0,5) = 4,9 мкм, d(0,9) = 11,9 мкм, виміряний шляхом лазерної дифрактометрії після мокрого диспергування (пристрій Mastersizer 2000 Ver. 5.54, виробник – компанія Malvern Instruments, Молверн, Великобританія). Фіг. 8: Хід процесу екструзії при застосуванні суміші із 50 % перемеленого месалазину / 49 % ® ® Compritol / 1 % високодисперсного діоксиду кремнію (Aerosil ), фільєрна пластина із діаметром фільєр 0,3 мм. Фіг. 9: Електростатичний заряд перед фільєрною пластиною в процесі екструзії із застосуванням суміші, вміщуючої 0,5 % чи 10 % ПЕГ 1500. Фіг. 10: Хід процесу екструзії при застосуванні суміші із 50 % перемеленого прази-квантелу / ® ® 39 % Dynasan 116 / 10 % ПЕГ 6000 / 1 % високодисперсного діоксиду кремнію (Aerosil ). Перелік літератури Adeyeye C.M., Price J.C., 1991. Development and Evaluation of Sustained-Release IbuprofenWax Microspheres. 1. Effect of Formulation Variables on Physical Characteristics. Pharm. Res. 8, 1377-1383. Adeyeye C.M., Price J.C., 1994. Development and Evaluation of Sustained-Release IbuprofenWax Microspheres. 2. In-Vitro Dissolution. Pharm. Res. 11, 575-579. Ahrens G., Mentrup E., Maas J., Radau M., 1998. Herstellung geschmackskaschierter Zubereitungen antibakteriell wirksamer Chinolonderivaten. EP 1998/0855183. Alderborn G., Nyström C., 1982. Studies on direct compression of tablets. 3. The effect on tablet strength of changes in particle-shape and texture obtained by milling. Acta Pharm. Suec. 19, 147-156. Al-Omran M.F., Al-Suwayeh S.A., El-Helw A.M., Saleh S.I., 2002. Taste masking of diclofenac sodium using microencapsulation. J. Microencapsul. 19, 45-52. Barra J., Lescure F., Doelker E., 1999. Taste masking as a consequence of the organisation of powder mixes. Pharm. Acta Helv. 74, 37-42. Barthelemy P., Laforet J.P., Farah N., Joachim J., 1999. Compritol® 888 ATO: an innovative hot 10 UA 105648 C2 5 10 15 20 25 30 35 40 45 50 55 60 melt coating agent for prolonged-release drug formulations. Eur. J. Pharm. Biopharm. 47, 87-90. Bienz M., 1996. Taste masking strategies for drug dosage forms. Manufacturing Chemist. 67, 1720. Breitkreutz J., El-Saleh F., Kiera C., Kleinebudde P., Wiedey W., 2003. Pediatric drug formulations of sodium benzoate: II. Coated granules with a lipophilic binder. Eur. J. Pharm. Biopharm. 56, 255260. Cabrera F.A., 2002. Solid Phase Dispersion of Quinolone-OR Naphthyridonecarboxylic acids. WO 2002/058669. Cerea M., Zheng W.J., Young C.R., McGinity J.W., 2004. A novel powder coating process for attaining taste masking and moisture protective films applied to tablets. Int. J. Pharm. 279, 127-139. Chun M.K., Choi H.K., 2004. Preparation and characterization of enrofloxacin/carbopol complex in aqueous solution. Arch. Pharm. Res. 27, 670-675. Farah N., Barthelemy P., Joachim J., 1998. Method for preparing a pharmaceutical composition with modified release of the active principle, comprising a matrix. WO 1998/14176. Huber G.R., Jones D.R., Kuenzi J.C., Kuenzi K.D., Cabrera F.A., 2003. Animal Feeds including Actives and Methods of using same. WO 2003/030653. Jbilou M., Ettabia A., Guyot-Hermann A.M., Guyot J.C., 1999. Ibuprofen Agglomerates Preparation by Phase Separation. Drug Dev. Ind. Pharm. 25, 297-305. Kalbe J., Hopkins T., 1998. Oral applizierbare Granulate von Hexahydropyrazinderivaten. WO 1998/03157. Katsuragi Y., Mitsui Y., Umeda T., Otsuji K., Yamasawa S., Kurihara K., 1997. Basic studies for the practical use of bitterness inhibitors: Selective inhibition of bitterness by phospholipids. Pharm. Res. 14, 720-724. Kim E.-H., Choi H.K., 2004. Preparation of various solid-lipid beads for Drug Delivery of Enrofloxacin. Drug Deliv. 11, 365-370. Li F.-Q., Hu J.-H., Deng J.-X., Su H., Xu S., Liu J.-Y., 2006. In vitro controlled release of sodium ferulate from Compritol® 888 ATO-based matrix tablets. Int. J. Pharm. 324, 152-157. Li S.P., Martellucci S.A., Bruce R.D., Kinyon A.C., Hay M.B., Higgins J.D., 2002. Evaluation of the film-coating properties of a hydroxyethyl cellulose/hydroxypropyl methylcellulose polymer system. Drug Dev. Ind. Pharm. 28, 389-401. Lovrecich M., Nobile F., Rubessa F., Zingone G., 1996. Effect of ageing on the release of indomethacin from solid dispersions with Eudragits. Int. J. Pharm. 131, 247-255. Lu M.Y.F., Borodkin S., Woodward L., Li P., Diesner C., Hernandez L., Vadnere M., 1991. A Polymer Carrier System for Taste Masking of Macrolide Antibiotics. Pharm. Res. 8, 706-712. Moisescu C., Jana C., Habelitz S., Carl G., Rüssel C., 1999. Oriented fluoroapatite glassceramics. J. Noncry. Sol. 248, 176-182. Mirghani A., Idkaidek N.M., Salem M.S., Najib N.M., 2000. Formulation and release behavior of diclofenac sodium in Compritol® 888 ATO matrix beads encapsulated in alginate. Drug Dev. Ind. Pharm. 26, 791-795. Nabil, F. et al., 1998. Method for preparing a pharmaceutical composition with modified release of the active principle, comprising a matrix method for preparing a pharmaceutical composition with modified release of the active principle, comprising a matrix. FR2753904 (A1). Ohta M., Buckton G., 2004. The use of inverse gas chromatography to assess the acid-base contributions to surface energies of cefditoren pivoxil and methacrylate copolymers and possible links to instability. Int. J. Pharm. 272, 121-128. Pearnchob N., Dashevsky A., Siepmann J., Bodmeier R., 2003a. Shellac used as coating material for solid pharmaceutical dosage forms: understanding the effects of formulation and processing variables. Stp Pharma Sciences. 13, 387-396. Pearnchob N., Siepmann J., Bodmeier R., 2003b. Pharmaceutical applications of shellac: Moisture protective and taste-masking coatings and extended-release matrix tablets. Drug Dev. Ind. Pharm. 29, 925-938. Petereit H.U., Weisbrod W., 1999. Formulation and process considerations affecting the stability of solid dosage forms formulated with methacrylate copolymers. Eur. J. Pharm. Biopharm. 47, 15-25. Petereit H.U., Meier C., Gryczke A., 2003. Schmelzextrusion von Wirkstoffsalzen. WO 2003/072083. Petereit H.U., Meier C., Gryczke A., 2004. Verfahren zur Herstellung einer oralen Arzneiform mit unmittelbarem Zerfall та Wirkstofffreisetzung. WO 2004/066976. Prompruk K., Govender T., Zhang S., Xiong C.D., Stolnik S., 2005. Synthesis of a novel PEGblockpoly (aspartic acid-stat-phenylalanine) copolymer shows potential for formation of a micellar drug carrier. Int. J. Pharm. 297, 242-253. 11 UA 105648 C2 5 10 15 20 25 30 35 40 45 50 55 Rasenack N., Müller B.W., 2002. Crystal habit and tableting behaviour. Int. J. Pharm. 244, 45-57. Reitz C., Kleinebudde P., 2007. Solid lipid extrudion of sustained release dosage forms. Eur. J. Pharm. Biopharm. 67, 440-448. Schubert M.A., Schicke B.C., Müller-Goymann C.C., 2005. Thermal analysis of the crystallization and melting behavior of lipid matrices and lipid nanoparticles containing high amounts of lecithin. Int. J. Pharm. 298, 242-254. Shirai Y., Sogo K., Yamamoto K., Kojima K., Fujioka H., Makita H., Nakamura Y., 1993. A Novel Fine Granule System for Masking Bitter Taste. Biol. Pharm. Bull. 16, 172-177. Sohi H., Sultana Y., Khar R.K., 2004. Taste masking technologies in oral pharmaceuticals: Recent developments and approaches. Drug Dev. Ind. Pharm. 30, 429-448. Suzuki H., Onishi H., Takahashi Y., Iwata M., Machida Y., 2003. Development of oral acetaminophen chewable tablets with inhibited bitter taste. Int. J. Pharm. 251, 123-132. Suzuki H., Onishi H., Hisamatsu S., Masuda K., Takahashi Y., Iwata M., Machida Y., 2004. Acetaminophen-containing chewable tablets with suppressed bitterness and improved oral feeling. Int. J. Pharm. 278, 51-61. Takagi S., Toko K., Wada K., Ohki T., 2001. Quantification of suppression of bitterness using an electronic tongue. J. Pharm. Sci. 90, 2042-2048. Thombre A.G., 2004. Palatable controlled-release formulations for companion animals. WO 2004/014346. Wang H., Zhang R., 1995. Compaction behaviour of paracetamol powders of different crystal shapes. Drug Dev. Ind. Pharm. 21, 863-868. Windbergs M., Strachan C.J., Kleinebudde P., 2008 Understanding the solid-state behaviour of triglyceride solid lipid extrudates and its influence on dissolution. Eur. J. Pharm. Biopharm. In Press. Wong L.W., Pilpel N., 1990. The effect of particle shape on the mechanical properties of powders. Int. J. Pharm. 59, 145-154. Yue Y., Moisescu C., Carl G., Rüssel C., 1999. Influence of suspended iso- and anisometric crystals on the flow behaviour of fluoroapatite glass melts during extrusion. Physics and Chemistry of Glasses. 40, 243-247. Zhou F., Vervaet C., Remon J.P., 1996. Matrix pellets based on the combination of waxes, starches and maltodextrins. Int. J. Pharm. 133, 155-160. Zhou F., Vervaet C., Schelkens M., Lefebvre R., Remon J.P., 1998. Bioavailability of ibuprofen from matrix pellets based on the combination of waxes and starch derivatives. Int. J. Pharm. 168, 7984. ФОРМУЛА ВИНАХОДУ 1. Екструдат, що містить принаймні одну фармацевтично активну речовину в формі голок, який відрізняються тим, що співвідношення між розміром частинок голчатої фармацевтично активної речовини та діаметром штрангу становить принаймні 1:25. 2. Екструдат за п. 1, у якого діаметр штрангу становить 0,5 мм або менше. 3. Екструдат за будь-яким із попередніх пунктів, який містить ліпідну основу як допоміжну речовину. 4. Екструдат за будь-яким із попередніх пунктів, який містить гліцериновий естер із С 12-С24жирними кислотами як ліпідну основу. 5. Екструдат за будь-яким із попередніх пунктів, який містить діестер гліцерину як ліпідну основу. 6. Екструдат за пунктом 5, який містить дибегенат гліцерину як ліпідну основу. 7. Екструдат за будь-яким із пунктів 1-4, який містить триестер гліцерину як ліпідну основу. 8. Екструдат за пунктом 7, який містить триміристат гліцерину, трипальмітат гліцерину або тристеарат гліцерину як ліпідну основу. 9. Екструдат за пунктом 8, який містить тристеарат гліцерину як ліпідну основу. 10. Екструдат за будь-яким із попередніх пунктів, який містить антистатик, зокрема поліетиленгліколь. 11. Екструдат за будь-яким із попередніх пунктів, одержаний шляхом екструзії при температурі нижче нижньої границі діапазону плавлення вміщеної в ньому основи. 12 UA 105648 C2 13 UA 105648 C2 14 UA 105648 C2 15 UA 105648 C2 16 UA 105648 C2 Комп’ютерна верстка Л. Бурлак Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 17
ДивитисяДодаткова інформація
Автори російськоюKanikanti, Venkata-Rangarao, Hamann, Hans-Juergen, Kleinebudde, Peter, Witzleb, Rieke
МПК / Мітки
МПК: A61K 9/16, A61K 9/14, A61K 47/44, A61K 9/00, A61K 47/14
Мітки: екструдати, речовинами, активними, голчатими
Код посилання
<a href="https://ua.patents.su/19-105648-ekstrudati-z-golchatimi-aktivnimi-rechovinami.html" target="_blank" rel="follow" title="База патентів України">Екструдати з голчатими активними речовинами</a>
Попередній патент: Арилпіперазини і їх застосування як антагоністів альфа2c
Наступний патент: Спосіб використання одержуваного у газогенераторі синтез-газу
Випадковий патент: Спосіб виготовлення елементів полюса перемикача з вакуумованою перемикальною камерою та зовнішньою ізоляційною оболонкою та елемент полюса перемикача