Похідні 4-(метиламінофенокси)піридин-3-ілбензаміду для лікування раку
Номер патенту: 110037
Опубліковано: 10.11.2015
Автори: Сіракура Масаміті, Харада Ясуо, Тераюті Юкі, Ямагуті Казуя, Накагава Такасі, Сакамото Макото, Суміда Такумі, Кодзіма Ютака
Формула / Реферат
1. Сполука, представлена наступною загальною формулою (1), або її сіль:
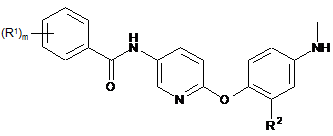 , (1)
, (1)
де R1 представляє атом галогену, арильну групу, арилоксигрупу або нижчу алкільну групу, вибірково заміщену одним або більше атомами галогену;
R2 представляє атом водню, атом галогену, нижчу алкільну групу або нижчу алкоксигрупу; й;
m представляє ціле від 1 до 3;
за умови, що, коли m представляє 2 або 3, R1 є однакові або різні.
2. Сполука згідно із пунктом 1 або її сіль, де R2 представляє атом водню.
3. Сполука згідно із пунктом 1 або її сіль, де R2 представляє атом галогену.
4. Сполука згідно із пунктом 1 або її сіль, де R2 представляє нижчу алкільну групу.
5. Сполука згідно із пунктом і або її сіль, де R2 представляє нижчу алкоксигрупу.
6. Сполука згідно із пунктом 1 або її сіль, яка вибрана з групи, що складається з:
N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензаміду,
N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксаміду,
N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
2-фтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
2,3,4-трифтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}бензаміду,
N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензаміду,
N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксаміду,
N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
2-фтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензаміду,
N-{6-[4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксаміду,
N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензаміду,
N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксаміду,
2-фтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
2,3,4-трифтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}бензаміду,
2,3,4-трифтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}бензаміду,
N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
2-фтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду й
2,3,4-трифтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}бензаміду.
7. Сполука згідно із пунктом 1, яка вибрана з групи, що складається з:
N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензаміду,
N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксаміду,
N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
2-фтор-N-(6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
2,3,4-трифтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}бензаміду,
N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензаміду,
N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксаміду,
N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
2-фтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензаміду,
N-{6-[4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксаміду,
N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензаміду,
N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксаміду,
2-фтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
2,3,4-трифтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}бензаміду,
2,3,4-трифтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}бензаміду,
N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
2-фтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду,
2,3,4-трифтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}бензаміду,
N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензаміду гідрохлориду,
2-фтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду гідрохлориду,
2,3,4-трифтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}бензаміду гідрохлориду.
N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду гідрохлориду,
2,3,4-трифтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}бензаміду гідрохлориду,
N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензаміду гідрохлориду,
N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду гідрохлориду,
2-фтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду гідрохлориду,
2,3,4-трифтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}бензаміду гідрохлориду,
N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду гідрохлориду,
2-фтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензаміду гідрохлориду й
2,3,4-трифтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}бензаміду гідрохлориду.
8. Фармацевтична композиція, що містить сполуку, представлену загальною формулою (1), або її сіль згідно із пунктом 1 й фармакологічно прийнятний носій.
9. Фармацевтична композиція згідно із пунктом 8 для запобігання й/або лікування раку.
10. Сполука, представлена загальною формулою (1), або її сіль згідно із пунктом 1 для застосування у фармацевтичній композиції.
11. Застосування сполуки, представленої загальною формулою (1), або її солі згідно із пунктом 1 як фармацевтичної композиції.
12. Застосування сполуки, представленої загальною формулою (1), або її солі згідно із пунктом 1 для виготовлення фармацевтичної композиції.
13. Спосіб запобігання й/або лікування раку, який передбачає введення пацієнту, який потребує такого лікування, сполуки, представленої загальною формулою (1), або її солі згідно із пунктом 1.
Текст
Реферат: У даному винаході запропонована нова сполука, що має винятковий протираковий ефект, стабільність й метаболічну стабільність. Сполука за даним винаходом представлена наступною загальною формулою (1) (R1)m H N NH O N O R 1 2 , (1) де R представляє атом галогену, арильну групу, арилоксигрупу або нижчу алкільну групу, вибірково заміщену одним або більше атомами галогену; 2 R представляє атом водню, атом галогену, нижчу алкільну групу або нижчу алкоксигрупу; й; m представляє ціле від 1 до 3; UA 110037 C2 (12) UA 110037 C2 1 за умови, що, коли m представляє 2 або 3, R є однакові або різні. UA 110037 C2 5 10 15 20 25 30 35 40 45 50 ГАЛУЗЬ ТЕХНІКИ Даний винахід стосується гетероциклічної сполуки. РІВЕНЬ ТЕХНІКИ Починаючи із клінічного застосування азотистого іприту у якості протиракового засобу у 1940 роках уперше в світі, було розроблено багато протиракових засобів. Фактично, клінічно застосовуються, наприклад, антиметаболіти, як от 5-флуорурацил, протиракові антибіотики, як от адріаміцин, платиновий комплекс, як от цисплатин, й карциностатики рослинного походження, як от віндезин. Але, більшість із цих карциностатиків мають значні побічні ефекти, як от розлади травлення, мієлосупресію й алопецію, оскільки вони є цитотоксичними також по відношенню до нормальних клітин. Завдяки цим бічним ефектам, ряд їх застосування є обмеженим, й далі, у більшості випадків їх терапевтична дія є частковою й короткою. Додатково до терапевтичного ефекту й побічних ефектів, метаболічна стабільність - це одна із важливих вимог до ліків, оскільки на фармакокінетику ліків у організмі людини значно впливає чутливість до метаболізму. Далі, стабільність зберігання фармацевтично активного інгредієнта, що міститься у лікарському засобі, є важливим для його комерційного застосування. Тому, важливим є оцінка метаболічної стабільності й стабільності зберігання запропонованого лікарського засобу. Була проведена розробка нових карциностатиків; але задовільні результати іще не одержані. Патентні документи 1, 2 й 3 описують певні види сполук, що мають фібрознопригнічувальну дію, протиракову дію й пригнічувальну дію щодо активації STAT3/5, відповідно. Але, сполуки окремо розкриті у даному винаході, відрізняються від тих, що окремо розкриті у цих патентних документах, і невідомо, чи сполуки за таким застосуванням мають протиракову дію. СПИСОК ЦИТУВАНЬ ПАТЕНТНА ЛІТЕРАТУРА [Патентний документ 1] WO/2006/014012 [Патентний документ 2] WO/2007/066784 [Патентний документ 3] WO/2008/044667 [Патентний документ 4] JP2001-89412 ОПИС ВИНАХОДУ ЗАВДАННЯ ВИНАХОДУ Предметом даного винаходу є відкриття сполуки, яка має не тільки протиракову дію з меншими побічними ефектами, але також метаболічну стабільність й придатну для лікарського засобу стабільність зберігання. ВИРІШЕННЯ ЗАВДАННЯ Автори даного винаходу провели інтенсивні дослідження щоб досягти вищевказаної мети винаходу. У результаті, було встановлено, що сполука, представлена загальною формулою (1) нижче та її сіль мають виняткову протиракову дію із меншими побічними ефектами, й метаболічною стабільністю й стабільністю зберігання, придатною для ліків. Тому, вони є корисними як медичний засіб для лікування або запобігання різних типів раку. Приклад раку включають рак, пов'язаний із статевими стероїдними гормонами (наприклад, рак простати, рак грудей, рак яєчників, рак матки, рак яєчка) й твердий рак (наприклад, рак легенів, рак кишківника, рак міхура, рак щитовидної залози, рак стравоходу, рак печінки, рак мозку, рак підшлункової залози, рак шлунку, меланома) й рак крові (наприклад, гостра лімфобластна лейкемія, хронічна лімфоцитна лейкемія, гостра мієлогенна лейкемія, хронічна мієлогенна лейкемія, множинна мієлома, лімфома). Термін "рак" у цьому описі включає в себе термін "пухлина". Даний винахід виконаний, базуючись на дослідженнях. Зокрема, даний винахід пропонує медичні засоби, заявлені у пункті 1. Пункт 1: Сполука, представлена наступною загальною формулою (1) або її сіль: (1) 1 де R представляє атом галогену, арильну групу, арилокси групу або нижчу алкільну групу, вибірково заміщену одним або більше атомами галогену; 1 UA 110037 C2 2 5 10 15 20 25 30 35 40 45 50 55 60 R представляє атом водню, атом галогену, нижчу алкільну групу або нижчу алкокси групу; й m представляє ціле від 1 до 3; 1 за умови, що коли m представляє 2 або 3, R є однакові або різні. 2 Пункт 2: Сполука згідно із пунктом 1 або її сіль, де R представляє атом водню. 2 Пункт 3: Сполука згідно із пунктом 1 або її сіль, де R представляє атом галогену. 2 Пункт 4: Сполука згідно із пунктом 1 або її сіль, де R представляє нижчу алкільну групу. 2 Пункт 5: Сполука згідно із пунктом 1 або її сіль, де R представляє нижчу алкокси група. Пункт 6: Сполука згідно із пунктом 1 або її сіль, яка обрана з групи, що складається : N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід, N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід, N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, 2-фтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, 2,3,4-трифтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}бензамід, N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід, N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід, N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, 2-фтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід, N-{6-[4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід, N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід, N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід, 2-фтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, 2,3,4-трифтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}бензамід, 2,3,4-трифтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}бензамід, N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, 2-фтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, й 2,3,4-трифтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}бензамід. Пункт 7: Сполука згідно із пунктом 1, яка обрана з групи, що складається: N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід, N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід, N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, 2-фтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, 2,3,4-трифтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}бензамід, N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід, N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід, N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, 2-фтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід, N-{6-[4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід, N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід, N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід, 2-фтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, 2,3,4-трифтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}бензамід, 2,3,4-трифтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}бензамід, N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, 2-фтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід, 2,3,4-трифтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}бензамід, N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід гідрохлорид, 2-фтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлорид, 2,3,4-трифтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}бензамід гідрохлорид, N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлорид, 2,3,4-трифтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}бензамід гідрохлорид, N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід гідрохлорид, N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлорид, 2-фтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлорид, 2 UA 110037 C2 5 10 15 20 25 30 35 40 45 50 55 2,3,4-трифтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}бензамід гідрохлорид, N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлорид, 2-фтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлорид, й 2,3,4-трифтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}бензамід гідрохлорид. Пункт 8: Фармацевтична композиція, що містить сполуку, представлену загальною формулою (1) або її сіль згідно із будь-яким з пунктів 1-7, й фармакологічно прийнятний носій. Пункт 9: Фармацевтична композиція згідно із пунктом 8 для запобігання й /або лікування раку. Пункт 10: Сполука, представлена загальною формулою (1) або її сіль згідно із будь-яким з пунктів 1-7 для застосування у фармацевтичній композиції. Пункт 11: Застосування сполуки, представленої загальною формулою (1) або її сіллю згідно із будь-яким з пунктів 1-7 як фармацевтичної композиції. Пункт 12: Застосування сполуки, представлена загальною формулою (1) або її сіллю згідно із будь-яким з пунктів 1-7 для виготовлення фармацевтичної композиції. Пункт 13: Спосіб запобігання й/або лікування раку, що містить введення пацієнту, що потребує цього, сполуки, представленої загальною формулою (1) або її солі згідно із будь-яким з пунктів 1-7. ОПИС ЗДІЙСНЕННЯ ВИНАХОДУ Далі наводяться окремі приклади індивідуальних груп, представлених у загальній формулі (1). Приклади нижчої алкокси групи включають лінійні або розгалужені алкокси групи, що мають 1-6 атомів вуглецю, як от метокси, етокси, пропокси, ізопропокси, бутокси, трет-бутокси, пентилокси, й гексилокси групи. Приклади нижчої алкільну групу включають лінійні або розгалужені алкільні групи, що мають 1-6 атомів вуглецю, як от метил, етил, пропил, ізопропил, 2,2-диметилпропил, 1-етилпропил, бутил, ізобутил, трет-бутил, ізопентил, пентил, й гексильні групи. Приклади нижчої алкільної групи, вибірково заміщеної одним або більше атомами галогену включають, додатково до вищеописаного, нижчі алкільні групи, лінійні або розгалужені алкільні групи, що мають 1-6 атомів вуглецю , які можуть бути заміщені 1-3 атомами галогену, як от трифторметил, трихлорметил, хлорметил, бромметил, фторметил, йодметил, дифторметил, дибромметил, дихлорметил, 2-хлоретил, 2,2,2-трифторетил, 2,2,2-трихлоретил, 3-хлорпропил, 2,3-дихлорпропил, 4,4,4-трихлорбутил, 4-фторбутил, 5-хлорпентил, 3-хлор-2-метилпропил, 5бромгексил, й 5,6-дибромгексильні групи. Приклади атому галогену включають атом фтору, атом хлору, атом брому й атом йоду. Приклади арильної групи включають C6-C 10 ароматичні групи, як от феніл, 1-нафтил, 2нафтил, o-толіл, m-толіл й p-толільні групи. Приклади арилокси групи включають C6-C10 арилокси групи, як от фенокси, 1-нафтилокси й 2- нафтилокси. Один переважний приклад - це сполука, представлена загальною формулою (1) або її сіль, де 1 R представляє арильну групу, арилокси групу або нижчу алкільну групу, вибірково заміщену одним або більше атомами галогену; 2 R представляє атом водню, атом галогену, нижчу алкільну групу або нижчу алкокси групу; й m представляє ціле від 1. Інший переважний приклад - це сполука, представлена загальною формулою (1) або її сіль, де 1 R представляє атом галогену; 2 R представляє атом водню, атом галогену, нижчу алкільну групу або нижчу алкокси група; й m представляє ціле від 1 до 3; 1 за умови, що коли m представляє 2 або 3, R s є однакові або різні. Іще один переважний приклад - це сполука, представлена загальною формулою (1) або її сіль, де 1 R представляє a галоген або нижчу алкільну групу, вибірково заміщену одним або більше атомами галогену; 2 R представляє атом водню, атом галогену, нижчу алкільну групу або нижчу алкокси група; й m представляє ціле від 2; 1 за умови, що R є однакові або різні. У таблиці 1 наведений перелік скорочень, застосованих у описі. 3 UA 110037 C2 Таблиця 1 Перелік скорочень Скорочення AcOEt AcONa BINAP AcOH mCPBA conc. DABCO DBN DBU DEAD DEPC ДИBAH ДИPEA DMA DMAP DMF DMSO dec. Et2O Et3N EtOH HOAT HOBT HOBT-H2O MeOH mp MsCl SRB TCA NaBH(OAc)3 n-BuLi NMP Pd(OAc)2 Pd(PPh3)4 Pd/C Pd2(dba)3 PPh3 PPTS OD Pt/C TBAF TBDMSCl TFA THF TMEDA TMPDA WSC WSC-HCl Опис етил ацетат ацетат натрію 2,2'-біс(дифенілфосфін)-1,1'-бінафтил оцтова кислота m-хлорпероксибензойна кислота концентрують 1,4-диазабіцикло[2.2.2]октан 1,5-диазабіцикло[4.3.0]нон-5-ен 1,8-диазабіцикло[5.4.0]ундец-7-ен диетил азодікарбоксилат диетил ціанофосфонат диізобутилалюміній гідрид N,N-диізопропилетиламін диметилацетамід 4-(N,N-диметиламіно)піридин N,N-диметилформамід диметил сульфоксид декомпозиція диетил ефір триетиламін етиловий спирт 1-гідрокси-7-азабензотриазол 1-гідроксибензотриазол 1-гідроксибензотриазол гідрат метиловий спирт точка топлення метансульфоніл хлорид сульфородамін B трихлороцтова кислота натрій триацетоксиборогідрид n-бутиллітій N-метилпірролідон паладій(II) ацетат тетракіс(трифенілфосфін)паладій(0) паладій на вуглеці трис(дибензиліденацетон)дипаладій(0) трифенілфосфін піридинiум p-толуолсульфонат оптична щільність платина на вуглеці тетра-n-бутиламоній фторид трет-бутилдиметилсиліл хлорид трифтороцтова кислота тетрагідрофуран тетраметилетилендиамін тетраметилпропилендиамін 1-(3-диметиламінопропил)-3-етилкарбодиімід 1-(3-диметиламінопропил)-3-етилкарбодиімід гідрохлорид Далі будуть описані способи одержання сполук згідно із даним винаходом. Гетероциклічна сполука за даним винаходом представлена загальною формулою (1) або її 4 UA 110037 C2 сіль може бути легко одержана фахівцем, застосовуючи технічні знання, базуючись на прикладах й посилальних прикладах даного опису. Наприклад, гетероциклічна сполука або її сіль може бути вироблена згідно із способами, показаними у наступних формулах реакцій. [Формула реакції 1] 5 1 10 15 20 25 30 35 40 2 де R , R , й m є як визначено вище, й P - це an аміно-захисна група. Сполука (1) може бути одержана шляхом зняття захисту сполуки (2). Оскільки умови для зняття захисту залежать у відповідності від видів аміно-захисної групи P, вони не мають обмежень, до тих пір поки проходить зняття захисту. Наприклад, зняття захисту може бути виконане згідно із способом, описаним у T.W. Green, Protective Groups in Organic Synthesis,4th edition, John Wiley & Sons, Inc., p. 696-926). Коли P - це трет-бутоксикарбоніл, зняття захисту може бути виконане у інертному розчиннику у присутності 1.0 - 100.0 молів кислоти на моль Сполуки (2). Приклади кислоти включають неорганічні кислоти, як от соляна кислота й сірна кислота; й органічні кислоти, як от TFA й метансульфонова кислота. Застосований розчинник не має особливих обмежень, окрім того, щоб він не пригнічував реакцію й дозволяв вихідному матеріалу розчинюватись до певного ступеню. Його переважні приклади включають AcOEt, MeOH, EtOH, 1,4-диоксан, метилен хлорид, хлороформ, ізопропанол, DMF й NMP. Реакцію звичайно виконують при температурі від -10 до 100°C, переважно 0-50°C, й звичайно завершують від 0.5 до 50 годин, переважно 1-20 годин. Далі детально роз’яснені формули реакцій A-C для одержання вихідної сполуки (2). [Формула реакції A] . 2 1 де R й P є як визначено вище, й X - це вихідна група. Сполука (5) може також бути одержана реакцією сполуки (3) зі сполукою (4). Реакція може бути виконана у присутності або відсутності основи, у інертному розчиннику або без будь-якого розчинника. 1 Приклади вихідної групи, представленох X включають галоген (наприклад, фтор, хлор, бром, йод), вибірково галогенований C1-6 алкілсульфонілокси (наприклад, метансульфонілокси, етансульфонілокси, трихлорметансульфонілокси, трифторметансульфонілокси, тощо), арилсульфонілокси (наприклад, C6-10 арилсульфонілокси (наприклад, фенілсульфонілокси, нафтилсульфонілокси) вибірково заміщений 1-3 замісниками, обраними з-поміж групи C1-6 алкільна група (наприклад, метил, етил, тощо), C1-6 алкокси (наприклад, метокси, етокси, тощо) й нітро група), галоацилокси (наприклад, трихлорацетокси, трифторацетокси й тому подібні), й тому подібні. Окремі приклади включають фенілсульфонілокси, m-нітрофенілсульфонілокси, pтолуолсульфонілокси, трихлорацетокси, трифторацетокси й тому подібні. Приклади інертного розчинника включають воду; ефіри як от диоксан, THF, Et 2O, диетилен гліколь диметил ефір й етилен гліколь диметил ефір; ароматичні гідрокарбони як от бензол, толуол й ксилол; галогеновані гідрокарбони як от дихлорметан, дихлоретан, хлороформ й карбон тетрахлорид; нижчі (C1-6) спирти як от MeOH, EtOH й ізопропанол; кетони як от ацетон й метил етил кетон; полярні розчинники як от DMF, DMSO, гексаметилфосфорний триамід й ацетoнітрил; й їх суміші. 5 UA 110037 C2 5 10 15 20 25 30 35 40 У якості основи може бути застосований широкий ряд відомих основ. Приклади основи включають неорганічні основи, наприклад, гідроксиди лужних металів як от гідроксид натрію, гідроксид калію, цезій гідроксид й літій гідроксид; карбонати лужних металів як от натрій карбонат, карбонат калію, карбонат цезію, карбонат літію, гідрогенкарбонат літію, гідрогенкарбонат натрію й гідрогенкарбонат калію; лужні метали як от натрій й калій; аміди металів як от амід натрію; гідриди металів як от натрій гідрид, й калій гідрид; алкоксиди лужних металів як от натрій метоксид, натрій етоксид, калій метоксид й калій етоксид; й органічні основи, наприклад, Et3N; ДИPEA; трипропиламін; піридин; хінолін; DBN; DBU; й DABCO. Ці основи можуть бути застосовані окремо або у комбінації із двох або більше. Вищевказана реакція може бути виконана додаванням до реакційної системи, за потреби, йодиду лужного metalу, що слугує як прискорювач реакції, як от калій йодид або натрій йодид. Сполука (4) звичайно застосовують у кількості принаймні 0.5 моль, переважно 1-5 молів, на моль сполуки (3). Основу звичайно застосовують у кількості 0.5-10 молів, переважно 1-6 молів, на моль сполуки (3). Реакцію звичайно виконують при температурі від 0 до 250°C, переважно 0-200°C, й звичайно завершують у 1-80 годин. [Формула реакції B] 2 де R й P є як визначено вище. Етап 1 Сполука (6) може бути одержана реакцією сполуки (5) з метилюючим реагентом. Реакція може бути виконана у присутності або відсутності основи, у інертному розчиннику або без будьякого розчинника. Приклади метилюючого реагенту включають йодметан, диметил сульфат, диметил карбонат, метил трифторметансульфонат, метилфторсульфонат, й тому подібні. Приклади інертного розчинника включають вода; ефіри як от диоксан, THF, Et 2O, діетилен гліколь диметил ефір й етилен гліколь диметил ефір; ароматичні гідрокарбони як от бензол, толуол й ксилол; галогенований гідрокарбони як от дихлорметан, дихлоретан, хлороформ й тетрахлорид вуглецю; нижчі (C1-6) спирти як от MeOH, EtOH й ізопропанол; кетони як от ацетон й метил етил кетон; полярні розчинники як от DMF, DMSO, гексаметилфосфорний триамід й ацетoнітрил; й їх суміші. У якості основ може бути застосований широкий ряд відомих основ. Приклади основи включають неорганічні основи, наприклад, гідроксиди лужних металів як от гідроксид натрію, гідроксид калію, цезій гідроксид й літій гідроксид; карбонати лужних металів як от натрій карбонат, карбонат калію, карбонат цезію, карбонат літію, гідрогенкарбонат літію, гідрогенкарбонат натрію й гідрогенкарбонат калію; лужні метали як от натрій й калій; аміди металів як от амід натрію; гідриди металів як от натрій гідрид, й калій гідрид; алкоксиди лужних металів як от натрій метоксид, натрій етоксид, калій метоксид й калій етоксид; й органічні основи, наприклад, Et3N; ДИPEA; трипропиламін; піридин; хінолін; DBN; DBU; й DABCO. Ці основи можуть бути застосовані окремо або у комбінації двох або більше.. Метилюючий засіб звичайно застосовують у кількості 0.9-10 молів, переважно 1-5 молів, на моль сполуки (5). Основу звичайно застосовують у кількості 0.5-10 молів, переважно 1-5 молів, на моль 6 UA 110037 C2 5 10 15 20 сполуки (5). Реакція звичайно виконують при температурі від -10°C to 100°C, переважно 0°C to 80°C, й звичайно завершують in 0.5 to 48 годин, переважно 1 to 24 годин. Етап 2 Сполука (7) може бути одержана відновленням сполуки (6). Відновлення може бути виконане у присутності відновлюючого каталітичним гідрогенуванням засобу , у інертному розчиннику. Приклади відновлюючого каталітичним гідрогенуванням засобу включають паладієву чернь, паладій вуглець, оксид платини, платинову чернь й нікель Ренея. Приклади інертного розчинника включають карбоксильні кислоти як от мурашина кислота й оцтова кислота; ефіри як от диоксан, THF, Et2O, діетилен гліколь диметил ефір, й етилен гліколь диметил ефір; естери як от метил ацетат, AcOEt й ізопропил ацетат; й нижчі (наприклад, C 1-6) спирти як от MeOH, EtOH й ізопропанол. Реакцію звичайно виконують у атмосфері водню при атмосферному тиску до біля 20 атм, й переважно атмосферному тиску до 10 атм; або у присутності донора водню, як от мурашина кислота, амоній формат, циклогексан, або гідрат гідразину. Засіб відновлюючого каталітичного гідрогенування звичайно застосовують у кількості 0.1-40 мас%, й переважно 1-20 мас%, базуючись на сполуці (6). Реакцію звичайно виконують при температурі від -30 до 100°C, й переважно 0°C-60°C. [Формула реакції C] 1 25 30 35 40 45 50 2 2 де R , R , m й P є як визначено вище, й X - це вихідна група як от атом галогену (фтор, хлор, бром й йод) й гідрокси. Сполука (2) може бути одержана реакцією сполуки (7) зі сполукою (8). 2 Коли X - це атом галогену, реакція може бути виконана у присутності або відсутності основи, у інертному розчиннику. Приклади інертного розчинник включають воду; ефіри як от диоксан, THF, Et2O, діетилен гліколь диметил ефір й етилен гліколь диметил ефір; естери як от метил ацетат, AcOEt й ізопропил ацетат; ароматичні гідрокарбони як от бензол, толуол й ксилол; галогенований гідрокарбони як от дихлорметан, дихлоретан, хлороформ й вуглець тетрахлорид; нижчі (C1-6) спирти як от MeOH, EtOH й ізопропанол; кетони як от ацетон й метил етил кетон; полярні розчинники як от DMF, DMSO, гексаметилфосфорний триамід й ацетoнітрил; й їх суміші. Широкий ряд відомих основ може бути застосований у якості основи. Приклади основи включають неорганічні основи, наприклад, гідроксиди лужних металів, як от гідроксид натрію, гідроксид калію, цезій гідроксид й літій гідроксид; карбонати лужних металів як от натрій карбонат, карбонат калію, карбонат цезію, карбонат літію, гідрогенкарбонат літію, гідрогенкарбонат натрію й гідрогенкарбонат калію; лужні метали як от натрій й калій; аміди металів як от амід натрію; гідриди металів як от натрій гідрид, й калій гідрид; алкоксиди лужних металів як от натрій метоксид, натрій етоксид, калій метоксид й калій етоксид; й органічні основи, наприклад, Et3N; ДИPEA; трипропиламін; піридин; хінолін; DBN; DBU; й DABCO. Ці основи можуть бути застосовані окремо або у комбінації двох або більше. У цій реакції, сполуку (8) звичайно застосовують у кількості принаймні 0.5 моль, переважно 1-5 молів, на моль сполуки (7). Основу звичайно застосовують у кількості 0.5-10 молів, переважно 1-5 молів, на моль сполуки (5). Реакцію звичайно виконують при температурі від -10°C до 100°C, переважно 0°C-80°C, й звичайно завершують від 5 хвилин до 48 годин, переважно 0.5-24 години. 2 Коли X - це гідрокси, сполука (2) може бути одержана реакцією сполуки (7) зі сполукою (8) згідно із відомою реакцією утворення амідного зв’язку. Умови для відомих реакцій утворення амідного зв’язку можуть бути легко застосовані у цій реакції утворення аміду. Наприклад, можуть бути застосовані наступні способи реакції: (i) спосіб змішаного кислотного ангідриду, у 7 UA 110037 C2 5 10 15 20 25 30 35 40 45 50 55 60 якому Сполука (8) реагує з алкіл галоформатом, утворюючи змішаний кислотний ангідрид, й потім змішаний кислотний ангідрид реагує зі сполукою (7); (ii) спосіб активного складного ефіру, у якому Сполуку (8) перетворюють на активований складний ефір як от феніл складний ефір, pнітрофеніл складний ефір, N-гідроксисукцинімід складний ефір, або 1-гідроксибензотриазол складний ефір, або на активований амід з бензоксазаолін-2-тіоном, й потім активований складний ефір або амід реагує зі сполукою (7); (iii) застосування активуючого засобу, у якому Сполуку (7) піддають реакції конденсації зі сполукою (8) у присутності активуючого засобу; й (iv) інші способи, наприклад, спосіб у якому Сполуку (8) перетворюють на карбоксильний ангідрид, використовуючи дегідратуючий засіб як от оцтовий ангідрид, й потім карбоксильний ангідрид реагує зі сполукою (7), спосіб у якому складний ефір сполуки (8) з C 1-6 спиртом реагує зі сполукою (7) при високому тиску й високій температурі, й спосіб, у якому галід кислоти сполуки (8), тобто, галідкарбоксильної кислоти , реагує зі сполукою (7). Взагалі, спосіб змішаного кислотного ангідриду (i) може бути виконаний у присутності або відсутності основи, у інертному розчиннику. Приклади інертного розчинника включають галогеновані гідрокарбони як от хлороформ, дихлорметан, дихлоретан й тетрахлорид вуглецю; ароматичні гідрокарбони як от бензол, толуол й ксилол; ефіри як от Et2O, диізопропил ефір, THF й диметоксиетан; естери як от метил ацетат, AcOEt й ізопропил ацетат; апротонні полярні розчинники як от DMF, диметилсульфоксид й гексаметилфосфорний триамід; й їх суміші. Приклади основи включають органічні основи як от Et3N, триметиламін, піридин, диметиланілін, ДИPEA, диметиламінопіридин, N-метилморфолін, DBN, DBU й DABCO; неорганічні основи, наприклад, карбонати як от натрій карбонат, карбонат калію, гідрогенкарбонат натрію й гідрогенкарбонат калію; гідроксиди металів як от гідроксид натрію, гідроксид калію й гідроксид кальцію; гідриди металів як от калій гідрид й натрій гідрид; метали як от калій й натрій; аміди металів як от амід натрію; й алкоксиди металів як от натрій метоксид й натрій етоксид. Приклади алкіл галоформату, застосованого у способізмішаного кислотного ангідриду , включають метил хлороформат, метил бромформат, етил хлороформат, етил бромформат й ізобутил хлороформат. У цьому способі, сполуку (7), алкіл галоформат, й сполуку (8) переважно застосовують у еквімолярних кількостях, але кожний із алкіл галоформату й сполуки(8) може також бути застосований у кількості 0.5-2 молів на моль сполуки (7). Реакцію звичайно виконують при від -20 до 150°C, переважно при від 10 до 50°C, звичайно завершують у 5 хвилин до 30 годин, переважно від 10 хвилин до 25 годин. Спосіб (iii), у якому реакцію конденсації виконують у присутності активуючого засобу, може бути виконаний у інертному розчиннику у присутності або відсутності основи. Приклади інертного розчинника включають галогеновані гідрокарбони, як от хлороформ, дихлорметан, дихлоретан й вуглець тетрахлорид; ароматичні гідрокарбони як от бензол, толуол й ксилол; ефіри як от Et2O, диізопропил ефір, THF й диметоксиетан; естери як от метил ацетат, AcOEt й ізопропил ацетат; апротонні полярні розчинники як от DMF, диметилсульфоксид й гексаметилфосфорний триамід; й їх суміші. Приклади основи включають органічні основи, як от Et3N, ДИPEA, триметиламін, піридин, диметиланілін, N-етилдиізопропиламін, диметиламінопіридин, N-метилморфолін, DBN, DBU, й DABCO; неорганічні основи, наприклад, карбонати, як от натрій карбонат, карбонат калію, гідрогенкарбонат натрію й гідрогенкарбонат калію; гідроксиди металів, як от гідроксид натрію, гідроксид калію й гідроксид кальцію; гідриди металів, як от калій гідрид й натрій гідрид; метали, як от калій й натрій; аміди металів, як от амід натрію; й алкоксиди металів, як от натрій метоксид й натрій етоксид. Приклади активуючого засобу включають дициклогексилкарбодиімід, WSC, DEPC, DMT-MM, трифенілфосфін, дифенілфосфініл хлорид, феніл-N-фенілфосфорамід хлоридат, диетил хлорфосфат, диетил ціанофосфат, дифенілфосфорний азид й біс(2-оксо-3оксазолідиніл)фосфінієвий хлорид й карбонілдиімідазол. Відповідна кількість активуючого засобу - це звичайно принаймні 0.9 моль, переважно 1-5 молів на моль сполуки (8). Домішка може бути застосована разом з активуючим засобом. Приклади домішки включають HOAT, HOBT, й тому подібні. Реакцію звичайно виконують при від -20 до 180°C, переважно при від 0 до 150°C, й звичайно завершують у 5 хвилин до 90 годин. Коли спосіб, у якому кислотний галід сполуки (7) реагує зі сполукою (8), що вказана визе, коли застосовуються один або інший способи (iv) реакція може бути виконана у присутності основи, у інертному розчиннику. Приклади основи включають широкий ряд відомих основ, як от ті, що подібні до основ, застосованих для способу змішаного кислотного ангідриду (i). Додатково 8 UA 110037 C2 5 10 15 20 25 30 35 40 45 50 55 60 до вищевказаних розчинників, приклади інертного розчинника включають спирти, як от метанол, етанол, ізопропанол, пропанол, бутанол, 3-метокси-1-бутанол, етил целлобсольв й метил целлобсольв; ацетoнітрил; піридин; ацетон; й воду. Відношення сполуки (7) до галіду кислоти сполуки (8) не обмежене, й може бути зручно обране з-поміж широкого ряду. Це звичайно придатне до застосування, наприклад, принаймні 0.9 моль, переважно 1-5 молів сполуки (7), на моль галіду кислоти сполуки (8). Реакцію звичайно виконують при від -20 до 180°C, переважно при від 0 до 150°C, й звичайно завершують у 5 хвилин до 30 годин. Вихідні сполуки й проміжні сполуки, наведені у кожній із вищевказаних формул реакцій, можуть бути піддані, за необхідності перед застосуванням у реакціях, захисту функціональної групи із відповідною захисною групою відомим способом, й зняттю захисту захисної групи відомим способом після завершення реакції. Додатково, сполуки у формі, у якій до вихідного матеріалу сполуки додають сольват (наприклад, гідрат, етанолат, тощо) й об’єкт сполуки наведеної у кожній із формул реакції, включають у кожну з формул. Сполука (1) згідно із даним винаходом включає стереоізомери й оптичні ізомери. Вихідний матеріал сполук й об'єкт сполук, представлених кожною з формул реакції, може бути застосований у відповідній формі солі. Об’єкт сполук, одержаних на кожному з етапів, може бути застосований на наступному етапі без виділення. Кожний з об’єктів сполук, одержаних згідно із вищевказаними формулами реакцій, може бути виділений й очищений від реакційної суміші, наприклад, після охолодження реакційної суміші, шляхом виконання процедури виділення, як от фільтрацією, концентрація, екстракція, тощо, щоб виділити сирий продукт реакції, й потім піддавання сирого продукту реакції загальній процедурі очищення, як от колонкова хроматографія, рекристалізація, тощо Серед сполук за даним винаходом, ті, що мають основну групу,можуть легко утворювати солі зі звичайними фармацевтично прийнятними кислотами. Приклади таких кислот включають соляну кислоту, бромоводневу кислоту, азотну кислоту, сірну кислоту, фосфорну кислоту й інші неорганічні кислоти, метансульфонову кислоту, p-толуолсульфонову кислоту, оцтову кислоту, лимонну кислоту, виннокам’яну кислоту, малеїнову кислоту, фумарову кислоту, яблучну кислоту, молочну кислоту й інші органічні кислоти, тощо. Серед сполук за даним винаходом, ті, що мають кислотну групу, можуть легко утворювати солі шляхом реакції з фармацевтично прийнятними основними сполуками. Приклади таких основних сполук включають гідроксид натрію, гідроксид калію, гідроксид кальцію, карбонат натрію, карбонат калію, гідрогенкарбонат натрію, гідрогенкарбонат калію, тощо. У сполуці за даним винаходом, один або більше атомів може бути заміщений одним або 2 3 більше ізотопними атомами. Приклади ізотопних атомів включають дейтерій ( H), тритій ( H), 13 14 18 C, N, O, тощо. Далі наведене роз’яснення фармацевтичних препаратів, що містять сполуку за даним винаходом у якості діючого інгредієнта. Такі фармацевтичні preparations одержують шляхом перетворення сполуки за даним винаходом у корисні фармацевтичні препарати, використовуючи звичайно застосовувані розбавники або наповнювачі, як от наповнюючі речовини, технічні наповнювачі, зв’язувачі, зволожуючі засоби, дезінтегранти, поверхнево-активні речовини, змащувачі, тощо. Форма таких фармацевтичних препаратів може бути обрана з-поміж різних форм згідно із завданням терапії. Типові приклади включають таблетки, пілюлі, порошки, розчини, суспензії, емульсії, гранули, капсули, суппозиторії, ін’єкції (розчини, суспензії, тощо) й тому подібні. Утворюючи таблетки, можуть бути застосовані будь-які різні відомі носії, включаючи, наприклад, лактозу, білий цукор, натрій хлорид, глюкозу, сечовину, крохмаль, кальцій карбонат, каолін, кристалічну целюлозу й інші наповнювачі; воду, етанол, пропанол, простий сироп, розчинм глюкози, розчини крохмалю, розчини желатину, карбоксиметилцелюлозу, шеллак, метилцелюлозу, калій фосфат, полівінілпірролідон й інші зв’язувачі; сухий крохмаль, натрій альгінат, порошку агару, порошку ламінаран, гідрогенкарбонат натрію, кальцій карбонат, естери аліфатичних кислот поліоксиетиленсорбітану, натрій лаурилсульфат, стеаринової кислоти моногліцерид, крохмаль, лактозу й інші дезінтегранти; білий цукор, стеарин, масло какао, гідрогеновані олії й інші пригнічувачі дезінтеграції; чвертинна основа амонію, натрій лаурил сульфат й інші промотори абсорбції; гліцерин, крохмаль й інші зволожуючі засоби; крохмаль, лактозу, каолін, бентоніт, коллоїдна кремнієва кислота й інші абсорбенти; очищений тальк, стеарати, порошку борної кислоти, поліетилен гліколь й інші змащувачі; тощо. Такі таблетки можуть бути покриті звичайними матеріалами для покриття, за потреби, щоб приготувати, наприклад, покриті цукром таблетки, покриті желатином таблетки, таблетки з 9 UA 110037 C2 5 10 15 20 25 30 35 40 45 50 55 60 кишково-розчинюваним покриттям, покриті плівкою таблетки, дво- або мультишарові таблетки, тощо. Утворюючи пілюлі, можуть бути застосовані будь-які різні відомі носії , включаючи, наприклад, глюкозу, лактозу, крохмаль, масло какао, гідрогеновані рослинні олії, каолін, тальк й інші наповнювачі; порошку гуміарабік, порошку трагактант, желатин, етанол й інші зв’язувачі; ламінаран, агар й інші дезінтегранти; тощо. Утворюючи супозиторії, можуть бути застосовані будь-які різні відомі носії, включаючи, наприклад, поліетилен гліколь, масло какао, вищі спирти, естери вищих спиртів, желатин, напівсинтетичні гліцериди, тощо. Утворюючи ін’єкції, розчин, емульсію або суспензію стерилізують й переважно роблять ізотонічною з кров’ю. Можуть бути застосовані будь-які різні відомі розбавники для одержання розчину, емульсії або суспензії. Приклади таких розбавників включають воду, етанол, пропилен гліколь, етоксильований ізостеариловий спирт, поліоксильований ізостеариловий спирт, естери аліфатичних кислот поліоксиетилен сорбітану, тощо. У цьому випадку, фармацевтичний препарат може містити натрій хлорид, глюкозу або гліцерин у кількості, достатній для одержання ізотонічного розчину, й може містити звичайні солюбілізатори, буферні речовини, анальгетичні засоби, тощо, й далі, за необхідності, барвники, консерванти, смакові добавки, підсолоджуючі засоби, тощо, й/або інші медикаменти. Пропорція сполуки за даним винаходом у фармацевтичному препараті не обмежена й може бути легко обрана з-поміж широкого ряду. Звичайно є переважним, що фармацевтична preparation містить сполуку за даним винаходом у пропорції від 1 до 70 мас.%. Шлях введення фармацевтичної preparation згідно із даним винаходом не обмежений, й preparation може бути введена шляхом, придатним для формування of the preparation, віку й статі пацієнта, стану захворювання, й інших умов. Наприклад, таблетки, пілюлі, розчини, суспензії, емульсії, гранули й капсули вводять орально. Ін’єкції вводять інтравенозно окремо або у суміші зі звичайними ін’єкційними трансфузіями як от розчини глюкози, розчини аміно кислот або тому подібні, або вводять окремо внутрішньом’язово, внутрішньошкірно, підшкірно або внутрішньобрюшинно, за бажанням. Супозиторії вводять ректально. Дозування фармацевтичної preparation зручно обирають відповідно до способу застосування, віку й статі пацієнта, серйозності захворювання, й інших умов, й звичайно 0.001100 мг/кг ваги тіла/день, й переважно 0.001-50 мг/кг ваги тіла/день, у одиничних або розділених дозах. Оскільки дозування залежить від різних умов, достатнім може бути дозування менше, ніж вищевказаний інтервал, або може бути необхідним дозування більше, ніж вищевказаний інтервал. ПРИКЛАДИ Нижче наводяться приклади виготовлення сполук, застосованих у винаході, які далі супроводжуються результатами фармакологічного тесту цих сполук. Посилальний Приклад 1 Виготовлення трет-бутил {3-метокси-4-[(5-нітропіридин-2-іл)окси]феніл}карбамату Суміш 2-метокси-4-нітрофенол (3.22 г), ди-трет-бутил дикарбонат (4.16 г) й паладій на вуглеці (5% мас., 2.03 г) у EtOH (100 мл) перемішують при 40°C 5 годин у атмосфері водню. Суміш фільтрують крізь пластину целіту й фільтрат концентрують при зниженому тиску даючи на виході коричневу олію. Олію розчиняють у DMF (80 мл). До розчину додають 2-хлор-5нітропіридин (3.02 г) й карбонат калію (3.95 г). Після перемішування при кімнатній температурі 1 годину й 50°C 3 години, суміш фільтрують крізь пластину целіту й фільтрат концентрують при зниженому тиску. Осад розбавляють у AcOEt й воді, й екстрагують з AcOEt. Органічний шар промивають з водою, насиченим водним NaCl, сушать над безводним Na 2SO4 й концентрують при зниженому тиску. До осаду додають Et2O/ ацетон й суміш перемішують при кімнатній температурі усю ніч. Одержану тверду частку збирають фільтрацією, й фільтрат очищують колонковою хроматографією на силікагелі (n-гексан/AcOEt = 9/1 - 3/1). Усе це поєднують щоб досягти цільової сполуки (5.44 г) у вигляді блідо-жовтої твердої речовини. 1 H-ЯМР (CDCl3) : 1.53 (9H, s), 3.76 (3H, s), 6.54 (1H, s), 6.76 (1H, dd, J = 8.5, 2.4 Hz), 6.997.06 (2H, m), 7.43 (1H, s), 8.44 (1H, dd, J = 9.0, 2.7 Hz), 9.00-9.02 (1H, m). Посилальний приклад 2 Виготовлення трет-бутил {3-метил-4-[(5-нітропіридин-2іл)окси]феніл}карбамату До розчину DMF (50 мл) трет-бутил (4-гідрокси-3-метилфеніл)карбамату (5.00 г) додають 2хлор-5-нітропіридин (3.91 г) й карбонат калію (4.64 г). Після перемішування при 80°C 4 години, суміш концентрують при зниженому тиску. Осад розбавляють у AcOEt й воді, й екстрагують з 10 UA 110037 C2 5 10 15 20 25 30 35 40 45 50 55 60 AcOEt. Органічні шари промивають з водою, насиченим водним NaCl, сушать над безводним Na2SO4 й концентрують при зниженому тиску. До осаду додають Et2O й суміш перемішують при кімнітній температура 2 години. Одержану тверду частку збирають фільтрацією щоб одержати цільову сполуку (6.04 г) у вигляді коричневого порошку. 1 H-ЯМР (CDCl3) : 1.52 (9H, s), 2.12 (3H, s), 6.49 (1H, brs), 6.98 (1H, d, J = 8.6 Hz), 6.99 (1H, d, J = 9.0 Hz), 7.21 (1H, dd, J = 8.5, 2.7 Hz), 7.39 (1H, s), 8.46 (1H, dd, J = 9.0, 2.9 Hz), 9.03 (1H, d, J = 2.9 Гц). Посилальний приклад 3 Виготовлення трет-бутил {3-метокси-4-[(5-нітропіридин-2-іл)окси]феніл}метилкарбамату До розчину DMF (80 мл) трет-бутил {3-метокси-4-[(5-нітропіридин-2-іл)окси]феніл}карбамату (4.42 г) додають NaH (60% у олії, 0.51 г) при 0°C. Після перемішування при 0°C 10 хвил, додають йодметан (1.91 г) й суміш перемішують при кімнітній температура 1 годину. Суміш занурюють у крижану воду й екстрагують з AcOEt. Органічний шар промивають з водою, насиченим водним NaCl й сушать над безводним Na2SO4. Розчинник видаляють при зниженому тиску, щоб одержати цільову сполуку (4.80 г) як коричневу олію. 1 H-ЯМР (CDCl3) : 1.49 (9H, s), 3.30 (3H, s), 3.74 (3H, s), 6.87 (1H, dd, J = 8.5, 2.4 Гц), 6.967.05 (2H, m), 7.09 (1H, d, J = 8.5 Гц), 8.45 (1H, dd, J = 9.0, 2.7 Гц), 9.02 (1H, d, J = 2.4 Гц). Наступні сполуки одержують практично таким самим чином, як у Посилальному прикладі 3, застосовуючи відповідні вихідні матеріали. Посилальний приклад 4 трет-Бутил {3-фтор-4-[(5-нітропіридин-2-іл)окси]феніл}метилкарбамат 1 H-ЯМР (CDCl3) : 1.49 (9H, s), 3.30 (3H, s), 7.07-7.24 (4H, m), 8.51 (1H, dd, J = 9.0, 2.7 Гц), 9.01 (1H, d, J = 2.7 Гц). Посилальний приклад 5 Виготовлення трет-бутил метил{3-метил-4-[(5-нітропіридин-2-іл)окси]феніл}карбамату До DMF (50 мл) суспензії NaH (60% у олії, 640 мг) додають трет-бутил {3-метил-4-[(5нітропіридин-2-іл)окси]феніл}карбамат (5.00 г) при 0°C. Після перемішування при 0°C 10 хвил, додають йодметан (3.08 г) й суміш перемішують 3 годину. Суміш занурюють у крижану воду й екстрагують з AcOEt. Органічний шар промивають з водою, насиченим водним NaCl й сушать над безводним Na2SO4. Розчинник видаляють при зниженому тиску. Осад очищують колонковою хроматографією на силікагелі (n-гептан/AcOEt = 6/1 to 1/1) щоб одержати цільову сполуку (4.35 г) у вигляді білої твердої речовини. 1 H-ЯМР (CDCl3) : 1.48 (9H, s), 2.14 (3H, s), 3.28 (3H, s), 7.01 (1H, dd, J = 9.2, 0.6 Гц), 7.02 (1H, d, J = 8.5 Гц), 7.15 (1H, dd, J = 8.5, 2.4 Гц), 7.18-7.23 (1H, br m), 8.47 (1H, dd, J = 9.2, 2.8 Гц), 9.04 (1H, dd, J = 2.7, 0.5 Гц). Посилальний приклад 6 Виготовлення трет-бутил метил {4-[(5-нітропіридин-2-іл)окси]феніл}карбамату До THF (30 мл) суспензії NaH (60% у олії, 1.22 г) додають трет-бутил {4-[(5-нітропіридин-2іл)окси]феніл}карбамат (7.77 г) при 0°C. Після перемішування при 0°C 10 хвил, додають йодметан (4.33 г) й суміш перемішують при кімнітній температурі 3 години. Суміш занурюють у крижану воду й екстрагують з AcOEt. Органічний шар промивають з водою, насиченим водним NaCl й сушать над безводним Na2SO4. Розчинник видаляють при зниженому тиску. Осад очищують колонковою хроматографією на силікагелі (n-гексан/AcOEt = 2/1) щоб одержати цільову сполуку (6.30 г) у вигляді блідо-жовтої речовини. 1 H-ЯМР (CDCl3) : 1.48 (9H, s), 3.30 (3H, s), 7.03 (1H, dd, J = 9.0, 0.5 Гц), 7.11-7.13 (2H, m), 7.31-7.34 (2H, m), 8.48 (1H, dd, J = 9.0, 2.7 Гц), 9.05 (1H, d, J = 2.7 Гц). Посилальний приклад 7 Виготовлення трет-бутил {4-[(5-амінопіридин-2-іл)окси]-3-метоксифеніл}метилкарбамату Суміш трет-бутил {3-метокси-4-[(5-нітропіридин-2-іл)окси]феніл}метилкарбамату (4.80 г) й паладію на вуглеці (5% мас., 1.36 г) у EtOH (100 мл) перемішують при 40°C 2 години у атмосфері водню. Суміш фільтрують крізь пластину целіту й фільтрат концентрують при зниженому тиску. Осад очищують колонковою хроматографією на силікагелі (n-гексан/AcOEt = 3/2 to 3/7) щоб одержати цільову сполуку (3.58 г) у вигляді жовтої олії. 1 H-ЯМР (CDCl3) : 1.46 (9H, s), 3.26 (3H, s), 3.46 (2H, brs), 3.77 (3H, s), 6.73-6.82 (2H, m), 6.886.93 (1H, m), 7.00 (1H, d, J = 8.3 Гц), 7.07 (1H, dd, J = 8.5, 2.9 Гц),7.66 (1H, d, J = 2.9 Гц). Посилальний приклад 8 Виготовлення трет-бутил {4-[(5-амінопіридин-2-іл)окси]-3-метилфеніл}метилкарбамату Суміш трет-бутил метил{3-метил-4-[(5-нітропіридин-2-іл)окси]феніл}карбамату (4.35 г) й паладію на вуглеці (10% мас., 620 мг) у AcOEt (80 мл) перемішують при 45°C 3 години у атмосфері водню. Суміш фільтрують крізь пластину целіту й фільтрат концентрують при 11 UA 110037 C2 5 10 15 20 25 30 35 40 45 50 55 60 зниженому тиску. Осад очищують колонковою хроматографією на силікагелі (n-гептан/AcOEt = 1/1 to 3/7) щоб одержати цільову сполуку (3.55 г) у вигляді білої твердої речовини. 1 H-ЯМР (CDCl3) : 1.46 (9H, s), 2.19 (3H, s), 3.24 (3H, s), 3.52 (2H, brs), 6.68 (1H, d, J = 8.5 Гц), 6.90 (1H, d, J = 8.8 Гц), 7.02 (1H, dd, J = 8.5, 2.4 Гц), 7.05 (1H, dd, J = 8.5, 2.9 Гц), 7.08-7.13 (1H, br m), 7.68 (1H, d, J = 2.9 Гц). Посилальний приклад 9 Виготовлення трет-бутил {4-[(5-амінопіридин-2-іл)окси]феніл}метилкарбамату Суміш трет-бутил метил{4-[(5-нітропіридин-2-іл)окси]феніл}карбамату (3.28 г) й паладій на вуглеці (10% мас., 328 мг) у EtOH (30 мл) перемішують при 50°C 4 годин у атмосфері водню. Суміш фільтрують крізь пластину целіту й фільтрат концентрують при зниженому тиску. Осад очищують колонковою хроматографією на силікагелі (n-гексан/AcOEt = 2/1) щоб одержати цільову сполуку (2.79 г) у вигляді блідо-жовтої речовини. 1 H-ЯМР (CDCl3) : 1.44 (9H, s), 3.24 (3H, s), 3.54 (2H, brs), 6.76 (1H, d, J = 8.5 Гц), 6.99-7.02 (2H, m), 7.08 (1H, dd, J = 8.5, 2.9 Гц), 7.17-7.19 (2H, m), 7.72 (1H, d, J = 2.9 Гц). Посилальний приклад 10 Виготовлення трет-бутил {4-[(5-амінопіридин-2-іл)окси]-3-фторфеніл}метилкарбамату Розчин трет-бутил {3-фтор-4-[(5-нітропіридин-2-іл)окси]феніл}метилкарбамату (2.79 г) у EtOH (57 мл) продувають з аргоном потім обробляють з платиною на вуглеці (5% мас.%, підтримка - активований вуглець, вологий, тип Degussa F101 ra/w) (0.6 г). Реакційну суміш потім поміщають у H2 атмосферу й ретельно перемішують при 40°C 2 год. Реакційну суміші фільтрують крізь пластину целіту, фільтрат концентрують при зниженому тиску, щоб одержати цільову сполуку у вигляді білого порошку (2.59 г). 1 H-ЯМР (CDCl3) : 1.45 (9H, s), 3.25 (3H, s), 3.48 (2H, brs), 6.82 (1H, d, J = 8.7 Гц), 6.98-7.03 (1H, m), 7.07-7.15 (3H, m), 7.64 (1H, dd, J = 3.1, 0.6 Гц). Посилальний приклад 11 Виготовлення трет-бутил [3-фтор-4-({5-[(4-феноксибензоїл)аміно]піридин-2іл}окси)феніл]метилкарбамату До AcOEt (12 мл) розчину трет-бутил {4-[(5-амінопіридин-2-іл)окси]-3фторфеніл}метилкарбамату (0.5 г) й триетиламіну (0.36 мл) додають AcOEt (5 мл) розчину 4феноксибензоїл хлориду (390 мг) при 0°C, потім одержану суміш перемішують при 0°C 10 хвил. Одержану тверду частку розділяють й промивають H2O й Et2O даючи на виході цільову сполуку у вигляді білого порошку (0.53 г). 1 H-ЯМР (CDCl3) : 1.48 (9H, s), 3.27 (3H, s), 7.01 (1H, d, J = 8.8 Гц), 7.03-7.23 (6H, m), 7.05 (2H, d, J = 8.8 Гц), 7.36-7.43 (2H, m), 7.77 (1H, s), 7.84 (2H, d, J = 8.8 Гц), 8.19 (1H, d, J = 2.2 Гц), 8.22 (1H, dd, J = 8.7, 2.8 Гц). Наступні сполуки одержують по суті таким чином, як у Посилальному прикладі 11, застосовуючи відповідні вихідні матеріали. Посилальний приклад 12 трет-Бутил [4-({5-[(біфеніл-4-ілкарбоніл)аміно]піридин-2-іл}окси)-3фторфеніл]метилкарбамат 1 H-ЯМР (CDCl3) : 1.48 (9H, s), 3.27 (3H, s), 7.03-7.08 (1H, m), 7.03 (1H, d, J = 8.8 Гц), 7.14 (1H, d, J = 11.7 Гц), 7.17 (1H, t, J = 8.7 Гц), 7.38-7.52 (3H, m), 7.61-7.65 (2H, m), 7.72 (2H, d, J = 8.5 Гц), 7.87 (1H, s), 7.95 (2H, d, J = 8.5 Гц), 8.23 (1H, d, J = 2.2 Гц), 8.27 (1H, dd, J = 8.7, 2.8 Гц). Посилальний приклад 13 трет-Бутил {3-фтор-4-[(5-{[4-(трифторметил)бензоїл]аміно}піридин-2іл)окси]феніл}метилкарбамат 1 H-ЯМР (CDCl3) : 1.48 (9H, s), 3.26 (3H, s), 6.96-7.18 (4H, m), 7.73 (2H, d, J = 8.1 Гц), 7.97 (2H, d, J = 8.1 Гц), 8.15 (1H, s), 8.20 (1H, dd, J = 8.9, 2.8 Гц), 8.22 (1H, s). Посилальний приклад 14 трет-Бутил {3-фтор-4-[(5-{[2-фтор-4-(трифторметил)бензоїл]аміно}піридин-2іл)окси]феніл}метилкарбамат 1 H-ЯМР (CDCl3) : 1.48 (9H, s), 3.28 (3H, s), 7.04 (1H, d, J = 9.0 Гц), 7.07 (1H, s), 7.14 (1H, d, J = 10.0 Гц), 7.18 (1H, t, J = 8.7 Гц), 7.49 (1H, d, J = 11.7 Гц), 7.61 (1H, d, J = 8.3 Гц), 8.21 (1H, dd, J = 8.9, 2.8 Гц), 8.27 (1H, d, J = 2.7 Гц), 8.28-8.38 (2H, m). Посилальний приклад 15 трет-Бутил [3-фтор-4-({5-[(2,3,4-трифторбензоїл)аміно]піридин-2іл}окси)феніл]метилкарбамат 1 H-ЯМР (CDCl3) : 1.48 (9H, s), 3.28 (3H, s), 7.03-7.08 (1H, m), 7.03 (1H, d, J = 9.0 Гц), 7.127.21 (3H, m), 7.89-7.99 (1H, m), 8.11-8.18 (1H, m), 8.17 (1H, dd, J = 8.8, 2.7 Гц), 8.25 (1H, d, J = 2.7 Гц). 12 UA 110037 C2 5 10 15 20 25 30 35 40 45 50 55 60 Посилальний приклад 16 трет-Бутил метил[3-метил-4-({5-[(4-феноксибензоїл)аміно]піридин-2-іл}окси)феніл]карбамат 1 H-ЯМР (CDCl3) : 1.47 (9H, s), 2.17 (3H, s), 3.26 (3H, s), 6.88 (1H, dd, J = 8.8, 0.8 Гц), 6.98 (1H, d, J = 8.5 Гц), 7.03-7.09 (5H, m), 7.12-7.16 (1H, br m), 7.18-7.22 (1H, m), 7.37-7.42 (2H, m), 7.847.86 (3H, m), 8.18-8.22 (2H, m). Посилальний приклад 17 трет-Бутил [4-({5-[(біфеніл-4-ілкарбоніл)аміно]піридин-2-іл}окси)-3метилфеніл]метилкарбамат 1 H-ЯМР (CDCl3) : 1.47 (9H, s), 2.17 (3H, s), 3.26 (3H, s), 6.89 (1H, d, J = 9.0 Гц), 6.99 (1H, d, J = 8.5 Гц), 7.08 (1H, dd, J = 8.5, 2.4 Гц), 7.12-7.17 (1H, br m), 7.40-7.42 (1H, m), 7.46-7.50 (2H, m), 7.62-7.64 (2H, m), 7.70-7.72 (2H, m), 7.94-7.97 (2H, m), 7.97-8.00 (1H, br m), 8.22-8.26 (2H, m). Посилальний приклад 18 Виготовлення трет-бутил метил{3-метил-4-[(5-{[4-(трифторметил)бензоїл]аміно} піридин-2іл)окси]феніл}карбамату До розчину AcOEt (15 мл) трет-бутил {4-[(5-амінопіридин-2-іл)окси]-3метилфеніл}метилкарбамату (0.5 г) й Et3N (0.32 мл) повільно додають 4-(трифторметил)бензоїл хлорид(237 мл) при 0°C, потім одержану суміш перемішують при кімнітній температурі 30 хвил. До розчину додають AcOEt (10 мл) й воду (10 мл), суміш екстрагують з AcOEt. Органічний шар промивають з насиченим водним NaHCO3 й насиченим водним NaCl, сушать над безводним Na2SO4, й концентрують при зниженому тиску. Після додавання гексану (20 мл), розчин енергійно перемішують. Одержану тверду частку збирають, одержуючи цільову сполуку (700 мг) у вигляді білої твердої речовини. 1 H-ЯМР (CDCl3) : 1.47 (9H, s), 2.13 (3H, s), 3.24 (3H, s), 6.86 (1H, d, J = 8.8 Гц), 6.95 (1H, d, J = 8.5 Гц), 7.01-7.08 (1H, m), 7.12 (1H, s), 7.73 (2H, d, J = 8.1 Гц), 7.98 (2H, d, J = 7.8 Гц), 8.06-8.31 (1H, br m), 8.17 (1H, d, J = 8.8 Гц), 8.26 (1H, d, J = 2.7 Гц). Наступні сполуки одержують по суті таким чином, як у Посилальному прикладі 18, застосовуючи відповідні вихідні матеріали. Посилальний приклад 19 трет-Бутил {4-[(5-{[2-фтор-4-(трифторметил)бензоїл]аміно}піридин-2-іл)окси]-3метилфеніл}метилкарбамат 1 H-ЯМР (CDCl3) : 1.47 (9H, s), 2.18 (3H, s), 3.27 (3H, s), 6.91 (1H, d, J = 8.8 Гц), 7.00 (1H, d, J = 8.5 Гц), 7.10 (1H, dd, J = 8.5, 2.4 Гц), 7.13-7.19 (1H, br m), 7.49 (1H, d, J = 11.7 Гц), 7.61 (1H, d, J = 8.3 Гц), 8.18 (1H, dd, J = 8.8, 2.8 Гц), 8.29-8.36 (3H, m). Посилальний приклад 20 трет-Бутил метил[4-({5-[(4-феноксибензоїл)аміно]піридин-2-іл}окси)феніл]карбамат 1 H-ЯМР (CDCl3) : 1.46 (9H, s), 3.26 (3H, s), 6.94 (1H, d, J = 8.8 Гц), 7.03-7.09 (6H, m), 7.187.25 (3H, m), 7.37-7.43 (2H, m), 7.84-7.87 (3H, m), 8.21 (1H, dd, J = 8.8, 2.7 Гц), 8.25 (1H, d, J = 2.7 Гц). Посилальний приклад 21 трет-Бутил [4-({5-[(біфеніл-4-ілкарбоніл)аміно]піридин-2-іл}окси)феніл]метилкарбамат 1 H-ЯМР (CDCl3) : 1.46 (9H, s), 3.26 (3H, s), 6.96 (1H, d, J = 8.8 Гц), 7.07-7.10 (2H, m), 7.237.25 (2H, m), 7.40-7.42 (1H, m), 7.46-7.50 (2H, m), 7.62-7.64 (2H, m), 7.71-7.73 (2H, m), 7.95-7.97 (3H, m), 8.26 (1H, dd, J = 8.8, 2.6 Гц), 8.30 (1H, d, J = 2.6 Гц). Приклад 1 Виготовлення N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід трет-Бутил [3-фтор-4-({5-[(4-феноксибензоїл)аміно]піридин-2-іл}окси)феніл]метилкарбамат (0.53 г) розчиняють у TFA (4 мл) й перемішують при кімнатній температурі 5 хвил. Суміш випарюють при зниженому тиску й осад розчиняють у AcOEt. Додають крижаний 5 M NaOH, щоб довести pH до 12, й суміш екстрагують з AcOEt. Органічний шар промивають з водою й насиченим водним NaCl, сушать над безводним MgSO 4, й концентрують при зниженому тиску. Осад розчиняють у Et2O , й розчин перемішують 1 день. Одержану тверду частку збирають й промивають Et2O, даючи на виході цільову сполуку у вигляді білого порошку (0.29 г). 1 H-ЯМР (CDCl3) : 2.83 (3H, s), 3.78 (1H, brs), 6.35-6.44 (2H, m), 6.96 (1H, d, J = 9.3 Гц), 6.997.09 (5H, m), 7.17-7.22 (1H, m), 7.36-7.43 (2H, m), 7.68 (1H, s), 7.84 (2H, d, J = 8.9 Гц), 8.16-8.23 (2H, m). Наступні сполуки одержують по суті таким чином, як у Прикладі 1, застосовуючи відповідні вихідні матеріали. Приклад 2 N-{6-[2-Фтор-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід mp: 190.0-190.5°C (дек.) 13 UA 110037 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 3 N-{6-[2-Фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід 1 H-ЯМР (CDCl3) : 2.82 (3H, s), 6.32-6.46 (2H, m), 6.91-7.06 (2H, m), 7.74 (2H, d, J = 8.1 Гц), 7.89 (1H, s), 7.97 (2H, d, J = 8.1 Гц), 8.19 (1H, dd, J = 8.7, 2.7 Гц), 8.20 (1H, s). Приклад 4 2-Фтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід 1 H-ЯМР (CDCl3) : 2.83 (3H, d, J = 5.1 Гц), 3.80 (1H, d, J = 4.9 Гц), 6.36-6.46 (2H, m), 6.98 (1H, d, J = 8.8 Гц), 7.03 (1H, t, J = 8.7 Гц), 7.49 (1H, d, J = 11.7 Гц), 7.60 (1H, d, J = 7.3 Гц), 8.17 (1H, dd, J = 8.8, 2.7 Гц), 8.26 (1H, d, J = 2.4 Гц), 8.27-8.35 (2H, m). Приклад 5 2,3,4-Трифтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}бензамід 1 H-ЯМР (CDCl3) : 2.83 (3H, s), 3.81 (1H, brs), 6.35-6.45 (2H, m), 6.97 (1H, d, J = 9.0 Гц), 7.03 (1H, t, J = 8.7 Гц), 7.10-7.19 (1H, m), 7.88-7.98 (1H, m), 8.12 (1H, brs), 8.13 (1H, dd, J = 8.8, 2.7 Гц), 8.24 (1H, d, J = 2.7 Гц). Приклад 6 N-{6-[2-Метил-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід 1 H-ЯМР (CDCl3) : 2.10 (3H, s), 2.83 (3H, s), 3.63 (1H, brs), 6.47 (1H, dd, J = 8.5, 2.7 Гц), -6.50 (1H, d, J = 2.4 Гц ), 6.82 (1H, d, J = 8.8 Гц), 6.89 (1H, d, J = 8.5 Гц), 7.03-7.08 (4H, m), 7.17-7.22 (1H, m), 7.38-7.41 (2H, m), 7.79 (1H, brs), 7.83-7.85 (2H, m), 8.15 (1H, dd, J = 8.8, 2.8 Гц), 8.18 (1H, d, J = 2.4 Гц). Приклад 7 N-{6-[2-Метил-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід 1 H-ЯМР (CDCl3) : 2.11 (3H, s), 2.83 (3H, s), 3.63 (1H, brs), 6.47 (1H, dd, J = 8.4, 2.8 Гц), 6.50 (1H, d, J = 2.8 Гц), 6.83 (1H, d, J = 8.8 Гц), 6.90 (1H, d, J = 8.4 Гц), 7.39-7.41 (1H, m), 7.46-7.49 (2H, m), 7.61-7.64 (2H, m), 7.69-7.71 (2H, m), 7.91 (1H, brs), 7.92-7.95 (2H, m), 8.19 (1H, dd, J = 8.8, 2.8 Гц), 8.22 (1H, d, J = 2.4 Гц). Приклад 8 N-{6-[2-Метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід Виготовлення N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4(трифторметил)бензаміду До розчину трет-бутил метил{3-метил-4-[(5-{[4-(трифторметил)бензоїл] аміно}піридин-2іл)окси]феніл}карбамату (0.60 г) у CH2Cl2 (1 мл) додають TFA (3.32 мл) трьома порціями при 0°C. Після перемішування при 0°C 30 хвил, суміш випарюють при зниженому тиску й осад розчиняють у AcOEt. Додають крижаний 2 M NaOH (10 мл), суміш екстрагують з AcOEt. Органічний шар промивають з водою й насиченим водним NaCl, сушать над безводним Na 2SO4, й концентрують при зниженому тиску. Після додавання Et2O (20 мл), розчин енергійно перемішують. Одержану тверду частку збирають й тверду частку рекристалізують від Et2O/AcOEt/Гексан, щоб одержати цільову сполуку (0.44 г) у вигляді білого порошку. 1 H-ЯМР (CDCl3) : 2.09 (3H, s), 2.83 (3H, s), 3.64 (1H, s), 6.46 (1H, dd, J = 8.5, 2.9 Гц), 6.49 (1H, d,J = 2.9 Гц), 6.83 (1H, d, J = 9.0 Гц), 6.88 (1H, d, J = 8.5 Гц), 7.74 (2H, d, J = 8.1 Гц), 7.92-8.01 (3H, m), 8.14 (1H, dd, J = 8.9, 2.8 Гц), 8.21 (1H, d, J = 2.7 Гц). Наступні сполуки одержують по суті таким чином, як у Прикладі 8, застосовуючи відповідні вихідні матеріали. Приклад 9 2-Фтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід 1 H-ЯМР (CDCl3) : 2.11 (3H, s), 2.84 (3H, s), 3.65 (1H, brs), 6.48 (1H, dd, J = 8.4, 2.8 Гц), 6.51 (1H, d, J = 2.4 Гц), 6.84 (1H, d, J = 8.8 Гц), 6.90 (1H, d, J = 8.4 Гц), 7.48 (1H, d, J = 11.7 Гц), 7.60 (1H, d, J = 8.1 Гц), 8.13 (1H, dd, J = 8.8, 2.8 Гц), 8.27 -8.34 (3H, m). Приклад 10 N-{6-[4-(Метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід 1 H-ЯМР (CDCl3) : 2.84 (3H, s), 6.61-6.64 (2H, m), 6.86 (1H, d, J = 8.8 Гц), 6.96-6.99 (2H, m), 7.03-7.07 (4H, m), 7.18-7.21 (1H, m), 7.38-7.41 (2H, m), 7.80 (1H, brs), 7.83-7.85 (2H, m), 8.15 (1H, dd, J = 8.8, 2.8 Гц), 8.20 (1H, d, J = 2.8 Гц). Приклад 11 N-{6-[4-(Метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід 1 H-ЯМР (CDCl3) : 2.84 (3H, s), 6.62-6.64 (2H, m), 6.87 (1H, d, J = 8.8 Гц), 6.98-6.99 (2H, m), 7.40-7.41 (1H, m), 7.46-7.49 (2H, m), 7.61-7.64 (2H, m), 7.69-7.71 (2H, m), 7.90 (1H, brs), 7.93-7.95 (2H, m), 8.19 (1H, dd, J = 8.8, 2.6 Гц), 8.24 (1H, d, J = 2.6 Гц). Приклад 12 Виготовлення N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4 14 UA 110037 C2 5 10 15 20 25 30 35 40 45 50 55 60 (трифторметил)бензаміду До розчину AcOEt (10 мл) трет-бутил {4-[(5-амінопіридин-2-іл)окси]-3метоксифеніл}метилкарбамату (0.60 г) й триетиламіну (0.26 г) додають 4(трифторметил)бензоїл хлорид (0.38 г) при 0°C. Суміш перемішують при кімнітній температурі 1 годину. Суміш занурюють у воду й екстрагують з AcOEt. Органічний шар промивають з водою, насиченим водним NaCl, сушать над безводним Na2SO4 й концентрують при зниженому тиску. Осад очищують колонковою хроматографією (n-гексан/AcOEt = 9/1 до 7/3) даючи на виході жовтий аморфний порошок. Порошок розчиняють у CH2Cl2 (10 мл), потім додають TFA (1 мл). Суміш перемішують при кімнатній температурі 2 години. Після видалення розчинника при зниженому тиску, осад занурюють into насиченим водним NaHCO 3 й екстрагують з AcOEt. Органічний шар промивають з водою, насиченим водним NaCl, сушать над безводним Na 2SO4 й концентрують при зниженому тиску. Осад очищують колонковою хроматографією на силікагелі (n-гексан/AcOEt = 7/3 до 3/7), щоб одержати цільову сполуку (0.42 г) у вигляді безбарвної олії. 1 H-ЯМР (CDCl3) : 2.84 (3H, s), 3.73 (3H, s), 6.20 (1H, dd, J = 8.5, 2.7 Гц), 6.25 (1H, d, J = 2.7 Гц), 6.89 (1H, d, J = 8.8 Гц), 6.95 (1H, d, J = 8.3 Гц), 7.74 (2H, d, J = 8.3 Гц), 7.94-8.02 (3H, m), 8.118.22 (2H, m). Наступні сполуки одержують по суті таким чином, як у Прикладі 12, використовуючи відповідні вихідні матеріали. Приклад 13 N-{6-[2-Метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід 1 H-ЯМР (CDCl3) : 2.84 (3H, s), 3.73 (3H, s), 3.74 (1H, s), 6.18-6.27 (2H, m), 6.88 (1H, d, J = 8.8 Гц), 6.94-6.98 (1H, m), 7.01-7.09 (4H, m), 7.17-7.22 (1H, m), 7.36-7.43 (2H, m), 7.72-7.87 (3H, m), 8.11-8.18 (2H, m). Приклад 14 N-{6-[2-Метокси-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід mp: 161.4-161.8°C Приклад 15 2-Фтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід 1 H-ЯМР (CDCl3) : 2.86 (3H, s), 3.65-3.85 (1H, brm), 3.75 (3H, s), 6.22 (1H, dd, J = 8.5, 2.7 Гц), 6.28 (1H, d, J = 2.4 Гц), 6.90 (1H, d, J = 8.8 Гц), 6.97 (1H, d, J =8.5 Гц), 7.48 (1H, d, J = 11.7 Гц), 7.60 (1H, d, J = 8.1 Гц), 8.12 (1H, dd, J = 8.8, 2.7 Гц), 8.24-8.35 (3H, m). Приклад 16 2,3,4-Трифтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}бензамід 1 H-ЯМР (CDCl3) : 2.86 (3H, s), 3.68-3.78 (4H, m), 6.22 (1H, dd, J = 8.5, 2.7 Гц), 6.27 (1H, d, J = 2.4 Гц), 6.90 (1H, d, J = 8.8 Гц), 6.97 (1H, d, J = 8.5 Гц), 7.10-7.19 (1H, m), 7.89-7.97 (1H, m), 8.068.16 (2H, m), 8.24 (1H, d, J = 2.7 Гц). Приклад 17 2,3,4-Трифтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}бензамід 1 H-ЯМР (CDCl3) : 2.11 (3H, s), 2.83 (3H, s), 3.57-3.72 (1H, m), 6.48 (1H, dd, J = 8.5, 2.9 Гц), 6.51 (1H, d, J = 2.9 Гц), 6.83 (1H, d, J = 8.8 Гц), 6.90 (1H, d, J = 8.5 Гц), 7.10-7.19 (1H, m), 7.87-7.96 (1H, m), 8.07-8.12 (1H, m), 8.12-8.21 (1H, m), 8.23-8.28 (1H, m). Приклад 18 N-{6-[4-(Метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід 1 H-ЯМР (CDCl3) : 2.84 (3H, s), 6.61-6.63 (2H, m), 6.87 (1H, d, J = 8.8 Гц), 6.94-6.97 (2H, m), 7.73-7.75 (2H, m), 7.97-7.99 (2H, m), 8.04 (1H, brs), 8.14 (1H, dd, J = 8.8, 2.6 Гц), 8.23 (1H, d, J = 2.6 Гц). Приклад 19 2-Фтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід 1 H-ЯМР (CDCl3) : 2.85 (3H, s), 3.70 (1H, brs), 6.63-6.65 (2H, m), 6.88 (1H, d, J = 8.8 Гц), 6.987.00 (2H, m), 7.49 (1H, d, J = 12.0 Гц), 7.60 (1H, dd, J = 8.3, 1.0 Гц), 8.14 (1H, dd, J = 8.8, 2.8 Гц), 8.28-8.34 (3H, m). Приклад 20 2,3,4-Трифтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}бензамід Виготовлення 2,3,4-трифтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}бензаміду До розчину AcOEt (10 мл) трет-бутил {4-[(5-амінопіридин-2-іл)окси]феніл}метилкарбамату (0.50 г) й триетиламіну (0.32 г) додають 2,3,4-трифторбензоїл хлорид (0.37 г) при 0°C. Суміш перемішують при кімнатній температурі 1 годину. Суміш занурюють у воду й екстрагують з AcOEt. Органічний шар промивають з водою, насиченим водним NaCl, сушать над безводним Na2SO4 й концентрують при зниженому тиску. Осад розчиняють у CH2Cl2 (10 мл), потім додають TFA (3 мл). Після перемішування при кімнатній температурі 2 години, суміш занурюють into 15 UA 110037 C2 5 10 15 20 25 30 35 40 45 50 55 60 насиченим водним NaHCO3 й екстрагують з AcOEt. Органічний шар промивають з водою, насиченим водним NaCl, сушать над безводним Na2SO4 й концентрують при зниженому тиску. Осад очищують колонковою хроматографією на силікагелі (n-гексан/AcOEt = 2/1) щоб одержати цільову сполуку (0.55 г) у вигляді білої твердої речовини. 1 H-ЯМР (CDCl3) : 2.84 (3H, s), 3.71 (1H, brs), 6.62-6.65 (2H, m), 6.87 (1H, d, J = 8.8 Гц), 6.976.99 (2H, m), 7.11-7.18 (1H, m), 7.89-7.95 (1H, m), 8.10 (1H, dd, J = 8.8, 2.7 Гц), 8.14-8.17 (1H, br m), 8.27 (1H, d, J = 2.7 Гц). Приклад 21 Виготовлення N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід гідрохлориду До EtOH (7 мл) розчину N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4феноксибензаміду (0.34 г) додають 6 M HCl (0.14 мл) при 0°C. Одержану суміш перемішують при 0°C. Одержану тверду частку рекристалізують із EtOH/H 2O даючи на виході цільову сполуку у вигляді білого порошку (0.28 г). 1 H-ЯМР (DMSO-d6) : 2.76 (3H, s), 6.60-6.69 (1H, m), 6.70-6.80 (1H, m), 7.06 (1H, d, J = 8.8 Гц), 7.08-7.17 (5H, m), 7.20-7.26 (1H, m), 7.43-7.49 (2H, m), 8.01 (2H, d, J = 9.4 Гц), 8.18 (1H, dd, J = 8.8, 2.7 Гц), 8.41 (1H, d, J = 2.2 Гц), 10.35 (1H, s). Наступні сполуки одержують по суті таким чином, як у Прикладі 21, використовуючи відповідні вихідні матеріали. Приклад 22 2-Фтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлорид 1 H-ЯМР (DMSO-d6) : 2.77 (3H, s), 6.66-6.76 (1H, m), 6.77-6.88 (1H, m), 7.10 (1H, d, J = 9.0 Гц), 7.17 (1H, t, J = 8.9 Гц), 7.75 (1H, d, J = 8.3 Гц), 7.87-7.95 (2H, m), 8.17 (1H, dd, J = 9.0, 2.7 Гц), 8.38 (1H, d, J = 2.4 Гц), 10.78 (1H, s). Приклад 23 2,3,4-Трифтор-N-{6-[2-фтор-4-(метиламіно)фенокси]піридин-3-іл}бензамід гідрохлорид 1 H-ЯМР (DMSO-d6) : 2.78 (3H, s), 6.70-6.81 (1H, m), 6.82-6.94 (1H, m), 7.10 (1H, d, J = 9.0 Гц), 7.19 (1H, t, J = 8.8 Гц), 7.44-7.54 (1H, m), 7.56-7.65 (1H, m), 8.16 (1H, dd, J = 8.8, 2.7 Гц), 8.37 (1H, d, J = 2.4 Гц), 10.70 (1H, s). Приклад 24 Виготовлення N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлориду До розчину EtOH (3 мл) N-{6-[2-Метил-4-(метиламіно)фенокси]піридин-3-іл}-4(трифторметил)бензаміду (0.30 г) додають 6 M водний HCl (0.13 мл) при 0°C. Одержану суміш перемішують при 0°C. Одержану тверду частку рекристалізують із EtOH/H 2O, даючи цільову сполуку у вигляді білого порошку (0.20 г). 1 H-ЯМР (DMSO-d6) : 2.14 (3H, s), 2.91 (3H, s), 7.11 (1H, d, J = 9.0 Гц), 7.17 (1H, d, J = 8.5 Гц), 7.32 (1H, dd, J = 8.5, 2.4 Гц), 7.36-7.43 (1H, m), 7.93 (2H, d, J = 8.3 Гц), 8.19 (2H, d, J = 8.1 Гц), 8.25 (1H, dd, J = 8.9, 2.8 Гц), 8.48 (1H, d, J = 2.4 Гц), 10.71 (1H, s). Наступні сполуки одержують по суті таким чином, як у Прикладі 24, використовуючи відповідні вихідні матеріали. Приклад 25 2,3,4-Трифтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}бензамід гідрохлорид mp: 222.9-225.4°C (dec.) Приклад 26 N-{6-[2-Метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід гідрохлорид mp: 202.2-202.3°C Приклад 27 N-{6-[2-Метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлорид mp: 217.6-218.2°C Приклад 28 2-Фтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлорид mp: 197.0-198.1°C Приклад 29 2,3,4-Трифтор-N-{6-[2-метокси-4-(метиламіно)фенокси]піридин-3-іл}бензамід гідрохлорид mp: 207.1-209.8°C Приклад 30 16 UA 110037 C2 5 10 15 20 25 30 35 40 45 50 55 60 N-{6-[4-(Метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлорид 1 H-ЯМР (DMSO-d6) : 2.90 (3H, s), 7.12 (1H, d, J = 8.8 Гц), 7.23-7.24 (2H, m), 7.42-7.44 (2H, m), 7.92-7.94 (2H, m), 8.18-8.20 (2H, m), 8.26 (1H, dd, J = 8.8, 2.6 Гц), 8.54 (1H, d, J = 2.6 Гц), 10.73 (1H, s). Приклад 31 2-Фтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлорид 1 H-ЯМР (DMSO-d6) : 2.89 (3H, s), 7.11 (1H, d, J = 8.8 Гц), 7.20-7.22 (2H, m), 7.37-7.39 (2H, m), 7.75 (1H, d, J = 8.1 Гц), 7.90-7.94 (2H, m), 8.20 (1H, dd, J = 8.8, 2.6 Гц), 8.46 (1H, d, J = 2.6 Гц), 10.83 (1H, s). Приклад 32 Виготовлення 2,3,4-трифтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}бензамід гідрохлориду (1:1) До розчину EtOH (10 мл) 2,3,4-трифтор-N-{6-[4-(метиламіно)фенокси]піридин-3-іл}бензаміду (0.55 г) додають 6 M HCl (0.27 мл) при кімнатній температурі. Одержану суміш перемішують при кімнітній температурі. Одержану тверду частку збирають фільтрацією, даючи на виході цільову сполуку у вигляді білого порошку (0.35 г). 1 H-ЯМР (DMSO-d6) : 2.89 (3H, s), 7.11 (1H, d, J = 8.8 Гц), 7.20-7.23 (2H, m), 7.38-7.40 (2H, m), 7.47-7.52 (1H, m), 7.58-7.64 (1H, m), 8.18 (1H, dd, J = 8.8, 2.7 Гц), 8.45 (1H, d, J = 2.7 Гц), 10.75 (1H, s). Наступні сполуки може бути одержана по суті таким чином, як у Прикладі 21, використовуючи відповідні вихідні матеріали. Приклад 33 N-{6-[2-Фтор-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід гідрохлорид Приклад 34 N-{6-[2-Фтор-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлорид Приклад 35 N-{6-[2-Метил-4-(метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід гідрохлорид Приклад 36 N-{6-[2-Метил-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід гідрохлорид Приклад 37 2-Фтор-N-{6-[2-метил-4-(метиламіно)фенокси]піридин-3-іл}-4-(трифторметил)бензамід гідрохлорид Приклад 38 N-{6-[4-(Метиламіно)фенокси]піридин-3-іл}-4-феноксибензамід гідрохлорид Приклад 39 N-{6-[4-(Метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід гідрохлорид Приклад 40 N-{6-[2-Метокси-4-(метиламіно)фенокси]піридин-3-іл}біфеніл-4-карбоксамід гідрохлорид Фармаколгічний тест Антипроліферативний ефект на ракові клітини (in vitro) Пригнічення росту людських ракових клітин печінки (HuH-7) визначають за допомогою способу сульфородаміну B, основаного на способі Skehan P. et al. (J Natl Cancer Inst. 1990 Jul 4; 82(13): 1107-12). У цьому дослідженні,HuH-7 клітини просіюють на DMEM середовищі, що містить 10% ембріональну бичачу сироватку у 96-чарунковій мікротарілці. Після 24-годинної інкубації при 37°C у присутності 5% диоксиду вуглецю, додають тестову сполуку й клітини інкубують іще 5 днів. Після інкубації, додають розчин трихлороцтової кислоти, щоб одержати кінцеву концентрацію 10% й клітинам дають відстоятися при 4°C 1 годину. Потім, клітини промивають з водою, щоб видалити середовище й трихлороцтову кислоту й сушать на повітрі. Висушені клітини зберігають при 4°C доки вони будуть протравлені сульфородаміном B. До кожної чарунки, додають 1% розчин оцтової кислоти, що містить 0.4% сульфородамін B й дають відстоятися від 20 до 30 хвилин при кімнатній температурі. Після видалення речовини, що сплила на поверхню, кожну чарунку промивають з 1% розчином оцтової кислоти, й додають 10 мМ розчин трис (трис-(гідроксиметил)амінометан) у процесі перемішування, щоб елюювати барву, прийняту клітинами. Потім, визначають оптичну щільність вимірюванням довжини хвилі 492 нм й довідкову довжину хвилі 690 нм, й обчислюють різницю. Активність росту клітин у кожній чарунці обчислюють як величину, визначену відніманням OD у контрольній чарунці, що не містить клітин (різниця у поглинанні між 492 нм й 690 нм), від величини у тестовій чарунці. 50% пригнічуючу концентрацію (IC50 (nM)) тестової сполуки визначають порівнянням активності росту клітин у чарунці,щомістить тестову сполуку, з контрольною, що не містить тестову сполуку. 17 UA 110037 C2 Результати наведені у Таблиці 2. Таблиця 2 Тестова сполука Сполука за Прикладом 2 Сполука за Прикладом 3 Сполука за Прикладом 6 Сполука за Прикладом 7 Сполука за Прикладом 9 Сполука за Прикладом 10 Сполука за Прикладом 11 Сполука за Прикладом 14 Сполука за Прикладом 21 Сполука за Прикладом 22 Сполука за Прикладом 23 Сполука за Прикладом 24 Сполука за Прикладом 25 Сполука за Прикладом 26 Сполука за Прикладом 27 Сполука за Прикладом 28 Сполука за Прикладом 30 Сполука за Прикладом 31 5 10 Тест метаболічної стабільності у мікротомах печінки У цьому дослідженні, 222.5 мкл за 0.22 мг/мл мікросом печінки розподіляють до кожної пробірки, й туди додають 2.5 мкл за 100 мкМ тестової сполуки . Потім, 22.5 мкл цієї суміші порозчиняють у 500 мкл за ацетoнітрилу, збагаченого IS як зразок 0 мін , й осад пре-інкубують при 37°C 5 хвил. Реакцію розпочинають додаванням 22.5 мкл 10 мМ NADH/NADPH, й після 10 й 20 хвил, 25 мкл реакційної суміші розділяють до 500 мкл збагаченим IS ацетoнітрилом. Зразки центрифугують (5700 об/хвил, 4°C, 10 хвил), й речовину, що сплила на поверхню, аналізують за допомогою LC/MS/MS. Обчислюють відхилення лінійної регресії від залишкового процентного відношення логарифму у порівнянні з співвідношенням часу інкубації (-ke), й обчислюють власний кліренс (CLint) за допомогою наступного рівняння. CL int k e 15 IC50(nM) 108.0 154.8 78.5 77.6 70.4 319.7 310.9 247.6 136.0 162.7 752.6 72.3 484.7 274.9 303.8 292.9 274.7 327.0 мклінкубація мг мікросоми/ г печінки мг мікросоми г печінки/кг ваги тіла Результати наведені у Таблиці 3. Таблиця 3 Тестова сполука Сполука за Прикладом 2 Сполука за Прикладом 3 Сполука за Прикладом 6 Сполука за Прикладом 7 Сполука за Прикладом 9 Сполука за Прикладом 14 Сполука за Прикладом 22 Сполука за Прикладом 24 Сполука за Прикладом 25 Сполука за Прикладом 26 Сполука за Прикладом 27 Сполука за Прикладом 28 Сполука за Прикладом 30 Сполука за Прикладом 31 CLint[μL/min/mg]
ДивитисяДодаткова інформація
Назва патенту англійською4-(methylaminophenoxy)pyridine-3-ylbenzamide derivatives for treatment of cancer
Автори англійськоюNakagawa, Takashi, Sakamoto, Makoto, Yamaguchi, Kazuya, Terauchi, Yuki, Shirakura, Masamichi, Harada, Yasuo, Kojima, Yutaka, Sumida, Takumi
Назва патенту російськоюПроизводные 4-(метиламинофенокси)пиридин-3-иллбензамида для лечения рака
Автори російськоюНакагава Такаси, Сакамото Макото, Ямагути Казуя, Тераюти Юки, Сиракура Масамити, Харада Ясуо, Кодзима Ютака, Сумида Такуми
МПК / Мітки
МПК: C07D 213/75, A61K 31/44, A61P 35/00
Мітки: 4-(метиламінофенокси)піридин-3-ілбензаміду, лікування, раку, похідні
Код посилання
<a href="https://ua.patents.su/22-110037-pokhidni-4-metilaminofenoksipiridin-3-ilbenzamidu-dlya-likuvannya-raku.html" target="_blank" rel="follow" title="База патентів України">Похідні 4-(метиламінофенокси)піридин-3-ілбензаміду для лікування раку</a>












