Похідні сульфаматів та сульфамідів для лікування епілепсії та супутніх розладів
Номер патенту: 91680
Опубліковано: 25.08.2010
Автори: Рейтц Ален Б., Паркер Майкл Н., Мар''янофф Брюс Е., МакКомсі Девід Ф.
Формула / Реферат
1. Сполука формули (II)
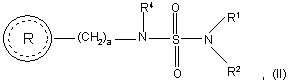
де
R1 та R2 кожний незалежно вибраний з групи, що містить водень та нижчий алкіл;
R4 вибраний з групи, що містить водень та нижчий алкіл;
а означає ціле число від 1 до 2;
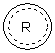 вибраний з групи, що містить
вибраний з групи, що містить
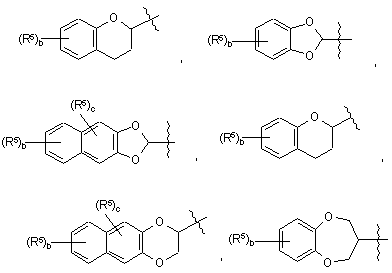 та
та
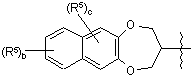 ,
,
де b означає ціле число від 0 до 4; та де с означає ціле число від 0 до 2;
кожний R5 незалежно вибраний з групи, що містить галоген, нижчий алкіл та нітро;
за умови, що, коли означає
означає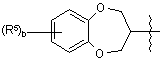 або
або
 , тоді а означає 1;
, тоді а означає 1;
або її фармацевтично прийнятна сіль.
2. Сполука за пунктом 1, де
R1 та R2 кожний незалежно вибраний з групи, що містить водень та нижчий алкіл;
R4 вибраний з групи, що містить водень та нижчий алкіл;
а означає ціле число від 1 до 2;
 вибраний з групи, що містить
вибраний з групи, що містить
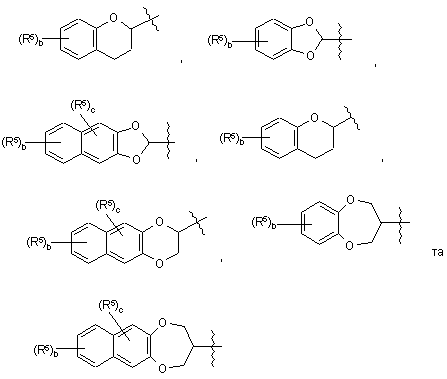 ,
,
де b означає ціле число від 0 до 2; та де с означає ціле число від 0 до 1;
кожний R5 незалежно вибраний з групи, що містить галоген, нижчий алкіл та нітро;
за умови, що, коли означає
означає або
або
 , тоді а означає 1;
, тоді а означає 1;
або її фармацевтично прийнятна сіль.
3. Сполука за пунктом 2, де
R1 та R2 кожний незалежно вибраний з групи, що містить водень та нижчий алкіл;
R4 вибраний з групи, що містить водень та нижчий алкіл;
а означає ціле число від 1 до 2;
 вибраний з групи, що містить
вибраний з групи, що містить
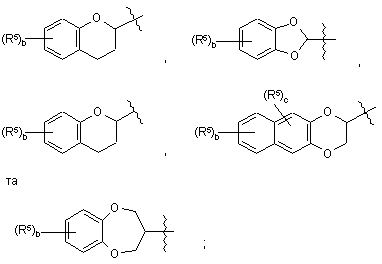
де b означає ціле число від 0 до 2; та де с означає 0;
кожний R5 незалежно вибраний з групи, що містить галоген, нижчий алкіл та нітро;
за умови, що, коли означає
означає , тоді а означає 1;
, тоді а означає 1;
або її фармацевтично прийнятна сіль.
4. Сполука за пунктом 3, де
R1 та R2 кожний незалежно вибраний з групи, що містить водень та нижчий алкіл;
R4 вибраний з групи, що містить водень та метил;
а означає ціле число від 1 до 2;
 вибраний з групи, що містить 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(бензо[1,3]діоксоліл), 3-(3,4-дигідро-2Н-бензо[1,4]діоксепініл), 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-фтор-2,3-дигідробензо[1,4]діоксиніл), 2-(хроманіл), 2-(5-фтор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлорбензо[1,3]діоксоліл), 2-(7-нітро-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(5-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл), 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл), 2-(8-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(2,3-дигідронафто[2,3-b][1,4]діоксиніл) та 2-(4-метилбензо[1,3]діоксоліл);
вибраний з групи, що містить 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(бензо[1,3]діоксоліл), 3-(3,4-дигідро-2Н-бензо[1,4]діоксепініл), 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-фтор-2,3-дигідробензо[1,4]діоксиніл), 2-(хроманіл), 2-(5-фтор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлорбензо[1,3]діоксоліл), 2-(7-нітро-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(5-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл), 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл), 2-(8-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(2,3-дигідронафто[2,3-b][1,4]діоксиніл) та 2-(4-метилбензо[1,3]діоксоліл);
за умови, що, коли  означає 3-(3,4-дигідро-2Н-бензо[1,4]діоксепініл), тоді а означає 1;
означає 3-(3,4-дигідро-2Н-бензо[1,4]діоксепініл), тоді а означає 1;
або її фармацевтично прийнятна сіль.
5. Сполука за пунктом 4, де
R1 та R2 кожний незалежно вибраний з групи, що містить водень та метил;
R4 вибраний з групи, що містить водень та метил;
а означає ціле число від 1 до 2;
 вибраний з групи, що містить 2-(бензо[1,3]діоксоліл), 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл) та 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл);
вибраний з групи, що містить 2-(бензо[1,3]діоксоліл), 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл) та 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл);
або її фармацевтично прийнятна сіль.
6. Сполука N-[(6-хлор-2,3-дигідро-1,4-бензодіоксин-2-іл)метил]-сульфамід та її фармацевтично прийнятні солі.
7. Сполука, представлена формулою
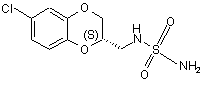 ,
,
та її фармацевтично прийнятні солі.
8. Сполука формули (III)
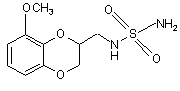 (III)
(III)
або її фармацевтично прийнятна сіль.
9. Фармацевтична композиція, що містить фармацевтично прийнятний носій та сполуку за пунктом 1.
10. Фармацевтична композиція, одержана за допомогою змішування сполуки за пунктом 1 з фармацевтично прийнятним носієм.
11. Спосіб одержання фармацевтичної композиції, в якому змішують сполуку за пунктом 1 з фармацевтично прийнятним носієм.
12. Спосіб лікування епілепсії або супутнього розладу у суб'єкта, що цього потребує, в якому вводять суб'єкту терапевтично ефективну кількість сполуки за пунктом 1.
13. Спосіб лікування епілепсії у суб'єкта, що цього потребує, в якому вводять суб'єкту терапевтично ефективну кількість сполуки за пунктом 1.
14. Спосіб за пунктом 12, де розлад вибраний з есенціального тремору або синдрому тремтіння кінцівок.
15. Застосування сполуки за пунктом 1 для виготовлення лікарського засобу для лікування епілепсії або супутнього розладу у суб'єкта, що цього потребує.
Текст
1. Сполука формули (II) R4 O R1 , 3 91680 або її фармацевтично прийнятна сіль. 2. Сполука за пунктом 1, де (R5)b R1 та R2 кожний незалежно вибраний з групи, що містить водень та нижчий алкіл; R4 вибраний з групи, що містить водень та нижчий алкіл; а означає ціле число від 1 до 2; (R5) 4 O O (R5)b O , (R5)c O O (R5)b b , R вибраний з групи, що містить , O та O O O (R5)b (R5)b (R5)b O , (R5)c де b означає ціле число від 0 до 2; та де с означає 0; кожний R5 незалежно вибраний з групи, що містить галоген, нижчий алкіл та нітро; O O (R5)b (R5)b , O , за умови, що, коли O (R5)c (R5)b O (R5)b O , O та R означає O (R5)b (R5)c O (R5)b O , де b означає ціле число від 0 до 2; та де с означає ціле число від 0 до 1; кожний R5 незалежно вибраний з групи, що містить галоген, нижчий алкіл та нітро; за умови, що, коли R означає O , тоді а означає 1; або її фармацевтично прийнятна сіль. 4. Сполука за пунктом 3, де R1 та R2 кожний незалежно вибраний з групи, що містить водень та нижчий алкіл; R4 вибраний з групи, що містить водень та метил; а означає ціле число від 1 до 2; R O (R5)b O або (R5)c O (R5)b O , тоді а означає 1; або її фармацевтично прийнятна сіль. 3. Сполука за пунктом 2, де R1 та R2 кожний незалежно вибраний з групи, що містить водень та нижчий алкіл; R4 вибраний з групи, що містить водень та нижчий алкіл; а означає ціле число від 1 до 2; R ; O , вибраний з групи, що містить 2-(2,3 дигідробензо[1,4]діоксиніл), 2-(бензо[1,3]діоксоліл), 3-(3,4-дигідро-2Н-бензо[1,4]діоксепініл), 2-(2,3дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3дигідробензо[1,4]діоксиніл), 2-(6-фтор-2,3дигідробензо[1,4]діоксиніл), 2-(хроманіл), 2-(5фтор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-хлор2,3-дигідробензо[1,4]діоксиніл), 2-(6хлорбензо[1,3]діоксоліл), 2-(7-нітро-2,3дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3дигідробензо[1,4]діоксиніл), 2-(5-хлор-2,3дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3дигідробензо[1,4]діоксиніл), 2-(6,7-дихлор-2,3дигідробензо[1,4]діоксиніл), 2-(8-хлор-2,3дигідробензо[1,4]діоксиніл), 2-(2,3дигідронафто[2,3-b][1,4]діоксиніл) та 2-(4метилбензо[1,3]діоксоліл); за умови, що, коли R означає 3-(3,4 вибраний з групи, що містить дигідро-2Н-бензо[1,4]діоксепініл), тоді а означає 1; або її фармацевтично прийнятна сіль. 5. Сполука за пунктом 4, де R1 та R2 кожний незалежно вибраний з групи, що містить водень та метил; R4 вибраний з групи, що містить водень та метил; а означає ціле число від 1 до 2; 5 91680 6 OCH3 R вибраний з групи, що містить 2 (бензо[1,3]діоксоліл), 2-(2,3дигідробензо[1,4]діоксиніл), 2-(2,3дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3дигідробензо[1,4]діоксиніл), 2-(7-хлор-2,3дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3дигідробензо[1,4]діоксиніл) та 2-(6,7-дихлор-2,3дигідробензо[1,4]діоксиніл); або її фармацевтично прийнятна сіль. 6. Сполука N-[(6-хлор-2,3-дигідро-1,4бензодіоксин-2-іл)метил]-сульфамід та її фармацевтично прийнятні солі. 7. Сполука, представлена формулою Cl O (S) O H N O O S NH2 , та її фармацевтично прийнятні солі. 8. Сполука формули (III) Дана заявка претендує на пріоритет попередньої заявки US 60/580J78, поданої 16 червня 2004 року, яка повністю включена в дану заявку за допомогою посилання. Даний винахід відноситься до нових похідних сульфаматів та сульфамідів, фармацевтичних композицій, що їх містять, та до їх застосування при лікуванні епілепсії та супутніх розладів. Епілепсія описується як стан, в якому особа має рецидивні напади, викликані хронічним основним процесом. Епілепсія відноситься, скоріше, до клінічного явища, ніж до окремої хвороби, бо існує багато форм та причин епілепсії. Використовуючи визначення епілепсії як двох чи більше неспровокованих нападів, інцидентність епілепсії оцінюється у, приблизно, 0,3-0,5 відсотків у різних народів по всьому світу, найбільша частота захворювань на епілепсію становить 5-10 осіб на 1000 осіб. Істотним етапом оцінки та контролю пацієнту з нападом є визначення типу нападу, що відбувся. Основною характеристикою, що відрізняє різні категорії нападів, є активність нападів: парціальна (синонімічна фокальній) чи генералізована. Парціальні напади - такі, в яких активність нападів обмежена окремими зонами кори головного мозку. Якщо свідомість повністю зберігається протягом нападу, то клінічні прояви вважаються відносно простими, а напад має назву простого парціального нападу. Якщо свідомість втрачається, тο напад має назву складного парціального нападу. Важлива додаткова підгрупа включає такі напади, O O N H S NH2 O O , (III) (III) або її фармацевтично прийнятна сіль. 9. Фармацевтична композиція, що містить фармацевтично прийнятний носій та сполуку за пунктом 1. 10. Фармацевтична композиція, одержана за допомогою змішування сполуки за пунктом 1 з фармацевтично прийнятним носієм. 11. Спосіб одержання фармацевтичної композиції, в якому змішують сполуку за пунктом 1 з фармацевтично прийнятним носієм. 12. Спосіб лікування епілепсії або супутнього розладу у суб'єкта, що цього потребує, в якому вводять суб'єкту терапевтично ефективну кількість сполуки за пунктом 1. 13. Спосіб лікування епілепсії у суб'єкта, що цього потребує, в якому вводять суб'єкту терапевтично ефективну кількість сполуки за пунктом 1. 14. Спосіб за пунктом 12, де розлад вибраний з есенціального тремору або синдрому тремтіння кінцівок. 15. Застосування сполуки за пунктом 1 для виготовлення лікарського засобу для лікування епілепсії або супутнього розладу у суб'єкта, що цього потребує. що починаються як парціальні напади, а потім дифузно розповсюджуються по всій корі, ці напади відомі як парціальні напади зі вторинною генералізацією. Генералізовані напади одночасно охоплюють дифузні області мозку двобічно-симетричним чином. Малі епілептичні напади характеризуються раптовими короткими періодами втрати свідомості без втрати постурального контролю. Атипові малі епілептичні напади типово включають більш тривалі проміжки втрати свідомості, менш раптовий початок та закінчення та більш явні моторні ознаки, що можуть включати фокальні або латералізаційні ознаки. Генералізовані тонічно-клонічні, або великі епілептичні напади, основний вид генералізованих нападів, характеризуються раптовим початком, без попередження. Початкова стадія нападу проявляється, зазвичай, тонічним скороченням м'язів, погіршенням дихання, значним посиленням симпатичною тонусу, що призводить до підвищення частоти серцебиттів, кров'яного тиску та до збільшення зіниць. Через 10-20 с тонічна стадія нападу типово розвивається у клонічну стадію, що утворюється шляхом накладення періодів релаксації м'язів та періодів тонічного скорочення м'язів. Періоди релаксації поступово збільшуються, доки не закінчиться іктальна стадія, яка зазвичай триває не більше 1 хвилини. Постіктальна стадія характеризується неприйнятністю, млявістю м'язів та надлишковою слинотечею, що може призвести до виникнення стридорозного ди 7 91680 8 хання та до часткової обструкції дихальних шляхів. Атонічні напади характеризуються раптовою втратою тонусу повільних м'язів, що триває 1-2 с. Свідомість швидко втрачається, проте, зазвичай, постіктальна сплутаність відсутня. Міоклонічні напади характеризуються раптовим та коротким скороченням м'язів, що може охоплювати одну частину тіла або все тіло (www.harrisonsonline.com, 29 березня 2001 р.). Інгібітори карбоангідрази (ΙΚA) широко використовувались у медицині, головним чином, як протиглаукомні та антисекреторні ліки або діуретичні агенти, та вони є цінними сполуками. Проте, системні протиглаукомні агенти (такі, як ацетозоламід) мають можливу небажану побічну дію, включаючи парестезії, нефролітіаз та втрату ваги. Топірамат є добре відомим протисудомним препаратом, що у мікромолярних дозах інгібує карбоангідразу, припускається, що це інгібування є причиде b означає ціле число від 0 до 4; та де с ною парестезій, відмічених у деяких пацієнтів, які означає ціле число від 0 до 2; приймають топірамат. кожний R3 незалежно вибраний з групи, що Все ще існує потреба у забезпеченні ефективвключає галоген, нижчий алкіл, нижчий алкіл, заною лікування епілепсії та супутніх розладів та у міщений гідрокси, -О-(нижчий алкіл), -S-(нижчий переважному лікуванні, при якому відсутня супуталкіл), нітро, ціано, аміно, нижчий алкіламіно, ня побічна дія, що притаманна інгібуванню карбоди(нижчий алкіл)аміно та -С(О)О-(нижчий алкіл); ангідрази. Даний винахід відноситься до нових похідних за умови, що коли означає сульфаматів та сульфамідів, фармацевтичних композицій, що їх містять, та до їх застосування при лікуванні епілепсії та супутніх розладів. Більш особливо, даний винахід відноситься до сполук формули (І) та сполук формули (II), які визначені далі. або Даний винахід відноситься до нових похідних сульфаматів, сполук формули (І) де R1 та R2 кожний незалежно вибраний з групи, щο включає водень та нижчий алкіл; а означає ціле число від 1 до 2; означає кільцеву структуру, вибрану з групи, що включає , тоді а означає 1; крім того, за умови, що коли R1 являє собою водень, R2 являє собою водень та а означає 1, тоді є відмінним від ; або їх фармацевтично прийнятної солі. Даний винахід, крім того, відноситься до нових похідних сульфамідів, сполук формули (II) де R1 та R2 кожний незалежно вибраний з групи, що включає водень та нижчий алкіл; R4 вибраний з групи, що включає водень та нижчий алкіл; а означає ціле число від 1 до 2; вибраний з групи, що включає 9 91680 10 Іншим прикладом винаходу є застосування будь-якої зі сполук, описаних в даній заявці, при одержанні лікарського засобу для лікування епілепсії або супутніх розладів у суб'єкта, що цього потребує. Даний винахід відноситься до сполук формули (І) та сполук формули (II) де де b означає ціле число від 0 до 4; та де с означає ціле число від 0 до 2; кожний R5 незалежно вибраний з групи, що включає галоген, нижчий алкіл та нітро; за умови, що коли означає або , тоді а означає 1; або їх фармацевтично прийнятної солі. Даний винахід, крім того, відноситься до сполуки формули (III) або її фармацевтично прийнятної солі. Прикладом винаходу є фармацевтична композиція, що містить фармацевтично прийнятний носій та будь-яку зі сполук, описаних вище. Прикладом винаходу є фармацевтична композиція, одержана за допомогою змінювання будь-якої зі сполук, описаних вище, з фармацевтично прийнятим носієм. Прикладом винаходу є спосіб одержання фармацевтичної композиції, який включає змішування будь-якої зі сполук, описаних вище, з фармацевтично прийнятним носієм. Прикладом винаходом є спосіб лікування епілепсії та супутніх розладів у суб'єкта, що цього потребує, який включає введення суб’єкту терапевтично ефективної кількості будь-якої зі сполук або фармацевтичних композицій, описаних вище. , R1, R2 та R4 є такими, як визначено в даній заявці. Даний винахід також відноситься до сполуки формули (III). Сполуки формули (І), формула (II) та формула (III) корисні для лікування епілепсії та супутніх розладів. Як використовується в даній заявці, якщо не зазначено інше, термін "галоген" означає хлор, бром, фтор та йод. Як використовується в даній заявці, якщо не зазначено інше, термін "алкіл", який використовується сам по собі або як частина заміщуючої групи, включає лінійні та розгалужені ланцюги. Наприклад, алкільні радикали включають метил, етил, пропіл, ізопропіл, бутил, ізобутил, вторбутил, трет-бутил, пентил та подібні. Якщо не зазначено інше, термін "нижчий", коли він використовується з алкілом, означає вуглецевий ланцюг, що містить 1-4 атоми вуглецю. Як використовується в даній заявці, якщо не зазначено інше, термін "алкокси" повинен означати кисневий ефірний радикал вище описаних алкільних груп з лінійним або розгалуженим ланцюгом. Наприклад, метокси, етокси, н-пропокси, вторбутокси, трет-бутокси, н-гексилокси та подібні. Як використовується в даній заявці, позначення "*" повинне означати присутність стереогенного центру. Коли конкретна група є "заміщеною" (наприклад, алкіл, арил, тощо), то група може мати один або більше замісників, переважно від одного до п’яти замісників, більш переважно від одного до трьох замісників, найбільш переважно від одного до двох замісників, незалежно вибраних з переліку замісників. При посиланні на замісники, термін "незалежно" означає, що коли можливі більше, ніж один з таких замісників, такі замісники можуть бути однаковими або відмінними один від одного. Згідно зі стандартною номенклатурою, що використовується в цьому описі, спочатку описується кінцева частина описуваного бічного ланцюга, а потім суміжна з нею функціональність в напрямку до точки приєднання. Таким чином, наприклад, замісник "феніл-алкіл-амідо-карбоніл-алкіл" відноситься до групи формули 11 Скорочення, що використовуються в даній заявці, особливо в Схемах та Прикладах, є такими, як вказано нижче: UCC = Дициклогсксил карбодіімід DCE = Дихлоретан DCM = Дихлорметан DIPEA або DIEA = Діізопропілетиламін DMF = Ν,Ν-Диметилформамід DMSO = Диметилсульфоксид ΕDC = Етилкарбодіімід Et3N або TEA = Триетиламін Et2O = Діетиловий ефір ЕА або ЕtOАс = Етил ацетат EtOH = Етанол ІРА = 2-пропанол Hерt = Гептан HOВТ = 1-Гідроксибензотриазол ВЕРХ = Високоефективна рідинна хроматографія LAH = Алюмогідрид літію Μ або МеОН = Метанол ЯМР = Ядерний магнітний резонанс Pd-C = Каталізатор паладій на вугіллі ОФ ВЕРХ = Обернено-фазова високоефективна рідинна хроматографія RT або rt = Кімнатна температура TEA = Триетиламін TFA = Трифтороцтова кислота THF = Тетрагідрофуран ТШХ = Тонкошарова хроматографія Як використовується в даній заявці, якщо не вказано інше, терміни "епілепсія та супутні розлади" або "епілепсія або супутній розлад" означають будь-який розлад, при якому суб'єкт (переважно доросла людина, дитина або новонароджена дитина) переносить один чи більше нападів та/або треморів. Придатні приклади включають, але не обмежуються, епілепсію (включаючи локалізаційно-обумовлені епілепсії, генералізовані епілепсії, епілепсії як з генералізованими, так і з локальними нападами, та подібні, але не обмежуючись ними), напади, якускладнення хвороби або стану (такі, як напади, пов'язані з енцефалопатією, фенілкетонурією, ювенільною хворобою Гаучера, прогресуючою міоклонус-епілепсією Лундборга, інсультом, травмою голови, стресом, гормональними змінами, вживанням або відміною наркотиків, вживанням або відміною алкоголю, порушенням сну та подібним), ессенціальний тремор, синдром тремтіння кінцівок та подібне, але не обмежуються цим. Переважно, розлад вибраний з епілепсії (незалежно від типу, основної причини або походження), ессенціального тремору або синдрому тремтіння кінцівок, більш переважно, розладом є епілепсія (незалежно від типу, основної причини або походження) або ессенціальний тремор. Термін "суб'єкт", як використовується в даній заявці, відноситься до тварини, переважно ссавця, найбільш переважно людини, яка є або була об'єктом лікування, нагляду або експерименту. 91680 12 Термін "терапевтично ефективна кількість", як використовується в даній заявці, означає, ту кількість активної сполуки або фармацевтичного агента, що викликає біологічну або лікарську реакцію в тканинній системі, тварині або людині, що шукає дослідник, ветеринар, медичний лікар або інший клінічній лікар, яка включає полегшення симптомів хвороби або розладу, що лікують. Як використовується в даній заявці, під терміном "композиція" мається на увазі продукт, що містить вказані інгредієнти у вказаних кількостях, а також будь-який продукт, який виникає, безпосередньо або побічно, з комбінації вказаних інгредієнтів у вказаних кількостях. В тих випадках, коли сполуки за даним винаходом мають, принаймні, один хіральний центр, вони можуть, відповідно, існувати у вигляді енантіомерів. Якщо сполуки мають два або більше хіральних центрів, вони можуть додатково існувати як діастереомери. Слід розуміти, що всі такі ізомери та їх суміші включені в межі даного винаходу. До того ж, деякі з кристалічних форм сполук можуть існувати у формі поліморфів, та зазначено, що такі поліформи включені в межі даного винаходу. Крім того, деякі зі сполук можуть утворювати сольвати з водою (наприклад гідрати) або зі звичайними органічними розчинниками, та також зазначено, що такі сольвати включені в межі даного винаходу. Коли способи одержання сполук за винаходом приводять до одержання суміші стереоізомерів, ці ізомери можуть бути розділені звичайними методами, такими як препаративна хроматографія. Сполуки можуть бути одержані у рацемічній формі або індивідуальні енантіомери можуть бути одержані або за допомогою енантіоспецифічного синтезу, або розділенням. Сполуки можуть, наприклад, бути розділені на їх складові енантіомери за допомогою стандартних методів, таких як утворення діастереомерних пар шляхом утворення солі з оптично активною кислотою, такою як (-)-дип-толуоїл-D-винна кислота та/або (+)-ди-п-толуоїлL-винна кислота з наступною фракційною кристалізацією та відновленням вільної основи. Сполуки можуть також бути розділені шляхом утворення діастереомерних ефірів або амідів з наступним хроматографічним розділенням та видаленням хіральної допоміжної речовини. Альтернативно, сполуки можуть бути розділені, використовуючи колонку для хіральної ВЕРХ. Протягом будь-якого з процесів одержання сполук за даним винаходом, може бути необхідним та/або бажаним захистити чутливі або хімічно активні групи на будь-якій з молекул, яких це стосується. Це може бути досягнуто за допомогою традиційних захисних груп, таких як описано в Protective Groups in Organic Chemistry, ed. J.F.W. McOmie, Plenum Press, 1973; та T.W. Greene & P.G.M. Wuts, Protective Groups in Organic Synthesis, John Wiley & Sons, 1991. Захисні групи можуть бути видалені на придатній подальшій стадії, використовуючи способи, відомі з рівня техніки. Даний винахід включає в свої межі проліки сполук за даним винаходом. Взагалі, такі проліки будуть функціональними похідними сполук, які легко перетворюються in vivo на бажану сполуку. 13 91680 14 Таким чином, в способах лікування за даним винаводні розчини, прийнятно ароматизовані сиропи, ходом термін "введення" включає лікування різних водні або маслянисті суспензії та ароматизовані описаних розладів конкретно розкритою сполукою емульсії з харчовими маслами, такими як бавовабо сполукою, яка може не бути розкрита конкретняне масло, масло сезаму, кокосове масло або но, але перетворюється на описану сполуку in vivo арахісове масло, а також еліксири та подібні фарпісля введення пацієнту. Традиційні процедури мацевтичні засоби. Прийнятні диспергуючі або виділення та одержання прийнятних пролікарських суспендуючі агенти для водних суспензій включапохідних описані, наприклад, в "Desimi of ють синтетичні та природні смоли, такі як трагаProdrugs", cd. H. Bundgaard, Elsevier, 1985. кант, гуміарабік, альгінат, декстран, натрієва карДаний винахід забезпечує фармацевтичні боксиметилцелюлоза, метилцелюлоза, композиції, які містять сполуку формули (І), сполуполівінілпіролідон або желатин. ку формули (II) та/або сполуку формули (III) в споДля одержання фармацевтичних композицій лученні з фармацевтично прийнятним носієм. Пеза даним винаходом сполуку Формули (І), сполуку реважно ці композиції знаходяться у формах формули (II) та/або сполуку формули (III) ретельно одиничного дозування, таких як таблетки, пілюлі, змішують з фармацевтичним носієм відповідно до капсули, порошки, гранули, стерильні парентерастандартних фармацевтичних способів змішуванльні розчини або суспензії, дозований аерозоль ня, цей носій може приймати різноманітні форми в або рідкі спреї, краплі, ампули, автоінжекторні залежності від форми препарату, бажаного для пристрої або супозиторії; для перорального, паревведення, наприклад, стерильні препарати, принтерального, інтраназального, під'язикового або йнятні для ін'єкцій, будуть одержані, використовуректального введення, або для введення шляхом ючи відповідні агенти солюбілізації. Одинична доінгаляції або інсуфляції. Альтернативно, композиза буде містити від приблизно 10 до приблизно ція може бути представлена у формі, прийнятій 300 мг активного інгредієнта. Таблетки містять для введення один раз на тиждень або один раз деякі або всі наступні інертні інгредієнти: водна на місяць; наприклад, нерозчинна сіль активної лактоза, пептизований крохмаль, мікрокристалічна сполуки, така як сіль деканової кислоти, може бути целюлоза, натрію крохмалю гліколат, стеарат магпристосована, щоб забезпечити запасну підготовнію, очищена вода, карнаубський віск, гідроксипку для внутрішньом'язової ін'єкції. Для одержання ропіл метилцелюлоза, діоксид титану, поліетилен твердих композицій, таких як таблетки, основний гліколь, синтетичний оксид заліза та полісорбат активний інгредієнт змішують з фармацевтичним 80. Фахівець в даній галузі техніки визнає, що пеносієм, наприклад традиційними таблетковими роральні таблетки, які містять сполуку формули (І), інгредієнтами, такими як кукурудзяний крохмаль, сполуку формули (II) та/або сполуку формули (III) лактоза, сахароза, сорбіт, тальк, стеаринова кисможуть бути одержані так само та можуть містити лота, стеарат магнію, фосфат дикальцію або каподібні інертні інгредієнти. мідь, та іншими фармацевтичними розріджувачаФахівець вданій галузі техніки визнає, що фами, наприклад водою, щоб отримати тверду рмацевтичні композиції, що місіять більше, ніж попередню композицію, яка містить однорідну суодин активний інгредієнт, можуть бути так само міш основного інгредієнту. Посилання на ці попеодержані відповідно до відомих методів. редні композиції як на однорідні, означає, що акУ втіленні даного винаходу R1 вибраний з грутивний інгредієнт рівномірно розподілений в усій пи, що включає водень та метил. В іншому втіленкомпозиції для того, щоб композиція легко могла ні даного винаходу R2 вибраний з групи, що вклюбути розділена на однаково ефективні форми дочає водень та метил. В ще іншому втіленні даного зування, такі як таблетки, пілюлі та капсули. Потім винаходу R1 та R2 кожний являє собою водень, цю тверду попередню композицію розділяють на або R1 та R2 кожний являє собою метил. види форм одиничної дози, які описані вище, що У втіленні даного винаходу -(СН2)а- вибраний з містять від приблизно 1 до приблизно 1000 мг акгрупи, що включає -СН2-та -СН2-СН2-. В іншому тивного інгредієнту за даним винаходом. Таблетки втіленні даного винаходу -(СН2)а- являє собою або пілюлі розкритих композицій можуть бути покСН2-. риті або комбіновані іншим шляхом, щоб забезпеУ втіленні даного винаходу R4 вибраний з гручити форму дозування, віддаючи перевагу пролонпи, що включає водень та метил, переважно, R4 гованій дії. Наприклад, таблетка або пілюля може являє собою водень. містити внутрішнє дозування та зовнішній компоУ втіленні даного винаходу а означає 1. нент дозування, останній буде у формі оболонки У втіленні даного винаходу b означає ціле чинад першим. Два компоненти можуть бути відділесло від 0 до 2. В іншому втіленні даного винаходу ні за допомогою кишкового прошарку, що підхос означає ціле число від 0 до 2. В іншому втіленні дить, щоб не піддаватися дезинтеграції в шлунку даного винаходу b означає ціле число від 0 до 1. В та дозволити внутрішньому компоненту пройти іншому втіленні даного винаходу с означає ціле непошкодженим в дванадцятипалу кишку або бути число від 0 до 1. В ще іншому втіленні даного визатриманим при вивільненні. Для таких кишкових находу сума b та с означає ціле число від 0 до 2, прошарків або покриттів можуть бути використані переважно ціле число від 0 до 1. В ще іншому втірізноманітні речовини, такі речовини включають ленні даного винаходу b означає ціле число від 0 ряд полімерних кислот з такими речовинами як до 2 та с означає 0. шелак, ацетиловий спирт та ацетат целюлози. Рідкі форми, в які нові композиції за даним винаходом можуть бути поєднані для введення перорально або за допомогою ін'єкції, включають 15 91680 У втіленні даного винаходу 16 означає кі льцеву структуру, вибрану з групи, що включає та , , . та В іншому втіленні даного винаходу вибраний з групи, що включає . В іншому втіленні даного винаходу озна , та чає кільцеву структуру, вибрану з групи, що включає . У втіленні даного винаходу та . У втіленні даного винаходу означає кі льцеву структуру, вибрану з групи, що включає 2(хроманіл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(бензо[1,3]діоксоліл), 2-(5хлор-2,3-дигідро-бензо[1,4]діоксиніл), 2-(7-нітро2,3-дигідро-бензо[1,4]діоксиніл), 2-(6,7-дихлор-2,3дигідро-бензо[1,4]діоксиніл), 2-(2,3-дигідронафто[2,3-b][1,4]діоксиніл) та 2-(7-хлорбензо[1,3]діоксоліл). В іншому втіленні даного винаходу означає кільцеву структуру, вибра ну з групи, що включає 2-(5-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-нітро-2,3-дигідробензо[1,4]діоксиніл), 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл) та 2-(2,3-дигідро-нафто[2,3b][,4]діоксиніл). У втіленні даного винаходу вибраний з групи, включає вибраний з групи, що включає 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(бензо[1,3]діоксоліл), 3-(3,4дигідро-бензо[1,4]діоксепініл), 2-(6-хлор-2,3дигідро-бензо[1,4]діоксиніл), 2-(6-фтор-2,3-дигідробензо[1,4]діоксиніл), 2-(хроманіл), 2-(5-фтор-2,3дигідро-бензо[1,4]діоксиніл), 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-бензо[ 1,3]діоксоліл), 2-(7-нітро-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(5-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл), 2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксиніл), 2-(8-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(2,3-дигідро-нафто[2,3b][1,4]діоксиніл) та 2-(4-метил-бензо[1,3]діоксоліл). В іншому втіленні даного винаходу вибраний з групи, що включає 2(бензо[1,3]діоксоліл), 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(6-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-хлор-2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл), 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл) та 2-(6,7-дихлор-2,3-дигідробензо[1,4|діоксиніл). В іншому втіленні даного винаходу , , , вибраний з групи, що включає 2-(2,3-дигідробензо[1,4]діоксиніл), 2-(7-метил-2,3-дигідробензо[1,4]діоксиніл) та 2-(6-бром-2,3-дигідробензо[1,4]діоксиніл). У втіленні даного винаходу R3 вибраний з групи, що включає галоген, нижчий алкіл, нижчий алкіл, заміщений гідрокси, -О-(нижчий алкіл), нітро, ціано, аміно, нижчий алкіламіно та ди(нижчий ал 17 91680 18 кіл)аміно. В іншому втіленні даного винаходу R3 суміші, де% енантіомерного збагачення (% ее) вибраний з групи, що включає галоген та нітро. В більший, ніж приблизно 75%, переважно більший, іншому втіленні даного винаходу R3 вибраний з ніж приблизно 90%, більш переважно більший, ніж групи, що включає хлор та нітро. приблизно 95%, найбільш переважно більший, ніж У втіленні даного винаходу R5 вибраний з груприблизно 98%. пи, що включає (II) галоген та нижчий алкіл. В інУ втіленні даного винаходу сполука формули шому втіленні даного винаходу R5 вибраний з хло(II) присутня у вигляді енантіомерно збагаченої ру, фтору, брому та метилу. суміші, де% енантіомерного збагачення (% ее) У втіленні даного винаходу в сполуці формули більший, ніж приблизно 75%, переважно більший, ніж приблизно 90%, більш переважно більший, ніж приблизно 95%, найбільш переважно більший, ніж (І) є відмінним від , приблизно 98%. Втіленням даного винаходу є сполуки форму3 де b означає 1 та R вибраний з групи, що включає ли (І), де активність MЕS при 100 мг/кг є більшою, галоген, нітро, ціано, аміно, нижчий алкіл, нижчий ніж або дорівнює 3/5 мишей. Іншим втіленням даалкокси та -С(О)О-(нижчий алкіл). В іншому втіного винаходу є сполуки формули (II), де активленні даного винаходу в сполуці формули (І) ність MES при 100 мг/кг є більшою, ніж або дорівнює 3/5 мишей. Характерні сполуки за даним винаходом є тає відмінним від , де кими, як наведено в Таблицях 1 та 2 нижче. Додаткові сполуки за даним винаходом є такими, як b означає 1. наведено в Таблиці 3. В Таблицях 1, 2 та 3 нижче, У втіленні даного винаходу, стерео-центр в в колонці "стерео" наведено стерео-конфігурацію сполуці формули (І) знаходиться в S-конфігурації. при атомі вуглецю гетероциклу, приєднаного при В іншому втіленні даного винаходу, стерео-центр в позначеному зірочкою зв'язку. Якщо не наведено сполуці формули (І) знаходиться в R-конфігурації. жодного позначення, то сполука була одержана у У втіленні даного винаходу, стерео-центр в вигляді суміші стерео-конфігурацій. Коли наведено сполуці формули (II) знаходиться в S-конфігурації. позначення "R" або "S", стерео-конфігурація базуВ іншому втіленні даного винаходу, стерео-центр в ється на енантіомерно збагаченій вихідній речовисполуці формули (II) знаходиться в R-конфігурації. ні. У втіленні даного винаходу сполука формули (І) присутня у вигляді енантіомерно збагаченої 19 91680 20 21 Сполуки формули (І) можуть бути одержані відповідно до способу, наведеному на Схемі 1. Схема 1 Відповідно, прийнятно заміщену сполуку формули (V), відому сполуку або сполуку, одержану за допомогою відомих способів, піддають реакції з прийнятно заміщеною сполукою формули (VI), відомою сполукою або сполукою, одержаною за допомогою відомих способів, в присутності основи, такої як NaH, TEA, DIPEA, піридин та подібна, в органічному розчиннику, такому як DMF, DMSO та подібний, з одержанням відповідної сполуки формули (І). Сполуки формули (II) можуть бути одержані відповідно до способу, наведеному на Схемі 2. Схема 2 Відповідно, прийнятно заміщену сполуку формули (VII), відому сполуку або сполуку, одержану за допомогою відомих способів, піддають реакції з сульфамідом, відомою сполукою, переважно, де сульфамід присутній в кількості в діапазоні від приблизно 2 до приблизно 5 еквівалентів, в органічному розчиннику, такому як THF, діоксан та подібний, переважно при підвищеній температурі в 91680 22 діапазоні від приблизно 50°С до приблизно 100°С, більш переважно при приблизно температурі кипіння зі зворотним холодильником, з одержанням відповідної сполуки формули (ІІа). Альтернативно, прийнятно заміщену сполуку формули (VII), відому сполуку або сполуку, одержану за допомогою відомих способів, піддають реакції з прийнятно заміщеною сполукою формули (VIII), відомою сполукою або сполукою, одержаною за допомогою відомих способів, в присутності основи, такої як TEA, DIPEA, піридин та подібна, в органічному розчиннику, такому як DMF, DMSO та подібний, з одержанням відповідної сполуки формули (II). Сполуки формули (V), в яких означає , може бути одержані відповідно до способу, наведеному на Схемі 3. Схема 3 Відповідно, прийнятно заміщену сполуку формули (X), відому сполуку або сполуку, одержану за допомогою відомих способів, піддають реакції з прийнятно заміщеною сполукою формули (XI), відомою сполукою або сполукою, одержаною за допомогою відомих способів, в присутності основи, такої як метоксид натрію, етоксид натрію, третбутоксид натрію, метоксид калію, трет-бутоксид 23 91680 24 калію та подібна, в органічному розчиннику, такому як метанол, етанол, ІРА та подібний, переважВідповідно, прийнятно заміщену сполуку форно при підвищеній температурі в діапазоні від примули (XV), відому сполуку або сполуку, одержану близно 50°С до приблизно 100°С, більш за допомогою відомих способів, піддають реакції з переважно при приблизно температурі кипіння зі 3-хлор-2-хлорметил-пропеном, відомою сполукою, зворотним холодильником, з одержанням відповів присутності основи, такої як карбонат калія, кардної сполуки формули (XII). бонат натрія, бікарбонат натрія, TEA, DIPHA та Сполуку формули (XII) піддають реакції з приподібна, в органічному розчиннику, такому як ацейнятно вибраним відновником, таким як LAH та тонітрил, THF, діоксан та подібний, переважно при подібний, в органічному розчиннику, такому як підвищеній температурі в діапазоні від приблизно THF, діетиловий ефір та подібний, з одержанням 50°С до приблизно 100°С, більш переважно, при відповідної сполуки формули (Va). приблизно температурі кипіння зі зворотним холодильником, з одержанням відповідної сполуки фоСполуки формули (VII), в яких означає рмули (XVI). Сполуку формули (XVI) піддають реакції з бораном в органічному розчиннику, такому як THF, , можуть бути одержані діоксан та подібний, з одержанням відповідної сполуки формули (XVII), яку переважно не виділяють. відповідно до способу, наведеному на Схемі 4. Сполуку формули (XVII) піддають реакції з аміносульфоновою кислотою, переважно при підвищеній температурі в діапазоні від приблизно 50°С до приблизно 100°С, більш переважно, при приблизно температурі кипіння зі зворотним холодильником, з одержанням відповідної сполуки формули (Vllb). Сполуки формули (V), в яких вибраний Схема 4 Відповідно, прийнятно заміщену сполуку формули (XIII), відому сполуку або сполуку, одержану за допомогою відомих способів (наприклад як описано на Схемі 3 вище), піддають реакції з ΝН4ΟН, відомою сполукою, необов’язково в органічному розчиннику, такому як ацетонітрил та подібний, з одержанням відповідної сполуки формули (XIV). Сполуку формули (XIV) піддають реакції з прийнято вибраним відновником, таким як LAH та подібний, в органічному розчиннику, такому як THF, діетиловий ефір та подібний, з одержанням відповідної сполуки формули (VІla). Сполуки формули (VII), в яких ний з вибра можуть бути оде ржані відповідно до способу, наведеному на Схемі 5. з можуть бути одержані відповідно до .способу, наведеному на Схемі 6. Схема 6 Відповідно, прийнятно заміщену сполуку формули (XVIII), сполуку, одержану, як наведено на Схемі 5 вище, піддають реакції з пероксидом, таким як пероксид водню та подібний, в присутності основи, такої як NaOН, KОH та подібна, в органічному розчиннику, такому як хлороформ, DCE, DCΜ та подібний, з одержанням відповідної сполуки формули (Vb). Сполуки формули (V), в яких з вибраний можуть бути одержані відповідно до способу, наведеному на Схемі 7. Схема 5 25 91680 26 Схема 7 Відповідно, прийнятно заміщену сполуку формули (XIX), відому сполуку або сполуку, одержану за допомогою відомих способів, піддають реакції з прийнятно вибраним відновником, таким як LAH та подібний, в органічному розчиннику, такому як THF, діетиловий ефір та подібний, з одержанням відповідної сполуки формули (Vc). Сполуки формули (VII), в яких ний з вибра можуть бути одер жані відповідно до способу, наведеному на Схемі 8. Схема 8 Відповідно, прийнятно заміщену сполуку формули (XX), відому сполуку або сполуку, одержану за допомогою відомих способів, піддають реакції з NH4OH, в присутності агента сполучення, такого як DCC та подібний, необов'язково в органічному розчиннику, такому як ацетонітрил та подібний, з одержанням відповідної сполуки формули (XXI). Сполуку формули (XXI) піддають реакції з прийнятно вибраним відновником, таким як LAH та подібний, в органічному розчиннику, такому як ТНF, діетиловий ефір та подібний, з одержанням відповідної сполуки формули (VIIc). Сполуки формули (V), в яких з вибраний ганічному розчиннику, такому як DMF, DMSO, ацетонітрил та подібний, переважно, при підвищеній температурі в діапазоні від приблизно 50°С до приблизно 100°С, більш переважно, при підвищеній температурі в діапазоні від приблизно 50°С до приблизно 75°С, з одержанням відповідної сполуки формули (Vd). Сполуки формули (VII), в яких ний з вибра та де а означає 2, можуть бути одержані відповідно до способу, наведеному на Схемі 10. та де а означає 1, мо жуть бути одержані відповідно до способу, наведеному на Схемі 9. Схема 10 Схема 9 Відповідно, прийнятно заміщену сполуку формули (XXII), відому сполуку або сполуку, одержану за допомогою відомих способів, піддають реакції з прийнятно заміщеною сполукою формули (XXIII), відомою сполукою або сполукою, одержаною за допомогою відомих способів, в присутності основи, такої як K2СO3, Na2СО3, NaHCO3 та подібна, в ор Відповідно, прийнятно заміщену сполуку формули (XXIV), в якій J1 являє собою прийнятну групу, що відходить, таку як Br, СІ, І, толіл, мезил, трифлат та подібну, відому сполуку або сполуку, одержану за допомогою відомих способів (наприклад, за допомогою активації відповідної сполуки, в якій J1 являє собою ОН), піддають реакції з ціанідом, таким як ціанід калію, ціанід натрію та подібний, в органічному розчиннику, такому як DMSO, 27 91680 DМF, ТHF та подібний, з одержанням відповідної сполуки формули (XXV). Сполуку формули (XXV) відновлюють відповідно до відомих способів, наприклад за допомогою реакції з прийнятним відновником, таким як LAN, боран та подібний, з одержанням відповідної сполуки формули (VІle). Сполуки формули (VII), в яких 28 вибраСхема 12 ний з та де а означає 1, можуть бути одержані відповідно до способу, наведеному на Схемі 11. Відповідно, прийнятно заміщену сполуку формули (XXVII), в якій J2 являє собою CN, відому сполуку або сполуку, одержану за допомогою відомих способів, гідролізують відповідно до відомих способів, наприклад за допомогою реакції з прийнятною кислотою або основою, з одержанням відповідної сполуки формули (XXIX). Сполуку формули (XXIX) відновлюють відповідно до відомих способів, наприклад за допомогою реакції з прийнятним відновником, таким як LAН та подібний, з одержанням відповідної сполуки формули (Ve). Фахівець в даній галузі техніки визнає, що сполуки формули (V) та (VII), в яких виб раний з Схема 11 Відповідно, прийнятно заміщену сполуку формули (XXVI), відому сполуку або сполуку, одержану за допомогою відомих способів (наприклад відповідно до способу, наведеному на Схемі 9 вище) активують, згідно відомого способу, з одержанням відповідної сполуки формули (XXVII), в якій J2 являє собою групу, що відходить, таку як тозилат, СІ, Br, І, мезилат, трифлат та подібну. Сполуку формули (XXVII) піддають реакції з сіллю фталіміду, такою як фталімід калію, фталімід натрію та подібний, в органічному розчиннику, такому як DMF, DMSO, ацетонітрил та подібний, переважно, при підвищеній температурі в діапазоні від 50°С до приблизно 200°С, більш переважно, при приблизно температурі кипіння зі зворотним холодильником, з одержанням відповідної сполуки формули (XXVIII). Сполуку формули (XXVI) піддають реакції з N2H4, відомою сполукою, в органічному розчиннику, такому як етанол, метанол та подібний, переважно, при підвищеній температурі в діапазоні від приблизно 50°С до приблизно 100°С, більш переважно, при приблизно температурі кипіння зі зворотним холодильником, та подібній, з одержанням відповідної сполуки формули (VIId). Сполуки формули (V), в яких з вибраний та де а означає 2, мо жуть бути подібно одержані відповідно до способу, наведеному на Схемі 12. можуть бути подібно одержані відповідно до способів, наведених на Схемах 3-12 вище, вибираючи та замінюючи бензо-конденсовані вихідні сполуки на відповідні нафтил-конденсовані сполуки (наприклад сполуки формули (X), (XIII), (XV), (XVIII), (XIX), (XX), (XXII), (XXIV) та т.п.). Фахівець в даній галузі техніки, крім того, визнає, що коли бажаним є окремий енантіомер (або суміш енантіомерів, де збагачений один енантіомер) сполуки формули (V) або сполуки формули (VII), можуть бути використані зазначені вище способи, які описані на Схемах 1-12, замінюючи відповідну вихідну речовину на окремий енантіомер (або суміш енантіомерів, де збагачений один енантіомер). Наступні Приклади наведені, щоб допомогти в розумінні винаходу, їх не потрібно аналізувати з метою обмеження будь-яким чином винаходу, 29 91680 30 який викладено у формулі винаходу, яку наведено N-(2,3-Дигiдpo-бeнзo[4,1]дioкcин-2-ілметил)після опису. сульфамід (Сполука № 1) Приклад 1 ((3,4-Дигідро-2Н-бензо[b][1,4]діоксепін-3іл)метил)сульфамід (Складовий № 3) Ортодіоксибензол (5,09 г, 46,2 ммоль) та карбонат калію об'єднували в ацетонітрилі та нагрівали до кипіння зі зворотним холодильником протягом однієї години. Додавали 2-хлорметил-3-хлор1-пропен (5,78 г, 46,2 ммоль) та реакцію продовжували при кипінні зі зворотним холодильником протягом 24 годин. Розчин охолоджували до кімнатної температури та фільтрували. Фільтрат випарювали та залишок розбавляли водою та екстрагували діетиловим ефіром (3 х). Об'єднаний органічний розчин сушили над MgSO4 та концентрували. Хроматографією (2% етилового ефіру в гексані) одержували 3-метилен-3,4-дигідро-2Нбензо[b][1,4]діоксепін у вигляді безбарвного масла. MS (ESI): 163,2 (М+Н+) 1 Н ЯМР (300 МГц, CDCl3) : 6,94 (m, 4H), 5,07 (s, 2H), 4,76 (s, 4H). 3-Метилен-3,4-дигідро-2Нбензо[b][1,4]діоксепін (5,00 г, 30,8 ммоль) розчиняли в сухому THF (100 мл). При 0°С додавали боран-ТНF (1,0 Μ в ТHF, 10,3 мл). Реакційну суміш перемішували при RT протягом 5 годин. Додавали аміносульфонову кислоту (6,97 г, 61,6 ммоль). Реакційну суміш нагрівали до кипіння зі зворотним холодильником протягом ночі. Реакційну суміш охолоджували до кімнатної температури та додавали водний гідроксид натрію (3,0 М, 100 мл). Розчин екстрагували етил ацетатом (3x100 мл). Об'єднаний органічний розчин сушили над MgSO4. Розчин концентрували під вакуумом та очищали за допомогою хроматографії (від 2% до 8% метанолу в дихлорметані), одержуючи ((3,4-дигідро-2Hбензо[b][1,4]діоксепін-3-іл)метил)амін у вигляді безбарвного масла. MS (ESI): 180,1 (М+Н+) 1 Н ЯМР (300 МГц, DMSO) : 6,92 (m, 4H), 4,21 (m, 2H), 4,07 (m, 2H), 3,33 (ушир., 2H), 3,16 (d, J=4 Гц, 1H), 2,72 (d, J=4 Гц, 1H), 2,30 (m, 1H). ((3,4-Дигідро-2H-бензо[b][1,4]діоксепін-3іл)метил)амін (2,90 г, 16,2 ммоль) та сульфамід (3,11 г, 32,4 ммоль) об'єднували в сухому діоксані (60 мл) та нагрівали до кипіння зі зворотним холодильником протягом ночі. Додавали хлороформ та осад видаляли фільтруванням. Фільтрат концентрували під вакуумом та очищали за допомогою хроматографії (від 2% до 8% ацетону в дихлорметані), одержуючи зазначену у заголовку сполуку у вигляді не зовсім білої твердої речовини. 258,8 (М+Н+) 1 Н ЯМР (300 МГц, DMSO) : 6,92 (m 4H), 6,71 (ушир., 1H), 6,59 (ушир., 2H), 4,19 (m, 2H), 4,04 (m, 2H), 3,00 (m, 2H), 2,39 (m, 1H). Приклад 2 Рацемічний 2,3-дигідро-1,4-бензодіоксин-2ілметиламін (4,4 г, 26 ммоль) та сульфамід (5,1 г, 53 ммоль) об'єднували в 1,4-діоксані (100 мл) та кип'ятили зі зворотним холодильником протягом 2 годин. Реакційну суміш охолоджували до кімнатної температури та невелику кількість твердої речовини відфільтровували та відкидали. Фільтрат випарювали у вакуумі та залишок очищали, використовуючи флеш колоночну хроматографію (DСМ:Мeтанол - 10:1), одержуючи білу тверду речовину. Тверду речовину перекристалізовували з DCM, одержуючи зазначену у заголовку сполуку у вигляді білої твердої речовини. Т.п.: 97,5 -98,5°С Анал. Розр.: С, 44,25; Н, 4,95; N, 11,47; S, 13,13 Анал. Знайд.: С, 44,28; Н, 4,66; N, 11,21; S, 13,15 1 Н ЯМР (DMSO d6) : 6,85 (m, 4H), 6,68 (bd s, 3H, NH), 4,28 (m, 2H), 3,97 (dd,J=6,9, 11,4 Гц, 1H), 3,20 (m, 1H), 3,10 (m, 1H). Приклад 3 (Бензо[1,3|діоксол-2-ілметил)сульфамід (Сполука № 2) Ортодіоксибензол (10,26 г, 93,2 ммоль), метоксид натрію (25% на вагу в метанолі, 40,3 г, 186 ммоль) та метил дихлорацетат (13,3 г, 93,2 ммоль) об'єднували в сухому метанолі (100 мл). Розчин нагрівали до кипіння зі зворотним холодильником протягом ночі. Реакційну суміш охолоджували до кімнатної температури, підкисляли додаванням концентрованої соляної кислоти та потім об'єм зменшували під вакуумом до приблизно 50 мл. Додавали воду та суміш екстрагували діетиловим ефіром (3х100 мл). Об'єднаний органічний розчин сушили MgSO4, концентрували до коричневої твердої речовини та хроматографували (2% етил ацетату в гексані), одержуючи метиловий ефір бензо[1,3]діоксол-2-карбонової кислоти у вигляді безбарвного масла. MS (ESI): 195,10 (М+Н+). 1 Н ЯМР (300 МГц, CDCl3) : 6,89 (ушир., 4Н), 6,29 (s, 1H), 4,34 (q, J=7 Гц, 2Н), 1,33 (t, J=7 Гц, 3Н). До метилового ефіру бензо[1,3]діоксол-2карбонової кислоти (7,21 г, 40,0 ммоль) додавали гідроксид амонію (29% у воді, 10 мл) та достатню кількість ацетонітрилу, щоб суміш стала однорідною (~5 мл). Розчин перемішували протягом двох годин при кімнатній температурі та потім додавали дистильовану воду. Амід бензо[1,3]діоксол-2 31 91680 32 карбонової кислоти осаджували у вигляді білої бавляли діетиловим ефіром (1 л) та 1 Ν HCl (1,2 речовини та збирали фільтруванням, та викорисл). Органічний шар відокремлювали та 2 рази товували без подальшого очищення. промивали 1 N HСІ (500 мл), 4 рази водою (150 MS (ESI): 160,00 (М+Н+) мл), один раз сольовим розчином, сушили 1 (MgSO4) та випарювали у вакуумі, одержуючи білу Н ЯМР (300 МГц, DMSO) : 7,99 (s, ушир., тверду речовину, яку очищали за допомогою 1H), 7,72 (s, ушир., 1H), 6,94 (m, 2H) 6,86 (m, 2Н), флеш колоночної хроматографії (Гепт:EА - 2:1), 6,30 (s, 1H). одержуючи (2S)-2,3-дигідро-бензо[1,4]діоксин-2Амід бензо[1,3]діоксол-2-карбонової кислоти ілметиловий ефір толуол-4-сульфонової кислоти у (5,44 г, 32,9 ммоль) розчиняли в теграгідрофурані вигляді білої твердої речовини. (THF, 100 мл). Алюмогідрид літію (LAН, 1 Μ в THF, Білу тверду речовину об'єднували з фталімі39,5 мл, 39,5 ммоль) повільно додавали до розчидом калію (14,4 г, 78 ммоль) в DMF (250 мл) та ну при кімнатній температурі. Реакційну суміш пенагрівали до кипіння зі зворотним холодильником ремішували при кімнатній температурі протягом 24 протягом 1 години, охолоджували до кімнатної годин. Додавали дистильовану воду, щоб нейтратемператури та виливали при сильному перемішулізували надлишок LAH. Додавали водний гідрокванні у воду (1,5 л) та перемішували протягом 30 сид натрію (3,0 М, 100 мл) та розчин екстрагували хв. Білу тверду речовину відфільтровували та твеетил ацетатом (3х100 мл). Об'єднаний органічний рду речовину промивали декілька разів водою, 2% розчин промивали водою та сушили над MgSO4. NaOH та знову водою та залишали сушитися на Розчинник випарювали, одержуючи Сповітрі, одержуючи (2S)-2-(2,3-Дигідробензо[1,3]діоксол-2-іл-метиламін у вигляді безбарбензо[1,4]діоксин-2-ілметил)-ізоіндол-1,3-діон у вного масла. вигляді білої порошкоподібної твердої речовини. MS (ЕSI): 152,1 (М+Н+) 1 Порошкоподібну білу тверду речовину об'єдН ЯМР (300 МГц, CDCl3) : 6,87 (m, 4Η), 6,09 нували з гідразином (2,75 г, 86 ммоль) в EtOH (225 (t, J=4 Гц, 1Н), 3,13 (d, J=4 Гц, 2Н). мл) та нагрівали при кипінні зі зворотним холодиС-Бензо[1,3]діоксол-2-іл-метиламін (2,94 г, льником протягом 2 годин, охолоджували до кім19,4 ммоль) та сульфамід (3,74 г, 38,9 ммоль) натної температури та додавали 1 N НСІ до рН 1,0 об'єднували в сухому діоксані (50 мл) та розчин та перемішували протягом 15 хв. Білу тверду ренагрівали до кипіння зі зворотним холодильником човину відфільтровували та промивали свіжим протягом ночі. Реакційну суміш концентрували та EtOH (тверду речовину відкидали) та фільтрат залишок хроматографували (від 2% до 10% ацевипарювали у вакуумі до твердої речовини, яку тону в дихлорметані), одержуючи зазначену у зарозділяли між діетиловим ефіром та розбавленим головку сполуку у вигляді білої твердої речовини. + водним NaOН. Розчин діетилового ефіру сушили MS (ESI): 230,0 (М+Н ) 1 (Na2SO4) та випаровували у вакуумі, одержуючи Н ЯМР (300 МГц, CDCl3) : 6,87 (m, 4H), 6,25 світло-жовте масло. Масло очищали за допомогою (t, J=4 Гц, 1H), 4,79 (ушир., 1Η), 4,62 (ушир., 1Η), флеш колоночної хроматографії (DCM:MeOH 3,64 (d, J=4 Гц, 2Н). 10:1), одержуючи масло. Частину масла (4,82 г, 29 Приклад 4 ммоль) в 2-пропанолі (250 мл) обробляли 1 N НСІ (2S)-(-)-N-(2,3-Дигідро-бензо[1,4]діоксин-2(30 мл) та нагрівали на паровій бані, поки суміш не ілметил)-сульфамід (Сполука № 4) стала однорідною, та потім залишали охолоджуватися до кімнатної температури. Через 3 години суміш охолоджували льодом протягом 2 годин. Білу шарувату тверду речовину (відповідна сіль НСІ (2S)-С-(2,3-Дигідро-бензо[1,4]діоксин-2-іл)метиламіну) відфільтровували та потім перекристалізовували з 2-пропанолу, одержуючи білу тверду речовину. Ортодіоксибензол (13,2 г, 0,12 моль) та карбо[ ]D=-69,6 (с=1,06, EtOH) нат калію (16,6 г, 0,12 моль) перемішували в DMF Білу тверду речовину розділяли між DCM та (250 мл) та додавали (2R)-гліцидил тозилат (22,8 г, розбавленим NaOH, тa DCΜ сушили (NaSO4) та 0,10 моль), та реакційну суміш перемішували при випарювали у вакуумі, одержуючи (2S)-С-(2,360°С протягом 24 годин. Реакційну суміш охолоДигідро-бензо[1,4]діоксин-2-іл)-метиламін у вигляді джували до кімнатної температури та розбавляли масла. льодяною водою (1 л) та екстрагували діетиловим [ ]D=-57,8 (с=1,40, СНСl3) ефіром (4 рази). Об'єднаний органічний розчин Масло (2,1 г, 12,7 ммоль) та сульфамід (2,44 г, тричі промивали 10% карбонатом калію, один раз 25,4 ммоль) кип'ятили зі зворотним холодильниводою, один раз сольовим розчином та випарюваком в діоксані (75 мл) протягом 2 годин та неочили у вакуумі, одержуючи білу тверду речовину, яку щений продукт очищали за допомогою флеш коочищали за допомогою флеш колоночної хроматолоночної хроматографії (DCM:MeOН 10:1), графії (DCM:Метанол - 50:1), одержуючи (2S)-2,3одержуючи білу тверду речовину, яку перекристадигідро-бензо[1,4]діоксин-2-іл)-метанол у вигляді лізовували з DCM, одержуючи зазначену у заголотвердої речовини. вку сполуку у вигляді білої кристалічної твердої Тверду речовину (13,3 г, 68 ммоль) розчиняли речовини. в піридині (85 мл), охолоджували до 0°С, додаваТ.п. 102-103°С ли п-толуолсульфоніл хлорид (13,0 г, 68 ммоль) [ ]D=-45,1° (c=1,05, Μ); реакційну суміш перемішували при кімнатній температурі протягом 20 годин. Реакційну суміш роз 33 91680 34 який розділяли між 1 N НСІ та діетиловим ефіром. Н ЯМР (DMSO d6) 6,86 (m, 4H), 6,81 (bd s, Водну фазу підлужували 1 N NaOH та екстрагува3H, NH), 4,3 (m, 2H), 3,97 (dd, J=6,9, 11,4 Гц, 1H), ли діетиловим ефіром. Органічну фазу сушили 3,20 (dd, J=5,5, 13,7 Гц, 1H), 3,10 (dd, J=6,9, 13,7 (MgSO4) та випарювали у вакуумі, одержуючи (2,3Гц, 1H). дигідро-бензо[1,4]діоксин-2-ілметил)-метил-амін у Aнал. Розр.: С, 44,25; H, 4,95; Ν, 11,47; S, вигляді масла. 13,13 MS 180 (МH+) Анал. Знайд.: С, 44,20; Η, 4,69; Ν, 11,40; S, 1 13,22. Н ЯМР (CDCl3) 6,85 (m, 4H), 4,30 (m, 2H), Приклад 5 4,02 (dd, J=7,9, 11,6 Гц, 1H), 2,85 (m, 2H), 2,50 (s, N-(2,3-Дигідро-бензо[1,4]діоксин-2-ілметил)3H). N',N'-диметилсульфамід (Сполука № 6) Масло (380 мг, 2,1 ммоль) та сульфамід (820 мг, 8,5 ммоль) об'єднували в діоксані (15 мл), кип'ятили зі зворотним холодильником протягом 1,5 годин та випарювали у вакуумі, одержуючи неочищений залишок. Залишок очищали за допомогою колоночної хроматографії (етил ацетат/гептан 1:1) та одержану тверду речовину перекристалізовували з етил ацетату/гексану, одержуючи зазначену у заголовку сполуку у вигляді білої твердої Рацемічний 2,3-дигідро-1,4-бензодіоксин-2речовини. ілметиламін (8,25 г, 5,0 ммоль) та триетиламін Т.п. 97-98°С (1,52 г, 15 ммоль) об'єднували в DMF (10 мл) та MS 257 (М-1) охолоджували на льодяній бані, поки додавали Анал. Розр.: С, 46,50; Н, 5,46; N, 10,85; S, диметилсульфамоїл хлорид (1,44 г, 10 ммоль). 12,41 Реакційну суміш потім перемішували протягом 3 Анал. Знайд.: С, 46,48; Н, 5,65; N, 10,90; S, годин, продовжуючи охолодження. Реакційну су12,07 міш розділяли між етил ацетатом та водою, та 1 Н ЯМР (CDCl3) 6,86 (m, 4H), 4,52 (bs, 2H), етил ацетатний розчин промивали сольовим роз4,46 (m, 1H), 4,29 (dd, J=2,3, 11,5 Гц, 1Η), 4,05 (dd, чином, сушили (MgSO4) та випарювали у вакуумі, J=6,5, 11,5 Гц, 1H), 3,51 (dd, J=6,7, 14,9 Гц, 1H), одержуючи масло. Масло очищали, використову3,40 (dd, J=5,9, 14,9 Гц, 1H), 2,99 (s, 3H). ючи флеш колоночну хроматографію (етил ацеПриклад 7 тат:гептан 1:1), одержуючи білу тверду речовину, (2S)-(-)-N-(6-Xлор)-2,3-дигідрояку перекристалізовували (етил ацетат/гексан), бензо[1,4]діоксин-2-ілметил)-сульфамід (Сполука одержуючи зазначену у заголовку сполуку у ви№ 8) гляді білої пластівчастої твердої речовини. Т.п. 76-78°С MS 273 (MH+) Анал. Розр.: С, 48,52; Н, 5,92; N, 10,29; S, 11,78 Анал. Знайд.: С, 48,63; Н, 5,62; N, 10,20; S, 11,90 Приклад 6 Слідуючи методиці, наведеній в Прикладі 4 N-(2,3-Дигідро-бензо[1,4]діоксин-2-ілметил)-Nвище, 4-хлорортодіоксибензол піддавали реакції, метилсульфамід (Сполука № 7) одержуючи суміш (2S)-C-(7-Xлор-2,3-дигідробензо[1,4]діоксин-2-іл)-метиламіну та (2S)-C-(6Xлор-2,3-дигідро-бензо[1,4]діоксин-2-іл)метиламіну (приблизно співвідношення 3:1 6хлор:7-хлор ізомерів за допомогою ОФ ВГРХ). Суміш розчиняли в 2-пропанолі (100 мл) та додавали 1 N HCl в діетиловому ефірі, поки рН не стало дорівнювати 1,0. Гідрохлоридну сіль, що Рацемічний 2,3-дигідро-1,4-бензодіоксин-2випала в осад, відфільтровували (2,65 г) та перекілметиламін (825 мг, 5 ммоль) розчиняли в етил ристалізовували з метанолу/ІРА, одержуючи білі форміаті (15 мл), кип'ятили зі зворотним холодикристали. Білі кристали розділяли між DCΜ та рольником протягом 30 хв та випарювали у вакуумі, збавленим NaOH. DCM сушили та випарювали у одержуючи Ν-(2,3-дигідро-бензо[1,4]діоксин-2вакуумі, одержуючи очищений (2S)-С-(6-Хлор-2,3ілметил)-формамід у вигляді масла. дигідро-бензо[1,4]діоксин-2-іл)-метиламін у вигляді Масло в діетиловому ефірі (25 мл) обробляли масла. 1 Μ LAН в THF (9,0 мл, 9,0 ммоль) при 0°С та пе[ ]D=-67,8 (c=1,51, СНСl3) ремішували протягом 5 годин при кімнатній темпеМасло (7,75 ммоль) та сульфамід (1,50 г, 15,5 ратурі. Реакційну суміш охолоджували на льодяній ммоль) об'єднували в діоксані (50 мл) та кип'ятили бані та гасили водою (0,50 мл), потім 3 N NaOH зі зворотним холодильником протягом 2,0 годин, (0,50 мл) та водою (0,50 мл). Суміш потім переміохолоджували до кімнатної температури та випашували при кімнатній температурі протягом 1 горювали у вакуумі, одержуючи тверду речовину. дини. Тверду речовину відфільтровували та фільПродукт очищали за допомогою флеш колоночної трат випарювали у вакуумі, одержуючи залишок, 1 35 91680 36 хроматографії, використовуючи DCM/метанол при кімнатній температурі протягом 20 годин. Реа20:1, одержуючи зазначену у заголовку сполуку у кцію гасили водою, перемішували протягом 2 говигляді білої твердої речовини. дин, розчин декантували, сушили (Na2SО4) та виMS 277 (М-1) парювали у вакуумі, одержуючи С-хроман-2-ілметиламін у вигляді маслянистого аміну. [ ]D=-59,9° (с=1,11, М) 1 Маслянистий амін (1,63 г, 10 ммоль) та сульН ЯМР (CDCl3) 6,90 (d, J=2,2 Гц, 1H), 6,81 фамід (1,92 г, 20 ммоль) об'єднували в діоксані (50 (m, 2H), 4,76 (m, 1H), 4,55 (s, 2H), 4,40 (m, 1H), 4,29 мл) та кип'ятили зі зворотним холодильником про(dd, J=2,4, 11,5 Гц, 1Н), 4,05 (dd, J=7,1, 11,5 Гц, тягом 2 годин. Розчин охолоджували та випарю1H), 3,45 (m, 2H). вали у вакуумі, одержуючи масло, яке очищали за Анал. Розр.: С, 38,78; Н, 3,98; Ν, 10,05 допомогою колоночної хроматографії Анал. Знайд.: С, 38,80; Н, 3,67; Ν, 9,99. (DCM:Meтанол 10:1), одержуючи білу тверду реФільтрати кристалізованої гідрохлоридної солі човину. Тверду речовину перекристалізовували з (2S)-C-(6-Хлор-2,3-дигідро-бензо[1,4]діоксин-2-іл)етил ацетату/гексану, одержуючи хроман-2метиламіну, одержаної вище, відновлювали (приілметилсульфамід у вигляді білої твердої речовиблизно 1:1 6-хлор:7-хлор ізомери) та випарювали ни. у вакуумі, одержуючи тверду речовину, яку роздіТ.п. 100-101°С ляли між DCM (200 мл) та розбавленим NaON (0,5 MS 241 (Μ-1) Μ, 50 мл). Розчин DCM промивали один раз соАнал. Розр.: С, 49,57; Н, 5,82; Ν, 11,56; S, льовим розчином, сушили (Na2SО4) та випарювали 13,23 у вакуумі, одержуючи масло, яке очищали за доАнал. Знайд.: С, 49,57; Н, 5,80; N, 11,75; S, помогою ОФ ВЕРХ (10-50% ACN з 0,16% TFA у 13,33. воді з 0,20% TFA), одержуючи (2S)-С-(7-Хлор-2,3Приклад 9 дигідро-бензо[1,4]діоксин-2-іл)-метиламін у вигляді Хроман-2-ілметилсульфамат (Сполука № 11) залишку. Залишок об'єднували з сульфамідом (0,90 г, 9,4 ммоль) в діоксані (25 мл) та кип'ятили зі зворотним холодильником протягом 2,5 годин, охолоджували до кімнатної температури та випарювали у вакуумі, одержуючи масло. Масло очищали за допомогою флеш колоночної хроматографії, використовуючи DCM/метанол - 10:1, одержуючи (2S)Хроман-2-карбонову кислоту (4,3 г, 24 ммоль) (-)-N-(7-Хлор-2,3-дигідро-бензо[1,4]діоксин-2в THF (70 мл) об'єднували з 1 Μ LAH в NHF (30 мл, ілметил)-сульфамід у вигляді білої твердої речо30 ммоль) та перемішували при кімнатній темпевини. -1 ратурі протягом 2 годин. Реакційну суміш гасили MS 277 (Μ ) 1 водою та потім перемішували протягом 2 годин. Н ЯМР (CDCl3/CD3OD) 6,88 (d, J=0,7 Гц, 1Η), Розчин THF декантували від твердої речовини, яку 6,81 (m, 2Η), 4,37 (m, 1H), 4,30 (dd, J=2,3, 11,6 Гц, промивали свіжим THF. Об'єднаний розчин THF 1H), 4,04 (dd, J=7,0, 11,6 Гц, 1H), 3,38 (m, 2H). сушили (Na2SО4) та випарювали у вакуумі, одерПриклад 8 жуючи хроман-2-іл-метанол у вигляді масла. Хроман-2-ілметилсульфамід (Сполука № 10) Хроман-2-іл-метанол (1,97 г, 12 ммоль) в DMF (30 мл) охолоджували на льодяній бані до приблизно 0°С під аргоном та об'єднували з 95% NaН (0.39 г, 15,6 ммоль), потім перемішували протягом 30 хв. Потім додавали сульфамоїл хлорид (2,78 г, 24 ммоль) та реакційну суміш перемішували протягом 1 години. Реакційну суміш розбавляли етил ацетатом (100 мл) та водою (100 мл). Етил ацетаХроман-2-карбонову кислоту (4,5 г, 25 ммоль) тний розчин відокремлювали та водну фазу двічі та НОВТ (3,86 г, 25 ммоль) об'єднували в DCM (40 екстрагували етил ацетатом. Об'єднану етил ацемл) та DMF (10 мл). При кімнатній температурі татну фазу сушили (MgSO4) та випарювали у вадодавали диметиламінопроніл етилкарбодіімід куумі, одержуючи масло, яке очищали за допомо(EDС, 4,84 г, 25 ммоль) та реакційну суміш перегою флеш колоночної хроматографії (етил мішували протягом 30 хв. Додавали гідроксид ацетат/гексан 1:2), одержуючи білу тверду речоамонія (2,26 мл, 33,4 ммоль) та реакційну суміш вину, яку перекристалізовували з етил ацетаперемішували протягом 16 годин. Реакційну суміш ту/гексану, одержуючи зазначену у заголовку спорозбавляли DCM (50 мл) та водою (50 мл) та рН луку у вигляді білої твердої речовини. суміші коректували до приблизно рН=3,0 1 N HCІ. Т.п. 87-90°С DCΜ відокремлювали та водну фазу двічі екстраMS [М-Н] 242,1 гували DCM. Об'єднану фазу DCM сушили Анал. Розр.: С, 49,37; Н, 5,39; N, 5,76; S, 13,18 (Na2SО4) та випарювали у вакуумі, одержуючи Aнал. Знайд.: С, 49,46; Н, 5,17; N, 5,72; S, масло, яке очищали за допомогою флеш колоноч13,09. ної хроматографії (етил ацетат), одержуючи масПриклад 10 ло. 2-(2,3-Дигідро-бензо[1,4]діоксин-2-іл)Масло (5,35 г, 30 ммоль) в ТНF (90 мл) переетилсульфамід (Сполука № 16) мішували, поки добавляли 1 Μ LAН в THF (36 мл, 36 ммоль), та реакційну суміш потім перемішували 37 Ціанід калію (2,05 г, 31,5 ммоль) додавали до 2-бромметил-(2,3-дигідробензо[1,4]діоксину) (6,87 г, 30 ммоль) в DMSO (90 мл) та перемішували при температурі навколишньою середовища протягом 20 годин. Реакційну суміш потім розбавляли водою (250 мл) та двічі екстрагували діетиловим ефіром. Діетиловий ефір промивали водою, потім двічі промивали сольовим розчином, сушили (Na2SО4) та випарювали у вакуумі, одержуючи 2ціанометил-(2,3-дигідробензо[1,4]діоксин) у вигляді білої твердої речовини. 1 Н ЯМР (CDCl3) 6,89 (m, 4H), 4,50 (m, 1H), 4,31 (dd, J=2,3, 11,5 Гц, 1H), 4,08 (dd, J=6,2, 11,6 Гц, 1H), 2,78 (d, J=6,1, Гц, 2H). 2-ціанометил-(2,3-дигідробензо[1,4]діоксин) розчиняли в THF (50 мл) та додавали 1 Μ ВН3 в THF (80 мл, 80 ммоль) та реакційну суміш кип'ятили зі зворотним холодильником протягом 5 годин, потім перемішували при температурі навколишнього середовища протягом 16 годин. При охолодженні на льодяній бані додавали 2Ν HCІ, поки не буде досягнутий pН=1,0. Реакційну суміш потім перемішували протя3 З N NaOH та діетиловим ефіром та розчин діетилового ефіру промивали сольовим розчином, сушили (Na2SО4) та випарювали у вакуумі, одержуючи неочищений 2-(2,3дигідробензо[1,4]діоксин-2-іл)етиламін. MS (M+H)+ 180. Неочищений 2-(2,3-дигідробензо[1,4|діоксин-2іл)етиламін в діоксані (100 мл) об'єднували з сульфамідом (3,0 г, 31 ммоль) та нагрівали до кипіння зі зворотним холодильником протягом 2 годин. Розчин охолоджували та випарювали у вакуумі, одержуючи оранжеву тверду речовину, яку очищали за допомогою колоночної хроматографії (DCM:MeOH - 10:1), одержуючи білу тверду речовину. Тверду речовину перекристалізовували з DCM, одержуючи зазначену у заголовку сполуку у вигляді твердої речовини. MS (M-1) 257 Т.п. 101-103°С (кор.) 1 Н ЯМР (CDCl3): 6,86 (m, 4H), 4,70 (m, 1H), 4,52 (s, 2H), 4,30 (m, 2H), 3,94 (dd, J=7,4, 11,3 Гц, 1Н), 3,43 (dd, J=6,4, 12,9 Гц, 2H), 1,94 (dd, J=6,5, 12,9, 2Н). Елементарний аналіз: Виміряно: С, 46,48; Н, 5,60; Ν, 10,81; S, 12,41 Розраховано: С, 46,50; Н, 5,46; Ν, 10,85; S, 12,41 Приклад 11 (2S)-(-)-N-(6,7-Дихлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)-сульфамід (Сполука № 29) 91680 38 4,5-Дихлоратехол (8,6 г, 48 ммоль) та карбонат калію (6,64 г, 48 ммоль) перемішували в DMF (200 мл). Додавали (2R)-гліцидил тозилат (9,12 г, 40 ммоль) та реакційну суміш перемішували при 60°С протягом 24 годин. Реакційну суміш охолоджували до кімнатної температури та потім розбавляли льодяною водою (600 мл) та екстрагували діетиловим ефіром (4 рази). Об'єднаний органічний розчин промивали 3 рази 10% карбонатом калію, двічі сольовим розчином, сушили (MgSO4) та випарювали у вакуумі, одержуючи (2S)-2-(6,7дихлор-2,3-дигідро-бензо[1,4]діоксин)метанол у вигляді в’язкого масла. (2S)-2-(6,7-дихлор-2,3-Дигідробензо[1,4]діоксин)метанол, у вигляді масла, (6,4 г, 27 ммоль) розчиняли в піридині (50 мл), охолодженому до 0°С. Потім додавали птолуолсульфоніл хлорид (5,2 г, 27 ммоль) та реакційну суміш перемішували при кімнатній температурі протягом 20 годин. Реакційну суміш розбавляли діетиловим ефіром та 1 N HCІ (750 мл) та органічний шар відокремлювали, та промивали 2 рази 1 N HCІ (250 мл), один раз водою (150 мл), двічі сольовим розчином, сушили (MgSO4) та випарювали у вакуумі, одержуючи (2S)-6,7-дихлор2,3-дигідро-бензо[1,4]діоксин-2-ілметиловий ефір толуол-4-сульфонової кислоти у вигляді світложовтої твердої речовини. 1 Н ЯМР (CDCl3): 7,79 (d, J=8,3 Гц, 2H), 7,36 (d, J=8,0 Гц, 2H), 6,94 (s, 1H), 6,83 (s, 1H), 4,37 (m, 1H), 4,2 (m, 3H), 4,03 (dd, J=6,3, 11,7 Гц, 1H), 2,47 (s, 3H). (2S)-6,7-дихлор-2,3-дигідро-бензо[1,4]діоксин2-ілметиловий ефір толуол-4-сульфонової кислоти (8,0 г, 20,5 ммоль) об'єднували з фталімідом калію (6,1 г, 33 ммоль) в DМF (75 мл) та нагрівали до кипіння зі зворотним холодильником протягом 1 години, охолоджували до кімнатної температури та виливали при сильному перемішуванні у воду (0,5 л) та потім перемішували протягом 30 хв. Білу тверду речовину відфільтровували та тверду речовину промивали декілька разів водою, 2% NaOH та знову водою, та потім залишали сушитися на повітрі, одержуючи (2S)-2-(6,7-дихлор-2,3-дигідробензо[1,4]діоксин-2-ілметил)-ізоіндол-1,3-діон (6,0 г, 80%) у вигляді білої порошкоподібної твердої речовини. Білу порошкоподібну тверду речовину об'єднували і гідразином (1,06 г, 33 ммоль) в ЕtOН (80 мл) та нагрівали при кипінні зі зворотним холодильником протягом 2 годин, потім охолоджували до кімнатної температури. Додавали 1 N НСІ, щоб скоректувати рН реакційної суміш до рН 1,0, та реакційну суміш потім перемішували протягом 15 хв. Білу тверду речовину відфільтровували та промивали свіжим ЕtOН (тверду речовину відкидали) та фільтрат випарювали у вакуумі до твердої речовини, яку розділяли між діетиловим ефіром та розбавленим водним NaOH. Розчин діетилового ефіру сушили (Na2SО4) та випарювали у вакуумі, одержуючи (2S)-2-амінометил-(6,7дихлор-2,3-дигідро-бензо[1,4]діоксин) у вигляді в'язкого масла. 39 91680 40 Н ЯМР (CDCl3): 6,98 (s, 1Н), 6,96 (s, 1Н), Зазначену у заголовку сполуку одержували ві4,25 (dd, J=2,0, 11,2 Гц, 1Н), 4,15 (m, 1H), 4,0 (m, дповідно до методики, описаної вище в Прикладі 1H), 2,97 (d, J=5,5 Гц, 2Н). 4, виходячи з 4-метилортодіоксибензолу, одержуЧастину масла (3,8 г, 16 ммоль) та сульфамід ючи білу тверду речовину, яку перекристалізову(3,1 г, 32,4 ммоль) кип'ятили зі зворотним холодивали з єтил ацетатy/гекеану, одержуючи зазначену льником в діоксані (100 мл) протягом 2 годин та у заголовку сполуку у вигляді білої твердої речонеочищений продукт очищали за допомогою флеш вини. колоночної хроматографії (DСМ:МеОН 20:1), одеMS [M-H] 257 ржуючи зазначену у заголовку сполуку у вигляді 1 білої твердої речовини, яку перекристалізовували Н ЯМР (CDCl3): 6,76 (m, 1H), 6,66 (m, 2H), з етил ацетату/гексану, одержуючи зазначену у 4,80 (m, 1H), 4,57 (bd s, 1H), 4,40 (m, 1H), 4,28 (m, заголовку сполуку у вигляді білої кристалічної тве1H), 4,03 (dd, J=6,9, 11,4 Гц, 1Н), 3,45 (m, 2H), 2,25 рдої речовини. (s, 3H). MS [M-H] 3111,0 Елементний аналіз: Т.п. 119-121°С Розраховано: С, 46,50; Н, 5,46; Ν, 10,85; S, 12,41 [ ]D=-53,4° (c=1,17, M) 1 Знайдено: С, 46,65; Н, 5,60; Ν, 10,84; S, 12,61. Н ЯМР (DMSO d6): 7,22 (s, 1H), 7,20 (s, 1H), Приклад 14 6,91 (bd s, 1H), 6,68 (bd s, 2H), 4,35 (m, 2H), 4,05 6,7-Дихлор-2,3-дигідро-бензо[1,4]діоксин-2(dd, J=6,5, 11,5 Гц, 1H), 3,15 (m, 2H). ілметиловий ефір сульфамінової кислоти (Сполука Елементний аналіз: № 27) Виміряно: С, 34,52; Η, 3,22; Ν, 8,95; СІ, 22,64; S, 10,24 Розраховано: С, 34,64; Н, 2,68; Ν, 8,87; СІ, 22,94; S, 10,35. Приклад 12 (2S)-(-)-N-(7-Aміно-2,3-дигідробензо[1,4]діоксин-2-ілметил)-сульфамід (Сполука № 36) (2S)-6,7-дихлор-2,3-дигідро-бензо[1,4]діоксин2-ілметанол (2,0 г, 8,5 ммоль), одержаний відповідно до методики, описаної вище в Прикладі 11, в DMF (20 мл) охолоджували на льодяній бані. Потім під аргоном додавали 95% гідриду натрію (0,28 г, 11 ммоль) та реакційну суміш перемішували протягом 30 хв. Додавали сульфамоїл хлорид (1,97 г, 17 ммоль) та реакційну суміш перемішува(2S)-(-)-N-(2,3-Дигідро-7-нітроли при охолодженні на льодяній бані. Через 1 гобензо[1,4]діоксин-2-ілметил)-сульфамід (1,2 г, 4,15 дину реакційну суміш розбавляли водою (50 мл) та ммоль) одержували з 4-нітроортодіоксибензолу тричі екстрагували етил ацетатом. Об'єднаний відповідно до способу, наведеному в Прикладі 4. етил ацетат промивали сольовим розчином, су(2S)-(-)-N-(2,3-Дигідро-7-нітро-бензо[1,4]діоксин-2шили (Na2SО4) та випарювали у вакуумі до масла, ілметил)-сульфамід потім об'єднували з 10% Pd/C яке очищали за допомогою флеш колоночної хров метанолі (120 мл) та струшували під атмосфематографії (етил ацетат/гептан 1:1), одержуючи рою водню (39 фунт/дюйм2) при кімнатній темпебілу тверду речовину. Білу іверу речовину перекратурі протягом 3 годин. Тверді речовини відфільристалізовували з бензолу, одержуючи зазначену тровували та промивали 10% Μ в DCM та у заголовку сполуку у вигляді білої твердої речофільтрат випарювали у вакуумі, одержуючи невини. очищений продукт. Неочищений продукт розчиняТ.п. 109-111°С ли в 0,2 N НСІ (25 мл), заморожували та ліофілізуMS [M-H] 312 вали, одержуючи зазначену у заголовку сполуку у 1 Н ЯМР (DMSO d6) 7,65 (s, 2Н), 7,26 (s, 1H), вигляді білої шаруватої твердої речовини у формі 7,25 (s, 1H), 4,58 (m, 1H), 4,41 (dd, J=2,5, 11,7 Гц, відповідної гідрохдоридної солі. 1H), 4,28 (m, 2H), 4,11 (dd, J=6,9, 11,7 Гц, 1H). MS (M+H)+ 260 1 Приклад 15 Н ЯМР (DMSO d6): 10,2 (bd s, 3H), 6,86 (m, 6-Хлор-2,3-дигідро-бензо[1,4]діоксин-21H), 6,85 (s, 1H), 6,74 (dd ,J=2,5, 8,4 Гц, 1H), 4,22 ілметиловий ефір сульфамінової кислоти (Сполука (m, 2H), 3,88 (dd, J=6,7, 11,4 Гц, 1H), 3,04 (m, 2H). № 12) Приклад 13 (2S)-(-)-N-(7-Метил-2,3-дигідробензо[1,4]діоксин-2-ілметил)-сульфамід (Сполука № 19) 1 (2S)-6-Хлор-2,3-дигідро-бензо[1,4]діоксин-2ілметанол (6,4 г, 32 ммоль), одержаний відповідно 41 91680 42 до методики, яка описана вище в Прикладі 7, в Значення ЕD50 тестової сполуки (розраховане, DMF (80 мл) охолоджували на льодяній бані. Поколи це було придатним) становило розраховану тім під аргоном протягом 20 хв додавали 95% гіддозу, потрібну для блокування компоненту тонічриду нагрію (1,06 г, 42 ммоль) та реакційну суміш ного екстензора задньої кінцівки нападу, викликаперемішували протягом 30 хв. Протягом 10 хв доною MEШ, у 50% протестованих гризунів. Для роздавали сульфамоїл хлорид (7,4 г, 64 ммоль) та рахунку ЕD50 та 95% фідуціальних меж (ФМ) був реакційну суміш перемішували при охолодженні на використаний пробіт-аналіз. льодяній бані. Через 1 годину реакційну суміш роХарактерні сполуки заданим винаходом були збавляли водою (300 мл) та тричі екстрагували протестовані відповідно до методики, описаної етил ацетатом. Об'єднаний етил ацетат промивавище, з результатами, наведеними в Таблиці 4 ли сольовим розчином, сушили (MgSO4) та випанижче. Результати представлені як співвідношенрювали у вакуумі, одержуючи масло, яке очищали ня кількості мишей з відверненим тонічним розтяза допомогою флеш колоночної хроматографії гуванням усього тіла до загальної кількості протес(етил ацетат/гексан 1:2), одержуючи білу тверду тованих мишей за заданий час (при заданому рівні речовину. Білу тверду речовину 3 рази перекрисдозування тестової сполуки). талізовували з бензолу, одержуючи зазначену у заголовку сполуку у вигляді білої твердої речовиТаблиця 4 ни. Т.п. 113-116°С МЕШ активність у мишей MS [M-H] 278 № МШИ активність [ ]D=-41,0° (с=1,32, Μ) 1 1 2/4 за 1 год (300 мг/кг) Н ЯМР (CDCl3) 6,91 (d, J=1,9 Гц, 1H), 6,84 2 4/4 за 2 год (100 мг/кг) (m, 2H), 4,82 (bd s, 2H), 4,50 (m, 1H), 4,41 (m, 2H), 4,31 (dd, J=2,3, 11,6 Гц, 1H), 4,12 (dd, J=6,3, 11,6 3 2/3 за 1 год (300 мг/кг) Гц, 1H). 4 5/5 за 1 год (300 мг/кг) Елементний аналіз: 5 1/5 за 2 год (300 мг/кг) Виміряно: С, 38,57; Η, 3,42; Ν, 4,92; S, 11,53 6 4/5 за 0,5 год (300 мг/кг) Розраховано: С, 38,65; Η, 3,60; Ν, 5,01; S, 7 3/3 за 0,5 год (300 мг/кг) 11,46 8 3/5 за 3 год (100 мг/кг) Приклад 16 9 1/5 за 1 год (300 мг/кг) Аналіз in vivo: тест максимальним електрошо10 1/5 за 1 год (100 мг/кг) ком (MEШ) 11 4/5 за 1 год (100 мг/кг) Протисудомна активність була визначена за 12 3/5 за 4 год (100 мг/кг) допомогою тесту MEШ, який проводили відповідно 13 2/5 за 0,5 год (10 мг/кг) до методики, детально описаної нижче Swinyard 14 3/5 за 4 год (100 мг/кг) EA, Woodhead JH, White HS, Franklin MR. 15 Неактивна при 100 мг/кг Experimental selection, quantification, and evaluation of anticonvulsants. In Levy RH, et al., eds. 16 5/5 за 0,5 год (300 мг/кг) Antiepileptic Drugs. 3rd ed. New York: Raven Press, 17 4/5 за 0,5 год (100 мг/кг) 1989:85-102. 18 Неактивна при 100 мг/кг Мишей-альбіносів чоловічої статі CF-1 (25-35 19 5/5 за 0,5 год (300 мг/кг) г) не годували протягом 16 годин до початку про20 1/5 за 2 год (100 мг/кг) ведення тесту. Мишей до контрольної та тестової 21 5/5 за 2 год (100 мг/кг) груп вибирали за методом випадкових чисел, тва22 1/5 за 4 год (100 мг/кг) ринам давали дозу основи або тестової сполуки у 23 Неактивна при 100 та 300 мг/кг різних концентраціях, відповідно. У день дослі24 5/5 за 4 год (300 мг/кг) дження, за 30 хвилин до того, як піддати їх шоку, 25 5/5 за 4 год (100 мг/кг) мишам перорально вводили дозу основи (0,5% 26 Неактивна при 100 та 300 мг/кг метилцелюлози) або тестової сполуки (100-300 27 5/5 за 4 год (100 мг/кг) мг/кг). Напади викликали електричним шоком че28 4/5 за 4 год (100 мг/кг) рез роговицю, використовуючи перемінний струм у 29 3/5 за 4 год (100 мг/кг) 60 Гц, 50 мА, протягом 0,2 с. Мишей у тестових групах піддавали електричному стимулюванню з 30 1/5 за 0,5 год (100 мг/кг) інтервалами часу від 15 хвилин до 4 годин після 31 3/5 за 0,5 год (100 мг/кг) введення тестової сполуки. Шок призводив до не32 Неактивна при 100 та 300 мг/кг гайного тонічного розтягування всього тіла. Тест 33 1/3 за 2 год (300 мг/кг) було закінчено, коли спостерігався весь курс кон34 Неактивна при 100 та 300 мг/кг вульсій (типово, менш, ніж через 1 хвилину після 35 Неактивна при 100 мг/кг електричної стимуляції), а мишей після цього не36 Неактивна при 100 та 300 мг/кг гайно умертвляли шляхом інгаляції діоксиду вуглецю. Приклад 17 За кінцеву точку тесту було прийнято видаЯк конкретне втілення пероральної композиції, лення з нападу компоненту тонічного екстензора 100 мі Сполуки № 8, одержаної, як описано в Приусього тіла. Відсутність цього компоненту вказувакладі 7, змішували з достатньою кількістю тонко ла на здатність тестової сполуки запобігати пошидиспергованої лактози, щоб забезпечити загальну ренню розряду нападу через нервову тканину. 43 91680 44 кількість від 580 до 590 мг для заповнення твердих з метою ілюстрації, слід розуміти, що застосування гелевих капсул розміром 0. винаходу включає всі звичайні варіації, адаптації Тоді як вищенаведений опис викладає принта/або модифікації, які входять в межі наступної ципи даного винаходу, з прикладами, наведеними формули винаходу, та їх еквівалент. Комп’ютерна верстка О. Гапоненко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюSulfamate and sulfamide derivatives for the treatment of epilepsy and related disorders
Автори англійськоюMccomsey David F., Parker Michael N., Reitz Alen B., Maryanoff Bruce E.
Назва патенту російськоюПроизводные сульфаматов и сульфамидов для лечения эпилепсии и сопутствующих расстройств
Автори російськоюМакКомси Девид Ф., Паркер Майкл Н., Рейтц Ален Б., Марьянофф Брюс Э.
МПК / Мітки
МПК: A61K 31/353, C07D 321/00, C07D 319/00, C07D 317/58, C07D 311/58, A61K 31/357, A61P 25/08
Мітки: сульфамідів, епілепсії, лікування, розладів, сульфаматів, похідні, супутніх
Код посилання
<a href="https://ua.patents.su/22-91680-pokhidni-sulfamativ-ta-sulfamidiv-dlya-likuvannya-epilepsi-ta-suputnikh-rozladiv.html" target="_blank" rel="follow" title="База патентів України">Похідні сульфаматів та сульфамідів для лікування епілепсії та супутніх розладів</a>
Попередній патент: Роз’ємне з’єднання та пристрій для ін’єкцій
Наступний патент: Косметичне використання електромагнітного випромінювання
Випадковий патент: Форсунка












