Оксициклогексил-4н,6н-5-окса-2,3,10b-триазабензо[e]азулени як антагоністи v1a
Формула / Реферат
1. Сполука формули І
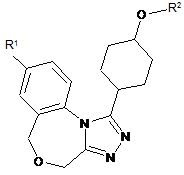 , І
, І
у якій:
R1 є атомом галогену, та
R2 вибраний з групи, що складається з:
і) гетероарилу, незаміщеного або заміщеного замісниками в кількості від 1 до 3, індивідуально вибраними з групи, що складається з ОН, галогену, ціано, С1-6-алкілу, С1-6-алкокси, галоген-С1-6-алкілу, галоген-С1-6-алкокси, С1-6-алкоксі-С1-6-алкілу і гідроксі-С1-6-алкілу;
іі) арилу, незаміщеного або заміщеного замісниками в кількості від 1 до 3, індивідуально вибраними з групи, що складається з ОН, атома галогену, ціано, С1-6-алкілу, С1-6-алкокси, галоген-С1-6-алкілу, галоген-С1-6-алкокси, С1-6-алкоксі-С1-6-алкілу і гідроксі-С1-6-алкілу;
ііі) С3-7-циклоалкілу, незаміщеного або заміщеного замісниками в кількості від 1 до 3, індивідуально вибраними з групи, що складається з ОН, атома галогену, ціано, С1-6-алкілу, С1-6-алкокси, галоген-С1-6-алкілу, галоген-С1-6-алкокси, С1-6-алкоксі-С1-6-алкілу і гідроксі-С1-6-алкілу; та
iv) С1-6-алкілу, незаміщеного або заміщеного замісниками в кількості від 1 до 3, індивідуально вибраними з групи, що складається з ОН, атома галогену, ціано, С1-6-алкокси і галоген-С1-6-алкокси;
або її фармацевтично прийнятні солі.
2. Сполука за п. 1, в якій R1 є атомом хлору.
3. Сполука за будь-яким з пп. 1 або 2, в якій R2 вибраний з групи, що складається з незаміщеного гетероарилу, незаміщеного арилу, незаміщеного С3-7-циклоалкілу і незаміщеного С1-6-алкілу.
4. Сполука за будь-яким з пп. 1-3, в якій R2 вибраний з піридинілу, піразинілу, фенілу, циклопентилу, ізопропілу та втор-бутилу.
5. Сполука за будь-яким з пп. 1-4, вибрана з групи, що складається з:
8-хлор-1-(4-ізопропоксициклогексил)-4Н,6Н-5-окса-2,3,10b-триазабензо[е]азулену,
1-(4-втор-бутоксициклогексил)-8-хлор-4Н,6Н-5-окса-2,3,10b-триазабензо[е]азулену,
8-хлор-1-(4-циклопентилоксициклогексил)-4Н,6Н-5-окса-2,3,10b-триазабензо[е]азулену,
8-хлор-1-(4-феноксициклогексил)-4Н,6Н-5-окса-2,3,10b-триазабензо[е]азулену,
8-хлор-1-[4-(піридин-2-ілокси)циклогексил-4H,6Н-5-окса-2,3,10b-триазабензо[e]азулену та
8-хлор-1-[4-(піразин-2-ілокси)циклогексил]-4Н,6Н-5-окса-2,3,10b-триазабензо[е]азулену
або їх фармацевтично прийнятних солей.
6. Спосіб одержання сполуки формули І, як визначено в будь-якому з пп. 1-5, що включає взаємодію сполуки формули II із сполукою формули III з одержанням сполуки формули І:
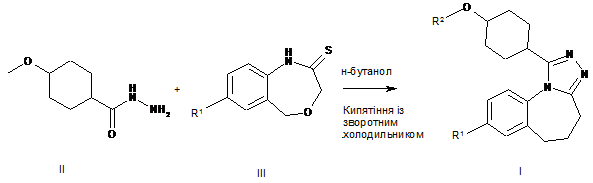 ,
,
де R1 та R2 є такими, як визначено в будь-якому з пп. 1-4.
7. Сполука формули І за будь-яким з пп. 1-5, одержана способом, як визначено в п. 6.
8. Сполука формули І за будь-яким з пп. 1-5 для застосування як терапевтично активної речовини.
9. Сполука формули І за пп. 1-5 для застосування як терапевтично активної речовини для терапевтичного та/або профілактичного лікування захворювань і розладів, пов'язаних з антагонізмом рецептора V1a.
10. Сполука формули І за пп. 1-5 для застосування як терапевтично активної речовини, що має периферичну і центральну дії при наступних станах: дисменорея, чоловіча або жіноча статева дисфункція, гіпертензія, хронічна серцева недостатність, неадекватна секреція вазопресину, цироз печінки, нефротичний синдром, тривожність, депресивні розлади, обсесивно-компульсивний розлад, розлади аутистичного спектра, шизофренія і агресивна поведінка.
11. Фармацевтична композиція, що містить сполуку формули І за будь-яким з пп. 1-5 і фармацевтично прийнятний носій та/або фармацевтично прийнятну допоміжну речовину.
12. Застосування сполуки формули І за будь-яким з пп. 1-5 для одержання лікарського засобу, що має периферичну і центральну дії при наступних станах: дисменорея, чоловіча або жіноча статева дисфункція, гіпертензія, хронічна серцева недостатність, неадекватна секреція вазопресину, цироз печінки, нефротичний синдром, тривожність, депресивні розлади, обсесивно-компульсивний розлад, розлади аутистичного спектра, шизофренія і агресивна поведінка.
13. Спосіб застосування сполуки за будь-яким з пп. 1-5, що має периферичну і центральну дії при наступних станах: дисменорея, чоловіча або жіноча статева дисфункція, гіпертензія, хронічна серцева недостатність, неадекватна секреція вазопресину, цироз печінки, нефротичний синдром, тривожність, депресивні розлади, обсесивно-компульсивний розлад, розлади аутистичного спектра, шизофренія і агресивна поведінка, де даний спосіб включає введення сполуки формули І людині або тварині.
Текст
Реферат: У даному винаході запропоновані 4Н,6Н-5-окса-2,3,10b-триазабензо[е]азулени, що діють як модулятори рецептора V1a, зокрема як антагоністи рецептора Via, їх одержання, фармацевтичні композиції, що їх містять, та їх застосування як лікарських засобів. Активні сполуки за даним винаходом корисні як терапевтичні засоби, периферично активні і центрально активні при наступних станах: дисменорея, чоловіча або жіноча статева дисфункція, гіпертензія, хронічна серцева недостатність, неадекватна секреція вазопресину, цироз печінки, нефротичний синдром, тривожність, депресивні розлади, обсесивно-компульсивний розлад, розлади аутистичного спектра, шизофренія і агресивна поведінка. UA 111623 C2 (12) UA 111623 C2 O R2 R1 N O N N І UA 111623 C2 5 10 У даному винаході запропоновані 4H,6H-5-окса-2,3,10b-триаза-бензо[e]азулени, що діють як модулятори рецептора V1a, і, зокрема, як антагоністи рецептора V1a, їх одержання, фармацевтичні композиції, що їх містять, та їх застосування як лікарських засобів. Сполуки за даним винаходом корисні як терапевтичні засоби, периферично-активні і центрально-активні при наступних станах: дисменорея, чоловіча або жіноча статева дисфункція, гіпертензія, хронічна серцева недостатність, неадекватна секреція вазопресину, цироз печінки, нефротичний синдром, тривожність, депресивні розлади, обсесивно-компульсивний розлад, розлад аутистичного спектру, шизофренія і агресивна поведінка. Область техніки У даному винаході запропонована сполука формули I 2 O R 1 R N O 15 20 25 30 35 40 45 50 N N I, у якій замісники і змінні групи є такими, як описано нижче та у формулі винаходу, або її фармацевтично прийнятна сіль. Дані сполуки є антагоністами рецептора V1a, корисними для лікування депресії. Попередній рівень техніки Вазопресином є 9-амінокислотний пептид, в основному, продукований паравентрикулярним ядром гіпоталамуса. На периферії вазопресин діє як нейрогормон і стимулює вазоконстрикцію, глікогеноліз і антидіурез. Відомі три рецептори вазопресину, що належать до класу I рецепторів, спряжених з Gбілком. Рецептор V1a експресується в головному мозку, печінці, гладкій мускулатурі кровоносних судин, легені, матці і сім’янику, рецептор V1b або V3 експресується в головному мозку і наднирковій залозі, рецептор V2 експресується в нирках, де він регулює реабсорбцію води і опосередковує антидіуретичні ефекти вазопресину (Robben, et al. (2006). Am J Physiol Renal Physiol. 291, F257-70, "Cell biological aspects of the vasopressin type-2 receptor and aquaporin 2 water channel in nephrogenic diabetes insipidus"). Сполуки, що мають активність при рецепторі V2, можуть, таким чином, викликати побічні дії на гомеостаз крові. Рецептор окситоцину відноситься до сімейства рецепторів вазопресину і опосередковує дії нейрогормона окситоцину в головному мозку і на периферії. Вважають, що окситоцин виявляє центральні анксіолітичні ефекти (Neumann (2008). J Neuroendocrinol. 20, 858-65, "Brain oxytocin: a key regulator of emotional and social behaviours in both females and males"). Отже, антагонізм центрального рецептора окситоцину може приводити до анксіогенних ефектів, які розглядають як небажані побічні ефекти. В головному мозку вазопресин діє як нейромодулятор, і його рівень підвищується в мигдалеподібному тілі під час стресу (Ebner, et al. (2002). Eur J Neurosci. 15, 384-8., "Forced swimming triggers vasopressin release within the amygdala to modulate stress-coping strategies in rats"). Відомо, що життя в умовах стресу може ініціювати тяжку депресію і тривожність (Kendler, et al. (2003). Arch Gen Psychiatry, 60, 789-96, "Life Event Dimensions of Loss, Humiliation, Entrapment, and Danger in the Prediction of Onsets of Major Depression and Generalized Anxiety"), і що обидва ці стани мають дуже високу коморбідність, причому, тривожність часто передує тяжкій депресії (Regier, et al. (1998). Br J Psychiatry Suppl. 24-8, "Prevalence of anxiety disorders and their comorbidity with mood and addictive disorders"). Рецептор V1a обширно експресується в головному мозку, і, зокрема, в лімбічних зонах, таких як мигдалеподібне тіло, латеральна перегородка і гіпокамп, які відіграють важливу роль в регуляції тривожності. Дійсно, у нокаутмишей за V1a виявляється зменшення тривожної поведінки в плюс-лабіринті, відкритому полі і темно-світлій камері (Bielsky, et al. (2004). Neuropsychopharmacology. 29, 483-93, "Profound impairment in social recognition and reduction in anxiety-like behavior in vasopressin V1a receptor knockout mice"). Знижуюча регуляція рецептора V1a з використанням ін'єкції антисмислового олігонуклеотиду в перегородку також викликає зменшення тривожної поведінки (Landgraf, et al. (1995). Regul Pept. 59, 229-39., "V1 vasopressin receptor antisense oligodeoxynucleotide into septum reduces vasopressin binding, social discrimination abilities, and anxiety-related behavior in rats"). Вазопресин або рецептор V1a також залучені в інші нейрофізіологічні розлади: генетичні 1 UA 111623 C2 5 10 15 20 25 30 35 40 45 50 55 60 дослідження недавно виявили зчеплення поліморфізму послідовності в промоторі рецептора V1a людини з розладами аутистичного спектру (Yirmiya, et al. (2006). 11, 488-94, "Association between the arginine vasopressin 1a receptor (AVPR1a) gene and autism in a family-based study: mediation by socialization skills"), Було показано, що інтраназальне введення вазопресину впливає на агресію у чоловіків (Thompson, et al. (2004). Psychoneuroendocrinology. 29, 35-48, "The effects of vasopressin on human facial responses related to social communication"), і було виявлено, що рівні вазопресину підвищені у пацієнтів з шизофренією (Raskind, et al. (1987). Biol Psychiatry. 22, 453-62, "Antipsychotic drugs and plasma vasopressin in normals and acute schizophrenic patients"), та у пацієнтів з обсесивно-компульсивним розладом (Altemus, et al. (1992). Arch Gen Psychiatry. 49, 9-20, "Abnormalities in the regulation of vasopressin and corticotropin releasing factor secretion in obsessive-compulsive disorder"). Рецептор V1a також опосередковує серцево-судинні ефекти вазопресину в головному мозку за рахунок центрального регулювання кров'яного тиску і частоти серцевих скорочень в ядрі одиночного шляху (Michelini and Morris (1999). Ann N Y Acad Sci. 897, 198-211, "Endogenous vasopressin modulates the cardiovascular responses to exercise"). На периферії він індукує скорочення гладких м'язів кровоносних судин, і постійне інгібування рецептора V1a поліпшує гемодинамічні параметри у пацюків з інфарктом міокарду (Van Kerckhoven, et al. (2002). Eur J Pharmacol. 449, 135-41, "Chronic vasopressin V(1A) but not V(2) receptor antagonism prevents heart failure in chronically infarcted rats"). Отже, очікується, що антагоністи V1a, що мають покращене проникнення через гематоенцефалічний бар'єр, мають перевагу. Показали, що антагоніст рецептора вазопресину V1a ефективний при зменшенні дисменореї в клінічних умовах (Brouard, et al. (2000). Bjog. 107, 614-9, "Effect of SR49059, an orally active V1a vasopressin receptor antagonist, in the prevention of dysmenorrhoea"). Антагонізм рецептора V1a також задіяний в лікуванні жіночої статевої дисфункції (Aughton, et al. (2008). Br J Pharmacol. doi:10.1038/bjp.2008.253, "Pharmacological profiling of neuropeptides on rabbit vaginal wall and vaginal artery smooth muscle in vitro"). У недавньому дослідженні було висунуто припущення, що антагоністи рецептора V1a відіграють терапевтичну роль як в еректильній дисфункції, так і в передчасній еякуляції (Gupta, et al. (2008). Br J Pharmacol. 155, 118-26, "Oxytocin-induced contractions within rat and rabbit ejaculatory tissues are mediated by vasopressin V(1A) receptors and not oxytocin receptors"). Детальний опис винаходу Об'єктом даного винаходу є сполука формули I та її фармацевтично прийнятні солі, одержання вищезазначених сполук, що містять їх лікарські препарати та їх одержання, а також застосування вищезазначених сполук при терапевтичному та/або профілактичному лікуванні захворювань і розладів, пов'язаних з модуляцією рецептора V1a, і, зокрема, з антагонізмом рецептора V1a. Наступним об'єктом винаходу є розробка селективних інгібіторів рецептора V1a, оскільки очікується, що селективність до рецептора V1a додає низький потенціал індукції небажаних, не пов'язаних з мішенню побічних ефектів, таких як обговорені раніше. Дані сполуки корисні як терапевтичні засоби, що мають периферичну і центральну дію, при наступних станах: дисменорея, чоловіча або жіноча статева дисфункція, гіпертензія, хронічна серцева недостатність, неадекватна секреція вазопресину, цироз печінки, нефротичний синдром, тривожність, депресивні розлади, обсесивно-компульсивний розлад, розлад аутистичного спектру, шизофренія і агресивна поведінка. Конкретними свідченнями відносно даного винаходу є наступні свідчення: лікування тривожності, депресивних розладів, обсесивнокомпульсивного розладу, розладів аутистичного спектру, шизофренії і агресивної поведінки. Наведені нижче визначення загальних термінів, використовуваних в даному винаході, застосовні незалежно від того, зустрічаються обговорювані терміни окремо чи в комбінації з іншими групами. Термін " C1-6-алкіл", окремо або в комбінації з іншими групами, означає вуглеводневий радикал, який може бути нормальним або розгалуженим, з одним або декількома розгалуженнями, де алкільна група, як правило, включає від 1 до 6 атомів вуглецю, наприклад, метил (Me), етил (Et), пропіл, ізопропіл (i-пропіл), н-бутил, i-бутил (ізобутил), 2-бутил (вторбутил), t-бутил (трет-бутил), ізопентіл, 2-етил-пропіл, 1,2-диметил-пропіл і тому подібне. Конкретні групи “ C1-6-алкіл” мають від 1 до 4 атомів вуглецю. Певними групами є групи ізопропіл та втор-бутил. Термін “галоген-C1-6-алкіл”, окремо або в комбінації з іншими групами, відноситься до C1-6алкілу, як визначено в даній роботі, заміщеному одним або декількома атомами галогену, зокрема, 1-5 атомами галогену, конкретніше 1-3 атомами галогену (“галоген-C1-3-алкіл”), зокрема, одним атомом галогену або 3 атомами галогену. Конкретним атомом галогену є атом фтору. Конкретний “галоген- C1-6-алкіл” є фтор- C1-6-алкіл. 2 UA 111623 C2 5 10 15 20 25 30 35 40 45 50 55 60 Термін “гідрокси-C1-6-алкіл”, окремо або в комбінації з іншими групами, відноситься до C1-6алкілу, як визначено в даній роботі, заміщеному однією абодекількома групами -OH, зокрема, 1-2 групами -OH, конкретніше однією групою -OH. Термін “ C1-6-алкокси-C1-6-алкіл”, окремо або в комбінації з іншими групами, відноситься до C1-6-алкілу, як визначено в даній роботі, заміщеному одній або множинними групами C1-6алкокси, як визначено в даній роботі, зокрема, 1-2 C1-6-алкоксигрупами, конкретніше однією C1-6алкоксигрупою. Термін “ціано”, окремо або в комбінації з іншими групами, відноситься до групи N≡C-(NC-). Термін “гідрокси”, окремо або в комбінації з іншими групами, відноситься до групи -OH. Термін "атом галогену", окремо або в комбінації з іншими групами, позначає атом хлору (Cl), йоду (I), фтору (F) і брому (Br). Зокрема “атомом галогену” є Cl та F. Переважно галогеном є Cl. Термін “арил", окремо або в комбінації з іншими групами, відноситься до ароматичної карбоциклічної групи, що містить від 6 до 14, зокрема, від 6 до 10, атомів вуглецю, і що має щонайменше одне ароматичне кільце або декілька конденсованих кілець, в яких щонайменше одне кільце є ароматичним. Приклади “арильних” груп включають бензил, дифеніл, інданіл, нафтил, феніл (Ph) і тому подібне. Переважною “арильною” групою є феніл. Термін "гетероарил", окремо або в комбінації з іншими групами, відноситься до ароматичної карбоциклічної групи, що має одне 4-8-членне кільце або декілька конденсованих кілець, що містять від 6 до 14, зокрема, від 6 до 10 кільцевих атомів, і таких що містять 1, 2 або 3 гетероатоми, індивідуально вибраних з N, O та S, зокрема, N та O, причому, в цій групі щонайменше одне карбоциклічне кільце є ароматичним. Приклади "гетероарильних" груп включають наступні групи: бензофурил, бензоімідазоліл, 1H-бензоімідазоліл, бензооксазиніл, бензоксазоліл, бензотіазиніл, бензотіазоліл, бензотієніл, бензотриазоліл, фурил, імідазоліл, індазоліл, 1H-індазоліл, індоліл, ізохінолініл, ізотіазоліл, ізоксазоліл, оксазоліл, піразиніл, піразоліл (піразил), 1H-піразоліл, піразоло[1,5-a]піридиніл, піридазиніл, піридиніл, піримідиніл, піроліл, хінолініл, тетразоліл, тіазоліл, тієніл, триазоліл, 6,7-дигідро-5H-[1]піридиніл і тому подібне. Зокрема, "гетероарильними" групами є піридиніл і піразиніл, переважними є піридин-2іл та піразин-2-іл. Термін " C1-6-алкокси", окремо або в комбінації з іншими групами, позначає -O-C1-6-алкільний радикал, який може бути нормальним або розгалуженим, з одиночним або множинним розгалуженням, в якому алкільна група, як правило, включає від 1 до 6 атомів вуглецю, наприклад, метокси (OMe, MeO), етокси (OEt), пропокси, ізопропокси (i-пропокси), н-бутокси, iбутокси (ізо-бутокси), 2-бутокси (втор-бутокси), t-бутокси (трет-бутокси), ізопентилокси (iпентилокси) і тому подібне. Конкретні групи “ C1-6-алкокси” мають від 1 до 4 атомів вуглецю (“C14-алкокси”). Термін “галоген- C1-6-алкокси”, окремо або в комбінації з іншими групами, відноситься до групи C1-6-алкокси, як визначено в даній роботі, заміщеній одним або декількома атомами галогену, зокрема, атомом фтору. Переважною групою “галоген-C1-6-алкокси” є фтор-C1-6алкокси. Термін “ C3-7-циклоалкіл” позначає одновалентну насичену моноциклічну або біциклічну вуглеводневу групу з кільцевих атомів вуглецю в кількості від 3 до 6. Біциклічна група означає групу, що складається з двох насичених карбоциклів, що мають один або більше загальних атомів вуглецю. Конкретні групи C3-6-циклоалкільні є моноциклічними. Прикладами моноциклічного циклоалкіла є наступні групи: циклопропіл, циклобутаніл, циклопентил, циклогексил або циклогептіл. Прикладами біциклічних циклоалкільних груп є біцикло[2.2.1]гептаніл або біцикло[2.2.2]октаніл. Конкретним прикладом “ C3-7-циклоалкільної” групи є циклопропіл. Термін "фармацевтично прийнятні солі" відноситься до солей, які підходять для застосування в контакті з тканинами людей і тварин. Прикладами відповідних солей з неорганічними і органічними кислотами є, але не обмежені ними, солі з наступними кислотами: оцтовою кислотою, лимонною кислотою, мурашиною кислотою, фумаровою кислотою, соляною кислотою, молочною кислотою, малеїновою кислотою, яблучною кислотою, метансульфоновою кислотою, азотною кислотою, фосфорною кислотою, пара-толуолсульфоновою кислотою, янтарною кислотою, сірчаною кислотою, сірчистою кислотою, винною кислотою, трифторооцтовою кислотою і тому подібне. Конкретними кислотами є мурашина кислота, трифторооцтова кислота і соляна кислота. Переважними кислотами є соляна кислота, трифторооцтова кислота і фумарова кислота. Терміни “фармацевтично прийнятний носій” і “фармацевтично прийнятна допоміжна речовина” відносяться до носіїв і допоміжних речовин, таким як розчинники або ексципієнти, 3 UA 111623 C2 5 10 15 20 25 30 35 40 45 50 55 сумісні з іншими інгредієнтами препарату. Термін "фармацевтична композиція" має на увазі продукт, що містить зазначені інгредієнти в зумовлених кількостях або долях, а також будь-який продукт, який є результатом, прямо або побічно, об'єднання зазначених інгредієнтів у зазначених кількостях. Зокрема, цей термін включає продукт, що містить один або декілька активних інгредієнтів, і необов'язкового носія, що включає інертні інгредієнти, а також будь-який продукт, який є результатом, прямо або побічно, об'єднання, комплексоформування або агрегації будь-яких двох або більше інгредієнтів, або дисоціацію одного або декількох інгредієнтів, або інші типи реакцій або взаємодій одного або декількох інгредієнтів. Термін “половинна максимальна інгибіторна концентрація” (IC50) позначає концентрацію конкретної сполуки, необхідну для одержання 50% інгібувань біологічного процесу in vitro. Значення IC50 можна логарифмічно перетворити в значення pIC50 (-log IC50), в яких більш високі значення указують на експоненціально вищу ефективність. Значення IC50 не є абсолютною величиною, а залежить від експериментальних умов, наприклад, від використовуваних концентрацій. Значення IC50 можна перетворити в абсолютну константу інгібування (Ki), використовуючи рівняння Ченга-Прусоффа (Biochem. Pharmacol. (1973) 22:3099). Термін “константа інгібування” (Ki) означає абсолютну спорідненість зв’язування конкретного інгібітора з рецептором. Її вимірюють, використовуючи аналізи конкурентного зв’язування, і вона рівна концентрації, при якій конкретний інгібітор займав би 50% рецепторів, якщо відсутній конкуруючий ліганд (наприклад, радіоліганд). Значення Ki можна логарифмічно перетворити в значення pKi (-log Ki), в яких більш високі значення указують на експоненціально вищу ефективність. Термін “антагоніст” позначає сполуку, зменшуючу або запобігаючу дію іншої сполуки, як визначено, наприклад, в роботі Goodman and Gilman's “The Pharmacological Basis of Therapeutics, 7th ed.” На сторінці 35, Macmillan Publ. Company, Canada, 1985. Зокрема, антагоністи відносяться до сполуки, що ослабляє дію агоніста. “Конкурентний антагоніст” зв'язується з тим же сайтом рецептора, що і агоніст, але не активує рецептор, блокуючи, таким чином, дію агоніста. “Неконкурентний антагоніст” зв'язується з алостерічним (не агоністичним) сайтом на рецепторі, запобігаючи активації рецептора. “Оборотний антагоніст” нековалентно зв'язується з рецептором, і, отже, його можна “відмити”. “Необоротний антагоніст” ковалентно зв'язується з рецептором, і не може бути витиснений якими-небудь конкурентними лігандами або відмиванням. “Терапевтично ефективна кількість” позначає кількість сполуки, яка при введенні суб'єктові для лікування хворобливого стану, є достатньою, щоб здійснити таке лікування хворобливого стану. “Терапевтично ефективна кількість” варіює залежно від сполуки, хворобливого стану, якій піддається лікуванню, тяжкості захворювання, яке піддається лікуванню, віку і відносного стану здоров'я суб'єкта, шляху і форми введення, думки лікаря-куратора або ветеринара та від інших факторів. Термін “як визначено в даному описі” та “як розкрито в даному описі” при віднесенні до змінної групи включає за допомогою посилання, як широке визначення цієї змінної групи, так і конкретні, конкретніші і найбільш конкретніші визначення, якщо вони є. Терміни “обробка”, “приведення в контакт” та “взаємодія” при віднесенні до хімічної реакції означають додавання або змішування двох або більше реагентів у відповідних умовах з одержанням зазначеного та/або бажаного продукту. Зрозуміло, що реакція, яка дає зазначений та/або бажаний продукт, може необов'язково бути прямим результатом об'єднання двох реагентів, які були спочатку додані, тобто може існувати одна або більше проміжних сполук, які утворюються в суміші, що зрештою приводить до утворення зазначеного та/або цільового продукту. Термін “ароматичний” означає традиційну ідею ароматичності, визначену в літературі, зокрема, в документі IUPAC - Compendium of Chemical Terminology, 2nd, A. D. Mcnaught & A. Wilkinson (Eds). Blackwell Scientific Publications, Oxford (1997). Термін “фармацевтично прийнятний ексципієнт” позначає будь-який інгредієнт, що не володіє терапевтичною активністю, і що є нетоксичним, такий як розпушувачі, зв'язуючі речовини, наповнювачі, розчинники, буфери, тонічні агенти, стабілізатори, антиоксиданти, поверхнево-активні речовини (ПАР) або змащуючі речовини, вживані при приготуванні фармацевтичних препаратів. Зокрема, в даному винаході запропоновані сполуки загальної формули I 4 UA 111623 C2 2 O R 1 R N O 5 10 15 20 25 30 35 40 45 50 N N I, в якій 1 R є атомом галогену, та 2 R вибраний з групи, яка складається з: i) гетероарилу, незаміщеного або заміщеного замісниками в кількості від 1 до 3, індивідуально вибраними з групи, що складається з OH, атома галогену, ціано, C1-6-алкілу, C1-6алкокси, галоген-C1-6-алкілу, галоген-C1-6-алкокси, C1-6-алкокси-C1-6-алкілу і гідрокси-C1-6-алкіл; ii) арилу, незаміщеного або заміщеного замісниками в кількості від 1 до 3, індивідуально вибраними з групи, що складається з OH, атома галогену, ціано, C1-6-алкілу, C1-6-алкокси, галоген-C1-6-алкілу, галоген-C1-6-алкокси, C1-6-алкокси-C1-6-алкілу і гідрокси-C1-6-алкілу; iii) C3-7-циклоалкілу, незаміщеного або заміщеного замісниками в кількості від 1 до 3, індивідуально вибраними з групи, що складається з OH, атома галогену, ціано, C1-6-алкілу, C1-6алкокси, галоген-C1-6-алкілу, галоген-C1-6-алкокси, C1-6-алкокси-C1-6-алкілу і гідрокси-C1-6-алкілу; та iv) C1-6-алкілу, незаміщеного або заміщеного замісниками в кількості від 1 до 3, індивідуально вибраними з групи, що складається з OH, атома галогену, ціано, C1-6-алкокси і галоген-C1-6-алкокси; або її фармацевтично прийнятні солі. 1 Одним втіленням винаходу є сполука, яка має формулу I, в якій R є атомом хлору. 2 Одним втіленням винаходу є сполука формули I, в якій R вибраний з групи, що складається з незаміщеного гетероарилу, незаміщеного арилу, незаміщеного C3-7-циклоалкілу і незаміщеного C1-6-алкілу. 2 Одним втіленням винаходу є сполука формули I, в якій R вибраний з піридинілу, піразинілу, фенілу, циклопентилу, ізопропілу та втор-бутилу. 2 Одним втіленням винаходу є сполука формули I, в якій R вибраний з піридин-2-ілу, піразин2-ілу, фенілу, циклопентилу, ізопропілу та втор-бутилу. 2 Одним втіленням винаходу є сполука формули I, в якій R є гетероарилом. 2 Одним втіленням винаходу є сполука формули I, в якій R є піридинілом. 2 Одним втіленням винаходу є сполука формули I, в якій R є піразинілом. 2 Одним втіленням винаходу є сполука формули I, в якій R є арилом. 2 Одним втіленням винаходу є сполука формули I, в якій R є фенілом. 2 Одним втіленням винаходу є сполука формули I, в якій R є C3-7-циклоалкілом. 2 Одним втіленням винаходу є сполука формули I, , в якій R є циклопентилом. 2 Одним втіленням винаходу є сполука формули I, в якій R є C1-6-алкілом. 2 Одним втіленням винаходу є сполука формули I, в якій R є ізопропілом. 2 Одним втіленням винаходу є сполука формули I, в якій R є втор-бутилом. Одним втіленням винаходу є сполука формули I, вибрана з групи, що складається з: 8-хлор-1-(4-ізопропокси-циклогексил)-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азулену, 1-(4-втор-бутокси-циклогексил)-8-хлор-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азулену, 8-хлор-1-(4-циклопентилокси-циклогексил)-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азулену, 8-хлор-1-(4-фенокси-циклогексил)-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азулену, 8-хлор-1-[4-(піридин-2-ілокси)-циклогексил]-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азулену, та 8-хлор-1-[4-(піразин-2-ілокси)-циклогексил]-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азулену або її фармацевтично прийнятних солей. Одним втіленням винаходу є сполука формули I, 8-хлор-1-(4-ізопропокси-циклогексил), що є-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азуленом. Одним втіленням винаходу є сполука формули I, 1-(4-втор-бутокси-циклогексил), що є-8хлор-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азуленом. Одним втіленням винаходу є сполука формули I, 8-хлор-1-(4-циклопентилокси-циклогексил), що є-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азуленом. Одним втіленням винаходу є сполука формули I, 8-хлор-1-(4-фенокси-циклогексил), що є 5 UA 111623 C2 5 10 15 20 25 30 35 40 45 50 4H,6H-5-окса-2,3,10b-триаза-бензо[e]азуленом. Одним втіленням винаходу є сполука формули I, 8-хлор-1-[4-(піридин-2-ілокси)циклогексил], що є-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азуленом. Одним втіленням винаходу є сполука формули I, 8-хлор-1-[4-(піразин-2-ілокси)-циклогексил], що є-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азуленом. Одним втіленням винаходу є спосіб синтезу сполука формули I, як розкрито в даному описі, що включає взаємодію сполуки формули II, із сполукою формули III, з одержанням сполуки формули I. 1 2 в якому R та R є такими, як визначено в данному описі. Одним втіленням винаходу є сполука формули I, у будь-якому випадку одержана способом, визначеним в даній роботі. Одним втіленням винаходу є сполука формули I, вживана як терапевтично активна речовина. Одним втіленням винаходу є сполука формули I, вживана як терапевтично активна речовина для терапевтичного та/або профілактичного лікування захворювань і розладів, пов'язаних з антагонізмом рецептора V1a. Одна форма здійснення винаходу є сполука формули I, вживана як терапевтично активна речовина, що має периферичну і центральну дії при наступних станах: дисменорея, чоловіча або жіноча статева дисфункція, гіпертензія, хронічна серцева недостатність, неадекватна секреція вазопресину, цироз печінки, нефротичний синдром, тривожність, депресивні розлади, обсесивно-компульсивний розлад, розлади аутистичного спектру, шизофренія і агресивна поведінка. Одне втілення винаходу є фармацевтичною композицією, що містить сполуку формули I, як розкрито в даному описі, і фармацевтично прийнятний носій та/або фармацевтично прийнятна допоміжна речовина. У одному втіленні винаходу запропоновано застосування сполуки формули I, як розкрито в даному описі, для одержання лікарського засобу периферичної і центральної дії при наступних станах: дисменорея, чоловіча або жіноча статева дисфункція, гіпертензія, хронічна серцева недостатність, неадекватна секреція вазопресину, цироз печінки, нефротичний синдром, тривожність, депресивні розлади, обсесивно-компульсивний розлад, розлади аутистичного спектру, шизофренія і агресивна поведінка. У одному втіленні винаходу запропонований спосіб застосування сполуки, як розкрито в даному описі, що має периферичну і центральну дії при наступних станах: дисменорея, чоловіча або жіноча статева дисфункція, гіпертензія, хронічна серцева недостатність, неадекватна секреція вазопресину, цироз печінки, нефротичний синдром, тривожність, депресивні розлади, обсесивно-компульсивний розлад, розлади аутистичного спектру, шизофренія і агресивна поведінка, де даний спосіб включає введення сполуки формули I людині або тварині. Крім того, винахід включає всі оптичні ізомери, тобто діастереоізомери, діастереомерні суміші, рацемічні суміші, всі їх відповідні енантіомери та/або таутомери, а також їх сольвати, сполук формули I. Сполуки формули I можуть містити один або більш асиметричних центрів, і, отже, можуть існувати у вигляді рацематів, рацемічних сумішей, окремих енантіомерів, діастереомерних сумішей та індивідуальних діастереомерів. Додаткові асиметричні центри можуть бути присутніми залежно від природи різних замісників на молекулі. Кожен такий асиметричний центр незалежно утворює два оптичні ізомери, і мають на увазі, що всі можливі оптичні ізомери і діастереомери у вигляді сумішей та у вигляді чистих або частково очищених сполук включені в об'єм даного винаходу. Мають на увазі, що в об'єм даного винаходу включені всі такі ізомерні форми цих сполук. Незалежні синтези цих діастереомерів або їх хроматографічні розділення можуть бути досягнуті, як відомо в даній області техніки, шляхом відповідної модифікації 6 UA 111623 C2 5 10 методології, розкритої в даній роботі. Їх абсолютна стереохімія може бути визначена за допомогою рентгенокристалографії кристалічних продуктів або кристалічних проміжних сполук, які є дериватизованими при необхідності реагентом, що містить асиметричний центр, який має відому абсолютну конфігурацію. За бажанням рацемічні суміші сполук можуть бути розділені так, щоб виділити індивідуальні енантіомери. Це розділення можна здійснити способами, добре відомими в даній області техніки, такими як поєднання рацемічної суміші сполук з енантіомерно чистою сполукою з утворенням діастереомерної суміші з подальшим розділенням індивідуальних діастереомерів стандартними способами, такими як фракційна кристалізація або хроматографія. Це застосовно, зокрема, до алкілциклогексилефірної кінцевій групі (HG; від англ. head group) сполук формули I, а саме 2 O R 4 1 15 20 25 30 35 40 45 HG 2 у якій щонайменше атоми вуглецю 1 і 4 є асиметричними атомами вуглецю, і R може додатково містити асиметричні атоми вуглецю. Зрозуміло, що в об'єм даного винаходу включені всі індивідуальні стереоізомери кінцевих груп та їх суміші. Приклади цих кінцевих груп HG зображені нижче, конкретним прикладом є HG-4. Крім того, зрозуміло, що всі втілення винаходу, розкриті в даній роботі, можна комбінувати один з одним. У тих втіленнях, в яких запропоновані оптично чисті енантіомери, оптично чистий енантіомер означає, що сполука містить більше 90 мас.% бажаного ізомеру, зокрема, більше 95 мас.% бажаного ізомеру, або конкретніше більше 99 мас.% бажаного ізомеру, де масовий відсоток заснований на сумарній масі ізомеру (ізомерів) сполуки. Хірально чисті або хірально збагачені сполуки можуть бути одержані шляхом стереоселективного синтезу або шляхом розділення енантіомерів. Розділення енантіомерів може бути виконане на кінцевому продукті або альтернативно на відповідній проміжній сполуці. Сполуки формули I можуть бути одержані відповідно до приведених нижче схем. Початкова речовина є у продажу абоможе бути одержана відповідно до відомих способів. Будь-які визначені вище залишки і змінні групи мають все те ж визначене вище значення, якщо не зазначене інше. Сполуки формули I можуть бути одержані за допомогою ряду шляхів синтезу, наприклад, як проілюстровано на схемах нижче. Одержання сполук формули I за даним винаходом може бути виконано в послідовних або конвергентних шляхах синтезу. Синтези сполук за винаходом представлені на наведених нижче схемах. Навички, необхідні для проведення взаємодії і очищення одержаних в результаті продуктів, відомі фахівцям в даній області техніки. Замісники і індекси, використовувані в наведеному нижче описі способів, мають значення, наведене в даній роботі нижче, якщо не зазначене протилежне. Конкретніше сполуки формули I можуть бути одержані наведеними нижче способами, способами, наведеними в прикладах, або аналогічними способами. Відповідні умови реакції для індивідуальних стадій реакцій відомі фахівцям в даній області техніки. Послідовність реакцій не обмежена послідовністю, зображеною на схемах, описаних нижче, проте, залежно від початкових речовин та їх відповідної реакційної здатності послідовність стадій реакцій може бути вільно змінена. Початкові речовини або є у продажу, або можуть бути одержані способами, 7 UA 111623 C2 аналогічними наведеним нижче способам, способами, розкритими в посиланнях, що цитуються в описі або в прикладах, або способами, відомими в даній області техніки. У певному втіленні сполуки формули (I) за винаходом можуть бути одержані способом, що включає стадію взаємодії сполуки формули (II) 5 2 R O H N NH2 O II із сполукою формули (III) S H N 1 R 10 O III 1 2 з одержанням сполуки формули (I), в якій R та R є такими, як визначено в даній роботі для формули I. Ці способи описані детальніше наведеними нижче загальними схемами і методами A-G. 2 2 R O H N R S H N O N N + NH2 N 1 R O O 1 R II 15 III O I Схема 1: Загальна схема A Сполуки формули (I) можуть бути одержані шляхом термоконденсації гідразидного похідного формули (II), та тіолактамного похідного формули (III). Синтез сполук формули (II) зображений на схемах C-G нижче. Сполуки формули (III) можуть бути одержані, слідуючи загальній схемі B, як розкрито в даному описі нижче. Загальна схема A додатково проілюстрована нижче загальним методом V. 20 25 30 Схема 2: Загальна схема B Тіолактамні похідні формули (III-1) можуть бути одержані, як описано нижче: Ацилування 2амінобензилового спирту формули (a) з одержанням бромацетаміду (BrCOCH2Br) формули (b) може бути досягнуте в умовах реакції Шоттена-Баумана (у двофазних водних умовах, наприклад, водного карбонату натрію (aq Na2CO3)) при кількісному виході. В результаті циклізації сполуки формули (b), трет-бутоксидом калію i(KOtBu) в 2-пропанолі (2- PrOH) при низьких температурах одержують сполуки формули (c). Тіолактамне похідне формули (III) одержують шляхом обробки сполуки формули (c) реагентом Лавессона (2,4-біс-(4метоксифеніл)-1,3,2,4-дитиадифосфетан-2,4-дисульфідом) або пентасульфідом фосфору при 8 UA 111623 C2 підвищеній температурі у відповідному розчиннику (наприклад, в тетрагідрофурані (ТГФ)). 5 10 15 20 25 Схема 3: Загальна схема C Складноефірні похідні 4-алкокси-циклогексанкарбонової кислоти формули (VII-1) можуть бути одержані шляхом відновної етерифікації, як описано нижче: Складний ефір 4-гідроксициклогексанкарбонової кислоти (IV) перетворюють в складний ефір 4-триметилсиланілоксициклогексанкарбонової кислоти (V) способами O-силілування, відомими в даній області техніки, наприклад, шляхом обробки силілуючим агентом, таким як триметилсилілхлорид (ТМС-Cl) або триметилсиліл трифлат (ТМС-OTf), у присутності основи, такої як імідазол або 2,6-лутидин, у відповідному розчиннику, такому як N,N-диметилформамід (ДМФ) або дихлорметан (CH2l2). Послідовна обробка складного ефіру 4-триметилсиланілокси-циклогексанкарбонової кислоти (V) і кетону або альдегіду формули (VI) триметилсилілтрифлатом в дихлорметані і поновлюючим агентом, таким як триетилсилан (Et3SiH), приводить до складноефірних похідних 4-алкокси-циклогексанкарбонової кислоти формули (VII-1) при кімнатній температурі (КТ). Сполуки формули (VII-1) зазвичай одержують у вигляді суміші цис- та транс-ізомерів, які в деяких випадках можна розділити хроматографічно з одержанням чистого складного ефіру транс-4-алкокси-циклогексанкарбонової кислоти формули (VII-1a) і складного ефіру цис-4алкокси-циклогексанкарбонової кислоти формули (VII-1b). Загальна схема C нижче додатково проілюстрована загальним методом I. Схема 4: Загальний метод D Альтернативно складноефірні похідні 4-алкокси-циклогексанкарбонової кислоти формули (VII-1) можуть бути одержані шляхом відновної етерифікації, як описано нижче: В результаті послідовної обробки алкокси-триметилсилану формули (IX) та етилового ефіру 4 9 UA 111623 C2 5 10 15 20 25 циклогексанонкарбонової кислоти (X) триметилсилілтрифлатом в дихлорметані і поновлюючим агентом, таким як триетилсилан, одержують складноефірні похідні 4-алкоксициклогексанкарбонової кислоти формули (VII-1). Сполуки формули (VII-1) зазвичай одержують у вигляді суміші цис- та транс-ізомерів, які в деяких випадках можна розділити хроматографічно з одержанням чистого складного ефіру транс-4-алкокси-циклогексанкарбонової кислоти формули (VII-1a) і складного ефіру цис-4-алкокси-циклогексанкарбонової кислоти формули (VII-1b). Алкокси-триметилсиланові похідні формули (IX) або є у продажу, або їх одержують, використовуючи способи O-силілування, відомі в даній області техніки, наприклад, шляхом обробки спирту, що має загальну формулу (VIII), силілуючим агентом, таким як триметилсилілхлорид або триметилсилілтрифлат, у присутності основи, такої як імідазол або 2,6-лутидин, у відповідному розчиннику, такому як N,N-диметилформамід або дихлорметан. Альтернативно алкокси-триметилсиланові похідні формули (IX) можуть бути одержані in situ без виділення перед стадією відновної етерифікації етиловим ефіром 4-циклогексанонкарбонової кислоти (X) шляхом обробки спирту загальної формули (VIII) триметилсилілтрифлатом і 2,6лутидином в дихлорметані. Загальна схема D нижче додатково проілюстрована загальними методами IIA і IIB. Схема 5: Загальна схема E Етерифікація складного ефіру 4-гідрокси-циклогексанкарбонової кислоти формули (IV) фенольним похідним формули (XI) в умовах реакції Міцунобу (диетилазодикарбоксилат (DEAD; від англ. diethylazodicarboxylate) та трифенілфосфін ((PPh3)) приводить до складного ефіру 4арилокси-циклогексанкарбонової кислоти формули (VII-2) при інверсії конфігурації. Таким чином, складні ефіри транс-4-арилокси-циклогексанкарбонової кислоти формули (VII-2a) одержують з складного ефіру цис-4-гідрокси-циклогексанкарбонової кислоти формули (IV-a), тоді як складні ефіри цис-4-арилокси-циклогексанкарбонової кислоти формули (VII-2b), одержують з складного ефіру транс-4-гідрокси-циклогексанкарбонової кислоти формули (IV-b). Загальна схема E нижче додатково проілюстрована загальним методом IIIA. 30 35 40 Схема 6: Загальна схема F 2 Сполуки формули (VII-3) (сполуки формули (VII), в яких R є гетероарилом), можуть бути одержані з складного ефіру 4-гідрокси-циклогексанкарбонової кислоти формули (IV), і гетероарилхлориду формули (XII) у присутності каталітичної або стехіометричної кількості метансульфінату натрію і основи, такої як карбонат калію (K2CO3), в диметилформаміді (ДМФ) при 120 °C або у присутності системи каталізаторів, утвореної з йодиду міді (CuI) і 1,10фенантроліну, і основи, такої як карбонат цезію (Cs2CO3), в толуолі при кип'ятінні із зворотним холодильником. Загальна схема F нижче додатково проілюстрована загальними методами IIIB і IIIC. 10 UA 111623 C2 5 10 15 20 25 30 35 40 45 Схема 7: Загальна схема G Складний ефір 4-алкокси- або арилоксициклогексанкарбонової кислоти формули (VII) може бути перетворений в гідразидне похідне формули (II) шляхом нагрівання з гідратом гідразину у відповідному розчиннику, такому як н-бутанол (n-BuOH). Альтернативно складноефірне похідне формули (VII) можна гідролізувати до карбоновокислотного похідного формули (XIII), використовуючи двофазну суміш водного розчину гідроксиду натрію або калію (NaOH або KOH) і ефірного розчинника, такого як діоксан. Гідразидне похідне формули (II) може бути одержано шляхом активації кислотного похідного формули (XIII), наприклад, етилхлорформіатом, тіонілхлоридом, оксалілхлоридом або реагентом амідного поєднання (таким як триетиламін (Et3N)), і подальшого поєднання з гідразином. Загальна схема G нижче додатково проілюстрована загальним методом IV. Відповідні фармацевтично прийнятні солі з кислотами можуть бути одержані стандартними способами, відомими фахівцям в даній області техніки, наприклад, шляхом розчинення сполуки формули I у відповідному розчиннику, такому як, наприклад, діоксан або ТГФ, і додавання відповідної кількості відповідної кислоти. Продукти можуть бути зазвичай виділені фільтруванням або хроматографією. Перетворення сполуки формули I у фармацевтично прийнятну сіль з основою може бути виконано шляхом обробки такої сполуки такою основою. Одним з можливих способів утворення такої солі є, наприклад, додавання 1/n еквівалентів основної солі, такої як, наприклад, M(OH)n, в якій M = катіон металу або амонію, і n = число гідроксидних аніонів, до розчину сполуки у відповідному розчиннику (наприклад, в етанолі, в суміші етанол-вода, в суміші тетрагідрофуран-вода) і видалення розчинника випаровуванням або ліофілізацією. Конкретними солями є гідрохлорид, форміат і трифторацетат. Якщо їх одержання не описане в прикладах, сполуки формули I, а також всі проміжні продукти можуть бути одержані аналогічними способами або способами, розкритими в даній роботі. Початкові речовини є у продажу, відомі в даній області техніки або можуть бути одержані способами, відомими в даній області техніки, або по аналогії з ними. Зрозуміло, що сполуки загальної формули I за даним винаходом можуть бути дериватизовані за функціональними групами з одержанням похідних, здібних до зворотного перетворення в початкову сполуку in vivo. Фармакологічні тести Рецептор V1a людини клонували за допомогою полімеразної ланцюгової реакції із зворотною транскрипцією (ЗТ-ПЛР) з сумарної РНК печінки людини. Кодуюча послідовність була субклонована в експресійному векторі після секвенування для підтвердження ідентичності ампліфікованої послідовності. Щоб продемонструвати спорідненість сполук за даним винаходом до рецептора V1a, проводили дослідження зв’язування. Препарати клітинних мембран готували з клітин HEK293, транзитно трансфікованих експресійним вектором і вирощених в 20-літрових ферментерах, за наведеним нижче протоколом. 50 г клітин ресуспендують в 30 мл свіжоприготованого, охолодженого в льоді буфера для лізису (50 мм 4-(2-гідроксиетил)-1-піперазин етансульфонова кислота (ГЕПЕС), 1 мм етилендіамінтетраоцетова кислота (ЕДТА), 10 мм MgCl2, доведено до pH= 7,4 + повна суміш інгібіторів протеаз (Roche Diagnostics)). Гомогенізують за допомогою Polytron протягом 1 хвилини і озвучують ультразвуком на льоду протягом 2x2 хвилин при 80% інтенсивності (ультразвуковий апарат Vibracell). Препарат центрифугують протягом 20 хвилин при 500хg при 4 °C, осад відкидають, і супернатант центрифугують протягом 1 години при 43000хg при 4 °C 11 UA 111623 C2 5 10 15 (19000об/хв). Осад ресуспендують в 12,5 буфера для лізису +12,5 мл 20% сахарози і гомогенізують, використовуючи Polytron, протягом 1-2 хвилин. Концентрацію білка визначають методом Бредфорда, і аліквоти зберігають при -80 °C до використання. Для досліджень зв’язування 60 міліграм гранул силікату ітрію SPA (Amersham) змішують з аліквотою мембрани в зв'язуючому буфері (50 мм Тріс, 120 мМ NaCl, 5 мМ KCl, 2 мМ CaCl2, 10 мМ MgCl2) протягом 15 хвилин при перемішуванні. Потім 50 мкл суміші гранул/мембран додають в кожну лунку 963 лункового планшета з подальшим додаванням 50 мкл 4 нМ H-вазопресину (American . Radiolabeled Chemicals) Для вимірювання сумарного зв’язування 100 мкл зв'язуючого буфера додають у відповідні лунки, для неспецифічного зв’язування 100 мкл 8,4 мМ холодного (неміченого) вазопресину і для тестування сполуки 100 мкл серійного розведення кожної сполуки в 2% диметилсульфоксиді (ДМСО). Планшет інкубують протягом 1 години при кімнатній температурі, центрифугують протягом 1 хвилини при 1000хg і рахують на лічильнику Packard Top-Count. Рахунок неспецифічного зв’язування віднімають з кожної лунки, і дані нормалізують за максимальним специфічним зв’язуванням, що приймається за 100%. Для обчислення IC50 криву приводять у відповідність, використовуючи модель нелінійної регресії (XLfit), і Ki обчислюють, використовуючи рівняння Ченга-Прусоффа. Наведені нижче репрезентативні дані показують антагоністичну активність сполук згідно даного винаходу проти рецептора V1a людини: Приклад Структура pKi hV1a O N N 1 N 7,72 O Cl O N 2 N 8,36 N O Cl O 3 9,39 N N N Cl O 12 UA 111623 C2 O 4 8,88 N N N O Cl N O 5 8,63 N N N O Cl N N O 6 7,57 N N N Cl 5 10 15 20 O Таблиця 1: Значення pKi вибраних прикладів Фармацевтичні композиції Сполуки формули I та їх фармацевтично прийнятні солі можна застосовувати як терапевтично активні речовини, наприклад, у формі фармацевтичних препаратів. Фармацевтичні препарати можна вводити перорально, наприклад, у формі пігулок, пігулок з покриттям, драже, твердих і м'яких желатинових капсул, розчинів, емульсій або суспензій. Введення можна, проте, також здійснювати ректально, наприклад, у формі супозиторіїв, або парентерально, наприклад, у формі ін'єкційних розчинів. Сполуки формули I та їх фармацевтично прийнятні солі можна обробляти фармацевтично інертними, неорганічними або органічними носіями, призначеними для одержання фармацевтичних препаратів. Лактозу, кукурудзяний крохмаль або його похідні, тальк, стеаринові кислоти або їх солі і тому подібне можна використовувати, наприклад, як такі носії для пігулок, пігулок з покриттям, драже і твердих желатинових капсул. Відповідними носіями для м'яких желатинових капсул є, наприклад, рослинні масла, віск, жири, напівтверді і рідкі поліоли і тому подібне. Проте, залежно від природи активної речовини у разі м'яких желатинових капсул носії зазвичай не потрібні. Відповідними носіями для одержання розчинів і сиропів є, наприклад, вода, поліоли, гліцерин, рослинне масло і тому подібне. Відповідними носіями для суппозіторіїв є, наприклад, натуральні або затверділі масла, віск, жири, напіврідкі або рідкі поліоли і тому подібне. Фармацевтичні препарати можуть, крім того, містити фармацевтично прийнятні допоміжні речовини, такі як консерванти, солюбілізатори, стабілізатори, зволожуючі агенти, емульгатори, підсолоджувачі, барвники, коригенти, солі для варіювання осмотичного тиску, буфери, маскуючі агенти або антиоксиданти. Ці препарати можуть також містити інші терапевтично цінні 13 UA 111623 C2 5 10 15 речовини. Лікарські засоби, що містять сполуку формули I або її фармацевтично прийнятну сіль і терапевтично інертний носій, також запропоновані даним винаходом, а також спосіб їх одержання, що включає наведення одної або більше сполук формули I та/або їх фармацевтично прийнятних солей і, якщо бажано, одної або більше інших терапевтично цінних речовин у форму галенова препарату для введення разом з одним або декількома терапевтично інертними носіями. Дозування може варіювати в широких межах і, звичайно, його слід регулювати за індивідуальними потребами у кожному конкретному випадку. У разі перорального введення доза для дорослих може варіювати від приблизно 0,01 міліграма до приблизно 1000 міліграма на добу сполуки загальної формули I або відповідної кількості її фармацевтично прийнятної солі. Добову дозу можна вводити у вигляді одноразової дози або в розділених дозах і, крім того, верхня межа може бути також перевищена, якщо виявлені показання до цього. Наведені нижче приклади ілюструють даний винахід без його обмеження, але служать виключно як репрезентативні. Фармацевтичні препарати зазвичай містять приблизно 1-500 міліграм, зокрема, 1-100 міліграм сполуки формули I. Прикладами композицій відповідно до винаходу є наступні композиції: Приклад A Пігулки, що мають наведену нижче композицію, готують звичайним способом: 20 Інгредієнт Сполука формули I Лактоза безводна DTG Sta-Rx 1500 Мікрокристалічна целюлоза Стеарат магнію Всього 25 мг/пігулка 25 25 105 6 30 1 167 5 5 125 6 30 1 167 100 100 30 6 30 1 167 500 500 150 60 450 1 831 Таблиця 2: можлива композиція пігулки Метод одержання 1. Змішують інгредієнти 1, 2, 3 та 4 і гранулюють з дистильованою водою. 2. Висушують гранули при 50 °C. 3. Пропускають гранули через відповідне устаткування для подрібнення. 4. Додають інгредієнт 5 і змішують протягом трьох хвилин; пресують на відповідному пресі. Приклад B-1 Готують капсули, що мають наведену нижче композицію: 30 Інгредієнт Сполука формули I Водна лактоза Кукурудзяний крохмаль Тальк Стеарат магнію Всього 35 40 5 5 159 25 10 1 200 мг/капсула 25 25 123 35 15 2 200 100 100 148 40 10 2 300 500 500 70 25 5 600 Таблиця 3: можлива композиція інгредієнтів капсули Метод одержання 1. Змішують інгредієнти 1, 2 і 3 у відповідному змішувачі протягом 30 хвилин. 2. Додають інгредієнти 4 і 5 та змішують протягом 3 хвилин. 3. Заповнюють у відповідну капсулу. Сполуку формули I, лактозу і кукурудзяний крохмаль спочатку змішують в змішувачі, а потім в подрібнюючому апараті. Суміш повертають в змішувач; додають до неї тальк і ретельно змішують. Суміш заповнюють за допомогою апарату у відповідні капсули, наприклад, в тверді желатинові капсули. Приклад B-2 Готують м'які желатинові капсули, що мають приведену нижче композицію: 14 UA 111623 C2 Інгредієнт Сполука формули I Жовтий віск Гідрогенізоване соєве масло Часткво гідрогенізовані рослинні масла Соєве масло Всього мг/капсула 5 8 8 34 110 165 Таблиця 4: можлива композиція інгредієнтів м'якої желатинової капсули Інгредієнт Желатин Гліцерин 85 % Karion 83 Диоксид титану Оксид заліза жовтий Всього мг/капсула 75 32 8 (суха речовина) 0,4 1,1 116,5 5 10 Таблиця 5: можлива композиція інгредієнтів м'якої желатинової капсули Метод одержання Сполуку формули I розчиняють в теплому розплаві інших інгредієнтів, і суміш заповнюють в м'які желатинові капсули відповідного розміру. Заповнені м'які желатинові капсули обробляють відповідно до звичайних методів. Приклад C Готують суппозіторії, що мають приведену нижче композицію: Інгредієнт мг/супозиторій 15 1285 1300 Сполука формули I Супозиторна маса Всього 15 20 Таблиця 6: можлива композиція супозиторію Метод одержання Супозиторну масу плавлять в скляній або сталевій судині, ретельно змішують і охолоджують до 45 °C. Після цього до неї додають тонкоподрібнену сполуку формули I і перемішують до тих пір, поки воно повністю не диспергує. Суміш заливають у форми для супозиторіїв відповідного розміру, залишають до охолоджування; потім супозиторії витягують з форм і упаковують індивідуально у вощений папір або металеву фольгу. Приклад D Готують ін'єкційні розчини, що мають наведену нижче композицію: Інгредієнт Сполука формули I Поліетиленгликоль 400 Оцтова кислота Вода для ін'єкційних розчинів мг/ін’єкційний розчин 3 150 достатня кількість до pH 5,0 до 1,0 мл 25 30 Таблица 7: можлива композиція ін'єкційних розчинів Метод одержання Сполуку формули I розчиняють в суміші поліетиленгликолю 400 і води для ін'єкцій (частини). Доводять pH до 5,0 оцтовою кислотою. Об’єм доводять до 1,0 мл додаванням залишенної кількості води. Розчин фільтрують, заповнюють у флакони, використовуючи підходящий допустимий надлишок, та стерилізують. Приклад E Готують пакети-саше, які мають наведену нижче композицію: 15 UA 111623 C2 Інгредієнт Сполука формули I Лактоза, дрібний порошок Мікрокристалічна целюлоза (AVICEL PH 102) Натрієва сіль карбоксиметилцелюлози Полівінілпіролідон K 30 Стеарат магнію Добавки коригентів Всього 5 10 15 20 25 30 35 40 45 50 мг/саше 50 1015 1400 14 10 10 1 2500 Таблиця 8: можлива композиція пакету-саше Метод одержання Сполуку формули I змішують з лактозою, мікрокристалічною целюлозою і натрієвою сіллю карбоксиметилцелюлози і гранулюють з сумішшю полівінілпіролідону у воді. Гранулят змішують із стеаратом магнію, додають добавки коригентів і заповнюють в пакети-саше. Опис прикладів здійснення винаходу Наведені нижче приклади запропоновані для ілюстрації винаходу. Їх не слід розглядати як винаходи, що обмежують об'єм, але виключно як репрезентативні приклади. Проміжна сполука формули (V) цис/транс-4-Триметилсиланілокси-циклогексанкарбонової кислоти етиловий ефір (2:1) До розчину цис/транс-4-гідроксициклогексанкарбонової кислоти етилового ефіру (2:1) (5,0 г, 29 ммоль) та імідазолу (4,4 г, 64 ммоль) в N,N-диметилформаміді (90 мл) додавали триметилсилілхлорид (4,0 мл, 32 ммоль) при 0-5 °C. Після перемішування протягом 1 години при кімнатній температурі суміш розподіляли між трет-бутилметиловим ефіром (300 мл) і водою (150 мл). Шари розділяли. Органічний шар промивали двома 150-мл порціями води і однією 50мл порцією розсолу, висушували над безводним сульфатом натрію і концентрували у вакуумі з одержанням сполуки, зазначеної в заголовку (6,7 г, 94%), у вигляді безбарвного масла. Мас+ спектрометрія (МС) m/e: 245 ([M+H] ). Складноефірні проміжні сполуки 4-алкокси-циклогексанкарбонової кислоти формули (VII-1) Відновна етерифікація Загальний спосіб I: До розчину цис/транс-4-триметилсиланілокси-циклогексанкарбонової кислоти етилового ефіру (2:1) в дихлорметані (0,1 M) послідовно додають кетон або альдегід формули (VI) (0,85 екв.) і триметилсилілтрифторметансульфонат (0,10 екв.) при -78 °C. Реакційну суміш перемішують протягом 1 години. Після додавання триетилсилану (1 екв.) охолоджуючу баню видаляють, і реакційній суміші дають підігрітися до кімнатної температури. Перемішування продовжують протягом ночі. Суміш гасять насиченим водним розчином бікарбонату натрію. Шари розділяють. Органічний шар висушують над безводним сульфатом натрію і концентрують у вакуумі. В результаті очищення флеш-хроматографією одержують складноефірну проміжну сполуку 4-алкокси-циклогексанкарбонової кислоти формули (VII-1). Загальний спосіб IIA: Алкокси-триметил-силанову проміжну сполуку формули (IX) утворюють in situ шляхом додавання триметилсилілтрифторметансульфонату (1 екв.) до розчину спиртного похідного формули (VIII) (1 екв.), та 2,6-лутидину (1 екв.) в дихлорметані (0,1 M) при -78 °C. Через 1 годину послідовно додають складний ефір 4-циклогексанонкарбонової кислоти формули (X) (0,85 екв.) і триметилсилілтрифторметансульфонат (0,1 екв.). Реакційну суміш перемішують протягом 1 години. Після додавання триетилсилану (2 екв.) охолоджуючу баню видаляють, і реакційній суміші дають підігрітися до кімнатної температури. Перемішування продовжують протягом ночі. Суміш гасять насиченим водним розчином бікарбонату натрію. Шари розділяють. Органічний шар висушують над безводним сульфатом натрію і концентрують у вакуумі. В результаті очищення флеш-хроматографією одержують складноефірну проміжну сполуку 4алкокси-циклогексанкарбонової кислоти формули (VII-1). Загальний спосіб IIB: Проміжну триметилсилілокси-сполуку формули (IX), яка є у продажу або може бути одержана способами, відомими в даній області техніки, розчиняють в дихлорметані (0,1 M). Послідовно додають складний ефір 4-циклогексанонкарбонової кислоти формули (X) (0,85 екв.), і триметилсилілтрифторметансульфонат (0,1 екв.) при -78 °C. Після додавання триетилсилану (2 екв.) охолоджуючу баню видаляють, і реакційній суміші дають підігрітися до кімнатної температури. Перемішування продовжують протягом ночі. Суміш гасять насиченим водним 16 UA 111623 C2 5 10 15 20 25 30 35 40 45 50 55 60 розчином бікарбонату натрію. Шари розділяють. Органічний шар висушують над безводним сульфатом натрію і концентрують у вакуумі. В результаті очищення флеш-хроматографією одержують складноефірну проміжну сполуку 4-алкокси-циклогексанкарбонової кислоти, яка має формулу (VII-1). Складний ефір 1 4-алкокси-циклогексанкарбонової кислоти транс-4-Ізопропокси-циклогексанкарбонової кислоти етиловий ефір транс-4-Ізопропокси-циклогексанкарбонової кислоти етиловий ефір одержували у вигляді безбарвного масла при виході 23% з ацетону згідно загальному способу I після очищення + колоночною флеш-хроматографією. МС m/e: 214 (M ). Складний ефір 2 4-алкокси-циклогексанкарбонової кислоти (RS)-транс-4-втор-бутокси-циклогексанкарбонової кислоти етиловий ефір (RS)-транс-4-втор-бутокси-циклогексанкарбонової кислоти етиловий ефір одержували у вигляді безбарвного масла при виході 22% з 2-бутанону згідно загальному способу I після очищення колоночною флеш-хроматографією. МС (іонізація електророзпилюванням (ІЕР)) m/e: + + + 228 (M , 1%), 199 ([M-C2H5] , 6%), 155 ([M-C4H9O] , 100%). Складний ефір 3 4-алкокси-циклогексанкарбонової кислоти транс-4-Циклопентилокси-циклогексанкарбонової кислоти етиловий ефір транс-4-Циклопентокси-циклогексанкарбонової кислоти етиловий ефір одержували у вигляді безбарвного масла при виході 22% з циклопентанону згідно загальному способу I після + + очищення колоночною флеш-хроматографією. МС (ІЕР) m/e: 240 (M , 1%), 155 [M-C5H9O] , 30%). Складноефірні проміжні сполуки 4-арилокси-циклогексанкарбонової кислоти формули (VII-2) і (VII-3) Загальний спосіб IIIA: Етерифікація в умовах реакції Міцунобу До розчину трифенілфосфіну (1,2 екв.) в сухому тетрагідрофурані (0,1 M) додають диетилазодикарбоксилат (1,2 екв.) при 0 °C. Через 20 хвилин послідовно додають фенольне похідне формули (XI) (1,2 екв.), і розчин складного ефіру 4-гідрокси-циклогексанкарбонової кислоти формули (IV) в тетрагідрофурані (1-3 M) при 5 °C. Після завершення додавання охолоджуючу баню видаляють, і реакційній суміші дають підігрітися до кімнатної температури і перемішують протягом 3-18 годин. Розчинник випаровують, і залишок розчиняють в етилацетаті. Етилацетатний розчин промивають однією - двома порціями 1 M водного розчину гідроксиду натрію. Водний шар екстрагують однією - двома порціями етилацетату. Об'єднані органічні шари висушують над безводним сульфатом натрію і концентрують у вакуумі. В результаті очищення флеш-хроматографією одержують складний ефір 4-арилоксициклогексанкарбонової кислоти, що має формулу (VII-2). Загальний спосіб IIIB: Арилювання, опосередковане метансульфінатом натрію До розчину складного ефіру 4-гідрокси-циклогексанкарбонової кислоти формули (IV) (1 екв.) і гетероарилхлоридного похідного формули (XII) (1 екв.) в сухому N,N-диметилформаміді (1 M) послідовно додають метансульфінат натрію (85%, 0,25 - 1 екв.) і карбонат калію (1,5 екв.). Після завершення додавання реакційну суміш перемішують при 120 °C протягом 3-18 годин. Після охолоджування до кімнатної температури реакційну суміш розподіляють між третбутилметиловим ефіром і водою. Шари розділяють, і водний шар екстрагують одній - двома порціями трет-бутилметилового ефіру. Об'єднані органічні шари промивають одній - двома порціями води, висушують над безводним сульфатом натрію і концентрують у вакуумі. В результаті очищення флеш-хроматографією одержують складний ефір 4-гетероарилоксициклогексанкарбонової кислоти, що має формулу (VII-3). Загальний спосіб IIIC: Арилювання, що каталізується міддю До суміші йодиду міді (0,1 екв.), 1,10-фенантроліну (0,2 екв.) і гетероарилхлоридного похідного формули (XII) (1 екв.) в толуолі (2 M) додають складний ефір 4-гідроксициклогексанкарбонової кислоти формули (IV) (1 екв.) і карбонат цезію (2 екв.). Реакційну суміш нагрівають із зворотним холодильником протягом 20 годин. Після охолоджування до кімнатної температури реакційну суміш розподіляють між етилацетатом і водою. Шари розділяють, і водний шар екстрагують однією - двома порціями етилацетату. Об'єднані органічні шари промивають однією - двома порціями 0,5 М водного розчину хлориду натрію, висушують над безводним сульфатом натрію і концентрують у вакуумі. В результаті очищення флешхроматографією одержують складний ефір 4-гетероарилокси-циклогексанкарбонової кислоти формули (VII-3). Складний ефір 1 4-арилокси-циклогексанкарбонової кислоти транс-4-Фенокси-циклогексанкарбонової кислоти метиловий ефір Сполука, зазначена в заголовку, була одержана у вигляді безбарвного масла при виході 23% згідно загальному методу IIIA з фенолу і транс-4-гідрокси-циклогексанкарбонової кислоти 17 UA 111623 C2 + 5 10 15 20 25 30 35 40 45 50 55 60 метилового ефіру. МС m/e: 234 (M ). Складний ефір 2 4-арилокси-циклогексанкарбонової кислоти транс-4-(Піридин-2-ілокси)-циклогексанкарбонової кислоти метиловий ефір Сполуку, зазначену в заголовку, одержували у вигляді світло-червоної твердої речовини при виході 36% згідно загальному способу IIIA з 2-гідроксипіридину і транс-4-гідрокси+ циклогексанкарбонової кислоти метилового ефіру. МС m/e: 236 ([M+H] ). Складний ефір 3 4-арилокси-циклогексанкарбонової кислоти цис/транс-4-(Піразин-2-ілокси)-циклогексанкарбонової кислоти етиловий ефір (1:1) Сполуку, зазначену в заголовку, одержували у вигляді білої твердої речовини при виході 15% згідно загальному способу IIIB з 2-хлорпіразину і цис/транс-4-гідрокси+ циклогексанкарбонової кислот етилового ефіру (2:1). МС m/e: 251 ([M+H] ). Гідразидні проміжні сполуки формули (II) Загальний спосіб IV: Утворення гідразиду із складного ефіру 4-алкокси- або 4-арилоксициклогексанкарбонової кислоти Суміш складного ефіру 4-алкокси- або 4-арилокси-циклогексанкарбонової кислоти формули (VII) (1 екв.), і гідрату гідразину (2-6 екв.) в н-бутанолі (0,2-1 M) нагрівають із зворотним холодильником протягом 16-72 годин. Після охолоджування до кімнатної температури реакційну суміш розподіляють між органічним розчинником, таким як етилацетат або дихлорметан, і водою. Шари розділяють, і водний шар екстрагують двома порціями органічного розчинника. Об'єднані органічні шари висушують над безводним сульфатом натрію і концентрують у вакуумі з одержанням сирого гідразидного похідного формули (II), яке зазвичай можна використовувати в наступній стадії без додаткового очищення. Гідразид 1 транс-4-Ізопропокси-циклогексанкарбонової кислоти гідразид Сполуку, зазначену в заголовку, одержували у вигляді білуватої твердої речовини при виході 70% з транс-4-ізопропокси-циклогексанкарбонової кислоти етилового ефіру згідно + загальному способу IV. МС m/e: 201 ([M+H] ). Гідразид 2 (RS)-транс-4-втор-бутокси-циклогексанкарбоновоЇ кислоти гідразид Сполуку, зазначену в заголовку, одержували у вигляді білої твердої речовини при виході 93% з (RS)-транс-4-втор-бутокси-циклогексанкарбоновоЇ кислоти етилового ефіру згідно + загальному способу IV. МС (EI) m/e: 214 (M ). Гідразид 3 транс-4-Циклопентилокси-циклогексанкарбоновоЇ кислоти гідразид Сполуку, зазначену в заголовку, одержували у вигляді білої твердої речовини при виході 80% з транс-4-циклопентилокси-циклогексанкарбоновоЇ кислоти етилового ефіру згідно + загальному способу IV. МС (EI) m/e: 226 (M ). Гідразид 4 транс-4-Фенокси-циклогексанкарбоновоЇ кислоти гідразид Сполуку, зазначену в заголовку, одержували у вигляді білої твердої речовини при кількісному виході з транс-4-фенокси-циклогексанкарбоновоЇ кислоти метилового ефіру згідно + загальному способу IV. МС m/e: 235 ([M+H] ). Гідразид 5 транс-4-(Піридин-2-ілокси)-циклогексанкарбонової кислоти гідразид Сполуку, зазначену в заголовку, було одержано у вигляді білої твердої речовини при виході 96% з транс-4-(піридин-2-ілокси)-циклогексанкарбонової кислоти метилового ефіру згідно + загальному методу IV. МС m/e: 236 ([M+H] ). Гідразид 6 транс-4-(Піразин-2-ілокси) -циклогексанкарбонової кислоти гідразид Суміш цис/транс-4-(піразин-2-ілокси)-циклогексанкарбонової кислоти етилового ефіру (1,11 г, 4,41 ммоль) і гідрату гідразину (0,442 г, 8,83 ммоль) нагрівали при 120 °C протягом 72 годин. Після охолоджування до кімнатної температури реакційну суміш розподіляли між етилацетатом (50 мл) і водою (30 мл). Органічний шар відокремлювали. Водний шар екстрагували двома 50мл порціями етилацетату. Об'єднані органічні шари промивали розсолом (30 мл), висушували над безводним сульфатом натрію і концентрували у вакуумі. Сирий цис/транс-гідразид розтирали в етилацетаті (5 мл). Осад збирали фільтруванням і висушували у вакуумі з одержанням сирої сполуки, зазначеної в заголовку (0,236 г, 23%), у вигляді білої твердої речовини, яку використовували в наступній стадії без додаткового очищення. МС m/e: 237 + ([M+H] ). Тіолактамна проміжна сполука формули (III) 18 UA 111623 C2 5 10 15 20 25 30 35 40 45 50 55 60 7-хлор-3,5-дигідробензо[e][1,4]оксазепін-2(1H)-тіон a) 2-Бром-N-(4-хлор-2-(гідроксиметил)феніл)ацетамід До розчину (2-аміно-5-хлорфеніл) метанолу (4,30 г, 27,3 ммоль) в дихлорметані (220 мл) додавали 2-бромацетилбромід (6,06 г, 2,61 мл, 30,0 ммоль) при 0-5 °C. Після перемішування протягом 5 хвилин додавали по краплях водний 2 M розчин карбонату натрію (130 мл) протягом приблизного 10 хвилин. Охолоджуючу баню видаляли, і перемішування продовжували протягом 2 годин. Розчинник видаляли у вакуумі. Водний залишок екстрагували трьома 100-мл порціями етилацетату. Об'єднані органічні шари промивали однією 50-мл порцією розсолу, висушували над безводним сульфатом натрію і концентрували у вакуумі з одержанням сполуки, зазначеної в заголовку (7,30 г, 96%), у вигляді світло-сірої твердої речовини, яку використовували в + наступній стадії без додаткового очищення. МС m/e: 276 ([M+H] ). b) 7-Хлор-3,5-дигідробензо[e][1,4]оксазепін-2(1H) -он До суспензії 2-бром-N-(4-хлор-2-(гідроксиметил)феніл)ацетаміду (3,60 г, 12,9 ммоль) в 2пропанолі (129 мл) додавали малими порціями трет-бутоксид калію (3,77 г, 33,6 ммоль) при 05 °C. Реакційну суміш перемішували протягом 90 хвилин, а потім виливали на крижану воду (500 мл). Осад збирали фільтруванням і промивали водою. Залишкову воду видаляли послідовним випаровуванням з двома 50-мл порціями толуолу з одержанням сполуки, зазначеної в заголовку (2,34 г, 92%), у вигляді світло-жовтої твердої речовини. МС m/e: 196 ([MH]-). c) 7-Хлор-3,5-дигідробензо[e][1,4]оксазепін-2(1H)-тіон До суспензії 7-хлор-3,5-дигідробензо[e][1,4]оксазепін-2(1H)-она (3,01 г, 15,2 ммоль) в тетрагідрофурані (102 мл) додавали 2,4-біс-(4-метоксифеніл)-1,3,2,4-дитіадифосфетан-2,4дисульфид (3,45 г, 8,53 ммоль) при кімнатній температурі. Реакційну суміш нагрівали із зворотним холодильником протягом 4 годин. Після охолоджування до кімнатної температури розчинник випаровували, і залишок кристалізували з гарячого етанолу з одержанням сполуки, зазначеної в заголовку (1,96 г, 60%), у вигляді світло-жовтої твердої речовини. МС m/e: 211,6 ([M-H] ). Загальний метод V: Конденсація гідразиду і тіолактаму з одержанням триазолу Суміш гідразидного похідного формули (II) (1-1,5 екв.) і тіолактаму формули (III) (1 екв.) в нбутанолі (0,1-0,2 M) нагрівають із зворотним холодильником протягом 16-72 годин. Після охолоджування до кімнатної температури розчинник випаровують, і залишок очищають флешхроматографією з одержанням сполуки формули (I). Приклад 1 транс-8-Хлор-1-(4-ізопропокси-циклогексил)-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азулен Сполуку, зазначену в заголовку, одержували у вигляді білої твердої речовини при виході 57%, використовуючи загальний спосіб V. Гідразид: транс-4-Ізопропокси-циклогексанкарбонової кислоти гідразид Тіолактам: 7-Хлор-3,5-дигідробензо[e][1,4]оксазепін-2(1H)-тіон + МС m/e: 362 ([M+H] ). Приклад 2 транс-1-(4-втор-бутокси-циклогексил)-8-хлор-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азулен Сполуку, зазначену в заголовку, одержували у вигляді білуватої твердої речовини при виході 63%, використовуючи загальний спосіб V. Гідразид: (RS)-транс-4-втор-бутокси-циклогексанкарбонової кислоти гідразид Тіолактам: 7-Хлор-3,5-дигідробензо[e][1,4]оксазепін-2(1H) -тіон + МС m/e: 376 ([M+H] ). Приклад 3 транс-8-Хлор-1-(4-циклопентилокси-циклогексил)-4H,6H-5-окса-2,3,10b-триазабензо[e]азулен Сполуку, зазначену в заголовку, одержували у вигляді білуватої твердої речовини при виході 72%, використовуючи загальний спосіб V. Гідразид: транс-4-Циклопентилокси-циклогексанкарбонової кислоти гідразид Тіолактам: 7-Хлор-3,5-дигідробензо[e][1,4]оксазепін-2(1H) -тіон + МС m/e: 388 ([M+H] ). Приклад 4 транс-8-Хлор-1-(4-фенокси-циклогексил)-4H,6H-5-окса-2,3,10b-триаза-бензо[e]азулен Сполуку, зазначену в заголовку, одержували у вигляді білої твердої речовини при виході 75%, використовуючи загальний спосіб V. Гідразид: транс-4-Фенокси-циклогексанкарбонової кислоти гідразид Тіолактам: 7-Хлор-3,5-дигідробензо[e][1,4]оксазепін-2(1H) -тіон 19 UA 111623 C2 + 5 10 15 МС m/e: 396 ([M+H] ). Приклад 5 транс-8-Хлор-1-[4-(піридин-2-ілокси)-циклогексил]-4H,6H-5-окса-2,3,10b-триазабензо[e]азулен Сполуку, зазначену в заголовку, одержували у вигляді білуватої твердої речовини при виході 71%, використовуючи загальний спосіб V. Гідразид: транс-4-(Піридин-2-ілокси) -циклогексанкарбонової кислоти гідразид Тіолактам: 7-Хлор-3,5-дигідробензо[e][1,4]оксазепін-2(1H)-тіон + МС m/e: 397 ([M+H] ). Приклад 6 транс-8-Хлор-1-[4-(піразин-2-ілокси)-циклогексил]-4H,6H-5-окса-2,3,10b-триазабензо[e]азулен Сполуку, зазначену в заголовку, одержували у вигляді білуватої твердої речовини при виході 37%, використовуючи загальний спосіб V. Гідразид: транс-4-(Піразин-2-ілокси) -циклогексанкарбонової кислоти гідразид Тіолактам: 7-Хлор-3,5-дигідробензо[e][1,4]оксазепін-2(1H)-тіон + МС m/e: 398 ([M+H] ). ФОРМУЛА ВИНАХОДУ 20 1. Сполука формули І O R2 R1 N O 25 30 35 40 45 50 N N ,І у якій: 1 R є атомом галогену, та 2 R вибраний з групи, що складається з: і) гетероарилу, незаміщеного або заміщеного замісниками в кількості від 1 до 3, індивідуально вибраними з групи, що складається з ОН, галогену, ціано, С 1-6-алкілу, С1-6-алкокси, галоген-С1-6алкілу, галоген-С1-6-алкокси, С1-6-алкоксі-С1-6-алкілу і гідроксі-С1-6-алкілу; іі) арилу, незаміщеного або заміщеного замісниками в кількості від 1 до 3, індивідуально вибраними з групи, що складається з ОН, атома галогену, ціано, С 1-6-алкілу, С1-6-алкокси, галоген-С1-6-алкілу, галоген-С1-6-алкокси, С1-6-алкоксі-С1-6-алкілу і гідроксі-С1-6-алкілу; ііі) С3-7-циклоалкілу, незаміщеного або заміщеного замісниками в кількості від 1 до 3, індивідуально вибраними з групи, що складається з ОН, атома галогену, ціано, С 1-6-алкілу, С1-6алкокси, галоген-С1-6-алкілу, галоген-С1-6-алкокси, С1-6-алкоксі-С1-6-алкілу і гідроксі-С1-6-алкілу; та iv) С1-6-алкілу, незаміщеного або заміщеного замісниками в кількості від 1 до 3, індивідуально вибраними з групи, що складається з ОН, атома галогену, ціано, С 1-6-алкокси і галоген-С1-6алкокси; або її фармацевтично прийнятні солі. 1 2. Сполука за п. 1, в якій R є атомом хлору. 2 3. Сполука за будь-яким з пп. 1 або 2, в якій R вибраний з групи, що складається з незаміщеного гетероарилу, незаміщеного арилу, незаміщеного С 3-7-циклоалкілу і незаміщеного С1-6-алкілу. 2 4. Сполука за будь-яким з пп. 1-3, в якій R вибраний з піридинілу, піразинілу, фенілу, циклопентилу, ізопропілу та втор-бутилу. 5. Сполука за будь-яким з пп. 1-4, вибрана з групи, що складається з: 8-хлор-1-(4-ізопропоксициклогексил)-4Н,6Н-5-окса-2,3,10b-триазабензо[е]азулену, 1-(4-втор-бутоксициклогексил)-8-хлор-4Н,6Н-5-окса-2,3,10b-триазабензо[е]азулену, 8-хлор-1-(4-циклопентилоксициклогексил)-4Н,6Н-5-окса-2,3,10b-триазабензо[е]азулену, 8-хлор-1-(4-феноксициклогексил)-4Н,6Н-5-окса-2,3,10b-триазабензо[е]азулену, 8-хлор-1-[4-(піридин-2-ілокси)циклогексил-4H,6Н-5-окса-2,3,10b-триазабензо[e]азулену та 20 UA 111623 C2 8-хлор-1-[4-(піразин-2-ілокси)циклогексил]-4Н,6Н-5-окса-2,3,10b-триазабензо[е]азулену або їх фармацевтично прийнятних солей. 6. Спосіб одержання сполуки формули І, як визначено в будь-якому з пп. 1-5, що включає взаємодію сполуки формули II із сполукою формули III з одержанням сполуки формули І: 5 O R2 S H N O H N 1 10 15 20 25 30 N N + NH2 O R1 O II N н-бутанол Кипятіння із зворотним холодильником R1 I III 2 , де R та R є такими, як визначено в будь-якому з пп. 1-4. 7. Сполука формули І за будь-яким з пп. 1-5, одержана способом, як визначено в п. 6. 8. Сполука формули І за будь-яким з пп. 1-5 для застосування як терапевтично активної речовини. 9. Сполука формули І за пп. 1-5 для застосування як терапевтично активної речовини для терапевтичного та/або профілактичного лікування захворювань і розладів, пов'язаних з антагонізмом рецептора V1a. 10. Сполука формули І за пп. 1-5 для застосування як терапевтично активної речовини, що має периферичну і центральну дії при наступних станах: дисменорея, чоловіча або жіноча статева дисфункція, гіпертензія, хронічна серцева недостатність, неадекватна секреція вазопресину, цироз печінки, нефротичний синдром, тривожність, депресивні розлади, обсесивнокомпульсивний розлад, розлади аутистичного спектра, шизофренія і агресивна поведінка. 11. Фармацевтична композиція, що містить сполуку формули І за будь-яким з пп. 1-5 і фармацевтично прийнятний носій та/або фармацевтично прийнятну допоміжну речовину. 12. Застосування сполуки формули І за будь-яким з пп. 1-5 для одержання лікарського засобу, що має периферичну і центральну дії при наступних станах: дисменорея, чоловіча або жіноча статева дисфункція, гіпертензія, хронічна серцева недостатність, неадекватна секреція вазопресину, цироз печінки, нефротичний синдром, тривожність, депресивні розлади, обсесивно-компульсивний розлад, розлади аутистичного спектра, шизофренія і агресивна поведінка. 13. Спосіб застосування сполуки за будь-яким з пп. 1-5, що має периферичну і центральну дії при наступних станах: дисменорея, чоловіча або жіноча статева дисфункція, гіпертензія, хронічна серцева недостатність, неадекватна секреція вазопресину, цироз печінки, нефротичний синдром, тривожність, депресивні розлади, обсесивно-компульсивний розлад, розлади аутистичного спектра, шизофренія і агресивна поведінка, де даний спосіб включає введення сполуки формули І людині або тварині. Комп’ютерна верстка Л. Бурлак Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 21
ДивитисяДодаткова інформація
Назва патенту англійськоюOxy-cyclohexyl-4h,6h-5-oxa-2,3,10b-triaza-benzo[e]azulenes as v1a antagonists
Автори англійськоюDolente, Cosimo, Schnider, Patrick
Автори російськоюДоленте Козимо, Шнидер Патрик
МПК / Мітки
МПК: C07D 498/04, A61P 9/12, A61K 31/553
Мітки: антагоністи, оксициклогексил-4н,6н-5-окса-2,3,10b-триазабензо[e]азулени
Код посилання
<a href="https://ua.patents.su/23-111623-oksiciklogeksil-4n6n-5-oksa-2310b-triazabenzoeazuleni-yak-antagonisti-v1a.html" target="_blank" rel="follow" title="База патентів України">Оксициклогексил-4н,6н-5-окса-2,3,10b-триазабензо[e]азулени як антагоністи v1a</a>
Попередній патент: Пристрій для нагрівання та спосіб нагрівання курильного матеріалу
Наступний патент: Багатосекційний курильний виріб
Випадковий патент: Спосіб отримання тонковолокнистого фільтрувального матеріалу