Кристалічна форма метилового естеру [9s-(9a,10b,12a)]-5,16-біс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1н-дііндоло[1,2,3-fg:3′,2′,1′-kl]піроло[3,4-і][1,6]бензодіазоцин-1
Номер патенту: 90259
Опубліковано: 26.04.2010
Автори: Лопес де Дієґо Хейді, Буур Аннерс, Хрістенсен Кім Лассе, Хауелз Марк, Нільсен Оле, Рок Майкл Харольд
Формула / Реферат
1. Кристалічна форма метилового естеру [9S-(9![]() ,10
,10![]() ,12
,12![]() )]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'-kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
)]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'-kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
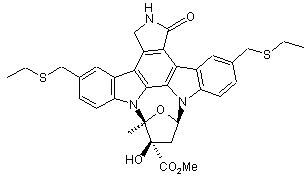 ,
,
яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK![]() -випромінювання, при кутах 2-тета: 5,2, 10,1, 10,4, 13,2, 15,1, 25,1.
-випромінювання, при кутах 2-тета: 5,2, 10,1, 10,4, 13,2, 15,1, 25,1.
2. Кристалічна форма за п. 1, яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK![]() -випромінювання, при кутах 2-тета: 5,2, 7,3, 8,1, 10,1, 10,4, 11,2, 13,2, 15,1, 15,5, 17,3, 21,7, 23,8, 25,1.
-випромінювання, при кутах 2-тета: 5,2, 7,3, 8,1, 10,1, 10,4, 11,2, 13,2, 15,1, 15,5, 17,3, 21,7, 23,8, 25,1.
3. Кристалічна форма за п. 1, яка характеризується кристалічною структурою з наступними характеристиками при 122 К: просторова група: P212121, розміри елементарної комірки: а = 10,227(2) Ǻ, b = 23,942(2) Ǻ і с = 24,240(2) Ǻ, ![]() = 90°,
= 90°, ![]() = 90°,
= 90°, ![]() = 90°, 2 молекули в асиметричній комірці.
= 90°, 2 молекули в асиметричній комірці.
4. Кристалічна форма метилового естеру [9S-(9![]() ,10
,10![]() ,12
,12![]() )]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'-kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
)]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'-kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
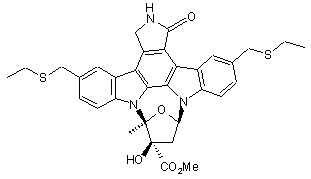 ,
,
яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK![]() -випромінювання, при кутах 2-тета: 6,6, 8,9, 10,7, 11,7, 24,4, 30,6.
-випромінювання, при кутах 2-тета: 6,6, 8,9, 10,7, 11,7, 24,4, 30,6.
5. Кристалічна форма за п. 4, яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK![]() -випромінювання, при кутах 2-тета: 6,6, 8,9, 10,7, 11,4, 11,7, 13,7, 17,0, 18,5, 18,8, 19,2, 20,3, 24,4, 30,6.
-випромінювання, при кутах 2-тета: 6,6, 8,9, 10,7, 11,4, 11,7, 13,7, 17,0, 18,5, 18,8, 19,2, 20,3, 24,4, 30,6.
6. Кристалічна форма метилового естеру [9S-(9![]() ,10
,10![]() ,12
,12![]() )]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
)]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
 ,
,
яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK![]() -випромінювання, при кутах 2-тета: 9,6, 11,5, 12,5, 16,7, 19,3, 28,1.
-випромінювання, при кутах 2-тета: 9,6, 11,5, 12,5, 16,7, 19,3, 28,1.
7. Кристалічна форма за п. 6, яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK![]() -випромінювання, при кутах 2-тета: 7,5, 8,3, 9,6, 11,5, 11,8, 12,5, 15,9, 16,3, 16,7, 17,2, 18,0, 19,3, 21,0, 28,1.
-випромінювання, при кутах 2-тета: 7,5, 8,3, 9,6, 11,5, 11,8, 12,5, 15,9, 16,3, 16,7, 17,2, 18,0, 19,3, 21,0, 28,1.
8. Кристалічна форма метилового естеру [9S-(9![]() ,10
,10![]() ,12
,12![]() )]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1H-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
)]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1H-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
 ,
,
яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK![]() -випромінювання, при кутах 2-тета: 9,7, 12,1, 16,1, 18,3, 22,1, 22,2, 25,7, 25,8.
-випромінювання, при кутах 2-тета: 9,7, 12,1, 16,1, 18,3, 22,1, 22,2, 25,7, 25,8.
9. Кристалічна форма за п. 8, яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK![]() -випромінювання, при кутах 2-тета: 7,3, 8,3, 9,7, 11,1, 11,7, 12,1, 15,6, 16,1, 17,3, 18,3, 20,9, 22,1, 22,2, 25,7, 25,8.
-випромінювання, при кутах 2-тета: 7,3, 8,3, 9,7, 11,1, 11,7, 12,1, 15,6, 16,1, 17,3, 18,3, 20,9, 22,1, 22,2, 25,7, 25,8.
10. Кристалічна форма метилового естеру [9S-(9![]() ,10
,10![]() ,12
,12![]() )]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'-kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
)]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'-kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
 ,
,
яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK![]() -випромінювання, при кутах 2-тета: 8,9, 9,2, 10,2, 14,6.
-випромінювання, при кутах 2-тета: 8,9, 9,2, 10,2, 14,6.
11. Кристалічна форма за п. 10, яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK![]() -випромінювання, при кутах 2-тета: 8,9, 9,2, 10,2, 12,6, 14,2, 14,6, 17,0, 18,6, 20,4, 21,1, 23,9, 25,2.
-випромінювання, при кутах 2-тета: 8,9, 9,2, 10,2, 12,6, 14,2, 14,6, 17,0, 18,6, 20,4, 21,1, 23,9, 25,2.
12. Тверда форма метилового естеру [9S-(9![]() ,10
,10![]() ,12
,12![]() )]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
)]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
 ,
,
яка містить кристалічну альфа-форму вищевказаної сполуки, як її визначено у будь-якому з пп. 1-3.
13. Тверда форма за п. 12, яка складається головним чином із згаданої альфа-форми.
14. Тверда форма метилового естеру [9S-(9![]() ,10
,10![]() ,12
,12![]() )]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
)]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
 ,
,
яка містить кристалічну бета-форму вищевказаної сполуки, як її визначено у будь-якому з пп. 4-5.
15. Тверда форма за п. 14, яка складається головним чином із згаданої бета-форми.
16. Тверда форма метилового естеру [9S-(9![]() ,10
,10![]() ,12
,12![]() )]-5,16-біс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
)]-5,16-біс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
 ,
,
яка містить кристалічну гамма-форму вищевказаної сполуки, як її визначено у будь-якому з пп. 6-7.
17. Тверда форма за п. 16, яка складається головним чином з вказаної гамма-форми.
18. Тверда форма метилового естеру [9S-(9![]() ,10
,10![]() ,12
,12![]() )]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
)]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
 ,
,
яка містить кристалічну дельта-форму вищевказаної сполуки, як її визначено у будь-якому з пп. 8-9.
19. Тверда форма за п. 18, яка складається головним чином із згаданої дельта-форми.
20. Тверда форма метилового естеру [9S-(9![]() ,10
,10![]() ,12
,12![]() )]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
)]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'- kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу
 ,
,
яка містить кристалічну епсилон-форму вищевказаної сполуки, як її визначено у будь-якому з пп. 10-11.
21. Тверда форма за п. 20, яка складається головним чином із згаданої епсилон-форми.
22. Спосіб лікування нейродегенеративного захворювання, при якому вводять фармацевтично ефективну кількість кристалічного метилового естеру [9S-(9![]() ,10
,10![]() ,12
,12![]() )]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'-kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти згідно з будь-яким з пп. 1-11.
)]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'-kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти згідно з будь-яким з пп. 1-11.
23. Спосіб за п. 22, де захворювання вибране з групи, яка складається з: хвороби Паркінсона, хвороби Альцгеймера, хвороби Хантінгтона, периферичної невропатії, деменції при СНІДі.
24. Спосіб лікування хвороби Паркінсона, при якому вводять фармацевтично ефективну кількість кристалічного метилового естеру [9S-(9![]() ,10
,10![]() ,12
,12![]() )]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'-kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти згідно з будь-яким з пп. 1-11.
)]-5,16-бiс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'-kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти згідно з будь-яким з пп. 1-11.
Текст
1. Кристалічна форма метилового естеру [9S(9 ,10 ,12 )]-5,16-бiс[(етилтіо)метил]2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу C2 2 (19) 1 3 90259 6. Кристалічна форма метилового естеру [9S(9 ,10 ,12 )]-5,16-бiс[(етилтіо)метил]2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу H N 4 H N O S S N O HO S S N O HO N , CO2Me , яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK випромінювання, при кутах 2-тета: 9,6, 11,5, 12,5, 16,7, 19,3, 28,1. 7. Кристалічна форма за п. 6, яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK випромінювання, при кутах 2-тета: 7,5, 8,3, 9,6, 11,5, 11,8, 12,5, 15,9, 16,3, 16,7, 17,2, 18,0, 19,3, 21,0, 28,1. 8. Кристалічна форма метилового естеру [9S(9 ,10 ,12 )]-5,16-бiс[(етилтіо)метил]2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1оксо-9,12-епокси-1H-дііндоло[1,2,3-fg:3',2',1'kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу H N S HO O N CO2Me , , яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK випромінювання, при кутах 2-тета: 9,7, 12,1, 16,1, 18,3, 22,1, 22,2, 25,7, 25,8. 9. Кристалічна форма за п. 8, яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK випромінювання, при кутах 2-тета: 7,3, 8,3, 9,7, 11,1, 11,7, 12,1, 15,6, 16,1, 17,3, 18,3, 20,9, 22,1, 22,2, 25,7, 25,8. 10. Кристалічна форма метилового естеру [9S(9 ,10 ,12 )]-5,16-бiс[(етилтіо)метил]2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу , CO2Me , яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK випромінювання, при кутах 2-тета: 8,9, 9,2, 10,2, 14,6. 11. Кристалічна форма за п. 10, яка характеризується відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuK випромінювання, при кутах 2-тета: 8,9, 9,2, 10,2, 12,6, 14,2, 14,6, 17,0, 18,6, 20,4, 21,1, 23,9, 25,2. 12. Тверда форма метилового естеру [9S(9 ,10 ,12 )]-5,16-бiс[(етилтіо)метил]2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу H N O S S N HO O S N N O N O , CO2Me , яка містить кристалічну альфа-форму вищевказаної сполуки, як її визначено у будь-якому з пп. 1-3. 13. Тверда форма за п. 12, яка складається головним чином із згаданої альфа-форми. 14. Тверда форма метилового естеру [9S(9 ,10 ,12 )]-5,16-бiс[(етилтіо)метил]2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу H N O S S N HO O N CO2Me , , яка містить кристалічну бета-форму вищевказаної сполуки, як її визначено у будь-якому з пп. 4-5. 15. Тверда форма за п. 14, яка складається головним чином із згаданої бета-форми. 16. Тверда форма метилового естеру [9S(9 ,10 ,12 )]-5,16-біс[(етилтіо)метил]2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу 5 H N 90259 6 H N O O S S S S N O HO N N , CO2Me , яка містить кристалічну гамма-форму вищевказаної сполуки, як її визначено у будь-якому з пп. 6-7. 17. Тверда форма за п. 16, яка складається головним чином з вказаної гамма-форми. 18. Тверда форма метилового естеру [9S(9 ,10 ,12 )]-5,16-бiс[(етилтіо)метил]2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу H N O S S N HO O N CO2Me , , яка містить кристалічну дельта-форму вищевказаної сполуки, як її визначено у будь-якому з пп. 8-9. 19. Тверда форма за п. 18, яка складається головним чином із згаданої дельта-форми. 20. Тверда форма метилового естеру [9S(9 ,10 ,12 )]-5,16-бiс[(етилтіо)метил]2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти, який має формулу Даний винахід відноситься до кристалічних форм сполуки і до застосування таких форм для приготування лікарського засобу, зокрема для лікування хвороби Паркінсона. Попередній рівень техніки Сполука із структурою, зображеною нижче, в даний час проходить стадію клінічних випробувань стосовно хвороби Паркінсона (Idrugs, 2003, 6(4), 377-383). Ця сполука в подальшому позначатиметься як "сполука І". Систематичною назвою сполуки І є "метиловий естер [9S-(9α;10β,12α)]-5,16біс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10гідрокси-9-метил-1-оксо-9,12-епокси-1Н HO O N CO2Me , , яка містить кристалічну епсилон-форму вищевказаної сполуки, як її визначено у будь-якому з пп. 10-11. 21. Тверда форма за п. 20, яка складається головним чином із згаданої епсилон-форми. 22. Спосіб лікування нейродегенеративного захворювання, при якому вводять фармацевтично ефективну кількість кристалічного метилового естеру [9S-(9 ,10 ,12 )]-5,16-бiс[(етилтіо)метил]2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти згідно з будь-яким з пп. 1-11. 23. Спосіб за п. 22, де захворювання вибране з групи, яка складається з: хвороби Паркінсона, хвороби Альцгеймера, хвороби Хантінгтона, периферичної невропатії, деменції при СНІДі. 24. Спосіб лікування хвороби Паркінсона, при якому вводять фармацевтично ефективну кількість кристалічного метилового естеру [9S(9 ,10 ,12 )]-5,16-бiс[(етилтіо)метил]2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1оксо-9,12-епокси-1Н-дііндоло[1,2,3-fg:3',2',1'kl]піроло[3,4-і][1,6]бензодіазоцин-10-карбонової кислоти згідно з будь-яким з пп. 1-11. дііндоло[1,2,3-fg: 3',2',1'-к1]піроло [3,4-і][1,6] бензодіазоцин-10-карбонової кислоти". Подальші посилання відносяться до сполуки І, зокрема до способів її одержання [J. Med. Chem. 1997, 40(12), 1863-1869; Curr. Med. Chem. - Central Nervous System Agents, 2002, 2(2), 143-155], та до її потенційних медичних застосувань, головним чином при захворюваннях центральної нервової системи (ЦНС), особливо для лікування нейродегенеративних захворювань, наприклад, хвороби Паркінсона, хвороби Альцгеймера, хвороби Хантінгтона, периферичної невропатії, деменції при СНІДі та ослаблення слуху, таке як індуковане шумом ослаблення слуху [Progress in Medicinal Chemistry (2002), 40, 23-62; Bioorg. Med. Chem. Lett. 2002, 12(2), 147-150; Neuroscience, Oxford, 1998, 86(2), 461-472; J. Neurochemistry (2001), 77(3), 849-863; J. Neuroscience (2000), 20(1), 43-50; J. Neurochemistry (2002), 82(6), 1424-1434; Hearing Research, 2002, 166(1-2), 33-43]. Наступні патенти відносяться до сполуки І, включаючи її медичне застосування і синтез: WO 7 9402488, WO 9749406, US 5621100, ЕР 0651754 і ЕР 112932. У відомих способах сполука І утворюється в твердій аморфній формі. У даному винаході автори вперше виявили 5 кристалічних форм сполуки І (а саме: альфа, бета, гама, дельта і епсилон), таким чином забезпечуючи сприятливу можливість для поліпшення процесу виробництва сполуки І і її фармацевтичного застосування. Існує необхідність в кристалічних формах, які можуть демонструвати бажані та корисні хімічні та фізичні властивості. Також існує необхідність в надійних і відтворних способах виробництва, очищення і одержання препаратів сполуки І, що дозволяють зробити її товаром, що легко продається. В першому аспекті даний винахід відноситься до кристалічної сполуки І, особливо до кристалічних форм сполуки І. Відповідно, винахід забезпечує кристалічну форму сполуки І, звану "альфа", яка характеризується одним або більше з наступного: (і) порошкова рентгенограма, показана на Фіг.1, одержана із застосуванням CuKα-випромінювання; (іі) порошкова рентгенограма, одержана із застосуванням CuKα-випромінювання, що має відбивання при кутах 2θ: 5,2, 7,3, 8,1, 10,1, 10,4, 11,2, 13,2, 15,1, 15,5, 17,3, 21,7, 23,8, 25,1; (ііі) твердотільний 13СЯМР спектр, показаний на Фіг.7; (iv) відбивний ІЧспектр в близькій ІЧ-області, показаний на Фіг.10. В другому аспекті винахід забезпечує кристалічну форму сполуки І, звану "бета", яка характеризується одним або більше з наступного: (і) порошкова рентгенограма, показана на Фіг.2, одержана із застосуванням CuKα-випромінювання; (іі) порошкова рентгенограма, одержана із застосуванням CuKα-випромінювання, що має відбивання при кутах 2θ: 6,6, 8,9, 10,7, 11,4, 11,7, 13,7, 17,0, 18,5, 18,8, 19,2, 20,3, 24,4, 30,6; (ііі) твердотільний 13С-ЯМР спектр, показаний на Фіг.8; (iv) відбивний ІЧ-спектр в близькій ІЧ-області, показаний на Фіг.11. В подальшому аспекті винахід забезпечує кристалічну форму сполуки І, звану "гама", яка характеризується одним або більше з наступного: (і) порошкова рентгенограма, показана на Фіг.3, одержана із застосуванням CuKα-випромінювання; (іі) порошкова рентгенограма, одержана із застосуванням CuKα-випромінювання, що має відбивання при кутах 2θ: 7,5, 8,3, 9,6, 11,5, 11,8, 12,5, 15,9, 16,3, 16,7, 17,2, 18,0, 19,3, 21,0, 28,1; (ііі) твердотільний 13С-ЯМР спектр, показаний на Фіг.9; (iv) відбивний ІЧ-спектр в близькій ІЧ-області, показаний на Фіг.12. В подальшому аспекті даний винахід забезпечує кристалічну форму сполуки І, звану "дельта", яка характеризується одним або більше з наступного: (і) порошкова рентгенограма, показана на Фіг.13, одержана із застосуванням CuKαвипромінювання; (іі) порошкова рентгенограма, одержана із застосуванням CuKα-випромінювання, що має відбивання при кутах 2θ: 7,3, 8,3, 9,7, 11,1, 11,7, 12,1, 15,6, 16,1, 17,3, 18,3, 20,9, 22,1, 22,2, 25,7, 25,8. В подальшому аспекті винахід забезпечує кристалічну форму сполуки І, звану "епсилон", яка 90259 8 характеризується одним або більше з наступного: (і) порошкова рентгенограма, показана на Фіг.15, одержана із застосуванням CuKα-випромінювання; (іі) порошкова рентгенограма, одержана із застосуванням CuKα-випромінювання, що має відбивання при кутах 2θ: 8,9, 9,2, 10,2, 12,6, 14,2, 14,6, 17,0, 18,6, 20,4, 21,1, 23,9, 25,2. Далі винахід відноситься до способів одержання кристалічних форм даного винаходу і до застосування таких форм для приготування лікарського засобу, який містить сполуку І як активний компонент. Стислий опис ілюстративних матеріалів Фіг.1: Показує порошкову рентгенограму альфа-форми сполуки І. Фіг.2: Показує порошкову рентгенограму бетаформи сполуки І. Фіг.3: Показує порошкову рентгенограму гамаформи сполуки І. Фіг.4: Показує диференціально-сканувальну калориметричну термограму альфа-форми сполуки І. Фіг.5: Показує диференціально-сканувальну калориметричну термограму бета-форми сполуки І. Фіг.6: Показує диференціально-сканувальну калориметричну термограму гама-форми сполуки І. Фіг.7: Показує твердотільний 13С-ЯМР спектр альфа-форми сполуки І. Фіг.8: Показує твердотільний 13С-ЯМР спектр бета-форми сполуки І. Фіг.9: Показує твердотільний 13С-ЯМР спектр гама-форми сполуки І. Фіг.10: Показує відбивний ІЧ-спектр в близькій ІЧ-області альфа-форми сполуки І. Фіг.11: Показує відбивний ІЧ-спектр в близькій ІЧ-області бета-форми сполуки І. Фіг.12: Показує відбивний ІЧ-спектр в близькій ІЧ-області гама-форми сполуки І. Фіг.13: Показує порошкову рентгенограму дельта-форми сполуки І. Фіг.14: Показує диференціально-сканувальну калориметричну термограму дельта-форми сполуки І. Фіг.15: Показує порошкову рентгенограму епсилон-форми сполуки І. Фіг.16: Показує диференціально-сканувальну калориметричну термограму епсилон-форми сполуки І. Фіг.17: Показує конформацію однієї з молекул (молекула 1) у альфа-формі сполуки І. Фіг.18: Показує конформацію однієї з молекул (молекула 2) у альфа-формі сполуки І. Фіг.19: Показує кристалічну упаковку молекул в альфа-формі сполуки І. Подальші деталі стосовно фігур представлені нижче в прикладах. Докладний опис переважного варіанту здійснення Відкриття кристалічної форми фармацевтично застосовної сполуки надає сприятливу можливість поліпшити експлуатаційні властивості фармацевтичного продукту та способу виробництва. 9 Відмінності у фізичних властивостях, таких як стабільність (період напіврозкладання), біодоступність, розчинність і швидкість розчинення, що проявляються різними твердими формами сполуки, є важливими чинниками у виробництві та таблетуванні сполуки. Відмінності в стабільності можуть походити від змін в хімічній реакційній здатності (наприклад, при окисненні) або від механічних змін (наприклад, кришіння пігулок при зберіганні може привести до конверсії в термодинамічно більш стабільну кристалічну форму) або від обох цих чинників. Фізичні властивості твердої форми важливі при обробці, наприклад якась тверда форма може важче фільтруватися і відмиватися від домішок. Це може бути завдяки відмінностям у розподілі частинок за формою та розмірами між однією кристалічною формою та іншою або по відношенню до аморфної форми. Крім того, для ліків, які існують в різних кристалічних формах і які продаються в твердій формі, завжди важливо як з медичних, так і з комерційних міркувань виробляти і продавати відомі кристалічні форми. Відкриття кристалічної сполуки І та існування 5 кристалічних форм дає можливість застосування певних кристалічних форм замість аморфної форми. Також, фізичні властивості кристалічної сполуки І пропонують переваги для цілей виробництва препаратів у вигляді таблеток, наприклад, пряме пресування полегшується, коли є певна кристалічна форма. Кристалічні сполуки є, загалом, більш стабільними, ніж відповідні аморфні сполуки, і це особливо важливо у разі чутливої до повітря і світла сполуки І. Експерименти в світловій камері Heraeus Santest CPS+ були виконані для кристалічних форм альфа, бета і гама, в яких тверда сполука опромінювалася світлом протягом 14 годин при 650 Вт. Обробка світлом призводила до майже 60% розкладання аморфної речовини, тоді як кристалічні форми показували менш ніж 30% розкладання. Сполука І містить два атоми сірки і легко окиснюється в складну суміш сульфонів і сульфоксидів. Ця чутливість до окиснення вимагає великої акуратності в процесі очищення сполуки І. Даний винахід, який робить можливим очищення сполуки І кристалізацією, зменшує рівень окиснених сполук в порівнянні з продуктом, одержаним, коли автори даного винаходу використовували інші методи очищення, такі як хроматографія. Крім того, сполука І містить активну естерну групу, яка може вступати в реакцію переестерифікації та може також бути чутливою до гідролізу. На фінальній стадії синтезу сполуки І, бажаний етилтіольний фрагмент вводиться із застосуванням етилмеркаптану як реактиву [J. Med. Chem. 1997, 40(12), 1863-1869; Curr. Med. Chem. - Central Nervous System Agents, 2002, 2(2), 143-155]. Етилмеркаптан має сильний характерний неприємний запах, який небажаний у фармацевтичному продукті. Виділення сполуки І як аморфної твердої речовини приводить до включення етилмеркаптану в твердий продукт, в той же час рівень цього небажаного реактиву зменшується при кристалізації. 90259 10 Крім того, фізичні характеристики кристалічних форм даного винаходу покращують стадію виділення, наприклад шляхом зменшення часу на фільтрацію в порівнянні з аморфною формою сполуки І, що має велике значення у разі виробництва сполуки І у великих масштабах. В цьому відношенні було знайдено, що дельта-форма має кращі фільтраційні властивості, ніж альфа-форма. Подальші відмінності у фізичних і хімічних властивостях кристалічних форм в порівнянні з аморфною формою полягають у більш високих точках плавлення, див. далі Таблицю 1 в прикладі 9, що може давати переваги при подальшій обробці. Як вказано вище, автори даного винаходу тепер вперше встановили, що сполука І може бути одержана в кристалічній формі та що існує принаймні 5 кристалічних форм сполуки І, тут звані як альфа, бета, гама, дельта і епсилон. Так, в широкому сенсі винахід відноситься до кристалічної сполуки І, зокрема до кристалічних форм сполуки І. Під використовуваним тут виразом "кристалічні форми сполуки І" розуміються будь-які кристалічні форми сполуки І, наприклад, у протилежність аморфній формі. Зокрема, термін "кристалічна сполука І" включає альфа, бета, гама, дельта та/або епсилон кристалічні форми сполуки І, які утворюються, як визначено тут. Кристалічні форми сполуки розрізняються за положеннями атомних ядер в елементарній комірці ствердлої сполуки. Ці відмінності призводять до різних макроскопічних властивостей, таких як термічна поведінка, проникність для пари та розчинність, які, як показано раніше, мають практичні наслідки у фармації. Різні форми, описані тут, можуть бути розрізнені одна від одної шляхом застосування різних аналітичних методів, відомих будьякому фахівцю в даній галузі. Такі методи включають, але не обмежуються тільки ними, порошковий рентгеноструктурний аналіз (XRD), диференціально-сканувальну калориметрію (DSC), спектроскопію твердотільного ядерного магнітного резонансу (NMR) і відбивну ІЧ-спектроскопію в близькій ІЧ-області (NIR). Кристалічні форми сполуки найлегше розрізняються рентгеноструктурним аналізом. Рентгеноструктурний аналіз монокристалів надає дані, які можуть бути використані для визначення положень ядер, які, у свою чергу, можна візуалізувати за допомогою комп'ютера або механічних моделей, забезпечуючи, таким чином, тривимірне зображення сполуки. Рентгенівські дослідження монокристалів надають незрівнянну інформацію, вони цінні та якісні, хоча ці дані іноді важко одержувати. Рентгеноструктурний аналіз використовується у фармацевтичній промисловості більш часто для характеризування кристалічних форм ліків, ніж рентгенівський аналіз монокристалів. Рентгеноструктурний аналіз створює фінгерпринт, який є унікальним для кристалічної форми та здатним відрізнити її від аморфної сполуки та всіх інших кристалічних форм сполуки. Відповідно, один з варіантів здійснення даного винаходу відноситься до кристалічної форми сполуки І, званої "альфа", охарактеризованої порошковою рентгенограмою, показаною на Фіг.1, одер 11 жаною із застосуванням CuKα-випромінювання. У наступному варіанті здійснення альфа-форма сполуки І охарактеризована відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuKα-випромінювання при кутах 2-тета: 5,2, 10,1, 10,4, 13,2, 15,1, 25,1. Альфа-форма сполуки І може також бути охарактеризована відбиваннями на рентгенівській дифрактограмі, одержаній із застосуванням CuKα-випромінювання при кутах 2θ: 5,2, 7,3, 8,1, 10,1, 10,4, 11,2, 13,2, 15,1, 15,5, 17,3, 21,7, 23,8, 25,1. Альфа-форма сполуки І може також бути охарактеризована твердотільним 13СЯМР спектром, показаним на Фіг.7. Альфа-форма сполуки І може також бути охарактеризована відбивним ІЧ-спектром в близькій ІЧ-області, представленим на Фіг.10. Альфа-форма сполуки І може також бути охарактеризована наявністю температури плавлення в діапазоні 180-190°С. Альфаформа сполуки І може також бути охарактеризована диференціально-сканувальною калориметричною термограмою, що суттєво узгоджується з тією, що показана на Фіг.4. Альфа-форма сполуки І може також бути охарактеризована диференціально-сканувальною калориметричною термограмою, що має ендотермію від приблизно 170°С до приблизно 200°С. Кристалічна структура альфаформи (приклад 8.5) має порожнечу в кристалічній решітці, яка може бути зайнята або може не бути зайнята невеликим розчинником, зокрема молекулою води або метанолу. Таким чином, кристалічна альфа-форма сполуки І сольватована в різному ступені водою та/або метанолом. Відповідно, даний винахід також відноситься до кристалічної форми, охарактеризованої наявністю кристалічної структури з наступними характеристиками при 122 K: просторова група: Р212121, розміри елементарної комірки: а=10,227(2) Å, b=23,942(2) Å і с=24,240(2) Å, α=90°, β=90°, γ=90°, 2 молекули в асиметричній комірці. Оскільки асиметрична комірка в цій кристалічній структурі містить 2 молекули сполуки І і одне місце для розчинника, повне займання місця розчинника веде до напівсольвату. Крім цього, даний винахід відноситься до представленої вище кристалічної структури, яка має положення атомів головним чином як визначено координатами в таблицях 2-4. Зрозуміло, що відбивання виражаються в градусах (при кутах 2θ, тобто при 2-тета кутах), коли тут наводяться дані порошкової рентгенограми: відбиттів (піків). Подальший варіант здійснення відноситься до кристалічної форми сполуки І, званої "бета", охарактеризованої порошковою рентгенограмою, показаною на Фіг.2, одержаною із застосуванням CuKα-випромінювання. У наступному варіанті здійснення бета-форма сполуки І охарактеризована відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuKα-випромінювання при кутах 2-тета: 6,6, 8,9, 10,7, 11,7, 24,4, 30,6. Бета-форма сполуки І може також бути охарактеризована відбиваннями на рентгенівській дифрактограмі, одержаній із застосуванням CuKαвипромінювання при кутах 2θ: 6,6, 8,9, 10,7, 11,4, 11,7, 13,7, 17,0, 18,5, 18,8, 19,2, 20,3, 24,4, 30,6. Бета-форма сполуки І може також бути охаракте 90259 12 ризована твердотільним 13С-ЯМР спектром, показаним на Фіг.8. Бета-форма сполуки І може також бути охарактеризована відбивним ІЧ-спектром в близькій 14-області, представленим на Фіг.11. Бета-форма сполуки І може також бути охарактеризована наявністю температури плавлення в діапазоні 209-213°С, переважно близько 211°С. Бетаформа сполуки І може також бути охарактеризована диференціально-сканувальною калориметричною термограмою, що в основному узгоджується з тією, що показана на Фіг.5. Бета-форма сполуки І може також бути охарактеризована диференціально-сканувальною калориметричною термограмою, що має ендотермію від приблизно 205°С до приблизно 220°С. Подальший варіант здійснення відноситься до кристалічної форми сполуки І, званої "гама", охарактеризованої порошковою рентгенограмою, показаною на Фіг.3, одержаною із застосуванням CuKα-випромінювання. У одному з варіантів здійснення гама-форма сполуки І охарактеризована відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuKα-випромінювання при кутах 2-тета: 9,6, 11,5, 12,5, 16,7, 19,3, 28,1. Гамаформа сполуки І може також бути охарактеризована відбиваннями на рентгенівській дифрактограмі, одержаній із застосуванням CuKαвипромінювання при кутах 2θ: 7,5, 8,3, 9,6,11,5, 11,8, 12,5, 15,9, 16,3,16,7,17,2, 18,0, 19,3,21,0,28,1. Гама-форма сполуки І може також бути охарактеризована твердотільним 13С-ЯМР спектром, показаним на Фіг.9. Гама-форма сполуки І може також бути охарактеризована відбивним ІЧ-спектром в близькій ІЧ-області, представленим на Фіг.12. Гама-форма сполуки І може також бути охарактеризована наявністю температури плавлення в діапазоні 212-218°С. Гама-форма сполуки І може також бути охарактеризована диференціальносканувальною калориметричною термограмою, що в основному узгоджується з тією, що показана на Фіг.6. Гама-форма сполуки І може також бути охарактеризована диференціально-сканувальною калориметричною термограмою, що має ендотермію від приблизно 210°С до приблизно 225°С. Інший варіант здійснення відноситься до кристалічної форми сполуки І, званої "дельта", охарактеризованої порошковою рентгенограмою, показаною на Фіг.13, одержаною із застосуванням CuKαвипромінювання. У одному з варіантів здійснення дельта-форма охарактеризована відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuKα-випромінювання при кутах 2-тета: 9,7, 12,1, 16,1, 18,3, 22,1, 22,2, 25,7, 25,8. Дельтаформа сполуки І може також бути охарактеризована відбиваннями на рентгенівській дифрактограмі, одержаній із застосуванням CuKαвипромінювання при кутах 2θ: 7,3, 8,3, 9,7, 11,1, 11,7, 12,1, 15,6, 16,1, 17,3, 18,3, 20,9, 22,1, 22,2, 25,7, 25,8. Дельта-форма сполуки І може також бути охарактеризована наявністю температури плавлення в діапазоні 211-223°С. Дельта-форма сполуки І може також бути охарактеризована диференціально-сканувальною калориметричною термограмою, яка в основному узгоджується з тією, що показана на Фіг.14. Дельта-форма сполуки 13 І може також бути охарактеризована диференціально-сканувальною калориметричною термограмою, яка має ендотермію від приблизно 210°С до приблизно 228°С. Інший варіант здійснення відноситься до кристалічної форми сполуки І, званої "епсилон", охарактеризованої порошковою рентгенограмою, показаною на Фіг.15, одержаною із застосуванням CuKα-випромінювання. У одному з варіантів здійснення епсилон-форма охарактеризована відбиваннями на порошковій рентгенограмі, одержаній із застосуванням CuKα-випромінювання при кутах 2-тета: 8,9, 9,2, 10,2, 14,6. Епсилон-форма сполуки І може також бути охарактеризована відбиваннями на рентгенівській дифрактограмі, одержаній із застосуванням CuKα-випромінювання при кутах 2θ: 8,9, 9,2, 10,2, 12,6, 14,2, 14,6, 17,0, 18,6, 20,4, 21,1, 23,9, 25,2. Епсилон-форма сполуки І може також бути охарактеризована наявністю температури плавлення в діапазоні 180-185°С. Епсилон-форма сполуки І може також бути охарактеризована диференціально-сканувальною калориметричною термограмою, що в основному узгоджується з тією, яка показана на Фіг.16. Епсилон-форма сполуки І може також бути охарактеризована диференціально-сканувальною калориметричною термограмою, що має ендотермію від приблизно 175 °С до приблизно 190°С. Крім цього, даний винахід відноситься до будь-яких сумішей кристалічних форм даного винаходу, наприклад, до суміші кристалічних форм альфа і гама сполуки І. Вживана тут фраза типу "кристалічна форма сполуки І, охарактеризована порошковою рентгенограмою, показаною на Фіг.1, одержаною із застосуванням CuKα-вппромінювання" означає кристалічну форму сполуки І, що має порошкову рентгенограму, в основному подібну Фіг.1, тобто порошкову рентгенограму, представленій на цій фігурі як зразок та виміряний за порівнянних умов, як описано в прикладі 7.1, або за будь-яким зіставним методом, що використовує CuKαвипромінювання. Це визначення також застосовує принцип "mutatis mutandis" ("зроби необхідні зміни") до NMR- і NIR-фігур і до усіх інших рентгенівських даних, описаних тут (наприклад, дані по рентгенівським пікам) для всіх п'яти ідентифікованих кристалічних форм, відповідно, наприклад альфа, бета, гама, дельта і епсилон, так що враховуються межі аналітичних варіацій. Твердотільні 13С-ЯМР спектри, що розглядаються тут, виміряні переважно при швидкості обертання ампули в спектрометрі, що складала 5000Гц, з СР-М AS-насадкою (кросполяризація/обертання при магічному куті). Так, ЯМР-спектри вимірювали переважно, як описано в прикладі 7.2 або будь-яким іншим зіставним методом. Відбивні ІЧ-спектри в близькій ІЧ-області, наведені тут, вимірювали переважно, як описано в прикладі 7.3 або будь-яким іншим зіставним методом, особливо з розділенням 2см-1 з корекцією нульової лінії та нахилу із застосуванням мультиплікативної корекції розкиду (MSC). 90259 14 У подальшому варіанті здійснення даний винахід відноситься до кристалічних форм сполуки І, які були в основному чистими. Термін "в основному чисті", вживаний тут, означає, що кристалічні форми сполуки І, наприклад альфа, бета, гама, дельта або епсилон-форма, мали чистоту принаймні близько 90%, включаючи, наприклад, принаймні близько 93% і принаймні близько 95%. Аморфна форма сполуки І плавиться при температурі біля 150°С, яку легко відрізнити від температур плавлення описаних тут кристалічних форм сполуки І, див. в таблиці 1 в прикладі 9. Відповідно, в даному винаході кристалічна сполука І має температуру плавлення принаймні 175°С або принаймні 180°С і може знаходитися в діапазоні 175°С-225°С, 180°С-225°С, 180°С-220°С, або 181°С-218°С, альтернативно в діапазоні 180°С190°С або 210-225°С. Термін "температура плавлення", вживаний тут, відноситься до початкової ділянки ендотерми плавлення, виміряної методом диференціальносканувальної калориметрії, див. приклад 7.4. Подальший варіант здійснення відноситься до твердої сполуки І, що містить альфа-форму кристалічної сполуки І. Даний винахід також відноситься до твердої сполуки І, що складається головним чином з описаної тут альфа-форми кристалічної сполуки І. Термін "головним чином" в даному контексті означає, що тверда сполука І складається з принаймні 75%, так як принаймні 80%, принаймні 90% або принаймні 95% кристалічної альфаформи від загального вмісту сполуки І. Подальший варіант здійснення винаходу відноситься до твердої сполуки І, що містить кристалічну бета-форму сполуки І. Даний винахід також відноситься до твердої сполуки І, що складається головним чином з описаної тут кристалічної бетаформи сполуки І. Термін "головним чином" в даному контексті означає, що сполука І складається з принаймні 75%, так як принаймні 80%, принаймні 90% або принаймні 95% кристалічної бета-форми від загального вмісту сполуки І. Подальший варіант здійснення винаходу відноситься до твердої сполуки І, що містить кристалічну гама-форму сполуки І. Даний винахід також відноситься до твердої сполуки І, що складається головним чином з описаної тут кристалічної гамаформи сполуки І. Термін "головним чином" в даному контексті означає, що тверда сполука І складається з принаймні 75%, так як принаймні 80%, принаймні 90% або принаймні 95% кристалічної гама-форми від загального вмісту сполуки І. Подальший варіант здійснення винаходу відноситься до твердої сполуки І, що містить кристалічну дельта-форму сполуки І. Даний винахід також відноситься до твердої сполуки І, що складається головним чином з описаної тут кристалічної дельта-форми сполуки І. Термін "головним чином" в даному контексті означає, що тверда сполука І складається з принаймні 75%, так як принаймні 80%, принаймні 90% або принаймні 95% кристалічної дельта-форми від загального вмісту сполуки І. Подальший варіант здійснення винаходу відноситься до твердої сполуки І, що містить криста 15 лічну епсилон-форму сполуки І. Даний винахід також відноситься до твердої сполуки І, що складається головним чином з описаної тут епсилонформи сполуки І. Термін "головним чином" в даному контексті означає, що тверда сполука І складається з принаймні 75%, так як принаймні 80%, принаймні 90% або принаймні 95% кристалічної епсилон-форми від загального вмісту сполуки І. Власне кажучи, нові кристалічні форми сполуки І можуть бути одержані різноманітними способами, включаючи, але не обмежуючись тільки ним, кристалізацію сполуки І з відповідного розчинника. Сполука І може бути одержана за способами, відомими фахівцям в цій галузі, такими як описані тут. За загальноприйнятим способом, сполука І може бути змішана з відповідним розчинником, який може бути нагрітий для полегшення розчинення сполуки І. Суміш розчинника і сполуки І може бути також нагріта для полегшення подальшої конверсії в кристалічну форму. Переважна температура для цього може змінюватися від приблизно 30°С до температури кипіння розчинника (наприклад, температури кипіння зі зворотним холодильником). Найбільш переважні температури можуть варіюватися від біля 60°С до температури кипіння розчинника. Одержана суміш розчинника та сполуки І може бути охолоджена для ініціації та/або продовження кристалізації. Переважно охолоджувати суміш (наприклад, включаючи самоохолодження до кімнатної температури) до температури від, наприклад, біля мінус 20°С до приблизно 20°С, наприклад, до кімнатної температури. Осади, що утворилися, можуть бути виділені з охолодженої суміші, наприклад, шляхом фільтрації або центрифугування, і, якщо необхідно, промиті відповідним розчинником, таким як, але не обмежуючись тільки ним, розчинник, використаний для кристалізації, а потім висушені у вакуумі при температурі навколишнього середовища або при злегка підвищеній температурі, наприклад у струмі азоту. Затравочні кристали можуть бути додані до суміші, що кристалізується, для ініціації кристалізації. Як показано раніше, кристалічна сполука І, особливо різні кристалічні форми даного винаходу можуть бути одержані шляхом (а) розчинення сполуки І у відповідному розчиннику, (b) кристалізації шляхом осадження сполуки І з розчинника, і (с) відділенням розчинника від одержаної кристалічної сполуки І; або, альтернативно, за способом, що включає стадії: (а) суспендування сполуки І у відповідному розчиннику на період часу, достатній для конверсії в кристалічні форми, і (b) відділення спирту від кристалічної сполуки І. Нижче описано, як різні розчинники можуть бути застосовані для одержання різних кристалічних форм сполуки І: альфа, бета, гама, дельта і епсилон. У переважному варіанті здійснення винаходу, спосіб даного винаходу для одержання кристалічної сполуки І, включаючи альфа-, бета-, гама-, дельта- або епсилон-форму, включає кристалізацію шляхом осадження сполуки І з відповідного розчинника та відділення цього розчинника від одержаної кристалічної сполуки І. Зрозуміло, що коли згадується 90259 16 одержання різних кристалічних форм даного винаходу, тоді продукт, який може бути одержаний, або, точніше, продукт, одержаний за такими способами, - це також відноситься до "твердої сполуки І, що містить кристалічну сполуку І" і зокрема до описаної вище "твердої сполуки І, що складається головним чином з однієї особливої кристалічної форми сполуки І", наприклад альфа, бета, гама, дельта або епсилон-форми. Відповідно, один аспект даного винаходу відноситься до способу одержання кристалічної сполуки І, який відрізняється тим, що згадану кристалічну сполуку І утворюють в розчиннику, вибраному з групи, яка складається з: (і) метанолу, що містить від 0% до приблизно 8% води; (іі) аліфатичного С3-С6 спирту (наприклад, 1-пропанолу, 1-бутанолу, 2-бутанолу, трет-бутанолу, 1пентанолу), що містить 4-8% води (наприклад, 1бутанол з 4% води; 1-пропанол з 4% води, 1пентанол з 4% води, трет-бутанол з 7% води, 2бутанол з 4% води); (ііі) естеру оцтової кислоти, що містить принаймні 4% води, де згаданий естер оцтової кислоти визначається формулою CH3CO2R, де R може бути C1-С6-алкілом; наприклад етилацетат або ізопропілацетат (наприклад, етилацетат з 4% води або ізопропілацетат з 6% води). Даний винахід також відноситься до кристалічної сполуки І, яка може бути одержана, або, зокрема, одержаної у такий спосіб. У переважному варіанті здійснення, цей спосіб призводить до одержання альфа-форми кристалічної сполуки І. Другий аспект даного винаходу відноситься до способу одержання кристалічної сполуки І, який відрізняється тим, що згадану кристалічну сполуку І утворюють в ізопропілацетаті. Даний винахід також відноситься до кристалічної сполуки І, яка може бути одержана, або, зокрема, одержаної у такий спосіб. У переважному варіанті здійснення, цей спосіб призводить до одержання бета-форми кристалічної сполуки І. У наступному аспекті даний винахід відноситься до способу одержання кристалічної сполуки І, який відрізняється тим, що згадану кристалічну сполуку І утворюють в розчиннику, вибраному з групи, що складається з: (і) аліфатичного C1-С3 нітрилу (наприклад, ацетонітрилу, пропіонітрилу), що містить аж до приблизно 12% води (наприклад, пропіонітрил з 4% води або ацетонітрил з 12% води), зрозуміло, що пропіонітрил (CH3CH2CN) є С3-нітрилом; (іі) етанолу, що містить від 0% до приблизно 8% води, (ііі) аліфатичних С3-С6 спиртів (наприклад, 1-пропанолу або 1-бутанолу) з принаймні приблизно 10% води (наприклад, 1пропанол з 10% води, 1-бутанол з 10% води); (iv) етилацетату реактивної чистоти. Під терміном "етилацетат реактивної чистоти" мається на увазі менш ніж 0,5% води. Даний винахід також відноситься до кристалічної сполуки І, яка може бути одержана, або, зокрема, одержаної у такий спосіб. У переважному варіанті здійснення, цей спосіб призводить до одержання гама-форми кристалічної сполуки І. У наступному варіанті здійснення, даний винахід відноситься до способу одержання кристалічної сполуки І, який відрізняється тим, що згадану 17 кристалічну сполуку І утворюють в розчиннику, вибраному з групи, що складається з: (і) аліфатичних С2-С6 спиртів (наприклад, етанолу, циклопропілметанолу або 1-пропанолу) з менш ніж 4% води, наприклад, менш ніж 3%, наприклад, близько 2% (наприклад, циклопропілметанол, 1-пропанол з 2% води, етанол з 2% води (без перемішування)). Даний винахід також відноситься до кристалічної сполуки І, яка може бути одержана, або, зокрема, одержаної у такий спосіб. У переважному варіанті здійснення, цей спосіб призводить до одержання дельта-форми кристалічної сполуки І. У наступному варіанті здійснення, даний винахід відноситься до способу одержання кристалічної сполуки І, який відрізняється тим, що згадану кристалічну сполуку І утворюють в бутиронітрилі (CH3CH2CH2CN). Даний винахід також відноситься до кристалічної сполуки І, яка може бути одержана, або, зокрема, одержаної у такий спосіб. У переважному варіанті здійснення, цей спосіб призводить до одержання епсилон-форми кристалічної сполуки І. Також було знайдено, що кожна з кристалічних форм альфа і бета може бути перетворена в кристалічну гама-форму, у присутності відповідного розчинника, зокрема ацетонітрилу, як показано в прикладі 6.1. Кристалічна бета-форма може бути перетворена в кристалічну альфа-форму в присутності метанолу, як показано в прикладі 6.1. Даний винахід також відноситься до кристалічного продукту, зокрема до кристалічних форм сполуки І, що можуть бути одержані, або в переважному варіанті здійснення одержаних за описаним тут способом одержання кристалічної сполуки І. В наступному аспекті даний винахід відноситься до способу одержання сполуки І, який містить перетворення кристалічної форми сполуки І (наприклад, описаних тут альфа-, бета- або гамаформи або будь-якої їх суміші) в аморфну форму сполуки І. Такий спосіб в переважному варіанті здійснення включає стадії (а): розчинення кристалічної сполуки І в ароматичному розчиннику, наприклад ароматичному вуглеводні, переважно алкілбензолі, такому як ксилол або толуол, (b) осадження сполуки І з ароматичного розчинника; і (с) відділення ароматичного розчинника від осадженої аморфної сполуки І. Як вказано раніше, утворення кристалічної сполуки І є вельми корисним, між іншим, також як стадія очищення при одержанні сполуки І для фармацевтичного застосування. Далі, даний винахід відноситься до способу одержання сполуки І, який включає описану тут стадію кристалізації. Так, один з варіантів здійснення даного винаходу відноситься до способу виробництва сполуки І, який містить стадію, де сполуку І перетворюють в кристалічну сполуку І. Зрозуміло, що кристалічна сполука І даного винаходу може бути одержана описаним тут способом, наприклад осадженням з розчинника сполуки І в кристалічній формі, як описано тут, і відділенням одержаної кристалічної сполуки І від розчинника. Зокрема, даний винахід відноситься до способу одержання сполуки І, в якому сполуку І перет 90259 18 ворюють в кристалічну сполуку, включаючи кристалічні форми даного винаходу, наприклад альфаабо гама-форму, з початкової суміші сполуки І. Термін "початкова суміш" в даному контексті означає, що суміш містить домішки, наприклад продукти окиснення, що походять із сполуки І, які бажано видалити. Початкова суміш може бути виділена з реакційної суміші безпосередньо або початкова реакційна суміш може бути піддана будь-якому попередньому очищенню, наприклад обробці основою. Далі даний винахід відноситься до застосування кристалічної сполуки І або твердої речовини даного винаходу для одержання лікарського засобу, що містить сполуку І як активний компонент. Відповідно, даний винахід також відноситься до способу одержання фармацевтичної композиції сполуки І, який включає одержання згаданої композиції з кристалічної сполуки І, як визначено тут, наприклад, одержаної за способом, описаним тут, включаючи кристалічну форму або тверду речовину даного винаходу. Один спеціальний варіант здійснення відноситься до такого застосування альфа- або гама-форми даного винаходу для одержання фармацевтичної композиції. Як описано раніше, одержання препаратів з певної кристалічної форми має перевагу стосовно підвищеної чистоти, виходу та наявності добре визначених властивостей, таких як розчинність. В цьому відношенні, даний винахід також забезпечує фармацевтичну композицію, яка містить достатню кількість сполуки І, яка може бути одержана, або одержаної за способом даного винаходу для одержання кристалічної сполуки І, включаючи кристалічні форми даного винаходу, наприклад з альфаабо гама-форм. Фармацевтична композиція може бути будь-якою композицією, придатною для вживання сполуки І, наприклад препаратом у вигляді твердої дисперсії або препаратів у вигляді твердого розчину. У одному з варіантів здійснення, кристалічний продукт даного винаходу, наприклад, включаючи зокрема альфа, бета, гама, дельта або епсилон кристалічну форму, або їх суміші, може бути приготований у вигляді препарату у формі твердого розчину або твердої дисперсії. Твердий розчин може бути одержаний шляхом розчинення кристалічного продукту даного винаходу в розплавленому носії. Твердий розчин утворюється при охолоджуванні до кімнатної температури. Тверда дисперсія може бути одержана шляхом диспергування кристалічного продукту даного винаходу в розплавленому носії. Тверда дисперсія утворюється при охолоджуванні до кімнатної температури. Носій, вживаний для одержання твердого розчину або твердої дисперсії, може бути одним компонентом або сумішшю декількох компонентів. Носій, вживаний для одержання твердого розчину або твердої дисперсії, звичайно є твердим або напівтвердим при кімнатній температурі та звичайно має липкий, масляний або восковий характер. Проте носій може також бути рідиною при кімнатній температурі або навіть при температурі нижче 5°С. Як приклади носіїв можуть бути згадані поліетиленгліколі (PEG), поліоксамери, естери 19 поліетиленгліколей, віск, гліцериди, спирти жирних кислот, жирні кислоти, цукрові спирти, вітамін Ε і похідні вітаміну Е. Твердий розчин або тверда дисперсія може бути застосована такою, як вона є, або альтернативно приготована у вигляді фармацевтичних композицій, таких як пігулки, капсули тощо. Твердий розчин та тверда дисперсія також можуть бути одержані іншими способами, як, наприклад, методом розчинника або методом плавлення (Serajuddin, A.T.M., Journal of Pharmaceutical Sciences, Vol.88, 1058-1066). Один з варіантів здійснення даного винаходу відноситься до фармацевтичної композиції, яка є твердим розчином, приготованим з кристалічної сполуки І даного винаходу, наприклад, з кристалічної альфа- або гама-форми даного винаходу. Так, кристалічний продукт даного винаходу, зокрема альфа, бета, гама, дельта або епсилон кристалічна форма, або їх суміші можуть бути застосовані для одержання фармацевтичної композиції із сполукою І в розчині, наприклад композиції, подібної до вперше описаної в US 6200968. До обсягу даного винаходу також входить фармацевтична композиція, яка містить ефективну кількість кристалічної сполуки І, описаної тут, зокрема альфа-, бета-, гама-, дельта- або епсилонформу, визначені тут, або їх суміші, та фармацевтично прийнятний носій. Кристалічний продукт даного винаходу, наприклад включаючи кристалічну альфа-, бета-, гама-, дельта- або епсилон-форму, або їх суміші, може бути включений в різноманітні фармацевтичні композиції. Прикладами таких рецептур, що містять кристалічний продукт даного винаходу (наприклад, кристалічну альфа-, бета-, гама-, дельтаабо епсилон-форму), є пігулки, капсули, гранули, порошки, супозиторії і суспензії. Вираз "кристалічний продукт даного винаходу" означає кристалічну сполуку І або тверду сполуку І, як описано тут, наприклад, під виразом "тверда сполука І" у даному контексті слід розуміти тверду сполуку І, яка складається головним чином з кристалічної сполуки І в порівнянні з аморфною сполукою. Фармацевтичні композиції за цим винаходом можуть бути приготовані з фармацевтично прийнятними носіями або розріджувачами, а також з іншими ад'ювантами та ексципієнтами, наприклад відповідно до методів, описаних в Remington: The Science and Practice of Pharmacy, 19 Edition, Gennaro, Ed., Mack Publishing Co., Easton, PA, 1995. Фармацевтичні композиції можуть бути приготовані спеціально для введення будь-яким відповідним способом, таким як пероральний, ректальний, назальний, легеневий, місцевий (включаючи букальний та під'язиковий), трансдермальний, інтрацистернальний, інтраперитонеальний, вагінальний і парентеральний (включаючи підшкірний, внутрішньом'язовий, інтратекальний, внутрівенний і внутрішньошкірний) способи, але пероральний спосіб є переважним. Буде зрозуміло, що переважний шлях залежатиме від загального стану і віку суб'єкта, що знаходиться на лікуванні, природи захворювання і вибраного активного компоненту. 90259 20 У варіанті здійснення фармацевтичної композиції, сполука І вводиться в кількості від приблизно 0,001 до приблизно 100мг/кг маси тіла на добу. Сполука І може, наприклад, вводитися в одиничній дозованій формі, що містить згадану сполуку в кількості від приблизно 0,01 до 100мг. Загальна добова доза може знаходитися, наприклад, в діапазоні приблизно 0,05-500мг. Рецептури можуть бути звичайно представлені в одиничній дозованій формі за допомогою методів, добре відомим фахівцям. Типова одинична дозована форма для перорального введення один або більше разів на добу, наприклад від 1 до 3 разів на добу, може містити від 0,01 до приблизно 1000мг, переважно від приблизно 0,05 до приблизно 500мг. Для парентеральних способів, таких як внутрівенний, інтратекальний, внутрішньом'язовий та їм подібні способи введення, дози звичайно складають половину від дози, вживаної при пероральному введенні. Як вказано вище, наступні варіанти здійснення знаходяться в межах даного винаходу: кристалічна сполука І для застосування як лікарський засіб, кристалічна альфа-форма для застосування як лікарський засіб, кристалічна бета-форма для застосування як лікарський засіб; кристалічна гамаформа для застосування як лікарський засіб, кристалічна дельта-форма для застосування як лікарський засіб; кристалічна епсилон-форма для застосування як лікарський засіб. Далі даний винахід відноситься до застосування кристалічної сполуки І, як описано тут, наприклад, альфа-, бета-, гама-, дельта- або епсилон-форм, описаних тут, або їх сумішей, для одержання лікарського засобу для лікування захворювань центральної нервової системи, наприклад, для лікування нейродегенеративних захворювань, таких як, наприклад, хвороба Паркінсона, хвороба Альцгеймера, хвороба Хантінгтона, периферична невропатія, деменція при СНІДі або ослаблення слуху, включаючи індуковане шумом ослаблення слуху. Аналогічно, в даному винаході також представлений спосіб лікування нейродегенеративних захворювань, таких як, наприклад, хвороба Паркінсона, хвороба Альцгеймера, хвороба Хантінгтона, периферична невропатія, деменція при СНІДі або ослаблення слуху, включаючи індуковане шумом ослаблення слуху, який включає введення фармацевтично ефективної кількості кристалічної сполуки І, як описано тут, наприклад, альфа-, бета-, гама-, дельта- або епсилон-форми, описані тут, або їх суміші. Згадані медичні застосування і фармацевтичні композиції, наприклад, для лікування хвороби Паркінсона, кристалічної сполуки І і кристалічної форми даного винаходу є також застосовними до сполуки І в твердій формі, визначеній тут, як такої, що містить кристалічну форму даного винаходу, зокрема до сполуки І в твердій формі, що складається головним чином з кристалічної форми даного винаходу. Вживаний тут у зв'язку із захворюванням термін "лікування" також включає профілактику мож 21 ливих випадків. Вживаний тут термін "хвороба" також включає розлади, як можливий випадок. Даний винахід, вперше описаний тут, далі буде проілюстрований прикладами, які не обмежують його. У подальшому початковий матеріал "сполука І" може бути одержаний, наприклад, як описано Kaneko Μ. et al в J. Med. Chem. 1997, 40,18631869. Приклад 1 Одержання кристалічної альфаформи сполуки І Спосіб І 6,0г аморфної сполуки І розчиняли в 30мл ацетону. Потім додавали 0,6г карбонату калію і перемішували суспензію при кімнатній температурі протягом 1 години до фільтрування для видалення можливих незначних домішок і неорганічних солей. Осад на фільтрі промивали ацетоном. Потім фільтрат випарювали на роторному випарнику при зниженому тиску при 60°С до об'єму 10мл, потім поволі додавали 100мл метанолу. Продукт відділявся у вигляді оливи, яка практично нерозчинна при нагріванні до кипіння. Потім нерозчинні в залишку домішки видаляли фільтрацією. Фільтрат залишали перемішуватися при кімнатній температурі. Кристалічну тверду речовину відокремлювали фільтруванням. Осад на фільтрі промивали метанолом і висушували у вакуумі при 60°С протягом ночі. Вихід 2,83г (47%). Т.пл.=182,4°С (початкове значення в диференціально-сканувальній калориметрії). Втрата маси при нагріванні: 0,5%. Дані елементних аналізів: 6,71% N, 63,93% С, 5,48% Н, розрахункові значення коректні для сольвату з 0,5% Н2О: 6,79% N, 64,05% С, 5,43% Н. Рентгенофазовий аналіз узгоджується з альфа-формою. Спосіб II 5г аморфної сполуки І розчиняли в 25мл ацетону при невеликому нагріванні. Дуже поволі додавали 10мл метанолу, поки розчин не став каламутним. Розчину дозволили охолодитися до кімнатної температури шляхом природного охолоджування. Профільтрували суспензію та відкидали осад на фільтрі. В процесі фільтрування у фільтраті випадала додаткова кількість осаду. Фільтрат нагрівали до повного розчинення осаду. Потім до розчину додавали холодний метанол до початку утворення осаду. Злегка каламутний розчин нагрівали до переходу всієї речовини в розчин. Розчину дозволили охолодитися до кімнатної температури та відокремлювали осад фільтруванням. Другий осад на фільтрі був відкинутий. В процесі фільтрування деяка кількість речовини випадала у фільтраті. Нагрівання припиняло початок кристалізації у фільтраті. Додавали до розчину холодний метанол до початку осадження. Нагрівали суспензію до одержання прозорого розчину. Розчину дозволили охолодитися до кімнатної температури шляхом природного охолоджування. Утворення осаду починалося через короткий період часу (15 хвилин). Осаджений блідо-жовтий продукт відокремлювали фільтрацією і висушували у вакуумі при 50°С протягом ночі. Τ.пл.=188,9°С (початкове значення диференціально-сканувальної калориметрії). Втрата маси при нагріванні: 0,3%· Дані елементних аналізів: 90259 22 6,53% Ν, 64,33% С, 5,43% Н, розрахункові значення: 6,82% Ν, 64,37% С, 5,37% Н. Рентгенофазовий аналіз узгоджується з альфа-формою. Спосіб III Нагрівали з перемішуванням до кипіння 0,5г сполуки І в суміші ізопропілацетату (10мл) і води (0,6мл). Сполука не розчинилася повністю і тому додавали ізопропілацетат (10мл) і воду (0,6мл) і нагрівали до кипіння. Перемішування припиняли і суміші дозволили охолодитися до кімнатної температури. Одержаний кристалічний продукт відокремлювали фільтруванням і висушували у вакуумі при 40°С. Вихід =0,25г, т.пл.=183,7°С (початкове значення в диференціально-сканувальній калориметрії). Рентгенофазовий аналіз узгоджується з альфа-формою. Спосіб IV 0,5г сполуки І в суміші етилацетату (10мл) і води (0,4мл) нагрівали до 70°С при перемішуванні. Суміші дозволили охолодитися до кімнатної температури. Одержаний кристалічний продукт відокремлювали фільтруванням і висушували у вакуумі при 40°С. Рентгенофазовий аналіз узгоджується з альфа-формою. Приклад 2 Одержання кристалічної бетаформи сполуки І 28,0г аморфної сполуки І розчиняли в 250мл тетрагідрофурану (THF) і випаровували на 60г силікагелю. Очищали сполуку колоночною хроматографією на силікагелі (діаметр: 10см, висота: 5см, елюент 2,7л суміші THF/гептан 2:1). Елюат, що містить бажані сполуки, випарювали на роторному випарнику при зниженому тиску при 50°С до твердого стану (26г). Суспендували твердий залишок в 600мл ізопропілацетату та нагрівали суспензію до кипіння до розчинення майже всієї речовини. Охолоджували суспензію на бані вода/лід. Профільтрували охолоджену суспензію і осад на фільтрі промивали ізопропілацетатом і висушували у вакуумі протягом ночі при 50°С. Вихід: 16,9г (61%), т.пл.=211,7°С (початкове значення в диференціально-сканувальній калориметрії), втрата маси при нагріванні: 0,2%, дані елементних аналізів: 6,59% N, 64,63% С, 5,41% Н, розрахункові значення: 6,82% N, 64,37% С, 5,40% Н. Рентгенофазовий аналіз узгоджується з бетаформою. Приклад 3 Одержання кристалічної гамаформи сполуки І Спосіб І 15г аморфної сполуки І розчиняли в 75мл ацетону. Додавали 1,5г карбонату калію та перемішували суспензію протягом 90 хвилин. Профільтрували суспензію. Фільтрат випарювали до приблизно 30мл на роторному випарнику при зниженому тиску при 60°С. Додавали 150мл метанолу до концентрованого фільтрату і відокремлювали деяку кількість липкої речовини. Нагрівали суспензію до кипіння. В процесі нагрівання вся речовина розчинялася. Розчину дозволили охолодитися до кімнатної температури природним чином, протягом цього періоду відокремилася деяка кількість твердої речовини. Суспензію залишили перемішуватися при кімнатній температурі протягом ночі. 23 Потім профільтрували суспензію та осад на фільтрі промивали метанолом. Осад на фільтрі висушували у вакуумі при 50°С протягом ночі. Вихід інтермедіату склав 10,2г (68%). Сухий осад на фільтрі суспендували в 100мл ацетонітрилу та нагрівали до кипіння. При кипінні був одержаний каламутний розчин. Додавали додаткову кількість ацетонітрилу до одержання прозорого розчину; всього на розчинення осаду з фільтру пішло 200мл ацетонітрилу, включаючи 100мл використаних для суспензії. Розчин охолоджували до кімнатної температури протягом ночі. Наступного дня кристалічний продукт виділяли фільтруванням. Осад на фільтрі промивали невеликою кількістю ацетонітрилу і висушували у вакуумі при 55°С протягом ночі. Вихід: 6,17г, 41%, т.пл.=218,0°С (початкове значення в диференціально-сканувальній калориметрії), втрата маси при нагріванні: 2ζ(Ι)]=:0,0699. Асиметрична комірка кристала містить дві молекули сполуки І і 0-1 молекулу розчинника. Молекулою розчинника може бути або метанол або вода. При визначенні структури атоми, відповідні розчиннику, були знайдені із заселеністю С2":0,70, O1":0,50 та O3":0,36. Оскільки асиметрична комірка містить 2 молекули сполуки І і одне місце для розчинника, повне заселення місць вело б до одержання полусольвату. Нумерація атомів та конформація двох молекул в асиметричній комірці показані на Фіг.17-18, а упаковка молекул в кристалі показана на Фіг.19. Координати атомів представлені нижче в таблицях 2-4. Таблиця 2 Координати атомів і теплові еліпсоїди для неводневих атомів в молекулі 1 29 90259 30 Таблиця 3 Координати атомів і теплові еліпсоїди для неводневих атомів в молекулі 2 Таблиця 4 Координати атомів, теплові еліпсоїди та заселеність атомами в порах для розчинника Приклад 9 Температури плавлення Температури плавлення (порівняй з Прикладом 7.4, вище), одержані для аморфної форми і кристалічних альфа-, бета-, гама-, дельта- і епсилон- твердих форм сполуки І, представлені нижче в таблиці 1. Таблиця 1 31 90259 Форма Аморфна α β γ δ ε 32 Приблизна температура плавлення приблизно 150°С 181-189°С приблизно 211°С 212-218°С 211-223 приблизно 182 33 90259 34 35 90259 36 37 90259 38 39 90259 40 41 90259 42 43 90259 44 45 90259 46 47 Комп’ютерна верстка Т. Чепелева 90259 Підписне 48 Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюCrystalline forms of [9s-(9,10,12)]-5,16-bis[(ethylthio)methyl]-2,3,9,10,11,12-hexahydro-10-hydroxy-9-methyl-1-oxo-9,12-epoxy-1h-diindolo[1,2,3-fg:3',2',1'-kl]pyrrolo[3,4-i][1,6]benzodia-zocine-10-carboxylic acid methyl ester (variants), solid form of [9s-(9,10,12)]-5,16-bis[(ethylthio)methyl]-2,3,9,10,11,12-hexahydro-10-hydroxy-9-methyl-1-oxo-9,12-epoxy-1h-diindolo[1,2,3-fg:3',2',1'-kl]pyrrolo[3,4-i][1,6]benzodiazocine-10-carboxylic acid methyl ester (variants), method for the treatment of neurodegenerative disease and parkinson's disease
Автори англійськоюRock Michael Harold, Lopez De Diego Heidi, Christensen Kim Lasse, Nielsen Ole, Buur Anders, Howells Mark
Назва патенту російськоюКристаллическая форма метилового эстера [9s-(9a,10b,12a)]-5,16-бис[(этилтио)метил]-2,3,9,10,11,12-гексагидро-10-гидрокси-9-метил-1-оксо-9,12- эпокси-1н-дииндоло[1,2,3-fg:3',2',1'-kl]пирроло[3,4-и][1,6]бензодиазоцин-10-карбоновой кислоты (варианты), твердая форма метилового эстера [9s-(9a,10b,12a)]-5,16-бис[(этилтио)метил]-2,3,9,10,11,12- гексагидро-10-гидрокси-9-метил-1-оксо-9,12-эпокси-1н-дииндоло[1,2,3-fg:3',2',1'-kl]пирроло[3,4-и][1,6]бензодиазоцин-10-карбоновой кислоты (варианты), способ лечения нейродегенеративного заболевания и способ лечения болезни паркинсона
Автори російськоюРок Майкл Харольд, Лопес де Диего Хейди, Христенсен Ким Лассе, Нильсен Оле, Буур Аннерс, Хауэлз Марк
МПК / Мітки
МПК: A61P 25/16, A61K 31/7056, C07H 19/23
Мітки: 9s-(9a,10b,12a)]-5,16-біс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1н-дііндоло[1,2,3-fg:3',2',1'-kl]піроло[3,4-і][1,6]бензодіазоцин-1, метилового, кристалічна, естеру, форма
Код посилання
<a href="https://ua.patents.su/24-90259-kristalichna-forma-metilovogo-esteru-9s-9a10b12a-516-bisetiltiometil-239101112-geksagidro-10-gidroksi-9-metil-1-okso-912-epoksi-1n-diindolo123-fg321-klpirolo34-i16benzodiazocin-1.html" target="_blank" rel="follow" title="База патентів України">Кристалічна форма метилового естеру [9s-(9a,10b,12a)]-5,16-біс[(етилтіо)метил]-2,3,9,10,11,12-гексагідро-10-гідрокси-9-метил-1-оксо-9,12-епокси-1н-дііндоло[1,2,3-fg:3′,2′,1′-kl]піроло[3,4-і][1,6]бензодіазоцин-1</a>
Попередній патент: Аерогенератор
Наступний патент: Культуральне середовище та спосіб одержання нитчастих грибів
Випадковий патент: Композиція












